Профессор Борис В. Афанасьев, главный редактор журнала «Клеточная Терапия и Трансплантация» (СТТ)
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20938" ["VALUE"]=> array(2) { ["TEXT"]=> string(6047) "<p style="text-align: justify;"> Уважаемые авторы и читатели журнала СТТ!<br> На протяжении нескольких последних лет были достигнуты весьма значительные успехи в лечении ряда злокачественных заболеваний у взрослых и, особенно – у детей с применением новых лекарственных агентов и технологий, т.е. биспецифических антител, активирующих Т-клетки (BITE), конъюгированных моноклональных антител, CAR-T-клеток, и ингибиторов иммунных контрольных точек. Вышеуказанные лекарственные средства могут сочетаться с аллогенной трансплантацией гемопоэтических клеток (алло-ТГСК), тем самым создавая основу для последующей успешной терапии.<br> Наибольший прогресс был достигнут при лимфопролиферативных заболеваниях, в т.ч. у больных с резистентной/рецидивирующей (R/R) лимфомой Ходжкина, в связи с внедрением Брентуксимаба Ведотина (BV) – конъюгированного специфического антитела. Ингибиторы иммунных контрольных точек также имеют высокую эффективность на кратких сроках, но, к сожалению, беспрогрессионная выживаемость в этих случаях остается относительно низкой. Тем не менее, комбинация этих препаратов с последующей алло-ТГСК перспективна в плане продления сроков беспрогрессионной выживаемости. <br> У пациентов группы R/R с острым лимфобластным лейкозом некоторые препараты, например Блинатумомаб (антитело типа BITE) или конъюгированные антитела (например – Инотузумаб) приводят к частому терапевтическому ответу, будучи особенно эффективными у пациентов с наличием минимальной остаточной болезни (МОБ). До сих пор неясно, какая тактика должна применяться для МОБ-негативных больных и требуют ли они дальнейшей консолидации. <br> Новые направления в иммунотерапии злокачественных новообразований связаны с разработкой средств клеточной терапии на основе CAR T-клеток, которые могут обеспечить таргетные эффекты в отношении специфических неоантигенов опухолей данного типа. Имеется лишь несколько небольших исследований с применением CAR-T-клеток у взрослых и детей. Эффективность лечения CAR-T-клетками при солидных опухолях еще предстоит определить, однако и в этой области наблюдается существенный прогресс. <br> Аспекты трансплантации злокачественных заболеваний детского возраста также часто освещаются в журнале Клеточная Терапия и Трансплантация. По сравнению с высокой эффективностью лечения при остром лимфобластном лейкозе, солидные опухоли у детей, такие как медуллобластома, саркома Юинга и другие менее чувствительны к иммунотерапии в связи с иной мутационной нагрузкой и экспрессией неоантигенов. Эти молекулярные маркеры, а также микросателлитная нестабильность могут иметь значение при оценке групп клинического риска. Определение оптимальной иммунотерапии с трансплантацией или без нее при солидных новообразованиях у детей является одной из ключевых задач педиатрической онкологии. <br> В заключение, мы ожидаем оригинальных и обзорных статей для нашего журнала от наших читателей-клиницистов по вопросам детской онкологии/гематологии с целью достижения оптимального специфического ответа в сочетании с меньшей токсичностью в отношении нормальных тканей, с применением новых подходов, в особенности – иммунотерапии опухолей детского возраста, а также использования трансплантации стволовых клеток при неопухолевых заболеваниях.<br> </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5983) "
Уважаемые авторы и читатели журнала СТТ!
На протяжении нескольких последних лет были достигнуты весьма значительные успехи в лечении ряда злокачественных заболеваний у взрослых и, особенно – у детей с применением новых лекарственных агентов и технологий, т.е. биспецифических антител, активирующих Т-клетки (BITE), конъюгированных моноклональных антител, CAR-T-клеток, и ингибиторов иммунных контрольных точек. Вышеуказанные лекарственные средства могут сочетаться с аллогенной трансплантацией гемопоэтических клеток (алло-ТГСК), тем самым создавая основу для последующей успешной терапии.
Наибольший прогресс был достигнут при лимфопролиферативных заболеваниях, в т.ч. у больных с резистентной/рецидивирующей (R/R) лимфомой Ходжкина, в связи с внедрением Брентуксимаба Ведотина (BV) – конъюгированного специфического антитела. Ингибиторы иммунных контрольных точек также имеют высокую эффективность на кратких сроках, но, к сожалению, беспрогрессионная выживаемость в этих случаях остается относительно низкой. Тем не менее, комбинация этих препаратов с последующей алло-ТГСК перспективна в плане продления сроков беспрогрессионной выживаемости.
У пациентов группы R/R с острым лимфобластным лейкозом некоторые препараты, например Блинатумомаб (антитело типа BITE) или конъюгированные антитела (например – Инотузумаб) приводят к частому терапевтическому ответу, будучи особенно эффективными у пациентов с наличием минимальной остаточной болезни (МОБ). До сих пор неясно, какая тактика должна применяться для МОБ-негативных больных и требуют ли они дальнейшей консолидации.
Новые направления в иммунотерапии злокачественных новообразований связаны с разработкой средств клеточной терапии на основе CAR T-клеток, которые могут обеспечить таргетные эффекты в отношении специфических неоантигенов опухолей данного типа. Имеется лишь несколько небольших исследований с применением CAR-T-клеток у взрослых и детей. Эффективность лечения CAR-T-клетками при солидных опухолях еще предстоит определить, однако и в этой области наблюдается существенный прогресс.
Аспекты трансплантации злокачественных заболеваний детского возраста также часто освещаются в журнале Клеточная Терапия и Трансплантация. По сравнению с высокой эффективностью лечения при остром лимфобластном лейкозе, солидные опухоли у детей, такие как медуллобластома, саркома Юинга и другие менее чувствительны к иммунотерапии в связи с иной мутационной нагрузкой и экспрессией неоантигенов. Эти молекулярные маркеры, а также микросателлитная нестабильность могут иметь значение при оценке групп клинического риска. Определение оптимальной иммунотерапии с трансплантацией или без нее при солидных новообразованиях у детей является одной из ключевых задач педиатрической онкологии.
В заключение, мы ожидаем оригинальных и обзорных статей для нашего журнала от наших читателей-клиницистов по вопросам детской онкологии/гематологии с целью достижения оптимального специфического ответа в сочетании с меньшей токсичностью в отношении нормальных тканей, с применением новых подходов, в особенности – иммунотерапии опухолей детского возраста, а также использования трансплантации стволовых клеток при неопухолевых заболеваниях.
Professor Boris V. Afanasyev, Editor-in-Chief, Cellular Therapy and Transplantation Journal
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20940" ["VALUE"]=> array(2) { ["TEXT"]=> string(3016) "<p style="text-align: justify"> Dear CTT authors and readers,<br> Over last several years, dramatic improvement has been achieved in treatment of some malignancies in adults, and, especially, in children by means of novel agents and technologies, i.e., bi-specific T-cell engager antibodies (BITE), conjugated monoclonal antibodies, CAR-T cells, and immune checkpoint inhibitors. The above-mentioned drugs may be combined with allogeneic hematopoietic stem cell transplantation (allo-HCT), thus creating a reliable basis for sequential successful therapy.<br> The largest progress was attained with lymphoproliferative disorders, e.g., in patients with R/R Hodgkin lymphoma, due to introduction of Brentuximab Vedotin (BV), conjugated antibody. The immune checkpoint inhibitors have also shown high short-term efficiency, but unfortunately, the progression-free survival in these cases remains relatively low. However, combination of these drugs with subsequent allo- HCT has promising efficacy in terms of progression-free survival. <br> In R/R patients with acute lymphoblastic leukemia, some drugs like Blinatumomab, a BITE antibody, or conjugated antibody Inotuzumab, have yielded high response rates, being especially efficient in the patients with detectable minimal residual disease (MRD). It is still unclear what strategy should be used for MRD-negative patients and do they require further consolidation. <br> Novel trends in immune therapy of malignant disorders are associated with development of CAR-T cell-based therapeutic tools which may provide a more targeted effects upon specific neoantigens of the given tumor type. There are only several limited studies of CAR-T application in adults and pediatric patients. The efficiency of CAR-T cell treatment in solid tumors is yet to be established, but sufficient progress is recently observed in this area. <br> Transplantation aspects of pediatric malignancies treatment are also often spotlighted in Cellular Therapy and Transplantation. When compared with high treatment efficiency in acute lymphoblastic leukemia, pediatric tumors, like medulloblastoma, Ewing sarcoma and others are less sensitive to immunotherapy approaches due to different mutation burden and expression of neoantigens. These molecular mar-kers, as well as microsatellite instability could be of value when assessing the clinical risk groups. Elucidation of the optimal immunotherapy with or without transplantation in pediatric solid tumors is one of crucial agendas in pediatric oncology.<br> In conclusion, we are expecting from our readers original and review articles for our Journal on pediatric oncology/hematology from our potential authors from different clinics, aiming to optimize the response rate with lesser toxicity to normal tissues by using novel approaches, especially, immune therapy of pediatric malignancies, as well as the use of stem cell transplantation in nonmalignant disorders.</p> " ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2958) "
Dear CTT authors and readers,
Over last several years, dramatic improvement has been achieved in treatment of some malignancies in adults, and, especially, in children by means of novel agents and technologies, i.e., bi-specific T-cell engager antibodies (BITE), conjugated monoclonal antibodies, CAR-T cells, and immune checkpoint inhibitors. The above-mentioned drugs may be combined with allogeneic hematopoietic stem cell transplantation (allo-HCT), thus creating a reliable basis for sequential successful therapy.
The largest progress was attained with lymphoproliferative disorders, e.g., in patients with R/R Hodgkin lymphoma, due to introduction of Brentuximab Vedotin (BV), conjugated antibody. The immune checkpoint inhibitors have also shown high short-term efficiency, but unfortunately, the progression-free survival in these cases remains relatively low. However, combination of these drugs with subsequent allo-
HCT has promising efficacy in terms of progression-free survival.
In R/R patients with acute lymphoblastic leukemia, some drugs like Blinatumomab, a BITE antibody, or conjugated antibody Inotuzumab, have yielded high response rates, being especially efficient in the patients with detectable minimal residual disease (MRD). It is still unclear what strategy should be used for MRD-negative patients and do they require further consolidation.
Novel trends in immune therapy of malignant disorders are associated with development of CAR-T cell-based therapeutic tools which may provide a more targeted effects upon specific neoantigens of the given tumor type. There are only several limited studies of CAR-T application in adults and pediatric patients. The efficiency of CAR-T cell treatment in solid tumors is yet to be established, but sufficient progress is recently observed in this area.
Transplantation aspects of pediatric malignancies treatment are also often spotlighted in Cellular Therapy and Transplantation. When compared with high treatment efficiency in acute lymphoblastic leukemia, pediatric tumors, like medulloblastoma, Ewing sarcoma and others are less sensitive to immunotherapy approaches due to different mutation burden and expression of neoantigens. These molecular mar-kers, as well as microsatellite instability could be of value when assessing the clinical risk groups. Elucidation of the optimal immunotherapy with or without transplantation in pediatric solid tumors is one of crucial agendas in pediatric oncology.
In conclusion, we are expecting from our readers original and review articles for our Journal on pediatric oncology/hematology from our potential authors from different clinics, aiming to optimize the response rate with lesser toxicity to normal tissues by using novel approaches, especially, immune therapy of pediatric malignancies, as well as the use of stem cell transplantation in nonmalignant disorders.
Professor Boris V. Afanasyev, Editor-in-Chief, Cellular Therapy and Transplantation Journal
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(107) "Professor Boris V. Afanasyev, Editor-in-Chief, Cellular Therapy and Transplantation Journal
" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20940" ["VALUE"]=> array(2) { ["TEXT"]=> string(3016) "<p style="text-align: justify"> Dear CTT authors and readers,<br> Over last several years, dramatic improvement has been achieved in treatment of some malignancies in adults, and, especially, in children by means of novel agents and technologies, i.e., bi-specific T-cell engager antibodies (BITE), conjugated monoclonal antibodies, CAR-T cells, and immune checkpoint inhibitors. The above-mentioned drugs may be combined with allogeneic hematopoietic stem cell transplantation (allo-HCT), thus creating a reliable basis for sequential successful therapy.<br> The largest progress was attained with lymphoproliferative disorders, e.g., in patients with R/R Hodgkin lymphoma, due to introduction of Brentuximab Vedotin (BV), conjugated antibody. The immune checkpoint inhibitors have also shown high short-term efficiency, but unfortunately, the progression-free survival in these cases remains relatively low. However, combination of these drugs with subsequent allo- HCT has promising efficacy in terms of progression-free survival. <br> In R/R patients with acute lymphoblastic leukemia, some drugs like Blinatumomab, a BITE antibody, or conjugated antibody Inotuzumab, have yielded high response rates, being especially efficient in the patients with detectable minimal residual disease (MRD). It is still unclear what strategy should be used for MRD-negative patients and do they require further consolidation. <br> Novel trends in immune therapy of malignant disorders are associated with development of CAR-T cell-based therapeutic tools which may provide a more targeted effects upon specific neoantigens of the given tumor type. There are only several limited studies of CAR-T application in adults and pediatric patients. The efficiency of CAR-T cell treatment in solid tumors is yet to be established, but sufficient progress is recently observed in this area. <br> Transplantation aspects of pediatric malignancies treatment are also often spotlighted in Cellular Therapy and Transplantation. When compared with high treatment efficiency in acute lymphoblastic leukemia, pediatric tumors, like medulloblastoma, Ewing sarcoma and others are less sensitive to immunotherapy approaches due to different mutation burden and expression of neoantigens. These molecular mar-kers, as well as microsatellite instability could be of value when assessing the clinical risk groups. Elucidation of the optimal immunotherapy with or without transplantation in pediatric solid tumors is one of crucial agendas in pediatric oncology.<br> In conclusion, we are expecting from our readers original and review articles for our Journal on pediatric oncology/hematology from our potential authors from different clinics, aiming to optimize the response rate with lesser toxicity to normal tissues by using novel approaches, especially, immune therapy of pediatric malignancies, as well as the use of stem cell transplantation in nonmalignant disorders.</p> " ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2958) "
Dear CTT authors and readers,
Over last several years, dramatic improvement has been achieved in treatment of some malignancies in adults, and, especially, in children by means of novel agents and technologies, i.e., bi-specific T-cell engager antibodies (BITE), conjugated monoclonal antibodies, CAR-T cells, and immune checkpoint inhibitors. The above-mentioned drugs may be combined with allogeneic hematopoietic stem cell transplantation (allo-HCT), thus creating a reliable basis for sequential successful therapy.
The largest progress was attained with lymphoproliferative disorders, e.g., in patients with R/R Hodgkin lymphoma, due to introduction of Brentuximab Vedotin (BV), conjugated antibody. The immune checkpoint inhibitors have also shown high short-term efficiency, but unfortunately, the progression-free survival in these cases remains relatively low. However, combination of these drugs with subsequent allo-
HCT has promising efficacy in terms of progression-free survival.
In R/R patients with acute lymphoblastic leukemia, some drugs like Blinatumomab, a BITE antibody, or conjugated antibody Inotuzumab, have yielded high response rates, being especially efficient in the patients with detectable minimal residual disease (MRD). It is still unclear what strategy should be used for MRD-negative patients and do they require further consolidation.
Novel trends in immune therapy of malignant disorders are associated with development of CAR-T cell-based therapeutic tools which may provide a more targeted effects upon specific neoantigens of the given tumor type. There are only several limited studies of CAR-T application in adults and pediatric patients. The efficiency of CAR-T cell treatment in solid tumors is yet to be established, but sufficient progress is recently observed in this area.
Transplantation aspects of pediatric malignancies treatment are also often spotlighted in Cellular Therapy and Transplantation. When compared with high treatment efficiency in acute lymphoblastic leukemia, pediatric tumors, like medulloblastoma, Ewing sarcoma and others are less sensitive to immunotherapy approaches due to different mutation burden and expression of neoantigens. These molecular mar-kers, as well as microsatellite instability could be of value when assessing the clinical risk groups. Elucidation of the optimal immunotherapy with or without transplantation in pediatric solid tumors is one of crucial agendas in pediatric oncology.
In conclusion, we are expecting from our readers original and review articles for our Journal on pediatric oncology/hematology from our potential authors from different clinics, aiming to optimize the response rate with lesser toxicity to normal tissues by using novel approaches, especially, immune therapy of pediatric malignancies, as well as the use of stem cell transplantation in nonmalignant disorders.
Dear CTT authors and readers,
Over last several years, dramatic improvement has been achieved in treatment of some malignancies in adults, and, especially, in children by means of novel agents and technologies, i.e., bi-specific T-cell engager antibodies (BITE), conjugated monoclonal antibodies, CAR-T cells, and immune checkpoint inhibitors. The above-mentioned drugs may be combined with allogeneic hematopoietic stem cell transplantation (allo-HCT), thus creating a reliable basis for sequential successful therapy.
The largest progress was attained with lymphoproliferative disorders, e.g., in patients with R/R Hodgkin lymphoma, due to introduction of Brentuximab Vedotin (BV), conjugated antibody. The immune checkpoint inhibitors have also shown high short-term efficiency, but unfortunately, the progression-free survival in these cases remains relatively low. However, combination of these drugs with subsequent allo-
HCT has promising efficacy in terms of progression-free survival.
In R/R patients with acute lymphoblastic leukemia, some drugs like Blinatumomab, a BITE antibody, or conjugated antibody Inotuzumab, have yielded high response rates, being especially efficient in the patients with detectable minimal residual disease (MRD). It is still unclear what strategy should be used for MRD-negative patients and do they require further consolidation.
Novel trends in immune therapy of malignant disorders are associated with development of CAR-T cell-based therapeutic tools which may provide a more targeted effects upon specific neoantigens of the given tumor type. There are only several limited studies of CAR-T application in adults and pediatric patients. The efficiency of CAR-T cell treatment in solid tumors is yet to be established, but sufficient progress is recently observed in this area.
Transplantation aspects of pediatric malignancies treatment are also often spotlighted in Cellular Therapy and Transplantation. When compared with high treatment efficiency in acute lymphoblastic leukemia, pediatric tumors, like medulloblastoma, Ewing sarcoma and others are less sensitive to immunotherapy approaches due to different mutation burden and expression of neoantigens. These molecular mar-kers, as well as microsatellite instability could be of value when assessing the clinical risk groups. Elucidation of the optimal immunotherapy with or without transplantation in pediatric solid tumors is one of crucial agendas in pediatric oncology.
In conclusion, we are expecting from our readers original and review articles for our Journal on pediatric oncology/hematology from our potential authors from different clinics, aiming to optimize the response rate with lesser toxicity to normal tissues by using novel approaches, especially, immune therapy of pediatric malignancies, as well as the use of stem cell transplantation in nonmalignant disorders.
Профессор Борис В. Афанасьев, главный редактор журнала «Клеточная Терапия и Трансплантация» (СТТ)
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(193) "Профессор Борис В. Афанасьев, главный редактор журнала «Клеточная Терапия и Трансплантация» (СТТ)
" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20938" ["VALUE"]=> array(2) { ["TEXT"]=> string(6047) "<p style="text-align: justify;"> Уважаемые авторы и читатели журнала СТТ!<br> На протяжении нескольких последних лет были достигнуты весьма значительные успехи в лечении ряда злокачественных заболеваний у взрослых и, особенно – у детей с применением новых лекарственных агентов и технологий, т.е. биспецифических антител, активирующих Т-клетки (BITE), конъюгированных моноклональных антител, CAR-T-клеток, и ингибиторов иммунных контрольных точек. Вышеуказанные лекарственные средства могут сочетаться с аллогенной трансплантацией гемопоэтических клеток (алло-ТГСК), тем самым создавая основу для последующей успешной терапии.<br> Наибольший прогресс был достигнут при лимфопролиферативных заболеваниях, в т.ч. у больных с резистентной/рецидивирующей (R/R) лимфомой Ходжкина, в связи с внедрением Брентуксимаба Ведотина (BV) – конъюгированного специфического антитела. Ингибиторы иммунных контрольных точек также имеют высокую эффективность на кратких сроках, но, к сожалению, беспрогрессионная выживаемость в этих случаях остается относительно низкой. Тем не менее, комбинация этих препаратов с последующей алло-ТГСК перспективна в плане продления сроков беспрогрессионной выживаемости. <br> У пациентов группы R/R с острым лимфобластным лейкозом некоторые препараты, например Блинатумомаб (антитело типа BITE) или конъюгированные антитела (например – Инотузумаб) приводят к частому терапевтическому ответу, будучи особенно эффективными у пациентов с наличием минимальной остаточной болезни (МОБ). До сих пор неясно, какая тактика должна применяться для МОБ-негативных больных и требуют ли они дальнейшей консолидации. <br> Новые направления в иммунотерапии злокачественных новообразований связаны с разработкой средств клеточной терапии на основе CAR T-клеток, которые могут обеспечить таргетные эффекты в отношении специфических неоантигенов опухолей данного типа. Имеется лишь несколько небольших исследований с применением CAR-T-клеток у взрослых и детей. Эффективность лечения CAR-T-клетками при солидных опухолях еще предстоит определить, однако и в этой области наблюдается существенный прогресс. <br> Аспекты трансплантации злокачественных заболеваний детского возраста также часто освещаются в журнале Клеточная Терапия и Трансплантация. По сравнению с высокой эффективностью лечения при остром лимфобластном лейкозе, солидные опухоли у детей, такие как медуллобластома, саркома Юинга и другие менее чувствительны к иммунотерапии в связи с иной мутационной нагрузкой и экспрессией неоантигенов. Эти молекулярные маркеры, а также микросателлитная нестабильность могут иметь значение при оценке групп клинического риска. Определение оптимальной иммунотерапии с трансплантацией или без нее при солидных новообразованиях у детей является одной из ключевых задач педиатрической онкологии. <br> В заключение, мы ожидаем оригинальных и обзорных статей для нашего журнала от наших читателей-клиницистов по вопросам детской онкологии/гематологии с целью достижения оптимального специфического ответа в сочетании с меньшей токсичностью в отношении нормальных тканей, с применением новых подходов, в особенности – иммунотерапии опухолей детского возраста, а также использования трансплантации стволовых клеток при неопухолевых заболеваниях.<br> </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5983) "
Уважаемые авторы и читатели журнала СТТ!
На протяжении нескольких последних лет были достигнуты весьма значительные успехи в лечении ряда злокачественных заболеваний у взрослых и, особенно – у детей с применением новых лекарственных агентов и технологий, т.е. биспецифических антител, активирующих Т-клетки (BITE), конъюгированных моноклональных антител, CAR-T-клеток, и ингибиторов иммунных контрольных точек. Вышеуказанные лекарственные средства могут сочетаться с аллогенной трансплантацией гемопоэтических клеток (алло-ТГСК), тем самым создавая основу для последующей успешной терапии.
Наибольший прогресс был достигнут при лимфопролиферативных заболеваниях, в т.ч. у больных с резистентной/рецидивирующей (R/R) лимфомой Ходжкина, в связи с внедрением Брентуксимаба Ведотина (BV) – конъюгированного специфического антитела. Ингибиторы иммунных контрольных точек также имеют высокую эффективность на кратких сроках, но, к сожалению, беспрогрессионная выживаемость в этих случаях остается относительно низкой. Тем не менее, комбинация этих препаратов с последующей алло-ТГСК перспективна в плане продления сроков беспрогрессионной выживаемости.
У пациентов группы R/R с острым лимфобластным лейкозом некоторые препараты, например Блинатумомаб (антитело типа BITE) или конъюгированные антитела (например – Инотузумаб) приводят к частому терапевтическому ответу, будучи особенно эффективными у пациентов с наличием минимальной остаточной болезни (МОБ). До сих пор неясно, какая тактика должна применяться для МОБ-негативных больных и требуют ли они дальнейшей консолидации.
Новые направления в иммунотерапии злокачественных новообразований связаны с разработкой средств клеточной терапии на основе CAR T-клеток, которые могут обеспечить таргетные эффекты в отношении специфических неоантигенов опухолей данного типа. Имеется лишь несколько небольших исследований с применением CAR-T-клеток у взрослых и детей. Эффективность лечения CAR-T-клетками при солидных опухолях еще предстоит определить, однако и в этой области наблюдается существенный прогресс.
Аспекты трансплантации злокачественных заболеваний детского возраста также часто освещаются в журнале Клеточная Терапия и Трансплантация. По сравнению с высокой эффективностью лечения при остром лимфобластном лейкозе, солидные опухоли у детей, такие как медуллобластома, саркома Юинга и другие менее чувствительны к иммунотерапии в связи с иной мутационной нагрузкой и экспрессией неоантигенов. Эти молекулярные маркеры, а также микросателлитная нестабильность могут иметь значение при оценке групп клинического риска. Определение оптимальной иммунотерапии с трансплантацией или без нее при солидных новообразованиях у детей является одной из ключевых задач педиатрической онкологии.
В заключение, мы ожидаем оригинальных и обзорных статей для нашего журнала от наших читателей-клиницистов по вопросам детской онкологии/гематологии с целью достижения оптимального специфического ответа в сочетании с меньшей токсичностью в отношении нормальных тканей, с применением новых подходов, в особенности – иммунотерапии опухолей детского возраста, а также использования трансплантации стволовых клеток при неопухолевых заболеваниях.
Уважаемые авторы и читатели журнала СТТ!
На протяжении нескольких последних лет были достигнуты весьма значительные успехи в лечении ряда злокачественных заболеваний у взрослых и, особенно – у детей с применением новых лекарственных агентов и технологий, т.е. биспецифических антител, активирующих Т-клетки (BITE), конъюгированных моноклональных антител, CAR-T-клеток, и ингибиторов иммунных контрольных точек. Вышеуказанные лекарственные средства могут сочетаться с аллогенной трансплантацией гемопоэтических клеток (алло-ТГСК), тем самым создавая основу для последующей успешной терапии.
Наибольший прогресс был достигнут при лимфопролиферативных заболеваниях, в т.ч. у больных с резистентной/рецидивирующей (R/R) лимфомой Ходжкина, в связи с внедрением Брентуксимаба Ведотина (BV) – конъюгированного специфического антитела. Ингибиторы иммунных контрольных точек также имеют высокую эффективность на кратких сроках, но, к сожалению, беспрогрессионная выживаемость в этих случаях остается относительно низкой. Тем не менее, комбинация этих препаратов с последующей алло-ТГСК перспективна в плане продления сроков беспрогрессионной выживаемости.
У пациентов группы R/R с острым лимфобластным лейкозом некоторые препараты, например Блинатумомаб (антитело типа BITE) или конъюгированные антитела (например – Инотузумаб) приводят к частому терапевтическому ответу, будучи особенно эффективными у пациентов с наличием минимальной остаточной болезни (МОБ). До сих пор неясно, какая тактика должна применяться для МОБ-негативных больных и требуют ли они дальнейшей консолидации.
Новые направления в иммунотерапии злокачественных новообразований связаны с разработкой средств клеточной терапии на основе CAR T-клеток, которые могут обеспечить таргетные эффекты в отношении специфических неоантигенов опухолей данного типа. Имеется лишь несколько небольших исследований с применением CAR-T-клеток у взрослых и детей. Эффективность лечения CAR-T-клетками при солидных опухолях еще предстоит определить, однако и в этой области наблюдается существенный прогресс.
Аспекты трансплантации злокачественных заболеваний детского возраста также часто освещаются в журнале Клеточная Терапия и Трансплантация. По сравнению с высокой эффективностью лечения при остром лимфобластном лейкозе, солидные опухоли у детей, такие как медуллобластома, саркома Юинга и другие менее чувствительны к иммунотерапии в связи с иной мутационной нагрузкой и экспрессией неоантигенов. Эти молекулярные маркеры, а также микросателлитная нестабильность могут иметь значение при оценке групп клинического риска. Определение оптимальной иммунотерапии с трансплантацией или без нее при солидных новообразованиях у детей является одной из ключевых задач педиатрической онкологии.
В заключение, мы ожидаем оригинальных и обзорных статей для нашего журнала от наших читателей-клиницистов по вопросам детской онкологии/гематологии с целью достижения оптимального специфического ответа в сочетании с меньшей токсичностью в отношении нормальных тканей, с применением новых подходов, в особенности – иммунотерапии опухолей детского возраста, а также использования трансплантации стволовых клеток при неопухолевых заболеваниях.
Introduction
Transplant-associated thrombotic microangiopathy (TA-TMA) is a relatively common complication of hematopoietic stem cell transplantation. It belongs to the early endothelial damage syndromes together with veno-occlusive disease or sinusoidal obstruction syndrome of the liver, diffuse alveolar hemorrhage, engraftment syndrome and capillary leak syndrome. TA-TMA manifests itself as generalized microangiopathy causing organ injury particularly in the kidneys but also in other organs [1].
The reported incidences of TA-TMA have varied greatly, in allogeneic transplantation between 0 and 76 per cent [2, 3]. At the present time, the incidences of clinically significant TA-TMA may commonly be 5-10%, depending on several factors including patient material, transplantation methods and the diagnostic criteria used. In autologous transplantation the incidence is generally lower; incidence figures between 0 and 27% have been reported [2].
The pathophysiology of TA-TMA is complex [3]. The central feature is endothelial injury. Important etiological factors include pretransplant conditioning, calcineurin inhibitors, infections and graft-versus-host disease. The role of complement activation in the pathophysiology has been increasingly recognized.
TA-TMA differs from idiopathic acquired TTP in several respects. There is an absence of severe ADAMTS 13 deficiency, the spectrum of clinical symptoms is different, and, in contrast to idiopathic TTP, the response to plasmapheresis is usually poor.
Significant developments have taken place in recent years, both in the diagnosis, understanding of the pathophysiology, and the treatment of TA-TMA.
Diagnosis of TA-TMA
A large variety of diagnostic criteria have been used over the years [4]. Recently, three sets of criteria have been mainly used, those produced by the International Working Group [5], the American Bone Marrow Transplant Clinical Trials Network criteria [6], and the “overall TA-TMA” criteria by Cho et al [7]. The most important components of these definitions have been the presence of schistocytes, thrombocytopenia, anemia or increased need for red cell transfusions, increased lactate dehydrogenase (LDH) concentration, decreased haptoglobin level, and negative Coombs test, in various combinations.
Recently, Jodele and coworkers [1] have presented new criteria for TA-TMA. In addition to the central elements of the previous definitions, schistocytes, LDH, thrombocytopenia and anemia/red cell transfusion need, two new criteria have been added: proteinuria/hypertension and the soluble complement factor C5b-9. Table 1 shows the diagnostic criteria by Jodele et al. Five or more of the listed TA-TMA-associated markers indicate a severe disease [8]. An important finding was that some of these signs, proteinuria, hypertension and LDH increase, manifest early and can be used to predict the development of advanced TA-TMA. If proteinuria and an increased level of sC5b-9 concentration are observed, there is a great risk of poor outcome, indicating the need for aggressive treatment.
Table 1. Diagnostic criteria for TA-TMA by Jodele et al [8]

Some clinical and morphological practices in the diagnosis of transplant-associated microangiopathy should be standardized, particularly schistocyte counts. A study was recently performed on behalf of the Transplant Complications Working Party of the EBMT on this issue [9]. A questionnaire of the diagnostic methods of TA-TMA was sent to clinicians and morphologists. Also, sets of blood slides from 10 patients with TA-TMA and from 10 controls were distributed among the transplant centers, and the morphologists were asked to assess the slides as to the presence and proportion of schistocytes.
The survey showed that the International Working Group criteria and the “Overall TA-TMA” criteria were used by 41% of the centers each, in 18% of the centers the diagnosis was made individually by the physician. Interestingly, the interpretation of the percentage of schistocytes varied greatly. This was mainly based on differences in institutional practices, caused by different morphological criteria for schistocytes at different laboratories leading to substantial differences in the interpretation of the presence and degree of schistocytosis (Fig. 1). There is a number of different morphological forms of schistocytes, and the centers differ in which types of abnormal erythrocytes are counted as schistocytes.

Figure 1. Variability of the schistocyte counts in blood smears
of 10 patients with TA-TMA (blue circles) and 10 control patients (red circles)
reported by different transplant centers [9]
Role of Complement in TA-TMA
In a proportion of TA-TMA patients the complement cascade has been shown to become activated resulting in the formation of the membrane attack complex and endothelial injury [10]. This is probably caused by inherited or acquired defects in the complement regulatory system, becoming apparent in HSCT-induced stress conditions [10]. Associations between TA-TMA and certain complement-related gene variants have been demonstrated. Complement regulators, gene variants of which have been suggested to be implicated in the pathophysiology of TA-TMA include complement factor H (CFH), complement factor I (CFI), thrombomodulin (THBD), CD46 or membrane cofactor protein (MCP), and CD55. Similarly, complement activators, with gene variants implicated, include complement factor B (CFB), C3, and C5 [2].
The role of complement-activating mechanisms in TA-TMA suggests wider application of complement-inhibiting treatments, especially anti-complement antibodies in the management of this complication.
Treatment of TA-TMA
The treatment of TA-TMA has been difficult and the outcome of severe cases poor. The discontinuation or dose reduction of possibly causative agents, such as cyclosporine, tacrolimus or sirolimus is a general policy, although the documentation of the efficacy of this approach is not completely solid [8]. Therapeutic plasma exchange is usually not effective in TA-TMA and its use has been discouraged in many reports, but this treatment may be indicated in some cases to remove mutated complement, antibodies against complement, or other triggering factors for endothelial dysfunction [11].
Defibrotide has been occasionally used for the treatment of TA-TMA since many years. More recent studies have reported encouraging results, approximately half or more of the patients with a severe TA-TMA responding without any major adverse effects documented [12, 13, 14]. Other agents including rituximab, daclizumab, etanercept, infliximab, and bosentan have been used without major success [3]. With the increasing understanding of the role of complement in the pathophysiology of TA-TMA, the possible use of complement-inhibiting treatments, especially anti-complement antibodies has recently been a topic of great interest. Most of the clinical experience is with equlizumab.
Equlizumab is a humanized monoclonal antibody. It is a C5 inhibitor and prevents the formation of the membrane attack complex (C5b-9) [15, 16]. The dosing schedule is not well established. Marked individual variation has been documented in the pharmacokinetics, and monitoring the concentrations to confirm adequate dosing may be indicated [8]. Equlizumab treatment can be discontinued after the resolution of TA-TMA, usually without relapse of this complication [3]. The treatment causes increased susceptibility to infections caused by encapsulated bacteria, but this problem may be ameliorated by adequate antibiotic prophylaxis [17]. The cost of this treatment is substantial, and its availability is limited in many countries. Most of the experience of equlizumab treatment is from pediatric studies. Jodele [10] treated 50 pediatric patients with TA-TMA and multiorgan dysfunction. Seventy-two per cent of the patients survived, compared to less than 10% among historical controls. Bohl et al [13] treated 15 adult patients. The response rate was 93%, but only 33% finally survived. Vasu et al. [18] treated 5 adult patients. Three of them recovered while two died of sepsis.
Several other complement inhibitors, targeting components of the classical, lectin or alternate pathway, are under development and are likely to affect the treatment scene in the next few years [3].
Conclusion
TA-TMA remains a challenging complication of HSCT, leading to increased morbidity and mortality. The understanding of the pathophysiology is increasing and may lead to improvements in the diagnostics. Aims at standardizing the criteria of this complication are important especially for study purposes. The therapy is improving, particularly due to the introduction of complement inhibitors. However, the indications and policy of administration of these drugs are not well established and need further study.
Conflict of interest
No conflicts of interest are reported.
References
- Jodele S, Davies SM, Lane A, Khoury J, Dandoy C, Goebel J, Myers K, Grimley M, Bleesing J, El-Bietar J, Wallace G, Chima RS, Paff Z, Laskin BL. Diagnostic and risk criteria for HSCT-associated thrombotic microangiopathy: a study in children and young adults. Blood. 2014; 124(4): 645-653.
- Gavriilaki E, Sakellari I, Anagnostopoulos A, Brodsky RA. Transplant-associated thrombotic microangiopathy: opening Pandora's box. Diagnostic and risk criteria for HSCT-associated thrombotic microangiopathy: a study in children and young adults. Bone Marrow Transplant. 2017; 52(10): 1355-1360.
- Khosla J, Yeh AC, Spitzer TR, Dey BR. Hematopoietic stem cell transplant-associated thrombotic microangiopathy: current paradigm and novel therapies. Bone Marrow Transplant. 2018; 53(2): 129-137.
- George JN, Li X, McMinn JR, Terrell DR, Vesely SK, Selby GB. Thrombotic thrombocytopenic purpura-hemolytic uremic syndrome following allogeneic HPC transplantation: a diagnostic dilemma. Transfusion 2004; 44: 294-304.
- Ruutu T, Barosi G, Benjamin RJ, Clark RE, George JN, Gratwohl A, Holler E, Iacobelli M, Kentouche K, Lämmle B, Moake JL, Richardson P, Socié G, Zeigler Z, Niederwieser D, Barbui T. Diagnostic criteria for hematopoietic stem cell transplant-associated microangiopathy: results of a consensus process by an International Working Group. Haematologica. 2007; 92: 95-100.
- Ho VT, Cutler C, Carter S, Martin P, Adams R, Horowitz M, Ferrara J, Soiffer R, Giralt S. Blood and Marrow Transplant Clinical Trials Network Toxicity Committee consensus summary: thrombotic microangiopathy after hematopoietic stem cell transplantation. Biol Blood Marrow Transplant. 2005; 11: 571-575.
- Cho BS, Yahng SA, Lee SE, Eom KS, Kim YJ, Kim HJ, Lee S, Min CK, Cho SG, Kim DW, Lee JW, Min WS, Park CW. Validation of recently proposed consensus criteria for thrombotic micoangiopathy after allogeneic hematopoietic stem-cell transplantation. Transplantation 2010; 90: 918-926.
- Jodele S, Laskin BL, Dandoy CE, Myers KC, El-Bietar J, Davies SM, Goebel J, Dixon BP. A new paradigm: Diagnosis and management of HSCT-associated thrombotic microangiopathy as multi-system endothelial injury. Blood Rev 2015; 29(3): 191-204.
- Moiseev IS, Tsvetkova T, Aljurf M, Alnounou RM, Bogardt J, Chalandon Y, Drokov MYu, Dvirnyk V, Faraci M, Smidstrup Friis L, Giglio F, Greinix HT, Kornblit BT, Koelper C, Koenecke C, Lewandowski K, Niederwieser D, Passweg JR, Peczynski C, Penack O, Peric Z, Piekarska A, Ronchi PE, Rovo A, Rzepecki P, Scuderi F, Sigrist D, Siitonen SM, Stoelzel F, Sulek K, Tsakiris DA, Wilkowojska U, Duarte RF, Ruutu T, Basak GW. Clinical and morphological practices in the diagnosis of transplant-associated microangiopathy: a study on behalf of Transplant Complications Working Party of the EBMT. Bone Marrow Trasplant 2018, Oct 25. doi: 10.1038/s41409-018-0374-3.
- Jodele S: Complement in pathophysiology and treatment of transplant-associated thrombotic microangiopathies. Semin Hematol 2018; 55: 159-166.
- Obut F, Kasinath V, Abdi R. Post-bone marrow transplant thrombotic miroangiopathy. Bone Marrow Transplant 2016; 51: 891-897.
- Uderzo C, Bonanomi S, Busca A, Renoldi M, Ferrari P, Iacobelli M, Morreale G, Lanino E, Annaloro C, Volpe AD, Alessandrino P, Longoni D, Locatelli F, Sangalli H, Rovelli A. Risk factors and severe outcome in thrombotic microangiopathy after allogeneic hematopoietic stem cell transplantation. Transplantation 2006; 82: 638-644.
- Bohl SR, Kuchenbauer F, von Harsdorf S, Kloevekorn N, Schönsteiner SS, Rouhi A, Schwarzwälder P, Döhner H, Bunjes D, Bommer M. Thrombotic microangiopathy after allogeneic stem cell transplantation: A comparison of eculizumab therapy and conventional therapy. Biol Blood Marrow Transplant. 2017; 23(12): 2172-2177.
- Yeates L, Slatter MA, Bonanomi S, Lim FLWI, Ong SY, Dalissier A, Barberi W, Shulz A, Duval M, Heilmann C, Willekens A, Hwang WHY, Uderzo C, Bader P, Gennery AR. Use of defibrotide to treat transplant-associated thrombotic microangiopathy: a retrospective study of the Paediatric Diseases and Inborn Errors Working Parties of the European Society of Blood and Marrow Transplantation. Bone Marrow Transplant 2017; 52: 762-764.
- Kim S, Patel M, Yum K, Keyzner A. Hematopoietic stem cell transplant-associated thrombotic microangiopathy: review of pharmacologic treatment options. Transfusion. 2015; 55: 452-458.
- Jodele S, Fukuda T, Mizuno K, Vinks AA, Laskin BL, Goebel J, Dixon BP, Chima RS, Hirsch R, Teusink A, Lazear D, Lane A, Myers KC, Dandoy CE, Davies SM. Variable eculizumab clearance requires pharmacodynamic monitoring to optimize therapy for thrombotic microangiopathy after hematopoietic stem cell transplantation. Biol Blood Marrow Transplant. 2016; 22: 307-315.
- Jodele S, Dandoy CE, Danziger-Isakov L, Myers KC, El-Bietar J, Nelson A, Wallace G, Teusink-Cross A, Davies SM. Terminal complement blockade after hematopoietic stem cell transplantation is safe without meningococcal vaccination. Biol Blood Marrow Transplant. 2016a; 22: 1337-1340.
- Vasu S, Wu H, Satoskar A, Puto M, Roddy J, Blum W, Klisovic R, Andritsos L, Hofmeister C, Benson DM, Efebera Y, Jaglowski S, Penza S, Cohen D, Devine S, Cataland S. Eculizumab therapy in adults with allogeneic hematopoietic cell transplant-associated thrombotic microangiopathy. Bone Marrow Transplant. 2016; 51(9): 1241-1244.
Introduction
Transplant-associated thrombotic microangiopathy (TA-TMA) is a relatively common complication of hematopoietic stem cell transplantation. It belongs to the early endothelial damage syndromes together with veno-occlusive disease or sinusoidal obstruction syndrome of the liver, diffuse alveolar hemorrhage, engraftment syndrome and capillary leak syndrome. TA-TMA manifests itself as generalized microangiopathy causing organ injury particularly in the kidneys but also in other organs [1].
The reported incidences of TA-TMA have varied greatly, in allogeneic transplantation between 0 and 76 per cent [2, 3]. At the present time, the incidences of clinically significant TA-TMA may commonly be 5-10%, depending on several factors including patient material, transplantation methods and the diagnostic criteria used. In autologous transplantation the incidence is generally lower; incidence figures between 0 and 27% have been reported [2].
The pathophysiology of TA-TMA is complex [3]. The central feature is endothelial injury. Important etiological factors include pretransplant conditioning, calcineurin inhibitors, infections and graft-versus-host disease. The role of complement activation in the pathophysiology has been increasingly recognized.
TA-TMA differs from idiopathic acquired TTP in several respects. There is an absence of severe ADAMTS 13 deficiency, the spectrum of clinical symptoms is different, and, in contrast to idiopathic TTP, the response to plasmapheresis is usually poor.
Significant developments have taken place in recent years, both in the diagnosis, understanding of the pathophysiology, and the treatment of TA-TMA.
Diagnosis of TA-TMA
A large variety of diagnostic criteria have been used over the years [4]. Recently, three sets of criteria have been mainly used, those produced by the International Working Group [5], the American Bone Marrow Transplant Clinical Trials Network criteria [6], and the “overall TA-TMA” criteria by Cho et al [7]. The most important components of these definitions have been the presence of schistocytes, thrombocytopenia, anemia or increased need for red cell transfusions, increased lactate dehydrogenase (LDH) concentration, decreased haptoglobin level, and negative Coombs test, in various combinations.
Recently, Jodele and coworkers [1] have presented new criteria for TA-TMA. In addition to the central elements of the previous definitions, schistocytes, LDH, thrombocytopenia and anemia/red cell transfusion need, two new criteria have been added: proteinuria/hypertension and the soluble complement factor C5b-9. Table 1 shows the diagnostic criteria by Jodele et al. Five or more of the listed TA-TMA-associated markers indicate a severe disease [8]. An important finding was that some of these signs, proteinuria, hypertension and LDH increase, manifest early and can be used to predict the development of advanced TA-TMA. If proteinuria and an increased level of sC5b-9 concentration are observed, there is a great risk of poor outcome, indicating the need for aggressive treatment.
Table 1. Diagnostic criteria for TA-TMA by Jodele et al [8]

Some clinical and morphological practices in the diagnosis of transplant-associated microangiopathy should be standardized, particularly schistocyte counts. A study was recently performed on behalf of the Transplant Complications Working Party of the EBMT on this issue [9]. A questionnaire of the diagnostic methods of TA-TMA was sent to clinicians and morphologists. Also, sets of blood slides from 10 patients with TA-TMA and from 10 controls were distributed among the transplant centers, and the morphologists were asked to assess the slides as to the presence and proportion of schistocytes.
The survey showed that the International Working Group criteria and the “Overall TA-TMA” criteria were used by 41% of the centers each, in 18% of the centers the diagnosis was made individually by the physician. Interestingly, the interpretation of the percentage of schistocytes varied greatly. This was mainly based on differences in institutional practices, caused by different morphological criteria for schistocytes at different laboratories leading to substantial differences in the interpretation of the presence and degree of schistocytosis (Fig. 1). There is a number of different morphological forms of schistocytes, and the centers differ in which types of abnormal erythrocytes are counted as schistocytes.

Figure 1. Variability of the schistocyte counts in blood smears
of 10 patients with TA-TMA (blue circles) and 10 control patients (red circles)
reported by different transplant centers [9]
Role of Complement in TA-TMA
In a proportion of TA-TMA patients the complement cascade has been shown to become activated resulting in the formation of the membrane attack complex and endothelial injury [10]. This is probably caused by inherited or acquired defects in the complement regulatory system, becoming apparent in HSCT-induced stress conditions [10]. Associations between TA-TMA and certain complement-related gene variants have been demonstrated. Complement regulators, gene variants of which have been suggested to be implicated in the pathophysiology of TA-TMA include complement factor H (CFH), complement factor I (CFI), thrombomodulin (THBD), CD46 or membrane cofactor protein (MCP), and CD55. Similarly, complement activators, with gene variants implicated, include complement factor B (CFB), C3, and C5 [2].
The role of complement-activating mechanisms in TA-TMA suggests wider application of complement-inhibiting treatments, especially anti-complement antibodies in the management of this complication.
Treatment of TA-TMA
The treatment of TA-TMA has been difficult and the outcome of severe cases poor. The discontinuation or dose reduction of possibly causative agents, such as cyclosporine, tacrolimus or sirolimus is a general policy, although the documentation of the efficacy of this approach is not completely solid [8]. Therapeutic plasma exchange is usually not effective in TA-TMA and its use has been discouraged in many reports, but this treatment may be indicated in some cases to remove mutated complement, antibodies against complement, or other triggering factors for endothelial dysfunction [11].
Defibrotide has been occasionally used for the treatment of TA-TMA since many years. More recent studies have reported encouraging results, approximately half or more of the patients with a severe TA-TMA responding without any major adverse effects documented [12, 13, 14]. Other agents including rituximab, daclizumab, etanercept, infliximab, and bosentan have been used without major success [3]. With the increasing understanding of the role of complement in the pathophysiology of TA-TMA, the possible use of complement-inhibiting treatments, especially anti-complement antibodies has recently been a topic of great interest. Most of the clinical experience is with equlizumab.
Equlizumab is a humanized monoclonal antibody. It is a C5 inhibitor and prevents the formation of the membrane attack complex (C5b-9) [15, 16]. The dosing schedule is not well established. Marked individual variation has been documented in the pharmacokinetics, and monitoring the concentrations to confirm adequate dosing may be indicated [8]. Equlizumab treatment can be discontinued after the resolution of TA-TMA, usually without relapse of this complication [3]. The treatment causes increased susceptibility to infections caused by encapsulated bacteria, but this problem may be ameliorated by adequate antibiotic prophylaxis [17]. The cost of this treatment is substantial, and its availability is limited in many countries. Most of the experience of equlizumab treatment is from pediatric studies. Jodele [10] treated 50 pediatric patients with TA-TMA and multiorgan dysfunction. Seventy-two per cent of the patients survived, compared to less than 10% among historical controls. Bohl et al [13] treated 15 adult patients. The response rate was 93%, but only 33% finally survived. Vasu et al. [18] treated 5 adult patients. Three of them recovered while two died of sepsis.
Several other complement inhibitors, targeting components of the classical, lectin or alternate pathway, are under development and are likely to affect the treatment scene in the next few years [3].
Conclusion
TA-TMA remains a challenging complication of HSCT, leading to increased morbidity and mortality. The understanding of the pathophysiology is increasing and may lead to improvements in the diagnostics. Aims at standardizing the criteria of this complication are important especially for study purposes. The therapy is improving, particularly due to the introduction of complement inhibitors. However, the indications and policy of administration of these drugs are not well established and need further study.
Conflict of interest
No conflicts of interest are reported.
References
- Jodele S, Davies SM, Lane A, Khoury J, Dandoy C, Goebel J, Myers K, Grimley M, Bleesing J, El-Bietar J, Wallace G, Chima RS, Paff Z, Laskin BL. Diagnostic and risk criteria for HSCT-associated thrombotic microangiopathy: a study in children and young adults. Blood. 2014; 124(4): 645-653.
- Gavriilaki E, Sakellari I, Anagnostopoulos A, Brodsky RA. Transplant-associated thrombotic microangiopathy: opening Pandora's box. Diagnostic and risk criteria for HSCT-associated thrombotic microangiopathy: a study in children and young adults. Bone Marrow Transplant. 2017; 52(10): 1355-1360.
- Khosla J, Yeh AC, Spitzer TR, Dey BR. Hematopoietic stem cell transplant-associated thrombotic microangiopathy: current paradigm and novel therapies. Bone Marrow Transplant. 2018; 53(2): 129-137.
- George JN, Li X, McMinn JR, Terrell DR, Vesely SK, Selby GB. Thrombotic thrombocytopenic purpura-hemolytic uremic syndrome following allogeneic HPC transplantation: a diagnostic dilemma. Transfusion 2004; 44: 294-304.
- Ruutu T, Barosi G, Benjamin RJ, Clark RE, George JN, Gratwohl A, Holler E, Iacobelli M, Kentouche K, Lämmle B, Moake JL, Richardson P, Socié G, Zeigler Z, Niederwieser D, Barbui T. Diagnostic criteria for hematopoietic stem cell transplant-associated microangiopathy: results of a consensus process by an International Working Group. Haematologica. 2007; 92: 95-100.
- Ho VT, Cutler C, Carter S, Martin P, Adams R, Horowitz M, Ferrara J, Soiffer R, Giralt S. Blood and Marrow Transplant Clinical Trials Network Toxicity Committee consensus summary: thrombotic microangiopathy after hematopoietic stem cell transplantation. Biol Blood Marrow Transplant. 2005; 11: 571-575.
- Cho BS, Yahng SA, Lee SE, Eom KS, Kim YJ, Kim HJ, Lee S, Min CK, Cho SG, Kim DW, Lee JW, Min WS, Park CW. Validation of recently proposed consensus criteria for thrombotic micoangiopathy after allogeneic hematopoietic stem-cell transplantation. Transplantation 2010; 90: 918-926.
- Jodele S, Laskin BL, Dandoy CE, Myers KC, El-Bietar J, Davies SM, Goebel J, Dixon BP. A new paradigm: Diagnosis and management of HSCT-associated thrombotic microangiopathy as multi-system endothelial injury. Blood Rev 2015; 29(3): 191-204.
- Moiseev IS, Tsvetkova T, Aljurf M, Alnounou RM, Bogardt J, Chalandon Y, Drokov MYu, Dvirnyk V, Faraci M, Smidstrup Friis L, Giglio F, Greinix HT, Kornblit BT, Koelper C, Koenecke C, Lewandowski K, Niederwieser D, Passweg JR, Peczynski C, Penack O, Peric Z, Piekarska A, Ronchi PE, Rovo A, Rzepecki P, Scuderi F, Sigrist D, Siitonen SM, Stoelzel F, Sulek K, Tsakiris DA, Wilkowojska U, Duarte RF, Ruutu T, Basak GW. Clinical and morphological practices in the diagnosis of transplant-associated microangiopathy: a study on behalf of Transplant Complications Working Party of the EBMT. Bone Marrow Trasplant 2018, Oct 25. doi: 10.1038/s41409-018-0374-3.
- Jodele S: Complement in pathophysiology and treatment of transplant-associated thrombotic microangiopathies. Semin Hematol 2018; 55: 159-166.
- Obut F, Kasinath V, Abdi R. Post-bone marrow transplant thrombotic miroangiopathy. Bone Marrow Transplant 2016; 51: 891-897.
- Uderzo C, Bonanomi S, Busca A, Renoldi M, Ferrari P, Iacobelli M, Morreale G, Lanino E, Annaloro C, Volpe AD, Alessandrino P, Longoni D, Locatelli F, Sangalli H, Rovelli A. Risk factors and severe outcome in thrombotic microangiopathy after allogeneic hematopoietic stem cell transplantation. Transplantation 2006; 82: 638-644.
- Bohl SR, Kuchenbauer F, von Harsdorf S, Kloevekorn N, Schönsteiner SS, Rouhi A, Schwarzwälder P, Döhner H, Bunjes D, Bommer M. Thrombotic microangiopathy after allogeneic stem cell transplantation: A comparison of eculizumab therapy and conventional therapy. Biol Blood Marrow Transplant. 2017; 23(12): 2172-2177.
- Yeates L, Slatter MA, Bonanomi S, Lim FLWI, Ong SY, Dalissier A, Barberi W, Shulz A, Duval M, Heilmann C, Willekens A, Hwang WHY, Uderzo C, Bader P, Gennery AR. Use of defibrotide to treat transplant-associated thrombotic microangiopathy: a retrospective study of the Paediatric Diseases and Inborn Errors Working Parties of the European Society of Blood and Marrow Transplantation. Bone Marrow Transplant 2017; 52: 762-764.
- Kim S, Patel M, Yum K, Keyzner A. Hematopoietic stem cell transplant-associated thrombotic microangiopathy: review of pharmacologic treatment options. Transfusion. 2015; 55: 452-458.
- Jodele S, Fukuda T, Mizuno K, Vinks AA, Laskin BL, Goebel J, Dixon BP, Chima RS, Hirsch R, Teusink A, Lazear D, Lane A, Myers KC, Dandoy CE, Davies SM. Variable eculizumab clearance requires pharmacodynamic monitoring to optimize therapy for thrombotic microangiopathy after hematopoietic stem cell transplantation. Biol Blood Marrow Transplant. 2016; 22: 307-315.
- Jodele S, Dandoy CE, Danziger-Isakov L, Myers KC, El-Bietar J, Nelson A, Wallace G, Teusink-Cross A, Davies SM. Terminal complement blockade after hematopoietic stem cell transplantation is safe without meningococcal vaccination. Biol Blood Marrow Transplant. 2016a; 22: 1337-1340.
- Vasu S, Wu H, Satoskar A, Puto M, Roddy J, Blum W, Klisovic R, Andritsos L, Hofmeister C, Benson DM, Efebera Y, Jaglowski S, Penza S, Cohen D, Devine S, Cataland S. Eculizumab therapy in adults with allogeneic hematopoietic cell transplant-associated thrombotic microangiopathy. Bone Marrow Transplant. 2016; 51(9): 1241-1244.
Тапани Рууту
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20968" ["VALUE"]=> array(2) { ["TEXT"]=> string(202) "<p> Клинический исследовательский институт, Университетский госпиталь Хельсинки,<br> Финляндия </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(184) "
Клинический исследовательский институт, Университетский госпиталь Хельсинки,
Финляндия
Трансплант-ассоциированная тромботическая микроангиопатия (ТА-ТМА) является сравнительно частым осложнением трансплантации гемопоэтических стволовых клеток (ТГСК). Ее патогенез весьма сложен, а центральным звеном является повреждение эндотелия. Все больше выясняется роль активации комплемента в патофизиологии процесса. Диагностические процедуры и интерпретация результатов существенно различаются между клиническими центрами, и здесь важны задачи стандартизации критериев диагностики этого осложнения особенно в исследовательских целях. Происходит совершенствование терапии, главным образом, благодаря применению ингибиторов комплемента.
Однако показания и тактика назначения этих препаратов еще недостаточно установилась и требует дальнейшего изучения.
Ключевые слова
Трансплантация гемопоэтических клеток, тромботическая микроангиопатия, диагностические методы, стандартизация, терапия, ингибиторы комплемента.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20950" ["VALUE"]=> string(36) "10.18620/ctt-1866-8836-2019-8-1-8-11" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(36) "10.18620/ctt-1866-8836-2019-8-1-8-11" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20951" ["VALUE"]=> array(2) { ["TEXT"]=> string(32) "<p>Tapani Ruutu </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(20) "Tapani Ruutu
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20952" ["VALUE"]=> array(2) { ["TEXT"]=> string(76) "<p>Clinical Research Institute, Helsinki University Hospital</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(64) "Clinical Research Institute, Helsinki University Hospital
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20953" ["VALUE"]=> array(2) { ["TEXT"]=> string(1024) "<p style="text-align: justify;"> Transplant-associated thrombotic microangiopathy (TA-TMA) is a relatively common complication of hematopoietic stem cell transplantation. The pathophysiology is complex, the central feature is endothelial injury. The role of complement activation in the pathophysiology has been increasingly recognized. The diagnostic procedures and interpretations vary considerably between centers, and aims at standardizing the criteria of this complication are important especially for study purposes. The therapy is improving, particularly due to the introduction of complement inhibitors. However, the indications and policy of administration of these drugs are not well established and need further study.</p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;">Hemopoietic stem cell transplantation, thrombotic microangiopathy, diagnostic techniques, standardization, therapy, complement inhibitors.</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(958) "Transplant-associated thrombotic microangiopathy (TA-TMA) is a relatively common complication of hematopoietic stem cell transplantation. The pathophysiology is complex, the central feature is endothelial injury. The role of complement activation in the pathophysiology has been increasingly recognized. The diagnostic procedures and interpretations vary considerably between centers, and aims at standardizing the criteria of this complication are important especially for study purposes. The therapy is improving, particularly due to the introduction of complement inhibitors. However, the indications and policy of administration of these drugs are not well established and need further study.
Keywords
Hemopoietic stem cell transplantation, thrombotic microangiopathy, diagnostic techniques, standardization, therapy, complement inhibitors.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20954" ["VALUE"]=> string(71) "Recent developments in transplant-associated thrombotic microangiopathy" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(71) "Recent developments in transplant-associated thrombotic microangiopathy" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20955" ["VALUE"]=> string(4) "1550" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1550" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20956" ["VALUE"]=> string(4) "1551" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1551" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(12) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20951" ["VALUE"]=> array(2) { ["TEXT"]=> string(32) "<p>Tapani Ruutu </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(20) "Tapani Ruutu
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(20) "Tapani Ruutu
" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20953" ["VALUE"]=> array(2) { ["TEXT"]=> string(1024) "<p style="text-align: justify;"> Transplant-associated thrombotic microangiopathy (TA-TMA) is a relatively common complication of hematopoietic stem cell transplantation. The pathophysiology is complex, the central feature is endothelial injury. The role of complement activation in the pathophysiology has been increasingly recognized. The diagnostic procedures and interpretations vary considerably between centers, and aims at standardizing the criteria of this complication are important especially for study purposes. The therapy is improving, particularly due to the introduction of complement inhibitors. However, the indications and policy of administration of these drugs are not well established and need further study.</p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;">Hemopoietic stem cell transplantation, thrombotic microangiopathy, diagnostic techniques, standardization, therapy, complement inhibitors.</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(958) "Transplant-associated thrombotic microangiopathy (TA-TMA) is a relatively common complication of hematopoietic stem cell transplantation. The pathophysiology is complex, the central feature is endothelial injury. The role of complement activation in the pathophysiology has been increasingly recognized. The diagnostic procedures and interpretations vary considerably between centers, and aims at standardizing the criteria of this complication are important especially for study purposes. The therapy is improving, particularly due to the introduction of complement inhibitors. However, the indications and policy of administration of these drugs are not well established and need further study.
Keywords
Hemopoietic stem cell transplantation, thrombotic microangiopathy, diagnostic techniques, standardization, therapy, complement inhibitors.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(958) "Transplant-associated thrombotic microangiopathy (TA-TMA) is a relatively common complication of hematopoietic stem cell transplantation. The pathophysiology is complex, the central feature is endothelial injury. The role of complement activation in the pathophysiology has been increasingly recognized. The diagnostic procedures and interpretations vary considerably between centers, and aims at standardizing the criteria of this complication are important especially for study purposes. The therapy is improving, particularly due to the introduction of complement inhibitors. However, the indications and policy of administration of these drugs are not well established and need further study.
Keywords
Hemopoietic stem cell transplantation, thrombotic microangiopathy, diagnostic techniques, standardization, therapy, complement inhibitors.
" } ["DOI"]=> array(37) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20950" ["VALUE"]=> string(36) "10.18620/ctt-1866-8836-2019-8-1-8-11" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(36) "10.18620/ctt-1866-8836-2019-8-1-8-11" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(36) "10.18620/ctt-1866-8836-2019-8-1-8-11" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20954" ["VALUE"]=> string(71) "Recent developments in transplant-associated thrombotic microangiopathy" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(71) "Recent developments in transplant-associated thrombotic microangiopathy" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(71) "Recent developments in transplant-associated thrombotic microangiopathy" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20952" ["VALUE"]=> array(2) { ["TEXT"]=> string(76) "<p>Clinical Research Institute, Helsinki University Hospital</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(64) "Clinical Research Institute, Helsinki University Hospital
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(64) "Clinical Research Institute, Helsinki University Hospital
" } ["AUTHORS"]=> array(38) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> array(1) { [0]=> string(5) "22020" } ["VALUE"]=> array(1) { [0]=> string(1) "7" } ["DESCRIPTION"]=> array(1) { [0]=> string(0) "" } ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(1) { [0]=> string(1) "7" } ["~DESCRIPTION"]=> array(1) { [0]=> string(0) "" } ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(53) "Tapani Ruutu" ["LINK_ELEMENT_VALUE"]=> bool(false) } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20967" ["VALUE"]=> array(2) { ["TEXT"]=> string(42) "<p>Тапани Рууту</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(30) "Тапани Рууту
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(30) "Тапани Рууту
" } ["SUBMITTED"]=> array(37) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20946" ["VALUE"]=> string(10) "21.01.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "21.01.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "21.01.2019" } ["ACCEPTED"]=> array(37) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20947" ["VALUE"]=> string(10) "15.03.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "15.03.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "15.03.2019" } ["CONTACT"]=> array(38) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20948" ["VALUE"]=> string(1) "7" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(1) "7" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(53) "Tapani Ruutu" ["LINK_ELEMENT_VALUE"]=> bool(false) } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20969" ["VALUE"]=> array(2) { ["TEXT"]=> string(1869) "<p style="text-align: justify;">Трансплант-ассоциированная тромботическая микроангиопатия (ТА-ТМА) является сравнительно частым осложнением трансплантации гемопоэтических стволовых клеток (ТГСК). Ее патогенез весьма сложен, а центральным звеном является повреждение эндотелия. Все больше выясняется роль активации комплемента в патофизиологии процесса. Диагностические процедуры и интерпретация результатов существенно различаются между клиническими центрами, и здесь важны задачи стандартизации критериев диагностики этого осложнения особенно в исследовательских целях. Происходит совершенствование терапии, главным образом, благодаря применению ингибиторов комплемента.<br> Однако показания и тактика назначения этих препаратов еще недостаточно установилась и требует дальнейшего изучения. </p> <h2>Ключевые слова</h2> <p style="text-align: justify;">Трансплантация гемопоэтических клеток, тромботическая микроангиопатия, диагностические методы, стандартизация, терапия, ингибиторы комплемента.</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1807) "Трансплант-ассоциированная тромботическая микроангиопатия (ТА-ТМА) является сравнительно частым осложнением трансплантации гемопоэтических стволовых клеток (ТГСК). Ее патогенез весьма сложен, а центральным звеном является повреждение эндотелия. Все больше выясняется роль активации комплемента в патофизиологии процесса. Диагностические процедуры и интерпретация результатов существенно различаются между клиническими центрами, и здесь важны задачи стандартизации критериев диагностики этого осложнения особенно в исследовательских целях. Происходит совершенствование терапии, главным образом, благодаря применению ингибиторов комплемента.
Однако показания и тактика назначения этих препаратов еще недостаточно установилась и требует дальнейшего изучения.
Ключевые слова
Трансплантация гемопоэтических клеток, тромботическая микроангиопатия, диагностические методы, стандартизация, терапия, ингибиторы комплемента.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(1807) "Трансплант-ассоциированная тромботическая микроангиопатия (ТА-ТМА) является сравнительно частым осложнением трансплантации гемопоэтических стволовых клеток (ТГСК). Ее патогенез весьма сложен, а центральным звеном является повреждение эндотелия. Все больше выясняется роль активации комплемента в патофизиологии процесса. Диагностические процедуры и интерпретация результатов существенно различаются между клиническими центрами, и здесь важны задачи стандартизации критериев диагностики этого осложнения особенно в исследовательских целях. Происходит совершенствование терапии, главным образом, благодаря применению ингибиторов комплемента.
Однако показания и тактика назначения этих препаратов еще недостаточно установилась и требует дальнейшего изучения.
Ключевые слова
Трансплантация гемопоэтических клеток, тромботическая микроангиопатия, диагностические методы, стандартизация, терапия, ингибиторы комплемента.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20968" ["VALUE"]=> array(2) { ["TEXT"]=> string(202) "<p> Клинический исследовательский институт, Университетский госпиталь Хельсинки,<br> Финляндия </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(184) "
Клинический исследовательский институт, Университетский госпиталь Хельсинки,
Финляндия
Клинический исследовательский институт, Университетский госпиталь Хельсинки,
Финляндия
Introduction
Additional therapeutic effects of “old”, drugs for novel clini-cal indications have been studied over last decades. Novel suggestions for repurposing of different medical drugs for cancer treatment have been made over recent years [1, 2].
There are three main reasons for these proposals: (1) limited efficiency of novel inhibitors or specific monoclonal antibodies targeted for oncogene-specific molecules; (2) new molecular targets were revealed for some drugs traditionally used to other therapeutic purposes; and (3) eventual decline of development costs for the new therapies performed by the “old” drugs.
A variety of drugs used in different somatic disorders is now considered as complementary tool for treatment of malignancies. These candidate compounds are listed in several indexes available online, e.g., the Drug Repurposing Portal supported by Excelra [3]. In addition, a number of recent review articles concern different aspects of old drug applications in cancer therapy [1, 4, 5].
It should be noted, however, that most cytostatic and anticancer effects of the repurposed drugs are shown in the in vitro models, or in experimental animals, thus suggesting a long way until their clinical implication. The big data collected from drug screening in different models are analyzed by different bioinformatic approaches, e.g. [6], thus accelerating the drug selection process to some degree.
The specific aim of our study was to discuss probable anticancer effects of some anti-infectious drugs which are now widely used in hematopoietic stem cell transplantation protocols.
Some candidate drugs intended for repurposing in cancer treatment are listed in Table 1.
Table 1. Summary of drugs used for treatment of common disorders, their primary indication, non-cancer and cancer targets


Drug repositioning for leukemia treatment
Metformin
This well-known anti-diabetic drug activates the AMF-regulated protein kinase pathway dependent on the tumor suppressor LKB1. The LKB1/AMPK signaling may be suppressed by ERK which is activated in a half of acute myeloid leukemia (AML) cases with appropriate mutations, e.g., FLT3-ITD mutation. These cases may be susceptible for metformin and the treatment efficiency may be increased in combination with sorafenib or other novel drugs [25, 26].
Chloroquines
Pre-clinical studies of the last decade have repeatedly confirmed distinct anticancer effects of well-known antimalarial drug chloroquine and its derivatives. In particular, chloroquine and hydroxychloroquine have relatively well-characterized toxicity profiles. Previously published review articles provide an excellent overview on diversity of chloroquine effects on cancer cells, both in the cell culture as well as on human tumors grafted into mice; and suggest incorporation of hydroxychloroquine in prospective combination schemes for clinical studies [9]. The authors discuss some common features in cancer cells that could be targeted by quinacrine and its derivatives, aiming for potential pharmaceutical intervention in oncology.
A recent work by Eriksson et al. [11] dealt with more specific quinacrine effects upon malignant blood cells. The authors have earlier selected quinacrine as the most plausible compound for its antileukemic effects, and tested this drug in vitro in combination with some common cytostatic agents (daunorubicin, cytarabine, azacitidine, etc.). Acute myeloid leukemia (AML) cell lines were cultured as a target population, then tested for cytotoxicity by fluorometric microculture. In most in vitro systems, the workers have shown distinct synergism between quinacrine and cytarabine, or azacitidine added to these cell cultures. Moreover, the in vivo usage of quinacrine (100 mg/kg, six injections for two weeks) in SCID mice bearing human AML cells caused a significant decrease in circulating blast cells and increased the median survival time of the animals. Hence, further studies may offer an “old-new”, less toxic drug for combined treatment of leukemia.
Fluoroquinolones
Quinolone-based antibiotics, especially, fluoroquinolones are used over decades to manage different bacterial and protozoal infections. Their microbicidal action is caused by inhibition of the ligase domain of the type II DNA topoisomerase, thus releasing endonuclease activities and irreversible DNA decay in the target cells, as reviewed by Idowu and Schweizer [12]. Such a universal cytotoxic effect presumes possible applications of fluoroquinolones for cancer treatment. These studies, however, are still in progress and should be substantiated in pre-clinical trials.
Tetracycline, and its derivatives
This class of antibacterials is known since 1948. Tetracyclines are widely used in medicine and agriculture to combat broad spectrum of bacteria [14]. Despite high proportion of tetracyclin-resistant microorganisms (due to powerful drug efflux), a new generation of these drugs was developed later on (e.g., Doxycycline, Tigecycline) which are now administered for empiric treatment, e.g., in immunocompromised patients following severe cytostatic treatment and bone marrow transplantation. Interestingly, doxorubicin, a popular anticancer antibiotic belongs to the same family of bioactive compounds.
All the tetracyclines inhibit protein assembly in Gram(+) and Gram(-) microbes by preventing the aminoacyl-tRNA binding to the acceptor sites at the ribosomes. Meanwhile, tetracyclines were also tested for treatment of a number of inflammatory diseases, due to their inhibition of matrix metalloproteinases, antiapoptotic, antioxidative, and antiinflammatory effects in humans [14].
Hence, the major antimicrobial effect of tetracyclines is due to their protein-inhibiting actions in bacteria. Moreover, they possess antiproliferative and pro-apoptotic effects in mammalian cancer cells, by suppressing mitochondrial ribosomes and energy metabolism [16]. More recently, they are also considered potential anticancer drugs. E.g., Tigecycline a structural homologue of tetracycline, being a potent glycylcycline antibiotic, is mostly used as a broad-spectrum drug against gram-positive and gram-negative pathogens. It reversibly binds the 30S subunit of the bacterial ribosomes, being also an inhibitor of mitochondrial biogenesis [27].
Ten malignant tumor cell lines of different origin were tested in vitro with tigecycline and doxycycline (another tetracycline derivative), showing. Tigecycline has shown its ability to inhibit the MCF7 and T47D spheroid cell growth, at the concentrations from 10 µM to 50 µM [16]. Moreover, tigecycline was previously shown to kill human AML differentiated blasts as well as leukemic stem cells in vitro and in vivo by blocking mitochondrial protein synthesis [28].
Another work concerned in vitro cytostatic effects of tigecycline on the acute lymphoblastic leukemia (ALL) showing decreased survival and suppression of clonogenic growth in malignant cell cultures [29]. Toxic effects upon normal hematopoietic cells were less pronounced. Pharmacokinetics and potential antitumor effects make this drug a promising option when sensitizing ALL cells for chemotherapy [30].
In particular, tigecycline was studied in the Phase 1 dose-escalation study of tigecycline administered intravenously daily 5 of 7 days for 2 weeks to patients with AML. A total of 27 adult patients with relapsed and refractory AML were enrolled [27]. The authors have shown relative safety and assessed maximal tolerable doses for the drug infused into the patients with relapsed/refractory AML, however, with no evident anticancer effects revealed.
Moreover, some small clinical trials with doxycycline were performed over last years in cancer clinics (primarily aiming for infection therapy, but not cancer treatment) showing some antitumor effects in cancer patients as reviewed by Lamb et al. [16]. Initial positive results of doxycycline trials obtained in advanced or treatment-resistant cases of B-cell lymphoma [30]. This clinical effect was not, however, confirmed in more extensive studies.
Erythromycin and other macrolides
These antibacterials may also inhibit various microflora by suppressing ribosome functions. Similarly, they can inhibit mitochondrial ribosomes in eukaryotic cells, as shown in several cancer cell lines [16]. Azithromycin is an improved erythromycin derivative which is widely used in post-transplant patients, being more slowly eliminated than erythromycin. Its anti-infectious effect is exploited for prevention of bacterial complications in chronic infectious conditions, e.g., at later terms post-HSCT.
Surprisingly, a probable antitumor effect of azithromycin was revealed in a study by Shamoun et al. [17] published as a short abstract, where a long-term drug administration (14 days) aimed to ameliorate chronic graft-versus-graft disease (GvHD) was accompanied by decreased rates of relapse and improved survivals in a combined group of with acute leukemia, MDS, malignant lymphomas, and chronic leukemia patients.
Clarithromycin (6-O-methyl erythromycin) is also a widely used semi-synthetic macrolide drug which also has previously shown a sufficient anticancer activity against some experimental tumors [31] when used after a course of cancer chemotherapy in mice.
A recent review by van Nuffel et al. [18] has summarized numerous data obtained in human studies showing complementary effects of clarithromycin as an antibacterial drug in combined treatment of multiple myeloma, CML and other blood malignancies, especially MALT lymphomas and Hodgkin’s disease studied over last 2 decades. Their general impression is that the effects of Clarithromycin may be also due to antibacterial action of the drug, thus requiring a search for tumor-targeted effects in these conditions. Clarithromycin significantly enhanced effect of cytostatic treatment by increasing natural killer cell activity and CD8+ T cell cytotoxicity, thus causing recovery from immunosuppression caused by the chemotherapy.
Studies on GvHD prevention
Distinct positive effects of azithromycin were shown in murine model of experimental GVHD were reported by a Japanese group [32]. Azithromycin was administered per os to recipient BALB/c mice during H-2 incompatible BMT. The treatment was performed from day -2 to day +2. As a result, the drug-treated animals exhibited significant suppression of lethal GVHD without sufficient inhibition of donor cell engraftment. Azithromycin administration was associated with mice 70% survival of transplanted animals versus death of all mice in control group. Accordingly, the typical GvHD lesions of intestinal and liver epithelium were only minimally expressed in AZM-treated animals. The authors suggest inhibition of recipient DCs as a possible cause of GVHD suppression.
Similar results were obtained by Radhakrishnan et al. [33] in lethally irradiated B6D2F1 mice in whom acute GVHD and noninfectious lung injury were induced by injection of bone marrow and spleen cells from allogeneic C57BL/6 mice. In experimental animals, azithromycin was given for a long time orally from day +14 until 6 or 14 weeks after transplantation. Generally, Azithromycin treatment resulted in improved survival and decreased lung injury, as shown by respiratory tests, and improved GvHD-associated injury of intestines and liver, depending, however, on the schedule of drug gavage.
A small clinical study with azithromycin for GVHD prophylaxis has yielded disappointing results in a randomized, placebo-controlled trial performed by Iranian group [34]. 96 patients with acute leukemia were subjected to HSCT from full-matched donors. All the patients received high-dose chemotherapy, standard immunosuppressive regimens. Azithromycin was administered 500 mg daily in 48 cases from day -6 to +12 posttransplant, and placebo was given in other 48 cases. As a result, incidence of acute GvHD grade III-IV and chronic graft-versus-host disease did not significantly differ between the two groups. Meanwhile, oral mucositis occurred in significantly lower number of patients treated with azithromycin.
Niclosamide
Niclosamide as an approved anthelmintic agent potential anticancer agent by various high-throughput screening campaigns [24]. Niclosamide not only inhibits the Wnt/β-catenin, mTORC1, STAT3, NF-κB and Notch signaling pathways, but also targets mitochondria in cancer cells. Therefore, some in vitro screening studies have shown its anticancer activity. In the study by Hamdoun et al. [23], niclosamide showed distinct suppressive effects upon cancer cell lines. Worth of note, it revealed higher activity against leukemia cell lines CCRF-CEM, CEM/ADR5000, and RPMI-8226 compared to the solid tumor cell lines. Cytocidal action of niclosamide may be associated with increase in reactive oxygen species and glutathione (GSH) in malignant cells, thus suggesting GSH synthetase (GS) as a target for niclosamide.
Salinomycin
Salinomycin is an ionophore successfully used in the patients with coccidiosis seems also to express anti-leukemic effects [22]. AML and MLLr cell lines, primary cells and patient samples were sensitive to submicromolar salinomycin. Interestingly, colony formation of normal hematopoietic cells was unaffected by salinomycin, thus promising safer usage of this drug in further clinical trials.
Antifungal drugs
Itraconazole, a common anti-fungal agent, has demonstrated potential anticancer activity, including P-glycoprotein-mediated resistance by modulating the Hedgehog signaling pathways which are a target of rapamycin and Wnt/β-catenin in cancer cells. Angiogiogenesis suppression is another known effect of itroconazole in the cancer microenvironment [35]. Small clinical trials suggested the clinical benefits of itraconazole monotherapy in different solid tumors [21].
Possible clinical effects of antibacterials due to posttransplant changes of gut microbiota
Firstly, antibacterial antibiotics, especially, for oral use, are prone for suppression of gut microbiota. E.g., Shono et al [36] have shown that some widely used antibacterials, e.g., piperacillin/tazobactam or imipenem/cilastatin are followed by higher GVHD-related death at 5 years, due to gut microflora imbalance. Therefore, an extending viewpoint suggests damaging effects of antibacterials upon normal microbiota, thus being potentially harmful to immune reconstitution after HSCT and affect clinical outcomes in the patients [37].
Conclusion
At the present time, there is a wide list of repurposed drugs potentially applicable in cancer therapy. Of course, most of these “old” drugs are tested in vitro or in pre-clinical animal models. Hundreds of the candidate compounds are subjected to screening in susceptible malignant cell lines, then treated by means of bioinformatics techniques. Only some drugs are proposed for further pre-clinical and clinical studies, thus presentibg some hopes for successful introduction of these medications within combined schedules of cancer chemotherapy.
Introduction of the “old-new” anticancer drugs should inevitably pass the step of cell culture testing, animal experiments and clinical trials, in order to confirm antitumor activities for different malignancies. Their testing for the therapy of oncohematological disorders has made a sufficient progress over last years, first of all, by in vitro screening studies of leukemic cell lines performed worldwide. The searched additional effects upon biological pathways in malignant cells may be discerned by means of functional genomics and “big data” mining technologies, thus providing comprehensive information concerning the drug targets [6]. The authors propose a novel functional concept of pharmacology implying artificial intelligence techniques for mining and knowledge discovery in “big data” providing comprehensive information about the drugs associated with activation or suppression of appropriate biological pathways. By this approach, the workers have designed indexes of optimal drugs for treatment of hypertension, analgesia, and candidate drugs for treatment of chronic lymphocytic leukemia. Likewise, the strategy provides successful selection of candidate drugs for repurposing tasks.
Conflict of interest
No conflicts of interest are reported.
References
- Dueñas-González A, García-López P, Herrera LA, Medina-Franco JL, González-Fierro A, CandelariaM. The prince and the pauper. A tale of anticancer targeted agents. Molecular Cancer 2008; 7:82 doi:10.1186/1476-4598-7-82.
- Sukhai MA, Spagnuolo PA, Weir S, Kasper J, Patton L, Schimmer AD. New sources of drugs for hematologic malignancies. Blood. 2011;117(25):6747-6755.
- Drug Repurposing Portal http://drugrepurposingportal.com/repurposed-drug-database.php
- Andresen V, Gjertsen BT. Drug repurposing for the treatment of acute myeloid leukemia. Front. Med. 2017. 4:211. doi:10.3389/fmed.2017.00211.
- Shah RR, Stonier PD. Repurposing old drugs in oncology: Opportunities with clinical and regulatory challenges ahead. J Clin Pharm Ther. 2019;44(1):6-22. doi: 10.1111/jcpt.12759.
- Lötsch J, Ultsch A. Process pharmacology: a pharmacological data science approach to drug development and therapy. CPT Pharmacometrics Syst Pharmacol. 2016 Apr;5(4):192-200. doi: 10.1002/psp4.12072.
- Ishida J, Konishi M, Ebner N, Springer J. Repurposing of approved cardiovascular drugs. J Transl Med. 2016;14:269. doi: 10.1186/s12967-016-1031-5.
- Pisanti S, Picardi P, Ciaglia E, D'Alessandro A, Bifulco M. Novel prospects of statins as therapeutic agents in cancer. Pharmacol Res. 2014;88:84-98. doi: 10.1016/j.phrs.2014.06.013.
- Vlahopoulos S, Critselis E, Voutsas IF, Perez SA, Moschovi M, Baxevanis CN, Chrousos GP. New use for old drugs? Prospective targets of chloroquines in cancer therapy. Curr Drug Targets. 2014;15(9):843-51.
- Plantone D, Koudriavtseva T. Current and future use of chloroquine and hydroxychloroquine in infectious, immune, neoplastic, and neurological diseases: A mini-review. Clin Drug Investig. 2018;38(8):653-671.
- Eriksson A, Chantzi E, Fryknäs M, Gullbo J, Nygren P, Gustafsson M, Höglund M, Larsson R. Towards repositioning of quinacrine for treatment of acute myeloid leukemia – Promising synergies and in vivo effects. Leuk Res. 2017;63:41-46. doi: 10.1016/j.leukres.2017.10.012.
- Idowu T, Schweizer F. Ubiquitous nature of fluoroquinolones: the oscillation between antibacterial and anticancer activities. Antibiotics. 2017; 6, 26; doi:10.3390/antibiotics6040026.
- Shehwaro N, Langlois AL, Gueutin V, Gauthier M, Casenave M, Izzedine H. Doxycycline or how to create new with the old? Therapie. 2014;69(2):129-141 (In French). doi: 10.2515/therapie/2013069.
- Fuoco D. Classification framework and chemical biology of tetracycline-structure-based drugs. Antibiotics 2012,1:1-13.
- Fu X, Liu W, Huang Q, Wang Y, Li H, Xiong Y. Targeting mitochondrial respiration selectively sensitizes pediatric acute lymphoblastic leukemia cell lines and patient samples to standard chemotherapy. Am J Cancer Res. 2017;7(12):2395-2405.
- Lamb R, Ozsvari B, Lisanti CL, Tanowitz HB, Howell A, Martinez-Outschoorn UE, Sotgia F, Lisanti MP. Antibiotics that target mitochondria effectively eradicate cancer stem cells, across multiple tumor types: Treating cancer like an infectious disease. Oncotarget; 2015; 6(7): 4569-4584.
- Shamoun M, Braun Th, Magenau JM, Choi SW, Reddy P, Pawarode A, Riwes MM, Kitko CL, Anand S, Ghosh M, Lugt MW, Bonifant C, Abusin G, Parkin B, Peltier D, Yanik GA.The effect of azithromycin on relapse in patients with moderate-severe chronic graft versus host disease (CGVHD). Biol Blood Marrow Transplant. 2019; 25 (Abstracts):S26-S27.
- Van Nuffel ANT, Sukhatme W, Pantziarka P, Meheus L, Sukhatme VP, Bouche G. Repurposing Drugs in Oncology (ReDO)-clarithromycin as an anti-cancer agent. ecancer 2015, 9:513 DOI: 10.3332/ecancer.2015.513
- Brüning A, Jückstock J, Kost B, Tsikouras P, Weissenbacher T, Mahner S, Mylonas I. Induction of DNA damage and apoptosis in human leukemia cells by efavirenz. Oncol Rep. 2017 ;37(1):617-621. doi: 10.3892/or.2016.5243. Epub 2016 Nov 15.
- Manzotti G, Parenti S, Ferrari-Amorotti G, Soliera AR, Cattelani S, Montanari M, Cavalli D, Ertel A, Grande A, Calabretta B. Monocyte-macrophage differentiation of acute myeloid leukemia cell lines by small molecules identified through interrogation of the Connectivity Map database. Cell Cycle. 2015; 14(16): 2578-2589.
- Pantziarka P, Sukhatme V, Bouche G, Meheus L, Sukhatme VP. Repurposing Drugs in Oncology (ReDO)- itraconazole as an anti-cancer agent. Ecancermedicalscience. 2015;9:521. doi: 10.3332/ecancer.2015.521.
- Roulston GDR, Burt CL, Kettyle LMJ, Matchett KB, Keenan HL, Mulgrew NM, RamseyJM, Dougan C, McKiernan J, Grishagin IV, Mills KI, Thompson A. Low-dose salinomycin induces anti-leukemic responses in AML and MLL. Oncotarget. 2016 7(45): 73448-73461. doi: 10.18632/oncotarget.11866.
- Hamdoun S, Jung P, Efferth T. Drug repurposing of the anthelmintic niclosamide to treat multidrug-resistant leukemia. Front Pharmacol. 2017;8:110. doi: 10.3389/fphar.2017.00110.
- Li Y, Li PK, Roberts MJ, Arend RC, Samant RS, Buchsbaum DJ. Multi-targeted therapy of cancer by niclosamide: A new application for an old drug. Cancer Lett. 2014;349(1):8-14. doi: 10.1016/j.canlet.2014.04.003.
- Wang F, Liu Z, Zeng J, Zhu H, Li J, Cheng X, et al. Metformin synergistically sensitizes FLT3-ITD-positive acute myeloid leukemia to sorafenib by promoting mTOR-mediated apoptosis and autophagy. Leuk Res. 2015; 39:1421–1427. doi:10.1016/j.leukres.2015.09.016.
- Sabnis HS, Bradley HL, Tripathi S, Yu WM, Tse W, Qu CK, et al. Synergistic cell death in FLT3-ITD positive acute myeloid leukemia by combined treatment with metformin and 6-benzylthioinosine. Leuk Res. 2016; 50:132–140. oi:10.1016/j.leukres.2016.10.004.
- Reed GA, Schiller GJ, Kambhampati S Tallman MS, Douer Dan, Minden MD, Yee KW, Gupta V, Brandwein J, Jitkova Yu, Gronda M, Hurren R, Shamas-Din A, Schuh AC, Skrtic M, Sriskanthadevan S, Jhas B, Gebbia M, Wang X, Wang Z, et al. 2011. Inhibition of mitochondrial translation as a therapeutic strategy for human acute myeloid leukemia. Cancer Cell; 20:674-688.
- Skrtić M, Sriskanthadevan S, Jhas B, Gebbia M, Wang X, Wang Z, Hurren R, Jitkova Y, Gronda M, Maclean N, Lai CK, Eberhard Y, Bartoszko J, Spagnuolo P, Rutledge AC, Datti A, Ketela T, Moffat J, Robinson BH, Cameron JH, Wrana J, Eaves CJ, Minden MD, Wang JC, Dick JE, Humphries K, Nislow C, Giaever G, Schimmer AD. Inhibition of mitochondrial translation as a therapeutic strategy for human acute myeloid leukemia. Cancer Cell. 2011; 20(5):674-88. doi: 10.1016/j.ccr.2011.10.015.
- Schimmer AD. A phase 1 study of intravenous infusions of tigecycline in patients with acute myeloid leukemia. Cancer Medicine, 2016; 5(11):3031-3040.
- Ferreri AJ, Ponzoni M, Guidoboni M, Resti AG, Politi LS, Cortelazzo S, Demeter J, Zallio F, Palmas A, Muti G, Dognini GP, Pasini E, Lettini AA, Sacchetti F, De Conciliis C, Doglioni C, Dolcetti R. Bacteria-eradicating therapy with doxycycline in ocular adnexal MALT lymphoma: a multicenter prospective trial. J Natl Cancer Inst. 2006; 98(19): 1375-1382.
- Sassa K, Mizushima Y, Fujishita T, Oosaki R, Kobayashi M. Therapeutic effect of clarithromycin on a transplanted tumor in rats. Antimicrob Agents Chemother. 1999;43(1):67-72.
- Iwamoto S., Azuma E., Kumamoto T., Hirayama M., Yoshida T., Ito M., Amano K., Ido M., Komada Y. Efficacy of azithromycin in preventing lethal graft-versus-host disease. Clinical and Experimental Immunology, 2012;171:338-345.
- Radhakrishnan SV, Palaniyandi S, Mueller G, Miklos S, Hager M, Spacenko E, Karlsson FG, Huber E, Kittan NA, Hildebrandt GC. Preventive azithromycin treatment reduces noninfectious lung injury and acute graft-versus-host disease in a murine model of allogeneic hematopoietic cell transplantation. Biol Blood Marrow Transplant. 2015;21:30-38.
- Barkhordar M, Mohammadi M, Hadjibabaie M, Ghavamzadeh A. SupplAzithromycin for prevention of graft-versus-host disease: A randomized placebo-controlled trial. Int J Hematol Oncol Stem Cell Res. 2018;12(2):77-83.
- Tsubamoto H, Ueda T, Inoue K, Sakata K, Shibahara H, Sonoda T. Repurposing itraconazole as an anticancer agent. Oncol Lett. 2017;14(2):1240-1246. doi: 10.3892/ol.2017.6325.
- Shono Y, Docampo MD, Peled JU, Perobelli SM, Velardi E, Tsai JJ, Slingerland AE, Smith OM, Young LF, Gupta J, Lieberman SR, Jay HV, Ahr KF, Porosnicu Rodriguez KA, Xu K, Calarfiore M, Poeck H, Caballero S, Devlin SM, Rapaport F, Dudakov JA, Hanash AM, Gyurkocza B, Murphy GF, Gomes C, Liu C, Moss EL, Falconer SB, Bhatt AS, Taur Y, Pamer EG, van den Brink MRM, Jenq RR. Increased GVHD-related mortality with broad-spectrum antibiotic use after allogeneic hematopoietic stem cell transplantation in human patients and mice. Sci Transl Med. 2016 May 18; 8(339): 339ra71.
- Goloshchapov OV, Kucher MA, Chukhlovin AB. Gut microbiome in hematopoietic stem cell transplantation: patient and treatment-related factors. Cell Ther Transpant. 2018; 7(4): 16-28.
Introduction
Additional therapeutic effects of “old”, drugs for novel clini-cal indications have been studied over last decades. Novel suggestions for repurposing of different medical drugs for cancer treatment have been made over recent years [1, 2].
There are three main reasons for these proposals: (1) limited efficiency of novel inhibitors or specific monoclonal antibodies targeted for oncogene-specific molecules; (2) new molecular targets were revealed for some drugs traditionally used to other therapeutic purposes; and (3) eventual decline of development costs for the new therapies performed by the “old” drugs.
A variety of drugs used in different somatic disorders is now considered as complementary tool for treatment of malignancies. These candidate compounds are listed in several indexes available online, e.g., the Drug Repurposing Portal supported by Excelra [3]. In addition, a number of recent review articles concern different aspects of old drug applications in cancer therapy [1, 4, 5].
It should be noted, however, that most cytostatic and anticancer effects of the repurposed drugs are shown in the in vitro models, or in experimental animals, thus suggesting a long way until their clinical implication. The big data collected from drug screening in different models are analyzed by different bioinformatic approaches, e.g. [6], thus accelerating the drug selection process to some degree.
The specific aim of our study was to discuss probable anticancer effects of some anti-infectious drugs which are now widely used in hematopoietic stem cell transplantation protocols.
Some candidate drugs intended for repurposing in cancer treatment are listed in Table 1.
Table 1. Summary of drugs used for treatment of common disorders, their primary indication, non-cancer and cancer targets


Drug repositioning for leukemia treatment
Metformin
This well-known anti-diabetic drug activates the AMF-regulated protein kinase pathway dependent on the tumor suppressor LKB1. The LKB1/AMPK signaling may be suppressed by ERK which is activated in a half of acute myeloid leukemia (AML) cases with appropriate mutations, e.g., FLT3-ITD mutation. These cases may be susceptible for metformin and the treatment efficiency may be increased in combination with sorafenib or other novel drugs [25, 26].
Chloroquines
Pre-clinical studies of the last decade have repeatedly confirmed distinct anticancer effects of well-known antimalarial drug chloroquine and its derivatives. In particular, chloroquine and hydroxychloroquine have relatively well-characterized toxicity profiles. Previously published review articles provide an excellent overview on diversity of chloroquine effects on cancer cells, both in the cell culture as well as on human tumors grafted into mice; and suggest incorporation of hydroxychloroquine in prospective combination schemes for clinical studies [9]. The authors discuss some common features in cancer cells that could be targeted by quinacrine and its derivatives, aiming for potential pharmaceutical intervention in oncology.
A recent work by Eriksson et al. [11] dealt with more specific quinacrine effects upon malignant blood cells. The authors have earlier selected quinacrine as the most plausible compound for its antileukemic effects, and tested this drug in vitro in combination with some common cytostatic agents (daunorubicin, cytarabine, azacitidine, etc.). Acute myeloid leukemia (AML) cell lines were cultured as a target population, then tested for cytotoxicity by fluorometric microculture. In most in vitro systems, the workers have shown distinct synergism between quinacrine and cytarabine, or azacitidine added to these cell cultures. Moreover, the in vivo usage of quinacrine (100 mg/kg, six injections for two weeks) in SCID mice bearing human AML cells caused a significant decrease in circulating blast cells and increased the median survival time of the animals. Hence, further studies may offer an “old-new”, less toxic drug for combined treatment of leukemia.
Fluoroquinolones
Quinolone-based antibiotics, especially, fluoroquinolones are used over decades to manage different bacterial and protozoal infections. Their microbicidal action is caused by inhibition of the ligase domain of the type II DNA topoisomerase, thus releasing endonuclease activities and irreversible DNA decay in the target cells, as reviewed by Idowu and Schweizer [12]. Such a universal cytotoxic effect presumes possible applications of fluoroquinolones for cancer treatment. These studies, however, are still in progress and should be substantiated in pre-clinical trials.
Tetracycline, and its derivatives
This class of antibacterials is known since 1948. Tetracyclines are widely used in medicine and agriculture to combat broad spectrum of bacteria [14]. Despite high proportion of tetracyclin-resistant microorganisms (due to powerful drug efflux), a new generation of these drugs was developed later on (e.g., Doxycycline, Tigecycline) which are now administered for empiric treatment, e.g., in immunocompromised patients following severe cytostatic treatment and bone marrow transplantation. Interestingly, doxorubicin, a popular anticancer antibiotic belongs to the same family of bioactive compounds.
All the tetracyclines inhibit protein assembly in Gram(+) and Gram(-) microbes by preventing the aminoacyl-tRNA binding to the acceptor sites at the ribosomes. Meanwhile, tetracyclines were also tested for treatment of a number of inflammatory diseases, due to their inhibition of matrix metalloproteinases, antiapoptotic, antioxidative, and antiinflammatory effects in humans [14].
Hence, the major antimicrobial effect of tetracyclines is due to their protein-inhibiting actions in bacteria. Moreover, they possess antiproliferative and pro-apoptotic effects in mammalian cancer cells, by suppressing mitochondrial ribosomes and energy metabolism [16]. More recently, they are also considered potential anticancer drugs. E.g., Tigecycline a structural homologue of tetracycline, being a potent glycylcycline antibiotic, is mostly used as a broad-spectrum drug against gram-positive and gram-negative pathogens. It reversibly binds the 30S subunit of the bacterial ribosomes, being also an inhibitor of mitochondrial biogenesis [27].
Ten malignant tumor cell lines of different origin were tested in vitro with tigecycline and doxycycline (another tetracycline derivative), showing. Tigecycline has shown its ability to inhibit the MCF7 and T47D spheroid cell growth, at the concentrations from 10 µM to 50 µM [16]. Moreover, tigecycline was previously shown to kill human AML differentiated blasts as well as leukemic stem cells in vitro and in vivo by blocking mitochondrial protein synthesis [28].
Another work concerned in vitro cytostatic effects of tigecycline on the acute lymphoblastic leukemia (ALL) showing decreased survival and suppression of clonogenic growth in malignant cell cultures [29]. Toxic effects upon normal hematopoietic cells were less pronounced. Pharmacokinetics and potential antitumor effects make this drug a promising option when sensitizing ALL cells for chemotherapy [30].
In particular, tigecycline was studied in the Phase 1 dose-escalation study of tigecycline administered intravenously daily 5 of 7 days for 2 weeks to patients with AML. A total of 27 adult patients with relapsed and refractory AML were enrolled [27]. The authors have shown relative safety and assessed maximal tolerable doses for the drug infused into the patients with relapsed/refractory AML, however, with no evident anticancer effects revealed.
Moreover, some small clinical trials with doxycycline were performed over last years in cancer clinics (primarily aiming for infection therapy, but not cancer treatment) showing some antitumor effects in cancer patients as reviewed by Lamb et al. [16]. Initial positive results of doxycycline trials obtained in advanced or treatment-resistant cases of B-cell lymphoma [30]. This clinical effect was not, however, confirmed in more extensive studies.
Erythromycin and other macrolides
These antibacterials may also inhibit various microflora by suppressing ribosome functions. Similarly, they can inhibit mitochondrial ribosomes in eukaryotic cells, as shown in several cancer cell lines [16]. Azithromycin is an improved erythromycin derivative which is widely used in post-transplant patients, being more slowly eliminated than erythromycin. Its anti-infectious effect is exploited for prevention of bacterial complications in chronic infectious conditions, e.g., at later terms post-HSCT.
Surprisingly, a probable antitumor effect of azithromycin was revealed in a study by Shamoun et al. [17] published as a short abstract, where a long-term drug administration (14 days) aimed to ameliorate chronic graft-versus-graft disease (GvHD) was accompanied by decreased rates of relapse and improved survivals in a combined group of with acute leukemia, MDS, malignant lymphomas, and chronic leukemia patients.
Clarithromycin (6-O-methyl erythromycin) is also a widely used semi-synthetic macrolide drug which also has previously shown a sufficient anticancer activity against some experimental tumors [31] when used after a course of cancer chemotherapy in mice.
A recent review by van Nuffel et al. [18] has summarized numerous data obtained in human studies showing complementary effects of clarithromycin as an antibacterial drug in combined treatment of multiple myeloma, CML and other blood malignancies, especially MALT lymphomas and Hodgkin’s disease studied over last 2 decades. Their general impression is that the effects of Clarithromycin may be also due to antibacterial action of the drug, thus requiring a search for tumor-targeted effects in these conditions. Clarithromycin significantly enhanced effect of cytostatic treatment by increasing natural killer cell activity and CD8+ T cell cytotoxicity, thus causing recovery from immunosuppression caused by the chemotherapy.
Studies on GvHD prevention
Distinct positive effects of azithromycin were shown in murine model of experimental GVHD were reported by a Japanese group [32]. Azithromycin was administered per os to recipient BALB/c mice during H-2 incompatible BMT. The treatment was performed from day -2 to day +2. As a result, the drug-treated animals exhibited significant suppression of lethal GVHD without sufficient inhibition of donor cell engraftment. Azithromycin administration was associated with mice 70% survival of transplanted animals versus death of all mice in control group. Accordingly, the typical GvHD lesions of intestinal and liver epithelium were only minimally expressed in AZM-treated animals. The authors suggest inhibition of recipient DCs as a possible cause of GVHD suppression.
Similar results were obtained by Radhakrishnan et al. [33] in lethally irradiated B6D2F1 mice in whom acute GVHD and noninfectious lung injury were induced by injection of bone marrow and spleen cells from allogeneic C57BL/6 mice. In experimental animals, azithromycin was given for a long time orally from day +14 until 6 or 14 weeks after transplantation. Generally, Azithromycin treatment resulted in improved survival and decreased lung injury, as shown by respiratory tests, and improved GvHD-associated injury of intestines and liver, depending, however, on the schedule of drug gavage.
A small clinical study with azithromycin for GVHD prophylaxis has yielded disappointing results in a randomized, placebo-controlled trial performed by Iranian group [34]. 96 patients with acute leukemia were subjected to HSCT from full-matched donors. All the patients received high-dose chemotherapy, standard immunosuppressive regimens. Azithromycin was administered 500 mg daily in 48 cases from day -6 to +12 posttransplant, and placebo was given in other 48 cases. As a result, incidence of acute GvHD grade III-IV and chronic graft-versus-host disease did not significantly differ between the two groups. Meanwhile, oral mucositis occurred in significantly lower number of patients treated with azithromycin.
Niclosamide
Niclosamide as an approved anthelmintic agent potential anticancer agent by various high-throughput screening campaigns [24]. Niclosamide not only inhibits the Wnt/β-catenin, mTORC1, STAT3, NF-κB and Notch signaling pathways, but also targets mitochondria in cancer cells. Therefore, some in vitro screening studies have shown its anticancer activity. In the study by Hamdoun et al. [23], niclosamide showed distinct suppressive effects upon cancer cell lines. Worth of note, it revealed higher activity against leukemia cell lines CCRF-CEM, CEM/ADR5000, and RPMI-8226 compared to the solid tumor cell lines. Cytocidal action of niclosamide may be associated with increase in reactive oxygen species and glutathione (GSH) in malignant cells, thus suggesting GSH synthetase (GS) as a target for niclosamide.
Salinomycin
Salinomycin is an ionophore successfully used in the patients with coccidiosis seems also to express anti-leukemic effects [22]. AML and MLLr cell lines, primary cells and patient samples were sensitive to submicromolar salinomycin. Interestingly, colony formation of normal hematopoietic cells was unaffected by salinomycin, thus promising safer usage of this drug in further clinical trials.
Antifungal drugs
Itraconazole, a common anti-fungal agent, has demonstrated potential anticancer activity, including P-glycoprotein-mediated resistance by modulating the Hedgehog signaling pathways which are a target of rapamycin and Wnt/β-catenin in cancer cells. Angiogiogenesis suppression is another known effect of itroconazole in the cancer microenvironment [35]. Small clinical trials suggested the clinical benefits of itraconazole monotherapy in different solid tumors [21].
Possible clinical effects of antibacterials due to posttransplant changes of gut microbiota
Firstly, antibacterial antibiotics, especially, for oral use, are prone for suppression of gut microbiota. E.g., Shono et al [36] have shown that some widely used antibacterials, e.g., piperacillin/tazobactam or imipenem/cilastatin are followed by higher GVHD-related death at 5 years, due to gut microflora imbalance. Therefore, an extending viewpoint suggests damaging effects of antibacterials upon normal microbiota, thus being potentially harmful to immune reconstitution after HSCT and affect clinical outcomes in the patients [37].
Conclusion
At the present time, there is a wide list of repurposed drugs potentially applicable in cancer therapy. Of course, most of these “old” drugs are tested in vitro or in pre-clinical animal models. Hundreds of the candidate compounds are subjected to screening in susceptible malignant cell lines, then treated by means of bioinformatics techniques. Only some drugs are proposed for further pre-clinical and clinical studies, thus presentibg some hopes for successful introduction of these medications within combined schedules of cancer chemotherapy.
Introduction of the “old-new” anticancer drugs should inevitably pass the step of cell culture testing, animal experiments and clinical trials, in order to confirm antitumor activities for different malignancies. Their testing for the therapy of oncohematological disorders has made a sufficient progress over last years, first of all, by in vitro screening studies of leukemic cell lines performed worldwide. The searched additional effects upon biological pathways in malignant cells may be discerned by means of functional genomics and “big data” mining technologies, thus providing comprehensive information concerning the drug targets [6]. The authors propose a novel functional concept of pharmacology implying artificial intelligence techniques for mining and knowledge discovery in “big data” providing comprehensive information about the drugs associated with activation or suppression of appropriate biological pathways. By this approach, the workers have designed indexes of optimal drugs for treatment of hypertension, analgesia, and candidate drugs for treatment of chronic lymphocytic leukemia. Likewise, the strategy provides successful selection of candidate drugs for repurposing tasks.
Conflict of interest
No conflicts of interest are reported.
References
- Dueñas-González A, García-López P, Herrera LA, Medina-Franco JL, González-Fierro A, CandelariaM. The prince and the pauper. A tale of anticancer targeted agents. Molecular Cancer 2008; 7:82 doi:10.1186/1476-4598-7-82.
- Sukhai MA, Spagnuolo PA, Weir S, Kasper J, Patton L, Schimmer AD. New sources of drugs for hematologic malignancies. Blood. 2011;117(25):6747-6755.
- Drug Repurposing Portal http://drugrepurposingportal.com/repurposed-drug-database.php
- Andresen V, Gjertsen BT. Drug repurposing for the treatment of acute myeloid leukemia. Front. Med. 2017. 4:211. doi:10.3389/fmed.2017.00211.
- Shah RR, Stonier PD. Repurposing old drugs in oncology: Opportunities with clinical and regulatory challenges ahead. J Clin Pharm Ther. 2019;44(1):6-22. doi: 10.1111/jcpt.12759.
- Lötsch J, Ultsch A. Process pharmacology: a pharmacological data science approach to drug development and therapy. CPT Pharmacometrics Syst Pharmacol. 2016 Apr;5(4):192-200. doi: 10.1002/psp4.12072.
- Ishida J, Konishi M, Ebner N, Springer J. Repurposing of approved cardiovascular drugs. J Transl Med. 2016;14:269. doi: 10.1186/s12967-016-1031-5.
- Pisanti S, Picardi P, Ciaglia E, D'Alessandro A, Bifulco M. Novel prospects of statins as therapeutic agents in cancer. Pharmacol Res. 2014;88:84-98. doi: 10.1016/j.phrs.2014.06.013.
- Vlahopoulos S, Critselis E, Voutsas IF, Perez SA, Moschovi M, Baxevanis CN, Chrousos GP. New use for old drugs? Prospective targets of chloroquines in cancer therapy. Curr Drug Targets. 2014;15(9):843-51.
- Plantone D, Koudriavtseva T. Current and future use of chloroquine and hydroxychloroquine in infectious, immune, neoplastic, and neurological diseases: A mini-review. Clin Drug Investig. 2018;38(8):653-671.
- Eriksson A, Chantzi E, Fryknäs M, Gullbo J, Nygren P, Gustafsson M, Höglund M, Larsson R. Towards repositioning of quinacrine for treatment of acute myeloid leukemia – Promising synergies and in vivo effects. Leuk Res. 2017;63:41-46. doi: 10.1016/j.leukres.2017.10.012.
- Idowu T, Schweizer F. Ubiquitous nature of fluoroquinolones: the oscillation between antibacterial and anticancer activities. Antibiotics. 2017; 6, 26; doi:10.3390/antibiotics6040026.
- Shehwaro N, Langlois AL, Gueutin V, Gauthier M, Casenave M, Izzedine H. Doxycycline or how to create new with the old? Therapie. 2014;69(2):129-141 (In French). doi: 10.2515/therapie/2013069.
- Fuoco D. Classification framework and chemical biology of tetracycline-structure-based drugs. Antibiotics 2012,1:1-13.
- Fu X, Liu W, Huang Q, Wang Y, Li H, Xiong Y. Targeting mitochondrial respiration selectively sensitizes pediatric acute lymphoblastic leukemia cell lines and patient samples to standard chemotherapy. Am J Cancer Res. 2017;7(12):2395-2405.
- Lamb R, Ozsvari B, Lisanti CL, Tanowitz HB, Howell A, Martinez-Outschoorn UE, Sotgia F, Lisanti MP. Antibiotics that target mitochondria effectively eradicate cancer stem cells, across multiple tumor types: Treating cancer like an infectious disease. Oncotarget; 2015; 6(7): 4569-4584.
- Shamoun M, Braun Th, Magenau JM, Choi SW, Reddy P, Pawarode A, Riwes MM, Kitko CL, Anand S, Ghosh M, Lugt MW, Bonifant C, Abusin G, Parkin B, Peltier D, Yanik GA.The effect of azithromycin on relapse in patients with moderate-severe chronic graft versus host disease (CGVHD). Biol Blood Marrow Transplant. 2019; 25 (Abstracts):S26-S27.
- Van Nuffel ANT, Sukhatme W, Pantziarka P, Meheus L, Sukhatme VP, Bouche G. Repurposing Drugs in Oncology (ReDO)-clarithromycin as an anti-cancer agent. ecancer 2015, 9:513 DOI: 10.3332/ecancer.2015.513
- Brüning A, Jückstock J, Kost B, Tsikouras P, Weissenbacher T, Mahner S, Mylonas I. Induction of DNA damage and apoptosis in human leukemia cells by efavirenz. Oncol Rep. 2017 ;37(1):617-621. doi: 10.3892/or.2016.5243. Epub 2016 Nov 15.
- Manzotti G, Parenti S, Ferrari-Amorotti G, Soliera AR, Cattelani S, Montanari M, Cavalli D, Ertel A, Grande A, Calabretta B. Monocyte-macrophage differentiation of acute myeloid leukemia cell lines by small molecules identified through interrogation of the Connectivity Map database. Cell Cycle. 2015; 14(16): 2578-2589.
- Pantziarka P, Sukhatme V, Bouche G, Meheus L, Sukhatme VP. Repurposing Drugs in Oncology (ReDO)- itraconazole as an anti-cancer agent. Ecancermedicalscience. 2015;9:521. doi: 10.3332/ecancer.2015.521.
- Roulston GDR, Burt CL, Kettyle LMJ, Matchett KB, Keenan HL, Mulgrew NM, RamseyJM, Dougan C, McKiernan J, Grishagin IV, Mills KI, Thompson A. Low-dose salinomycin induces anti-leukemic responses in AML and MLL. Oncotarget. 2016 7(45): 73448-73461. doi: 10.18632/oncotarget.11866.
- Hamdoun S, Jung P, Efferth T. Drug repurposing of the anthelmintic niclosamide to treat multidrug-resistant leukemia. Front Pharmacol. 2017;8:110. doi: 10.3389/fphar.2017.00110.
- Li Y, Li PK, Roberts MJ, Arend RC, Samant RS, Buchsbaum DJ. Multi-targeted therapy of cancer by niclosamide: A new application for an old drug. Cancer Lett. 2014;349(1):8-14. doi: 10.1016/j.canlet.2014.04.003.
- Wang F, Liu Z, Zeng J, Zhu H, Li J, Cheng X, et al. Metformin synergistically sensitizes FLT3-ITD-positive acute myeloid leukemia to sorafenib by promoting mTOR-mediated apoptosis and autophagy. Leuk Res. 2015; 39:1421–1427. doi:10.1016/j.leukres.2015.09.016.
- Sabnis HS, Bradley HL, Tripathi S, Yu WM, Tse W, Qu CK, et al. Synergistic cell death in FLT3-ITD positive acute myeloid leukemia by combined treatment with metformin and 6-benzylthioinosine. Leuk Res. 2016; 50:132–140. oi:10.1016/j.leukres.2016.10.004.
- Reed GA, Schiller GJ, Kambhampati S Tallman MS, Douer Dan, Minden MD, Yee KW, Gupta V, Brandwein J, Jitkova Yu, Gronda M, Hurren R, Shamas-Din A, Schuh AC, Skrtic M, Sriskanthadevan S, Jhas B, Gebbia M, Wang X, Wang Z, et al. 2011. Inhibition of mitochondrial translation as a therapeutic strategy for human acute myeloid leukemia. Cancer Cell; 20:674-688.
- Skrtić M, Sriskanthadevan S, Jhas B, Gebbia M, Wang X, Wang Z, Hurren R, Jitkova Y, Gronda M, Maclean N, Lai CK, Eberhard Y, Bartoszko J, Spagnuolo P, Rutledge AC, Datti A, Ketela T, Moffat J, Robinson BH, Cameron JH, Wrana J, Eaves CJ, Minden MD, Wang JC, Dick JE, Humphries K, Nislow C, Giaever G, Schimmer AD. Inhibition of mitochondrial translation as a therapeutic strategy for human acute myeloid leukemia. Cancer Cell. 2011; 20(5):674-88. doi: 10.1016/j.ccr.2011.10.015.
- Schimmer AD. A phase 1 study of intravenous infusions of tigecycline in patients with acute myeloid leukemia. Cancer Medicine, 2016; 5(11):3031-3040.
- Ferreri AJ, Ponzoni M, Guidoboni M, Resti AG, Politi LS, Cortelazzo S, Demeter J, Zallio F, Palmas A, Muti G, Dognini GP, Pasini E, Lettini AA, Sacchetti F, De Conciliis C, Doglioni C, Dolcetti R. Bacteria-eradicating therapy with doxycycline in ocular adnexal MALT lymphoma: a multicenter prospective trial. J Natl Cancer Inst. 2006; 98(19): 1375-1382.
- Sassa K, Mizushima Y, Fujishita T, Oosaki R, Kobayashi M. Therapeutic effect of clarithromycin on a transplanted tumor in rats. Antimicrob Agents Chemother. 1999;43(1):67-72.
- Iwamoto S., Azuma E., Kumamoto T., Hirayama M., Yoshida T., Ito M., Amano K., Ido M., Komada Y. Efficacy of azithromycin in preventing lethal graft-versus-host disease. Clinical and Experimental Immunology, 2012;171:338-345.
- Radhakrishnan SV, Palaniyandi S, Mueller G, Miklos S, Hager M, Spacenko E, Karlsson FG, Huber E, Kittan NA, Hildebrandt GC. Preventive azithromycin treatment reduces noninfectious lung injury and acute graft-versus-host disease in a murine model of allogeneic hematopoietic cell transplantation. Biol Blood Marrow Transplant. 2015;21:30-38.
- Barkhordar M, Mohammadi M, Hadjibabaie M, Ghavamzadeh A. SupplAzithromycin for prevention of graft-versus-host disease: A randomized placebo-controlled trial. Int J Hematol Oncol Stem Cell Res. 2018;12(2):77-83.
- Tsubamoto H, Ueda T, Inoue K, Sakata K, Shibahara H, Sonoda T. Repurposing itraconazole as an anticancer agent. Oncol Lett. 2017;14(2):1240-1246. doi: 10.3892/ol.2017.6325.
- Shono Y, Docampo MD, Peled JU, Perobelli SM, Velardi E, Tsai JJ, Slingerland AE, Smith OM, Young LF, Gupta J, Lieberman SR, Jay HV, Ahr KF, Porosnicu Rodriguez KA, Xu K, Calarfiore M, Poeck H, Caballero S, Devlin SM, Rapaport F, Dudakov JA, Hanash AM, Gyurkocza B, Murphy GF, Gomes C, Liu C, Moss EL, Falconer SB, Bhatt AS, Taur Y, Pamer EG, van den Brink MRM, Jenq RR. Increased GVHD-related mortality with broad-spectrum antibiotic use after allogeneic hematopoietic stem cell transplantation in human patients and mice. Sci Transl Med. 2016 May 18; 8(339): 339ra71.
- Goloshchapov OV, Kucher MA, Chukhlovin AB. Gut microbiome in hematopoietic stem cell transplantation: patient and treatment-related factors. Cell Ther Transpant. 2018; 7(4): 16-28.
Алексей Б. Чухловин
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20994" ["VALUE"]=> array(2) { ["TEXT"]=> string(356) "<p>НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия<p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(344) "
НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20995" ["VALUE"]=> array(2) { ["TEXT"]=> string(4025) "<p style="text-align: justify;">В течение последнего десятилетия появился целый ряд исследований, касающихся возможного применения «старых» медицинских препаратов в качестве дополнительных средств для лечения злокачественных новообразований. Есть следующие главные причины подобного расширения показаний для этих препаратов: (1) ограниченная эффективность и высокая стоимость новых таргетных ингибиторов онкогенных белков, или моноклональных антител для терапии; (2) выявление новых молекулярных мишеней для ряда препаратов, ранее внедренных по другим показаниям; (3) существенное снижение затрат на разработку новых средств терапии, осуществляемой «старыми» препаратами. Перечень таких «перенацеленных» препаратов сейчас включает десятки лекарств, которые часто используются, в частности, для лечения сердечно-сосудистых заболеваний, сахарного диабета, эпилепсии, различных воспалительных заболеваний. Данный обзор касается, главным образом, «переназначения» антиинфекционных препаратов, в т.ч. тех, которые используются для профилактики и лечения инфекционных осложнений, возникающих при цитостатической терапии лейкозов и лимфом, в частности – тетрациклинов, производных эритромицина, а также фторхинолонов, антивирусных препаратов и др. Противоопухолевые эффекты этих препаратов-кандидатов для «переназначение» были показаны при скрининге их цитостатических эффектов на линиях лейкозных и других злокачественных клеток. Некоторые исследования проведены на экспериментальных животных-опухоленосителях. Немногие клинические испытания были проведеныe в группах пациентов с лейкозами и лимфомами после трансплантации гемопоэтических стволовых клеток (ТГСК), которые показали некоторые позитивные эффекты антибактериальных препаратов в плане профилактики реакции «трансплантат против хозяина» (РТПХ) или увеличения продолжительности жизни пациентов. В этих целях необходимы контролируемые клинические исследования часто применяемых антиинфекционных препаратов. <p> <h2>Ключевые слова</h2> <p style="text-align: justify;">Антибактериальные препараты, переназначение, противоопухолевые эффекты, терапия лейкозов, трансплантация гемопоэтических стволовых клеток.</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3969) "
В течение последнего десятилетия появился целый ряд исследований, касающихся возможного применения «старых» медицинских препаратов в качестве дополнительных средств для лечения злокачественных новообразований. Есть следующие главные причины подобного расширения показаний для этих препаратов: (1) ограниченная эффективность и высокая стоимость новых таргетных ингибиторов онкогенных белков, или моноклональных антител для терапии; (2) выявление новых молекулярных мишеней для ряда препаратов, ранее внедренных по другим показаниям; (3) существенное снижение затрат на разработку новых средств терапии, осуществляемой «старыми» препаратами. Перечень таких «перенацеленных» препаратов сейчас включает десятки лекарств, которые часто используются, в частности, для лечения сердечно-сосудистых заболеваний, сахарного диабета, эпилепсии, различных воспалительных заболеваний. Данный обзор касается, главным образом, «переназначения» антиинфекционных препаратов, в т.ч. тех, которые используются для профилактики и лечения инфекционных осложнений, возникающих при цитостатической терапии лейкозов и лимфом, в частности – тетрациклинов, производных эритромицина, а также фторхинолонов, антивирусных препаратов и др. Противоопухолевые эффекты этих препаратов-кандидатов для «переназначение» были показаны при скрининге их цитостатических эффектов на линиях лейкозных и других злокачественных клеток. Некоторые исследования проведены на экспериментальных животных-опухоленосителях. Немногие клинические испытания были проведеныe в группах пациентов с лейкозами и лимфомами после трансплантации гемопоэтических стволовых клеток (ТГСК), которые показали некоторые позитивные эффекты антибактериальных препаратов в плане профилактики реакции «трансплантат против хозяина» (РТПХ) или увеличения продолжительности жизни пациентов. В этих целях необходимы контролируемые клинические исследования часто применяемых антиинфекционных препаратов.
Ключевые слова
Антибактериальные препараты, переназначение, противоопухолевые эффекты, терапия лейкозов, трансплантация гемопоэтических стволовых клеток.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20976" ["VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-12-19" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-12-19" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20977" ["VALUE"]=> array(2) { ["TEXT"]=> string(39) "<p>Alexey B. Chukhlovin <p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(27) "Alexey B. Chukhlovin
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20978" ["VALUE"]=> array(2) { ["TEXT"]=> string(197) "<p>R.Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(185) "
R.Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20979" ["VALUE"]=> array(2) { ["TEXT"]=> string(1941) "<p style="text-align: justify;">Over last decade, a number of studies has concerned possible implications of “old” medical drugs, as additional tools for cancer treatment. The main reasons for extension of drug indications are as follows: (1) limited efficiency or high costs of targeted oncogene protein inhibitors or specific monoclonal antibodies for therapy; (2) new molecular targets were revealed for some drugs traditionally used to other therapeutic purposes; and (3) sufficient decline of development costs for the new therapies performed by the “old” drugs. The list of such repurposed drugs now includes dozens of medications commonly used for treatment of cardiovascular diseases, diabetes mellitus, epilepsia, different inflammatory disorders. The present review deals, mainly, repurposing of anti-infectious drugs, including those used in prevention and management of infectious complications occurring in cytostatic therapy of leukemia and lymphomas, e.g., tetracyclines, erythromycin derivatives, as well as fluoroquinolones, antiviral compounds etc. <br> The antitumor effects were of these candidates for repurposing were demonstrated upon screening of their cytostatic effects in leukemic and other cancer cell lines. Some studies were performed in experimental tumor-bearing animals. Only few clinical trials were carried out in patients with leukemias and lymphomas following hematopoietic stem cell transplantation (HSCT), which showed some positive effects of antibacterial drugs in terms of graft-versus-host disease (GvHD) prevention, or prolonged survival of the patients. Controlled clinical trials of common anti-infectious drugs are required for this repurposing.</p> <h2>Keywords</h2> <p style="text-align: justify;">Antibacterial drugs, repurposing, anticancer effects, leukemia treatment, hematopoietic stem cell transplantation. </p> " ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1879) "Over last decade, a number of studies has concerned possible implications of “old” medical drugs, as additional tools for cancer treatment. The main reasons for extension of drug indications are as follows: (1) limited efficiency or high costs of targeted oncogene protein inhibitors or specific monoclonal antibodies for therapy; (2) new molecular targets were revealed for some drugs traditionally used to other therapeutic purposes; and (3) sufficient decline of development costs for the new therapies performed by the “old” drugs. The list of such repurposed drugs now includes dozens of medications commonly used for treatment of cardiovascular diseases, diabetes mellitus, epilepsia, different inflammatory disorders. The present review deals, mainly, repurposing of anti-infectious drugs, including those used in prevention and management of infectious complications occurring in cytostatic therapy of leukemia and lymphomas, e.g., tetracyclines, erythromycin derivatives, as well as fluoroquinolones, antiviral compounds etc.
The antitumor effects were of these candidates for repurposing were demonstrated upon screening of their cytostatic effects in leukemic and other cancer cell lines. Some studies were performed in experimental tumor-bearing animals. Only few clinical trials were carried out in patients with leukemias and lymphomas following hematopoietic stem cell transplantation (HSCT), which showed some positive effects of antibacterial drugs in terms of graft-versus-host disease (GvHD) prevention, or prolonged survival of the patients. Controlled clinical trials of common anti-infectious drugs are required for this repurposing.
Keywords
Antibacterial drugs, repurposing, anticancer effects, leukemia treatment, hematopoietic stem cell transplantation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20980" ["VALUE"]=> string(83) "Drug repurposing in leukemia treatment and hematopoietic stem cell transplantation " ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(83) "Drug repurposing in leukemia treatment and hematopoietic stem cell transplantation " ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20996" ["VALUE"]=> string(4) "1563" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1563" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20981" ["VALUE"]=> string(4) "1562" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1562" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(12) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20977" ["VALUE"]=> array(2) { ["TEXT"]=> string(39) "<p>Alexey B. Chukhlovin <p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(27) "Alexey B. Chukhlovin
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(27) "
Alexey B. Chukhlovin
" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20979" ["VALUE"]=> array(2) { ["TEXT"]=> string(1941) "<p style="text-align: justify;">Over last decade, a number of studies has concerned possible implications of “old” medical drugs, as additional tools for cancer treatment. The main reasons for extension of drug indications are as follows: (1) limited efficiency or high costs of targeted oncogene protein inhibitors or specific monoclonal antibodies for therapy; (2) new molecular targets were revealed for some drugs traditionally used to other therapeutic purposes; and (3) sufficient decline of development costs for the new therapies performed by the “old” drugs. The list of such repurposed drugs now includes dozens of medications commonly used for treatment of cardiovascular diseases, diabetes mellitus, epilepsia, different inflammatory disorders. The present review deals, mainly, repurposing of anti-infectious drugs, including those used in prevention and management of infectious complications occurring in cytostatic therapy of leukemia and lymphomas, e.g., tetracyclines, erythromycin derivatives, as well as fluoroquinolones, antiviral compounds etc. <br> The antitumor effects were of these candidates for repurposing were demonstrated upon screening of their cytostatic effects in leukemic and other cancer cell lines. Some studies were performed in experimental tumor-bearing animals. Only few clinical trials were carried out in patients with leukemias and lymphomas following hematopoietic stem cell transplantation (HSCT), which showed some positive effects of antibacterial drugs in terms of graft-versus-host disease (GvHD) prevention, or prolonged survival of the patients. Controlled clinical trials of common anti-infectious drugs are required for this repurposing.</p> <h2>Keywords</h2> <p style="text-align: justify;">Antibacterial drugs, repurposing, anticancer effects, leukemia treatment, hematopoietic stem cell transplantation. </p> " ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1879) "
Over last decade, a number of studies has concerned possible implications of “old” medical drugs, as additional tools for cancer treatment. The main reasons for extension of drug indications are as follows: (1) limited efficiency or high costs of targeted oncogene protein inhibitors or specific monoclonal antibodies for therapy; (2) new molecular targets were revealed for some drugs traditionally used to other therapeutic purposes; and (3) sufficient decline of development costs for the new therapies performed by the “old” drugs. The list of such repurposed drugs now includes dozens of medications commonly used for treatment of cardiovascular diseases, diabetes mellitus, epilepsia, different inflammatory disorders. The present review deals, mainly, repurposing of anti-infectious drugs, including those used in prevention and management of infectious complications occurring in cytostatic therapy of leukemia and lymphomas, e.g., tetracyclines, erythromycin derivatives, as well as fluoroquinolones, antiviral compounds etc.
The antitumor effects were of these candidates for repurposing were demonstrated upon screening of their cytostatic effects in leukemic and other cancer cell lines. Some studies were performed in experimental tumor-bearing animals. Only few clinical trials were carried out in patients with leukemias and lymphomas following hematopoietic stem cell transplantation (HSCT), which showed some positive effects of antibacterial drugs in terms of graft-versus-host disease (GvHD) prevention, or prolonged survival of the patients. Controlled clinical trials of common anti-infectious drugs are required for this repurposing.
Keywords
Antibacterial drugs, repurposing, anticancer effects, leukemia treatment, hematopoietic stem cell transplantation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(1879) "Over last decade, a number of studies has concerned possible implications of “old” medical drugs, as additional tools for cancer treatment. The main reasons for extension of drug indications are as follows: (1) limited efficiency or high costs of targeted oncogene protein inhibitors or specific monoclonal antibodies for therapy; (2) new molecular targets were revealed for some drugs traditionally used to other therapeutic purposes; and (3) sufficient decline of development costs for the new therapies performed by the “old” drugs. The list of such repurposed drugs now includes dozens of medications commonly used for treatment of cardiovascular diseases, diabetes mellitus, epilepsia, different inflammatory disorders. The present review deals, mainly, repurposing of anti-infectious drugs, including those used in prevention and management of infectious complications occurring in cytostatic therapy of leukemia and lymphomas, e.g., tetracyclines, erythromycin derivatives, as well as fluoroquinolones, antiviral compounds etc.
The antitumor effects were of these candidates for repurposing were demonstrated upon screening of their cytostatic effects in leukemic and other cancer cell lines. Some studies were performed in experimental tumor-bearing animals. Only few clinical trials were carried out in patients with leukemias and lymphomas following hematopoietic stem cell transplantation (HSCT), which showed some positive effects of antibacterial drugs in terms of graft-versus-host disease (GvHD) prevention, or prolonged survival of the patients. Controlled clinical trials of common anti-infectious drugs are required for this repurposing.
Keywords
Antibacterial drugs, repurposing, anticancer effects, leukemia treatment, hematopoietic stem cell transplantation.
" } ["DOI"]=> array(37) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20976" ["VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-12-19" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-12-19" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-12-19" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20980" ["VALUE"]=> string(83) "Drug repurposing in leukemia treatment and hematopoietic stem cell transplantation " ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(83) "Drug repurposing in leukemia treatment and hematopoietic stem cell transplantation " ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(83) "Drug repurposing in leukemia treatment and hematopoietic stem cell transplantation " } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20978" ["VALUE"]=> array(2) { ["TEXT"]=> string(197) "<p>R.Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(185) "R.Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(185) "R.Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
" } ["AUTHORS"]=> array(38) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> array(1) { [0]=> string(5) "22002" } ["VALUE"]=> array(1) { [0]=> string(3) "119" } ["DESCRIPTION"]=> array(1) { [0]=> string(0) "" } ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(1) { [0]=> string(3) "119" } ["~DESCRIPTION"]=> array(1) { [0]=> string(0) "" } ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(63) "Alexei B. Chukhlovin" ["LINK_ELEMENT_VALUE"]=> bool(false) } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20993" ["VALUE"]=> array(2) { ["TEXT"]=> string(54) "<p>Алексей Б. Чухловин <p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(42) "Алексей Б. Чухловин
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(42) "
Алексей Б. Чухловин
" } ["SUBMITTED"]=> array(37) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20972" ["VALUE"]=> string(10) "04.03.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "04.03.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "04.03.2019" } ["ACCEPTED"]=> array(37) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20973" ["VALUE"]=> string(10) "12.04.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "12.04.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "12.04.2019" } ["CONTACT"]=> array(38) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20974" ["VALUE"]=> string(3) "119" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(3) "119" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(63) "Alexei B. Chukhlovin" ["LINK_ELEMENT_VALUE"]=> bool(false) } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20995" ["VALUE"]=> array(2) { ["TEXT"]=> string(4025) "<p style="text-align: justify;">В течение последнего десятилетия появился целый ряд исследований, касающихся возможного применения «старых» медицинских препаратов в качестве дополнительных средств для лечения злокачественных новообразований. Есть следующие главные причины подобного расширения показаний для этих препаратов: (1) ограниченная эффективность и высокая стоимость новых таргетных ингибиторов онкогенных белков, или моноклональных антител для терапии; (2) выявление новых молекулярных мишеней для ряда препаратов, ранее внедренных по другим показаниям; (3) существенное снижение затрат на разработку новых средств терапии, осуществляемой «старыми» препаратами. Перечень таких «перенацеленных» препаратов сейчас включает десятки лекарств, которые часто используются, в частности, для лечения сердечно-сосудистых заболеваний, сахарного диабета, эпилепсии, различных воспалительных заболеваний. Данный обзор касается, главным образом, «переназначения» антиинфекционных препаратов, в т.ч. тех, которые используются для профилактики и лечения инфекционных осложнений, возникающих при цитостатической терапии лейкозов и лимфом, в частности – тетрациклинов, производных эритромицина, а также фторхинолонов, антивирусных препаратов и др. Противоопухолевые эффекты этих препаратов-кандидатов для «переназначение» были показаны при скрининге их цитостатических эффектов на линиях лейкозных и других злокачественных клеток. Некоторые исследования проведены на экспериментальных животных-опухоленосителях. Немногие клинические испытания были проведеныe в группах пациентов с лейкозами и лимфомами после трансплантации гемопоэтических стволовых клеток (ТГСК), которые показали некоторые позитивные эффекты антибактериальных препаратов в плане профилактики реакции «трансплантат против хозяина» (РТПХ) или увеличения продолжительности жизни пациентов. В этих целях необходимы контролируемые клинические исследования часто применяемых антиинфекционных препаратов. <p> <h2>Ключевые слова</h2> <p style="text-align: justify;">Антибактериальные препараты, переназначение, противоопухолевые эффекты, терапия лейкозов, трансплантация гемопоэтических стволовых клеток.</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3969) "
В течение последнего десятилетия появился целый ряд исследований, касающихся возможного применения «старых» медицинских препаратов в качестве дополнительных средств для лечения злокачественных новообразований. Есть следующие главные причины подобного расширения показаний для этих препаратов: (1) ограниченная эффективность и высокая стоимость новых таргетных ингибиторов онкогенных белков, или моноклональных антител для терапии; (2) выявление новых молекулярных мишеней для ряда препаратов, ранее внедренных по другим показаниям; (3) существенное снижение затрат на разработку новых средств терапии, осуществляемой «старыми» препаратами. Перечень таких «перенацеленных» препаратов сейчас включает десятки лекарств, которые часто используются, в частности, для лечения сердечно-сосудистых заболеваний, сахарного диабета, эпилепсии, различных воспалительных заболеваний. Данный обзор касается, главным образом, «переназначения» антиинфекционных препаратов, в т.ч. тех, которые используются для профилактики и лечения инфекционных осложнений, возникающих при цитостатической терапии лейкозов и лимфом, в частности – тетрациклинов, производных эритромицина, а также фторхинолонов, антивирусных препаратов и др. Противоопухолевые эффекты этих препаратов-кандидатов для «переназначение» были показаны при скрининге их цитостатических эффектов на линиях лейкозных и других злокачественных клеток. Некоторые исследования проведены на экспериментальных животных-опухоленосителях. Немногие клинические испытания были проведеныe в группах пациентов с лейкозами и лимфомами после трансплантации гемопоэтических стволовых клеток (ТГСК), которые показали некоторые позитивные эффекты антибактериальных препаратов в плане профилактики реакции «трансплантат против хозяина» (РТПХ) или увеличения продолжительности жизни пациентов. В этих целях необходимы контролируемые клинические исследования часто применяемых антиинфекционных препаратов.
Ключевые слова
Антибактериальные препараты, переназначение, противоопухолевые эффекты, терапия лейкозов, трансплантация гемопоэтических стволовых клеток.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3969) "В течение последнего десятилетия появился целый ряд исследований, касающихся возможного применения «старых» медицинских препаратов в качестве дополнительных средств для лечения злокачественных новообразований. Есть следующие главные причины подобного расширения показаний для этих препаратов: (1) ограниченная эффективность и высокая стоимость новых таргетных ингибиторов онкогенных белков, или моноклональных антител для терапии; (2) выявление новых молекулярных мишеней для ряда препаратов, ранее внедренных по другим показаниям; (3) существенное снижение затрат на разработку новых средств терапии, осуществляемой «старыми» препаратами. Перечень таких «перенацеленных» препаратов сейчас включает десятки лекарств, которые часто используются, в частности, для лечения сердечно-сосудистых заболеваний, сахарного диабета, эпилепсии, различных воспалительных заболеваний. Данный обзор касается, главным образом, «переназначения» антиинфекционных препаратов, в т.ч. тех, которые используются для профилактики и лечения инфекционных осложнений, возникающих при цитостатической терапии лейкозов и лимфом, в частности – тетрациклинов, производных эритромицина, а также фторхинолонов, антивирусных препаратов и др. Противоопухолевые эффекты этих препаратов-кандидатов для «переназначение» были показаны при скрининге их цитостатических эффектов на линиях лейкозных и других злокачественных клеток. Некоторые исследования проведены на экспериментальных животных-опухоленосителях. Немногие клинические испытания были проведеныe в группах пациентов с лейкозами и лимфомами после трансплантации гемопоэтических стволовых клеток (ТГСК), которые показали некоторые позитивные эффекты антибактериальных препаратов в плане профилактики реакции «трансплантат против хозяина» (РТПХ) или увеличения продолжительности жизни пациентов. В этих целях необходимы контролируемые клинические исследования часто применяемых антиинфекционных препаратов.
Ключевые слова
Антибактериальные препараты, переназначение, противоопухолевые эффекты, терапия лейкозов, трансплантация гемопоэтических стволовых клеток.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20994" ["VALUE"]=> array(2) { ["TEXT"]=> string(356) "<p>НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия<p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(344) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(344) "
НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
" } } } [3]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "120" ["~IBLOCK_SECTION_ID"]=> string(3) "120" ["ID"]=> string(4) "1628" ["~ID"]=> string(4) "1628" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(184) "Альтернативные методы преодоления диастаза поврежденного периферического нерва (обзор литературы)" ["~NAME"]=> string(184) "Альтернативные методы преодоления диастаза поврежденного периферического нерва (обзор литературы)" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "03.06.2019 14:00:18" ["~TIMESTAMP_X"]=> string(19) "03.06.2019 14:00:18" ["DETAIL_PAGE_URL"]=> string(139) "/ru/archive/tom-8-nomer-1/obzornye-stati/alternativnye-metody-preodoleniya-diastaza-povrezhdennogo-perifericheskogo-nerva-obzor-literatury/" ["~DETAIL_PAGE_URL"]=> string(139) "/ru/archive/tom-8-nomer-1/obzornye-stati/alternativnye-metody-preodoleniya-diastaza-povrezhdennogo-perifericheskogo-nerva-obzor-literatury/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(19748) "
Introduction
Autologous nerve transplantation still remains a golden standard for reconstruction of peripheral nerves. Autologous sural nerve is mostly often harvested and transplanted into the gap dividing two ends of the damaged nerve. The main problem of this approach occurs due to the area of the nerve harvesting which may be associated with its functional loss and risk of painful neurinoma. Moreover, the material for grafting is available only in limited amounts. Hence, full reconstruction seems to be impossible, especially in extensive nerve lesions (i.e., of brachial plexus) [1].
This problem may be resolved by means of an implant (conduit) allowing to join the ends of damaged nerve, thus promoting invasion of nervous fibers from its central segment to peripheral part. Different materials were proposed for implantation that may be classified into distinct groups, i.e., biological implants (veins, skeletal muscles) [2, 3], or synthetic materials. Moreover, the synthetic conduits may be resorbable, such as chitosan conduit, polylactide tubule, conduits of biodegradable polyurethane, neurotube of polyglycolic acid), and non-resorbable implants, e.g., silicon tubes [1]. Therefore, we present a review of literature on the surgery of peripheral nerves ruptures with diastasis. We have collected the data of efficiency of different methods used for overcoming diastasis of the injured peripheral nerves.
Biological implant materials
Usage of venous grafts in order to overlap a gap between the ends of damaged nerve shows some benefits including simple access, minor associated injury during the vein harvest, wide choice of veins with different-diameters. Moreover, the venous wall is permeable for the nutrients; basal lamina of veins is enriched with laminin, thus improving nerve regeneration, whereas the venous matter is a non-immunogenic substance [2, 3].
Meanwhile, Guerra et al. [2] have shown that the empty venous graft tends for collapse. Therefore, it is reasonable to fill the conduit with different substances in order to provide its structural properties and improve the nerve regeneration processes [2].
Synthetic materials
An ideal material for a synthetic conduit should meet the following requirements: biocompatibility, structural and mechanical properties corresponding to natural nervous tissue, appropriate biodegradation rates that should provide structural support during the entire regeneration period, however, without a risk of nerve compression. The biodegradation products should be non-toxic and optimal porosity of this material should be of 70-98%; It should be hard and flexible [4, 5].
Over last years, a number of workers have proposed different synthetic biodegradable materials meeting these criteria, i.e., chitosan, polylactide, their derivates, as well as electroconductive polymers.
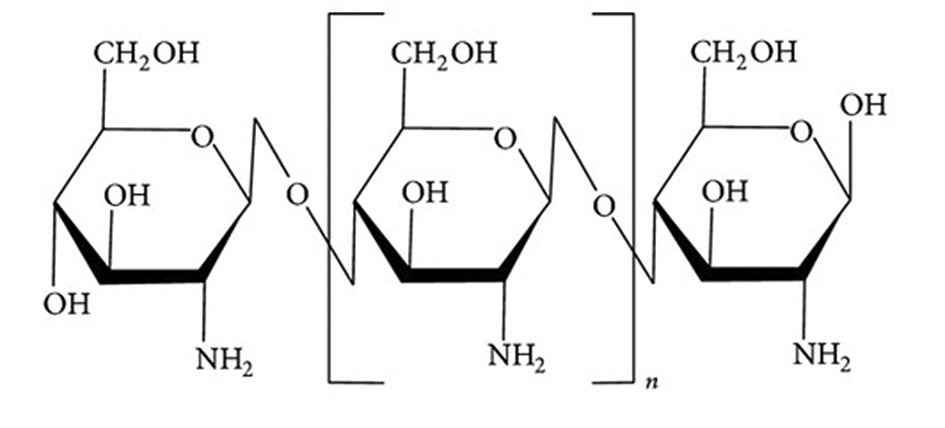
Figure 1. Chitosan structure [4]
Chitosan is a derivative obtained by alkaline deacelylation of the chitin polymer (Fig. 1). I.e., the deacetylation degree in chitosan is a key characteristic which determines its physical, chemical and biological features. This parameter sufficiently determines the rates of the polymer degradation, due to controlled deacetylation processes during chitosan preparation (the chitosan degradation rate is reversely proportional to the polymer crystallinity and, therefore, to its decatylation degree). Moreover, the regulated porosity of the chitosan scaffolds (80 to 90%, with the pore size of 50 to 250 mcm) is faforable to angiogenesis which plays a fundamental role in survival and functioning of regenerated nerve fibres. Chitosan is depolymerized in the tissues by means of enzymatic hydrolysis mediated by different hydrolases including lysozyme, pectinases, cellulases, hemicellulases, lipases and amylases. The chitin degradation results into oligosaccharides and monosaccharides, netural metabolites of glucosaminoglycanes, or glucoaminoproteins [4].
Due to all these characteristics, chitosan is considered plausible material for usage in the nerve tubulization. When performing comparative evaluation of axon repair after the defect reconstruction by hollow chitosan conduits of different acetylation degrees, donor nerve autograft, and silicon tube, the best results were obtained in the “golden standard” group. The least efficiency was documented with the silicon conduits. Moreover, they have revealed better regeneration with chitosan acetylated for 5%, than with 2% acetyl groups [7].
The results comparable with autoneural inserts could be achieved by endoneurium modeling due to supplement of a hollow chitosan conduit by the biologically active filler medium consisting of stabilized collagen and enriched by fibronectin [8].
Addition of pro-regenerative cells (Schwann, mesenchimal cells) to the mentioned enriched scaffold restores a natural nerve environment which could be provided by autotransplant. Some workers (Gonzalez-Perez et al.) report on 100% success in nerve regeneration when using the given method with Schwann cell supplementation. E.g., usage of the scaffolds the scaffolds enriched by mesenchymal cells and extracellular matrix substances is associated with 90% success in nerve repair, whereas hollow chitosan tubes bring about 75% success rates [9].
Hence, a combination of chitosan conduits with enriched extracellular matrix and pro-regeneration cells represents a good alternative to the usage of autotransplants in order to restore longitudinal gaps after the nerve injury [8, 9].
A number of other works described chitosan applications combined with other substances, both as conduit, or filling medium (Table 1) [11]. The authors report on good results of nerve regeneration when using tubulization with composite polymeric grafts based on chitosan with polyglycols [10]. Wang et al. [10] did not reveal any statistically significant differences in nerve recovery when testing the mentioned polymeric tubes and “gloden standard”.
Table 1. Results of chitosan application combined with other substances and polymers [11]

Otherwise, the chitosan conduits have shown good results when applying them for restoration of the human nerve integrity (Fan et al.) [12].
Polylactide
Polylactide is a biodegradable thermoplastic polyesther. Polylactide was used as a hollow tibe as a conduit for the nerve reconstruction, as well as a component of composite polymers combined with polycaprolactone or polyglycolide. Polylactide tube was superior to polycaprolactone scaffold, having been compatible with autoneural transplant by its efficiency [13].
Copolyesther-based conduits comprising combinations of polylactide and polycaprolactone, (Neurolac1), and those based on a combination of polylactide and polyglycolide (PLGA) did not show statistically significant differences against the model with autologous donor nerve. However, the polyesther-based scaffolds exhibited a longer biodegradation period as compared with PLGA scaffolds (16-20 and 12 weeks, respectively). Moreover, the biodegradation rate for PLGA conduites correlates with its monomeric composition (i.e., the glycolic-to-lactic acid ratio). The authors also note that degradation products of this polymer show acid reaction, thus leading to decreased tissue pH and development of immune response. Co-polyester provides lesser amounts of acid products upon its biodegradation. PLGA, however, has a benefit due to its microporosity [14].
Some authors reported on better recovery nerve functions when using the co-polyesther when compared to the approved “golden standard” [15, 16]. Moreover, some studies dealt with abovementioned hollow polymeric tubes combined with different filling media (Table 2, 3) [11].
Table 2. Studies with PLGA-based conduites with different filling substances [11]

Table 3. Conduites based on caprolactone with different fillers [11]

Electroconductive polymers
Due to limited nerve regeneration capacity, their reconstitution often requires different biological factors which may control cellular metabolic activity including cell adhesion, differentiation and cytokine secretion. Electric signals are among such factors [17]. Therefore, development of a biodegradable scaffold able to conduct electricity was an important challenge to the workers.
A need for electroconductive polymers was initiated by a study which led to a 10-million-fold increase of polyacetylene conductivity by means of oxydation in iodine vapor. (Normally, polyacethylene is a semi-conductor). This modification, called doping, is the major condition for acquiring the polymer conductivity. The doping process proceeds during the polymer synthesis, or it may be performed by chemical, electrochemical methods, or by means of photo-doping. Moreover, this process may proceed in two ways: p-doping with polymer oxidation and getting the positive charge; and n-doping with polymer reduction and its negative charging. In brief, the polymer (semi-conductor, insulator) is supplied with small amounts of an additive agent which removes or adds an electron to the polymeric chain which eliminates or adds an electron to the polymer chain, this resulting into a delocalized electric charge (Fig. 2, А) [18]. Thereafter, a localization of the charge by a point distorsion of a crystal grid, i.e., the polaron formation (Fig. 2, В, С) [18]. Polaron is able to migrate along the polymer chain, thus allowing it to conduct electricity (Fig. 2, D) [18].
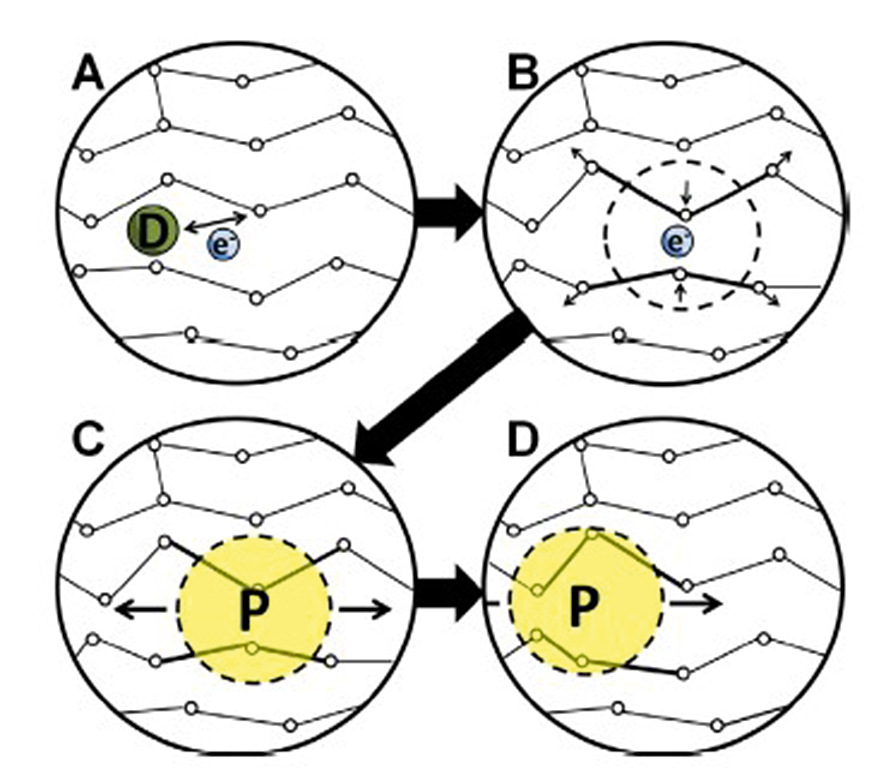
Figure 2. Simplified description of electroconductivity for conducting polymers: (А) removal or addition of an electron to the polymer chain using a doping additive, thus leading to formation of a delocalized charge; (B, C), the charge localization and its surrounding by a local distortion of crystal grid (polaron formation); (D), polaron migration along the polymer chain, thus providing electric conductivity [18]
Polypyrrole is the most studied electroconductive polymer. Chen et al. [19] have used a polypyrrole tube for reconstitution of injured N.ischiadicus in rats. As a result, the authors have revealed that the given polymer is biocompatible and suitable for the nerve electrostimulation procedures [19].
A derivative of polytiophen (PEDOT) is also a promising electroconductive polymer for applications in the nerve regeneration, due to its biocompatibility, electroconductivity and higher electric stability than in polypyrrols. Moreover, carboxymethylchitosan (CMCS), a composite electroconductive polymer was also developed and used. CMSC served as the main macromolecular network able for biodegradation, whereas poly-3,4-ethylenedioxythophen (PEDOT) was applied as a conductive polymeric layer. Herewith, the samples of such polymer show maximal electric conductivity at the polyethylenedioxythophen concentration of 0.2 M. Worth of note, this composite scaffold dose not exert any toxic effect upon the cells, and, alternatively, supports their adhesion survival and proliferation [20]. These characteristics make it an appropriate material for designing a scaffold for the nerve regeneration.
Therefore, usage of the nerve tubulization techniques with biodegradable polymeric conduits is mostly showing a statistically and clinically significant regeneration efficiency which is comparable with autoneural insertion. Upon the conduit functionalization by a biologically active medium and pro-regeneratory cells, one may achieve even better results than with autologous transplants [2, 8, 9, 10, 12, 13, 14]. Additionally, this approach may avoid some problems with harvesting of donors’ nerve which occur in autotransplantation method, the approved “golden standard” [1, 5, 7, 11]. Moreover, when developing electroconductive polymeric scaffolds, one may combine the benefits of biodegradable polymers with electroconductivity, as a factor enabling nerve cell differentiation, enhance neurite growth and peripheral nerve regeneration. Therefore, this mode of bioengineering is quite promising for usage in the surgery of peripheral nerves, thus requiring further studies in the field [17-20].
Conclusion
Injury of peripheral nerves is often accomplished by a sufficient diastasis (gap) between the ends of damaged nerve, thus making it difficult to perform a standard manual suture using surgical threads. As based on analysis of published data, some effective methods are proposed for surgical treatment of peripheral nerve injuries with diastasis. Moreover, some problems of autoneural plastics are revealed. Thus, the aspects of overcoming such diastasis remain to be timely, especially in cases of longitudinal and multiple nerve defects. An alternative option in resolving such problems is offered, i.e., usage of implants allowing to connect the ends of a damaged nerve and promoting invasion of neural fibres from the central to peripheral processus of the damaged nerve. Usage of biocompatible and biodegradable polymers as a neural prosthesis promotes a more safe regeneration, and does not require switching off the donor nerve and its function. Moreover, some new options allow to influence regeneration rates and quality of the damaged peripheral nerves. As shown by the mentioned data, one may state that application of the proposed methods in many observations brings about statistically and clinically significant results that may objectively compete with results of autoneural grafting. Hence, further studies of the tubulization method open a prospective in surgical treatment of damaged peripheral nerves with diastasis. Therefore, further studies in tubulization method is a promising direction in this field, providing a serious potential for successful reconstructive surgical interventions.
Conflict of interests
None of the authors report any conflicts of interest.
References
- Comparative neuro tissue engineering using different nerve guide implants / N. Sinis, H.-E. Schaller, C. Schulte-Eversum, T. Lanaras, B. Schlosshauer, M. Doser, K. Dietz, H. Rоsner, H.-W. Muller, M. Haerle. Acta Neurochir (Suppl). 2007 100: 61-64.
- Sabongi RG, Fernandes M, Dos Santos JB. Peripheral nerve regeneration with conduits: use of vein tubes. Neur Regener Res. 2015;10(4):529-533.
- Bueno CRS, Pereira M, Aparecido I Favaretto-Júnior, Buchaim RL, Andreo JC, Rodrigues AC, Marco G Rosa-Júnior. Comparative study between standard and inside-out vein graft techniques on sciatic nerve repair of rats. Muscular and functional analysis. Acta Cir Bras. 2017;32(3):287-296.
- Yao K, Li J, Yao F, Yin Y. Chitosan-based hydrogels: functions and applications. 2012 by Taylor & Francis Group, LLC: 408-409.
- Bauback S, Buncke G. Autograft substitutes conduits and processed nerve allografts. Hand Clin. 2016; 32: 127-140.
- Kuffler DP. Promoting axon regeneration and neurological recovery following traumatic peripheral nerve injuries. Int J Neurorehabilitation. 2015, 2:1.
- Gonzalez-Perez F, Cobianchi S, Geuna S, Barwig C, Freier T., Udina E, Navarro X. Tubulization with chitosan guides for the repair of long gap peripheral nerve injury in the rat. Microsurgery. 2015;35(4):300-308.
- Gonzalez-Perez F, Cobianchi S, Heimann C, Phillips JB, Udina E, Navarro X. Stabilization, rolling, and addition of other extracellular matrix proteins to collagen hydrogels improve regeneration in chitosan guides for long peripheral nerve gaps in rats. Neurosurgery. 2017; 80(3):465-474.
- Gonzalez-Perez F, Hernández J, Heimann C, Phillips JB, Udina E, Navarro X. Schwann cells and mesenchymal stem cells in laminin- or fibronectin-aligned matrices and regeneration across a critical size defect of 15 mm in the rat sciatic nerve. J Neurosurg Spine 2017; 28(1): 109-118.
- Wang X, Hu W, Cao Y, Yao J, Wu J, Gu X. Dog sciatic nerve regeneration across a 30-mm defect bridged by a chitosan/PGA artificial nerve graft Brain. 2005; 128(8): 1897-1910.
- Pinho AC, Fonseca AC, Serra AC, Santos JD, Coelho JF. Peripheral nerve regeneration: current status and new strategies using polymeric materials. Adv Healthc Mater. 2016; 5(21): 2732–2744.
- Fan W, Gu J, Hu W, Deng A, Ma Y, Liu J, Ding F, Gu X. Repairing a 35-mm-long median nerve defect with a chitosan/PGA artificial nerve graft in the human: a case study. Microsurgery. 2008; 28(4):238-242.
- Goulart CO, Lopes FR, Monte ZO, Dantas SV Jr, Souto A, Oliveira JT, Almeida FM, Tonda-Turo C, Pereira CC, Borges CP, Martinez AM. Evaluation of biodegradable polymer conduits – poly (L-lactic acid) – for guiding sciatic nerve regeneration in mice. Methods. 2015; 99:28-36.
- Luis AL, Rodrigues JM, Amado S, Veloso AP, Armada-Da-Silva PA, Raimondo S, Fregnan F, Ferreira AJ, Lopes MA, Santos JD, Geuna S, Varejão AS, Maurício AC. PLGA 90/10 and caprolactone biodegradable nerve guides for the reconstruction of the rat sciatic nerve. Microsurgery. 2007; 27(2):125-137.
- Den Dunnen WFA, Van der Lei B, Schakenraad JM, Stokroos I, Blaauw E, Bartels H, Pennings AJ, Robinson PH. Poly(DL-lactide-e-caprolactone) nerve guides perform better than autologous nerve grafts. Microsurgery 1996; 17: 348-357.
- den Dunnen WF, van der Lei B, Robinson PH, Holwerda A, Pennings AJ, Schakenraad JM. Biological performance of a degradable poly (lactic acid-epsilon-caprolactone) nerve guide: Influence of tube dimensions. J Biomed Mater Res. 1995; 29(6): 757-766.
- Song S, George PM. Conductive polymer scaffolds to improve neural recovery. Neural Regen Res.2017; 12(12):1976-1978.
- Balint R, Cassidy NJ, Cartmell SH. Conductive polymers: towards a smart biomaterial for tissue engineering. Acta Biomater. 2014;10(6):2341-2353.
- Kabiri M, Oraee-Yazdani S, Dodel M, Hanaee-Ahvaz H, Soudi S, Seyedjafari E, Salehi M, Soleimani M. Cytocompatibility of a conductive nanofibrous carbon nanotube/poly (l-lactic acid) composite scaffold intended for nerve tissue engineering. EXCLI J. 2015;14:851-860.
- Xu C, Guan S, Wang S, Gong W, Liu T, Ma X, Sun C. Biodegradable and electroconductive poly(3,4-ethylenedioxythiophene)/ carboxymethyl chitosan hydrogels for neural tissue engineering. Mater Sci Eng C Mater Biol Appl. 2018;84:32-43.
Introduction
Autologous nerve transplantation still remains a golden standard for reconstruction of peripheral nerves. Autologous sural nerve is mostly often harvested and transplanted into the gap dividing two ends of the damaged nerve. The main problem of this approach occurs due to the area of the nerve harvesting which may be associated with its functional loss and risk of painful neurinoma. Moreover, the material for grafting is available only in limited amounts. Hence, full reconstruction seems to be impossible, especially in extensive nerve lesions (i.e., of brachial plexus) [1].
This problem may be resolved by means of an implant (conduit) allowing to join the ends of damaged nerve, thus promoting invasion of nervous fibers from its central segment to peripheral part. Different materials were proposed for implantation that may be classified into distinct groups, i.e., biological implants (veins, skeletal muscles) [2, 3], or synthetic materials. Moreover, the synthetic conduits may be resorbable, such as chitosan conduit, polylactide tubule, conduits of biodegradable polyurethane, neurotube of polyglycolic acid), and non-resorbable implants, e.g., silicon tubes [1]. Therefore, we present a review of literature on the surgery of peripheral nerves ruptures with diastasis. We have collected the data of efficiency of different methods used for overcoming diastasis of the injured peripheral nerves.
Biological implant materials
Usage of venous grafts in order to overlap a gap between the ends of damaged nerve shows some benefits including simple access, minor associated injury during the vein harvest, wide choice of veins with different-diameters. Moreover, the venous wall is permeable for the nutrients; basal lamina of veins is enriched with laminin, thus improving nerve regeneration, whereas the venous matter is a non-immunogenic substance [2, 3].
Meanwhile, Guerra et al. [2] have shown that the empty venous graft tends for collapse. Therefore, it is reasonable to fill the conduit with different substances in order to provide its structural properties and improve the nerve regeneration processes [2].
Synthetic materials
An ideal material for a synthetic conduit should meet the following requirements: biocompatibility, structural and mechanical properties corresponding to natural nervous tissue, appropriate biodegradation rates that should provide structural support during the entire regeneration period, however, without a risk of nerve compression. The biodegradation products should be non-toxic and optimal porosity of this material should be of 70-98%; It should be hard and flexible [4, 5].
Over last years, a number of workers have proposed different synthetic biodegradable materials meeting these criteria, i.e., chitosan, polylactide, their derivates, as well as electroconductive polymers.

Figure 1. Chitosan structure [4]
Chitosan is a derivative obtained by alkaline deacelylation of the chitin polymer (Fig. 1). I.e., the deacetylation degree in chitosan is a key characteristic which determines its physical, chemical and biological features. This parameter sufficiently determines the rates of the polymer degradation, due to controlled deacetylation processes during chitosan preparation (the chitosan degradation rate is reversely proportional to the polymer crystallinity and, therefore, to its decatylation degree). Moreover, the regulated porosity of the chitosan scaffolds (80 to 90%, with the pore size of 50 to 250 mcm) is faforable to angiogenesis which plays a fundamental role in survival and functioning of regenerated nerve fibres. Chitosan is depolymerized in the tissues by means of enzymatic hydrolysis mediated by different hydrolases including lysozyme, pectinases, cellulases, hemicellulases, lipases and amylases. The chitin degradation results into oligosaccharides and monosaccharides, netural metabolites of glucosaminoglycanes, or glucoaminoproteins [4].
Due to all these characteristics, chitosan is considered plausible material for usage in the nerve tubulization. When performing comparative evaluation of axon repair after the defect reconstruction by hollow chitosan conduits of different acetylation degrees, donor nerve autograft, and silicon tube, the best results were obtained in the “golden standard” group. The least efficiency was documented with the silicon conduits. Moreover, they have revealed better regeneration with chitosan acetylated for 5%, than with 2% acetyl groups [7].
The results comparable with autoneural inserts could be achieved by endoneurium modeling due to supplement of a hollow chitosan conduit by the biologically active filler medium consisting of stabilized collagen and enriched by fibronectin [8].
Addition of pro-regenerative cells (Schwann, mesenchimal cells) to the mentioned enriched scaffold restores a natural nerve environment which could be provided by autotransplant. Some workers (Gonzalez-Perez et al.) report on 100% success in nerve regeneration when using the given method with Schwann cell supplementation. E.g., usage of the scaffolds the scaffolds enriched by mesenchymal cells and extracellular matrix substances is associated with 90% success in nerve repair, whereas hollow chitosan tubes bring about 75% success rates [9].
Hence, a combination of chitosan conduits with enriched extracellular matrix and pro-regeneration cells represents a good alternative to the usage of autotransplants in order to restore longitudinal gaps after the nerve injury [8, 9].
A number of other works described chitosan applications combined with other substances, both as conduit, or filling medium (Table 1) [11]. The authors report on good results of nerve regeneration when using tubulization with composite polymeric grafts based on chitosan with polyglycols [10]. Wang et al. [10] did not reveal any statistically significant differences in nerve recovery when testing the mentioned polymeric tubes and “gloden standard”.
Table 1. Results of chitosan application combined with other substances and polymers [11]

Otherwise, the chitosan conduits have shown good results when applying them for restoration of the human nerve integrity (Fan et al.) [12].
Polylactide
Polylactide is a biodegradable thermoplastic polyesther. Polylactide was used as a hollow tibe as a conduit for the nerve reconstruction, as well as a component of composite polymers combined with polycaprolactone or polyglycolide. Polylactide tube was superior to polycaprolactone scaffold, having been compatible with autoneural transplant by its efficiency [13].
Copolyesther-based conduits comprising combinations of polylactide and polycaprolactone, (Neurolac1), and those based on a combination of polylactide and polyglycolide (PLGA) did not show statistically significant differences against the model with autologous donor nerve. However, the polyesther-based scaffolds exhibited a longer biodegradation period as compared with PLGA scaffolds (16-20 and 12 weeks, respectively). Moreover, the biodegradation rate for PLGA conduites correlates with its monomeric composition (i.e., the glycolic-to-lactic acid ratio). The authors also note that degradation products of this polymer show acid reaction, thus leading to decreased tissue pH and development of immune response. Co-polyester provides lesser amounts of acid products upon its biodegradation. PLGA, however, has a benefit due to its microporosity [14].
Some authors reported on better recovery nerve functions when using the co-polyesther when compared to the approved “golden standard” [15, 16]. Moreover, some studies dealt with abovementioned hollow polymeric tubes combined with different filling media (Table 2, 3) [11].
Table 2. Studies with PLGA-based conduites with different filling substances [11]

Table 3. Conduites based on caprolactone with different fillers [11]

Electroconductive polymers
Due to limited nerve regeneration capacity, their reconstitution often requires different biological factors which may control cellular metabolic activity including cell adhesion, differentiation and cytokine secretion. Electric signals are among such factors [17]. Therefore, development of a biodegradable scaffold able to conduct electricity was an important challenge to the workers.
A need for electroconductive polymers was initiated by a study which led to a 10-million-fold increase of polyacetylene conductivity by means of oxydation in iodine vapor. (Normally, polyacethylene is a semi-conductor). This modification, called doping, is the major condition for acquiring the polymer conductivity. The doping process proceeds during the polymer synthesis, or it may be performed by chemical, electrochemical methods, or by means of photo-doping. Moreover, this process may proceed in two ways: p-doping with polymer oxidation and getting the positive charge; and n-doping with polymer reduction and its negative charging. In brief, the polymer (semi-conductor, insulator) is supplied with small amounts of an additive agent which removes or adds an electron to the polymeric chain which eliminates or adds an electron to the polymer chain, this resulting into a delocalized electric charge (Fig. 2, А) [18]. Thereafter, a localization of the charge by a point distorsion of a crystal grid, i.e., the polaron formation (Fig. 2, В, С) [18]. Polaron is able to migrate along the polymer chain, thus allowing it to conduct electricity (Fig. 2, D) [18].

Figure 2. Simplified description of electroconductivity for conducting polymers: (А) removal or addition of an electron to the polymer chain using a doping additive, thus leading to formation of a delocalized charge; (B, C), the charge localization and its surrounding by a local distortion of crystal grid (polaron formation); (D), polaron migration along the polymer chain, thus providing electric conductivity [18]
Polypyrrole is the most studied electroconductive polymer. Chen et al. [19] have used a polypyrrole tube for reconstitution of injured N.ischiadicus in rats. As a result, the authors have revealed that the given polymer is biocompatible and suitable for the nerve electrostimulation procedures [19].
A derivative of polytiophen (PEDOT) is also a promising electroconductive polymer for applications in the nerve regeneration, due to its biocompatibility, electroconductivity and higher electric stability than in polypyrrols. Moreover, carboxymethylchitosan (CMCS), a composite electroconductive polymer was also developed and used. CMSC served as the main macromolecular network able for biodegradation, whereas poly-3,4-ethylenedioxythophen (PEDOT) was applied as a conductive polymeric layer. Herewith, the samples of such polymer show maximal electric conductivity at the polyethylenedioxythophen concentration of 0.2 M. Worth of note, this composite scaffold dose not exert any toxic effect upon the cells, and, alternatively, supports their adhesion survival and proliferation [20]. These characteristics make it an appropriate material for designing a scaffold for the nerve regeneration.
Therefore, usage of the nerve tubulization techniques with biodegradable polymeric conduits is mostly showing a statistically and clinically significant regeneration efficiency which is comparable with autoneural insertion. Upon the conduit functionalization by a biologically active medium and pro-regeneratory cells, one may achieve even better results than with autologous transplants [2, 8, 9, 10, 12, 13, 14]. Additionally, this approach may avoid some problems with harvesting of donors’ nerve which occur in autotransplantation method, the approved “golden standard” [1, 5, 7, 11]. Moreover, when developing electroconductive polymeric scaffolds, one may combine the benefits of biodegradable polymers with electroconductivity, as a factor enabling nerve cell differentiation, enhance neurite growth and peripheral nerve regeneration. Therefore, this mode of bioengineering is quite promising for usage in the surgery of peripheral nerves, thus requiring further studies in the field [17-20].
Conclusion
Injury of peripheral nerves is often accomplished by a sufficient diastasis (gap) between the ends of damaged nerve, thus making it difficult to perform a standard manual suture using surgical threads. As based on analysis of published data, some effective methods are proposed for surgical treatment of peripheral nerve injuries with diastasis. Moreover, some problems of autoneural plastics are revealed. Thus, the aspects of overcoming such diastasis remain to be timely, especially in cases of longitudinal and multiple nerve defects. An alternative option in resolving such problems is offered, i.e., usage of implants allowing to connect the ends of a damaged nerve and promoting invasion of neural fibres from the central to peripheral processus of the damaged nerve. Usage of biocompatible and biodegradable polymers as a neural prosthesis promotes a more safe regeneration, and does not require switching off the donor nerve and its function. Moreover, some new options allow to influence regeneration rates and quality of the damaged peripheral nerves. As shown by the mentioned data, one may state that application of the proposed methods in many observations brings about statistically and clinically significant results that may objectively compete with results of autoneural grafting. Hence, further studies of the tubulization method open a prospective in surgical treatment of damaged peripheral nerves with diastasis. Therefore, further studies in tubulization method is a promising direction in this field, providing a serious potential for successful reconstructive surgical interventions.
Conflict of interests
None of the authors report any conflicts of interest.
References
- Comparative neuro tissue engineering using different nerve guide implants / N. Sinis, H.-E. Schaller, C. Schulte-Eversum, T. Lanaras, B. Schlosshauer, M. Doser, K. Dietz, H. Rоsner, H.-W. Muller, M. Haerle. Acta Neurochir (Suppl). 2007 100: 61-64.
- Sabongi RG, Fernandes M, Dos Santos JB. Peripheral nerve regeneration with conduits: use of vein tubes. Neur Regener Res. 2015;10(4):529-533.
- Bueno CRS, Pereira M, Aparecido I Favaretto-Júnior, Buchaim RL, Andreo JC, Rodrigues AC, Marco G Rosa-Júnior. Comparative study between standard and inside-out vein graft techniques on sciatic nerve repair of rats. Muscular and functional analysis. Acta Cir Bras. 2017;32(3):287-296.
- Yao K, Li J, Yao F, Yin Y. Chitosan-based hydrogels: functions and applications. 2012 by Taylor & Francis Group, LLC: 408-409.
- Bauback S, Buncke G. Autograft substitutes conduits and processed nerve allografts. Hand Clin. 2016; 32: 127-140.
- Kuffler DP. Promoting axon regeneration and neurological recovery following traumatic peripheral nerve injuries. Int J Neurorehabilitation. 2015, 2:1.
- Gonzalez-Perez F, Cobianchi S, Geuna S, Barwig C, Freier T., Udina E, Navarro X. Tubulization with chitosan guides for the repair of long gap peripheral nerve injury in the rat. Microsurgery. 2015;35(4):300-308.
- Gonzalez-Perez F, Cobianchi S, Heimann C, Phillips JB, Udina E, Navarro X. Stabilization, rolling, and addition of other extracellular matrix proteins to collagen hydrogels improve regeneration in chitosan guides for long peripheral nerve gaps in rats. Neurosurgery. 2017; 80(3):465-474.
- Gonzalez-Perez F, Hernández J, Heimann C, Phillips JB, Udina E, Navarro X. Schwann cells and mesenchymal stem cells in laminin- or fibronectin-aligned matrices and regeneration across a critical size defect of 15 mm in the rat sciatic nerve. J Neurosurg Spine 2017; 28(1): 109-118.
- Wang X, Hu W, Cao Y, Yao J, Wu J, Gu X. Dog sciatic nerve regeneration across a 30-mm defect bridged by a chitosan/PGA artificial nerve graft Brain. 2005; 128(8): 1897-1910.
- Pinho AC, Fonseca AC, Serra AC, Santos JD, Coelho JF. Peripheral nerve regeneration: current status and new strategies using polymeric materials. Adv Healthc Mater. 2016; 5(21): 2732–2744.
- Fan W, Gu J, Hu W, Deng A, Ma Y, Liu J, Ding F, Gu X. Repairing a 35-mm-long median nerve defect with a chitosan/PGA artificial nerve graft in the human: a case study. Microsurgery. 2008; 28(4):238-242.
- Goulart CO, Lopes FR, Monte ZO, Dantas SV Jr, Souto A, Oliveira JT, Almeida FM, Tonda-Turo C, Pereira CC, Borges CP, Martinez AM. Evaluation of biodegradable polymer conduits – poly (L-lactic acid) – for guiding sciatic nerve regeneration in mice. Methods. 2015; 99:28-36.
- Luis AL, Rodrigues JM, Amado S, Veloso AP, Armada-Da-Silva PA, Raimondo S, Fregnan F, Ferreira AJ, Lopes MA, Santos JD, Geuna S, Varejão AS, Maurício AC. PLGA 90/10 and caprolactone biodegradable nerve guides for the reconstruction of the rat sciatic nerve. Microsurgery. 2007; 27(2):125-137.
- Den Dunnen WFA, Van der Lei B, Schakenraad JM, Stokroos I, Blaauw E, Bartels H, Pennings AJ, Robinson PH. Poly(DL-lactide-e-caprolactone) nerve guides perform better than autologous nerve grafts. Microsurgery 1996; 17: 348-357.
- den Dunnen WF, van der Lei B, Robinson PH, Holwerda A, Pennings AJ, Schakenraad JM. Biological performance of a degradable poly (lactic acid-epsilon-caprolactone) nerve guide: Influence of tube dimensions. J Biomed Mater Res. 1995; 29(6): 757-766.
- Song S, George PM. Conductive polymer scaffolds to improve neural recovery. Neural Regen Res.2017; 12(12):1976-1978.
- Balint R, Cassidy NJ, Cartmell SH. Conductive polymers: towards a smart biomaterial for tissue engineering. Acta Biomater. 2014;10(6):2341-2353.
- Kabiri M, Oraee-Yazdani S, Dodel M, Hanaee-Ahvaz H, Soudi S, Seyedjafari E, Salehi M, Soleimani M. Cytocompatibility of a conductive nanofibrous carbon nanotube/poly (l-lactic acid) composite scaffold intended for nerve tissue engineering. EXCLI J. 2015;14:851-860.
- Xu C, Guan S, Wang S, Gong W, Liu T, Ma X, Sun C. Biodegradable and electroconductive poly(3,4-ethylenedioxythiophene)/ carboxymethyl chitosan hydrogels for neural tissue engineering. Mater Sci Eng C Mater Biol Appl. 2018;84:32-43.
Олег В. Галибин1, Герман В. Медведев2, Павел В. Попрядухин3, Павел А. Кулагин1, Александр А. Гусев1, Галина П. Косякова1, Наталья В. Михайлова1, Вероника Д. Новак1, Денис Н. Соломицкий1, Игорь О. Шемякин1, Вадим С. Гаджиагаев1, Максат Х. Гурбанназаров1
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21162" ["VALUE"]=> array(2) { ["TEXT"]=> string(563) "<p><sup>1</sup> Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова <br> <sup>2</sup> Российский НИИ травматологии и ортопедии им. Р. Р. Вредена, Санкт-Петербург, Россия<br> <sup>3</sup> Институт высокомолекулярных соединений РАН, Санкт-Петербург, Россия </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(503) "1 Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова
2 Российский НИИ травматологии и ортопедии им. Р. Р. Вредена, Санкт-Петербург, Россия
3 Институт высокомолекулярных соединений РАН, Санкт-Петербург, Россия
Повреждение периферических нервов нередко сопровождается значительным диастазом (первичным или вторичным) между концами поврежденного нерва, что затрудняет выполнение стандартного ручного шва нерва с помощью хирургических нитей. На основании анализа данных опубликованных исследований выявлены эффективные способы хирургического лечения повреждений периферических нервов с диастазом. Кроме того, достоверно выявлены недостатки метода аутоневральной пластики, в связи с чем проблема преодоления диастаза поврежденного периферического нерва остается актуальной и в настоящее время, особенно при протяженных и множественных дефектах нервных стволов. Альтернативным вариантом в решении данной проблемы может служит использование имплантов, позволяющих соединить концы поврежденного нерва и способствующих прорастанию нервных волокон из центрального в периферический отросток поврежденного нерва. Использование биосовместимых и биодеградируемых полимеров в качестве неврального протеза способствует более безопасной регенерации и не требует выключения донорского нерва и связанной с ним функции, кроме того, разработаны и продолжают совершенствоваться опции, позволяющие влиять на скорость и качество регенерации поврежденного периферического нерва.
Ключевые слова
Нерв, травма, диастаз, имплант, полимерная основа, хитозан.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21099" ["VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-20-25" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-20-25" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21122" ["VALUE"]=> array(2) { ["TEXT"]=> string(557) "<p>Oleg V. Galibin<sup>1</sup>, German V. Medvedev<sup>2</sup>, Pavel V. Popryadukhin<sup>3</sup>, Pavel A. Kulagin<sup>1</sup>, Alexandr A. Gusev<sup>1</sup>, Galina P. Kossyakova<sup>1</sup>, Natalia V. Mikhailova<sup>1</sup>, Veronika D. Novak<sup>1</sup>, Denis N. Solomitskiy<sup>1</sup>, Igor O. Shemiakin<sup>1</sup>, Vadim S. Gadzhiagaev<sup>1</sup>, Maksat Kh. Gurbannazarov<sup>1</sup> </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(401) "Oleg V. Galibin1, German V. Medvedev2, Pavel V. Popryadukhin3, Pavel A. Kulagin1, Alexandr A. Gusev1, Galina P. Kossyakova1, Natalia V. Mikhailova1, Veronika D. Novak1, Denis N. Solomitskiy1, Igor O. Shemiakin1, Vadim S. Gadzhiagaev1, Maksat Kh. Gurbannazarov1
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21123" ["VALUE"]=> array(2) { ["TEXT"]=> string(379) "<p><sup>1</sup> First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia<br> <sup>2</sup> Russian R. R.Wreden Research Institute of Traumatology and Orthopedy, St. Petersburg, Russia<br> <sup>3</sup> Institute of Macromolecular Compounds, Russian Academy of Sciences, St. Petersburg, Russia</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(319) "1 First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
2 Russian R. R.Wreden Research Institute of Traumatology and Orthopedy, St. Petersburg, Russia
3 Institute of Macromolecular Compounds, Russian Academy of Sciences, St. Petersburg, Russia
Damage of peripheral nerves is often accompanied by a primary or secondary diastasis (gap, spread) between the neural ends, thus complicating a standard manual nerve stitching by means of surgical threads. As based on analysis of published data, the effective techniques were proposed for surgical treatment of peripheral nerve damage accompanied by diastasis. Moreover, some limitations of autoneural plastics are clearly revealed. Therefore, overcoming of nerve diastasis following damage remains to be a strong need, especially when treating prolonged and multiple defects of nerve trunks. Usage of implants providing repair and junction of the damaged nerve seems to be an alternative option allowing end-to-end connection of the damaged nerve from its central to distal segment. Application of biocompatible and bio-degradable polymers as a neural prosthesis promotes more safe regeneration and does not require switching-off a donor nerve and its functions. Moreover, the options are improved which allow to influence rates and quality of the nerve damage repair.
Keywords
Nerve, damage, diastasis, implant, polymeric scaffolds, chitosan.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21100" ["VALUE"]=> string(91) "Alternative approaches to overcome diastasis of damaged peripheral nerves. A review article" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(91) "Alternative approaches to overcome diastasis of damaged peripheral nerves. A review article" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21165" ["VALUE"]=> string(4) "1565" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1565" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21124" ["VALUE"]=> string(4) "1564" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1564" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(12) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21122" ["VALUE"]=> array(2) { ["TEXT"]=> string(557) "<p>Oleg V. Galibin<sup>1</sup>, German V. Medvedev<sup>2</sup>, Pavel V. Popryadukhin<sup>3</sup>, Pavel A. Kulagin<sup>1</sup>, Alexandr A. Gusev<sup>1</sup>, Galina P. Kossyakova<sup>1</sup>, Natalia V. Mikhailova<sup>1</sup>, Veronika D. Novak<sup>1</sup>, Denis N. Solomitskiy<sup>1</sup>, Igor O. Shemiakin<sup>1</sup>, Vadim S. Gadzhiagaev<sup>1</sup>, Maksat Kh. Gurbannazarov<sup>1</sup> </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(401) "Oleg V. Galibin1, German V. Medvedev2, Pavel V. Popryadukhin3, Pavel A. Kulagin1, Alexandr A. Gusev1, Galina P. Kossyakova1, Natalia V. Mikhailova1, Veronika D. Novak1, Denis N. Solomitskiy1, Igor O. Shemiakin1, Vadim S. Gadzhiagaev1, Maksat Kh. Gurbannazarov1
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(401) "Oleg V. Galibin1, German V. Medvedev2, Pavel V. Popryadukhin3, Pavel A. Kulagin1, Alexandr A. Gusev1, Galina P. Kossyakova1, Natalia V. Mikhailova1, Veronika D. Novak1, Denis N. Solomitskiy1, Igor O. Shemiakin1, Vadim S. Gadzhiagaev1, Maksat Kh. Gurbannazarov1
" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21164" ["VALUE"]=> array(2) { ["TEXT"]=> string(1284) "<p style="text-align: justify;">Damage of peripheral nerves is often accompanied by a primary or secondary diastasis (gap, spread) between the neural ends, thus complicating a standard manual nerve stitching by means of surgical threads. As based on analysis of published data, the effective techniques were proposed for surgical treatment of peripheral nerve damage accompanied by diastasis. Moreover, some limitations of autoneural plastics are clearly revealed. Therefore, overcoming of nerve diastasis following damage remains to be a strong need, especially when treating prolonged and multiple defects of nerve trunks. Usage of implants providing repair and junction of the damaged nerve seems to be an alternative option allowing end-to-end connection of the damaged nerve from its central to distal segment. Application of biocompatible and bio-degradable polymers as a neural prosthesis promotes more safe regeneration and does not require switching-off a donor nerve and its functions. Moreover, the options are improved which allow to influence rates and quality of the nerve damage repair. <p> <h2>Keywords</h2> <p style="text-align: justify;">Nerve, damage, diastasis, implant, polymeric scaffolds, chitosan. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1228) "Damage of peripheral nerves is often accompanied by a primary or secondary diastasis (gap, spread) between the neural ends, thus complicating a standard manual nerve stitching by means of surgical threads. As based on analysis of published data, the effective techniques were proposed for surgical treatment of peripheral nerve damage accompanied by diastasis. Moreover, some limitations of autoneural plastics are clearly revealed. Therefore, overcoming of nerve diastasis following damage remains to be a strong need, especially when treating prolonged and multiple defects of nerve trunks. Usage of implants providing repair and junction of the damaged nerve seems to be an alternative option allowing end-to-end connection of the damaged nerve from its central to distal segment. Application of biocompatible and bio-degradable polymers as a neural prosthesis promotes more safe regeneration and does not require switching-off a donor nerve and its functions. Moreover, the options are improved which allow to influence rates and quality of the nerve damage repair.
Keywords
Nerve, damage, diastasis, implant, polymeric scaffolds, chitosan.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(1228) "Damage of peripheral nerves is often accompanied by a primary or secondary diastasis (gap, spread) between the neural ends, thus complicating a standard manual nerve stitching by means of surgical threads. As based on analysis of published data, the effective techniques were proposed for surgical treatment of peripheral nerve damage accompanied by diastasis. Moreover, some limitations of autoneural plastics are clearly revealed. Therefore, overcoming of nerve diastasis following damage remains to be a strong need, especially when treating prolonged and multiple defects of nerve trunks. Usage of implants providing repair and junction of the damaged nerve seems to be an alternative option allowing end-to-end connection of the damaged nerve from its central to distal segment. Application of biocompatible and bio-degradable polymers as a neural prosthesis promotes more safe regeneration and does not require switching-off a donor nerve and its functions. Moreover, the options are improved which allow to influence rates and quality of the nerve damage repair.
Keywords
Nerve, damage, diastasis, implant, polymeric scaffolds, chitosan.
" } ["DOI"]=> array(37) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21099" ["VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-20-25" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-20-25" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-20-25" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21100" ["VALUE"]=> string(91) "Alternative approaches to overcome diastasis of damaged peripheral nerves. A review article" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(91) "Alternative approaches to overcome diastasis of damaged peripheral nerves. A review article" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(91) "Alternative approaches to overcome diastasis of damaged peripheral nerves. A review article" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21123" ["VALUE"]=> array(2) { ["TEXT"]=> string(379) "<p><sup>1</sup> First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia<br> <sup>2</sup> Russian R. R.Wreden Research Institute of Traumatology and Orthopedy, St. Petersburg, Russia<br> <sup>3</sup> Institute of Macromolecular Compounds, Russian Academy of Sciences, St. Petersburg, Russia</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(319) "1 First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
2 Russian R. R.Wreden Research Institute of Traumatology and Orthopedy, St. Petersburg, Russia
3 Institute of Macromolecular Compounds, Russian Academy of Sciences, St. Petersburg, Russia
1 First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
2 Russian R. R.Wreden Research Institute of Traumatology and Orthopedy, St. Petersburg, Russia
3 Institute of Macromolecular Compounds, Russian Academy of Sciences, St. Petersburg, Russia
Олег В. Галибин1, Герман В. Медведев2, Павел В. Попрядухин3, Павел А. Кулагин1, Александр А. Гусев1, Галина П. Косякова1, Наталья В. Михайлова1, Вероника Д. Новак1, Денис Н. Соломицкий1, Игорь О. Шемякин1, Вадим С. Гаджиагаев1, Максат Х. Гурбанназаров1
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(573) "Олег В. Галибин1, Герман В. Медведев2, Павел В. Попрядухин3, Павел А. Кулагин1, Александр А. Гусев1, Галина П. Косякова1, Наталья В. Михайлова1, Вероника Д. Новак1, Денис Н. Соломицкий1, Игорь О. Шемякин1, Вадим С. Гаджиагаев1, Максат Х. Гурбанназаров1
" } ["SUBMITTED"]=> array(37) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21108" ["VALUE"]=> string(10) "26.11.2018" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "26.11.2018" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "26.11.2018" } ["ACCEPTED"]=> array(37) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21109" ["VALUE"]=> string(10) "15.03.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "15.03.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "15.03.2019" } ["CONTACT"]=> array(38) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21086" ["VALUE"]=> string(3) "525" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(3) "525" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(58) "Oleg V. Galibin" ["LINK_ELEMENT_VALUE"]=> bool(false) } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21163" ["VALUE"]=> array(2) { ["TEXT"]=> string(2612) "<p style="text-align: justify;">Повреждение периферических нервов нередко сопровождается значительным диастазом (первичным или вторичным) между концами поврежденного нерва, что затрудняет выполнение стандартного ручного шва нерва с помощью хирургических нитей. На основании анализа данных опубликованных исследований выявлены эффективные способы хирургического лечения повреждений периферических нервов с диастазом. Кроме того, достоверно выявлены недостатки метода аутоневральной пластики, в связи с чем проблема преодоления диастаза поврежденного периферического нерва остается актуальной и в настоящее время, особенно при протяженных и множественных дефектах нервных стволов. Альтернативным вариантом в решении данной проблемы может служит использование имплантов, позволяющих соединить концы поврежденного нерва и способствующих прорастанию нервных волокон из центрального в периферический отросток поврежденного нерва. Использование биосовместимых и биодеградируемых полимеров в качестве неврального протеза способствует более безопасной регенерации и не требует выключения донорского нерва и связанной с ним функции, кроме того, разработаны и продолжают совершенствоваться опции, позволяющие влиять на скорость и качество регенерации поврежденного периферического нерва. </p> <h2>Ключевые слова</h2> <p style="text-align: justify;">Нерв, травма, диастаз, имплант, полимерная основа, хитозан. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2556) "Повреждение периферических нервов нередко сопровождается значительным диастазом (первичным или вторичным) между концами поврежденного нерва, что затрудняет выполнение стандартного ручного шва нерва с помощью хирургических нитей. На основании анализа данных опубликованных исследований выявлены эффективные способы хирургического лечения повреждений периферических нервов с диастазом. Кроме того, достоверно выявлены недостатки метода аутоневральной пластики, в связи с чем проблема преодоления диастаза поврежденного периферического нерва остается актуальной и в настоящее время, особенно при протяженных и множественных дефектах нервных стволов. Альтернативным вариантом в решении данной проблемы может служит использование имплантов, позволяющих соединить концы поврежденного нерва и способствующих прорастанию нервных волокон из центрального в периферический отросток поврежденного нерва. Использование биосовместимых и биодеградируемых полимеров в качестве неврального протеза способствует более безопасной регенерации и не требует выключения донорского нерва и связанной с ним функции, кроме того, разработаны и продолжают совершенствоваться опции, позволяющие влиять на скорость и качество регенерации поврежденного периферического нерва.
Ключевые слова
Нерв, травма, диастаз, имплант, полимерная основа, хитозан.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2556) "Повреждение периферических нервов нередко сопровождается значительным диастазом (первичным или вторичным) между концами поврежденного нерва, что затрудняет выполнение стандартного ручного шва нерва с помощью хирургических нитей. На основании анализа данных опубликованных исследований выявлены эффективные способы хирургического лечения повреждений периферических нервов с диастазом. Кроме того, достоверно выявлены недостатки метода аутоневральной пластики, в связи с чем проблема преодоления диастаза поврежденного периферического нерва остается актуальной и в настоящее время, особенно при протяженных и множественных дефектах нервных стволов. Альтернативным вариантом в решении данной проблемы может служит использование имплантов, позволяющих соединить концы поврежденного нерва и способствующих прорастанию нервных волокон из центрального в периферический отросток поврежденного нерва. Использование биосовместимых и биодеградируемых полимеров в качестве неврального протеза способствует более безопасной регенерации и не требует выключения донорского нерва и связанной с ним функции, кроме того, разработаны и продолжают совершенствоваться опции, позволяющие влиять на скорость и качество регенерации поврежденного периферического нерва.
Ключевые слова
Нерв, травма, диастаз, имплант, полимерная основа, хитозан.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21162" ["VALUE"]=> array(2) { ["TEXT"]=> string(563) "<p><sup>1</sup> Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова <br> <sup>2</sup> Российский НИИ травматологии и ортопедии им. Р. Р. Вредена, Санкт-Петербург, Россия<br> <sup>3</sup> Институт высокомолекулярных соединений РАН, Санкт-Петербург, Россия </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(503) "1 Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова
2 Российский НИИ травматологии и ортопедии им. Р. Р. Вредена, Санкт-Петербург, Россия
3 Институт высокомолекулярных соединений РАН, Санкт-Петербург, Россия
1 Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова
2 Российский НИИ травматологии и ортопедии им. Р. Р. Вредена, Санкт-Петербург, Россия
3 Институт высокомолекулярных соединений РАН, Санкт-Петербург, Россия
Introduction
Myelodysplastic syndrome (MDS) is a heterogeneous group of clonal bone marrow disorders characterized by ineffective hematopoiesis, and increased propensity to evolve to acute myeloid leukemia (AML). Currently allogeneic hematopoietic stem cell transplantation (allo-HSCT) is the only treatment option with curative potential in MDS patients. However, allo-HSCT is associated with risk of significant toxicity – 1-year non-relapse mortality (NRM) is reaching 17% to 25% [1, 2]. Thereby transplant- and disease-related risks should be carefully weighed against the benefits of transplantation. Several prognostic scoring indexes such as International prognostic scoring system (IPSS) [3], revised IPSS [4], WHO-classification-based IPSS (WPSS) [5] are widely used to predict MDS disease course and optimize timing of allo-HSCT according to disease related factors. Allo-HSCT is indicated in patients with high/very high and even in very low/ low or intermediate IPSS-R risk with poor features (poor risk cytogenetics, life-threatening cytopenias, severe transfusion dependence and persistently increasing blast count) [6]. Multiparametric prognostic models IPSS, WPSS and IPSS-R were developed to assess disease risk at diagnosis. In contrast disease related index (DRI) [7] and prognostic models defined by Kroeger et al. [8] and Armand et al. [9] were designed directly for the posttransplant outcome evaluation. Patient-related risk factors such as comorbidities and age should be also taken into consideration. They are included in several prognostic scoring systems such as EBMT score [10], Pretransplant Assessment of Mortality score (PAM) [11] or Hematopoietic Cell Transplantation-specific Comorbidity Index HCT-CI [12]. Here we evaluate aforementioned disease- and transplant-related prognostic indexes in MDS patients treated with allo-HSCT in one center.
Patients and methods
All consecutive primary allogeneic transplants performed for the diagnosis MDS in the time period 2002-2018 and complete information to calculate all of the prognostic indexes were included in the analysis. Pediatric patients and patients transformed to AML were excluded. Main patient characteristics, transplantation parameters, outcomes and complications are summarized in Table 1.
Median of age was 44 years (range 18-67). Twenty four percent of patients were grafted from a matched related donor, and 73% were transplanted from the 9-10/10 HLA-matched unrelated donors. MDS with excess blasts I or II was documented in seventy-six percent of the patients. Twenty-two percent were treated with hypomethylating drugs before transplant. Conditioning regimen was myeloablative in 1/4 of patients, and consisted of oral busulfan 16 mg/kg and cyclophosphamide 120 mg/kg. Reduced-intensity conditioning comprised fludarabine 180 mg/m2 and oral busulfan 8-10 mg/kg. The reduced-intensity conditioning was used in all the patients after first analysis of the RICMAC trial [2] in 2012. Graft-versus-host disease (GVHD) prophylaxis included posttransplant cyclophosphamide in 37% of patients, while the rest of them received calcineurin-based prophylaxis with short-course methotrexate, or mycophenolate mofetil and antithymocyte globulin in case of unrelated grafts.
Table 1. Patient characteristics and overall transplantation outcomes




Clinical outcomes
Time-to-disease relapse, acute GVHD (aGVHD), moderate to severe GVHD (chGVHD), non-relapse mortality (NRM), overall survival (OS), event-free survival (EFS), and GVHD-relapse free survival (GRFS) were defined as the time from transplantation to the event. Graft failure without evidence of the disease after transplantation was not considered an event. Patients were censored at the time of last contact or a second transplantation for all outcomes. The disease relapse was defined as morphologic or cytogenetic evidence of disease with pre-transplant characteristics. Disease staging, including bone marrow aspirate, was routinely performed on days +30,+60,+100, +180, +365 post-transplant. Primary graft failure was defined as the complete absence of donor chimerism in bone marrow aspirate by day +40. Time to engraftment was calculated as time from HSCT to unsupported neutrophil count >500/ul and white blood cell count >1000/ul for 3 consecutive days. Toxicity was assessed with CTCAE ver. 4.03. Sepsis and severe sepsis were diagnosed based on International Guidelines for Management of Severe Sepsis and Septic Shock [13]. Invasive mycosis was diagnosed in case of probable or proven infection according to EORTC/MSG guidelines [14]. HCT-CI [12], DRI [7], IPSS [3], IPSS-R [4], WPSS [5], PAM [11], Armand et al. risk score [9], Kroeger et al. risk score [8] were calculated based on the published scoring systems.
Statistical Analysis
All tests were two-sided, and differences with p values less than 0.05 were considered significant. The difference in grading between indexes was accessed using Friedman test. The survival distributions for OS, EFS, GRFS were calculated using Kaplan-Meier methodology with 95% confidence intervals. Appropriate survival curves are provided in Supplementary files (see online version) Cumulative incidence analysis with competing risks was used for relapse and NRM. Five-year OS was used as an outcome to test all prognostic systems, because most of them were created based overall survival with follow up for 5 years and more [3, 4, 5, 9]. The univariate comparisons were made using the log-rank test. Proportional hazard modeling was used for the multivariate analysis. Based on the number of events 3 most significant factors from univariate analysis were included in the model. The MDS risk indexes were added in the series of tests. The final multivariate confidence intervals are the result of meta-analysis with fixed effect modeling. The heterogeneity of confidence intervals was tested with Cochran Q test. The C-statistic for the predictive factors was produced from logistic regression with death during five years after transplantation as an outcome. The predictive values were presented as area under the curve (AUC) with confidence intervals. Analyses were conducted in R 3.4.1 and SAS 9.3 (SAS Institute, Inc.).
Results
Distribution of patients by different scoring systems
We analyzed the distribution of patients by disease specific scoring systems such as IPSS, WPSS and IPSS-R and MDS prognostic indexes for patients undergoing allo-HSCT developed by Kroeger et al. and Armand et al. (Fig. 1). Fifty-four percent of patients were transplanted in high or very high IPSS-R risk. Forty-eight percent of patients with high/very high WPSS or IPSS-R risk were reclassified into intermediate risk according to pretransplant Kroeger et al. MDS score and 60% into intermediate risk, according to pretransplant Armand et al. score. There was a difference between disease- and pretransplant prognostic systems especially in distinction between high/very high and intermediate risk (p<0.001).

Figure 1. Distribution of patients by different prognostic scoring systems
Clinical outcomes
Platelet and leukocyte engraftment was documented in 48 (81%) of patients. Primary graft failure was observed in six cases (10%). Four patients out of them died (in one case, due to disease progression, and three patients deceased due to infections). The median time to leukocyte engraftment was 18 days (range 11-30), neutrophil engraftment, 20 days (range 10-30), platelet engraftment, 17 days (range 11-130). Overall, 50% of patients developed aGVHD with severe aGVHD grade 3-4 registered only in 15% of cases. The rate of chronic GVHD was 30%, which proved to be extensive in 28% of the patients (Table 1).
Cumulative incidence of relapse at 5 years was 37% (95% CI 25-57%). The cumulative incidence of non-relapse mortality (NRM) at 1 year was 25% (95% CI 16-40%). Thirty patients died during the follow-up study. The main reasons of death were disease progression or relapse in 26%; GVHD, 26%; infections, 37%; hemorrhagic events, 7%; acute myocardial infarction, in 4% of cases.
With a median follow-up of 36 months (range 3 to 135), the 5-year OS, EFS and GRFS was 34%, 33% and 29%, respectively. In univariate analysis, the significant factors for prolonged OS were as follows: aGVHD grade 1-2 (62% vs 18% p=0.004), quantities of donor СD34+ cells (p=0.006), and absence of septic episodes before engraftment (44 % vs 17%, p=0.003). The disease-specific prognostic indexes (IPSS, WPSS, IPSS-R), and transplant comorbidity indexes (PAM, EBMT, HCT-CI) did not predict OS . However, differences in OS rates between the risk groups according to disease-related prognostic systems such as Disease-Related Index, DRI (p=0.049), and risk score by Kroeger et al. (p=0.071) have shown a trend towards statistical significance (Supplement, Fig. 1-7. The supplemental files could be found in electronic version of this paper at www.cttjournal.com). The 5-year OS in low risk group, according to transplant risk score proposed by Kroeger et al. was 61%, thus being significantly higher compared to intermediate and high/very high risk – 26% (p=0.041). Surprisingly, we found no difference in OS between intermediate and high/very high risk groups (28% and 22%, respectively). This might be a reason for the failure of the index used by Kroeger et al. to achieve statistical significance. Interestingly, that the causes of death were nearly the same in both risk groups, i.e., ca. 50% of patients died due to transplant related factors.
ROC analysis shows influence of different prognostic systems and factors upon OS in the MDS patients. Amount of transplanted CD34+ donor cells proved to be the only factor which significantly affected transplant outcome (p=0.006) in this analysis (Fig. 2).

Figure 2. Influence of different prognostic systems and factors on OS in MDS patients, receiver-operating-curve (ROC) analysis
Note: C-statistics for the potential predictors of overall survival. Results of the ROC analysis treated in logistic regression with 5-year overall survival as an outcome. The non-significant parameters (p>0.05) are shown in grey. The significant (p<0.05) parameters are shown in black. The 95% confidence intervals of sensitivity and specificity are produced from individual results of all the parameters tested. C-statistic values of the variables were: CD34 positive cells in the graft 0.7080 (95% CI 0.5740-0.8421), Kroger et al. 0.5862 (95% CI 0.4391-0.7333), Armand et al. 0.5339 (95% CI 0.3850-0.6828), IPSS 0.5534 (95% CI 0.4121-0.6948), WPSS 0.5672 (95% CI 0.4354-0.6991), IPSS-R 0.5885 (0.4430-0.7340), DRI 0.5747 (0.4429-0.7065), EBMT 0.5230 (0.3758-0.6702), serum ferritin 0.4500 (0.2861-0.6139), PAM index 0.5584 (0.4037-0.7131), CRP before conditioning 0.4845 (0.3234-0.6456).
However, only presence of aGVHD grade 1-2 (p=0.013), absence of septic episodes (p=0.006), and DRI (p=0.037) retained their statistical significance in the multivariate analysis (Fig. 3). Other prognostic scores, except of DRI, did not show a statistical significance.

Figure 3. Analysis of the prognostic value of risk indexes in the multivariate model
Note: Multivariate analysis of overall survival. Acute GVHD, graft CD34+ cells and sepsis in aplasia were included based on univariate selection of the most predictive variables. The indexes were added as the fourth co-variable separately in a series of tests. The cumulative confidence intervals for the clinical variables were produced with fixed effect model from the individual hazards in the series.
Discussion
The major question in every MDS patient with currently existing treatments is whether he will benefit from allo-HSCT. Despite the fact that all existing treatments in most cases lead to only temporary responses, the results of allo-HSCT in MDS unfortunately are also one of the most disappointing compared to other diseases [15]. According to our 5-year observation data, the OS level in allotransplanted MDS patients is 34%. The other studies are showing nearly the same results: from 45% to 37% [1, 16]. This is due to relatively high NRM [3], but also due to high relapse rate [2, 17]. Currently used indexes of the natural course of the disease such as IPSS, WPSS, IPSS-R are established to evaluate risk of death and transformation to acute myeloid leukemia in untreated MDS patients [3, 4, 5]. All of these indexes are well validated in large patient cohorts [17]. However, their role in predicting the outcome after allo-HSCT is not so well defined.
Lee et al. [18] evaluated prognostic impact of IPSS before allo-HSCT. The authors showed significant differences in OS after allo-HSCT between low/intermediate and intermediate/high groups. Further it was shown that WPSS has a relevant prognostic value in posttransplant outcome of patients with MDS [19]. Modified prognostic model IPSS-R was assessed pre-transplant as a predictor of transplant outcome by C. Scheid et al. [20]. In that study, IPSS-R significantly influenced OS after allo-HSCT, but OS in high and intermediate groups were comparable: 47% and 44%, respectively. This was due to high and comparable NRM in these groups. In our study we have also observed high NRM in the favorable prognostic groups based on IPSS or IPSS-R.
The potential causes for early mortality in this group are relatively well discussed in the literature. They include primary graft failure [21], iron overload which results in higher incidence of liver veno-occlusive disease [22] and infectious complications [23]. It should be noted that, according to our data, the rate of primary graft failure is 10% being considered relatively high. The incidence of graft failure varies from 2 to 13% [2, 16, 24]. We didn’t find any correlation between rate of graft failure and type of stem cell source or rate of СD34+ cells in the graft, as reported in previous studies [21]. According to the results of large study by Olsson et al. [21], MDS diagnosis itself is associated with increased risk of graft failure, along with other hematologic malignancies, e.g., myeloproliferative disorders and chronic lymphocytic leukemia. Poor graft function may be another documented cause of NRM that leads to increased incidence of opportunistic infections and hemorrhagic complications [25]. Thus, high NRM rate was the main reason of non-significant predictive value of classical indexes after allo-HSCT found in our study.
A number of indexes accounting for NRM based on previous treatment burden, like as duration of the disease in EBMT index, or comorbidity burden, like in HCT-CI, or prediction of viral reactivations based on serological markers, like in PAM. However, there are conflicting results about influence of the comorbidity indexes on OS in MDS patients. Guilfoyle et al. did not find associations between HCT-CI and OS in MDS patients [26]. On the other hand, a large retrospective study showed that EBMT score accurately predicted OS and NRM [27]. In the present study, we have not observed any predictive impact of these indexes on the disease outcome. The published data and results of our study indicate that biological mechanisms behind NRM might be in certain cases different in MDS compared to the other diseases [28].
Several new prognostic indexes have been recently developed aiming for precise evaluation of transplant outcome in MDS patients. Kroeger et al. have combined the disease-related factors (cytogenetics, blood blasts, and platelets) and patient-related factors (performance status and age) into a common prognostic system [8]. Armand et al. added ferritin level and type of a conditioning regimen to the disease-related risk factors [9]. The disease risk index was another prognostic system evaluated in our study. It includes cytogenetics and remission status of MDS patients at transplant [7]. These indexes, except of DRI, were assessed in large data sets to specifically account for the risk of relapse and the risk of NRM. There is only a limited number of studies validating these indexes [29]. Interestingly, about half of IPSS-R high/very high risk patients were reclassified as more favorable category, the intermediate-1, according to risk score by Kroeger et al. and Armand et al. [8, 9]. Thereby, the disease- and transplant-specific scoring systems determine the transplant outcome in different ways. According to our data, only DRI significantly influenced OS values among all the mentioned prognostic scores. In our study, these transplant-specific indexes were shown to define well the group with good prognosis and adverse prognosis. However, we observed that clinical prognosis for the intermediate group proved to be as adverse as for the high-risk patients.
Thus, our study indicates that current prognostic indexes do not well define the intermediate prognosis. It is likely that most of the heterogeneity of the disease fall into this category, including patients with stromal and miRNA signaling deficiency [30], pyroptosis of hematopoietic stem cells [31], certain mutations without cytogenetic abnormalities [32]. Any of these pathogenetic variants might manifest in different mechanisms of NRM and relapse risk. Pooling the patients into large cohorts alleviate these differences by creation of risk indexes. However, small-group or individual prediction might not be so accurate, due to the causes mentioned above. Thus, future development of indexes and predictive systems for allo-HSCT should incorporate molecular data, at least, for the intermediate risk groups in MDS.
Conclusion
our relatively small single-center study, we have observed little predictive value of currently existing scoring systems, particularly due to adverse results in the intermediate risk patients. Further characterization of this “intermediate” patents is required to broaden the clinical application of the scoring systems for individual treatment planning.
Acknowledgments
We thank our patients, research and medical staff for making this study possible. This work was done as part of Russian Science Foundation grant №17-75-20145.
Disclosure statement
Authors confirm the absence of any conflicts of interests.
References
- Luger SM, Ringdén O, Zhang MJ, Pérez WS, Bishop MR, Bornhauser M, Bredeson CN, Cairo MS, Copelan EA, Gale RP, Giralt SA, Gulbas Z, Gupta V, Hale GA, Lazarus HM, et al. Similar outcomes using myeloablative vs reduced-intensity allogeneic transplant preparative regimens for AML or MDS. Bone Marrow Transplant. 2012;47(2):203-211.
- Kröger N, Iacobelli S, Franke GN, Platzbecker U, Uddin R, Hübel K, Scheid C, Weber T, Robin M, Stelljes M, Afanasyev B, Heim D, Deliliers GL, Onida F, Dreger P, et al. Dose-reduced versus standard conditioning followed by allogeneic stem-cell transplantation for patients with myelodysplastic syndrome: a prospective randomized phase III study of the EBMT (RICMAC Trial). J Clin Oncol. 2017;35(19):2157-2164.
- Greenberg P, Cox C, LeBeau MM, Fenaux P, Morel P, Sanz G, Sanz M, Vallespi T, Hamblin T, Oscier D, Ohyashiki K, Toyama K, Aul C, Mufti G, Bennett J. International scoring system for evaluating prognosis in myelodysplastic syndromes. Blood. 1997;89(6):2079-2088.
- Greenberg PL, Tuechler H, Schanz J, Sanz G, Garcia- Manero G, Solé F, Bennett JM, Bowen D, Fenaux P, Dreyfus F, Kantarjian H, Kuendgen A, Levis A, Malcovati L, Cazzola M, et al. Revised international prognostic scoring system for myelodysplastic syndromes. Blood. 2012; 120(12):2454-2465.
- Malcovati L, Germing U, Kuendgen A, Della Porta MG, Pascutto C, Invernizzi R, Giagounidis A, Hildebrandt B, Bernasconi P, Knipp S, Strupp C, Lazzarino M, Aul C, Cazzola M., et al. Time-dependent prognostic scoring system for predicting survival and leukemic evolution in myelodysplastic syndromes. J Clin Oncol. 2007;25(23):3503-3510.
- de Witte T, Bowen D, Robin M, Malcovati L, Niederwieser D, Yakoub-Agha I, Mufti GJ, Fenaux P, Sanz G, Martino R, Alessandrino EP, Onida F, Symeonidis A, Passweg J, Kobbe G, Ganser A, et al. Allogeneic hematopoietic stem cell transplantation for MDS and CMML: recommendations from an international expert panel. Blood. 2017;129(13):1753-1762.
- Armand P, Kim HT, Logan BR, Wang Z, Alyea EP, Kalaycio ME, Maziarz RT, Antin JH, Soiffer RJ, Weisdorf DJ, Rizzo JD, Horowitz MM, Saber W, et al. Validation and refinement of the Disease Risk Index for allogeneic stem cell transplantation. Blood. 2014;123(23):3664-3671.
- Gagelmann N, Eikema DJ, Stelljes M, Beelen D, de Wreede L, Mufti G, Knelange NS, Niederwieser D, Friis LS, Ehnninger G, Nagler A, Yakoub-Agha I, Meijer E, Ljungman P, Maertens J, et al. Optimized EBMT transplant-specific risk score in myelodysplastic syndromes after allogeneic stem-cell transplantation. Haematologica. 2019. pii: haematol.2018.200808. doi: 10.3324/haematol.2018.200808.
- Armand P, Kim HT, Cutler CS, Ho VT, Koreth J, Ritz J, Alyea EP, Antin JH, Soiffer RJ. A prognostic score for patients with acute leukemia or myelodysplastic syndromes undergoing allogeneic stem cell transplantation. Biol Blood Marrow Transplant. 2008;14(1):28-35.
- Gratwohl A. The EBMT risk score. Bone Marrow Transplant. 2012;47(6):749-756.
- Au BK, Gooley TA, Armand P, Fang M, Madtes DK, Sorror ML, Boeckh MJ, Gibson CJ, Deeg HJ, Storb R, Appelbaum FR, Chien JW, Martin PJ. Reevaluation of the Pretransplant Assessment of Mortality score after allogeneic hematopoietic transplantation. Biol Blood Marrow Transplant. 2015;21(5):848-854.
- Sorror ML, Maris MB, Storb R, Baron F, Sandmaier BM, Maloney DG, Storer B. Hematopoietic cell transplantation (HCT)-specific comorbidity index: a new tool for risk assessment before allogeneic HCT. Blood. 2005;106(8):2912-2919.
- Singer M, Deutschman CS, Seymour CW, Shankar-Hari M, Annane D, Bauer M, Bellomo R, Bernard GR, Chiche JD, Coopersmith CM, Hotchkiss RS, Levy MM, Marshall JC, Martin GS, Opal SM, et al. The third international consensus definitions for sepsis and septic shock. JAMA. 2016;315(8):801-810.
- De Pauw B, Walsh TJ, Donnelly JP, Stevens DA, Edwards JE, Calandra T, Pappas PG, Maertens J, Lortholary O, Kauffman CA, Denning DW, Patterson TF, Maschmeyer G, Bille J, Dismukes WE, et al. Revised definitions of invasive fungal disease from the European Organization for Research and Treatment of Cancer/invasive fungal infections cooperative group and the National Institute of Allergy and Infectious Diseases Mycoses Study Group (EORTC/MSG) Consensus Group. Clin Infect Dis. 2008;46(12):1813-1821.
- Raiola A, Dominietto A, Varaldo R, Ghiso A, Galaverna F, Bramanti S, Todisco E, Sarina B, Giordano L, Ibatici A, Santoro A, Clavio M, Bacigalupo A, Castagna L. Unmanipulated haploidentical BMT following non-myeloablative conditioning and post-transplantation CY for advanced Hodgkin’s lymphoma. Bone Marrow Transplant. 2014;49(2):190-194.
- Litzow MR, Tarima S, Pérez WS, Bolwell BJ, Cairo MS, Camitta BM, Cutler CS, de Lima M, Dipersio JF, Gale RP, Keating A, Lazarus HM, Luger S, Marks DI, Maziarz RT, et al. Allogeneic transplantation for therapy-related myelodysplastic syndrome and acute myeloid leukemia. Blood. 2016;115(9):1850-1858.
- Della Porta MG, Tuechler H, Malcovati L, Schanz J, Sanz G, Garcia-Manero G, Solé F, Bennett JM, Bowen D, Fenaux P, Dreyfus F, Kantarjian H, Kuendgen A, Levis A, Cermak J, et al. Validation of WHO classification-based Prognostic Scoring System (WPSS) for myelodysplastic syndromes and comparison with the revised International Prognostic Scoring System (IPSS-R). A study of the International Working Group for Prognosis in Myelodysplasia (IWG-PM). Leukemia. 2015;29(7):1502-1513.
- Lee JH, Lee JH, Lim SN, Kim DY, Kim SH, Lee YS, Kang YA, Kang SI, Jeon MJ, Seol M, Seo EJ, Chi HS, Park CJ, Jang S, Yun SC, et al. Allogeneic hematopoietic cell transplantation for myelodysplastic syndrome: Prognostic significance of pre-transplant IPSS score and comorbidity. Bone Marrow Transplant. 2010;45(3):450-457.
- Alessandrino EP, Della Porta MG, Bacigalupo A, Van Lint MT, Falda M, Onida F, Bernardi M, Iori AP, Rambaldi A, Cerretti R, Marenco P, Pioltelli P, Malcovati L, Pascutto C, Oneto R, et al. WHO classification and WPSS predict posttransplantation outcome in patients with myelodysplastic syndrome: a study from the Gruppo ItalianoTrapianto di Midollo Osseo (GITMO). Blood.2008;112(3):895-902.
- Scheid C, de Wreede L, van Biezen A, Koenecke C, Göhring G, Volin L, Maertens J, Finke J, Passweg J, Beelen D, Cornelissen JJ, Itälä-Remes M, Chevallier P, Russell N, Petersen E, et al. Validation of the revised IPSS at transplant in patients with myelodysplastic syndrome/transformed acute myelogenous leukemia receiving allogeneic stem cell transplantation: A retrospective analysis of the EBMT chronic malignancies working party. Bone Marrow Transplant. 2017;52(11):1519-1525.
- Olsson RF, Logan BR, Chaudhury S, Zhu X, Akpek G, Bolwell BJ, Bredeson CN, Dvorak CC, Gupta V, Ho VT, Lazarus HM, Marks DI, Ringdén OT, Pasquini MC, Schriber JR, et al. Primary graft failure after myeloablative allogeneic hematopoietic cell transplantation for hematologic malignancies Leukemia. 2015;29(8):1754-1762.
- Armand P, Kim HT, Cutler CS, Ho VT, Koreth J, Alyea EP, Soiffer RJ, Antin JH. Prognostic impact of elevated pretransplantation serum ferritin in patients undergoing myeloablative stem cell transplantation. Blood. 2007;109(10):4586-4588.
- Shaheen M, Ivanova MO, Moiseev IS, Bondarchuk SV, Afanasyev BV. Impact of initial serum ferritin on early post-HSCT complications: A single-center study. Cell Ther Transplant. 2016;5(2):40-48.
- Castro-Malaspina H, Harris RE, Gajewski J, Ramsay N, Collins R, Dharan B, King R, Deeg HJ. Unrelated donor marrow transplantation for myelodysplastic syndromes: Outcome analysis in 510 transplants facilitated by the National Marrow Donor Program. Blood.2002;99(6):1943-1951.
- Shimomura Y, Hara M, Katoh D, Hashimoto H, Ishikawa T. Enlarged spleen is associated with low neutrophil and platelet engraftment rates and poor survival after allogeneic stem cell transplantation in patients with acute myeloid leukemia and myelodysplastic syndrome. Ann Hematol. 2018;97(6):1049-1056.
- Guilfoyle R, Demers A, Bredeson C, Richardson E, Rubinger M, Szwajcer D, Seftel MD. Performance status, but not the Hematopoietic Cell Transplantation Comorbidity Index (HCT-CI), predicts mortality at a Canadian transplant center. Bone Marrow Transplant. 2009;43(2):133-139.
- Lozano S, Olavarria E, Iacobelli S, van Biezen A, Beelen DW, Finke J, Mufti GJ, Niederwieser D, Ehninger G, Ganser A, Stuhler G, Maertens J, Bacigalupo A, Volin L, Nagler A et al. The EBMT score predicts transplant related mortality and overall survival after allogeneic stem cell transplantation for myelodysplastic syndromes [Abstract]. Proc ASH. 2015, 3223.
- Ferrer RA, Wobus M, List C, Wehner R, Schönefeldt C, Brocard B, Mohr B, Rauner M, Schmitz M, Stiehler M, Ehninger G, Hofbauer LC, Bornhäuser M, Platzbecker U. Mesenchymal stromal cells from patients with myelodyplastic syndrome display distinct functional alterations that are modulated by lenalidomide. Haematologica. 2013;98(11):1677-1685.
- Beauverd Y, Roosnek E, Tirefort Y, Nagy-Hulliger M, Bernimoulin M, Tsopra O, Ansari M, Dantin C, Casini A, Grandjean AP, Chigrinova E, Masouridi-Levrat S, Chalandon Y. Validation of the disease risk index for outcome of patients undergoing allogeneic hematopoietic stem cell transplantation after T cell depletion. Biol Blood Marrow Transplant. 2014;20(9):1322-1328.
- Zhao Y, Wu D, Fei C, Guo J, Gu S, Zhu Y, Xu F, Zhang Z, Wu L, Li X, Chang C. Down-regulation of Dicer1 promotes cellular senescence and decreases the differentiation and stem cell-supporting capacities of mesenchymal stromal cells in patients with myelodysplastic syndrome. Haematologica. 2015;100(2):194-204.
- Basiorka AA, McGraw KL, Eksioglu EA, Chen X, Johnson J, Zhang L, Zhang Q, Irvine BA, Cluzeau T, Sallman DA, Padron E, Komrokji R, Sokol L, Coll RC, Robertson AA, et al. The NLRP3 inflammasome functions as a driver of the myelodysplastic syndrome phenotype. Blood. 2016;128(25):2960-2975.
- Yoshizato T, Nannya Y, Atsuta Y, Shiozawa Y, Iijima- Yamashita Y, Yoshida K, Shiraishi Y, Suzuki H, Nagata Y, Sato Y, Kakiuchi N, Matsuo K, Onizuka M, Kataoka K, Chiba K, et al. Genetic abnormalities in myelodysplasia and secondary acute myeloid leukemia: impact on outcome of stem cell transplantation. Blood. 2017;129(17):2347-2358.
Introduction
Myelodysplastic syndrome (MDS) is a heterogeneous group of clonal bone marrow disorders characterized by ineffective hematopoiesis, and increased propensity to evolve to acute myeloid leukemia (AML). Currently allogeneic hematopoietic stem cell transplantation (allo-HSCT) is the only treatment option with curative potential in MDS patients. However, allo-HSCT is associated with risk of significant toxicity – 1-year non-relapse mortality (NRM) is reaching 17% to 25% [1, 2]. Thereby transplant- and disease-related risks should be carefully weighed against the benefits of transplantation. Several prognostic scoring indexes such as International prognostic scoring system (IPSS) [3], revised IPSS [4], WHO-classification-based IPSS (WPSS) [5] are widely used to predict MDS disease course and optimize timing of allo-HSCT according to disease related factors. Allo-HSCT is indicated in patients with high/very high and even in very low/ low or intermediate IPSS-R risk with poor features (poor risk cytogenetics, life-threatening cytopenias, severe transfusion dependence and persistently increasing blast count) [6]. Multiparametric prognostic models IPSS, WPSS and IPSS-R were developed to assess disease risk at diagnosis. In contrast disease related index (DRI) [7] and prognostic models defined by Kroeger et al. [8] and Armand et al. [9] were designed directly for the posttransplant outcome evaluation. Patient-related risk factors such as comorbidities and age should be also taken into consideration. They are included in several prognostic scoring systems such as EBMT score [10], Pretransplant Assessment of Mortality score (PAM) [11] or Hematopoietic Cell Transplantation-specific Comorbidity Index HCT-CI [12]. Here we evaluate aforementioned disease- and transplant-related prognostic indexes in MDS patients treated with allo-HSCT in one center.
Patients and methods
All consecutive primary allogeneic transplants performed for the diagnosis MDS in the time period 2002-2018 and complete information to calculate all of the prognostic indexes were included in the analysis. Pediatric patients and patients transformed to AML were excluded. Main patient characteristics, transplantation parameters, outcomes and complications are summarized in Table 1.
Median of age was 44 years (range 18-67). Twenty four percent of patients were grafted from a matched related donor, and 73% were transplanted from the 9-10/10 HLA-matched unrelated donors. MDS with excess blasts I or II was documented in seventy-six percent of the patients. Twenty-two percent were treated with hypomethylating drugs before transplant. Conditioning regimen was myeloablative in 1/4 of patients, and consisted of oral busulfan 16 mg/kg and cyclophosphamide 120 mg/kg. Reduced-intensity conditioning comprised fludarabine 180 mg/m2 and oral busulfan 8-10 mg/kg. The reduced-intensity conditioning was used in all the patients after first analysis of the RICMAC trial [2] in 2012. Graft-versus-host disease (GVHD) prophylaxis included posttransplant cyclophosphamide in 37% of patients, while the rest of them received calcineurin-based prophylaxis with short-course methotrexate, or mycophenolate mofetil and antithymocyte globulin in case of unrelated grafts.
Table 1. Patient characteristics and overall transplantation outcomes




Clinical outcomes
Time-to-disease relapse, acute GVHD (aGVHD), moderate to severe GVHD (chGVHD), non-relapse mortality (NRM), overall survival (OS), event-free survival (EFS), and GVHD-relapse free survival (GRFS) were defined as the time from transplantation to the event. Graft failure without evidence of the disease after transplantation was not considered an event. Patients were censored at the time of last contact or a second transplantation for all outcomes. The disease relapse was defined as morphologic or cytogenetic evidence of disease with pre-transplant characteristics. Disease staging, including bone marrow aspirate, was routinely performed on days +30,+60,+100, +180, +365 post-transplant. Primary graft failure was defined as the complete absence of donor chimerism in bone marrow aspirate by day +40. Time to engraftment was calculated as time from HSCT to unsupported neutrophil count >500/ul and white blood cell count >1000/ul for 3 consecutive days. Toxicity was assessed with CTCAE ver. 4.03. Sepsis and severe sepsis were diagnosed based on International Guidelines for Management of Severe Sepsis and Septic Shock [13]. Invasive mycosis was diagnosed in case of probable or proven infection according to EORTC/MSG guidelines [14]. HCT-CI [12], DRI [7], IPSS [3], IPSS-R [4], WPSS [5], PAM [11], Armand et al. risk score [9], Kroeger et al. risk score [8] were calculated based on the published scoring systems.
Statistical Analysis
All tests were two-sided, and differences with p values less than 0.05 were considered significant. The difference in grading between indexes was accessed using Friedman test. The survival distributions for OS, EFS, GRFS were calculated using Kaplan-Meier methodology with 95% confidence intervals. Appropriate survival curves are provided in Supplementary files (see online version) Cumulative incidence analysis with competing risks was used for relapse and NRM. Five-year OS was used as an outcome to test all prognostic systems, because most of them were created based overall survival with follow up for 5 years and more [3, 4, 5, 9]. The univariate comparisons were made using the log-rank test. Proportional hazard modeling was used for the multivariate analysis. Based on the number of events 3 most significant factors from univariate analysis were included in the model. The MDS risk indexes were added in the series of tests. The final multivariate confidence intervals are the result of meta-analysis with fixed effect modeling. The heterogeneity of confidence intervals was tested with Cochran Q test. The C-statistic for the predictive factors was produced from logistic regression with death during five years after transplantation as an outcome. The predictive values were presented as area under the curve (AUC) with confidence intervals. Analyses were conducted in R 3.4.1 and SAS 9.3 (SAS Institute, Inc.).
Results
Distribution of patients by different scoring systems
We analyzed the distribution of patients by disease specific scoring systems such as IPSS, WPSS and IPSS-R and MDS prognostic indexes for patients undergoing allo-HSCT developed by Kroeger et al. and Armand et al. (Fig. 1). Fifty-four percent of patients were transplanted in high or very high IPSS-R risk. Forty-eight percent of patients with high/very high WPSS or IPSS-R risk were reclassified into intermediate risk according to pretransplant Kroeger et al. MDS score and 60% into intermediate risk, according to pretransplant Armand et al. score. There was a difference between disease- and pretransplant prognostic systems especially in distinction between high/very high and intermediate risk (p<0.001).

Figure 1. Distribution of patients by different prognostic scoring systems
Clinical outcomes
Platelet and leukocyte engraftment was documented in 48 (81%) of patients. Primary graft failure was observed in six cases (10%). Four patients out of them died (in one case, due to disease progression, and three patients deceased due to infections). The median time to leukocyte engraftment was 18 days (range 11-30), neutrophil engraftment, 20 days (range 10-30), platelet engraftment, 17 days (range 11-130). Overall, 50% of patients developed aGVHD with severe aGVHD grade 3-4 registered only in 15% of cases. The rate of chronic GVHD was 30%, which proved to be extensive in 28% of the patients (Table 1).
Cumulative incidence of relapse at 5 years was 37% (95% CI 25-57%). The cumulative incidence of non-relapse mortality (NRM) at 1 year was 25% (95% CI 16-40%). Thirty patients died during the follow-up study. The main reasons of death were disease progression or relapse in 26%; GVHD, 26%; infections, 37%; hemorrhagic events, 7%; acute myocardial infarction, in 4% of cases.
With a median follow-up of 36 months (range 3 to 135), the 5-year OS, EFS and GRFS was 34%, 33% and 29%, respectively. In univariate analysis, the significant factors for prolonged OS were as follows: aGVHD grade 1-2 (62% vs 18% p=0.004), quantities of donor СD34+ cells (p=0.006), and absence of septic episodes before engraftment (44 % vs 17%, p=0.003). The disease-specific prognostic indexes (IPSS, WPSS, IPSS-R), and transplant comorbidity indexes (PAM, EBMT, HCT-CI) did not predict OS . However, differences in OS rates between the risk groups according to disease-related prognostic systems such as Disease-Related Index, DRI (p=0.049), and risk score by Kroeger et al. (p=0.071) have shown a trend towards statistical significance (Supplement, Fig. 1-7. The supplemental files could be found in electronic version of this paper at www.cttjournal.com). The 5-year OS in low risk group, according to transplant risk score proposed by Kroeger et al. was 61%, thus being significantly higher compared to intermediate and high/very high risk – 26% (p=0.041). Surprisingly, we found no difference in OS between intermediate and high/very high risk groups (28% and 22%, respectively). This might be a reason for the failure of the index used by Kroeger et al. to achieve statistical significance. Interestingly, that the causes of death were nearly the same in both risk groups, i.e., ca. 50% of patients died due to transplant related factors.
ROC analysis shows influence of different prognostic systems and factors upon OS in the MDS patients. Amount of transplanted CD34+ donor cells proved to be the only factor which significantly affected transplant outcome (p=0.006) in this analysis (Fig. 2).

Figure 2. Influence of different prognostic systems and factors on OS in MDS patients, receiver-operating-curve (ROC) analysis
Note: C-statistics for the potential predictors of overall survival. Results of the ROC analysis treated in logistic regression with 5-year overall survival as an outcome. The non-significant parameters (p>0.05) are shown in grey. The significant (p<0.05) parameters are shown in black. The 95% confidence intervals of sensitivity and specificity are produced from individual results of all the parameters tested. C-statistic values of the variables were: CD34 positive cells in the graft 0.7080 (95% CI 0.5740-0.8421), Kroger et al. 0.5862 (95% CI 0.4391-0.7333), Armand et al. 0.5339 (95% CI 0.3850-0.6828), IPSS 0.5534 (95% CI 0.4121-0.6948), WPSS 0.5672 (95% CI 0.4354-0.6991), IPSS-R 0.5885 (0.4430-0.7340), DRI 0.5747 (0.4429-0.7065), EBMT 0.5230 (0.3758-0.6702), serum ferritin 0.4500 (0.2861-0.6139), PAM index 0.5584 (0.4037-0.7131), CRP before conditioning 0.4845 (0.3234-0.6456).
However, only presence of aGVHD grade 1-2 (p=0.013), absence of septic episodes (p=0.006), and DRI (p=0.037) retained their statistical significance in the multivariate analysis (Fig. 3). Other prognostic scores, except of DRI, did not show a statistical significance.

Figure 3. Analysis of the prognostic value of risk indexes in the multivariate model
Note: Multivariate analysis of overall survival. Acute GVHD, graft CD34+ cells and sepsis in aplasia were included based on univariate selection of the most predictive variables. The indexes were added as the fourth co-variable separately in a series of tests. The cumulative confidence intervals for the clinical variables were produced with fixed effect model from the individual hazards in the series.
Discussion
The major question in every MDS patient with currently existing treatments is whether he will benefit from allo-HSCT. Despite the fact that all existing treatments in most cases lead to only temporary responses, the results of allo-HSCT in MDS unfortunately are also one of the most disappointing compared to other diseases [15]. According to our 5-year observation data, the OS level in allotransplanted MDS patients is 34%. The other studies are showing nearly the same results: from 45% to 37% [1, 16]. This is due to relatively high NRM [3], but also due to high relapse rate [2, 17]. Currently used indexes of the natural course of the disease such as IPSS, WPSS, IPSS-R are established to evaluate risk of death and transformation to acute myeloid leukemia in untreated MDS patients [3, 4, 5]. All of these indexes are well validated in large patient cohorts [17]. However, their role in predicting the outcome after allo-HSCT is not so well defined.
Lee et al. [18] evaluated prognostic impact of IPSS before allo-HSCT. The authors showed significant differences in OS after allo-HSCT between low/intermediate and intermediate/high groups. Further it was shown that WPSS has a relevant prognostic value in posttransplant outcome of patients with MDS [19]. Modified prognostic model IPSS-R was assessed pre-transplant as a predictor of transplant outcome by C. Scheid et al. [20]. In that study, IPSS-R significantly influenced OS after allo-HSCT, but OS in high and intermediate groups were comparable: 47% and 44%, respectively. This was due to high and comparable NRM in these groups. In our study we have also observed high NRM in the favorable prognostic groups based on IPSS or IPSS-R.
The potential causes for early mortality in this group are relatively well discussed in the literature. They include primary graft failure [21], iron overload which results in higher incidence of liver veno-occlusive disease [22] and infectious complications [23]. It should be noted that, according to our data, the rate of primary graft failure is 10% being considered relatively high. The incidence of graft failure varies from 2 to 13% [2, 16, 24]. We didn’t find any correlation between rate of graft failure and type of stem cell source or rate of СD34+ cells in the graft, as reported in previous studies [21]. According to the results of large study by Olsson et al. [21], MDS diagnosis itself is associated with increased risk of graft failure, along with other hematologic malignancies, e.g., myeloproliferative disorders and chronic lymphocytic leukemia. Poor graft function may be another documented cause of NRM that leads to increased incidence of opportunistic infections and hemorrhagic complications [25]. Thus, high NRM rate was the main reason of non-significant predictive value of classical indexes after allo-HSCT found in our study.
A number of indexes accounting for NRM based on previous treatment burden, like as duration of the disease in EBMT index, or comorbidity burden, like in HCT-CI, or prediction of viral reactivations based on serological markers, like in PAM. However, there are conflicting results about influence of the comorbidity indexes on OS in MDS patients. Guilfoyle et al. did not find associations between HCT-CI and OS in MDS patients [26]. On the other hand, a large retrospective study showed that EBMT score accurately predicted OS and NRM [27]. In the present study, we have not observed any predictive impact of these indexes on the disease outcome. The published data and results of our study indicate that biological mechanisms behind NRM might be in certain cases different in MDS compared to the other diseases [28].
Several new prognostic indexes have been recently developed aiming for precise evaluation of transplant outcome in MDS patients. Kroeger et al. have combined the disease-related factors (cytogenetics, blood blasts, and platelets) and patient-related factors (performance status and age) into a common prognostic system [8]. Armand et al. added ferritin level and type of a conditioning regimen to the disease-related risk factors [9]. The disease risk index was another prognostic system evaluated in our study. It includes cytogenetics and remission status of MDS patients at transplant [7]. These indexes, except of DRI, were assessed in large data sets to specifically account for the risk of relapse and the risk of NRM. There is only a limited number of studies validating these indexes [29]. Interestingly, about half of IPSS-R high/very high risk patients were reclassified as more favorable category, the intermediate-1, according to risk score by Kroeger et al. and Armand et al. [8, 9]. Thereby, the disease- and transplant-specific scoring systems determine the transplant outcome in different ways. According to our data, only DRI significantly influenced OS values among all the mentioned prognostic scores. In our study, these transplant-specific indexes were shown to define well the group with good prognosis and adverse prognosis. However, we observed that clinical prognosis for the intermediate group proved to be as adverse as for the high-risk patients.
Thus, our study indicates that current prognostic indexes do not well define the intermediate prognosis. It is likely that most of the heterogeneity of the disease fall into this category, including patients with stromal and miRNA signaling deficiency [30], pyroptosis of hematopoietic stem cells [31], certain mutations without cytogenetic abnormalities [32]. Any of these pathogenetic variants might manifest in different mechanisms of NRM and relapse risk. Pooling the patients into large cohorts alleviate these differences by creation of risk indexes. However, small-group or individual prediction might not be so accurate, due to the causes mentioned above. Thus, future development of indexes and predictive systems for allo-HSCT should incorporate molecular data, at least, for the intermediate risk groups in MDS.
Conclusion
our relatively small single-center study, we have observed little predictive value of currently existing scoring systems, particularly due to adverse results in the intermediate risk patients. Further characterization of this “intermediate” patents is required to broaden the clinical application of the scoring systems for individual treatment planning.
Acknowledgments
We thank our patients, research and medical staff for making this study possible. This work was done as part of Russian Science Foundation grant №17-75-20145.
Disclosure statement
Authors confirm the absence of any conflicts of interests.
References
- Luger SM, Ringdén O, Zhang MJ, Pérez WS, Bishop MR, Bornhauser M, Bredeson CN, Cairo MS, Copelan EA, Gale RP, Giralt SA, Gulbas Z, Gupta V, Hale GA, Lazarus HM, et al. Similar outcomes using myeloablative vs reduced-intensity allogeneic transplant preparative regimens for AML or MDS. Bone Marrow Transplant. 2012;47(2):203-211.
- Kröger N, Iacobelli S, Franke GN, Platzbecker U, Uddin R, Hübel K, Scheid C, Weber T, Robin M, Stelljes M, Afanasyev B, Heim D, Deliliers GL, Onida F, Dreger P, et al. Dose-reduced versus standard conditioning followed by allogeneic stem-cell transplantation for patients with myelodysplastic syndrome: a prospective randomized phase III study of the EBMT (RICMAC Trial). J Clin Oncol. 2017;35(19):2157-2164.
- Greenberg P, Cox C, LeBeau MM, Fenaux P, Morel P, Sanz G, Sanz M, Vallespi T, Hamblin T, Oscier D, Ohyashiki K, Toyama K, Aul C, Mufti G, Bennett J. International scoring system for evaluating prognosis in myelodysplastic syndromes. Blood. 1997;89(6):2079-2088.
- Greenberg PL, Tuechler H, Schanz J, Sanz G, Garcia- Manero G, Solé F, Bennett JM, Bowen D, Fenaux P, Dreyfus F, Kantarjian H, Kuendgen A, Levis A, Malcovati L, Cazzola M, et al. Revised international prognostic scoring system for myelodysplastic syndromes. Blood. 2012; 120(12):2454-2465.
- Malcovati L, Germing U, Kuendgen A, Della Porta MG, Pascutto C, Invernizzi R, Giagounidis A, Hildebrandt B, Bernasconi P, Knipp S, Strupp C, Lazzarino M, Aul C, Cazzola M., et al. Time-dependent prognostic scoring system for predicting survival and leukemic evolution in myelodysplastic syndromes. J Clin Oncol. 2007;25(23):3503-3510.
- de Witte T, Bowen D, Robin M, Malcovati L, Niederwieser D, Yakoub-Agha I, Mufti GJ, Fenaux P, Sanz G, Martino R, Alessandrino EP, Onida F, Symeonidis A, Passweg J, Kobbe G, Ganser A, et al. Allogeneic hematopoietic stem cell transplantation for MDS and CMML: recommendations from an international expert panel. Blood. 2017;129(13):1753-1762.
- Armand P, Kim HT, Logan BR, Wang Z, Alyea EP, Kalaycio ME, Maziarz RT, Antin JH, Soiffer RJ, Weisdorf DJ, Rizzo JD, Horowitz MM, Saber W, et al. Validation and refinement of the Disease Risk Index for allogeneic stem cell transplantation. Blood. 2014;123(23):3664-3671.
- Gagelmann N, Eikema DJ, Stelljes M, Beelen D, de Wreede L, Mufti G, Knelange NS, Niederwieser D, Friis LS, Ehnninger G, Nagler A, Yakoub-Agha I, Meijer E, Ljungman P, Maertens J, et al. Optimized EBMT transplant-specific risk score in myelodysplastic syndromes after allogeneic stem-cell transplantation. Haematologica. 2019. pii: haematol.2018.200808. doi: 10.3324/haematol.2018.200808.
- Armand P, Kim HT, Cutler CS, Ho VT, Koreth J, Ritz J, Alyea EP, Antin JH, Soiffer RJ. A prognostic score for patients with acute leukemia or myelodysplastic syndromes undergoing allogeneic stem cell transplantation. Biol Blood Marrow Transplant. 2008;14(1):28-35.
- Gratwohl A. The EBMT risk score. Bone Marrow Transplant. 2012;47(6):749-756.
- Au BK, Gooley TA, Armand P, Fang M, Madtes DK, Sorror ML, Boeckh MJ, Gibson CJ, Deeg HJ, Storb R, Appelbaum FR, Chien JW, Martin PJ. Reevaluation of the Pretransplant Assessment of Mortality score after allogeneic hematopoietic transplantation. Biol Blood Marrow Transplant. 2015;21(5):848-854.
- Sorror ML, Maris MB, Storb R, Baron F, Sandmaier BM, Maloney DG, Storer B. Hematopoietic cell transplantation (HCT)-specific comorbidity index: a new tool for risk assessment before allogeneic HCT. Blood. 2005;106(8):2912-2919.
- Singer M, Deutschman CS, Seymour CW, Shankar-Hari M, Annane D, Bauer M, Bellomo R, Bernard GR, Chiche JD, Coopersmith CM, Hotchkiss RS, Levy MM, Marshall JC, Martin GS, Opal SM, et al. The third international consensus definitions for sepsis and septic shock. JAMA. 2016;315(8):801-810.
- De Pauw B, Walsh TJ, Donnelly JP, Stevens DA, Edwards JE, Calandra T, Pappas PG, Maertens J, Lortholary O, Kauffman CA, Denning DW, Patterson TF, Maschmeyer G, Bille J, Dismukes WE, et al. Revised definitions of invasive fungal disease from the European Organization for Research and Treatment of Cancer/invasive fungal infections cooperative group and the National Institute of Allergy and Infectious Diseases Mycoses Study Group (EORTC/MSG) Consensus Group. Clin Infect Dis. 2008;46(12):1813-1821.
- Raiola A, Dominietto A, Varaldo R, Ghiso A, Galaverna F, Bramanti S, Todisco E, Sarina B, Giordano L, Ibatici A, Santoro A, Clavio M, Bacigalupo A, Castagna L. Unmanipulated haploidentical BMT following non-myeloablative conditioning and post-transplantation CY for advanced Hodgkin’s lymphoma. Bone Marrow Transplant. 2014;49(2):190-194.
- Litzow MR, Tarima S, Pérez WS, Bolwell BJ, Cairo MS, Camitta BM, Cutler CS, de Lima M, Dipersio JF, Gale RP, Keating A, Lazarus HM, Luger S, Marks DI, Maziarz RT, et al. Allogeneic transplantation for therapy-related myelodysplastic syndrome and acute myeloid leukemia. Blood. 2016;115(9):1850-1858.
- Della Porta MG, Tuechler H, Malcovati L, Schanz J, Sanz G, Garcia-Manero G, Solé F, Bennett JM, Bowen D, Fenaux P, Dreyfus F, Kantarjian H, Kuendgen A, Levis A, Cermak J, et al. Validation of WHO classification-based Prognostic Scoring System (WPSS) for myelodysplastic syndromes and comparison with the revised International Prognostic Scoring System (IPSS-R). A study of the International Working Group for Prognosis in Myelodysplasia (IWG-PM). Leukemia. 2015;29(7):1502-1513.
- Lee JH, Lee JH, Lim SN, Kim DY, Kim SH, Lee YS, Kang YA, Kang SI, Jeon MJ, Seol M, Seo EJ, Chi HS, Park CJ, Jang S, Yun SC, et al. Allogeneic hematopoietic cell transplantation for myelodysplastic syndrome: Prognostic significance of pre-transplant IPSS score and comorbidity. Bone Marrow Transplant. 2010;45(3):450-457.
- Alessandrino EP, Della Porta MG, Bacigalupo A, Van Lint MT, Falda M, Onida F, Bernardi M, Iori AP, Rambaldi A, Cerretti R, Marenco P, Pioltelli P, Malcovati L, Pascutto C, Oneto R, et al. WHO classification and WPSS predict posttransplantation outcome in patients with myelodysplastic syndrome: a study from the Gruppo ItalianoTrapianto di Midollo Osseo (GITMO). Blood.2008;112(3):895-902.
- Scheid C, de Wreede L, van Biezen A, Koenecke C, Göhring G, Volin L, Maertens J, Finke J, Passweg J, Beelen D, Cornelissen JJ, Itälä-Remes M, Chevallier P, Russell N, Petersen E, et al. Validation of the revised IPSS at transplant in patients with myelodysplastic syndrome/transformed acute myelogenous leukemia receiving allogeneic stem cell transplantation: A retrospective analysis of the EBMT chronic malignancies working party. Bone Marrow Transplant. 2017;52(11):1519-1525.
- Olsson RF, Logan BR, Chaudhury S, Zhu X, Akpek G, Bolwell BJ, Bredeson CN, Dvorak CC, Gupta V, Ho VT, Lazarus HM, Marks DI, Ringdén OT, Pasquini MC, Schriber JR, et al. Primary graft failure after myeloablative allogeneic hematopoietic cell transplantation for hematologic malignancies Leukemia. 2015;29(8):1754-1762.
- Armand P, Kim HT, Cutler CS, Ho VT, Koreth J, Alyea EP, Soiffer RJ, Antin JH. Prognostic impact of elevated pretransplantation serum ferritin in patients undergoing myeloablative stem cell transplantation. Blood. 2007;109(10):4586-4588.
- Shaheen M, Ivanova MO, Moiseev IS, Bondarchuk SV, Afanasyev BV. Impact of initial serum ferritin on early post-HSCT complications: A single-center study. Cell Ther Transplant. 2016;5(2):40-48.
- Castro-Malaspina H, Harris RE, Gajewski J, Ramsay N, Collins R, Dharan B, King R, Deeg HJ. Unrelated donor marrow transplantation for myelodysplastic syndromes: Outcome analysis in 510 transplants facilitated by the National Marrow Donor Program. Blood.2002;99(6):1943-1951.
- Shimomura Y, Hara M, Katoh D, Hashimoto H, Ishikawa T. Enlarged spleen is associated with low neutrophil and platelet engraftment rates and poor survival after allogeneic stem cell transplantation in patients with acute myeloid leukemia and myelodysplastic syndrome. Ann Hematol. 2018;97(6):1049-1056.
- Guilfoyle R, Demers A, Bredeson C, Richardson E, Rubinger M, Szwajcer D, Seftel MD. Performance status, but not the Hematopoietic Cell Transplantation Comorbidity Index (HCT-CI), predicts mortality at a Canadian transplant center. Bone Marrow Transplant. 2009;43(2):133-139.
- Lozano S, Olavarria E, Iacobelli S, van Biezen A, Beelen DW, Finke J, Mufti GJ, Niederwieser D, Ehninger G, Ganser A, Stuhler G, Maertens J, Bacigalupo A, Volin L, Nagler A et al. The EBMT score predicts transplant related mortality and overall survival after allogeneic stem cell transplantation for myelodysplastic syndromes [Abstract]. Proc ASH. 2015, 3223.
- Ferrer RA, Wobus M, List C, Wehner R, Schönefeldt C, Brocard B, Mohr B, Rauner M, Schmitz M, Stiehler M, Ehninger G, Hofbauer LC, Bornhäuser M, Platzbecker U. Mesenchymal stromal cells from patients with myelodyplastic syndrome display distinct functional alterations that are modulated by lenalidomide. Haematologica. 2013;98(11):1677-1685.
- Beauverd Y, Roosnek E, Tirefort Y, Nagy-Hulliger M, Bernimoulin M, Tsopra O, Ansari M, Dantin C, Casini A, Grandjean AP, Chigrinova E, Masouridi-Levrat S, Chalandon Y. Validation of the disease risk index for outcome of patients undergoing allogeneic hematopoietic stem cell transplantation after T cell depletion. Biol Blood Marrow Transplant. 2014;20(9):1322-1328.
- Zhao Y, Wu D, Fei C, Guo J, Gu S, Zhu Y, Xu F, Zhang Z, Wu L, Li X, Chang C. Down-regulation of Dicer1 promotes cellular senescence and decreases the differentiation and stem cell-supporting capacities of mesenchymal stromal cells in patients with myelodysplastic syndrome. Haematologica. 2015;100(2):194-204.
- Basiorka AA, McGraw KL, Eksioglu EA, Chen X, Johnson J, Zhang L, Zhang Q, Irvine BA, Cluzeau T, Sallman DA, Padron E, Komrokji R, Sokol L, Coll RC, Robertson AA, et al. The NLRP3 inflammasome functions as a driver of the myelodysplastic syndrome phenotype. Blood. 2016;128(25):2960-2975.
- Yoshizato T, Nannya Y, Atsuta Y, Shiozawa Y, Iijima- Yamashita Y, Yoshida K, Shiraishi Y, Suzuki H, Nagata Y, Sato Y, Kakiuchi N, Matsuo K, Onizuka M, Kataoka K, Chiba K, et al. Genetic abnormalities in myelodysplasia and secondary acute myeloid leukemia: impact on outcome of stem cell transplantation. Blood. 2017;129(17):2347-2358.
Елена В. Морозова, Мария В. Барабанщикова, Николай Ю. Цветков, Ксения В. Мельситова, Юлия В. Рудницкая, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21572" ["VALUE"]=> array(2) { ["TEXT"]=> string(366) "<p>НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета им. И. П. Павлова, Санкт-Петербург, Россия</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(354) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета им. И. П. Павлова, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21573" ["VALUE"]=> array(2) { ["TEXT"]=> string(3764) "<p style="text-align: justify;">Разработан ряд предиктивных индексов для прогнозирования исхода у пациентов с миелодиспластическим синдромом (МДС). Целью нашего исследования была оценка прогностического вклада показателей заболевания и трансплантации в результаты аллогенной трансплантации гемопоэтических клеток (ТГСК) пациентам с МДС.</p> <h3>Пациенты и методы</h3> <p style="text-align: justify;">В ретроспективное исследование была включена группа из 53 пациентов с МДС (за исключением вторичного острого миелобластного лейкоза), леченных с применением алло-ТГСК. Целью работы была оценка предиктивной значимости следующих прогностических индексов: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), а также прогностической системы, предложенной Kroeger et al., Armand et al., индекса претрансплантационной оценки смертности (PAM), оценки риска по EBMT и ТГСК-специфичного индекса коморбидности (HCT-CI).</p> <h3>Результаты</h3> <p style="text-align: justify;">В результате работы показана достоверная разница в оценке риска при сравнении отдельных индексов (p <0,001). Были отмечены следующие клинические факторы, значимые для общей выживаемости (ОВ) в одно- и многофакторном анализе: острая реакция «трансплантат против хозяина» (ОРТПХ) I-II степени (HR 0,.223; 95% CI 0.059-0,721; p=0,0134) и возникновение сепсиса в период аплазии (HR 3,636; 95% CI 1,438-8,673; p=0,0059). Несмотря на значительный вклад числа CD34+ клеток в трансплантате, (p=0,006), выявленного посредством ROC-анализа, только индекс DRI являлся существенным средством прогноза 5-летней выживаемости в многофакторной модели (HR 1,857; 95% CI 1,036-3,328; p=0,037). Более низкая эффективность других МДС-специфичных индексов в прогнозировании исходов алло-ТГСК связана, по-видимому, с неблагоприятными исходами в группе промежуточного риска. В заключение мы должны отметить необходимость дальнейшей характеризации пациентов промежуточной группы риска при прогнозировании исхода лечения. </p> <h2>Ключевые слова</h2> <p style="text-align: justify;">Миелодиспластический синдром, аллогенная трансплантация гемопоэтических стволовых клеток, прогностические индексы, оценка риска.</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3637) "Разработан ряд предиктивных индексов для прогнозирования исхода у пациентов с миелодиспластическим синдромом (МДС). Целью нашего исследования была оценка прогностического вклада показателей заболевания и трансплантации в результаты аллогенной трансплантации гемопоэтических клеток (ТГСК) пациентам с МДС.
Пациенты и методы
В ретроспективное исследование была включена группа из 53 пациентов с МДС (за исключением вторичного острого миелобластного лейкоза), леченных с применением алло-ТГСК. Целью работы была оценка предиктивной значимости следующих прогностических индексов: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), а также прогностической системы, предложенной Kroeger et al., Armand et al., индекса претрансплантационной оценки смертности (PAM), оценки риска по EBMT и ТГСК-специфичного индекса коморбидности (HCT-CI).
Результаты
В результате работы показана достоверная разница в оценке риска при сравнении отдельных индексов (p <0,001). Были отмечены следующие клинические факторы, значимые для общей выживаемости (ОВ) в одно- и многофакторном анализе: острая реакция «трансплантат против хозяина» (ОРТПХ) I-II степени (HR 0,.223; 95% CI 0.059-0,721; p=0,0134) и возникновение сепсиса в период аплазии (HR 3,636; 95% CI 1,438-8,673; p=0,0059). Несмотря на значительный вклад числа CD34+ клеток в трансплантате, (p=0,006), выявленного посредством ROC-анализа, только индекс DRI являлся существенным средством прогноза 5-летней выживаемости в многофакторной модели (HR 1,857; 95% CI 1,036-3,328; p=0,037). Более низкая эффективность других МДС-специфичных индексов в прогнозировании исходов алло-ТГСК связана, по-видимому, с неблагоприятными исходами в группе промежуточного риска. В заключение мы должны отметить необходимость дальнейшей характеризации пациентов промежуточной группы риска при прогнозировании исхода лечения.
Ключевые слова
Миелодиспластический синдром, аллогенная трансплантация гемопоэтических стволовых клеток, прогностические индексы, оценка риска.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21554" ["VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-36-45" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-36-45" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21584" ["VALUE"]=> array(2) { ["TEXT"]=> string(204) "<p>Elena V. Morozova, Maria V. Barabanshikova, Nikolai Yu. Tcvetkov, Ksenia V. Melsitova, Julia V. Rudnitskaya, Elena I. Darskaya, Sergey N. Bondarenko, Ivan S. Moiseev, Boris V. Afanasyev</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(192) "Elena V. Morozova, Maria V. Barabanshikova, Nikolai Yu. Tcvetkov, Ksenia V. Melsitova, Julia V. Rudnitskaya, Elena I. Darskaya, Sergey N. Bondarenko, Ivan S. Moiseev, Boris V. Afanasyev
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21585" ["VALUE"]=> array(2) { ["TEXT"]=> string(209) "<p>R. Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation, The First Pavlov St. Petersburg State Medical University, St. Petersburg, Russian Federation</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(197) "R. Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation, The First Pavlov St. Petersburg State Medical University, St. Petersburg, Russian Federation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21586" ["VALUE"]=> array(2) { ["TEXT"]=> string(2109) "<p style="text-align: justify;">Several prognostic indexes were developed to predict outcome in patients with myelodysplastic syndrome (MDS). The aim of our study was to evaluate prognostic impact of disease- and transplant-specific indexes on the results of allogeneic hematopoietic stem cell transplantation (allo-HSCT) in MDS patients.</p> <h3>Patients and methods</h3> <p style="text-align: justify;">A retrospective cohort of fifty-nine MDS patients (excluding secondary acute myeloid leukemia) and treated with allo-HSCT was used to evaluate the predictive value of the following prognostic indexes: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), prognostic systems developed by Kroeger et al., Armand et al., Pretransplant Assessment of Mortality Score (PAM), EBMT risk score and Hematopoietic Cell Transplantation-specific Comorbidity Index (HCT-CI).</p> <h3>Results</h3> <p style="text-align: justify;">There was a significant difference in risk estimation between indexes (p<0.001). Clinical factors significant for overall survival (OS) in the univariate and multivariate analyses were as follows: acute graft-versus-host disease (GVHD) grade I-II (HR 0.223, 95% CI 0.059-0.721, p=0.0134) and occurrence of sepsis during aplasia (HR 3.636, 95% CI 1.438-8.673, p=0.0059). Despite significant impact of CD34+ cell contents in hematopoietic graft (p=0.006) revealed in ROC analysis, only DRI remained a significant predictor of 5-year OS in the multivariate model (HR 1.857, 95% CI 1.036-3.328, p=0.037). Inferiority of other MDS-specific indexes to predict the outcome for allo-HSCT seems to be associated with adverse results in the intermediate risk group. In conclusion, we presume a need for further characterization of the intermediate risk patients when predicting the therapy outcomes. </p> <h2>Keywords</h2> <p style="text-align: justify;">Myelodysplastic syndrome, allogeneic hematopoietic stem cell transplantation, prognostic indexes, risk estimation. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1982) "Several prognostic indexes were developed to predict outcome in patients with myelodysplastic syndrome (MDS). The aim of our study was to evaluate prognostic impact of disease- and transplant-specific indexes on the results of allogeneic hematopoietic stem cell transplantation (allo-HSCT) in MDS patients.
Patients and methods
A retrospective cohort of fifty-nine MDS patients (excluding secondary acute myeloid leukemia) and treated with allo-HSCT was used to evaluate the predictive value of the following prognostic indexes: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), prognostic systems developed by Kroeger et al., Armand et al., Pretransplant Assessment of Mortality Score (PAM), EBMT risk score and Hematopoietic Cell Transplantation-specific Comorbidity Index (HCT-CI).
Results
There was a significant difference in risk estimation between indexes (p<0.001). Clinical factors significant for overall survival (OS) in the univariate and multivariate analyses were as follows: acute graft-versus-host disease (GVHD) grade I-II (HR 0.223, 95% CI 0.059-0.721, p=0.0134) and occurrence of sepsis during aplasia (HR 3.636, 95% CI 1.438-8.673, p=0.0059). Despite significant impact of CD34+ cell contents in hematopoietic graft (p=0.006) revealed in ROC analysis, only DRI remained a significant predictor of 5-year OS in the multivariate model (HR 1.857, 95% CI 1.036-3.328, p=0.037). Inferiority of other MDS-specific indexes to predict the outcome for allo-HSCT seems to be associated with adverse results in the intermediate risk group. In conclusion, we presume a need for further characterization of the intermediate risk patients when predicting the therapy outcomes.
Keywords
Myelodysplastic syndrome, allogeneic hematopoietic stem cell transplantation, prognostic indexes, risk estimation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21555" ["VALUE"]=> string(158) "Application of standard and novel prognostic systems in patients with myelodys- plastic syndrome undergoing allogeneic hematopoietic stem cell transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(158) "Application of standard and novel prognostic systems in patients with myelodys- plastic syndrome undergoing allogeneic hematopoietic stem cell transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21574" ["VALUE"]=> string(4) "1586" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1586" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21587" ["VALUE"]=> string(4) "1588" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1588" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(12) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21584" ["VALUE"]=> array(2) { ["TEXT"]=> string(204) "<p>Elena V. Morozova, Maria V. Barabanshikova, Nikolai Yu. Tcvetkov, Ksenia V. Melsitova, Julia V. Rudnitskaya, Elena I. Darskaya, Sergey N. Bondarenko, Ivan S. Moiseev, Boris V. Afanasyev</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(192) "Elena V. Morozova, Maria V. Barabanshikova, Nikolai Yu. Tcvetkov, Ksenia V. Melsitova, Julia V. Rudnitskaya, Elena I. Darskaya, Sergey N. Bondarenko, Ivan S. Moiseev, Boris V. Afanasyev
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(192) "Elena V. Morozova, Maria V. Barabanshikova, Nikolai Yu. Tcvetkov, Ksenia V. Melsitova, Julia V. Rudnitskaya, Elena I. Darskaya, Sergey N. Bondarenko, Ivan S. Moiseev, Boris V. Afanasyev
" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21586" ["VALUE"]=> array(2) { ["TEXT"]=> string(2109) "<p style="text-align: justify;">Several prognostic indexes were developed to predict outcome in patients with myelodysplastic syndrome (MDS). The aim of our study was to evaluate prognostic impact of disease- and transplant-specific indexes on the results of allogeneic hematopoietic stem cell transplantation (allo-HSCT) in MDS patients.</p> <h3>Patients and methods</h3> <p style="text-align: justify;">A retrospective cohort of fifty-nine MDS patients (excluding secondary acute myeloid leukemia) and treated with allo-HSCT was used to evaluate the predictive value of the following prognostic indexes: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), prognostic systems developed by Kroeger et al., Armand et al., Pretransplant Assessment of Mortality Score (PAM), EBMT risk score and Hematopoietic Cell Transplantation-specific Comorbidity Index (HCT-CI).</p> <h3>Results</h3> <p style="text-align: justify;">There was a significant difference in risk estimation between indexes (p<0.001). Clinical factors significant for overall survival (OS) in the univariate and multivariate analyses were as follows: acute graft-versus-host disease (GVHD) grade I-II (HR 0.223, 95% CI 0.059-0.721, p=0.0134) and occurrence of sepsis during aplasia (HR 3.636, 95% CI 1.438-8.673, p=0.0059). Despite significant impact of CD34+ cell contents in hematopoietic graft (p=0.006) revealed in ROC analysis, only DRI remained a significant predictor of 5-year OS in the multivariate model (HR 1.857, 95% CI 1.036-3.328, p=0.037). Inferiority of other MDS-specific indexes to predict the outcome for allo-HSCT seems to be associated with adverse results in the intermediate risk group. In conclusion, we presume a need for further characterization of the intermediate risk patients when predicting the therapy outcomes. </p> <h2>Keywords</h2> <p style="text-align: justify;">Myelodysplastic syndrome, allogeneic hematopoietic stem cell transplantation, prognostic indexes, risk estimation. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1982) "Several prognostic indexes were developed to predict outcome in patients with myelodysplastic syndrome (MDS). The aim of our study was to evaluate prognostic impact of disease- and transplant-specific indexes on the results of allogeneic hematopoietic stem cell transplantation (allo-HSCT) in MDS patients.
Patients and methods
A retrospective cohort of fifty-nine MDS patients (excluding secondary acute myeloid leukemia) and treated with allo-HSCT was used to evaluate the predictive value of the following prognostic indexes: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), prognostic systems developed by Kroeger et al., Armand et al., Pretransplant Assessment of Mortality Score (PAM), EBMT risk score and Hematopoietic Cell Transplantation-specific Comorbidity Index (HCT-CI).
Results
There was a significant difference in risk estimation between indexes (p<0.001). Clinical factors significant for overall survival (OS) in the univariate and multivariate analyses were as follows: acute graft-versus-host disease (GVHD) grade I-II (HR 0.223, 95% CI 0.059-0.721, p=0.0134) and occurrence of sepsis during aplasia (HR 3.636, 95% CI 1.438-8.673, p=0.0059). Despite significant impact of CD34+ cell contents in hematopoietic graft (p=0.006) revealed in ROC analysis, only DRI remained a significant predictor of 5-year OS in the multivariate model (HR 1.857, 95% CI 1.036-3.328, p=0.037). Inferiority of other MDS-specific indexes to predict the outcome for allo-HSCT seems to be associated with adverse results in the intermediate risk group. In conclusion, we presume a need for further characterization of the intermediate risk patients when predicting the therapy outcomes.
Keywords
Myelodysplastic syndrome, allogeneic hematopoietic stem cell transplantation, prognostic indexes, risk estimation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(1982) "Several prognostic indexes were developed to predict outcome in patients with myelodysplastic syndrome (MDS). The aim of our study was to evaluate prognostic impact of disease- and transplant-specific indexes on the results of allogeneic hematopoietic stem cell transplantation (allo-HSCT) in MDS patients.
Patients and methods
A retrospective cohort of fifty-nine MDS patients (excluding secondary acute myeloid leukemia) and treated with allo-HSCT was used to evaluate the predictive value of the following prognostic indexes: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), prognostic systems developed by Kroeger et al., Armand et al., Pretransplant Assessment of Mortality Score (PAM), EBMT risk score and Hematopoietic Cell Transplantation-specific Comorbidity Index (HCT-CI).
Results
There was a significant difference in risk estimation between indexes (p<0.001). Clinical factors significant for overall survival (OS) in the univariate and multivariate analyses were as follows: acute graft-versus-host disease (GVHD) grade I-II (HR 0.223, 95% CI 0.059-0.721, p=0.0134) and occurrence of sepsis during aplasia (HR 3.636, 95% CI 1.438-8.673, p=0.0059). Despite significant impact of CD34+ cell contents in hematopoietic graft (p=0.006) revealed in ROC analysis, only DRI remained a significant predictor of 5-year OS in the multivariate model (HR 1.857, 95% CI 1.036-3.328, p=0.037). Inferiority of other MDS-specific indexes to predict the outcome for allo-HSCT seems to be associated with adverse results in the intermediate risk group. In conclusion, we presume a need for further characterization of the intermediate risk patients when predicting the therapy outcomes.
Keywords
Myelodysplastic syndrome, allogeneic hematopoietic stem cell transplantation, prognostic indexes, risk estimation.
" } ["DOI"]=> array(37) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21554" ["VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-36-45" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-36-45" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-36-45" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21555" ["VALUE"]=> string(158) "Application of standard and novel prognostic systems in patients with myelodys- plastic syndrome undergoing allogeneic hematopoietic stem cell transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(158) "Application of standard and novel prognostic systems in patients with myelodys- plastic syndrome undergoing allogeneic hematopoietic stem cell transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(158) "Application of standard and novel prognostic systems in patients with myelodys- plastic syndrome undergoing allogeneic hematopoietic stem cell transplantation" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21585" ["VALUE"]=> array(2) { ["TEXT"]=> string(209) "<p>R. Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation, The First Pavlov St. Petersburg State Medical University, St. Petersburg, Russian Federation</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(197) "R. Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation, The First Pavlov St. Petersburg State Medical University, St. Petersburg, Russian Federation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(197) "R. Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation, The First Pavlov St. Petersburg State Medical University, St. Petersburg, Russian Federation
" } ["AUTHORS"]=> array(38) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> array(9) { [0]=> string(5) "21606" [1]=> string(5) "21607" [2]=> string(5) "21608" [3]=> string(5) "21609" [4]=> string(5) "21610" [5]=> string(5) "21611" [6]=> string(5) "21612" [7]=> string(5) "21613" [8]=> string(5) "21614" } ["VALUE"]=> array(9) { [0]=> string(3) "147" [1]=> string(3) "146" [2]=> string(4) "1633" [3]=> string(4) "1634" [4]=> string(4) "1635" [5]=> string(3) "285" [6]=> string(4) "1631" [7]=> string(2) "60" [8]=> string(2) "34" } ["DESCRIPTION"]=> array(9) { [0]=> string(0) "" [1]=> string(0) "" [2]=> string(0) "" [3]=> string(0) "" [4]=> string(0) "" [5]=> string(0) "" [6]=> string(0) "" [7]=> string(0) "" [8]=> string(0) "" } ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(9) { [0]=> string(3) "147" [1]=> string(3) "146" [2]=> string(4) "1633" [3]=> string(4) "1634" [4]=> string(4) "1635" [5]=> string(3) "285" [6]=> string(4) "1631" [7]=> string(2) "60" [8]=> string(2) "34" } ["~DESCRIPTION"]=> array(9) { [0]=> string(0) "" [1]=> string(0) "" [2]=> string(0) "" [3]=> string(0) "" [4]=> string(0) "" [5]=> string(0) "" [6]=> string(0) "" [7]=> string(0) "" [8]=> string(0) "" } ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> array(9) { [0]=> string(60) "Elena V. Morozova" [1]=> string(66) "Maria V. Barabanshikova" [2]=> string(64) "Nikolai Yu. Tcvetkov" [3]=> string(63) "Ksenia V. Melsitova" [4]=> string(64) "Julia V. Rudnitskaya" [5]=> string(60) "Elena I. Darskaya" [6]=> string(64) "Sergey N. Bondarenko" [7]=> string(57) "Ivan S. Moiseev" [8]=> string(60) "Boris V. Afanasyev" } ["LINK_ELEMENT_VALUE"]=> bool(false) } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21571" ["VALUE"]=> array(2) { ["TEXT"]=> string(334) "<p>Елена В. Морозова, Мария В. Барабанщикова, Николай Ю. Цветков, Ксения В. Мельситова, Юлия В. Рудницкая, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(322) "Елена В. Морозова, Мария В. Барабанщикова, Николай Ю. Цветков, Ксения В. Мельситова, Юлия В. Рудницкая, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(322) "Елена В. Морозова, Мария В. Барабанщикова, Николай Ю. Цветков, Ксения В. Мельситова, Юлия В. Рудницкая, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев
" } ["SUBMITTED"]=> array(37) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21542" ["VALUE"]=> string(10) "06.03.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "06.03.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "06.03.2019" } ["ACCEPTED"]=> array(37) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21543" ["VALUE"]=> string(10) "15.03.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "15.03.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "15.03.2019" } ["CONTACT"]=> array(38) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21544" ["VALUE"]=> string(3) "146" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(3) "146" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(66) "Maria V. Barabanshikova" ["LINK_ELEMENT_VALUE"]=> bool(false) } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21573" ["VALUE"]=> array(2) { ["TEXT"]=> string(3764) "<p style="text-align: justify;">Разработан ряд предиктивных индексов для прогнозирования исхода у пациентов с миелодиспластическим синдромом (МДС). Целью нашего исследования была оценка прогностического вклада показателей заболевания и трансплантации в результаты аллогенной трансплантации гемопоэтических клеток (ТГСК) пациентам с МДС.</p> <h3>Пациенты и методы</h3> <p style="text-align: justify;">В ретроспективное исследование была включена группа из 53 пациентов с МДС (за исключением вторичного острого миелобластного лейкоза), леченных с применением алло-ТГСК. Целью работы была оценка предиктивной значимости следующих прогностических индексов: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), а также прогностической системы, предложенной Kroeger et al., Armand et al., индекса претрансплантационной оценки смертности (PAM), оценки риска по EBMT и ТГСК-специфичного индекса коморбидности (HCT-CI).</p> <h3>Результаты</h3> <p style="text-align: justify;">В результате работы показана достоверная разница в оценке риска при сравнении отдельных индексов (p <0,001). Были отмечены следующие клинические факторы, значимые для общей выживаемости (ОВ) в одно- и многофакторном анализе: острая реакция «трансплантат против хозяина» (ОРТПХ) I-II степени (HR 0,.223; 95% CI 0.059-0,721; p=0,0134) и возникновение сепсиса в период аплазии (HR 3,636; 95% CI 1,438-8,673; p=0,0059). Несмотря на значительный вклад числа CD34+ клеток в трансплантате, (p=0,006), выявленного посредством ROC-анализа, только индекс DRI являлся существенным средством прогноза 5-летней выживаемости в многофакторной модели (HR 1,857; 95% CI 1,036-3,328; p=0,037). Более низкая эффективность других МДС-специфичных индексов в прогнозировании исходов алло-ТГСК связана, по-видимому, с неблагоприятными исходами в группе промежуточного риска. В заключение мы должны отметить необходимость дальнейшей характеризации пациентов промежуточной группы риска при прогнозировании исхода лечения. </p> <h2>Ключевые слова</h2> <p style="text-align: justify;">Миелодиспластический синдром, аллогенная трансплантация гемопоэтических стволовых клеток, прогностические индексы, оценка риска.</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3637) "Разработан ряд предиктивных индексов для прогнозирования исхода у пациентов с миелодиспластическим синдромом (МДС). Целью нашего исследования была оценка прогностического вклада показателей заболевания и трансплантации в результаты аллогенной трансплантации гемопоэтических клеток (ТГСК) пациентам с МДС.
Пациенты и методы
В ретроспективное исследование была включена группа из 53 пациентов с МДС (за исключением вторичного острого миелобластного лейкоза), леченных с применением алло-ТГСК. Целью работы была оценка предиктивной значимости следующих прогностических индексов: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), а также прогностической системы, предложенной Kroeger et al., Armand et al., индекса претрансплантационной оценки смертности (PAM), оценки риска по EBMT и ТГСК-специфичного индекса коморбидности (HCT-CI).
Результаты
В результате работы показана достоверная разница в оценке риска при сравнении отдельных индексов (p <0,001). Были отмечены следующие клинические факторы, значимые для общей выживаемости (ОВ) в одно- и многофакторном анализе: острая реакция «трансплантат против хозяина» (ОРТПХ) I-II степени (HR 0,.223; 95% CI 0.059-0,721; p=0,0134) и возникновение сепсиса в период аплазии (HR 3,636; 95% CI 1,438-8,673; p=0,0059). Несмотря на значительный вклад числа CD34+ клеток в трансплантате, (p=0,006), выявленного посредством ROC-анализа, только индекс DRI являлся существенным средством прогноза 5-летней выживаемости в многофакторной модели (HR 1,857; 95% CI 1,036-3,328; p=0,037). Более низкая эффективность других МДС-специфичных индексов в прогнозировании исходов алло-ТГСК связана, по-видимому, с неблагоприятными исходами в группе промежуточного риска. В заключение мы должны отметить необходимость дальнейшей характеризации пациентов промежуточной группы риска при прогнозировании исхода лечения.
Ключевые слова
Миелодиспластический синдром, аллогенная трансплантация гемопоэтических стволовых клеток, прогностические индексы, оценка риска.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3637) "Разработан ряд предиктивных индексов для прогнозирования исхода у пациентов с миелодиспластическим синдромом (МДС). Целью нашего исследования была оценка прогностического вклада показателей заболевания и трансплантации в результаты аллогенной трансплантации гемопоэтических клеток (ТГСК) пациентам с МДС.
Пациенты и методы
В ретроспективное исследование была включена группа из 53 пациентов с МДС (за исключением вторичного острого миелобластного лейкоза), леченных с применением алло-ТГСК. Целью работы была оценка предиктивной значимости следующих прогностических индексов: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), а также прогностической системы, предложенной Kroeger et al., Armand et al., индекса претрансплантационной оценки смертности (PAM), оценки риска по EBMT и ТГСК-специфичного индекса коморбидности (HCT-CI).
Результаты
В результате работы показана достоверная разница в оценке риска при сравнении отдельных индексов (p <0,001). Были отмечены следующие клинические факторы, значимые для общей выживаемости (ОВ) в одно- и многофакторном анализе: острая реакция «трансплантат против хозяина» (ОРТПХ) I-II степени (HR 0,.223; 95% CI 0.059-0,721; p=0,0134) и возникновение сепсиса в период аплазии (HR 3,636; 95% CI 1,438-8,673; p=0,0059). Несмотря на значительный вклад числа CD34+ клеток в трансплантате, (p=0,006), выявленного посредством ROC-анализа, только индекс DRI являлся существенным средством прогноза 5-летней выживаемости в многофакторной модели (HR 1,857; 95% CI 1,036-3,328; p=0,037). Более низкая эффективность других МДС-специфичных индексов в прогнозировании исходов алло-ТГСК связана, по-видимому, с неблагоприятными исходами в группе промежуточного риска. В заключение мы должны отметить необходимость дальнейшей характеризации пациентов промежуточной группы риска при прогнозировании исхода лечения.
Ключевые слова
Миелодиспластический синдром, аллогенная трансплантация гемопоэтических стволовых клеток, прогностические индексы, оценка риска.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21572" ["VALUE"]=> array(2) { ["TEXT"]=> string(366) "<p>НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета им. И. П. Павлова, Санкт-Петербург, Россия</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(354) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета им. И. П. Павлова, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(354) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета им. И. П. Павлова, Санкт-Петербург, Россия
" } } } [5]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "121" ["~IBLOCK_SECTION_ID"]=> string(3) "121" ["ID"]=> string(4) "1632" ["~ID"]=> string(4) "1632" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(241) "Гаплоидентичная трансплантация костного мозга для лечения взрослых пациентов с различными заболеваниями: опыт одного центра (CIC725)" ["~NAME"]=> string(241) "Гаплоидентичная трансплантация костного мозга для лечения взрослых пациентов с различными заболеваниями: опыт одного центра (CIC725)" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "03.06.2019 14:02:17" ["~TIMESTAMP_X"]=> string(19) "03.06.2019 14:02:17" ["DETAIL_PAGE_URL"]=> string(154) "/ru/archive/tom-8-nomer-1/klinicheskie-issledovaniya/gaploidentichnaya-transplantatsiya-kostnogo-mozga-dlya-lecheniya-vzroslykh-patsientov-s-razlichnymi-/" ["~DETAIL_PAGE_URL"]=> string(154) "/ru/archive/tom-8-nomer-1/klinicheskie-issledovaniya/gaploidentichnaya-transplantatsiya-kostnogo-mozga-dlya-lecheniya-vzroslykh-patsientov-s-razlichnymi-/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(33939) "Introduction
Allogeneic HSCT (allo-HSCT) is potentially curative option for a wide variety of malignant and nonmalignant disorders of hematopoiesis [1-4]. Historically, the best outcomes of allo-HSCT were obtained in cases when a donor was an HLA-matched sibling [5]. The probability of having an HLA-matched sibling donor is approximately thirty percent [6]. For patients who lack an HLA-matched sibling, alternative sources of donor grafts can be found in suitable HLA-matched adult unrelated donors (MUD), unrelated umbilical cord blood (UCB) donors, and partially HLA-mismatched-unrelated donors (mMUD) or HLA-haploidentical related donors (haplo-HSCT) [1, 8]. Despite the increasing number of volunteers in unrelated donor registries, the likelihood of finding a suitable matched unrelated donor is modest [6, 7]. However, haploidentical donor can be found for nearly every patient. The use of haploidentical donors is not limited by racial/ethnic HLA diversity or unusual HLA phenotypes due to mixed racial ancestry [6]. The benefits of haplo-HSCT include immediate donor availability for patients who need the transplant as soon as possible. Besides, post-transplant donor-derived cellular therapy is more easily accessible with the use of a related donor. In addition, the greater HLA mismatch associated with haploidentical HSCT (haplo-HSCT) may potentiate graft-versus-tumor (GVT) effects. However, this method was historically associated with poor engraftment, high risk of early death, and severe graft-versus-host disease (GVHD).
Earlier attempts at using unmanipulated haploidentical transplant were associated with an unacceptably high rate of GVHD related mortality. Several strategies have been evolved over the past decade to avoid these disadvantages. The advent of T-cell depleted haplo-SCT has allowed better control of the severe GVHD risk [9]. However, this approach was associated with a high rate of graft failure due to host T-lymphocytes that survived the conditioning regimen [10-12]. Later studies have shown that murine and human hematopoietic stem cells have veto cell activity and infusion of a large number of donor hematopoietic stem cells can overcome the MHC barrier and promote engraftment [13-15]. Megadose human CD34+ stem cells (on average >10×106 CD34+ cells/kg body weight) with minimal T cell contamination (a median of 1×104/kg weight) have been successfully used in haploidentical transplantation, which results in high-level engraftment of MHC disparate stem cells. The use of intensive conditioning without additional GVHD prophylaxis led to the result that nearly 80% of patients achieved primary engraftment and only 18% of the patients developed grade II-IV acute GVHD [16, 17]. The major disadvantages of T-cell depleted grafts are both high rate of relapse and nonrelapse mortality (NRM) due to slow immune reconstitution and, thus, infectious complications [18].
Another method to manipulate the T-cell depleted graft is co-infusion of donor-derived regulatory T-cells (Tregs). CD4+CD25+ regulatory T-cells have been shown to suppress proliferative responses of CD4+CD25− T-cells to allo-antigenic stimulation in vitro and are required for ex vivo tolerization of donor T-cells, which results in their reduced potential to induce aGVHD [19, 20]. Despite promising results, this approach is costly and technically demanding, which limits its application to experienced centers.
Another innovative approach is to selectively deplete T-cells responsible for GVHD (TCR alpha-beta) while sparing gamma-delta T-cells (γδ T-cells). Gamma-delta T-cells account for 1% to 10% of peripheral T-cells and have MHC-unrestricted innate cytotoxic activity against tumor cells [21-23]. The use of TCRαβ/CD19-depleted stem cells essentially accelerated immune recovery.
A more recent strategy is to selectively deplete naive T-cells to separate GVHD and the GVL effect. Naive T-cells with CD45RA expression demonstrate to be the most allo-reactive among the T-cell subsets. Ex vivo depletion of CD45RA T-cells and adoptive transfer of CD45RA-memory T-cells accelerate the immune reconstitution, increase the GVL effect while abrogating GVHD [24].
A group of Chinese researchers used a method based on G-CSF-stimulation of the donor, intensified immunosuppression, antithymocyte globulin as in vivo T-cell depletion, and combination of peripheral blood stem cell and bone marrow allografts. Despite satisfactory relapse-free survival rates, acceptable NRM and engraftment, relatively high incidence of severe acute and chronic GVHD was observed. In addition, the standard-risk patients often suffered with opportunistic infections [25, 26].
Trying to improve these results, Italian research team modified this approach through using only BM allografts and adding basiliximab which allowed them to achieve a lower rate of chronic GVHD that included both forms, limited and extensive [27].
Another approach to allo-HSCT was developed in Baltimore (USA) based on non-manipulated graft followed by post-transplant cyclophosphamide injection (PtCy) [28, 29]. This approach has overcome most obstacles historically connected with haplo-HSCT. Thus, recent changes in haplo- HSCT methodology have allowed to improve its results.
The aim of this study was to compare the efficiency of various haplo-HSCT approaches used in our HSCT center.
Patients and methods
The study included 119 patients transplanted from a haploidentical donor (haplo-HSCT) between 2006 and 2018 at the R. M. Gorbacheva Institute of Children Oncology (CIC 725). Their clinical parameters are shown in Table 1. Nine patients received second haplo-HSCT, due to graft failure in 8 cases and relapse in one patient. Eight patients were transplanted from the same donor and one patient from the other donor. Median age was 26 years (18-63), 61 patients were males (51%). Most frequent diagnosis in transplanted patients was acute leukemia (77%, n=92). Primary diagnoses were ALL (31%, n=37), AML (45%, n=53), ABL (2%, n=2), myeloproliferative neoplasms (8%, n=9), lymphoproliferative disorders (13%, n=16), severe aplastic anemia (1%, n=2). Median follow-up was 371 days (1-2219). A total of 46 patients with acute leukemia (38%) had complete remission at the time of HSCT (the first complete remission – 80%, n=37, the 2d or greater remission – 20%, n=9), 33% patients (n=30) had relapse, 15% patients (n=14) had refractory disease. Thus, 67 (56%) patients in the general group received haplo-HSCT as salvage therapy. Non-myeloablative, or reduced-intensity conditioning (RIC) was employed in 81% (n=96) and the myeloablative treatment (MAC) was used in 19% (n=23). Seventy-seven patients (65%) received busulfan, 14 patients (12%), melphalan, and 28 patients (23%) were administered other alkylating agents. Bone marrow was the graft source for 61% patients (n=73), peripheral blood (PBSC) – 39% patients (n=46). Mean transplant CD34+cell and CD3+cell dose was 5×106/kg (1.5-10) and 10×107/kg (2-44) respectively for bone marrow as a graft source, whereas it was 5.1×106/kg (1-16.6) and 10×107/kg (3-47) respectively for recipients who received PBSC as a source of graft.
GVHD prophylaxis based on рost-transplant cyclophosphamide (PTCY-based GVHD prophylaxis) 50 mg/kg at day+3, +4 was employed in 78 patients (66%), also these recipients received tacrolimus 0.03 mg/kg/day and MMF 30-45 mg/kg starting from day +5. Eleven patients (9%) received a T-cell manipulated transplant. The protocol of depletion and HSCT included conditioning according to the GIAC protocol, depleted PBSC in combination with native BM and ATGAM, tacrolimus, MMF.
A total of 30 patients (25%) received GVHD prophylaxis with ATGAM- 31 (26%) and alemtuzumab in 5 patients (4%). Tacrolimus was used for GVHD prophylaxis in 93 patients (72%), cyclosporin A – in 18 patients (14%). Clinical characteristics of the study group are presented in Table 1.
Table 1. Clinical characteristics of the study group

Clinical diagnosis of acute (aGVHD) and chronic GVHD (cGVHD) was based on standard criteria and confirmed by histological analysis of skin and/or rectal biopsy specimens. First-line and second-line therapy for GVHD was provided according to institutional protocols. For statistical evaluation, SPSS Statistics v.17 was used. Two-year time frame was selected for all outcomes. In the group description overall survival (OS), event-free survival (EFS) and GVHD-free/relapse-free survival (GRFS) were calculated using Kaplan-Meier methodology.
The comparisons were made using the log-rank test. The difference levels of p<0.05 were considered significant. Cumulative incidence analysis was used for aGVHD, cGVHD, relapse incidence and NRM. The comparisons were made using Gray test. The parameters with p.value <0.1 were selected for further Fyne-Gray regression analysis.
Results
Hematopoietic recovery
Stem cell engraftment after haplo-HSCT was documented in 61% of total group of patients (n=72). CD34+cell level less than 3×106/kg significantly reduced the engraftment rate (p=0.02). Median neutrophil engraftment time (absolute neutrophil count reached ≥0.5×109/L for 3 consecutive days) was day +22 (11-58) and median platelet engraftment time (platelet count reached ≥20×109/L for 7 consecutive days without transfusion) was day +23 (11-60). In group PTCY-based GVHD prophylaxis the engraftment time was delayed (Fig. 1). 21 recipient (18%) had primary graft failure, including resistant relapse in 6 patients.

Figure 1. Engraftment terms for the patients with different GvHD prophylaxis. Abscissa, observation terms, days; ordinate, graft failure probability. Red graphs, recovery in cyclophosphamide-based GvHD prophylaxis; blue graphs, Cy-free regimens.
Box A, platelet engraftment time; Box B, neutrophil engraftment time
Survival data
Two-year overall survival (OS) in general group proved to be 40.3% after haplo-HSCT (Fig. 2). Particularly, the two-year OS in patients transplanted in remission of ALL and AML was 57% and 46% respectively as compared to 22% and 19% for the patients transplanted in adverse disease status (р=0.07). Overall survival for patients with lymphoproliferative disorders, acute leukemia and other diseases proved to be 82%, 31%, and 54% respectively (p=0.002, Fig. 2). For patients who received haplo-HSCT as salvage therapy two-year OS was 29% as compared to 57% for patients transplanted in remissions of diseases (р=0.001). Two-year event-free survival (EFS) and GVHD-free/relapse-free survival (GRFS) group proved to be 35.7% and 21% respectively (Fig. 3). Event-free survival for patients with lymphoproliferative disorders was significant higher compared with other groups: 76% vs 26% for patient with acute leukemia and 54% for patients with the other diseases (p=0.01, Fig. 2). With the current sample size GVHD prophylaxis based on рost-transplant cyclophosphamide had no significant impact for two-year OS and EFS (p=0.15 for OS and p=0.28 for EFS, Fig. 2).

Figure 2. Clinical outcomes of haplo-HSCT. Abscissa, observation terms, days; ordinate, survival probability
Note: A, B, two-year overall survival and event-free survival in general group; C, D, two-year overall survival and event-free survival depending on the GVHD prophylaxis (PTCY, post-transplant cyclophosphamide; TCD, T-cell depleted, ATG-based GVHD prophylaxis with ATGAM); E, F, two-year overall survival and event-free survival among patients with different disorders.

Figure 3. GVHD-free/relapse-free survival in general group.
Abscissa, observation terms, days; ordinate, survival probability
In the multivariate analysis, we found that advanced disease phase (p=0.03, 95%CI HR 1.074-4.286), acute GVHD (p=0.0039, 95%CI HR 0.145-0.69), and the earlier terms after transplantation (p=0.0042, 95%CI HR 0.711-0.938) were negative predictors of survival
(Fig. 4).

Figure 4. Subgroup analysis of event- free survival post-HSCT and relative risk factors (a Forest plot)
Posttransplant complications
Out of the 72 patients with engraftment, the cumulative incidence of acute GVHD grade II-IV and severe aGVHD grade III-IV was 19% and 10% respectively. Use of manipulated transplants and PBSC as a source of graft significantly increased the incidence of aGVHD. However, in regression analysis these parameters had no significant impact. The cumulative incidence of chronic GVHD (cGVHD) was 16%. The only factor that significantly increased the risk of cGVHD was the preceeding aGVHD (p=0.03).
The cumulative incidence of relapse was 21%. In multivariate analysis, we found that BM as a source of graft (p=0.003, 95%CI HR 0.10-0.64), high/very high DRI group (p=0.04, 95%CI HR 1.02-2.72) were associated with a significantly increased incidence of relapse.
The overall transplant-associated mortality was 43% in the studied group. For patients who received haplo-HSCT as salvage therapy (47% vs 36%, p=0.03) and also in the group of patients with acute leukemia (48% vs 38% for patients with the other diseases, p=0.04) overall transplant-associated mortality was significantly higher. In multivariate analysis only advanced disease status did significantly impact the transplant-associated mortality (p=0.03, 95%CI HR 1.03-3.1).
Eighty-four recipients (65%) developed clinically significant complications. The main complications were as follows: grade II-III mucositis (53 recipients, 63%); hemorrhagic cystitis (20 recipients, 24%); sepsis (41 recipients, 49%); severe sepsis with septic shock (30 recipients, 36%); invasive fungal disease (17 recipients, 20%); clinically significant CMV reactivation (27 recipients, 32%).
The main cause of death up to day +100 (n=48) were infectious complications (n=32, 67%). Clinical and molecular relapses up to 100 days were observed in 7 recipients (15%).
Causes of death at later post-transplant period (n=28) were presented by infectious complications (n=13, 46%) and progression of primary disease (n=15, 54%).
Discussion
Allo-HSCT of the non-manipulated primed bone marrow from a haploidentical donor proved to be an effective approach to achieve clinical remission in children and adolescents with malignant disorders of hematopoiesis [30]. However, the role of this type of transplantation in the treatment of adult patients is still not completely determined. Immediate availability of a haploidentical donor makes this approach an attractive treatment option for patients who lack an HLA-identical donor or those for whom a MUD cannot be found in a timely manner. In recent years, use of post-transplant cyclophosphamide for GVHD prophylaxis after T-cell repleted haploidentical HSCT has yielded encouraging results in adults. In terms of survival, the outcomes following haploidentical HSCT with post-transplant cyclophosphamide have been comparable to MRD or MUD transplant in several non-randomized studies. Particularly, in cases where an HLA-identical sibling donor is not available for an AML patient with adverse disease a haploidentical donor may be used with the expectation of similar results, compared with those achieved with 10/10 matched and 9/10 mismatched UD unrelated donors. In our study, in a group of patients with acute leukemia, both in remission and in relapse, we obtained results comparable to the results of multicenter studies.
PTCy-based haplo-HSCT is associated with similar results with respect to NRM, OS, and EFS with those of conventional transplantations for patients with Hodgkin lymphoma. In a recent study by Martínez С et al, overall survival, relapse incidences and non-relapse mortality were 67%, 39% and 17% [31]. In the group of patients transplanted in our BMT center, these results were as follows: OS was 79%, relapse incidences – 15% and non-relapse mortality was 14%. In addition, several studies demonstrated the advantages for haplo-HSCT compared with the conventional transplantations for patients with r/r Hodgkin lymphoma allowing long-term remissions with limited toxicity, low GVHD incidence and early immune reconstitution to be achieved [32]. The data obtained allow of considering haplo-HSCT to be an acceptable option for patients with refractory/resistant (R/R) Hodgkin lymphoma.
The main causes of death according to our results were infectious complications in the pre-engraftment period and due to slow immune reconstitution after HSCT. The majority of patients were patients with relapsed/refractory acute leukemia who previously received significant number of chemotherapy courses. It is known, that the risk for colonization resistant bacteria is highest among patients with acute leukemia or high-risk MDS. Importantly, the treatment of these diseases prior to allo-HSCT typically requires one or more hospital admissions for high-dose chemotherapy and broad-spectrum antibiotics for fever and neutropenia, which presumably increases the risk of colonization multidrug resistant bacteria. Bacterial colonization in the setting of allo-HSCT confers an extraordinarily high risk for bloodstream infection in the early post-transplant period, with a considerable decrement in survival [33]. An additional adverse factor for patients with refractory disease was iron overload due to multiple blood transfusions. In accordance with our previous findings, we observed that the baseline increase of serum ferritin contents is associated with higher risk of febrile episodes, infectious conditions, and slower recovery of myeloid cells [34].
Post-transplant relapses represent the major problem for these patients. High percentage of relapses in our group of patients (39%) may be explained by the disease status at the time of haplo-HSCT. The majority of the patients (56%, n=67) received haplo-HSCT as a salvage therapy. According to the data published by Italian group, the relapse rates may reach 50% in this subset of patients [35, 36]. A strong graft-versus-leukemia effect mediated by alloreactive NK cells, resulting in reduced risk for relapse, was documented in adult patients with acute myeloid leukemia, undergoing T-cell-depleted HLA-haploidentical HSCT. Among receptors influencing NK cell function, the killer-cell immunoglobulin-like receptors (KIRs) are of particular importance. Two basic KIR haplotypes can be found in humans: the group A and the group B haplotypes [37]. Noteworthy, in a recent study by Michaelis et al, 57 adults with hematological malignancies given T-cell-depleted haploidentical HSCT were found to have a reduced risk for relapse when transplanted from a KIR haplotype B donor [38]. The presence of activating KIR, as seen in KIR haplotype B might reduce relapse in myeloid malignancies [39]. In our study, KIR genotyping was not carried out.
Graft failure remains a serious obstacle to the success of haplo-HSCT. Our haplo-HSCT data show unsatisfactory primary graft failure rate (18%). Most commonly, graft failure mediated by residual cellular immunity (recipient T-cells or NK-mediated allograft rejection) or humoral immunity (HLA-specific antibodies). In our study, we did not screen HLA -antibodies. Patients sensitized by blood transfusions, but also by pregnancy are at increased risk of rejection. The question of effective depletion of NK- cells still remains unresolved. Another major status for graft failure which may explain the observed results is the advanced disease status [40]. This might have significantly contributed to our results. The approach to dealing with the graft failure is the implementation of novel bridge therapies.
Conclusion
In summary, our results show that unmanipulated haplo-HSCT is a reasonable treatment option for adult patients with different malignant disorders of hematopoiesis. The major advantage of haploidentical HSCT is the almost universal availability of highly motivated donors who can be mobilized in a short time at a relatively low cost. However, the problematic issue is the higher rate of graft failure, increased non-relapse mortality (NRM) and post-transplant relapses. To improve the results of haplo-HSCT, the appropriate multicenter studies are required.
Conflict of interest
The authors report no conflicts of interest.
References
- Bashey A, Solomon SR. T-cell replete haploidentical donor transplantation using post-transplant CY: an emerging standard-of-care option for patients who lack an HLA-identical sibling donor. Bone Marrow Transplant. 2014; 49(8):999-1008.
- Santoro N, Ruggeri A, Labopin M, Bacigalupo A, Ciceri F, Gülbaş Z, Huang H, Afanasyev B, Arcese W, Wu D, Koc Y, Tischer J, Santarone S, Giebel S, Mohty M, Nagler A. Unmanipulated haploidentical stem cell transplantation in adults with acute lymphoblastic leukemia: a study on behalf of the Acute Leukemia Working Party of the EBMT. J Hematol Oncol. 2017;10(1):113. doi: 10.1186/s13045-017-0480-5.
- Brissot E, Labopin M, Ehninger G, Stelljes M, Brecht A, Ganser A, Tischer J, Kröger N, Afanasyev B, Finke J, Elmaagacli A, Einsele H, Mohty M, Nagler A. Haploidentical versus unrelated allogeneic stem cell transplantation for relapsed/refractory acute myeloid leukemia: a report on 1578 patients from the Acute Leukemia Working Party of the EBMT. Haematologica. 2019;104(3):524-532.
- Thomas' Hematopoietic Cell Transplantation. 3rd ed. Blackwell Publishing, Malden, MA; 2004.
- Szydlo R, Goldman JM, Klein JP, Gale RP, Ash RC, Bach FH, Bradley BA, Casper JT, Flomenberg N, Gajewski JL, Gluckman E, Henslee-Downey PJ, Hows JM, Jacobsen N, Kolb HJ et al. Results of allogeneic bone marrow transplants for leukemia using donors other than HLA-identical siblings. J Clin Oncol. 1997;15(5):1767-1777.
- Gragert L, Eapen M, Williams E, Freeman J, Spellman S, Baitty R, Hartzman R, Rizzo JD, Horowitz M, Confer D, Maiers M. HLA match likelihoods for hematopoietic stem-cell grafts in the U.S. registry. N Engl J Med. 2014; 371(4):339-348.
- Fabricius WA, Ramanathan M. Review on haploidentical hematopoietic cell transplantation in patients with hematologic malignancies. Adv Hematol. 2016; 2016:5726132. doi: 10.1155/2016/5726132.
- Bejanyan N, Haddad H, Brunstein C. Alternative donor transplantation for acute myeloid leukemia. J Clin Med. 2015; 4(6):1240-1268.
- Reisner Y, Kapoor N, Kirkpatrick D, Pollack MS, Cunningham-Rundles S, Dupont B, Hodes MZ, Good RA, O'Reilly RJ. Transplantation for severe combined immunodeficiency with HLA-A,B,D,DR incompatible parental marrow cells fractionated by soybean agglutinin and sheep red blood cells. Blood. 1983;61(2):341-348.
- Kernan NA, Flomenberg N, Dupont B, R. J. O'Reilly. Graft rejection in recipients of T-cell-depleted HLA-nonidentical marrow transplants for leukemia. Identification of host-derived antidonor allocytotoxic T lymphocytes. Transplantation. 1987;43(6):842-7.
- Martin PJ. The role of donor lymphoid cells in allogeneic marrow engraftment. Bone Marrow Transplant. 1990; 6:283-289.
- Reisner Y, Ben-Bassat I, Douer D, Kaploon A, Schwartz E, Ramot B. Demonstration of clonable alloreactive host T cells in a primate model for bone marrow transplantation. Proc Natl Acad Sci USA. 1986;83:4012-4015.
- Bachar-Lustig E, Rachamim N, Li HW, Lan F , Reisner Y. Megadose of T cell-depleted bone marrow overcomes MHC barriers in sublethally irradiated mice. Nat Med. 1995; 1 (12): 1268-73.
- Gur H, Krauthgamer R, Berrebi A, Klein T , Nagler A , Tabilio A , Martelli MF , Reisner Y .Tolerance induction by megadose hematopoietic progenitor cells: expansion of veto cells by short-term culture of purified human CD34(+) cells. Blood. 2002;99(11):4174-81.
- Reisner Y, Gur H, Reich-Zeliger S, Martelli MF, Bachar-Lustig E. Hematopoietic stem cell transplantation across major genetic barriers: tolerance induction by megadose CD34 cells and other veto cells. Ann NY Acad Sci. 2005;1044:70-83. Review.
- Aversa F, Tabilio A, Terenzi A, Velardi A, Falecetti F, Giannoni C, Iacucci R, Zei T, Martelli MP, Gambelunghe C. Successful engraftment of T-cell-depleted haploidentical “three-loci” incompatible transplants in leukemia patients by addition of recombinant human granulocyte colony-stimulating factor-mobilized peripheral blood progenitor cells to bone marrow inoculum. Blood. 1994;84(11):3948-3955.
- Aversa F, Velardi A, Tabilio A, Reisner Y, Hammers MF. Haploidentical stem cell transplantation in leukemia. Blood Rev. 2001;15(3):111-119.
- Ciceri F, Labopin M, Aversa F, Rowe JM, Bunjes D, Lewalle P, Nagler A, Di Bartolomeo P, Lacerda JF, Lupo Stanghellini MT, Polge E, Frassoni F, Martelli MF, Rocha V. A survey of fully haploidentical hematopoietic stem cell transplantation in adults with high-risk acute leukemia: a risk factor analysis of outcomes for patients in remission at transplantation. Blood. 2008;112:3574-3581.
- Hoffmann P, Ermann J, Edinger M, Fathman CG, Strober S. Donor-type CD4(+)CD25(+) regulatory T cells suppress lethal acute graft-versus-host disease after allogeneic bone marrow transplantation. J Exp Med. 2002;196(3):389-399.
- Nguyen VH, Shashidhar S, Chang DS, Ho L, Kambham N, Bachmann M, Brown JM, Negrin RS. The impact of regulatory T cells on T-cell immunity following hematopoietic cell transplantation. Blood. 2008;111(2):945-953.
- Minculescu L, Sengeløv H. The role of gamma delta T cells in haematopoietic stem cell transplantation. Scand J Immunol. 2015;81:459-468.
- Lang P, Feuchtinger T, Teltschik HM, Schwinger W, Schlegel P, Pfeiffer M, Schumm M, Lang AM, Lang B, Schwarze CP, Ebinger M, Urban C, Handgretinger R. Improved immune recovery after transplantation of TCRαβ/CD19-depleted allografts from haploidentical donors in pediatric patients. Bone Marrow Transplant. 2015;50 Suppl 2:S6-10.
- Maschan MA. Alpha/beta- T lymphocyte depletion: a reliable platform for development of hematopoietic stem cell transplants from haploidentical donors. Russian J Pediatric Hematol Oncol. 2015; 2(3): 34-38 (In Russian).
- Teschner D, Distler E, Wehler D, Frey M, Marandiuc D, Langeveld K, Theobald M, Thomas S, Herr W. Depletion of naive T cells using clinical grade magnetic CD45RA beads: a new approach for GVHD prophylaxis. Bone Marrow Transplant. 2014;49(1):138-144.
- D.-P. Lu, L. Dong, T. Wu, Huang XJ, Zhang MJ, Han W, Chen H, Liu DH, Gao ZY, Chen YH, Xu LP, Zhang YC, Ren HY, Li D, Liu KY.Conditioning including antithymocyte globulin followed by unmanipulated HLA-mismatched/haploidentical blood and marrow transplantation can achieve comparable outcomes with HLA-identical sibling transplantation. Blood. 2006; 107(8): 3065-3073.
- X. J. Huang, D. H. Liu, K. Y. Liu, Xu LP, Chen H, Han W, Chen YH, Wang JZ, Gao ZY, Zhang YC, Jiang Q, Shi HX, Lu DP. Haploidentical hematopoietic stem cell transplantation without in vitro T-cell depletion for the treatment of hematological malignancies. Bone Marrow Transplant. 2006; 38:291-297.
- P. Di Bartolomeo, S. Santarone, G. De Angelis. Haploidentical, unmanipulated, G-CSF-primed bone marrow transplantation for patients with high-risk hematologic malignancies. Blood. 2013; 121(5):849-857.
- Luznik L, O'Donnell PV, Symons HJ, Chen AR, Leffell MS, Zahurak M, Gooley TA, Piantadosi S, Kaup M, Ambinder RF, Huff CA, Matsui W, Bolaños-Meade J, Borrello I, Powell JD, et al. HLA-haploidentical bone marrow transplantation for hematologic malignancies using nonmyeloablative conditioning and high-dose, post transplantation cyclophosphamide. Biol Blood Marrow Transplant. 2008; 14(6):641-650.
- Moiseev IS, Pirogova OV, Alyanski AL, Babenko EV, Gindina TL, Darskaya EI, Slesarchuk OA, Bondarenko SN, Afanasyev BV. Graft-versus-host disease prophylaxis in unrelated peripheral blood stem cell transplantation with post-transplantation cyclophosphamide, tacrolimus and mycophenalate mofetil. Biol Blood Marrow Transplant. 2016; 22(6):1037-1042.
- Paina OV, Kozhokar PV, Borovkova AS, Frolova AS, Ekushov KA, Bykova TA, Rakhmanova ZZ, Galas MA, Khabirova AG, Markova IV, Semenova EV, Bondarenko SN, Babenko EV, Gindina TL, Alyanskiy AL et al. Ten-year experience of allogeneic haploidentical hematopoietic stem cell transplantation with non-manipulated grafts in children and adolescents with high-risk acute leukemia. Cell Ther Transplant. 2018: 7(2): 20-27.
- Martinez C, Gayoso J, Channels C, Finel H, Peggs K, Dominietto A, Castagna L, Afanasyev B, Robinson S, Blaise D, Corradini P, Itälä-Remes M, Bermúdez A, Forcade E, Russo D, Potter M, McQuaker G, Yakoub-Agha I, Scheid C, Bloor A, Montoto S, Dreger P, Sureda A. Post-transplantation cyclophosphamide-based haploidentical transplantation as alternative to matched sibling or unrelated donor transplantation for Hodgkin lymphoma: A registry study of the Lymphoma Working Party of the European Society for Blood and Marrow Transplantation. J Clin Oncol. 2017;35(30):3425-3432.
- Burroughs LM, O'Donnell PV, Sandmaier BM, Storer BE, Luznik L, Symons HJ, Jones RJ, Ambinder RF, Maris MB, Blume KG, Niederwieser DW, Bruno B, Maziarz RT, Pulsipher MA, Petersen FB, Storb R, Fuchs EJ, Maloney DG. Comparison of outcomes of HLA-matched related, unrelated, or HLA-haploidentical related hematopoietic cell transplantation following nonmyeloablative conditioning for relapsed or refractory Hodgkin lymphoma. Biol Blood Marrow Transplant. 2008;14(11):1279-1287.
- Marasco V, Forcina A, Lorentino F, Greco R. Pre-transplant colonization by a multidrug-resistant Gram negative bacteria has no impact on overall survival and mortality after hematopoietic stem cell transplantation: A single-center experience in 362 patients. J. Blood 2016 128:5743.
- Mostafa Shaheen, Maria O. Ivanova, Ivan S. Moiseev, Sergey V. Bondarchuk, Boris V.Afanasyev. Impact of initial serum ferritin on early post-HSCT complications: a single- center study. Cell Ther Transplant. 2016;5(2): 40-49.
- Solomon SR, Sizemore CA, SanacoreM, Zhang X, Brown S, Holland HK, Morris LE, Bashey A. Haploidentical transplantation using T cell replete peripheral blood stem cells and myeloablative conditioning in patients with high-risk hematological malignancies who lack conventional donors is well tolerated and produces excellent relapse-free survival: results of a prospective phase II trial. Biol Blood Marrow Transplant. 2012;18:1859-1866.
- Aversa F, Terenzi A, Tabilio A et al. Full haplotype mismatched hematopoietic stem-cell transplantation: a phase II study in patients with acute leukemia at high risk of relapse. J Clin Oncol. 2005; 23(15):3447-3454.
- Oevermann L, Michaelis SU, Mezger M et al. KIR B haplotype donors confer a reduced risk for relapse after haploidentical transplantation in children with ALL. Blood. 2014;124(17):2744-2747.
- Michaelis SU, Mezger M, Bornhäuser M, Trenschel R, Stuhler G, Federmann B, Oevermann L, Kanz L, Handgretinger R, Bethge WA. KIR haplotype B donors but not KIR-ligand mismatch result in a reduced incidence of relapse after haploidentical transplantation using reduced intensity conditioning and CD3/CD19-depleted grafts. Ann Hematol. 2014;93(9):1579-1586.
- Heidenreich S, Kröger N. Reduction of relapse after unrelated donor stem cell transplantation by KIR-based graft selection. Front Immunol. 2017; 8:41. Published 2017 Feb 8. doi:10.3389/fimmu.2017.00041.
- Mattsson J, Ringdén O, Storb R. Graft failure after allogeneic hematopoietic cell transplantation. Biol Blood Marrow Transplant. 2008;14(1 Suppl 1):165-170.
Introduction
Allogeneic HSCT (allo-HSCT) is potentially curative option for a wide variety of malignant and nonmalignant disorders of hematopoiesis [1-4]. Historically, the best outcomes of allo-HSCT were obtained in cases when a donor was an HLA-matched sibling [5]. The probability of having an HLA-matched sibling donor is approximately thirty percent [6]. For patients who lack an HLA-matched sibling, alternative sources of donor grafts can be found in suitable HLA-matched adult unrelated donors (MUD), unrelated umbilical cord blood (UCB) donors, and partially HLA-mismatched-unrelated donors (mMUD) or HLA-haploidentical related donors (haplo-HSCT) [1, 8]. Despite the increasing number of volunteers in unrelated donor registries, the likelihood of finding a suitable matched unrelated donor is modest [6, 7]. However, haploidentical donor can be found for nearly every patient. The use of haploidentical donors is not limited by racial/ethnic HLA diversity or unusual HLA phenotypes due to mixed racial ancestry [6]. The benefits of haplo-HSCT include immediate donor availability for patients who need the transplant as soon as possible. Besides, post-transplant donor-derived cellular therapy is more easily accessible with the use of a related donor. In addition, the greater HLA mismatch associated with haploidentical HSCT (haplo-HSCT) may potentiate graft-versus-tumor (GVT) effects. However, this method was historically associated with poor engraftment, high risk of early death, and severe graft-versus-host disease (GVHD).
Earlier attempts at using unmanipulated haploidentical transplant were associated with an unacceptably high rate of GVHD related mortality. Several strategies have been evolved over the past decade to avoid these disadvantages. The advent of T-cell depleted haplo-SCT has allowed better control of the severe GVHD risk [9]. However, this approach was associated with a high rate of graft failure due to host T-lymphocytes that survived the conditioning regimen [10-12]. Later studies have shown that murine and human hematopoietic stem cells have veto cell activity and infusion of a large number of donor hematopoietic stem cells can overcome the MHC barrier and promote engraftment [13-15]. Megadose human CD34+ stem cells (on average >10×106 CD34+ cells/kg body weight) with minimal T cell contamination (a median of 1×104/kg weight) have been successfully used in haploidentical transplantation, which results in high-level engraftment of MHC disparate stem cells. The use of intensive conditioning without additional GVHD prophylaxis led to the result that nearly 80% of patients achieved primary engraftment and only 18% of the patients developed grade II-IV acute GVHD [16, 17]. The major disadvantages of T-cell depleted grafts are both high rate of relapse and nonrelapse mortality (NRM) due to slow immune reconstitution and, thus, infectious complications [18].
Another method to manipulate the T-cell depleted graft is co-infusion of donor-derived regulatory T-cells (Tregs). CD4+CD25+ regulatory T-cells have been shown to suppress proliferative responses of CD4+CD25− T-cells to allo-antigenic stimulation in vitro and are required for ex vivo tolerization of donor T-cells, which results in their reduced potential to induce aGVHD [19, 20]. Despite promising results, this approach is costly and technically demanding, which limits its application to experienced centers.
Another innovative approach is to selectively deplete T-cells responsible for GVHD (TCR alpha-beta) while sparing gamma-delta T-cells (γδ T-cells). Gamma-delta T-cells account for 1% to 10% of peripheral T-cells and have MHC-unrestricted innate cytotoxic activity against tumor cells [21-23]. The use of TCRαβ/CD19-depleted stem cells essentially accelerated immune recovery.
A more recent strategy is to selectively deplete naive T-cells to separate GVHD and the GVL effect. Naive T-cells with CD45RA expression demonstrate to be the most allo-reactive among the T-cell subsets. Ex vivo depletion of CD45RA T-cells and adoptive transfer of CD45RA-memory T-cells accelerate the immune reconstitution, increase the GVL effect while abrogating GVHD [24].
A group of Chinese researchers used a method based on G-CSF-stimulation of the donor, intensified immunosuppression, antithymocyte globulin as in vivo T-cell depletion, and combination of peripheral blood stem cell and bone marrow allografts. Despite satisfactory relapse-free survival rates, acceptable NRM and engraftment, relatively high incidence of severe acute and chronic GVHD was observed. In addition, the standard-risk patients often suffered with opportunistic infections [25, 26].
Trying to improve these results, Italian research team modified this approach through using only BM allografts and adding basiliximab which allowed them to achieve a lower rate of chronic GVHD that included both forms, limited and extensive [27].
Another approach to allo-HSCT was developed in Baltimore (USA) based on non-manipulated graft followed by post-transplant cyclophosphamide injection (PtCy) [28, 29]. This approach has overcome most obstacles historically connected with haplo-HSCT. Thus, recent changes in haplo- HSCT methodology have allowed to improve its results.
The aim of this study was to compare the efficiency of various haplo-HSCT approaches used in our HSCT center.
Patients and methods
The study included 119 patients transplanted from a haploidentical donor (haplo-HSCT) between 2006 and 2018 at the R. M. Gorbacheva Institute of Children Oncology (CIC 725). Their clinical parameters are shown in Table 1. Nine patients received second haplo-HSCT, due to graft failure in 8 cases and relapse in one patient. Eight patients were transplanted from the same donor and one patient from the other donor. Median age was 26 years (18-63), 61 patients were males (51%). Most frequent diagnosis in transplanted patients was acute leukemia (77%, n=92). Primary diagnoses were ALL (31%, n=37), AML (45%, n=53), ABL (2%, n=2), myeloproliferative neoplasms (8%, n=9), lymphoproliferative disorders (13%, n=16), severe aplastic anemia (1%, n=2). Median follow-up was 371 days (1-2219). A total of 46 patients with acute leukemia (38%) had complete remission at the time of HSCT (the first complete remission – 80%, n=37, the 2d or greater remission – 20%, n=9), 33% patients (n=30) had relapse, 15% patients (n=14) had refractory disease. Thus, 67 (56%) patients in the general group received haplo-HSCT as salvage therapy. Non-myeloablative, or reduced-intensity conditioning (RIC) was employed in 81% (n=96) and the myeloablative treatment (MAC) was used in 19% (n=23). Seventy-seven patients (65%) received busulfan, 14 patients (12%), melphalan, and 28 patients (23%) were administered other alkylating agents. Bone marrow was the graft source for 61% patients (n=73), peripheral blood (PBSC) – 39% patients (n=46). Mean transplant CD34+cell and CD3+cell dose was 5×106/kg (1.5-10) and 10×107/kg (2-44) respectively for bone marrow as a graft source, whereas it was 5.1×106/kg (1-16.6) and 10×107/kg (3-47) respectively for recipients who received PBSC as a source of graft.
GVHD prophylaxis based on рost-transplant cyclophosphamide (PTCY-based GVHD prophylaxis) 50 mg/kg at day+3, +4 was employed in 78 patients (66%), also these recipients received tacrolimus 0.03 mg/kg/day and MMF 30-45 mg/kg starting from day +5. Eleven patients (9%) received a T-cell manipulated transplant. The protocol of depletion and HSCT included conditioning according to the GIAC protocol, depleted PBSC in combination with native BM and ATGAM, tacrolimus, MMF.
A total of 30 patients (25%) received GVHD prophylaxis with ATGAM- 31 (26%) and alemtuzumab in 5 patients (4%). Tacrolimus was used for GVHD prophylaxis in 93 patients (72%), cyclosporin A – in 18 patients (14%). Clinical characteristics of the study group are presented in Table 1.
Table 1. Clinical characteristics of the study group

Clinical diagnosis of acute (aGVHD) and chronic GVHD (cGVHD) was based on standard criteria and confirmed by histological analysis of skin and/or rectal biopsy specimens. First-line and second-line therapy for GVHD was provided according to institutional protocols. For statistical evaluation, SPSS Statistics v.17 was used. Two-year time frame was selected for all outcomes. In the group description overall survival (OS), event-free survival (EFS) and GVHD-free/relapse-free survival (GRFS) were calculated using Kaplan-Meier methodology.
The comparisons were made using the log-rank test. The difference levels of p<0.05 were considered significant. Cumulative incidence analysis was used for aGVHD, cGVHD, relapse incidence and NRM. The comparisons were made using Gray test. The parameters with p.value <0.1 were selected for further Fyne-Gray regression analysis.
Results
Hematopoietic recovery
Stem cell engraftment after haplo-HSCT was documented in 61% of total group of patients (n=72). CD34+cell level less than 3×106/kg significantly reduced the engraftment rate (p=0.02). Median neutrophil engraftment time (absolute neutrophil count reached ≥0.5×109/L for 3 consecutive days) was day +22 (11-58) and median platelet engraftment time (platelet count reached ≥20×109/L for 7 consecutive days without transfusion) was day +23 (11-60). In group PTCY-based GVHD prophylaxis the engraftment time was delayed (Fig. 1). 21 recipient (18%) had primary graft failure, including resistant relapse in 6 patients.

Figure 1. Engraftment terms for the patients with different GvHD prophylaxis. Abscissa, observation terms, days; ordinate, graft failure probability. Red graphs, recovery in cyclophosphamide-based GvHD prophylaxis; blue graphs, Cy-free regimens.
Box A, platelet engraftment time; Box B, neutrophil engraftment time
Survival data
Two-year overall survival (OS) in general group proved to be 40.3% after haplo-HSCT (Fig. 2). Particularly, the two-year OS in patients transplanted in remission of ALL and AML was 57% and 46% respectively as compared to 22% and 19% for the patients transplanted in adverse disease status (р=0.07). Overall survival for patients with lymphoproliferative disorders, acute leukemia and other diseases proved to be 82%, 31%, and 54% respectively (p=0.002, Fig. 2). For patients who received haplo-HSCT as salvage therapy two-year OS was 29% as compared to 57% for patients transplanted in remissions of diseases (р=0.001). Two-year event-free survival (EFS) and GVHD-free/relapse-free survival (GRFS) group proved to be 35.7% and 21% respectively (Fig. 3). Event-free survival for patients with lymphoproliferative disorders was significant higher compared with other groups: 76% vs 26% for patient with acute leukemia and 54% for patients with the other diseases (p=0.01, Fig. 2). With the current sample size GVHD prophylaxis based on рost-transplant cyclophosphamide had no significant impact for two-year OS and EFS (p=0.15 for OS and p=0.28 for EFS, Fig. 2).

Figure 2. Clinical outcomes of haplo-HSCT. Abscissa, observation terms, days; ordinate, survival probability
Note: A, B, two-year overall survival and event-free survival in general group; C, D, two-year overall survival and event-free survival depending on the GVHD prophylaxis (PTCY, post-transplant cyclophosphamide; TCD, T-cell depleted, ATG-based GVHD prophylaxis with ATGAM); E, F, two-year overall survival and event-free survival among patients with different disorders.

Figure 3. GVHD-free/relapse-free survival in general group.
Abscissa, observation terms, days; ordinate, survival probability
In the multivariate analysis, we found that advanced disease phase (p=0.03, 95%CI HR 1.074-4.286), acute GVHD (p=0.0039, 95%CI HR 0.145-0.69), and the earlier terms after transplantation (p=0.0042, 95%CI HR 0.711-0.938) were negative predictors of survival
(Fig. 4).

Figure 4. Subgroup analysis of event- free survival post-HSCT and relative risk factors (a Forest plot)
Posttransplant complications
Out of the 72 patients with engraftment, the cumulative incidence of acute GVHD grade II-IV and severe aGVHD grade III-IV was 19% and 10% respectively. Use of manipulated transplants and PBSC as a source of graft significantly increased the incidence of aGVHD. However, in regression analysis these parameters had no significant impact. The cumulative incidence of chronic GVHD (cGVHD) was 16%. The only factor that significantly increased the risk of cGVHD was the preceeding aGVHD (p=0.03).
The cumulative incidence of relapse was 21%. In multivariate analysis, we found that BM as a source of graft (p=0.003, 95%CI HR 0.10-0.64), high/very high DRI group (p=0.04, 95%CI HR 1.02-2.72) were associated with a significantly increased incidence of relapse.
The overall transplant-associated mortality was 43% in the studied group. For patients who received haplo-HSCT as salvage therapy (47% vs 36%, p=0.03) and also in the group of patients with acute leukemia (48% vs 38% for patients with the other diseases, p=0.04) overall transplant-associated mortality was significantly higher. In multivariate analysis only advanced disease status did significantly impact the transplant-associated mortality (p=0.03, 95%CI HR 1.03-3.1).
Eighty-four recipients (65%) developed clinically significant complications. The main complications were as follows: grade II-III mucositis (53 recipients, 63%); hemorrhagic cystitis (20 recipients, 24%); sepsis (41 recipients, 49%); severe sepsis with septic shock (30 recipients, 36%); invasive fungal disease (17 recipients, 20%); clinically significant CMV reactivation (27 recipients, 32%).
The main cause of death up to day +100 (n=48) were infectious complications (n=32, 67%). Clinical and molecular relapses up to 100 days were observed in 7 recipients (15%).
Causes of death at later post-transplant period (n=28) were presented by infectious complications (n=13, 46%) and progression of primary disease (n=15, 54%).
Discussion
Allo-HSCT of the non-manipulated primed bone marrow from a haploidentical donor proved to be an effective approach to achieve clinical remission in children and adolescents with malignant disorders of hematopoiesis [30]. However, the role of this type of transplantation in the treatment of adult patients is still not completely determined. Immediate availability of a haploidentical donor makes this approach an attractive treatment option for patients who lack an HLA-identical donor or those for whom a MUD cannot be found in a timely manner. In recent years, use of post-transplant cyclophosphamide for GVHD prophylaxis after T-cell repleted haploidentical HSCT has yielded encouraging results in adults. In terms of survival, the outcomes following haploidentical HSCT with post-transplant cyclophosphamide have been comparable to MRD or MUD transplant in several non-randomized studies. Particularly, in cases where an HLA-identical sibling donor is not available for an AML patient with adverse disease a haploidentical donor may be used with the expectation of similar results, compared with those achieved with 10/10 matched and 9/10 mismatched UD unrelated donors. In our study, in a group of patients with acute leukemia, both in remission and in relapse, we obtained results comparable to the results of multicenter studies.
PTCy-based haplo-HSCT is associated with similar results with respect to NRM, OS, and EFS with those of conventional transplantations for patients with Hodgkin lymphoma. In a recent study by Martínez С et al, overall survival, relapse incidences and non-relapse mortality were 67%, 39% and 17% [31]. In the group of patients transplanted in our BMT center, these results were as follows: OS was 79%, relapse incidences – 15% and non-relapse mortality was 14%. In addition, several studies demonstrated the advantages for haplo-HSCT compared with the conventional transplantations for patients with r/r Hodgkin lymphoma allowing long-term remissions with limited toxicity, low GVHD incidence and early immune reconstitution to be achieved [32]. The data obtained allow of considering haplo-HSCT to be an acceptable option for patients with refractory/resistant (R/R) Hodgkin lymphoma.
The main causes of death according to our results were infectious complications in the pre-engraftment period and due to slow immune reconstitution after HSCT. The majority of patients were patients with relapsed/refractory acute leukemia who previously received significant number of chemotherapy courses. It is known, that the risk for colonization resistant bacteria is highest among patients with acute leukemia or high-risk MDS. Importantly, the treatment of these diseases prior to allo-HSCT typically requires one or more hospital admissions for high-dose chemotherapy and broad-spectrum antibiotics for fever and neutropenia, which presumably increases the risk of colonization multidrug resistant bacteria. Bacterial colonization in the setting of allo-HSCT confers an extraordinarily high risk for bloodstream infection in the early post-transplant period, with a considerable decrement in survival [33]. An additional adverse factor for patients with refractory disease was iron overload due to multiple blood transfusions. In accordance with our previous findings, we observed that the baseline increase of serum ferritin contents is associated with higher risk of febrile episodes, infectious conditions, and slower recovery of myeloid cells [34].
Post-transplant relapses represent the major problem for these patients. High percentage of relapses in our group of patients (39%) may be explained by the disease status at the time of haplo-HSCT. The majority of the patients (56%, n=67) received haplo-HSCT as a salvage therapy. According to the data published by Italian group, the relapse rates may reach 50% in this subset of patients [35, 36]. A strong graft-versus-leukemia effect mediated by alloreactive NK cells, resulting in reduced risk for relapse, was documented in adult patients with acute myeloid leukemia, undergoing T-cell-depleted HLA-haploidentical HSCT. Among receptors influencing NK cell function, the killer-cell immunoglobulin-like receptors (KIRs) are of particular importance. Two basic KIR haplotypes can be found in humans: the group A and the group B haplotypes [37]. Noteworthy, in a recent study by Michaelis et al, 57 adults with hematological malignancies given T-cell-depleted haploidentical HSCT were found to have a reduced risk for relapse when transplanted from a KIR haplotype B donor [38]. The presence of activating KIR, as seen in KIR haplotype B might reduce relapse in myeloid malignancies [39]. In our study, KIR genotyping was not carried out.
Graft failure remains a serious obstacle to the success of haplo-HSCT. Our haplo-HSCT data show unsatisfactory primary graft failure rate (18%). Most commonly, graft failure mediated by residual cellular immunity (recipient T-cells or NK-mediated allograft rejection) or humoral immunity (HLA-specific antibodies). In our study, we did not screen HLA -antibodies. Patients sensitized by blood transfusions, but also by pregnancy are at increased risk of rejection. The question of effective depletion of NK- cells still remains unresolved. Another major status for graft failure which may explain the observed results is the advanced disease status [40]. This might have significantly contributed to our results. The approach to dealing with the graft failure is the implementation of novel bridge therapies.
Conclusion
In summary, our results show that unmanipulated haplo-HSCT is a reasonable treatment option for adult patients with different malignant disorders of hematopoiesis. The major advantage of haploidentical HSCT is the almost universal availability of highly motivated donors who can be mobilized in a short time at a relatively low cost. However, the problematic issue is the higher rate of graft failure, increased non-relapse mortality (NRM) and post-transplant relapses. To improve the results of haplo-HSCT, the appropriate multicenter studies are required.
Conflict of interest
The authors report no conflicts of interest.
References
- Bashey A, Solomon SR. T-cell replete haploidentical donor transplantation using post-transplant CY: an emerging standard-of-care option for patients who lack an HLA-identical sibling donor. Bone Marrow Transplant. 2014; 49(8):999-1008.
- Santoro N, Ruggeri A, Labopin M, Bacigalupo A, Ciceri F, Gülbaş Z, Huang H, Afanasyev B, Arcese W, Wu D, Koc Y, Tischer J, Santarone S, Giebel S, Mohty M, Nagler A. Unmanipulated haploidentical stem cell transplantation in adults with acute lymphoblastic leukemia: a study on behalf of the Acute Leukemia Working Party of the EBMT. J Hematol Oncol. 2017;10(1):113. doi: 10.1186/s13045-017-0480-5.
- Brissot E, Labopin M, Ehninger G, Stelljes M, Brecht A, Ganser A, Tischer J, Kröger N, Afanasyev B, Finke J, Elmaagacli A, Einsele H, Mohty M, Nagler A. Haploidentical versus unrelated allogeneic stem cell transplantation for relapsed/refractory acute myeloid leukemia: a report on 1578 patients from the Acute Leukemia Working Party of the EBMT. Haematologica. 2019;104(3):524-532.
- Thomas' Hematopoietic Cell Transplantation. 3rd ed. Blackwell Publishing, Malden, MA; 2004.
- Szydlo R, Goldman JM, Klein JP, Gale RP, Ash RC, Bach FH, Bradley BA, Casper JT, Flomenberg N, Gajewski JL, Gluckman E, Henslee-Downey PJ, Hows JM, Jacobsen N, Kolb HJ et al. Results of allogeneic bone marrow transplants for leukemia using donors other than HLA-identical siblings. J Clin Oncol. 1997;15(5):1767-1777.
- Gragert L, Eapen M, Williams E, Freeman J, Spellman S, Baitty R, Hartzman R, Rizzo JD, Horowitz M, Confer D, Maiers M. HLA match likelihoods for hematopoietic stem-cell grafts in the U.S. registry. N Engl J Med. 2014; 371(4):339-348.
- Fabricius WA, Ramanathan M. Review on haploidentical hematopoietic cell transplantation in patients with hematologic malignancies. Adv Hematol. 2016; 2016:5726132. doi: 10.1155/2016/5726132.
- Bejanyan N, Haddad H, Brunstein C. Alternative donor transplantation for acute myeloid leukemia. J Clin Med. 2015; 4(6):1240-1268.
- Reisner Y, Kapoor N, Kirkpatrick D, Pollack MS, Cunningham-Rundles S, Dupont B, Hodes MZ, Good RA, O'Reilly RJ. Transplantation for severe combined immunodeficiency with HLA-A,B,D,DR incompatible parental marrow cells fractionated by soybean agglutinin and sheep red blood cells. Blood. 1983;61(2):341-348.
- Kernan NA, Flomenberg N, Dupont B, R. J. O'Reilly. Graft rejection in recipients of T-cell-depleted HLA-nonidentical marrow transplants for leukemia. Identification of host-derived antidonor allocytotoxic T lymphocytes. Transplantation. 1987;43(6):842-7.
- Martin PJ. The role of donor lymphoid cells in allogeneic marrow engraftment. Bone Marrow Transplant. 1990; 6:283-289.
- Reisner Y, Ben-Bassat I, Douer D, Kaploon A, Schwartz E, Ramot B. Demonstration of clonable alloreactive host T cells in a primate model for bone marrow transplantation. Proc Natl Acad Sci USA. 1986;83:4012-4015.
- Bachar-Lustig E, Rachamim N, Li HW, Lan F , Reisner Y. Megadose of T cell-depleted bone marrow overcomes MHC barriers in sublethally irradiated mice. Nat Med. 1995; 1 (12): 1268-73.
- Gur H, Krauthgamer R, Berrebi A, Klein T , Nagler A , Tabilio A , Martelli MF , Reisner Y .Tolerance induction by megadose hematopoietic progenitor cells: expansion of veto cells by short-term culture of purified human CD34(+) cells. Blood. 2002;99(11):4174-81.
- Reisner Y, Gur H, Reich-Zeliger S, Martelli MF, Bachar-Lustig E. Hematopoietic stem cell transplantation across major genetic barriers: tolerance induction by megadose CD34 cells and other veto cells. Ann NY Acad Sci. 2005;1044:70-83. Review.
- Aversa F, Tabilio A, Terenzi A, Velardi A, Falecetti F, Giannoni C, Iacucci R, Zei T, Martelli MP, Gambelunghe C. Successful engraftment of T-cell-depleted haploidentical “three-loci” incompatible transplants in leukemia patients by addition of recombinant human granulocyte colony-stimulating factor-mobilized peripheral blood progenitor cells to bone marrow inoculum. Blood. 1994;84(11):3948-3955.
- Aversa F, Velardi A, Tabilio A, Reisner Y, Hammers MF. Haploidentical stem cell transplantation in leukemia. Blood Rev. 2001;15(3):111-119.
- Ciceri F, Labopin M, Aversa F, Rowe JM, Bunjes D, Lewalle P, Nagler A, Di Bartolomeo P, Lacerda JF, Lupo Stanghellini MT, Polge E, Frassoni F, Martelli MF, Rocha V. A survey of fully haploidentical hematopoietic stem cell transplantation in adults with high-risk acute leukemia: a risk factor analysis of outcomes for patients in remission at transplantation. Blood. 2008;112:3574-3581.
- Hoffmann P, Ermann J, Edinger M, Fathman CG, Strober S. Donor-type CD4(+)CD25(+) regulatory T cells suppress lethal acute graft-versus-host disease after allogeneic bone marrow transplantation. J Exp Med. 2002;196(3):389-399.
- Nguyen VH, Shashidhar S, Chang DS, Ho L, Kambham N, Bachmann M, Brown JM, Negrin RS. The impact of regulatory T cells on T-cell immunity following hematopoietic cell transplantation. Blood. 2008;111(2):945-953.
- Minculescu L, Sengeløv H. The role of gamma delta T cells in haematopoietic stem cell transplantation. Scand J Immunol. 2015;81:459-468.
- Lang P, Feuchtinger T, Teltschik HM, Schwinger W, Schlegel P, Pfeiffer M, Schumm M, Lang AM, Lang B, Schwarze CP, Ebinger M, Urban C, Handgretinger R. Improved immune recovery after transplantation of TCRαβ/CD19-depleted allografts from haploidentical donors in pediatric patients. Bone Marrow Transplant. 2015;50 Suppl 2:S6-10.
- Maschan MA. Alpha/beta- T lymphocyte depletion: a reliable platform for development of hematopoietic stem cell transplants from haploidentical donors. Russian J Pediatric Hematol Oncol. 2015; 2(3): 34-38 (In Russian).
- Teschner D, Distler E, Wehler D, Frey M, Marandiuc D, Langeveld K, Theobald M, Thomas S, Herr W. Depletion of naive T cells using clinical grade magnetic CD45RA beads: a new approach for GVHD prophylaxis. Bone Marrow Transplant. 2014;49(1):138-144.
- D.-P. Lu, L. Dong, T. Wu, Huang XJ, Zhang MJ, Han W, Chen H, Liu DH, Gao ZY, Chen YH, Xu LP, Zhang YC, Ren HY, Li D, Liu KY.Conditioning including antithymocyte globulin followed by unmanipulated HLA-mismatched/haploidentical blood and marrow transplantation can achieve comparable outcomes with HLA-identical sibling transplantation. Blood. 2006; 107(8): 3065-3073.
- X. J. Huang, D. H. Liu, K. Y. Liu, Xu LP, Chen H, Han W, Chen YH, Wang JZ, Gao ZY, Zhang YC, Jiang Q, Shi HX, Lu DP. Haploidentical hematopoietic stem cell transplantation without in vitro T-cell depletion for the treatment of hematological malignancies. Bone Marrow Transplant. 2006; 38:291-297.
- P. Di Bartolomeo, S. Santarone, G. De Angelis. Haploidentical, unmanipulated, G-CSF-primed bone marrow transplantation for patients with high-risk hematologic malignancies. Blood. 2013; 121(5):849-857.
- Luznik L, O'Donnell PV, Symons HJ, Chen AR, Leffell MS, Zahurak M, Gooley TA, Piantadosi S, Kaup M, Ambinder RF, Huff CA, Matsui W, Bolaños-Meade J, Borrello I, Powell JD, et al. HLA-haploidentical bone marrow transplantation for hematologic malignancies using nonmyeloablative conditioning and high-dose, post transplantation cyclophosphamide. Biol Blood Marrow Transplant. 2008; 14(6):641-650.
- Moiseev IS, Pirogova OV, Alyanski AL, Babenko EV, Gindina TL, Darskaya EI, Slesarchuk OA, Bondarenko SN, Afanasyev BV. Graft-versus-host disease prophylaxis in unrelated peripheral blood stem cell transplantation with post-transplantation cyclophosphamide, tacrolimus and mycophenalate mofetil. Biol Blood Marrow Transplant. 2016; 22(6):1037-1042.
- Paina OV, Kozhokar PV, Borovkova AS, Frolova AS, Ekushov KA, Bykova TA, Rakhmanova ZZ, Galas MA, Khabirova AG, Markova IV, Semenova EV, Bondarenko SN, Babenko EV, Gindina TL, Alyanskiy AL et al. Ten-year experience of allogeneic haploidentical hematopoietic stem cell transplantation with non-manipulated grafts in children and adolescents with high-risk acute leukemia. Cell Ther Transplant. 2018: 7(2): 20-27.
- Martinez C, Gayoso J, Channels C, Finel H, Peggs K, Dominietto A, Castagna L, Afanasyev B, Robinson S, Blaise D, Corradini P, Itälä-Remes M, Bermúdez A, Forcade E, Russo D, Potter M, McQuaker G, Yakoub-Agha I, Scheid C, Bloor A, Montoto S, Dreger P, Sureda A. Post-transplantation cyclophosphamide-based haploidentical transplantation as alternative to matched sibling or unrelated donor transplantation for Hodgkin lymphoma: A registry study of the Lymphoma Working Party of the European Society for Blood and Marrow Transplantation. J Clin Oncol. 2017;35(30):3425-3432.
- Burroughs LM, O'Donnell PV, Sandmaier BM, Storer BE, Luznik L, Symons HJ, Jones RJ, Ambinder RF, Maris MB, Blume KG, Niederwieser DW, Bruno B, Maziarz RT, Pulsipher MA, Petersen FB, Storb R, Fuchs EJ, Maloney DG. Comparison of outcomes of HLA-matched related, unrelated, or HLA-haploidentical related hematopoietic cell transplantation following nonmyeloablative conditioning for relapsed or refractory Hodgkin lymphoma. Biol Blood Marrow Transplant. 2008;14(11):1279-1287.
- Marasco V, Forcina A, Lorentino F, Greco R. Pre-transplant colonization by a multidrug-resistant Gram negative bacteria has no impact on overall survival and mortality after hematopoietic stem cell transplantation: A single-center experience in 362 patients. J. Blood 2016 128:5743.
- Mostafa Shaheen, Maria O. Ivanova, Ivan S. Moiseev, Sergey V. Bondarchuk, Boris V.Afanasyev. Impact of initial serum ferritin on early post-HSCT complications: a single- center study. Cell Ther Transplant. 2016;5(2): 40-49.
- Solomon SR, Sizemore CA, SanacoreM, Zhang X, Brown S, Holland HK, Morris LE, Bashey A. Haploidentical transplantation using T cell replete peripheral blood stem cells and myeloablative conditioning in patients with high-risk hematological malignancies who lack conventional donors is well tolerated and produces excellent relapse-free survival: results of a prospective phase II trial. Biol Blood Marrow Transplant. 2012;18:1859-1866.
- Aversa F, Terenzi A, Tabilio A et al. Full haplotype mismatched hematopoietic stem-cell transplantation: a phase II study in patients with acute leukemia at high risk of relapse. J Clin Oncol. 2005; 23(15):3447-3454.
- Oevermann L, Michaelis SU, Mezger M et al. KIR B haplotype donors confer a reduced risk for relapse after haploidentical transplantation in children with ALL. Blood. 2014;124(17):2744-2747.
- Michaelis SU, Mezger M, Bornhäuser M, Trenschel R, Stuhler G, Federmann B, Oevermann L, Kanz L, Handgretinger R, Bethge WA. KIR haplotype B donors but not KIR-ligand mismatch result in a reduced incidence of relapse after haploidentical transplantation using reduced intensity conditioning and CD3/CD19-depleted grafts. Ann Hematol. 2014;93(9):1579-1586.
- Heidenreich S, Kröger N. Reduction of relapse after unrelated donor stem cell transplantation by KIR-based graft selection. Front Immunol. 2017; 8:41. Published 2017 Feb 8. doi:10.3389/fimmu.2017.00041.
- Mattsson J, Ringdén O, Storb R. Graft failure after allogeneic hematopoietic cell transplantation. Biol Blood Marrow Transplant. 2008;14(1 Suppl 1):165-170.
Анастасия В. Бейнарович, Елена В. Бабенко, Иван С. Моисеев, Олеся В. Паина, Ольга В. Пирогова, Татьяна А. Рудакова, Татьяна Л. Гиндина, Елена И. Дарская, Елена В. Морозова, Сергей Н. Бондаренко, Людмила С. Зубаровская, Борис В. Афанасьев
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21341" ["VALUE"]=> array(2) { ["TEXT"]=> string(337) "<p>НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета, Санкт-Петербург, Россия</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(325) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21342" ["VALUE"]=> array(2) { ["TEXT"]=> string(4755) "<p style="text-align: justify;">Аллогенная трансплантация костного мозга (алло- ТГСК) является потенциальной возможностью излечения злокачественных и незлокачественных заболеваний кроветворения. Для пациентов, у которых отсутствует HLA-совместимый сиблинг, можно использовать HLA-гаплоидентичного донора (гапло-ТГСК) в качестве альтернативного источника трансплантата. Преимуществом гапло-ТГСК является немедленная доступность донора для пациентов, которым необходимо выполнение трансплантации в короткие сроки. Кроме того, наличие родственного донора делает более доступной клеточную терапию после трансплантации. Также, большее несоответствие по генам HLA-системы в случае гаплоидентичной трансплантации, может потенциировать эффект «трансплантат против опухоли». В этом отчете представлен анализ результатов гапло-ТГСК, выполненных в нашем центре взрослым пациентам с различными злокачественными заболеваниями, при использовании неманипулированного трансплантата. На момент анализа медиана наблюдения составила 371 день (1-2219). Основным диагонозом был острый лейкоз. Шестидесяти семи пациентам (56%) гапло-ТГСК была выполнена в качестве терапии спасения. Общая выживаемость в течении 2 лет в исследуемой группе составила 40,3%. В частности, двухлетняя общая выживаемость у пациентов с ОЛЛ и ОМЛ в ремиссии заболевания, составила 57% и 46% соответственно в сравнении с 22% и 15% у пациентов с продвинутыми стадиями заболеваний. Безрецидивная выживаемость в течение 2 лет, а также выживаемость без проявлений оРТПХ и рецидива заболевания в общей группе составили 35,7% и 21% соответственно. Частота возникновения острой РТПХ II-IV степени и тяжелой РТПХ III-IV степени составили 19% и 10% соответственно. Частота хронической РТПХ составила 16%. Частота возникновения рецидива заболевания составила 21%. Трансплантационная летальность исследуемой группе 43%. В заключение необходимо отметить, что наши результаты показывают, что гапло-ТГСК с использованием неманипулированного трансплантата является приемлемым методом лечения взрослых пациентов с различными злокачественными заболеваниями кроветворения. Однако такие проблемы, как высокая частота неприживления, высокая трансплантационная летальность, а также посттрасплантационные рецидивы остаются чрезвычайно актуальными. </p> <h2>Ключевые слова</h2> <p style="text-align: justify;">Аллогенная трансплантация гемопоэтических стволовых клеток, гаплоидентичная, взрослые пациенты, общая выживаемость, рецидив после трансплантации, реакция «трансплантат против хозяина», неприживление трансплантатата, посттрансплантационный циклофосфамид. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4699) "Аллогенная трансплантация костного мозга (алло- ТГСК) является потенциальной возможностью излечения злокачественных и незлокачественных заболеваний кроветворения. Для пациентов, у которых отсутствует HLA-совместимый сиблинг, можно использовать HLA-гаплоидентичного донора (гапло-ТГСК) в качестве альтернативного источника трансплантата. Преимуществом гапло-ТГСК является немедленная доступность донора для пациентов, которым необходимо выполнение трансплантации в короткие сроки. Кроме того, наличие родственного донора делает более доступной клеточную терапию после трансплантации. Также, большее несоответствие по генам HLA-системы в случае гаплоидентичной трансплантации, может потенциировать эффект «трансплантат против опухоли». В этом отчете представлен анализ результатов гапло-ТГСК, выполненных в нашем центре взрослым пациентам с различными злокачественными заболеваниями, при использовании неманипулированного трансплантата. На момент анализа медиана наблюдения составила 371 день (1-2219). Основным диагонозом был острый лейкоз. Шестидесяти семи пациентам (56%) гапло-ТГСК была выполнена в качестве терапии спасения. Общая выживаемость в течении 2 лет в исследуемой группе составила 40,3%. В частности, двухлетняя общая выживаемость у пациентов с ОЛЛ и ОМЛ в ремиссии заболевания, составила 57% и 46% соответственно в сравнении с 22% и 15% у пациентов с продвинутыми стадиями заболеваний. Безрецидивная выживаемость в течение 2 лет, а также выживаемость без проявлений оРТПХ и рецидива заболевания в общей группе составили 35,7% и 21% соответственно. Частота возникновения острой РТПХ II-IV степени и тяжелой РТПХ III-IV степени составили 19% и 10% соответственно. Частота хронической РТПХ составила 16%. Частота возникновения рецидива заболевания составила 21%. Трансплантационная летальность исследуемой группе 43%. В заключение необходимо отметить, что наши результаты показывают, что гапло-ТГСК с использованием неманипулированного трансплантата является приемлемым методом лечения взрослых пациентов с различными злокачественными заболеваниями кроветворения. Однако такие проблемы, как высокая частота неприживления, высокая трансплантационная летальность, а также посттрасплантационные рецидивы остаются чрезвычайно актуальными.
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, гаплоидентичная, взрослые пациенты, общая выживаемость, рецидив после трансплантации, реакция «трансплантат против хозяина», неприживление трансплантатата, посттрансплантационный циклофосфамид.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21343" ["VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-26-35" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-26-35" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21394" ["VALUE"]=> array(2) { ["TEXT"]=> string(260) "<p>Anastasia V. Beynarovich, Elena V. Babenko, Ivan S. Moiseev, Olesya V. Paina, Olga V. Pirogova, Tatiana A. Rudakova, Tatyana L. Gindina, Elena I. Darskaya, Elena V. Morozova, Sergey N. Bondarenko, Ludmila S. Zubarovskaya, Boris V. Afanasyev</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(248) "Anastasia V. Beynarovich, Elena V. Babenko, Ivan S. Moiseev, Olesya V. Paina, Olga V. Pirogova, Tatiana A. Rudakova, Tatyana L. Gindina, Elena I. Darskaya, Elena V. Morozova, Sergey N. Bondarenko, Ludmila S. Zubarovskaya, Boris V. Afanasyev
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21395" ["VALUE"]=> array(2) { ["TEXT"]=> string(176) "<p>R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantology at the First St. Petersburg State I. Pavlov Medical University</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(164) "R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantology at the First St. Petersburg State I. Pavlov Medical University
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21396" ["VALUE"]=> array(2) { ["TEXT"]=> string(2506) "<p style="text-align: justify;">Allogeneic HSCT (allo-HSCT) is potentially curative option for a wide variety of malignant and nonmalignant disorders of hematopoiesis. For patients who lack an HLA-matched sibling, HLA-haploidentical related donors (haplo-HSCT) can be considered as alternative sources of donor grafts. The benefits of haplo-HSCT include immediate donor availability for patients who are in urgent need of the transplant. Besides, an availability of a related donor makes post-transplant donor-derived cellular therapy more easily accessible. In addition, the greater HLA mismatch associated with haploidentical HSCT (haplo-HSCT) may potentiate graft-versus-tumor (GVT) effects. The aim of our study was to summarize our single-center experience of haplo-HSCT performed with non-manipulated grafts in adult patients with different malignant diseases. The study included a total of 119 patients with different hematological disorders subjected to haplo-HSCT. At the time of analysis, median follow-up was 371 days (1-2219). Most frequent diagnosis in transplanted patients was acute leukemia. 67 (56%) patients received haplo-HSCT as salvage therapy.<br> Overall survival with an observation term of 2 years was 40.3% for the general group. In particular, the two-year OS in patients transplanted in remissions of ALL and AML was 57% and 46% respectively as compared to 22% and 15% for the patients transplanted in adverse disease status). Two-year event-free survival (EFS) and GVHD-free/relapse-free survival (GRFS) group proved to be 35.7% and 21% respectively. The cumulative incidence of acute GVHD grade II-IV and severe aGVHD grade III-IV was 19% and 10% respectively. The cumulative incidence of chronic GVHD (cGVHD) was 16%.The cumulative incidence of relapse was 21%. The overall transplant-associated mortality was 43% in the studied group. In conclusion, our results show that unmanipulated haplo-HSCT is reasonable treatment option for adult patients with different malignant disorders of hematopoiesis. However, such problems as higher rate graft failure, increased nonrelapse mortality (NRM) and post-transplant relapses remain extremely relevant. </p> <h2>Keywords</h2> <p style="text-align: justify;">Allogeneic hematopoietic stem cell transplantation, haploidentical, adult patients, overall survival, post-transplant relapse, graft-versus-host disease, graft failure, post-transplant cyclophosphamide.</p> " ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2444) "Allogeneic HSCT (allo-HSCT) is potentially curative option for a wide variety of malignant and nonmalignant disorders of hematopoiesis. For patients who lack an HLA-matched sibling, HLA-haploidentical related donors (haplo-HSCT) can be considered as alternative sources of donor grafts. The benefits of haplo-HSCT include immediate donor availability for patients who are in urgent need of the transplant. Besides, an availability of a related donor makes post-transplant donor-derived cellular therapy more easily accessible. In addition, the greater HLA mismatch associated with haploidentical HSCT (haplo-HSCT) may potentiate graft-versus-tumor (GVT) effects. The aim of our study was to summarize our single-center experience of haplo-HSCT performed with non-manipulated grafts in adult patients with different malignant diseases. The study included a total of 119 patients with different hematological disorders subjected to haplo-HSCT. At the time of analysis, median follow-up was 371 days (1-2219). Most frequent diagnosis in transplanted patients was acute leukemia. 67 (56%) patients received haplo-HSCT as salvage therapy.
Overall survival with an observation term of 2 years was 40.3% for the general group. In particular, the two-year OS in patients transplanted in remissions of ALL and AML was 57% and 46% respectively as compared to 22% and 15% for the patients transplanted in adverse disease status). Two-year event-free survival (EFS) and GVHD-free/relapse-free survival (GRFS) group proved to be 35.7% and 21% respectively. The cumulative incidence of acute GVHD grade II-IV and severe aGVHD grade III-IV was 19% and 10% respectively. The cumulative incidence of chronic GVHD (cGVHD) was 16%.The cumulative incidence of relapse was 21%. The overall transplant-associated mortality was 43% in the studied group. In conclusion, our results show that unmanipulated haplo-HSCT is reasonable treatment option for adult patients with different malignant disorders of hematopoiesis. However, such problems as higher rate graft failure, increased nonrelapse mortality (NRM) and post-transplant relapses remain extremely relevant.
Keywords
Allogeneic hematopoietic stem cell transplantation, haploidentical, adult patients, overall survival, post-transplant relapse, graft-versus-host disease, graft failure, post-transplant cyclophosphamide.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21344" ["VALUE"]=> string(130) "Haploidentical stem cell transplantation in adults for the treatment of hematologic diseases: results of a single center (CIC725) " ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(130) "Haploidentical stem cell transplantation in adults for the treatment of hematologic diseases: results of a single center (CIC725) " ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21345" ["VALUE"]=> string(4) "1578" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1578" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21397" ["VALUE"]=> string(4) "1579" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1579" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(12) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21394" ["VALUE"]=> array(2) { ["TEXT"]=> string(260) "<p>Anastasia V. Beynarovich, Elena V. Babenko, Ivan S. Moiseev, Olesya V. Paina, Olga V. Pirogova, Tatiana A. Rudakova, Tatyana L. Gindina, Elena I. Darskaya, Elena V. Morozova, Sergey N. Bondarenko, Ludmila S. Zubarovskaya, Boris V. Afanasyev</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(248) "Anastasia V. Beynarovich, Elena V. Babenko, Ivan S. Moiseev, Olesya V. Paina, Olga V. Pirogova, Tatiana A. Rudakova, Tatyana L. Gindina, Elena I. Darskaya, Elena V. Morozova, Sergey N. Bondarenko, Ludmila S. Zubarovskaya, Boris V. Afanasyev
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(248) "Anastasia V. Beynarovich, Elena V. Babenko, Ivan S. Moiseev, Olesya V. Paina, Olga V. Pirogova, Tatiana A. Rudakova, Tatyana L. Gindina, Elena I. Darskaya, Elena V. Morozova, Sergey N. Bondarenko, Ludmila S. Zubarovskaya, Boris V. Afanasyev
" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21396" ["VALUE"]=> array(2) { ["TEXT"]=> string(2506) "<p style="text-align: justify;">Allogeneic HSCT (allo-HSCT) is potentially curative option for a wide variety of malignant and nonmalignant disorders of hematopoiesis. For patients who lack an HLA-matched sibling, HLA-haploidentical related donors (haplo-HSCT) can be considered as alternative sources of donor grafts. The benefits of haplo-HSCT include immediate donor availability for patients who are in urgent need of the transplant. Besides, an availability of a related donor makes post-transplant donor-derived cellular therapy more easily accessible. In addition, the greater HLA mismatch associated with haploidentical HSCT (haplo-HSCT) may potentiate graft-versus-tumor (GVT) effects. The aim of our study was to summarize our single-center experience of haplo-HSCT performed with non-manipulated grafts in adult patients with different malignant diseases. The study included a total of 119 patients with different hematological disorders subjected to haplo-HSCT. At the time of analysis, median follow-up was 371 days (1-2219). Most frequent diagnosis in transplanted patients was acute leukemia. 67 (56%) patients received haplo-HSCT as salvage therapy.<br> Overall survival with an observation term of 2 years was 40.3% for the general group. In particular, the two-year OS in patients transplanted in remissions of ALL and AML was 57% and 46% respectively as compared to 22% and 15% for the patients transplanted in adverse disease status). Two-year event-free survival (EFS) and GVHD-free/relapse-free survival (GRFS) group proved to be 35.7% and 21% respectively. The cumulative incidence of acute GVHD grade II-IV and severe aGVHD grade III-IV was 19% and 10% respectively. The cumulative incidence of chronic GVHD (cGVHD) was 16%.The cumulative incidence of relapse was 21%. The overall transplant-associated mortality was 43% in the studied group. In conclusion, our results show that unmanipulated haplo-HSCT is reasonable treatment option for adult patients with different malignant disorders of hematopoiesis. However, such problems as higher rate graft failure, increased nonrelapse mortality (NRM) and post-transplant relapses remain extremely relevant. </p> <h2>Keywords</h2> <p style="text-align: justify;">Allogeneic hematopoietic stem cell transplantation, haploidentical, adult patients, overall survival, post-transplant relapse, graft-versus-host disease, graft failure, post-transplant cyclophosphamide.</p> " ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2444) "Allogeneic HSCT (allo-HSCT) is potentially curative option for a wide variety of malignant and nonmalignant disorders of hematopoiesis. For patients who lack an HLA-matched sibling, HLA-haploidentical related donors (haplo-HSCT) can be considered as alternative sources of donor grafts. The benefits of haplo-HSCT include immediate donor availability for patients who are in urgent need of the transplant. Besides, an availability of a related donor makes post-transplant donor-derived cellular therapy more easily accessible. In addition, the greater HLA mismatch associated with haploidentical HSCT (haplo-HSCT) may potentiate graft-versus-tumor (GVT) effects. The aim of our study was to summarize our single-center experience of haplo-HSCT performed with non-manipulated grafts in adult patients with different malignant diseases. The study included a total of 119 patients with different hematological disorders subjected to haplo-HSCT. At the time of analysis, median follow-up was 371 days (1-2219). Most frequent diagnosis in transplanted patients was acute leukemia. 67 (56%) patients received haplo-HSCT as salvage therapy.
Overall survival with an observation term of 2 years was 40.3% for the general group. In particular, the two-year OS in patients transplanted in remissions of ALL and AML was 57% and 46% respectively as compared to 22% and 15% for the patients transplanted in adverse disease status). Two-year event-free survival (EFS) and GVHD-free/relapse-free survival (GRFS) group proved to be 35.7% and 21% respectively. The cumulative incidence of acute GVHD grade II-IV and severe aGVHD grade III-IV was 19% and 10% respectively. The cumulative incidence of chronic GVHD (cGVHD) was 16%.The cumulative incidence of relapse was 21%. The overall transplant-associated mortality was 43% in the studied group. In conclusion, our results show that unmanipulated haplo-HSCT is reasonable treatment option for adult patients with different malignant disorders of hematopoiesis. However, such problems as higher rate graft failure, increased nonrelapse mortality (NRM) and post-transplant relapses remain extremely relevant.
Keywords
Allogeneic hematopoietic stem cell transplantation, haploidentical, adult patients, overall survival, post-transplant relapse, graft-versus-host disease, graft failure, post-transplant cyclophosphamide.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2444) "Allogeneic HSCT (allo-HSCT) is potentially curative option for a wide variety of malignant and nonmalignant disorders of hematopoiesis. For patients who lack an HLA-matched sibling, HLA-haploidentical related donors (haplo-HSCT) can be considered as alternative sources of donor grafts. The benefits of haplo-HSCT include immediate donor availability for patients who are in urgent need of the transplant. Besides, an availability of a related donor makes post-transplant donor-derived cellular therapy more easily accessible. In addition, the greater HLA mismatch associated with haploidentical HSCT (haplo-HSCT) may potentiate graft-versus-tumor (GVT) effects. The aim of our study was to summarize our single-center experience of haplo-HSCT performed with non-manipulated grafts in adult patients with different malignant diseases. The study included a total of 119 patients with different hematological disorders subjected to haplo-HSCT. At the time of analysis, median follow-up was 371 days (1-2219). Most frequent diagnosis in transplanted patients was acute leukemia. 67 (56%) patients received haplo-HSCT as salvage therapy.
Overall survival with an observation term of 2 years was 40.3% for the general group. In particular, the two-year OS in patients transplanted in remissions of ALL and AML was 57% and 46% respectively as compared to 22% and 15% for the patients transplanted in adverse disease status). Two-year event-free survival (EFS) and GVHD-free/relapse-free survival (GRFS) group proved to be 35.7% and 21% respectively. The cumulative incidence of acute GVHD grade II-IV and severe aGVHD grade III-IV was 19% and 10% respectively. The cumulative incidence of chronic GVHD (cGVHD) was 16%.The cumulative incidence of relapse was 21%. The overall transplant-associated mortality was 43% in the studied group. In conclusion, our results show that unmanipulated haplo-HSCT is reasonable treatment option for adult patients with different malignant disorders of hematopoiesis. However, such problems as higher rate graft failure, increased nonrelapse mortality (NRM) and post-transplant relapses remain extremely relevant.
Keywords
Allogeneic hematopoietic stem cell transplantation, haploidentical, adult patients, overall survival, post-transplant relapse, graft-versus-host disease, graft failure, post-transplant cyclophosphamide.
" } ["DOI"]=> array(37) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21343" ["VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-26-35" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-26-35" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-26-35" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21344" ["VALUE"]=> string(130) "Haploidentical stem cell transplantation in adults for the treatment of hematologic diseases: results of a single center (CIC725) " ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(130) "Haploidentical stem cell transplantation in adults for the treatment of hematologic diseases: results of a single center (CIC725) " ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(130) "Haploidentical stem cell transplantation in adults for the treatment of hematologic diseases: results of a single center (CIC725) " } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21395" ["VALUE"]=> array(2) { ["TEXT"]=> string(176) "<p>R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantology at the First St. Petersburg State I. Pavlov Medical University</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(164) "R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantology at the First St. Petersburg State I. Pavlov Medical University
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(164) "R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantology at the First St. Petersburg State I. Pavlov Medical University
" } ["AUTHORS"]=> array(38) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> array(12) { [0]=> string(5) "22033" [1]=> string(5) "22034" [2]=> string(5) "22035" [3]=> string(5) "22036" [4]=> string(5) "22037" [5]=> string(5) "22038" [6]=> string(5) "22039" [7]=> string(5) "22040" [8]=> string(5) "22041" [9]=> string(5) "22042" [10]=> string(5) "22043" [11]=> string(5) "22044" } ["VALUE"]=> array(12) { [0]=> string(4) "1629" [1]=> string(3) "500" [2]=> string(2) "60" [3]=> string(3) "130" [4]=> string(3) "180" [5]=> string(4) "1630" [6]=> string(3) "499" [7]=> string(3) "285" [8]=> string(3) "147" [9]=> string(4) "1631" [10]=> string(2) "42" [11]=> string(2) "34" } ["DESCRIPTION"]=> array(12) { [0]=> string(0) "" [1]=> string(0) "" [2]=> string(0) "" [3]=> string(0) "" [4]=> string(0) "" [5]=> string(0) "" [6]=> string(0) "" [7]=> string(0) "" [8]=> string(0) "" [9]=> string(0) "" [10]=> string(0) "" [11]=> string(0) "" } ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(12) { [0]=> string(4) "1629" [1]=> string(3) "500" [2]=> string(2) "60" [3]=> string(3) "130" [4]=> string(3) "180" [5]=> string(4) "1630" [6]=> string(3) "499" [7]=> string(3) "285" [8]=> string(3) "147" [9]=> string(4) "1631" [10]=> string(2) "42" [11]=> string(2) "34" } ["~DESCRIPTION"]=> array(12) { [0]=> string(0) "" [1]=> string(0) "" [2]=> string(0) "" [3]=> string(0) "" [4]=> string(0) "" [5]=> string(0) "" [6]=> string(0) "" [7]=> string(0) "" [8]=> string(0) "" [9]=> string(0) "" [10]=> string(0) "" [11]=> string(0) "" } ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> array(12) { [0]=> string(68) "Anastasia V. Beynarovich" [1]=> string(59) "Elena V. Babenko" [2]=> string(57) "Ivan S. Moiseev" [3]=> string(58) "Olesya V. Paina" [4]=> string(59) "Olga V. Pirogova" [5]=> string(63) "Tatiana A. Rudakova" [6]=> string(61) "Tatyana L. Gindina" [7]=> string(60) "Elena I. Darskaya" [8]=> string(60) "Elena V. Morozova" [9]=> string(64) "Sergey N. Bondarenko" [10]=> string(65) "Ludmila S. Zubarovskaya" [11]=> string(60) "Boris V. Afanasyev" } ["LINK_ELEMENT_VALUE"]=> bool(false) } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21340" ["VALUE"]=> array(2) { ["TEXT"]=> string(437) "<p>Анастасия В. Бейнарович, Елена В. Бабенко, Иван С. Моисеев, Олеся В. Паина, Ольга В. Пирогова, Татьяна А. Рудакова, Татьяна Л. Гиндина, Елена И. Дарская, Елена В. Морозова, Сергей Н. Бондаренко, Людмила С. Зубаровская, Борис В. Афанасьев</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(425) "Анастасия В. Бейнарович, Елена В. Бабенко, Иван С. Моисеев, Олеся В. Паина, Ольга В. Пирогова, Татьяна А. Рудакова, Татьяна Л. Гиндина, Елена И. Дарская, Елена В. Морозова, Сергей Н. Бондаренко, Людмила С. Зубаровская, Борис В. Афанасьев
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(425) "Анастасия В. Бейнарович, Елена В. Бабенко, Иван С. Моисеев, Олеся В. Паина, Ольга В. Пирогова, Татьяна А. Рудакова, Татьяна Л. Гиндина, Елена И. Дарская, Елена В. Морозова, Сергей Н. Бондаренко, Людмила С. Зубаровская, Борис В. Афанасьев
" } ["SUBMITTED"]=> array(37) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21325" ["VALUE"]=> string(10) "14.03.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "14.03.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "14.03.2019" } ["ACCEPTED"]=> array(37) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21326" ["VALUE"]=> string(10) "12.04.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "12.04.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "12.04.2019" } ["CONTACT"]=> array(38) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21327" ["VALUE"]=> string(4) "1629" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1629" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(68) "Anastasia V. Beynarovich" ["LINK_ELEMENT_VALUE"]=> bool(false) } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21342" ["VALUE"]=> array(2) { ["TEXT"]=> string(4755) "<p style="text-align: justify;">Аллогенная трансплантация костного мозга (алло- ТГСК) является потенциальной возможностью излечения злокачественных и незлокачественных заболеваний кроветворения. Для пациентов, у которых отсутствует HLA-совместимый сиблинг, можно использовать HLA-гаплоидентичного донора (гапло-ТГСК) в качестве альтернативного источника трансплантата. Преимуществом гапло-ТГСК является немедленная доступность донора для пациентов, которым необходимо выполнение трансплантации в короткие сроки. Кроме того, наличие родственного донора делает более доступной клеточную терапию после трансплантации. Также, большее несоответствие по генам HLA-системы в случае гаплоидентичной трансплантации, может потенциировать эффект «трансплантат против опухоли». В этом отчете представлен анализ результатов гапло-ТГСК, выполненных в нашем центре взрослым пациентам с различными злокачественными заболеваниями, при использовании неманипулированного трансплантата. На момент анализа медиана наблюдения составила 371 день (1-2219). Основным диагонозом был острый лейкоз. Шестидесяти семи пациентам (56%) гапло-ТГСК была выполнена в качестве терапии спасения. Общая выживаемость в течении 2 лет в исследуемой группе составила 40,3%. В частности, двухлетняя общая выживаемость у пациентов с ОЛЛ и ОМЛ в ремиссии заболевания, составила 57% и 46% соответственно в сравнении с 22% и 15% у пациентов с продвинутыми стадиями заболеваний. Безрецидивная выживаемость в течение 2 лет, а также выживаемость без проявлений оРТПХ и рецидива заболевания в общей группе составили 35,7% и 21% соответственно. Частота возникновения острой РТПХ II-IV степени и тяжелой РТПХ III-IV степени составили 19% и 10% соответственно. Частота хронической РТПХ составила 16%. Частота возникновения рецидива заболевания составила 21%. Трансплантационная летальность исследуемой группе 43%. В заключение необходимо отметить, что наши результаты показывают, что гапло-ТГСК с использованием неманипулированного трансплантата является приемлемым методом лечения взрослых пациентов с различными злокачественными заболеваниями кроветворения. Однако такие проблемы, как высокая частота неприживления, высокая трансплантационная летальность, а также посттрасплантационные рецидивы остаются чрезвычайно актуальными. </p> <h2>Ключевые слова</h2> <p style="text-align: justify;">Аллогенная трансплантация гемопоэтических стволовых клеток, гаплоидентичная, взрослые пациенты, общая выживаемость, рецидив после трансплантации, реакция «трансплантат против хозяина», неприживление трансплантатата, посттрансплантационный циклофосфамид. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4699) "Аллогенная трансплантация костного мозга (алло- ТГСК) является потенциальной возможностью излечения злокачественных и незлокачественных заболеваний кроветворения. Для пациентов, у которых отсутствует HLA-совместимый сиблинг, можно использовать HLA-гаплоидентичного донора (гапло-ТГСК) в качестве альтернативного источника трансплантата. Преимуществом гапло-ТГСК является немедленная доступность донора для пациентов, которым необходимо выполнение трансплантации в короткие сроки. Кроме того, наличие родственного донора делает более доступной клеточную терапию после трансплантации. Также, большее несоответствие по генам HLA-системы в случае гаплоидентичной трансплантации, может потенциировать эффект «трансплантат против опухоли». В этом отчете представлен анализ результатов гапло-ТГСК, выполненных в нашем центре взрослым пациентам с различными злокачественными заболеваниями, при использовании неманипулированного трансплантата. На момент анализа медиана наблюдения составила 371 день (1-2219). Основным диагонозом был острый лейкоз. Шестидесяти семи пациентам (56%) гапло-ТГСК была выполнена в качестве терапии спасения. Общая выживаемость в течении 2 лет в исследуемой группе составила 40,3%. В частности, двухлетняя общая выживаемость у пациентов с ОЛЛ и ОМЛ в ремиссии заболевания, составила 57% и 46% соответственно в сравнении с 22% и 15% у пациентов с продвинутыми стадиями заболеваний. Безрецидивная выживаемость в течение 2 лет, а также выживаемость без проявлений оРТПХ и рецидива заболевания в общей группе составили 35,7% и 21% соответственно. Частота возникновения острой РТПХ II-IV степени и тяжелой РТПХ III-IV степени составили 19% и 10% соответственно. Частота хронической РТПХ составила 16%. Частота возникновения рецидива заболевания составила 21%. Трансплантационная летальность исследуемой группе 43%. В заключение необходимо отметить, что наши результаты показывают, что гапло-ТГСК с использованием неманипулированного трансплантата является приемлемым методом лечения взрослых пациентов с различными злокачественными заболеваниями кроветворения. Однако такие проблемы, как высокая частота неприживления, высокая трансплантационная летальность, а также посттрасплантационные рецидивы остаются чрезвычайно актуальными.
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, гаплоидентичная, взрослые пациенты, общая выживаемость, рецидив после трансплантации, реакция «трансплантат против хозяина», неприживление трансплантатата, посттрансплантационный циклофосфамид.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4699) "Аллогенная трансплантация костного мозга (алло- ТГСК) является потенциальной возможностью излечения злокачественных и незлокачественных заболеваний кроветворения. Для пациентов, у которых отсутствует HLA-совместимый сиблинг, можно использовать HLA-гаплоидентичного донора (гапло-ТГСК) в качестве альтернативного источника трансплантата. Преимуществом гапло-ТГСК является немедленная доступность донора для пациентов, которым необходимо выполнение трансплантации в короткие сроки. Кроме того, наличие родственного донора делает более доступной клеточную терапию после трансплантации. Также, большее несоответствие по генам HLA-системы в случае гаплоидентичной трансплантации, может потенциировать эффект «трансплантат против опухоли». В этом отчете представлен анализ результатов гапло-ТГСК, выполненных в нашем центре взрослым пациентам с различными злокачественными заболеваниями, при использовании неманипулированного трансплантата. На момент анализа медиана наблюдения составила 371 день (1-2219). Основным диагонозом был острый лейкоз. Шестидесяти семи пациентам (56%) гапло-ТГСК была выполнена в качестве терапии спасения. Общая выживаемость в течении 2 лет в исследуемой группе составила 40,3%. В частности, двухлетняя общая выживаемость у пациентов с ОЛЛ и ОМЛ в ремиссии заболевания, составила 57% и 46% соответственно в сравнении с 22% и 15% у пациентов с продвинутыми стадиями заболеваний. Безрецидивная выживаемость в течение 2 лет, а также выживаемость без проявлений оРТПХ и рецидива заболевания в общей группе составили 35,7% и 21% соответственно. Частота возникновения острой РТПХ II-IV степени и тяжелой РТПХ III-IV степени составили 19% и 10% соответственно. Частота хронической РТПХ составила 16%. Частота возникновения рецидива заболевания составила 21%. Трансплантационная летальность исследуемой группе 43%. В заключение необходимо отметить, что наши результаты показывают, что гапло-ТГСК с использованием неманипулированного трансплантата является приемлемым методом лечения взрослых пациентов с различными злокачественными заболеваниями кроветворения. Однако такие проблемы, как высокая частота неприживления, высокая трансплантационная летальность, а также посттрасплантационные рецидивы остаются чрезвычайно актуальными.
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, гаплоидентичная, взрослые пациенты, общая выживаемость, рецидив после трансплантации, реакция «трансплантат против хозяина», неприживление трансплантатата, посттрансплантационный циклофосфамид.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21341" ["VALUE"]=> array(2) { ["TEXT"]=> string(337) "<p>НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета, Санкт-Петербург, Россия</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(325) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(325) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета, Санкт-Петербург, Россия
" } } } [6]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "121" ["~IBLOCK_SECTION_ID"]=> string(3) "121" ["ID"]=> string(4) "1641" ["~ID"]=> string(4) "1641" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(239) "Особенности течения, диагностики и лечения синуситов у детей и подростков после трансплантации гемопоэтических стволовых клеток" ["~NAME"]=> string(239) "Особенности течения, диагностики и лечения синуситов у детей и подростков после трансплантации гемопоэтических стволовых клеток" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "03.06.2019 11:37:29" ["~TIMESTAMP_X"]=> string(19) "03.06.2019 11:37:29" ["DETAIL_PAGE_URL"]=> string(154) "/ru/archive/tom-8-nomer-1/klinicheskie-issledovaniya/osobennosti-techeniya-diagnostiki-i-lecheniya-sinusitov-u-detey-i-podrostkov-posle-transplantatsii-g/" ["~DETAIL_PAGE_URL"]=> string(154) "/ru/archive/tom-8-nomer-1/klinicheskie-issledovaniya/osobennosti-techeniya-diagnostiki-i-lecheniya-sinusitov-u-detey-i-podrostkov-posle-transplantatsii-g/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(28472) "Introduction
One of the urgent problems of modern otorhinolaryngology and clinical medicine are inflammatory lesions of the paranasal sinuses (PS). Over the past decade, the incidence of sinusitis has increased 3 times [1]. According to different authors, acute or chronic sinusitis suffer from 5 to 15% of the adult population and about 5-13% of children [2, 3]. In the structure of stationary pathology acute sinusitis is 15-36% [4]. Every year, the number of hospitalizations for this reason increases by 1.5-2% [1].
Infections are a relevant problem for hematopoietic stem cell transplantation (HSCT) and cause of failure in the treatment of patients after transplantation. At the same time, there has been an increase in the number of immunocompromised patients, due to increased usage of HSCT for various oncological, hematological and hereditary diseases [5]. As a result, the risk of bacterial, viral, fungal infections increases at various sites, including the defeat clinically significant lesions of paranasal sinuses (PS) in such patients [6-14]. According to the published studies, the incidence of sinusitis among adult patients subjected to HSCT ranges from 21% to 36% [11, 15, 16]. Appropriate data on children and adolescents are absent in available literature.
Currently we know about several retrospective studies of the factors associated with allo-HSCT procedure which increase the risk of PS affection in adults. Such studies are lacking in children and adolescents undergoing HSCT.
The patients with post-transplant leukocytopenia do not exhibit a typical inflammatory response, unlike immunocompetent patients. In this regard, the symptoms of PS lesions may be absent, or mildly expressed [11], thus making it difficult to diagnose these conditions. In addition, invasive procedures in HSCT recipients, e.g., diagnostic and therapeutic punctures of maxillary sinuses or mucosal biopsy in invasive PS mycosis, or PS lesion, as a manifestation of the underlying disease, may be associated with development of severe complications that aggravate general condition of the patient [17]. Meanwhile, X-ray diagnostics of PS at the specialized radiological units for detection of sinusitis at early terms after allo-HSCT is difficult due to limited access for the patients over the aplastic period since they have to be isolated in the wards equipped with laminar air flow and HEPA filtration.
Evolving sinusitis may be a factor contributing to development of other infectious complications (bronchitis, pneumonia) at the early and late terms after allo-HSCT [18].
Thus, the study of risk factors, diagnostic issues and therapy of inflammatory PS lesions in children and adolescents is a necessary condition preventing infectious complications after HSCT and, ultimately, providing a clinical success.
The aim of our study was to improve diagnosis and treatment of sinusitis in children and adolescents after allogeneic transplantation of hematopoietic stem cells. We have identified a subgroup of patients with increased risk for infectious complications after allo-HSCT, in particular, sinusitis, thus allowing to develop methods of its prevention and diagnosis, as well as early therapy of this condition.
Patients and Methods
The work was performed on the basis of retrospective and prospective analysis of medical records on the patients 0 to 21 years of age after autologous or allogeneic hematopoietic stem cell transplantation (HSCT), performed in R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University over the period of 2008 to 2013.
The main group of the study consisted of 352 recipients (67% of total) subjected to allo-HSCT at the age ranging from 4 months to 21 years (median, 12 years; gender ratio: 213 males and 139 females). The comparison group consisted of 172 recipients (33%) who underwent autologous HSCT (auto- HSCT), 1 to 21 years old (median of 12 years, the group included 101 males and 71 females). The spectrum of underlying disorders in HSCT recipients is presented in Table 1.
Table 1. Clinical characteristics of primary disease in the patients subjected to allo- or auto-HSCT

Remission of the underlying disease was observed in 195 patients with allo-HSCT, relapse, in 157 patients. At the auto-HSCT, 147 patients were in complete remission; 25 patients were in partial remission. Bone marrow (BM) was used as a stem cell source in 244 patients (69%) allo-HSCT; peripheral blood stem cells (PBSC) were applied in 108 cases (31%). For auto-HSCT, BM was used in 139 patients (81%); PBSC were transfused to 33 recipients (19%). The conditioning regimen for ALLO-HSCT was chosen with respect to the patient's age, primary diagnosis, previous treatment, complications associated with therapy, and somatic status at the time of HSCT. Myeloablative regimens (MR) were used in 148 patient (42%)s scheduled for allo-HSCT, and in 172 cases (100%) intended for auto-HSCT. Non-myeloablative regimens and reduced-intensity doses (NR/RID) were applied to 204 (58%) patients for allo-HSCT.
Allo-HSCT was performed from related or unrelated donors that were completely or partially compatible for HLA antigens. Related donors were used for 166 patients (47%) including 51 patients (31%) transplanted from HLA-compatible donors, and 115 patients (69%) with haploidentical stem cells. Matched unrelated donors were used in 186 patients (53%), including 166 patients (89%) with HLA-compatible genes (11%) and 20 patients with HLA – partially compatible genes (89%).
The patients with sinusitis as an infectious complication after allo-HSCT were considered a separate clinical subgroup. The group of patients with sinusitis consisted of 78 recipients of allo-HSCT at the age of 2 to 21 years (median of 13 years; the M/F ratio was 51:27). Forty-three patients were classified as children (2 – 13 years, median age – 9 years), and 35 patients were considered adolescents and young adults (14 – 21 years, median age – 18 years). The primary diagnoses in the group of patients with sinusitis after allo-HSCT are shown in Table 2.
Table 2. Spectrum of underlying diseases in the group of patients with sinusitis after allo-HSCT (n=78)

Diagnostic criteria of sinusitis in children and adolescents were based on the common recommendations [19]. The main research methods were as follows: collection of the patients’ medical history and complaints to assess overall severity of sinusitis manifestations in the post-transplant patients. A visual analogue scale was graded from 0 (minimal symptomatics) to 10 (maximal severity of symptoms) [19, 20]. Routine otorhinolaryngological examination was also performed, i.e., anterior and posterior rhinoscopy, pharyngoscopy, otoscopy, indirect laryngoscopy. Endoscopic inspection of nasal cavity was performed using a rigid endoscope with a viewing angle of 0° (Karl Storz, Germany). Visible changes in mucous membrane of the nasal cavity and nature of secretions the discharge in the nasal passages were evaluated by the endoscopy. The results of this study were recorded on digital media for subsequent analysis. Rigid endoscopes with different angles (Karl Storz, Germany) were also used for endovideoscopy and functional surgery of paranasal sinuses.
The cases of sinusitis were confirmed by X-ray examination, computed tomography (CT) or magnetic resonance imaging (MRI) of the area. PS alterations revealed with CT and MRI techniques were classified by a modified version of Lund method [21]. The degree of PS lesions was scored from 0 to 2. A score of 0 corresponded to absence of the PS disease; 1, partial shading or thickening of the PS mucous membrane; 2, total shading or fluid levels in PS. Ostiomeatal complexes on the PS images obtained by CT and MRI were evaluated as 0 or 2 points, respectively, free or blocked.
Taking material from the paranasal sinuses for bacteriological and mycological studies was performed by aspiration of the contents of maxillary sinuses during a diagnostic puncture.
Biopsy material was obtained intraoperatively under the control of rigid endoscopes with a viewing angle of 0°, 45°, 30°. Prevention of infectious complications was commenced from the first day of conditioning treatment, using the second-generation fluoroquinolones (ciprofloxacin) at a daily dose of 10-15 mg/kg in 2 injections. To prevent pneumonias, trimethoprim/sulfamethoxazole (Biseptol) was used at a dose of 10 mg/kg/day (trimethoprim), depending on age, twice a day, 3 times a week. Acyclovir was used at a dose of 200 mg 3 times a day as antiviral prophylaxis, starting from the day of hematopoietic restoration.
Primary prophylaxis of fungal infection was performed with drugs from the azole group (triazoles) of different generations (e.g., Fluсonazole), at a dose of 1-2 mg/kg/day. Secondary prevention proceeded with Voriconazole at a dose of 100-200 mg every 12 hours; Posaconazole at a dose of 600-800 mg/day, or a drug from the group of echinocandins (Сaspofungin), 50-70 mg/day, starting on the first day of conditioning and continuing until ceasing the immunosuppressive therapy in the absence of invasive mycoses.
All the patients underwent routine blood and differential leukocyte counts, serum biochemical analysis. Engraftment of donor hematopoietic cells was controlled by the results of clinical blood cell counts, and molecular biology methods (donor chimerism assays). The day of engraftment was defined as achieving neutrophil levels of >0.5×109/l without prior stimulation by G-CSF for 3 days, reaching platelet counts of >25.0×109/l without prior transfusion of platelet concentrate for 3 days. Severity of thrombocytopenia and neutropenia was assessed in accordance with the World Health Organization classification.
Statistical analysis was performed in Statistica version 10.0 (StatSoft, USA) using nonparametric methods for comparing groups by the quantitative Mann-Whitney criteria, the groups with qualitative characteristics were compared using conjugated tables, t-test, Chi-square and Fisher exact tests. Correlation analysis was performed with Spearman method, log-linear multifactorial analysis. The differences were considered significant by р<0.05.
Results
Occurrence and severity of sinusitis post-transplant
The incidence of sinusitis after allo-HSCT was 22.2% among our patients. It was found that the frequency of sinusitis after allo-HSCT (22.2%) was significantly higher than after auto-HSCT (1.7%, p <0.001). Over recent years, the number of performed allo-HSCT has increased by 33%. Meanwhile, the frequency of sinusitis after allo-HSCT has significantly decreased, i.e., from 39.2% in 2010 to 10.8% in 2013 (p=0.001), as shown in Fig. 1.

Figure 1. Annual numbers of allo-HSCTs and relative frequencies of sinusitis in the cohorts studied
The largest incidence of sinusitis among children and adolescents was observed in 2010 (respectively, 40.5% and 36.8%). In 2013, the sinusitis occurence is progressively reduced to 14.8% (p=0.018) in the groups of children, and to 6.8% among adolescents (p=0.026).
The frequency of sinusitis proved to be higher at later terms (>100 days after allo-HSCT). Incidence of sinusitis within 100 days post-transplant was 9.6%, as compared to 17.7% after D+100 (p=0.006).
Distribution of the PS lesions by their volume in patients after allo-HSCT was as follows: the maxillary sinus (MS) was involved in 24 patients (30.8%) including unilateral MS affection in 1 case; the MS lesions combined with other PS were detected in 51 cases (65.4%), including 13 patients with all the sinuses affected (16.7%). Isolated lesion of the main sinus was observed in 2 cases (2.5%). Inflammation of PS without MS affection was documented in 3 cases (3.8%).
A decrease in the number of clinical symptoms of sinusitis (p=0.008), and an increase in cases of mild sinusitis on a visual analog scale (p=0.032) was registered since 100 days post-transplant (Fig. 2).

Figure 2. Time-dependent dynamics of clinical sinusitis manifestations according to visual analogue scale period after allo-HSCT
In the patients with neutropenia of I–IV degree at several weeks post-HSCT, severe changes in paranasal sinuses were more often noted by means of CT technique (p=0.018). However, in 50% of cases (24/48). In view of clinical severity of PS affection detected by CT, there were changes in severe-grade cases, and such changes in PS were more common after >100 days post-transplant (p=0.014) (Fig. 3).

Figure 3. Dynamics of changes in the sinuses detected by computer tomography, depending on the time period after allo-HSCT
Endoscopy pattern
Endoscopic images showed non-specific changes in the patients with sinusitis after allo-HSCT. Hyperemia of the nasal mucosa was significantly less common (17%) than mucosal pallor in the nasal cavities (83%, p <0.001). Oedematous nasal mucosa was observed in 38.5% of the cases. In 51% of cases, there was a discharge secretion in the nasal passages, with slimy discharge being a dominating type (80%). The secretions revealed in the nasal passages in patients with sinusitis after allo-HSCT are classified in Fig. 4.

Figure 4. Incidence of secretions revealed in the nasal passages by endoscopy of the nasal cavity in patients with sinusitis post-allo-HSCT
Infectious agents in sinusitis
In the course of this study, 41 bacteriological and mycological analyses of the samples from maxillary sinuses were performed. The specimens were obtained during diagnostic and therapeutic puncture. Briefly, any pathogen growth was not detected in 10 cases (24.4%), bacterial monocultures were isolated in 15 cases (36.6%); fungal monocultures were obtained from two samples (4.9%). The results concerning maxillary sinus aspirate were as follows: inflammation associated with bacteria in 51.2% of cases (n=21), fungal cultures were obtained in 19.5% of cases (n=8), and mixed infection was revealed in 2 cases (4.9%), as shown in Fig. 5.

Figure 5. Results of microbiological cultures of maxillary sinus aspirate from the sinusitis patients
The main sinusitis-associated pathogens in allo-HSCT recipients were Gram-positive bacteria: Staphylococcus epidermidis (30%), Streptococcus viridans (30%); Gram-negative Klebsiella pneumoniae (17.5%). The frequency of fungal sinusitis after allo-HSCT was 5%; association of bacteria and fungi was observed in 20% of cases. Aspergillus moulds proved to be the main causative agents in fungal sinusitis (80% of positive samples).
After 100 days from allo-HSCT, a larger proportion of sinus secretions showed the absence of microflora growth (p=0.022). It should be noted that the bacterial monocultures predominated up to 100 days from allo-HSCT (p=0.011). Incidence of bacterial sinusitis up to 100 days from allo-HSCT was 74% (14/19); after 100 days from allo-HSCT it was 32% (7/22) (p=0.018).
A comparative analysis of children and adolescent groups has revealed that combined infections were more often observed in adolescent patients with sinusitis (p=0.042).
Treatment of sinusitis
When assessing duration of sinusitis treatment, we have noted that the patients after auto-HSCs recovered faster than the patients after allo-HSCT (p=0.007). In our study, a recovery from sinusitis occurred within 15 days in 5% of patients after allo-HSCT, whereas 92.5% of such patients received therapy for >30 days. In 2.5% of cases, the treatment period was more than 100 days. Terms of treatment and methods of therapy for different age groups are presented in Table 3.
Table 3. Duration of treatment of sinusitis in groups and with different methods of therapy

The sinusitis treatment in pediatric patients was longer than in adolescent group (p=0.018). Usage of MS puncture in combination with antimicrobial therapy significantly reduces the duration of sinusitis treatment (p=0.024), especially in severe changes in the sinuses on CT (p=0.035).
Diagnostic and treatment punctures were performed in 41 (52.6%) patients with mandatory sampling of biomaterial for bacteriological and mycological examinations. Age of patients at the time of puncture ranged from 4 years to 21 years. In the children under 7 years, the procedure was carried out under the endotracheal anesthesia in the operating room.
At the time of the puncture, 26/41 (63.4%) patients had a blood platelet level <100.0×109/L. Of them, 20/26 (77%) patients did not exceed the level of 50.0×109/L (p=0.0001). We have not confirmed a relationship between the frequency of bleeding after the procedure and platelet levels (p=0.935).
Pneumonia and bronchitis after a sinus infection in recipients of HSCT was observed in 70.5% of cases (55/78). When analyzing the incidence of lung lesions due to sinusitis in HSCT recipients, depending on the period after allo-HSCT, we have revealed that the pulmonary lesions were observed more often before D+100 after allo-HSCT (28/34, 82%) than after 100 days (27/44, 61%, p=0.049).
The endoscopic sinus surgery was performed in 4 patients (5%) under general anaesthesia, indications for the operation were: orbital complications (reactive edema of the eyelids and local face areas), invasive fungal infection. At the time of surgical treatment, the blood platelet levels in patients ranged from 15.0 to 50.0×109/L, complications after surgery were not observed.
The mono- and multifactorial analysis have revealed several risk factors for sinusitis after allo-HSCT: a story of sinusitis before allo-HSCT (p <0.001), acute (p=0.022) or chronic graft-versus-host disease (p <0.001). In unifactorial analysis, the duration of neutropenia more than 10 days was also associated with sinusitis risk (p=0.054).
Discussion
According to different studies, the frequency of sinusitis in adult patients after allo-HSCT ranges from 11 to 51% [3, 8, 15, 16, 18]. In our group of patients, the frequency of sinusitis after allo-HSCT was 22.2%. Our study has also shown that the sinusitis frequency after allo-HSCT is higher than after auto-HSCT (p <0.001), which coincides with results from other groups [8, 11, 18].
Previous studies have noted that the presence of acute or chronic graft-versus-host reaction (GVHD) comprises a risk factor for sinusitis after allo-HSCT [18]. In our study, we found a correlation between these factors and sinusitis occurrence. Presence of acute (p=0.022) or chronic GVHD (p <0.001) was associated with significant increase of paranasal sinus pathology after allo-HSCT.
In the patients with immunodeficiency of either origin (neutropenia, HSC recipients, HIV infection) nosocomial infections were more common associated with Gram-negative bacteria (Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, Proteus spp., Enterobacter spp., Citrobacter), as well as Gram-positive bacteria such as Staphylococcus aureus (15.3%), Streptococcus pneumoniae, Enterococcus faecalis [18, 22]. In our study, the main local causative agents of sinusitis revealed in allo-HSCT recipients were Gram-positive bacteria Staphylococcus epidermidis (30%), Streptococcus viridans (30%), or Gram-negative bacteria, e.g., Klebsiella pneumoniae (17.5%). It was found that the proportion of negative cultures from the sinuses was higher at the terms of >100 days after allo-HSCT (p=0.022). It should be noted that the monocultures of bacteria prevailed up to 100 days from allo-HSCT (p=0.011). The findings for combined sinusitis-associated infections were more often observed in adolescent patients, in comparison with children group (p=0.042).
In assessing the duration of sinusitis treatment, we have noted that the patients after auto-HSCT recovered faster than patients after allo-HSCT (p=0.007). This fact may be associated with a faster recovery of the body's defense mechanisms after auto-HSCT than following allo-HSCT, as well as the lack of immunosuppressive therapy in autologous transplants. In our study, recovery from sinusitis occurred within 15 days in 5% of patients after allo-HSCT; 92.5% of patients received therapy for 30 days or more. In 2.5% of patients, the treatment period exceeded 100 days post-transplant. The use of PPP puncture in combination with antimicrobial therapy significantly reduces the duration of sinusitis treatment (p=0.024), especially in cases with severe changes in paranasal sinuses registered by CT and MRI (p=0.035). In pediatric patients, sinusitis treatment was longer than in the adolescent group (p=0.018).
Conclusion
1. Sinusitis folowing allogeneic HSCT occurs more frequently than in auto-transplants;
2. The significant factors for the post-transplant sinusitis are: sufficient immunosuppression, e.g., associated to acute or chronic GVHD;
3. Opportunistic microflora in local samples from the sinusitis patients was found in a half of microbiological cultures.
Conflict of interest
The authors report no conflicts of interest.
References
- Ivanchenko OA, Lopatin AS. Chronic rhinosinusitis: epidemiology, classification, etiology, pathogenesis. Mo-dern view on the problem. Vestn Otorhinolaryngol. 2012; 2: 91-96 (In Russian).
- Pluzhnikov MS, Lavrenova GV, Katinas EB. Basic prin- ciples of immunocorrecting therapy in otorhinolaryngology. Vestn Otorhinolaryngol. 2008. № 4:7-12 (In Russian).
- Arulrajah S, Symons H, Cahoon EK, Tekes A, Thierry A, Huisman G M, Izbudak I. Relationship between clinical sinusitis symptoms and sinus CT severity in pediatric post bone marrow transplant and immunocompetent patients. Eur J Pediatr. 2012; 171(2): 375-381.
- Slavsky AN, Pshonkina DM, Svistushkin VM. Bacteriophages in the complex treatment of acute bacterial rhinosinusitis. Rus Med J. 2014; 2:1925-1928 (In Russian).
- Bento LR, Ortiz E, Nicola EM, Vigorito AC. Sinonasal disorders in hematopoietic stem cell transplantation. Braz J Otorhinolaryngol. 2014; 80(4): 285-289.
- Afanasyev BV, Volkova OY, Ganapiev AA. In: Afanasyev, BV (Ed). Hematology: A Guide for Doctors. St.Petersburg: Speclit. 2008. - 238 p (In Russian).
- Weinberg К, Blazar BR, Wagner JE, Agura E, Hill BJ, Smogorzewska M, Koup RA, Betts MR, Collins RH, Douek DC. Factors affecting thymic function after allogeneic hematopoietic stem cell transplantation. Blood. 2001; 97(5): 1458-1466.
- Thompson AM, Couch M, Zahurak ML, Johnson C, Vogelsang GB. Risk factors for post-stem cell transplant sinusitis. Bone Marrow Transplant. 2002; 29(3): 257-261.
- Appelbaum FR. Hematopoietic-cell transplantation at 50. New Engl J Med. 2007; 357(15):1472-1475.
- Gratwohl A, Baldomero H, Aljurf M, Pasquini MC. Hematopoietic stem cell transplantation. A global perspective. J Am Med Ass. 2010;303(16):1617-1624.
- Won YW, Yi SY, Jang JH, Kim K, Kim SJ, Kim WS, Jung CW, Kim DH. Retrospective analysis of paranasal sinusitis in patients receiving hematopoietic stem cell transplantation. Int J Hematol. 2011; 93(3):383-388.
- Inaba H, Hartford CM, Pei D, Posner MJ, Yang J, Hayden RT, Srinivasan A, Triplett BM, McCulllers JA, Pui CH, Leung W. Longitudinal analysis of antibody response to immunization in paediatric survivors after allogeneic haematopoietic stem cell transplantation. Br J Haematol. 2012; 156(1): 109-117.
- Meng L, Huang XJ. Allogeneic hematopoietic stem cell transplantation in China: where we are and where to go. J Hematol Oncol. 2012. 5(1):10.
- Mortellaro C, Mortellaro C, Barat V, Nesi F, L. Bello, G. Bologna, D. Farronato, A. G. Lucchina, A. Linari. Intercurrent infectious diseases in post-stem cell transplant patients: paranasal sinusitis. J Craniofac Surg. 2012; 23(1):153-157.
- Meyers JD. Infection in bone marrow transplant recipients Am J Med. 1986; 81(1):27-38.
- Shibuya TY, Momin F, Abella E, Jacobs JR, Karanes C, Ratanatharathorn V, Sensenbrenner LL, Lum LG. Sinus disease in the bone marrow transplant population: incidence, risk factors, and complications. Otolaryngol Head Neck Surg. 1995; 113(6):705-711.
- Deutsch JH, Hudgins PA, Siegel JL, Peterman SB, Devine SM, York R, Wingard JR. The paranasal sinuses of patients with acute graft-versus-host disease. Am J Neuroradiol. 1995; 16(6):1287-1291.
- Savage DG, Taylor P, Blackwel J, Chen F, Szydlo RM, Rule SAJ, Spencer A, Apperley JF, Goldman JM. Paranasal sinusitis following allogeneic bone marrow transplant. Bone Marrow Transplant. 1997; 19(1):55-59.
- Fokkens WJ, Lund VJ, Mullol J, Bachert C, Alobid I, Baroody F, Cohen N, Cervin A, Douglas R, Gevaert P, Georgalas C, Goossens H, Harvey R, Hellings P, Hopkins C, Jones N, Joos G, et al. European Position Paper on Rhinosinusitis and Nasal Polyps Group: European position paper on rhinosinusitis and nasal polyps 2012. Rhinology. 2012; 50 (Suppl 23): 1-329.
- Lim М, Lew Gor S, Darby Y. The relationship between subjective assessment instruments in chronic rhinosinusitis. Rhinology. 2007; 45(2):144-147.
- Lund VJ, Kennedy DW. Staging for chronic rhinosinusitis. Otolaryngol Head Neck Surg. 1997: 117(1):35-40.
- Imamura R, Voegels R, Sperandio F. Microbiology of sinusitis in patients undergoing bone marrow transplantation. Otolaryngol Head Neck Surg. 1999; 120(2): 279-282.
Introduction
One of the urgent problems of modern otorhinolaryngology and clinical medicine are inflammatory lesions of the paranasal sinuses (PS). Over the past decade, the incidence of sinusitis has increased 3 times [1]. According to different authors, acute or chronic sinusitis suffer from 5 to 15% of the adult population and about 5-13% of children [2, 3]. In the structure of stationary pathology acute sinusitis is 15-36% [4]. Every year, the number of hospitalizations for this reason increases by 1.5-2% [1].
Infections are a relevant problem for hematopoietic stem cell transplantation (HSCT) and cause of failure in the treatment of patients after transplantation. At the same time, there has been an increase in the number of immunocompromised patients, due to increased usage of HSCT for various oncological, hematological and hereditary diseases [5]. As a result, the risk of bacterial, viral, fungal infections increases at various sites, including the defeat clinically significant lesions of paranasal sinuses (PS) in such patients [6-14]. According to the published studies, the incidence of sinusitis among adult patients subjected to HSCT ranges from 21% to 36% [11, 15, 16]. Appropriate data on children and adolescents are absent in available literature.
Currently we know about several retrospective studies of the factors associated with allo-HSCT procedure which increase the risk of PS affection in adults. Such studies are lacking in children and adolescents undergoing HSCT.
The patients with post-transplant leukocytopenia do not exhibit a typical inflammatory response, unlike immunocompetent patients. In this regard, the symptoms of PS lesions may be absent, or mildly expressed [11], thus making it difficult to diagnose these conditions. In addition, invasive procedures in HSCT recipients, e.g., diagnostic and therapeutic punctures of maxillary sinuses or mucosal biopsy in invasive PS mycosis, or PS lesion, as a manifestation of the underlying disease, may be associated with development of severe complications that aggravate general condition of the patient [17]. Meanwhile, X-ray diagnostics of PS at the specialized radiological units for detection of sinusitis at early terms after allo-HSCT is difficult due to limited access for the patients over the aplastic period since they have to be isolated in the wards equipped with laminar air flow and HEPA filtration.
Evolving sinusitis may be a factor contributing to development of other infectious complications (bronchitis, pneumonia) at the early and late terms after allo-HSCT [18].
Thus, the study of risk factors, diagnostic issues and therapy of inflammatory PS lesions in children and adolescents is a necessary condition preventing infectious complications after HSCT and, ultimately, providing a clinical success.
The aim of our study was to improve diagnosis and treatment of sinusitis in children and adolescents after allogeneic transplantation of hematopoietic stem cells. We have identified a subgroup of patients with increased risk for infectious complications after allo-HSCT, in particular, sinusitis, thus allowing to develop methods of its prevention and diagnosis, as well as early therapy of this condition.
Patients and Methods
The work was performed on the basis of retrospective and prospective analysis of medical records on the patients 0 to 21 years of age after autologous or allogeneic hematopoietic stem cell transplantation (HSCT), performed in R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University over the period of 2008 to 2013.
The main group of the study consisted of 352 recipients (67% of total) subjected to allo-HSCT at the age ranging from 4 months to 21 years (median, 12 years; gender ratio: 213 males and 139 females). The comparison group consisted of 172 recipients (33%) who underwent autologous HSCT (auto- HSCT), 1 to 21 years old (median of 12 years, the group included 101 males and 71 females). The spectrum of underlying disorders in HSCT recipients is presented in Table 1.
Table 1. Clinical characteristics of primary disease in the patients subjected to allo- or auto-HSCT

Remission of the underlying disease was observed in 195 patients with allo-HSCT, relapse, in 157 patients. At the auto-HSCT, 147 patients were in complete remission; 25 patients were in partial remission. Bone marrow (BM) was used as a stem cell source in 244 patients (69%) allo-HSCT; peripheral blood stem cells (PBSC) were applied in 108 cases (31%). For auto-HSCT, BM was used in 139 patients (81%); PBSC were transfused to 33 recipients (19%). The conditioning regimen for ALLO-HSCT was chosen with respect to the patient's age, primary diagnosis, previous treatment, complications associated with therapy, and somatic status at the time of HSCT. Myeloablative regimens (MR) were used in 148 patient (42%)s scheduled for allo-HSCT, and in 172 cases (100%) intended for auto-HSCT. Non-myeloablative regimens and reduced-intensity doses (NR/RID) were applied to 204 (58%) patients for allo-HSCT.
Allo-HSCT was performed from related or unrelated donors that were completely or partially compatible for HLA antigens. Related donors were used for 166 patients (47%) including 51 patients (31%) transplanted from HLA-compatible donors, and 115 patients (69%) with haploidentical stem cells. Matched unrelated donors were used in 186 patients (53%), including 166 patients (89%) with HLA-compatible genes (11%) and 20 patients with HLA – partially compatible genes (89%).
The patients with sinusitis as an infectious complication after allo-HSCT were considered a separate clinical subgroup. The group of patients with sinusitis consisted of 78 recipients of allo-HSCT at the age of 2 to 21 years (median of 13 years; the M/F ratio was 51:27). Forty-three patients were classified as children (2 – 13 years, median age – 9 years), and 35 patients were considered adolescents and young adults (14 – 21 years, median age – 18 years). The primary diagnoses in the group of patients with sinusitis after allo-HSCT are shown in Table 2.
Table 2. Spectrum of underlying diseases in the group of patients with sinusitis after allo-HSCT (n=78)

Diagnostic criteria of sinusitis in children and adolescents were based on the common recommendations [19]. The main research methods were as follows: collection of the patients’ medical history and complaints to assess overall severity of sinusitis manifestations in the post-transplant patients. A visual analogue scale was graded from 0 (minimal symptomatics) to 10 (maximal severity of symptoms) [19, 20]. Routine otorhinolaryngological examination was also performed, i.e., anterior and posterior rhinoscopy, pharyngoscopy, otoscopy, indirect laryngoscopy. Endoscopic inspection of nasal cavity was performed using a rigid endoscope with a viewing angle of 0° (Karl Storz, Germany). Visible changes in mucous membrane of the nasal cavity and nature of secretions the discharge in the nasal passages were evaluated by the endoscopy. The results of this study were recorded on digital media for subsequent analysis. Rigid endoscopes with different angles (Karl Storz, Germany) were also used for endovideoscopy and functional surgery of paranasal sinuses.
The cases of sinusitis were confirmed by X-ray examination, computed tomography (CT) or magnetic resonance imaging (MRI) of the area. PS alterations revealed with CT and MRI techniques were classified by a modified version of Lund method [21]. The degree of PS lesions was scored from 0 to 2. A score of 0 corresponded to absence of the PS disease; 1, partial shading or thickening of the PS mucous membrane; 2, total shading or fluid levels in PS. Ostiomeatal complexes on the PS images obtained by CT and MRI were evaluated as 0 or 2 points, respectively, free or blocked.
Taking material from the paranasal sinuses for bacteriological and mycological studies was performed by aspiration of the contents of maxillary sinuses during a diagnostic puncture.
Biopsy material was obtained intraoperatively under the control of rigid endoscopes with a viewing angle of 0°, 45°, 30°. Prevention of infectious complications was commenced from the first day of conditioning treatment, using the second-generation fluoroquinolones (ciprofloxacin) at a daily dose of 10-15 mg/kg in 2 injections. To prevent pneumonias, trimethoprim/sulfamethoxazole (Biseptol) was used at a dose of 10 mg/kg/day (trimethoprim), depending on age, twice a day, 3 times a week. Acyclovir was used at a dose of 200 mg 3 times a day as antiviral prophylaxis, starting from the day of hematopoietic restoration.
Primary prophylaxis of fungal infection was performed with drugs from the azole group (triazoles) of different generations (e.g., Fluсonazole), at a dose of 1-2 mg/kg/day. Secondary prevention proceeded with Voriconazole at a dose of 100-200 mg every 12 hours; Posaconazole at a dose of 600-800 mg/day, or a drug from the group of echinocandins (Сaspofungin), 50-70 mg/day, starting on the first day of conditioning and continuing until ceasing the immunosuppressive therapy in the absence of invasive mycoses.
All the patients underwent routine blood and differential leukocyte counts, serum biochemical analysis. Engraftment of donor hematopoietic cells was controlled by the results of clinical blood cell counts, and molecular biology methods (donor chimerism assays). The day of engraftment was defined as achieving neutrophil levels of >0.5×109/l without prior stimulation by G-CSF for 3 days, reaching platelet counts of >25.0×109/l without prior transfusion of platelet concentrate for 3 days. Severity of thrombocytopenia and neutropenia was assessed in accordance with the World Health Organization classification.
Statistical analysis was performed in Statistica version 10.0 (StatSoft, USA) using nonparametric methods for comparing groups by the quantitative Mann-Whitney criteria, the groups with qualitative characteristics were compared using conjugated tables, t-test, Chi-square and Fisher exact tests. Correlation analysis was performed with Spearman method, log-linear multifactorial analysis. The differences were considered significant by р<0.05.
Results
Occurrence and severity of sinusitis post-transplant
The incidence of sinusitis after allo-HSCT was 22.2% among our patients. It was found that the frequency of sinusitis after allo-HSCT (22.2%) was significantly higher than after auto-HSCT (1.7%, p <0.001). Over recent years, the number of performed allo-HSCT has increased by 33%. Meanwhile, the frequency of sinusitis after allo-HSCT has significantly decreased, i.e., from 39.2% in 2010 to 10.8% in 2013 (p=0.001), as shown in Fig. 1.

Figure 1. Annual numbers of allo-HSCTs and relative frequencies of sinusitis in the cohorts studied
The largest incidence of sinusitis among children and adolescents was observed in 2010 (respectively, 40.5% and 36.8%). In 2013, the sinusitis occurence is progressively reduced to 14.8% (p=0.018) in the groups of children, and to 6.8% among adolescents (p=0.026).
The frequency of sinusitis proved to be higher at later terms (>100 days after allo-HSCT). Incidence of sinusitis within 100 days post-transplant was 9.6%, as compared to 17.7% after D+100 (p=0.006).
Distribution of the PS lesions by their volume in patients after allo-HSCT was as follows: the maxillary sinus (MS) was involved in 24 patients (30.8%) including unilateral MS affection in 1 case; the MS lesions combined with other PS were detected in 51 cases (65.4%), including 13 patients with all the sinuses affected (16.7%). Isolated lesion of the main sinus was observed in 2 cases (2.5%). Inflammation of PS without MS affection was documented in 3 cases (3.8%).
A decrease in the number of clinical symptoms of sinusitis (p=0.008), and an increase in cases of mild sinusitis on a visual analog scale (p=0.032) was registered since 100 days post-transplant (Fig. 2).

Figure 2. Time-dependent dynamics of clinical sinusitis manifestations according to visual analogue scale period after allo-HSCT
In the patients with neutropenia of I–IV degree at several weeks post-HSCT, severe changes in paranasal sinuses were more often noted by means of CT technique (p=0.018). However, in 50% of cases (24/48). In view of clinical severity of PS affection detected by CT, there were changes in severe-grade cases, and such changes in PS were more common after >100 days post-transplant (p=0.014) (Fig. 3).

Figure 3. Dynamics of changes in the sinuses detected by computer tomography, depending on the time period after allo-HSCT
Endoscopy pattern
Endoscopic images showed non-specific changes in the patients with sinusitis after allo-HSCT. Hyperemia of the nasal mucosa was significantly less common (17%) than mucosal pallor in the nasal cavities (83%, p <0.001). Oedematous nasal mucosa was observed in 38.5% of the cases. In 51% of cases, there was a discharge secretion in the nasal passages, with slimy discharge being a dominating type (80%). The secretions revealed in the nasal passages in patients with sinusitis after allo-HSCT are classified in Fig. 4.

Figure 4. Incidence of secretions revealed in the nasal passages by endoscopy of the nasal cavity in patients with sinusitis post-allo-HSCT
Infectious agents in sinusitis
In the course of this study, 41 bacteriological and mycological analyses of the samples from maxillary sinuses were performed. The specimens were obtained during diagnostic and therapeutic puncture. Briefly, any pathogen growth was not detected in 10 cases (24.4%), bacterial monocultures were isolated in 15 cases (36.6%); fungal monocultures were obtained from two samples (4.9%). The results concerning maxillary sinus aspirate were as follows: inflammation associated with bacteria in 51.2% of cases (n=21), fungal cultures were obtained in 19.5% of cases (n=8), and mixed infection was revealed in 2 cases (4.9%), as shown in Fig. 5.

Figure 5. Results of microbiological cultures of maxillary sinus aspirate from the sinusitis patients
The main sinusitis-associated pathogens in allo-HSCT recipients were Gram-positive bacteria: Staphylococcus epidermidis (30%), Streptococcus viridans (30%); Gram-negative Klebsiella pneumoniae (17.5%). The frequency of fungal sinusitis after allo-HSCT was 5%; association of bacteria and fungi was observed in 20% of cases. Aspergillus moulds proved to be the main causative agents in fungal sinusitis (80% of positive samples).
After 100 days from allo-HSCT, a larger proportion of sinus secretions showed the absence of microflora growth (p=0.022). It should be noted that the bacterial monocultures predominated up to 100 days from allo-HSCT (p=0.011). Incidence of bacterial sinusitis up to 100 days from allo-HSCT was 74% (14/19); after 100 days from allo-HSCT it was 32% (7/22) (p=0.018).
A comparative analysis of children and adolescent groups has revealed that combined infections were more often observed in adolescent patients with sinusitis (p=0.042).
Treatment of sinusitis
When assessing duration of sinusitis treatment, we have noted that the patients after auto-HSCs recovered faster than the patients after allo-HSCT (p=0.007). In our study, a recovery from sinusitis occurred within 15 days in 5% of patients after allo-HSCT, whereas 92.5% of such patients received therapy for >30 days. In 2.5% of cases, the treatment period was more than 100 days. Terms of treatment and methods of therapy for different age groups are presented in Table 3.
Table 3. Duration of treatment of sinusitis in groups and with different methods of therapy

The sinusitis treatment in pediatric patients was longer than in adolescent group (p=0.018). Usage of MS puncture in combination with antimicrobial therapy significantly reduces the duration of sinusitis treatment (p=0.024), especially in severe changes in the sinuses on CT (p=0.035).
Diagnostic and treatment punctures were performed in 41 (52.6%) patients with mandatory sampling of biomaterial for bacteriological and mycological examinations. Age of patients at the time of puncture ranged from 4 years to 21 years. In the children under 7 years, the procedure was carried out under the endotracheal anesthesia in the operating room.
At the time of the puncture, 26/41 (63.4%) patients had a blood platelet level <100.0×109/L. Of them, 20/26 (77%) patients did not exceed the level of 50.0×109/L (p=0.0001). We have not confirmed a relationship between the frequency of bleeding after the procedure and platelet levels (p=0.935).
Pneumonia and bronchitis after a sinus infection in recipients of HSCT was observed in 70.5% of cases (55/78). When analyzing the incidence of lung lesions due to sinusitis in HSCT recipients, depending on the period after allo-HSCT, we have revealed that the pulmonary lesions were observed more often before D+100 after allo-HSCT (28/34, 82%) than after 100 days (27/44, 61%, p=0.049).
The endoscopic sinus surgery was performed in 4 patients (5%) under general anaesthesia, indications for the operation were: orbital complications (reactive edema of the eyelids and local face areas), invasive fungal infection. At the time of surgical treatment, the blood platelet levels in patients ranged from 15.0 to 50.0×109/L, complications after surgery were not observed.
The mono- and multifactorial analysis have revealed several risk factors for sinusitis after allo-HSCT: a story of sinusitis before allo-HSCT (p <0.001), acute (p=0.022) or chronic graft-versus-host disease (p <0.001). In unifactorial analysis, the duration of neutropenia more than 10 days was also associated with sinusitis risk (p=0.054).
Discussion
According to different studies, the frequency of sinusitis in adult patients after allo-HSCT ranges from 11 to 51% [3, 8, 15, 16, 18]. In our group of patients, the frequency of sinusitis after allo-HSCT was 22.2%. Our study has also shown that the sinusitis frequency after allo-HSCT is higher than after auto-HSCT (p <0.001), which coincides with results from other groups [8, 11, 18].
Previous studies have noted that the presence of acute or chronic graft-versus-host reaction (GVHD) comprises a risk factor for sinusitis after allo-HSCT [18]. In our study, we found a correlation between these factors and sinusitis occurrence. Presence of acute (p=0.022) or chronic GVHD (p <0.001) was associated with significant increase of paranasal sinus pathology after allo-HSCT.
In the patients with immunodeficiency of either origin (neutropenia, HSC recipients, HIV infection) nosocomial infections were more common associated with Gram-negative bacteria (Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, Proteus spp., Enterobacter spp., Citrobacter), as well as Gram-positive bacteria such as Staphylococcus aureus (15.3%), Streptococcus pneumoniae, Enterococcus faecalis [18, 22]. In our study, the main local causative agents of sinusitis revealed in allo-HSCT recipients were Gram-positive bacteria Staphylococcus epidermidis (30%), Streptococcus viridans (30%), or Gram-negative bacteria, e.g., Klebsiella pneumoniae (17.5%). It was found that the proportion of negative cultures from the sinuses was higher at the terms of >100 days after allo-HSCT (p=0.022). It should be noted that the monocultures of bacteria prevailed up to 100 days from allo-HSCT (p=0.011). The findings for combined sinusitis-associated infections were more often observed in adolescent patients, in comparison with children group (p=0.042).
In assessing the duration of sinusitis treatment, we have noted that the patients after auto-HSCT recovered faster than patients after allo-HSCT (p=0.007). This fact may be associated with a faster recovery of the body's defense mechanisms after auto-HSCT than following allo-HSCT, as well as the lack of immunosuppressive therapy in autologous transplants. In our study, recovery from sinusitis occurred within 15 days in 5% of patients after allo-HSCT; 92.5% of patients received therapy for 30 days or more. In 2.5% of patients, the treatment period exceeded 100 days post-transplant. The use of PPP puncture in combination with antimicrobial therapy significantly reduces the duration of sinusitis treatment (p=0.024), especially in cases with severe changes in paranasal sinuses registered by CT and MRI (p=0.035). In pediatric patients, sinusitis treatment was longer than in the adolescent group (p=0.018).
Conclusion
1. Sinusitis folowing allogeneic HSCT occurs more frequently than in auto-transplants;
2. The significant factors for the post-transplant sinusitis are: sufficient immunosuppression, e.g., associated to acute or chronic GVHD;
3. Opportunistic microflora in local samples from the sinusitis patients was found in a half of microbiological cultures.
Conflict of interest
The authors report no conflicts of interest.
References
- Ivanchenko OA, Lopatin AS. Chronic rhinosinusitis: epidemiology, classification, etiology, pathogenesis. Mo-dern view on the problem. Vestn Otorhinolaryngol. 2012; 2: 91-96 (In Russian).
- Pluzhnikov MS, Lavrenova GV, Katinas EB. Basic prin- ciples of immunocorrecting therapy in otorhinolaryngology. Vestn Otorhinolaryngol. 2008. № 4:7-12 (In Russian).
- Arulrajah S, Symons H, Cahoon EK, Tekes A, Thierry A, Huisman G M, Izbudak I. Relationship between clinical sinusitis symptoms and sinus CT severity in pediatric post bone marrow transplant and immunocompetent patients. Eur J Pediatr. 2012; 171(2): 375-381.
- Slavsky AN, Pshonkina DM, Svistushkin VM. Bacteriophages in the complex treatment of acute bacterial rhinosinusitis. Rus Med J. 2014; 2:1925-1928 (In Russian).
- Bento LR, Ortiz E, Nicola EM, Vigorito AC. Sinonasal disorders in hematopoietic stem cell transplantation. Braz J Otorhinolaryngol. 2014; 80(4): 285-289.
- Afanasyev BV, Volkova OY, Ganapiev AA. In: Afanasyev, BV (Ed). Hematology: A Guide for Doctors. St.Petersburg: Speclit. 2008. - 238 p (In Russian).
- Weinberg К, Blazar BR, Wagner JE, Agura E, Hill BJ, Smogorzewska M, Koup RA, Betts MR, Collins RH, Douek DC. Factors affecting thymic function after allogeneic hematopoietic stem cell transplantation. Blood. 2001; 97(5): 1458-1466.
- Thompson AM, Couch M, Zahurak ML, Johnson C, Vogelsang GB. Risk factors for post-stem cell transplant sinusitis. Bone Marrow Transplant. 2002; 29(3): 257-261.
- Appelbaum FR. Hematopoietic-cell transplantation at 50. New Engl J Med. 2007; 357(15):1472-1475.
- Gratwohl A, Baldomero H, Aljurf M, Pasquini MC. Hematopoietic stem cell transplantation. A global perspective. J Am Med Ass. 2010;303(16):1617-1624.
- Won YW, Yi SY, Jang JH, Kim K, Kim SJ, Kim WS, Jung CW, Kim DH. Retrospective analysis of paranasal sinusitis in patients receiving hematopoietic stem cell transplantation. Int J Hematol. 2011; 93(3):383-388.
- Inaba H, Hartford CM, Pei D, Posner MJ, Yang J, Hayden RT, Srinivasan A, Triplett BM, McCulllers JA, Pui CH, Leung W. Longitudinal analysis of antibody response to immunization in paediatric survivors after allogeneic haematopoietic stem cell transplantation. Br J Haematol. 2012; 156(1): 109-117.
- Meng L, Huang XJ. Allogeneic hematopoietic stem cell transplantation in China: where we are and where to go. J Hematol Oncol. 2012. 5(1):10.
- Mortellaro C, Mortellaro C, Barat V, Nesi F, L. Bello, G. Bologna, D. Farronato, A. G. Lucchina, A. Linari. Intercurrent infectious diseases in post-stem cell transplant patients: paranasal sinusitis. J Craniofac Surg. 2012; 23(1):153-157.
- Meyers JD. Infection in bone marrow transplant recipients Am J Med. 1986; 81(1):27-38.
- Shibuya TY, Momin F, Abella E, Jacobs JR, Karanes C, Ratanatharathorn V, Sensenbrenner LL, Lum LG. Sinus disease in the bone marrow transplant population: incidence, risk factors, and complications. Otolaryngol Head Neck Surg. 1995; 113(6):705-711.
- Deutsch JH, Hudgins PA, Siegel JL, Peterman SB, Devine SM, York R, Wingard JR. The paranasal sinuses of patients with acute graft-versus-host disease. Am J Neuroradiol. 1995; 16(6):1287-1291.
- Savage DG, Taylor P, Blackwel J, Chen F, Szydlo RM, Rule SAJ, Spencer A, Apperley JF, Goldman JM. Paranasal sinusitis following allogeneic bone marrow transplant. Bone Marrow Transplant. 1997; 19(1):55-59.
- Fokkens WJ, Lund VJ, Mullol J, Bachert C, Alobid I, Baroody F, Cohen N, Cervin A, Douglas R, Gevaert P, Georgalas C, Goossens H, Harvey R, Hellings P, Hopkins C, Jones N, Joos G, et al. European Position Paper on Rhinosinusitis and Nasal Polyps Group: European position paper on rhinosinusitis and nasal polyps 2012. Rhinology. 2012; 50 (Suppl 23): 1-329.
- Lim М, Lew Gor S, Darby Y. The relationship between subjective assessment instruments in chronic rhinosinusitis. Rhinology. 2007; 45(2):144-147.
- Lund VJ, Kennedy DW. Staging for chronic rhinosinusitis. Otolaryngol Head Neck Surg. 1997: 117(1):35-40.
- Imamura R, Voegels R, Sperandio F. Microbiology of sinusitis in patients undergoing bone marrow transplantation. Otolaryngol Head Neck Surg. 1999; 120(2): 279-282.
Екатерина С. Утимишева1, Олег И. Долгов1, Олеся В. Паина1, Кирилл А. Екушов1, Алина А. Витрищак1, Борис И. Смирнов2, Людмила С. Зубаровская 1, Сергей А. Карпищенко1, Борис В. Афанасьев1
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21675" ["VALUE"]=> array(2) { ["TEXT"]=> string(425) "<p><sup>1</sup> Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Россия<br> <sup>2</sup> Санкт-Петербургский государственный электротехнический университет «ЛЭТИ», Россия</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(383) "1 Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Россия
2 Санкт-Петербургский государственный электротехнический университет «ЛЭТИ», Россия
Синусит после аллогенной трансплантации гемопоэтических стволовых клеток возникает в 22,2% случаев с более высокой частотой после 100 дня от алло-ТГСК, чем до 100 (р=0,006). Основными факторами риска возникновения синусита после аллогенной трансплантации гемопоэтических стволовых клеток являлись: синусит до алло-ТГСК (р <0,001), длительность нейтропении более 10 дней (р=0,054), наличие у пациентов острой (р=0,022) или хронической «реакции трансплантат против хозяина» (р <0,001). Основными возбудителями острых синуситов у реципиентов алло-ТГСК в исследовании являлись грамположительные бактерии Staphylococcus epidermidis (30%), Streptococcus viridans (30%), грамотрицательные бактерии Klebsiella pneumoniae (17,5%). Монокультура бактерий преобладала до 100 дня от алло-ТГСК (р=0,011). У пациентов подросткового возраста чаще наблюдался полиэтиологичный характер возбудителей синусита по сравнению с группой «дети». Степень тяжести изменений околоносовых пазух на компьютерной томографии после 100 дня от алло-ТГСК более выражена (р=0,014), что находится в дисбалансе с меньшим количеством клинических симптомов синусита (р=0,008) и более частым течением синусита в легкой степени при оценке по визуальной аналоговой шкале (р=0,032) в этот период. Применение пункций верхнечелюстных пазух в сочетании с противомикробной терапией сокращает сроки лечения синусита у этих пациентов (р=0,024).
Ключевые слова
Синусит, дети, трансплантация гемопоэтических клеток, клинические особенности.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21677" ["VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-46-53" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-46-53" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21689" ["VALUE"]=> array(2) { ["TEXT"]=> string(418) "<p>Ekaterina S. Utimisheva<sup>1</sup>, Oleg I. Dolgov<sup>1</sup>, Olesya V. Paina<sup>1</sup>, Kirill A. Ekushov<sup>1</sup>, Alina A. Vitrischak<sup>1</sup>, Boris I. Smirnov<sup>2</sup>, Ludmila S. Zubarovskaya<sup>1</sup>, Sergey A. Karpischenko<sup>1</sup>, Boris V. Afanasyev<sup>1</sup></p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(298) "Ekaterina S. Utimisheva1, Oleg I. Dolgov1, Olesya V. Paina1, Kirill A. Ekushov1, Alina A. Vitrischak1, Boris I. Smirnov2, Ludmila S. Zubarovskaya1, Sergey A. Karpischenko1, Boris V. Afanasyev1
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21690" ["VALUE"]=> array(2) { ["TEXT"]=> string(234) "<p><sup>1</sup> Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia<br> <sup>2</sup> St. Petersburg State Electrotechnical University LETI, St. Petersburg, Russia</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(192) "1 Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia
2 St. Petersburg State Electrotechnical University LETI, St. Petersburg, Russia
Sinusitis after allogeneic transplantation of hematopoietic stem cells occurs in 22.2% of cases being more frequent at >100 days following allo-HSCT, than at earlier terms (p=0.006). The main risk factors for sinusitis after allogeneic stem cell transplantation were as follows: sinusitis before allo-HSCT (p <0.001), neutropenia duration for more than 10 days (p=0.054), acute (p=0.022) or chronic graft-versus-host disease (p <0.001) in the patients. The main pathogens of sinusitis revealed in allo-HSCT recipients during the study were: Gram-positive Staphylococcus epidermidis (30%), Streptococcus viridans (30%); Gram-negative Klebsiella pneumoniae (17.5%). A monoculture of bacteria predominated within 100 days posttransplant (p=0.011). Poly-etiological origin of the causative bacterial agents in sinusitis was more likely in adolescent patients, in comparison to the younger children group. The severity of changes in paranasal sinuses, as registered with computed tomography after 100 days after allo-HSCT, was more pronounced (p=0.014) than at earlier terms, thus being discordant with less common clinical signs of sinusitis (p=0.008), and milder clinical course of sinusitis assessed by a visual analogue scale (p=0.032) during this period. Punctures of maxillary sinuses combined with antimicrobial therapy proved to shorten the duration of sinusitis treatment in these patients (p=0.024).
Keywords
Sinusitis, children, hematopoietic stem cell transplantation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21678" ["VALUE"]=> string(121) "Incidence, diagnosis and treatment of sinusitis in children and adolescents after hematopoietic stem cell transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(121) "Incidence, diagnosis and treatment of sinusitis in children and adolescents after hematopoietic stem cell transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21679" ["VALUE"]=> string(4) "1595" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1595" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21692" ["VALUE"]=> string(4) "1597" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1597" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(12) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21689" ["VALUE"]=> array(2) { ["TEXT"]=> string(418) "<p>Ekaterina S. Utimisheva<sup>1</sup>, Oleg I. Dolgov<sup>1</sup>, Olesya V. Paina<sup>1</sup>, Kirill A. Ekushov<sup>1</sup>, Alina A. Vitrischak<sup>1</sup>, Boris I. Smirnov<sup>2</sup>, Ludmila S. Zubarovskaya<sup>1</sup>, Sergey A. Karpischenko<sup>1</sup>, Boris V. Afanasyev<sup>1</sup></p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(298) "Ekaterina S. Utimisheva1, Oleg I. Dolgov1, Olesya V. Paina1, Kirill A. Ekushov1, Alina A. Vitrischak1, Boris I. Smirnov2, Ludmila S. Zubarovskaya1, Sergey A. Karpischenko1, Boris V. Afanasyev1
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(298) "Ekaterina S. Utimisheva1, Oleg I. Dolgov1, Olesya V. Paina1, Kirill A. Ekushov1, Alina A. Vitrischak1, Boris I. Smirnov2, Ludmila S. Zubarovskaya1, Sergey A. Karpischenko1, Boris V. Afanasyev1
" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21691" ["VALUE"]=> array(2) { ["TEXT"]=> string(1680) "<p style="text-align: justify;">Sinusitis after allogeneic transplantation of hematopoietic stem cells occurs in 22.2% of cases being more frequent at >100 days following allo-HSCT, than at earlier terms (p=0.006). The main risk factors for sinusitis after allogeneic stem cell transplantation were as follows: sinusitis before allo-HSCT (p <0.001), neutropenia duration for more than 10 days (p=0.054), acute (p=0.022) or chronic graft-versus-host disease (p <0.001) in the patients. The main pathogens of sinusitis revealed in allo-HSCT recipients during the study were: Gram-positive <i>Staphylococcus epidermidis</i> (30%), <i>Streptococcus viridans</i> (30%); Gram-negative <i>Klebsiella pneumoniae</i> (17.5%). A monoculture of bacteria predominated within 100 days posttransplant (p=0.011). Poly-etiological origin of the causative bacterial agents in sinusitis was more likely in adolescent patients, in comparison to the younger children group. The severity of changes in paranasal sinuses, as registered with computed tomography after 100 days after allo-HSCT, was more pronounced (p=0.014) than at earlier terms, thus being discordant with less common clinical signs of sinusitis (p=0.008), and milder clinical course of sinusitis assessed by a visual analogue scale (p=0.032) during this period. Punctures of maxillary sinuses combined with antimicrobial therapy proved to shorten the duration of sinusitis treatment in these patients (p=0.024).</p> <h2>Keywords</h2> <p style="text-align: justify;">Sinusitis, children, hematopoietic stem cell transplantation.</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1579) "Sinusitis after allogeneic transplantation of hematopoietic stem cells occurs in 22.2% of cases being more frequent at >100 days following allo-HSCT, than at earlier terms (p=0.006). The main risk factors for sinusitis after allogeneic stem cell transplantation were as follows: sinusitis before allo-HSCT (p <0.001), neutropenia duration for more than 10 days (p=0.054), acute (p=0.022) or chronic graft-versus-host disease (p <0.001) in the patients. The main pathogens of sinusitis revealed in allo-HSCT recipients during the study were: Gram-positive Staphylococcus epidermidis (30%), Streptococcus viridans (30%); Gram-negative Klebsiella pneumoniae (17.5%). A monoculture of bacteria predominated within 100 days posttransplant (p=0.011). Poly-etiological origin of the causative bacterial agents in sinusitis was more likely in adolescent patients, in comparison to the younger children group. The severity of changes in paranasal sinuses, as registered with computed tomography after 100 days after allo-HSCT, was more pronounced (p=0.014) than at earlier terms, thus being discordant with less common clinical signs of sinusitis (p=0.008), and milder clinical course of sinusitis assessed by a visual analogue scale (p=0.032) during this period. Punctures of maxillary sinuses combined with antimicrobial therapy proved to shorten the duration of sinusitis treatment in these patients (p=0.024).
Keywords
Sinusitis, children, hematopoietic stem cell transplantation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(1579) "Sinusitis after allogeneic transplantation of hematopoietic stem cells occurs in 22.2% of cases being more frequent at >100 days following allo-HSCT, than at earlier terms (p=0.006). The main risk factors for sinusitis after allogeneic stem cell transplantation were as follows: sinusitis before allo-HSCT (p <0.001), neutropenia duration for more than 10 days (p=0.054), acute (p=0.022) or chronic graft-versus-host disease (p <0.001) in the patients. The main pathogens of sinusitis revealed in allo-HSCT recipients during the study were: Gram-positive Staphylococcus epidermidis (30%), Streptococcus viridans (30%); Gram-negative Klebsiella pneumoniae (17.5%). A monoculture of bacteria predominated within 100 days posttransplant (p=0.011). Poly-etiological origin of the causative bacterial agents in sinusitis was more likely in adolescent patients, in comparison to the younger children group. The severity of changes in paranasal sinuses, as registered with computed tomography after 100 days after allo-HSCT, was more pronounced (p=0.014) than at earlier terms, thus being discordant with less common clinical signs of sinusitis (p=0.008), and milder clinical course of sinusitis assessed by a visual analogue scale (p=0.032) during this period. Punctures of maxillary sinuses combined with antimicrobial therapy proved to shorten the duration of sinusitis treatment in these patients (p=0.024).
Keywords
Sinusitis, children, hematopoietic stem cell transplantation.
" } ["DOI"]=> array(37) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21677" ["VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-46-53" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-46-53" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-46-53" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21678" ["VALUE"]=> string(121) "Incidence, diagnosis and treatment of sinusitis in children and adolescents after hematopoietic stem cell transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(121) "Incidence, diagnosis and treatment of sinusitis in children and adolescents after hematopoietic stem cell transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(121) "Incidence, diagnosis and treatment of sinusitis in children and adolescents after hematopoietic stem cell transplantation" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21690" ["VALUE"]=> array(2) { ["TEXT"]=> string(234) "<p><sup>1</sup> Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia<br> <sup>2</sup> St. Petersburg State Electrotechnical University LETI, St. Petersburg, Russia</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(192) "1 Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia
2 St. Petersburg State Electrotechnical University LETI, St. Petersburg, Russia
1 Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia
2 St. Petersburg State Electrotechnical University LETI, St. Petersburg, Russia
Екатерина С. Утимишева1, Олег И. Долгов1, Олеся В. Паина1, Кирилл А. Екушов1, Алина А. Витрищак1, Борис И. Смирнов2, Людмила С. Зубаровская 1, Сергей А. Карпищенко1, Борис В. Афанасьев1
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(423) "Екатерина С. Утимишева1, Олег И. Долгов1, Олеся В. Паина1, Кирилл А. Екушов1, Алина А. Витрищак1, Борис И. Смирнов2, Людмила С. Зубаровская 1, Сергей А. Карпищенко1, Борис В. Афанасьев1
" } ["SUBMITTED"]=> array(37) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21662" ["VALUE"]=> string(10) "06.04.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "06.04.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "06.04.2019" } ["ACCEPTED"]=> array(37) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21663" ["VALUE"]=> string(10) "15.04.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "15.04.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "15.04.2019" } ["CONTACT"]=> array(38) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21664" ["VALUE"]=> string(4) "1637" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1637" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(67) "Ekaterina S. Utimisheva" ["LINK_ELEMENT_VALUE"]=> bool(false) } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21676" ["VALUE"]=> array(2) { ["TEXT"]=> string(2799) "<p style="text-align: justify;">Синусит после аллогенной трансплантации гемопоэтических стволовых клеток возникает в 22,2% случаев с более высокой частотой после 100 дня от алло-ТГСК, чем до 100 (р=0,006). Основными факторами риска возникновения синусита после аллогенной трансплантации гемопоэтических стволовых клеток являлись: синусит до алло-ТГСК (р <0,001), длительность нейтропении более 10 дней (р=0,054), наличие у пациентов острой (р=0,022) или хронической «реакции трансплантат против хозяина» (р <0,001). Основными возбудителями острых синуситов у реципиентов алло-ТГСК в исследовании являлись грамположительные бактерии <i>Staphylococcus epidermidis </i>(30%), <i>Streptococcus viridans</i> (30%), грамотрицательные бактерии <i>Klebsiella pneumoniae</i> (17,5%). Монокультура бактерий преобладала до 100 дня от алло-ТГСК (р=0,011). У пациентов подросткового возраста чаще наблюдался полиэтиологичный характер возбудителей синусита по сравнению с группой «дети». Степень тяжести изменений околоносовых пазух на компьютерной томографии после 100 дня от алло-ТГСК более выражена (р=0,014), что находится в дисбалансе с меньшим количеством клинических симптомов синусита (р=0,008) и более частым течением синусита в легкой степени при оценке по визуальной аналоговой шкале (р=0,032) в этот период. Применение пункций верхнечелюстных пазух в сочетании с противомикробной терапией сокращает сроки лечения синусита у этих пациентов (р=0,024). </p> <h2>Ключевые слова</h2> <p style="text-align: justify;">Синусит, дети, трансплантация гемопоэтических клеток, клинические особенности.</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2701) "Синусит после аллогенной трансплантации гемопоэтических стволовых клеток возникает в 22,2% случаев с более высокой частотой после 100 дня от алло-ТГСК, чем до 100 (р=0,006). Основными факторами риска возникновения синусита после аллогенной трансплантации гемопоэтических стволовых клеток являлись: синусит до алло-ТГСК (р <0,001), длительность нейтропении более 10 дней (р=0,054), наличие у пациентов острой (р=0,022) или хронической «реакции трансплантат против хозяина» (р <0,001). Основными возбудителями острых синуситов у реципиентов алло-ТГСК в исследовании являлись грамположительные бактерии Staphylococcus epidermidis (30%), Streptococcus viridans (30%), грамотрицательные бактерии Klebsiella pneumoniae (17,5%). Монокультура бактерий преобладала до 100 дня от алло-ТГСК (р=0,011). У пациентов подросткового возраста чаще наблюдался полиэтиологичный характер возбудителей синусита по сравнению с группой «дети». Степень тяжести изменений околоносовых пазух на компьютерной томографии после 100 дня от алло-ТГСК более выражена (р=0,014), что находится в дисбалансе с меньшим количеством клинических симптомов синусита (р=0,008) и более частым течением синусита в легкой степени при оценке по визуальной аналоговой шкале (р=0,032) в этот период. Применение пункций верхнечелюстных пазух в сочетании с противомикробной терапией сокращает сроки лечения синусита у этих пациентов (р=0,024).
Ключевые слова
Синусит, дети, трансплантация гемопоэтических клеток, клинические особенности.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2701) "Синусит после аллогенной трансплантации гемопоэтических стволовых клеток возникает в 22,2% случаев с более высокой частотой после 100 дня от алло-ТГСК, чем до 100 (р=0,006). Основными факторами риска возникновения синусита после аллогенной трансплантации гемопоэтических стволовых клеток являлись: синусит до алло-ТГСК (р <0,001), длительность нейтропении более 10 дней (р=0,054), наличие у пациентов острой (р=0,022) или хронической «реакции трансплантат против хозяина» (р <0,001). Основными возбудителями острых синуситов у реципиентов алло-ТГСК в исследовании являлись грамположительные бактерии Staphylococcus epidermidis (30%), Streptococcus viridans (30%), грамотрицательные бактерии Klebsiella pneumoniae (17,5%). Монокультура бактерий преобладала до 100 дня от алло-ТГСК (р=0,011). У пациентов подросткового возраста чаще наблюдался полиэтиологичный характер возбудителей синусита по сравнению с группой «дети». Степень тяжести изменений околоносовых пазух на компьютерной томографии после 100 дня от алло-ТГСК более выражена (р=0,014), что находится в дисбалансе с меньшим количеством клинических симптомов синусита (р=0,008) и более частым течением синусита в легкой степени при оценке по визуальной аналоговой шкале (р=0,032) в этот период. Применение пункций верхнечелюстных пазух в сочетании с противомикробной терапией сокращает сроки лечения синусита у этих пациентов (р=0,024).
Ключевые слова
Синусит, дети, трансплантация гемопоэтических клеток, клинические особенности.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21675" ["VALUE"]=> array(2) { ["TEXT"]=> string(425) "<p><sup>1</sup> Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Россия<br> <sup>2</sup> Санкт-Петербургский государственный электротехнический университет «ЛЭТИ», Россия</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(383) "1 Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Россия
2 Санкт-Петербургский государственный электротехнический университет «ЛЭТИ», Россия
1 Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Россия
2 Санкт-Петербургский государственный электротехнический университет «ЛЭТИ», Россия
Introduction
Hemophagocytic lymphohistiocytosis (HLH) is a common name for a number of potentially fatal inborn and acquired diseases, which are characterised by the changes in the immune response regulation, leading to uncontrolled proliferation of cytotoxic T-lymphocytes and macrophages, systemic inflammation. Due to the lack of specific clinical features and laboratory data, long-lasting fever, unclear cytopenias, unexplained liver failure, and elevated inflammation markers should lead to the suspicion for HLH.
Our case presentation was aimed for demonstration of different clinical pattern in HLH associated with the UNC13D genetic mutation.
Case presentation
Sibling 1
The patient was from a family without known hereditary disorders. A girl was born after the second full-term non-complicated pregnancy. Perinatal period proceeded without any specific features. Physical development was to the age until 2.4 years old, when a systemic disorder has manifested with high fever (40.5°C) and lymphadenopathy. Despite the ongoing therapy with interferon and antibacterial treatment, the fever lasted for 14 days, and lymphadenopathy was presented by enlarged cervical lymph node group (<2 cm in size) and inguinal nodes (<1.5 cm). Hepatomegaly and enlarged spleen were also registered (respectively, to 2.0 cm, and 1.5- 2.0 cm). Clinical blood counts showed mild anemia, neutropenia, lymphocytosis, plasmacytosis, thrombocytopenia. PCR virological testing showed activation of Epstein-Barr virus (EBV) and cytomegalovirus (CMV) (blood).
The primary disorder was initially diagnosed as severe acute infectious mononucleosis with liver damage. Antiviral therapy with intravenous immunoglobulins was started. However, the patient's condition worsened due to persistent fever up to 40.5°C, progressing hepatosplenomegaly, pancytopenia, hemorrhagic syndrome and oedema. Biochemical liver test panel showed hypoalbuminemia, hypofibrinogenemia, increased serum bilirubin (both direct and indirect fractions), enhanced ALT, AST, and GGTP activities. Hypertriglyceridemia and increased serum ferritin levels were also present.
On the basis of typical clinical picture and laboratory criteria, a hemophagocytic lymphohistiocytosis (HLH) was suspected [1]. Morphological study of bone marrow aspirate has revealed specific forms of phagocytizing monocytes with engulfed mature red blood cells in their cytoplasm. The cerebrospinal fluid protein test was 0.6 g/l, lymphocytic cytosis – 32/3. Cytogenetic study of the bone marrow cells showed no abnormalities.
DNA sequencing of selected amplicons of known HLH-associate genes, i.e., STX11 (exons 1-2), STXBP2 (exons 1 to 19), PRF1 (exons 1 to 3) and adjacent intronic segments did not reveal any homozygous mutations. In STXBP2 gene (exon 18), the analysis has shown an ATA→GTA substitution in с.1609an (Ile537Val) in heterozygous state. This polymorphism is rather common in population (0.264). Hence, the data from Sanger DNA sequencing analysis showed a heterozygous state for STXBP2 and UNC13D gene mutations which indirectly supported the HLH diagnosis.
Due to suspected primary HLH and rapid clinical progression of disease, the HLH-94 protocol therapy with VP-16, dexamethasone, Cyclosporin A, and intratecal cytostatic therapy was started before receiving the genetic test results. According to the HLA typing data, the siblings were haploidentical.
Partial clinical response (apyrexia, lymph node size reduction, normalization of liver function) was achieved within 4 weeks after initiating the therapy, but the CMV reactivation associated with the disease progressed followed by fatal outcome at the age of 2 years 7 months.
Sibling 2
A boy from the 4th normal full-term pregnancy, without specific symptoms during postnatal period. At the age of 1.3 y.o., the child presented with fever which lasted for up to 8 days. Viral infection was suggested as a primary diagnosis, and symptomatic therapy was started. Positive dynamics was achieved, but the sub-febrile body temperature still persisted. Cytopenia was detected in routine blood counts (total leucocyte count – 7.0×109/l, absolute neutrophil count – 0.42×109/l, platelet count – 60×109/l). The serum ALT and AST levels exceeded five-fold the normal values. A differential diagnosis was made between infectious mononucleosis, viral hepatitis, and Yersinia infection.
The laboratory tests have shown pancytopenia, atypical mononuclear cells (blood); hypofibrinogenemia; hypertriglyceridemia; serum ferritin level within normal limits; the viral hepatitis markers (HAV, HBV, HCV) were negative. PCR tests for HSV type 6 (blood) were positive, as well as EBV DNA was found in saliva. Hepatomegaly was up to +2.0 cm, and splenomegaly, up to +3.0 cm.
Despite the symptomatic therapy the patient showed further cytopenia, febrile fever, lymphoproliferative syndrome without progression. Hemophagocytosis was not detectable in the bone marrow aspirate and cerebrospinal fluid.
Like as in sibling 1, a direct gene sequencing showed heterozygous mutation found in exon 31 of the UNC13D gene, i.e., single-nucleotide deletion (c.3082delC) and duplication (c.3037dupG) in the same exon, without reported associations with any inherited conditions.
The patient underwent specific therapy according to the HLH-94 protocol with achievement of a complete response by the end of initial treatment course. The prolonged therapy was continued over 9 weeks (dexamethasone pulse treatment at 10 mg/m2 for 3 days every second week and VP-16 infusions 150 mg/m2 every alternating second week with daily oral CSA), the clinical remission still persisted.
The patient and his sister were HLA-haploidentical. An unrelated donor was found in the International Donor Registry (9/10 compatibility for the main HLA loci, with only mismatch in locus C) and used for HSCT in this case.
A myeloablative reduced-toxicity conditioning with Treosulfan, Fludarabin and Thiotepa,was chosen for hematopoietic stem cell transplantation (HSCT). GvHD prophylaxis consisted of post-transplant cyclophosphamide, tacrolimus, and Cellsept. The patient has tolerated the conditioning regimen without significant associated toxicity. Engraftment was achieved on the D + 27 post-transplant. The follow-up period after allo-HSCT is one year. The hematopoietic graft functions satisfactorily with engraftment at the level of complete donor chimerism, there is no dependence on blood transfusions, with persisting remission of the disease.
Sibling 3
In view of the family history, the eldest child (sister) in the family was also observed. A mutation in the heterozygous state was also detected in the UNC13D gene by Sanger sequencing analysis. At the time of the survey, the girl was 12 years old. The physical development of the child is age appropriate. No signs of HLH have been shown so far, thus suggesting a sufficient phenotypic heterogeneity among the siblings observed.
Discussion
HLH is a severe clinical syndrome of the immune system, requiring early diagnosis, which allows combined immunosuppressive and chemotherapy to be started in time and may be followed by allo-HSCT, thus significantly increasing the chances for a favorable outcome of the disease [2].
The primary, genetically determined cases of HLH evolve as a result of genetically determined defect of the cellular cytotoxicity, and due to secondary hemophagocytic syndrome. The incidence of primary HLH is 1 in 50.000 newborns per year. Up to 70-80% of the primary HLH cases are diagnosed over the first year of life, whereas 20% manifest at the age of >3 years [3]. Secondary HLH may be associated with infectious, systemic autoimmune, malignant diseases and hereditary metabolic errors, depending on the distinct causal factors (Table 1).
Table 1. Causal and pathogenetic factors for secondary HLH [4, 5, 6]

Clinically, HLH is manifested by prolonged fever refractory to antimicrobial therapy; progressive cytopenia; lymphoproliferative, oedemas and hemorrhagic syndromes; hepatic dysfunction; symptoms of damage to the central nervous system (irritability, convulsions, meningeal symptoms, altered consciousness). Infections, mostly caused by herpesviruses, seem to be the main trigger leading to the HLH manifestations [7]. In the absence of specific therapy, the disease progresses rapidly and may end fatally. Sometimes, however, it may have a chronic, relapsed clinical course.
Appropriate clinical findings in HLH are non-specific, despite the severity of the manifestations. Therefore, it is possible to establish the diagnosis only on the basis of some characteristic laboratory tests. To establish the HLH diagnosis, at least 5 of 8 diagnostic criteria proposed by the International Society of Histiocytosis should be present in the patient, as follows: fever over 38.5 with a duration of at least 7 days, splenomegaly (>3.0 cm), bicytopenia (hemoglobin <90 g/l, platelet count <100×109/l, neutrophil count <1×109/l), hypertriglyceridemia (>2.0 mmol/L), and/or hypofibrinogenemia (<1.5 g/L), increased serum ferritin (more than 500 µg/L), decreased activity of peripheral NK cells, soluble CD25+ over 2500 U/L, evidence of hemophagocytosis in the bone marrow, lymphatic nodes, cerebrospinal fluid [1].
In young patients, HLH should be differentiated from sepsis, generalized perinatal infections, Wiscott-Aldrich syndrome, acute leukemia, juvenile myelomonocytic leukemia, histiocytosis originating from Langerhans cells, autoimmune lymphoproliferative syndrome. In older patients, hemophagocytic syndrome also needs to be differentiated from sepsis, hemoblastosis, viral hepatitis, viral encephalitis.
Early onset of the disease (1st year of life), family history (related marriage, sibling death in infancy), persistence of cellular cytotoxicity defects after achieving clinical/laboratory remission, recurrence of the disease, may be indicative for its hereditary nature. The final diagnosis of primary HLH is generally supported by identified mutations in one of candidate genes (PRF1, MUNC13D, STX11, STXBP) [6].
All the patients with suspected primary HLH should receive combined immunosuppressive chemotherapy to control systemic inflammation and prevent irreversible organ damage. Detection of pathogenic mutations is currently a necessary diagnostic criterion for predicting the time of onset and severity of clinical manifestations in primary forms of HLH, but these may be present and also occur in patients without signs of disease, as confirmed in one of the largest studies of HLH patients from Italy [8].
In the case of asymptomatic carriage of a potentially pathogenic mutation, the patient management strategies are determined by the nature of presumed defect. E.g., the patients with UNC13D mutation are kept under dynamic observation, while PRF1 and RAB27A mutations have an unfavorable prognosis, and the patients who underwent allo-HSCT prior to the development of clinical HLH symptoms have better survival rates [9].
Allogeneic transplantation of hematopoietic stem cells (allo-HSCT) is indicated in cases of proven primary HLH. Allo-HSCT is a preferable option in remission of the disease, but the absence of remission is not a contraindication for it. If planning a related allo-HSCT, it is necessary to make sure that the potential donor (sibling) who has no phenotypic features of the disorder doesn’t suffer from familial HLH.
References
- Henter JI, Horne A, Aricó M, Egeler RM, Filipovich AH, Imashuku S, Ladisch S, McClain K, Webb D, Winiarski J, Janka G. HLH-2004: diagnostic and therapeutic guidelines for hemophagocytic lymphohistiocytosis. Pediat Blood Cancer. 2007;48(2):124-131.
- Janka GE, Lehmberg K. Hemophagocytic syndromes – an update. Blood Rev. 2014: 2014;28(4):135-142.
- George MR. Hemophagocytic lymphohistiocytosis: review of etiologies and management, J Blood Med. 2014;5:69-86.
- Contino A, Trombatore G, Timeus F. Hemophagocytic lymphohistiocytosis in pediatric patients: a review. J Blood Disord Symptoms Treat. 2018; 2(1): 011.
- Maschan MA, Novichkova GA, Federal Clinical Guidelines for the Diagnosis and Treatment of Hemophagocytic Lymphohistiocytosis, 2014 (in Russian).
- Zhang K, Filipovich AH, Johnson J, Marsh RA, Villanueva J, Hemophagocytic lymphohistiocytosis, familial, Gene- Reviews [Internet]. Seattle (WA). 2006; Mar 22 [updated 2013 Jan 17].
- Brisse E, Wouters CH, Andrei G, Matthys P. How viruses contribute to the pathogenesis of hemophagocytic lymphohistiocytosis. Front Immunol. 2017 Sep 7;8:1102. doi: 10.3389/fimmu.2017.01102.
- Cetica V, Sieni E, Pende D, Danesino C, De Fusco C, Locatelli F, Micalizzi C, Putti MC, Biondi A, Fagioli F, Moretta L, Griffiths GM, Luzzatto L, Arico M. Genetic predisposition to hemophagocytic lymphohistiocytosis: Report on 500 patients from the Italian registry, J Allergy Clin Immunol. 2016;137(1):188-196.e4
- Lucchini G, Marsh R, Gilmour K, Worth A, Nademi Z, Rao A, Booth C, Amrolia P, Silva J, Chiesa R, Wynn R, Lehmberg K, Astigarraga I, Gungor T, Stary J, Moshous D, Ifversen M, Zinn D, Jordan M, Kumar A, Yasumi T, Vey P, Rao K. Treatment dilemmas in asymptomatic children with primary haemophagocytic lymphohistiocytosis. Blood, 2018;132(19):2088-2096.
Introduction
Hemophagocytic lymphohistiocytosis (HLH) is a common name for a number of potentially fatal inborn and acquired diseases, which are characterised by the changes in the immune response regulation, leading to uncontrolled proliferation of cytotoxic T-lymphocytes and macrophages, systemic inflammation. Due to the lack of specific clinical features and laboratory data, long-lasting fever, unclear cytopenias, unexplained liver failure, and elevated inflammation markers should lead to the suspicion for HLH.
Our case presentation was aimed for demonstration of different clinical pattern in HLH associated with the UNC13D genetic mutation.
Case presentation
Sibling 1
The patient was from a family without known hereditary disorders. A girl was born after the second full-term non-complicated pregnancy. Perinatal period proceeded without any specific features. Physical development was to the age until 2.4 years old, when a systemic disorder has manifested with high fever (40.5°C) and lymphadenopathy. Despite the ongoing therapy with interferon and antibacterial treatment, the fever lasted for 14 days, and lymphadenopathy was presented by enlarged cervical lymph node group (<2 cm in size) and inguinal nodes (<1.5 cm). Hepatomegaly and enlarged spleen were also registered (respectively, to 2.0 cm, and 1.5- 2.0 cm). Clinical blood counts showed mild anemia, neutropenia, lymphocytosis, plasmacytosis, thrombocytopenia. PCR virological testing showed activation of Epstein-Barr virus (EBV) and cytomegalovirus (CMV) (blood).
The primary disorder was initially diagnosed as severe acute infectious mononucleosis with liver damage. Antiviral therapy with intravenous immunoglobulins was started. However, the patient's condition worsened due to persistent fever up to 40.5°C, progressing hepatosplenomegaly, pancytopenia, hemorrhagic syndrome and oedema. Biochemical liver test panel showed hypoalbuminemia, hypofibrinogenemia, increased serum bilirubin (both direct and indirect fractions), enhanced ALT, AST, and GGTP activities. Hypertriglyceridemia and increased serum ferritin levels were also present.
On the basis of typical clinical picture and laboratory criteria, a hemophagocytic lymphohistiocytosis (HLH) was suspected [1]. Morphological study of bone marrow aspirate has revealed specific forms of phagocytizing monocytes with engulfed mature red blood cells in their cytoplasm. The cerebrospinal fluid protein test was 0.6 g/l, lymphocytic cytosis – 32/3. Cytogenetic study of the bone marrow cells showed no abnormalities.
DNA sequencing of selected amplicons of known HLH-associate genes, i.e., STX11 (exons 1-2), STXBP2 (exons 1 to 19), PRF1 (exons 1 to 3) and adjacent intronic segments did not reveal any homozygous mutations. In STXBP2 gene (exon 18), the analysis has shown an ATA→GTA substitution in с.1609an (Ile537Val) in heterozygous state. This polymorphism is rather common in population (0.264). Hence, the data from Sanger DNA sequencing analysis showed a heterozygous state for STXBP2 and UNC13D gene mutations which indirectly supported the HLH diagnosis.
Due to suspected primary HLH and rapid clinical progression of disease, the HLH-94 protocol therapy with VP-16, dexamethasone, Cyclosporin A, and intratecal cytostatic therapy was started before receiving the genetic test results. According to the HLA typing data, the siblings were haploidentical.
Partial clinical response (apyrexia, lymph node size reduction, normalization of liver function) was achieved within 4 weeks after initiating the therapy, but the CMV reactivation associated with the disease progressed followed by fatal outcome at the age of 2 years 7 months.
Sibling 2
A boy from the 4th normal full-term pregnancy, without specific symptoms during postnatal period. At the age of 1.3 y.o., the child presented with fever which lasted for up to 8 days. Viral infection was suggested as a primary diagnosis, and symptomatic therapy was started. Positive dynamics was achieved, but the sub-febrile body temperature still persisted. Cytopenia was detected in routine blood counts (total leucocyte count – 7.0×109/l, absolute neutrophil count – 0.42×109/l, platelet count – 60×109/l). The serum ALT and AST levels exceeded five-fold the normal values. A differential diagnosis was made between infectious mononucleosis, viral hepatitis, and Yersinia infection.
The laboratory tests have shown pancytopenia, atypical mononuclear cells (blood); hypofibrinogenemia; hypertriglyceridemia; serum ferritin level within normal limits; the viral hepatitis markers (HAV, HBV, HCV) were negative. PCR tests for HSV type 6 (blood) were positive, as well as EBV DNA was found in saliva. Hepatomegaly was up to +2.0 cm, and splenomegaly, up to +3.0 cm.
Despite the symptomatic therapy the patient showed further cytopenia, febrile fever, lymphoproliferative syndrome without progression. Hemophagocytosis was not detectable in the bone marrow aspirate and cerebrospinal fluid.
Like as in sibling 1, a direct gene sequencing showed heterozygous mutation found in exon 31 of the UNC13D gene, i.e., single-nucleotide deletion (c.3082delC) and duplication (c.3037dupG) in the same exon, without reported associations with any inherited conditions.
The patient underwent specific therapy according to the HLH-94 protocol with achievement of a complete response by the end of initial treatment course. The prolonged therapy was continued over 9 weeks (dexamethasone pulse treatment at 10 mg/m2 for 3 days every second week and VP-16 infusions 150 mg/m2 every alternating second week with daily oral CSA), the clinical remission still persisted.
The patient and his sister were HLA-haploidentical. An unrelated donor was found in the International Donor Registry (9/10 compatibility for the main HLA loci, with only mismatch in locus C) and used for HSCT in this case.
A myeloablative reduced-toxicity conditioning with Treosulfan, Fludarabin and Thiotepa,was chosen for hematopoietic stem cell transplantation (HSCT). GvHD prophylaxis consisted of post-transplant cyclophosphamide, tacrolimus, and Cellsept. The patient has tolerated the conditioning regimen without significant associated toxicity. Engraftment was achieved on the D + 27 post-transplant. The follow-up period after allo-HSCT is one year. The hematopoietic graft functions satisfactorily with engraftment at the level of complete donor chimerism, there is no dependence on blood transfusions, with persisting remission of the disease.
Sibling 3
In view of the family history, the eldest child (sister) in the family was also observed. A mutation in the heterozygous state was also detected in the UNC13D gene by Sanger sequencing analysis. At the time of the survey, the girl was 12 years old. The physical development of the child is age appropriate. No signs of HLH have been shown so far, thus suggesting a sufficient phenotypic heterogeneity among the siblings observed.
Discussion
HLH is a severe clinical syndrome of the immune system, requiring early diagnosis, which allows combined immunosuppressive and chemotherapy to be started in time and may be followed by allo-HSCT, thus significantly increasing the chances for a favorable outcome of the disease [2].
The primary, genetically determined cases of HLH evolve as a result of genetically determined defect of the cellular cytotoxicity, and due to secondary hemophagocytic syndrome. The incidence of primary HLH is 1 in 50.000 newborns per year. Up to 70-80% of the primary HLH cases are diagnosed over the first year of life, whereas 20% manifest at the age of >3 years [3]. Secondary HLH may be associated with infectious, systemic autoimmune, malignant diseases and hereditary metabolic errors, depending on the distinct causal factors (Table 1).
Table 1. Causal and pathogenetic factors for secondary HLH [4, 5, 6]

Clinically, HLH is manifested by prolonged fever refractory to antimicrobial therapy; progressive cytopenia; lymphoproliferative, oedemas and hemorrhagic syndromes; hepatic dysfunction; symptoms of damage to the central nervous system (irritability, convulsions, meningeal symptoms, altered consciousness). Infections, mostly caused by herpesviruses, seem to be the main trigger leading to the HLH manifestations [7]. In the absence of specific therapy, the disease progresses rapidly and may end fatally. Sometimes, however, it may have a chronic, relapsed clinical course.
Appropriate clinical findings in HLH are non-specific, despite the severity of the manifestations. Therefore, it is possible to establish the diagnosis only on the basis of some characteristic laboratory tests. To establish the HLH diagnosis, at least 5 of 8 diagnostic criteria proposed by the International Society of Histiocytosis should be present in the patient, as follows: fever over 38.5 with a duration of at least 7 days, splenomegaly (>3.0 cm), bicytopenia (hemoglobin <90 g/l, platelet count <100×109/l, neutrophil count <1×109/l), hypertriglyceridemia (>2.0 mmol/L), and/or hypofibrinogenemia (<1.5 g/L), increased serum ferritin (more than 500 µg/L), decreased activity of peripheral NK cells, soluble CD25+ over 2500 U/L, evidence of hemophagocytosis in the bone marrow, lymphatic nodes, cerebrospinal fluid [1].
In young patients, HLH should be differentiated from sepsis, generalized perinatal infections, Wiscott-Aldrich syndrome, acute leukemia, juvenile myelomonocytic leukemia, histiocytosis originating from Langerhans cells, autoimmune lymphoproliferative syndrome. In older patients, hemophagocytic syndrome also needs to be differentiated from sepsis, hemoblastosis, viral hepatitis, viral encephalitis.
Early onset of the disease (1st year of life), family history (related marriage, sibling death in infancy), persistence of cellular cytotoxicity defects after achieving clinical/laboratory remission, recurrence of the disease, may be indicative for its hereditary nature. The final diagnosis of primary HLH is generally supported by identified mutations in one of candidate genes (PRF1, MUNC13D, STX11, STXBP) [6].
All the patients with suspected primary HLH should receive combined immunosuppressive chemotherapy to control systemic inflammation and prevent irreversible organ damage. Detection of pathogenic mutations is currently a necessary diagnostic criterion for predicting the time of onset and severity of clinical manifestations in primary forms of HLH, but these may be present and also occur in patients without signs of disease, as confirmed in one of the largest studies of HLH patients from Italy [8].
In the case of asymptomatic carriage of a potentially pathogenic mutation, the patient management strategies are determined by the nature of presumed defect. E.g., the patients with UNC13D mutation are kept under dynamic observation, while PRF1 and RAB27A mutations have an unfavorable prognosis, and the patients who underwent allo-HSCT prior to the development of clinical HLH symptoms have better survival rates [9].
Allogeneic transplantation of hematopoietic stem cells (allo-HSCT) is indicated in cases of proven primary HLH. Allo-HSCT is a preferable option in remission of the disease, but the absence of remission is not a contraindication for it. If planning a related allo-HSCT, it is necessary to make sure that the potential donor (sibling) who has no phenotypic features of the disorder doesn’t suffer from familial HLH.
References
- Henter JI, Horne A, Aricó M, Egeler RM, Filipovich AH, Imashuku S, Ladisch S, McClain K, Webb D, Winiarski J, Janka G. HLH-2004: diagnostic and therapeutic guidelines for hemophagocytic lymphohistiocytosis. Pediat Blood Cancer. 2007;48(2):124-131.
- Janka GE, Lehmberg K. Hemophagocytic syndromes – an update. Blood Rev. 2014: 2014;28(4):135-142.
- George MR. Hemophagocytic lymphohistiocytosis: review of etiologies and management, J Blood Med. 2014;5:69-86.
- Contino A, Trombatore G, Timeus F. Hemophagocytic lymphohistiocytosis in pediatric patients: a review. J Blood Disord Symptoms Treat. 2018; 2(1): 011.
- Maschan MA, Novichkova GA, Federal Clinical Guidelines for the Diagnosis and Treatment of Hemophagocytic Lymphohistiocytosis, 2014 (in Russian).
- Zhang K, Filipovich AH, Johnson J, Marsh RA, Villanueva J, Hemophagocytic lymphohistiocytosis, familial, Gene- Reviews [Internet]. Seattle (WA). 2006; Mar 22 [updated 2013 Jan 17].
- Brisse E, Wouters CH, Andrei G, Matthys P. How viruses contribute to the pathogenesis of hemophagocytic lymphohistiocytosis. Front Immunol. 2017 Sep 7;8:1102. doi: 10.3389/fimmu.2017.01102.
- Cetica V, Sieni E, Pende D, Danesino C, De Fusco C, Locatelli F, Micalizzi C, Putti MC, Biondi A, Fagioli F, Moretta L, Griffiths GM, Luzzatto L, Arico M. Genetic predisposition to hemophagocytic lymphohistiocytosis: Report on 500 patients from the Italian registry, J Allergy Clin Immunol. 2016;137(1):188-196.e4
- Lucchini G, Marsh R, Gilmour K, Worth A, Nademi Z, Rao A, Booth C, Amrolia P, Silva J, Chiesa R, Wynn R, Lehmberg K, Astigarraga I, Gungor T, Stary J, Moshous D, Ifversen M, Zinn D, Jordan M, Kumar A, Yasumi T, Vey P, Rao K. Treatment dilemmas in asymptomatic children with primary haemophagocytic lymphohistiocytosis. Blood, 2018;132(19):2088-2096.
Татьяна А. Быкова, Варвара Н. Овечкина, Анна А. Осипова, Андрей В. Козлов, Александр Л. Алянский, Елена В. Семенова, Людмила С. Зубаровская, Борис В. Афанасьев
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21778" ["VALUE"]=> array(2) { ["TEXT"]=> string(466) "<p>НИИ детской онкологии, гематологии и тнрансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(454) "НИИ детской онкологии, гематологии и тнрансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21779" ["VALUE"]=> array(2) { ["TEXT"]=> string(1660) "<p style="text-align: justify;">Семейный гемофагоцитарный лимфогистиоцитоз (гемофагоцитарный синдром) – редкое наследственное заболевание, в основе которого лежит нарушение регуляции иммунного ответа, приводящее к пролиферации и активации гистиоцитов, фагоцитозу клеток периферической крови. Своевременная диагностика и специфическая комбинированная иммуносупрессивная и химиотерапия с последующей алло-ТГСК значительно увеличивают вероятность благоприятного исхода болезни. Описывается случай семейного гемофагоцитарного лимфогистиоцитоза у трех сибсов, который был ассоциирован с мутацией <i>UNC13D</i> в гетерозиготной форме. Экспрессия клинической симптоматики у сибсов была различной как по характеру течения, так и по прогнозу заболевания. </p> <h2>Ключевые слова</h2> <p style="text-align: justify;">Семейный гемофагоцитарный лимфогистиоцитоз, гемофагоцитарный синдром, алло-ТГСК.</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1592) "Семейный гемофагоцитарный лимфогистиоцитоз (гемофагоцитарный синдром) – редкое наследственное заболевание, в основе которого лежит нарушение регуляции иммунного ответа, приводящее к пролиферации и активации гистиоцитов, фагоцитозу клеток периферической крови. Своевременная диагностика и специфическая комбинированная иммуносупрессивная и химиотерапия с последующей алло-ТГСК значительно увеличивают вероятность благоприятного исхода болезни. Описывается случай семейного гемофагоцитарного лимфогистиоцитоза у трех сибсов, который был ассоциирован с мутацией UNC13D в гетерозиготной форме. Экспрессия клинической симптоматики у сибсов была различной как по характеру течения, так и по прогнозу заболевания.
Ключевые слова
Семейный гемофагоцитарный лимфогистиоцитоз, гемофагоцитарный синдром, алло-ТГСК.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21780" ["VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-54-57" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-54-57" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21791" ["VALUE"]=> array(2) { ["TEXT"]=> string(181) "<p>Tatiana A. Bykova, Varvara N. Ovechkina, Anna A. Osipova, Andrey V. Kozlov, Alexander L. Alyanskiy, Elena V. Semenova, Ludmila S. Zubarovskaya, Boris V. Afanasyev</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(169) "Tatiana A. Bykova, Varvara N. Ovechkina, Anna A. Osipova, Andrey V. Kozlov, Alexander L. Alyanskiy, Elena V. Semenova, Ludmila S. Zubarovskaya, Boris V. Afanasyev
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21792" ["VALUE"]=> array(2) { ["TEXT"]=> string(259) "<p>R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation; Department of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I.Pavlov Medical University, St. Petersburg, Russia</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(247) "R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation; Department of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I.Pavlov Medical University, St. Petersburg, Russia
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21793" ["VALUE"]=> array(2) { ["TEXT"]=> string(908) "<p style="text-align: justify;">Familial hemophagocytic lymphohistiocytosis (hemophagocytic syndrome) is a rare hereditary disease, characterized by dysregulation of the immune response, leading to the proliferation and activation of histiocytes, phagocytosis of peripheral blood cells. Timely diagnostics, specific combined immunosuppressive therapy and chemotherapy followed by allo-HSCT significantly increase the chances for a favorable outcome. We are presenting a case of family hemophagocytic lymphohistiocytosis associated with <i>UNC13D</i> mutation which was found in three siblings who exhibited quite different course of the disease and clinical prognosis. </p> <h2>Keywords</h2> <p style="text-align: justify;">Familial hemophagocytic lymphohistiocytosis, hemophagocytic syndrome, hematopoietic stem cell transplantation.</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(840) "Familial hemophagocytic lymphohistiocytosis (hemophagocytic syndrome) is a rare hereditary disease, characterized by dysregulation of the immune response, leading to the proliferation and activation of histiocytes, phagocytosis of peripheral blood cells. Timely diagnostics, specific combined immunosuppressive therapy and chemotherapy followed by allo-HSCT significantly increase the chances for a favorable outcome. We are presenting a case of family hemophagocytic lymphohistiocytosis associated with UNC13D mutation which was found in three siblings who exhibited quite different course of the disease and clinical prognosis.
Keywords
Familial hemophagocytic lymphohistiocytosis, hemophagocytic syndrome, hematopoietic stem cell transplantation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21781" ["VALUE"]=> string(62) "A clinical case of familial hemophagocytic lymphohistiocytosis" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(62) "A clinical case of familial hemophagocytic lymphohistiocytosis" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21782" ["VALUE"]=> string(4) "1607" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1607" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21794" ["VALUE"]=> string(4) "1608" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1608" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(12) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21791" ["VALUE"]=> array(2) { ["TEXT"]=> string(181) "<p>Tatiana A. Bykova, Varvara N. Ovechkina, Anna A. Osipova, Andrey V. Kozlov, Alexander L. Alyanskiy, Elena V. Semenova, Ludmila S. Zubarovskaya, Boris V. Afanasyev</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(169) "Tatiana A. Bykova, Varvara N. Ovechkina, Anna A. Osipova, Andrey V. Kozlov, Alexander L. Alyanskiy, Elena V. Semenova, Ludmila S. Zubarovskaya, Boris V. Afanasyev
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(169) "Tatiana A. Bykova, Varvara N. Ovechkina, Anna A. Osipova, Andrey V. Kozlov, Alexander L. Alyanskiy, Elena V. Semenova, Ludmila S. Zubarovskaya, Boris V. Afanasyev
" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21793" ["VALUE"]=> array(2) { ["TEXT"]=> string(908) "<p style="text-align: justify;">Familial hemophagocytic lymphohistiocytosis (hemophagocytic syndrome) is a rare hereditary disease, characterized by dysregulation of the immune response, leading to the proliferation and activation of histiocytes, phagocytosis of peripheral blood cells. Timely diagnostics, specific combined immunosuppressive therapy and chemotherapy followed by allo-HSCT significantly increase the chances for a favorable outcome. We are presenting a case of family hemophagocytic lymphohistiocytosis associated with <i>UNC13D</i> mutation which was found in three siblings who exhibited quite different course of the disease and clinical prognosis. </p> <h2>Keywords</h2> <p style="text-align: justify;">Familial hemophagocytic lymphohistiocytosis, hemophagocytic syndrome, hematopoietic stem cell transplantation.</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(840) "Familial hemophagocytic lymphohistiocytosis (hemophagocytic syndrome) is a rare hereditary disease, characterized by dysregulation of the immune response, leading to the proliferation and activation of histiocytes, phagocytosis of peripheral blood cells. Timely diagnostics, specific combined immunosuppressive therapy and chemotherapy followed by allo-HSCT significantly increase the chances for a favorable outcome. We are presenting a case of family hemophagocytic lymphohistiocytosis associated with UNC13D mutation which was found in three siblings who exhibited quite different course of the disease and clinical prognosis.
Keywords
Familial hemophagocytic lymphohistiocytosis, hemophagocytic syndrome, hematopoietic stem cell transplantation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(840) "Familial hemophagocytic lymphohistiocytosis (hemophagocytic syndrome) is a rare hereditary disease, characterized by dysregulation of the immune response, leading to the proliferation and activation of histiocytes, phagocytosis of peripheral blood cells. Timely diagnostics, specific combined immunosuppressive therapy and chemotherapy followed by allo-HSCT significantly increase the chances for a favorable outcome. We are presenting a case of family hemophagocytic lymphohistiocytosis associated with UNC13D mutation which was found in three siblings who exhibited quite different course of the disease and clinical prognosis.
Keywords
Familial hemophagocytic lymphohistiocytosis, hemophagocytic syndrome, hematopoietic stem cell transplantation.
" } ["DOI"]=> array(37) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21780" ["VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-54-57" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-54-57" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-54-57" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21781" ["VALUE"]=> string(62) "A clinical case of familial hemophagocytic lymphohistiocytosis" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(62) "A clinical case of familial hemophagocytic lymphohistiocytosis" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(62) "A clinical case of familial hemophagocytic lymphohistiocytosis" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21792" ["VALUE"]=> array(2) { ["TEXT"]=> string(259) "<p>R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation; Department of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I.Pavlov Medical University, St. Petersburg, Russia</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(247) "R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation; Department of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I.Pavlov Medical University, St. Petersburg, Russia
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(247) "R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation; Department of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I.Pavlov Medical University, St. Petersburg, Russia
" } ["AUTHORS"]=> array(38) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> array(8) { [0]=> string(5) "21803" [1]=> string(5) "21804" [2]=> string(5) "21805" [3]=> string(5) "21806" [4]=> string(5) "21807" [5]=> string(5) "21808" [6]=> string(5) "21809" [7]=> string(5) "21810" } ["VALUE"]=> array(8) { [0]=> string(4) "1642" [1]=> string(3) "303" [2]=> string(4) "1643" [3]=> string(3) "133" [4]=> string(3) "498" [5]=> string(3) "502" [6]=> string(2) "42" [7]=> string(2) "34" } ["DESCRIPTION"]=> array(8) { [0]=> string(0) "" [1]=> string(0) "" [2]=> string(0) "" [3]=> string(0) "" [4]=> string(0) "" [5]=> string(0) "" [6]=> string(0) "" [7]=> string(0) "" } ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(8) { [0]=> string(4) "1642" [1]=> string(3) "303" [2]=> string(4) "1643" [3]=> string(3) "133" [4]=> string(3) "498" [5]=> string(3) "502" [6]=> string(2) "42" [7]=> string(2) "34" } ["~DESCRIPTION"]=> array(8) { [0]=> string(0) "" [1]=> string(0) "" [2]=> string(0) "" [3]=> string(0) "" [4]=> string(0) "" [5]=> string(0) "" [6]=> string(0) "" [7]=> string(0) "" } ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> array(8) { [0]=> string(61) "Tatiana A. Bykova" [1]=> string(63) "Varvara N. Ovechkina" [2]=> string(59) "Anna A. Osipova" [3]=> string(59) "Andrey V. Kozlov" [4]=> string(65) "Alexander L. Alyanskiy" [5]=> string(60) "Elena V. Semenova" [6]=> string(65) "Ludmila S. Zubarovskaya" [7]=> string(60) "Boris V. Afanasyev" } ["LINK_ELEMENT_VALUE"]=> bool(false) } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21777" ["VALUE"]=> array(2) { ["TEXT"]=> string(300) "<p>Татьяна А. Быкова, Варвара Н. Овечкина, Анна А. Осипова, Андрей В. Козлов, Александр Л. Алянский, Елена В. Семенова, Людмила С. Зубаровская, Борис В. Афанасьев</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(288) "Татьяна А. Быкова, Варвара Н. Овечкина, Анна А. Осипова, Андрей В. Козлов, Александр Л. Алянский, Елена В. Семенова, Людмила С. Зубаровская, Борис В. Афанасьев
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(288) "Татьяна А. Быкова, Варвара Н. Овечкина, Анна А. Осипова, Андрей В. Козлов, Александр Л. Алянский, Елена В. Семенова, Людмила С. Зубаровская, Борис В. Афанасьев
" } ["SUBMITTED"]=> array(37) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21766" ["VALUE"]=> string(10) "08.04.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "08.04.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "08.04.2019" } ["ACCEPTED"]=> array(37) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21767" ["VALUE"]=> string(10) "26.04.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "26.04.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "26.04.2019" } ["CONTACT"]=> array(38) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21768" ["VALUE"]=> string(4) "1642" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1642" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(61) "Tatiana A. Bykova" ["LINK_ELEMENT_VALUE"]=> bool(false) } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21779" ["VALUE"]=> array(2) { ["TEXT"]=> string(1660) "<p style="text-align: justify;">Семейный гемофагоцитарный лимфогистиоцитоз (гемофагоцитарный синдром) – редкое наследственное заболевание, в основе которого лежит нарушение регуляции иммунного ответа, приводящее к пролиферации и активации гистиоцитов, фагоцитозу клеток периферической крови. Своевременная диагностика и специфическая комбинированная иммуносупрессивная и химиотерапия с последующей алло-ТГСК значительно увеличивают вероятность благоприятного исхода болезни. Описывается случай семейного гемофагоцитарного лимфогистиоцитоза у трех сибсов, который был ассоциирован с мутацией <i>UNC13D</i> в гетерозиготной форме. Экспрессия клинической симптоматики у сибсов была различной как по характеру течения, так и по прогнозу заболевания. </p> <h2>Ключевые слова</h2> <p style="text-align: justify;">Семейный гемофагоцитарный лимфогистиоцитоз, гемофагоцитарный синдром, алло-ТГСК.</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1592) "Семейный гемофагоцитарный лимфогистиоцитоз (гемофагоцитарный синдром) – редкое наследственное заболевание, в основе которого лежит нарушение регуляции иммунного ответа, приводящее к пролиферации и активации гистиоцитов, фагоцитозу клеток периферической крови. Своевременная диагностика и специфическая комбинированная иммуносупрессивная и химиотерапия с последующей алло-ТГСК значительно увеличивают вероятность благоприятного исхода болезни. Описывается случай семейного гемофагоцитарного лимфогистиоцитоза у трех сибсов, который был ассоциирован с мутацией UNC13D в гетерозиготной форме. Экспрессия клинической симптоматики у сибсов была различной как по характеру течения, так и по прогнозу заболевания.
Ключевые слова
Семейный гемофагоцитарный лимфогистиоцитоз, гемофагоцитарный синдром, алло-ТГСК.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(1592) "Семейный гемофагоцитарный лимфогистиоцитоз (гемофагоцитарный синдром) – редкое наследственное заболевание, в основе которого лежит нарушение регуляции иммунного ответа, приводящее к пролиферации и активации гистиоцитов, фагоцитозу клеток периферической крови. Своевременная диагностика и специфическая комбинированная иммуносупрессивная и химиотерапия с последующей алло-ТГСК значительно увеличивают вероятность благоприятного исхода болезни. Описывается случай семейного гемофагоцитарного лимфогистиоцитоза у трех сибсов, который был ассоциирован с мутацией UNC13D в гетерозиготной форме. Экспрессия клинической симптоматики у сибсов была различной как по характеру течения, так и по прогнозу заболевания.
Ключевые слова
Семейный гемофагоцитарный лимфогистиоцитоз, гемофагоцитарный синдром, алло-ТГСК.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21778" ["VALUE"]=> array(2) { ["TEXT"]=> string(466) "<p>НИИ детской онкологии, гематологии и тнрансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(454) "НИИ детской онкологии, гематологии и тнрансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(454) "НИИ детской онкологии, гематологии и тнрансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
" } } } [8]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "123" ["~IBLOCK_SECTION_ID"]=> string(3) "123" ["ID"]=> string(4) "1649" ["~ID"]=> string(4) "1649" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(212) "Митотическая активность клеток грудного протока кроликов связана с возрастом и абсолютным количеством лимфоцитов" ["~NAME"]=> string(212) "Митотическая активность клеток грудного протока кроликов связана с возрастом и абсолютным количеством лимфоцитов" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "03.06.2019 13:47:00" ["~TIMESTAMP_X"]=> string(19) "03.06.2019 13:47:00" ["DETAIL_PAGE_URL"]=> string(158) "/ru/archive/tom-8-nomer-1/eksperimentalnye-issledovaniya/mitoticheskaya-aktivnost-kletok-grudnogo-protoka-krolikov-svyazana-s-vozrastom-i-absolyutnym-koliche/" ["~DETAIL_PAGE_URL"]=> string(158) "/ru/archive/tom-8-nomer-1/eksperimentalnye-issledovaniya/mitoticheskaya-aktivnost-kletok-grudnogo-protoka-krolikov-svyazana-s-vozrastom-i-absolyutnym-koliche/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(29859) "Introduction
Proliferation of normal immune cells is a key process in immunogenesis, especially in immature organism. Multiplication and differentiation of immature and naive lymphoid cells occurs upon their contacts with foreign and own antigens, respectively, in thymus and Peyer patches as primary lymphoid organs. Transportation of lymphoid cells and their precursor proceeds via lymphatic system. E.g., both mature and immature immune cells migrating from intestines, mesenterial lymph nodes and other peripheral lymph organs are collected into the common lymph thoracic duct (TD) [1]. Further trafficking via thoracic duct to peripheral blood, and antigen-dependent selection of mature T- and B cell populations is followed by their maturation in secondary lymphoid organs and local lymphatic tissue [2, 3]. Immature lymphoid cells after entering thoracic duct, may prepare for cell division by forming a "mitotic spindle" made of microtubules and many associated proteins. However, distinct mechanisms of mitosis regulation are still unknown [4, 5]. A proportion of thoracic duct cells is comprised by the nonlymphoid monocyte-like cells [6]. Hence, a sufficient immune population obtained from lymph may undergo expansion. This mitotic activity could be dependent on the stage of immunogenesis. Maturation of immune system in mammals proceeds just after birth, upon initial antigenic contacts.
Numerous workers focused on age-dependent changes of various crucial immune structures and appropriate regulators of cell proliferation and protection [7-11]. It should be taken into account that different antigen-presenting cells (APC), e.g., T cells, monocytes etc., may also migrate from vascular flow to peripheral and TD lymph [12].
Using bone marrow transplantation approach, homing experiments, and parabiotic mice, we have found that the hematopoietic stem and progenitor cells (HSPC) originate from the marrow and permanently migrate to different extramedullary tissues, where they reside for several days until entering the draining lymphatics, then returning to the bloodstream. The migratory pathways of HSPCs differ from those of lymphocytes. Therefore, the circulating HSPCs reach their target hematopoietic tissues, they do not require secondary lymphoid organs to recirculate [13].
There are only scarce data on mitotic activity of lymphoid cells in peripheral and central lymph of intact mammals. E.g., we have earlier shown sufficient mitotic activity of thoracic lymph duct cells in young rabbits [14, 15], being a further step to the recent concept of a "lymph humor/proliferation factor" [16]. Therefore, it is necessary to study age-related mitoses in TDL. The aim of the research was to assess correlations between rabbit MTDL, rabbit’s age and LTDL. We emphasize that the features of LTDL morphology and their function are of particular interest, both in the aspect of postnatal development, and also in LTDL role for repopulation/reconstitution of lymphoid tissue and lymphoid organs in physiological and pathological states (in oncological diseases in particular). In particular, the thoracic duct lymphoid population could be important for recovery of cellular and humoral immunity after intensive cytostatic treatment, e.g., radiation therapy, as initially shown by Strober [17].
A significant proportion of white blood cells consisting of lymphocytes by 98% is permanently passing via the thoracic duct to bloodstream. Hence, any details on their cytokinetics may have implications to the production rate, circulation and fate of the lymphocytes in immune response [18]. The murine thoracic duct lymph contains hematopoietic stem and progenitor cells (HSPCs) that possess short- and long-term multi-lineage reconstitution capacity. The TD-derived HSPCs originate from bone marrow (BM), enter the blood, and move to different peripheral organs, where they reside for, at least, 36 hr before entering draining lymphatics, then returning to the bloodstream and, eventually, to bone marrow (BM). The migrating HSPCs proliferate within extramedullary tissues and give rise to tissue-resident myeloid cells, preferentially dendritic cells. HSPCs may invade peripheral organs and foster the local production of tissue-resident innate immune cells under both steady-state conditions and in response to inflammatory signals [19].
The aim of our study was to assess correlations between rabbit mitotic thoracic duct cells, rabbit’s age, and numbers of lymphocytes in thoracic duct.
Materials and methods
Experimental animals
The study was carried out in 29 male Chinchilla rabbits of different ages (1.5 to 36 weeks), weighing, respectively, 120 to 1800 g (Table 1). All the animals were kept during the experiment at the animal facility of B. Atchabarov Research Institute of Fundamental and Practical Medicine (Almaty, Kazakhstan), getting standard feeding and water ad libitum.
Table 1. Distribution of rabbits into different age groups and their parameters

Ethical Approval
We understand the ethical principles under which the journal operates and our work complies with the animal ethics checklist as outlined in The ABC of Animal Experiments 2010 FELASA Accredited Scientists' Competence (Category C) course at Viikki Campus of the University of Helsinki www.helsinki.fi/weboodi and The Journal of Physiology and Experimental Physiology by D. Grundy, The Journal of Physiology, 593: 2547-2549, doi: 10.1113/JP270818.5.
Lymph harvesting
The invasive procedures were made following intravenous anaesthesia with calypsol-ketamine and lystenonum at the doses of 50 mg and 10 mg/kg body weight, respectively. Infiltration of 1% novocaine solution was used as local anesthesia. Lymph was drawn from thoracic duct. Intubation of trachea and artificial lung ventilation were made in the SIMV mode. A rabbit was fixed on the back by its extremities, and intravenous anesthesia was made. Hair was removed from the frontside of abdomen followed by local anesthesia of abdominal wall. Thereafter, a midline laparotomy was performed. The longitudinal incision line was made along the projection of left kidney. The surgical wound was widened to the left, and the intestinal loops were moved medially. The left kidney with its vessels was located on the back side of the abdominal cavity. Novocaine anesthesia of perinephric cellular tissue was made. Left kidney and its vessels were released from fixation beginning from the lateral edge of the kidney up to the origin of the A. renalis and removed medially. The thoracic duct cistern was found dorsally from abdominal aorta according to the beginning of the A. renalis (Fig. 1). The cisternal lymph was obtained by punching with original glass micropipettes (Russian patent No 1465076, 1987) [20, 21]. The lymph samples (0.01 mL) were transferred to microscopic slides. The cell smears were dried and stained according to Giemsa technique. The smears were studied by LEICA DM1000 light microscope at X400, or X1000 magnification with oil immersion. The number of mitoses per 100 cells was calculated in rabbit lymph by a routine method. Absolute number of leukocytes was calculated manually in the Bürker chamber. Their numbers were expressed as 1×109 per 1000 mL.

Figure 1. A surgical access to the thoracic duct cistern in rabbit. LK, left kidney; KV, left kidney vein; TDC, thoracic duct cistern (the scale bar is 1 cm)
Statistics
We calculated mean values, and standard deviation (SD) for the distinct groups, variance values, using Student factor (freedom degree is: n-1). The obtained results were statistically calculated using confidence intervals of mean values for the groups compared. The error of average values from arithmetical average did not exceed 5%. The differences were considered statistically significant if two-tailed P values of <0.05 (*) and P<0.001 (**). Moreover, we have calculated statistical relationships between mitotic numbers and rabbit’s age, as well as between the mitotic numbers and lymphocyte numbers, using Pearson correlation quotient. All the data were expressed as the mean ± SEM. The data were analyzed by Microsoft Office Excel 2007 software.
Results
We have revealed a number of cells at various stages of mitosis when studying thoracic lymph smears from immature rabbits (Fig. 2).

Figure 2. Mitotic events observed in smears of TD cells from immature rabbits (a, b, c, d) , stained by Giemsa, photomicrograph at 1000x magnification: (a), prophase; (b), metaphase; (c); early anaphase; (d), late anaphase; (e), telophase
The data are expressed as mean ± SEM. The differences between the mitotic cell ratios for various age groups and between TD cell numbers in these groups were considered statistically significant, if two-tailed P<0.05 (*) and P<0.001 (**).
The minimal numbers of mitotic cells were observed in thoracic duct populations of mature rabbits at the age of 36 weeks.
A maximal percentage of mitoses (23.0 ± 0.14, P=0.02, n=6) was registered in the animals 1.5 weeks of age and remained high (19.0 ± 0.12, P=0.01, n=5) at the age of 2.5 weeks (body mass 240 ± 20 g). At later terms, the mitotic index progressively decreased two-fold by 4.5 weeks of age (11.0 ± 0.14, P<0.05, n=4), and even more at 13.5 weeks (6.3 ± 0.08, P=0.04), when compared to initial values of 1.5 weeks (Fig. 3). With advancing age, the numbers of mitotic cells dropped down to 4.0 ± 0.04 (P=0.03, n=4) by 27 weeks, reaching a minimum of 1.0 ± 0.01 (P=0.02, n=6) by 36 weeks of age. The mitoses were virtually absent at the age of 36 weeks. Most TD cells counted in the lymph smears of mature rabbits (by 36 weeks) had the interphase morphology.

Figure 3. Changes of mitotic cell numbers in thoracic duct (MTDL) and total number of thoracic duct cells (LTDL) in rabbits aged from 1.5 to 36 weeks. Differences were considered statistically significant if two-tailed P<0.05 (*), P<0.001 (**)
By the contrast, total numbers of thoracic duct lymphocytes increased within 36 weeks (2.8 ± 0.03×109, P=0.04, n=6; 3.3 ± 0.05×109; P=0.05, n=5; 4.0×109 ± 0.04, p=0.02, n=4; 4.7 ± 0.04×109, p=0.03, n=4; 5.4 ± 0.03×109, P=0.02, n=4; 5.9 ± 0.05×109, P=0.03, n=6 (at 1.5, 2.5, 4.5, 13.5, 27, 36 weeks, respectively). The total number of thoracic duct cells significantly increased in 4.5, 13.5 and 36 weeks old rabbits in comparison with the total TD cell number in 1.5 weeks old rabbits. A strong negative correlation was found between mitotic activity of thoracic duct cells and age, like as between total TD cell counts and age (R2=0.7, R2=0.96 and R2=0.8 respectively) of immature rabbits at the age range of 1.5 weeks and 36 weeks (Fig. 4, 5, and 6, respectively).

Figure 4. Pearson’s correlation coefficient (very high negative correlation, R2=0.7) between the mitotic thoracic duct cells (MTDL) (1x109) and age of rabbits (weeks)
A very high negative correlation (R2=0.96) between the mitotic activity and total cell counts detected in thoracic duct lymph (Fig. 5). By contrast, a significant positive correlation (R2=0.8), between the TD cell numbers and age was revealed (Fig. 6).

Discussion
In the present study, we have for the first time demonstrated very high levels of proliferating TD cells at early maturation terms (1.5-2.5 weeks), followed by a pronounced age-dependent decrease of mitotic activity in these cell populations, as well as their correlation with increasing absolute TD cell counts in the intact immature rabbits up to 13.5 weeks of age.
Mitotic activity of lymphoid cells is the key index of physiological immune response and its maturation with time. Numerous researchers focused on age changes of various crucial immune structures and some regulators of proliferation and protection. However, most of these studies concerned the aspects of immune response in aging animals [7, 9, 10]. Meanwhile, we would like to address maturation of immune system in the very young organism, e.g., rabbit pups since the age of 10-20 days.
Our study is a part of the recent concept aiming for detection of a lymph-derived humoral factor in thoracic duct of rabbits [16]. Our current knowledge of changing TD cell numbers in rabbits allows to select the animals with optimal level or combination of cytokines or other bioactive factors in thoracic lymph duct which may have a huge impact upon the mitotic activity. A search for optimized adjuvant protocols to achieve a regulated cells proliferation is important [22].
The results of this study show that the numbers of mitotic TD cells correlate with age and LTDL of intact immature rabbits. The maximal mitotic ratio and minimal total numbers of TD cells were revealed in immature newborn rabbits, thus suggesting a huge immune potential developing in the immature rabbits.
There is also a problem of an approach to sampling TDL. However, despite numerous approaches to sampling thoracic duct lymph, researchers still propose novel techniques to this purpose. Since 1987, we have introduced an original access for sampling the thoracic duct lymph which works with no failure. Moreover, the ongoing studies in thoracic duct cannulation and lymphatic fluid collection in animals [23] and humans [24] are performed over last years, thus allowing to take lymph samples and to perform lymph drainage, e.g., for in vivo T cell exhaustion in human patients [25].
In conclusion, our current findings show for the first time that a correlation between the mitotic activity, absolute TD cell concentrations and rabbit’s age. A very strong correlation between the mitotic cell ratio, total TD cell counts and immature rabbit’s age (between 1.5 weeks-13.5 weeks) was detected. In our study the mitotic TD cell activity was compared between the intact immature male rabbits (aged 1.5-2.5-4.5 weeks), and adult animals (aged 13.5-36 weeks). The mentioned results allow us to select the age of immature rabbits with maximal numbers of mitotic cells and to perform more exact search for the suggested lymph proliferation factor. The data suggest that the age-related changes of mitotic activity suggest distinct effects of cytokines and other bioactive factors in TD cell populations, e.g., a hypothetical lymphopoietic factor revealed several decades ago [16].
We have found an evident increase in TD cell numbers in the 4.5 week-old rabbits which may result from increased lymphopoiesis at this age confirmed by high mitotic activity of TD cells. A correlation between mitotic activity, TD cell numbers and rabbit age can be used as a new experimental model applicable in different fields of biology and pharmacology. Studies in cytokines and hormone combinations as well as antigenic environment causing high cell proliferation in younger age groups of animals are worth of further studies.
The features of TD lymphocyte morphology and their function are of particular interest not only in the age aspect of postnatal development, but also in the repopulation/reconstitution of lymphoid tissue and lymphoid organs in physiological and pathological conditions, especially, in therapy of malignancies, including bone marrow transplantation techniques.
It has been known for many years, large numbers of white cells, 98 per cent of them lymphocytes, are constantly passing into the blood stream from the thoracic duct. The findings may have implications as to the generation, circulation and fate of the lymphocytes passing the thoracic duct [18].
Moreover, the thoracic duct (TD) lymph contains HSPCs (hematopoietic stem and progenitor cells) that possess short- and long-term multiline age reconstitution capacity. In murine model, the TD-derived HSPCs originate in the BM, enter the blood, and traffic to multiple peripheral organs, where they reside for at least 36 hr before entering draining lymphatics to return to the blood and, eventually, the BM (bone marrow). Migratory HSPCs proliferate within extramedullary tissues and give rise to tissue-resident myeloid cells, preferentially dendritic cells. Thus, HSPCs can survey peripheral organs and can foster the local production of tissue-resident innate immune cells under both steady-state conditions and in response to inflammatory signals [19]. Therefore, we may suggest that, at least, a fraction of the mitotic cells found in TD of newborn rabbits may contain numerous hematopoietic precursors at different steps of differentiation which then migrate to their homing areas.
Thoracic duct (TD) provides a sufficient lymphocyte traffic: 0.65 ± 0.21×10⁶ lymphocytes/min (the baseline lymphocyte flux) to 6.10 ± 0.99×10⁶ lymphocytes/min (after lymphatic pump techniques) [26], hematopoietic and progenitor cells (HSPCs) [19].
TD lymphocytes migrate into lymph nodes [27, 28, 29, 30, 31, 32] and spleen [27, 28, 29, 31, 32], bone marrow [19], enter the thymus gland [28, 29].
It is known for decades that, at least in adult mammals, large amounts of immune cells, mostly T- and B lymphocytes, with a small portion of monocytes and dendritic cell precursors are continuously trafficking from the gut tissues and lymph nodes to the bloodstream via thoracic duct to the bloodstream [18]. Thus, our findings on the TD traffic of immature cells may have implications for production, circulation and fate of the lymphocytes. Later, our experimental techniques were confirmed by other workers [23].
Thoracic duct lymphocytes, like as bone marrow cells from normal rats are efficient in restoring the spleen marginal-zone cellularity in cyclophosphamide-treated rats, thus being able for renewal and proliferaiton. Thoracic duct cells passaged through an irradiated intermediate host and collected from that host's thoracic duct were also efficient at achieving marginal-zone reconstitution [30]. Moreover, many years ago, a special population of lymphokine- activated killer (LAK) cells and their precursors was found to be distributed in the thymus, bone marrow, spleen, lymph node, and thoracic duct [33]. The LAK cells are now considered a promising tool for immunotherapy of different malignancies, including leukemia and lymphoma.
Of interest are some data obtained in experiments with calf fetuses [34]. The lymphoid cell contents in thoracic duct increased ca. 50-fold from day 120 to the pre-birth levels, in parallel to expanded total pool of circulating lymphocytes. A proportion of lymphocytes bearing detectable surface immunoglobulin in fetal lymph ranged from 2.1% to 8.7%. The recirculating lymphocytes from fetal calves produced strong proliferative responses when stimulated by T-cell mitogens but responded poorly to B-cell mitogens. Fetal lymphocytes also responded to stimulation by allogeneic cells and stimulated other cells to proliferate during mixed lymphocyte culture.
Interestingy, the mitotic cells in TD stream were rarely detected young adult rabbits, thus being in accordance with the data reported in other adult animal models [23, 35]. Hence, our work has highlighted an intensive traffic of immature cell via thoracic duct at the during first weeks of life. This observation should be confirmed in other mammalian species. In general, the thoracic duct cells may be considered a significant intrinsic reserve of immune and hematopoietic cells in cytopenias induced by cytostatic treatment, e.g., during experimental bone marrow transplantation in the infants.
Conclusion
Proliferative activity of cells and total cell concentrations in thoracic lymph duct (TD) were studied in our experimental work. This study concerned mitotic activity in TD cells of newborn, very young to mature rabbits. Extremely high mitotic indexes were revealed in the 10-20 days old infant animals, thus showing high-level trafficking of immature lymphoid, and, probably, less differentiated hematopoietic cells which require further phenotypic characterization. This proliferating cell fraction may be also induced by some lymphopoietic factor(s) present in thoracic lymph. With body growth, the mitotic activity of TD cells rapidly dropped to minimal levels, along with increased cell concentrations in thoracic duct. These findings may be important in studying production, circulation and fate of TD lymphocytes in physiological and pathological states, in treatment of malignant diseases and, especially, in bone marrow transplantation based in many aspects on cellular immune therapy. Functioning of lymph ducts and differences in cellular content during infancy and at very young age may be useful for further advances in pediatric oncohematology.
Competing interests
No conflicts of interest, financial or otherwise by the authors.
Acknowledgement
This work was supported by B. Atchabarov Research Institute of Fundamental and Practical Medicine. We wish also to express our sincere thanks to Galina Igorevna Kuznetsova for help in translating the article into English.
References
- Fanous MYZ, Phillips AJ, Windsor JA. Mesenteric lymph: the bridge to future management of critical illness. J Pancreas. 2007; 8(4):374-399.
- Sato J, Chida K, Suda T, Sato A, Nakamura H. Migratory patterns of thoracic duct lymphocytes into bronchus- associated lymphoid tissue of immunized rats. Lung. 2000; 178:295-308.
- Ganusov VV, Auerbach J. Mathematical modeling reveals kinetics of lymphocyte recirculation in the whole organism. PLoS Comput Biol. 2014; 10(5): e1003586.
- McIntosh JR. Mitosis. Cold Spring Harb Perspect Biol. 2016; DOI: 10.1101/cshperspect.a023218.
- Kim HS, Fernandes G, Lee CW. Protein phosphatases involved in regulating mitosis: facts and hypotheses. Mol Cells. 2016;39(9):654-662.
- Pugh CW, McPherson GG, Steer HW. Characterization of nonlymphoid cells derived from rat peripheral lymph. J Exp Med. 1983; 157:1758-1779.
- Agrawal S, Ganguly S, Tran A, Sundaram P, Agrawal A. Retinoic acid treated human dendritic cells induce T regulatory cells via the expression of CD141 and GARP which is impaired with age. Aging (NY). 2016;8(6):1223-1235.
- Keyes BE, Liu S, Asare A, Nailk S, Levorse J, Polak L, Lu CP, Nikolova M, Pasolli HA, Fuchs E. Impaired epidermal to dendritic T cell signaling slows wound repair in aged skin. Cell. 2016;167(5):1323-1338.e14.
- Xie J, Zhang J, Wu H, Tang X, Liu J, Cheng G, Li P. The influences of age on T lymphocyte subsets in C57BL/6 mice. Saudi J Biol Sci. 2017;24(1):108-113.
- Zhang Q, Yang K, Yangyang P, He J,Yu S, Cui Y. Age-related changes in the morphology and protein expression of the thymus of healthy yaks (Bos grunniens). Am J Vet Res. 2016; 77(6):567-574.
- Montgomery RR. Age-related alterations in immune responses to West Nile virus infection. Clin Exp Immunol. 2017;187(1):26-34.
- Hunter MC, Teijeira A, Halin C. T cell trafficking through lymphatic vessels. Front Immunol. 2016;7:613. doi: 10.3389/fimmu.2016.00613.
- Massberg S, von Andrian UH. Novel trafficking routes for hematopoietic stem and progenitor cell. Ann N Y Acad Sci. 2009;1176:87-93.
- Kuznetsov AV. Mitoses in thoracic duct lymph of rabbits. Scientia Agriculturae. 2015; DOI:10.15192/PSCP.SA.2015.9.2.8992.
- Kuznetsov AV. Dendritic cells mitoses in thoracic duct lymph of immature rabbits. Transylvanian Review. 2017; 24:3678-3681.
- Yamashita A, Fukumoto T, Miyamoto M. Studies on lymph humoral factor. Biological characteristics of a lymphocytopoietic factor in rat thoracic duct lymph. Immunology. 1976;32: 651-656.
- Strober S. Initiation of antibody responses by different classes of lymphocytes. III. Differences in the proliferative rates of thoracic duct lymphocytes involved in primary and secondary responses. J Immunol. 1970; 105(3):734-737.
- Matsuno K, Ueta H, Shu Z, Xue-Dong X, Sawanobori Y, Kitazawa Y, Bin Y, Yamashita M, Shi C. The microstructure of secondary lymphoid organs that support immune cell trafficking. Arch Histol Cytol. 2010;73(1):1-21.
- Massberg S, Schaerli P, Knezevic-Maramica I, Köllnberger M, Tubo N, Moseman EA, Huff IV, Junt T, Wagers AJ, Mazo IB, von Andrian UH. Immunosurveillance by hematopoietic progenitor cells trafficking through blood, lymph, and peripheral tissues. Cell. 2007; 131: 994-1008.
- Kuznetsov AV. A new procedure for sampling lymph in animals. Bull Exp Biol Med. 1993; 116: 329-331 (in Russian).
- Kuznetsov AV. Dendritic (Langerhans) cells in central lymph of rabbits. Lymphology. 2000; 33: 67-68.
- Yin X, Xu X, Zhao Y, Wang ZJ, Wang HY, Hu ZB. Comparison of several optimization schemes for the induction and expansion of antibody-mediated high efficiency CIK (AMHE-CIK) in vitro. Zhongguo Shi Yan Xue Ye Xue Za Zhi. 2016; 24(1):191-196. (In Chinese).
- Hardie RJ, Sheehan NK. A lateral thoracotomy approach for thoracic duct cannulation and lymphatic fluid collection in a feline model. Lab Anim. 2016;50(5):390-396.
- Wang HW, Escott AB, Phang KL, Petrov MS, Phillips AR, Windsor JA (). Indications, techniques, and clinical outcomes of thoracic duct interventions in patients: a forgotten literature? J Surg Res. 2016;204(1):213-227.
- Cicciarelli JC., Iwaki Y, Terasaki PI, Guidera K, Shirahama S, Billing R, Hermes M, Cardman L, Kano T, Iwatsuki S, Koep L. Weil R, Starzl TE. Preliminary evidence of dual-marked lymphocytes in thoracic duct lymph fluid. Transplant Proc. 1980; 12(3):490-492.
- Huff JB, Schander A, Downey HF, Hodge LM. Lymphatic pump treatment augments lymphatic flux of lymphocytes in rats. Lymphat Res Biol. 2010; 8: 183-187.
- Sparshott SM, Sharma H, Kelly JD, Ford WL. Factors influencing the fate of 111indium-labelled lymphocytes after transfer to syngeneic rats. J Immunol Meth. 1981; 41: 303-320.
- Yamashita A, Fukumoto T, Nawa Y, Kotani M, Fujii H, Era I. The generation of large pyroninophilic cells in the lymphoid tissues of rats infused with cell-free lymph. Aust J Exp Biol Med. Sci. 1975; 53: 11-26.
- Westermann J, Smith T, Peters U, Tschernig T, Pabst R, Steinhoff G, Sparshott SM, Bell EB. Both activated and nonactivated leukocytes from the periphery continuously enter the thymic medulla of adult rats: phenotypes, sources and magnitude of traffic. Eur J Immunol. 1996; 26: 1866-1874.
- Kumararatne DS, MacLennan IC. Cells of the marginal zone of the spleen are lymphocytes derived from recirculating precursors. Eur J Immunol. 1981; 11:865-869.
- Everett NB, Reinhardt WO, Yoffey JM. The appearance of labeled cells in the thoracic duct lymph of the guinea pig after the administration of tritiated thymidine. Blood. 1960; 15: 82-94.
- Ramsden CS, Drayson MT, Bell EB. Lymphocyte targeted ricin as a potential therapy for lymphoid malignancy. I. Targeting efficiency. Br J Cancer. 1991; 63: 699-704.
- Grimm EA, Ramsey KM, Mazumder A, Wilson DJ, Djeu JY, Rosenberg SA. Lymphokine-activated killer cell phenomenon. II. Precursor phenotype is serologically distinct from peripheral T lymphocytes, memory cytotoxic thymus-derived lymphocytes, and natural killer cells. J Exp Med. 1983; 157: 884-897.
- Hein WR, Shelton JN, Simpson-Morgan MW, Morris B. Traffic and proliferative responses of recirculating lymphocytes in fetal calves. Immunology. 1988; 64: 621-626.
- Rieeke WO, Schwarz MR Protein synthesis in rat lymphocytes: radioautographic studies of availability and utilization of labeled amino acids in vivo. Blood.1964; 23: 502-516.
Introduction
Proliferation of normal immune cells is a key process in immunogenesis, especially in immature organism. Multiplication and differentiation of immature and naive lymphoid cells occurs upon their contacts with foreign and own antigens, respectively, in thymus and Peyer patches as primary lymphoid organs. Transportation of lymphoid cells and their precursor proceeds via lymphatic system. E.g., both mature and immature immune cells migrating from intestines, mesenterial lymph nodes and other peripheral lymph organs are collected into the common lymph thoracic duct (TD) [1]. Further trafficking via thoracic duct to peripheral blood, and antigen-dependent selection of mature T- and B cell populations is followed by their maturation in secondary lymphoid organs and local lymphatic tissue [2, 3]. Immature lymphoid cells after entering thoracic duct, may prepare for cell division by forming a "mitotic spindle" made of microtubules and many associated proteins. However, distinct mechanisms of mitosis regulation are still unknown [4, 5]. A proportion of thoracic duct cells is comprised by the nonlymphoid monocyte-like cells [6]. Hence, a sufficient immune population obtained from lymph may undergo expansion. This mitotic activity could be dependent on the stage of immunogenesis. Maturation of immune system in mammals proceeds just after birth, upon initial antigenic contacts.
Numerous workers focused on age-dependent changes of various crucial immune structures and appropriate regulators of cell proliferation and protection [7-11]. It should be taken into account that different antigen-presenting cells (APC), e.g., T cells, monocytes etc., may also migrate from vascular flow to peripheral and TD lymph [12].
Using bone marrow transplantation approach, homing experiments, and parabiotic mice, we have found that the hematopoietic stem and progenitor cells (HSPC) originate from the marrow and permanently migrate to different extramedullary tissues, where they reside for several days until entering the draining lymphatics, then returning to the bloodstream. The migratory pathways of HSPCs differ from those of lymphocytes. Therefore, the circulating HSPCs reach their target hematopoietic tissues, they do not require secondary lymphoid organs to recirculate [13].
There are only scarce data on mitotic activity of lymphoid cells in peripheral and central lymph of intact mammals. E.g., we have earlier shown sufficient mitotic activity of thoracic lymph duct cells in young rabbits [14, 15], being a further step to the recent concept of a "lymph humor/proliferation factor" [16]. Therefore, it is necessary to study age-related mitoses in TDL. The aim of the research was to assess correlations between rabbit MTDL, rabbit’s age and LTDL. We emphasize that the features of LTDL morphology and their function are of particular interest, both in the aspect of postnatal development, and also in LTDL role for repopulation/reconstitution of lymphoid tissue and lymphoid organs in physiological and pathological states (in oncological diseases in particular). In particular, the thoracic duct lymphoid population could be important for recovery of cellular and humoral immunity after intensive cytostatic treatment, e.g., radiation therapy, as initially shown by Strober [17].
A significant proportion of white blood cells consisting of lymphocytes by 98% is permanently passing via the thoracic duct to bloodstream. Hence, any details on their cytokinetics may have implications to the production rate, circulation and fate of the lymphocytes in immune response [18]. The murine thoracic duct lymph contains hematopoietic stem and progenitor cells (HSPCs) that possess short- and long-term multi-lineage reconstitution capacity. The TD-derived HSPCs originate from bone marrow (BM), enter the blood, and move to different peripheral organs, where they reside for, at least, 36 hr before entering draining lymphatics, then returning to the bloodstream and, eventually, to bone marrow (BM). The migrating HSPCs proliferate within extramedullary tissues and give rise to tissue-resident myeloid cells, preferentially dendritic cells. HSPCs may invade peripheral organs and foster the local production of tissue-resident innate immune cells under both steady-state conditions and in response to inflammatory signals [19].
The aim of our study was to assess correlations between rabbit mitotic thoracic duct cells, rabbit’s age, and numbers of lymphocytes in thoracic duct.
Materials and methods
Experimental animals
The study was carried out in 29 male Chinchilla rabbits of different ages (1.5 to 36 weeks), weighing, respectively, 120 to 1800 g (Table 1). All the animals were kept during the experiment at the animal facility of B. Atchabarov Research Institute of Fundamental and Practical Medicine (Almaty, Kazakhstan), getting standard feeding and water ad libitum.
Table 1. Distribution of rabbits into different age groups and their parameters

Ethical Approval
We understand the ethical principles under which the journal operates and our work complies with the animal ethics checklist as outlined in The ABC of Animal Experiments 2010 FELASA Accredited Scientists' Competence (Category C) course at Viikki Campus of the University of Helsinki www.helsinki.fi/weboodi and The Journal of Physiology and Experimental Physiology by D. Grundy, The Journal of Physiology, 593: 2547-2549, doi: 10.1113/JP270818.5.
Lymph harvesting
The invasive procedures were made following intravenous anaesthesia with calypsol-ketamine and lystenonum at the doses of 50 mg and 10 mg/kg body weight, respectively. Infiltration of 1% novocaine solution was used as local anesthesia. Lymph was drawn from thoracic duct. Intubation of trachea and artificial lung ventilation were made in the SIMV mode. A rabbit was fixed on the back by its extremities, and intravenous anesthesia was made. Hair was removed from the frontside of abdomen followed by local anesthesia of abdominal wall. Thereafter, a midline laparotomy was performed. The longitudinal incision line was made along the projection of left kidney. The surgical wound was widened to the left, and the intestinal loops were moved medially. The left kidney with its vessels was located on the back side of the abdominal cavity. Novocaine anesthesia of perinephric cellular tissue was made. Left kidney and its vessels were released from fixation beginning from the lateral edge of the kidney up to the origin of the A. renalis and removed medially. The thoracic duct cistern was found dorsally from abdominal aorta according to the beginning of the A. renalis (Fig. 1). The cisternal lymph was obtained by punching with original glass micropipettes (Russian patent No 1465076, 1987) [20, 21]. The lymph samples (0.01 mL) were transferred to microscopic slides. The cell smears were dried and stained according to Giemsa technique. The smears were studied by LEICA DM1000 light microscope at X400, or X1000 magnification with oil immersion. The number of mitoses per 100 cells was calculated in rabbit lymph by a routine method. Absolute number of leukocytes was calculated manually in the Bürker chamber. Their numbers were expressed as 1×109 per 1000 mL.

Figure 1. A surgical access to the thoracic duct cistern in rabbit. LK, left kidney; KV, left kidney vein; TDC, thoracic duct cistern (the scale bar is 1 cm)
Statistics
We calculated mean values, and standard deviation (SD) for the distinct groups, variance values, using Student factor (freedom degree is: n-1). The obtained results were statistically calculated using confidence intervals of mean values for the groups compared. The error of average values from arithmetical average did not exceed 5%. The differences were considered statistically significant if two-tailed P values of <0.05 (*) and P<0.001 (**). Moreover, we have calculated statistical relationships between mitotic numbers and rabbit’s age, as well as between the mitotic numbers and lymphocyte numbers, using Pearson correlation quotient. All the data were expressed as the mean ± SEM. The data were analyzed by Microsoft Office Excel 2007 software.
Results
We have revealed a number of cells at various stages of mitosis when studying thoracic lymph smears from immature rabbits (Fig. 2).

Figure 2. Mitotic events observed in smears of TD cells from immature rabbits (a, b, c, d) , stained by Giemsa, photomicrograph at 1000x magnification: (a), prophase; (b), metaphase; (c); early anaphase; (d), late anaphase; (e), telophase
The data are expressed as mean ± SEM. The differences between the mitotic cell ratios for various age groups and between TD cell numbers in these groups were considered statistically significant, if two-tailed P<0.05 (*) and P<0.001 (**).
The minimal numbers of mitotic cells were observed in thoracic duct populations of mature rabbits at the age of 36 weeks.
A maximal percentage of mitoses (23.0 ± 0.14, P=0.02, n=6) was registered in the animals 1.5 weeks of age and remained high (19.0 ± 0.12, P=0.01, n=5) at the age of 2.5 weeks (body mass 240 ± 20 g). At later terms, the mitotic index progressively decreased two-fold by 4.5 weeks of age (11.0 ± 0.14, P<0.05, n=4), and even more at 13.5 weeks (6.3 ± 0.08, P=0.04), when compared to initial values of 1.5 weeks (Fig. 3). With advancing age, the numbers of mitotic cells dropped down to 4.0 ± 0.04 (P=0.03, n=4) by 27 weeks, reaching a minimum of 1.0 ± 0.01 (P=0.02, n=6) by 36 weeks of age. The mitoses were virtually absent at the age of 36 weeks. Most TD cells counted in the lymph smears of mature rabbits (by 36 weeks) had the interphase morphology.

Figure 3. Changes of mitotic cell numbers in thoracic duct (MTDL) and total number of thoracic duct cells (LTDL) in rabbits aged from 1.5 to 36 weeks. Differences were considered statistically significant if two-tailed P<0.05 (*), P<0.001 (**)
By the contrast, total numbers of thoracic duct lymphocytes increased within 36 weeks (2.8 ± 0.03×109, P=0.04, n=6; 3.3 ± 0.05×109; P=0.05, n=5; 4.0×109 ± 0.04, p=0.02, n=4; 4.7 ± 0.04×109, p=0.03, n=4; 5.4 ± 0.03×109, P=0.02, n=4; 5.9 ± 0.05×109, P=0.03, n=6 (at 1.5, 2.5, 4.5, 13.5, 27, 36 weeks, respectively). The total number of thoracic duct cells significantly increased in 4.5, 13.5 and 36 weeks old rabbits in comparison with the total TD cell number in 1.5 weeks old rabbits. A strong negative correlation was found between mitotic activity of thoracic duct cells and age, like as between total TD cell counts and age (R2=0.7, R2=0.96 and R2=0.8 respectively) of immature rabbits at the age range of 1.5 weeks and 36 weeks (Fig. 4, 5, and 6, respectively).

Figure 4. Pearson’s correlation coefficient (very high negative correlation, R2=0.7) between the mitotic thoracic duct cells (MTDL) (1x109) and age of rabbits (weeks)
A very high negative correlation (R2=0.96) between the mitotic activity and total cell counts detected in thoracic duct lymph (Fig. 5). By contrast, a significant positive correlation (R2=0.8), between the TD cell numbers and age was revealed (Fig. 6).

Discussion
In the present study, we have for the first time demonstrated very high levels of proliferating TD cells at early maturation terms (1.5-2.5 weeks), followed by a pronounced age-dependent decrease of mitotic activity in these cell populations, as well as their correlation with increasing absolute TD cell counts in the intact immature rabbits up to 13.5 weeks of age.
Mitotic activity of lymphoid cells is the key index of physiological immune response and its maturation with time. Numerous researchers focused on age changes of various crucial immune structures and some regulators of proliferation and protection. However, most of these studies concerned the aspects of immune response in aging animals [7, 9, 10]. Meanwhile, we would like to address maturation of immune system in the very young organism, e.g., rabbit pups since the age of 10-20 days.
Our study is a part of the recent concept aiming for detection of a lymph-derived humoral factor in thoracic duct of rabbits [16]. Our current knowledge of changing TD cell numbers in rabbits allows to select the animals with optimal level or combination of cytokines or other bioactive factors in thoracic lymph duct which may have a huge impact upon the mitotic activity. A search for optimized adjuvant protocols to achieve a regulated cells proliferation is important [22].
The results of this study show that the numbers of mitotic TD cells correlate with age and LTDL of intact immature rabbits. The maximal mitotic ratio and minimal total numbers of TD cells were revealed in immature newborn rabbits, thus suggesting a huge immune potential developing in the immature rabbits.
There is also a problem of an approach to sampling TDL. However, despite numerous approaches to sampling thoracic duct lymph, researchers still propose novel techniques to this purpose. Since 1987, we have introduced an original access for sampling the thoracic duct lymph which works with no failure. Moreover, the ongoing studies in thoracic duct cannulation and lymphatic fluid collection in animals [23] and humans [24] are performed over last years, thus allowing to take lymph samples and to perform lymph drainage, e.g., for in vivo T cell exhaustion in human patients [25].
In conclusion, our current findings show for the first time that a correlation between the mitotic activity, absolute TD cell concentrations and rabbit’s age. A very strong correlation between the mitotic cell ratio, total TD cell counts and immature rabbit’s age (between 1.5 weeks-13.5 weeks) was detected. In our study the mitotic TD cell activity was compared between the intact immature male rabbits (aged 1.5-2.5-4.5 weeks), and adult animals (aged 13.5-36 weeks). The mentioned results allow us to select the age of immature rabbits with maximal numbers of mitotic cells and to perform more exact search for the suggested lymph proliferation factor. The data suggest that the age-related changes of mitotic activity suggest distinct effects of cytokines and other bioactive factors in TD cell populations, e.g., a hypothetical lymphopoietic factor revealed several decades ago [16].
We have found an evident increase in TD cell numbers in the 4.5 week-old rabbits which may result from increased lymphopoiesis at this age confirmed by high mitotic activity of TD cells. A correlation between mitotic activity, TD cell numbers and rabbit age can be used as a new experimental model applicable in different fields of biology and pharmacology. Studies in cytokines and hormone combinations as well as antigenic environment causing high cell proliferation in younger age groups of animals are worth of further studies.
The features of TD lymphocyte morphology and their function are of particular interest not only in the age aspect of postnatal development, but also in the repopulation/reconstitution of lymphoid tissue and lymphoid organs in physiological and pathological conditions, especially, in therapy of malignancies, including bone marrow transplantation techniques.
It has been known for many years, large numbers of white cells, 98 per cent of them lymphocytes, are constantly passing into the blood stream from the thoracic duct. The findings may have implications as to the generation, circulation and fate of the lymphocytes passing the thoracic duct [18].
Moreover, the thoracic duct (TD) lymph contains HSPCs (hematopoietic stem and progenitor cells) that possess short- and long-term multiline age reconstitution capacity. In murine model, the TD-derived HSPCs originate in the BM, enter the blood, and traffic to multiple peripheral organs, where they reside for at least 36 hr before entering draining lymphatics to return to the blood and, eventually, the BM (bone marrow). Migratory HSPCs proliferate within extramedullary tissues and give rise to tissue-resident myeloid cells, preferentially dendritic cells. Thus, HSPCs can survey peripheral organs and can foster the local production of tissue-resident innate immune cells under both steady-state conditions and in response to inflammatory signals [19]. Therefore, we may suggest that, at least, a fraction of the mitotic cells found in TD of newborn rabbits may contain numerous hematopoietic precursors at different steps of differentiation which then migrate to their homing areas.
Thoracic duct (TD) provides a sufficient lymphocyte traffic: 0.65 ± 0.21×10⁶ lymphocytes/min (the baseline lymphocyte flux) to 6.10 ± 0.99×10⁶ lymphocytes/min (after lymphatic pump techniques) [26], hematopoietic and progenitor cells (HSPCs) [19].
TD lymphocytes migrate into lymph nodes [27, 28, 29, 30, 31, 32] and spleen [27, 28, 29, 31, 32], bone marrow [19], enter the thymus gland [28, 29].
It is known for decades that, at least in adult mammals, large amounts of immune cells, mostly T- and B lymphocytes, with a small portion of monocytes and dendritic cell precursors are continuously trafficking from the gut tissues and lymph nodes to the bloodstream via thoracic duct to the bloodstream [18]. Thus, our findings on the TD traffic of immature cells may have implications for production, circulation and fate of the lymphocytes. Later, our experimental techniques were confirmed by other workers [23].
Thoracic duct lymphocytes, like as bone marrow cells from normal rats are efficient in restoring the spleen marginal-zone cellularity in cyclophosphamide-treated rats, thus being able for renewal and proliferaiton. Thoracic duct cells passaged through an irradiated intermediate host and collected from that host's thoracic duct were also efficient at achieving marginal-zone reconstitution [30]. Moreover, many years ago, a special population of lymphokine- activated killer (LAK) cells and their precursors was found to be distributed in the thymus, bone marrow, spleen, lymph node, and thoracic duct [33]. The LAK cells are now considered a promising tool for immunotherapy of different malignancies, including leukemia and lymphoma.
Of interest are some data obtained in experiments with calf fetuses [34]. The lymphoid cell contents in thoracic duct increased ca. 50-fold from day 120 to the pre-birth levels, in parallel to expanded total pool of circulating lymphocytes. A proportion of lymphocytes bearing detectable surface immunoglobulin in fetal lymph ranged from 2.1% to 8.7%. The recirculating lymphocytes from fetal calves produced strong proliferative responses when stimulated by T-cell mitogens but responded poorly to B-cell mitogens. Fetal lymphocytes also responded to stimulation by allogeneic cells and stimulated other cells to proliferate during mixed lymphocyte culture.
Interestingy, the mitotic cells in TD stream were rarely detected young adult rabbits, thus being in accordance with the data reported in other adult animal models [23, 35]. Hence, our work has highlighted an intensive traffic of immature cell via thoracic duct at the during first weeks of life. This observation should be confirmed in other mammalian species. In general, the thoracic duct cells may be considered a significant intrinsic reserve of immune and hematopoietic cells in cytopenias induced by cytostatic treatment, e.g., during experimental bone marrow transplantation in the infants.
Conclusion
Proliferative activity of cells and total cell concentrations in thoracic lymph duct (TD) were studied in our experimental work. This study concerned mitotic activity in TD cells of newborn, very young to mature rabbits. Extremely high mitotic indexes were revealed in the 10-20 days old infant animals, thus showing high-level trafficking of immature lymphoid, and, probably, less differentiated hematopoietic cells which require further phenotypic characterization. This proliferating cell fraction may be also induced by some lymphopoietic factor(s) present in thoracic lymph. With body growth, the mitotic activity of TD cells rapidly dropped to minimal levels, along with increased cell concentrations in thoracic duct. These findings may be important in studying production, circulation and fate of TD lymphocytes in physiological and pathological states, in treatment of malignant diseases and, especially, in bone marrow transplantation based in many aspects on cellular immune therapy. Functioning of lymph ducts and differences in cellular content during infancy and at very young age may be useful for further advances in pediatric oncohematology.
Competing interests
No conflicts of interest, financial or otherwise by the authors.
Acknowledgement
This work was supported by B. Atchabarov Research Institute of Fundamental and Practical Medicine. We wish also to express our sincere thanks to Galina Igorevna Kuznetsova for help in translating the article into English.
References
- Fanous MYZ, Phillips AJ, Windsor JA. Mesenteric lymph: the bridge to future management of critical illness. J Pancreas. 2007; 8(4):374-399.
- Sato J, Chida K, Suda T, Sato A, Nakamura H. Migratory patterns of thoracic duct lymphocytes into bronchus- associated lymphoid tissue of immunized rats. Lung. 2000; 178:295-308.
- Ganusov VV, Auerbach J. Mathematical modeling reveals kinetics of lymphocyte recirculation in the whole organism. PLoS Comput Biol. 2014; 10(5): e1003586.
- McIntosh JR. Mitosis. Cold Spring Harb Perspect Biol. 2016; DOI: 10.1101/cshperspect.a023218.
- Kim HS, Fernandes G, Lee CW. Protein phosphatases involved in regulating mitosis: facts and hypotheses. Mol Cells. 2016;39(9):654-662.
- Pugh CW, McPherson GG, Steer HW. Characterization of nonlymphoid cells derived from rat peripheral lymph. J Exp Med. 1983; 157:1758-1779.
- Agrawal S, Ganguly S, Tran A, Sundaram P, Agrawal A. Retinoic acid treated human dendritic cells induce T regulatory cells via the expression of CD141 and GARP which is impaired with age. Aging (NY). 2016;8(6):1223-1235.
- Keyes BE, Liu S, Asare A, Nailk S, Levorse J, Polak L, Lu CP, Nikolova M, Pasolli HA, Fuchs E. Impaired epidermal to dendritic T cell signaling slows wound repair in aged skin. Cell. 2016;167(5):1323-1338.e14.
- Xie J, Zhang J, Wu H, Tang X, Liu J, Cheng G, Li P. The influences of age on T lymphocyte subsets in C57BL/6 mice. Saudi J Biol Sci. 2017;24(1):108-113.
- Zhang Q, Yang K, Yangyang P, He J,Yu S, Cui Y. Age-related changes in the morphology and protein expression of the thymus of healthy yaks (Bos grunniens). Am J Vet Res. 2016; 77(6):567-574.
- Montgomery RR. Age-related alterations in immune responses to West Nile virus infection. Clin Exp Immunol. 2017;187(1):26-34.
- Hunter MC, Teijeira A, Halin C. T cell trafficking through lymphatic vessels. Front Immunol. 2016;7:613. doi: 10.3389/fimmu.2016.00613.
- Massberg S, von Andrian UH. Novel trafficking routes for hematopoietic stem and progenitor cell. Ann N Y Acad Sci. 2009;1176:87-93.
- Kuznetsov AV. Mitoses in thoracic duct lymph of rabbits. Scientia Agriculturae. 2015; DOI:10.15192/PSCP.SA.2015.9.2.8992.
- Kuznetsov AV. Dendritic cells mitoses in thoracic duct lymph of immature rabbits. Transylvanian Review. 2017; 24:3678-3681.
- Yamashita A, Fukumoto T, Miyamoto M. Studies on lymph humoral factor. Biological characteristics of a lymphocytopoietic factor in rat thoracic duct lymph. Immunology. 1976;32: 651-656.
- Strober S. Initiation of antibody responses by different classes of lymphocytes. III. Differences in the proliferative rates of thoracic duct lymphocytes involved in primary and secondary responses. J Immunol. 1970; 105(3):734-737.
- Matsuno K, Ueta H, Shu Z, Xue-Dong X, Sawanobori Y, Kitazawa Y, Bin Y, Yamashita M, Shi C. The microstructure of secondary lymphoid organs that support immune cell trafficking. Arch Histol Cytol. 2010;73(1):1-21.
- Massberg S, Schaerli P, Knezevic-Maramica I, Köllnberger M, Tubo N, Moseman EA, Huff IV, Junt T, Wagers AJ, Mazo IB, von Andrian UH. Immunosurveillance by hematopoietic progenitor cells trafficking through blood, lymph, and peripheral tissues. Cell. 2007; 131: 994-1008.
- Kuznetsov AV. A new procedure for sampling lymph in animals. Bull Exp Biol Med. 1993; 116: 329-331 (in Russian).
- Kuznetsov AV. Dendritic (Langerhans) cells in central lymph of rabbits. Lymphology. 2000; 33: 67-68.
- Yin X, Xu X, Zhao Y, Wang ZJ, Wang HY, Hu ZB. Comparison of several optimization schemes for the induction and expansion of antibody-mediated high efficiency CIK (AMHE-CIK) in vitro. Zhongguo Shi Yan Xue Ye Xue Za Zhi. 2016; 24(1):191-196. (In Chinese).
- Hardie RJ, Sheehan NK. A lateral thoracotomy approach for thoracic duct cannulation and lymphatic fluid collection in a feline model. Lab Anim. 2016;50(5):390-396.
- Wang HW, Escott AB, Phang KL, Petrov MS, Phillips AR, Windsor JA (). Indications, techniques, and clinical outcomes of thoracic duct interventions in patients: a forgotten literature? J Surg Res. 2016;204(1):213-227.
- Cicciarelli JC., Iwaki Y, Terasaki PI, Guidera K, Shirahama S, Billing R, Hermes M, Cardman L, Kano T, Iwatsuki S, Koep L. Weil R, Starzl TE. Preliminary evidence of dual-marked lymphocytes in thoracic duct lymph fluid. Transplant Proc. 1980; 12(3):490-492.
- Huff JB, Schander A, Downey HF, Hodge LM. Lymphatic pump treatment augments lymphatic flux of lymphocytes in rats. Lymphat Res Biol. 2010; 8: 183-187.
- Sparshott SM, Sharma H, Kelly JD, Ford WL. Factors influencing the fate of 111indium-labelled lymphocytes after transfer to syngeneic rats. J Immunol Meth. 1981; 41: 303-320.
- Yamashita A, Fukumoto T, Nawa Y, Kotani M, Fujii H, Era I. The generation of large pyroninophilic cells in the lymphoid tissues of rats infused with cell-free lymph. Aust J Exp Biol Med. Sci. 1975; 53: 11-26.
- Westermann J, Smith T, Peters U, Tschernig T, Pabst R, Steinhoff G, Sparshott SM, Bell EB. Both activated and nonactivated leukocytes from the periphery continuously enter the thymic medulla of adult rats: phenotypes, sources and magnitude of traffic. Eur J Immunol. 1996; 26: 1866-1874.
- Kumararatne DS, MacLennan IC. Cells of the marginal zone of the spleen are lymphocytes derived from recirculating precursors. Eur J Immunol. 1981; 11:865-869.
- Everett NB, Reinhardt WO, Yoffey JM. The appearance of labeled cells in the thoracic duct lymph of the guinea pig after the administration of tritiated thymidine. Blood. 1960; 15: 82-94.
- Ramsden CS, Drayson MT, Bell EB. Lymphocyte targeted ricin as a potential therapy for lymphoid malignancy. I. Targeting efficiency. Br J Cancer. 1991; 63: 699-704.
- Grimm EA, Ramsey KM, Mazumder A, Wilson DJ, Djeu JY, Rosenberg SA. Lymphokine-activated killer cell phenomenon. II. Precursor phenotype is serologically distinct from peripheral T lymphocytes, memory cytotoxic thymus-derived lymphocytes, and natural killer cells. J Exp Med. 1983; 157: 884-897.
- Hein WR, Shelton JN, Simpson-Morgan MW, Morris B. Traffic and proliferative responses of recirculating lymphocytes in fetal calves. Immunology. 1988; 64: 621-626.
- Rieeke WO, Schwarz MR Protein synthesis in rat lymphocytes: radioautographic studies of availability and utilization of labeled amino acids in vivo. Blood.1964; 23: 502-516.
Александр В. Кузнецов1, Ильдар Р. Фахрадиев2, Ыдырыс А. Алмабаев3, Айгуль Ы. Алмабаева4
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21853" ["VALUE"]=> array(2) { ["TEXT"]=> string(1012) "<p><sup>1</sup> Доктор медицинских наук, преподаватель кафедры анатомии человека НГМУ, Новосибирск, Россия<br> <sup>2</sup> Заведующий лабораторией экспериментальной медицины, КазНМУ им. С. Д. Асфендиярова, Республика Казахстан<br> <sup>3</sup> Доктор медицинских наук, профессор, заведующий кафедрой клинической анатомии и оперативной хирургии в КазНМУ им. С. Д. Асфендиярова, Республика Казахстан<br> <sup>4</sup> Профессор, кафедра анатомии с оперативной хирургией, Медицинский университет Астана, г. Астана, Республика Казахстан</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(934) "1 Доктор медицинских наук, преподаватель кафедры анатомии человека НГМУ, Новосибирск, Россия
2 Заведующий лабораторией экспериментальной медицины, КазНМУ им. С. Д. Асфендиярова, Республика Казахстан
3 Доктор медицинских наук, профессор, заведующий кафедрой клинической анатомии и оперативной хирургии
в КазНМУ им. С. Д. Асфендиярова, Республика Казахстан
4 Профессор, кафедра анатомии с оперативной хирургией, Медицинский университет Астана, г. Астана, Республика Казахстан
Целью нашей работы было определение возможных взаимосвязей между уровнем митозов клеток в лимфе грудного протока (ГЛП), возрастом организма и числом лимфоцитов в эксперименте (27 интактных кроликов Шиншилла, 120-2,500 гр. в возрасте 1,5-36 недель). Образцы клеток забирали из цистерны грудного протока анестезированных животных. Количество митотических клеток подсчитывали в процентах от общего количества лимфоцитов и в абсолютных значениях после учета в мазках, окрашенных по Гимза. Результаты обрабатывались статистическими методами с помощью Microsoft Office Excel 2007. Корреляция между указанными выше данными определялась с помощью критерия Пирсона. Количество митотических клеточных форм в лимфе ГЛП уменьшалось по мере увеличения возраста кроликов (от 1,5-36 недель, новорожденные и растущие особи). Максимум митотической активности обнаружен у кроликов 1,5 недельного возраста (23,0 ± 0,14, P=0.02) в сравнении с таковым у кроликов 4,5 и 13,5 недельного возраста (11,0 ± 0,14*, P<0,05 и 6,3 ± 0,08**, P<0,001, соответственно). Абсолютное же количество клеток лимфы в ГЛП повышалось с возрастом животных. Минимальную концентрацию клеток обнаруживали у 1,5 недельных кроликов (2,8 ± 0,03, P=0.04), в сравнении с уровнями у 36-недельных кроликов (5,9 ± 0,05, P=0,03). Сильная негативная корреляция найдена между митотической активностью клеток ГЛП и возрастом, а также общей клеточностью лимфы. Выявлена положительная корреляция между числом клеток в ГЛП и возрастом животных (соответственно, R2=0,7; R2=0,96 и R2=0,8) (диапазон возраста – от 1,5 до 36 недель). Найденная взаимосвязь между пролиферацией и числом клеток грудного протока у растущих животных обнаружена впервые. Полученные данные позволяют предположить наличие оптимальных комбинаций цитокинов и других биоактивных факторов, регулирующих митотическую активность клеток грудного протока с возрастом.
Ключевые слова
Грудной лимфатический проток, клеточная популяция, кролики, митотическая активность, возрастные изменения.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21855" ["VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-58-65" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-58-65" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21856" ["VALUE"]=> array(2) { ["TEXT"]=> string(201) "<p>Alexander V. Kuznetsov<sup>1</sup>, Ildar R. Fakhradiyev<sup>2</sup>, Ydyrys A. Almabayev<sup>3</sup>, Aigul Y. Almabayeva<sup>4</sup></p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(141) "Alexander V. Kuznetsov1, Ildar R. Fakhradiyev2, Ydyrys A. Almabayev3, Aigul Y. Almabayeva4
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21857" ["VALUE"]=> array(2) { ["TEXT"]=> string(501) "<p><sup>1</sup> Department of Human Anatomy, Novosibirsk State Medical University, Russia <br> <sup>2</sup> Laboratory of Experimental Medicine, Kazakh National Medical University, Republic of Kazakhstan<br> <sup>3</sup> Department of Clinical Anatomy, Kazakh National Medical University, Republic of Kazakhstan<br> <sup>4</sup> Department of Human Anatomy with O.S. Medical University Astana, Republic of Kazakhstan</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(423) "1 Department of Human Anatomy, Novosibirsk State Medical University, Russia
2 Laboratory of Experimental Medicine, Kazakh National Medical University, Republic of Kazakhstan
3 Department of Clinical Anatomy, Kazakh National Medical University, Republic of Kazakhstan
4 Department of Human Anatomy with O.S. Medical University Astana, Republic of Kazakhstan
The aim of this study was to assess correlations between rabbit mitotic thoracic duct (TD) cells, rabbit’s age, and TD lymphocytes. The experiments were carried out in 27 intact male Chinchilla rabbits weighing 120-2.500 g (at the age of 1.5 weeks to 36 weeks). TD lymph specimens were drawn from the cisterna chyli of anaesthetised rabbits. The numbers of mitotic cells from TD per 100 cells, and absolute numbers of TD lymphocytes were counted in the Giemsa-stained cell smears by means of routine light microscope methods, and routine hemocytometric counts. We have performed statistical evaluation of the data by Microsoft Office Excel 2007 software. Correlations between the TD mitotic cell ratio, lymphocyte numbers, and animal age was estimated by Pearson’s criteria. The mitotic cell number in TD lymph decreased from the age of 1.5 weeks (infant animals) to 36 weeks (young adult rabbits). Maximal mitotic activity was found in rabbits at 1.5 week of age (23.0 ± 0.14, P=0.02) in comparison with appropriate indexes in rabbits at 4.5 and 13.5 weeks of age (11.0 ± 0.14*, P<0.05 and 6.3 ± 0.08**, P<0.001 respectively). In contrast to mitotic cell amounts, the absolute TD lymphocyte numbers were increased in older rabbits. The minimal TD; lymphocyte number in the 1.5-week old rabbits aged was 2.8 ± 0.03, being significantly different (P=0.04) against the lymphocyte numbers in rabbits aged 36 week (5.9 ± 0.05, P=0.03). Hence, strong negative correlations were found between the TD mitotic activity and age, mitotic cells and total TD lymphocyte numbers, as well as positive correlation between the TD lymphocytes and age (respectively, R2=0.7, R2=0.96 and R2=0.8) in immature rabbits (age from 1.5 weeks to 36 weeks). To our knowledge, these interrelations for TD lymph cells in the very young animals were detected for the first time. We conclude that the age-related correlation between mitotic activity and total lymphocyte amounts in TD allows presume optimal combinations of cytokines and other bioactive factors that regulate mitotic activity of thoracic duct cells with advancing age.
Keywords
Thoracic lymphatic duct, cell population, mitotic activity, age-dependent changes.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21859" ["VALUE"]=> string(99) "Mitotic activity of thoracic duct cells in rabbits correlates with age and total lymphocyte numbers" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(99) "Mitotic activity of thoracic duct cells in rabbits correlates with age and total lymphocyte numbers" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21860" ["VALUE"]=> string(4) "1616" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1616" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21861" ["VALUE"]=> string(4) "1617" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1617" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(12) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21856" ["VALUE"]=> array(2) { ["TEXT"]=> string(201) "<p>Alexander V. Kuznetsov<sup>1</sup>, Ildar R. Fakhradiyev<sup>2</sup>, Ydyrys A. Almabayev<sup>3</sup>, Aigul Y. Almabayeva<sup>4</sup></p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(141) "Alexander V. Kuznetsov1, Ildar R. Fakhradiyev2, Ydyrys A. Almabayev3, Aigul Y. Almabayeva4
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(141) "Alexander V. Kuznetsov1, Ildar R. Fakhradiyev2, Ydyrys A. Almabayev3, Aigul Y. Almabayeva4
" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21858" ["VALUE"]=> array(2) { ["TEXT"]=> string(2440) "<p style="text-align: justify;">The aim of this study was to assess correlations between rabbit mitotic thoracic duct (TD) cells, rabbit’s age, and TD lymphocytes. The experiments were carried out in 27 intact male Chinchilla rabbits weighing 120-2.500 g (at the age of 1.5 weeks to 36 weeks). TD lymph specimens were drawn from the cisterna chyli of anaesthetised rabbits. The numbers of mitotic cells from TD <i>per</i> 100 cells, and absolute numbers of TD lymphocytes were counted in the Giemsa-stained cell smears by means of routine light microscope methods, and routine hemocytometric counts. We have performed statistical evaluation of the data by Microsoft Office Excel 2007 software. Correlations between the TD mitotic cell ratio, lymphocyte numbers, and animal age was estimated by Pearson’s criteria. The mitotic cell number in TD lymph decreased from the age of 1.5 weeks (infant animals) to 36 weeks (young adult rabbits). Maximal mitotic activity was found in rabbits at 1.5 week of age (23.0 ± 0.14, P=0.02) in comparison with appropriate indexes in rabbits at 4.5 and 13.5 weeks of age (11.0 ± 0.14*, P<0.05 and 6.3 ± 0.08**, P<0.001 respectively). In contrast to mitotic cell amounts, the absolute TD lymphocyte numbers were increased in older rabbits. The minimal TD; lymphocyte number in the 1.5-week old rabbits aged was 2.8 ± 0.03, being significantly different (P=0.04) against the lymphocyte numbers in rabbits aged 36 week (5.9 ± 0.05, P=0.03). Hence, strong negative correlations were found between the TD mitotic activity and age, mitotic cells and total TD lymphocyte numbers, as well as positive correlation between the TD lymphocytes and age (respectively, R<sup>2</sup>=0.7, R<sup>2</sup>=0.96 and R<sup>2</sup>=0.8) in immature rabbits (age from 1.5 weeks to 36 weeks). To our knowledge, these interrelations for TD lymph cells in the very young animals were detected for the first time. We conclude that the age-related correlation between mitotic activity and total lymphocyte amounts in TD allows presume optimal combinations of cytokines and other bioactive factors that regulate mitotic activity of thoracic duct cells with advancing age.</p> <h2>Keywords</h2> <p style="text-align: justify;">Thoracic lymphatic duct, cell population, mitotic activity, age-dependent changes.</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2330) "The aim of this study was to assess correlations between rabbit mitotic thoracic duct (TD) cells, rabbit’s age, and TD lymphocytes. The experiments were carried out in 27 intact male Chinchilla rabbits weighing 120-2.500 g (at the age of 1.5 weeks to 36 weeks). TD lymph specimens were drawn from the cisterna chyli of anaesthetised rabbits. The numbers of mitotic cells from TD per 100 cells, and absolute numbers of TD lymphocytes were counted in the Giemsa-stained cell smears by means of routine light microscope methods, and routine hemocytometric counts. We have performed statistical evaluation of the data by Microsoft Office Excel 2007 software. Correlations between the TD mitotic cell ratio, lymphocyte numbers, and animal age was estimated by Pearson’s criteria. The mitotic cell number in TD lymph decreased from the age of 1.5 weeks (infant animals) to 36 weeks (young adult rabbits). Maximal mitotic activity was found in rabbits at 1.5 week of age (23.0 ± 0.14, P=0.02) in comparison with appropriate indexes in rabbits at 4.5 and 13.5 weeks of age (11.0 ± 0.14*, P<0.05 and 6.3 ± 0.08**, P<0.001 respectively). In contrast to mitotic cell amounts, the absolute TD lymphocyte numbers were increased in older rabbits. The minimal TD; lymphocyte number in the 1.5-week old rabbits aged was 2.8 ± 0.03, being significantly different (P=0.04) against the lymphocyte numbers in rabbits aged 36 week (5.9 ± 0.05, P=0.03). Hence, strong negative correlations were found between the TD mitotic activity and age, mitotic cells and total TD lymphocyte numbers, as well as positive correlation between the TD lymphocytes and age (respectively, R2=0.7, R2=0.96 and R2=0.8) in immature rabbits (age from 1.5 weeks to 36 weeks). To our knowledge, these interrelations for TD lymph cells in the very young animals were detected for the first time. We conclude that the age-related correlation between mitotic activity and total lymphocyte amounts in TD allows presume optimal combinations of cytokines and other bioactive factors that regulate mitotic activity of thoracic duct cells with advancing age.
Keywords
Thoracic lymphatic duct, cell population, mitotic activity, age-dependent changes.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2330) "The aim of this study was to assess correlations between rabbit mitotic thoracic duct (TD) cells, rabbit’s age, and TD lymphocytes. The experiments were carried out in 27 intact male Chinchilla rabbits weighing 120-2.500 g (at the age of 1.5 weeks to 36 weeks). TD lymph specimens were drawn from the cisterna chyli of anaesthetised rabbits. The numbers of mitotic cells from TD per 100 cells, and absolute numbers of TD lymphocytes were counted in the Giemsa-stained cell smears by means of routine light microscope methods, and routine hemocytometric counts. We have performed statistical evaluation of the data by Microsoft Office Excel 2007 software. Correlations between the TD mitotic cell ratio, lymphocyte numbers, and animal age was estimated by Pearson’s criteria. The mitotic cell number in TD lymph decreased from the age of 1.5 weeks (infant animals) to 36 weeks (young adult rabbits). Maximal mitotic activity was found in rabbits at 1.5 week of age (23.0 ± 0.14, P=0.02) in comparison with appropriate indexes in rabbits at 4.5 and 13.5 weeks of age (11.0 ± 0.14*, P<0.05 and 6.3 ± 0.08**, P<0.001 respectively). In contrast to mitotic cell amounts, the absolute TD lymphocyte numbers were increased in older rabbits. The minimal TD; lymphocyte number in the 1.5-week old rabbits aged was 2.8 ± 0.03, being significantly different (P=0.04) against the lymphocyte numbers in rabbits aged 36 week (5.9 ± 0.05, P=0.03). Hence, strong negative correlations were found between the TD mitotic activity and age, mitotic cells and total TD lymphocyte numbers, as well as positive correlation between the TD lymphocytes and age (respectively, R2=0.7, R2=0.96 and R2=0.8) in immature rabbits (age from 1.5 weeks to 36 weeks). To our knowledge, these interrelations for TD lymph cells in the very young animals were detected for the first time. We conclude that the age-related correlation between mitotic activity and total lymphocyte amounts in TD allows presume optimal combinations of cytokines and other bioactive factors that regulate mitotic activity of thoracic duct cells with advancing age.
Keywords
Thoracic lymphatic duct, cell population, mitotic activity, age-dependent changes.
" } ["DOI"]=> array(37) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21855" ["VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-58-65" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-58-65" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(37) "10.18620/ctt-1866-8836-2019-8-1-58-65" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21859" ["VALUE"]=> string(99) "Mitotic activity of thoracic duct cells in rabbits correlates with age and total lymphocyte numbers" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(99) "Mitotic activity of thoracic duct cells in rabbits correlates with age and total lymphocyte numbers" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(99) "Mitotic activity of thoracic duct cells in rabbits correlates with age and total lymphocyte numbers" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21857" ["VALUE"]=> array(2) { ["TEXT"]=> string(501) "<p><sup>1</sup> Department of Human Anatomy, Novosibirsk State Medical University, Russia <br> <sup>2</sup> Laboratory of Experimental Medicine, Kazakh National Medical University, Republic of Kazakhstan<br> <sup>3</sup> Department of Clinical Anatomy, Kazakh National Medical University, Republic of Kazakhstan<br> <sup>4</sup> Department of Human Anatomy with O.S. Medical University Astana, Republic of Kazakhstan</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(423) "1 Department of Human Anatomy, Novosibirsk State Medical University, Russia
2 Laboratory of Experimental Medicine, Kazakh National Medical University, Republic of Kazakhstan
3 Department of Clinical Anatomy, Kazakh National Medical University, Republic of Kazakhstan
4 Department of Human Anatomy with O.S. Medical University Astana, Republic of Kazakhstan
1 Department of Human Anatomy, Novosibirsk State Medical University, Russia
2 Laboratory of Experimental Medicine, Kazakh National Medical University, Republic of Kazakhstan
3 Department of Clinical Anatomy, Kazakh National Medical University, Republic of Kazakhstan
4 Department of Human Anatomy with O.S. Medical University Astana, Republic of Kazakhstan
Александр В. Кузнецов1, Ильдар Р. Фахрадиев2, Ыдырыс А. Алмабаев3, Айгуль Ы. Алмабаева4
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(203) "Александр В. Кузнецов1, Ильдар Р. Фахрадиев2, Ыдырыс А. Алмабаев3, Айгуль Ы. Алмабаева4
" } ["SUBMITTED"]=> array(37) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21845" ["VALUE"]=> string(10) "20.03.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "20.03.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "20.03.2019" } ["ACCEPTED"]=> array(37) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21846" ["VALUE"]=> string(10) "15.04.2019" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(10) "15.04.2019" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL ["DISPLAY_VALUE"]=> string(10) "15.04.2019" } ["CONTACT"]=> array(38) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21847" ["VALUE"]=> string(4) "1645" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1645" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(66) "Alexander V. Kuznetsov" ["LINK_ELEMENT_VALUE"]=> bool(false) } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21854" ["VALUE"]=> array(2) { ["TEXT"]=> string(3739) "<p style="text-align: justify;">Целью нашей работы было определение возможных взаимосвязей между уровнем митозов клеток в лимфе грудного протока (ГЛП), возрастом организма и числом лимфоцитов в эксперименте (27 интактных кроликов Шиншилла, 120-2,500 гр. в возрасте 1,5-36 недель). Образцы клеток забирали из цистерны грудного протока анестезированных животных. Количество митотических клеток подсчитывали в процентах от общего количества лимфоцитов и в абсолютных значениях после учета в мазках, окрашенных по Гимза. Результаты обрабатывались статистическими методами с помощью Microsoft Office Excel 2007. Корреляция между указанными выше данными определялась с помощью критерия Пирсона. Количество митотических клеточных форм в лимфе ГЛП уменьшалось по мере увеличения возраста кроликов (от 1,5-36 недель, новорожденные и растущие особи). Максимум митотической активности обнаружен у кроликов 1,5 недельного возраста (23,0 ± 0,14, P=0.02) в сравнении с таковым у кроликов 4,5 и 13,5 недельного возраста (11,0 ± 0,14*, P<0,05 и 6,3 ± 0,08**, P<0,001, соответственно). Абсолютное же количество клеток лимфы в ГЛП повышалось с возрастом животных. Минимальную концентрацию клеток обнаруживали у 1,5 недельных кроликов (2,8 ± 0,03, P=0.04), в сравнении с уровнями у 36-недельных кроликов (5,9 ± 0,05, P=0,03). Сильная негативная корреляция найдена между митотической активностью клеток ГЛП и возрастом, а также общей клеточностью лимфы. Выявлена положительная корреляция между числом клеток в ГЛП и возрастом животных (соответственно, R<sup>2</sup>=0,7; R<sup>2</sup>=0,96 и R<sup>2</sup>=0,8) (диапазон возраста – от 1,5 до 36 недель). Найденная взаимосвязь между пролиферацией и числом клеток грудного протока у растущих животных обнаружена впервые. Полученные данные позволяют предположить наличие оптимальных комбинаций цитокинов и других биоактивных факторов, регулирующих митотическую активность клеток грудного протока с возрастом. </p> <h2>Ключевые слова</h2> <p style="text-align: justify;">Грудной лимфатический проток, клеточная популяция, кролики, митотическая активность, возрастные изменения. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3641) "Целью нашей работы было определение возможных взаимосвязей между уровнем митозов клеток в лимфе грудного протока (ГЛП), возрастом организма и числом лимфоцитов в эксперименте (27 интактных кроликов Шиншилла, 120-2,500 гр. в возрасте 1,5-36 недель). Образцы клеток забирали из цистерны грудного протока анестезированных животных. Количество митотических клеток подсчитывали в процентах от общего количества лимфоцитов и в абсолютных значениях после учета в мазках, окрашенных по Гимза. Результаты обрабатывались статистическими методами с помощью Microsoft Office Excel 2007. Корреляция между указанными выше данными определялась с помощью критерия Пирсона. Количество митотических клеточных форм в лимфе ГЛП уменьшалось по мере увеличения возраста кроликов (от 1,5-36 недель, новорожденные и растущие особи). Максимум митотической активности обнаружен у кроликов 1,5 недельного возраста (23,0 ± 0,14, P=0.02) в сравнении с таковым у кроликов 4,5 и 13,5 недельного возраста (11,0 ± 0,14*, P<0,05 и 6,3 ± 0,08**, P<0,001, соответственно). Абсолютное же количество клеток лимфы в ГЛП повышалось с возрастом животных. Минимальную концентрацию клеток обнаруживали у 1,5 недельных кроликов (2,8 ± 0,03, P=0.04), в сравнении с уровнями у 36-недельных кроликов (5,9 ± 0,05, P=0,03). Сильная негативная корреляция найдена между митотической активностью клеток ГЛП и возрастом, а также общей клеточностью лимфы. Выявлена положительная корреляция между числом клеток в ГЛП и возрастом животных (соответственно, R2=0,7; R2=0,96 и R2=0,8) (диапазон возраста – от 1,5 до 36 недель). Найденная взаимосвязь между пролиферацией и числом клеток грудного протока у растущих животных обнаружена впервые. Полученные данные позволяют предположить наличие оптимальных комбинаций цитокинов и других биоактивных факторов, регулирующих митотическую активность клеток грудного протока с возрастом.
Ключевые слова
Грудной лимфатический проток, клеточная популяция, кролики, митотическая активность, возрастные изменения.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3641) "Целью нашей работы было определение возможных взаимосвязей между уровнем митозов клеток в лимфе грудного протока (ГЛП), возрастом организма и числом лимфоцитов в эксперименте (27 интактных кроликов Шиншилла, 120-2,500 гр. в возрасте 1,5-36 недель). Образцы клеток забирали из цистерны грудного протока анестезированных животных. Количество митотических клеток подсчитывали в процентах от общего количества лимфоцитов и в абсолютных значениях после учета в мазках, окрашенных по Гимза. Результаты обрабатывались статистическими методами с помощью Microsoft Office Excel 2007. Корреляция между указанными выше данными определялась с помощью критерия Пирсона. Количество митотических клеточных форм в лимфе ГЛП уменьшалось по мере увеличения возраста кроликов (от 1,5-36 недель, новорожденные и растущие особи). Максимум митотической активности обнаружен у кроликов 1,5 недельного возраста (23,0 ± 0,14, P=0.02) в сравнении с таковым у кроликов 4,5 и 13,5 недельного возраста (11,0 ± 0,14*, P<0,05 и 6,3 ± 0,08**, P<0,001, соответственно). Абсолютное же количество клеток лимфы в ГЛП повышалось с возрастом животных. Минимальную концентрацию клеток обнаруживали у 1,5 недельных кроликов (2,8 ± 0,03, P=0.04), в сравнении с уровнями у 36-недельных кроликов (5,9 ± 0,05, P=0,03). Сильная негативная корреляция найдена между митотической активностью клеток ГЛП и возрастом, а также общей клеточностью лимфы. Выявлена положительная корреляция между числом клеток в ГЛП и возрастом животных (соответственно, R2=0,7; R2=0,96 и R2=0,8) (диапазон возраста – от 1,5 до 36 недель). Найденная взаимосвязь между пролиферацией и числом клеток грудного протока у растущих животных обнаружена впервые. Полученные данные позволяют предположить наличие оптимальных комбинаций цитокинов и других биоактивных факторов, регулирующих митотическую активность клеток грудного протока с возрастом.
Ключевые слова
Грудной лимфатический проток, клеточная популяция, кролики, митотическая активность, возрастные изменения.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "21853" ["VALUE"]=> array(2) { ["TEXT"]=> string(1012) "<p><sup>1</sup> Доктор медицинских наук, преподаватель кафедры анатомии человека НГМУ, Новосибирск, Россия<br> <sup>2</sup> Заведующий лабораторией экспериментальной медицины, КазНМУ им. С. Д. Асфендиярова, Республика Казахстан<br> <sup>3</sup> Доктор медицинских наук, профессор, заведующий кафедрой клинической анатомии и оперативной хирургии в КазНМУ им. С. Д. Асфендиярова, Республика Казахстан<br> <sup>4</sup> Профессор, кафедра анатомии с оперативной хирургией, Медицинский университет Астана, г. Астана, Республика Казахстан</p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(934) "1 Доктор медицинских наук, преподаватель кафедры анатомии человека НГМУ, Новосибирск, Россия
2 Заведующий лабораторией экспериментальной медицины, КазНМУ им. С. Д. Асфендиярова, Республика Казахстан
3 Доктор медицинских наук, профессор, заведующий кафедрой клинической анатомии и оперативной хирургии
в КазНМУ им. С. Д. Асфендиярова, Республика Казахстан
4 Профессор, кафедра анатомии с оперативной хирургией, Медицинский университет Астана, г. Астана, Республика Казахстан
1 Доктор медицинских наук, преподаватель кафедры анатомии человека НГМУ, Новосибирск, Россия
2 Заведующий лабораторией экспериментальной медицины, КазНМУ им. С. Д. Асфендиярова, Республика Казахстан
3 Доктор медицинских наук, профессор, заведующий кафедрой клинической анатомии и оперативной хирургии
в КазНМУ им. С. Д. Асфендиярова, Республика Казахстан
4 Профессор, кафедра анатомии с оперативной хирургией, Медицинский университет Астана, г. Астана, Республика Казахстан
30.03.2019

Афанасьев Б. В. (Санкт-Петербург, Россия)
Вагемакер Г. (Роттердам, Нидерланды)
Цандер А. Р. (Гамбург, Германия)
Фезе Б. (Гамбург, Германия)
Чухловин А. Б. (Санкт-Петербург, Россия)
Алейникова О. В. (Минск, Беларусь)
Борсет М. (Трондхейм, Норвегия)
Галибин О. В. (Санкт-Петербург, Россия)
Зубаровская Л. С. (Санкт-Петербург, Россия)
Климко Н. Н. (Санкт-Петербург, Россия)
Кольб Х. (Мюнхен, Германия)
Крегер Н. (Гамбург, Германия)
Кулагин А. Д. (Санкт-Петербург, Россия)
Ланге К. (Гамбург, Германия)
Мамаев Н. Н. (Санкт-Петербург, Россия)
Михайлова Н. Б. (Санкт-Петербург, Россия)
Моисеев И. С. (Санкт-Петербург, Россия)
Наглер А. (Тель-Авив, Израиль)
Немков А. С. (Санкт-Петербург, Россия)
Парамонов И. В. (Киров, Россия)
Румянцев А. Г. (Москва, Россия)
Савченко В. Г. (Москва, Россия)
Смирнов А. В. (Санкт-Петербург, Россия)
Усс А. Л. (Минск, Беларусь)
Фиббе В. (Лейден, Нидерланды)
Хельтцер Д. (Франкфурт-на-Майне, Германия)
Чечеткин А. В. (Санкт-Петербург, Россия)
Другая обзорная статья О. В. Галибина и соавт. касается естественных и синтетических матриц, разработанных для более быстрой и эффективной регенерации поврежденных нервов. Особая роль отводится хитозан-содержащим полимерам и биодеградируемым, элкетропроводным синтетическим носителям, позволяющим осуществлять процедуры, усиливающие регенерацию.
Статья А. Б. Чухловина касается некоторых «старых» препаратов, применяемых при многих неонкологических заболеваниях, которые могут, кроме того, быть использованы для терапии злокачественных новообразований, главным образом, как компоненты комбинированной терапии.
Клинические результаты ТГСК от гаплоидентичных доноров (например – родителей пациентов) представлены в статье А. В. Бейнарович и соавт., которая рассматривает, главным образом, клинические исходы (выживаемость на ранних и поздних сроках, частоту рецидивов и др.), на основании опыта отдельного центра.
Прогностические шкалы для пациентов с миелодиспластическим синдромом (МДС) показывают различную эффективность, особенно при использовании новых видов лечения. Е. Б. Морозова и соавт. проводят сравнение различных прогностических шкал при МДС с учетом соответствующих клинических исходов при длительных сроках наблюдения.
Специализированная медицинская помощь необходима больным после ТГСК с ЛОР-осложнениями. Е. С. Утимишева и соавт. рассматривают эти проблемы связанные с синуситами, сопутствующими бактериальными патогенами, результатами местного лечения, в том числе – эффективности пункций максиллярных синусов у пациентов.
Специальный клинический случай описывается Т. А. Быковой и соавт., которые приводят случай семейного гемофагоцитарного лимфогистиоцитоза – редкого клинического синдрома, который в некоторых случаях имеет генетическую предрасположенность.
Экспериментальное исследование Александра И. Кузнецова и соавт. содержит оригинальные данные о митотической активности и клеточности лимфы грудного лимфатического протока у кроликов в возрасте от новорожденности до взрослого состояния. Доказательства митотической активности клеток позволяют использовать эти результаты для задач восстановления иммунитета у очень молодых животных и экстраполировать их на развитие человека, что имеет потенциальную важность при цитостатической терапии.
Редакционная статья
Профессор Борис В. Афанасьев, главный редактор журнала «Клеточная Терапия и Трансплантация» (СТТ)
Обзорные статьи
Тапани Рууту
Алексей Б. Чухловин
Олег В. Галибин1, Герман В. Медведев2, Павел В. Попрядухин3, Павел А. Кулагин1, Александр А. Гусев1, Галина П. Косякова1, Наталья В. Михайлова1, Вероника Д. Новак1, Денис Н. Соломицкий1, Игорь О. Шемякин1, Вадим С. Гаджиагаев1, Максат Х. Гурбанназаров1
Клинические исследования
Елена В. Морозова, Мария В. Барабанщикова, Николай Ю. Цветков, Ксения В. Мельситова, Юлия В. Рудницкая, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев
Анастасия В. Бейнарович, Елена В. Бабенко, Иван С. Моисеев, Олеся В. Паина, Ольга В. Пирогова, Татьяна А. Рудакова, Татьяна Л. Гиндина, Елена И. Дарская, Елена В. Морозова, Сергей Н. Бондаренко, Людмила С. Зубаровская, Борис В. Афанасьев
Екатерина С. Утимишева1, Олег И. Долгов1, Олеся В. Паина1, Кирилл А. Екушов1, Алина А. Витрищак1, Борис И. Смирнов2, Людмила С. Зубаровская 1, Сергей А. Карпищенко1, Борис В. Афанасьев1
Клинический случай
Татьяна А. Быкова, Варвара Н. Овечкина, Анна А. Осипова, Андрей В. Козлов, Александр Л. Алянский, Елена В. Семенова, Людмила С. Зубаровская, Борис В. Афанасьев
Экспериментальные исследования
Александр В. Кузнецов1, Ильдар Р. Фахрадиев2, Ыдырыс А. Алмабаев3, Айгуль Ы. Алмабаева4
Редакционная статья
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 20945
)
[VALUE] => Array
(
[0] => 34
)
[DESCRIPTION] => Array
(
[0] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 34
)
[~DESCRIPTION] => Array
(
[0] =>
)
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20937
[VALUE] => Array
(
[TEXT] => <p>Профессор Борис В. Афанасьев, главный редактор журнала <i>«Клеточная Терапия и Трансплантация»</i> (СТТ)</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Профессор Борис В. Афанасьев, главный редактор журнала «Клеточная Терапия и Трансплантация» (СТТ)
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20938
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">
Уважаемые авторы и читатели журнала СТТ!<br>
На протяжении нескольких последних лет были достигнуты весьма значительные успехи в лечении ряда злокачественных заболеваний у взрослых и, особенно – у детей с применением новых лекарственных агентов и технологий, т.е. биспецифических антител, активирующих Т-клетки (BITE), конъюгированных моноклональных антител, CAR-T-клеток, и ингибиторов иммунных контрольных точек. Вышеуказанные лекарственные средства могут сочетаться с аллогенной трансплантацией гемопоэтических клеток (алло-ТГСК), тем самым создавая основу для последующей успешной терапии.<br>
Наибольший прогресс был достигнут при лимфопролиферативных заболеваниях, в т.ч. у больных с резистентной/рецидивирующей (R/R) лимфомой Ходжкина, в связи с внедрением Брентуксимаба Ведотина (BV) – конъюгированного специфического антитела. Ингибиторы иммунных контрольных точек также имеют высокую эффективность на кратких сроках, но, к сожалению, беспрогрессионная выживаемость в этих случаях остается относительно низкой. Тем не менее, комбинация этих препаратов с последующей алло-ТГСК перспективна в плане продления сроков беспрогрессионной выживаемости. <br>
У пациентов группы R/R с острым лимфобластным лейкозом некоторые препараты, например Блинатумомаб (антитело типа BITE) или конъюгированные антитела (например – Инотузумаб) приводят к частому терапевтическому ответу, будучи особенно эффективными у пациентов с наличием минимальной остаточной болезни (МОБ). До сих пор неясно, какая тактика должна применяться для МОБ-негативных больных и требуют ли они дальнейшей консолидации. <br>
Новые направления в иммунотерапии злокачественных новообразований связаны с разработкой средств клеточной терапии на основе CAR T-клеток, которые могут обеспечить таргетные эффекты в отношении специфических неоантигенов опухолей данного типа. Имеется лишь несколько небольших исследований с применением CAR-T-клеток у взрослых и детей. Эффективность лечения CAR-T-клетками при солидных опухолях еще предстоит определить, однако и в этой области наблюдается существенный прогресс. <br>
Аспекты трансплантации злокачественных заболеваний детского возраста также часто освещаются в журнале Клеточная Терапия и Трансплантация. По сравнению с высокой эффективностью лечения при остром лимфобластном лейкозе, солидные опухоли у детей, такие как медуллобластома, саркома Юинга и другие менее чувствительны к иммунотерапии в связи с иной мутационной нагрузкой и экспрессией неоантигенов. Эти молекулярные маркеры, а также микросателлитная нестабильность могут иметь значение при оценке групп клинического риска. Определение оптимальной иммунотерапии с трансплантацией или без нее при солидных новообразованиях у детей является одной из ключевых задач педиатрической онкологии. <br>
В заключение, мы ожидаем оригинальных и обзорных статей для нашего журнала от наших читателей-клиницистов по вопросам детской онкологии/гематологии с целью достижения оптимального специфического ответа в сочетании с меньшей токсичностью в отношении нормальных тканей, с применением новых подходов, в особенности – иммунотерапии опухолей детского возраста, а также использования трансплантации стволовых клеток при неопухолевых заболеваниях.<br>
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Уважаемые авторы и читатели журнала СТТ!
На протяжении нескольких последних лет были достигнуты весьма значительные успехи в лечении ряда злокачественных заболеваний у взрослых и, особенно – у детей с применением новых лекарственных агентов и технологий, т.е. биспецифических антител, активирующих Т-клетки (BITE), конъюгированных моноклональных антител, CAR-T-клеток, и ингибиторов иммунных контрольных точек. Вышеуказанные лекарственные средства могут сочетаться с аллогенной трансплантацией гемопоэтических клеток (алло-ТГСК), тем самым создавая основу для последующей успешной терапии.
Наибольший прогресс был достигнут при лимфопролиферативных заболеваниях, в т.ч. у больных с резистентной/рецидивирующей (R/R) лимфомой Ходжкина, в связи с внедрением Брентуксимаба Ведотина (BV) – конъюгированного специфического антитела. Ингибиторы иммунных контрольных точек также имеют высокую эффективность на кратких сроках, но, к сожалению, беспрогрессионная выживаемость в этих случаях остается относительно низкой. Тем не менее, комбинация этих препаратов с последующей алло-ТГСК перспективна в плане продления сроков беспрогрессионной выживаемости.
У пациентов группы R/R с острым лимфобластным лейкозом некоторые препараты, например Блинатумомаб (антитело типа BITE) или конъюгированные антитела (например – Инотузумаб) приводят к частому терапевтическому ответу, будучи особенно эффективными у пациентов с наличием минимальной остаточной болезни (МОБ). До сих пор неясно, какая тактика должна применяться для МОБ-негативных больных и требуют ли они дальнейшей консолидации.
Новые направления в иммунотерапии злокачественных новообразований связаны с разработкой средств клеточной терапии на основе CAR T-клеток, которые могут обеспечить таргетные эффекты в отношении специфических неоантигенов опухолей данного типа. Имеется лишь несколько небольших исследований с применением CAR-T-клеток у взрослых и детей. Эффективность лечения CAR-T-клетками при солидных опухолях еще предстоит определить, однако и в этой области наблюдается существенный прогресс.
Аспекты трансплантации злокачественных заболеваний детского возраста также часто освещаются в журнале Клеточная Терапия и Трансплантация. По сравнению с высокой эффективностью лечения при остром лимфобластном лейкозе, солидные опухоли у детей, такие как медуллобластома, саркома Юинга и другие менее чувствительны к иммунотерапии в связи с иной мутационной нагрузкой и экспрессией неоантигенов. Эти молекулярные маркеры, а также микросателлитная нестабильность могут иметь значение при оценке групп клинического риска. Определение оптимальной иммунотерапии с трансплантацией или без нее при солидных новообразованиях у детей является одной из ключевых задач педиатрической онкологии.
В заключение, мы ожидаем оригинальных и обзорных статей для нашего журнала от наших читателей-клиницистов по вопросам детской онкологии/гематологии с целью достижения оптимального специфического ответа в сочетании с меньшей токсичностью в отношении нормальных тканей, с применением новых подходов, в особенности – иммунотерапии опухолей детского возраста, а также использования трансплантации стволовых клеток при неопухолевых заболеваниях.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20939
[VALUE] => Array
(
[TEXT] => <p>Professor Boris V. Afanasyev, Editor-in-Chief, <i>Cellular Therapy and Transplantation Journal</i></p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Professor Boris V. Afanasyev, Editor-in-Chief, Cellular Therapy and Transplantation Journal
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20940
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify">
Dear CTT authors and readers,<br>
Over last several years, dramatic improvement has been achieved in treatment of some malignancies in adults, and, especially, in children by means of novel agents and technologies, i.e., bi-specific T-cell engager antibodies (BITE), conjugated monoclonal antibodies, CAR-T cells, and immune checkpoint inhibitors. The above-mentioned drugs may be combined with allogeneic hematopoietic stem cell transplantation (allo-HCT), thus creating a reliable basis for sequential successful therapy.<br>
The largest progress was attained with lymphoproliferative disorders, e.g., in patients with R/R Hodgkin lymphoma, due to introduction of Brentuximab Vedotin (BV), conjugated antibody. The immune checkpoint inhibitors have also shown high short-term efficiency, but unfortunately, the progression-free survival in these cases remains relatively low. However, combination of these drugs with subsequent allo-
HCT has promising efficacy in terms of progression-free survival. <br>
In R/R patients with acute lymphoblastic leukemia, some drugs like Blinatumomab, a BITE antibody, or conjugated antibody Inotuzumab, have yielded high response rates, being especially efficient in the patients with detectable minimal residual disease (MRD). It is still unclear what strategy should be used for MRD-negative patients and do they require further consolidation. <br>
Novel trends in immune therapy of malignant disorders are associated with development of CAR-T cell-based therapeutic tools which may provide a more targeted effects upon specific neoantigens of the given tumor type. There are only several limited studies of CAR-T application in adults and pediatric patients. The efficiency of CAR-T cell treatment in solid tumors is yet to be established, but sufficient progress is recently observed in this area. <br>
Transplantation aspects of pediatric malignancies treatment are also often spotlighted in Cellular Therapy and Transplantation. When compared with high treatment efficiency in acute lymphoblastic leukemia, pediatric tumors, like medulloblastoma, Ewing sarcoma and others are less sensitive to immunotherapy approaches due to different mutation burden and expression of neoantigens. These molecular mar-kers, as well as microsatellite instability could be of value when assessing the clinical risk groups. Elucidation of the optimal immunotherapy with or without transplantation in pediatric solid tumors is one of crucial agendas in pediatric oncology.<br>
In conclusion, we are expecting from our readers original and review articles for our Journal on pediatric oncology/hematology from our potential authors from different clinics, aiming to optimize the response rate with lesser toxicity to normal tissues by using novel approaches, especially, immune therapy of pediatric malignancies, as well as the use of stem cell transplantation in nonmalignant disorders.</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Dear CTT authors and readers,
Over last several years, dramatic improvement has been achieved in treatment of some malignancies in adults, and, especially, in children by means of novel agents and technologies, i.e., bi-specific T-cell engager antibodies (BITE), conjugated monoclonal antibodies, CAR-T cells, and immune checkpoint inhibitors. The above-mentioned drugs may be combined with allogeneic hematopoietic stem cell transplantation (allo-HCT), thus creating a reliable basis for sequential successful therapy.
The largest progress was attained with lymphoproliferative disorders, e.g., in patients with R/R Hodgkin lymphoma, due to introduction of Brentuximab Vedotin (BV), conjugated antibody. The immune checkpoint inhibitors have also shown high short-term efficiency, but unfortunately, the progression-free survival in these cases remains relatively low. However, combination of these drugs with subsequent allo-
HCT has promising efficacy in terms of progression-free survival.
In R/R patients with acute lymphoblastic leukemia, some drugs like Blinatumomab, a BITE antibody, or conjugated antibody Inotuzumab, have yielded high response rates, being especially efficient in the patients with detectable minimal residual disease (MRD). It is still unclear what strategy should be used for MRD-negative patients and do they require further consolidation.
Novel trends in immune therapy of malignant disorders are associated with development of CAR-T cell-based therapeutic tools which may provide a more targeted effects upon specific neoantigens of the given tumor type. There are only several limited studies of CAR-T application in adults and pediatric patients. The efficiency of CAR-T cell treatment in solid tumors is yet to be established, but sufficient progress is recently observed in this area.
Transplantation aspects of pediatric malignancies treatment are also often spotlighted in Cellular Therapy and Transplantation. When compared with high treatment efficiency in acute lymphoblastic leukemia, pediatric tumors, like medulloblastoma, Ewing sarcoma and others are less sensitive to immunotherapy approaches due to different mutation burden and expression of neoantigens. These molecular mar-kers, as well as microsatellite instability could be of value when assessing the clinical risk groups. Elucidation of the optimal immunotherapy with or without transplantation in pediatric solid tumors is one of crucial agendas in pediatric oncology.
In conclusion, we are expecting from our readers original and review articles for our Journal on pediatric oncology/hematology from our potential authors from different clinics, aiming to optimize the response rate with lesser toxicity to normal tissues by using novel approaches, especially, immune therapy of pediatric malignancies, as well as the use of stem cell transplantation in nonmalignant disorders.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20941
[VALUE] => Editorial article
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Editorial article
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20943
[VALUE] => 1547
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1547
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20944
[VALUE] => 1548
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1548
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Профессор Борис В. Афанасьев, главный редактор журнала «Клеточная Терапия и Трансплантация» (СТТ)
Уважаемые авторы и читатели журнала СТТ!
На протяжении нескольких последних лет были достигнуты весьма значительные успехи в лечении ряда злокачественных заболеваний у взрослых и, особенно – у детей с применением новых лекарственных агентов и технологий, т.е. биспецифических антител, активирующих Т-клетки (BITE), конъюгированных моноклональных антител, CAR-T-клеток, и ингибиторов иммунных контрольных точек. Вышеуказанные лекарственные средства могут сочетаться с аллогенной трансплантацией гемопоэтических клеток (алло-ТГСК), тем самым создавая основу для последующей успешной терапии.
Наибольший прогресс был достигнут при лимфопролиферативных заболеваниях, в т.ч. у больных с резистентной/рецидивирующей (R/R) лимфомой Ходжкина, в связи с внедрением Брентуксимаба Ведотина (BV) – конъюгированного специфического антитела. Ингибиторы иммунных контрольных точек также имеют высокую эффективность на кратких сроках, но, к сожалению, беспрогрессионная выживаемость в этих случаях остается относительно низкой. Тем не менее, комбинация этих препаратов с последующей алло-ТГСК перспективна в плане продления сроков беспрогрессионной выживаемости.
У пациентов группы R/R с острым лимфобластным лейкозом некоторые препараты, например Блинатумомаб (антитело типа BITE) или конъюгированные антитела (например – Инотузумаб) приводят к частому терапевтическому ответу, будучи особенно эффективными у пациентов с наличием минимальной остаточной болезни (МОБ). До сих пор неясно, какая тактика должна применяться для МОБ-негативных больных и требуют ли они дальнейшей консолидации.
Новые направления в иммунотерапии злокачественных новообразований связаны с разработкой средств клеточной терапии на основе CAR T-клеток, которые могут обеспечить таргетные эффекты в отношении специфических неоантигенов опухолей данного типа. Имеется лишь несколько небольших исследований с применением CAR-T-клеток у взрослых и детей. Эффективность лечения CAR-T-клетками при солидных опухолях еще предстоит определить, однако и в этой области наблюдается существенный прогресс.
Аспекты трансплантации злокачественных заболеваний детского возраста также часто освещаются в журнале Клеточная Терапия и Трансплантация. По сравнению с высокой эффективностью лечения при остром лимфобластном лейкозе, солидные опухоли у детей, такие как медуллобластома, саркома Юинга и другие менее чувствительны к иммунотерапии в связи с иной мутационной нагрузкой и экспрессией неоантигенов. Эти молекулярные маркеры, а также микросателлитная нестабильность могут иметь значение при оценке групп клинического риска. Определение оптимальной иммунотерапии с трансплантацией или без нее при солидных новообразованиях у детей является одной из ключевых задач педиатрической онкологии.
В заключение, мы ожидаем оригинальных и обзорных статей для нашего журнала от наших читателей-клиницистов по вопросам детской онкологии/гематологии с целью достижения оптимального специфического ответа в сочетании с меньшей токсичностью в отношении нормальных тканей, с применением новых подходов, в особенности – иммунотерапии опухолей детского возраста, а также использования трансплантации стволовых клеток при неопухолевых заболеваниях.
Обзорные статьи
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20946
[VALUE] => 21.01.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 21.01.2019
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20947
[VALUE] => 15.03.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 15.03.2019
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20948
[VALUE] => 7
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 7
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 22020
)
[VALUE] => Array
(
[0] => 7
)
[DESCRIPTION] => Array
(
[0] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 7
)
[~DESCRIPTION] => Array
(
[0] =>
)
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20967
[VALUE] => Array
(
[TEXT] => <p>Тапани Рууту</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Тапани Рууту
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20968
[VALUE] => Array
(
[TEXT] => <p>
Клинический исследовательский институт, Университетский госпиталь Хельсинки,<br>
Финляндия
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Клинический исследовательский институт, Университетский госпиталь Хельсинки,
Финляндия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20969
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">Трансплант-ассоциированная тромботическая микроангиопатия (ТА-ТМА) является сравнительно частым осложнением трансплантации гемопоэтических стволовых клеток (ТГСК). Ее патогенез весьма сложен, а центральным звеном является повреждение эндотелия. Все больше выясняется роль активации комплемента в патофизиологии процесса. Диагностические процедуры и интерпретация результатов существенно различаются между клиническими центрами, и здесь важны задачи стандартизации критериев диагностики этого осложнения особенно в исследовательских целях. Происходит совершенствование терапии, главным образом, благодаря применению ингибиторов комплемента.<br>
Однако показания и тактика назначения этих препаратов еще недостаточно установилась и требует дальнейшего изучения. </p>
<h2>Ключевые слова</h2>
<p style="text-align: justify;">Трансплантация гемопоэтических клеток, тромботическая микроангиопатия, диагностические методы, стандартизация, терапия, ингибиторы комплемента.</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Трансплант-ассоциированная тромботическая микроангиопатия (ТА-ТМА) является сравнительно частым осложнением трансплантации гемопоэтических стволовых клеток (ТГСК). Ее патогенез весьма сложен, а центральным звеном является повреждение эндотелия. Все больше выясняется роль активации комплемента в патофизиологии процесса. Диагностические процедуры и интерпретация результатов существенно различаются между клиническими центрами, и здесь важны задачи стандартизации критериев диагностики этого осложнения особенно в исследовательских целях. Происходит совершенствование терапии, главным образом, благодаря применению ингибиторов комплемента.
Однако показания и тактика назначения этих препаратов еще недостаточно установилась и требует дальнейшего изучения.
Ключевые слова
Трансплантация гемопоэтических клеток, тромботическая микроангиопатия, диагностические методы, стандартизация, терапия, ингибиторы комплемента.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20950
[VALUE] => 10.18620/ctt-1866-8836-2019-8-1-8-11
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 10.18620/ctt-1866-8836-2019-8-1-8-11
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20951
[VALUE] => Array
(
[TEXT] => <p>Tapani Ruutu </p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Tapani Ruutu
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20952
[VALUE] => Array
(
[TEXT] => <p>Clinical Research Institute, Helsinki University Hospital</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Clinical Research Institute, Helsinki University Hospital
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20953
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">
Transplant-associated thrombotic microangiopathy (TA-TMA) is a relatively common complication of hematopoietic stem cell transplantation. The pathophysiology is complex, the central feature is endothelial injury. The role of complement activation in the pathophysiology has been increasingly recognized. The diagnostic procedures and interpretations vary considerably between centers, and aims at standardizing the criteria of this complication are important especially for study purposes. The therapy is improving, particularly due to the introduction of complement inhibitors. However, the indications and policy of administration of these drugs are not well established and need further study.</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">Hemopoietic stem cell transplantation, thrombotic microangiopathy, diagnostic techniques, standardization, therapy, complement inhibitors.</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Transplant-associated thrombotic microangiopathy (TA-TMA) is a relatively common complication of hematopoietic stem cell transplantation. The pathophysiology is complex, the central feature is endothelial injury. The role of complement activation in the pathophysiology has been increasingly recognized. The diagnostic procedures and interpretations vary considerably between centers, and aims at standardizing the criteria of this complication are important especially for study purposes. The therapy is improving, particularly due to the introduction of complement inhibitors. However, the indications and policy of administration of these drugs are not well established and need further study.
Keywords
Hemopoietic stem cell transplantation, thrombotic microangiopathy, diagnostic techniques, standardization, therapy, complement inhibitors.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20954
[VALUE] => Recent developments in transplant-associated thrombotic microangiopathy
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Recent developments in transplant-associated thrombotic microangiopathy
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20955
[VALUE] => 1550
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1550
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20956
[VALUE] => 1551
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1551
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Тапани Рууту
Клинический исследовательский институт, Университетский госпиталь Хельсинки,
Финляндия
Трансплант-ассоциированная тромботическая микроангиопатия (ТА-ТМА) является сравнительно частым осложнением трансплантации гемопоэтических стволовых клеток (ТГСК). Ее патогенез весьма сложен, а центральным звеном является повреждение эндотелия. Все больше выясняется роль активации комплемента в патофизиологии процесса. Диагностические процедуры и интерпретация результатов существенно различаются между клиническими центрами, и здесь важны задачи стандартизации критериев диагностики этого осложнения особенно в исследовательских целях. Происходит совершенствование терапии, главным образом, благодаря применению ингибиторов комплемента.
Однако показания и тактика назначения этих препаратов еще недостаточно установилась и требует дальнейшего изучения.
Ключевые слова
Трансплантация гемопоэтических клеток, тромботическая микроангиопатия, диагностические методы, стандартизация, терапия, ингибиторы комплемента.
Обзорные статьи
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20972
[VALUE] => 04.03.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 04.03.2019
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20973
[VALUE] => 12.04.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 12.04.2019
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20974
[VALUE] => 119
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 119
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 22002
)
[VALUE] => Array
(
[0] => 119
)
[DESCRIPTION] => Array
(
[0] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 119
)
[~DESCRIPTION] => Array
(
[0] =>
)
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20993
[VALUE] => Array
(
[TEXT] => <p>Алексей Б. Чухловин <p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Алексей Б. Чухловин
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20994
[VALUE] => Array
(
[TEXT] => <p>НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия<p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20995
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">В течение последнего десятилетия появился целый ряд исследований, касающихся возможного применения «старых» медицинских препаратов в качестве дополнительных средств для лечения злокачественных новообразований. Есть следующие главные причины подобного расширения показаний для этих препаратов: (1) ограниченная эффективность и высокая стоимость новых таргетных ингибиторов онкогенных белков, или моноклональных антител для терапии; (2) выявление новых молекулярных мишеней для ряда препаратов, ранее внедренных по другим показаниям; (3) существенное снижение затрат на разработку новых средств терапии, осуществляемой «старыми» препаратами. Перечень таких «перенацеленных» препаратов сейчас включает десятки лекарств, которые часто используются, в частности, для лечения сердечно-сосудистых заболеваний, сахарного диабета, эпилепсии, различных воспалительных заболеваний. Данный обзор касается, главным образом, «переназначения» антиинфекционных препаратов, в т.ч. тех, которые используются для профилактики и лечения инфекционных осложнений, возникающих при цитостатической терапии лейкозов и лимфом, в частности – тетрациклинов, производных эритромицина, а также фторхинолонов, антивирусных препаратов и др. Противоопухолевые эффекты этих препаратов-кандидатов для «переназначение» были показаны при скрининге их цитостатических эффектов на линиях лейкозных и других злокачественных клеток. Некоторые исследования проведены на экспериментальных животных-опухоленосителях. Немногие клинические испытания были проведеныe в группах пациентов с лейкозами и лимфомами после трансплантации гемопоэтических стволовых клеток (ТГСК), которые показали некоторые позитивные эффекты антибактериальных препаратов в плане профилактики реакции «трансплантат против хозяина» (РТПХ) или увеличения продолжительности жизни пациентов. В этих целях необходимы контролируемые клинические исследования часто применяемых антиинфекционных препаратов. <p>
<h2>Ключевые слова</h2>
<p style="text-align: justify;">Антибактериальные препараты, переназначение, противоопухолевые эффекты, терапия лейкозов, трансплантация гемопоэтических стволовых клеток.</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
В течение последнего десятилетия появился целый ряд исследований, касающихся возможного применения «старых» медицинских препаратов в качестве дополнительных средств для лечения злокачественных новообразований. Есть следующие главные причины подобного расширения показаний для этих препаратов: (1) ограниченная эффективность и высокая стоимость новых таргетных ингибиторов онкогенных белков, или моноклональных антител для терапии; (2) выявление новых молекулярных мишеней для ряда препаратов, ранее внедренных по другим показаниям; (3) существенное снижение затрат на разработку новых средств терапии, осуществляемой «старыми» препаратами. Перечень таких «перенацеленных» препаратов сейчас включает десятки лекарств, которые часто используются, в частности, для лечения сердечно-сосудистых заболеваний, сахарного диабета, эпилепсии, различных воспалительных заболеваний. Данный обзор касается, главным образом, «переназначения» антиинфекционных препаратов, в т.ч. тех, которые используются для профилактики и лечения инфекционных осложнений, возникающих при цитостатической терапии лейкозов и лимфом, в частности – тетрациклинов, производных эритромицина, а также фторхинолонов, антивирусных препаратов и др. Противоопухолевые эффекты этих препаратов-кандидатов для «переназначение» были показаны при скрининге их цитостатических эффектов на линиях лейкозных и других злокачественных клеток. Некоторые исследования проведены на экспериментальных животных-опухоленосителях. Немногие клинические испытания были проведеныe в группах пациентов с лейкозами и лимфомами после трансплантации гемопоэтических стволовых клеток (ТГСК), которые показали некоторые позитивные эффекты антибактериальных препаратов в плане профилактики реакции «трансплантат против хозяина» (РТПХ) или увеличения продолжительности жизни пациентов. В этих целях необходимы контролируемые клинические исследования часто применяемых антиинфекционных препаратов.
Ключевые слова
Антибактериальные препараты, переназначение, противоопухолевые эффекты, терапия лейкозов, трансплантация гемопоэтических стволовых клеток.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20976
[VALUE] => 10.18620/ctt-1866-8836-2019-8-1-12-19
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 10.18620/ctt-1866-8836-2019-8-1-12-19
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20977
[VALUE] => Array
(
[TEXT] => <p>Alexey B. Chukhlovin <p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Alexey B. Chukhlovin
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20978
[VALUE] => Array
(
[TEXT] => <p>R.Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
R.Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20979
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">Over last decade, a number of studies has concerned possible implications of “old” medical drugs, as additional tools for cancer treatment. The main reasons for extension of drug indications are as follows: (1) limited efficiency or high costs of targeted oncogene protein inhibitors or specific monoclonal antibodies for therapy; (2) new molecular targets were revealed for some drugs traditionally used to other therapeutic purposes; and (3) sufficient decline of development costs for the new therapies performed by the “old” drugs. The list of such repurposed drugs now includes dozens of medications commonly used for treatment of cardiovascular diseases, diabetes mellitus, epilepsia, different inflammatory disorders. The present review deals, mainly, repurposing of anti-infectious drugs, including those used in prevention and management of infectious complications occurring in cytostatic therapy of leukemia and lymphomas, e.g., tetracyclines, erythromycin derivatives, as well as fluoroquinolones, antiviral compounds etc. <br>
The antitumor effects were of these candidates for repurposing were demonstrated upon screening of their cytostatic effects in leukemic and other cancer cell lines. Some studies were performed in experimental tumor-bearing animals. Only few clinical trials were carried out in patients with leukemias and lymphomas following hematopoietic stem cell transplantation (HSCT), which showed some positive effects of antibacterial drugs in terms of graft-versus-host disease (GvHD) prevention, or prolonged survival of the patients. Controlled clinical trials of common anti-infectious drugs are required for this repurposing.</p>
<h2>Keywords</h2>
<p style="text-align: justify;">Antibacterial drugs, repurposing, anticancer effects, leukemia treatment, hematopoietic stem cell transplantation. </p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Over last decade, a number of studies has concerned possible implications of “old” medical drugs, as additional tools for cancer treatment. The main reasons for extension of drug indications are as follows: (1) limited efficiency or high costs of targeted oncogene protein inhibitors or specific monoclonal antibodies for therapy; (2) new molecular targets were revealed for some drugs traditionally used to other therapeutic purposes; and (3) sufficient decline of development costs for the new therapies performed by the “old” drugs. The list of such repurposed drugs now includes dozens of medications commonly used for treatment of cardiovascular diseases, diabetes mellitus, epilepsia, different inflammatory disorders. The present review deals, mainly, repurposing of anti-infectious drugs, including those used in prevention and management of infectious complications occurring in cytostatic therapy of leukemia and lymphomas, e.g., tetracyclines, erythromycin derivatives, as well as fluoroquinolones, antiviral compounds etc.
The antitumor effects were of these candidates for repurposing were demonstrated upon screening of their cytostatic effects in leukemic and other cancer cell lines. Some studies were performed in experimental tumor-bearing animals. Only few clinical trials were carried out in patients with leukemias and lymphomas following hematopoietic stem cell transplantation (HSCT), which showed some positive effects of antibacterial drugs in terms of graft-versus-host disease (GvHD) prevention, or prolonged survival of the patients. Controlled clinical trials of common anti-infectious drugs are required for this repurposing.
Keywords
Antibacterial drugs, repurposing, anticancer effects, leukemia treatment, hematopoietic stem cell transplantation.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20980
[VALUE] => Drug repurposing in leukemia treatment and hematopoietic stem cell transplantation
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Drug repurposing in leukemia treatment and hematopoietic stem cell transplantation
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20996
[VALUE] => 1563
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1563
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20981
[VALUE] => 1562
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1562
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Алексей Б. Чухловин
НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
В течение последнего десятилетия появился целый ряд исследований, касающихся возможного применения «старых» медицинских препаратов в качестве дополнительных средств для лечения злокачественных новообразований. Есть следующие главные причины подобного расширения показаний для этих препаратов: (1) ограниченная эффективность и высокая стоимость новых таргетных ингибиторов онкогенных белков, или моноклональных антител для терапии; (2) выявление новых молекулярных мишеней для ряда препаратов, ранее внедренных по другим показаниям; (3) существенное снижение затрат на разработку новых средств терапии, осуществляемой «старыми» препаратами. Перечень таких «перенацеленных» препаратов сейчас включает десятки лекарств, которые часто используются, в частности, для лечения сердечно-сосудистых заболеваний, сахарного диабета, эпилепсии, различных воспалительных заболеваний. Данный обзор касается, главным образом, «переназначения» антиинфекционных препаратов, в т.ч. тех, которые используются для профилактики и лечения инфекционных осложнений, возникающих при цитостатической терапии лейкозов и лимфом, в частности – тетрациклинов, производных эритромицина, а также фторхинолонов, антивирусных препаратов и др. Противоопухолевые эффекты этих препаратов-кандидатов для «переназначение» были показаны при скрининге их цитостатических эффектов на линиях лейкозных и других злокачественных клеток. Некоторые исследования проведены на экспериментальных животных-опухоленосителях. Немногие клинические испытания были проведеныe в группах пациентов с лейкозами и лимфомами после трансплантации гемопоэтических стволовых клеток (ТГСК), которые показали некоторые позитивные эффекты антибактериальных препаратов в плане профилактики реакции «трансплантат против хозяина» (РТПХ) или увеличения продолжительности жизни пациентов. В этих целях необходимы контролируемые клинические исследования часто применяемых антиинфекционных препаратов.
Ключевые слова
Антибактериальные препараты, переназначение, противоопухолевые эффекты, терапия лейкозов, трансплантация гемопоэтических стволовых клеток.
Обзорные статьи
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21108
[VALUE] => 26.11.2018
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 26.11.2018
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21109
[VALUE] => 15.03.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 15.03.2019
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21086
[VALUE] => 525
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 525
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 22007
[1] => 22008
[2] => 22009
[3] => 22010
[4] => 22011
[5] => 22012
[6] => 22013
[7] => 22014
[8] => 22015
[9] => 22016
[10] => 22017
[11] => 22018
)
[VALUE] => Array
(
[0] => 525
[1] => 1617
[2] => 1618
[3] => 1619
[4] => 1620
[5] => 1621
[6] => 1622
[7] => 1623
[8] => 1624
[9] => 1625
[10] => 1626
[11] => 1627
)
[DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
[4] =>
[5] =>
[6] =>
[7] =>
[8] =>
[9] =>
[10] =>
[11] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 525
[1] => 1617
[2] => 1618
[3] => 1619
[4] => 1620
[5] => 1621
[6] => 1622
[7] => 1623
[8] => 1624
[9] => 1625
[10] => 1626
[11] => 1627
)
[~DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
[4] =>
[5] =>
[6] =>
[7] =>
[8] =>
[9] =>
[10] =>
[11] =>
)
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21161
[VALUE] => Array
(
[TEXT] => <p>Олег В. Галибин<sup>1</sup>, Герман В. Медведев<sup>2</sup>, Павел В. Попрядухин<sup>3</sup>, Павел А. Кулагин<sup>1</sup>, Александр А. Гусев<sup>1</sup>, Галина П. Косякова<sup>1</sup>, Наталья В. Михайлова<sup>1</sup>, Вероника Д. Новак<sup>1</sup>, Денис Н. Соломицкий<sup>1</sup>, Игорь О. Шемякин<sup>1</sup>, Вадим С. Гаджиагаев<sup>1</sup>, Максат Х. Гурбанназаров<sup>1</sup></p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Олег В. Галибин1, Герман В. Медведев2, Павел В. Попрядухин3, Павел А. Кулагин1, Александр А. Гусев1, Галина П. Косякова1, Наталья В. Михайлова1, Вероника Д. Новак1, Денис Н. Соломицкий1, Игорь О. Шемякин1, Вадим С. Гаджиагаев1, Максат Х. Гурбанназаров1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21162
[VALUE] => Array
(
[TEXT] => <p><sup>1</sup> Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова <br>
<sup>2</sup> Российский НИИ травматологии и ортопедии им. Р. Р. Вредена, Санкт-Петербург, Россия<br>
<sup>3</sup> Институт высокомолекулярных соединений РАН, Санкт-Петербург, Россия </p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова
2 Российский НИИ травматологии и ортопедии им. Р. Р. Вредена, Санкт-Петербург, Россия
3 Институт высокомолекулярных соединений РАН, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21163
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">Повреждение периферических нервов нередко сопровождается значительным диастазом (первичным или вторичным) между концами поврежденного нерва, что затрудняет выполнение стандартного ручного шва нерва с помощью хирургических нитей. На основании анализа данных опубликованных исследований выявлены эффективные способы хирургического лечения повреждений периферических нервов с диастазом. Кроме того, достоверно выявлены недостатки метода аутоневральной пластики, в связи с чем проблема преодоления диастаза поврежденного периферического нерва остается актуальной и в настоящее время, особенно при протяженных и множественных дефектах нервных стволов. Альтернативным вариантом в решении данной проблемы может служит использование имплантов, позволяющих соединить концы поврежденного нерва и способствующих прорастанию нервных волокон из центрального в периферический отросток поврежденного нерва. Использование биосовместимых и биодеградируемых полимеров в качестве неврального протеза способствует более безопасной регенерации и не требует выключения донорского нерва и связанной с ним функции, кроме того, разработаны и продолжают совершенствоваться опции, позволяющие влиять на скорость и качество регенерации поврежденного периферического нерва. </p>
<h2>Ключевые слова</h2>
<p style="text-align: justify;">Нерв, травма, диастаз, имплант, полимерная основа, хитозан. </p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Повреждение периферических нервов нередко сопровождается значительным диастазом (первичным или вторичным) между концами поврежденного нерва, что затрудняет выполнение стандартного ручного шва нерва с помощью хирургических нитей. На основании анализа данных опубликованных исследований выявлены эффективные способы хирургического лечения повреждений периферических нервов с диастазом. Кроме того, достоверно выявлены недостатки метода аутоневральной пластики, в связи с чем проблема преодоления диастаза поврежденного периферического нерва остается актуальной и в настоящее время, особенно при протяженных и множественных дефектах нервных стволов. Альтернативным вариантом в решении данной проблемы может служит использование имплантов, позволяющих соединить концы поврежденного нерва и способствующих прорастанию нервных волокон из центрального в периферический отросток поврежденного нерва. Использование биосовместимых и биодеградируемых полимеров в качестве неврального протеза способствует более безопасной регенерации и не требует выключения донорского нерва и связанной с ним функции, кроме того, разработаны и продолжают совершенствоваться опции, позволяющие влиять на скорость и качество регенерации поврежденного периферического нерва.
Ключевые слова
Нерв, травма, диастаз, имплант, полимерная основа, хитозан.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21099
[VALUE] => 10.18620/ctt-1866-8836-2019-8-1-20-25
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 10.18620/ctt-1866-8836-2019-8-1-20-25
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21122
[VALUE] => Array
(
[TEXT] => <p>Oleg V. Galibin<sup>1</sup>, German V. Medvedev<sup>2</sup>, Pavel V. Popryadukhin<sup>3</sup>, Pavel A. Kulagin<sup>1</sup>, Alexandr A. Gusev<sup>1</sup>, Galina P. Kossyakova<sup>1</sup>, Natalia V. Mikhailova<sup>1</sup>, Veronika D. Novak<sup>1</sup>, Denis N. Solomitskiy<sup>1</sup>, Igor O. Shemiakin<sup>1</sup>, Vadim S. Gadzhiagaev<sup>1</sup>, Maksat Kh. Gurbannazarov<sup>1</sup>
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Oleg V. Galibin1, German V. Medvedev2, Pavel V. Popryadukhin3, Pavel A. Kulagin1, Alexandr A. Gusev1, Galina P. Kossyakova1, Natalia V. Mikhailova1, Veronika D. Novak1, Denis N. Solomitskiy1, Igor O. Shemiakin1, Vadim S. Gadzhiagaev1, Maksat Kh. Gurbannazarov1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21123
[VALUE] => Array
(
[TEXT] => <p><sup>1</sup> First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia<br>
<sup>2</sup> Russian R. R.Wreden Research Institute of Traumatology and Orthopedy, St. Petersburg, Russia<br>
<sup>3</sup> Institute of Macromolecular Compounds, Russian Academy of Sciences, St. Petersburg, Russia</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
2 Russian R. R.Wreden Research Institute of Traumatology and Orthopedy, St. Petersburg, Russia
3 Institute of Macromolecular Compounds, Russian Academy of Sciences, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21164
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">Damage of peripheral nerves is often accompanied by a primary or secondary diastasis (gap, spread) between the neural ends, thus complicating a standard manual nerve stitching by means of surgical threads. As based on analysis of published data, the effective techniques were proposed for surgical treatment of peripheral nerve damage accompanied by diastasis. Moreover, some limitations of autoneural plastics are clearly revealed. Therefore, overcoming of nerve diastasis following damage remains to be a strong need, especially when treating prolonged and multiple defects of nerve trunks. Usage of implants providing repair and junction of the damaged nerve seems to be an alternative option allowing end-to-end connection of the damaged nerve from its central to distal segment. Application of biocompatible and bio-degradable polymers as a neural prosthesis promotes more safe regeneration and does not require switching-off a donor nerve and its functions. Moreover, the options are improved which allow to influence rates and quality of the nerve damage repair. <p>
<h2>Keywords</h2>
<p style="text-align: justify;">Nerve, damage, diastasis, implant, polymeric scaffolds, chitosan. </p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Damage of peripheral nerves is often accompanied by a primary or secondary diastasis (gap, spread) between the neural ends, thus complicating a standard manual nerve stitching by means of surgical threads. As based on analysis of published data, the effective techniques were proposed for surgical treatment of peripheral nerve damage accompanied by diastasis. Moreover, some limitations of autoneural plastics are clearly revealed. Therefore, overcoming of nerve diastasis following damage remains to be a strong need, especially when treating prolonged and multiple defects of nerve trunks. Usage of implants providing repair and junction of the damaged nerve seems to be an alternative option allowing end-to-end connection of the damaged nerve from its central to distal segment. Application of biocompatible and bio-degradable polymers as a neural prosthesis promotes more safe regeneration and does not require switching-off a donor nerve and its functions. Moreover, the options are improved which allow to influence rates and quality of the nerve damage repair.
Keywords
Nerve, damage, diastasis, implant, polymeric scaffolds, chitosan.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21100
[VALUE] => Alternative approaches to overcome diastasis of damaged peripheral nerves. A review article
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Alternative approaches to overcome diastasis of damaged peripheral nerves. A review article
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21165
[VALUE] => 1565
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1565
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21124
[VALUE] => 1564
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1564
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Олег В. Галибин1, Герман В. Медведев2, Павел В. Попрядухин3, Павел А. Кулагин1, Александр А. Гусев1, Галина П. Косякова1, Наталья В. Михайлова1, Вероника Д. Новак1, Денис Н. Соломицкий1, Игорь О. Шемякин1, Вадим С. Гаджиагаев1, Максат Х. Гурбанназаров1
1 Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова
2 Российский НИИ травматологии и ортопедии им. Р. Р. Вредена, Санкт-Петербург, Россия
3 Институт высокомолекулярных соединений РАН, Санкт-Петербург, Россия
Повреждение периферических нервов нередко сопровождается значительным диастазом (первичным или вторичным) между концами поврежденного нерва, что затрудняет выполнение стандартного ручного шва нерва с помощью хирургических нитей. На основании анализа данных опубликованных исследований выявлены эффективные способы хирургического лечения повреждений периферических нервов с диастазом. Кроме того, достоверно выявлены недостатки метода аутоневральной пластики, в связи с чем проблема преодоления диастаза поврежденного периферического нерва остается актуальной и в настоящее время, особенно при протяженных и множественных дефектах нервных стволов. Альтернативным вариантом в решении данной проблемы может служит использование имплантов, позволяющих соединить концы поврежденного нерва и способствующих прорастанию нервных волокон из центрального в периферический отросток поврежденного нерва. Использование биосовместимых и биодеградируемых полимеров в качестве неврального протеза способствует более безопасной регенерации и не требует выключения донорского нерва и связанной с ним функции, кроме того, разработаны и продолжают совершенствоваться опции, позволяющие влиять на скорость и качество регенерации поврежденного периферического нерва.
Ключевые слова
Нерв, травма, диастаз, имплант, полимерная основа, хитозан.
Клинические исследования
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21542
[VALUE] => 06.03.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 06.03.2019
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21543
[VALUE] => 15.03.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 15.03.2019
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21544
[VALUE] => 146
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 146
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 21606
[1] => 21607
[2] => 21608
[3] => 21609
[4] => 21610
[5] => 21611
[6] => 21612
[7] => 21613
[8] => 21614
)
[VALUE] => Array
(
[0] => 147
[1] => 146
[2] => 1633
[3] => 1634
[4] => 1635
[5] => 285
[6] => 1631
[7] => 60
[8] => 34
)
[DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
[4] =>
[5] =>
[6] =>
[7] =>
[8] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 147
[1] => 146
[2] => 1633
[3] => 1634
[4] => 1635
[5] => 285
[6] => 1631
[7] => 60
[8] => 34
)
[~DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
[4] =>
[5] =>
[6] =>
[7] =>
[8] =>
)
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21571
[VALUE] => Array
(
[TEXT] => <p>Елена В. Морозова, Мария В. Барабанщикова, Николай Ю. Цветков, Ксения В. Мельситова, Юлия В. Рудницкая, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Елена В. Морозова, Мария В. Барабанщикова, Николай Ю. Цветков, Ксения В. Мельситова, Юлия В. Рудницкая, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21572
[VALUE] => Array
(
[TEXT] => <p>НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета им. И. П. Павлова, Санкт-Петербург, Россия</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета им. И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21573
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">Разработан ряд предиктивных индексов для прогнозирования исхода у пациентов с миелодиспластическим синдромом (МДС). Целью нашего исследования была оценка прогностического вклада показателей заболевания и трансплантации в результаты аллогенной трансплантации гемопоэтических клеток (ТГСК) пациентам с МДС.</p>
<h3>Пациенты и методы</h3>
<p style="text-align: justify;">В ретроспективное исследование была включена группа из 53 пациентов с МДС (за исключением вторичного острого миелобластного лейкоза), леченных с применением алло-ТГСК. Целью работы была оценка предиктивной значимости следующих прогностических индексов: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), а также прогностической системы, предложенной Kroeger et al., Armand et al., индекса претрансплантационной оценки смертности (PAM), оценки риска по EBMT и ТГСК-специфичного индекса коморбидности (HCT-CI).</p>
<h3>Результаты</h3>
<p style="text-align: justify;">В результате работы показана достоверная разница в оценке риска при сравнении отдельных индексов (p <0,001). Были отмечены следующие клинические факторы, значимые для общей выживаемости (ОВ) в одно- и многофакторном анализе: острая реакция «трансплантат против хозяина» (ОРТПХ) I-II степени (HR 0,.223; 95% CI 0.059-0,721; p=0,0134) и возникновение сепсиса в период аплазии (HR 3,636; 95% CI 1,438-8,673; p=0,0059). Несмотря на значительный вклад числа CD34+ клеток в трансплантате, (p=0,006), выявленного посредством ROC-анализа, только индекс DRI являлся существенным средством прогноза 5-летней выживаемости в многофакторной модели (HR 1,857; 95% CI 1,036-3,328; p=0,037). Более низкая эффективность других МДС-специфичных индексов в прогнозировании исходов алло-ТГСК связана, по-видимому, с неблагоприятными исходами в группе промежуточного риска. В заключение мы должны отметить необходимость дальнейшей характеризации пациентов промежуточной группы риска при прогнозировании исхода лечения. </p>
<h2>Ключевые слова</h2>
<p style="text-align: justify;">Миелодиспластический синдром, аллогенная трансплантация гемопоэтических стволовых клеток, прогностические индексы, оценка риска.</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Разработан ряд предиктивных индексов для прогнозирования исхода у пациентов с миелодиспластическим синдромом (МДС). Целью нашего исследования была оценка прогностического вклада показателей заболевания и трансплантации в результаты аллогенной трансплантации гемопоэтических клеток (ТГСК) пациентам с МДС.
Пациенты и методы
В ретроспективное исследование была включена группа из 53 пациентов с МДС (за исключением вторичного острого миелобластного лейкоза), леченных с применением алло-ТГСК. Целью работы была оценка предиктивной значимости следующих прогностических индексов: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), а также прогностической системы, предложенной Kroeger et al., Armand et al., индекса претрансплантационной оценки смертности (PAM), оценки риска по EBMT и ТГСК-специфичного индекса коморбидности (HCT-CI).
Результаты
В результате работы показана достоверная разница в оценке риска при сравнении отдельных индексов (p <0,001). Были отмечены следующие клинические факторы, значимые для общей выживаемости (ОВ) в одно- и многофакторном анализе: острая реакция «трансплантат против хозяина» (ОРТПХ) I-II степени (HR 0,.223; 95% CI 0.059-0,721; p=0,0134) и возникновение сепсиса в период аплазии (HR 3,636; 95% CI 1,438-8,673; p=0,0059). Несмотря на значительный вклад числа CD34+ клеток в трансплантате, (p=0,006), выявленного посредством ROC-анализа, только индекс DRI являлся существенным средством прогноза 5-летней выживаемости в многофакторной модели (HR 1,857; 95% CI 1,036-3,328; p=0,037). Более низкая эффективность других МДС-специфичных индексов в прогнозировании исходов алло-ТГСК связана, по-видимому, с неблагоприятными исходами в группе промежуточного риска. В заключение мы должны отметить необходимость дальнейшей характеризации пациентов промежуточной группы риска при прогнозировании исхода лечения.
Ключевые слова
Миелодиспластический синдром, аллогенная трансплантация гемопоэтических стволовых клеток, прогностические индексы, оценка риска.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21554
[VALUE] => 10.18620/ctt-1866-8836-2019-8-1-36-45
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 10.18620/ctt-1866-8836-2019-8-1-36-45
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21584
[VALUE] => Array
(
[TEXT] => <p>Elena V. Morozova, Maria V. Barabanshikova, Nikolai Yu. Tcvetkov, Ksenia V. Melsitova, Julia V. Rudnitskaya, Elena I. Darskaya, Sergey N. Bondarenko, Ivan S. Moiseev, Boris V. Afanasyev</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Elena V. Morozova, Maria V. Barabanshikova, Nikolai Yu. Tcvetkov, Ksenia V. Melsitova, Julia V. Rudnitskaya, Elena I. Darskaya, Sergey N. Bondarenko, Ivan S. Moiseev, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21585
[VALUE] => Array
(
[TEXT] => <p>R. Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation, The First Pavlov St. Petersburg State Medical University, St. Petersburg, Russian Federation</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => R. Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation, The First Pavlov St. Petersburg State Medical University, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21586
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">Several prognostic indexes were developed to predict outcome in patients with myelodysplastic syndrome (MDS). The aim of our study was to evaluate prognostic impact of disease- and transplant-specific indexes on the results of allogeneic hematopoietic stem cell transplantation (allo-HSCT) in MDS patients.</p>
<h3>Patients and methods</h3>
<p style="text-align: justify;">A retrospective cohort of fifty-nine MDS patients (excluding secondary acute myeloid leukemia) and treated with allo-HSCT was used to evaluate the predictive value of the following prognostic indexes: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), prognostic systems developed by Kroeger et al., Armand et al., Pretransplant Assessment of Mortality Score (PAM), EBMT risk score and Hematopoietic Cell Transplantation-specific Comorbidity Index (HCT-CI).</p>
<h3>Results</h3>
<p style="text-align: justify;">There was a significant difference in risk estimation between indexes (p<0.001). Clinical factors significant for overall survival (OS) in the univariate and multivariate analyses were as follows: acute graft-versus-host disease (GVHD) grade I-II (HR 0.223, 95% CI 0.059-0.721, p=0.0134) and occurrence of sepsis during aplasia (HR 3.636, 95% CI 1.438-8.673, p=0.0059). Despite significant impact of CD34+ cell contents in hematopoietic graft (p=0.006) revealed in ROC analysis, only DRI remained a significant predictor of 5-year OS in the multivariate model (HR 1.857, 95% CI 1.036-3.328, p=0.037). Inferiority of other MDS-specific indexes to predict the outcome for allo-HSCT seems to be associated with adverse results in the intermediate risk group. In conclusion, we presume a need for further characterization of the intermediate risk patients when predicting the therapy outcomes. </p>
<h2>Keywords</h2>
<p style="text-align: justify;">Myelodysplastic syndrome, allogeneic hematopoietic stem cell transplantation, prognostic indexes, risk estimation. </p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Several prognostic indexes were developed to predict outcome in patients with myelodysplastic syndrome (MDS). The aim of our study was to evaluate prognostic impact of disease- and transplant-specific indexes on the results of allogeneic hematopoietic stem cell transplantation (allo-HSCT) in MDS patients.
Patients and methods
A retrospective cohort of fifty-nine MDS patients (excluding secondary acute myeloid leukemia) and treated with allo-HSCT was used to evaluate the predictive value of the following prognostic indexes: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), prognostic systems developed by Kroeger et al., Armand et al., Pretransplant Assessment of Mortality Score (PAM), EBMT risk score and Hematopoietic Cell Transplantation-specific Comorbidity Index (HCT-CI).
Results
There was a significant difference in risk estimation between indexes (p<0.001). Clinical factors significant for overall survival (OS) in the univariate and multivariate analyses were as follows: acute graft-versus-host disease (GVHD) grade I-II (HR 0.223, 95% CI 0.059-0.721, p=0.0134) and occurrence of sepsis during aplasia (HR 3.636, 95% CI 1.438-8.673, p=0.0059). Despite significant impact of CD34+ cell contents in hematopoietic graft (p=0.006) revealed in ROC analysis, only DRI remained a significant predictor of 5-year OS in the multivariate model (HR 1.857, 95% CI 1.036-3.328, p=0.037). Inferiority of other MDS-specific indexes to predict the outcome for allo-HSCT seems to be associated with adverse results in the intermediate risk group. In conclusion, we presume a need for further characterization of the intermediate risk patients when predicting the therapy outcomes.
Keywords
Myelodysplastic syndrome, allogeneic hematopoietic stem cell transplantation, prognostic indexes, risk estimation.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21555
[VALUE] => Application of standard and novel prognostic systems in patients with myelodys- plastic syndrome undergoing allogeneic hematopoietic stem cell transplantation
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Application of standard and novel prognostic systems in patients with myelodys- plastic syndrome undergoing allogeneic hematopoietic stem cell transplantation
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21574
[VALUE] => 1586
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1586
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21587
[VALUE] => 1588
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1588
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Елена В. Морозова, Мария В. Барабанщикова, Николай Ю. Цветков, Ксения В. Мельситова, Юлия В. Рудницкая, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев
НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета им. И. П. Павлова, Санкт-Петербург, Россия
Разработан ряд предиктивных индексов для прогнозирования исхода у пациентов с миелодиспластическим синдромом (МДС). Целью нашего исследования была оценка прогностического вклада показателей заболевания и трансплантации в результаты аллогенной трансплантации гемопоэтических клеток (ТГСК) пациентам с МДС.
Пациенты и методы
В ретроспективное исследование была включена группа из 53 пациентов с МДС (за исключением вторичного острого миелобластного лейкоза), леченных с применением алло-ТГСК. Целью работы была оценка предиктивной значимости следующих прогностических индексов: IPSS, IPSS-R, WPSS, Disease Risk Index (DRI), а также прогностической системы, предложенной Kroeger et al., Armand et al., индекса претрансплантационной оценки смертности (PAM), оценки риска по EBMT и ТГСК-специфичного индекса коморбидности (HCT-CI).
Результаты
В результате работы показана достоверная разница в оценке риска при сравнении отдельных индексов (p <0,001). Были отмечены следующие клинические факторы, значимые для общей выживаемости (ОВ) в одно- и многофакторном анализе: острая реакция «трансплантат против хозяина» (ОРТПХ) I-II степени (HR 0,.223; 95% CI 0.059-0,721; p=0,0134) и возникновение сепсиса в период аплазии (HR 3,636; 95% CI 1,438-8,673; p=0,0059). Несмотря на значительный вклад числа CD34+ клеток в трансплантате, (p=0,006), выявленного посредством ROC-анализа, только индекс DRI являлся существенным средством прогноза 5-летней выживаемости в многофакторной модели (HR 1,857; 95% CI 1,036-3,328; p=0,037). Более низкая эффективность других МДС-специфичных индексов в прогнозировании исходов алло-ТГСК связана, по-видимому, с неблагоприятными исходами в группе промежуточного риска. В заключение мы должны отметить необходимость дальнейшей характеризации пациентов промежуточной группы риска при прогнозировании исхода лечения.
Ключевые слова
Миелодиспластический синдром, аллогенная трансплантация гемопоэтических стволовых клеток, прогностические индексы, оценка риска.
Клинические исследования
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21325
[VALUE] => 14.03.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 14.03.2019
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21326
[VALUE] => 12.04.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 12.04.2019
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21327
[VALUE] => 1629
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1629
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 22033
[1] => 22034
[2] => 22035
[3] => 22036
[4] => 22037
[5] => 22038
[6] => 22039
[7] => 22040
[8] => 22041
[9] => 22042
[10] => 22043
[11] => 22044
)
[VALUE] => Array
(
[0] => 1629
[1] => 500
[2] => 60
[3] => 130
[4] => 180
[5] => 1630
[6] => 499
[7] => 285
[8] => 147
[9] => 1631
[10] => 42
[11] => 34
)
[DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
[4] =>
[5] =>
[6] =>
[7] =>
[8] =>
[9] =>
[10] =>
[11] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 1629
[1] => 500
[2] => 60
[3] => 130
[4] => 180
[5] => 1630
[6] => 499
[7] => 285
[8] => 147
[9] => 1631
[10] => 42
[11] => 34
)
[~DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
[4] =>
[5] =>
[6] =>
[7] =>
[8] =>
[9] =>
[10] =>
[11] =>
)
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21340
[VALUE] => Array
(
[TEXT] => <p>Анастасия В. Бейнарович, Елена В. Бабенко, Иван С. Моисеев, Олеся В. Паина, Ольга В. Пирогова,
Татьяна А. Рудакова, Татьяна Л. Гиндина, Елена И. Дарская, Елена В. Морозова, Сергей Н. Бондаренко,
Людмила С. Зубаровская, Борис В. Афанасьев</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Анастасия В. Бейнарович, Елена В. Бабенко, Иван С. Моисеев, Олеся В. Паина, Ольга В. Пирогова,
Татьяна А. Рудакова, Татьяна Л. Гиндина, Елена И. Дарская, Елена В. Морозова, Сергей Н. Бондаренко,
Людмила С. Зубаровская, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21341
[VALUE] => Array
(
[TEXT] => <p>НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета, Санкт-Петербург, Россия</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21342
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">Аллогенная трансплантация костного мозга (алло-
ТГСК) является потенциальной возможностью излечения злокачественных и незлокачественных заболеваний кроветворения. Для пациентов, у которых отсутствует HLA-совместимый сиблинг, можно использовать HLA-гаплоидентичного донора (гапло-ТГСК) в качестве альтернативного источника трансплантата. Преимуществом гапло-ТГСК является немедленная доступность донора для пациентов, которым необходимо выполнение трансплантации в короткие сроки. Кроме того, наличие родственного донора делает более доступной клеточную терапию после трансплантации. Также, большее несоответствие по генам HLA-системы в случае гаплоидентичной трансплантации, может потенциировать эффект «трансплантат против опухоли». В этом отчете представлен анализ результатов гапло-ТГСК, выполненных в нашем центре взрослым пациентам с различными злокачественными заболеваниями, при использовании неманипулированного трансплантата. На момент анализа медиана наблюдения составила 371 день (1-2219). Основным диагонозом был острый лейкоз. Шестидесяти семи пациентам (56%) гапло-ТГСК была выполнена в качестве терапии спасения. Общая выживаемость в течении 2 лет в исследуемой группе составила 40,3%. В частности, двухлетняя общая выживаемость у пациентов с ОЛЛ и ОМЛ в ремиссии заболевания, составила 57% и 46% соответственно в сравнении с 22% и 15% у пациентов с продвинутыми стадиями заболеваний. Безрецидивная выживаемость в течение 2 лет, а также выживаемость без проявлений оРТПХ и рецидива заболевания в общей группе составили 35,7% и 21% соответственно. Частота возникновения острой РТПХ II-IV степени и тяжелой РТПХ III-IV степени составили 19% и 10% соответственно. Частота хронической РТПХ составила 16%. Частота возникновения рецидива заболевания составила 21%. Трансплантационная летальность исследуемой группе 43%. В заключение необходимо отметить, что наши результаты показывают, что гапло-ТГСК с использованием неманипулированного трансплантата является приемлемым методом лечения взрослых пациентов с различными злокачественными заболеваниями кроветворения. Однако такие проблемы, как высокая частота неприживления, высокая трансплантационная летальность, а также посттрасплантационные рецидивы остаются чрезвычайно актуальными. </p>
<h2>Ключевые слова</h2>
<p style="text-align: justify;">Аллогенная трансплантация гемопоэтических стволовых клеток, гаплоидентичная, взрослые пациенты, общая выживаемость, рецидив после трансплантации, реакция «трансплантат против хозяина», неприживление трансплантатата, посттрансплантационный циклофосфамид. </p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Аллогенная трансплантация костного мозга (алло-
ТГСК) является потенциальной возможностью излечения злокачественных и незлокачественных заболеваний кроветворения. Для пациентов, у которых отсутствует HLA-совместимый сиблинг, можно использовать HLA-гаплоидентичного донора (гапло-ТГСК) в качестве альтернативного источника трансплантата. Преимуществом гапло-ТГСК является немедленная доступность донора для пациентов, которым необходимо выполнение трансплантации в короткие сроки. Кроме того, наличие родственного донора делает более доступной клеточную терапию после трансплантации. Также, большее несоответствие по генам HLA-системы в случае гаплоидентичной трансплантации, может потенциировать эффект «трансплантат против опухоли». В этом отчете представлен анализ результатов гапло-ТГСК, выполненных в нашем центре взрослым пациентам с различными злокачественными заболеваниями, при использовании неманипулированного трансплантата. На момент анализа медиана наблюдения составила 371 день (1-2219). Основным диагонозом был острый лейкоз. Шестидесяти семи пациентам (56%) гапло-ТГСК была выполнена в качестве терапии спасения. Общая выживаемость в течении 2 лет в исследуемой группе составила 40,3%. В частности, двухлетняя общая выживаемость у пациентов с ОЛЛ и ОМЛ в ремиссии заболевания, составила 57% и 46% соответственно в сравнении с 22% и 15% у пациентов с продвинутыми стадиями заболеваний. Безрецидивная выживаемость в течение 2 лет, а также выживаемость без проявлений оРТПХ и рецидива заболевания в общей группе составили 35,7% и 21% соответственно. Частота возникновения острой РТПХ II-IV степени и тяжелой РТПХ III-IV степени составили 19% и 10% соответственно. Частота хронической РТПХ составила 16%. Частота возникновения рецидива заболевания составила 21%. Трансплантационная летальность исследуемой группе 43%. В заключение необходимо отметить, что наши результаты показывают, что гапло-ТГСК с использованием неманипулированного трансплантата является приемлемым методом лечения взрослых пациентов с различными злокачественными заболеваниями кроветворения. Однако такие проблемы, как высокая частота неприживления, высокая трансплантационная летальность, а также посттрасплантационные рецидивы остаются чрезвычайно актуальными.
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, гаплоидентичная, взрослые пациенты, общая выживаемость, рецидив после трансплантации, реакция «трансплантат против хозяина», неприживление трансплантатата, посттрансплантационный циклофосфамид.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21343
[VALUE] => 10.18620/ctt-1866-8836-2019-8-1-26-35
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 10.18620/ctt-1866-8836-2019-8-1-26-35
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21394
[VALUE] => Array
(
[TEXT] => <p>Anastasia V. Beynarovich, Elena V. Babenko, Ivan S. Moiseev, Olesya V. Paina, Olga V. Pirogova, Tatiana A. Rudakova, Tatyana L. Gindina, Elena I. Darskaya, Elena V. Morozova, Sergey N. Bondarenko, Ludmila S. Zubarovskaya,
Boris V. Afanasyev</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Anastasia V. Beynarovich, Elena V. Babenko, Ivan S. Moiseev, Olesya V. Paina, Olga V. Pirogova, Tatiana A. Rudakova, Tatyana L. Gindina, Elena I. Darskaya, Elena V. Morozova, Sergey N. Bondarenko, Ludmila S. Zubarovskaya,
Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21395
[VALUE] => Array
(
[TEXT] => <p>R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantology at the First St. Petersburg State I. Pavlov Medical University</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantology at the First St. Petersburg State I. Pavlov Medical University
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21396
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">Allogeneic HSCT (allo-HSCT) is potentially curative option for a wide variety of malignant and nonmalignant disorders of hematopoiesis. For patients who lack an HLA-matched sibling, HLA-haploidentical related donors (haplo-HSCT) can be considered as alternative sources of donor grafts. The benefits of haplo-HSCT include immediate donor availability for patients who are in urgent need of the transplant. Besides, an availability of a related donor makes post-transplant donor-derived cellular therapy more easily accessible. In addition, the greater HLA mismatch associated with haploidentical HSCT (haplo-HSCT) may potentiate graft-versus-tumor (GVT) effects. The aim of our study was to summarize our single-center experience of haplo-HSCT performed with non-manipulated grafts in adult patients with different malignant diseases. The study included a total of 119 patients with different hematological disorders subjected to haplo-HSCT. At the time of analysis, median follow-up was 371 days (1-2219). Most frequent diagnosis in transplanted patients was acute leukemia. 67 (56%) patients received haplo-HSCT as salvage therapy.<br>
Overall survival with an observation term of 2 years was 40.3% for the general group. In particular, the two-year OS in patients transplanted in remissions of ALL and AML was 57% and 46% respectively as compared to 22% and 15% for the patients transplanted in adverse disease status). Two-year event-free survival (EFS) and GVHD-free/relapse-free survival (GRFS) group proved to be 35.7% and 21% respectively. The cumulative incidence of acute GVHD grade II-IV and severe aGVHD grade III-IV was 19% and 10% respectively. The cumulative incidence of chronic GVHD (cGVHD) was 16%.The cumulative incidence of relapse was 21%. The overall transplant-associated mortality was 43% in the studied group. In conclusion, our results show that unmanipulated haplo-HSCT is reasonable treatment option for adult patients with different malignant disorders of hematopoiesis. However, such problems as higher rate graft failure, increased nonrelapse mortality (NRM) and post-transplant relapses remain extremely relevant. </p>
<h2>Keywords</h2>
<p style="text-align: justify;">Allogeneic hematopoietic stem cell transplantation, haploidentical, adult patients, overall survival, post-transplant relapse, graft-versus-host disease, graft failure, post-transplant cyclophosphamide.</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Allogeneic HSCT (allo-HSCT) is potentially curative option for a wide variety of malignant and nonmalignant disorders of hematopoiesis. For patients who lack an HLA-matched sibling, HLA-haploidentical related donors (haplo-HSCT) can be considered as alternative sources of donor grafts. The benefits of haplo-HSCT include immediate donor availability for patients who are in urgent need of the transplant. Besides, an availability of a related donor makes post-transplant donor-derived cellular therapy more easily accessible. In addition, the greater HLA mismatch associated with haploidentical HSCT (haplo-HSCT) may potentiate graft-versus-tumor (GVT) effects. The aim of our study was to summarize our single-center experience of haplo-HSCT performed with non-manipulated grafts in adult patients with different malignant diseases. The study included a total of 119 patients with different hematological disorders subjected to haplo-HSCT. At the time of analysis, median follow-up was 371 days (1-2219). Most frequent diagnosis in transplanted patients was acute leukemia. 67 (56%) patients received haplo-HSCT as salvage therapy.
Overall survival with an observation term of 2 years was 40.3% for the general group. In particular, the two-year OS in patients transplanted in remissions of ALL and AML was 57% and 46% respectively as compared to 22% and 15% for the patients transplanted in adverse disease status). Two-year event-free survival (EFS) and GVHD-free/relapse-free survival (GRFS) group proved to be 35.7% and 21% respectively. The cumulative incidence of acute GVHD grade II-IV and severe aGVHD grade III-IV was 19% and 10% respectively. The cumulative incidence of chronic GVHD (cGVHD) was 16%.The cumulative incidence of relapse was 21%. The overall transplant-associated mortality was 43% in the studied group. In conclusion, our results show that unmanipulated haplo-HSCT is reasonable treatment option for adult patients with different malignant disorders of hematopoiesis. However, such problems as higher rate graft failure, increased nonrelapse mortality (NRM) and post-transplant relapses remain extremely relevant.
Keywords
Allogeneic hematopoietic stem cell transplantation, haploidentical, adult patients, overall survival, post-transplant relapse, graft-versus-host disease, graft failure, post-transplant cyclophosphamide.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21344
[VALUE] => Haploidentical stem cell transplantation in adults for the treatment of hematologic diseases: results of a single center (CIC725)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Haploidentical stem cell transplantation in adults for the treatment of hematologic diseases: results of a single center (CIC725)
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21345
[VALUE] => 1578
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1578
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21397
[VALUE] => 1579
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1579
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Анастасия В. Бейнарович, Елена В. Бабенко, Иван С. Моисеев, Олеся В. Паина, Ольга В. Пирогова, Татьяна А. Рудакова, Татьяна Л. Гиндина, Елена И. Дарская, Елена В. Морозова, Сергей Н. Бондаренко, Людмила С. Зубаровская, Борис В. Афанасьев
НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета, Санкт-Петербург, Россия
Аллогенная трансплантация костного мозга (алло- ТГСК) является потенциальной возможностью излечения злокачественных и незлокачественных заболеваний кроветворения. Для пациентов, у которых отсутствует HLA-совместимый сиблинг, можно использовать HLA-гаплоидентичного донора (гапло-ТГСК) в качестве альтернативного источника трансплантата. Преимуществом гапло-ТГСК является немедленная доступность донора для пациентов, которым необходимо выполнение трансплантации в короткие сроки. Кроме того, наличие родственного донора делает более доступной клеточную терапию после трансплантации. Также, большее несоответствие по генам HLA-системы в случае гаплоидентичной трансплантации, может потенциировать эффект «трансплантат против опухоли». В этом отчете представлен анализ результатов гапло-ТГСК, выполненных в нашем центре взрослым пациентам с различными злокачественными заболеваниями, при использовании неманипулированного трансплантата. На момент анализа медиана наблюдения составила 371 день (1-2219). Основным диагонозом был острый лейкоз. Шестидесяти семи пациентам (56%) гапло-ТГСК была выполнена в качестве терапии спасения. Общая выживаемость в течении 2 лет в исследуемой группе составила 40,3%. В частности, двухлетняя общая выживаемость у пациентов с ОЛЛ и ОМЛ в ремиссии заболевания, составила 57% и 46% соответственно в сравнении с 22% и 15% у пациентов с продвинутыми стадиями заболеваний. Безрецидивная выживаемость в течение 2 лет, а также выживаемость без проявлений оРТПХ и рецидива заболевания в общей группе составили 35,7% и 21% соответственно. Частота возникновения острой РТПХ II-IV степени и тяжелой РТПХ III-IV степени составили 19% и 10% соответственно. Частота хронической РТПХ составила 16%. Частота возникновения рецидива заболевания составила 21%. Трансплантационная летальность исследуемой группе 43%. В заключение необходимо отметить, что наши результаты показывают, что гапло-ТГСК с использованием неманипулированного трансплантата является приемлемым методом лечения взрослых пациентов с различными злокачественными заболеваниями кроветворения. Однако такие проблемы, как высокая частота неприживления, высокая трансплантационная летальность, а также посттрасплантационные рецидивы остаются чрезвычайно актуальными.
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, гаплоидентичная, взрослые пациенты, общая выживаемость, рецидив после трансплантации, реакция «трансплантат против хозяина», неприживление трансплантатата, посттрансплантационный циклофосфамид.
Клинические исследования
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21662
[VALUE] => 06.04.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 06.04.2019
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21663
[VALUE] => 15.04.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 15.04.2019
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21664
[VALUE] => 1637
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1637
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 21738
[1] => 21739
[2] => 21740
[3] => 21741
[4] => 21742
[5] => 21743
[6] => 21744
[7] => 21745
[8] => 21746
)
[VALUE] => Array
(
[0] => 1637
[1] => 1638
[2] => 130
[3] => 132
[4] => 1639
[5] => 764
[6] => 42
[7] => 1640
[8] => 34
)
[DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
[4] =>
[5] =>
[6] =>
[7] =>
[8] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 1637
[1] => 1638
[2] => 130
[3] => 132
[4] => 1639
[5] => 764
[6] => 42
[7] => 1640
[8] => 34
)
[~DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
[4] =>
[5] =>
[6] =>
[7] =>
[8] =>
)
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21674
[VALUE] => Array
(
[TEXT] => <p>Екатерина С. Утимишева<sup>1</sup>, Олег И. Долгов<sup>1</sup>, Олеся В. Паина<sup>1</sup>, Кирилл А. Екушов<sup>1</sup>, Алина А. Витрищак<sup>1</sup>, Борис И. Смирнов<sup>2</sup>, Людмила С. Зубаровская <sup>1</sup>, Сергей А. Карпищенко<sup>1</sup>, Борис В. Афанасьев<sup>1</sup></p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Екатерина С. Утимишева1, Олег И. Долгов1, Олеся В. Паина1, Кирилл А. Екушов1, Алина А. Витрищак1, Борис И. Смирнов2, Людмила С. Зубаровская 1, Сергей А. Карпищенко1, Борис В. Афанасьев1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21675
[VALUE] => Array
(
[TEXT] => <p><sup>1</sup> Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Россия<br>
<sup>2</sup> Санкт-Петербургский государственный электротехнический университет «ЛЭТИ», Россия</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Россия
2 Санкт-Петербургский государственный электротехнический университет «ЛЭТИ», Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21676
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">Синусит после аллогенной трансплантации гемопоэтических стволовых клеток возникает в 22,2% случаев с более высокой частотой после 100 дня от алло-ТГСК, чем до 100 (р=0,006). Основными факторами риска возникновения синусита после аллогенной трансплантации гемопоэтических стволовых клеток являлись: синусит до алло-ТГСК (р <0,001), длительность нейтропении более 10 дней (р=0,054), наличие у пациентов острой (р=0,022) или хронической «реакции трансплантат против хозяина»
(р <0,001). Основными возбудителями острых синуситов у реципиентов алло-ТГСК в исследовании являлись грамположительные бактерии <i>Staphylococcus epidermidis </i>(30%), <i>Streptococcus viridans</i> (30%), грамотрицательные бактерии <i>Klebsiella pneumoniae</i> (17,5%). Монокультура бактерий преобладала до 100 дня от алло-ТГСК (р=0,011). У пациентов подросткового возраста чаще наблюдался полиэтиологичный характер возбудителей синусита по сравнению с группой «дети». Степень тяжести изменений околоносовых пазух на компьютерной томографии после 100 дня от алло-ТГСК более выражена (р=0,014), что находится в дисбалансе с меньшим количеством клинических симптомов синусита (р=0,008) и более частым течением синусита в легкой степени при оценке по визуальной аналоговой шкале (р=0,032) в этот период. Применение пункций верхнечелюстных пазух в сочетании с противомикробной терапией сокращает сроки лечения синусита у этих пациентов (р=0,024). </p>
<h2>Ключевые слова</h2>
<p style="text-align: justify;">Синусит, дети, трансплантация гемопоэтических клеток, клинические особенности.</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Синусит после аллогенной трансплантации гемопоэтических стволовых клеток возникает в 22,2% случаев с более высокой частотой после 100 дня от алло-ТГСК, чем до 100 (р=0,006). Основными факторами риска возникновения синусита после аллогенной трансплантации гемопоэтических стволовых клеток являлись: синусит до алло-ТГСК (р <0,001), длительность нейтропении более 10 дней (р=0,054), наличие у пациентов острой (р=0,022) или хронической «реакции трансплантат против хозяина»
(р <0,001). Основными возбудителями острых синуситов у реципиентов алло-ТГСК в исследовании являлись грамположительные бактерии Staphylococcus epidermidis (30%), Streptococcus viridans (30%), грамотрицательные бактерии Klebsiella pneumoniae (17,5%). Монокультура бактерий преобладала до 100 дня от алло-ТГСК (р=0,011). У пациентов подросткового возраста чаще наблюдался полиэтиологичный характер возбудителей синусита по сравнению с группой «дети». Степень тяжести изменений околоносовых пазух на компьютерной томографии после 100 дня от алло-ТГСК более выражена (р=0,014), что находится в дисбалансе с меньшим количеством клинических симптомов синусита (р=0,008) и более частым течением синусита в легкой степени при оценке по визуальной аналоговой шкале (р=0,032) в этот период. Применение пункций верхнечелюстных пазух в сочетании с противомикробной терапией сокращает сроки лечения синусита у этих пациентов (р=0,024).
Ключевые слова
Синусит, дети, трансплантация гемопоэтических клеток, клинические особенности.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21677
[VALUE] => 10.18620/ctt-1866-8836-2019-8-1-46-53
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 10.18620/ctt-1866-8836-2019-8-1-46-53
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21689
[VALUE] => Array
(
[TEXT] => <p>Ekaterina S. Utimisheva<sup>1</sup>, Oleg I. Dolgov<sup>1</sup>, Olesya V. Paina<sup>1</sup>, Kirill A. Ekushov<sup>1</sup>, Alina A. Vitrischak<sup>1</sup>, Boris I. Smirnov<sup>2</sup>, Ludmila S. Zubarovskaya<sup>1</sup>, Sergey A. Karpischenko<sup>1</sup>, Boris V. Afanasyev<sup>1</sup></p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Ekaterina S. Utimisheva1, Oleg I. Dolgov1, Olesya V. Paina1, Kirill A. Ekushov1, Alina A. Vitrischak1, Boris I. Smirnov2, Ludmila S. Zubarovskaya1, Sergey A. Karpischenko1, Boris V. Afanasyev1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21690
[VALUE] => Array
(
[TEXT] => <p><sup>1</sup> Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia<br>
<sup>2</sup> St. Petersburg State Electrotechnical University LETI, St. Petersburg, Russia</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia
2 St. Petersburg State Electrotechnical University LETI, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21691
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">Sinusitis after allogeneic transplantation of hematopoietic stem cells occurs in 22.2% of cases being more frequent at >100 days following allo-HSCT, than at earlier terms (p=0.006). The main risk factors for sinusitis after allogeneic stem cell transplantation were as follows: sinusitis before allo-HSCT (p <0.001), neutropenia duration for more than 10 days (p=0.054), acute (p=0.022) or chronic graft-versus-host disease (p <0.001) in the patients. The main pathogens of sinusitis revealed in allo-HSCT recipients during the study were: Gram-positive <i>Staphylococcus epidermidis</i> (30%), <i>Streptococcus viridans</i> (30%); Gram-negative <i>Klebsiella pneumoniae</i> (17.5%). A monoculture of bacteria predominated within 100 days posttransplant (p=0.011). Poly-etiological origin of the causative bacterial agents in sinusitis was more likely in adolescent patients, in comparison to the younger children group. The severity of changes in paranasal sinuses, as registered with computed tomography after 100 days after allo-HSCT, was more pronounced (p=0.014) than at earlier terms, thus being discordant with less common clinical signs of sinusitis (p=0.008), and milder clinical course of sinusitis assessed by a visual analogue scale (p=0.032) during this period. Punctures of maxillary sinuses combined with antimicrobial therapy proved to shorten the duration of sinusitis treatment in these patients (p=0.024).</p>
<h2>Keywords</h2>
<p style="text-align: justify;">Sinusitis, children, hematopoietic stem cell transplantation.</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Sinusitis after allogeneic transplantation of hematopoietic stem cells occurs in 22.2% of cases being more frequent at >100 days following allo-HSCT, than at earlier terms (p=0.006). The main risk factors for sinusitis after allogeneic stem cell transplantation were as follows: sinusitis before allo-HSCT (p <0.001), neutropenia duration for more than 10 days (p=0.054), acute (p=0.022) or chronic graft-versus-host disease (p <0.001) in the patients. The main pathogens of sinusitis revealed in allo-HSCT recipients during the study were: Gram-positive Staphylococcus epidermidis (30%), Streptococcus viridans (30%); Gram-negative Klebsiella pneumoniae (17.5%). A monoculture of bacteria predominated within 100 days posttransplant (p=0.011). Poly-etiological origin of the causative bacterial agents in sinusitis was more likely in adolescent patients, in comparison to the younger children group. The severity of changes in paranasal sinuses, as registered with computed tomography after 100 days after allo-HSCT, was more pronounced (p=0.014) than at earlier terms, thus being discordant with less common clinical signs of sinusitis (p=0.008), and milder clinical course of sinusitis assessed by a visual analogue scale (p=0.032) during this period. Punctures of maxillary sinuses combined with antimicrobial therapy proved to shorten the duration of sinusitis treatment in these patients (p=0.024).
Keywords
Sinusitis, children, hematopoietic stem cell transplantation.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21678
[VALUE] => Incidence, diagnosis and treatment of sinusitis in children and adolescents after hematopoietic stem cell transplantation
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Incidence, diagnosis and treatment of sinusitis in children and adolescents after hematopoietic stem cell transplantation
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21679
[VALUE] => 1595
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1595
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21692
[VALUE] => 1597
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1597
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Екатерина С. Утимишева1, Олег И. Долгов1, Олеся В. Паина1, Кирилл А. Екушов1, Алина А. Витрищак1, Борис И. Смирнов2, Людмила С. Зубаровская 1, Сергей А. Карпищенко1, Борис В. Афанасьев1
1 Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Россия
2 Санкт-Петербургский государственный электротехнический университет «ЛЭТИ», Россия
Синусит после аллогенной трансплантации гемопоэтических стволовых клеток возникает в 22,2% случаев с более высокой частотой после 100 дня от алло-ТГСК, чем до 100 (р=0,006). Основными факторами риска возникновения синусита после аллогенной трансплантации гемопоэтических стволовых клеток являлись: синусит до алло-ТГСК (р <0,001), длительность нейтропении более 10 дней (р=0,054), наличие у пациентов острой (р=0,022) или хронической «реакции трансплантат против хозяина» (р <0,001). Основными возбудителями острых синуситов у реципиентов алло-ТГСК в исследовании являлись грамположительные бактерии Staphylococcus epidermidis (30%), Streptococcus viridans (30%), грамотрицательные бактерии Klebsiella pneumoniae (17,5%). Монокультура бактерий преобладала до 100 дня от алло-ТГСК (р=0,011). У пациентов подросткового возраста чаще наблюдался полиэтиологичный характер возбудителей синусита по сравнению с группой «дети». Степень тяжести изменений околоносовых пазух на компьютерной томографии после 100 дня от алло-ТГСК более выражена (р=0,014), что находится в дисбалансе с меньшим количеством клинических симптомов синусита (р=0,008) и более частым течением синусита в легкой степени при оценке по визуальной аналоговой шкале (р=0,032) в этот период. Применение пункций верхнечелюстных пазух в сочетании с противомикробной терапией сокращает сроки лечения синусита у этих пациентов (р=0,024).
Ключевые слова
Синусит, дети, трансплантация гемопоэтических клеток, клинические особенности.
Клинический случай
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21766
[VALUE] => 08.04.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 08.04.2019
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21767
[VALUE] => 26.04.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 26.04.2019
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21768
[VALUE] => 1642
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1642
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 21803
[1] => 21804
[2] => 21805
[3] => 21806
[4] => 21807
[5] => 21808
[6] => 21809
[7] => 21810
)
[VALUE] => Array
(
[0] => 1642
[1] => 303
[2] => 1643
[3] => 133
[4] => 498
[5] => 502
[6] => 42
[7] => 34
)
[DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
[4] =>
[5] =>
[6] =>
[7] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 1642
[1] => 303
[2] => 1643
[3] => 133
[4] => 498
[5] => 502
[6] => 42
[7] => 34
)
[~DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
[4] =>
[5] =>
[6] =>
[7] =>
)
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21777
[VALUE] => Array
(
[TEXT] => <p>Татьяна А. Быкова, Варвара Н. Овечкина, Анна А. Осипова, Андрей В. Козлов, Александр Л. Алянский,
Елена В. Семенова, Людмила С. Зубаровская, Борис В. Афанасьев</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Татьяна А. Быкова, Варвара Н. Овечкина, Анна А. Осипова, Андрей В. Козлов, Александр Л. Алянский,
Елена В. Семенова, Людмила С. Зубаровская, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21778
[VALUE] => Array
(
[TEXT] => <p>НИИ детской онкологии, гематологии и тнрансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и тнрансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21779
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">Семейный гемофагоцитарный лимфогистиоцитоз (гемофагоцитарный синдром) – редкое наследственное заболевание, в основе которого лежит нарушение регуляции иммунного ответа, приводящее к пролиферации и активации гистиоцитов, фагоцитозу клеток периферической крови. Своевременная диагностика и специфическая комбинированная иммуносупрессивная и химиотерапия с последующей алло-ТГСК значительно увеличивают вероятность благоприятного исхода болезни. Описывается случай семейного гемофагоцитарного лимфогистиоцитоза у трех сибсов, который был ассоциирован с мутацией <i>UNC13D</i> в гетерозиготной форме. Экспрессия клинической симптоматики у сибсов была различной как по характеру течения, так и по прогнозу заболевания. </p>
<h2>Ключевые слова</h2>
<p style="text-align: justify;">Семейный гемофагоцитарный лимфогистиоцитоз, гемофагоцитарный синдром, алло-ТГСК.</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Семейный гемофагоцитарный лимфогистиоцитоз (гемофагоцитарный синдром) – редкое наследственное заболевание, в основе которого лежит нарушение регуляции иммунного ответа, приводящее к пролиферации и активации гистиоцитов, фагоцитозу клеток периферической крови. Своевременная диагностика и специфическая комбинированная иммуносупрессивная и химиотерапия с последующей алло-ТГСК значительно увеличивают вероятность благоприятного исхода болезни. Описывается случай семейного гемофагоцитарного лимфогистиоцитоза у трех сибсов, который был ассоциирован с мутацией UNC13D в гетерозиготной форме. Экспрессия клинической симптоматики у сибсов была различной как по характеру течения, так и по прогнозу заболевания.
Ключевые слова
Семейный гемофагоцитарный лимфогистиоцитоз, гемофагоцитарный синдром, алло-ТГСК.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21780
[VALUE] => 10.18620/ctt-1866-8836-2019-8-1-54-57
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 10.18620/ctt-1866-8836-2019-8-1-54-57
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21791
[VALUE] => Array
(
[TEXT] => <p>Tatiana A. Bykova, Varvara N. Ovechkina, Anna A. Osipova, Andrey V. Kozlov, Alexander L. Alyanskiy, Elena V. Semenova, Ludmila S. Zubarovskaya, Boris V. Afanasyev</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Tatiana A. Bykova, Varvara N. Ovechkina, Anna A. Osipova, Andrey V. Kozlov, Alexander L. Alyanskiy, Elena V. Semenova, Ludmila S. Zubarovskaya, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21792
[VALUE] => Array
(
[TEXT] => <p>R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation; Department of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I.Pavlov Medical University, St. Petersburg, Russia</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation; Department of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I.Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21793
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">Familial hemophagocytic lymphohistiocytosis (hemophagocytic syndrome) is a rare hereditary disease, characterized by dysregulation of the immune response, leading to the proliferation and activation of histiocytes, phagocytosis of peripheral blood cells. Timely diagnostics, specific combined immunosuppressive therapy and chemotherapy followed by allo-HSCT significantly increase the chances for a favorable outcome. We are presenting a case of family hemophagocytic lymphohistiocytosis associated with <i>UNC13D</i> mutation which was found in three siblings who exhibited quite different course of the disease and clinical prognosis. </p>
<h2>Keywords</h2>
<p style="text-align: justify;">Familial hemophagocytic lymphohistiocytosis, hemophagocytic syndrome, hematopoietic stem cell transplantation.</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Familial hemophagocytic lymphohistiocytosis (hemophagocytic syndrome) is a rare hereditary disease, characterized by dysregulation of the immune response, leading to the proliferation and activation of histiocytes, phagocytosis of peripheral blood cells. Timely diagnostics, specific combined immunosuppressive therapy and chemotherapy followed by allo-HSCT significantly increase the chances for a favorable outcome. We are presenting a case of family hemophagocytic lymphohistiocytosis associated with UNC13D mutation which was found in three siblings who exhibited quite different course of the disease and clinical prognosis.
Keywords
Familial hemophagocytic lymphohistiocytosis, hemophagocytic syndrome, hematopoietic stem cell transplantation.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21781
[VALUE] => A clinical case of familial hemophagocytic lymphohistiocytosis
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => A clinical case of familial hemophagocytic lymphohistiocytosis
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21782
[VALUE] => 1607
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1607
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21794
[VALUE] => 1608
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1608
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Татьяна А. Быкова, Варвара Н. Овечкина, Анна А. Осипова, Андрей В. Козлов, Александр Л. Алянский, Елена В. Семенова, Людмила С. Зубаровская, Борис В. Афанасьев
НИИ детской онкологии, гематологии и тнрансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
Семейный гемофагоцитарный лимфогистиоцитоз (гемофагоцитарный синдром) – редкое наследственное заболевание, в основе которого лежит нарушение регуляции иммунного ответа, приводящее к пролиферации и активации гистиоцитов, фагоцитозу клеток периферической крови. Своевременная диагностика и специфическая комбинированная иммуносупрессивная и химиотерапия с последующей алло-ТГСК значительно увеличивают вероятность благоприятного исхода болезни. Описывается случай семейного гемофагоцитарного лимфогистиоцитоза у трех сибсов, который был ассоциирован с мутацией UNC13D в гетерозиготной форме. Экспрессия клинической симптоматики у сибсов была различной как по характеру течения, так и по прогнозу заболевания.
Ключевые слова
Семейный гемофагоцитарный лимфогистиоцитоз, гемофагоцитарный синдром, алло-ТГСК.
Экспериментальные исследования
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21845
[VALUE] => 20.03.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 20.03.2019
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21846
[VALUE] => 15.04.2019
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 15.04.2019
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21847
[VALUE] => 1645
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1645
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] => Array
(
[0] => 21848
[1] => 21849
[2] => 21850
[3] => 21851
)
[VALUE] => Array
(
[0] => 1645
[1] => 1646
[2] => 1647
[3] => 1648
)
[DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
)
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[0] => 1645
[1] => 1646
[2] => 1647
[3] => 1648
)
[~DESCRIPTION] => Array
(
[0] =>
[1] =>
[2] =>
[3] =>
)
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21852
[VALUE] => Array
(
[TEXT] => <p>Александр В. Кузнецов<sup>1</sup>, Ильдар Р. Фахрадиев<sup>2</sup>, Ыдырыс А. Алмабаев<sup>3</sup>, Айгуль Ы. Алмабаева<sup>4</sup></p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Александр В. Кузнецов1, Ильдар Р. Фахрадиев2, Ыдырыс А. Алмабаев3, Айгуль Ы. Алмабаева4
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21853
[VALUE] => Array
(
[TEXT] => <p><sup>1</sup> Доктор медицинских наук, преподаватель кафедры анатомии человека НГМУ, Новосибирск, Россия<br>
<sup>2</sup> Заведующий лабораторией экспериментальной медицины, КазНМУ им. С. Д. Асфендиярова, Республика Казахстан<br>
<sup>3</sup> Доктор медицинских наук, профессор, заведующий кафедрой клинической анатомии и оперативной хирургии
в КазНМУ им. С. Д. Асфендиярова, Республика Казахстан<br>
<sup>4</sup> Профессор, кафедра анатомии с оперативной хирургией, Медицинский университет Астана, г. Астана, Республика Казахстан</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Доктор медицинских наук, преподаватель кафедры анатомии человека НГМУ, Новосибирск, Россия
2 Заведующий лабораторией экспериментальной медицины, КазНМУ им. С. Д. Асфендиярова, Республика Казахстан
3 Доктор медицинских наук, профессор, заведующий кафедрой клинической анатомии и оперативной хирургии
в КазНМУ им. С. Д. Асфендиярова, Республика Казахстан
4 Профессор, кафедра анатомии с оперативной хирургией, Медицинский университет Астана, г. Астана, Республика Казахстан
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21854
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">Целью нашей работы было определение возможных взаимосвязей между уровнем митозов клеток в лимфе грудного протока (ГЛП), возрастом организма и числом лимфоцитов в эксперименте (27 интактных кроликов Шиншилла, 120-2,500 гр. в возрасте 1,5-36 недель). Образцы клеток забирали из цистерны грудного протока анестезированных животных. Количество митотических клеток подсчитывали в процентах от общего количества лимфоцитов и в абсолютных значениях после учета в мазках, окрашенных по Гимза. Результаты обрабатывались статистическими методами с помощью Microsoft Office Excel 2007. Корреляция между указанными выше данными определялась с помощью критерия Пирсона. Количество митотических клеточных форм в лимфе ГЛП уменьшалось по мере увеличения возраста кроликов (от 1,5-36 недель, новорожденные и растущие особи). Максимум митотической активности обнаружен у кроликов 1,5 недельного возраста (23,0 ± 0,14, P=0.02) в сравнении с таковым у кроликов 4,5 и 13,5 недельного возраста (11,0 ± 0,14*,
P<0,05 и 6,3 ± 0,08**, P<0,001, соответственно).
Абсолютное же количество клеток лимфы в ГЛП повышалось с возрастом животных. Минимальную концентрацию клеток обнаруживали у 1,5 недельных кроликов (2,8 ± 0,03, P=0.04), в сравнении с уровнями у 36-недельных кроликов (5,9 ± 0,05, P=0,03). Сильная негативная корреляция найдена между митотической активностью клеток ГЛП и возрастом, а также общей клеточностью лимфы. Выявлена положительная корреляция между числом клеток в ГЛП и возрастом животных (соответственно, R<sup>2</sup>=0,7; R<sup>2</sup>=0,96 и R<sup>2</sup>=0,8) (диапазон возраста – от 1,5 до 36 недель). Найденная взаимосвязь между пролиферацией и числом клеток грудного протока у растущих животных обнаружена впервые. Полученные данные позволяют предположить наличие оптимальных комбинаций цитокинов и других биоактивных факторов, регулирующих митотическую активность клеток грудного протока с возрастом. </p>
<h2>Ключевые слова</h2>
<p style="text-align: justify;">Грудной лимфатический проток, клеточная популяция, кролики, митотическая активность, возрастные изменения. </p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Целью нашей работы было определение возможных взаимосвязей между уровнем митозов клеток в лимфе грудного протока (ГЛП), возрастом организма и числом лимфоцитов в эксперименте (27 интактных кроликов Шиншилла, 120-2,500 гр. в возрасте 1,5-36 недель). Образцы клеток забирали из цистерны грудного протока анестезированных животных. Количество митотических клеток подсчитывали в процентах от общего количества лимфоцитов и в абсолютных значениях после учета в мазках, окрашенных по Гимза. Результаты обрабатывались статистическими методами с помощью Microsoft Office Excel 2007. Корреляция между указанными выше данными определялась с помощью критерия Пирсона. Количество митотических клеточных форм в лимфе ГЛП уменьшалось по мере увеличения возраста кроликов (от 1,5-36 недель, новорожденные и растущие особи). Максимум митотической активности обнаружен у кроликов 1,5 недельного возраста (23,0 ± 0,14, P=0.02) в сравнении с таковым у кроликов 4,5 и 13,5 недельного возраста (11,0 ± 0,14*,
P<0,05 и 6,3 ± 0,08**, P<0,001, соответственно).
Абсолютное же количество клеток лимфы в ГЛП повышалось с возрастом животных. Минимальную концентрацию клеток обнаруживали у 1,5 недельных кроликов (2,8 ± 0,03, P=0.04), в сравнении с уровнями у 36-недельных кроликов (5,9 ± 0,05, P=0,03). Сильная негативная корреляция найдена между митотической активностью клеток ГЛП и возрастом, а также общей клеточностью лимфы. Выявлена положительная корреляция между числом клеток в ГЛП и возрастом животных (соответственно, R2=0,7; R2=0,96 и R2=0,8) (диапазон возраста – от 1,5 до 36 недель). Найденная взаимосвязь между пролиферацией и числом клеток грудного протока у растущих животных обнаружена впервые. Полученные данные позволяют предположить наличие оптимальных комбинаций цитокинов и других биоактивных факторов, регулирующих митотическую активность клеток грудного протока с возрастом.
Ключевые слова
Грудной лимфатический проток, клеточная популяция, кролики, митотическая активность, возрастные изменения.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21855
[VALUE] => 10.18620/ctt-1866-8836-2019-8-1-58-65
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 10.18620/ctt-1866-8836-2019-8-1-58-65
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21856
[VALUE] => Array
(
[TEXT] => <p>Alexander V. Kuznetsov<sup>1</sup>, Ildar R. Fakhradiyev<sup>2</sup>, Ydyrys A. Almabayev<sup>3</sup>, Aigul Y. Almabayeva<sup>4</sup></p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Alexander V. Kuznetsov1, Ildar R. Fakhradiyev2, Ydyrys A. Almabayev3, Aigul Y. Almabayeva4
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21857
[VALUE] => Array
(
[TEXT] => <p><sup>1</sup> Department of Human Anatomy, Novosibirsk State Medical University, Russia <br>
<sup>2</sup> Laboratory of Experimental Medicine, Kazakh National Medical University, Republic of Kazakhstan<br>
<sup>3</sup> Department of Clinical Anatomy, Kazakh National Medical University, Republic of Kazakhstan<br>
<sup>4</sup> Department of Human Anatomy with O.S. Medical University Astana, Republic of Kazakhstan</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Department of Human Anatomy, Novosibirsk State Medical University, Russia
2 Laboratory of Experimental Medicine, Kazakh National Medical University, Republic of Kazakhstan
3 Department of Clinical Anatomy, Kazakh National Medical University, Republic of Kazakhstan
4 Department of Human Anatomy with O.S. Medical University Astana, Republic of Kazakhstan
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 21858
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">The aim of this study was to assess correlations between rabbit mitotic thoracic duct (TD) cells, rabbit’s age, and TD lymphocytes. The experiments were carried out in 27 intact male Chinchilla rabbits weighing 120-2.500 g (at the age of 1.5 weeks to 36 weeks). TD lymph specimens were drawn from the cisterna chyli of anaesthetised rabbits. The numbers of mitotic cells from TD <i>per</i> 100 cells, and absolute numbers of TD lymphocytes were counted in the Giemsa-stained cell smears by means of routine light microscope methods, and routine hemocytometric counts. We have performed statistical evaluation of the data by Microsoft Office Excel 2007 software. Correlations between the TD mitotic cell ratio, lymphocyte numbers, and animal age was estimated by Pearson’s criteria. The mitotic cell number in TD lymph decreased from the age of 1.5 weeks (infant animals) to 36 weeks (young adult rabbits). Maximal mitotic activity was found in rabbits at 1.5 week of age (23.0 ± 0.14, P=0.02) in comparison with appropriate indexes in rabbits at 4.5 and 13.5 weeks of age (11.0 ± 0.14*, P<0.05 and 6.3 ± 0.08**, P<0.001 respectively). In contrast to mitotic cell amounts, the absolute TD lymphocyte numbers were increased in older rabbits. The minimal TD; lymphocyte number in the 1.5-week old rabbits aged was 2.8 ± 0.03, being significantly different (P=0.04) against the lymphocyte numbers in rabbits aged 36 week (5.9 ± 0.05, P=0.03). Hence, strong negative correlations were found between the TD mitotic activity and age, mitotic cells and total TD lymphocyte numbers, as well as positive correlation between the TD lymphocytes and age (respectively, R<sup>2</sup>=0.7, R<sup>2</sup>=0.96 and R<sup>2</sup>=0.8) in immature rabbits (age from 1.5 weeks to 36 weeks). To our knowledge, these interrelations for TD lymph cells in the very young animals were detected for the first time. We conclude that the age-related correlation between mitotic activity and total lymphocyte amounts in TD allows presume optimal combinations of cytokines and other bioactive factors that regulate mitotic activity of thoracic duct cells with advancing age.</p>
<h2>Keywords</h2>
<p style="text-align: justify;">Thoracic lymphatic duct, cell population, mitotic activity, age-dependent changes.</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => The aim of this study was to assess correlations between rabbit mitotic thoracic duct (TD) cells, rabbit’s age, and TD lymphocytes. The experiments were carried out in 27 intact male Chinchilla rabbits weighing 120-2.500 g (at the age of 1.5 weeks to 36 weeks). TD lymph specimens were drawn from the cisterna chyli of anaesthetised rabbits. The numbers of mitotic cells from TD per 100 cells, and absolute numbers of TD lymphocytes were counted in the Giemsa-stained cell smears by means of routine light microscope methods, and routine hemocytometric counts. We have performed statistical evaluation of the data by Microsoft Office Excel 2007 software. Correlations between the TD mitotic cell ratio, lymphocyte numbers, and animal age was estimated by Pearson’s criteria. The mitotic cell number in TD lymph decreased from the age of 1.5 weeks (infant animals) to 36 weeks (young adult rabbits). Maximal mitotic activity was found in rabbits at 1.5 week of age (23.0 ± 0.14, P=0.02) in comparison with appropriate indexes in rabbits at 4.5 and 13.5 weeks of age (11.0 ± 0.14*, P<0.05 and 6.3 ± 0.08**, P<0.001 respectively). In contrast to mitotic cell amounts, the absolute TD lymphocyte numbers were increased in older rabbits. The minimal TD; lymphocyte number in the 1.5-week old rabbits aged was 2.8 ± 0.03, being significantly different (P=0.04) against the lymphocyte numbers in rabbits aged 36 week (5.9 ± 0.05, P=0.03). Hence, strong negative correlations were found between the TD mitotic activity and age, mitotic cells and total TD lymphocyte numbers, as well as positive correlation between the TD lymphocytes and age (respectively, R2=0.7, R2=0.96 and R2=0.8) in immature rabbits (age from 1.5 weeks to 36 weeks). To our knowledge, these interrelations for TD lymph cells in the very young animals were detected for the first time. We conclude that the age-related correlation between mitotic activity and total lymphocyte amounts in TD allows presume optimal combinations of cytokines and other bioactive factors that regulate mitotic activity of thoracic duct cells with advancing age.
Keywords
Thoracic lymphatic duct, cell population, mitotic activity, age-dependent changes.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21859
[VALUE] => Mitotic activity of thoracic duct cells in rabbits correlates with age and total lymphocyte numbers
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Mitotic activity of thoracic duct cells in rabbits correlates with age and total lymphocyte numbers
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21860
[VALUE] => 1616
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1616
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 21861
[VALUE] => 1617
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1617
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Александр В. Кузнецов1, Ильдар Р. Фахрадиев2, Ыдырыс А. Алмабаев3, Айгуль Ы. Алмабаева4
1 Доктор медицинских наук, преподаватель кафедры анатомии человека НГМУ, Новосибирск, Россия
2 Заведующий лабораторией экспериментальной медицины, КазНМУ им. С. Д. Асфендиярова, Республика Казахстан
3 Доктор медицинских наук, профессор, заведующий кафедрой клинической анатомии и оперативной хирургии
в КазНМУ им. С. Д. Асфендиярова, Республика Казахстан
4 Профессор, кафедра анатомии с оперативной хирургией, Медицинский университет Астана, г. Астана, Республика Казахстан
Целью нашей работы было определение возможных взаимосвязей между уровнем митозов клеток в лимфе грудного протока (ГЛП), возрастом организма и числом лимфоцитов в эксперименте (27 интактных кроликов Шиншилла, 120-2,500 гр. в возрасте 1,5-36 недель). Образцы клеток забирали из цистерны грудного протока анестезированных животных. Количество митотических клеток подсчитывали в процентах от общего количества лимфоцитов и в абсолютных значениях после учета в мазках, окрашенных по Гимза. Результаты обрабатывались статистическими методами с помощью Microsoft Office Excel 2007. Корреляция между указанными выше данными определялась с помощью критерия Пирсона. Количество митотических клеточных форм в лимфе ГЛП уменьшалось по мере увеличения возраста кроликов (от 1,5-36 недель, новорожденные и растущие особи). Максимум митотической активности обнаружен у кроликов 1,5 недельного возраста (23,0 ± 0,14, P=0.02) в сравнении с таковым у кроликов 4,5 и 13,5 недельного возраста (11,0 ± 0,14*, P<0,05 и 6,3 ± 0,08**, P<0,001, соответственно). Абсолютное же количество клеток лимфы в ГЛП повышалось с возрастом животных. Минимальную концентрацию клеток обнаруживали у 1,5 недельных кроликов (2,8 ± 0,03, P=0.04), в сравнении с уровнями у 36-недельных кроликов (5,9 ± 0,05, P=0,03). Сильная негативная корреляция найдена между митотической активностью клеток ГЛП и возрастом, а также общей клеточностью лимфы. Выявлена положительная корреляция между числом клеток в ГЛП и возрастом животных (соответственно, R2=0,7; R2=0,96 и R2=0,8) (диапазон возраста – от 1,5 до 36 недель). Найденная взаимосвязь между пролиферацией и числом клеток грудного протока у растущих животных обнаружена впервые. Полученные данные позволяют предположить наличие оптимальных комбинаций цитокинов и других биоактивных факторов, регулирующих митотическую активность клеток грудного протока с возрастом.
Ключевые слова
Грудной лимфатический проток, клеточная популяция, кролики, митотическая активность, возрастные изменения.

