Введение
Роль аптеки в детской больнице и предоставляемые услуги сейчас значительно шире, чем 5 лет назад. Во всей Европе больницы стремятся переложить ответственность за приготовление препаратов, особенно стерильных, на фармацевтов, тем самым облегчив труд медсестер. Цель приготовления препаратов в больничной аптеке – получить качественный, стерильный, готовый для ввода пациенту препарат, приготовленный в особых, удобных и безопасных для работников условиях с соблюдением рационального использования медикаментов.
Цели
Наши задачи были следующими: а) Выяснить, какие условия необходимо соблюсти для создания асептического блока в больничной аптеке. Изучить требования, необходимые проверки, проблемы; б) Выяснить, какие есть особенности безопасного и качественного приготовления и оборота в больнице цитотоксичных препаратов; в) Исследовать трудности приготовления антибиотиков для парэнтерального ввода в больничной аптеке; г) Исследовать нужды больницы и рецепты парэнтерального питания, его оборот и приготовление с помощью аппарата (компаундера).
Результаты
А) Для работы асептического блока в больничной аптеке необходимы чистые помещения, специальная вентиляция, ламинарные шкафы, микробиологическая валидация, валидация работников, особенные одноразовые одежды и принадлежности, санитарный график. Чтобы не столкнуться с проблемами, рекомендуется заранее разработать проект с четкой целью, какие препараты аптека будет готовить. Б) Для цитотоксичных препаратов необходимо негативное давление в отдельном помещении для готовки, специальный ламинарный шкаф для цитотоксичных препаратов, защитные очки и маска, специальные перчатки, обученный персонал, специальные одноразовые принадлежности, в том числе закрытые системы переноса лекарств, а также может быть очень полезна программатура для приготовления и назначения препаратов. В) Обеспечивая парэнтеральными антибиотиками пациентов больницы можно столкнуться с разными проблемами, как то: плохой контакт с врачебным персоналом, частая смена доз антибиотиков, частая смена антибиотиков в связи с анализами, отмена уже приготовленных антибиотиков, короткая стабильность антибактериальных препаратов, а также отсутствие материальной выгоды в централизации готовки дешевых антибиотиков. Г) Пациентам больницы необходима как индивидуальная рецептура парэнтерального питания, так и стандартные смеси, введенные в пользование для младенцев, детей от 3 до 15 кг и от 15 до 30 кг. Компаундера улучшает качество рабочих условий персонала, уменьшает количество ручного труда, ускоряет время приготовления, но требует минимум двух человек для обслуживания.
Выводы
У централизованного приготовления парэнтеральных препаратов в аптеке Детской больницы есть свои преимущества и недостатки. Одни из главных преимуществ – длительный срок годности приготовленных препаратов, безопасность приготовления токсичных лекарств для персонала, минимизация мануального труда работников, рациональное использование лекарственных средств. В больничной аптеке можно добиться нужного качества и условий приготовления, централизовав процесс, пройдя необходимые проверки, поддерживая уровень чистоты каждый день и наладив контакты с врачебным персоналом. Процесс можно бесконечно улучшать. Главные цели на будущее: обоюдное сотрудничество с врачебным персоналом, механизирование однообразных процессов, компьютеризирование всех рецептов, проверки несовместимостей препаратов и усовершенствование способа заказа препаратов врачами.
Ключевые слова
Парэнтеральное лечение, цитотоксические препараты, аптека, правила работы, логистика, детская больница.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20437" ["VALUE"]=> array(2) { ["TEXT"]=> string(21) "Svetlana A. Griskjane" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(21) "Svetlana A. Griskjane" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20438" ["VALUE"]=> array(2) { ["TEXT"]=> string(56) "Children’s Clinical University Hospital, Riga, Latvija" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(56) "Children’s Clinical University Hospital, Riga, Latvija" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20439" ["VALUE"]=> array(2) { ["TEXT"]=> string(4262) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> The role of pharmacy in the Children’s Hospital and the services provided are now much wider than 5 years ago. In Europe hospitals are trying to shift the responsibility for preparing drugs, especially sterile ones, for pharmacists, thereby facilitating the work of nurses. The purpose of preparing drugs in a hospital pharmacy is to obtain a high-quality, sterile, ready-for-use medication prepared in special, convenient and safe conditions for workers, ensuring rational use of medicines. </p> <h2 style="text-align: justify;">Aims</h2> <p style="text-align: justify;"> Our aims were as follows: (a) To find out what conditions must be met to create an aseptic unit in a hospital pharmacy, to study appropriate requirements, necessary inspections, current problems; (b) To assess features of safe and quality preparation and turnover of cytotoxic drugs in the hospital; (c) To investigate the difficulties of preparing antibiotics for parenteral administration in a hospital pharmacy, and (d) To investigate the needs of the hospital and variety of prescriptions of parenteral nutrition, their turnover and preparation with automatic compounder device. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> (a) For aseptic unit in a hospital pharmacy clean room, special ventilation, laminar flow cabinets, microbiological validation, validation of employees, special disposable clothing and accessories, sanitary schedule are necessary. In order not to face problems, it is recommended to develop a project in advance with a clear goal, which preparations the pharmacy will prepare. (b) For cytotoxic drugs, negative pressure is required in a separate preparation area, a special laminar flow cabinet for cytotoxic drugs, goggles and a mask, special gloves, trained personnel, special disposable supplies, including closed drug transfer systems, and also a program for preparation and prescription of drugs could be useful. (c) Providing parenteral antibiotics to hospital patients can face various problems, such as: poor contact with medical staff, frequent changes of antibiotic doses, frequent changes in antibiotics due to analysis, cancellation of already prepared antibiotics, short stability of antibacterial drugs, and lack of material benefit in centralized preparation of cheap antibiotics. (d) The patients at the hospital need both individual formulas of parenteral nutrition, and standard mixtures introduced for administration to infants, children from 3 to 15 kg and from 15 to 30 kg body mass. The compounder devices improve quality of working conditions for personnel, reduce the amount of manual labor, speed up the preparation time, but require a minimum of two persons for their maintenance. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> The centralized preparation of parenteral drugs at the pharmacy of the Children’s Hospital has its advantages and disadvantages. One of the main advantages is the long shelf-life of the prepared medications, the safety of preparation of toxic drugs for personnel, the minimization of the manual labor for employees, the rational use of medicines. In the hospital pharmacy, you can achieve the desired quality and preparation conditions, centralizing the process, passing the required checks, maintaining purity levels every day, and establishing contacts with medical personnel. The process can be improved permanently. The main future goals are as follows: mutual cooperation with medical personnel, mechanization of monotonous processes, computer-assisted support of all prescriptions, incompatibility checking, and improving the way of ordering drugs by the doctors. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Parenteral treatment, cytotoxic preparations, pharmacy, working regulations, logistics, pediatric hospital. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4030) "Introduction
The role of pharmacy in the Children’s Hospital and the services provided are now much wider than 5 years ago. In Europe hospitals are trying to shift the responsibility for preparing drugs, especially sterile ones, for pharmacists, thereby facilitating the work of nurses. The purpose of preparing drugs in a hospital pharmacy is to obtain a high-quality, sterile, ready-for-use medication prepared in special, convenient and safe conditions for workers, ensuring rational use of medicines.
Aims
Our aims were as follows: (a) To find out what conditions must be met to create an aseptic unit in a hospital pharmacy, to study appropriate requirements, necessary inspections, current problems; (b) To assess features of safe and quality preparation and turnover of cytotoxic drugs in the hospital; (c) To investigate the difficulties of preparing antibiotics for parenteral administration in a hospital pharmacy, and (d) To investigate the needs of the hospital and variety of prescriptions of parenteral nutrition, their turnover and preparation with automatic compounder device.
Results
(a) For aseptic unit in a hospital pharmacy clean room, special ventilation, laminar flow cabinets, microbiological validation, validation of employees, special disposable clothing and accessories, sanitary schedule are necessary. In order not to face problems, it is recommended to develop a project in advance with a clear goal, which preparations the pharmacy will prepare. (b) For cytotoxic drugs, negative pressure is required in a separate preparation area, a special laminar flow cabinet for cytotoxic drugs, goggles and a mask, special gloves, trained personnel, special disposable supplies, including closed drug transfer systems, and also a program for preparation and prescription of drugs could be useful. (c) Providing parenteral antibiotics to hospital patients can face various problems, such as: poor contact with medical staff, frequent changes of antibiotic doses, frequent changes in antibiotics due to analysis, cancellation of already prepared antibiotics, short stability of antibacterial drugs, and lack of material benefit in centralized preparation of cheap antibiotics. (d) The patients at the hospital need both individual formulas of parenteral nutrition, and standard mixtures introduced for administration to infants, children from 3 to 15 kg and from 15 to 30 kg body mass. The compounder devices improve quality of working conditions for personnel, reduce the amount of manual labor, speed up the preparation time, but require a minimum of two persons for their maintenance.
Conclusions
The centralized preparation of parenteral drugs at the pharmacy of the Children’s Hospital has its advantages and disadvantages. One of the main advantages is the long shelf-life of the prepared medications, the safety of preparation of toxic drugs for personnel, the minimization of the manual labor for employees, the rational use of medicines. In the hospital pharmacy, you can achieve the desired quality and preparation conditions, centralizing the process, passing the required checks, maintaining purity levels every day, and establishing contacts with medical personnel. The process can be improved permanently. The main future goals are as follows: mutual cooperation with medical personnel, mechanization of monotonous processes, computer-assisted support of all prescriptions, incompatibility checking, and improving the way of ordering drugs by the doctors.
Keywords
Parenteral treatment, cytotoxic preparations, pharmacy, working regulations, logistics, pediatric hospital.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20440" ["VALUE"]=> string(100) "Preparation of parenteral medications in Riga Children’s Clinical University Hospital’s pharmacy" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(100) "Preparation of parenteral medications in Riga Children’s Clinical University Hospital’s pharmacy" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20767" ["VALUE"]=> string(4) "1403" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1403" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20768" ["VALUE"]=> string(4) "1404" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1404" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20437" ["VALUE"]=> array(2) { ["TEXT"]=> string(21) "Svetlana A. Griskjane" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(21) "Svetlana A. Griskjane" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(21) "Svetlana A. Griskjane" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20439" ["VALUE"]=> array(2) { ["TEXT"]=> string(4262) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> The role of pharmacy in the Children’s Hospital and the services provided are now much wider than 5 years ago. In Europe hospitals are trying to shift the responsibility for preparing drugs, especially sterile ones, for pharmacists, thereby facilitating the work of nurses. The purpose of preparing drugs in a hospital pharmacy is to obtain a high-quality, sterile, ready-for-use medication prepared in special, convenient and safe conditions for workers, ensuring rational use of medicines. </p> <h2 style="text-align: justify;">Aims</h2> <p style="text-align: justify;"> Our aims were as follows: (a) To find out what conditions must be met to create an aseptic unit in a hospital pharmacy, to study appropriate requirements, necessary inspections, current problems; (b) To assess features of safe and quality preparation and turnover of cytotoxic drugs in the hospital; (c) To investigate the difficulties of preparing antibiotics for parenteral administration in a hospital pharmacy, and (d) To investigate the needs of the hospital and variety of prescriptions of parenteral nutrition, their turnover and preparation with automatic compounder device. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> (a) For aseptic unit in a hospital pharmacy clean room, special ventilation, laminar flow cabinets, microbiological validation, validation of employees, special disposable clothing and accessories, sanitary schedule are necessary. In order not to face problems, it is recommended to develop a project in advance with a clear goal, which preparations the pharmacy will prepare. (b) For cytotoxic drugs, negative pressure is required in a separate preparation area, a special laminar flow cabinet for cytotoxic drugs, goggles and a mask, special gloves, trained personnel, special disposable supplies, including closed drug transfer systems, and also a program for preparation and prescription of drugs could be useful. (c) Providing parenteral antibiotics to hospital patients can face various problems, such as: poor contact with medical staff, frequent changes of antibiotic doses, frequent changes in antibiotics due to analysis, cancellation of already prepared antibiotics, short stability of antibacterial drugs, and lack of material benefit in centralized preparation of cheap antibiotics. (d) The patients at the hospital need both individual formulas of parenteral nutrition, and standard mixtures introduced for administration to infants, children from 3 to 15 kg and from 15 to 30 kg body mass. The compounder devices improve quality of working conditions for personnel, reduce the amount of manual labor, speed up the preparation time, but require a minimum of two persons for their maintenance. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> The centralized preparation of parenteral drugs at the pharmacy of the Children’s Hospital has its advantages and disadvantages. One of the main advantages is the long shelf-life of the prepared medications, the safety of preparation of toxic drugs for personnel, the minimization of the manual labor for employees, the rational use of medicines. In the hospital pharmacy, you can achieve the desired quality and preparation conditions, centralizing the process, passing the required checks, maintaining purity levels every day, and establishing contacts with medical personnel. The process can be improved permanently. The main future goals are as follows: mutual cooperation with medical personnel, mechanization of monotonous processes, computer-assisted support of all prescriptions, incompatibility checking, and improving the way of ordering drugs by the doctors. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Parenteral treatment, cytotoxic preparations, pharmacy, working regulations, logistics, pediatric hospital. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4030) "Introduction
The role of pharmacy in the Children’s Hospital and the services provided are now much wider than 5 years ago. In Europe hospitals are trying to shift the responsibility for preparing drugs, especially sterile ones, for pharmacists, thereby facilitating the work of nurses. The purpose of preparing drugs in a hospital pharmacy is to obtain a high-quality, sterile, ready-for-use medication prepared in special, convenient and safe conditions for workers, ensuring rational use of medicines.
Aims
Our aims were as follows: (a) To find out what conditions must be met to create an aseptic unit in a hospital pharmacy, to study appropriate requirements, necessary inspections, current problems; (b) To assess features of safe and quality preparation and turnover of cytotoxic drugs in the hospital; (c) To investigate the difficulties of preparing antibiotics for parenteral administration in a hospital pharmacy, and (d) To investigate the needs of the hospital and variety of prescriptions of parenteral nutrition, their turnover and preparation with automatic compounder device.
Results
(a) For aseptic unit in a hospital pharmacy clean room, special ventilation, laminar flow cabinets, microbiological validation, validation of employees, special disposable clothing and accessories, sanitary schedule are necessary. In order not to face problems, it is recommended to develop a project in advance with a clear goal, which preparations the pharmacy will prepare. (b) For cytotoxic drugs, negative pressure is required in a separate preparation area, a special laminar flow cabinet for cytotoxic drugs, goggles and a mask, special gloves, trained personnel, special disposable supplies, including closed drug transfer systems, and also a program for preparation and prescription of drugs could be useful. (c) Providing parenteral antibiotics to hospital patients can face various problems, such as: poor contact with medical staff, frequent changes of antibiotic doses, frequent changes in antibiotics due to analysis, cancellation of already prepared antibiotics, short stability of antibacterial drugs, and lack of material benefit in centralized preparation of cheap antibiotics. (d) The patients at the hospital need both individual formulas of parenteral nutrition, and standard mixtures introduced for administration to infants, children from 3 to 15 kg and from 15 to 30 kg body mass. The compounder devices improve quality of working conditions for personnel, reduce the amount of manual labor, speed up the preparation time, but require a minimum of two persons for their maintenance.
Conclusions
The centralized preparation of parenteral drugs at the pharmacy of the Children’s Hospital has its advantages and disadvantages. One of the main advantages is the long shelf-life of the prepared medications, the safety of preparation of toxic drugs for personnel, the minimization of the manual labor for employees, the rational use of medicines. In the hospital pharmacy, you can achieve the desired quality and preparation conditions, centralizing the process, passing the required checks, maintaining purity levels every day, and establishing contacts with medical personnel. The process can be improved permanently. The main future goals are as follows: mutual cooperation with medical personnel, mechanization of monotonous processes, computer-assisted support of all prescriptions, incompatibility checking, and improving the way of ordering drugs by the doctors.
Keywords
Parenteral treatment, cytotoxic preparations, pharmacy, working regulations, logistics, pediatric hospital.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4030) "Introduction
The role of pharmacy in the Children’s Hospital and the services provided are now much wider than 5 years ago. In Europe hospitals are trying to shift the responsibility for preparing drugs, especially sterile ones, for pharmacists, thereby facilitating the work of nurses. The purpose of preparing drugs in a hospital pharmacy is to obtain a high-quality, sterile, ready-for-use medication prepared in special, convenient and safe conditions for workers, ensuring rational use of medicines.
Aims
Our aims were as follows: (a) To find out what conditions must be met to create an aseptic unit in a hospital pharmacy, to study appropriate requirements, necessary inspections, current problems; (b) To assess features of safe and quality preparation and turnover of cytotoxic drugs in the hospital; (c) To investigate the difficulties of preparing antibiotics for parenteral administration in a hospital pharmacy, and (d) To investigate the needs of the hospital and variety of prescriptions of parenteral nutrition, their turnover and preparation with automatic compounder device.
Results
(a) For aseptic unit in a hospital pharmacy clean room, special ventilation, laminar flow cabinets, microbiological validation, validation of employees, special disposable clothing and accessories, sanitary schedule are necessary. In order not to face problems, it is recommended to develop a project in advance with a clear goal, which preparations the pharmacy will prepare. (b) For cytotoxic drugs, negative pressure is required in a separate preparation area, a special laminar flow cabinet for cytotoxic drugs, goggles and a mask, special gloves, trained personnel, special disposable supplies, including closed drug transfer systems, and also a program for preparation and prescription of drugs could be useful. (c) Providing parenteral antibiotics to hospital patients can face various problems, such as: poor contact with medical staff, frequent changes of antibiotic doses, frequent changes in antibiotics due to analysis, cancellation of already prepared antibiotics, short stability of antibacterial drugs, and lack of material benefit in centralized preparation of cheap antibiotics. (d) The patients at the hospital need both individual formulas of parenteral nutrition, and standard mixtures introduced for administration to infants, children from 3 to 15 kg and from 15 to 30 kg body mass. The compounder devices improve quality of working conditions for personnel, reduce the amount of manual labor, speed up the preparation time, but require a minimum of two persons for their maintenance.
Conclusions
The centralized preparation of parenteral drugs at the pharmacy of the Children’s Hospital has its advantages and disadvantages. One of the main advantages is the long shelf-life of the prepared medications, the safety of preparation of toxic drugs for personnel, the minimization of the manual labor for employees, the rational use of medicines. In the hospital pharmacy, you can achieve the desired quality and preparation conditions, centralizing the process, passing the required checks, maintaining purity levels every day, and establishing contacts with medical personnel. The process can be improved permanently. The main future goals are as follows: mutual cooperation with medical personnel, mechanization of monotonous processes, computer-assisted support of all prescriptions, incompatibility checking, and improving the way of ordering drugs by the doctors.
Keywords
Parenteral treatment, cytotoxic preparations, pharmacy, working regulations, logistics, pediatric hospital.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20440" ["VALUE"]=> string(100) "Preparation of parenteral medications in Riga Children’s Clinical University Hospital’s pharmacy" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(100) "Preparation of parenteral medications in Riga Children’s Clinical University Hospital’s pharmacy" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(100) "Preparation of parenteral medications in Riga Children’s Clinical University Hospital’s pharmacy" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20438" ["VALUE"]=> array(2) { ["TEXT"]=> string(56) "Children’s Clinical University Hospital, Riga, Latvija" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(56) "Children’s Clinical University Hospital, Riga, Latvija" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(56) "Children’s Clinical University Hospital, Riga, Latvija" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20434" ["VALUE"]=> array(2) { ["TEXT"]=> string(37) "Светлана А. Гришкяне" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(37) "Светлана А. Гришкяне" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(37) "Светлана А. Гришкяне" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20436" ["VALUE"]=> array(2) { ["TEXT"]=> string(7295) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Роль аптеки в детской больнице и предоставляемые услуги сейчас значительно шире, чем 5 лет назад. Во всей Европе больницы стремятся переложить ответственность за приготовление препаратов, особенно стерильных, на фармацевтов, тем самым облегчив труд медсестер. Цель приготовления препаратов в больничной аптеке – получить качественный, стерильный, готовый для ввода пациенту препарат, приготовленный в особых, удобных и безопасных для работников условиях с соблюдением рационального использования медикаментов. </p> <h2 style="text-align: justify;">Цели</h2> <p style="text-align: justify;"> Наши задачи были следующими: а) Выяснить, какие условия необходимо соблюсти для создания асептического блока в больничной аптеке. Изучить требования, необходимые проверки, проблемы; б) Выяснить, какие есть особенности безопасного и качественного приготовления и оборота в больнице цитотоксичных препаратов; в) Исследовать трудности приготовления антибиотиков для парэнтерального ввода в больничной аптеке; г) Исследовать нужды больницы и рецепты парэнтерального питания, его оборот и приготовление с помощью аппарата (компаундера). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> А) Для работы асептического блока в больничной аптеке необходимы чистые помещения, специальная вентиляция, ламинарные шкафы, микробиологическая валидация, валидация работников, особенные одноразовые одежды и принадлежности, санитарный график. Чтобы не столкнуться с проблемами, рекомендуется заранее разработать проект с четкой целью, какие препараты аптека будет готовить. Б) Для цитотоксичных препаратов необходимо негативное давление в отдельном помещении для готовки, специальный ламинарный шкаф для цитотоксичных препаратов, защитные очки и маска, специальные перчатки, обученный персонал, специальные одноразовые принадлежности, в том числе закрытые системы переноса лекарств, а также может быть очень полезна программатура для приготовления и назначения препаратов. В) Обеспечивая парэнтеральными антибиотиками пациентов больницы можно столкнуться с разными проблемами, как то: плохой контакт с врачебным персоналом, частая смена доз антибиотиков, частая смена антибиотиков в связи с анализами, отмена уже приготовленных антибиотиков, короткая стабильность антибактериальных препаратов, а также отсутствие материальной выгоды в централизации готовки дешевых антибиотиков. Г) Пациентам больницы необходима как индивидуальная рецептура парэнтерального питания, так и стандартные смеси, введенные в пользование для младенцев, детей от 3 до 15 кг и от 15 до 30 кг. Компаундера улучшает качество рабочих условий персонала, уменьшает количество ручного труда, ускоряет время приготовления, но требует минимум двух человек для обслуживания. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> У централизованного приготовления парэнтеральных препаратов в аптеке Детской больницы есть свои преимущества и недостатки. Одни из главных преимуществ – длительный срок годности приготовленных препаратов, безопасность приготовления токсичных лекарств для персонала, минимизация мануального труда работников, рациональное использование лекарственных средств. В больничной аптеке можно добиться нужного качества и условий приготовления, централизовав процесс, пройдя необходимые проверки, поддерживая уровень чистоты каждый день и наладив контакты с врачебным персоналом. Процесс можно бесконечно улучшать. Главные цели на будущее: обоюдное сотрудничество с врачебным персоналом, механизирование однообразных процессов, компьютеризирование всех рецептов, проверки несовместимостей препаратов и усовершенствование способа заказа препаратов врачами. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Парэнтеральное лечение, цитотоксические препараты, аптека, правила работы, логистика, детская больница. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7063) "Введение
Роль аптеки в детской больнице и предоставляемые услуги сейчас значительно шире, чем 5 лет назад. Во всей Европе больницы стремятся переложить ответственность за приготовление препаратов, особенно стерильных, на фармацевтов, тем самым облегчив труд медсестер. Цель приготовления препаратов в больничной аптеке – получить качественный, стерильный, готовый для ввода пациенту препарат, приготовленный в особых, удобных и безопасных для работников условиях с соблюдением рационального использования медикаментов.
Цели
Наши задачи были следующими: а) Выяснить, какие условия необходимо соблюсти для создания асептического блока в больничной аптеке. Изучить требования, необходимые проверки, проблемы; б) Выяснить, какие есть особенности безопасного и качественного приготовления и оборота в больнице цитотоксичных препаратов; в) Исследовать трудности приготовления антибиотиков для парэнтерального ввода в больничной аптеке; г) Исследовать нужды больницы и рецепты парэнтерального питания, его оборот и приготовление с помощью аппарата (компаундера).
Результаты
А) Для работы асептического блока в больничной аптеке необходимы чистые помещения, специальная вентиляция, ламинарные шкафы, микробиологическая валидация, валидация работников, особенные одноразовые одежды и принадлежности, санитарный график. Чтобы не столкнуться с проблемами, рекомендуется заранее разработать проект с четкой целью, какие препараты аптека будет готовить. Б) Для цитотоксичных препаратов необходимо негативное давление в отдельном помещении для готовки, специальный ламинарный шкаф для цитотоксичных препаратов, защитные очки и маска, специальные перчатки, обученный персонал, специальные одноразовые принадлежности, в том числе закрытые системы переноса лекарств, а также может быть очень полезна программатура для приготовления и назначения препаратов. В) Обеспечивая парэнтеральными антибиотиками пациентов больницы можно столкнуться с разными проблемами, как то: плохой контакт с врачебным персоналом, частая смена доз антибиотиков, частая смена антибиотиков в связи с анализами, отмена уже приготовленных антибиотиков, короткая стабильность антибактериальных препаратов, а также отсутствие материальной выгоды в централизации готовки дешевых антибиотиков. Г) Пациентам больницы необходима как индивидуальная рецептура парэнтерального питания, так и стандартные смеси, введенные в пользование для младенцев, детей от 3 до 15 кг и от 15 до 30 кг. Компаундера улучшает качество рабочих условий персонала, уменьшает количество ручного труда, ускоряет время приготовления, но требует минимум двух человек для обслуживания.
Выводы
У централизованного приготовления парэнтеральных препаратов в аптеке Детской больницы есть свои преимущества и недостатки. Одни из главных преимуществ – длительный срок годности приготовленных препаратов, безопасность приготовления токсичных лекарств для персонала, минимизация мануального труда работников, рациональное использование лекарственных средств. В больничной аптеке можно добиться нужного качества и условий приготовления, централизовав процесс, пройдя необходимые проверки, поддерживая уровень чистоты каждый день и наладив контакты с врачебным персоналом. Процесс можно бесконечно улучшать. Главные цели на будущее: обоюдное сотрудничество с врачебным персоналом, механизирование однообразных процессов, компьютеризирование всех рецептов, проверки несовместимостей препаратов и усовершенствование способа заказа препаратов врачами.
Ключевые слова
Парэнтеральное лечение, цитотоксические препараты, аптека, правила работы, логистика, детская больница.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(7063) "Введение
Роль аптеки в детской больнице и предоставляемые услуги сейчас значительно шире, чем 5 лет назад. Во всей Европе больницы стремятся переложить ответственность за приготовление препаратов, особенно стерильных, на фармацевтов, тем самым облегчив труд медсестер. Цель приготовления препаратов в больничной аптеке – получить качественный, стерильный, готовый для ввода пациенту препарат, приготовленный в особых, удобных и безопасных для работников условиях с соблюдением рационального использования медикаментов.
Цели
Наши задачи были следующими: а) Выяснить, какие условия необходимо соблюсти для создания асептического блока в больничной аптеке. Изучить требования, необходимые проверки, проблемы; б) Выяснить, какие есть особенности безопасного и качественного приготовления и оборота в больнице цитотоксичных препаратов; в) Исследовать трудности приготовления антибиотиков для парэнтерального ввода в больничной аптеке; г) Исследовать нужды больницы и рецепты парэнтерального питания, его оборот и приготовление с помощью аппарата (компаундера).
Результаты
А) Для работы асептического блока в больничной аптеке необходимы чистые помещения, специальная вентиляция, ламинарные шкафы, микробиологическая валидация, валидация работников, особенные одноразовые одежды и принадлежности, санитарный график. Чтобы не столкнуться с проблемами, рекомендуется заранее разработать проект с четкой целью, какие препараты аптека будет готовить. Б) Для цитотоксичных препаратов необходимо негативное давление в отдельном помещении для готовки, специальный ламинарный шкаф для цитотоксичных препаратов, защитные очки и маска, специальные перчатки, обученный персонал, специальные одноразовые принадлежности, в том числе закрытые системы переноса лекарств, а также может быть очень полезна программатура для приготовления и назначения препаратов. В) Обеспечивая парэнтеральными антибиотиками пациентов больницы можно столкнуться с разными проблемами, как то: плохой контакт с врачебным персоналом, частая смена доз антибиотиков, частая смена антибиотиков в связи с анализами, отмена уже приготовленных антибиотиков, короткая стабильность антибактериальных препаратов, а также отсутствие материальной выгоды в централизации готовки дешевых антибиотиков. Г) Пациентам больницы необходима как индивидуальная рецептура парэнтерального питания, так и стандартные смеси, введенные в пользование для младенцев, детей от 3 до 15 кг и от 15 до 30 кг. Компаундера улучшает качество рабочих условий персонала, уменьшает количество ручного труда, ускоряет время приготовления, но требует минимум двух человек для обслуживания.
Выводы
У централизованного приготовления парэнтеральных препаратов в аптеке Детской больницы есть свои преимущества и недостатки. Одни из главных преимуществ – длительный срок годности приготовленных препаратов, безопасность приготовления токсичных лекарств для персонала, минимизация мануального труда работников, рациональное использование лекарственных средств. В больничной аптеке можно добиться нужного качества и условий приготовления, централизовав процесс, пройдя необходимые проверки, поддерживая уровень чистоты каждый день и наладив контакты с врачебным персоналом. Процесс можно бесконечно улучшать. Главные цели на будущее: обоюдное сотрудничество с врачебным персоналом, механизирование однообразных процессов, компьютеризирование всех рецептов, проверки несовместимостей препаратов и усовершенствование способа заказа препаратов врачами.
Ключевые слова
Парэнтеральное лечение, цитотоксические препараты, аптека, правила работы, логистика, детская больница.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20435" ["VALUE"]=> array(2) { ["TEXT"]=> string(111) "Университетский детский клинический госпиталь, Рига, Латвия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(111) "Университетский детский клинический госпиталь, Рига, Латвия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(111) "Университетский детский клинический госпиталь, Рига, Латвия" } } } [1]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1568" ["~ID"]=> string(4) "1568" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(159) "Гистологические и плазменные изменения после гетеротопической трансплантации сердца" ["~NAME"]=> string(159) "Гистологические и плазменные изменения после гетеротопической трансплантации сердца" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:33:11" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:33:11" ["DETAIL_PAGE_URL"]=> string(138) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/gistologicheskie-i-plazmennye-izmeneniya-posle-geterotopicheskoy-transplantatsii-serdtsa/" ["~DETAIL_PAGE_URL"]=> string(138) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/gistologicheskie-i-plazmennye-izmeneniya-posle-geterotopicheskoy-transplantatsii-serdtsa/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(88) "gistologicheskie-i-plazmennye-izmeneniya-posle-geterotopicheskoy-transplantatsii-serdtsa" ["~CODE"]=> string(88) "gistologicheskie-i-plazmennye-izmeneniya-posle-geterotopicheskoy-transplantatsii-serdtsa" ["EXTERNAL_ID"]=> string(4) "1568" ["~EXTERNAL_ID"]=> string(4) "1568" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(159) "Гистологические и плазменные изменения после гетеротопической трансплантации сердца" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(245) "Гистологические и плазменные изменения после гетеротопической трансплантации сердцаHistological features and blood plasma changes after heterotopic heart transplantation" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(3032) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Одним из эффективных методов лечения тяжелой сердечной недостаточности является трансплантация сердца. Тем не менее, не решенной проблемой является отторжение трансплантата. Актуальным является изучение гистологических и молекулярных иммунных механизмов отторжения трансплантата. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель работы состояла в оценке гистологических изменений трансплантата после гетеротопической трансплантации сердца, а также изменения в плазме крови реципиента. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Двум белым новозеландским кроликам выполнена гетеротопическая трансплантация сердца в брюшную полость, после чего, ежедневно выполнялось измерение миелопероксидазы в плазме крови. Один кролик получал циклоспорин А в дозировке 10 мг/кг в сутки, другой кролик был без иммуносупрессивной терапии. После гибели кроликов выполнено гистологическое исследование пересаженных сердец. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Получены данные о динамике миелопероксидазы лейкоцитов после трансплантации сердца и гистологических изменениях в виде дистрофии и кальциноза миокарда в пересаженном сердце у кролика, не получавшего иммуносупрессию. В трансплантате кролика, получавшего циклоспорин А, признаков кальциноза или дистрофии не наблюдалось. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Гетеротопическая трансплантация сердца, миелопероксидаза, маркеры отторжения трансплантата. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(159) "Гистологические и плазменные изменения после гетеротопической трансплантации сердца" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(159) "Гистологические и плазменные изменения после гетеротопической трансплантации сердца" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(159) "Гистологические и плазменные изменения после гетеротопической трансплантации сердца" ["SECTION_META_TITLE"]=> string(159) "Гистологические и плазменные изменения после гетеротопической трансплантации сердца" ["SECTION_META_KEYWORDS"]=> string(159) "Гистологические и плазменные изменения после гетеротопической трансплантации сердца" ["SECTION_META_DESCRIPTION"]=> string(159) "Гистологические и плазменные изменения после гетеротопической трансплантации сердца" ["SECTION_PICTURE_FILE_ALT"]=> string(159) "Гистологические и плазменные изменения после гетеротопической трансплантации сердца" ["SECTION_PICTURE_FILE_TITLE"]=> string(159) "Гистологические и плазменные изменения после гетеротопической трансплантации сердца" ["SECTION_PICTURE_FILE_NAME"]=> string(92) "gistologicheskie-i-plazmennye-izmeneniya-posle-geterotopicheskoy-transplantatsii-serdtsa-img" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(159) "Гистологические и плазменные изменения после гетеротопической трансплантации сердца" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(159) "Гистологические и плазменные изменения после гетеротопической трансплантации сердца" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(92) "gistologicheskie-i-plazmennye-izmeneniya-posle-geterotopicheskoy-transplantatsii-serdtsa-img" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(92) "gistologicheskie-i-plazmennye-izmeneniya-posle-geterotopicheskoy-transplantatsii-serdtsa-img" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(92) "gistologicheskie-i-plazmennye-izmeneniya-posle-geterotopicheskoy-transplantatsii-serdtsa-img" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20443" ["VALUE"]=> array(2) { ["TEXT"]=> string(816) "Никита В. Грудинин <sup>1</sup>, Вадим Е. Карев <sup>2</sup>, Николай С. Буненков <sup>3</sup>, Владимир В. Комок <sup>3</sup>, Валерия А. Костевич <sup>4</sup>, Николай П. Горбунов <sup>4</sup>, Алексей В. Соколов <sup>4</sup>, Андрей А. Карпов <sup>3</sup>, Кирилл В. Лепик <sup>3</sup>, Александр Н. Швецов <sup>3</sup>, Юрий А. Серов <sup>3</sup>, Олег В. Галибин <sup>3</sup>, Александр С. Немков <sup>3</sup>, Геннадий Г. Хубулава <sup>3</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(648) "Никита В. Грудинин 1, Вадим Е. Карев 2, Николай С. Буненков 3, Владимир В. Комок 3, Валерия А. Костевич 4, Николай П. Горбунов 4, Алексей В. Соколов 4, Андрей А. Карпов 3, Кирилл В. Лепик 3, Александр Н. Швецов 3, Юрий А. Серов 3, Олег В. Галибин 3, Александр С. Немков 3, Геннадий Г. Хубулава 3" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20444" ["VALUE"]=> array(2) { ["TEXT"]=> string(726) "<sup>1</sup> НМИЦ трансплантологии и искусственных органов имени академика В. И. Шумакова, Москва, Россия <sup>2</sup> ФГБУ Детский научно-клинический центр инфекционных болезней ФМБУ РФ, Санкт-Петербург, Россия <sup>3</sup> Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова <sup>4</sup> ФГБНУ институт экспериментальной медицины, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(678) "1 НМИЦ трансплантологии и искусственных органов имени академика В. И. Шумакова, Москва, Россия 2 ФГБУ Детский научно-клинический центр инфекционных болезней ФМБУ РФ, Санкт-Петербург, Россия 3 Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова 4 ФГБНУ институт экспериментальной медицины, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20445" ["VALUE"]=> array(2) { ["TEXT"]=> string(3032) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Одним из эффективных методов лечения тяжелой сердечной недостаточности является трансплантация сердца. Тем не менее, не решенной проблемой является отторжение трансплантата. Актуальным является изучение гистологических и молекулярных иммунных механизмов отторжения трансплантата. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель работы состояла в оценке гистологических изменений трансплантата после гетеротопической трансплантации сердца, а также изменения в плазме крови реципиента. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Двум белым новозеландским кроликам выполнена гетеротопическая трансплантация сердца в брюшную полость, после чего, ежедневно выполнялось измерение миелопероксидазы в плазме крови. Один кролик получал циклоспорин А в дозировке 10 мг/кг в сутки, другой кролик был без иммуносупрессивной терапии. После гибели кроликов выполнено гистологическое исследование пересаженных сердец. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Получены данные о динамике миелопероксидазы лейкоцитов после трансплантации сердца и гистологических изменениях в виде дистрофии и кальциноза миокарда в пересаженном сердце у кролика, не получавшего иммуносупрессию. В трансплантате кролика, получавшего циклоспорин А, признаков кальциноза или дистрофии не наблюдалось. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Гетеротопическая трансплантация сердца, миелопероксидаза, маркеры отторжения трансплантата. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2812) "Введение
Одним из эффективных методов лечения тяжелой сердечной недостаточности является трансплантация сердца. Тем не менее, не решенной проблемой является отторжение трансплантата. Актуальным является изучение гистологических и молекулярных иммунных механизмов отторжения трансплантата.
Цель
Цель работы состояла в оценке гистологических изменений трансплантата после гетеротопической трансплантации сердца, а также изменения в плазме крови реципиента.
Материалы и методы
Двум белым новозеландским кроликам выполнена гетеротопическая трансплантация сердца в брюшную полость, после чего, ежедневно выполнялось измерение миелопероксидазы в плазме крови. Один кролик получал циклоспорин А в дозировке 10 мг/кг в сутки, другой кролик был без иммуносупрессивной терапии. После гибели кроликов выполнено гистологическое исследование пересаженных сердец.
Результаты
Получены данные о динамике миелопероксидазы лейкоцитов после трансплантации сердца и гистологических изменениях в виде дистрофии и кальциноза миокарда в пересаженном сердце у кролика, не получавшего иммуносупрессию. В трансплантате кролика, получавшего циклоспорин А, признаков кальциноза или дистрофии не наблюдалось.
Ключевые слова
Гетеротопическая трансплантация сердца, миелопероксидаза, маркеры отторжения трансплантата.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20446" ["VALUE"]=> array(2) { ["TEXT"]=> string(622) "Nikita V. Grudinin <sup>1</sup>, Vadim E. Karev <sup>2</sup>, Nikolai S. Bunenkov <sup>1</sup>, Vladimir V. Komok <sup>3</sup>, Valeria V. Kostevitch <sup>4</sup>, Nikolai P. Gorbunov <sup>4</sup>, Alexei V. Sokolov <sup>4</sup>, Andrey A. Karpov <sup>3</sup>, Kirill V. Lepik <sup>3</sup>, Alexander N. Shvetsov <sup>3</sup>, Youri A. Serov <sup>3</sup>, Oleg V. Galibin <sup>3</sup>, Alexander S. Nemkov <sup>3</sup>, Gennadiy G. Khubulava <sup>3</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(454) "Nikita V. Grudinin 1, Vadim E. Karev 2, Nikolai S. Bunenkov 1, Vladimir V. Komok 3, Valeria V. Kostevitch 4, Nikolai P. Gorbunov 4, Alexei V. Sokolov 4, Andrey A. Karpov 3, Kirill V. Lepik 3, Alexander N. Shvetsov 3, Youri A. Serov 3, Oleg V. Galibin 3, Alexander S. Nemkov 3, Gennadiy G. Khubulava 3" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20447" ["VALUE"]=> array(2) { ["TEXT"]=> string(393) "<sup>1</sup> V. I. Shumakov Federal Research Center of Transplantology and Artificial Organs, Moscow, Russia <sup>2</sup> St. Petersburg Research Institute of Children’s Infections <sup>3</sup> The First Pavlov State Medical University of St. Petersburg <sup>4</sup> St. Petersburg Institute of Experimental Medicine, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(345) "1 V. I. Shumakov Federal Research Center of Transplantology and Artificial Organs, Moscow, Russia 2 St. Petersburg Research Institute of Children’s Infections 3 The First Pavlov State Medical University of St. Petersburg 4 St. Petersburg Institute of Experimental Medicine, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20448" ["VALUE"]=> array(2) { ["TEXT"]=> string(1914) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> One of the effective methods for treating severe heart failure is the heart transplantation. On the other hand, the unresolved problem is the rejection of the graft. The study of histological and molecular immune mechanisms of graft rejection is significant. </p> <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> Objective of the study was to evaluate the histological changes of the graft after heterotopic heart transplantation, as well as changes in the blood plasma of the recipient. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> Two white New Zealand’s rabbits underwent heterotopic heart transplantation, after which a daily measurement of myeloperoxidase in the blood plasma performed. One rabbit received cyclosporine A at a dosage of 10 mg/kg per day and another rabbit was immunosuppressive. The histological examination of transplanted hearts was performed after the rabbits were deceased. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Data on the dynamics of leukocyte myeloperoxidase were obtained after cardiac transplantation and histological changes in the transplanted heart. There are calcification and dystrophy in transplanted heart found in a rabbit without immunosuppression. No signs of graft calcinosis or dystrophy were observed in the cyclosporine-treated animal. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Heterotopic heart transplantation, myeloperoxidase, markers of the graft rejection. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1694) "Introduction
One of the effective methods for treating severe heart failure is the heart transplantation. On the other hand, the unresolved problem is the rejection of the graft. The study of histological and molecular immune mechanisms of graft rejection is significant.
Aim
Objective of the study was to evaluate the histological changes of the graft after heterotopic heart transplantation, as well as changes in the blood plasma of the recipient.
Materials and methods
Two white New Zealand’s rabbits underwent heterotopic heart transplantation, after which a daily measurement of myeloperoxidase in the blood plasma performed. One rabbit received cyclosporine A at a dosage of 10 mg/kg per day and another rabbit was immunosuppressive. The histological examination of transplanted hearts was performed after the rabbits were deceased.
Results
Data on the dynamics of leukocyte myeloperoxidase were obtained after cardiac transplantation and histological changes in the transplanted heart. There are calcification and dystrophy in transplanted heart found in a rabbit without immunosuppression. No signs of graft calcinosis or dystrophy were observed in the cyclosporine-treated animal.
Keywords
Heterotopic heart transplantation, myeloperoxidase, markers of the graft rejection.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20449" ["VALUE"]=> string(86) "Histological features and blood plasma changes after heterotopic heart transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(86) "Histological features and blood plasma changes after heterotopic heart transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20769" ["VALUE"]=> string(4) "1405" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1405" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20770" ["VALUE"]=> string(4) "1406" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1406" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20446" ["VALUE"]=> array(2) { ["TEXT"]=> string(622) "Nikita V. Grudinin <sup>1</sup>, Vadim E. Karev <sup>2</sup>, Nikolai S. Bunenkov <sup>1</sup>, Vladimir V. Komok <sup>3</sup>, Valeria V. Kostevitch <sup>4</sup>, Nikolai P. Gorbunov <sup>4</sup>, Alexei V. Sokolov <sup>4</sup>, Andrey A. Karpov <sup>3</sup>, Kirill V. Lepik <sup>3</sup>, Alexander N. Shvetsov <sup>3</sup>, Youri A. Serov <sup>3</sup>, Oleg V. Galibin <sup>3</sup>, Alexander S. Nemkov <sup>3</sup>, Gennadiy G. Khubulava <sup>3</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(454) "Nikita V. Grudinin 1, Vadim E. Karev 2, Nikolai S. Bunenkov 1, Vladimir V. Komok 3, Valeria V. Kostevitch 4, Nikolai P. Gorbunov 4, Alexei V. Sokolov 4, Andrey A. Karpov 3, Kirill V. Lepik 3, Alexander N. Shvetsov 3, Youri A. Serov 3, Oleg V. Galibin 3, Alexander S. Nemkov 3, Gennadiy G. Khubulava 3" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(454) "Nikita V. Grudinin 1, Vadim E. Karev 2, Nikolai S. Bunenkov 1, Vladimir V. Komok 3, Valeria V. Kostevitch 4, Nikolai P. Gorbunov 4, Alexei V. Sokolov 4, Andrey A. Karpov 3, Kirill V. Lepik 3, Alexander N. Shvetsov 3, Youri A. Serov 3, Oleg V. Galibin 3, Alexander S. Nemkov 3, Gennadiy G. Khubulava 3" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20448" ["VALUE"]=> array(2) { ["TEXT"]=> string(1914) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> One of the effective methods for treating severe heart failure is the heart transplantation. On the other hand, the unresolved problem is the rejection of the graft. The study of histological and molecular immune mechanisms of graft rejection is significant. </p> <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> Objective of the study was to evaluate the histological changes of the graft after heterotopic heart transplantation, as well as changes in the blood plasma of the recipient. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> Two white New Zealand’s rabbits underwent heterotopic heart transplantation, after which a daily measurement of myeloperoxidase in the blood plasma performed. One rabbit received cyclosporine A at a dosage of 10 mg/kg per day and another rabbit was immunosuppressive. The histological examination of transplanted hearts was performed after the rabbits were deceased. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Data on the dynamics of leukocyte myeloperoxidase were obtained after cardiac transplantation and histological changes in the transplanted heart. There are calcification and dystrophy in transplanted heart found in a rabbit without immunosuppression. No signs of graft calcinosis or dystrophy were observed in the cyclosporine-treated animal. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Heterotopic heart transplantation, myeloperoxidase, markers of the graft rejection. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1694) "Introduction
One of the effective methods for treating severe heart failure is the heart transplantation. On the other hand, the unresolved problem is the rejection of the graft. The study of histological and molecular immune mechanisms of graft rejection is significant.
Aim
Objective of the study was to evaluate the histological changes of the graft after heterotopic heart transplantation, as well as changes in the blood plasma of the recipient.
Materials and methods
Two white New Zealand’s rabbits underwent heterotopic heart transplantation, after which a daily measurement of myeloperoxidase in the blood plasma performed. One rabbit received cyclosporine A at a dosage of 10 mg/kg per day and another rabbit was immunosuppressive. The histological examination of transplanted hearts was performed after the rabbits were deceased.
Results
Data on the dynamics of leukocyte myeloperoxidase were obtained after cardiac transplantation and histological changes in the transplanted heart. There are calcification and dystrophy in transplanted heart found in a rabbit without immunosuppression. No signs of graft calcinosis or dystrophy were observed in the cyclosporine-treated animal.
Keywords
Heterotopic heart transplantation, myeloperoxidase, markers of the graft rejection.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(1694) "Introduction
One of the effective methods for treating severe heart failure is the heart transplantation. On the other hand, the unresolved problem is the rejection of the graft. The study of histological and molecular immune mechanisms of graft rejection is significant.
Aim
Objective of the study was to evaluate the histological changes of the graft after heterotopic heart transplantation, as well as changes in the blood plasma of the recipient.
Materials and methods
Two white New Zealand’s rabbits underwent heterotopic heart transplantation, after which a daily measurement of myeloperoxidase in the blood plasma performed. One rabbit received cyclosporine A at a dosage of 10 mg/kg per day and another rabbit was immunosuppressive. The histological examination of transplanted hearts was performed after the rabbits were deceased.
Results
Data on the dynamics of leukocyte myeloperoxidase were obtained after cardiac transplantation and histological changes in the transplanted heart. There are calcification and dystrophy in transplanted heart found in a rabbit without immunosuppression. No signs of graft calcinosis or dystrophy were observed in the cyclosporine-treated animal.
Keywords
Heterotopic heart transplantation, myeloperoxidase, markers of the graft rejection.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20449" ["VALUE"]=> string(86) "Histological features and blood plasma changes after heterotopic heart transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(86) "Histological features and blood plasma changes after heterotopic heart transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(86) "Histological features and blood plasma changes after heterotopic heart transplantation" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20447" ["VALUE"]=> array(2) { ["TEXT"]=> string(393) "<sup>1</sup> V. I. Shumakov Federal Research Center of Transplantology and Artificial Organs, Moscow, Russia <sup>2</sup> St. Petersburg Research Institute of Children’s Infections <sup>3</sup> The First Pavlov State Medical University of St. Petersburg <sup>4</sup> St. Petersburg Institute of Experimental Medicine, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(345) "1 V. I. Shumakov Federal Research Center of Transplantology and Artificial Organs, Moscow, Russia 2 St. Petersburg Research Institute of Children’s Infections 3 The First Pavlov State Medical University of St. Petersburg 4 St. Petersburg Institute of Experimental Medicine, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(345) "1 V. I. Shumakov Federal Research Center of Transplantology and Artificial Organs, Moscow, Russia 2 St. Petersburg Research Institute of Children’s Infections 3 The First Pavlov State Medical University of St. Petersburg 4 St. Petersburg Institute of Experimental Medicine, St. Petersburg, Russia" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20443" ["VALUE"]=> array(2) { ["TEXT"]=> string(816) "Никита В. Грудинин <sup>1</sup>, Вадим Е. Карев <sup>2</sup>, Николай С. Буненков <sup>3</sup>, Владимир В. Комок <sup>3</sup>, Валерия А. Костевич <sup>4</sup>, Николай П. Горбунов <sup>4</sup>, Алексей В. Соколов <sup>4</sup>, Андрей А. Карпов <sup>3</sup>, Кирилл В. Лепик <sup>3</sup>, Александр Н. Швецов <sup>3</sup>, Юрий А. Серов <sup>3</sup>, Олег В. Галибин <sup>3</sup>, Александр С. Немков <sup>3</sup>, Геннадий Г. Хубулава <sup>3</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(648) "Никита В. Грудинин 1, Вадим Е. Карев 2, Николай С. Буненков 3, Владимир В. Комок 3, Валерия А. Костевич 4, Николай П. Горбунов 4, Алексей В. Соколов 4, Андрей А. Карпов 3, Кирилл В. Лепик 3, Александр Н. Швецов 3, Юрий А. Серов 3, Олег В. Галибин 3, Александр С. Немков 3, Геннадий Г. Хубулава 3" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(648) "Никита В. Грудинин 1, Вадим Е. Карев 2, Николай С. Буненков 3, Владимир В. Комок 3, Валерия А. Костевич 4, Николай П. Горбунов 4, Алексей В. Соколов 4, Андрей А. Карпов 3, Кирилл В. Лепик 3, Александр Н. Швецов 3, Юрий А. Серов 3, Олег В. Галибин 3, Александр С. Немков 3, Геннадий Г. Хубулава 3" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20445" ["VALUE"]=> array(2) { ["TEXT"]=> string(3032) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Одним из эффективных методов лечения тяжелой сердечной недостаточности является трансплантация сердца. Тем не менее, не решенной проблемой является отторжение трансплантата. Актуальным является изучение гистологических и молекулярных иммунных механизмов отторжения трансплантата. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель работы состояла в оценке гистологических изменений трансплантата после гетеротопической трансплантации сердца, а также изменения в плазме крови реципиента. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Двум белым новозеландским кроликам выполнена гетеротопическая трансплантация сердца в брюшную полость, после чего, ежедневно выполнялось измерение миелопероксидазы в плазме крови. Один кролик получал циклоспорин А в дозировке 10 мг/кг в сутки, другой кролик был без иммуносупрессивной терапии. После гибели кроликов выполнено гистологическое исследование пересаженных сердец. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Получены данные о динамике миелопероксидазы лейкоцитов после трансплантации сердца и гистологических изменениях в виде дистрофии и кальциноза миокарда в пересаженном сердце у кролика, не получавшего иммуносупрессию. В трансплантате кролика, получавшего циклоспорин А, признаков кальциноза или дистрофии не наблюдалось. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Гетеротопическая трансплантация сердца, миелопероксидаза, маркеры отторжения трансплантата. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2812) "Введение
Одним из эффективных методов лечения тяжелой сердечной недостаточности является трансплантация сердца. Тем не менее, не решенной проблемой является отторжение трансплантата. Актуальным является изучение гистологических и молекулярных иммунных механизмов отторжения трансплантата.
Цель
Цель работы состояла в оценке гистологических изменений трансплантата после гетеротопической трансплантации сердца, а также изменения в плазме крови реципиента.
Материалы и методы
Двум белым новозеландским кроликам выполнена гетеротопическая трансплантация сердца в брюшную полость, после чего, ежедневно выполнялось измерение миелопероксидазы в плазме крови. Один кролик получал циклоспорин А в дозировке 10 мг/кг в сутки, другой кролик был без иммуносупрессивной терапии. После гибели кроликов выполнено гистологическое исследование пересаженных сердец.
Результаты
Получены данные о динамике миелопероксидазы лейкоцитов после трансплантации сердца и гистологических изменениях в виде дистрофии и кальциноза миокарда в пересаженном сердце у кролика, не получавшего иммуносупрессию. В трансплантате кролика, получавшего циклоспорин А, признаков кальциноза или дистрофии не наблюдалось.
Ключевые слова
Гетеротопическая трансплантация сердца, миелопероксидаза, маркеры отторжения трансплантата.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2812) "Введение
Одним из эффективных методов лечения тяжелой сердечной недостаточности является трансплантация сердца. Тем не менее, не решенной проблемой является отторжение трансплантата. Актуальным является изучение гистологических и молекулярных иммунных механизмов отторжения трансплантата.
Цель
Цель работы состояла в оценке гистологических изменений трансплантата после гетеротопической трансплантации сердца, а также изменения в плазме крови реципиента.
Материалы и методы
Двум белым новозеландским кроликам выполнена гетеротопическая трансплантация сердца в брюшную полость, после чего, ежедневно выполнялось измерение миелопероксидазы в плазме крови. Один кролик получал циклоспорин А в дозировке 10 мг/кг в сутки, другой кролик был без иммуносупрессивной терапии. После гибели кроликов выполнено гистологическое исследование пересаженных сердец.
Результаты
Получены данные о динамике миелопероксидазы лейкоцитов после трансплантации сердца и гистологических изменениях в виде дистрофии и кальциноза миокарда в пересаженном сердце у кролика, не получавшего иммуносупрессию. В трансплантате кролика, получавшего циклоспорин А, признаков кальциноза или дистрофии не наблюдалось.
Ключевые слова
Гетеротопическая трансплантация сердца, миелопероксидаза, маркеры отторжения трансплантата.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20444" ["VALUE"]=> array(2) { ["TEXT"]=> string(726) "<sup>1</sup> НМИЦ трансплантологии и искусственных органов имени академика В. И. Шумакова, Москва, Россия <sup>2</sup> ФГБУ Детский научно-клинический центр инфекционных болезней ФМБУ РФ, Санкт-Петербург, Россия <sup>3</sup> Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова <sup>4</sup> ФГБНУ институт экспериментальной медицины, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(678) "1 НМИЦ трансплантологии и искусственных органов имени академика В. И. Шумакова, Москва, Россия 2 ФГБУ Детский научно-клинический центр инфекционных болезней ФМБУ РФ, Санкт-Петербург, Россия 3 Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова 4 ФГБНУ институт экспериментальной медицины, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(678) "1 НМИЦ трансплантологии и искусственных органов имени академика В. И. Шумакова, Москва, Россия 2 ФГБУ Детский научно-клинический центр инфекционных болезней ФМБУ РФ, Санкт-Петербург, Россия 3 Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова 4 ФГБНУ институт экспериментальной медицины, Санкт-Петербург, Россия" } } } [2]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1566" ["~ID"]=> string(4) "1566" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(214) "Трансплантация фекальной микробиоты у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток" ["~NAME"]=> string(214) "Трансплантация фекальной микробиоты у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:32:28" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:32:28" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/transplantatsiya-fekalnoy-mikrobioty-u-patsientov-posle-allogennoy-transplantatsii-gemopoeticheskikh/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/transplantatsiya-fekalnoy-mikrobioty-u-patsientov-posle-allogennoy-transplantatsii-gemopoeticheskikh/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "transplantatsiya-fekalnoy-mikrobioty-u-patsientov-posle-allogennoy-transplantatsii-gemopoeticheskikh" ["~CODE"]=> string(100) "transplantatsiya-fekalnoy-mikrobioty-u-patsientov-posle-allogennoy-transplantatsii-gemopoeticheskikh" ["EXTERNAL_ID"]=> string(4) "1566" ["~EXTERNAL_ID"]=> string(4) "1566" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(214) "Трансплантация фекальной микробиоты у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(315) "Трансплантация фекальной микробиоты у пациентов после аллогенной трансплантации гемопоэтических стволовых клетокFecal microbiota transplantation in patients after allogeneic hematopoietic stem cell transplantation" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(8450) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод терапии онкологических, гематологических и наследственных заболеваний. Распространенными осложнениями алло-ТГСК, которые приводят к снижению эффективности лечения, являются: инфекционное поражение желудочно-кишечного тракта вирусной этиологии и/или ассоциированное с Clostridium difficile на фоне иммунодефицита; антибиотикассоциированная диарея; реакция трансплантат против хозяина (РТПХ). Трансплантация фекальной микробиоты (ТФМ) от здорового донора может приводить к эрадикации патогенных микроорганизмов, модуляции иммунной системы реципиента и как следствие к снижению активности РТПХ кишечника. Целью работы является повыщение эффективности лечения осложнений у пациентов после алло-ТГСК ассоциированных с Clostridium difficile и РТПХ кишечника. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> С 2015 по 2018 год в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой в одноцентровое, проспективное исследование включено 11 пациентов после алло-ТГСК от неродственного донора – 36,5% (n=4), родственного – 9% (n=1), гаплоидентичного – 54,5% (n=6) с целью терапии острого лимфобластного лейкоза – 18,3% (n=2), острого миелоидного лейкоза – 27,4% (n=3), миелодиспластического синдрома – 18,3% (n=2), бета-талассемии – 9% (n=1), хронического миелолейкоза – 9% (n=1), Лимфомы Ходжкина – 9% (n=1), анемии Фанкони – 9% (n=1). Для лечения посттрансплантационных осложнений всем пациентам была выполнена ТФМ. Медиана возраста составила 24 года (2-45). Из исследования исключено трое больных из-за нарушения техники ТФМ (n=2), развития тяжелого синдрома системного воспалительного ответа (n=1). Длительность диареи перед ТФМ составила от 1 до 6 мес. (медиана – 2,3) и наблюдалась у всех пациентов. У 5 (45,5%) больных регистрировали активное кишечное кровотечение с необходимостью ежедневных гемотрансфузий для коррекции анемического синдрома, еще у 4 (36,4%) больных в стуле определялись прожилки крови. В состоянии сепсиса было 5 пациентов (45,5%), а один пациент находился в состоянии септического шока (Klebsiella pneumoniае) и получал антибактериальную терапию, вазопрессоры, искусственную вентиляцию легких. Абдоминальный болевой синдром, требующий анальгезии наркотическими анальгетиками отмечали у 9 (81,8%) пациентов. Парез кишечника наблюдали у 5 (45,5%) больных. У 8 (72,7%) пациентов выявлен положительный клостридиальный токсин-В в стуле, повышенный уровень фекального кальпротектина до ТФМ у 7 (63,6%) пациентов 600 мкг/г (220-6706). Введение фекального трансплантата выполняли на Д+168 (27-1107). Донорами микробиоты были родственники пациентов и неродственные доноры, которые соответствовали требованиям инфекционной безопасности. До и после ТФМ в дни +3, +8, +16, +30, +45, +60, +75, +90 для определения основных групп кишечных микроорганизмов проведено исследование стула методом мультиплексной ПЦР («Колонофлор-16»). Трем пациентам до ТФМ выполнено 16S РНК секвенирование образцов стула. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> У 64% пациентов отмечен полный клинический ответ. Сокращение частоты и объема диареи в 2 раза наблюдали на Д+18 (1-39) и Д+14 (1-11) после ТФМ соответственно. Полный регресс патологических примесей в стуле (кровь, слизь) регистрировали на Д+13 (2-11), Д+30 (1- 97) и абдоминального болевого синдрома на Д+15 (5-31) соответственно. Клостридиальный токсин-В в образцах стула на Д+30 не определялся у 4 (50%) ранее положительных пациентов. Результаты мультиплексной ПЦР показали изменение микробиоты кишечника после ТФМ. Максимальное увеличение основных групп кишечных микроорганизмов регистрировали после ТФМ для общей бактериальной массы на Д+8 с 3E+08 (9,E+05/1E+11) до 1,65E+12 (7E+10/7E+12), для Lactobacillus spp. на Д+3 с 7E+05 (1E+04/2E+09) до 3E+08 (7E+05/3E+09), для Bifidobacterium spp. на Д+30 с 3E+06 (9E+04/3E+08) до 1E+08 (3E+06/6E+09), для Escherichia coli на Д+3 с 7E+05 (0,0E+00/7E+06) до 3E+07 (2E+06/3E+09), для Bacteroides fragilis group на Д+8 с 1,1E+07 (0,0E+00/4E+08) до 1,6E+12 (3E+06/7E+12), для Faecalibacterium prausnitzii на Д+3 с 3E+05 (0,0E+00/8E+07) до 3E+08 (1E+05/3E+09). 16S РНК-секвенирование образцов стула до ТФМ выявило выраженные нарушения микробиоты кишечника с преобладанием микроорганизмов следующих семейств: Streptococcaceae, Staphylococcaceae, Enterococcaceae. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> ТФМ имеет высокую клиническую эффективность и безопасность у пациентов после алло-ТГСК при развитии инфекции, ассоциированной с Clostridium difficile и РТПХ кишечника. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, трансплантация фекальной микробиоты, реакция трансплантат против хозяина. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(214) "Трансплантация фекальной микробиоты у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(214) "Трансплантация фекальной микробиоты у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(214) "Трансплантация фекальной микробиоты у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_META_TITLE"]=> string(214) "Трансплантация фекальной микробиоты у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_META_KEYWORDS"]=> string(214) "Трансплантация фекальной микробиоты у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_META_DESCRIPTION"]=> string(214) "Трансплантация фекальной микробиоты у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_ALT"]=> string(214) "Трансплантация фекальной микробиоты у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_TITLE"]=> string(214) "Трансплантация фекальной микробиоты у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "transplantatsiya-fekalnoy-mikrobioty-u-patsientov-posle-allogennoy-transplantatsii-gemopoeticheskikh" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(214) "Трансплантация фекальной микробиоты у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(214) "Трансплантация фекальной микробиоты у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "transplantatsiya-fekalnoy-mikrobioty-u-patsientov-posle-allogennoy-transplantatsii-gemopoeticheskikh" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "transplantatsiya-fekalnoy-mikrobioty-u-patsientov-posle-allogennoy-transplantatsii-gemopoeticheskikh" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "transplantatsiya-fekalnoy-mikrobioty-u-patsientov-posle-allogennoy-transplantatsii-gemopoeticheskikh" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20425" ["VALUE"]=> array(2) { ["TEXT"]=> string(846) "Олег В. Голощапов <sup>1</sup>, Максим А. Кучер <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Александр Н. Швецов <sup>1</sup>, Руслана В. Клементьева <sup>1</sup>, Александр А. Щербаков <sup>1</sup>, Сергей В. Сидоренко <sup>2</sup>, Владимир А. Гостев <sup>2</sup>, Мария А. Суворова <sup>3</sup>, Оксана В. Станевич <sup>1</sup>, Евгений А. Бакин <sup>1</sup>, Алексей Б. Чухловин <sup>1</sup>, Людмила С. Зубаровская <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(678) "Олег В. Голощапов 1, Максим А. Кучер 1, Иван С. Моисеев 1, Александр Н. Швецов 1, Руслана В. Клементьева 1, Александр А. Щербаков 1, Сергей В. Сидоренко 2, Владимир А. Гостев 2, Мария А. Суворова 3, Оксана В. Станевич 1, Евгений А. Бакин 1, Алексей Б. Чухловин 1, Людмила С. Зубаровская 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20426" ["VALUE"]=> array(2) { ["TEXT"]=> string(707) "<sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия <sup>2</sup> ФГБУ Детский научно-клинический центр инфекционных болезней, Санкт-Петербург, Россия <sup>3</sup> Научно-исследовательская лаборатория Explana, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(671) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия 2 ФГБУ Детский научно-клинический центр инфекционных болезней, Санкт-Петербург, Россия 3 Научно-исследовательская лаборатория Explana, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20427" ["VALUE"]=> array(2) { ["TEXT"]=> string(8450) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод терапии онкологических, гематологических и наследственных заболеваний. Распространенными осложнениями алло-ТГСК, которые приводят к снижению эффективности лечения, являются: инфекционное поражение желудочно-кишечного тракта вирусной этиологии и/или ассоциированное с Clostridium difficile на фоне иммунодефицита; антибиотикассоциированная диарея; реакция трансплантат против хозяина (РТПХ). Трансплантация фекальной микробиоты (ТФМ) от здорового донора может приводить к эрадикации патогенных микроорганизмов, модуляции иммунной системы реципиента и как следствие к снижению активности РТПХ кишечника. Целью работы является повыщение эффективности лечения осложнений у пациентов после алло-ТГСК ассоциированных с Clostridium difficile и РТПХ кишечника. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> С 2015 по 2018 год в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой в одноцентровое, проспективное исследование включено 11 пациентов после алло-ТГСК от неродственного донора – 36,5% (n=4), родственного – 9% (n=1), гаплоидентичного – 54,5% (n=6) с целью терапии острого лимфобластного лейкоза – 18,3% (n=2), острого миелоидного лейкоза – 27,4% (n=3), миелодиспластического синдрома – 18,3% (n=2), бета-талассемии – 9% (n=1), хронического миелолейкоза – 9% (n=1), Лимфомы Ходжкина – 9% (n=1), анемии Фанкони – 9% (n=1). Для лечения посттрансплантационных осложнений всем пациентам была выполнена ТФМ. Медиана возраста составила 24 года (2-45). Из исследования исключено трое больных из-за нарушения техники ТФМ (n=2), развития тяжелого синдрома системного воспалительного ответа (n=1). Длительность диареи перед ТФМ составила от 1 до 6 мес. (медиана – 2,3) и наблюдалась у всех пациентов. У 5 (45,5%) больных регистрировали активное кишечное кровотечение с необходимостью ежедневных гемотрансфузий для коррекции анемического синдрома, еще у 4 (36,4%) больных в стуле определялись прожилки крови. В состоянии сепсиса было 5 пациентов (45,5%), а один пациент находился в состоянии септического шока (Klebsiella pneumoniае) и получал антибактериальную терапию, вазопрессоры, искусственную вентиляцию легких. Абдоминальный болевой синдром, требующий анальгезии наркотическими анальгетиками отмечали у 9 (81,8%) пациентов. Парез кишечника наблюдали у 5 (45,5%) больных. У 8 (72,7%) пациентов выявлен положительный клостридиальный токсин-В в стуле, повышенный уровень фекального кальпротектина до ТФМ у 7 (63,6%) пациентов 600 мкг/г (220-6706). Введение фекального трансплантата выполняли на Д+168 (27-1107). Донорами микробиоты были родственники пациентов и неродственные доноры, которые соответствовали требованиям инфекционной безопасности. До и после ТФМ в дни +3, +8, +16, +30, +45, +60, +75, +90 для определения основных групп кишечных микроорганизмов проведено исследование стула методом мультиплексной ПЦР («Колонофлор-16»). Трем пациентам до ТФМ выполнено 16S РНК секвенирование образцов стула. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> У 64% пациентов отмечен полный клинический ответ. Сокращение частоты и объема диареи в 2 раза наблюдали на Д+18 (1-39) и Д+14 (1-11) после ТФМ соответственно. Полный регресс патологических примесей в стуле (кровь, слизь) регистрировали на Д+13 (2-11), Д+30 (1- 97) и абдоминального болевого синдрома на Д+15 (5-31) соответственно. Клостридиальный токсин-В в образцах стула на Д+30 не определялся у 4 (50%) ранее положительных пациентов. Результаты мультиплексной ПЦР показали изменение микробиоты кишечника после ТФМ. Максимальное увеличение основных групп кишечных микроорганизмов регистрировали после ТФМ для общей бактериальной массы на Д+8 с 3E+08 (9,E+05/1E+11) до 1,65E+12 (7E+10/7E+12), для Lactobacillus spp. на Д+3 с 7E+05 (1E+04/2E+09) до 3E+08 (7E+05/3E+09), для Bifidobacterium spp. на Д+30 с 3E+06 (9E+04/3E+08) до 1E+08 (3E+06/6E+09), для Escherichia coli на Д+3 с 7E+05 (0,0E+00/7E+06) до 3E+07 (2E+06/3E+09), для Bacteroides fragilis group на Д+8 с 1,1E+07 (0,0E+00/4E+08) до 1,6E+12 (3E+06/7E+12), для Faecalibacterium prausnitzii на Д+3 с 3E+05 (0,0E+00/8E+07) до 3E+08 (1E+05/3E+09). 16S РНК-секвенирование образцов стула до ТФМ выявило выраженные нарушения микробиоты кишечника с преобладанием микроорганизмов следующих семейств: Streptococcaceae, Staphylococcaceae, Enterococcaceae. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> ТФМ имеет высокую клиническую эффективность и безопасность у пациентов после алло-ТГСК при развитии инфекции, ассоциированной с Clostridium difficile и РТПХ кишечника. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, трансплантация фекальной микробиоты, реакция трансплантат против хозяина. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(8230) "Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод терапии онкологических, гематологических и наследственных заболеваний. Распространенными осложнениями алло-ТГСК, которые приводят к снижению эффективности лечения, являются: инфекционное поражение желудочно-кишечного тракта вирусной этиологии и/или ассоциированное с Clostridium difficile на фоне иммунодефицита; антибиотикассоциированная диарея; реакция трансплантат против хозяина (РТПХ). Трансплантация фекальной микробиоты (ТФМ) от здорового донора может приводить к эрадикации патогенных микроорганизмов, модуляции иммунной системы реципиента и как следствие к снижению активности РТПХ кишечника. Целью работы является повыщение эффективности лечения осложнений у пациентов после алло-ТГСК ассоциированных с Clostridium difficile и РТПХ кишечника.
Пациенты и методы
С 2015 по 2018 год в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой в одноцентровое, проспективное исследование включено 11 пациентов после алло-ТГСК от неродственного донора – 36,5% (n=4), родственного – 9% (n=1), гаплоидентичного – 54,5% (n=6) с целью терапии острого лимфобластного лейкоза – 18,3% (n=2), острого миелоидного лейкоза – 27,4% (n=3), миелодиспластического синдрома – 18,3% (n=2), бета-талассемии – 9% (n=1), хронического миелолейкоза – 9% (n=1), Лимфомы Ходжкина – 9% (n=1), анемии Фанкони – 9% (n=1). Для лечения посттрансплантационных осложнений всем пациентам была выполнена ТФМ. Медиана возраста составила 24 года (2-45). Из исследования исключено трое больных из-за нарушения техники ТФМ (n=2), развития тяжелого синдрома системного воспалительного ответа (n=1). Длительность диареи перед ТФМ составила от 1 до 6 мес. (медиана – 2,3) и наблюдалась у всех пациентов. У 5 (45,5%) больных регистрировали активное кишечное кровотечение с необходимостью ежедневных гемотрансфузий для коррекции анемического синдрома, еще у 4 (36,4%) больных в стуле определялись прожилки крови. В состоянии сепсиса было 5 пациентов (45,5%), а один пациент находился в состоянии септического шока (Klebsiella pneumoniае) и получал антибактериальную терапию, вазопрессоры, искусственную вентиляцию легких. Абдоминальный болевой синдром, требующий анальгезии наркотическими анальгетиками отмечали у 9 (81,8%) пациентов. Парез кишечника наблюдали у 5 (45,5%) больных. У 8 (72,7%) пациентов выявлен положительный клостридиальный токсин-В в стуле, повышенный уровень фекального кальпротектина до ТФМ у 7 (63,6%) пациентов 600 мкг/г (220-6706). Введение фекального трансплантата выполняли на Д+168 (27-1107). Донорами микробиоты были родственники пациентов и неродственные доноры, которые соответствовали требованиям инфекционной безопасности. До и после ТФМ в дни +3, +8, +16, +30, +45, +60, +75, +90 для определения основных групп кишечных микроорганизмов проведено исследование стула методом мультиплексной ПЦР («Колонофлор-16»). Трем пациентам до ТФМ выполнено 16S РНК секвенирование образцов стула.
Результаты
У 64% пациентов отмечен полный клинический ответ. Сокращение частоты и объема диареи в 2 раза наблюдали на Д+18 (1-39) и Д+14 (1-11) после ТФМ соответственно. Полный регресс патологических примесей в стуле (кровь, слизь) регистрировали на Д+13 (2-11), Д+30 (1- 97) и абдоминального болевого синдрома на Д+15 (5-31) соответственно. Клостридиальный токсин-В в образцах стула на Д+30 не определялся у 4 (50%) ранее положительных пациентов. Результаты мультиплексной ПЦР показали изменение микробиоты кишечника после ТФМ. Максимальное увеличение основных групп кишечных микроорганизмов регистрировали после ТФМ для общей бактериальной массы на Д+8 с 3E+08 (9,E+05/1E+11) до 1,65E+12 (7E+10/7E+12), для Lactobacillus spp. на Д+3 с 7E+05 (1E+04/2E+09) до 3E+08 (7E+05/3E+09), для Bifidobacterium spp. на Д+30 с 3E+06 (9E+04/3E+08) до 1E+08 (3E+06/6E+09), для Escherichia coli на Д+3 с 7E+05 (0,0E+00/7E+06) до 3E+07 (2E+06/3E+09), для Bacteroides fragilis group на Д+8 с 1,1E+07 (0,0E+00/4E+08) до 1,6E+12 (3E+06/7E+12), для Faecalibacterium prausnitzii на Д+3 с 3E+05 (0,0E+00/8E+07) до 3E+08 (1E+05/3E+09). 16S РНК-секвенирование образцов стула до ТФМ выявило выраженные нарушения микробиоты кишечника с преобладанием микроорганизмов следующих семейств: Streptococcaceae, Staphylococcaceae, Enterococcaceae.
Выводы
ТФМ имеет высокую клиническую эффективность и безопасность у пациентов после алло-ТГСК при развитии инфекции, ассоциированной с Clostridium difficile и РТПХ кишечника.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, трансплантация фекальной микробиоты, реакция трансплантат против хозяина.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20428" ["VALUE"]=> array(2) { ["TEXT"]=> string(641) "Oleg V. Goloshchapov <sup>1</sup>, Maxim A. Kucher <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Alexander N. Shvetcov <sup>1</sup>, Ruslana V. Klementeva <sup>1</sup>, Alexander A. Shcherbakov <sup>1</sup>, Sergey V. Sidorenko <sup>2</sup>, Vladimir A. Gostev <sup>2</sup>, Maria A. Suvorova <sup>3</sup>, Oksana V. Stanevich <sup>1</sup>, Evgeny A. Bakin <sup>1</sup>, Alexey B. Chukhlovin <sup>1</sup>, Ludmila S. Zubarovskaya <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(473) "Oleg V. Goloshchapov 1, Maxim A. Kucher 1, Ivan S. Moiseev 1, Alexander N. Shvetcov 1, Ruslana V. Klementeva 1, Alexander A. Shcherbakov 1, Sergey V. Sidorenko 2, Vladimir A. Gostev 2, Maria A. Suvorova 3, Oksana V. Stanevich 1, Evgeny A. Bakin 1, Alexey B. Chukhlovin 1, Ludmila S. Zubarovskaya 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20429" ["VALUE"]=> array(2) { ["TEXT"]=> string(368) "<sup>1</sup> Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University <sup>2</sup> Pediatric Research and Clinical Center for Infectious Diseases, St. Petersburg, Russia <sup>3</sup> Explana Research Laboratory, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(332) "1 Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University 2 Pediatric Research and Clinical Center for Infectious Diseases, St. Petersburg, Russia 3 Explana Research Laboratory, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20430" ["VALUE"]=> array(2) { ["TEXT"]=> string(5153) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is effective method of treatment of malignant, hematological and hereditary diseases. Common complications after allo-HSCT, which may decrease its effectiveness, include infectious lesions of the gastrointestinal tract of viral etiology and Clostridium difficile on the background of immunodeficiency, antibiotic-associated diarrhea and graftversus-host disease (GvHD). Transplantation of fecal microbiota (FMT) from a healthy donor can lead to eradication of pathogens, modulation of the recipient’s immune system and as a consequence to a decrease in intestinal GVHD activity. Aim of our study was to increase treatment efficiency of complications associated with Clostridium difficile and intestinal GvHD in patients after allo-HSCT. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> From 2015 to 2018 in Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation 11 patients after allo-HSCT from matched unrelated donor – 36.5% (n=4), related donor – 9% (n=1), haploidentical donor – 54.5% (n=6) with acute lymphoblastic leukemia – 18.3% (n=2), acute myeloid leukemia – 27.4% (n=3), myelodysplastic syndrome – 18.3% (n=2), beta-thalassemia – 9% (n=1), chronic myeloid leukemia – 9% (n=1), Hodgkin’s lymphoma – 9% (n=1), Fanconi’s anemia – 9% (n=1) were included in a single-center prospective study. All patients underwent FMT for the treatment of posttransplant complications. The median age was 24 years (2-45). Three patients were excluded from the study due to violation of FMT technique (n=2), development of severe systemic inflammatory response syndrome (n=1). The duration of diarrhea before FMT was from 1 to 6 months (median – 2.3) and was observed in all patients. Active intestinal bleeding with the need of daily blood transfusions for the correction of anemic syndrome was registered in 5 (45.5%) patients, additionally blood impurity in stool was determined in 4 (36.4%) patients. 5 patients had sepsis (45.5%) and one patient was in septic shock associated with Klebsiella pneumoniae and received antibiotic therapy, vasopressors, mechanical ventilation. Abdominal pain requiring analgesia with opioids was noted in 9 (81.8%) patients. Gastrointestinal paresis was observed in 5 (45.5%) patients. 8 (72.7%) patients had positive clostridial toxin-B in stool. Elevated fecal calprotectin level – 600 μg/g (220-6706) before FMT was identified in 7 (63.6%) patients. FMT was performed on D+168 (27-1107). Microbiota donors were patient’s relatives or unrelated donors who met all infectious safety requirements. Before and after FMT D+3, D+8, D+16, D+30, D+45, D+60, D+75, D+90 real-time multiplex PCR (“Colonoflor-16”) was performed to determine the main groups of intestinal microorganisms. 3 patients underwent 16S RNA stool sequencing prior FMT. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> A complete clinical response was observed in 64% of patients. The reduction in the frequency and volume of diarrhea by 2 times was observed on D+18 (1 – 39) and D+14 (1 – 11) after FMT, respectively. Complete regression of pathological impurities in the stool (blood, mucus) was recorded at D+13 (2-11), D+30 (1-97) and abdominal pain syndrome at D+15 (5-31), respectively. Clostridial toxin-B in stool samples at D+30 was not detected in 4 (50%) previously positive cases. The results of multiplex PCR showed changes in gut microbiota after FMT. The maximum increase in the main groups of intestinal microorganisms was recorded after FMT for the total bacterial mass at D+8 from 3E+08 (9,E+05/ 1E+11) to 1,65 E+12 (7E+10/ 7E+12), for Lactobacillus spp. on D+3 7E+05 (1E+04/2E+09) to 3E+08 (7E+05/ 3E+09) and for Bifidobacterium spp. on D+30 3E+06 (9E+04/ 3E+08) to 1E+08 (3E+06/ 6E+09), Escherichia coli on D+3 7E+05 (0.0 E+00/7E+06) to 3E+07 (2E+06/ 3E+09), for Bacteroides fragilis group on D+8 1.1 E+07 (0.0 E+00/4E+08) to 1.6 E+12 (3E+06/7E+12), Faecalibacterium prausnitzii on D+3 3E+05 (0.0 E+00/8E+07) to 3E+08 (1E+05/ 3E+09). 16S RNA stool sequencing before FMT revealed marked disturbances of intestinal microbiota with predominance of microorganisms of the following families: Streptococcaceae, Staphylococcaceae, Enterococcaceae. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> FMT is effective and safe method of treatment for infectious complications associated with Clostridium difficile and intestinal GvHD in patients after allo-HCST. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cell transplantation, fecal microbiota transplantation, graft-versus-host disease. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4933) "Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is effective method of treatment of malignant, hematological and hereditary diseases. Common complications after allo-HSCT, which may decrease its effectiveness, include infectious lesions of the gastrointestinal tract of viral etiology and Clostridium difficile on the background of immunodeficiency, antibiotic-associated diarrhea and graftversus-host disease (GvHD). Transplantation of fecal microbiota (FMT) from a healthy donor can lead to eradication of pathogens, modulation of the recipient’s immune system and as a consequence to a decrease in intestinal GVHD activity. Aim of our study was to increase treatment efficiency of complications associated with Clostridium difficile and intestinal GvHD in patients after allo-HSCT.
Patients and methods
From 2015 to 2018 in Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation 11 patients after allo-HSCT from matched unrelated donor – 36.5% (n=4), related donor – 9% (n=1), haploidentical donor – 54.5% (n=6) with acute lymphoblastic leukemia – 18.3% (n=2), acute myeloid leukemia – 27.4% (n=3), myelodysplastic syndrome – 18.3% (n=2), beta-thalassemia – 9% (n=1), chronic myeloid leukemia – 9% (n=1), Hodgkin’s lymphoma – 9% (n=1), Fanconi’s anemia – 9% (n=1) were included in a single-center prospective study. All patients underwent FMT for the treatment of posttransplant complications. The median age was 24 years (2-45). Three patients were excluded from the study due to violation of FMT technique (n=2), development of severe systemic inflammatory response syndrome (n=1). The duration of diarrhea before FMT was from 1 to 6 months (median – 2.3) and was observed in all patients. Active intestinal bleeding with the need of daily blood transfusions for the correction of anemic syndrome was registered in 5 (45.5%) patients, additionally blood impurity in stool was determined in 4 (36.4%) patients. 5 patients had sepsis (45.5%) and one patient was in septic shock associated with Klebsiella pneumoniae and received antibiotic therapy, vasopressors, mechanical ventilation. Abdominal pain requiring analgesia with opioids was noted in 9 (81.8%) patients. Gastrointestinal paresis was observed in 5 (45.5%) patients. 8 (72.7%) patients had positive clostridial toxin-B in stool. Elevated fecal calprotectin level – 600 μg/g (220-6706) before FMT was identified in 7 (63.6%) patients. FMT was performed on D+168 (27-1107). Microbiota donors were patient’s relatives or unrelated donors who met all infectious safety requirements. Before and after FMT D+3, D+8, D+16, D+30, D+45, D+60, D+75, D+90 real-time multiplex PCR (“Colonoflor-16”) was performed to determine the main groups of intestinal microorganisms. 3 patients underwent 16S RNA stool sequencing prior FMT.
Results
A complete clinical response was observed in 64% of patients. The reduction in the frequency and volume of diarrhea by 2 times was observed on D+18 (1 – 39) and D+14 (1 – 11) after FMT, respectively. Complete regression of pathological impurities in the stool (blood, mucus) was recorded at D+13 (2-11), D+30 (1-97) and abdominal pain syndrome at D+15 (5-31), respectively. Clostridial toxin-B in stool samples at D+30 was not detected in 4 (50%) previously positive cases. The results of multiplex PCR showed changes in gut microbiota after FMT. The maximum increase in the main groups of intestinal microorganisms was recorded after FMT for the total bacterial mass at D+8 from 3E+08 (9,E+05/ 1E+11) to 1,65 E+12 (7E+10/ 7E+12), for Lactobacillus spp. on D+3 7E+05 (1E+04/2E+09) to 3E+08 (7E+05/ 3E+09) and for Bifidobacterium spp. on D+30 3E+06 (9E+04/ 3E+08) to 1E+08 (3E+06/ 6E+09), Escherichia coli on D+3 7E+05 (0.0 E+00/7E+06) to 3E+07 (2E+06/ 3E+09), for Bacteroides fragilis group on D+8 1.1 E+07 (0.0 E+00/4E+08) to 1.6 E+12 (3E+06/7E+12), Faecalibacterium prausnitzii on D+3 3E+05 (0.0 E+00/8E+07) to 3E+08 (1E+05/ 3E+09). 16S RNA stool sequencing before FMT revealed marked disturbances of intestinal microbiota with predominance of microorganisms of the following families: Streptococcaceae, Staphylococcaceae, Enterococcaceae.
Conclusion
FMT is effective and safe method of treatment for infectious complications associated with Clostridium difficile and intestinal GvHD in patients after allo-HCST.
Keywords
Hematopoietic stem cell transplantation, fecal microbiota transplantation, graft-versus-host disease.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20431" ["VALUE"]=> string(101) "Fecal microbiota transplantation in patients after allogeneic hematopoietic stem cell transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(101) "Fecal microbiota transplantation in patients after allogeneic hematopoietic stem cell transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20765" ["VALUE"]=> string(4) "1401" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1401" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20766" ["VALUE"]=> string(4) "1402" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1402" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20428" ["VALUE"]=> array(2) { ["TEXT"]=> string(641) "Oleg V. Goloshchapov <sup>1</sup>, Maxim A. Kucher <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Alexander N. Shvetcov <sup>1</sup>, Ruslana V. Klementeva <sup>1</sup>, Alexander A. Shcherbakov <sup>1</sup>, Sergey V. Sidorenko <sup>2</sup>, Vladimir A. Gostev <sup>2</sup>, Maria A. Suvorova <sup>3</sup>, Oksana V. Stanevich <sup>1</sup>, Evgeny A. Bakin <sup>1</sup>, Alexey B. Chukhlovin <sup>1</sup>, Ludmila S. Zubarovskaya <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(473) "Oleg V. Goloshchapov 1, Maxim A. Kucher 1, Ivan S. Moiseev 1, Alexander N. Shvetcov 1, Ruslana V. Klementeva 1, Alexander A. Shcherbakov 1, Sergey V. Sidorenko 2, Vladimir A. Gostev 2, Maria A. Suvorova 3, Oksana V. Stanevich 1, Evgeny A. Bakin 1, Alexey B. Chukhlovin 1, Ludmila S. Zubarovskaya 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(473) "Oleg V. Goloshchapov 1, Maxim A. Kucher 1, Ivan S. Moiseev 1, Alexander N. Shvetcov 1, Ruslana V. Klementeva 1, Alexander A. Shcherbakov 1, Sergey V. Sidorenko 2, Vladimir A. Gostev 2, Maria A. Suvorova 3, Oksana V. Stanevich 1, Evgeny A. Bakin 1, Alexey B. Chukhlovin 1, Ludmila S. Zubarovskaya 1, Boris V. Afanasyev 1" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20430" ["VALUE"]=> array(2) { ["TEXT"]=> string(5153) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is effective method of treatment of malignant, hematological and hereditary diseases. Common complications after allo-HSCT, which may decrease its effectiveness, include infectious lesions of the gastrointestinal tract of viral etiology and Clostridium difficile on the background of immunodeficiency, antibiotic-associated diarrhea and graftversus-host disease (GvHD). Transplantation of fecal microbiota (FMT) from a healthy donor can lead to eradication of pathogens, modulation of the recipient’s immune system and as a consequence to a decrease in intestinal GVHD activity. Aim of our study was to increase treatment efficiency of complications associated with Clostridium difficile and intestinal GvHD in patients after allo-HSCT. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> From 2015 to 2018 in Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation 11 patients after allo-HSCT from matched unrelated donor – 36.5% (n=4), related donor – 9% (n=1), haploidentical donor – 54.5% (n=6) with acute lymphoblastic leukemia – 18.3% (n=2), acute myeloid leukemia – 27.4% (n=3), myelodysplastic syndrome – 18.3% (n=2), beta-thalassemia – 9% (n=1), chronic myeloid leukemia – 9% (n=1), Hodgkin’s lymphoma – 9% (n=1), Fanconi’s anemia – 9% (n=1) were included in a single-center prospective study. All patients underwent FMT for the treatment of posttransplant complications. The median age was 24 years (2-45). Three patients were excluded from the study due to violation of FMT technique (n=2), development of severe systemic inflammatory response syndrome (n=1). The duration of diarrhea before FMT was from 1 to 6 months (median – 2.3) and was observed in all patients. Active intestinal bleeding with the need of daily blood transfusions for the correction of anemic syndrome was registered in 5 (45.5%) patients, additionally blood impurity in stool was determined in 4 (36.4%) patients. 5 patients had sepsis (45.5%) and one patient was in septic shock associated with Klebsiella pneumoniae and received antibiotic therapy, vasopressors, mechanical ventilation. Abdominal pain requiring analgesia with opioids was noted in 9 (81.8%) patients. Gastrointestinal paresis was observed in 5 (45.5%) patients. 8 (72.7%) patients had positive clostridial toxin-B in stool. Elevated fecal calprotectin level – 600 μg/g (220-6706) before FMT was identified in 7 (63.6%) patients. FMT was performed on D+168 (27-1107). Microbiota donors were patient’s relatives or unrelated donors who met all infectious safety requirements. Before and after FMT D+3, D+8, D+16, D+30, D+45, D+60, D+75, D+90 real-time multiplex PCR (“Colonoflor-16”) was performed to determine the main groups of intestinal microorganisms. 3 patients underwent 16S RNA stool sequencing prior FMT. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> A complete clinical response was observed in 64% of patients. The reduction in the frequency and volume of diarrhea by 2 times was observed on D+18 (1 – 39) and D+14 (1 – 11) after FMT, respectively. Complete regression of pathological impurities in the stool (blood, mucus) was recorded at D+13 (2-11), D+30 (1-97) and abdominal pain syndrome at D+15 (5-31), respectively. Clostridial toxin-B in stool samples at D+30 was not detected in 4 (50%) previously positive cases. The results of multiplex PCR showed changes in gut microbiota after FMT. The maximum increase in the main groups of intestinal microorganisms was recorded after FMT for the total bacterial mass at D+8 from 3E+08 (9,E+05/ 1E+11) to 1,65 E+12 (7E+10/ 7E+12), for Lactobacillus spp. on D+3 7E+05 (1E+04/2E+09) to 3E+08 (7E+05/ 3E+09) and for Bifidobacterium spp. on D+30 3E+06 (9E+04/ 3E+08) to 1E+08 (3E+06/ 6E+09), Escherichia coli on D+3 7E+05 (0.0 E+00/7E+06) to 3E+07 (2E+06/ 3E+09), for Bacteroides fragilis group on D+8 1.1 E+07 (0.0 E+00/4E+08) to 1.6 E+12 (3E+06/7E+12), Faecalibacterium prausnitzii on D+3 3E+05 (0.0 E+00/8E+07) to 3E+08 (1E+05/ 3E+09). 16S RNA stool sequencing before FMT revealed marked disturbances of intestinal microbiota with predominance of microorganisms of the following families: Streptococcaceae, Staphylococcaceae, Enterococcaceae. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> FMT is effective and safe method of treatment for infectious complications associated with Clostridium difficile and intestinal GvHD in patients after allo-HCST. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cell transplantation, fecal microbiota transplantation, graft-versus-host disease. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4933) "Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is effective method of treatment of malignant, hematological and hereditary diseases. Common complications after allo-HSCT, which may decrease its effectiveness, include infectious lesions of the gastrointestinal tract of viral etiology and Clostridium difficile on the background of immunodeficiency, antibiotic-associated diarrhea and graftversus-host disease (GvHD). Transplantation of fecal microbiota (FMT) from a healthy donor can lead to eradication of pathogens, modulation of the recipient’s immune system and as a consequence to a decrease in intestinal GVHD activity. Aim of our study was to increase treatment efficiency of complications associated with Clostridium difficile and intestinal GvHD in patients after allo-HSCT.
Patients and methods
From 2015 to 2018 in Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation 11 patients after allo-HSCT from matched unrelated donor – 36.5% (n=4), related donor – 9% (n=1), haploidentical donor – 54.5% (n=6) with acute lymphoblastic leukemia – 18.3% (n=2), acute myeloid leukemia – 27.4% (n=3), myelodysplastic syndrome – 18.3% (n=2), beta-thalassemia – 9% (n=1), chronic myeloid leukemia – 9% (n=1), Hodgkin’s lymphoma – 9% (n=1), Fanconi’s anemia – 9% (n=1) were included in a single-center prospective study. All patients underwent FMT for the treatment of posttransplant complications. The median age was 24 years (2-45). Three patients were excluded from the study due to violation of FMT technique (n=2), development of severe systemic inflammatory response syndrome (n=1). The duration of diarrhea before FMT was from 1 to 6 months (median – 2.3) and was observed in all patients. Active intestinal bleeding with the need of daily blood transfusions for the correction of anemic syndrome was registered in 5 (45.5%) patients, additionally blood impurity in stool was determined in 4 (36.4%) patients. 5 patients had sepsis (45.5%) and one patient was in septic shock associated with Klebsiella pneumoniae and received antibiotic therapy, vasopressors, mechanical ventilation. Abdominal pain requiring analgesia with opioids was noted in 9 (81.8%) patients. Gastrointestinal paresis was observed in 5 (45.5%) patients. 8 (72.7%) patients had positive clostridial toxin-B in stool. Elevated fecal calprotectin level – 600 μg/g (220-6706) before FMT was identified in 7 (63.6%) patients. FMT was performed on D+168 (27-1107). Microbiota donors were patient’s relatives or unrelated donors who met all infectious safety requirements. Before and after FMT D+3, D+8, D+16, D+30, D+45, D+60, D+75, D+90 real-time multiplex PCR (“Colonoflor-16”) was performed to determine the main groups of intestinal microorganisms. 3 patients underwent 16S RNA stool sequencing prior FMT.
Results
A complete clinical response was observed in 64% of patients. The reduction in the frequency and volume of diarrhea by 2 times was observed on D+18 (1 – 39) and D+14 (1 – 11) after FMT, respectively. Complete regression of pathological impurities in the stool (blood, mucus) was recorded at D+13 (2-11), D+30 (1-97) and abdominal pain syndrome at D+15 (5-31), respectively. Clostridial toxin-B in stool samples at D+30 was not detected in 4 (50%) previously positive cases. The results of multiplex PCR showed changes in gut microbiota after FMT. The maximum increase in the main groups of intestinal microorganisms was recorded after FMT for the total bacterial mass at D+8 from 3E+08 (9,E+05/ 1E+11) to 1,65 E+12 (7E+10/ 7E+12), for Lactobacillus spp. on D+3 7E+05 (1E+04/2E+09) to 3E+08 (7E+05/ 3E+09) and for Bifidobacterium spp. on D+30 3E+06 (9E+04/ 3E+08) to 1E+08 (3E+06/ 6E+09), Escherichia coli on D+3 7E+05 (0.0 E+00/7E+06) to 3E+07 (2E+06/ 3E+09), for Bacteroides fragilis group on D+8 1.1 E+07 (0.0 E+00/4E+08) to 1.6 E+12 (3E+06/7E+12), Faecalibacterium prausnitzii on D+3 3E+05 (0.0 E+00/8E+07) to 3E+08 (1E+05/ 3E+09). 16S RNA stool sequencing before FMT revealed marked disturbances of intestinal microbiota with predominance of microorganisms of the following families: Streptococcaceae, Staphylococcaceae, Enterococcaceae.
Conclusion
FMT is effective and safe method of treatment for infectious complications associated with Clostridium difficile and intestinal GvHD in patients after allo-HCST.
Keywords
Hematopoietic stem cell transplantation, fecal microbiota transplantation, graft-versus-host disease.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4933) "Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is effective method of treatment of malignant, hematological and hereditary diseases. Common complications after allo-HSCT, which may decrease its effectiveness, include infectious lesions of the gastrointestinal tract of viral etiology and Clostridium difficile on the background of immunodeficiency, antibiotic-associated diarrhea and graftversus-host disease (GvHD). Transplantation of fecal microbiota (FMT) from a healthy donor can lead to eradication of pathogens, modulation of the recipient’s immune system and as a consequence to a decrease in intestinal GVHD activity. Aim of our study was to increase treatment efficiency of complications associated with Clostridium difficile and intestinal GvHD in patients after allo-HSCT.
Patients and methods
From 2015 to 2018 in Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation 11 patients after allo-HSCT from matched unrelated donor – 36.5% (n=4), related donor – 9% (n=1), haploidentical donor – 54.5% (n=6) with acute lymphoblastic leukemia – 18.3% (n=2), acute myeloid leukemia – 27.4% (n=3), myelodysplastic syndrome – 18.3% (n=2), beta-thalassemia – 9% (n=1), chronic myeloid leukemia – 9% (n=1), Hodgkin’s lymphoma – 9% (n=1), Fanconi’s anemia – 9% (n=1) were included in a single-center prospective study. All patients underwent FMT for the treatment of posttransplant complications. The median age was 24 years (2-45). Three patients were excluded from the study due to violation of FMT technique (n=2), development of severe systemic inflammatory response syndrome (n=1). The duration of diarrhea before FMT was from 1 to 6 months (median – 2.3) and was observed in all patients. Active intestinal bleeding with the need of daily blood transfusions for the correction of anemic syndrome was registered in 5 (45.5%) patients, additionally blood impurity in stool was determined in 4 (36.4%) patients. 5 patients had sepsis (45.5%) and one patient was in septic shock associated with Klebsiella pneumoniae and received antibiotic therapy, vasopressors, mechanical ventilation. Abdominal pain requiring analgesia with opioids was noted in 9 (81.8%) patients. Gastrointestinal paresis was observed in 5 (45.5%) patients. 8 (72.7%) patients had positive clostridial toxin-B in stool. Elevated fecal calprotectin level – 600 μg/g (220-6706) before FMT was identified in 7 (63.6%) patients. FMT was performed on D+168 (27-1107). Microbiota donors were patient’s relatives or unrelated donors who met all infectious safety requirements. Before and after FMT D+3, D+8, D+16, D+30, D+45, D+60, D+75, D+90 real-time multiplex PCR (“Colonoflor-16”) was performed to determine the main groups of intestinal microorganisms. 3 patients underwent 16S RNA stool sequencing prior FMT.
Results
A complete clinical response was observed in 64% of patients. The reduction in the frequency and volume of diarrhea by 2 times was observed on D+18 (1 – 39) and D+14 (1 – 11) after FMT, respectively. Complete regression of pathological impurities in the stool (blood, mucus) was recorded at D+13 (2-11), D+30 (1-97) and abdominal pain syndrome at D+15 (5-31), respectively. Clostridial toxin-B in stool samples at D+30 was not detected in 4 (50%) previously positive cases. The results of multiplex PCR showed changes in gut microbiota after FMT. The maximum increase in the main groups of intestinal microorganisms was recorded after FMT for the total bacterial mass at D+8 from 3E+08 (9,E+05/ 1E+11) to 1,65 E+12 (7E+10/ 7E+12), for Lactobacillus spp. on D+3 7E+05 (1E+04/2E+09) to 3E+08 (7E+05/ 3E+09) and for Bifidobacterium spp. on D+30 3E+06 (9E+04/ 3E+08) to 1E+08 (3E+06/ 6E+09), Escherichia coli on D+3 7E+05 (0.0 E+00/7E+06) to 3E+07 (2E+06/ 3E+09), for Bacteroides fragilis group on D+8 1.1 E+07 (0.0 E+00/4E+08) to 1.6 E+12 (3E+06/7E+12), Faecalibacterium prausnitzii on D+3 3E+05 (0.0 E+00/8E+07) to 3E+08 (1E+05/ 3E+09). 16S RNA stool sequencing before FMT revealed marked disturbances of intestinal microbiota with predominance of microorganisms of the following families: Streptococcaceae, Staphylococcaceae, Enterococcaceae.
Conclusion
FMT is effective and safe method of treatment for infectious complications associated with Clostridium difficile and intestinal GvHD in patients after allo-HCST.
Keywords
Hematopoietic stem cell transplantation, fecal microbiota transplantation, graft-versus-host disease.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20431" ["VALUE"]=> string(101) "Fecal microbiota transplantation in patients after allogeneic hematopoietic stem cell transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(101) "Fecal microbiota transplantation in patients after allogeneic hematopoietic stem cell transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(101) "Fecal microbiota transplantation in patients after allogeneic hematopoietic stem cell transplantation" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20429" ["VALUE"]=> array(2) { ["TEXT"]=> string(368) "<sup>1</sup> Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University <sup>2</sup> Pediatric Research and Clinical Center for Infectious Diseases, St. Petersburg, Russia <sup>3</sup> Explana Research Laboratory, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(332) "1 Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University 2 Pediatric Research and Clinical Center for Infectious Diseases, St. Petersburg, Russia 3 Explana Research Laboratory, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(332) "1 Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University 2 Pediatric Research and Clinical Center for Infectious Diseases, St. Petersburg, Russia 3 Explana Research Laboratory, St. Petersburg, Russia" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20425" ["VALUE"]=> array(2) { ["TEXT"]=> string(846) "Олег В. Голощапов <sup>1</sup>, Максим А. Кучер <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Александр Н. Швецов <sup>1</sup>, Руслана В. Клементьева <sup>1</sup>, Александр А. Щербаков <sup>1</sup>, Сергей В. Сидоренко <sup>2</sup>, Владимир А. Гостев <sup>2</sup>, Мария А. Суворова <sup>3</sup>, Оксана В. Станевич <sup>1</sup>, Евгений А. Бакин <sup>1</sup>, Алексей Б. Чухловин <sup>1</sup>, Людмила С. Зубаровская <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(678) "Олег В. Голощапов 1, Максим А. Кучер 1, Иван С. Моисеев 1, Александр Н. Швецов 1, Руслана В. Клементьева 1, Александр А. Щербаков 1, Сергей В. Сидоренко 2, Владимир А. Гостев 2, Мария А. Суворова 3, Оксана В. Станевич 1, Евгений А. Бакин 1, Алексей Б. Чухловин 1, Людмила С. Зубаровская 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(678) "Олег В. Голощапов 1, Максим А. Кучер 1, Иван С. Моисеев 1, Александр Н. Швецов 1, Руслана В. Клементьева 1, Александр А. Щербаков 1, Сергей В. Сидоренко 2, Владимир А. Гостев 2, Мария А. Суворова 3, Оксана В. Станевич 1, Евгений А. Бакин 1, Алексей Б. Чухловин 1, Людмила С. Зубаровская 1, Борис В. Афанасьев 1" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20427" ["VALUE"]=> array(2) { ["TEXT"]=> string(8450) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод терапии онкологических, гематологических и наследственных заболеваний. Распространенными осложнениями алло-ТГСК, которые приводят к снижению эффективности лечения, являются: инфекционное поражение желудочно-кишечного тракта вирусной этиологии и/или ассоциированное с Clostridium difficile на фоне иммунодефицита; антибиотикассоциированная диарея; реакция трансплантат против хозяина (РТПХ). Трансплантация фекальной микробиоты (ТФМ) от здорового донора может приводить к эрадикации патогенных микроорганизмов, модуляции иммунной системы реципиента и как следствие к снижению активности РТПХ кишечника. Целью работы является повыщение эффективности лечения осложнений у пациентов после алло-ТГСК ассоциированных с Clostridium difficile и РТПХ кишечника. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> С 2015 по 2018 год в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой в одноцентровое, проспективное исследование включено 11 пациентов после алло-ТГСК от неродственного донора – 36,5% (n=4), родственного – 9% (n=1), гаплоидентичного – 54,5% (n=6) с целью терапии острого лимфобластного лейкоза – 18,3% (n=2), острого миелоидного лейкоза – 27,4% (n=3), миелодиспластического синдрома – 18,3% (n=2), бета-талассемии – 9% (n=1), хронического миелолейкоза – 9% (n=1), Лимфомы Ходжкина – 9% (n=1), анемии Фанкони – 9% (n=1). Для лечения посттрансплантационных осложнений всем пациентам была выполнена ТФМ. Медиана возраста составила 24 года (2-45). Из исследования исключено трое больных из-за нарушения техники ТФМ (n=2), развития тяжелого синдрома системного воспалительного ответа (n=1). Длительность диареи перед ТФМ составила от 1 до 6 мес. (медиана – 2,3) и наблюдалась у всех пациентов. У 5 (45,5%) больных регистрировали активное кишечное кровотечение с необходимостью ежедневных гемотрансфузий для коррекции анемического синдрома, еще у 4 (36,4%) больных в стуле определялись прожилки крови. В состоянии сепсиса было 5 пациентов (45,5%), а один пациент находился в состоянии септического шока (Klebsiella pneumoniае) и получал антибактериальную терапию, вазопрессоры, искусственную вентиляцию легких. Абдоминальный болевой синдром, требующий анальгезии наркотическими анальгетиками отмечали у 9 (81,8%) пациентов. Парез кишечника наблюдали у 5 (45,5%) больных. У 8 (72,7%) пациентов выявлен положительный клостридиальный токсин-В в стуле, повышенный уровень фекального кальпротектина до ТФМ у 7 (63,6%) пациентов 600 мкг/г (220-6706). Введение фекального трансплантата выполняли на Д+168 (27-1107). Донорами микробиоты были родственники пациентов и неродственные доноры, которые соответствовали требованиям инфекционной безопасности. До и после ТФМ в дни +3, +8, +16, +30, +45, +60, +75, +90 для определения основных групп кишечных микроорганизмов проведено исследование стула методом мультиплексной ПЦР («Колонофлор-16»). Трем пациентам до ТФМ выполнено 16S РНК секвенирование образцов стула. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> У 64% пациентов отмечен полный клинический ответ. Сокращение частоты и объема диареи в 2 раза наблюдали на Д+18 (1-39) и Д+14 (1-11) после ТФМ соответственно. Полный регресс патологических примесей в стуле (кровь, слизь) регистрировали на Д+13 (2-11), Д+30 (1- 97) и абдоминального болевого синдрома на Д+15 (5-31) соответственно. Клостридиальный токсин-В в образцах стула на Д+30 не определялся у 4 (50%) ранее положительных пациентов. Результаты мультиплексной ПЦР показали изменение микробиоты кишечника после ТФМ. Максимальное увеличение основных групп кишечных микроорганизмов регистрировали после ТФМ для общей бактериальной массы на Д+8 с 3E+08 (9,E+05/1E+11) до 1,65E+12 (7E+10/7E+12), для Lactobacillus spp. на Д+3 с 7E+05 (1E+04/2E+09) до 3E+08 (7E+05/3E+09), для Bifidobacterium spp. на Д+30 с 3E+06 (9E+04/3E+08) до 1E+08 (3E+06/6E+09), для Escherichia coli на Д+3 с 7E+05 (0,0E+00/7E+06) до 3E+07 (2E+06/3E+09), для Bacteroides fragilis group на Д+8 с 1,1E+07 (0,0E+00/4E+08) до 1,6E+12 (3E+06/7E+12), для Faecalibacterium prausnitzii на Д+3 с 3E+05 (0,0E+00/8E+07) до 3E+08 (1E+05/3E+09). 16S РНК-секвенирование образцов стула до ТФМ выявило выраженные нарушения микробиоты кишечника с преобладанием микроорганизмов следующих семейств: Streptococcaceae, Staphylococcaceae, Enterococcaceae. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> ТФМ имеет высокую клиническую эффективность и безопасность у пациентов после алло-ТГСК при развитии инфекции, ассоциированной с Clostridium difficile и РТПХ кишечника. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, трансплантация фекальной микробиоты, реакция трансплантат против хозяина. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(8230) "Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод терапии онкологических, гематологических и наследственных заболеваний. Распространенными осложнениями алло-ТГСК, которые приводят к снижению эффективности лечения, являются: инфекционное поражение желудочно-кишечного тракта вирусной этиологии и/или ассоциированное с Clostridium difficile на фоне иммунодефицита; антибиотикассоциированная диарея; реакция трансплантат против хозяина (РТПХ). Трансплантация фекальной микробиоты (ТФМ) от здорового донора может приводить к эрадикации патогенных микроорганизмов, модуляции иммунной системы реципиента и как следствие к снижению активности РТПХ кишечника. Целью работы является повыщение эффективности лечения осложнений у пациентов после алло-ТГСК ассоциированных с Clostridium difficile и РТПХ кишечника.
Пациенты и методы
С 2015 по 2018 год в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой в одноцентровое, проспективное исследование включено 11 пациентов после алло-ТГСК от неродственного донора – 36,5% (n=4), родственного – 9% (n=1), гаплоидентичного – 54,5% (n=6) с целью терапии острого лимфобластного лейкоза – 18,3% (n=2), острого миелоидного лейкоза – 27,4% (n=3), миелодиспластического синдрома – 18,3% (n=2), бета-талассемии – 9% (n=1), хронического миелолейкоза – 9% (n=1), Лимфомы Ходжкина – 9% (n=1), анемии Фанкони – 9% (n=1). Для лечения посттрансплантационных осложнений всем пациентам была выполнена ТФМ. Медиана возраста составила 24 года (2-45). Из исследования исключено трое больных из-за нарушения техники ТФМ (n=2), развития тяжелого синдрома системного воспалительного ответа (n=1). Длительность диареи перед ТФМ составила от 1 до 6 мес. (медиана – 2,3) и наблюдалась у всех пациентов. У 5 (45,5%) больных регистрировали активное кишечное кровотечение с необходимостью ежедневных гемотрансфузий для коррекции анемического синдрома, еще у 4 (36,4%) больных в стуле определялись прожилки крови. В состоянии сепсиса было 5 пациентов (45,5%), а один пациент находился в состоянии септического шока (Klebsiella pneumoniае) и получал антибактериальную терапию, вазопрессоры, искусственную вентиляцию легких. Абдоминальный болевой синдром, требующий анальгезии наркотическими анальгетиками отмечали у 9 (81,8%) пациентов. Парез кишечника наблюдали у 5 (45,5%) больных. У 8 (72,7%) пациентов выявлен положительный клостридиальный токсин-В в стуле, повышенный уровень фекального кальпротектина до ТФМ у 7 (63,6%) пациентов 600 мкг/г (220-6706). Введение фекального трансплантата выполняли на Д+168 (27-1107). Донорами микробиоты были родственники пациентов и неродственные доноры, которые соответствовали требованиям инфекционной безопасности. До и после ТФМ в дни +3, +8, +16, +30, +45, +60, +75, +90 для определения основных групп кишечных микроорганизмов проведено исследование стула методом мультиплексной ПЦР («Колонофлор-16»). Трем пациентам до ТФМ выполнено 16S РНК секвенирование образцов стула.
Результаты
У 64% пациентов отмечен полный клинический ответ. Сокращение частоты и объема диареи в 2 раза наблюдали на Д+18 (1-39) и Д+14 (1-11) после ТФМ соответственно. Полный регресс патологических примесей в стуле (кровь, слизь) регистрировали на Д+13 (2-11), Д+30 (1- 97) и абдоминального болевого синдрома на Д+15 (5-31) соответственно. Клостридиальный токсин-В в образцах стула на Д+30 не определялся у 4 (50%) ранее положительных пациентов. Результаты мультиплексной ПЦР показали изменение микробиоты кишечника после ТФМ. Максимальное увеличение основных групп кишечных микроорганизмов регистрировали после ТФМ для общей бактериальной массы на Д+8 с 3E+08 (9,E+05/1E+11) до 1,65E+12 (7E+10/7E+12), для Lactobacillus spp. на Д+3 с 7E+05 (1E+04/2E+09) до 3E+08 (7E+05/3E+09), для Bifidobacterium spp. на Д+30 с 3E+06 (9E+04/3E+08) до 1E+08 (3E+06/6E+09), для Escherichia coli на Д+3 с 7E+05 (0,0E+00/7E+06) до 3E+07 (2E+06/3E+09), для Bacteroides fragilis group на Д+8 с 1,1E+07 (0,0E+00/4E+08) до 1,6E+12 (3E+06/7E+12), для Faecalibacterium prausnitzii на Д+3 с 3E+05 (0,0E+00/8E+07) до 3E+08 (1E+05/3E+09). 16S РНК-секвенирование образцов стула до ТФМ выявило выраженные нарушения микробиоты кишечника с преобладанием микроорганизмов следующих семейств: Streptococcaceae, Staphylococcaceae, Enterococcaceae.
Выводы
ТФМ имеет высокую клиническую эффективность и безопасность у пациентов после алло-ТГСК при развитии инфекции, ассоциированной с Clostridium difficile и РТПХ кишечника.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, трансплантация фекальной микробиоты, реакция трансплантат против хозяина.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(8230) "Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод терапии онкологических, гематологических и наследственных заболеваний. Распространенными осложнениями алло-ТГСК, которые приводят к снижению эффективности лечения, являются: инфекционное поражение желудочно-кишечного тракта вирусной этиологии и/или ассоциированное с Clostridium difficile на фоне иммунодефицита; антибиотикассоциированная диарея; реакция трансплантат против хозяина (РТПХ). Трансплантация фекальной микробиоты (ТФМ) от здорового донора может приводить к эрадикации патогенных микроорганизмов, модуляции иммунной системы реципиента и как следствие к снижению активности РТПХ кишечника. Целью работы является повыщение эффективности лечения осложнений у пациентов после алло-ТГСК ассоциированных с Clostridium difficile и РТПХ кишечника.
Пациенты и методы
С 2015 по 2018 год в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой в одноцентровое, проспективное исследование включено 11 пациентов после алло-ТГСК от неродственного донора – 36,5% (n=4), родственного – 9% (n=1), гаплоидентичного – 54,5% (n=6) с целью терапии острого лимфобластного лейкоза – 18,3% (n=2), острого миелоидного лейкоза – 27,4% (n=3), миелодиспластического синдрома – 18,3% (n=2), бета-талассемии – 9% (n=1), хронического миелолейкоза – 9% (n=1), Лимфомы Ходжкина – 9% (n=1), анемии Фанкони – 9% (n=1). Для лечения посттрансплантационных осложнений всем пациентам была выполнена ТФМ. Медиана возраста составила 24 года (2-45). Из исследования исключено трое больных из-за нарушения техники ТФМ (n=2), развития тяжелого синдрома системного воспалительного ответа (n=1). Длительность диареи перед ТФМ составила от 1 до 6 мес. (медиана – 2,3) и наблюдалась у всех пациентов. У 5 (45,5%) больных регистрировали активное кишечное кровотечение с необходимостью ежедневных гемотрансфузий для коррекции анемического синдрома, еще у 4 (36,4%) больных в стуле определялись прожилки крови. В состоянии сепсиса было 5 пациентов (45,5%), а один пациент находился в состоянии септического шока (Klebsiella pneumoniае) и получал антибактериальную терапию, вазопрессоры, искусственную вентиляцию легких. Абдоминальный болевой синдром, требующий анальгезии наркотическими анальгетиками отмечали у 9 (81,8%) пациентов. Парез кишечника наблюдали у 5 (45,5%) больных. У 8 (72,7%) пациентов выявлен положительный клостридиальный токсин-В в стуле, повышенный уровень фекального кальпротектина до ТФМ у 7 (63,6%) пациентов 600 мкг/г (220-6706). Введение фекального трансплантата выполняли на Д+168 (27-1107). Донорами микробиоты были родственники пациентов и неродственные доноры, которые соответствовали требованиям инфекционной безопасности. До и после ТФМ в дни +3, +8, +16, +30, +45, +60, +75, +90 для определения основных групп кишечных микроорганизмов проведено исследование стула методом мультиплексной ПЦР («Колонофлор-16»). Трем пациентам до ТФМ выполнено 16S РНК секвенирование образцов стула.
Результаты
У 64% пациентов отмечен полный клинический ответ. Сокращение частоты и объема диареи в 2 раза наблюдали на Д+18 (1-39) и Д+14 (1-11) после ТФМ соответственно. Полный регресс патологических примесей в стуле (кровь, слизь) регистрировали на Д+13 (2-11), Д+30 (1- 97) и абдоминального болевого синдрома на Д+15 (5-31) соответственно. Клостридиальный токсин-В в образцах стула на Д+30 не определялся у 4 (50%) ранее положительных пациентов. Результаты мультиплексной ПЦР показали изменение микробиоты кишечника после ТФМ. Максимальное увеличение основных групп кишечных микроорганизмов регистрировали после ТФМ для общей бактериальной массы на Д+8 с 3E+08 (9,E+05/1E+11) до 1,65E+12 (7E+10/7E+12), для Lactobacillus spp. на Д+3 с 7E+05 (1E+04/2E+09) до 3E+08 (7E+05/3E+09), для Bifidobacterium spp. на Д+30 с 3E+06 (9E+04/3E+08) до 1E+08 (3E+06/6E+09), для Escherichia coli на Д+3 с 7E+05 (0,0E+00/7E+06) до 3E+07 (2E+06/3E+09), для Bacteroides fragilis group на Д+8 с 1,1E+07 (0,0E+00/4E+08) до 1,6E+12 (3E+06/7E+12), для Faecalibacterium prausnitzii на Д+3 с 3E+05 (0,0E+00/8E+07) до 3E+08 (1E+05/3E+09). 16S РНК-секвенирование образцов стула до ТФМ выявило выраженные нарушения микробиоты кишечника с преобладанием микроорганизмов следующих семейств: Streptococcaceae, Staphylococcaceae, Enterococcaceae.
Выводы
ТФМ имеет высокую клиническую эффективность и безопасность у пациентов после алло-ТГСК при развитии инфекции, ассоциированной с Clostridium difficile и РТПХ кишечника.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, трансплантация фекальной микробиоты, реакция трансплантат против хозяина.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20426" ["VALUE"]=> array(2) { ["TEXT"]=> string(707) "<sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия <sup>2</sup> ФГБУ Детский научно-клинический центр инфекционных болезней, Санкт-Петербург, Россия <sup>3</sup> Научно-исследовательская лаборатория Explana, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(671) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия 2 ФГБУ Детский научно-клинический центр инфекционных болезней, Санкт-Петербург, Россия 3 Научно-исследовательская лаборатория Explana, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(671) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия 2 ФГБУ Детский научно-клинический центр инфекционных болезней, Санкт-Петербург, Россия 3 Научно-исследовательская лаборатория Explana, Санкт-Петербург, Россия" } } } [3]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1565" ["~ID"]=> string(4) "1565" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(331) "Цитогенетическая эволюция при рецидивах острого лейкоза после аллогенной трансплантации гемопоэтических клеток: ассоциация с кондиционирующим режимом и влияние на выживаемость" ["~NAME"]=> string(331) "Цитогенетическая эволюция при рецидивах острого лейкоза после аллогенной трансплантации гемопоэтических клеток: ассоциация с кондиционирующим режимом и влияние на выживаемость" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:31:19" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:31:19" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/tsitogeneticheskaya-evolyutsiya-pri-retsidivakh-ostrogo-leykoza-posle-allogennoy-transplantatsii-gem/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/tsitogeneticheskaya-evolyutsiya-pri-retsidivakh-ostrogo-leykoza-posle-allogennoy-transplantatsii-gem/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "tsitogeneticheskaya-evolyutsiya-pri-retsidivakh-ostrogo-leykoza-posle-allogennoy-transplantatsii-gem" ["~CODE"]=> string(100) "tsitogeneticheskaya-evolyutsiya-pri-retsidivakh-ostrogo-leykoza-posle-allogennoy-transplantatsii-gem" ["EXTERNAL_ID"]=> string(4) "1565" ["~EXTERNAL_ID"]=> string(4) "1565" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(331) "Цитогенетическая эволюция при рецидивах острого лейкоза после аллогенной трансплантации гемопоэтических клеток: ассоциация с кондиционирующим режимом и влияние на выживаемость" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(495) "Цитогенетическая эволюция при рецидивах острого лейкоза после аллогенной трансплантации гемопоэтических клеток: ассоциация с кондиционирующим режимом и влияние на выживаемостьCytogenetic evolution in acute leukemia at relapse after allogeneic hematopoietic cell transplantation: association with regimen conditioning and effect on survival" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(6388) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Цель исследования – охарактеризовать цитогенетические изменения у больных с посттрансплантационными рецидивами (ПТР) острых лейкозов в рецидивах после алло-ТГСК, оценить влияние цитогенетической эволюции на их выживаемость и уточнить связь эволюции кариотипа с режимом кондиционирования. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В наше исследование вощли 73 пациента (35 женщин и 38 мужчин в возрасте 0,8-60 лет) с диагнозом острый миелоидный лейкоз (ОМЛ) или острый лимфобластный лейкоз (ОЛЛ), которым была проведена алло-ТГСК в нашем Универcитете в период с 2009 по 2016 год. Изменения кариотипа клеток костного мозга в посттрансплантационном рецидиве сравнивали с таковым, выявленным до алло-ТГСК. Медиана времени от трансплантации до рецидива составила 87 (диапазон, 18-1280) дней. Миелоаблативный режим кондиционирования и режим со сниженной интенсивностью доз применяли у 39 (53%) и 34 (47%) больных соответственно. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Изменения кариотипа в ПТР были отмечены у 29 больных ОМЛ (71%) и 23 больных ОЛЛ (72%). Цитогенетические изменения были разделены на следующие 5 групп: a) клоновую эволюцию кариотипа в ПТР (n=30); б) клоновую регрессию (n=1); в) клоновую эволюцию кариотипа в комбинации с регрессией (n=15); г) новый неродственный клон (n=5); и д) смену нормального кариотипа в ПТР аномальным (n=1). Два и более цитогенетических подклона были обнаружены у 6 (8%) пациентов до алло-ТГСК и у 24 (33%) больных в ПТР (p<0.0002). Были установлены 8 различных путей формирования родственных подклонов. Самыми частымм цитогенетическими изменениями в ПТР были появление 3 или более новых хромосомных аномалий, а также несбалансированных аномалий и анеуплоидии. У пациентов ОМЛ общие потери касались регионов 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, и 20q, тогда как приобретения – 1q, 11q 13q, 15q и 21q. У больных ОЛЛ часто удалялись регионы 1p, 8p, 11p, 11q, 17p, тогда как приобретения касались 1q, 8q, 18p, 18q, 21q и Xp. Миелоаблативное кондиционирование в группе больных с цитогенетической эволюцией в ПТР применяли чаще (p=0,01). В то же время цитогенетическая клоновая эволюция чаще всего встречалась (p=0,02) у больных с неблагоприятной предтрансплантационной группой, содержащих 3 и более сложных хромосомных аберраций на метафазу. Общая выживаемость после ТГСК и выживаемость после ПТР (ВПТР) были ниже в группе больных с изменениями кариотипа в ПТР (38% vs. 17%, p=0,03 and 41% vs. 6%, p=0,006, соответственно), также как в группе больных с 2 или более аномальными цитогенетическими клонами в ПТР (31%vs. 9%; р=0,04 только для ОВ). Появление нового неродственного клона было связано с уменьшением выживаемости после ПТР (17% vs. 0%, p=0,04). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Цитогенетическая эволюция в ПТР встречается чаще а) после применения миелоаблативного кондиционирования; б) при комплексном кариотипе перед трансплантацией; и в) сочетается с клональной гетерогенностью. Большинство общих цитогенетических аберраций в ПТР при ОМЛ и ОЛЛ различны. ОВ и выживаемость после посттрансплантационного рецидива ниже в группах пациентов с цитогенетической эволюцией (для ОВ и ВПТР), клональной гетерогенностью (для ОВ) и появлением нового неродственного клона (для ВПТР) в ПТР. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый лейкоз, посттрансплантационный рецидив, цитогенетическая эволюция, режим кондиционирования, исходы. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(331) "Цитогенетическая эволюция при рецидивах острого лейкоза после аллогенной трансплантации гемопоэтических клеток: ассоциация с кондиционирующим режимом и влияние на выживаемость" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(331) "Цитогенетическая эволюция при рецидивах острого лейкоза после аллогенной трансплантации гемопоэтических клеток: ассоциация с кондиционирующим режимом и влияние на выживаемость" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(331) "Цитогенетическая эволюция при рецидивах острого лейкоза после аллогенной трансплантации гемопоэтических клеток: ассоциация с кондиционирующим режимом и влияние на выживаемость" ["SECTION_META_TITLE"]=> string(331) "Цитогенетическая эволюция при рецидивах острого лейкоза после аллогенной трансплантации гемопоэтических клеток: ассоциация с кондиционирующим режимом и влияние на выживаемость" ["SECTION_META_KEYWORDS"]=> string(331) "Цитогенетическая эволюция при рецидивах острого лейкоза после аллогенной трансплантации гемопоэтических клеток: ассоциация с кондиционирующим режимом и влияние на выживаемость" ["SECTION_META_DESCRIPTION"]=> string(331) "Цитогенетическая эволюция при рецидивах острого лейкоза после аллогенной трансплантации гемопоэтических клеток: ассоциация с кондиционирующим режимом и влияние на выживаемость" ["SECTION_PICTURE_FILE_ALT"]=> string(331) "Цитогенетическая эволюция при рецидивах острого лейкоза после аллогенной трансплантации гемопоэтических клеток: ассоциация с кондиционирующим режимом и влияние на выживаемость" ["SECTION_PICTURE_FILE_TITLE"]=> string(331) "Цитогенетическая эволюция при рецидивах острого лейкоза после аллогенной трансплантации гемопоэтических клеток: ассоциация с кондиционирующим режимом и влияние на выживаемость" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "tsitogeneticheskaya-evolyutsiya-pri-retsidivakh-ostrogo-leykoza-posle-allogennoy-transplantatsii-gem" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(331) "Цитогенетическая эволюция при рецидивах острого лейкоза после аллогенной трансплантации гемопоэтических клеток: ассоциация с кондиционирующим режимом и влияние на выживаемость" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(331) "Цитогенетическая эволюция при рецидивах острого лейкоза после аллогенной трансплантации гемопоэтических клеток: ассоциация с кондиционирующим режимом и влияние на выживаемость" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "tsitogeneticheskaya-evolyutsiya-pri-retsidivakh-ostrogo-leykoza-posle-allogennoy-transplantatsii-gem" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "tsitogeneticheskaya-evolyutsiya-pri-retsidivakh-ostrogo-leykoza-posle-allogennoy-transplantatsii-gem" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "tsitogeneticheskaya-evolyutsiya-pri-retsidivakh-ostrogo-leykoza-posle-allogennoy-transplantatsii-gem" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20416" ["VALUE"]=> array(2) { ["TEXT"]=> string(396) "Татьяна Л. Гиндина, Николай Н. Мамаев, Елена С. Рябикова, Мария В. Латыпова, Ирина А. Петрова, Диана С. Ильясова, Мария В. Власова, Олеся В. Паина, Елена В. Семенова, Елена И. Дарская, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(396) "Татьяна Л. Гиндина, Николай Н. Мамаев, Елена С. Рябикова, Мария В. Латыпова, Ирина А. Петрова, Диана С. Ильясова, Мария В. Власова, Олеся В. Паина, Елена В. Семенова, Елена И. Дарская, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20417" ["VALUE"]=> array(2) { ["TEXT"]=> string(389) "НИИ детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(389) "НИИ детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20418" ["VALUE"]=> array(2) { ["TEXT"]=> string(6388) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Цель исследования – охарактеризовать цитогенетические изменения у больных с посттрансплантационными рецидивами (ПТР) острых лейкозов в рецидивах после алло-ТГСК, оценить влияние цитогенетической эволюции на их выживаемость и уточнить связь эволюции кариотипа с режимом кондиционирования. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В наше исследование вощли 73 пациента (35 женщин и 38 мужчин в возрасте 0,8-60 лет) с диагнозом острый миелоидный лейкоз (ОМЛ) или острый лимфобластный лейкоз (ОЛЛ), которым была проведена алло-ТГСК в нашем Универcитете в период с 2009 по 2016 год. Изменения кариотипа клеток костного мозга в посттрансплантационном рецидиве сравнивали с таковым, выявленным до алло-ТГСК. Медиана времени от трансплантации до рецидива составила 87 (диапазон, 18-1280) дней. Миелоаблативный режим кондиционирования и режим со сниженной интенсивностью доз применяли у 39 (53%) и 34 (47%) больных соответственно. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Изменения кариотипа в ПТР были отмечены у 29 больных ОМЛ (71%) и 23 больных ОЛЛ (72%). Цитогенетические изменения были разделены на следующие 5 групп: a) клоновую эволюцию кариотипа в ПТР (n=30); б) клоновую регрессию (n=1); в) клоновую эволюцию кариотипа в комбинации с регрессией (n=15); г) новый неродственный клон (n=5); и д) смену нормального кариотипа в ПТР аномальным (n=1). Два и более цитогенетических подклона были обнаружены у 6 (8%) пациентов до алло-ТГСК и у 24 (33%) больных в ПТР (p<0.0002). Были установлены 8 различных путей формирования родственных подклонов. Самыми частымм цитогенетическими изменениями в ПТР были появление 3 или более новых хромосомных аномалий, а также несбалансированных аномалий и анеуплоидии. У пациентов ОМЛ общие потери касались регионов 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, и 20q, тогда как приобретения – 1q, 11q 13q, 15q и 21q. У больных ОЛЛ часто удалялись регионы 1p, 8p, 11p, 11q, 17p, тогда как приобретения касались 1q, 8q, 18p, 18q, 21q и Xp. Миелоаблативное кондиционирование в группе больных с цитогенетической эволюцией в ПТР применяли чаще (p=0,01). В то же время цитогенетическая клоновая эволюция чаще всего встречалась (p=0,02) у больных с неблагоприятной предтрансплантационной группой, содержащих 3 и более сложных хромосомных аберраций на метафазу. Общая выживаемость после ТГСК и выживаемость после ПТР (ВПТР) были ниже в группе больных с изменениями кариотипа в ПТР (38% vs. 17%, p=0,03 and 41% vs. 6%, p=0,006, соответственно), также как в группе больных с 2 или более аномальными цитогенетическими клонами в ПТР (31%vs. 9%; р=0,04 только для ОВ). Появление нового неродственного клона было связано с уменьшением выживаемости после ПТР (17% vs. 0%, p=0,04). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Цитогенетическая эволюция в ПТР встречается чаще а) после применения миелоаблативного кондиционирования; б) при комплексном кариотипе перед трансплантацией; и в) сочетается с клональной гетерогенностью. Большинство общих цитогенетических аберраций в ПТР при ОМЛ и ОЛЛ различны. ОВ и выживаемость после посттрансплантационного рецидива ниже в группах пациентов с цитогенетической эволюцией (для ОВ и ВПТР), клональной гетерогенностью (для ОВ) и появлением нового неродственного клона (для ВПТР) в ПТР. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый лейкоз, посттрансплантационный рецидив, цитогенетическая эволюция, режим кондиционирования, исходы. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6164) "Введение
Цель исследования – охарактеризовать цитогенетические изменения у больных с посттрансплантационными рецидивами (ПТР) острых лейкозов в рецидивах после алло-ТГСК, оценить влияние цитогенетической эволюции на их выживаемость и уточнить связь эволюции кариотипа с режимом кондиционирования.
Материалы и методы
В наше исследование вощли 73 пациента (35 женщин и 38 мужчин в возрасте 0,8-60 лет) с диагнозом острый миелоидный лейкоз (ОМЛ) или острый лимфобластный лейкоз (ОЛЛ), которым была проведена алло-ТГСК в нашем Универcитете в период с 2009 по 2016 год. Изменения кариотипа клеток костного мозга в посттрансплантационном рецидиве сравнивали с таковым, выявленным до алло-ТГСК. Медиана времени от трансплантации до рецидива составила 87 (диапазон, 18-1280) дней. Миелоаблативный режим кондиционирования и режим со сниженной интенсивностью доз применяли у 39 (53%) и 34 (47%) больных соответственно.
Результаты
Изменения кариотипа в ПТР были отмечены у 29 больных ОМЛ (71%) и 23 больных ОЛЛ (72%). Цитогенетические изменения были разделены на следующие 5 групп: a) клоновую эволюцию кариотипа в ПТР (n=30); б) клоновую регрессию (n=1); в) клоновую эволюцию кариотипа в комбинации с регрессией (n=15); г) новый неродственный клон (n=5); и д) смену нормального кариотипа в ПТР аномальным (n=1). Два и более цитогенетических подклона были обнаружены у 6 (8%) пациентов до алло-ТГСК и у 24 (33%) больных в ПТР (p<0.0002). Были установлены 8 различных путей формирования родственных подклонов. Самыми частымм цитогенетическими изменениями в ПТР были появление 3 или более новых хромосомных аномалий, а также несбалансированных аномалий и анеуплоидии. У пациентов ОМЛ общие потери касались регионов 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, и 20q, тогда как приобретения – 1q, 11q 13q, 15q и 21q. У больных ОЛЛ часто удалялись регионы 1p, 8p, 11p, 11q, 17p, тогда как приобретения касались 1q, 8q, 18p, 18q, 21q и Xp. Миелоаблативное кондиционирование в группе больных с цитогенетической эволюцией в ПТР применяли чаще (p=0,01). В то же время цитогенетическая клоновая эволюция чаще всего встречалась (p=0,02) у больных с неблагоприятной предтрансплантационной группой, содержащих 3 и более сложных хромосомных аберраций на метафазу. Общая выживаемость после ТГСК и выживаемость после ПТР (ВПТР) были ниже в группе больных с изменениями кариотипа в ПТР (38% vs. 17%, p=0,03 and 41% vs. 6%, p=0,006, соответственно), также как в группе больных с 2 или более аномальными цитогенетическими клонами в ПТР (31%vs. 9%; р=0,04 только для ОВ). Появление нового неродственного клона было связано с уменьшением выживаемости после ПТР (17% vs. 0%, p=0,04).
Заключение
Цитогенетическая эволюция в ПТР встречается чаще а) после применения миелоаблативного кондиционирования; б) при комплексном кариотипе перед трансплантацией; и в) сочетается с клональной гетерогенностью. Большинство общих цитогенетических аберраций в ПТР при ОМЛ и ОЛЛ различны. ОВ и выживаемость после посттрансплантационного рецидива ниже в группах пациентов с цитогенетической эволюцией (для ОВ и ВПТР), клональной гетерогенностью (для ОВ) и появлением нового неродственного клона (для ВПТР) в ПТР.
Ключевые слова
Острый лейкоз, посттрансплантационный рецидив, цитогенетическая эволюция, режим кондиционирования, исходы.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20419" ["VALUE"]=> array(2) { ["TEXT"]=> string(241) "Tatiana L. Gindina, Nikolay N. Mamaev, Elena S. Ryabikova, Maria V. Latypova, Irina A. Petrova, Diana S. Ilyasova, Maria E. Vlasova, Olesya V. Paina, Elena V. Semenova, Elena I. Darskaya, Ludmila S. Zubarovskaya, Boris V. Afanasyev<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(235) "Tatiana L. Gindina, Nikolay N. Mamaev, Elena S. Ryabikova, Maria V. Latypova, Irina A. Petrova, Diana S. Ilyasova, Maria E. Vlasova, Olesya V. Paina, Elena V. Semenova, Elena I. Darskaya, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20420" ["VALUE"]=> array(2) { ["TEXT"]=> string(190) "Raisa Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(184) "Raisa Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20421" ["VALUE"]=> array(2) { ["TEXT"]=> string(3456) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> The aim of this study was to characterize patterns of cytogenetic changes in patients with acute leukemia who relapsed after allo-HSCT, to assess the effect of сytogenetic evolution upon survival; and to elucidate associations of cytogenetic evolution with conditioning regimen. </p> <h2>Materials and methods</h2> <p style="text-align: justify;"> Our study included seventy-three patients (35 females and 38 males, at the age of 0.8 to 60 years) diagnosed with acute myeloblastic leukemia (AML) or acute lymphoblastic leukemia (ALL) who underwent allo-HSCT at our University from 2009 to 2016. The bone marrow karyotypic changes in posttransplant relapse (PTR) were compared with those observed before allo-HSCT. Median time from transplant to relapse was 87 days (range, 18 to 1280). Myeloablative conditioning and reduced intensity conditioning was performed in 39 (53%) and 34 (47%) patients, respectively. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Karyotypic changes at PTR were noted in 29 AML patients (71%) and 23 ALL patients (72%). The cytogenetic changes were divided into five following groups: a) clonal evolution of karyotype at PTR (n=30); b) clonal regression (n=1); c) new unrelated clones (n=5); d) clonal evolution of karyotype, combined with clonal regression (n=15); and e) changing of normal karyotype into abnormal at PTR (n=1). Moreover, two or more cytogenetic subclones were detected in 6 (8%) patients before allo-HSCT and in 24 (33%) patients at PTR (p<0.0002). Eight different ways of subclone formation has been identified. Acquisition of 3 or more new chromosomal abnormalities was the most frequent cytogenetic change, followed by acquisition of both unbalanced abnormalities and aneuploidy. The common losses in AML patients were 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, and 20q, whereas gains concerned 1q, 11q 13q, 15q, and 21q. The common losses in ALL patients were 1p, 8p, 11p, 11q, 17p, whereas the gains concerned 1q, 8q, 18p, 18q, 21q, and Xp. In the group with cytogenetic evolution at PTR, myeloablative conditioning was used more often (p=0.01). Cytogenetic clonal evolution frequently occurred in an unfavorable pre-transplant group with complex chromosome aberrations (3 and more per metaphase) (p=0.02). Overall survival after HSCT and survival after PTR were shortened in the group of patients with karyotype changes in PTR (38% vs. 17%, p=0.03 and 41% vs. 6%, p=0.006, respectively) as well as in the group of patients with two or more abnormal cytogenetic clones in PTR (31% vs. 9%; р=0.04 only for OS). The emergence of a new unrelated clone was associated with decreasing of survival after PTR (17% vs. 0%, p=0.04). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> We have revealed evidence for a significant impact of cytogenetic evolution to clinical progression in acute leukemia treated with allo-HSCT. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Acute leukemia, posttransplant relapse, cytogenetic evolution, conditioning regimen, outcomes. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3242) "
Introduction
The aim of this study was to characterize patterns of cytogenetic changes in patients with acute leukemia who relapsed after allo-HSCT, to assess the effect of сytogenetic evolution upon survival; and to elucidate associations of cytogenetic evolution with conditioning regimen.
Materials and methods
Our study included seventy-three patients (35 females and 38 males, at the age of 0.8 to 60 years) diagnosed with acute myeloblastic leukemia (AML) or acute lymphoblastic leukemia (ALL) who underwent allo-HSCT at our University from 2009 to 2016. The bone marrow karyotypic changes in posttransplant relapse (PTR) were compared with those observed before allo-HSCT. Median time from transplant to relapse was 87 days (range, 18 to 1280). Myeloablative conditioning and reduced intensity conditioning was performed in 39 (53%) and 34 (47%) patients, respectively.
Results
Karyotypic changes at PTR were noted in 29 AML patients (71%) and 23 ALL patients (72%). The cytogenetic changes were divided into five following groups: a) clonal evolution of karyotype at PTR (n=30); b) clonal regression (n=1); c) new unrelated clones (n=5); d) clonal evolution of karyotype, combined with clonal regression (n=15); and e) changing of normal karyotype into abnormal at PTR (n=1). Moreover, two or more cytogenetic subclones were detected in 6 (8%) patients before allo-HSCT and in 24 (33%) patients at PTR (p<0.0002). Eight different ways of subclone formation has been identified. Acquisition of 3 or more new chromosomal abnormalities was the most frequent cytogenetic change, followed by acquisition of both unbalanced abnormalities and aneuploidy. The common losses in AML patients were 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, and 20q, whereas gains concerned 1q, 11q 13q, 15q, and 21q. The common losses in ALL patients were 1p, 8p, 11p, 11q, 17p, whereas the gains concerned 1q, 8q, 18p, 18q, 21q, and Xp. In the group with cytogenetic evolution at PTR, myeloablative conditioning was used more often (p=0.01). Cytogenetic clonal evolution frequently occurred in an unfavorable pre-transplant group with complex chromosome aberrations (3 and more per metaphase) (p=0.02). Overall survival after HSCT and survival after PTR were shortened in the group of patients with karyotype changes in PTR (38% vs. 17%, p=0.03 and 41% vs. 6%, p=0.006, respectively) as well as in the group of patients with two or more abnormal cytogenetic clones in PTR (31% vs. 9%; р=0.04 only for OS). The emergence of a new unrelated clone was associated with decreasing of survival after PTR (17% vs. 0%, p=0.04).
Conclusion
We have revealed evidence for a significant impact of cytogenetic evolution to clinical progression in acute leukemia treated with allo-HSCT.
Keywords
Acute leukemia, posttransplant relapse, cytogenetic evolution, conditioning regimen, outcomes.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20422" ["VALUE"]=> string(164) "Cytogenetic evolution in acute leukemia at relapse after allogeneic hematopoietic cell transplantation: association with regimen conditioning and effect on survival" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(164) "Cytogenetic evolution in acute leukemia at relapse after allogeneic hematopoietic cell transplantation: association with regimen conditioning and effect on survival" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20763" ["VALUE"]=> string(4) "1399" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1399" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20764" ["VALUE"]=> string(4) "1400" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1400" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20419" ["VALUE"]=> array(2) { ["TEXT"]=> string(241) "Tatiana L. Gindina, Nikolay N. Mamaev, Elena S. Ryabikova, Maria V. Latypova, Irina A. Petrova, Diana S. Ilyasova, Maria E. Vlasova, Olesya V. Paina, Elena V. Semenova, Elena I. Darskaya, Ludmila S. Zubarovskaya, Boris V. Afanasyev<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(235) "Tatiana L. Gindina, Nikolay N. Mamaev, Elena S. Ryabikova, Maria V. Latypova, Irina A. Petrova, Diana S. Ilyasova, Maria E. Vlasova, Olesya V. Paina, Elena V. Semenova, Elena I. Darskaya, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(235) "Tatiana L. Gindina, Nikolay N. Mamaev, Elena S. Ryabikova, Maria V. Latypova, Irina A. Petrova, Diana S. Ilyasova, Maria E. Vlasova, Olesya V. Paina, Elena V. Semenova, Elena I. Darskaya, Ludmila S. Zubarovskaya, Boris V. Afanasyev
" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20421" ["VALUE"]=> array(2) { ["TEXT"]=> string(3456) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> The aim of this study was to characterize patterns of cytogenetic changes in patients with acute leukemia who relapsed after allo-HSCT, to assess the effect of сytogenetic evolution upon survival; and to elucidate associations of cytogenetic evolution with conditioning regimen. </p> <h2>Materials and methods</h2> <p style="text-align: justify;"> Our study included seventy-three patients (35 females and 38 males, at the age of 0.8 to 60 years) diagnosed with acute myeloblastic leukemia (AML) or acute lymphoblastic leukemia (ALL) who underwent allo-HSCT at our University from 2009 to 2016. The bone marrow karyotypic changes in posttransplant relapse (PTR) were compared with those observed before allo-HSCT. Median time from transplant to relapse was 87 days (range, 18 to 1280). Myeloablative conditioning and reduced intensity conditioning was performed in 39 (53%) and 34 (47%) patients, respectively. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Karyotypic changes at PTR were noted in 29 AML patients (71%) and 23 ALL patients (72%). The cytogenetic changes were divided into five following groups: a) clonal evolution of karyotype at PTR (n=30); b) clonal regression (n=1); c) new unrelated clones (n=5); d) clonal evolution of karyotype, combined with clonal regression (n=15); and e) changing of normal karyotype into abnormal at PTR (n=1). Moreover, two or more cytogenetic subclones were detected in 6 (8%) patients before allo-HSCT and in 24 (33%) patients at PTR (p<0.0002). Eight different ways of subclone formation has been identified. Acquisition of 3 or more new chromosomal abnormalities was the most frequent cytogenetic change, followed by acquisition of both unbalanced abnormalities and aneuploidy. The common losses in AML patients were 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, and 20q, whereas gains concerned 1q, 11q 13q, 15q, and 21q. The common losses in ALL patients were 1p, 8p, 11p, 11q, 17p, whereas the gains concerned 1q, 8q, 18p, 18q, 21q, and Xp. In the group with cytogenetic evolution at PTR, myeloablative conditioning was used more often (p=0.01). Cytogenetic clonal evolution frequently occurred in an unfavorable pre-transplant group with complex chromosome aberrations (3 and more per metaphase) (p=0.02). Overall survival after HSCT and survival after PTR were shortened in the group of patients with karyotype changes in PTR (38% vs. 17%, p=0.03 and 41% vs. 6%, p=0.006, respectively) as well as in the group of patients with two or more abnormal cytogenetic clones in PTR (31% vs. 9%; р=0.04 only for OS). The emergence of a new unrelated clone was associated with decreasing of survival after PTR (17% vs. 0%, p=0.04). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> We have revealed evidence for a significant impact of cytogenetic evolution to clinical progression in acute leukemia treated with allo-HSCT. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Acute leukemia, posttransplant relapse, cytogenetic evolution, conditioning regimen, outcomes. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3242) "
Introduction
The aim of this study was to characterize patterns of cytogenetic changes in patients with acute leukemia who relapsed after allo-HSCT, to assess the effect of сytogenetic evolution upon survival; and to elucidate associations of cytogenetic evolution with conditioning regimen.
Materials and methods
Our study included seventy-three patients (35 females and 38 males, at the age of 0.8 to 60 years) diagnosed with acute myeloblastic leukemia (AML) or acute lymphoblastic leukemia (ALL) who underwent allo-HSCT at our University from 2009 to 2016. The bone marrow karyotypic changes in posttransplant relapse (PTR) were compared with those observed before allo-HSCT. Median time from transplant to relapse was 87 days (range, 18 to 1280). Myeloablative conditioning and reduced intensity conditioning was performed in 39 (53%) and 34 (47%) patients, respectively.
Results
Karyotypic changes at PTR were noted in 29 AML patients (71%) and 23 ALL patients (72%). The cytogenetic changes were divided into five following groups: a) clonal evolution of karyotype at PTR (n=30); b) clonal regression (n=1); c) new unrelated clones (n=5); d) clonal evolution of karyotype, combined with clonal regression (n=15); and e) changing of normal karyotype into abnormal at PTR (n=1). Moreover, two or more cytogenetic subclones were detected in 6 (8%) patients before allo-HSCT and in 24 (33%) patients at PTR (p<0.0002). Eight different ways of subclone formation has been identified. Acquisition of 3 or more new chromosomal abnormalities was the most frequent cytogenetic change, followed by acquisition of both unbalanced abnormalities and aneuploidy. The common losses in AML patients were 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, and 20q, whereas gains concerned 1q, 11q 13q, 15q, and 21q. The common losses in ALL patients were 1p, 8p, 11p, 11q, 17p, whereas the gains concerned 1q, 8q, 18p, 18q, 21q, and Xp. In the group with cytogenetic evolution at PTR, myeloablative conditioning was used more often (p=0.01). Cytogenetic clonal evolution frequently occurred in an unfavorable pre-transplant group with complex chromosome aberrations (3 and more per metaphase) (p=0.02). Overall survival after HSCT and survival after PTR were shortened in the group of patients with karyotype changes in PTR (38% vs. 17%, p=0.03 and 41% vs. 6%, p=0.006, respectively) as well as in the group of patients with two or more abnormal cytogenetic clones in PTR (31% vs. 9%; р=0.04 only for OS). The emergence of a new unrelated clone was associated with decreasing of survival after PTR (17% vs. 0%, p=0.04).
Conclusion
We have revealed evidence for a significant impact of cytogenetic evolution to clinical progression in acute leukemia treated with allo-HSCT.
Keywords
Acute leukemia, posttransplant relapse, cytogenetic evolution, conditioning regimen, outcomes.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3242) "Introduction
The aim of this study was to characterize patterns of cytogenetic changes in patients with acute leukemia who relapsed after allo-HSCT, to assess the effect of сytogenetic evolution upon survival; and to elucidate associations of cytogenetic evolution with conditioning regimen.
Materials and methods
Our study included seventy-three patients (35 females and 38 males, at the age of 0.8 to 60 years) diagnosed with acute myeloblastic leukemia (AML) or acute lymphoblastic leukemia (ALL) who underwent allo-HSCT at our University from 2009 to 2016. The bone marrow karyotypic changes in posttransplant relapse (PTR) were compared with those observed before allo-HSCT. Median time from transplant to relapse was 87 days (range, 18 to 1280). Myeloablative conditioning and reduced intensity conditioning was performed in 39 (53%) and 34 (47%) patients, respectively.
Results
Karyotypic changes at PTR were noted in 29 AML patients (71%) and 23 ALL patients (72%). The cytogenetic changes were divided into five following groups: a) clonal evolution of karyotype at PTR (n=30); b) clonal regression (n=1); c) new unrelated clones (n=5); d) clonal evolution of karyotype, combined with clonal regression (n=15); and e) changing of normal karyotype into abnormal at PTR (n=1). Moreover, two or more cytogenetic subclones were detected in 6 (8%) patients before allo-HSCT and in 24 (33%) patients at PTR (p<0.0002). Eight different ways of subclone formation has been identified. Acquisition of 3 or more new chromosomal abnormalities was the most frequent cytogenetic change, followed by acquisition of both unbalanced abnormalities and aneuploidy. The common losses in AML patients were 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, and 20q, whereas gains concerned 1q, 11q 13q, 15q, and 21q. The common losses in ALL patients were 1p, 8p, 11p, 11q, 17p, whereas the gains concerned 1q, 8q, 18p, 18q, 21q, and Xp. In the group with cytogenetic evolution at PTR, myeloablative conditioning was used more often (p=0.01). Cytogenetic clonal evolution frequently occurred in an unfavorable pre-transplant group with complex chromosome aberrations (3 and more per metaphase) (p=0.02). Overall survival after HSCT and survival after PTR were shortened in the group of patients with karyotype changes in PTR (38% vs. 17%, p=0.03 and 41% vs. 6%, p=0.006, respectively) as well as in the group of patients with two or more abnormal cytogenetic clones in PTR (31% vs. 9%; р=0.04 only for OS). The emergence of a new unrelated clone was associated with decreasing of survival after PTR (17% vs. 0%, p=0.04).
Conclusion
We have revealed evidence for a significant impact of cytogenetic evolution to clinical progression in acute leukemia treated with allo-HSCT.
Keywords
Acute leukemia, posttransplant relapse, cytogenetic evolution, conditioning regimen, outcomes.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20422" ["VALUE"]=> string(164) "Cytogenetic evolution in acute leukemia at relapse after allogeneic hematopoietic cell transplantation: association with regimen conditioning and effect on survival" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(164) "Cytogenetic evolution in acute leukemia at relapse after allogeneic hematopoietic cell transplantation: association with regimen conditioning and effect on survival" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(164) "Cytogenetic evolution in acute leukemia at relapse after allogeneic hematopoietic cell transplantation: association with regimen conditioning and effect on survival" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20420" ["VALUE"]=> array(2) { ["TEXT"]=> string(190) "Raisa Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(184) "Raisa Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(184) "Raisa Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20416" ["VALUE"]=> array(2) { ["TEXT"]=> string(396) "Татьяна Л. Гиндина, Николай Н. Мамаев, Елена С. Рябикова, Мария В. Латыпова, Ирина А. Петрова, Диана С. Ильясова, Мария В. Власова, Олеся В. Паина, Елена В. Семенова, Елена И. Дарская, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(396) "Татьяна Л. Гиндина, Николай Н. Мамаев, Елена С. Рябикова, Мария В. Латыпова, Ирина А. Петрова, Диана С. Ильясова, Мария В. Власова, Олеся В. Паина, Елена В. Семенова, Елена И. Дарская, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(396) "Татьяна Л. Гиндина, Николай Н. Мамаев, Елена С. Рябикова, Мария В. Латыпова, Ирина А. Петрова, Диана С. Ильясова, Мария В. Власова, Олеся В. Паина, Елена В. Семенова, Елена И. Дарская, Людмила С. Зубаровская, Борис В. Афанасьев" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20418" ["VALUE"]=> array(2) { ["TEXT"]=> string(6388) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Цель исследования – охарактеризовать цитогенетические изменения у больных с посттрансплантационными рецидивами (ПТР) острых лейкозов в рецидивах после алло-ТГСК, оценить влияние цитогенетической эволюции на их выживаемость и уточнить связь эволюции кариотипа с режимом кондиционирования. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В наше исследование вощли 73 пациента (35 женщин и 38 мужчин в возрасте 0,8-60 лет) с диагнозом острый миелоидный лейкоз (ОМЛ) или острый лимфобластный лейкоз (ОЛЛ), которым была проведена алло-ТГСК в нашем Универcитете в период с 2009 по 2016 год. Изменения кариотипа клеток костного мозга в посттрансплантационном рецидиве сравнивали с таковым, выявленным до алло-ТГСК. Медиана времени от трансплантации до рецидива составила 87 (диапазон, 18-1280) дней. Миелоаблативный режим кондиционирования и режим со сниженной интенсивностью доз применяли у 39 (53%) и 34 (47%) больных соответственно. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Изменения кариотипа в ПТР были отмечены у 29 больных ОМЛ (71%) и 23 больных ОЛЛ (72%). Цитогенетические изменения были разделены на следующие 5 групп: a) клоновую эволюцию кариотипа в ПТР (n=30); б) клоновую регрессию (n=1); в) клоновую эволюцию кариотипа в комбинации с регрессией (n=15); г) новый неродственный клон (n=5); и д) смену нормального кариотипа в ПТР аномальным (n=1). Два и более цитогенетических подклона были обнаружены у 6 (8%) пациентов до алло-ТГСК и у 24 (33%) больных в ПТР (p<0.0002). Были установлены 8 различных путей формирования родственных подклонов. Самыми частымм цитогенетическими изменениями в ПТР были появление 3 или более новых хромосомных аномалий, а также несбалансированных аномалий и анеуплоидии. У пациентов ОМЛ общие потери касались регионов 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, и 20q, тогда как приобретения – 1q, 11q 13q, 15q и 21q. У больных ОЛЛ часто удалялись регионы 1p, 8p, 11p, 11q, 17p, тогда как приобретения касались 1q, 8q, 18p, 18q, 21q и Xp. Миелоаблативное кондиционирование в группе больных с цитогенетической эволюцией в ПТР применяли чаще (p=0,01). В то же время цитогенетическая клоновая эволюция чаще всего встречалась (p=0,02) у больных с неблагоприятной предтрансплантационной группой, содержащих 3 и более сложных хромосомных аберраций на метафазу. Общая выживаемость после ТГСК и выживаемость после ПТР (ВПТР) были ниже в группе больных с изменениями кариотипа в ПТР (38% vs. 17%, p=0,03 and 41% vs. 6%, p=0,006, соответственно), также как в группе больных с 2 или более аномальными цитогенетическими клонами в ПТР (31%vs. 9%; р=0,04 только для ОВ). Появление нового неродственного клона было связано с уменьшением выживаемости после ПТР (17% vs. 0%, p=0,04). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Цитогенетическая эволюция в ПТР встречается чаще а) после применения миелоаблативного кондиционирования; б) при комплексном кариотипе перед трансплантацией; и в) сочетается с клональной гетерогенностью. Большинство общих цитогенетических аберраций в ПТР при ОМЛ и ОЛЛ различны. ОВ и выживаемость после посттрансплантационного рецидива ниже в группах пациентов с цитогенетической эволюцией (для ОВ и ВПТР), клональной гетерогенностью (для ОВ) и появлением нового неродственного клона (для ВПТР) в ПТР. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый лейкоз, посттрансплантационный рецидив, цитогенетическая эволюция, режим кондиционирования, исходы. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6164) "
Введение
Цель исследования – охарактеризовать цитогенетические изменения у больных с посттрансплантационными рецидивами (ПТР) острых лейкозов в рецидивах после алло-ТГСК, оценить влияние цитогенетической эволюции на их выживаемость и уточнить связь эволюции кариотипа с режимом кондиционирования.
Материалы и методы
В наше исследование вощли 73 пациента (35 женщин и 38 мужчин в возрасте 0,8-60 лет) с диагнозом острый миелоидный лейкоз (ОМЛ) или острый лимфобластный лейкоз (ОЛЛ), которым была проведена алло-ТГСК в нашем Универcитете в период с 2009 по 2016 год. Изменения кариотипа клеток костного мозга в посттрансплантационном рецидиве сравнивали с таковым, выявленным до алло-ТГСК. Медиана времени от трансплантации до рецидива составила 87 (диапазон, 18-1280) дней. Миелоаблативный режим кондиционирования и режим со сниженной интенсивностью доз применяли у 39 (53%) и 34 (47%) больных соответственно.
Результаты
Изменения кариотипа в ПТР были отмечены у 29 больных ОМЛ (71%) и 23 больных ОЛЛ (72%). Цитогенетические изменения были разделены на следующие 5 групп: a) клоновую эволюцию кариотипа в ПТР (n=30); б) клоновую регрессию (n=1); в) клоновую эволюцию кариотипа в комбинации с регрессией (n=15); г) новый неродственный клон (n=5); и д) смену нормального кариотипа в ПТР аномальным (n=1). Два и более цитогенетических подклона были обнаружены у 6 (8%) пациентов до алло-ТГСК и у 24 (33%) больных в ПТР (p<0.0002). Были установлены 8 различных путей формирования родственных подклонов. Самыми частымм цитогенетическими изменениями в ПТР были появление 3 или более новых хромосомных аномалий, а также несбалансированных аномалий и анеуплоидии. У пациентов ОМЛ общие потери касались регионов 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, и 20q, тогда как приобретения – 1q, 11q 13q, 15q и 21q. У больных ОЛЛ часто удалялись регионы 1p, 8p, 11p, 11q, 17p, тогда как приобретения касались 1q, 8q, 18p, 18q, 21q и Xp. Миелоаблативное кондиционирование в группе больных с цитогенетической эволюцией в ПТР применяли чаще (p=0,01). В то же время цитогенетическая клоновая эволюция чаще всего встречалась (p=0,02) у больных с неблагоприятной предтрансплантационной группой, содержащих 3 и более сложных хромосомных аберраций на метафазу. Общая выживаемость после ТГСК и выживаемость после ПТР (ВПТР) были ниже в группе больных с изменениями кариотипа в ПТР (38% vs. 17%, p=0,03 and 41% vs. 6%, p=0,006, соответственно), также как в группе больных с 2 или более аномальными цитогенетическими клонами в ПТР (31%vs. 9%; р=0,04 только для ОВ). Появление нового неродственного клона было связано с уменьшением выживаемости после ПТР (17% vs. 0%, p=0,04).
Заключение
Цитогенетическая эволюция в ПТР встречается чаще а) после применения миелоаблативного кондиционирования; б) при комплексном кариотипе перед трансплантацией; и в) сочетается с клональной гетерогенностью. Большинство общих цитогенетических аберраций в ПТР при ОМЛ и ОЛЛ различны. ОВ и выживаемость после посттрансплантационного рецидива ниже в группах пациентов с цитогенетической эволюцией (для ОВ и ВПТР), клональной гетерогенностью (для ОВ) и появлением нового неродственного клона (для ВПТР) в ПТР.
Ключевые слова
Острый лейкоз, посттрансплантационный рецидив, цитогенетическая эволюция, режим кондиционирования, исходы.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6164) "Введение
Цель исследования – охарактеризовать цитогенетические изменения у больных с посттрансплантационными рецидивами (ПТР) острых лейкозов в рецидивах после алло-ТГСК, оценить влияние цитогенетической эволюции на их выживаемость и уточнить связь эволюции кариотипа с режимом кондиционирования.
Материалы и методы
В наше исследование вощли 73 пациента (35 женщин и 38 мужчин в возрасте 0,8-60 лет) с диагнозом острый миелоидный лейкоз (ОМЛ) или острый лимфобластный лейкоз (ОЛЛ), которым была проведена алло-ТГСК в нашем Универcитете в период с 2009 по 2016 год. Изменения кариотипа клеток костного мозга в посттрансплантационном рецидиве сравнивали с таковым, выявленным до алло-ТГСК. Медиана времени от трансплантации до рецидива составила 87 (диапазон, 18-1280) дней. Миелоаблативный режим кондиционирования и режим со сниженной интенсивностью доз применяли у 39 (53%) и 34 (47%) больных соответственно.
Результаты
Изменения кариотипа в ПТР были отмечены у 29 больных ОМЛ (71%) и 23 больных ОЛЛ (72%). Цитогенетические изменения были разделены на следующие 5 групп: a) клоновую эволюцию кариотипа в ПТР (n=30); б) клоновую регрессию (n=1); в) клоновую эволюцию кариотипа в комбинации с регрессией (n=15); г) новый неродственный клон (n=5); и д) смену нормального кариотипа в ПТР аномальным (n=1). Два и более цитогенетических подклона были обнаружены у 6 (8%) пациентов до алло-ТГСК и у 24 (33%) больных в ПТР (p<0.0002). Были установлены 8 различных путей формирования родственных подклонов. Самыми частымм цитогенетическими изменениями в ПТР были появление 3 или более новых хромосомных аномалий, а также несбалансированных аномалий и анеуплоидии. У пациентов ОМЛ общие потери касались регионов 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, и 20q, тогда как приобретения – 1q, 11q 13q, 15q и 21q. У больных ОЛЛ часто удалялись регионы 1p, 8p, 11p, 11q, 17p, тогда как приобретения касались 1q, 8q, 18p, 18q, 21q и Xp. Миелоаблативное кондиционирование в группе больных с цитогенетической эволюцией в ПТР применяли чаще (p=0,01). В то же время цитогенетическая клоновая эволюция чаще всего встречалась (p=0,02) у больных с неблагоприятной предтрансплантационной группой, содержащих 3 и более сложных хромосомных аберраций на метафазу. Общая выживаемость после ТГСК и выживаемость после ПТР (ВПТР) были ниже в группе больных с изменениями кариотипа в ПТР (38% vs. 17%, p=0,03 and 41% vs. 6%, p=0,006, соответственно), также как в группе больных с 2 или более аномальными цитогенетическими клонами в ПТР (31%vs. 9%; р=0,04 только для ОВ). Появление нового неродственного клона было связано с уменьшением выживаемости после ПТР (17% vs. 0%, p=0,04).
Заключение
Цитогенетическая эволюция в ПТР встречается чаще а) после применения миелоаблативного кондиционирования; б) при комплексном кариотипе перед трансплантацией; и в) сочетается с клональной гетерогенностью. Большинство общих цитогенетических аберраций в ПТР при ОМЛ и ОЛЛ различны. ОВ и выживаемость после посттрансплантационного рецидива ниже в группах пациентов с цитогенетической эволюцией (для ОВ и ВПТР), клональной гетерогенностью (для ОВ) и появлением нового неродственного клона (для ВПТР) в ПТР.
Ключевые слова
Острый лейкоз, посттрансплантационный рецидив, цитогенетическая эволюция, режим кондиционирования, исходы.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20417" ["VALUE"]=> array(2) { ["TEXT"]=> string(389) "НИИ детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(389) "НИИ детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(389) "НИИ детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Санкт-Петербург, Российская Федерация" } } } [4]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1564" ["~ID"]=> string(4) "1564" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(261) "Промежуточный анализ эффективности и безопасности терапии ниволумабом в дозе 40 мг в лечении рецидивирующей и реф- рактерной лимфомы Ходжкина" ["~NAME"]=> string(261) "Промежуточный анализ эффективности и безопасности терапии ниволумабом в дозе 40 мг в лечении рецидивирующей и реф- рактерной лимфомы Ходжкина" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:30:50" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:30:50" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/promezhutochnyy-analiz-effektivnosti-i-bezopasnosti-terapii-nivolumabom-v-doze-40-mg-v-lechenii-rets/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/promezhutochnyy-analiz-effektivnosti-i-bezopasnosti-terapii-nivolumabom-v-doze-40-mg-v-lechenii-rets/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "promezhutochnyy-analiz-effektivnosti-i-bezopasnosti-terapii-nivolumabom-v-doze-40-mg-v-lechenii-rets" ["~CODE"]=> string(100) "promezhutochnyy-analiz-effektivnosti-i-bezopasnosti-terapii-nivolumabom-v-doze-40-mg-v-lechenii-rets" ["EXTERNAL_ID"]=> string(4) "1564" ["~EXTERNAL_ID"]=> string(4) "1564" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(261) "Промежуточный анализ эффективности и безопасности терапии ниволумабом в дозе 40 мг в лечении рецидивирующей и реф- рактерной лимфомы Ходжкина" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(364) "Промежуточный анализ эффективности и безопасности терапии ниволумабом в дозе 40 мг в лечении рецидивирующей и реф- рактерной лимфомы ХоджкинаInterim analysis of effectiveness and safety of Nivolumab 40 mg in relapsed/refractory Hodgkin lymphoma" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(4302) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Целью работы была оценка эффективности и безопасности терапии ниволумабом в дозе 40 мг у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В промежуточный анализ были включены 14 пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина. Ниволумаб в дозе 40 мг вводился 1 раз в 2 недели до прогрессирования заболевания или развития тяжелых нежелательных явлений. Каждые 3 месяца (6 введений) производилась оценка ответа на терапию при использовании критериев LYRIC по данным ПЭТ/КТ, а также оценка наличия нежелательных явлений на терапию в соответствии с критериями NCI CTCAE 4.03. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Медиана наблюдения составила 10 месяцев. Медиана введений ниволумаба 17 (12-22). Медиана дозы препарата составила 0,56 мг/кг (0,4-0,91 мг/кг). Объективный ответ был получен у 9 (64,3%) пациентов, полный ответ у 5 (35,7%) и частичный ответ у 4 (28,6%) пациентов. Неопределенный ответ установлен у 4 (28,6%) пациентов. За время наблюдения у 2 (14,3%) пациентов было зафиксировано прогрессирование заболевания (после 12 и 18 введений). Нежелательные явления любой степени тяжести были представлены у 10 (71,4%) пациентов, при этом 3/4 степени тяжести только у 3 (21%), в виде анемии, артрита и гепатита. В целом, терапия хорошо переносилась пациентами, а профиль токсичности был сопоставим с ранее опубликованными данными. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> По данным промежуточного анализа, структура ответа на терапию у пациентов, получавших ниволумаб в дозе 40 мг, сопоставима с пациентами, получавшими препарат в полной дозе (3 мг/кг). Распределение частоты встречаемости, времени появления и вариантов нежелательных явлений также схожи с группой пациентов, получающих стандартную терапию. Таким образом, можно предположить, что данный режим дозирования будет эффективен и безопасен у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина, однако необходимо продолжить исследование для получения заключительных результатов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфома Ходжкина, ниволумаб, иммунотерапия, PD1-ингибиторы, рецидивирующие лимфомы, резистентные лимфомы. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(261) "Промежуточный анализ эффективности и безопасности терапии ниволумабом в дозе 40 мг в лечении рецидивирующей и реф- рактерной лимфомы Ходжкина" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(261) "Промежуточный анализ эффективности и безопасности терапии ниволумабом в дозе 40 мг в лечении рецидивирующей и реф- рактерной лимфомы Ходжкина" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(261) "Промежуточный анализ эффективности и безопасности терапии ниволумабом в дозе 40 мг в лечении рецидивирующей и реф- рактерной лимфомы Ходжкина" ["SECTION_META_TITLE"]=> string(261) "Промежуточный анализ эффективности и безопасности терапии ниволумабом в дозе 40 мг в лечении рецидивирующей и реф- рактерной лимфомы Ходжкина" ["SECTION_META_KEYWORDS"]=> string(261) "Промежуточный анализ эффективности и безопасности терапии ниволумабом в дозе 40 мг в лечении рецидивирующей и реф- рактерной лимфомы Ходжкина" ["SECTION_META_DESCRIPTION"]=> string(261) "Промежуточный анализ эффективности и безопасности терапии ниволумабом в дозе 40 мг в лечении рецидивирующей и реф- рактерной лимфомы Ходжкина" ["SECTION_PICTURE_FILE_ALT"]=> string(261) "Промежуточный анализ эффективности и безопасности терапии ниволумабом в дозе 40 мг в лечении рецидивирующей и реф- рактерной лимфомы Ходжкина" ["SECTION_PICTURE_FILE_TITLE"]=> string(261) "Промежуточный анализ эффективности и безопасности терапии ниволумабом в дозе 40 мг в лечении рецидивирующей и реф- рактерной лимфомы Ходжкина" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "promezhutochnyy-analiz-effektivnosti-i-bezopasnosti-terapii-nivolumabom-v-doze-40-mg-v-lechenii-rets" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(261) "Промежуточный анализ эффективности и безопасности терапии ниволумабом в дозе 40 мг в лечении рецидивирующей и реф- рактерной лимфомы Ходжкина" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(261) "Промежуточный анализ эффективности и безопасности терапии ниволумабом в дозе 40 мг в лечении рецидивирующей и реф- рактерной лимфомы Ходжкина" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "promezhutochnyy-analiz-effektivnosti-i-bezopasnosti-terapii-nivolumabom-v-doze-40-mg-v-lechenii-rets" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "promezhutochnyy-analiz-effektivnosti-i-bezopasnosti-terapii-nivolumabom-v-doze-40-mg-v-lechenii-rets" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "promezhutochnyy-analiz-effektivnosti-i-bezopasnosti-terapii-nivolumabom-v-doze-40-mg-v-lechenii-rets" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20407" ["VALUE"]=> array(2) { ["TEXT"]=> string(408) "Людмила В. Федорова, Кирилл В. Лепик, Наталия Б. Михайлова, Елена В. Кондакова, Юрий Р. Залялов, Анастасия В. Бейнарович, Елена Е. Давыдова, Любовь А. Цветкова, Вадим В. Байков, Елена В. Бабенко, Лилия В. Стельмах, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(408) "Людмила В. Федорова, Кирилл В. Лепик, Наталия Б. Михайлова, Елена В. Кондакова, Юрий Р. Залялов, Анастасия В. Бейнарович, Елена Е. Давыдова, Любовь А. Цветкова, Вадим В. Байков, Елена В. Бабенко, Лилия В. Стельмах, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20408" ["VALUE"]=> array(2) { ["TEXT"]=> string(390) "НИИ детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(390) "НИИ детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20409" ["VALUE"]=> array(2) { ["TEXT"]=> string(4302) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Целью работы была оценка эффективности и безопасности терапии ниволумабом в дозе 40 мг у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В промежуточный анализ были включены 14 пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина. Ниволумаб в дозе 40 мг вводился 1 раз в 2 недели до прогрессирования заболевания или развития тяжелых нежелательных явлений. Каждые 3 месяца (6 введений) производилась оценка ответа на терапию при использовании критериев LYRIC по данным ПЭТ/КТ, а также оценка наличия нежелательных явлений на терапию в соответствии с критериями NCI CTCAE 4.03. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Медиана наблюдения составила 10 месяцев. Медиана введений ниволумаба 17 (12-22). Медиана дозы препарата составила 0,56 мг/кг (0,4-0,91 мг/кг). Объективный ответ был получен у 9 (64,3%) пациентов, полный ответ у 5 (35,7%) и частичный ответ у 4 (28,6%) пациентов. Неопределенный ответ установлен у 4 (28,6%) пациентов. За время наблюдения у 2 (14,3%) пациентов было зафиксировано прогрессирование заболевания (после 12 и 18 введений). Нежелательные явления любой степени тяжести были представлены у 10 (71,4%) пациентов, при этом 3/4 степени тяжести только у 3 (21%), в виде анемии, артрита и гепатита. В целом, терапия хорошо переносилась пациентами, а профиль токсичности был сопоставим с ранее опубликованными данными. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> По данным промежуточного анализа, структура ответа на терапию у пациентов, получавших ниволумаб в дозе 40 мг, сопоставима с пациентами, получавшими препарат в полной дозе (3 мг/кг). Распределение частоты встречаемости, времени появления и вариантов нежелательных явлений также схожи с группой пациентов, получающих стандартную терапию. Таким образом, можно предположить, что данный режим дозирования будет эффективен и безопасен у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина, однако необходимо продолжить исследование для получения заключительных результатов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфома Ходжкина, ниволумаб, иммунотерапия, PD1-ингибиторы, рецидивирующие лимфомы, резистентные лимфомы. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4082) "Введение
Целью работы была оценка эффективности и безопасности терапии ниволумабом в дозе 40 мг у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина.
Материалы и методы
В промежуточный анализ были включены 14 пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина. Ниволумаб в дозе 40 мг вводился 1 раз в 2 недели до прогрессирования заболевания или развития тяжелых нежелательных явлений. Каждые 3 месяца (6 введений) производилась оценка ответа на терапию при использовании критериев LYRIC по данным ПЭТ/КТ, а также оценка наличия нежелательных явлений на терапию в соответствии с критериями NCI CTCAE 4.03.
Результаты
Медиана наблюдения составила 10 месяцев. Медиана введений ниволумаба 17 (12-22). Медиана дозы препарата составила 0,56 мг/кг (0,4-0,91 мг/кг). Объективный ответ был получен у 9 (64,3%) пациентов, полный ответ у 5 (35,7%) и частичный ответ у 4 (28,6%) пациентов. Неопределенный ответ установлен у 4 (28,6%) пациентов. За время наблюдения у 2 (14,3%) пациентов было зафиксировано прогрессирование заболевания (после 12 и 18 введений). Нежелательные явления любой степени тяжести были представлены у 10 (71,4%) пациентов, при этом 3/4 степени тяжести только у 3 (21%), в виде анемии, артрита и гепатита. В целом, терапия хорошо переносилась пациентами, а профиль токсичности был сопоставим с ранее опубликованными данными.
Заключение
По данным промежуточного анализа, структура ответа на терапию у пациентов, получавших ниволумаб в дозе 40 мг, сопоставима с пациентами, получавшими препарат в полной дозе (3 мг/кг). Распределение частоты встречаемости, времени появления и вариантов нежелательных явлений также схожи с группой пациентов, получающих стандартную терапию. Таким образом, можно предположить, что данный режим дозирования будет эффективен и безопасен у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина, однако необходимо продолжить исследование для получения заключительных результатов.
Ключевые слова
Лимфома Ходжкина, ниволумаб, иммунотерапия, PD1-ингибиторы, рецидивирующие лимфомы, резистентные лимфомы.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20410" ["VALUE"]=> array(2) { ["TEXT"]=> string(248) "Liudmila V. Fedorova, Kirill V. Lepik, Natalia B. Mikhailova, Elena V. Kondakova, Yuri R. Zalyalov, Anastasia V. Beynarovich, Elena E. Davydova, Luibov A. Tsvetkova, Vadim V. Baykov, Elena V. Babenko, Lilia V. Stelmakh, Boris V. Afanasyev<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(242) "Liudmila V. Fedorova, Kirill V. Lepik, Natalia B. Mikhailova, Elena V. Kondakova, Yuri R. Zalyalov, Anastasia V. Beynarovich, Elena E. Davydova, Luibov A. Tsvetkova, Vadim V. Baykov, Elena V. Babenko, Lilia V. Stelmakh, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20411" ["VALUE"]=> array(2) { ["TEXT"]=> string(190) "Raisa Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(184) "Raisa Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20412" ["VALUE"]=> array(2) { ["TEXT"]=> string(2515) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Aim of the study was to determine effectiveness and safety of therapy with Nivolumab 40 mg in patients with relapsed/refractory Hodgkin lymphoma. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> Intermediate analysis included 14 patients with relapsed/refractory Hodgkin lymphoma who were treated with nivolumab 40 mg once per 14 days until disease progression/unacceptable toxicity. Response was assessed by PET/CT using LYRIC criteria every 3 month (6 cycles). The safety was estimated by registration adverse effects according to NCI CTCAE 4.03. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Median follow‐up time was 10 months. Median number of treatment cycles with nivolumab was 17 (12-22). Median dose of drug was 0,56 mg/kg (0.4-0.91 mg/kg). 9 patients (64.3%) achieved an objective response, 5 (35.7%) a complete response (CR), and 4 patients (28.6%) a partial response. 4 patients (28.6%) had intermediate response as their best response. Two (14.3%) patients had progressive disease (at the moment of 12th and 18th cycles). Ten (71.4%) patients had adverse effects (AE). Grade ¾ AE were reported in 3 (21%) patients and included an anemia, arthritis and hepatitis. In general, the treatment was well tolerated and the toxicity profile was similar to the previously published data. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> According to the intermediate analysis, the structure of the response to therapy in patients treated with nivolumab 40 mg was comparable to patients treated with nivolumab in standard dose (3 mg/kg). The distribution of frequency, time of occurence and structure of adverse events was also similar to the standard therapy group. In conclusion, our data indicates that nivolumab 40 mg can be an effective and safety treatment option for R/R HL patients, but it’s nessesary to continue the study to obtain the final results. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hodgkin lymphoma, nivolumab, immunotherapy, PD1 inhibitors, relapsed lymphoma, refractory lymphoma. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2295) "
Introduction
Aim of the study was to determine effectiveness and safety of therapy with Nivolumab 40 mg in patients with relapsed/refractory Hodgkin lymphoma.
Materials and methods
Intermediate analysis included 14 patients with relapsed/refractory Hodgkin lymphoma who were treated with nivolumab 40 mg once per 14 days until disease progression/unacceptable toxicity. Response was assessed by PET/CT using LYRIC criteria every 3 month (6 cycles). The safety was estimated by registration adverse effects according to NCI CTCAE 4.03.
Results
Median follow‐up time was 10 months. Median number of treatment cycles with nivolumab was 17 (12-22). Median dose of drug was 0,56 mg/kg (0.4-0.91 mg/kg). 9 patients (64.3%) achieved an objective response, 5 (35.7%) a complete response (CR), and 4 patients (28.6%) a partial response. 4 patients (28.6%) had intermediate response as their best response. Two (14.3%) patients had progressive disease (at the moment of 12th and 18th cycles). Ten (71.4%) patients had adverse effects (AE). Grade ¾ AE were reported in 3 (21%) patients and included an anemia, arthritis and hepatitis. In general, the treatment was well tolerated and the toxicity profile was similar to the previously published data.
Conclusion
According to the intermediate analysis, the structure of the response to therapy in patients treated with nivolumab 40 mg was comparable to patients treated with nivolumab in standard dose (3 mg/kg). The distribution of frequency, time of occurence and structure of adverse events was also similar to the standard therapy group. In conclusion, our data indicates that nivolumab 40 mg can be an effective and safety treatment option for R/R HL patients, but it’s nessesary to continue the study to obtain the final results.
Keywords
Hodgkin lymphoma, nivolumab, immunotherapy, PD1 inhibitors, relapsed lymphoma, refractory lymphoma.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20413" ["VALUE"]=> string(103) "Interim analysis of effectiveness and safety of Nivolumab 40 mg in relapsed/refractory Hodgkin lymphoma" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(103) "Interim analysis of effectiveness and safety of Nivolumab 40 mg in relapsed/refractory Hodgkin lymphoma" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20761" ["VALUE"]=> string(4) "1397" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1397" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20762" ["VALUE"]=> string(4) "1398" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1398" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20410" ["VALUE"]=> array(2) { ["TEXT"]=> string(248) "Liudmila V. Fedorova, Kirill V. Lepik, Natalia B. Mikhailova, Elena V. Kondakova, Yuri R. Zalyalov, Anastasia V. Beynarovich, Elena E. Davydova, Luibov A. Tsvetkova, Vadim V. Baykov, Elena V. Babenko, Lilia V. Stelmakh, Boris V. Afanasyev<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(242) "Liudmila V. Fedorova, Kirill V. Lepik, Natalia B. Mikhailova, Elena V. Kondakova, Yuri R. Zalyalov, Anastasia V. Beynarovich, Elena E. Davydova, Luibov A. Tsvetkova, Vadim V. Baykov, Elena V. Babenko, Lilia V. Stelmakh, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(242) "Liudmila V. Fedorova, Kirill V. Lepik, Natalia B. Mikhailova, Elena V. Kondakova, Yuri R. Zalyalov, Anastasia V. Beynarovich, Elena E. Davydova, Luibov A. Tsvetkova, Vadim V. Baykov, Elena V. Babenko, Lilia V. Stelmakh, Boris V. Afanasyev
" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20412" ["VALUE"]=> array(2) { ["TEXT"]=> string(2515) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Aim of the study was to determine effectiveness and safety of therapy with Nivolumab 40 mg in patients with relapsed/refractory Hodgkin lymphoma. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> Intermediate analysis included 14 patients with relapsed/refractory Hodgkin lymphoma who were treated with nivolumab 40 mg once per 14 days until disease progression/unacceptable toxicity. Response was assessed by PET/CT using LYRIC criteria every 3 month (6 cycles). The safety was estimated by registration adverse effects according to NCI CTCAE 4.03. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Median follow‐up time was 10 months. Median number of treatment cycles with nivolumab was 17 (12-22). Median dose of drug was 0,56 mg/kg (0.4-0.91 mg/kg). 9 patients (64.3%) achieved an objective response, 5 (35.7%) a complete response (CR), and 4 patients (28.6%) a partial response. 4 patients (28.6%) had intermediate response as their best response. Two (14.3%) patients had progressive disease (at the moment of 12th and 18th cycles). Ten (71.4%) patients had adverse effects (AE). Grade ¾ AE were reported in 3 (21%) patients and included an anemia, arthritis and hepatitis. In general, the treatment was well tolerated and the toxicity profile was similar to the previously published data. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> According to the intermediate analysis, the structure of the response to therapy in patients treated with nivolumab 40 mg was comparable to patients treated with nivolumab in standard dose (3 mg/kg). The distribution of frequency, time of occurence and structure of adverse events was also similar to the standard therapy group. In conclusion, our data indicates that nivolumab 40 mg can be an effective and safety treatment option for R/R HL patients, but it’s nessesary to continue the study to obtain the final results. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hodgkin lymphoma, nivolumab, immunotherapy, PD1 inhibitors, relapsed lymphoma, refractory lymphoma. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2295) "
Introduction
Aim of the study was to determine effectiveness and safety of therapy with Nivolumab 40 mg in patients with relapsed/refractory Hodgkin lymphoma.
Materials and methods
Intermediate analysis included 14 patients with relapsed/refractory Hodgkin lymphoma who were treated with nivolumab 40 mg once per 14 days until disease progression/unacceptable toxicity. Response was assessed by PET/CT using LYRIC criteria every 3 month (6 cycles). The safety was estimated by registration adverse effects according to NCI CTCAE 4.03.
Results
Median follow‐up time was 10 months. Median number of treatment cycles with nivolumab was 17 (12-22). Median dose of drug was 0,56 mg/kg (0.4-0.91 mg/kg). 9 patients (64.3%) achieved an objective response, 5 (35.7%) a complete response (CR), and 4 patients (28.6%) a partial response. 4 patients (28.6%) had intermediate response as their best response. Two (14.3%) patients had progressive disease (at the moment of 12th and 18th cycles). Ten (71.4%) patients had adverse effects (AE). Grade ¾ AE were reported in 3 (21%) patients and included an anemia, arthritis and hepatitis. In general, the treatment was well tolerated and the toxicity profile was similar to the previously published data.
Conclusion
According to the intermediate analysis, the structure of the response to therapy in patients treated with nivolumab 40 mg was comparable to patients treated with nivolumab in standard dose (3 mg/kg). The distribution of frequency, time of occurence and structure of adverse events was also similar to the standard therapy group. In conclusion, our data indicates that nivolumab 40 mg can be an effective and safety treatment option for R/R HL patients, but it’s nessesary to continue the study to obtain the final results.
Keywords
Hodgkin lymphoma, nivolumab, immunotherapy, PD1 inhibitors, relapsed lymphoma, refractory lymphoma.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2295) "Introduction
Aim of the study was to determine effectiveness and safety of therapy with Nivolumab 40 mg in patients with relapsed/refractory Hodgkin lymphoma.
Materials and methods
Intermediate analysis included 14 patients with relapsed/refractory Hodgkin lymphoma who were treated with nivolumab 40 mg once per 14 days until disease progression/unacceptable toxicity. Response was assessed by PET/CT using LYRIC criteria every 3 month (6 cycles). The safety was estimated by registration adverse effects according to NCI CTCAE 4.03.
Results
Median follow‐up time was 10 months. Median number of treatment cycles with nivolumab was 17 (12-22). Median dose of drug was 0,56 mg/kg (0.4-0.91 mg/kg). 9 patients (64.3%) achieved an objective response, 5 (35.7%) a complete response (CR), and 4 patients (28.6%) a partial response. 4 patients (28.6%) had intermediate response as their best response. Two (14.3%) patients had progressive disease (at the moment of 12th and 18th cycles). Ten (71.4%) patients had adverse effects (AE). Grade ¾ AE were reported in 3 (21%) patients and included an anemia, arthritis and hepatitis. In general, the treatment was well tolerated and the toxicity profile was similar to the previously published data.
Conclusion
According to the intermediate analysis, the structure of the response to therapy in patients treated with nivolumab 40 mg was comparable to patients treated with nivolumab in standard dose (3 mg/kg). The distribution of frequency, time of occurence and structure of adverse events was also similar to the standard therapy group. In conclusion, our data indicates that nivolumab 40 mg can be an effective and safety treatment option for R/R HL patients, but it’s nessesary to continue the study to obtain the final results.
Keywords
Hodgkin lymphoma, nivolumab, immunotherapy, PD1 inhibitors, relapsed lymphoma, refractory lymphoma.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20413" ["VALUE"]=> string(103) "Interim analysis of effectiveness and safety of Nivolumab 40 mg in relapsed/refractory Hodgkin lymphoma" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(103) "Interim analysis of effectiveness and safety of Nivolumab 40 mg in relapsed/refractory Hodgkin lymphoma" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(103) "Interim analysis of effectiveness and safety of Nivolumab 40 mg in relapsed/refractory Hodgkin lymphoma" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20411" ["VALUE"]=> array(2) { ["TEXT"]=> string(190) "Raisa Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(184) "Raisa Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(184) "Raisa Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20407" ["VALUE"]=> array(2) { ["TEXT"]=> string(408) "Людмила В. Федорова, Кирилл В. Лепик, Наталия Б. Михайлова, Елена В. Кондакова, Юрий Р. Залялов, Анастасия В. Бейнарович, Елена Е. Давыдова, Любовь А. Цветкова, Вадим В. Байков, Елена В. Бабенко, Лилия В. Стельмах, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(408) "Людмила В. Федорова, Кирилл В. Лепик, Наталия Б. Михайлова, Елена В. Кондакова, Юрий Р. Залялов, Анастасия В. Бейнарович, Елена Е. Давыдова, Любовь А. Цветкова, Вадим В. Байков, Елена В. Бабенко, Лилия В. Стельмах, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(408) "Людмила В. Федорова, Кирилл В. Лепик, Наталия Б. Михайлова, Елена В. Кондакова, Юрий Р. Залялов, Анастасия В. Бейнарович, Елена Е. Давыдова, Любовь А. Цветкова, Вадим В. Байков, Елена В. Бабенко, Лилия В. Стельмах, Борис В. Афанасьев" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20409" ["VALUE"]=> array(2) { ["TEXT"]=> string(4302) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Целью работы была оценка эффективности и безопасности терапии ниволумабом в дозе 40 мг у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В промежуточный анализ были включены 14 пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина. Ниволумаб в дозе 40 мг вводился 1 раз в 2 недели до прогрессирования заболевания или развития тяжелых нежелательных явлений. Каждые 3 месяца (6 введений) производилась оценка ответа на терапию при использовании критериев LYRIC по данным ПЭТ/КТ, а также оценка наличия нежелательных явлений на терапию в соответствии с критериями NCI CTCAE 4.03. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Медиана наблюдения составила 10 месяцев. Медиана введений ниволумаба 17 (12-22). Медиана дозы препарата составила 0,56 мг/кг (0,4-0,91 мг/кг). Объективный ответ был получен у 9 (64,3%) пациентов, полный ответ у 5 (35,7%) и частичный ответ у 4 (28,6%) пациентов. Неопределенный ответ установлен у 4 (28,6%) пациентов. За время наблюдения у 2 (14,3%) пациентов было зафиксировано прогрессирование заболевания (после 12 и 18 введений). Нежелательные явления любой степени тяжести были представлены у 10 (71,4%) пациентов, при этом 3/4 степени тяжести только у 3 (21%), в виде анемии, артрита и гепатита. В целом, терапия хорошо переносилась пациентами, а профиль токсичности был сопоставим с ранее опубликованными данными. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> По данным промежуточного анализа, структура ответа на терапию у пациентов, получавших ниволумаб в дозе 40 мг, сопоставима с пациентами, получавшими препарат в полной дозе (3 мг/кг). Распределение частоты встречаемости, времени появления и вариантов нежелательных явлений также схожи с группой пациентов, получающих стандартную терапию. Таким образом, можно предположить, что данный режим дозирования будет эффективен и безопасен у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина, однако необходимо продолжить исследование для получения заключительных результатов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфома Ходжкина, ниволумаб, иммунотерапия, PD1-ингибиторы, рецидивирующие лимфомы, резистентные лимфомы. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4082) "
Введение
Целью работы была оценка эффективности и безопасности терапии ниволумабом в дозе 40 мг у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина.
Материалы и методы
В промежуточный анализ были включены 14 пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина. Ниволумаб в дозе 40 мг вводился 1 раз в 2 недели до прогрессирования заболевания или развития тяжелых нежелательных явлений. Каждые 3 месяца (6 введений) производилась оценка ответа на терапию при использовании критериев LYRIC по данным ПЭТ/КТ, а также оценка наличия нежелательных явлений на терапию в соответствии с критериями NCI CTCAE 4.03.
Результаты
Медиана наблюдения составила 10 месяцев. Медиана введений ниволумаба 17 (12-22). Медиана дозы препарата составила 0,56 мг/кг (0,4-0,91 мг/кг). Объективный ответ был получен у 9 (64,3%) пациентов, полный ответ у 5 (35,7%) и частичный ответ у 4 (28,6%) пациентов. Неопределенный ответ установлен у 4 (28,6%) пациентов. За время наблюдения у 2 (14,3%) пациентов было зафиксировано прогрессирование заболевания (после 12 и 18 введений). Нежелательные явления любой степени тяжести были представлены у 10 (71,4%) пациентов, при этом 3/4 степени тяжести только у 3 (21%), в виде анемии, артрита и гепатита. В целом, терапия хорошо переносилась пациентами, а профиль токсичности был сопоставим с ранее опубликованными данными.
Заключение
По данным промежуточного анализа, структура ответа на терапию у пациентов, получавших ниволумаб в дозе 40 мг, сопоставима с пациентами, получавшими препарат в полной дозе (3 мг/кг). Распределение частоты встречаемости, времени появления и вариантов нежелательных явлений также схожи с группой пациентов, получающих стандартную терапию. Таким образом, можно предположить, что данный режим дозирования будет эффективен и безопасен у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина, однако необходимо продолжить исследование для получения заключительных результатов.
Ключевые слова
Лимфома Ходжкина, ниволумаб, иммунотерапия, PD1-ингибиторы, рецидивирующие лимфомы, резистентные лимфомы.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4082) "Введение
Целью работы была оценка эффективности и безопасности терапии ниволумабом в дозе 40 мг у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина.
Материалы и методы
В промежуточный анализ были включены 14 пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина. Ниволумаб в дозе 40 мг вводился 1 раз в 2 недели до прогрессирования заболевания или развития тяжелых нежелательных явлений. Каждые 3 месяца (6 введений) производилась оценка ответа на терапию при использовании критериев LYRIC по данным ПЭТ/КТ, а также оценка наличия нежелательных явлений на терапию в соответствии с критериями NCI CTCAE 4.03.
Результаты
Медиана наблюдения составила 10 месяцев. Медиана введений ниволумаба 17 (12-22). Медиана дозы препарата составила 0,56 мг/кг (0,4-0,91 мг/кг). Объективный ответ был получен у 9 (64,3%) пациентов, полный ответ у 5 (35,7%) и частичный ответ у 4 (28,6%) пациентов. Неопределенный ответ установлен у 4 (28,6%) пациентов. За время наблюдения у 2 (14,3%) пациентов было зафиксировано прогрессирование заболевания (после 12 и 18 введений). Нежелательные явления любой степени тяжести были представлены у 10 (71,4%) пациентов, при этом 3/4 степени тяжести только у 3 (21%), в виде анемии, артрита и гепатита. В целом, терапия хорошо переносилась пациентами, а профиль токсичности был сопоставим с ранее опубликованными данными.
Заключение
По данным промежуточного анализа, структура ответа на терапию у пациентов, получавших ниволумаб в дозе 40 мг, сопоставима с пациентами, получавшими препарат в полной дозе (3 мг/кг). Распределение частоты встречаемости, времени появления и вариантов нежелательных явлений также схожи с группой пациентов, получающих стандартную терапию. Таким образом, можно предположить, что данный режим дозирования будет эффективен и безопасен у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина, однако необходимо продолжить исследование для получения заключительных результатов.
Ключевые слова
Лимфома Ходжкина, ниволумаб, иммунотерапия, PD1-ингибиторы, рецидивирующие лимфомы, резистентные лимфомы.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20408" ["VALUE"]=> array(2) { ["TEXT"]=> string(390) "НИИ детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(390) "НИИ детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(390) "НИИ детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Санкт-Петербург, Российская Федерация" } } } [5]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1569" ["~ID"]=> string(4) "1569" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(321) "Значение экспрессии гена WT1 для прогноза рецидивов и выживаемости после аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым миелоидным лейкозом" ["~NAME"]=> string(321) "Значение экспрессии гена WT1 для прогноза рецидивов и выживаемости после аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым миелоидным лейкозом" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:33:35" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:33:35" ["DETAIL_PAGE_URL"]=> string(151) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/znachenie-ekspressii-gena-wt1-dlya-prognoza-retsidivov-i-vyzhivaemosti-posle-allogennoy-transplantats/" ["~DETAIL_PAGE_URL"]=> string(151) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/znachenie-ekspressii-gena-wt1-dlya-prognoza-retsidivov-i-vyzhivaemosti-posle-allogennoy-transplantats/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(101) "znachenie-ekspressii-gena-wt1-dlya-prognoza-retsidivov-i-vyzhivaemosti-posle-allogennoy-transplantats" ["~CODE"]=> string(101) "znachenie-ekspressii-gena-wt1-dlya-prognoza-retsidivov-i-vyzhivaemosti-posle-allogennoy-transplantats" ["EXTERNAL_ID"]=> string(4) "1569" ["~EXTERNAL_ID"]=> string(4) "1569" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(321) "Значение экспрессии гена WT1 для прогноза рецидивов и выживаемости после аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым миелоидным лейкозом" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(448) "Значение экспрессии гена WT1 для прогноза рецидивов и выживаемости после аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым миелоидным лейкозомThe prognostic value of the WT1 gene expression on relapse and survival AML patients after allogeneic stem cell transplantation" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(8781) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) в настоящее время считается лучшим методом лечения ОМЛ с плохим прогнозом, который часто сопровождается посттрансплантационными рецидивами (ПТР). Среди ПТР могут быть молекулярные и цитологические варианты (мПТР и цПТР соответственно). Известно, что уровень экспрессии гена WT1 является хорошим индикатором массы продуцирующих его бластных элементов. С помощью этого теста имеется возможность ранней диагностики мПТР и оценка общей и бессобытийной выживаемости (ОВ и БСВ соответственно) и кумулятивной частоты рецидивов (КЧР) больных ОМЛ, леченных с использованием алло-ТГСК. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Исследование включало 88 пациентов с ОМЛ в возрасте от 2 до 68 лет (медиана – 30 лет), которым была выполнена алло-ТГСК в нашем Центре в период с 2011 по 2017 годы. Уровни экспрессии гена WT1 измеряли серийно количественной ПЦР в реальном времени, а содержание бластов в тех же аспиратах костного мозга определяли в стандартно выбранных контрольных временных точках: перед трансплантацией (Д0) и в дни Д+30, Д+60 и Д+100 после ее выполнения. Пороговый уровень экспрессии гена WT1 был определен на основании измерения уровня экспрессии гена WT1 в аспиратах костного мозга здоровых доноров и равнялся 250 копиям WT1/10<sup>4</sup> копий гена ABL. Во всех временных точках были сформированы группы больных с повышенным и нормализованным уровнями экспрессии гена WT1 (>250 копий <250 копий соответственно) и рассчитана разница в 2-летней ОВ, БСВ и КЧР. Поскольку повышение уровня экспрессии гена WT1, отражающее содержание секретирующих этот ген бластов, может опережать по времени определяемые морфологом цПТР, мы измерили этот временный интервал у всех обследованных больных ОМЛ и сопоставили его с проведенной посттрансплантационной терапией. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Уровни экспрессии гена WT1 перед режимом кондиционирования варьировали от 0 до 56884 копий WT1/10<sup>4 </sup>копий гена ABL (медиана – 253 копии). По данным критериям лог-ранга, существенная разница в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 перед алло-ТГСК выглядела следующим образом: 79,5%, 69,8% и 28,2% против 31,8%, 22,7% и 58,9%, при p<0,001, p<0,001 и p=0,0019 соответственно. Различий в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 на день Д+30 после выполнения алло-ТГСК не было. Достоверные различия в 2-летней ОВ и КЧР наблюдались между этими группами на день Д+60 после выполнения алло-ТГСК (66,2% и 42,3% против 35,7% и 61,5% при p=0,012 и р=0,01 соответственно), в то время как достоверные различия в БСВ отсутствовали (52,3% против 38,5%, р=0,084). Наибольшие различия в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 имели место в контрольной временной точке Д+100 после алло-ТГСК (28,6%, 19% и 77,8% против 75,4%, 63,2% и 32,7% при р<0,001, р<0,001 и р<0,001 соответственно) (Рис.1). На основе пропорциональных рисков Кокса, независимое позитивное влияние на ОВ и БСВ сохранилось только для нормализованного во временной точке Д+100 после выполнения алло-ТГСК уровня экспрессии гена WT1 (р=0,011 и р=0,041) и наличия у больных хрРТПХ (р=0,038 и р=0,03). При этом отношение риска рецидива (125) было максимальным также на день Д+100. По нашим данным, мПТР и цПТР были зарегистрированы у 55/88 (62,5%) и 33/88 (37,5%) пациентов соответственно. У 33,3% пациентов (11/33) мПТР и цПТР по времени появления совпадали, в то время как в 22 наблюдениях цПТР отставали от мПТР на 13-321 день (медиана – 35). Задержка цПТР от мПТР частично может быть объяснено проводимой в клинике терапией, в частности, инфузиями донорских лимфоцитов и наличием у больных хронической РТПХ, что хорошо согласуется с данными литературы [Pozzi et al, 2013]. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Уровень повышенной и нормализованной экспрессии гена WT1 является удобным и полезным для клиники маркером молекулярно контролируемых ПТР и ремиссий ОМЛ. Оптимальной временной точкой для измерения уровня экспрессии гена WT1 в диагностике ПТР является Д+100, за которой, по мере снижения значимости, следуют Д0, Д+60 и Д+30. По нашим данным наудлинение продолжительности ОВ и БСВ сказывается также наличие у больных ОМЛ признаков хрРТПХ, что объясняется наметившуюся в клинике тенденцию лечить иммунотерапией диагностированные при серийном измерении уровни экспрессии гена WT1 мПТР [Di Grazia et al, 2016]. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток, острый миелоидный лейкоз, WT1, рецидив, молекулярный мониторинг. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(321) "Значение экспрессии гена WT1 для прогноза рецидивов и выживаемости после аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым миелоидным лейкозом" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(321) "Значение экспрессии гена WT1 для прогноза рецидивов и выживаемости после аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым миелоидным лейкозом" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(321) "Значение экспрессии гена WT1 для прогноза рецидивов и выживаемости после аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым миелоидным лейкозом" ["SECTION_META_TITLE"]=> string(321) "Значение экспрессии гена WT1 для прогноза рецидивов и выживаемости после аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым миелоидным лейкозом" ["SECTION_META_KEYWORDS"]=> string(321) "Значение экспрессии гена WT1 для прогноза рецидивов и выживаемости после аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым миелоидным лейкозом" ["SECTION_META_DESCRIPTION"]=> string(321) "Значение экспрессии гена WT1 для прогноза рецидивов и выживаемости после аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым миелоидным лейкозом" ["SECTION_PICTURE_FILE_ALT"]=> string(321) "Значение экспрессии гена WT1 для прогноза рецидивов и выживаемости после аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым миелоидным лейкозом" ["SECTION_PICTURE_FILE_TITLE"]=> string(321) "Значение экспрессии гена WT1 для прогноза рецидивов и выживаемости после аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым миелоидным лейкозом" ["SECTION_PICTURE_FILE_NAME"]=> string(101) "znachenie-ekspressii-gena-wt1-dlya-prognoza-retsidivov-i-vyzhivaemosti-posle-allogennoy-transplantats" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(321) "Значение экспрессии гена WT1 для прогноза рецидивов и выживаемости после аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым миелоидным лейкозом" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(321) "Значение экспрессии гена WT1 для прогноза рецидивов и выживаемости после аллогенной трансплантации гемопоэтических стволовых клеток у пациентов с острым миелоидным лейкозом" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(101) "znachenie-ekspressii-gena-wt1-dlya-prognoza-retsidivov-i-vyzhivaemosti-posle-allogennoy-transplantats" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(101) "znachenie-ekspressii-gena-wt1-dlya-prognoza-retsidivov-i-vyzhivaemosti-posle-allogennoy-transplantats" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(101) "znachenie-ekspressii-gena-wt1-dlya-prognoza-retsidivov-i-vyzhivaemosti-posle-allogennoy-transplantats" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20452" ["VALUE"]=> array(2) { ["TEXT"]=> string(364) "Яна В. Гудожникова, Николай Н. Мамаев, Ильдар М. Бархатов, Алена И. Шакирова, Валерия А. Катерина, Сергей Н. Бондаренко, Татьяна Л. Гиндина, Валентина М. Кравцова, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(364) "Яна В. Гудожникова, Николай Н. Мамаев, Ильдар М. Бархатов, Алена И. Шакирова, Валерия А. Катерина, Сергей Н. Бондаренко, Татьяна Л. Гиндина, Валентина М. Кравцова, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20453" ["VALUE"]=> array(2) { ["TEXT"]=> string(406) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(406) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20454" ["VALUE"]=> array(2) { ["TEXT"]=> string(8781) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) в настоящее время считается лучшим методом лечения ОМЛ с плохим прогнозом, который часто сопровождается посттрансплантационными рецидивами (ПТР). Среди ПТР могут быть молекулярные и цитологические варианты (мПТР и цПТР соответственно). Известно, что уровень экспрессии гена WT1 является хорошим индикатором массы продуцирующих его бластных элементов. С помощью этого теста имеется возможность ранней диагностики мПТР и оценка общей и бессобытийной выживаемости (ОВ и БСВ соответственно) и кумулятивной частоты рецидивов (КЧР) больных ОМЛ, леченных с использованием алло-ТГСК. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Исследование включало 88 пациентов с ОМЛ в возрасте от 2 до 68 лет (медиана – 30 лет), которым была выполнена алло-ТГСК в нашем Центре в период с 2011 по 2017 годы. Уровни экспрессии гена WT1 измеряли серийно количественной ПЦР в реальном времени, а содержание бластов в тех же аспиратах костного мозга определяли в стандартно выбранных контрольных временных точках: перед трансплантацией (Д0) и в дни Д+30, Д+60 и Д+100 после ее выполнения. Пороговый уровень экспрессии гена WT1 был определен на основании измерения уровня экспрессии гена WT1 в аспиратах костного мозга здоровых доноров и равнялся 250 копиям WT1/10<sup>4</sup> копий гена ABL. Во всех временных точках были сформированы группы больных с повышенным и нормализованным уровнями экспрессии гена WT1 (>250 копий <250 копий соответственно) и рассчитана разница в 2-летней ОВ, БСВ и КЧР. Поскольку повышение уровня экспрессии гена WT1, отражающее содержание секретирующих этот ген бластов, может опережать по времени определяемые морфологом цПТР, мы измерили этот временный интервал у всех обследованных больных ОМЛ и сопоставили его с проведенной посттрансплантационной терапией. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Уровни экспрессии гена WT1 перед режимом кондиционирования варьировали от 0 до 56884 копий WT1/10<sup>4 </sup>копий гена ABL (медиана – 253 копии). По данным критериям лог-ранга, существенная разница в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 перед алло-ТГСК выглядела следующим образом: 79,5%, 69,8% и 28,2% против 31,8%, 22,7% и 58,9%, при p<0,001, p<0,001 и p=0,0019 соответственно. Различий в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 на день Д+30 после выполнения алло-ТГСК не было. Достоверные различия в 2-летней ОВ и КЧР наблюдались между этими группами на день Д+60 после выполнения алло-ТГСК (66,2% и 42,3% против 35,7% и 61,5% при p=0,012 и р=0,01 соответственно), в то время как достоверные различия в БСВ отсутствовали (52,3% против 38,5%, р=0,084). Наибольшие различия в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 имели место в контрольной временной точке Д+100 после алло-ТГСК (28,6%, 19% и 77,8% против 75,4%, 63,2% и 32,7% при р<0,001, р<0,001 и р<0,001 соответственно) (Рис.1). На основе пропорциональных рисков Кокса, независимое позитивное влияние на ОВ и БСВ сохранилось только для нормализованного во временной точке Д+100 после выполнения алло-ТГСК уровня экспрессии гена WT1 (р=0,011 и р=0,041) и наличия у больных хрРТПХ (р=0,038 и р=0,03). При этом отношение риска рецидива (125) было максимальным также на день Д+100. По нашим данным, мПТР и цПТР были зарегистрированы у 55/88 (62,5%) и 33/88 (37,5%) пациентов соответственно. У 33,3% пациентов (11/33) мПТР и цПТР по времени появления совпадали, в то время как в 22 наблюдениях цПТР отставали от мПТР на 13-321 день (медиана – 35). Задержка цПТР от мПТР частично может быть объяснено проводимой в клинике терапией, в частности, инфузиями донорских лимфоцитов и наличием у больных хронической РТПХ, что хорошо согласуется с данными литературы [Pozzi et al, 2013]. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Уровень повышенной и нормализованной экспрессии гена WT1 является удобным и полезным для клиники маркером молекулярно контролируемых ПТР и ремиссий ОМЛ. Оптимальной временной точкой для измерения уровня экспрессии гена WT1 в диагностике ПТР является Д+100, за которой, по мере снижения значимости, следуют Д0, Д+60 и Д+30. По нашим данным наудлинение продолжительности ОВ и БСВ сказывается также наличие у больных ОМЛ признаков хрРТПХ, что объясняется наметившуюся в клинике тенденцию лечить иммунотерапией диагностированные при серийном измерении уровни экспрессии гена WT1 мПТР [Di Grazia et al, 2016]. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток, острый миелоидный лейкоз, WT1, рецидив, молекулярный мониторинг. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(8497) "Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) в настоящее время считается лучшим методом лечения ОМЛ с плохим прогнозом, который часто сопровождается посттрансплантационными рецидивами (ПТР). Среди ПТР могут быть молекулярные и цитологические варианты (мПТР и цПТР соответственно). Известно, что уровень экспрессии гена WT1 является хорошим индикатором массы продуцирующих его бластных элементов. С помощью этого теста имеется возможность ранней диагностики мПТР и оценка общей и бессобытийной выживаемости (ОВ и БСВ соответственно) и кумулятивной частоты рецидивов (КЧР) больных ОМЛ, леченных с использованием алло-ТГСК.
Пациенты и методы
Исследование включало 88 пациентов с ОМЛ в возрасте от 2 до 68 лет (медиана – 30 лет), которым была выполнена алло-ТГСК в нашем Центре в период с 2011 по 2017 годы. Уровни экспрессии гена WT1 измеряли серийно количественной ПЦР в реальном времени, а содержание бластов в тех же аспиратах костного мозга определяли в стандартно выбранных контрольных временных точках: перед трансплантацией (Д0) и в дни Д+30, Д+60 и Д+100 после ее выполнения. Пороговый уровень экспрессии гена WT1 был определен на основании измерения уровня экспрессии гена WT1 в аспиратах костного мозга здоровых доноров и равнялся 250 копиям WT1/104 копий гена ABL. Во всех временных точках были сформированы группы больных с повышенным и нормализованным уровнями экспрессии гена WT1 (>250 копий <250 копий соответственно) и рассчитана разница в 2-летней ОВ, БСВ и КЧР. Поскольку повышение уровня экспрессии гена WT1, отражающее содержание секретирующих этот ген бластов, может опережать по времени определяемые морфологом цПТР, мы измерили этот временный интервал у всех обследованных больных ОМЛ и сопоставили его с проведенной посттрансплантационной терапией.
Результаты
Уровни экспрессии гена WT1 перед режимом кондиционирования варьировали от 0 до 56884 копий WT1/104 копий гена ABL (медиана – 253 копии). По данным критериям лог-ранга, существенная разница в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 перед алло-ТГСК выглядела следующим образом: 79,5%, 69,8% и 28,2% против 31,8%, 22,7% и 58,9%, при p<0,001, p<0,001 и p=0,0019 соответственно. Различий в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 на день Д+30 после выполнения алло-ТГСК не было. Достоверные различия в 2-летней ОВ и КЧР наблюдались между этими группами на день Д+60 после выполнения алло-ТГСК (66,2% и 42,3% против 35,7% и 61,5% при p=0,012 и р=0,01 соответственно), в то время как достоверные различия в БСВ отсутствовали (52,3% против 38,5%, р=0,084). Наибольшие различия в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 имели место в контрольной временной точке Д+100 после алло-ТГСК (28,6%, 19% и 77,8% против 75,4%, 63,2% и 32,7% при р<0,001, р<0,001 и р<0,001 соответственно) (Рис.1). На основе пропорциональных рисков Кокса, независимое позитивное влияние на ОВ и БСВ сохранилось только для нормализованного во временной точке Д+100 после выполнения алло-ТГСК уровня экспрессии гена WT1 (р=0,011 и р=0,041) и наличия у больных хрРТПХ (р=0,038 и р=0,03). При этом отношение риска рецидива (125) было максимальным также на день Д+100. По нашим данным, мПТР и цПТР были зарегистрированы у 55/88 (62,5%) и 33/88 (37,5%) пациентов соответственно. У 33,3% пациентов (11/33) мПТР и цПТР по времени появления совпадали, в то время как в 22 наблюдениях цПТР отставали от мПТР на 13-321 день (медиана – 35). Задержка цПТР от мПТР частично может быть объяснено проводимой в клинике терапией, в частности, инфузиями донорских лимфоцитов и наличием у больных хронической РТПХ, что хорошо согласуется с данными литературы [Pozzi et al, 2013].
Заключение
Уровень повышенной и нормализованной экспрессии гена WT1 является удобным и полезным для клиники маркером молекулярно контролируемых ПТР и ремиссий ОМЛ. Оптимальной временной точкой для измерения уровня экспрессии гена WT1 в диагностике ПТР является Д+100, за которой, по мере снижения значимости, следуют Д0, Д+60 и Д+30. По нашим данным наудлинение продолжительности ОВ и БСВ сказывается также наличие у больных ОМЛ признаков хрРТПХ, что объясняется наметившуюся в клинике тенденцию лечить иммунотерапией диагностированные при серийном измерении уровни экспрессии гена WT1 мПТР [Di Grazia et al, 2016].
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, острый миелоидный лейкоз, WT1, рецидив, молекулярный мониторинг.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20455" ["VALUE"]=> array(2) { ["TEXT"]=> string(212) "Yana V. Gudozhnikova, Nikolay N. Mamaev, Ildar M. Barkhatov, Аlena I. Shakirova, Valeria A. Katerina, Sergey N. Bondarenko, Tatiana L. Gindina, Valentina M. Kravtsova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(212) "Yana V. Gudozhnikova, Nikolay N. Mamaev, Ildar M. Barkhatov, Аlena I. Shakirova, Valeria A. Katerina, Sergey N. Bondarenko, Tatiana L. Gindina, Valentina M. Kravtsova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20456" ["VALUE"]=> array(2) { ["TEXT"]=> string(191) "R. M. Gorbacheva Memorial Research Institute of Pediatric Oncology, Hematology and Transplantation, 1st Saint Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(191) "R. M. Gorbacheva Memorial Research Institute of Pediatric Oncology, Hematology and Transplantation, 1st Saint Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20457" ["VALUE"]=> array(2) { ["TEXT"]=> string(5518) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is now considered the best treatment of AML with poor prognosis, which is, however, often followed by posttransplant relapses (PTR). Among PTR, molecular and cytological variants (mPTR and cPTR, respectively) are recognized. The WT1 gene is known to be an independent prognostic indicator of the mass of blast cells producing it. The serial measurement of WT1 expression levels provides a real possibility for early diagnosis of mPTR and an evaluation of the overall and event-free survival (OS and EFS, respectively) and the cumulative frequency of relapse (CIR) in patients with AML treated with allo-HSCT. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> The study included 88 AML patients aged 2 to 68 (median, 30 y.o.) who underwent allo-HSCT at our University between 2011 and 2017. WT1 gene expression levels were serially measured by real-time quantitative PCR, and marrow blast counts were performed in marrow samples at the standard control time points: before transplantation (D0) and on days D+30, D+60 and D+100 after transplantation. The WT1 threshold value was selected, as based on the measurement of expression levels of WT1 gene in bone marrow aspirates of healthy donors and determined as 250 WT1 copies/104 copies of ABL gene. At all the time points, groups of patients with elevated and normalized levels of WT1 gene expression (> 250 copies and < 250 copies, respectively) were formed, which allowed for calculating the difference in the 2-year OS, EFS and CIR. Since the increase in the expression of the WT1 gene reflecting the content of the blasts secreting this gene can precede the morphologically identified cPTR, we measured this time interval for all the examined AML patients taking in consideration the posttransplantation<br> therapy. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The levels of WT1 gene expression at allo-HSCT ranged from 0 to 56884 WT1/104 ABL copies (median – 253). According to the log-rank criteria, the difference in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression before allo-HSCT was as follows: 79.5%, 69.8%, 28.2% vs. 31.8%, 22.7% and 58.9%, at p<0.001, p<0.001, and p=0.0019, respectively. On D+30, we found no difference in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression. Significant differences in the 2-year OS and CIR in the two groups were found on D+60 (66.2% and 42.3% vs. 35.7% and 61.5% at p=0.012 and р=0.01, respectively), while there was still no significant difference in the EFS (52.3% vs. 38.5%, p=0.084). The greatest differences in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression occurred at the control time point D+100 (28.6%, 19% and 77.8% vs. 75.4% 63.2% and 32.7% at p<0.001, p<0.001, and p<0.001, respectively) (Fig.1). On the basis of proportional Cox risks, the independent positive effect on OS and EFS was preserved only for the normalized level of the WT1 gene expression (p=0.011 and p=0.041) at the time point D+100 after the allo-HSCT and in the presence of chronic GVHD (p=0.038 and p=0.03). In this case, the ratio of the risk of relapse (125) was maximal also on D+100. Concerning mPTR and cPTR, they were documented in 55/88 (62.5%) and 33/88 (37.5%) patients, respectively. In 33.3% of patients (11/33), mPTR and cPTR coincided in time, while in 22 cases cPTR occurred 13-321 (median – 35) days later than mPTR. According to the data obtained, this delay of cPTR from mPTR can be partially ascribed to the therapy performed at the clinic, in particular, donor lymphocyte infusions, and to presence of chronic GVHD in patients, thus being in good agreement with other research data [Pozzi et al, 2013]. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Elevated and normalized levels of WT1 gene expression are convenient and clinically useful markers of molecularly controlled mPTR and remission of AML. The optimal point for measuring the level of WT1 gene expression in PTR diagnostics is D+100, followed by D0, D+60 and D+30, as the significance decreases. According to our data, the duration of OS and EFS is also positively affected by the presence of chronic GVHD in AML patients after allo-HSCT, which explains the tendency to use immunotherapy to treat mPTR diagnosed by serial measurements of the WT1 gene expression levels [Di Grazia et al, 2016]. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Allogeneic stem cell transplantation, acute myeloid leukemia, WT1, relapse, molecular monitoring. </p> <p style="text-align: justify;"> <img width="805" alt="20_Figure1-2.png" src="/upload/medialibrary/376/20_figure1_2.png" height="711" title="20_Figure1-2.png"><br> </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5168) "Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is now considered the best treatment of AML with poor prognosis, which is, however, often followed by posttransplant relapses (PTR). Among PTR, molecular and cytological variants (mPTR and cPTR, respectively) are recognized. The WT1 gene is known to be an independent prognostic indicator of the mass of blast cells producing it. The serial measurement of WT1 expression levels provides a real possibility for early diagnosis of mPTR and an evaluation of the overall and event-free survival (OS and EFS, respectively) and the cumulative frequency of relapse (CIR) in patients with AML treated with allo-HSCT.
Patients and methods
The study included 88 AML patients aged 2 to 68 (median, 30 y.o.) who underwent allo-HSCT at our University between 2011 and 2017. WT1 gene expression levels were serially measured by real-time quantitative PCR, and marrow blast counts were performed in marrow samples at the standard control time points: before transplantation (D0) and on days D+30, D+60 and D+100 after transplantation. The WT1 threshold value was selected, as based on the measurement of expression levels of WT1 gene in bone marrow aspirates of healthy donors and determined as 250 WT1 copies/104 copies of ABL gene. At all the time points, groups of patients with elevated and normalized levels of WT1 gene expression (> 250 copies and < 250 copies, respectively) were formed, which allowed for calculating the difference in the 2-year OS, EFS and CIR. Since the increase in the expression of the WT1 gene reflecting the content of the blasts secreting this gene can precede the morphologically identified cPTR, we measured this time interval for all the examined AML patients taking in consideration the posttransplantation
therapy.
Results
The levels of WT1 gene expression at allo-HSCT ranged from 0 to 56884 WT1/104 ABL copies (median – 253). According to the log-rank criteria, the difference in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression before allo-HSCT was as follows: 79.5%, 69.8%, 28.2% vs. 31.8%, 22.7% and 58.9%, at p<0.001, p<0.001, and p=0.0019, respectively. On D+30, we found no difference in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression. Significant differences in the 2-year OS and CIR in the two groups were found on D+60 (66.2% and 42.3% vs. 35.7% and 61.5% at p=0.012 and р=0.01, respectively), while there was still no significant difference in the EFS (52.3% vs. 38.5%, p=0.084). The greatest differences in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression occurred at the control time point D+100 (28.6%, 19% and 77.8% vs. 75.4% 63.2% and 32.7% at p<0.001, p<0.001, and p<0.001, respectively) (Fig.1). On the basis of proportional Cox risks, the independent positive effect on OS and EFS was preserved only for the normalized level of the WT1 gene expression (p=0.011 and p=0.041) at the time point D+100 after the allo-HSCT and in the presence of chronic GVHD (p=0.038 and p=0.03). In this case, the ratio of the risk of relapse (125) was maximal also on D+100. Concerning mPTR and cPTR, they were documented in 55/88 (62.5%) and 33/88 (37.5%) patients, respectively. In 33.3% of patients (11/33), mPTR and cPTR coincided in time, while in 22 cases cPTR occurred 13-321 (median – 35) days later than mPTR. According to the data obtained, this delay of cPTR from mPTR can be partially ascribed to the therapy performed at the clinic, in particular, donor lymphocyte infusions, and to presence of chronic GVHD in patients, thus being in good agreement with other research data [Pozzi et al, 2013].
Conclusion
Elevated and normalized levels of WT1 gene expression are convenient and clinically useful markers of molecularly controlled mPTR and remission of AML. The optimal point for measuring the level of WT1 gene expression in PTR diagnostics is D+100, followed by D0, D+60 and D+30, as the significance decreases. According to our data, the duration of OS and EFS is also positively affected by the presence of chronic GVHD in AML patients after allo-HSCT, which explains the tendency to use immunotherapy to treat mPTR diagnosed by serial measurements of the WT1 gene expression levels [Di Grazia et al, 2016].
Keywords
Allogeneic stem cell transplantation, acute myeloid leukemia, WT1, relapse, molecular monitoring.
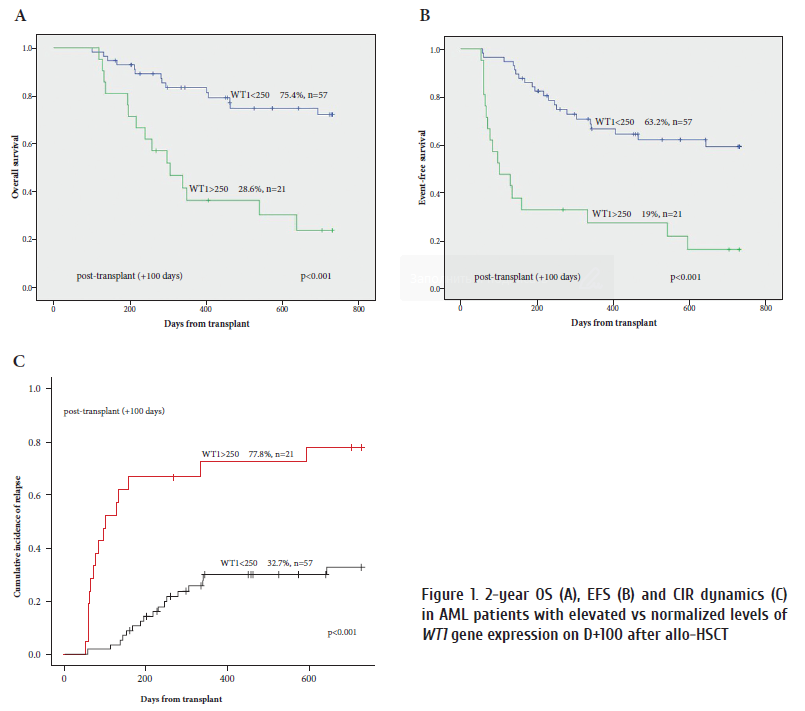
Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is now considered the best treatment of AML with poor prognosis, which is, however, often followed by posttransplant relapses (PTR). Among PTR, molecular and cytological variants (mPTR and cPTR, respectively) are recognized. The WT1 gene is known to be an independent prognostic indicator of the mass of blast cells producing it. The serial measurement of WT1 expression levels provides a real possibility for early diagnosis of mPTR and an evaluation of the overall and event-free survival (OS and EFS, respectively) and the cumulative frequency of relapse (CIR) in patients with AML treated with allo-HSCT.
Patients and methods
The study included 88 AML patients aged 2 to 68 (median, 30 y.o.) who underwent allo-HSCT at our University between 2011 and 2017. WT1 gene expression levels were serially measured by real-time quantitative PCR, and marrow blast counts were performed in marrow samples at the standard control time points: before transplantation (D0) and on days D+30, D+60 and D+100 after transplantation. The WT1 threshold value was selected, as based on the measurement of expression levels of WT1 gene in bone marrow aspirates of healthy donors and determined as 250 WT1 copies/104 copies of ABL gene. At all the time points, groups of patients with elevated and normalized levels of WT1 gene expression (> 250 copies and < 250 copies, respectively) were formed, which allowed for calculating the difference in the 2-year OS, EFS and CIR. Since the increase in the expression of the WT1 gene reflecting the content of the blasts secreting this gene can precede the morphologically identified cPTR, we measured this time interval for all the examined AML patients taking in consideration the posttransplantation
therapy.
Results
The levels of WT1 gene expression at allo-HSCT ranged from 0 to 56884 WT1/104 ABL copies (median – 253). According to the log-rank criteria, the difference in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression before allo-HSCT was as follows: 79.5%, 69.8%, 28.2% vs. 31.8%, 22.7% and 58.9%, at p<0.001, p<0.001, and p=0.0019, respectively. On D+30, we found no difference in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression. Significant differences in the 2-year OS and CIR in the two groups were found on D+60 (66.2% and 42.3% vs. 35.7% and 61.5% at p=0.012 and р=0.01, respectively), while there was still no significant difference in the EFS (52.3% vs. 38.5%, p=0.084). The greatest differences in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression occurred at the control time point D+100 (28.6%, 19% and 77.8% vs. 75.4% 63.2% and 32.7% at p<0.001, p<0.001, and p<0.001, respectively) (Fig.1). On the basis of proportional Cox risks, the independent positive effect on OS and EFS was preserved only for the normalized level of the WT1 gene expression (p=0.011 and p=0.041) at the time point D+100 after the allo-HSCT and in the presence of chronic GVHD (p=0.038 and p=0.03). In this case, the ratio of the risk of relapse (125) was maximal also on D+100. Concerning mPTR and cPTR, they were documented in 55/88 (62.5%) and 33/88 (37.5%) patients, respectively. In 33.3% of patients (11/33), mPTR and cPTR coincided in time, while in 22 cases cPTR occurred 13-321 (median – 35) days later than mPTR. According to the data obtained, this delay of cPTR from mPTR can be partially ascribed to the therapy performed at the clinic, in particular, donor lymphocyte infusions, and to presence of chronic GVHD in patients, thus being in good agreement with other research data [Pozzi et al, 2013].
Conclusion
Elevated and normalized levels of WT1 gene expression are convenient and clinically useful markers of molecularly controlled mPTR and remission of AML. The optimal point for measuring the level of WT1 gene expression in PTR diagnostics is D+100, followed by D0, D+60 and D+30, as the significance decreases. According to our data, the duration of OS and EFS is also positively affected by the presence of chronic GVHD in AML patients after allo-HSCT, which explains the tendency to use immunotherapy to treat mPTR diagnosed by serial measurements of the WT1 gene expression levels [Di Grazia et al, 2016].
Keywords
Allogeneic stem cell transplantation, acute myeloid leukemia, WT1, relapse, molecular monitoring.

Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is now considered the best treatment of AML with poor prognosis, which is, however, often followed by posttransplant relapses (PTR). Among PTR, molecular and cytological variants (mPTR and cPTR, respectively) are recognized. The WT1 gene is known to be an independent prognostic indicator of the mass of blast cells producing it. The serial measurement of WT1 expression levels provides a real possibility for early diagnosis of mPTR and an evaluation of the overall and event-free survival (OS and EFS, respectively) and the cumulative frequency of relapse (CIR) in patients with AML treated with allo-HSCT.
Patients and methods
The study included 88 AML patients aged 2 to 68 (median, 30 y.o.) who underwent allo-HSCT at our University between 2011 and 2017. WT1 gene expression levels were serially measured by real-time quantitative PCR, and marrow blast counts were performed in marrow samples at the standard control time points: before transplantation (D0) and on days D+30, D+60 and D+100 after transplantation. The WT1 threshold value was selected, as based on the measurement of expression levels of WT1 gene in bone marrow aspirates of healthy donors and determined as 250 WT1 copies/104 copies of ABL gene. At all the time points, groups of patients with elevated and normalized levels of WT1 gene expression (> 250 copies and < 250 copies, respectively) were formed, which allowed for calculating the difference in the 2-year OS, EFS and CIR. Since the increase in the expression of the WT1 gene reflecting the content of the blasts secreting this gene can precede the morphologically identified cPTR, we measured this time interval for all the examined AML patients taking in consideration the posttransplantation
therapy.
Results
The levels of WT1 gene expression at allo-HSCT ranged from 0 to 56884 WT1/104 ABL copies (median – 253). According to the log-rank criteria, the difference in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression before allo-HSCT was as follows: 79.5%, 69.8%, 28.2% vs. 31.8%, 22.7% and 58.9%, at p<0.001, p<0.001, and p=0.0019, respectively. On D+30, we found no difference in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression. Significant differences in the 2-year OS and CIR in the two groups were found on D+60 (66.2% and 42.3% vs. 35.7% and 61.5% at p=0.012 and р=0.01, respectively), while there was still no significant difference in the EFS (52.3% vs. 38.5%, p=0.084). The greatest differences in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression occurred at the control time point D+100 (28.6%, 19% and 77.8% vs. 75.4% 63.2% and 32.7% at p<0.001, p<0.001, and p<0.001, respectively) (Fig.1). On the basis of proportional Cox risks, the independent positive effect on OS and EFS was preserved only for the normalized level of the WT1 gene expression (p=0.011 and p=0.041) at the time point D+100 after the allo-HSCT and in the presence of chronic GVHD (p=0.038 and p=0.03). In this case, the ratio of the risk of relapse (125) was maximal also on D+100. Concerning mPTR and cPTR, they were documented in 55/88 (62.5%) and 33/88 (37.5%) patients, respectively. In 33.3% of patients (11/33), mPTR and cPTR coincided in time, while in 22 cases cPTR occurred 13-321 (median – 35) days later than mPTR. According to the data obtained, this delay of cPTR from mPTR can be partially ascribed to the therapy performed at the clinic, in particular, donor lymphocyte infusions, and to presence of chronic GVHD in patients, thus being in good agreement with other research data [Pozzi et al, 2013].
Conclusion
Elevated and normalized levels of WT1 gene expression are convenient and clinically useful markers of molecularly controlled mPTR and remission of AML. The optimal point for measuring the level of WT1 gene expression in PTR diagnostics is D+100, followed by D0, D+60 and D+30, as the significance decreases. According to our data, the duration of OS and EFS is also positively affected by the presence of chronic GVHD in AML patients after allo-HSCT, which explains the tendency to use immunotherapy to treat mPTR diagnosed by serial measurements of the WT1 gene expression levels [Di Grazia et al, 2016].
Keywords
Allogeneic stem cell transplantation, acute myeloid leukemia, WT1, relapse, molecular monitoring.

Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) в настоящее время считается лучшим методом лечения ОМЛ с плохим прогнозом, который часто сопровождается посттрансплантационными рецидивами (ПТР). Среди ПТР могут быть молекулярные и цитологические варианты (мПТР и цПТР соответственно). Известно, что уровень экспрессии гена WT1 является хорошим индикатором массы продуцирующих его бластных элементов. С помощью этого теста имеется возможность ранней диагностики мПТР и оценка общей и бессобытийной выживаемости (ОВ и БСВ соответственно) и кумулятивной частоты рецидивов (КЧР) больных ОМЛ, леченных с использованием алло-ТГСК.
Пациенты и методы
Исследование включало 88 пациентов с ОМЛ в возрасте от 2 до 68 лет (медиана – 30 лет), которым была выполнена алло-ТГСК в нашем Центре в период с 2011 по 2017 годы. Уровни экспрессии гена WT1 измеряли серийно количественной ПЦР в реальном времени, а содержание бластов в тех же аспиратах костного мозга определяли в стандартно выбранных контрольных временных точках: перед трансплантацией (Д0) и в дни Д+30, Д+60 и Д+100 после ее выполнения. Пороговый уровень экспрессии гена WT1 был определен на основании измерения уровня экспрессии гена WT1 в аспиратах костного мозга здоровых доноров и равнялся 250 копиям WT1/104 копий гена ABL. Во всех временных точках были сформированы группы больных с повышенным и нормализованным уровнями экспрессии гена WT1 (>250 копий <250 копий соответственно) и рассчитана разница в 2-летней ОВ, БСВ и КЧР. Поскольку повышение уровня экспрессии гена WT1, отражающее содержание секретирующих этот ген бластов, может опережать по времени определяемые морфологом цПТР, мы измерили этот временный интервал у всех обследованных больных ОМЛ и сопоставили его с проведенной посттрансплантационной терапией.
Результаты
Уровни экспрессии гена WT1 перед режимом кондиционирования варьировали от 0 до 56884 копий WT1/104 копий гена ABL (медиана – 253 копии). По данным критериям лог-ранга, существенная разница в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 перед алло-ТГСК выглядела следующим образом: 79,5%, 69,8% и 28,2% против 31,8%, 22,7% и 58,9%, при p<0,001, p<0,001 и p=0,0019 соответственно. Различий в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 на день Д+30 после выполнения алло-ТГСК не было. Достоверные различия в 2-летней ОВ и КЧР наблюдались между этими группами на день Д+60 после выполнения алло-ТГСК (66,2% и 42,3% против 35,7% и 61,5% при p=0,012 и р=0,01 соответственно), в то время как достоверные различия в БСВ отсутствовали (52,3% против 38,5%, р=0,084). Наибольшие различия в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 имели место в контрольной временной точке Д+100 после алло-ТГСК (28,6%, 19% и 77,8% против 75,4%, 63,2% и 32,7% при р<0,001, р<0,001 и р<0,001 соответственно) (Рис.1). На основе пропорциональных рисков Кокса, независимое позитивное влияние на ОВ и БСВ сохранилось только для нормализованного во временной точке Д+100 после выполнения алло-ТГСК уровня экспрессии гена WT1 (р=0,011 и р=0,041) и наличия у больных хрРТПХ (р=0,038 и р=0,03). При этом отношение риска рецидива (125) было максимальным также на день Д+100. По нашим данным, мПТР и цПТР были зарегистрированы у 55/88 (62,5%) и 33/88 (37,5%) пациентов соответственно. У 33,3% пациентов (11/33) мПТР и цПТР по времени появления совпадали, в то время как в 22 наблюдениях цПТР отставали от мПТР на 13-321 день (медиана – 35). Задержка цПТР от мПТР частично может быть объяснено проводимой в клинике терапией, в частности, инфузиями донорских лимфоцитов и наличием у больных хронической РТПХ, что хорошо согласуется с данными литературы [Pozzi et al, 2013].
Заключение
Уровень повышенной и нормализованной экспрессии гена WT1 является удобным и полезным для клиники маркером молекулярно контролируемых ПТР и ремиссий ОМЛ. Оптимальной временной точкой для измерения уровня экспрессии гена WT1 в диагностике ПТР является Д+100, за которой, по мере снижения значимости, следуют Д0, Д+60 и Д+30. По нашим данным наудлинение продолжительности ОВ и БСВ сказывается также наличие у больных ОМЛ признаков хрРТПХ, что объясняется наметившуюся в клинике тенденцию лечить иммунотерапией диагностированные при серийном измерении уровни экспрессии гена WT1 мПТР [Di Grazia et al, 2016].
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, острый миелоидный лейкоз, WT1, рецидив, молекулярный мониторинг.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(8497) "Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) в настоящее время считается лучшим методом лечения ОМЛ с плохим прогнозом, который часто сопровождается посттрансплантационными рецидивами (ПТР). Среди ПТР могут быть молекулярные и цитологические варианты (мПТР и цПТР соответственно). Известно, что уровень экспрессии гена WT1 является хорошим индикатором массы продуцирующих его бластных элементов. С помощью этого теста имеется возможность ранней диагностики мПТР и оценка общей и бессобытийной выживаемости (ОВ и БСВ соответственно) и кумулятивной частоты рецидивов (КЧР) больных ОМЛ, леченных с использованием алло-ТГСК.
Пациенты и методы
Исследование включало 88 пациентов с ОМЛ в возрасте от 2 до 68 лет (медиана – 30 лет), которым была выполнена алло-ТГСК в нашем Центре в период с 2011 по 2017 годы. Уровни экспрессии гена WT1 измеряли серийно количественной ПЦР в реальном времени, а содержание бластов в тех же аспиратах костного мозга определяли в стандартно выбранных контрольных временных точках: перед трансплантацией (Д0) и в дни Д+30, Д+60 и Д+100 после ее выполнения. Пороговый уровень экспрессии гена WT1 был определен на основании измерения уровня экспрессии гена WT1 в аспиратах костного мозга здоровых доноров и равнялся 250 копиям WT1/104 копий гена ABL. Во всех временных точках были сформированы группы больных с повышенным и нормализованным уровнями экспрессии гена WT1 (>250 копий <250 копий соответственно) и рассчитана разница в 2-летней ОВ, БСВ и КЧР. Поскольку повышение уровня экспрессии гена WT1, отражающее содержание секретирующих этот ген бластов, может опережать по времени определяемые морфологом цПТР, мы измерили этот временный интервал у всех обследованных больных ОМЛ и сопоставили его с проведенной посттрансплантационной терапией.
Результаты
Уровни экспрессии гена WT1 перед режимом кондиционирования варьировали от 0 до 56884 копий WT1/104 копий гена ABL (медиана – 253 копии). По данным критериям лог-ранга, существенная разница в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 перед алло-ТГСК выглядела следующим образом: 79,5%, 69,8% и 28,2% против 31,8%, 22,7% и 58,9%, при p<0,001, p<0,001 и p=0,0019 соответственно. Различий в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 на день Д+30 после выполнения алло-ТГСК не было. Достоверные различия в 2-летней ОВ и КЧР наблюдались между этими группами на день Д+60 после выполнения алло-ТГСК (66,2% и 42,3% против 35,7% и 61,5% при p=0,012 и р=0,01 соответственно), в то время как достоверные различия в БСВ отсутствовали (52,3% против 38,5%, р=0,084). Наибольшие различия в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 имели место в контрольной временной точке Д+100 после алло-ТГСК (28,6%, 19% и 77,8% против 75,4%, 63,2% и 32,7% при р<0,001, р<0,001 и р<0,001 соответственно) (Рис.1). На основе пропорциональных рисков Кокса, независимое позитивное влияние на ОВ и БСВ сохранилось только для нормализованного во временной точке Д+100 после выполнения алло-ТГСК уровня экспрессии гена WT1 (р=0,011 и р=0,041) и наличия у больных хрРТПХ (р=0,038 и р=0,03). При этом отношение риска рецидива (125) было максимальным также на день Д+100. По нашим данным, мПТР и цПТР были зарегистрированы у 55/88 (62,5%) и 33/88 (37,5%) пациентов соответственно. У 33,3% пациентов (11/33) мПТР и цПТР по времени появления совпадали, в то время как в 22 наблюдениях цПТР отставали от мПТР на 13-321 день (медиана – 35). Задержка цПТР от мПТР частично может быть объяснено проводимой в клинике терапией, в частности, инфузиями донорских лимфоцитов и наличием у больных хронической РТПХ, что хорошо согласуется с данными литературы [Pozzi et al, 2013].
Заключение
Уровень повышенной и нормализованной экспрессии гена WT1 является удобным и полезным для клиники маркером молекулярно контролируемых ПТР и ремиссий ОМЛ. Оптимальной временной точкой для измерения уровня экспрессии гена WT1 в диагностике ПТР является Д+100, за которой, по мере снижения значимости, следуют Д0, Д+60 и Д+30. По нашим данным наудлинение продолжительности ОВ и БСВ сказывается также наличие у больных ОМЛ признаков хрРТПХ, что объясняется наметившуюся в клинике тенденцию лечить иммунотерапией диагностированные при серийном измерении уровни экспрессии гена WT1 мПТР [Di Grazia et al, 2016].
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, острый миелоидный лейкоз, WT1, рецидив, молекулярный мониторинг.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20453" ["VALUE"]=> array(2) { ["TEXT"]=> string(406) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(406) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(406) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия" } } } [6]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1570" ["~ID"]=> string(4) "1570" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(168) "Опыт применения гипометилирующих препаратов при аллогенной трансплантации костного мозга" ["~NAME"]=> string(168) "Опыт применения гипометилирующих препаратов при аллогенной трансплантации костного мозга" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:34:02" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:34:02" ["DETAIL_PAGE_URL"]=> string(145) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/opyt-primeneniya-gipometiliruyushchikh-preparatov-pri-allogennoy-transplantatsii-kostnogo-mozga/" ["~DETAIL_PAGE_URL"]=> string(145) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/opyt-primeneniya-gipometiliruyushchikh-preparatov-pri-allogennoy-transplantatsii-kostnogo-mozga/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(95) "opyt-primeneniya-gipometiliruyushchikh-preparatov-pri-allogennoy-transplantatsii-kostnogo-mozga" ["~CODE"]=> string(95) "opyt-primeneniya-gipometiliruyushchikh-preparatov-pri-allogennoy-transplantatsii-kostnogo-mozga" ["EXTERNAL_ID"]=> string(4) "1570" ["~EXTERNAL_ID"]=> string(4) "1570" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(168) "Опыт применения гипометилирующих препаратов при аллогенной трансплантации костного мозга" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(270) "Опыт применения гипометилирующих препаратов при аллогенной трансплантации костного мозгаExperience with hypomethylating drug application in allogeneic hematopoietic stem cell transplantation" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(10544) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелобластным лейкозом (ОМЛ) высокого риска. Тем не менее, рецидив заболевания развивается у 40-70% пациентов в течение первого года после трансплантации, а достижение повторных ремиссий возможно лишь у 15-30% больных. Гипометилирующая (эпигенетическая) терапия представляется перспективным подходом у этой категории больных. Механизм действия гипометилирующих препаратов заключается в их способности увеличивать уровень регуляторных Т-клеток (Тregs, CD4+CD25+FOXP3+), которые играют ключевую роль в развитии иммунологической толерантности в посттрансплантационном периоде, снижая степень развития и выраженности реакции «трансплантат против хозяина» (РТПХ). Кроме того, отмечено стимулирующее действие этих препаратов на пул цитотоксических CD8+ Т-лимфоцитов, обеспечивающих реализацию опухолеспецифического ответа в реакции «трансплантат против лейкоза» (РТПЛ). </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель исследования состояла в оценке результатов применения азацитидина после алло-ТГСК у пациентов с ОМЛ. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В 2015-2018 гг. в клинике Федерального государственного бюджетного учреждения науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства» (КНИИГиПК) выполнено 20 алло-ТГСК пациентам с ОМЛ. Из них 18 – взрослым пациентам (14 женщин и 4 мужчин) и 2 – детям. Миелоаблативный режим кондиционирования использовался в 5 (25%) случаях, в 15 (75%) – режим со сниженной интенсивностью. Родственная алло-ТГСК выполнена 15 (75%) пациентам, из них гаплоидентичная – 4, неродственная от полностью совместимого донора – 5. Из 20 больных, на момент оценки живы 9 (45%). 11 (55%) пациентов погибли в разные сроки после алло-ТГСК: причинами смерти являлись тяжелые инфекционные осложнения, тяжелая острая реакция трансплантат против хозяина, тромботическая микроангиопатия, ранний рецидив заболевания. Курсы азацитидина с профилактической целью получили 7 пациентов с ОМЛ высокого риска. Из них 6 женщин и 1 мужчина, с медианой возраста 36,7 лет (диапазон: 20-50 лет). Терапию азацитидином начинали после восстановления кроветворения в среднем на Д+85 (диапазон: 40–121 день), при отсутствии тяжелых инфекционных и других осложнений. Препарат назначали по схеме 35 мг/м2 подкожно в течение 5-7 суток, каждые 28 дней, медиана 8 курсов. В 3 случаях азацитидин комбинировали с инфузией донорских лимфоцитов (DLI – donor lymphocyte infusion). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Все больные, получавшие азацитидин, на момент исследования живы. У 6 из них сохраняется ремиссия заболевания. Перед назначением азацитидина полное донорское кроветворение имели 2 пациента, у 1 полный донорский химеризм достигнут через 2 месяца терапии, у 4 отмечался смешанный донорский химеризм. У 1 из них возник поздний рецидив заболевания после 3 курсов азацитидина, в настоящее время он получает противорецидивную химиотерапию (ХТ). </p> <h2 style="text-align: justify;">Клинический случай</h2> <p style="text-align: justify;"> Пациентка Т., 22 лет, ОМЛ, t(8;21), ПР 3 неродственная аллоТГСК выполнена в марте 2016 г. Интервал от начала лечения до аллоТГСК составил 27 мес. Профилактическое введение азацитидина начато на +56 день после аллоТГСК в дозе 35 мг\м2 каждые 5 дней 28 дневного цикла №6, терапия закончена в октябре 2016 г. Мониторинг общего и линейного химеризма проводился в дни +30, +56, +84, +119, +147, +174 и +360 и показал наличие стойкого полного донорского кроветворения. Ремиссия заболевания подтверждена результатами миелограммы. Однако, на Д+414 выявлен поздний рецидив-3 заболевания (в миелограмме 30% бластов), снижение общего донорского химеризма (41,3% собственных клеток). С целью достижения ремиссии – 4 проведен курс FLAG с DLI. Восстановление лейкоцитов отмечалось на +25 сутки после ХТ. Достижение ремиссии-4 подтверждено результатами миелограммы, молекулярным исследованием. С июня по июль 2017 г. проведено два 5-дневных курса азацитидина 75 мг/м2 с DLI в возрастающей дозе, после чего достигнут полный донорский химеризм. В течение последующего года пациентка получила суммарно 12 курсов азацитидина 75 мг/м2 с эскалацией дозы донорских лимфоцитов. У больной сохраняется полная клинико-гематологическая и молекулярная ремиссия заболевания. Планируется продолжить профилактическое введение донорских лимфоцитов в монорежиме. Учитывая небольшую группу пациентов (7 человек), оценка эффективности терапии азацитидином преждевременна. Медиана наблюдения составила 408 дней. Наиболее частыми нежелательными явлениями при применении азацитидина были периферические цитопении 1 степени, не требующие отмены препарата или коррекции дозы. Среди негематологических побочных эффектов отмечались реакции в месте инъекции, тошнота, диарея и слабость, в большинстве случаев не выходившие за пределы I-II степени токсичности. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Принимая во внимание положительный опыт применения препарата у пациентов с ОМЛ высокого риска после алло-ТГСК, терапия азацитидином представляется перспективной опцией как для профилактики рецидивов, так и в целях достижения повторных ремиссий заболевания. Для оценки влияния азацитидина, в том числе в сочетании с DLI, на безрецидивную и общую выживаемость требуется дальнейшее накопление клинического опыта. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый миелобластный лейкоз, аллогенная трансплантация гемопоэтических стволовых клеток, азацитидин, химеризм, инфузия донорских лимфоцитов. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(168) "Опыт применения гипометилирующих препаратов при аллогенной трансплантации костного мозга" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(168) "Опыт применения гипометилирующих препаратов при аллогенной трансплантации костного мозга" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(168) "Опыт применения гипометилирующих препаратов при аллогенной трансплантации костного мозга" ["SECTION_META_TITLE"]=> string(168) "Опыт применения гипометилирующих препаратов при аллогенной трансплантации костного мозга" ["SECTION_META_KEYWORDS"]=> string(168) "Опыт применения гипометилирующих препаратов при аллогенной трансплантации костного мозга" ["SECTION_META_DESCRIPTION"]=> string(168) "Опыт применения гипометилирующих препаратов при аллогенной трансплантации костного мозга" ["SECTION_PICTURE_FILE_ALT"]=> string(168) "Опыт применения гипометилирующих препаратов при аллогенной трансплантации костного мозга" ["SECTION_PICTURE_FILE_TITLE"]=> string(168) "Опыт применения гипометилирующих препаратов при аллогенной трансплантации костного мозга" ["SECTION_PICTURE_FILE_NAME"]=> string(99) "opyt-primeneniya-gipometiliruyushchikh-preparatov-pri-allogennoy-transplantatsii-kostnogo-mozga-img" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(168) "Опыт применения гипометилирующих препаратов при аллогенной трансплантации костного мозга" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(168) "Опыт применения гипометилирующих препаратов при аллогенной трансплантации костного мозга" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(99) "opyt-primeneniya-gipometiliruyushchikh-preparatov-pri-allogennoy-transplantatsii-kostnogo-mozga-img" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(99) "opyt-primeneniya-gipometiliruyushchikh-preparatov-pri-allogennoy-transplantatsii-kostnogo-mozga-img" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(99) "opyt-primeneniya-gipometiliruyushchikh-preparatov-pri-allogennoy-transplantatsii-kostnogo-mozga-img" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20466" ["VALUE"]=> array(2) { ["TEXT"]=> string(210) "Марина Н. Хоробрых, Наталья В. Минаева, Наталья А. Зорина, Екатерина Н. Зотина, Светлана В. Самарина, Елена Л. Назарова" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(210) "Марина Н. Хоробрых, Наталья В. Минаева, Наталья А. Зорина, Екатерина Н. Зотина, Светлана В. Самарина, Елена Л. Назарова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20467" ["VALUE"]=> array(2) { ["TEXT"]=> string(364) "Федеральное государственное бюджетное учреждение науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства», Киров, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(364) "Федеральное государственное бюджетное учреждение науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства», Киров, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20468" ["VALUE"]=> array(2) { ["TEXT"]=> string(10544) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелобластным лейкозом (ОМЛ) высокого риска. Тем не менее, рецидив заболевания развивается у 40-70% пациентов в течение первого года после трансплантации, а достижение повторных ремиссий возможно лишь у 15-30% больных. Гипометилирующая (эпигенетическая) терапия представляется перспективным подходом у этой категории больных. Механизм действия гипометилирующих препаратов заключается в их способности увеличивать уровень регуляторных Т-клеток (Тregs, CD4+CD25+FOXP3+), которые играют ключевую роль в развитии иммунологической толерантности в посттрансплантационном периоде, снижая степень развития и выраженности реакции «трансплантат против хозяина» (РТПХ). Кроме того, отмечено стимулирующее действие этих препаратов на пул цитотоксических CD8+ Т-лимфоцитов, обеспечивающих реализацию опухолеспецифического ответа в реакции «трансплантат против лейкоза» (РТПЛ). </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель исследования состояла в оценке результатов применения азацитидина после алло-ТГСК у пациентов с ОМЛ. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В 2015-2018 гг. в клинике Федерального государственного бюджетного учреждения науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства» (КНИИГиПК) выполнено 20 алло-ТГСК пациентам с ОМЛ. Из них 18 – взрослым пациентам (14 женщин и 4 мужчин) и 2 – детям. Миелоаблативный режим кондиционирования использовался в 5 (25%) случаях, в 15 (75%) – режим со сниженной интенсивностью. Родственная алло-ТГСК выполнена 15 (75%) пациентам, из них гаплоидентичная – 4, неродственная от полностью совместимого донора – 5. Из 20 больных, на момент оценки живы 9 (45%). 11 (55%) пациентов погибли в разные сроки после алло-ТГСК: причинами смерти являлись тяжелые инфекционные осложнения, тяжелая острая реакция трансплантат против хозяина, тромботическая микроангиопатия, ранний рецидив заболевания. Курсы азацитидина с профилактической целью получили 7 пациентов с ОМЛ высокого риска. Из них 6 женщин и 1 мужчина, с медианой возраста 36,7 лет (диапазон: 20-50 лет). Терапию азацитидином начинали после восстановления кроветворения в среднем на Д+85 (диапазон: 40–121 день), при отсутствии тяжелых инфекционных и других осложнений. Препарат назначали по схеме 35 мг/м2 подкожно в течение 5-7 суток, каждые 28 дней, медиана 8 курсов. В 3 случаях азацитидин комбинировали с инфузией донорских лимфоцитов (DLI – donor lymphocyte infusion). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Все больные, получавшие азацитидин, на момент исследования живы. У 6 из них сохраняется ремиссия заболевания. Перед назначением азацитидина полное донорское кроветворение имели 2 пациента, у 1 полный донорский химеризм достигнут через 2 месяца терапии, у 4 отмечался смешанный донорский химеризм. У 1 из них возник поздний рецидив заболевания после 3 курсов азацитидина, в настоящее время он получает противорецидивную химиотерапию (ХТ). </p> <h2 style="text-align: justify;">Клинический случай</h2> <p style="text-align: justify;"> Пациентка Т., 22 лет, ОМЛ, t(8;21), ПР 3 неродственная аллоТГСК выполнена в марте 2016 г. Интервал от начала лечения до аллоТГСК составил 27 мес. Профилактическое введение азацитидина начато на +56 день после аллоТГСК в дозе 35 мг\м2 каждые 5 дней 28 дневного цикла №6, терапия закончена в октябре 2016 г. Мониторинг общего и линейного химеризма проводился в дни +30, +56, +84, +119, +147, +174 и +360 и показал наличие стойкого полного донорского кроветворения. Ремиссия заболевания подтверждена результатами миелограммы. Однако, на Д+414 выявлен поздний рецидив-3 заболевания (в миелограмме 30% бластов), снижение общего донорского химеризма (41,3% собственных клеток). С целью достижения ремиссии – 4 проведен курс FLAG с DLI. Восстановление лейкоцитов отмечалось на +25 сутки после ХТ. Достижение ремиссии-4 подтверждено результатами миелограммы, молекулярным исследованием. С июня по июль 2017 г. проведено два 5-дневных курса азацитидина 75 мг/м2 с DLI в возрастающей дозе, после чего достигнут полный донорский химеризм. В течение последующего года пациентка получила суммарно 12 курсов азацитидина 75 мг/м2 с эскалацией дозы донорских лимфоцитов. У больной сохраняется полная клинико-гематологическая и молекулярная ремиссия заболевания. Планируется продолжить профилактическое введение донорских лимфоцитов в монорежиме. Учитывая небольшую группу пациентов (7 человек), оценка эффективности терапии азацитидином преждевременна. Медиана наблюдения составила 408 дней. Наиболее частыми нежелательными явлениями при применении азацитидина были периферические цитопении 1 степени, не требующие отмены препарата или коррекции дозы. Среди негематологических побочных эффектов отмечались реакции в месте инъекции, тошнота, диарея и слабость, в большинстве случаев не выходившие за пределы I-II степени токсичности. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Принимая во внимание положительный опыт применения препарата у пациентов с ОМЛ высокого риска после алло-ТГСК, терапия азацитидином представляется перспективной опцией как для профилактики рецидивов, так и в целях достижения повторных ремиссий заболевания. Для оценки влияния азацитидина, в том числе в сочетании с DLI, на безрецидивную и общую выживаемость требуется дальнейшее накопление клинического опыта. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый миелобластный лейкоз, аллогенная трансплантация гемопоэтических стволовых клеток, азацитидин, химеризм, инфузия донорских лимфоцитов. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(10236) "Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелобластным лейкозом (ОМЛ) высокого риска. Тем не менее, рецидив заболевания развивается у 40-70% пациентов в течение первого года после трансплантации, а достижение повторных ремиссий возможно лишь у 15-30% больных. Гипометилирующая (эпигенетическая) терапия представляется перспективным подходом у этой категории больных. Механизм действия гипометилирующих препаратов заключается в их способности увеличивать уровень регуляторных Т-клеток (Тregs, CD4+CD25+FOXP3+), которые играют ключевую роль в развитии иммунологической толерантности в посттрансплантационном периоде, снижая степень развития и выраженности реакции «трансплантат против хозяина» (РТПХ). Кроме того, отмечено стимулирующее действие этих препаратов на пул цитотоксических CD8+ Т-лимфоцитов, обеспечивающих реализацию опухолеспецифического ответа в реакции «трансплантат против лейкоза» (РТПЛ).
Цель
Цель исследования состояла в оценке результатов применения азацитидина после алло-ТГСК у пациентов с ОМЛ.
Пациенты и методы
В 2015-2018 гг. в клинике Федерального государственного бюджетного учреждения науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства» (КНИИГиПК) выполнено 20 алло-ТГСК пациентам с ОМЛ. Из них 18 – взрослым пациентам (14 женщин и 4 мужчин) и 2 – детям. Миелоаблативный режим кондиционирования использовался в 5 (25%) случаях, в 15 (75%) – режим со сниженной интенсивностью. Родственная алло-ТГСК выполнена 15 (75%) пациентам, из них гаплоидентичная – 4, неродственная от полностью совместимого донора – 5. Из 20 больных, на момент оценки живы 9 (45%). 11 (55%) пациентов погибли в разные сроки после алло-ТГСК: причинами смерти являлись тяжелые инфекционные осложнения, тяжелая острая реакция трансплантат против хозяина, тромботическая микроангиопатия, ранний рецидив заболевания. Курсы азацитидина с профилактической целью получили 7 пациентов с ОМЛ высокого риска. Из них 6 женщин и 1 мужчина, с медианой возраста 36,7 лет (диапазон: 20-50 лет). Терапию азацитидином начинали после восстановления кроветворения в среднем на Д+85 (диапазон: 40–121 день), при отсутствии тяжелых инфекционных и других осложнений. Препарат назначали по схеме 35 мг/м2 подкожно в течение 5-7 суток, каждые 28 дней, медиана 8 курсов. В 3 случаях азацитидин комбинировали с инфузией донорских лимфоцитов (DLI – donor lymphocyte infusion).
Результаты
Все больные, получавшие азацитидин, на момент исследования живы. У 6 из них сохраняется ремиссия заболевания. Перед назначением азацитидина полное донорское кроветворение имели 2 пациента, у 1 полный донорский химеризм достигнут через 2 месяца терапии, у 4 отмечался смешанный донорский химеризм. У 1 из них возник поздний рецидив заболевания после 3 курсов азацитидина, в настоящее время он получает противорецидивную химиотерапию (ХТ).
Клинический случай
Пациентка Т., 22 лет, ОМЛ, t(8;21), ПР 3 неродственная аллоТГСК выполнена в марте 2016 г. Интервал от начала лечения до аллоТГСК составил 27 мес. Профилактическое введение азацитидина начато на +56 день после аллоТГСК в дозе 35 мг\м2 каждые 5 дней 28 дневного цикла №6, терапия закончена в октябре 2016 г. Мониторинг общего и линейного химеризма проводился в дни +30, +56, +84, +119, +147, +174 и +360 и показал наличие стойкого полного донорского кроветворения. Ремиссия заболевания подтверждена результатами миелограммы. Однако, на Д+414 выявлен поздний рецидив-3 заболевания (в миелограмме 30% бластов), снижение общего донорского химеризма (41,3% собственных клеток). С целью достижения ремиссии – 4 проведен курс FLAG с DLI. Восстановление лейкоцитов отмечалось на +25 сутки после ХТ. Достижение ремиссии-4 подтверждено результатами миелограммы, молекулярным исследованием. С июня по июль 2017 г. проведено два 5-дневных курса азацитидина 75 мг/м2 с DLI в возрастающей дозе, после чего достигнут полный донорский химеризм. В течение последующего года пациентка получила суммарно 12 курсов азацитидина 75 мг/м2 с эскалацией дозы донорских лимфоцитов. У больной сохраняется полная клинико-гематологическая и молекулярная ремиссия заболевания. Планируется продолжить профилактическое введение донорских лимфоцитов в монорежиме. Учитывая небольшую группу пациентов (7 человек), оценка эффективности терапии азацитидином преждевременна. Медиана наблюдения составила 408 дней. Наиболее частыми нежелательными явлениями при применении азацитидина были периферические цитопении 1 степени, не требующие отмены препарата или коррекции дозы. Среди негематологических побочных эффектов отмечались реакции в месте инъекции, тошнота, диарея и слабость, в большинстве случаев не выходившие за пределы I-II степени токсичности.
Заключение
Принимая во внимание положительный опыт применения препарата у пациентов с ОМЛ высокого риска после алло-ТГСК, терапия азацитидином представляется перспективной опцией как для профилактики рецидивов, так и в целях достижения повторных ремиссий заболевания. Для оценки влияния азацитидина, в том числе в сочетании с DLI, на безрецидивную и общую выживаемость требуется дальнейшее накопление клинического опыта.
Ключевые слова
Острый миелобластный лейкоз, аллогенная трансплантация гемопоэтических стволовых клеток, азацитидин, химеризм, инфузия донорских лимфоцитов.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20469" ["VALUE"]=> array(2) { ["TEXT"]=> string(120) "Marina N. Horobrykh, Natalia V. Minaeva, Natalia A. Zorina, Ekaterina N. Zotina, Svetlana V. Samarina, Elena L. Nazarova" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(120) "Marina N. Horobrykh, Natalia V. Minaeva, Natalia A. Zorina, Ekaterina N. Zotina, Svetlana V. Samarina, Elena L. Nazarova" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20470" ["VALUE"]=> array(2) { ["TEXT"]=> string(87) "Kirov Research Institute of Hematology and Blood Transfusion, Kirov, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(87) "Kirov Research Institute of Hematology and Blood Transfusion, Kirov, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20471" ["VALUE"]=> array(2) { ["TEXT"]=> string(6366) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is an effective treatment method in patients with high-risk acute myeloid leukemia (AML). Nevertheless, disease relapse develops in 40-70% of patients during the first posttransplant year, and achievement of repeated remissions is possible only in 15-30% of patients. Hypomethylating, or epigenetic therapy (HM) appears to be a promising approach to these patients. The mechanism of HM drug action includes their ability to increase the levels of regulatory T-cells (Тregs, CD4+CD25+FOXP3+), which play a key role in the development of immunological tolerance in the post-transplant period, reducing the degree of development and severity of “graft-versus-host disease” (GVHD). In addition, the stimulating effect of these drugs on the pool of cytotoxic CD8+T-lymphocytes provides implementation of a tumor-specific response in the graft-versus-leukemia (GVL) effect. </p> <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> Objective of this study was to evaluate the results of the azacitidine application after allo-HSCT in patients with AML. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Twenty patients with AML were transplanted between 2015 and 2018 at the Federal State Institute of Science “Kirov Research Institute of Hematology and Blood Transfusion of the Federal Medical and Biological Agency of Russia” including 18 adult patients (14 women and 4 men) and 2 children. Myeloablative conditioning was used in 5 (25%) cases. In 15 (75%) patients, the reduced intensity regimen was applied. Related allo-HSCT was performed in 15 (75%) patients, 4 of them were transplanted from HLA-haploidentical donors. Unrelated allo-HSCT was carried out from fully matched donors in 5 cases. Out of 20 patients, 9 (45%) patients were alive at the time of evaluation. Eleven (55%) patients died at different times after alloHSCT due to severe infectious complications, severe acute GVHD, thrombotic microangiopathy, early relapse of the disease. Preventive azacitidine courses were given to 7 patients with high-risk AML. Of these, 6 women and 1 man, with a median age of 36.7 years (range: 20-50 years). Azacitidine therapy was started after hematopoietic recovery on the average at day +85 (range: 40-121 days) in the absence of severe infectious and other complications. The drug was administered according to the scheme: 35 mg/m2 subcutaneously for 5-7 days, every 28 days, with a median of 8 courses. In 3 cases, azacitidine was combined with donor lymphocyte infusions (DLI). </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> All the patients who received azacitidine at the time of the study are alive. Six of them have a disease remission. Prior to the azacitidine administration, 2 patients had complete donor hematopoiesis, in 1 complete donor chimerism was achieved in 2 months of therapy, in 4 there was a mixed donor chimerism. In 1 of them, a late relapse occurred after 3 courses of azacitidine, and now he receives antirelapse chemotherapy (ChT). </p> <h2 style="text-align: justify;">Clinical case</h2> <p style="text-align: justify;"> Patient T., female, 22 years old, AML, t(8;21), complete remission-3, unrelated allo-HSCT was performed in March 2016. The interval from treatment initiation to allo-HSCT was 27 months. The azacitidine prophylactic administration was started at day +56 after allo-HSCT at a dose of 35mg/m2 every 5 days of the 28-day cycle, for up to 6 cycles, and the therapy was completed in October 2016. Monitoring of general and lineage-specific chimerism was carried out at days +30, +56, +84, +119, +147, +174 and +360 and showed the presence of strong complete donor hematopoiesis. The disease remission is confirmed by the bone marrow evaluation. However, a late relapse-3 of the disease was shown at day +414 (30% of blast cells in the bone marrow), along with decrease in complete donor chimerism (41.3% of its own cells). In order to achieve remission-4, a course of FLAG with DLI was conducted. Recovery of leukocytes was observed at day +25 after ChT. Achievement of remission-4 was confirmed by the bone marrow evaluation and molecular assays. From June to July 2017, two 5-day courses of azacitidine 75 mg/m2 with DLI at an increasing dose were carried out, followed by achievement of complete donor chimerism. Over the following year, the patient received a total of 12 azacitidine courses (75 mg/m2), with escalated dose of donor lymphocytes. The patient retains a complete clinical, hematological and molecular remission of the disease. It is planned to continue prophylactic donor lymphocytes administration as a monotherapy. Given the small group of patients (7 people), it is premature to evaluate efficiency of azacitidine therapy. The median follow-up was 408 days. Peripheral cytopenia (grade 1) was the most frequent adverse event of azacitidine treatment, which did not require drug withdrawal or dose adjustment. Among non-hematological side effects, we observed reactions at the injection site, nausea, diarrhea and weakness, in most cases not exceeding I-II degree of toxicity. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Taking into account the positive experience with azacitidine usage in the patients with high-risk AML after allo-HSCT, this therapy appears to be a promising option both for relapse prevention and for achievement of repeated disease remissions. To assess azacitidine influence upon relapse-free and overall survival, including its combination with DLI, further accumulation of clinical experience is required. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Acute myeloid leukemia, allogeneic hematopoietic stem cell transplantation, azacitidine, chimerism, donor lymphocyte infusion. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6058) "Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is an effective treatment method in patients with high-risk acute myeloid leukemia (AML). Nevertheless, disease relapse develops in 40-70% of patients during the first posttransplant year, and achievement of repeated remissions is possible only in 15-30% of patients. Hypomethylating, or epigenetic therapy (HM) appears to be a promising approach to these patients. The mechanism of HM drug action includes their ability to increase the levels of regulatory T-cells (Тregs, CD4+CD25+FOXP3+), which play a key role in the development of immunological tolerance in the post-transplant period, reducing the degree of development and severity of “graft-versus-host disease” (GVHD). In addition, the stimulating effect of these drugs on the pool of cytotoxic CD8+T-lymphocytes provides implementation of a tumor-specific response in the graft-versus-leukemia (GVL) effect.
Aim
Objective of this study was to evaluate the results of the azacitidine application after allo-HSCT in patients with AML.
Patients and methods
Twenty patients with AML were transplanted between 2015 and 2018 at the Federal State Institute of Science “Kirov Research Institute of Hematology and Blood Transfusion of the Federal Medical and Biological Agency of Russia” including 18 adult patients (14 women and 4 men) and 2 children. Myeloablative conditioning was used in 5 (25%) cases. In 15 (75%) patients, the reduced intensity regimen was applied. Related allo-HSCT was performed in 15 (75%) patients, 4 of them were transplanted from HLA-haploidentical donors. Unrelated allo-HSCT was carried out from fully matched donors in 5 cases. Out of 20 patients, 9 (45%) patients were alive at the time of evaluation. Eleven (55%) patients died at different times after alloHSCT due to severe infectious complications, severe acute GVHD, thrombotic microangiopathy, early relapse of the disease. Preventive azacitidine courses were given to 7 patients with high-risk AML. Of these, 6 women and 1 man, with a median age of 36.7 years (range: 20-50 years). Azacitidine therapy was started after hematopoietic recovery on the average at day +85 (range: 40-121 days) in the absence of severe infectious and other complications. The drug was administered according to the scheme: 35 mg/m2 subcutaneously for 5-7 days, every 28 days, with a median of 8 courses. In 3 cases, azacitidine was combined with donor lymphocyte infusions (DLI).
Results
All the patients who received azacitidine at the time of the study are alive. Six of them have a disease remission. Prior to the azacitidine administration, 2 patients had complete donor hematopoiesis, in 1 complete donor chimerism was achieved in 2 months of therapy, in 4 there was a mixed donor chimerism. In 1 of them, a late relapse occurred after 3 courses of azacitidine, and now he receives antirelapse chemotherapy (ChT).
Clinical case
Patient T., female, 22 years old, AML, t(8;21), complete remission-3, unrelated allo-HSCT was performed in March 2016. The interval from treatment initiation to allo-HSCT was 27 months. The azacitidine prophylactic administration was started at day +56 after allo-HSCT at a dose of 35mg/m2 every 5 days of the 28-day cycle, for up to 6 cycles, and the therapy was completed in October 2016. Monitoring of general and lineage-specific chimerism was carried out at days +30, +56, +84, +119, +147, +174 and +360 and showed the presence of strong complete donor hematopoiesis. The disease remission is confirmed by the bone marrow evaluation. However, a late relapse-3 of the disease was shown at day +414 (30% of blast cells in the bone marrow), along with decrease in complete donor chimerism (41.3% of its own cells). In order to achieve remission-4, a course of FLAG with DLI was conducted. Recovery of leukocytes was observed at day +25 after ChT. Achievement of remission-4 was confirmed by the bone marrow evaluation and molecular assays. From June to July 2017, two 5-day courses of azacitidine 75 mg/m2 with DLI at an increasing dose were carried out, followed by achievement of complete donor chimerism. Over the following year, the patient received a total of 12 azacitidine courses (75 mg/m2), with escalated dose of donor lymphocytes. The patient retains a complete clinical, hematological and molecular remission of the disease. It is planned to continue prophylactic donor lymphocytes administration as a monotherapy. Given the small group of patients (7 people), it is premature to evaluate efficiency of azacitidine therapy. The median follow-up was 408 days. Peripheral cytopenia (grade 1) was the most frequent adverse event of azacitidine treatment, which did not require drug withdrawal or dose adjustment. Among non-hematological side effects, we observed reactions at the injection site, nausea, diarrhea and weakness, in most cases not exceeding I-II degree of toxicity.
Conclusion
Taking into account the positive experience with azacitidine usage in the patients with high-risk AML after allo-HSCT, this therapy appears to be a promising option both for relapse prevention and for achievement of repeated disease remissions. To assess azacitidine influence upon relapse-free and overall survival, including its combination with DLI, further accumulation of clinical experience is required.
Keywords
Acute myeloid leukemia, allogeneic hematopoietic stem cell transplantation, azacitidine, chimerism, donor lymphocyte infusion.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20472" ["VALUE"]=> string(102) "Experience with hypomethylating drug application in allogeneic hematopoietic stem cell transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(102) "Experience with hypomethylating drug application in allogeneic hematopoietic stem cell transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20473" ["VALUE"]=> string(4) "1409" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1409" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20474" ["VALUE"]=> string(4) "1410" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1410" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20469" ["VALUE"]=> array(2) { ["TEXT"]=> string(120) "Marina N. Horobrykh, Natalia V. Minaeva, Natalia A. Zorina, Ekaterina N. Zotina, Svetlana V. Samarina, Elena L. Nazarova" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(120) "Marina N. Horobrykh, Natalia V. Minaeva, Natalia A. Zorina, Ekaterina N. Zotina, Svetlana V. Samarina, Elena L. Nazarova" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(120) "Marina N. Horobrykh, Natalia V. Minaeva, Natalia A. Zorina, Ekaterina N. Zotina, Svetlana V. Samarina, Elena L. Nazarova" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20471" ["VALUE"]=> array(2) { ["TEXT"]=> string(6366) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is an effective treatment method in patients with high-risk acute myeloid leukemia (AML). Nevertheless, disease relapse develops in 40-70% of patients during the first posttransplant year, and achievement of repeated remissions is possible only in 15-30% of patients. Hypomethylating, or epigenetic therapy (HM) appears to be a promising approach to these patients. The mechanism of HM drug action includes their ability to increase the levels of regulatory T-cells (Тregs, CD4+CD25+FOXP3+), which play a key role in the development of immunological tolerance in the post-transplant period, reducing the degree of development and severity of “graft-versus-host disease” (GVHD). In addition, the stimulating effect of these drugs on the pool of cytotoxic CD8+T-lymphocytes provides implementation of a tumor-specific response in the graft-versus-leukemia (GVL) effect. </p> <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> Objective of this study was to evaluate the results of the azacitidine application after allo-HSCT in patients with AML. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Twenty patients with AML were transplanted between 2015 and 2018 at the Federal State Institute of Science “Kirov Research Institute of Hematology and Blood Transfusion of the Federal Medical and Biological Agency of Russia” including 18 adult patients (14 women and 4 men) and 2 children. Myeloablative conditioning was used in 5 (25%) cases. In 15 (75%) patients, the reduced intensity regimen was applied. Related allo-HSCT was performed in 15 (75%) patients, 4 of them were transplanted from HLA-haploidentical donors. Unrelated allo-HSCT was carried out from fully matched donors in 5 cases. Out of 20 patients, 9 (45%) patients were alive at the time of evaluation. Eleven (55%) patients died at different times after alloHSCT due to severe infectious complications, severe acute GVHD, thrombotic microangiopathy, early relapse of the disease. Preventive azacitidine courses were given to 7 patients with high-risk AML. Of these, 6 women and 1 man, with a median age of 36.7 years (range: 20-50 years). Azacitidine therapy was started after hematopoietic recovery on the average at day +85 (range: 40-121 days) in the absence of severe infectious and other complications. The drug was administered according to the scheme: 35 mg/m2 subcutaneously for 5-7 days, every 28 days, with a median of 8 courses. In 3 cases, azacitidine was combined with donor lymphocyte infusions (DLI). </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> All the patients who received azacitidine at the time of the study are alive. Six of them have a disease remission. Prior to the azacitidine administration, 2 patients had complete donor hematopoiesis, in 1 complete donor chimerism was achieved in 2 months of therapy, in 4 there was a mixed donor chimerism. In 1 of them, a late relapse occurred after 3 courses of azacitidine, and now he receives antirelapse chemotherapy (ChT). </p> <h2 style="text-align: justify;">Clinical case</h2> <p style="text-align: justify;"> Patient T., female, 22 years old, AML, t(8;21), complete remission-3, unrelated allo-HSCT was performed in March 2016. The interval from treatment initiation to allo-HSCT was 27 months. The azacitidine prophylactic administration was started at day +56 after allo-HSCT at a dose of 35mg/m2 every 5 days of the 28-day cycle, for up to 6 cycles, and the therapy was completed in October 2016. Monitoring of general and lineage-specific chimerism was carried out at days +30, +56, +84, +119, +147, +174 and +360 and showed the presence of strong complete donor hematopoiesis. The disease remission is confirmed by the bone marrow evaluation. However, a late relapse-3 of the disease was shown at day +414 (30% of blast cells in the bone marrow), along with decrease in complete donor chimerism (41.3% of its own cells). In order to achieve remission-4, a course of FLAG with DLI was conducted. Recovery of leukocytes was observed at day +25 after ChT. Achievement of remission-4 was confirmed by the bone marrow evaluation and molecular assays. From June to July 2017, two 5-day courses of azacitidine 75 mg/m2 with DLI at an increasing dose were carried out, followed by achievement of complete donor chimerism. Over the following year, the patient received a total of 12 azacitidine courses (75 mg/m2), with escalated dose of donor lymphocytes. The patient retains a complete clinical, hematological and molecular remission of the disease. It is planned to continue prophylactic donor lymphocytes administration as a monotherapy. Given the small group of patients (7 people), it is premature to evaluate efficiency of azacitidine therapy. The median follow-up was 408 days. Peripheral cytopenia (grade 1) was the most frequent adverse event of azacitidine treatment, which did not require drug withdrawal or dose adjustment. Among non-hematological side effects, we observed reactions at the injection site, nausea, diarrhea and weakness, in most cases not exceeding I-II degree of toxicity. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Taking into account the positive experience with azacitidine usage in the patients with high-risk AML after allo-HSCT, this therapy appears to be a promising option both for relapse prevention and for achievement of repeated disease remissions. To assess azacitidine influence upon relapse-free and overall survival, including its combination with DLI, further accumulation of clinical experience is required. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Acute myeloid leukemia, allogeneic hematopoietic stem cell transplantation, azacitidine, chimerism, donor lymphocyte infusion. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6058) "Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is an effective treatment method in patients with high-risk acute myeloid leukemia (AML). Nevertheless, disease relapse develops in 40-70% of patients during the first posttransplant year, and achievement of repeated remissions is possible only in 15-30% of patients. Hypomethylating, or epigenetic therapy (HM) appears to be a promising approach to these patients. The mechanism of HM drug action includes their ability to increase the levels of regulatory T-cells (Тregs, CD4+CD25+FOXP3+), which play a key role in the development of immunological tolerance in the post-transplant period, reducing the degree of development and severity of “graft-versus-host disease” (GVHD). In addition, the stimulating effect of these drugs on the pool of cytotoxic CD8+T-lymphocytes provides implementation of a tumor-specific response in the graft-versus-leukemia (GVL) effect.
Aim
Objective of this study was to evaluate the results of the azacitidine application after allo-HSCT in patients with AML.
Patients and methods
Twenty patients with AML were transplanted between 2015 and 2018 at the Federal State Institute of Science “Kirov Research Institute of Hematology and Blood Transfusion of the Federal Medical and Biological Agency of Russia” including 18 adult patients (14 women and 4 men) and 2 children. Myeloablative conditioning was used in 5 (25%) cases. In 15 (75%) patients, the reduced intensity regimen was applied. Related allo-HSCT was performed in 15 (75%) patients, 4 of them were transplanted from HLA-haploidentical donors. Unrelated allo-HSCT was carried out from fully matched donors in 5 cases. Out of 20 patients, 9 (45%) patients were alive at the time of evaluation. Eleven (55%) patients died at different times after alloHSCT due to severe infectious complications, severe acute GVHD, thrombotic microangiopathy, early relapse of the disease. Preventive azacitidine courses were given to 7 patients with high-risk AML. Of these, 6 women and 1 man, with a median age of 36.7 years (range: 20-50 years). Azacitidine therapy was started after hematopoietic recovery on the average at day +85 (range: 40-121 days) in the absence of severe infectious and other complications. The drug was administered according to the scheme: 35 mg/m2 subcutaneously for 5-7 days, every 28 days, with a median of 8 courses. In 3 cases, azacitidine was combined with donor lymphocyte infusions (DLI).
Results
All the patients who received azacitidine at the time of the study are alive. Six of them have a disease remission. Prior to the azacitidine administration, 2 patients had complete donor hematopoiesis, in 1 complete donor chimerism was achieved in 2 months of therapy, in 4 there was a mixed donor chimerism. In 1 of them, a late relapse occurred after 3 courses of azacitidine, and now he receives antirelapse chemotherapy (ChT).
Clinical case
Patient T., female, 22 years old, AML, t(8;21), complete remission-3, unrelated allo-HSCT was performed in March 2016. The interval from treatment initiation to allo-HSCT was 27 months. The azacitidine prophylactic administration was started at day +56 after allo-HSCT at a dose of 35mg/m2 every 5 days of the 28-day cycle, for up to 6 cycles, and the therapy was completed in October 2016. Monitoring of general and lineage-specific chimerism was carried out at days +30, +56, +84, +119, +147, +174 and +360 and showed the presence of strong complete donor hematopoiesis. The disease remission is confirmed by the bone marrow evaluation. However, a late relapse-3 of the disease was shown at day +414 (30% of blast cells in the bone marrow), along with decrease in complete donor chimerism (41.3% of its own cells). In order to achieve remission-4, a course of FLAG with DLI was conducted. Recovery of leukocytes was observed at day +25 after ChT. Achievement of remission-4 was confirmed by the bone marrow evaluation and molecular assays. From June to July 2017, two 5-day courses of azacitidine 75 mg/m2 with DLI at an increasing dose were carried out, followed by achievement of complete donor chimerism. Over the following year, the patient received a total of 12 azacitidine courses (75 mg/m2), with escalated dose of donor lymphocytes. The patient retains a complete clinical, hematological and molecular remission of the disease. It is planned to continue prophylactic donor lymphocytes administration as a monotherapy. Given the small group of patients (7 people), it is premature to evaluate efficiency of azacitidine therapy. The median follow-up was 408 days. Peripheral cytopenia (grade 1) was the most frequent adverse event of azacitidine treatment, which did not require drug withdrawal or dose adjustment. Among non-hematological side effects, we observed reactions at the injection site, nausea, diarrhea and weakness, in most cases not exceeding I-II degree of toxicity.
Conclusion
Taking into account the positive experience with azacitidine usage in the patients with high-risk AML after allo-HSCT, this therapy appears to be a promising option both for relapse prevention and for achievement of repeated disease remissions. To assess azacitidine influence upon relapse-free and overall survival, including its combination with DLI, further accumulation of clinical experience is required.
Keywords
Acute myeloid leukemia, allogeneic hematopoietic stem cell transplantation, azacitidine, chimerism, donor lymphocyte infusion.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6058) "Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is an effective treatment method in patients with high-risk acute myeloid leukemia (AML). Nevertheless, disease relapse develops in 40-70% of patients during the first posttransplant year, and achievement of repeated remissions is possible only in 15-30% of patients. Hypomethylating, or epigenetic therapy (HM) appears to be a promising approach to these patients. The mechanism of HM drug action includes their ability to increase the levels of regulatory T-cells (Тregs, CD4+CD25+FOXP3+), which play a key role in the development of immunological tolerance in the post-transplant period, reducing the degree of development and severity of “graft-versus-host disease” (GVHD). In addition, the stimulating effect of these drugs on the pool of cytotoxic CD8+T-lymphocytes provides implementation of a tumor-specific response in the graft-versus-leukemia (GVL) effect.
Aim
Objective of this study was to evaluate the results of the azacitidine application after allo-HSCT in patients with AML.
Patients and methods
Twenty patients with AML were transplanted between 2015 and 2018 at the Federal State Institute of Science “Kirov Research Institute of Hematology and Blood Transfusion of the Federal Medical and Biological Agency of Russia” including 18 adult patients (14 women and 4 men) and 2 children. Myeloablative conditioning was used in 5 (25%) cases. In 15 (75%) patients, the reduced intensity regimen was applied. Related allo-HSCT was performed in 15 (75%) patients, 4 of them were transplanted from HLA-haploidentical donors. Unrelated allo-HSCT was carried out from fully matched donors in 5 cases. Out of 20 patients, 9 (45%) patients were alive at the time of evaluation. Eleven (55%) patients died at different times after alloHSCT due to severe infectious complications, severe acute GVHD, thrombotic microangiopathy, early relapse of the disease. Preventive azacitidine courses were given to 7 patients with high-risk AML. Of these, 6 women and 1 man, with a median age of 36.7 years (range: 20-50 years). Azacitidine therapy was started after hematopoietic recovery on the average at day +85 (range: 40-121 days) in the absence of severe infectious and other complications. The drug was administered according to the scheme: 35 mg/m2 subcutaneously for 5-7 days, every 28 days, with a median of 8 courses. In 3 cases, azacitidine was combined with donor lymphocyte infusions (DLI).
Results
All the patients who received azacitidine at the time of the study are alive. Six of them have a disease remission. Prior to the azacitidine administration, 2 patients had complete donor hematopoiesis, in 1 complete donor chimerism was achieved in 2 months of therapy, in 4 there was a mixed donor chimerism. In 1 of them, a late relapse occurred after 3 courses of azacitidine, and now he receives antirelapse chemotherapy (ChT).
Clinical case
Patient T., female, 22 years old, AML, t(8;21), complete remission-3, unrelated allo-HSCT was performed in March 2016. The interval from treatment initiation to allo-HSCT was 27 months. The azacitidine prophylactic administration was started at day +56 after allo-HSCT at a dose of 35mg/m2 every 5 days of the 28-day cycle, for up to 6 cycles, and the therapy was completed in October 2016. Monitoring of general and lineage-specific chimerism was carried out at days +30, +56, +84, +119, +147, +174 and +360 and showed the presence of strong complete donor hematopoiesis. The disease remission is confirmed by the bone marrow evaluation. However, a late relapse-3 of the disease was shown at day +414 (30% of blast cells in the bone marrow), along with decrease in complete donor chimerism (41.3% of its own cells). In order to achieve remission-4, a course of FLAG with DLI was conducted. Recovery of leukocytes was observed at day +25 after ChT. Achievement of remission-4 was confirmed by the bone marrow evaluation and molecular assays. From June to July 2017, two 5-day courses of azacitidine 75 mg/m2 with DLI at an increasing dose were carried out, followed by achievement of complete donor chimerism. Over the following year, the patient received a total of 12 azacitidine courses (75 mg/m2), with escalated dose of donor lymphocytes. The patient retains a complete clinical, hematological and molecular remission of the disease. It is planned to continue prophylactic donor lymphocytes administration as a monotherapy. Given the small group of patients (7 people), it is premature to evaluate efficiency of azacitidine therapy. The median follow-up was 408 days. Peripheral cytopenia (grade 1) was the most frequent adverse event of azacitidine treatment, which did not require drug withdrawal or dose adjustment. Among non-hematological side effects, we observed reactions at the injection site, nausea, diarrhea and weakness, in most cases not exceeding I-II degree of toxicity.
Conclusion
Taking into account the positive experience with azacitidine usage in the patients with high-risk AML after allo-HSCT, this therapy appears to be a promising option both for relapse prevention and for achievement of repeated disease remissions. To assess azacitidine influence upon relapse-free and overall survival, including its combination with DLI, further accumulation of clinical experience is required.
Keywords
Acute myeloid leukemia, allogeneic hematopoietic stem cell transplantation, azacitidine, chimerism, donor lymphocyte infusion.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20472" ["VALUE"]=> string(102) "Experience with hypomethylating drug application in allogeneic hematopoietic stem cell transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(102) "Experience with hypomethylating drug application in allogeneic hematopoietic stem cell transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(102) "Experience with hypomethylating drug application in allogeneic hematopoietic stem cell transplantation" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20470" ["VALUE"]=> array(2) { ["TEXT"]=> string(87) "Kirov Research Institute of Hematology and Blood Transfusion, Kirov, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(87) "Kirov Research Institute of Hematology and Blood Transfusion, Kirov, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(87) "Kirov Research Institute of Hematology and Blood Transfusion, Kirov, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20466" ["VALUE"]=> array(2) { ["TEXT"]=> string(210) "Марина Н. Хоробрых, Наталья В. Минаева, Наталья А. Зорина, Екатерина Н. Зотина, Светлана В. Самарина, Елена Л. Назарова" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(210) "Марина Н. Хоробрых, Наталья В. Минаева, Наталья А. Зорина, Екатерина Н. Зотина, Светлана В. Самарина, Елена Л. Назарова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(210) "Марина Н. Хоробрых, Наталья В. Минаева, Наталья А. Зорина, Екатерина Н. Зотина, Светлана В. Самарина, Елена Л. Назарова" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20468" ["VALUE"]=> array(2) { ["TEXT"]=> string(10544) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелобластным лейкозом (ОМЛ) высокого риска. Тем не менее, рецидив заболевания развивается у 40-70% пациентов в течение первого года после трансплантации, а достижение повторных ремиссий возможно лишь у 15-30% больных. Гипометилирующая (эпигенетическая) терапия представляется перспективным подходом у этой категории больных. Механизм действия гипометилирующих препаратов заключается в их способности увеличивать уровень регуляторных Т-клеток (Тregs, CD4+CD25+FOXP3+), которые играют ключевую роль в развитии иммунологической толерантности в посттрансплантационном периоде, снижая степень развития и выраженности реакции «трансплантат против хозяина» (РТПХ). Кроме того, отмечено стимулирующее действие этих препаратов на пул цитотоксических CD8+ Т-лимфоцитов, обеспечивающих реализацию опухолеспецифического ответа в реакции «трансплантат против лейкоза» (РТПЛ). </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель исследования состояла в оценке результатов применения азацитидина после алло-ТГСК у пациентов с ОМЛ. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В 2015-2018 гг. в клинике Федерального государственного бюджетного учреждения науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства» (КНИИГиПК) выполнено 20 алло-ТГСК пациентам с ОМЛ. Из них 18 – взрослым пациентам (14 женщин и 4 мужчин) и 2 – детям. Миелоаблативный режим кондиционирования использовался в 5 (25%) случаях, в 15 (75%) – режим со сниженной интенсивностью. Родственная алло-ТГСК выполнена 15 (75%) пациентам, из них гаплоидентичная – 4, неродственная от полностью совместимого донора – 5. Из 20 больных, на момент оценки живы 9 (45%). 11 (55%) пациентов погибли в разные сроки после алло-ТГСК: причинами смерти являлись тяжелые инфекционные осложнения, тяжелая острая реакция трансплантат против хозяина, тромботическая микроангиопатия, ранний рецидив заболевания. Курсы азацитидина с профилактической целью получили 7 пациентов с ОМЛ высокого риска. Из них 6 женщин и 1 мужчина, с медианой возраста 36,7 лет (диапазон: 20-50 лет). Терапию азацитидином начинали после восстановления кроветворения в среднем на Д+85 (диапазон: 40–121 день), при отсутствии тяжелых инфекционных и других осложнений. Препарат назначали по схеме 35 мг/м2 подкожно в течение 5-7 суток, каждые 28 дней, медиана 8 курсов. В 3 случаях азацитидин комбинировали с инфузией донорских лимфоцитов (DLI – donor lymphocyte infusion). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Все больные, получавшие азацитидин, на момент исследования живы. У 6 из них сохраняется ремиссия заболевания. Перед назначением азацитидина полное донорское кроветворение имели 2 пациента, у 1 полный донорский химеризм достигнут через 2 месяца терапии, у 4 отмечался смешанный донорский химеризм. У 1 из них возник поздний рецидив заболевания после 3 курсов азацитидина, в настоящее время он получает противорецидивную химиотерапию (ХТ). </p> <h2 style="text-align: justify;">Клинический случай</h2> <p style="text-align: justify;"> Пациентка Т., 22 лет, ОМЛ, t(8;21), ПР 3 неродственная аллоТГСК выполнена в марте 2016 г. Интервал от начала лечения до аллоТГСК составил 27 мес. Профилактическое введение азацитидина начато на +56 день после аллоТГСК в дозе 35 мг\м2 каждые 5 дней 28 дневного цикла №6, терапия закончена в октябре 2016 г. Мониторинг общего и линейного химеризма проводился в дни +30, +56, +84, +119, +147, +174 и +360 и показал наличие стойкого полного донорского кроветворения. Ремиссия заболевания подтверждена результатами миелограммы. Однако, на Д+414 выявлен поздний рецидив-3 заболевания (в миелограмме 30% бластов), снижение общего донорского химеризма (41,3% собственных клеток). С целью достижения ремиссии – 4 проведен курс FLAG с DLI. Восстановление лейкоцитов отмечалось на +25 сутки после ХТ. Достижение ремиссии-4 подтверждено результатами миелограммы, молекулярным исследованием. С июня по июль 2017 г. проведено два 5-дневных курса азацитидина 75 мг/м2 с DLI в возрастающей дозе, после чего достигнут полный донорский химеризм. В течение последующего года пациентка получила суммарно 12 курсов азацитидина 75 мг/м2 с эскалацией дозы донорских лимфоцитов. У больной сохраняется полная клинико-гематологическая и молекулярная ремиссия заболевания. Планируется продолжить профилактическое введение донорских лимфоцитов в монорежиме. Учитывая небольшую группу пациентов (7 человек), оценка эффективности терапии азацитидином преждевременна. Медиана наблюдения составила 408 дней. Наиболее частыми нежелательными явлениями при применении азацитидина были периферические цитопении 1 степени, не требующие отмены препарата или коррекции дозы. Среди негематологических побочных эффектов отмечались реакции в месте инъекции, тошнота, диарея и слабость, в большинстве случаев не выходившие за пределы I-II степени токсичности. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Принимая во внимание положительный опыт применения препарата у пациентов с ОМЛ высокого риска после алло-ТГСК, терапия азацитидином представляется перспективной опцией как для профилактики рецидивов, так и в целях достижения повторных ремиссий заболевания. Для оценки влияния азацитидина, в том числе в сочетании с DLI, на безрецидивную и общую выживаемость требуется дальнейшее накопление клинического опыта. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый миелобластный лейкоз, аллогенная трансплантация гемопоэтических стволовых клеток, азацитидин, химеризм, инфузия донорских лимфоцитов. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(10236) "Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелобластным лейкозом (ОМЛ) высокого риска. Тем не менее, рецидив заболевания развивается у 40-70% пациентов в течение первого года после трансплантации, а достижение повторных ремиссий возможно лишь у 15-30% больных. Гипометилирующая (эпигенетическая) терапия представляется перспективным подходом у этой категории больных. Механизм действия гипометилирующих препаратов заключается в их способности увеличивать уровень регуляторных Т-клеток (Тregs, CD4+CD25+FOXP3+), которые играют ключевую роль в развитии иммунологической толерантности в посттрансплантационном периоде, снижая степень развития и выраженности реакции «трансплантат против хозяина» (РТПХ). Кроме того, отмечено стимулирующее действие этих препаратов на пул цитотоксических CD8+ Т-лимфоцитов, обеспечивающих реализацию опухолеспецифического ответа в реакции «трансплантат против лейкоза» (РТПЛ).
Цель
Цель исследования состояла в оценке результатов применения азацитидина после алло-ТГСК у пациентов с ОМЛ.
Пациенты и методы
В 2015-2018 гг. в клинике Федерального государственного бюджетного учреждения науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства» (КНИИГиПК) выполнено 20 алло-ТГСК пациентам с ОМЛ. Из них 18 – взрослым пациентам (14 женщин и 4 мужчин) и 2 – детям. Миелоаблативный режим кондиционирования использовался в 5 (25%) случаях, в 15 (75%) – режим со сниженной интенсивностью. Родственная алло-ТГСК выполнена 15 (75%) пациентам, из них гаплоидентичная – 4, неродственная от полностью совместимого донора – 5. Из 20 больных, на момент оценки живы 9 (45%). 11 (55%) пациентов погибли в разные сроки после алло-ТГСК: причинами смерти являлись тяжелые инфекционные осложнения, тяжелая острая реакция трансплантат против хозяина, тромботическая микроангиопатия, ранний рецидив заболевания. Курсы азацитидина с профилактической целью получили 7 пациентов с ОМЛ высокого риска. Из них 6 женщин и 1 мужчина, с медианой возраста 36,7 лет (диапазон: 20-50 лет). Терапию азацитидином начинали после восстановления кроветворения в среднем на Д+85 (диапазон: 40–121 день), при отсутствии тяжелых инфекционных и других осложнений. Препарат назначали по схеме 35 мг/м2 подкожно в течение 5-7 суток, каждые 28 дней, медиана 8 курсов. В 3 случаях азацитидин комбинировали с инфузией донорских лимфоцитов (DLI – donor lymphocyte infusion).
Результаты
Все больные, получавшие азацитидин, на момент исследования живы. У 6 из них сохраняется ремиссия заболевания. Перед назначением азацитидина полное донорское кроветворение имели 2 пациента, у 1 полный донорский химеризм достигнут через 2 месяца терапии, у 4 отмечался смешанный донорский химеризм. У 1 из них возник поздний рецидив заболевания после 3 курсов азацитидина, в настоящее время он получает противорецидивную химиотерапию (ХТ).
Клинический случай
Пациентка Т., 22 лет, ОМЛ, t(8;21), ПР 3 неродственная аллоТГСК выполнена в марте 2016 г. Интервал от начала лечения до аллоТГСК составил 27 мес. Профилактическое введение азацитидина начато на +56 день после аллоТГСК в дозе 35 мг\м2 каждые 5 дней 28 дневного цикла №6, терапия закончена в октябре 2016 г. Мониторинг общего и линейного химеризма проводился в дни +30, +56, +84, +119, +147, +174 и +360 и показал наличие стойкого полного донорского кроветворения. Ремиссия заболевания подтверждена результатами миелограммы. Однако, на Д+414 выявлен поздний рецидив-3 заболевания (в миелограмме 30% бластов), снижение общего донорского химеризма (41,3% собственных клеток). С целью достижения ремиссии – 4 проведен курс FLAG с DLI. Восстановление лейкоцитов отмечалось на +25 сутки после ХТ. Достижение ремиссии-4 подтверждено результатами миелограммы, молекулярным исследованием. С июня по июль 2017 г. проведено два 5-дневных курса азацитидина 75 мг/м2 с DLI в возрастающей дозе, после чего достигнут полный донорский химеризм. В течение последующего года пациентка получила суммарно 12 курсов азацитидина 75 мг/м2 с эскалацией дозы донорских лимфоцитов. У больной сохраняется полная клинико-гематологическая и молекулярная ремиссия заболевания. Планируется продолжить профилактическое введение донорских лимфоцитов в монорежиме. Учитывая небольшую группу пациентов (7 человек), оценка эффективности терапии азацитидином преждевременна. Медиана наблюдения составила 408 дней. Наиболее частыми нежелательными явлениями при применении азацитидина были периферические цитопении 1 степени, не требующие отмены препарата или коррекции дозы. Среди негематологических побочных эффектов отмечались реакции в месте инъекции, тошнота, диарея и слабость, в большинстве случаев не выходившие за пределы I-II степени токсичности.
Заключение
Принимая во внимание положительный опыт применения препарата у пациентов с ОМЛ высокого риска после алло-ТГСК, терапия азацитидином представляется перспективной опцией как для профилактики рецидивов, так и в целях достижения повторных ремиссий заболевания. Для оценки влияния азацитидина, в том числе в сочетании с DLI, на безрецидивную и общую выживаемость требуется дальнейшее накопление клинического опыта.
Ключевые слова
Острый миелобластный лейкоз, аллогенная трансплантация гемопоэтических стволовых клеток, азацитидин, химеризм, инфузия донорских лимфоцитов.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(10236) "Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелобластным лейкозом (ОМЛ) высокого риска. Тем не менее, рецидив заболевания развивается у 40-70% пациентов в течение первого года после трансплантации, а достижение повторных ремиссий возможно лишь у 15-30% больных. Гипометилирующая (эпигенетическая) терапия представляется перспективным подходом у этой категории больных. Механизм действия гипометилирующих препаратов заключается в их способности увеличивать уровень регуляторных Т-клеток (Тregs, CD4+CD25+FOXP3+), которые играют ключевую роль в развитии иммунологической толерантности в посттрансплантационном периоде, снижая степень развития и выраженности реакции «трансплантат против хозяина» (РТПХ). Кроме того, отмечено стимулирующее действие этих препаратов на пул цитотоксических CD8+ Т-лимфоцитов, обеспечивающих реализацию опухолеспецифического ответа в реакции «трансплантат против лейкоза» (РТПЛ).
Цель
Цель исследования состояла в оценке результатов применения азацитидина после алло-ТГСК у пациентов с ОМЛ.
Пациенты и методы
В 2015-2018 гг. в клинике Федерального государственного бюджетного учреждения науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства» (КНИИГиПК) выполнено 20 алло-ТГСК пациентам с ОМЛ. Из них 18 – взрослым пациентам (14 женщин и 4 мужчин) и 2 – детям. Миелоаблативный режим кондиционирования использовался в 5 (25%) случаях, в 15 (75%) – режим со сниженной интенсивностью. Родственная алло-ТГСК выполнена 15 (75%) пациентам, из них гаплоидентичная – 4, неродственная от полностью совместимого донора – 5. Из 20 больных, на момент оценки живы 9 (45%). 11 (55%) пациентов погибли в разные сроки после алло-ТГСК: причинами смерти являлись тяжелые инфекционные осложнения, тяжелая острая реакция трансплантат против хозяина, тромботическая микроангиопатия, ранний рецидив заболевания. Курсы азацитидина с профилактической целью получили 7 пациентов с ОМЛ высокого риска. Из них 6 женщин и 1 мужчина, с медианой возраста 36,7 лет (диапазон: 20-50 лет). Терапию азацитидином начинали после восстановления кроветворения в среднем на Д+85 (диапазон: 40–121 день), при отсутствии тяжелых инфекционных и других осложнений. Препарат назначали по схеме 35 мг/м2 подкожно в течение 5-7 суток, каждые 28 дней, медиана 8 курсов. В 3 случаях азацитидин комбинировали с инфузией донорских лимфоцитов (DLI – donor lymphocyte infusion).
Результаты
Все больные, получавшие азацитидин, на момент исследования живы. У 6 из них сохраняется ремиссия заболевания. Перед назначением азацитидина полное донорское кроветворение имели 2 пациента, у 1 полный донорский химеризм достигнут через 2 месяца терапии, у 4 отмечался смешанный донорский химеризм. У 1 из них возник поздний рецидив заболевания после 3 курсов азацитидина, в настоящее время он получает противорецидивную химиотерапию (ХТ).
Клинический случай
Пациентка Т., 22 лет, ОМЛ, t(8;21), ПР 3 неродственная аллоТГСК выполнена в марте 2016 г. Интервал от начала лечения до аллоТГСК составил 27 мес. Профилактическое введение азацитидина начато на +56 день после аллоТГСК в дозе 35 мг\м2 каждые 5 дней 28 дневного цикла №6, терапия закончена в октябре 2016 г. Мониторинг общего и линейного химеризма проводился в дни +30, +56, +84, +119, +147, +174 и +360 и показал наличие стойкого полного донорского кроветворения. Ремиссия заболевания подтверждена результатами миелограммы. Однако, на Д+414 выявлен поздний рецидив-3 заболевания (в миелограмме 30% бластов), снижение общего донорского химеризма (41,3% собственных клеток). С целью достижения ремиссии – 4 проведен курс FLAG с DLI. Восстановление лейкоцитов отмечалось на +25 сутки после ХТ. Достижение ремиссии-4 подтверждено результатами миелограммы, молекулярным исследованием. С июня по июль 2017 г. проведено два 5-дневных курса азацитидина 75 мг/м2 с DLI в возрастающей дозе, после чего достигнут полный донорский химеризм. В течение последующего года пациентка получила суммарно 12 курсов азацитидина 75 мг/м2 с эскалацией дозы донорских лимфоцитов. У больной сохраняется полная клинико-гематологическая и молекулярная ремиссия заболевания. Планируется продолжить профилактическое введение донорских лимфоцитов в монорежиме. Учитывая небольшую группу пациентов (7 человек), оценка эффективности терапии азацитидином преждевременна. Медиана наблюдения составила 408 дней. Наиболее частыми нежелательными явлениями при применении азацитидина были периферические цитопении 1 степени, не требующие отмены препарата или коррекции дозы. Среди негематологических побочных эффектов отмечались реакции в месте инъекции, тошнота, диарея и слабость, в большинстве случаев не выходившие за пределы I-II степени токсичности.
Заключение
Принимая во внимание положительный опыт применения препарата у пациентов с ОМЛ высокого риска после алло-ТГСК, терапия азацитидином представляется перспективной опцией как для профилактики рецидивов, так и в целях достижения повторных ремиссий заболевания. Для оценки влияния азацитидина, в том числе в сочетании с DLI, на безрецидивную и общую выживаемость требуется дальнейшее накопление клинического опыта.
Ключевые слова
Острый миелобластный лейкоз, аллогенная трансплантация гемопоэтических стволовых клеток, азацитидин, химеризм, инфузия донорских лимфоцитов.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20467" ["VALUE"]=> array(2) { ["TEXT"]=> string(364) "Федеральное государственное бюджетное учреждение науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства», Киров, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(364) "Федеральное государственное бюджетное учреждение науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства», Киров, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(364) "Федеральное государственное бюджетное учреждение науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства», Киров, Россия" } } } [7]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1574" ["~ID"]=> string(4) "1574" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(210) "Аутологичная трансплантация гемопоэтических стволовых клеток у детей и подростков, страдающих лимфомой Ходжкина" ["~NAME"]=> string(210) "Аутологичная трансплантация гемопоэтических стволовых клеток у детей и подростков, страдающих лимфомой Ходжкина" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:36:21" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:36:21" ["DETAIL_PAGE_URL"]=> string(151) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/autologichnaya-transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-u-detey-i-podrostkov-stradayushch/" ["~DETAIL_PAGE_URL"]=> string(151) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/autologichnaya-transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-u-detey-i-podrostkov-stradayushch/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(101) "autologichnaya-transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-u-detey-i-podrostkov-stradayushch" ["~CODE"]=> string(101) "autologichnaya-transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-u-detey-i-podrostkov-stradayushch" ["EXTERNAL_ID"]=> string(4) "1574" ["~EXTERNAL_ID"]=> string(4) "1574" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(210) "Аутологичная трансплантация гемопоэтических стволовых клеток у детей и подростков, страдающих лимфомой Ходжкина" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(312) "Аутологичная трансплантация гемопоэтических стволовых клеток у детей и подростков, страдающих лимфомой ХоджкинаAutologous hematopoietic stem cell transplantation in children and teenagers with Hodgkin’s lymphoma" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(5519) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Применение стандартных схем терапии удается излечивает до 70-90% пациентов, страдающих лимфомой Ходжкина (ЛХ). Аутологичная трансплантация гемопоэтических стволовых клеток (ауто-ТГСК) является эффективным способом терапии в случае химиочувствительного рецидива или достижения ремиссии при первично рефрактерном течении ЛХ. Несмотря на уже многолетнее использование, наличие крупных рандомизированных исследований, подтвердивших эффективность данного метода у взрослых, роль ауто-ТГСК у детей с ЛХ изучена в меньшей степени и количество крупных публикаций, посвященных данному вопросу, невелико. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В работу включено 66 пациентов с ЛХ в возрасте от 4 до 18 лет (медиана возраста – 16), пролеченных за период 1993-2017 гг. Распределение по гистологическому варианту было следующим: нодулярный склероз – 59 человек (89%), смешанно-клеточный вариант – 6 (9%), лимфоидное истощение – 1 (2%). На момент постановки диагноза у 29 (44%) отмечалась IV стадия ЛХ, 18 (27%) – III стадия, 17 (26%) – II стадия, 2 (3%) – I стадия, В-симптомы – 43 человека (65%), рецидивирующее течение – 45 (68%), рефрактерное течение – 21 (32%). Первая линия терапии проводилась по протоколу GPOH-HD у 37 пациентов (56%), по протоколу BEACOPP – 21 (32%), по протоколу ABVD – 8 (12%). Вторая линия терапия – IEP/ABVD в случае использования протокола GPOHHD и в случае использования других протоколов – DHAP или ICE. Ранний рецидив ЛХ (<12 месяцев) отмечался у 26 человек (58%), поздний рецидив – 19 (42%). Медиана линий терапии перед ауто-ТГСК – 2 (1-6). Полная ремиссия на момент ауто-ТГСК была диагностирована у 25 человек (38%), частичная ремиссия – 25 (38%), стабилизация – 6 (9%) и прогрессия заболевания – 10 (15%). В рамках ауто-ТГСК назначались следующие режимы кондиционирования: BEAM – 24 пациента (36%), BeEAM – 22 (33%), CBV – 13 (20%), другие режимы кондиционирования – 7 (11%). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Долгосрочная общая выживаемость (ОВ) всех пациентов составила 48% и выживаемость без прогрессирования – 41%. ОВ в случае химиочувствительного и химиорезистентного течения – 64% и 33%, соответственно (p=0,005). Общая выживаемость при использовании режима кондиционирования BeEAM составила 62%, BEAM– 51%. (p=0,6). Трансплантационная летальность составила 4,5%. Причины летального исхода: инфекционные осложнения – 2 человека, токсические осложнения – 1 (фиброз легких). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> При использовании ауто-ТГСК удается излечить примерно половину детей и подростков, страдающих рецидивирующим или рефрактерным течением ЛХ. Показанием для ауто-ТГСК у детей, как и у взрослых, является химиочувствительное течение. Режимы кондиционирования BEAM и BeEAM одинаково эффективны.</p><h2 style="text-align: justify;"> Ключевые слова</h2> <p style="text-align: justify;">Лимфома Ходжкина, детский возраст, трансплантация гемопоэтических стволовых клеток, аутологичная, уровни выживаемости. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(210) "Аутологичная трансплантация гемопоэтических стволовых клеток у детей и подростков, страдающих лимфомой Ходжкина" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(210) "Аутологичная трансплантация гемопоэтических стволовых клеток у детей и подростков, страдающих лимфомой Ходжкина" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(210) "Аутологичная трансплантация гемопоэтических стволовых клеток у детей и подростков, страдающих лимфомой Ходжкина" ["SECTION_META_TITLE"]=> string(210) "Аутологичная трансплантация гемопоэтических стволовых клеток у детей и подростков, страдающих лимфомой Ходжкина" ["SECTION_META_KEYWORDS"]=> string(210) "Аутологичная трансплантация гемопоэтических стволовых клеток у детей и подростков, страдающих лимфомой Ходжкина" ["SECTION_META_DESCRIPTION"]=> string(210) "Аутологичная трансплантация гемопоэтических стволовых клеток у детей и подростков, страдающих лимфомой Ходжкина" ["SECTION_PICTURE_FILE_ALT"]=> string(210) "Аутологичная трансплантация гемопоэтических стволовых клеток у детей и подростков, страдающих лимфомой Ходжкина" ["SECTION_PICTURE_FILE_TITLE"]=> string(210) "Аутологичная трансплантация гемопоэтических стволовых клеток у детей и подростков, страдающих лимфомой Ходжкина" ["SECTION_PICTURE_FILE_NAME"]=> string(101) "autologichnaya-transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-u-detey-i-podrostkov-stradayushch" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(210) "Аутологичная трансплантация гемопоэтических стволовых клеток у детей и подростков, страдающих лимфомой Ходжкина" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(210) "Аутологичная трансплантация гемопоэтических стволовых клеток у детей и подростков, страдающих лимфомой Ходжкина" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(101) "autologichnaya-transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-u-detey-i-podrostkov-stradayushch" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(101) "autologichnaya-transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-u-detey-i-podrostkov-stradayushch" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(101) "autologichnaya-transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-u-detey-i-podrostkov-stradayushch" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20502" ["VALUE"]=> array(2) { ["TEXT"]=> string(468) "Андрей В. Козлов, Илья В. Казанцев, Елена В. Морозова, Татьяна В. Юхта, Полина С. Толкунова, Асмик Г. Геворгян, Михаил М. Канунников, Кирилл В. Лепик, Юрий Р. Залялов, Елена В. Бабенко, Мария А. Эстрина, Наталья Б. Михайлова, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(468) "Андрей В. Козлов, Илья В. Казанцев, Елена В. Морозова, Татьяна В. Юхта, Полина С. Толкунова, Асмик Г. Геворгян, Михаил М. Канунников, Кирилл В. Лепик, Юрий Р. Залялов, Елена В. Бабенко, Мария А. Эстрина, Наталья Б. Михайлова, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20503" ["VALUE"]=> array(2) { ["TEXT"]=> string(348) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(348) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20504" ["VALUE"]=> array(2) { ["TEXT"]=> string(5519) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Применение стандартных схем терапии удается излечивает до 70-90% пациентов, страдающих лимфомой Ходжкина (ЛХ). Аутологичная трансплантация гемопоэтических стволовых клеток (ауто-ТГСК) является эффективным способом терапии в случае химиочувствительного рецидива или достижения ремиссии при первично рефрактерном течении ЛХ. Несмотря на уже многолетнее использование, наличие крупных рандомизированных исследований, подтвердивших эффективность данного метода у взрослых, роль ауто-ТГСК у детей с ЛХ изучена в меньшей степени и количество крупных публикаций, посвященных данному вопросу, невелико. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В работу включено 66 пациентов с ЛХ в возрасте от 4 до 18 лет (медиана возраста – 16), пролеченных за период 1993-2017 гг. Распределение по гистологическому варианту было следующим: нодулярный склероз – 59 человек (89%), смешанно-клеточный вариант – 6 (9%), лимфоидное истощение – 1 (2%). На момент постановки диагноза у 29 (44%) отмечалась IV стадия ЛХ, 18 (27%) – III стадия, 17 (26%) – II стадия, 2 (3%) – I стадия, В-симптомы – 43 человека (65%), рецидивирующее течение – 45 (68%), рефрактерное течение – 21 (32%). Первая линия терапии проводилась по протоколу GPOH-HD у 37 пациентов (56%), по протоколу BEACOPP – 21 (32%), по протоколу ABVD – 8 (12%). Вторая линия терапия – IEP/ABVD в случае использования протокола GPOHHD и в случае использования других протоколов – DHAP или ICE. Ранний рецидив ЛХ (<12 месяцев) отмечался у 26 человек (58%), поздний рецидив – 19 (42%). Медиана линий терапии перед ауто-ТГСК – 2 (1-6). Полная ремиссия на момент ауто-ТГСК была диагностирована у 25 человек (38%), частичная ремиссия – 25 (38%), стабилизация – 6 (9%) и прогрессия заболевания – 10 (15%). В рамках ауто-ТГСК назначались следующие режимы кондиционирования: BEAM – 24 пациента (36%), BeEAM – 22 (33%), CBV – 13 (20%), другие режимы кондиционирования – 7 (11%). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Долгосрочная общая выживаемость (ОВ) всех пациентов составила 48% и выживаемость без прогрессирования – 41%. ОВ в случае химиочувствительного и химиорезистентного течения – 64% и 33%, соответственно (p=0,005). Общая выживаемость при использовании режима кондиционирования BeEAM составила 62%, BEAM– 51%. (p=0,6). Трансплантационная летальность составила 4,5%. Причины летального исхода: инфекционные осложнения – 2 человека, токсические осложнения – 1 (фиброз легких). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> При использовании ауто-ТГСК удается излечить примерно половину детей и подростков, страдающих рецидивирующим или рефрактерным течением ЛХ. Показанием для ауто-ТГСК у детей, как и у взрослых, является химиочувствительное течение. Режимы кондиционирования BEAM и BeEAM одинаково эффективны.</p><h2 style="text-align: justify;"> Ключевые слова</h2> <p style="text-align: justify;">Лимфома Ходжкина, детский возраст, трансплантация гемопоэтических стволовых клеток, аутологичная, уровни выживаемости. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5283) "Введение
Применение стандартных схем терапии удается излечивает до 70-90% пациентов, страдающих лимфомой Ходжкина (ЛХ). Аутологичная трансплантация гемопоэтических стволовых клеток (ауто-ТГСК) является эффективным способом терапии в случае химиочувствительного рецидива или достижения ремиссии при первично рефрактерном течении ЛХ. Несмотря на уже многолетнее использование, наличие крупных рандомизированных исследований, подтвердивших эффективность данного метода у взрослых, роль ауто-ТГСК у детей с ЛХ изучена в меньшей степени и количество крупных публикаций, посвященных данному вопросу, невелико.
Материалы и методы
В работу включено 66 пациентов с ЛХ в возрасте от 4 до 18 лет (медиана возраста – 16), пролеченных за период 1993-2017 гг. Распределение по гистологическому варианту было следующим: нодулярный склероз – 59 человек (89%), смешанно-клеточный вариант – 6 (9%), лимфоидное истощение – 1 (2%). На момент постановки диагноза у 29 (44%) отмечалась IV стадия ЛХ, 18 (27%) – III стадия, 17 (26%) – II стадия, 2 (3%) – I стадия, В-симптомы – 43 человека (65%), рецидивирующее течение – 45 (68%), рефрактерное течение – 21 (32%). Первая линия терапии проводилась по протоколу GPOH-HD у 37 пациентов (56%), по протоколу BEACOPP – 21 (32%), по протоколу ABVD – 8 (12%). Вторая линия терапия – IEP/ABVD в случае использования протокола GPOHHD и в случае использования других протоколов – DHAP или ICE. Ранний рецидив ЛХ (<12 месяцев) отмечался у 26 человек (58%), поздний рецидив – 19 (42%). Медиана линий терапии перед ауто-ТГСК – 2 (1-6). Полная ремиссия на момент ауто-ТГСК была диагностирована у 25 человек (38%), частичная ремиссия – 25 (38%), стабилизация – 6 (9%) и прогрессия заболевания – 10 (15%). В рамках ауто-ТГСК назначались следующие режимы кондиционирования: BEAM – 24 пациента (36%), BeEAM – 22 (33%), CBV – 13 (20%), другие режимы кондиционирования – 7 (11%).
Результаты
Долгосрочная общая выживаемость (ОВ) всех пациентов составила 48% и выживаемость без прогрессирования – 41%. ОВ в случае химиочувствительного и химиорезистентного течения – 64% и 33%, соответственно (p=0,005). Общая выживаемость при использовании режима кондиционирования BeEAM составила 62%, BEAM– 51%. (p=0,6). Трансплантационная летальность составила 4,5%. Причины летального исхода: инфекционные осложнения – 2 человека, токсические осложнения – 1 (фиброз легких).
Выводы
При использовании ауто-ТГСК удается излечить примерно половину детей и подростков, страдающих рецидивирующим или рефрактерным течением ЛХ. Показанием для ауто-ТГСК у детей, как и у взрослых, является химиочувствительное течение. Режимы кондиционирования BEAM и BeEAM одинаково эффективны.
Ключевые слова
Лимфома Ходжкина, детский возраст, трансплантация гемопоэтических стволовых клеток, аутологичная, уровни выживаемости.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20505" ["VALUE"]=> array(2) { ["TEXT"]=> string(275) "Andrey V. Kozlov, Ilya V. Kazantsev, Elena V. Morozova, Tatiana V. Iuchta, Polina S. Tolkunova, Asmik G. Gevorgian, Mihail M. Kanunnikov, Kirill V. Lepik, Yuri R. Zalyalov, Elena V. Babenko, Maria A. Estrina, Natalia B. Mikhailova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(275) "Andrey V. Kozlov, Ilya V. Kazantsev, Elena V. Morozova, Tatiana V. Iuchta, Polina S. Tolkunova, Asmik G. Gevorgian, Mihail M. Kanunnikov, Kirill V. Lepik, Yuri R. Zalyalov, Elena V. Babenko, Maria A. Estrina, Natalia B. Mikhailova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20506" ["VALUE"]=> array(2) { ["TEXT"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20507" ["VALUE"]=> array(2) { ["TEXT"]=> string(3131) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Standard therapy cures 70-90% of patients with Hodgkin’s lymphoma (HL). Autologous hematopoietic stem cell transplantation (auto-HSCT) is an effective treatment option in chemosensitive relapsed or refractory disease. Despite longterm experience the data on the role of auto-HSCT in children are limited. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> Between 1993-2017, sixty-six HL patients at the median age of 16 (4-18) received auto-HSCT. Nodular sclerosis was diagnosed in 59 patients (89%), mixed cellularity type, in 6 (9%), lymphocyte depletion form, in 1 (2%). Clinical stage IV was assessed in 29 patients (44%), stage III, in 18 (27%), stage II, in 17 (26%), stage I, in 2 cases (3%); В symptoms were documented in 43 cases (65%). Relapsing course of the disease was revealed in 45 children and teenagers (68%), and refractory disease was confirmed in 21cases (32%). First-line therapy was carried out according to GPOH-HD protocol in 37 patients (56%); BEACOPP was applied in 21 cases (32%); ABVD, in 8 cases (12%). Second-line therapy included IEP/ABVD in GPOH-HD group, and DHAP or ICE in BEACOPP or ABVD groups. Early HL relapses (<12 months) were diagnosed in 26 children and teenagers (58%), and late relapse was stated in 19 patients (42%). Median number of therapy lines prior to auto-HSCT was 2 (1 to 6). Complete remission at the moment of auto-HSCT was achieved in 25 patients (38%), partial remission, in 25 (38%), stabilization, in 6 (9%), and progression of the disease was observed in 10 (15%). The conditioning regimens included BEAM (n=24, 36%), BeEAM (n=22, 33%), CBV (n=13, 20%), others (n=7, 11%). </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Long-term overall survival (OS) was 48%, and progression free survival was 41%. The OS values in cases of chemosensitive disease were 64%, and in chemoresistant disease, 33%, (p=0.005). BeEAM and BEAM conditioning regimens have shown comparable effectiveness (OS, 62% and 51%, respectively, p=0.6). Transplant-related mortality was 4.5%. Lethal complications were associated with infections in 2 patients and high-dose chemotherapy toxicity in 1 patient (lung fibrosis). </p> <h2 style="text-align: justify;">Сonclusion</h2> <p style="text-align: justify;"> Auto-HSCT cures approximately half of children and teenagers with relapsed or refractory HL. Chemosensitivity of the disease is an essential factor for the success of auto-HSCT. BEAM and BeEAM conditioning regimens are equally effective in children. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hodgkin’s lymphoma, pediatric, hematopoietic stem cell transplantation, autologous, survival rates. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2895) "Introduction
Standard therapy cures 70-90% of patients with Hodgkin’s lymphoma (HL). Autologous hematopoietic stem cell transplantation (auto-HSCT) is an effective treatment option in chemosensitive relapsed or refractory disease. Despite longterm experience the data on the role of auto-HSCT in children are limited.
Materials and methods
Between 1993-2017, sixty-six HL patients at the median age of 16 (4-18) received auto-HSCT. Nodular sclerosis was diagnosed in 59 patients (89%), mixed cellularity type, in 6 (9%), lymphocyte depletion form, in 1 (2%). Clinical stage IV was assessed in 29 patients (44%), stage III, in 18 (27%), stage II, in 17 (26%), stage I, in 2 cases (3%); В symptoms were documented in 43 cases (65%). Relapsing course of the disease was revealed in 45 children and teenagers (68%), and refractory disease was confirmed in 21cases (32%). First-line therapy was carried out according to GPOH-HD protocol in 37 patients (56%); BEACOPP was applied in 21 cases (32%); ABVD, in 8 cases (12%). Second-line therapy included IEP/ABVD in GPOH-HD group, and DHAP or ICE in BEACOPP or ABVD groups. Early HL relapses (<12 months) were diagnosed in 26 children and teenagers (58%), and late relapse was stated in 19 patients (42%). Median number of therapy lines prior to auto-HSCT was 2 (1 to 6). Complete remission at the moment of auto-HSCT was achieved in 25 patients (38%), partial remission, in 25 (38%), stabilization, in 6 (9%), and progression of the disease was observed in 10 (15%). The conditioning regimens included BEAM (n=24, 36%), BeEAM (n=22, 33%), CBV (n=13, 20%), others (n=7, 11%).
Results
Long-term overall survival (OS) was 48%, and progression free survival was 41%. The OS values in cases of chemosensitive disease were 64%, and in chemoresistant disease, 33%, (p=0.005). BeEAM and BEAM conditioning regimens have shown comparable effectiveness (OS, 62% and 51%, respectively, p=0.6). Transplant-related mortality was 4.5%. Lethal complications were associated with infections in 2 patients and high-dose chemotherapy toxicity in 1 patient (lung fibrosis).
Сonclusion
Auto-HSCT cures approximately half of children and teenagers with relapsed or refractory HL. Chemosensitivity of the disease is an essential factor for the success of auto-HSCT. BEAM and BeEAM conditioning regimens are equally effective in children.
Keywords
Hodgkin’s lymphoma, pediatric, hematopoietic stem cell transplantation, autologous, survival rates.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20508" ["VALUE"]=> string(102) "Autologous hematopoietic stem cell transplantation in children and teenagers with Hodgkin’s lymphoma" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(102) "Autologous hematopoietic stem cell transplantation in children and teenagers with Hodgkin’s lymphoma" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20781" ["VALUE"]=> string(4) "1419" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1419" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20782" ["VALUE"]=> string(4) "1420" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1420" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20505" ["VALUE"]=> array(2) { ["TEXT"]=> string(275) "Andrey V. Kozlov, Ilya V. Kazantsev, Elena V. Morozova, Tatiana V. Iuchta, Polina S. Tolkunova, Asmik G. Gevorgian, Mihail M. Kanunnikov, Kirill V. Lepik, Yuri R. Zalyalov, Elena V. Babenko, Maria A. Estrina, Natalia B. Mikhailova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(275) "Andrey V. Kozlov, Ilya V. Kazantsev, Elena V. Morozova, Tatiana V. Iuchta, Polina S. Tolkunova, Asmik G. Gevorgian, Mihail M. Kanunnikov, Kirill V. Lepik, Yuri R. Zalyalov, Elena V. Babenko, Maria A. Estrina, Natalia B. Mikhailova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(275) "Andrey V. Kozlov, Ilya V. Kazantsev, Elena V. Morozova, Tatiana V. Iuchta, Polina S. Tolkunova, Asmik G. Gevorgian, Mihail M. Kanunnikov, Kirill V. Lepik, Yuri R. Zalyalov, Elena V. Babenko, Maria A. Estrina, Natalia B. Mikhailova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20507" ["VALUE"]=> array(2) { ["TEXT"]=> string(3131) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Standard therapy cures 70-90% of patients with Hodgkin’s lymphoma (HL). Autologous hematopoietic stem cell transplantation (auto-HSCT) is an effective treatment option in chemosensitive relapsed or refractory disease. Despite longterm experience the data on the role of auto-HSCT in children are limited. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> Between 1993-2017, sixty-six HL patients at the median age of 16 (4-18) received auto-HSCT. Nodular sclerosis was diagnosed in 59 patients (89%), mixed cellularity type, in 6 (9%), lymphocyte depletion form, in 1 (2%). Clinical stage IV was assessed in 29 patients (44%), stage III, in 18 (27%), stage II, in 17 (26%), stage I, in 2 cases (3%); В symptoms were documented in 43 cases (65%). Relapsing course of the disease was revealed in 45 children and teenagers (68%), and refractory disease was confirmed in 21cases (32%). First-line therapy was carried out according to GPOH-HD protocol in 37 patients (56%); BEACOPP was applied in 21 cases (32%); ABVD, in 8 cases (12%). Second-line therapy included IEP/ABVD in GPOH-HD group, and DHAP or ICE in BEACOPP or ABVD groups. Early HL relapses (<12 months) were diagnosed in 26 children and teenagers (58%), and late relapse was stated in 19 patients (42%). Median number of therapy lines prior to auto-HSCT was 2 (1 to 6). Complete remission at the moment of auto-HSCT was achieved in 25 patients (38%), partial remission, in 25 (38%), stabilization, in 6 (9%), and progression of the disease was observed in 10 (15%). The conditioning regimens included BEAM (n=24, 36%), BeEAM (n=22, 33%), CBV (n=13, 20%), others (n=7, 11%). </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Long-term overall survival (OS) was 48%, and progression free survival was 41%. The OS values in cases of chemosensitive disease were 64%, and in chemoresistant disease, 33%, (p=0.005). BeEAM and BEAM conditioning regimens have shown comparable effectiveness (OS, 62% and 51%, respectively, p=0.6). Transplant-related mortality was 4.5%. Lethal complications were associated with infections in 2 patients and high-dose chemotherapy toxicity in 1 patient (lung fibrosis). </p> <h2 style="text-align: justify;">Сonclusion</h2> <p style="text-align: justify;"> Auto-HSCT cures approximately half of children and teenagers with relapsed or refractory HL. Chemosensitivity of the disease is an essential factor for the success of auto-HSCT. BEAM and BeEAM conditioning regimens are equally effective in children. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hodgkin’s lymphoma, pediatric, hematopoietic stem cell transplantation, autologous, survival rates. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2895) "Introduction
Standard therapy cures 70-90% of patients with Hodgkin’s lymphoma (HL). Autologous hematopoietic stem cell transplantation (auto-HSCT) is an effective treatment option in chemosensitive relapsed or refractory disease. Despite longterm experience the data on the role of auto-HSCT in children are limited.
Materials and methods
Between 1993-2017, sixty-six HL patients at the median age of 16 (4-18) received auto-HSCT. Nodular sclerosis was diagnosed in 59 patients (89%), mixed cellularity type, in 6 (9%), lymphocyte depletion form, in 1 (2%). Clinical stage IV was assessed in 29 patients (44%), stage III, in 18 (27%), stage II, in 17 (26%), stage I, in 2 cases (3%); В symptoms were documented in 43 cases (65%). Relapsing course of the disease was revealed in 45 children and teenagers (68%), and refractory disease was confirmed in 21cases (32%). First-line therapy was carried out according to GPOH-HD protocol in 37 patients (56%); BEACOPP was applied in 21 cases (32%); ABVD, in 8 cases (12%). Second-line therapy included IEP/ABVD in GPOH-HD group, and DHAP or ICE in BEACOPP or ABVD groups. Early HL relapses (<12 months) were diagnosed in 26 children and teenagers (58%), and late relapse was stated in 19 patients (42%). Median number of therapy lines prior to auto-HSCT was 2 (1 to 6). Complete remission at the moment of auto-HSCT was achieved in 25 patients (38%), partial remission, in 25 (38%), stabilization, in 6 (9%), and progression of the disease was observed in 10 (15%). The conditioning regimens included BEAM (n=24, 36%), BeEAM (n=22, 33%), CBV (n=13, 20%), others (n=7, 11%).
Results
Long-term overall survival (OS) was 48%, and progression free survival was 41%. The OS values in cases of chemosensitive disease were 64%, and in chemoresistant disease, 33%, (p=0.005). BeEAM and BEAM conditioning regimens have shown comparable effectiveness (OS, 62% and 51%, respectively, p=0.6). Transplant-related mortality was 4.5%. Lethal complications were associated with infections in 2 patients and high-dose chemotherapy toxicity in 1 patient (lung fibrosis).
Сonclusion
Auto-HSCT cures approximately half of children and teenagers with relapsed or refractory HL. Chemosensitivity of the disease is an essential factor for the success of auto-HSCT. BEAM and BeEAM conditioning regimens are equally effective in children.
Keywords
Hodgkin’s lymphoma, pediatric, hematopoietic stem cell transplantation, autologous, survival rates.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2895) "Introduction
Standard therapy cures 70-90% of patients with Hodgkin’s lymphoma (HL). Autologous hematopoietic stem cell transplantation (auto-HSCT) is an effective treatment option in chemosensitive relapsed or refractory disease. Despite longterm experience the data on the role of auto-HSCT in children are limited.
Materials and methods
Between 1993-2017, sixty-six HL patients at the median age of 16 (4-18) received auto-HSCT. Nodular sclerosis was diagnosed in 59 patients (89%), mixed cellularity type, in 6 (9%), lymphocyte depletion form, in 1 (2%). Clinical stage IV was assessed in 29 patients (44%), stage III, in 18 (27%), stage II, in 17 (26%), stage I, in 2 cases (3%); В symptoms were documented in 43 cases (65%). Relapsing course of the disease was revealed in 45 children and teenagers (68%), and refractory disease was confirmed in 21cases (32%). First-line therapy was carried out according to GPOH-HD protocol in 37 patients (56%); BEACOPP was applied in 21 cases (32%); ABVD, in 8 cases (12%). Second-line therapy included IEP/ABVD in GPOH-HD group, and DHAP or ICE in BEACOPP or ABVD groups. Early HL relapses (<12 months) were diagnosed in 26 children and teenagers (58%), and late relapse was stated in 19 patients (42%). Median number of therapy lines prior to auto-HSCT was 2 (1 to 6). Complete remission at the moment of auto-HSCT was achieved in 25 patients (38%), partial remission, in 25 (38%), stabilization, in 6 (9%), and progression of the disease was observed in 10 (15%). The conditioning regimens included BEAM (n=24, 36%), BeEAM (n=22, 33%), CBV (n=13, 20%), others (n=7, 11%).
Results
Long-term overall survival (OS) was 48%, and progression free survival was 41%. The OS values in cases of chemosensitive disease were 64%, and in chemoresistant disease, 33%, (p=0.005). BeEAM and BEAM conditioning regimens have shown comparable effectiveness (OS, 62% and 51%, respectively, p=0.6). Transplant-related mortality was 4.5%. Lethal complications were associated with infections in 2 patients and high-dose chemotherapy toxicity in 1 patient (lung fibrosis).
Сonclusion
Auto-HSCT cures approximately half of children and teenagers with relapsed or refractory HL. Chemosensitivity of the disease is an essential factor for the success of auto-HSCT. BEAM and BeEAM conditioning regimens are equally effective in children.
Keywords
Hodgkin’s lymphoma, pediatric, hematopoietic stem cell transplantation, autologous, survival rates.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20508" ["VALUE"]=> string(102) "Autologous hematopoietic stem cell transplantation in children and teenagers with Hodgkin’s lymphoma" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(102) "Autologous hematopoietic stem cell transplantation in children and teenagers with Hodgkin’s lymphoma" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(102) "Autologous hematopoietic stem cell transplantation in children and teenagers with Hodgkin’s lymphoma" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20506" ["VALUE"]=> array(2) { ["TEXT"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20502" ["VALUE"]=> array(2) { ["TEXT"]=> string(468) "Андрей В. Козлов, Илья В. Казанцев, Елена В. Морозова, Татьяна В. Юхта, Полина С. Толкунова, Асмик Г. Геворгян, Михаил М. Канунников, Кирилл В. Лепик, Юрий Р. Залялов, Елена В. Бабенко, Мария А. Эстрина, Наталья Б. Михайлова, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(468) "Андрей В. Козлов, Илья В. Казанцев, Елена В. Морозова, Татьяна В. Юхта, Полина С. Толкунова, Асмик Г. Геворгян, Михаил М. Канунников, Кирилл В. Лепик, Юрий Р. Залялов, Елена В. Бабенко, Мария А. Эстрина, Наталья Б. Михайлова, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(468) "Андрей В. Козлов, Илья В. Казанцев, Елена В. Морозова, Татьяна В. Юхта, Полина С. Толкунова, Асмик Г. Геворгян, Михаил М. Канунников, Кирилл В. Лепик, Юрий Р. Залялов, Елена В. Бабенко, Мария А. Эстрина, Наталья Б. Михайлова, Людмила С. Зубаровская, Борис В. Афанасьев" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20504" ["VALUE"]=> array(2) { ["TEXT"]=> string(5519) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Применение стандартных схем терапии удается излечивает до 70-90% пациентов, страдающих лимфомой Ходжкина (ЛХ). Аутологичная трансплантация гемопоэтических стволовых клеток (ауто-ТГСК) является эффективным способом терапии в случае химиочувствительного рецидива или достижения ремиссии при первично рефрактерном течении ЛХ. Несмотря на уже многолетнее использование, наличие крупных рандомизированных исследований, подтвердивших эффективность данного метода у взрослых, роль ауто-ТГСК у детей с ЛХ изучена в меньшей степени и количество крупных публикаций, посвященных данному вопросу, невелико. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В работу включено 66 пациентов с ЛХ в возрасте от 4 до 18 лет (медиана возраста – 16), пролеченных за период 1993-2017 гг. Распределение по гистологическому варианту было следующим: нодулярный склероз – 59 человек (89%), смешанно-клеточный вариант – 6 (9%), лимфоидное истощение – 1 (2%). На момент постановки диагноза у 29 (44%) отмечалась IV стадия ЛХ, 18 (27%) – III стадия, 17 (26%) – II стадия, 2 (3%) – I стадия, В-симптомы – 43 человека (65%), рецидивирующее течение – 45 (68%), рефрактерное течение – 21 (32%). Первая линия терапии проводилась по протоколу GPOH-HD у 37 пациентов (56%), по протоколу BEACOPP – 21 (32%), по протоколу ABVD – 8 (12%). Вторая линия терапия – IEP/ABVD в случае использования протокола GPOHHD и в случае использования других протоколов – DHAP или ICE. Ранний рецидив ЛХ (<12 месяцев) отмечался у 26 человек (58%), поздний рецидив – 19 (42%). Медиана линий терапии перед ауто-ТГСК – 2 (1-6). Полная ремиссия на момент ауто-ТГСК была диагностирована у 25 человек (38%), частичная ремиссия – 25 (38%), стабилизация – 6 (9%) и прогрессия заболевания – 10 (15%). В рамках ауто-ТГСК назначались следующие режимы кондиционирования: BEAM – 24 пациента (36%), BeEAM – 22 (33%), CBV – 13 (20%), другие режимы кондиционирования – 7 (11%). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Долгосрочная общая выживаемость (ОВ) всех пациентов составила 48% и выживаемость без прогрессирования – 41%. ОВ в случае химиочувствительного и химиорезистентного течения – 64% и 33%, соответственно (p=0,005). Общая выживаемость при использовании режима кондиционирования BeEAM составила 62%, BEAM– 51%. (p=0,6). Трансплантационная летальность составила 4,5%. Причины летального исхода: инфекционные осложнения – 2 человека, токсические осложнения – 1 (фиброз легких). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> При использовании ауто-ТГСК удается излечить примерно половину детей и подростков, страдающих рецидивирующим или рефрактерным течением ЛХ. Показанием для ауто-ТГСК у детей, как и у взрослых, является химиочувствительное течение. Режимы кондиционирования BEAM и BeEAM одинаково эффективны.</p><h2 style="text-align: justify;"> Ключевые слова</h2> <p style="text-align: justify;">Лимфома Ходжкина, детский возраст, трансплантация гемопоэтических стволовых клеток, аутологичная, уровни выживаемости. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5283) "Введение
Применение стандартных схем терапии удается излечивает до 70-90% пациентов, страдающих лимфомой Ходжкина (ЛХ). Аутологичная трансплантация гемопоэтических стволовых клеток (ауто-ТГСК) является эффективным способом терапии в случае химиочувствительного рецидива или достижения ремиссии при первично рефрактерном течении ЛХ. Несмотря на уже многолетнее использование, наличие крупных рандомизированных исследований, подтвердивших эффективность данного метода у взрослых, роль ауто-ТГСК у детей с ЛХ изучена в меньшей степени и количество крупных публикаций, посвященных данному вопросу, невелико.
Материалы и методы
В работу включено 66 пациентов с ЛХ в возрасте от 4 до 18 лет (медиана возраста – 16), пролеченных за период 1993-2017 гг. Распределение по гистологическому варианту было следующим: нодулярный склероз – 59 человек (89%), смешанно-клеточный вариант – 6 (9%), лимфоидное истощение – 1 (2%). На момент постановки диагноза у 29 (44%) отмечалась IV стадия ЛХ, 18 (27%) – III стадия, 17 (26%) – II стадия, 2 (3%) – I стадия, В-симптомы – 43 человека (65%), рецидивирующее течение – 45 (68%), рефрактерное течение – 21 (32%). Первая линия терапии проводилась по протоколу GPOH-HD у 37 пациентов (56%), по протоколу BEACOPP – 21 (32%), по протоколу ABVD – 8 (12%). Вторая линия терапия – IEP/ABVD в случае использования протокола GPOHHD и в случае использования других протоколов – DHAP или ICE. Ранний рецидив ЛХ (<12 месяцев) отмечался у 26 человек (58%), поздний рецидив – 19 (42%). Медиана линий терапии перед ауто-ТГСК – 2 (1-6). Полная ремиссия на момент ауто-ТГСК была диагностирована у 25 человек (38%), частичная ремиссия – 25 (38%), стабилизация – 6 (9%) и прогрессия заболевания – 10 (15%). В рамках ауто-ТГСК назначались следующие режимы кондиционирования: BEAM – 24 пациента (36%), BeEAM – 22 (33%), CBV – 13 (20%), другие режимы кондиционирования – 7 (11%).
Результаты
Долгосрочная общая выживаемость (ОВ) всех пациентов составила 48% и выживаемость без прогрессирования – 41%. ОВ в случае химиочувствительного и химиорезистентного течения – 64% и 33%, соответственно (p=0,005). Общая выживаемость при использовании режима кондиционирования BeEAM составила 62%, BEAM– 51%. (p=0,6). Трансплантационная летальность составила 4,5%. Причины летального исхода: инфекционные осложнения – 2 человека, токсические осложнения – 1 (фиброз легких).
Выводы
При использовании ауто-ТГСК удается излечить примерно половину детей и подростков, страдающих рецидивирующим или рефрактерным течением ЛХ. Показанием для ауто-ТГСК у детей, как и у взрослых, является химиочувствительное течение. Режимы кондиционирования BEAM и BeEAM одинаково эффективны.
Ключевые слова
Лимфома Ходжкина, детский возраст, трансплантация гемопоэтических стволовых клеток, аутологичная, уровни выживаемости.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(5283) "Введение
Применение стандартных схем терапии удается излечивает до 70-90% пациентов, страдающих лимфомой Ходжкина (ЛХ). Аутологичная трансплантация гемопоэтических стволовых клеток (ауто-ТГСК) является эффективным способом терапии в случае химиочувствительного рецидива или достижения ремиссии при первично рефрактерном течении ЛХ. Несмотря на уже многолетнее использование, наличие крупных рандомизированных исследований, подтвердивших эффективность данного метода у взрослых, роль ауто-ТГСК у детей с ЛХ изучена в меньшей степени и количество крупных публикаций, посвященных данному вопросу, невелико.
Материалы и методы
В работу включено 66 пациентов с ЛХ в возрасте от 4 до 18 лет (медиана возраста – 16), пролеченных за период 1993-2017 гг. Распределение по гистологическому варианту было следующим: нодулярный склероз – 59 человек (89%), смешанно-клеточный вариант – 6 (9%), лимфоидное истощение – 1 (2%). На момент постановки диагноза у 29 (44%) отмечалась IV стадия ЛХ, 18 (27%) – III стадия, 17 (26%) – II стадия, 2 (3%) – I стадия, В-симптомы – 43 человека (65%), рецидивирующее течение – 45 (68%), рефрактерное течение – 21 (32%). Первая линия терапии проводилась по протоколу GPOH-HD у 37 пациентов (56%), по протоколу BEACOPP – 21 (32%), по протоколу ABVD – 8 (12%). Вторая линия терапия – IEP/ABVD в случае использования протокола GPOHHD и в случае использования других протоколов – DHAP или ICE. Ранний рецидив ЛХ (<12 месяцев) отмечался у 26 человек (58%), поздний рецидив – 19 (42%). Медиана линий терапии перед ауто-ТГСК – 2 (1-6). Полная ремиссия на момент ауто-ТГСК была диагностирована у 25 человек (38%), частичная ремиссия – 25 (38%), стабилизация – 6 (9%) и прогрессия заболевания – 10 (15%). В рамках ауто-ТГСК назначались следующие режимы кондиционирования: BEAM – 24 пациента (36%), BeEAM – 22 (33%), CBV – 13 (20%), другие режимы кондиционирования – 7 (11%).
Результаты
Долгосрочная общая выживаемость (ОВ) всех пациентов составила 48% и выживаемость без прогрессирования – 41%. ОВ в случае химиочувствительного и химиорезистентного течения – 64% и 33%, соответственно (p=0,005). Общая выживаемость при использовании режима кондиционирования BeEAM составила 62%, BEAM– 51%. (p=0,6). Трансплантационная летальность составила 4,5%. Причины летального исхода: инфекционные осложнения – 2 человека, токсические осложнения – 1 (фиброз легких).
Выводы
При использовании ауто-ТГСК удается излечить примерно половину детей и подростков, страдающих рецидивирующим или рефрактерным течением ЛХ. Показанием для ауто-ТГСК у детей, как и у взрослых, является химиочувствительное течение. Режимы кондиционирования BEAM и BeEAM одинаково эффективны.
Ключевые слова
Лимфома Ходжкина, детский возраст, трансплантация гемопоэтических стволовых клеток, аутологичная, уровни выживаемости.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20503" ["VALUE"]=> array(2) { ["TEXT"]=> string(348) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(348) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(348) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия" } } } [8]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1575" ["~ID"]=> string(4) "1575" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(193) "Новый способ введения ДМСО повышает сохранность криоконсервированных гемопоэтических стволовых клеток" ["~NAME"]=> string(193) "Новый способ введения ДМСО повышает сохранность криоконсервированных гемопоэтических стволовых клеток" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:36:02" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:36:02" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/novyy-sposob-vvedeniya-dmso-povyshaet-sokhrannost-kriokonservirovannykh-gemopoeticheskikh-stvolovykh/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/novyy-sposob-vvedeniya-dmso-povyshaet-sokhrannost-kriokonservirovannykh-gemopoeticheskikh-stvolovykh/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "novyy-sposob-vvedeniya-dmso-povyshaet-sokhrannost-kriokonservirovannykh-gemopoeticheskikh-stvolovykh" ["~CODE"]=> string(100) "novyy-sposob-vvedeniya-dmso-povyshaet-sokhrannost-kriokonservirovannykh-gemopoeticheskikh-stvolovykh" ["EXTERNAL_ID"]=> string(4) "1575" ["~EXTERNAL_ID"]=> string(4) "1575" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(193) "Новый способ введения ДМСО повышает сохранность криоконсервированных гемопоэтических стволовых клеток" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(306) "Новый способ введения ДМСО повышает сохранность криоконсервированных гемопоэтических стволовых клетокA novel method of dimethyl sulfoxide introduction improves preservation of cryopreserved hematopoietic stem cells" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(11551) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Обеспечение высокой и прогнозируемой сохранности гемопоэтических стволовых клеток (ГСК) после их размораживания и проведения аутологичной трансплантации – одно из ключевых условий для дальнейшего успешного восстановления гемопоэза после высокодозной химиотерапии у пациентов с гемобластозами. Считается, что методика криоконсервирования ГСК давно отработана и приводит к ожидаемым результатам, поэтому обычно учитывается только заготовленная доза ГСК. Однако, при использовании современного и достоверного контроля качества, повсеместно применяемые методы криоконсервации ГСК не всегда могут гарантировать достаточную сохранность данных клеток (Табл. 1). Общеизвестно, что сохранность ГСК при хранении обеспечивает криопротектор, защищающий клетки от осмотического шока при их замораживании. Криопротектор с ДМСО общепринято вводить при помощи шприца в трансплантат ГСК. При этом конечная концентрация ДМСО в 5-10% достигается уже в криопакете с трансплантатом. Однако криопротектор с концентрированным ДМСО (более 50%) при контакте с клеткой, ввиду своих физико-химических свойств, может привести к ее частичной деструкции еще до замораживания. Таким образом, повысить сохранность ГСК можно снизив деструктивное воздействие, которое может быть связано с исходной высокой концентрацией ДМСО в криопротекторе. Для этого нами разработан и апробирован новый способ введения ДМСО в трансплантат ГСК при помощи специального сконструированного аппарата – автоматизированной системы введения ДМСО (на стадии патентования). Принцип действия данной системы исключает продолжительный контакт концентрированного ДМСО с трансплантатом ГСК. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель работы состояла в сравнении сохранности ГСК при использовании автоматизированного и ручного способа введения ДМСО. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Лейкоконцентрат ГСК периферической крови (n=25), полученный путем афереза у пациентов с онкогематологическими заболеваниями. Контрольная группа I – введение ДМСО в криопакет с трансплантатом ГСК выполняли ручным способом. Опытная группа II – введение ДМСО в трансплантат ГСК выполняли новым автоматизированным способом. Использовали стандартный криопротектор (55% DMSO Dex 40), конечная концентрация ДМСО – 7,5%. Замораживание (одновременно группы I и II) проводили на программном замораживателе по валидированной 6-ти ступенчатой программе. Хранение осуществляли в жидком азоте. Размораживание криопакетов проводили на водяной бане при +40 в течение 1 мин. Анализ количества жизнеспособных ГСК и их суммарной колониеобразующей активности (КОЕ) выполнялся до и после введения криопротектора, а также после размораживания. После размораживания для достоверности пробы отбирались из криопакетов. Количество ГСК оценивалось по фенотипу CD34+/CD45dim/7AAD проточной цитометрией по протоколу ISHAGE. Колониеобразующая активность ГСК оценивалась путем их культивирования в течение 14 суток (Methocult H4435) с последующим подсчетом суммарных колоний (КОЕ). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Согласно представленным в таблице 2 результатам, сохранность ГСК в группах I и II после введения ДМСО не отличается. Идентичные результаты, вероятно, обусловлены одинаковым инкубационным воздействием ДМСО на ГСК, связанным с продолжительностью проведения анализа методом проточной цитометрии. Тем самым моделируется экспозиционное воздействие ДМСО на ГСК. Из этого следует, что при отсутствии немедленного замораживания ГСК после введения ДМСО, повреждающие эффекты связаны с деструктивными физико-химическими свойствами ДМСО по отношению к клеткам, причем не зависимо от способа введения ДМСО.<br> Общепринято немедленно замораживать трансплантат сразу после введения ДМСО. В этот короткий временной промежуток будут законсервированы только те повреждения клеток, которые проявились сразу после первичного воздействия ДМСО. Поэтому зависимость контроля качества сохранности ГСК после введения криопротектора по методу 2 может быть оценена с большей достоверностью после размораживания. Контроль качества после размораживания отражен на рис. 1. Согласно представленным на рисунке результатам, сохранность ГСК после размораживания достоверно выше на 14% (p≤0.05) при использовании автоматизированной системы в сравнении с ручным способом. При прочих равных условиях исследования, суммарные потери ГСК после размораживания при ручном способе составили в среднем 20%, при автоматизированном – 6%. Они включают потери ГСК при введении ДМСО, а также утрату ГСК в процессе замораживания. Поэтому потери, вызванные замораживанием, можно принять как одинаковые при использовании разных способов введения ДМСО. Следовательно, при ручном способе потери связаны с этапом введения ДМСО. Мы полагаем, что средняя сохранность в 94% обусловлена способом введения ДМСО с использованием автоматизированной системы. Принцип работы автоматизированной системы позволяет снизить одномоментное повреждающее влияние исходного концентрированногораствора ДМСО на ГСК и обеспечить его более плавное разбавление до необходимой конечной концентрации ДМСО в 7,5%. Результаты, представленные в таблице и на рисунке, также показывают, что ДМСО на этапе его введения при экспозиции может оказывать большее негативное воздействие на ГСК, чем процедура замораживания трансплантата. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Сохранность ГСК при использовании автоматизированной системы введения ДМСО достоверно (на 14%) выше в сравнении с ручным способом. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Гемопоэтические стволовые клетки, криоконсервация, димитилсульфоксид, аутологичная трансплантация.<br> <img width="783" alt="25_таблицы.png" src="/upload/medialibrary/804/25_tablitsy.png" height="369" title="25_таблицы.png"><br> <br> <img width="375" alt="25_Рисунок.png" src="/upload/medialibrary/c2f/25_risunok.png" height="219" title="25_Рисунок.png"> </p> <h2 style="text-align: justify;">Рисунок 1. Выход гемопоэтических клеток после ручного или автоматизированного введения ДМСО и криоконсервирования по различным критериям</h2> <h2></h2> <br>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(193) "Новый способ введения ДМСО повышает сохранность криоконсервированных гемопоэтических стволовых клеток" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(193) "Новый способ введения ДМСО повышает сохранность криоконсервированных гемопоэтических стволовых клеток" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(193) "Новый способ введения ДМСО повышает сохранность криоконсервированных гемопоэтических стволовых клеток" ["SECTION_META_TITLE"]=> string(193) "Новый способ введения ДМСО повышает сохранность криоконсервированных гемопоэтических стволовых клеток" ["SECTION_META_KEYWORDS"]=> string(193) "Новый способ введения ДМСО повышает сохранность криоконсервированных гемопоэтических стволовых клеток" ["SECTION_META_DESCRIPTION"]=> string(193) "Новый способ введения ДМСО повышает сохранность криоконсервированных гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_ALT"]=> string(193) "Новый способ введения ДМСО повышает сохранность криоконсервированных гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_TITLE"]=> string(193) "Новый способ введения ДМСО повышает сохранность криоконсервированных гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "novyy-sposob-vvedeniya-dmso-povyshaet-sokhrannost-kriokonservirovannykh-gemopoeticheskikh-stvolovykh" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(193) "Новый способ введения ДМСО повышает сохранность криоконсервированных гемопоэтических стволовых клеток" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(193) "Новый способ введения ДМСО повышает сохранность криоконсервированных гемопоэтических стволовых клеток" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "novyy-sposob-vvedeniya-dmso-povyshaet-sokhrannost-kriokonservirovannykh-gemopoeticheskikh-stvolovykh" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "novyy-sposob-vvedeniya-dmso-povyshaet-sokhrannost-kriokonservirovannykh-gemopoeticheskikh-stvolovykh" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "novyy-sposob-vvedeniya-dmso-povyshaet-sokhrannost-kriokonservirovannykh-gemopoeticheskikh-stvolovykh" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20511" ["VALUE"]=> array(2) { ["TEXT"]=> string(228) "Евгений В. Коротаев, Сергей В. Андрюнькин, Андрей А. Степанов, Сергей А. Пономарев, Алексей Н. Косарев, Светлана С. Каракальчева" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(228) "Евгений В. Коротаев, Сергей В. Андрюнькин, Андрей А. Степанов, Сергей А. Пономарев, Алексей Н. Косарев, Светлана С. Каракальчева" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20512" ["VALUE"]=> array(2) { ["TEXT"]=> string(142) "АУ «Югорский НИИ клеточных технологий», Ханты-Мансийск, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(142) "АУ «Югорский НИИ клеточных технологий», Ханты-Мансийск, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20513" ["VALUE"]=> array(2) { ["TEXT"]=> string(11551) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Обеспечение высокой и прогнозируемой сохранности гемопоэтических стволовых клеток (ГСК) после их размораживания и проведения аутологичной трансплантации – одно из ключевых условий для дальнейшего успешного восстановления гемопоэза после высокодозной химиотерапии у пациентов с гемобластозами. Считается, что методика криоконсервирования ГСК давно отработана и приводит к ожидаемым результатам, поэтому обычно учитывается только заготовленная доза ГСК. Однако, при использовании современного и достоверного контроля качества, повсеместно применяемые методы криоконсервации ГСК не всегда могут гарантировать достаточную сохранность данных клеток (Табл. 1). Общеизвестно, что сохранность ГСК при хранении обеспечивает криопротектор, защищающий клетки от осмотического шока при их замораживании. Криопротектор с ДМСО общепринято вводить при помощи шприца в трансплантат ГСК. При этом конечная концентрация ДМСО в 5-10% достигается уже в криопакете с трансплантатом. Однако криопротектор с концентрированным ДМСО (более 50%) при контакте с клеткой, ввиду своих физико-химических свойств, может привести к ее частичной деструкции еще до замораживания. Таким образом, повысить сохранность ГСК можно снизив деструктивное воздействие, которое может быть связано с исходной высокой концентрацией ДМСО в криопротекторе. Для этого нами разработан и апробирован новый способ введения ДМСО в трансплантат ГСК при помощи специального сконструированного аппарата – автоматизированной системы введения ДМСО (на стадии патентования). Принцип действия данной системы исключает продолжительный контакт концентрированного ДМСО с трансплантатом ГСК. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель работы состояла в сравнении сохранности ГСК при использовании автоматизированного и ручного способа введения ДМСО. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Лейкоконцентрат ГСК периферической крови (n=25), полученный путем афереза у пациентов с онкогематологическими заболеваниями. Контрольная группа I – введение ДМСО в криопакет с трансплантатом ГСК выполняли ручным способом. Опытная группа II – введение ДМСО в трансплантат ГСК выполняли новым автоматизированным способом. Использовали стандартный криопротектор (55% DMSO Dex 40), конечная концентрация ДМСО – 7,5%. Замораживание (одновременно группы I и II) проводили на программном замораживателе по валидированной 6-ти ступенчатой программе. Хранение осуществляли в жидком азоте. Размораживание криопакетов проводили на водяной бане при +40 в течение 1 мин. Анализ количества жизнеспособных ГСК и их суммарной колониеобразующей активности (КОЕ) выполнялся до и после введения криопротектора, а также после размораживания. После размораживания для достоверности пробы отбирались из криопакетов. Количество ГСК оценивалось по фенотипу CD34+/CD45dim/7AAD проточной цитометрией по протоколу ISHAGE. Колониеобразующая активность ГСК оценивалась путем их культивирования в течение 14 суток (Methocult H4435) с последующим подсчетом суммарных колоний (КОЕ). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Согласно представленным в таблице 2 результатам, сохранность ГСК в группах I и II после введения ДМСО не отличается. Идентичные результаты, вероятно, обусловлены одинаковым инкубационным воздействием ДМСО на ГСК, связанным с продолжительностью проведения анализа методом проточной цитометрии. Тем самым моделируется экспозиционное воздействие ДМСО на ГСК. Из этого следует, что при отсутствии немедленного замораживания ГСК после введения ДМСО, повреждающие эффекты связаны с деструктивными физико-химическими свойствами ДМСО по отношению к клеткам, причем не зависимо от способа введения ДМСО.<br> Общепринято немедленно замораживать трансплантат сразу после введения ДМСО. В этот короткий временной промежуток будут законсервированы только те повреждения клеток, которые проявились сразу после первичного воздействия ДМСО. Поэтому зависимость контроля качества сохранности ГСК после введения криопротектора по методу 2 может быть оценена с большей достоверностью после размораживания. Контроль качества после размораживания отражен на рис. 1. Согласно представленным на рисунке результатам, сохранность ГСК после размораживания достоверно выше на 14% (p≤0.05) при использовании автоматизированной системы в сравнении с ручным способом. При прочих равных условиях исследования, суммарные потери ГСК после размораживания при ручном способе составили в среднем 20%, при автоматизированном – 6%. Они включают потери ГСК при введении ДМСО, а также утрату ГСК в процессе замораживания. Поэтому потери, вызванные замораживанием, можно принять как одинаковые при использовании разных способов введения ДМСО. Следовательно, при ручном способе потери связаны с этапом введения ДМСО. Мы полагаем, что средняя сохранность в 94% обусловлена способом введения ДМСО с использованием автоматизированной системы. Принцип работы автоматизированной системы позволяет снизить одномоментное повреждающее влияние исходного концентрированногораствора ДМСО на ГСК и обеспечить его более плавное разбавление до необходимой конечной концентрации ДМСО в 7,5%. Результаты, представленные в таблице и на рисунке, также показывают, что ДМСО на этапе его введения при экспозиции может оказывать большее негативное воздействие на ГСК, чем процедура замораживания трансплантата. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Сохранность ГСК при использовании автоматизированной системы введения ДМСО достоверно (на 14%) выше в сравнении с ручным способом. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Гемопоэтические стволовые клетки, криоконсервация, димитилсульфоксид, аутологичная трансплантация.<br> <img width="783" alt="25_таблицы.png" src="/upload/medialibrary/804/25_tablitsy.png" height="369" title="25_таблицы.png"><br> <br> <img width="375" alt="25_Рисунок.png" src="/upload/medialibrary/c2f/25_risunok.png" height="219" title="25_Рисунок.png"> </p> <h2 style="text-align: justify;">Рисунок 1. Выход гемопоэтических клеток после ручного или автоматизированного введения ДМСО и криоконсервирования по различным критериям</h2> <h2></h2> <br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(11111) "Введение
Обеспечение высокой и прогнозируемой сохранности гемопоэтических стволовых клеток (ГСК) после их размораживания и проведения аутологичной трансплантации – одно из ключевых условий для дальнейшего успешного восстановления гемопоэза после высокодозной химиотерапии у пациентов с гемобластозами. Считается, что методика криоконсервирования ГСК давно отработана и приводит к ожидаемым результатам, поэтому обычно учитывается только заготовленная доза ГСК. Однако, при использовании современного и достоверного контроля качества, повсеместно применяемые методы криоконсервации ГСК не всегда могут гарантировать достаточную сохранность данных клеток (Табл. 1). Общеизвестно, что сохранность ГСК при хранении обеспечивает криопротектор, защищающий клетки от осмотического шока при их замораживании. Криопротектор с ДМСО общепринято вводить при помощи шприца в трансплантат ГСК. При этом конечная концентрация ДМСО в 5-10% достигается уже в криопакете с трансплантатом. Однако криопротектор с концентрированным ДМСО (более 50%) при контакте с клеткой, ввиду своих физико-химических свойств, может привести к ее частичной деструкции еще до замораживания. Таким образом, повысить сохранность ГСК можно снизив деструктивное воздействие, которое может быть связано с исходной высокой концентрацией ДМСО в криопротекторе. Для этого нами разработан и апробирован новый способ введения ДМСО в трансплантат ГСК при помощи специального сконструированного аппарата – автоматизированной системы введения ДМСО (на стадии патентования). Принцип действия данной системы исключает продолжительный контакт концентрированного ДМСО с трансплантатом ГСК.
Цель
Цель работы состояла в сравнении сохранности ГСК при использовании автоматизированного и ручного способа введения ДМСО.
Материалы и методы
Лейкоконцентрат ГСК периферической крови (n=25), полученный путем афереза у пациентов с онкогематологическими заболеваниями. Контрольная группа I – введение ДМСО в криопакет с трансплантатом ГСК выполняли ручным способом. Опытная группа II – введение ДМСО в трансплантат ГСК выполняли новым автоматизированным способом. Использовали стандартный криопротектор (55% DMSO Dex 40), конечная концентрация ДМСО – 7,5%. Замораживание (одновременно группы I и II) проводили на программном замораживателе по валидированной 6-ти ступенчатой программе. Хранение осуществляли в жидком азоте. Размораживание криопакетов проводили на водяной бане при +40 в течение 1 мин. Анализ количества жизнеспособных ГСК и их суммарной колониеобразующей активности (КОЕ) выполнялся до и после введения криопротектора, а также после размораживания. После размораживания для достоверности пробы отбирались из криопакетов. Количество ГСК оценивалось по фенотипу CD34+/CD45dim/7AAD проточной цитометрией по протоколу ISHAGE. Колониеобразующая активность ГСК оценивалась путем их культивирования в течение 14 суток (Methocult H4435) с последующим подсчетом суммарных колоний (КОЕ).
Результаты
Согласно представленным в таблице 2 результатам, сохранность ГСК в группах I и II после введения ДМСО не отличается. Идентичные результаты, вероятно, обусловлены одинаковым инкубационным воздействием ДМСО на ГСК, связанным с продолжительностью проведения анализа методом проточной цитометрии. Тем самым моделируется экспозиционное воздействие ДМСО на ГСК. Из этого следует, что при отсутствии немедленного замораживания ГСК после введения ДМСО, повреждающие эффекты связаны с деструктивными физико-химическими свойствами ДМСО по отношению к клеткам, причем не зависимо от способа введения ДМСО.
Общепринято немедленно замораживать трансплантат сразу после введения ДМСО. В этот короткий временной промежуток будут законсервированы только те повреждения клеток, которые проявились сразу после первичного воздействия ДМСО. Поэтому зависимость контроля качества сохранности ГСК после введения криопротектора по методу 2 может быть оценена с большей достоверностью после размораживания. Контроль качества после размораживания отражен на рис. 1. Согласно представленным на рисунке результатам, сохранность ГСК после размораживания достоверно выше на 14% (p≤0.05) при использовании автоматизированной системы в сравнении с ручным способом. При прочих равных условиях исследования, суммарные потери ГСК после размораживания при ручном способе составили в среднем 20%, при автоматизированном – 6%. Они включают потери ГСК при введении ДМСО, а также утрату ГСК в процессе замораживания. Поэтому потери, вызванные замораживанием, можно принять как одинаковые при использовании разных способов введения ДМСО. Следовательно, при ручном способе потери связаны с этапом введения ДМСО. Мы полагаем, что средняя сохранность в 94% обусловлена способом введения ДМСО с использованием автоматизированной системы. Принцип работы автоматизированной системы позволяет снизить одномоментное повреждающее влияние исходного концентрированногораствора ДМСО на ГСК и обеспечить его более плавное разбавление до необходимой конечной концентрации ДМСО в 7,5%. Результаты, представленные в таблице и на рисунке, также показывают, что ДМСО на этапе его введения при экспозиции может оказывать большее негативное воздействие на ГСК, чем процедура замораживания трансплантата.
Заключение
Сохранность ГСК при использовании автоматизированной системы введения ДМСО достоверно (на 14%) выше в сравнении с ручным способом.
Ключевые слова
Гемопоэтические стволовые клетки, криоконсервация, димитилсульфоксид, аутологичная трансплантация.


Рисунок 1. Выход гемопоэтических клеток после ручного или автоматизированного введения ДМСО и криоконсервирования по различным критериям
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20514" ["VALUE"]=> array(2) { ["TEXT"]=> string(127) "Evgeniy V. Korotaev, Sergey V. Andrunkin, Andrey A. Stepanov, Sergey S. Ponomarev, Aleksey N. Kosarev, Svetlana S. Karakalcheva" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(127) "Evgeniy V. Korotaev, Sergey V. Andrunkin, Andrey A. Stepanov, Sergey S. Ponomarev, Aleksey N. Kosarev, Svetlana S. Karakalcheva" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20515" ["VALUE"]=> array(2) { ["TEXT"]=> string(94) "Yugra Research Institute of Cellular Technologies with Stem Cell Bank, Khanty-Mansiysk, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(94) "Yugra Research Institute of Cellular Technologies with Stem Cell Bank, Khanty-Mansiysk, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20516" ["VALUE"]=> array(2) { ["TEXT"]=> string(6709) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Ensuring high and predictable safety of stored hematopoietic stem cells (HSC) after their thawing and performing autologous transplantation is one of the main conditions for the further successful recovery of hemopoiesis after high-dose chemotherapy in patients with hemoblastosis. It is believed that the method of cryopreservation HSC has long been worked out and leads to the expected results, therefore usually used harvested HSC dose only. However, with the use of modern and reliable quality control, universally applied cryopreservation methods of HSC cannot always warrant sufficient integrity of these cells (Table 1). It is well known that the safety of stored HSC is provided by a cryoprotectant, which prevents the cells from osmotic shock when they are frozen and thawed. A cryoprotectant with dimethyl sulfoxide (DMSO) is generally introduced via a syringe into the HSC suspension. At the same time, the final DMSO concentration in 5-10% is reached already in the cryopacket with the graft. However, a cryoprotectant with concentrated DMSO (more than 50%) upon contact with the cell, in view of its physicochemical properties, can lead to its partial destruction before freezing. Thus, increasing safety for HSC can be reduced by destructive effects, which may be due to the initially high concentration of DMSO in the cryoprotectant. To this end, we developed and tested a new method for introducing DMSO into the HSC transplant using a specially designed apparatus, i.e., an automated DMSO introduction system (patent pending). The principle of operation of this system excludes prolonged contact of concentrated DMSO with HSC transplant. </p> <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> The aim of our study was to compare the safety of HSCs using an automated and manual method of DMSO introduction. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> Peripheral blood stem cell samples (n=25) were obtained by apheresis from the patients with oncohematological diseases. For the control series (group I), DMSO introduction into a cryopacket with HSC graft was performed manually. In experimental series (group II), DMSO was introduced into the HSC transplant by a new automated method. A standard cryoprotectant (55% DMSO Dex 40) was used, the final DMSO concentration was 7.5%. Freezing (at the same time groups I and II) was performed in a software-assisted freezer with a validated 6-step program. Storage was carried out in liquid nitrogen. The cryopackets were thawed in a water bath at +40 for 1 min. Evaluation of viable HSCs numbers and their total colony-forming activity (CFU) was performed before and after the cryoprotection, as well as after thawing. To get more reliable results, the defrosted samples were taken from the cryopackets. The amounts of HSC was estimated by flow cytometric assay (CD34+/CD45dim/7AAD phenotype), according to the ISHAGE protocol. The colony-forming activity of HSC was evaluated by culturing them for 14 days (Methocult H4435) followed by counting total colonies (CFU).<br> <img width="781" alt="25_Tables.png" src="/upload/medialibrary/3ac/25_tables.png" height="360" title="25_Tables.png"> </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Similar viability indexes were revealed when testing the samples from the treatment series I and II. This fact may be due to the same incubation effect of DMSO on HSC, related to the duration of the analysis by flow cytometry. Thus, the exposure effect of DMSO on HSC is modelled. Hence, in absence of immediate freezing of HSC after DMSO introduction, the damaging effects are associated with the destructive physico-chemical effects of DMSO to cells, regardless of the manner of DMSO introduction. It is generally accepted to freeze the transplant immediately after DMSO introduction. During this short time interval, only those cell lesions that are manifested immediately after the initial exposure to DMSO are conserved. Therefore, the dependence of the quality control of HSC safety after introducing the cryoprotectant by the method 2 could be more reliably estimated after defrosting.<br> <img width="377" alt="25_Figure.png" src="/upload/medialibrary/b22/25_figure.png" height="223" title="25_Figure.png"> </p> <h2 style="text-align: justify;">Figure 1. Recovery of total HSCs, viable cells and colony- forming units in cryopreserved HSCs treated with DMSO at different regimens</h2> <p style="text-align: justify;"> According to the results shown in the figure 1, the safety of HSC after defrosting is significantly higher by 14% (p≤0.05) when using the automated system in comparison with manual mode. Given all other equal conditions, the total losses of HSC after defrosting with the manual method averaged 20%, with an automated technique, 6%. At the same time, 6% include both HSC losses when DMSO is introduced, and HSC losses during the freezing procedure. Therefore, the losses caused by freezing can be assumed to be the same when using different methods of introducing DMSO. Therefore, in the manual process, the losses are associated with the step of DMSO introduction. We are thinking that the average preservation rate of 94% is due to the method of introducing DMSO using an automated system. The principle of operation of the automated system allows one to reduce the momentary damaging effect of the initial concentrated DMSO solution on HSC and to ensure its smoother dilution to the required final DMSO concentration of 7.5%. The results presented in the table and in the figure also show that DMSO at the stage of introduction at exposure may have a greater negative impact on HSC than the procedure for freezing the graft. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The safety of HSC when using an automated system is significantly higher by 14% compared to manual mode. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cells, cryopreservation, dimethyl sulfoxide, autologous transplantation. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6277) "
Introduction
Ensuring high and predictable safety of stored hematopoietic stem cells (HSC) after their thawing and performing autologous transplantation is one of the main conditions for the further successful recovery of hemopoiesis after high-dose chemotherapy in patients with hemoblastosis. It is believed that the method of cryopreservation HSC has long been worked out and leads to the expected results, therefore usually used harvested HSC dose only. However, with the use of modern and reliable quality control, universally applied cryopreservation methods of HSC cannot always warrant sufficient integrity of these cells (Table 1). It is well known that the safety of stored HSC is provided by a cryoprotectant, which prevents the cells from osmotic shock when they are frozen and thawed. A cryoprotectant with dimethyl sulfoxide (DMSO) is generally introduced via a syringe into the HSC suspension. At the same time, the final DMSO concentration in 5-10% is reached already in the cryopacket with the graft. However, a cryoprotectant with concentrated DMSO (more than 50%) upon contact with the cell, in view of its physicochemical properties, can lead to its partial destruction before freezing. Thus, increasing safety for HSC can be reduced by destructive effects, which may be due to the initially high concentration of DMSO in the cryoprotectant. To this end, we developed and tested a new method for introducing DMSO into the HSC transplant using a specially designed apparatus, i.e., an automated DMSO introduction system (patent pending). The principle of operation of this system excludes prolonged contact of concentrated DMSO with HSC transplant.
Aim
The aim of our study was to compare the safety of HSCs using an automated and manual method of DMSO introduction.
Materials and methods
Peripheral blood stem cell samples (n=25) were obtained by apheresis from the patients with oncohematological diseases. For the control series (group I), DMSO introduction into a cryopacket with HSC graft was performed manually. In experimental series (group II), DMSO was introduced into the HSC transplant by a new automated method. A standard cryoprotectant (55% DMSO Dex 40) was used, the final DMSO concentration was 7.5%. Freezing (at the same time groups I and II) was performed in a software-assisted freezer with a validated 6-step program. Storage was carried out in liquid nitrogen. The cryopackets were thawed in a water bath at +40 for 1 min. Evaluation of viable HSCs numbers and their total colony-forming activity (CFU) was performed before and after the cryoprotection, as well as after thawing. To get more reliable results, the defrosted samples were taken from the cryopackets. The amounts of HSC was estimated by flow cytometric assay (CD34+/CD45dim/7AAD phenotype), according to the ISHAGE protocol. The colony-forming activity of HSC was evaluated by culturing them for 14 days (Methocult H4435) followed by counting total colonies (CFU).

Results
Similar viability indexes were revealed when testing the samples from the treatment series I and II. This fact may be due to the same incubation effect of DMSO on HSC, related to the duration of the analysis by flow cytometry. Thus, the exposure effect of DMSO on HSC is modelled. Hence, in absence of immediate freezing of HSC after DMSO introduction, the damaging effects are associated with the destructive physico-chemical effects of DMSO to cells, regardless of the manner of DMSO introduction. It is generally accepted to freeze the transplant immediately after DMSO introduction. During this short time interval, only those cell lesions that are manifested immediately after the initial exposure to DMSO are conserved. Therefore, the dependence of the quality control of HSC safety after introducing the cryoprotectant by the method 2 could be more reliably estimated after defrosting.

Figure 1. Recovery of total HSCs, viable cells and colony- forming units in cryopreserved HSCs treated with DMSO at different regimens
According to the results shown in the figure 1, the safety of HSC after defrosting is significantly higher by 14% (p≤0.05) when using the automated system in comparison with manual mode. Given all other equal conditions, the total losses of HSC after defrosting with the manual method averaged 20%, with an automated technique, 6%. At the same time, 6% include both HSC losses when DMSO is introduced, and HSC losses during the freezing procedure. Therefore, the losses caused by freezing can be assumed to be the same when using different methods of introducing DMSO. Therefore, in the manual process, the losses are associated with the step of DMSO introduction. We are thinking that the average preservation rate of 94% is due to the method of introducing DMSO using an automated system. The principle of operation of the automated system allows one to reduce the momentary damaging effect of the initial concentrated DMSO solution on HSC and to ensure its smoother dilution to the required final DMSO concentration of 7.5%. The results presented in the table and in the figure also show that DMSO at the stage of introduction at exposure may have a greater negative impact on HSC than the procedure for freezing the graft.
Conclusion
The safety of HSC when using an automated system is significantly higher by 14% compared to manual mode.
Keywords
Hematopoietic stem cells, cryopreservation, dimethyl sulfoxide, autologous transplantation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20517" ["VALUE"]=> string(113) "A novel method of dimethyl sulfoxide introduction improves preservation of cryopreserved hematopoietic stem cells" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(113) "A novel method of dimethyl sulfoxide introduction improves preservation of cryopreserved hematopoietic stem cells" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20779" ["VALUE"]=> string(4) "1417" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1417" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20780" ["VALUE"]=> string(4) "1418" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1418" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20514" ["VALUE"]=> array(2) { ["TEXT"]=> string(127) "Evgeniy V. Korotaev, Sergey V. Andrunkin, Andrey A. Stepanov, Sergey S. Ponomarev, Aleksey N. Kosarev, Svetlana S. Karakalcheva" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(127) "Evgeniy V. Korotaev, Sergey V. Andrunkin, Andrey A. Stepanov, Sergey S. Ponomarev, Aleksey N. Kosarev, Svetlana S. Karakalcheva" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(127) "Evgeniy V. Korotaev, Sergey V. Andrunkin, Andrey A. Stepanov, Sergey S. Ponomarev, Aleksey N. Kosarev, Svetlana S. Karakalcheva" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20516" ["VALUE"]=> array(2) { ["TEXT"]=> string(6709) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Ensuring high and predictable safety of stored hematopoietic stem cells (HSC) after their thawing and performing autologous transplantation is one of the main conditions for the further successful recovery of hemopoiesis after high-dose chemotherapy in patients with hemoblastosis. It is believed that the method of cryopreservation HSC has long been worked out and leads to the expected results, therefore usually used harvested HSC dose only. However, with the use of modern and reliable quality control, universally applied cryopreservation methods of HSC cannot always warrant sufficient integrity of these cells (Table 1). It is well known that the safety of stored HSC is provided by a cryoprotectant, which prevents the cells from osmotic shock when they are frozen and thawed. A cryoprotectant with dimethyl sulfoxide (DMSO) is generally introduced via a syringe into the HSC suspension. At the same time, the final DMSO concentration in 5-10% is reached already in the cryopacket with the graft. However, a cryoprotectant with concentrated DMSO (more than 50%) upon contact with the cell, in view of its physicochemical properties, can lead to its partial destruction before freezing. Thus, increasing safety for HSC can be reduced by destructive effects, which may be due to the initially high concentration of DMSO in the cryoprotectant. To this end, we developed and tested a new method for introducing DMSO into the HSC transplant using a specially designed apparatus, i.e., an automated DMSO introduction system (patent pending). The principle of operation of this system excludes prolonged contact of concentrated DMSO with HSC transplant. </p> <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> The aim of our study was to compare the safety of HSCs using an automated and manual method of DMSO introduction. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> Peripheral blood stem cell samples (n=25) were obtained by apheresis from the patients with oncohematological diseases. For the control series (group I), DMSO introduction into a cryopacket with HSC graft was performed manually. In experimental series (group II), DMSO was introduced into the HSC transplant by a new automated method. A standard cryoprotectant (55% DMSO Dex 40) was used, the final DMSO concentration was 7.5%. Freezing (at the same time groups I and II) was performed in a software-assisted freezer with a validated 6-step program. Storage was carried out in liquid nitrogen. The cryopackets were thawed in a water bath at +40 for 1 min. Evaluation of viable HSCs numbers and their total colony-forming activity (CFU) was performed before and after the cryoprotection, as well as after thawing. To get more reliable results, the defrosted samples were taken from the cryopackets. The amounts of HSC was estimated by flow cytometric assay (CD34+/CD45dim/7AAD phenotype), according to the ISHAGE protocol. The colony-forming activity of HSC was evaluated by culturing them for 14 days (Methocult H4435) followed by counting total colonies (CFU).<br> <img width="781" alt="25_Tables.png" src="/upload/medialibrary/3ac/25_tables.png" height="360" title="25_Tables.png"> </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Similar viability indexes were revealed when testing the samples from the treatment series I and II. This fact may be due to the same incubation effect of DMSO on HSC, related to the duration of the analysis by flow cytometry. Thus, the exposure effect of DMSO on HSC is modelled. Hence, in absence of immediate freezing of HSC after DMSO introduction, the damaging effects are associated with the destructive physico-chemical effects of DMSO to cells, regardless of the manner of DMSO introduction. It is generally accepted to freeze the transplant immediately after DMSO introduction. During this short time interval, only those cell lesions that are manifested immediately after the initial exposure to DMSO are conserved. Therefore, the dependence of the quality control of HSC safety after introducing the cryoprotectant by the method 2 could be more reliably estimated after defrosting.<br> <img width="377" alt="25_Figure.png" src="/upload/medialibrary/b22/25_figure.png" height="223" title="25_Figure.png"> </p> <h2 style="text-align: justify;">Figure 1. Recovery of total HSCs, viable cells and colony- forming units in cryopreserved HSCs treated with DMSO at different regimens</h2> <p style="text-align: justify;"> According to the results shown in the figure 1, the safety of HSC after defrosting is significantly higher by 14% (p≤0.05) when using the automated system in comparison with manual mode. Given all other equal conditions, the total losses of HSC after defrosting with the manual method averaged 20%, with an automated technique, 6%. At the same time, 6% include both HSC losses when DMSO is introduced, and HSC losses during the freezing procedure. Therefore, the losses caused by freezing can be assumed to be the same when using different methods of introducing DMSO. Therefore, in the manual process, the losses are associated with the step of DMSO introduction. We are thinking that the average preservation rate of 94% is due to the method of introducing DMSO using an automated system. The principle of operation of the automated system allows one to reduce the momentary damaging effect of the initial concentrated DMSO solution on HSC and to ensure its smoother dilution to the required final DMSO concentration of 7.5%. The results presented in the table and in the figure also show that DMSO at the stage of introduction at exposure may have a greater negative impact on HSC than the procedure for freezing the graft. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The safety of HSC when using an automated system is significantly higher by 14% compared to manual mode. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cells, cryopreservation, dimethyl sulfoxide, autologous transplantation. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6277) "Introduction
Ensuring high and predictable safety of stored hematopoietic stem cells (HSC) after their thawing and performing autologous transplantation is one of the main conditions for the further successful recovery of hemopoiesis after high-dose chemotherapy in patients with hemoblastosis. It is believed that the method of cryopreservation HSC has long been worked out and leads to the expected results, therefore usually used harvested HSC dose only. However, with the use of modern and reliable quality control, universally applied cryopreservation methods of HSC cannot always warrant sufficient integrity of these cells (Table 1). It is well known that the safety of stored HSC is provided by a cryoprotectant, which prevents the cells from osmotic shock when they are frozen and thawed. A cryoprotectant with dimethyl sulfoxide (DMSO) is generally introduced via a syringe into the HSC suspension. At the same time, the final DMSO concentration in 5-10% is reached already in the cryopacket with the graft. However, a cryoprotectant with concentrated DMSO (more than 50%) upon contact with the cell, in view of its physicochemical properties, can lead to its partial destruction before freezing. Thus, increasing safety for HSC can be reduced by destructive effects, which may be due to the initially high concentration of DMSO in the cryoprotectant. To this end, we developed and tested a new method for introducing DMSO into the HSC transplant using a specially designed apparatus, i.e., an automated DMSO introduction system (patent pending). The principle of operation of this system excludes prolonged contact of concentrated DMSO with HSC transplant.
Aim
The aim of our study was to compare the safety of HSCs using an automated and manual method of DMSO introduction.
Materials and methods
Peripheral blood stem cell samples (n=25) were obtained by apheresis from the patients with oncohematological diseases. For the control series (group I), DMSO introduction into a cryopacket with HSC graft was performed manually. In experimental series (group II), DMSO was introduced into the HSC transplant by a new automated method. A standard cryoprotectant (55% DMSO Dex 40) was used, the final DMSO concentration was 7.5%. Freezing (at the same time groups I and II) was performed in a software-assisted freezer with a validated 6-step program. Storage was carried out in liquid nitrogen. The cryopackets were thawed in a water bath at +40 for 1 min. Evaluation of viable HSCs numbers and their total colony-forming activity (CFU) was performed before and after the cryoprotection, as well as after thawing. To get more reliable results, the defrosted samples were taken from the cryopackets. The amounts of HSC was estimated by flow cytometric assay (CD34+/CD45dim/7AAD phenotype), according to the ISHAGE protocol. The colony-forming activity of HSC was evaluated by culturing them for 14 days (Methocult H4435) followed by counting total colonies (CFU).

Results
Similar viability indexes were revealed when testing the samples from the treatment series I and II. This fact may be due to the same incubation effect of DMSO on HSC, related to the duration of the analysis by flow cytometry. Thus, the exposure effect of DMSO on HSC is modelled. Hence, in absence of immediate freezing of HSC after DMSO introduction, the damaging effects are associated with the destructive physico-chemical effects of DMSO to cells, regardless of the manner of DMSO introduction. It is generally accepted to freeze the transplant immediately after DMSO introduction. During this short time interval, only those cell lesions that are manifested immediately after the initial exposure to DMSO are conserved. Therefore, the dependence of the quality control of HSC safety after introducing the cryoprotectant by the method 2 could be more reliably estimated after defrosting.

Figure 1. Recovery of total HSCs, viable cells and colony- forming units in cryopreserved HSCs treated with DMSO at different regimens
According to the results shown in the figure 1, the safety of HSC after defrosting is significantly higher by 14% (p≤0.05) when using the automated system in comparison with manual mode. Given all other equal conditions, the total losses of HSC after defrosting with the manual method averaged 20%, with an automated technique, 6%. At the same time, 6% include both HSC losses when DMSO is introduced, and HSC losses during the freezing procedure. Therefore, the losses caused by freezing can be assumed to be the same when using different methods of introducing DMSO. Therefore, in the manual process, the losses are associated with the step of DMSO introduction. We are thinking that the average preservation rate of 94% is due to the method of introducing DMSO using an automated system. The principle of operation of the automated system allows one to reduce the momentary damaging effect of the initial concentrated DMSO solution on HSC and to ensure its smoother dilution to the required final DMSO concentration of 7.5%. The results presented in the table and in the figure also show that DMSO at the stage of introduction at exposure may have a greater negative impact on HSC than the procedure for freezing the graft.
Conclusion
The safety of HSC when using an automated system is significantly higher by 14% compared to manual mode.
Keywords
Hematopoietic stem cells, cryopreservation, dimethyl sulfoxide, autologous transplantation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6277) "Introduction
Ensuring high and predictable safety of stored hematopoietic stem cells (HSC) after their thawing and performing autologous transplantation is one of the main conditions for the further successful recovery of hemopoiesis after high-dose chemotherapy in patients with hemoblastosis. It is believed that the method of cryopreservation HSC has long been worked out and leads to the expected results, therefore usually used harvested HSC dose only. However, with the use of modern and reliable quality control, universally applied cryopreservation methods of HSC cannot always warrant sufficient integrity of these cells (Table 1). It is well known that the safety of stored HSC is provided by a cryoprotectant, which prevents the cells from osmotic shock when they are frozen and thawed. A cryoprotectant with dimethyl sulfoxide (DMSO) is generally introduced via a syringe into the HSC suspension. At the same time, the final DMSO concentration in 5-10% is reached already in the cryopacket with the graft. However, a cryoprotectant with concentrated DMSO (more than 50%) upon contact with the cell, in view of its physicochemical properties, can lead to its partial destruction before freezing. Thus, increasing safety for HSC can be reduced by destructive effects, which may be due to the initially high concentration of DMSO in the cryoprotectant. To this end, we developed and tested a new method for introducing DMSO into the HSC transplant using a specially designed apparatus, i.e., an automated DMSO introduction system (patent pending). The principle of operation of this system excludes prolonged contact of concentrated DMSO with HSC transplant.
Aim
The aim of our study was to compare the safety of HSCs using an automated and manual method of DMSO introduction.
Materials and methods
Peripheral blood stem cell samples (n=25) were obtained by apheresis from the patients with oncohematological diseases. For the control series (group I), DMSO introduction into a cryopacket with HSC graft was performed manually. In experimental series (group II), DMSO was introduced into the HSC transplant by a new automated method. A standard cryoprotectant (55% DMSO Dex 40) was used, the final DMSO concentration was 7.5%. Freezing (at the same time groups I and II) was performed in a software-assisted freezer with a validated 6-step program. Storage was carried out in liquid nitrogen. The cryopackets were thawed in a water bath at +40 for 1 min. Evaluation of viable HSCs numbers and their total colony-forming activity (CFU) was performed before and after the cryoprotection, as well as after thawing. To get more reliable results, the defrosted samples were taken from the cryopackets. The amounts of HSC was estimated by flow cytometric assay (CD34+/CD45dim/7AAD phenotype), according to the ISHAGE protocol. The colony-forming activity of HSC was evaluated by culturing them for 14 days (Methocult H4435) followed by counting total colonies (CFU).

Results
Similar viability indexes were revealed when testing the samples from the treatment series I and II. This fact may be due to the same incubation effect of DMSO on HSC, related to the duration of the analysis by flow cytometry. Thus, the exposure effect of DMSO on HSC is modelled. Hence, in absence of immediate freezing of HSC after DMSO introduction, the damaging effects are associated with the destructive physico-chemical effects of DMSO to cells, regardless of the manner of DMSO introduction. It is generally accepted to freeze the transplant immediately after DMSO introduction. During this short time interval, only those cell lesions that are manifested immediately after the initial exposure to DMSO are conserved. Therefore, the dependence of the quality control of HSC safety after introducing the cryoprotectant by the method 2 could be more reliably estimated after defrosting.

Figure 1. Recovery of total HSCs, viable cells and colony- forming units in cryopreserved HSCs treated with DMSO at different regimens
According to the results shown in the figure 1, the safety of HSC after defrosting is significantly higher by 14% (p≤0.05) when using the automated system in comparison with manual mode. Given all other equal conditions, the total losses of HSC after defrosting with the manual method averaged 20%, with an automated technique, 6%. At the same time, 6% include both HSC losses when DMSO is introduced, and HSC losses during the freezing procedure. Therefore, the losses caused by freezing can be assumed to be the same when using different methods of introducing DMSO. Therefore, in the manual process, the losses are associated with the step of DMSO introduction. We are thinking that the average preservation rate of 94% is due to the method of introducing DMSO using an automated system. The principle of operation of the automated system allows one to reduce the momentary damaging effect of the initial concentrated DMSO solution on HSC and to ensure its smoother dilution to the required final DMSO concentration of 7.5%. The results presented in the table and in the figure also show that DMSO at the stage of introduction at exposure may have a greater negative impact on HSC than the procedure for freezing the graft.
Conclusion
The safety of HSC when using an automated system is significantly higher by 14% compared to manual mode.
Keywords
Hematopoietic stem cells, cryopreservation, dimethyl sulfoxide, autologous transplantation.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20517" ["VALUE"]=> string(113) "A novel method of dimethyl sulfoxide introduction improves preservation of cryopreserved hematopoietic stem cells" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(113) "A novel method of dimethyl sulfoxide introduction improves preservation of cryopreserved hematopoietic stem cells" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(113) "A novel method of dimethyl sulfoxide introduction improves preservation of cryopreserved hematopoietic stem cells" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20515" ["VALUE"]=> array(2) { ["TEXT"]=> string(94) "Yugra Research Institute of Cellular Technologies with Stem Cell Bank, Khanty-Mansiysk, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(94) "Yugra Research Institute of Cellular Technologies with Stem Cell Bank, Khanty-Mansiysk, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(94) "Yugra Research Institute of Cellular Technologies with Stem Cell Bank, Khanty-Mansiysk, Russia" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20511" ["VALUE"]=> array(2) { ["TEXT"]=> string(228) "Евгений В. Коротаев, Сергей В. Андрюнькин, Андрей А. Степанов, Сергей А. Пономарев, Алексей Н. Косарев, Светлана С. Каракальчева" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(228) "Евгений В. Коротаев, Сергей В. Андрюнькин, Андрей А. Степанов, Сергей А. Пономарев, Алексей Н. Косарев, Светлана С. Каракальчева" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(228) "Евгений В. Коротаев, Сергей В. Андрюнькин, Андрей А. Степанов, Сергей А. Пономарев, Алексей Н. Косарев, Светлана С. Каракальчева" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20513" ["VALUE"]=> array(2) { ["TEXT"]=> string(11551) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Обеспечение высокой и прогнозируемой сохранности гемопоэтических стволовых клеток (ГСК) после их размораживания и проведения аутологичной трансплантации – одно из ключевых условий для дальнейшего успешного восстановления гемопоэза после высокодозной химиотерапии у пациентов с гемобластозами. Считается, что методика криоконсервирования ГСК давно отработана и приводит к ожидаемым результатам, поэтому обычно учитывается только заготовленная доза ГСК. Однако, при использовании современного и достоверного контроля качества, повсеместно применяемые методы криоконсервации ГСК не всегда могут гарантировать достаточную сохранность данных клеток (Табл. 1). Общеизвестно, что сохранность ГСК при хранении обеспечивает криопротектор, защищающий клетки от осмотического шока при их замораживании. Криопротектор с ДМСО общепринято вводить при помощи шприца в трансплантат ГСК. При этом конечная концентрация ДМСО в 5-10% достигается уже в криопакете с трансплантатом. Однако криопротектор с концентрированным ДМСО (более 50%) при контакте с клеткой, ввиду своих физико-химических свойств, может привести к ее частичной деструкции еще до замораживания. Таким образом, повысить сохранность ГСК можно снизив деструктивное воздействие, которое может быть связано с исходной высокой концентрацией ДМСО в криопротекторе. Для этого нами разработан и апробирован новый способ введения ДМСО в трансплантат ГСК при помощи специального сконструированного аппарата – автоматизированной системы введения ДМСО (на стадии патентования). Принцип действия данной системы исключает продолжительный контакт концентрированного ДМСО с трансплантатом ГСК. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель работы состояла в сравнении сохранности ГСК при использовании автоматизированного и ручного способа введения ДМСО. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Лейкоконцентрат ГСК периферической крови (n=25), полученный путем афереза у пациентов с онкогематологическими заболеваниями. Контрольная группа I – введение ДМСО в криопакет с трансплантатом ГСК выполняли ручным способом. Опытная группа II – введение ДМСО в трансплантат ГСК выполняли новым автоматизированным способом. Использовали стандартный криопротектор (55% DMSO Dex 40), конечная концентрация ДМСО – 7,5%. Замораживание (одновременно группы I и II) проводили на программном замораживателе по валидированной 6-ти ступенчатой программе. Хранение осуществляли в жидком азоте. Размораживание криопакетов проводили на водяной бане при +40 в течение 1 мин. Анализ количества жизнеспособных ГСК и их суммарной колониеобразующей активности (КОЕ) выполнялся до и после введения криопротектора, а также после размораживания. После размораживания для достоверности пробы отбирались из криопакетов. Количество ГСК оценивалось по фенотипу CD34+/CD45dim/7AAD проточной цитометрией по протоколу ISHAGE. Колониеобразующая активность ГСК оценивалась путем их культивирования в течение 14 суток (Methocult H4435) с последующим подсчетом суммарных колоний (КОЕ). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Согласно представленным в таблице 2 результатам, сохранность ГСК в группах I и II после введения ДМСО не отличается. Идентичные результаты, вероятно, обусловлены одинаковым инкубационным воздействием ДМСО на ГСК, связанным с продолжительностью проведения анализа методом проточной цитометрии. Тем самым моделируется экспозиционное воздействие ДМСО на ГСК. Из этого следует, что при отсутствии немедленного замораживания ГСК после введения ДМСО, повреждающие эффекты связаны с деструктивными физико-химическими свойствами ДМСО по отношению к клеткам, причем не зависимо от способа введения ДМСО.<br> Общепринято немедленно замораживать трансплантат сразу после введения ДМСО. В этот короткий временной промежуток будут законсервированы только те повреждения клеток, которые проявились сразу после первичного воздействия ДМСО. Поэтому зависимость контроля качества сохранности ГСК после введения криопротектора по методу 2 может быть оценена с большей достоверностью после размораживания. Контроль качества после размораживания отражен на рис. 1. Согласно представленным на рисунке результатам, сохранность ГСК после размораживания достоверно выше на 14% (p≤0.05) при использовании автоматизированной системы в сравнении с ручным способом. При прочих равных условиях исследования, суммарные потери ГСК после размораживания при ручном способе составили в среднем 20%, при автоматизированном – 6%. Они включают потери ГСК при введении ДМСО, а также утрату ГСК в процессе замораживания. Поэтому потери, вызванные замораживанием, можно принять как одинаковые при использовании разных способов введения ДМСО. Следовательно, при ручном способе потери связаны с этапом введения ДМСО. Мы полагаем, что средняя сохранность в 94% обусловлена способом введения ДМСО с использованием автоматизированной системы. Принцип работы автоматизированной системы позволяет снизить одномоментное повреждающее влияние исходного концентрированногораствора ДМСО на ГСК и обеспечить его более плавное разбавление до необходимой конечной концентрации ДМСО в 7,5%. Результаты, представленные в таблице и на рисунке, также показывают, что ДМСО на этапе его введения при экспозиции может оказывать большее негативное воздействие на ГСК, чем процедура замораживания трансплантата. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Сохранность ГСК при использовании автоматизированной системы введения ДМСО достоверно (на 14%) выше в сравнении с ручным способом. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Гемопоэтические стволовые клетки, криоконсервация, димитилсульфоксид, аутологичная трансплантация.<br> <img width="783" alt="25_таблицы.png" src="/upload/medialibrary/804/25_tablitsy.png" height="369" title="25_таблицы.png"><br> <br> <img width="375" alt="25_Рисунок.png" src="/upload/medialibrary/c2f/25_risunok.png" height="219" title="25_Рисунок.png"> </p> <h2 style="text-align: justify;">Рисунок 1. Выход гемопоэтических клеток после ручного или автоматизированного введения ДМСО и криоконсервирования по различным критериям</h2> <h2></h2> <br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(11111) "Введение
Обеспечение высокой и прогнозируемой сохранности гемопоэтических стволовых клеток (ГСК) после их размораживания и проведения аутологичной трансплантации – одно из ключевых условий для дальнейшего успешного восстановления гемопоэза после высокодозной химиотерапии у пациентов с гемобластозами. Считается, что методика криоконсервирования ГСК давно отработана и приводит к ожидаемым результатам, поэтому обычно учитывается только заготовленная доза ГСК. Однако, при использовании современного и достоверного контроля качества, повсеместно применяемые методы криоконсервации ГСК не всегда могут гарантировать достаточную сохранность данных клеток (Табл. 1). Общеизвестно, что сохранность ГСК при хранении обеспечивает криопротектор, защищающий клетки от осмотического шока при их замораживании. Криопротектор с ДМСО общепринято вводить при помощи шприца в трансплантат ГСК. При этом конечная концентрация ДМСО в 5-10% достигается уже в криопакете с трансплантатом. Однако криопротектор с концентрированным ДМСО (более 50%) при контакте с клеткой, ввиду своих физико-химических свойств, может привести к ее частичной деструкции еще до замораживания. Таким образом, повысить сохранность ГСК можно снизив деструктивное воздействие, которое может быть связано с исходной высокой концентрацией ДМСО в криопротекторе. Для этого нами разработан и апробирован новый способ введения ДМСО в трансплантат ГСК при помощи специального сконструированного аппарата – автоматизированной системы введения ДМСО (на стадии патентования). Принцип действия данной системы исключает продолжительный контакт концентрированного ДМСО с трансплантатом ГСК.
Цель
Цель работы состояла в сравнении сохранности ГСК при использовании автоматизированного и ручного способа введения ДМСО.
Материалы и методы
Лейкоконцентрат ГСК периферической крови (n=25), полученный путем афереза у пациентов с онкогематологическими заболеваниями. Контрольная группа I – введение ДМСО в криопакет с трансплантатом ГСК выполняли ручным способом. Опытная группа II – введение ДМСО в трансплантат ГСК выполняли новым автоматизированным способом. Использовали стандартный криопротектор (55% DMSO Dex 40), конечная концентрация ДМСО – 7,5%. Замораживание (одновременно группы I и II) проводили на программном замораживателе по валидированной 6-ти ступенчатой программе. Хранение осуществляли в жидком азоте. Размораживание криопакетов проводили на водяной бане при +40 в течение 1 мин. Анализ количества жизнеспособных ГСК и их суммарной колониеобразующей активности (КОЕ) выполнялся до и после введения криопротектора, а также после размораживания. После размораживания для достоверности пробы отбирались из криопакетов. Количество ГСК оценивалось по фенотипу CD34+/CD45dim/7AAD проточной цитометрией по протоколу ISHAGE. Колониеобразующая активность ГСК оценивалась путем их культивирования в течение 14 суток (Methocult H4435) с последующим подсчетом суммарных колоний (КОЕ).
Результаты
Согласно представленным в таблице 2 результатам, сохранность ГСК в группах I и II после введения ДМСО не отличается. Идентичные результаты, вероятно, обусловлены одинаковым инкубационным воздействием ДМСО на ГСК, связанным с продолжительностью проведения анализа методом проточной цитометрии. Тем самым моделируется экспозиционное воздействие ДМСО на ГСК. Из этого следует, что при отсутствии немедленного замораживания ГСК после введения ДМСО, повреждающие эффекты связаны с деструктивными физико-химическими свойствами ДМСО по отношению к клеткам, причем не зависимо от способа введения ДМСО.
Общепринято немедленно замораживать трансплантат сразу после введения ДМСО. В этот короткий временной промежуток будут законсервированы только те повреждения клеток, которые проявились сразу после первичного воздействия ДМСО. Поэтому зависимость контроля качества сохранности ГСК после введения криопротектора по методу 2 может быть оценена с большей достоверностью после размораживания. Контроль качества после размораживания отражен на рис. 1. Согласно представленным на рисунке результатам, сохранность ГСК после размораживания достоверно выше на 14% (p≤0.05) при использовании автоматизированной системы в сравнении с ручным способом. При прочих равных условиях исследования, суммарные потери ГСК после размораживания при ручном способе составили в среднем 20%, при автоматизированном – 6%. Они включают потери ГСК при введении ДМСО, а также утрату ГСК в процессе замораживания. Поэтому потери, вызванные замораживанием, можно принять как одинаковые при использовании разных способов введения ДМСО. Следовательно, при ручном способе потери связаны с этапом введения ДМСО. Мы полагаем, что средняя сохранность в 94% обусловлена способом введения ДМСО с использованием автоматизированной системы. Принцип работы автоматизированной системы позволяет снизить одномоментное повреждающее влияние исходного концентрированногораствора ДМСО на ГСК и обеспечить его более плавное разбавление до необходимой конечной концентрации ДМСО в 7,5%. Результаты, представленные в таблице и на рисунке, также показывают, что ДМСО на этапе его введения при экспозиции может оказывать большее негативное воздействие на ГСК, чем процедура замораживания трансплантата.
Заключение
Сохранность ГСК при использовании автоматизированной системы введения ДМСО достоверно (на 14%) выше в сравнении с ручным способом.
Ключевые слова
Гемопоэтические стволовые клетки, криоконсервация, димитилсульфоксид, аутологичная трансплантация.


Рисунок 1. Выход гемопоэтических клеток после ручного или автоматизированного введения ДМСО и криоконсервирования по различным критериям
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(11111) "
Введение
Обеспечение высокой и прогнозируемой сохранности гемопоэтических стволовых клеток (ГСК) после их размораживания и проведения аутологичной трансплантации – одно из ключевых условий для дальнейшего успешного восстановления гемопоэза после высокодозной химиотерапии у пациентов с гемобластозами. Считается, что методика криоконсервирования ГСК давно отработана и приводит к ожидаемым результатам, поэтому обычно учитывается только заготовленная доза ГСК. Однако, при использовании современного и достоверного контроля качества, повсеместно применяемые методы криоконсервации ГСК не всегда могут гарантировать достаточную сохранность данных клеток (Табл. 1). Общеизвестно, что сохранность ГСК при хранении обеспечивает криопротектор, защищающий клетки от осмотического шока при их замораживании. Криопротектор с ДМСО общепринято вводить при помощи шприца в трансплантат ГСК. При этом конечная концентрация ДМСО в 5-10% достигается уже в криопакете с трансплантатом. Однако криопротектор с концентрированным ДМСО (более 50%) при контакте с клеткой, ввиду своих физико-химических свойств, может привести к ее частичной деструкции еще до замораживания. Таким образом, повысить сохранность ГСК можно снизив деструктивное воздействие, которое может быть связано с исходной высокой концентрацией ДМСО в криопротекторе. Для этого нами разработан и апробирован новый способ введения ДМСО в трансплантат ГСК при помощи специального сконструированного аппарата – автоматизированной системы введения ДМСО (на стадии патентования). Принцип действия данной системы исключает продолжительный контакт концентрированного ДМСО с трансплантатом ГСК.
Цель
Цель работы состояла в сравнении сохранности ГСК при использовании автоматизированного и ручного способа введения ДМСО.
Материалы и методы
Лейкоконцентрат ГСК периферической крови (n=25), полученный путем афереза у пациентов с онкогематологическими заболеваниями. Контрольная группа I – введение ДМСО в криопакет с трансплантатом ГСК выполняли ручным способом. Опытная группа II – введение ДМСО в трансплантат ГСК выполняли новым автоматизированным способом. Использовали стандартный криопротектор (55% DMSO Dex 40), конечная концентрация ДМСО – 7,5%. Замораживание (одновременно группы I и II) проводили на программном замораживателе по валидированной 6-ти ступенчатой программе. Хранение осуществляли в жидком азоте. Размораживание криопакетов проводили на водяной бане при +40 в течение 1 мин. Анализ количества жизнеспособных ГСК и их суммарной колониеобразующей активности (КОЕ) выполнялся до и после введения криопротектора, а также после размораживания. После размораживания для достоверности пробы отбирались из криопакетов. Количество ГСК оценивалось по фенотипу CD34+/CD45dim/7AAD проточной цитометрией по протоколу ISHAGE. Колониеобразующая активность ГСК оценивалась путем их культивирования в течение 14 суток (Methocult H4435) с последующим подсчетом суммарных колоний (КОЕ).
Результаты
Согласно представленным в таблице 2 результатам, сохранность ГСК в группах I и II после введения ДМСО не отличается. Идентичные результаты, вероятно, обусловлены одинаковым инкубационным воздействием ДМСО на ГСК, связанным с продолжительностью проведения анализа методом проточной цитометрии. Тем самым моделируется экспозиционное воздействие ДМСО на ГСК. Из этого следует, что при отсутствии немедленного замораживания ГСК после введения ДМСО, повреждающие эффекты связаны с деструктивными физико-химическими свойствами ДМСО по отношению к клеткам, причем не зависимо от способа введения ДМСО.
Общепринято немедленно замораживать трансплантат сразу после введения ДМСО. В этот короткий временной промежуток будут законсервированы только те повреждения клеток, которые проявились сразу после первичного воздействия ДМСО. Поэтому зависимость контроля качества сохранности ГСК после введения криопротектора по методу 2 может быть оценена с большей достоверностью после размораживания. Контроль качества после размораживания отражен на рис. 1. Согласно представленным на рисунке результатам, сохранность ГСК после размораживания достоверно выше на 14% (p≤0.05) при использовании автоматизированной системы в сравнении с ручным способом. При прочих равных условиях исследования, суммарные потери ГСК после размораживания при ручном способе составили в среднем 20%, при автоматизированном – 6%. Они включают потери ГСК при введении ДМСО, а также утрату ГСК в процессе замораживания. Поэтому потери, вызванные замораживанием, можно принять как одинаковые при использовании разных способов введения ДМСО. Следовательно, при ручном способе потери связаны с этапом введения ДМСО. Мы полагаем, что средняя сохранность в 94% обусловлена способом введения ДМСО с использованием автоматизированной системы. Принцип работы автоматизированной системы позволяет снизить одномоментное повреждающее влияние исходного концентрированногораствора ДМСО на ГСК и обеспечить его более плавное разбавление до необходимой конечной концентрации ДМСО в 7,5%. Результаты, представленные в таблице и на рисунке, также показывают, что ДМСО на этапе его введения при экспозиции может оказывать большее негативное воздействие на ГСК, чем процедура замораживания трансплантата.
Заключение
Сохранность ГСК при использовании автоматизированной системы введения ДМСО достоверно (на 14%) выше в сравнении с ручным способом.
Ключевые слова
Гемопоэтические стволовые клетки, криоконсервация, димитилсульфоксид, аутологичная трансплантация.


Рисунок 1. Выход гемопоэтических клеток после ручного или автоматизированного введения ДМСО и криоконсервирования по различным критериям
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20512" ["VALUE"]=> array(2) { ["TEXT"]=> string(142) "АУ «Югорский НИИ клеточных технологий», Ханты-Мансийск, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(142) "АУ «Югорский НИИ клеточных технологий», Ханты-Мансийск, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(142) "АУ «Югорский НИИ клеточных технологий», Ханты-Мансийск, Российская Федерация" } } } [9]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1573" ["~ID"]=> string(4) "1573" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(194) "Эпидемиологические характеристики и эффективность терапии у пациентов с ВИЧ-ассоциированными лимфомами" ["~NAME"]=> string(194) "Эпидемиологические характеристики и эффективность терапии у пациентов с ВИЧ-ассоциированными лимфомами" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:34:57" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:34:57" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/epidemiologicheskie-kharakteristiki-i-effektivnost-terapii-u-patsientov-s-vich-assotsiirovannymi-lim/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/epidemiologicheskie-kharakteristiki-i-effektivnost-terapii-u-patsientov-s-vich-assotsiirovannymi-lim/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "epidemiologicheskie-kharakteristiki-i-effektivnost-terapii-u-patsientov-s-vich-assotsiirovannymi-lim" ["~CODE"]=> string(100) "epidemiologicheskie-kharakteristiki-i-effektivnost-terapii-u-patsientov-s-vich-assotsiirovannymi-lim" ["EXTERNAL_ID"]=> string(4) "1573" ["~EXTERNAL_ID"]=> string(4) "1573" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(194) "Эпидемиологические характеристики и эффективность терапии у пациентов с ВИЧ-ассоциированными лимфомами" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(272) "Эпидемиологические характеристики и эффективность терапии у пациентов с ВИЧ-ассоциированными лимфомамиEpidemiological features and efficacy of treatment in HIV-associated lymphomas" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(7185) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Пациенты, инфицированные ВИЧ, относятся к группе высокого риска развития злокачественных опухолей. Увеличение числа больных НХЛ среди ВИЧ-инфицированных составляет 5,6% в год по сравнению с 0,015% в общей популяции [1]. У ВИЧ-инфицированных пациентов, согласно исследованиям, оглашенным на 22-й Международной конференции по СПИДу (AIDS 2018), риск развития лимфомы Ходжкина – в 33 раза выше чем в общей популяции. Антиретровирусная терапия (АРВТ) в значительной степени влияет на риск развития злокачественных опухолей, которые зависят от уровня CD4-лимфоцитов, и позволяет резко повысить эффективность лечения [2]. Применение АРВТ позволяет увеличить уровень CD4 клеток, снизить риск инфекционных осложнений и применять полихимиотерапию в стандартных дозах, тем не менее лимфомы у пациентов с ВИЧ по-прежнему остаются одной из ведущих причин смерти [3]. Целью нашего исследования было определить эпидемиологические характеристики и оценить эффективность терапии у пациентов с лимфомами на фоне ВИЧ-инфекции. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В ретроспективное исследование включены 12 пациентов, наблюдавшихся на базе ГБУЗ НСО ГКБ №2 «Городской гематологический центр» в период с 2013 по 2017 год (5 лет), с диагнозом лимфома на фоне ВИЧ-инфекции. Средний возраст пациентов 37,4±6,8 лет. Распределение по полу: мужчины – 8 (67%), женщины – 4 (33%). Статистическую обработку результатов проводили c помощью программ статистической обработки данных MSExcel, Statistica 12.0. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> ВИЧ-ассоциированные лимфомы были представлены следующими нозологиями: диффузная В-крупноклеточная лимфома (ДВККЛ) – 7 (58,3%), лимфома Ходжкина – 4 (33,4%), плазмобластная лимфома – 1 (8%). Экстранодальная локализация лимфомы отмечена у 50% больных. У пациентов с ДВККЛ был рассчитан прогностический индекс для ВИЧ-ассоциированных лимфом (ARL-IPI): в группу высокого риска вошел 1 пациент (14,29%), промежуточного риска – 5 больных (71,43%), низкого риска – 1 человек (14,29%). Все больные на момент дебюта злокачественной лимфомы имели ВИЧ-статус в течение 5-10 лет и не получали АРВТ в связи с низкой вирусной нагрузкой: менее 100 копий/мл. На момент первичной диагностики лимфомы вирусная нагрузка возрастала в несколько раз (94-1700000 копий/мл). Коинфекции: гепатит В – 25%, гепатит С – 58,33%. Пациенты с плазмобластной лимфомой и ДВККЛ получили курсы ПХТ по протоколу R-CHOP и R-MPV, пациенты с лимфомой Ходжкина – по протоколу ABVD. Девяти пациентам (75%) проведено лечение в объеме 4-8 курсов ПХТ. Полная ремиссия заболевания достигнута у 6 пациентов (66,7%), частичная ремиссия – у 1 пациента (22,2%), рецидив зафиксирован у 1 больного (11,1%) на фоне самостоятельной отмены АРВТ, прогрессирование – у 1 пациента (11,1%). У всех больных, получивших терапию, неудача лечения коррелирует с длительностью ВИЧ-инфекции (r=0.67, p<0.05). У больных, ответивших на терапию (n=8), была достигнута низкая вирусная нагрузка на фоне АРВТ: менее 100 копий/мл. Трое пациентов (25%) получили лишь 1-2 курса ПХТ в связи с коморбидностью или низкой приверженностью к терапии. Данные пациенты не получали АРВТ по различным причинам и ремиссии не достигли. Общая 2х летняя выживаемость пациентов, которым выполненная программная ПХТ с лимфомами на фоне ВИЧ (n=9) составила: 89%; лимфома Ходжкина – 100%, ДВККЛ – 75%. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> В нозологической структуре ВИЧ-ассоциированных лимфом преобладают ДВККЛ с агрессивным течением заболевания. Неудача лечения лимфомы коррелирует с длительностью ВИЧ-инфекции. Благодаря АРВТ, ПХТ может быть проведена в полном объеме с общей выживаемостью, близкой к общей популяции. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> ВИЧ-инфекция, лимфома, диффузная В-крупноклеточная лимфома, лимфома Ходжкина, химиотерапия, онкогематология. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(194) "Эпидемиологические характеристики и эффективность терапии у пациентов с ВИЧ-ассоциированными лимфомами" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(194) "Эпидемиологические характеристики и эффективность терапии у пациентов с ВИЧ-ассоциированными лимфомами" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(194) "Эпидемиологические характеристики и эффективность терапии у пациентов с ВИЧ-ассоциированными лимфомами" ["SECTION_META_TITLE"]=> string(194) "Эпидемиологические характеристики и эффективность терапии у пациентов с ВИЧ-ассоциированными лимфомами" ["SECTION_META_KEYWORDS"]=> string(194) "Эпидемиологические характеристики и эффективность терапии у пациентов с ВИЧ-ассоциированными лимфомами" ["SECTION_META_DESCRIPTION"]=> string(194) "Эпидемиологические характеристики и эффективность терапии у пациентов с ВИЧ-ассоциированными лимфомами" ["SECTION_PICTURE_FILE_ALT"]=> string(194) "Эпидемиологические характеристики и эффективность терапии у пациентов с ВИЧ-ассоциированными лимфомами" ["SECTION_PICTURE_FILE_TITLE"]=> string(194) "Эпидемиологические характеристики и эффективность терапии у пациентов с ВИЧ-ассоциированными лимфомами" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "epidemiologicheskie-kharakteristiki-i-effektivnost-terapii-u-patsientov-s-vich-assotsiirovannymi-lim" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(194) "Эпидемиологические характеристики и эффективность терапии у пациентов с ВИЧ-ассоциированными лимфомами" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(194) "Эпидемиологические характеристики и эффективность терапии у пациентов с ВИЧ-ассоциированными лимфомами" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "epidemiologicheskie-kharakteristiki-i-effektivnost-terapii-u-patsientov-s-vich-assotsiirovannymi-lim" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "epidemiologicheskie-kharakteristiki-i-effektivnost-terapii-u-patsientov-s-vich-assotsiirovannymi-lim" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "epidemiologicheskie-kharakteristiki-i-effektivnost-terapii-u-patsientov-s-vich-assotsiirovannymi-lim" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20493" ["VALUE"]=> array(2) { ["TEXT"]=> string(142) "Мария А. Колесникова, Ирина Н. Нечунаева, Марина О. Попова, Татьяна И. Поспелова" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(142) "Мария А. Колесникова, Ирина Н. Нечунаева, Марина О. Попова, Татьяна И. Поспелова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20494" ["VALUE"]=> array(2) { ["TEXT"]=> string(245) "Кафедра терапии, гематологии, трансфузиологии ФПК и ППВ, Новосибирский государственный медицинский университет, Новосибирск, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(245) "Кафедра терапии, гематологии, трансфузиологии ФПК и ППВ, Новосибирский государственный медицинский университет, Новосибирск, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20495" ["VALUE"]=> array(2) { ["TEXT"]=> string(7185) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Пациенты, инфицированные ВИЧ, относятся к группе высокого риска развития злокачественных опухолей. Увеличение числа больных НХЛ среди ВИЧ-инфицированных составляет 5,6% в год по сравнению с 0,015% в общей популяции [1]. У ВИЧ-инфицированных пациентов, согласно исследованиям, оглашенным на 22-й Международной конференции по СПИДу (AIDS 2018), риск развития лимфомы Ходжкина – в 33 раза выше чем в общей популяции. Антиретровирусная терапия (АРВТ) в значительной степени влияет на риск развития злокачественных опухолей, которые зависят от уровня CD4-лимфоцитов, и позволяет резко повысить эффективность лечения [2]. Применение АРВТ позволяет увеличить уровень CD4 клеток, снизить риск инфекционных осложнений и применять полихимиотерапию в стандартных дозах, тем не менее лимфомы у пациентов с ВИЧ по-прежнему остаются одной из ведущих причин смерти [3]. Целью нашего исследования было определить эпидемиологические характеристики и оценить эффективность терапии у пациентов с лимфомами на фоне ВИЧ-инфекции. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В ретроспективное исследование включены 12 пациентов, наблюдавшихся на базе ГБУЗ НСО ГКБ №2 «Городской гематологический центр» в период с 2013 по 2017 год (5 лет), с диагнозом лимфома на фоне ВИЧ-инфекции. Средний возраст пациентов 37,4±6,8 лет. Распределение по полу: мужчины – 8 (67%), женщины – 4 (33%). Статистическую обработку результатов проводили c помощью программ статистической обработки данных MSExcel, Statistica 12.0. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> ВИЧ-ассоциированные лимфомы были представлены следующими нозологиями: диффузная В-крупноклеточная лимфома (ДВККЛ) – 7 (58,3%), лимфома Ходжкина – 4 (33,4%), плазмобластная лимфома – 1 (8%). Экстранодальная локализация лимфомы отмечена у 50% больных. У пациентов с ДВККЛ был рассчитан прогностический индекс для ВИЧ-ассоциированных лимфом (ARL-IPI): в группу высокого риска вошел 1 пациент (14,29%), промежуточного риска – 5 больных (71,43%), низкого риска – 1 человек (14,29%). Все больные на момент дебюта злокачественной лимфомы имели ВИЧ-статус в течение 5-10 лет и не получали АРВТ в связи с низкой вирусной нагрузкой: менее 100 копий/мл. На момент первичной диагностики лимфомы вирусная нагрузка возрастала в несколько раз (94-1700000 копий/мл). Коинфекции: гепатит В – 25%, гепатит С – 58,33%. Пациенты с плазмобластной лимфомой и ДВККЛ получили курсы ПХТ по протоколу R-CHOP и R-MPV, пациенты с лимфомой Ходжкина – по протоколу ABVD. Девяти пациентам (75%) проведено лечение в объеме 4-8 курсов ПХТ. Полная ремиссия заболевания достигнута у 6 пациентов (66,7%), частичная ремиссия – у 1 пациента (22,2%), рецидив зафиксирован у 1 больного (11,1%) на фоне самостоятельной отмены АРВТ, прогрессирование – у 1 пациента (11,1%). У всех больных, получивших терапию, неудача лечения коррелирует с длительностью ВИЧ-инфекции (r=0.67, p<0.05). У больных, ответивших на терапию (n=8), была достигнута низкая вирусная нагрузка на фоне АРВТ: менее 100 копий/мл. Трое пациентов (25%) получили лишь 1-2 курса ПХТ в связи с коморбидностью или низкой приверженностью к терапии. Данные пациенты не получали АРВТ по различным причинам и ремиссии не достигли. Общая 2х летняя выживаемость пациентов, которым выполненная программная ПХТ с лимфомами на фоне ВИЧ (n=9) составила: 89%; лимфома Ходжкина – 100%, ДВККЛ – 75%. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> В нозологической структуре ВИЧ-ассоциированных лимфом преобладают ДВККЛ с агрессивным течением заболевания. Неудача лечения лимфомы коррелирует с длительностью ВИЧ-инфекции. Благодаря АРВТ, ПХТ может быть проведена в полном объеме с общей выживаемостью, близкой к общей популяции. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> ВИЧ-инфекция, лимфома, диффузная В-крупноклеточная лимфома, лимфома Ходжкина, химиотерапия, онкогематология. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6961) "
Введение
Пациенты, инфицированные ВИЧ, относятся к группе высокого риска развития злокачественных опухолей. Увеличение числа больных НХЛ среди ВИЧ-инфицированных составляет 5,6% в год по сравнению с 0,015% в общей популяции [1]. У ВИЧ-инфицированных пациентов, согласно исследованиям, оглашенным на 22-й Международной конференции по СПИДу (AIDS 2018), риск развития лимфомы Ходжкина – в 33 раза выше чем в общей популяции. Антиретровирусная терапия (АРВТ) в значительной степени влияет на риск развития злокачественных опухолей, которые зависят от уровня CD4-лимфоцитов, и позволяет резко повысить эффективность лечения [2]. Применение АРВТ позволяет увеличить уровень CD4 клеток, снизить риск инфекционных осложнений и применять полихимиотерапию в стандартных дозах, тем не менее лимфомы у пациентов с ВИЧ по-прежнему остаются одной из ведущих причин смерти [3]. Целью нашего исследования было определить эпидемиологические характеристики и оценить эффективность терапии у пациентов с лимфомами на фоне ВИЧ-инфекции.
Пациенты и методы
В ретроспективное исследование включены 12 пациентов, наблюдавшихся на базе ГБУЗ НСО ГКБ №2 «Городской гематологический центр» в период с 2013 по 2017 год (5 лет), с диагнозом лимфома на фоне ВИЧ-инфекции. Средний возраст пациентов 37,4±6,8 лет. Распределение по полу: мужчины – 8 (67%), женщины – 4 (33%). Статистическую обработку результатов проводили c помощью программ статистической обработки данных MSExcel, Statistica 12.0.
Результаты
ВИЧ-ассоциированные лимфомы были представлены следующими нозологиями: диффузная В-крупноклеточная лимфома (ДВККЛ) – 7 (58,3%), лимфома Ходжкина – 4 (33,4%), плазмобластная лимфома – 1 (8%). Экстранодальная локализация лимфомы отмечена у 50% больных. У пациентов с ДВККЛ был рассчитан прогностический индекс для ВИЧ-ассоциированных лимфом (ARL-IPI): в группу высокого риска вошел 1 пациент (14,29%), промежуточного риска – 5 больных (71,43%), низкого риска – 1 человек (14,29%). Все больные на момент дебюта злокачественной лимфомы имели ВИЧ-статус в течение 5-10 лет и не получали АРВТ в связи с низкой вирусной нагрузкой: менее 100 копий/мл. На момент первичной диагностики лимфомы вирусная нагрузка возрастала в несколько раз (94-1700000 копий/мл). Коинфекции: гепатит В – 25%, гепатит С – 58,33%. Пациенты с плазмобластной лимфомой и ДВККЛ получили курсы ПХТ по протоколу R-CHOP и R-MPV, пациенты с лимфомой Ходжкина – по протоколу ABVD. Девяти пациентам (75%) проведено лечение в объеме 4-8 курсов ПХТ. Полная ремиссия заболевания достигнута у 6 пациентов (66,7%), частичная ремиссия – у 1 пациента (22,2%), рецидив зафиксирован у 1 больного (11,1%) на фоне самостоятельной отмены АРВТ, прогрессирование – у 1 пациента (11,1%). У всех больных, получивших терапию, неудача лечения коррелирует с длительностью ВИЧ-инфекции (r=0.67, p<0.05). У больных, ответивших на терапию (n=8), была достигнута низкая вирусная нагрузка на фоне АРВТ: менее 100 копий/мл. Трое пациентов (25%) получили лишь 1-2 курса ПХТ в связи с коморбидностью или низкой приверженностью к терапии. Данные пациенты не получали АРВТ по различным причинам и ремиссии не достигли. Общая 2х летняя выживаемость пациентов, которым выполненная программная ПХТ с лимфомами на фоне ВИЧ (n=9) составила: 89%; лимфома Ходжкина – 100%, ДВККЛ – 75%.
Заключение
В нозологической структуре ВИЧ-ассоциированных лимфом преобладают ДВККЛ с агрессивным течением заболевания. Неудача лечения лимфомы коррелирует с длительностью ВИЧ-инфекции. Благодаря АРВТ, ПХТ может быть проведена в полном объеме с общей выживаемостью, близкой к общей популяции.
Ключевые слова
ВИЧ-инфекция, лимфома, диффузная В-крупноклеточная лимфома, лимфома Ходжкина, химиотерапия, онкогематология.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20496" ["VALUE"]=> array(2) { ["TEXT"]=> string(81) "Maria A. Kolesnikova, Irina N. Nechunaeva, Marina O. Popova, Tatiana I. Pospelova" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(81) "Maria A. Kolesnikova, Irina N. Nechunaeva, Marina O. Popova, Tatiana I. Pospelova" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20497" ["VALUE"]=> array(2) { ["TEXT"]=> string(99) "Hematology and Transfusiology Department, Novosibirsk State Medical University, Novosibirsk, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(99) "Hematology and Transfusiology Department, Novosibirsk State Medical University, Novosibirsk, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20498" ["VALUE"]=> array(2) { ["TEXT"]=> string(5234) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> HIV-infected patients are at high risk for cancer. The number of patients with NHL among HIV+ individuals is 5.6% per year, compared with 0.015% of the general population [1]. Risk of Hodgkin’s lymphoma in HIV-infected patients is higher in 33 times than the general population, according to studies announced at the 22nd International AIDS Conference (AIDS 2018). Antiretroviral therapy (ART) significantly influences on the risk of cancer which depend on the level of CD4-lymphocytes, and improve the effectiveness of treatment [2]. The ART increase the level of CD4 cells, reduce the risk of infectious complications and allow administering chemotherapy in standard doses, however, HIV-associated lymphomas continue to be one of the leading causes of death [3]. The aim of our study was to determine the epidemiological characteristics and evaluate the effectiveness of treatment of HIV-associated lymphomas. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> A retrospective study included 12 patients who were observed on the basis of the National Clinical Hospital No. 2 City Hematology Center from 2013 to 2017 (5 years), diagnosed with HIV- lymphomas. The average age of the patients was 37.4 ± 6.8 years. Distribution by sex: men, 8 (67%), women, 4 (33%). The statistical analysis was performed using MSExcel, Statistica 12.0 software. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> HIV-associated lymphomas were represented by the following clinical types: diffuse large B-cell lymphoma (DLBCL), 7 (58.3%); Hodgkin’s lymphoma, 4 (33.4%); plasmablastic lymphoma, 1 (8%). Extranodal localization of lymphoma was diagnosed in 50% of patients. A prognostic index for HIV-associated lymphomas (ARL-IPI) was calculated for DLBCL: 1 patient (14.29%) entered high-risk group; 5 patients were at intermediate risk (71.43%); 1 person was at low risk (14.29%). Before the diagnosis of lymphoma, all the patients had HIV-positive status for 5-10 years and did not receive ART because of low viral loads (<100 copies/mL). A several-fold increase of viral load (94 to 1700000 copies/mL) was registered at the time of lymphoma diagnosis. Co-infections were detected: hepatitis B, 25%; C, 58.33% of the cases. Patients with plasmablastic lymphoma and DLBCL were treated with R-CHOP and R-MPV; Hodgkin’s lymphoma, according to ABVD protocol. Nine patients (75%) have received 4-8 courses of chemotherapy. Complete remission of the disease was achieved in 6 patients (66.7%); partial remission, in 1 patient (22.2%); relapse was registered in 1 patient (11.1%) associated with self-withdrawal of ART; progression was documented in one case (11.1%). Treatment failure correlated with duration of HIV infection (r = 0.67, p <0.05). The patients who responded to chemotherapy (n=8) achieved low viral load on the background of ART, i.e., less than 100 copies/ml. Three patients (25%) received only 1-2 courses of chemotherapy due to co-morbidity or low adherence to the therapy. These patients did not receive ART for various reasons and did not achieve remission. The overall 2-years survival of 9 patients with HIV-associated lymphomas who completed programmed chemotherapy was 89%; in Hodgkin’s lymphoma, 100%; in DLBCL – 75%. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Diffuse large B-cell lymphomas with aggressive course were more often diagnosed in HIV-infected patients. The chemotherapy failure correlated with duration of HIV infection before lymphoma diagnosis. Overall survival at 2 years in treated patients was 89%. Due to ART, the entire program of chemotherapy can be fulfilled, and good overall survival rates can be achieved in HIV-associated lymphomas, being<br> close to general patient cohorts. </p> <h2 style="text-align: justify;">References</h2> <p style="text-align: justify;"> 1. MH Bateganya, J. Stanaway, P.E. Brentlingeret et al. MHPredictors of Survival After Diagnosis of Non-Hodgkin Lymphoma in a Resource-Limited Setting: A Retrospective Study on the Impact of HIV Infection and Its Treatment // J. of Acquired Immune Deficiency Syndromes. 2011. 56 (4). P. 312-319.<br> 2. Shiels MS, Pfeiffer RM, Gail MH, et al. Cancer Burden in the HIV-Infected Population in the United States. JNCI Journal of the National Cancer Institute. 2011;103(9):753-762.<br> 3. Binnet F, Lewden C, May T, et al. Malignancy related causes of death in human immunodeficiency virus infected patients in the era of highly active antiretroviral therapy. Cancer. 2004;10:317–324. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> HIV infection, lymphoma, diffuse large B-cell lymphoma, Hodgkin’s lymphoma, chemotherapy, oncohematology. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4944) "Introduction
HIV-infected patients are at high risk for cancer. The number of patients with NHL among HIV+ individuals is 5.6% per year, compared with 0.015% of the general population [1]. Risk of Hodgkin’s lymphoma in HIV-infected patients is higher in 33 times than the general population, according to studies announced at the 22nd International AIDS Conference (AIDS 2018). Antiretroviral therapy (ART) significantly influences on the risk of cancer which depend on the level of CD4-lymphocytes, and improve the effectiveness of treatment [2]. The ART increase the level of CD4 cells, reduce the risk of infectious complications and allow administering chemotherapy in standard doses, however, HIV-associated lymphomas continue to be one of the leading causes of death [3]. The aim of our study was to determine the epidemiological characteristics and evaluate the effectiveness of treatment of HIV-associated lymphomas.
Patients and methods
A retrospective study included 12 patients who were observed on the basis of the National Clinical Hospital No. 2 City Hematology Center from 2013 to 2017 (5 years), diagnosed with HIV- lymphomas. The average age of the patients was 37.4 ± 6.8 years. Distribution by sex: men, 8 (67%), women, 4 (33%). The statistical analysis was performed using MSExcel, Statistica 12.0 software.
Results
HIV-associated lymphomas were represented by the following clinical types: diffuse large B-cell lymphoma (DLBCL), 7 (58.3%); Hodgkin’s lymphoma, 4 (33.4%); plasmablastic lymphoma, 1 (8%). Extranodal localization of lymphoma was diagnosed in 50% of patients. A prognostic index for HIV-associated lymphomas (ARL-IPI) was calculated for DLBCL: 1 patient (14.29%) entered high-risk group; 5 patients were at intermediate risk (71.43%); 1 person was at low risk (14.29%). Before the diagnosis of lymphoma, all the patients had HIV-positive status for 5-10 years and did not receive ART because of low viral loads (<100 copies/mL). A several-fold increase of viral load (94 to 1700000 copies/mL) was registered at the time of lymphoma diagnosis. Co-infections were detected: hepatitis B, 25%; C, 58.33% of the cases. Patients with plasmablastic lymphoma and DLBCL were treated with R-CHOP and R-MPV; Hodgkin’s lymphoma, according to ABVD protocol. Nine patients (75%) have received 4-8 courses of chemotherapy. Complete remission of the disease was achieved in 6 patients (66.7%); partial remission, in 1 patient (22.2%); relapse was registered in 1 patient (11.1%) associated with self-withdrawal of ART; progression was documented in one case (11.1%). Treatment failure correlated with duration of HIV infection (r = 0.67, p <0.05). The patients who responded to chemotherapy (n=8) achieved low viral load on the background of ART, i.e., less than 100 copies/ml. Three patients (25%) received only 1-2 courses of chemotherapy due to co-morbidity or low adherence to the therapy. These patients did not receive ART for various reasons and did not achieve remission. The overall 2-years survival of 9 patients with HIV-associated lymphomas who completed programmed chemotherapy was 89%; in Hodgkin’s lymphoma, 100%; in DLBCL – 75%.
Conclusion
Diffuse large B-cell lymphomas with aggressive course were more often diagnosed in HIV-infected patients. The chemotherapy failure correlated with duration of HIV infection before lymphoma diagnosis. Overall survival at 2 years in treated patients was 89%. Due to ART, the entire program of chemotherapy can be fulfilled, and good overall survival rates can be achieved in HIV-associated lymphomas, being
close to general patient cohorts.
References
1. MH Bateganya, J. Stanaway, P.E. Brentlingeret et al. MHPredictors of Survival After Diagnosis of Non-Hodgkin Lymphoma in a Resource-Limited Setting: A Retrospective Study on the Impact of HIV Infection and Its Treatment // J. of Acquired Immune Deficiency Syndromes. 2011. 56 (4). P. 312-319.
2. Shiels MS, Pfeiffer RM, Gail MH, et al. Cancer Burden in the HIV-Infected Population in the United States. JNCI Journal of the National Cancer Institute. 2011;103(9):753-762.
3. Binnet F, Lewden C, May T, et al. Malignancy related causes of death in human immunodeficiency virus infected patients in the era of highly active antiretroviral therapy. Cancer. 2004;10:317–324.
Keywords
HIV infection, lymphoma, diffuse large B-cell lymphoma, Hodgkin’s lymphoma, chemotherapy, oncohematology.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20499" ["VALUE"]=> string(78) "Epidemiological features and efficacy of treatment in HIV-associated lymphomas" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(78) "Epidemiological features and efficacy of treatment in HIV-associated lymphomas" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20775" ["VALUE"]=> string(4) "1413" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1413" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20776" ["VALUE"]=> string(4) "1414" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1414" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20496" ["VALUE"]=> array(2) { ["TEXT"]=> string(81) "Maria A. Kolesnikova, Irina N. Nechunaeva, Marina O. Popova, Tatiana I. Pospelova" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(81) "Maria A. Kolesnikova, Irina N. Nechunaeva, Marina O. Popova, Tatiana I. Pospelova" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(81) "Maria A. Kolesnikova, Irina N. Nechunaeva, Marina O. Popova, Tatiana I. Pospelova" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20498" ["VALUE"]=> array(2) { ["TEXT"]=> string(5234) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> HIV-infected patients are at high risk for cancer. The number of patients with NHL among HIV+ individuals is 5.6% per year, compared with 0.015% of the general population [1]. Risk of Hodgkin’s lymphoma in HIV-infected patients is higher in 33 times than the general population, according to studies announced at the 22nd International AIDS Conference (AIDS 2018). Antiretroviral therapy (ART) significantly influences on the risk of cancer which depend on the level of CD4-lymphocytes, and improve the effectiveness of treatment [2]. The ART increase the level of CD4 cells, reduce the risk of infectious complications and allow administering chemotherapy in standard doses, however, HIV-associated lymphomas continue to be one of the leading causes of death [3]. The aim of our study was to determine the epidemiological characteristics and evaluate the effectiveness of treatment of HIV-associated lymphomas. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> A retrospective study included 12 patients who were observed on the basis of the National Clinical Hospital No. 2 City Hematology Center from 2013 to 2017 (5 years), diagnosed with HIV- lymphomas. The average age of the patients was 37.4 ± 6.8 years. Distribution by sex: men, 8 (67%), women, 4 (33%). The statistical analysis was performed using MSExcel, Statistica 12.0 software. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> HIV-associated lymphomas were represented by the following clinical types: diffuse large B-cell lymphoma (DLBCL), 7 (58.3%); Hodgkin’s lymphoma, 4 (33.4%); plasmablastic lymphoma, 1 (8%). Extranodal localization of lymphoma was diagnosed in 50% of patients. A prognostic index for HIV-associated lymphomas (ARL-IPI) was calculated for DLBCL: 1 patient (14.29%) entered high-risk group; 5 patients were at intermediate risk (71.43%); 1 person was at low risk (14.29%). Before the diagnosis of lymphoma, all the patients had HIV-positive status for 5-10 years and did not receive ART because of low viral loads (<100 copies/mL). A several-fold increase of viral load (94 to 1700000 copies/mL) was registered at the time of lymphoma diagnosis. Co-infections were detected: hepatitis B, 25%; C, 58.33% of the cases. Patients with plasmablastic lymphoma and DLBCL were treated with R-CHOP and R-MPV; Hodgkin’s lymphoma, according to ABVD protocol. Nine patients (75%) have received 4-8 courses of chemotherapy. Complete remission of the disease was achieved in 6 patients (66.7%); partial remission, in 1 patient (22.2%); relapse was registered in 1 patient (11.1%) associated with self-withdrawal of ART; progression was documented in one case (11.1%). Treatment failure correlated with duration of HIV infection (r = 0.67, p <0.05). The patients who responded to chemotherapy (n=8) achieved low viral load on the background of ART, i.e., less than 100 copies/ml. Three patients (25%) received only 1-2 courses of chemotherapy due to co-morbidity or low adherence to the therapy. These patients did not receive ART for various reasons and did not achieve remission. The overall 2-years survival of 9 patients with HIV-associated lymphomas who completed programmed chemotherapy was 89%; in Hodgkin’s lymphoma, 100%; in DLBCL – 75%. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Diffuse large B-cell lymphomas with aggressive course were more often diagnosed in HIV-infected patients. The chemotherapy failure correlated with duration of HIV infection before lymphoma diagnosis. Overall survival at 2 years in treated patients was 89%. Due to ART, the entire program of chemotherapy can be fulfilled, and good overall survival rates can be achieved in HIV-associated lymphomas, being<br> close to general patient cohorts. </p> <h2 style="text-align: justify;">References</h2> <p style="text-align: justify;"> 1. MH Bateganya, J. Stanaway, P.E. Brentlingeret et al. MHPredictors of Survival After Diagnosis of Non-Hodgkin Lymphoma in a Resource-Limited Setting: A Retrospective Study on the Impact of HIV Infection and Its Treatment // J. of Acquired Immune Deficiency Syndromes. 2011. 56 (4). P. 312-319.<br> 2. Shiels MS, Pfeiffer RM, Gail MH, et al. Cancer Burden in the HIV-Infected Population in the United States. JNCI Journal of the National Cancer Institute. 2011;103(9):753-762.<br> 3. Binnet F, Lewden C, May T, et al. Malignancy related causes of death in human immunodeficiency virus infected patients in the era of highly active antiretroviral therapy. Cancer. 2004;10:317–324. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> HIV infection, lymphoma, diffuse large B-cell lymphoma, Hodgkin’s lymphoma, chemotherapy, oncohematology. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4944) "Introduction
HIV-infected patients are at high risk for cancer. The number of patients with NHL among HIV+ individuals is 5.6% per year, compared with 0.015% of the general population [1]. Risk of Hodgkin’s lymphoma in HIV-infected patients is higher in 33 times than the general population, according to studies announced at the 22nd International AIDS Conference (AIDS 2018). Antiretroviral therapy (ART) significantly influences on the risk of cancer which depend on the level of CD4-lymphocytes, and improve the effectiveness of treatment [2]. The ART increase the level of CD4 cells, reduce the risk of infectious complications and allow administering chemotherapy in standard doses, however, HIV-associated lymphomas continue to be one of the leading causes of death [3]. The aim of our study was to determine the epidemiological characteristics and evaluate the effectiveness of treatment of HIV-associated lymphomas.
Patients and methods
A retrospective study included 12 patients who were observed on the basis of the National Clinical Hospital No. 2 City Hematology Center from 2013 to 2017 (5 years), diagnosed with HIV- lymphomas. The average age of the patients was 37.4 ± 6.8 years. Distribution by sex: men, 8 (67%), women, 4 (33%). The statistical analysis was performed using MSExcel, Statistica 12.0 software.
Results
HIV-associated lymphomas were represented by the following clinical types: diffuse large B-cell lymphoma (DLBCL), 7 (58.3%); Hodgkin’s lymphoma, 4 (33.4%); plasmablastic lymphoma, 1 (8%). Extranodal localization of lymphoma was diagnosed in 50% of patients. A prognostic index for HIV-associated lymphomas (ARL-IPI) was calculated for DLBCL: 1 patient (14.29%) entered high-risk group; 5 patients were at intermediate risk (71.43%); 1 person was at low risk (14.29%). Before the diagnosis of lymphoma, all the patients had HIV-positive status for 5-10 years and did not receive ART because of low viral loads (<100 copies/mL). A several-fold increase of viral load (94 to 1700000 copies/mL) was registered at the time of lymphoma diagnosis. Co-infections were detected: hepatitis B, 25%; C, 58.33% of the cases. Patients with plasmablastic lymphoma and DLBCL were treated with R-CHOP and R-MPV; Hodgkin’s lymphoma, according to ABVD protocol. Nine patients (75%) have received 4-8 courses of chemotherapy. Complete remission of the disease was achieved in 6 patients (66.7%); partial remission, in 1 patient (22.2%); relapse was registered in 1 patient (11.1%) associated with self-withdrawal of ART; progression was documented in one case (11.1%). Treatment failure correlated with duration of HIV infection (r = 0.67, p <0.05). The patients who responded to chemotherapy (n=8) achieved low viral load on the background of ART, i.e., less than 100 copies/ml. Three patients (25%) received only 1-2 courses of chemotherapy due to co-morbidity or low adherence to the therapy. These patients did not receive ART for various reasons and did not achieve remission. The overall 2-years survival of 9 patients with HIV-associated lymphomas who completed programmed chemotherapy was 89%; in Hodgkin’s lymphoma, 100%; in DLBCL – 75%.
Conclusion
Diffuse large B-cell lymphomas with aggressive course were more often diagnosed in HIV-infected patients. The chemotherapy failure correlated with duration of HIV infection before lymphoma diagnosis. Overall survival at 2 years in treated patients was 89%. Due to ART, the entire program of chemotherapy can be fulfilled, and good overall survival rates can be achieved in HIV-associated lymphomas, being
close to general patient cohorts.
References
1. MH Bateganya, J. Stanaway, P.E. Brentlingeret et al. MHPredictors of Survival After Diagnosis of Non-Hodgkin Lymphoma in a Resource-Limited Setting: A Retrospective Study on the Impact of HIV Infection and Its Treatment // J. of Acquired Immune Deficiency Syndromes. 2011. 56 (4). P. 312-319.
2. Shiels MS, Pfeiffer RM, Gail MH, et al. Cancer Burden in the HIV-Infected Population in the United States. JNCI Journal of the National Cancer Institute. 2011;103(9):753-762.
3. Binnet F, Lewden C, May T, et al. Malignancy related causes of death in human immunodeficiency virus infected patients in the era of highly active antiretroviral therapy. Cancer. 2004;10:317–324.
Keywords
HIV infection, lymphoma, diffuse large B-cell lymphoma, Hodgkin’s lymphoma, chemotherapy, oncohematology.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4944) "Introduction
HIV-infected patients are at high risk for cancer. The number of patients with NHL among HIV+ individuals is 5.6% per year, compared with 0.015% of the general population [1]. Risk of Hodgkin’s lymphoma in HIV-infected patients is higher in 33 times than the general population, according to studies announced at the 22nd International AIDS Conference (AIDS 2018). Antiretroviral therapy (ART) significantly influences on the risk of cancer which depend on the level of CD4-lymphocytes, and improve the effectiveness of treatment [2]. The ART increase the level of CD4 cells, reduce the risk of infectious complications and allow administering chemotherapy in standard doses, however, HIV-associated lymphomas continue to be one of the leading causes of death [3]. The aim of our study was to determine the epidemiological characteristics and evaluate the effectiveness of treatment of HIV-associated lymphomas.
Patients and methods
A retrospective study included 12 patients who were observed on the basis of the National Clinical Hospital No. 2 City Hematology Center from 2013 to 2017 (5 years), diagnosed with HIV- lymphomas. The average age of the patients was 37.4 ± 6.8 years. Distribution by sex: men, 8 (67%), women, 4 (33%). The statistical analysis was performed using MSExcel, Statistica 12.0 software.
Results
HIV-associated lymphomas were represented by the following clinical types: diffuse large B-cell lymphoma (DLBCL), 7 (58.3%); Hodgkin’s lymphoma, 4 (33.4%); plasmablastic lymphoma, 1 (8%). Extranodal localization of lymphoma was diagnosed in 50% of patients. A prognostic index for HIV-associated lymphomas (ARL-IPI) was calculated for DLBCL: 1 patient (14.29%) entered high-risk group; 5 patients were at intermediate risk (71.43%); 1 person was at low risk (14.29%). Before the diagnosis of lymphoma, all the patients had HIV-positive status for 5-10 years and did not receive ART because of low viral loads (<100 copies/mL). A several-fold increase of viral load (94 to 1700000 copies/mL) was registered at the time of lymphoma diagnosis. Co-infections were detected: hepatitis B, 25%; C, 58.33% of the cases. Patients with plasmablastic lymphoma and DLBCL were treated with R-CHOP and R-MPV; Hodgkin’s lymphoma, according to ABVD protocol. Nine patients (75%) have received 4-8 courses of chemotherapy. Complete remission of the disease was achieved in 6 patients (66.7%); partial remission, in 1 patient (22.2%); relapse was registered in 1 patient (11.1%) associated with self-withdrawal of ART; progression was documented in one case (11.1%). Treatment failure correlated with duration of HIV infection (r = 0.67, p <0.05). The patients who responded to chemotherapy (n=8) achieved low viral load on the background of ART, i.e., less than 100 copies/ml. Three patients (25%) received only 1-2 courses of chemotherapy due to co-morbidity or low adherence to the therapy. These patients did not receive ART for various reasons and did not achieve remission. The overall 2-years survival of 9 patients with HIV-associated lymphomas who completed programmed chemotherapy was 89%; in Hodgkin’s lymphoma, 100%; in DLBCL – 75%.
Conclusion
Diffuse large B-cell lymphomas with aggressive course were more often diagnosed in HIV-infected patients. The chemotherapy failure correlated with duration of HIV infection before lymphoma diagnosis. Overall survival at 2 years in treated patients was 89%. Due to ART, the entire program of chemotherapy can be fulfilled, and good overall survival rates can be achieved in HIV-associated lymphomas, being
close to general patient cohorts.
References
1. MH Bateganya, J. Stanaway, P.E. Brentlingeret et al. MHPredictors of Survival After Diagnosis of Non-Hodgkin Lymphoma in a Resource-Limited Setting: A Retrospective Study on the Impact of HIV Infection and Its Treatment // J. of Acquired Immune Deficiency Syndromes. 2011. 56 (4). P. 312-319.
2. Shiels MS, Pfeiffer RM, Gail MH, et al. Cancer Burden in the HIV-Infected Population in the United States. JNCI Journal of the National Cancer Institute. 2011;103(9):753-762.
3. Binnet F, Lewden C, May T, et al. Malignancy related causes of death in human immunodeficiency virus infected patients in the era of highly active antiretroviral therapy. Cancer. 2004;10:317–324.
Keywords
HIV infection, lymphoma, diffuse large B-cell lymphoma, Hodgkin’s lymphoma, chemotherapy, oncohematology.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20499" ["VALUE"]=> string(78) "Epidemiological features and efficacy of treatment in HIV-associated lymphomas" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(78) "Epidemiological features and efficacy of treatment in HIV-associated lymphomas" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(78) "Epidemiological features and efficacy of treatment in HIV-associated lymphomas" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20497" ["VALUE"]=> array(2) { ["TEXT"]=> string(99) "Hematology and Transfusiology Department, Novosibirsk State Medical University, Novosibirsk, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(99) "Hematology and Transfusiology Department, Novosibirsk State Medical University, Novosibirsk, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(99) "Hematology and Transfusiology Department, Novosibirsk State Medical University, Novosibirsk, Russia" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20493" ["VALUE"]=> array(2) { ["TEXT"]=> string(142) "Мария А. Колесникова, Ирина Н. Нечунаева, Марина О. Попова, Татьяна И. Поспелова" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(142) "Мария А. Колесникова, Ирина Н. Нечунаева, Марина О. Попова, Татьяна И. Поспелова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(142) "Мария А. Колесникова, Ирина Н. Нечунаева, Марина О. Попова, Татьяна И. Поспелова" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20495" ["VALUE"]=> array(2) { ["TEXT"]=> string(7185) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Пациенты, инфицированные ВИЧ, относятся к группе высокого риска развития злокачественных опухолей. Увеличение числа больных НХЛ среди ВИЧ-инфицированных составляет 5,6% в год по сравнению с 0,015% в общей популяции [1]. У ВИЧ-инфицированных пациентов, согласно исследованиям, оглашенным на 22-й Международной конференции по СПИДу (AIDS 2018), риск развития лимфомы Ходжкина – в 33 раза выше чем в общей популяции. Антиретровирусная терапия (АРВТ) в значительной степени влияет на риск развития злокачественных опухолей, которые зависят от уровня CD4-лимфоцитов, и позволяет резко повысить эффективность лечения [2]. Применение АРВТ позволяет увеличить уровень CD4 клеток, снизить риск инфекционных осложнений и применять полихимиотерапию в стандартных дозах, тем не менее лимфомы у пациентов с ВИЧ по-прежнему остаются одной из ведущих причин смерти [3]. Целью нашего исследования было определить эпидемиологические характеристики и оценить эффективность терапии у пациентов с лимфомами на фоне ВИЧ-инфекции. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В ретроспективное исследование включены 12 пациентов, наблюдавшихся на базе ГБУЗ НСО ГКБ №2 «Городской гематологический центр» в период с 2013 по 2017 год (5 лет), с диагнозом лимфома на фоне ВИЧ-инфекции. Средний возраст пациентов 37,4±6,8 лет. Распределение по полу: мужчины – 8 (67%), женщины – 4 (33%). Статистическую обработку результатов проводили c помощью программ статистической обработки данных MSExcel, Statistica 12.0. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> ВИЧ-ассоциированные лимфомы были представлены следующими нозологиями: диффузная В-крупноклеточная лимфома (ДВККЛ) – 7 (58,3%), лимфома Ходжкина – 4 (33,4%), плазмобластная лимфома – 1 (8%). Экстранодальная локализация лимфомы отмечена у 50% больных. У пациентов с ДВККЛ был рассчитан прогностический индекс для ВИЧ-ассоциированных лимфом (ARL-IPI): в группу высокого риска вошел 1 пациент (14,29%), промежуточного риска – 5 больных (71,43%), низкого риска – 1 человек (14,29%). Все больные на момент дебюта злокачественной лимфомы имели ВИЧ-статус в течение 5-10 лет и не получали АРВТ в связи с низкой вирусной нагрузкой: менее 100 копий/мл. На момент первичной диагностики лимфомы вирусная нагрузка возрастала в несколько раз (94-1700000 копий/мл). Коинфекции: гепатит В – 25%, гепатит С – 58,33%. Пациенты с плазмобластной лимфомой и ДВККЛ получили курсы ПХТ по протоколу R-CHOP и R-MPV, пациенты с лимфомой Ходжкина – по протоколу ABVD. Девяти пациентам (75%) проведено лечение в объеме 4-8 курсов ПХТ. Полная ремиссия заболевания достигнута у 6 пациентов (66,7%), частичная ремиссия – у 1 пациента (22,2%), рецидив зафиксирован у 1 больного (11,1%) на фоне самостоятельной отмены АРВТ, прогрессирование – у 1 пациента (11,1%). У всех больных, получивших терапию, неудача лечения коррелирует с длительностью ВИЧ-инфекции (r=0.67, p<0.05). У больных, ответивших на терапию (n=8), была достигнута низкая вирусная нагрузка на фоне АРВТ: менее 100 копий/мл. Трое пациентов (25%) получили лишь 1-2 курса ПХТ в связи с коморбидностью или низкой приверженностью к терапии. Данные пациенты не получали АРВТ по различным причинам и ремиссии не достигли. Общая 2х летняя выживаемость пациентов, которым выполненная программная ПХТ с лимфомами на фоне ВИЧ (n=9) составила: 89%; лимфома Ходжкина – 100%, ДВККЛ – 75%. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> В нозологической структуре ВИЧ-ассоциированных лимфом преобладают ДВККЛ с агрессивным течением заболевания. Неудача лечения лимфомы коррелирует с длительностью ВИЧ-инфекции. Благодаря АРВТ, ПХТ может быть проведена в полном объеме с общей выживаемостью, близкой к общей популяции. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> ВИЧ-инфекция, лимфома, диффузная В-крупноклеточная лимфома, лимфома Ходжкина, химиотерапия, онкогематология. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6961) "Введение
Пациенты, инфицированные ВИЧ, относятся к группе высокого риска развития злокачественных опухолей. Увеличение числа больных НХЛ среди ВИЧ-инфицированных составляет 5,6% в год по сравнению с 0,015% в общей популяции [1]. У ВИЧ-инфицированных пациентов, согласно исследованиям, оглашенным на 22-й Международной конференции по СПИДу (AIDS 2018), риск развития лимфомы Ходжкина – в 33 раза выше чем в общей популяции. Антиретровирусная терапия (АРВТ) в значительной степени влияет на риск развития злокачественных опухолей, которые зависят от уровня CD4-лимфоцитов, и позволяет резко повысить эффективность лечения [2]. Применение АРВТ позволяет увеличить уровень CD4 клеток, снизить риск инфекционных осложнений и применять полихимиотерапию в стандартных дозах, тем не менее лимфомы у пациентов с ВИЧ по-прежнему остаются одной из ведущих причин смерти [3]. Целью нашего исследования было определить эпидемиологические характеристики и оценить эффективность терапии у пациентов с лимфомами на фоне ВИЧ-инфекции.
Пациенты и методы
В ретроспективное исследование включены 12 пациентов, наблюдавшихся на базе ГБУЗ НСО ГКБ №2 «Городской гематологический центр» в период с 2013 по 2017 год (5 лет), с диагнозом лимфома на фоне ВИЧ-инфекции. Средний возраст пациентов 37,4±6,8 лет. Распределение по полу: мужчины – 8 (67%), женщины – 4 (33%). Статистическую обработку результатов проводили c помощью программ статистической обработки данных MSExcel, Statistica 12.0.
Результаты
ВИЧ-ассоциированные лимфомы были представлены следующими нозологиями: диффузная В-крупноклеточная лимфома (ДВККЛ) – 7 (58,3%), лимфома Ходжкина – 4 (33,4%), плазмобластная лимфома – 1 (8%). Экстранодальная локализация лимфомы отмечена у 50% больных. У пациентов с ДВККЛ был рассчитан прогностический индекс для ВИЧ-ассоциированных лимфом (ARL-IPI): в группу высокого риска вошел 1 пациент (14,29%), промежуточного риска – 5 больных (71,43%), низкого риска – 1 человек (14,29%). Все больные на момент дебюта злокачественной лимфомы имели ВИЧ-статус в течение 5-10 лет и не получали АРВТ в связи с низкой вирусной нагрузкой: менее 100 копий/мл. На момент первичной диагностики лимфомы вирусная нагрузка возрастала в несколько раз (94-1700000 копий/мл). Коинфекции: гепатит В – 25%, гепатит С – 58,33%. Пациенты с плазмобластной лимфомой и ДВККЛ получили курсы ПХТ по протоколу R-CHOP и R-MPV, пациенты с лимфомой Ходжкина – по протоколу ABVD. Девяти пациентам (75%) проведено лечение в объеме 4-8 курсов ПХТ. Полная ремиссия заболевания достигнута у 6 пациентов (66,7%), частичная ремиссия – у 1 пациента (22,2%), рецидив зафиксирован у 1 больного (11,1%) на фоне самостоятельной отмены АРВТ, прогрессирование – у 1 пациента (11,1%). У всех больных, получивших терапию, неудача лечения коррелирует с длительностью ВИЧ-инфекции (r=0.67, p<0.05). У больных, ответивших на терапию (n=8), была достигнута низкая вирусная нагрузка на фоне АРВТ: менее 100 копий/мл. Трое пациентов (25%) получили лишь 1-2 курса ПХТ в связи с коморбидностью или низкой приверженностью к терапии. Данные пациенты не получали АРВТ по различным причинам и ремиссии не достигли. Общая 2х летняя выживаемость пациентов, которым выполненная программная ПХТ с лимфомами на фоне ВИЧ (n=9) составила: 89%; лимфома Ходжкина – 100%, ДВККЛ – 75%.
Заключение
В нозологической структуре ВИЧ-ассоциированных лимфом преобладают ДВККЛ с агрессивным течением заболевания. Неудача лечения лимфомы коррелирует с длительностью ВИЧ-инфекции. Благодаря АРВТ, ПХТ может быть проведена в полном объеме с общей выживаемостью, близкой к общей популяции.
Ключевые слова
ВИЧ-инфекция, лимфома, диффузная В-крупноклеточная лимфома, лимфома Ходжкина, химиотерапия, онкогематология.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6961) "Введение
Пациенты, инфицированные ВИЧ, относятся к группе высокого риска развития злокачественных опухолей. Увеличение числа больных НХЛ среди ВИЧ-инфицированных составляет 5,6% в год по сравнению с 0,015% в общей популяции [1]. У ВИЧ-инфицированных пациентов, согласно исследованиям, оглашенным на 22-й Международной конференции по СПИДу (AIDS 2018), риск развития лимфомы Ходжкина – в 33 раза выше чем в общей популяции. Антиретровирусная терапия (АРВТ) в значительной степени влияет на риск развития злокачественных опухолей, которые зависят от уровня CD4-лимфоцитов, и позволяет резко повысить эффективность лечения [2]. Применение АРВТ позволяет увеличить уровень CD4 клеток, снизить риск инфекционных осложнений и применять полихимиотерапию в стандартных дозах, тем не менее лимфомы у пациентов с ВИЧ по-прежнему остаются одной из ведущих причин смерти [3]. Целью нашего исследования было определить эпидемиологические характеристики и оценить эффективность терапии у пациентов с лимфомами на фоне ВИЧ-инфекции.
Пациенты и методы
В ретроспективное исследование включены 12 пациентов, наблюдавшихся на базе ГБУЗ НСО ГКБ №2 «Городской гематологический центр» в период с 2013 по 2017 год (5 лет), с диагнозом лимфома на фоне ВИЧ-инфекции. Средний возраст пациентов 37,4±6,8 лет. Распределение по полу: мужчины – 8 (67%), женщины – 4 (33%). Статистическую обработку результатов проводили c помощью программ статистической обработки данных MSExcel, Statistica 12.0.
Результаты
ВИЧ-ассоциированные лимфомы были представлены следующими нозологиями: диффузная В-крупноклеточная лимфома (ДВККЛ) – 7 (58,3%), лимфома Ходжкина – 4 (33,4%), плазмобластная лимфома – 1 (8%). Экстранодальная локализация лимфомы отмечена у 50% больных. У пациентов с ДВККЛ был рассчитан прогностический индекс для ВИЧ-ассоциированных лимфом (ARL-IPI): в группу высокого риска вошел 1 пациент (14,29%), промежуточного риска – 5 больных (71,43%), низкого риска – 1 человек (14,29%). Все больные на момент дебюта злокачественной лимфомы имели ВИЧ-статус в течение 5-10 лет и не получали АРВТ в связи с низкой вирусной нагрузкой: менее 100 копий/мл. На момент первичной диагностики лимфомы вирусная нагрузка возрастала в несколько раз (94-1700000 копий/мл). Коинфекции: гепатит В – 25%, гепатит С – 58,33%. Пациенты с плазмобластной лимфомой и ДВККЛ получили курсы ПХТ по протоколу R-CHOP и R-MPV, пациенты с лимфомой Ходжкина – по протоколу ABVD. Девяти пациентам (75%) проведено лечение в объеме 4-8 курсов ПХТ. Полная ремиссия заболевания достигнута у 6 пациентов (66,7%), частичная ремиссия – у 1 пациента (22,2%), рецидив зафиксирован у 1 больного (11,1%) на фоне самостоятельной отмены АРВТ, прогрессирование – у 1 пациента (11,1%). У всех больных, получивших терапию, неудача лечения коррелирует с длительностью ВИЧ-инфекции (r=0.67, p<0.05). У больных, ответивших на терапию (n=8), была достигнута низкая вирусная нагрузка на фоне АРВТ: менее 100 копий/мл. Трое пациентов (25%) получили лишь 1-2 курса ПХТ в связи с коморбидностью или низкой приверженностью к терапии. Данные пациенты не получали АРВТ по различным причинам и ремиссии не достигли. Общая 2х летняя выживаемость пациентов, которым выполненная программная ПХТ с лимфомами на фоне ВИЧ (n=9) составила: 89%; лимфома Ходжкина – 100%, ДВККЛ – 75%.
Заключение
В нозологической структуре ВИЧ-ассоциированных лимфом преобладают ДВККЛ с агрессивным течением заболевания. Неудача лечения лимфомы коррелирует с длительностью ВИЧ-инфекции. Благодаря АРВТ, ПХТ может быть проведена в полном объеме с общей выживаемостью, близкой к общей популяции.
Ключевые слова
ВИЧ-инфекция, лимфома, диффузная В-крупноклеточная лимфома, лимфома Ходжкина, химиотерапия, онкогематология.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20494" ["VALUE"]=> array(2) { ["TEXT"]=> string(245) "Кафедра терапии, гематологии, трансфузиологии ФПК и ППВ, Новосибирский государственный медицинский университет, Новосибирск, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(245) "Кафедра терапии, гематологии, трансфузиологии ФПК и ППВ, Новосибирский государственный медицинский университет, Новосибирск, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(245) "Кафедра терапии, гематологии, трансфузиологии ФПК и ППВ, Новосибирский государственный медицинский университет, Новосибирск, Россия" } } } [10]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1572" ["~ID"]=> string(4) "1572" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(226) "Влияние различных видов физической активности у пациентов на результаты трансплантации гемопоэтических стволовых клеток" ["~NAME"]=> string(226) "Влияние различных видов физической активности у пациентов на результаты трансплантации гемопоэтических стволовых клеток" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:35:33" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:35:33" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vliyanie-razlichnykh-vidov-fizicheskoy-aktivnosti-u-patsientov-na-rezultaty-transplantatsii-gemopoet/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vliyanie-razlichnykh-vidov-fizicheskoy-aktivnosti-u-patsientov-na-rezultaty-transplantatsii-gemopoet/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "vliyanie-razlichnykh-vidov-fizicheskoy-aktivnosti-u-patsientov-na-rezultaty-transplantatsii-gemopoet" ["~CODE"]=> string(100) "vliyanie-razlichnykh-vidov-fizicheskoy-aktivnosti-u-patsientov-na-rezultaty-transplantatsii-gemopoet" ["EXTERNAL_ID"]=> string(4) "1572" ["~EXTERNAL_ID"]=> string(4) "1572" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(226) "Влияние различных видов физической активности у пациентов на результаты трансплантации гемопоэтических стволовых клеток" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(337) "Влияние различных видов физической активности у пациентов на результаты трансплантации гемопоэтических стволовых клетокEffects of various physical activities of patients upon the outcomes of hematopoietic stem cell transplantation" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(5235) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения для пациентов с онкогематологическими заболеваниями, например, с о. лейкозом. Однако, пациенты страдают от многочисленных побочных эффектов, связанных с этим видом лечения. Также высока смертность среди этих больных. В последнее время изучается влияние физических упражнений для этой группы пациентов. Целью нашего исследования было оценить безопасность физических нагрузок после ТКМ в период панцитопении. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Мы обследовали 11 пациентов за 3 месяца в период ТКМ в возрасте от 20 до 56 лет с различными онкогематологическими заболеваниями, из них 8 пациентов (66%) с диагнозом – о. лейкоз. У 6 пациентов был немиелоаблативный режим кондиционирования, у 5 – миелоаблативный. Для всех пациентов это была первая трансплантация. Источником трансплантата у 2 пациентов был костный мозг, у 9 – периферические стволовые клетки. Для определения физической выносливости мы использовали 6-ти минутный тест, для определения мышечной силы – динамометрию, которые проводили до трансплантации и после приживления трансплантата. 11 пациентов получали различные виды физических нагрузок до восстановления гемопоэза, даже в период глубокой цитопении. У 2 пациентов была аэробная физическая нагрузка (велотренажер) от 5 до 15 минут в зависимости от состояния и показателей клинического анализа крови. 9 пациентов выполняли комплексы упражнений в исходном положении сидя или лежа в зависимости от самочувствия и показателей крови. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Все пациенты прошли курс физической терапии. Ни один пациент не имел осложнений после проведенных занятий. Приживление трансплантата зафиксировано у всех пациентов в нормальные сроки (от Д+17 до Д+31). Только 2 пациентам (16%) требовалось применение КСФ. 6-минутный тест, проведенный после приживления трансплантата, показал различные результаты: у 6 пациентов наблюдались лучшие результаты этого теста – увеличение пройденного расстояния. Только у 3 пациентов увеличилась мышечная сила по результатам динамометрии. Все пациенты отмечали улучшение настроения после физической активности. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Пилотное исследование показало, что физическая нагрузка безопасна весь период цитопении после трансплантации. Для оценки влияние на исходы трансплантации необходимо проведение дальнейших исследований с группой контроля. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток, цитопения, 6-минутная ходьба, динамометрия, физические упражнения. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(226) "Влияние различных видов физической активности у пациентов на результаты трансплантации гемопоэтических стволовых клеток" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(226) "Влияние различных видов физической активности у пациентов на результаты трансплантации гемопоэтических стволовых клеток" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(226) "Влияние различных видов физической активности у пациентов на результаты трансплантации гемопоэтических стволовых клеток" ["SECTION_META_TITLE"]=> string(226) "Влияние различных видов физической активности у пациентов на результаты трансплантации гемопоэтических стволовых клеток" ["SECTION_META_KEYWORDS"]=> string(226) "Влияние различных видов физической активности у пациентов на результаты трансплантации гемопоэтических стволовых клеток" ["SECTION_META_DESCRIPTION"]=> string(226) "Влияние различных видов физической активности у пациентов на результаты трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_ALT"]=> string(226) "Влияние различных видов физической активности у пациентов на результаты трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_TITLE"]=> string(226) "Влияние различных видов физической активности у пациентов на результаты трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "vliyanie-razlichnykh-vidov-fizicheskoy-aktivnosti-u-patsientov-na-rezultaty-transplantatsii-gemopoet" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(226) "Влияние различных видов физической активности у пациентов на результаты трансплантации гемопоэтических стволовых клеток" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(226) "Влияние различных видов физической активности у пациентов на результаты трансплантации гемопоэтических стволовых клеток" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vliyanie-razlichnykh-vidov-fizicheskoy-aktivnosti-u-patsientov-na-rezultaty-transplantatsii-gemopoet" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "vliyanie-razlichnykh-vidov-fizicheskoy-aktivnosti-u-patsientov-na-rezultaty-transplantatsii-gemopoet" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vliyanie-razlichnykh-vidov-fizicheskoy-aktivnosti-u-patsientov-na-rezultaty-transplantatsii-gemopoet" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20484" ["VALUE"]=> array(2) { ["TEXT"]=> string(159) "Анна А. Колобова, Марина Н. Браеску, Алиса Г. Волкова, Елена И. Дарская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(159) "Анна А. Колобова, Марина Н. Браеску, Алиса Г. Волкова, Елена И. Дарская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20485" ["VALUE"]=> array(2) { ["TEXT"]=> string(347) "НИИ детской гематологии и трансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, СПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(347) "НИИ детской гематологии и трансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, СПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20486" ["VALUE"]=> array(2) { ["TEXT"]=> string(5235) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения для пациентов с онкогематологическими заболеваниями, например, с о. лейкозом. Однако, пациенты страдают от многочисленных побочных эффектов, связанных с этим видом лечения. Также высока смертность среди этих больных. В последнее время изучается влияние физических упражнений для этой группы пациентов. Целью нашего исследования было оценить безопасность физических нагрузок после ТКМ в период панцитопении. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Мы обследовали 11 пациентов за 3 месяца в период ТКМ в возрасте от 20 до 56 лет с различными онкогематологическими заболеваниями, из них 8 пациентов (66%) с диагнозом – о. лейкоз. У 6 пациентов был немиелоаблативный режим кондиционирования, у 5 – миелоаблативный. Для всех пациентов это была первая трансплантация. Источником трансплантата у 2 пациентов был костный мозг, у 9 – периферические стволовые клетки. Для определения физической выносливости мы использовали 6-ти минутный тест, для определения мышечной силы – динамометрию, которые проводили до трансплантации и после приживления трансплантата. 11 пациентов получали различные виды физических нагрузок до восстановления гемопоэза, даже в период глубокой цитопении. У 2 пациентов была аэробная физическая нагрузка (велотренажер) от 5 до 15 минут в зависимости от состояния и показателей клинического анализа крови. 9 пациентов выполняли комплексы упражнений в исходном положении сидя или лежа в зависимости от самочувствия и показателей крови. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Все пациенты прошли курс физической терапии. Ни один пациент не имел осложнений после проведенных занятий. Приживление трансплантата зафиксировано у всех пациентов в нормальные сроки (от Д+17 до Д+31). Только 2 пациентам (16%) требовалось применение КСФ. 6-минутный тест, проведенный после приживления трансплантата, показал различные результаты: у 6 пациентов наблюдались лучшие результаты этого теста – увеличение пройденного расстояния. Только у 3 пациентов увеличилась мышечная сила по результатам динамометрии. Все пациенты отмечали улучшение настроения после физической активности. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Пилотное исследование показало, что физическая нагрузка безопасна весь период цитопении после трансплантации. Для оценки влияние на исходы трансплантации необходимо проведение дальнейших исследований с группой контроля. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток, цитопения, 6-минутная ходьба, динамометрия, физические упражнения. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5003) "Введение
Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения для пациентов с онкогематологическими заболеваниями, например, с о. лейкозом. Однако, пациенты страдают от многочисленных побочных эффектов, связанных с этим видом лечения. Также высока смертность среди этих больных. В последнее время изучается влияние физических упражнений для этой группы пациентов. Целью нашего исследования было оценить безопасность физических нагрузок после ТКМ в период панцитопении.
Материалы и методы
Мы обследовали 11 пациентов за 3 месяца в период ТКМ в возрасте от 20 до 56 лет с различными онкогематологическими заболеваниями, из них 8 пациентов (66%) с диагнозом – о. лейкоз. У 6 пациентов был немиелоаблативный режим кондиционирования, у 5 – миелоаблативный. Для всех пациентов это была первая трансплантация. Источником трансплантата у 2 пациентов был костный мозг, у 9 – периферические стволовые клетки. Для определения физической выносливости мы использовали 6-ти минутный тест, для определения мышечной силы – динамометрию, которые проводили до трансплантации и после приживления трансплантата. 11 пациентов получали различные виды физических нагрузок до восстановления гемопоэза, даже в период глубокой цитопении. У 2 пациентов была аэробная физическая нагрузка (велотренажер) от 5 до 15 минут в зависимости от состояния и показателей клинического анализа крови. 9 пациентов выполняли комплексы упражнений в исходном положении сидя или лежа в зависимости от самочувствия и показателей крови.
Результаты
Все пациенты прошли курс физической терапии. Ни один пациент не имел осложнений после проведенных занятий. Приживление трансплантата зафиксировано у всех пациентов в нормальные сроки (от Д+17 до Д+31). Только 2 пациентам (16%) требовалось применение КСФ. 6-минутный тест, проведенный после приживления трансплантата, показал различные результаты: у 6 пациентов наблюдались лучшие результаты этого теста – увеличение пройденного расстояния. Только у 3 пациентов увеличилась мышечная сила по результатам динамометрии. Все пациенты отмечали улучшение настроения после физической активности.
Заключение
Пилотное исследование показало, что физическая нагрузка безопасна весь период цитопении после трансплантации. Для оценки влияние на исходы трансплантации необходимо проведение дальнейших исследований с группой контроля.
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, цитопения, 6-минутная ходьба, динамометрия, физические упражнения.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20487" ["VALUE"]=> array(2) { ["TEXT"]=> string(92) "Anna A. Kolobova, Marina N. Braesku, Alisa G. Volkova, Elena I. Darskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(92) "Anna A. Kolobova, Marina N. Braesku, Alisa G. Volkova, Elena I. Darskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20488" ["VALUE"]=> array(2) { ["TEXT"]=> string(230) "R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantation, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(230) "R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantation, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20489" ["VALUE"]=> array(2) { ["TEXT"]=> string(3475) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic stem cell transplantation (allo-HCT) is an effective curative treatment for patients with haematological malignancies in high-risk diseases e.g. acute leukaemia. However, patients suffer from numerous treatment related side-effects and complications, and the transplant-related mortality is high. Exercise is a promising intervention approach for this group of patients. Over the last years, several clinical trials have contributed to the growing body of evidence showing the beneficial effects of exercise in cancer patients. The purpose of our study was to evaluate the effect of various types of physical activity on the recovery of hemopoiesis after BMT. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> We examined 11 patients for 3 months in the period of BMT (20-56 years) with haematological diseases undergoing allogeneic stem cell transplantion, of these, 8 patients (66%) were diagnosed with acute leukemia. 6 patients had a non-myeloablative conditioning regimen, and 5 had a myeloablative regimen. Criteria for patients included in this sample were: no symptoms of coronary illness or uncontrolled high blood pressure, being over 18 years of age. For all patients, this was the first transplantation. The source of the transplant in 2 patients is BM, in 9 patients the PBSC. We determined physical endurance with a 6-minute walk test, and muscular strength with a dynamometer. These tests were performed before transplantation and immediately after the signs of transplant engraftment. All 11 patients received various physical loads throughout the time until the recovery of hemopoiesis, even in the period of deep cytopenia. Two patients had an aerobic exercise (an exercise bike), from 5 to 15 minutes, depending on the state of health and the results of blood tests. 9 patients performed physical exercises in the initial sitting or lying position, depending on the state of health and the results of blood tests. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> All patients underwent a course of physical therapy. No patient quit training. Engraftment of the graft was recorded in all patients during normal periods (from D + 17 to D + 31). Only 2 patients (16%) required the use of CSF. A 6-minute test, performed after engraftment of the transplant, showed different results: in 6 patients the results of this test were observed – an increase in the distance traveled. Only in 3 patients muscular strength increased by the results of dynamometry.<br> All patients reported improvement in mood after physical activity. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Physical exercise is feasible in patients with pancytopenia after allo-HCT. Further controlled studies are required to evaluate if physical activity improves the outcomes of transplantation. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Allogeneic stem cell transplantation, cytopenia, 6-minute walk test, dynamometry, physical exercise. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3237) "Introduction
Allogeneic stem cell transplantation (allo-HCT) is an effective curative treatment for patients with haematological malignancies in high-risk diseases e.g. acute leukaemia. However, patients suffer from numerous treatment related side-effects and complications, and the transplant-related mortality is high. Exercise is a promising intervention approach for this group of patients. Over the last years, several clinical trials have contributed to the growing body of evidence showing the beneficial effects of exercise in cancer patients. The purpose of our study was to evaluate the effect of various types of physical activity on the recovery of hemopoiesis after BMT.
Materials and methods
We examined 11 patients for 3 months in the period of BMT (20-56 years) with haematological diseases undergoing allogeneic stem cell transplantion, of these, 8 patients (66%) were diagnosed with acute leukemia. 6 patients had a non-myeloablative conditioning regimen, and 5 had a myeloablative regimen. Criteria for patients included in this sample were: no symptoms of coronary illness or uncontrolled high blood pressure, being over 18 years of age. For all patients, this was the first transplantation. The source of the transplant in 2 patients is BM, in 9 patients the PBSC. We determined physical endurance with a 6-minute walk test, and muscular strength with a dynamometer. These tests were performed before transplantation and immediately after the signs of transplant engraftment. All 11 patients received various physical loads throughout the time until the recovery of hemopoiesis, even in the period of deep cytopenia. Two patients had an aerobic exercise (an exercise bike), from 5 to 15 minutes, depending on the state of health and the results of blood tests. 9 patients performed physical exercises in the initial sitting or lying position, depending on the state of health and the results of blood tests.
Results
All patients underwent a course of physical therapy. No patient quit training. Engraftment of the graft was recorded in all patients during normal periods (from D + 17 to D + 31). Only 2 patients (16%) required the use of CSF. A 6-minute test, performed after engraftment of the transplant, showed different results: in 6 patients the results of this test were observed – an increase in the distance traveled. Only in 3 patients muscular strength increased by the results of dynamometry.
All patients reported improvement in mood after physical activity.
Conclusion
Physical exercise is feasible in patients with pancytopenia after allo-HCT. Further controlled studies are required to evaluate if physical activity improves the outcomes of transplantation.
Keywords
Allogeneic stem cell transplantation, cytopenia, 6-minute walk test, dynamometry, physical exercise.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20490" ["VALUE"]=> string(111) "Effects of various physical activities of patients upon the outcomes of hematopoietic stem cell transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(111) "Effects of various physical activities of patients upon the outcomes of hematopoietic stem cell transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20777" ["VALUE"]=> string(4) "1415" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1415" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20778" ["VALUE"]=> string(4) "1416" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1416" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20487" ["VALUE"]=> array(2) { ["TEXT"]=> string(92) "Anna A. Kolobova, Marina N. Braesku, Alisa G. Volkova, Elena I. Darskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(92) "Anna A. Kolobova, Marina N. Braesku, Alisa G. Volkova, Elena I. Darskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(92) "Anna A. Kolobova, Marina N. Braesku, Alisa G. Volkova, Elena I. Darskaya, Boris V. Afanasyev" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20489" ["VALUE"]=> array(2) { ["TEXT"]=> string(3475) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic stem cell transplantation (allo-HCT) is an effective curative treatment for patients with haematological malignancies in high-risk diseases e.g. acute leukaemia. However, patients suffer from numerous treatment related side-effects and complications, and the transplant-related mortality is high. Exercise is a promising intervention approach for this group of patients. Over the last years, several clinical trials have contributed to the growing body of evidence showing the beneficial effects of exercise in cancer patients. The purpose of our study was to evaluate the effect of various types of physical activity on the recovery of hemopoiesis after BMT. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> We examined 11 patients for 3 months in the period of BMT (20-56 years) with haematological diseases undergoing allogeneic stem cell transplantion, of these, 8 patients (66%) were diagnosed with acute leukemia. 6 patients had a non-myeloablative conditioning regimen, and 5 had a myeloablative regimen. Criteria for patients included in this sample were: no symptoms of coronary illness or uncontrolled high blood pressure, being over 18 years of age. For all patients, this was the first transplantation. The source of the transplant in 2 patients is BM, in 9 patients the PBSC. We determined physical endurance with a 6-minute walk test, and muscular strength with a dynamometer. These tests were performed before transplantation and immediately after the signs of transplant engraftment. All 11 patients received various physical loads throughout the time until the recovery of hemopoiesis, even in the period of deep cytopenia. Two patients had an aerobic exercise (an exercise bike), from 5 to 15 minutes, depending on the state of health and the results of blood tests. 9 patients performed physical exercises in the initial sitting or lying position, depending on the state of health and the results of blood tests. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> All patients underwent a course of physical therapy. No patient quit training. Engraftment of the graft was recorded in all patients during normal periods (from D + 17 to D + 31). Only 2 patients (16%) required the use of CSF. A 6-minute test, performed after engraftment of the transplant, showed different results: in 6 patients the results of this test were observed – an increase in the distance traveled. Only in 3 patients muscular strength increased by the results of dynamometry.<br> All patients reported improvement in mood after physical activity. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Physical exercise is feasible in patients with pancytopenia after allo-HCT. Further controlled studies are required to evaluate if physical activity improves the outcomes of transplantation. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Allogeneic stem cell transplantation, cytopenia, 6-minute walk test, dynamometry, physical exercise. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3237) "Introduction
Allogeneic stem cell transplantation (allo-HCT) is an effective curative treatment for patients with haematological malignancies in high-risk diseases e.g. acute leukaemia. However, patients suffer from numerous treatment related side-effects and complications, and the transplant-related mortality is high. Exercise is a promising intervention approach for this group of patients. Over the last years, several clinical trials have contributed to the growing body of evidence showing the beneficial effects of exercise in cancer patients. The purpose of our study was to evaluate the effect of various types of physical activity on the recovery of hemopoiesis after BMT.
Materials and methods
We examined 11 patients for 3 months in the period of BMT (20-56 years) with haematological diseases undergoing allogeneic stem cell transplantion, of these, 8 patients (66%) were diagnosed with acute leukemia. 6 patients had a non-myeloablative conditioning regimen, and 5 had a myeloablative regimen. Criteria for patients included in this sample were: no symptoms of coronary illness or uncontrolled high blood pressure, being over 18 years of age. For all patients, this was the first transplantation. The source of the transplant in 2 patients is BM, in 9 patients the PBSC. We determined physical endurance with a 6-minute walk test, and muscular strength with a dynamometer. These tests were performed before transplantation and immediately after the signs of transplant engraftment. All 11 patients received various physical loads throughout the time until the recovery of hemopoiesis, even in the period of deep cytopenia. Two patients had an aerobic exercise (an exercise bike), from 5 to 15 minutes, depending on the state of health and the results of blood tests. 9 patients performed physical exercises in the initial sitting or lying position, depending on the state of health and the results of blood tests.
Results
All patients underwent a course of physical therapy. No patient quit training. Engraftment of the graft was recorded in all patients during normal periods (from D + 17 to D + 31). Only 2 patients (16%) required the use of CSF. A 6-minute test, performed after engraftment of the transplant, showed different results: in 6 patients the results of this test were observed – an increase in the distance traveled. Only in 3 patients muscular strength increased by the results of dynamometry.
All patients reported improvement in mood after physical activity.
Conclusion
Physical exercise is feasible in patients with pancytopenia after allo-HCT. Further controlled studies are required to evaluate if physical activity improves the outcomes of transplantation.
Keywords
Allogeneic stem cell transplantation, cytopenia, 6-minute walk test, dynamometry, physical exercise.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3237) "Introduction
Allogeneic stem cell transplantation (allo-HCT) is an effective curative treatment for patients with haematological malignancies in high-risk diseases e.g. acute leukaemia. However, patients suffer from numerous treatment related side-effects and complications, and the transplant-related mortality is high. Exercise is a promising intervention approach for this group of patients. Over the last years, several clinical trials have contributed to the growing body of evidence showing the beneficial effects of exercise in cancer patients. The purpose of our study was to evaluate the effect of various types of physical activity on the recovery of hemopoiesis after BMT.
Materials and methods
We examined 11 patients for 3 months in the period of BMT (20-56 years) with haematological diseases undergoing allogeneic stem cell transplantion, of these, 8 patients (66%) were diagnosed with acute leukemia. 6 patients had a non-myeloablative conditioning regimen, and 5 had a myeloablative regimen. Criteria for patients included in this sample were: no symptoms of coronary illness or uncontrolled high blood pressure, being over 18 years of age. For all patients, this was the first transplantation. The source of the transplant in 2 patients is BM, in 9 patients the PBSC. We determined physical endurance with a 6-minute walk test, and muscular strength with a dynamometer. These tests were performed before transplantation and immediately after the signs of transplant engraftment. All 11 patients received various physical loads throughout the time until the recovery of hemopoiesis, even in the period of deep cytopenia. Two patients had an aerobic exercise (an exercise bike), from 5 to 15 minutes, depending on the state of health and the results of blood tests. 9 patients performed physical exercises in the initial sitting or lying position, depending on the state of health and the results of blood tests.
Results
All patients underwent a course of physical therapy. No patient quit training. Engraftment of the graft was recorded in all patients during normal periods (from D + 17 to D + 31). Only 2 patients (16%) required the use of CSF. A 6-minute test, performed after engraftment of the transplant, showed different results: in 6 patients the results of this test were observed – an increase in the distance traveled. Only in 3 patients muscular strength increased by the results of dynamometry.
All patients reported improvement in mood after physical activity.
Conclusion
Physical exercise is feasible in patients with pancytopenia after allo-HCT. Further controlled studies are required to evaluate if physical activity improves the outcomes of transplantation.
Keywords
Allogeneic stem cell transplantation, cytopenia, 6-minute walk test, dynamometry, physical exercise.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20490" ["VALUE"]=> string(111) "Effects of various physical activities of patients upon the outcomes of hematopoietic stem cell transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(111) "Effects of various physical activities of patients upon the outcomes of hematopoietic stem cell transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(111) "Effects of various physical activities of patients upon the outcomes of hematopoietic stem cell transplantation" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20488" ["VALUE"]=> array(2) { ["TEXT"]=> string(230) "R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantation, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(230) "R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantation, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(230) "R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantation, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20484" ["VALUE"]=> array(2) { ["TEXT"]=> string(159) "Анна А. Колобова, Марина Н. Браеску, Алиса Г. Волкова, Елена И. Дарская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(159) "Анна А. Колобова, Марина Н. Браеску, Алиса Г. Волкова, Елена И. Дарская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(159) "Анна А. Колобова, Марина Н. Браеску, Алиса Г. Волкова, Елена И. Дарская, Борис В. Афанасьев" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20486" ["VALUE"]=> array(2) { ["TEXT"]=> string(5235) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения для пациентов с онкогематологическими заболеваниями, например, с о. лейкозом. Однако, пациенты страдают от многочисленных побочных эффектов, связанных с этим видом лечения. Также высока смертность среди этих больных. В последнее время изучается влияние физических упражнений для этой группы пациентов. Целью нашего исследования было оценить безопасность физических нагрузок после ТКМ в период панцитопении. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Мы обследовали 11 пациентов за 3 месяца в период ТКМ в возрасте от 20 до 56 лет с различными онкогематологическими заболеваниями, из них 8 пациентов (66%) с диагнозом – о. лейкоз. У 6 пациентов был немиелоаблативный режим кондиционирования, у 5 – миелоаблативный. Для всех пациентов это была первая трансплантация. Источником трансплантата у 2 пациентов был костный мозг, у 9 – периферические стволовые клетки. Для определения физической выносливости мы использовали 6-ти минутный тест, для определения мышечной силы – динамометрию, которые проводили до трансплантации и после приживления трансплантата. 11 пациентов получали различные виды физических нагрузок до восстановления гемопоэза, даже в период глубокой цитопении. У 2 пациентов была аэробная физическая нагрузка (велотренажер) от 5 до 15 минут в зависимости от состояния и показателей клинического анализа крови. 9 пациентов выполняли комплексы упражнений в исходном положении сидя или лежа в зависимости от самочувствия и показателей крови. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Все пациенты прошли курс физической терапии. Ни один пациент не имел осложнений после проведенных занятий. Приживление трансплантата зафиксировано у всех пациентов в нормальные сроки (от Д+17 до Д+31). Только 2 пациентам (16%) требовалось применение КСФ. 6-минутный тест, проведенный после приживления трансплантата, показал различные результаты: у 6 пациентов наблюдались лучшие результаты этого теста – увеличение пройденного расстояния. Только у 3 пациентов увеличилась мышечная сила по результатам динамометрии. Все пациенты отмечали улучшение настроения после физической активности. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Пилотное исследование показало, что физическая нагрузка безопасна весь период цитопении после трансплантации. Для оценки влияние на исходы трансплантации необходимо проведение дальнейших исследований с группой контроля. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток, цитопения, 6-минутная ходьба, динамометрия, физические упражнения. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5003) "Введение
Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения для пациентов с онкогематологическими заболеваниями, например, с о. лейкозом. Однако, пациенты страдают от многочисленных побочных эффектов, связанных с этим видом лечения. Также высока смертность среди этих больных. В последнее время изучается влияние физических упражнений для этой группы пациентов. Целью нашего исследования было оценить безопасность физических нагрузок после ТКМ в период панцитопении.
Материалы и методы
Мы обследовали 11 пациентов за 3 месяца в период ТКМ в возрасте от 20 до 56 лет с различными онкогематологическими заболеваниями, из них 8 пациентов (66%) с диагнозом – о. лейкоз. У 6 пациентов был немиелоаблативный режим кондиционирования, у 5 – миелоаблативный. Для всех пациентов это была первая трансплантация. Источником трансплантата у 2 пациентов был костный мозг, у 9 – периферические стволовые клетки. Для определения физической выносливости мы использовали 6-ти минутный тест, для определения мышечной силы – динамометрию, которые проводили до трансплантации и после приживления трансплантата. 11 пациентов получали различные виды физических нагрузок до восстановления гемопоэза, даже в период глубокой цитопении. У 2 пациентов была аэробная физическая нагрузка (велотренажер) от 5 до 15 минут в зависимости от состояния и показателей клинического анализа крови. 9 пациентов выполняли комплексы упражнений в исходном положении сидя или лежа в зависимости от самочувствия и показателей крови.
Результаты
Все пациенты прошли курс физической терапии. Ни один пациент не имел осложнений после проведенных занятий. Приживление трансплантата зафиксировано у всех пациентов в нормальные сроки (от Д+17 до Д+31). Только 2 пациентам (16%) требовалось применение КСФ. 6-минутный тест, проведенный после приживления трансплантата, показал различные результаты: у 6 пациентов наблюдались лучшие результаты этого теста – увеличение пройденного расстояния. Только у 3 пациентов увеличилась мышечная сила по результатам динамометрии. Все пациенты отмечали улучшение настроения после физической активности.
Заключение
Пилотное исследование показало, что физическая нагрузка безопасна весь период цитопении после трансплантации. Для оценки влияние на исходы трансплантации необходимо проведение дальнейших исследований с группой контроля.
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, цитопения, 6-минутная ходьба, динамометрия, физические упражнения.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(5003) "Введение
Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения для пациентов с онкогематологическими заболеваниями, например, с о. лейкозом. Однако, пациенты страдают от многочисленных побочных эффектов, связанных с этим видом лечения. Также высока смертность среди этих больных. В последнее время изучается влияние физических упражнений для этой группы пациентов. Целью нашего исследования было оценить безопасность физических нагрузок после ТКМ в период панцитопении.
Материалы и методы
Мы обследовали 11 пациентов за 3 месяца в период ТКМ в возрасте от 20 до 56 лет с различными онкогематологическими заболеваниями, из них 8 пациентов (66%) с диагнозом – о. лейкоз. У 6 пациентов был немиелоаблативный режим кондиционирования, у 5 – миелоаблативный. Для всех пациентов это была первая трансплантация. Источником трансплантата у 2 пациентов был костный мозг, у 9 – периферические стволовые клетки. Для определения физической выносливости мы использовали 6-ти минутный тест, для определения мышечной силы – динамометрию, которые проводили до трансплантации и после приживления трансплантата. 11 пациентов получали различные виды физических нагрузок до восстановления гемопоэза, даже в период глубокой цитопении. У 2 пациентов была аэробная физическая нагрузка (велотренажер) от 5 до 15 минут в зависимости от состояния и показателей клинического анализа крови. 9 пациентов выполняли комплексы упражнений в исходном положении сидя или лежа в зависимости от самочувствия и показателей крови.
Результаты
Все пациенты прошли курс физической терапии. Ни один пациент не имел осложнений после проведенных занятий. Приживление трансплантата зафиксировано у всех пациентов в нормальные сроки (от Д+17 до Д+31). Только 2 пациентам (16%) требовалось применение КСФ. 6-минутный тест, проведенный после приживления трансплантата, показал различные результаты: у 6 пациентов наблюдались лучшие результаты этого теста – увеличение пройденного расстояния. Только у 3 пациентов увеличилась мышечная сила по результатам динамометрии. Все пациенты отмечали улучшение настроения после физической активности.
Заключение
Пилотное исследование показало, что физическая нагрузка безопасна весь период цитопении после трансплантации. Для оценки влияние на исходы трансплантации необходимо проведение дальнейших исследований с группой контроля.
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, цитопения, 6-минутная ходьба, динамометрия, физические упражнения.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20485" ["VALUE"]=> array(2) { ["TEXT"]=> string(347) "НИИ детской гематологии и трансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, СПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(347) "НИИ детской гематологии и трансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, СПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(347) "НИИ детской гематологии и трансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, СПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" } } } [11]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1571" ["~ID"]=> string(4) "1571" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(444) "Клинический и фармакоэкономический анализ использования пегилированной и непегилированной форм колониестимулирующих факторов для стимуляции лейкопоэза после аутологичной трансплантации периферических гемопоэтических стволовых клеток" ["~NAME"]=> string(444) "Клинический и фармакоэкономический анализ использования пегилированной и непегилированной форм колониестимулирующих факторов для стимуляции лейкопоэза после аутологичной трансплантации периферических гемопоэтических стволовых клеток" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:34:23" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:34:23" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/klinicheskiy-i-farmakoekonomicheskiy-analiz-ispolzovaniya-pegilirovannoy-i-nepegilirovannoy-form-kol/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/klinicheskiy-i-farmakoekonomicheskiy-analiz-ispolzovaniya-pegilirovannoy-i-nepegilirovannoy-form-kol/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "klinicheskiy-i-farmakoekonomicheskiy-analiz-ispolzovaniya-pegilirovannoy-i-nepegilirovannoy-form-kol" ["~CODE"]=> string(100) "klinicheskiy-i-farmakoekonomicheskiy-analiz-ispolzovaniya-pegilirovannoy-i-nepegilirovannoy-form-kol" ["EXTERNAL_ID"]=> string(4) "1571" ["~EXTERNAL_ID"]=> string(4) "1571" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(444) "Клинический и фармакоэкономический анализ использования пегилированной и непегилированной форм колониестимулирующих факторов для стимуляции лейкопоэза после аутологичной трансплантации периферических гемопоэтических стволовых клеток" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(655) "Клинический и фармакоэкономический анализ использования пегилированной и непегилированной форм колониестимулирующих факторов для стимуляции лейкопоэза после аутологичной трансплантации периферических гемопоэтических стволовых клетокClinical and pharmacoeconomic analysis of pegylated and nonpegylated forms of colony-stimulating factors after autologous transplantation of hematopoietic stem cells in patients with lymphoproliferative diseases" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(12215) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Проведение высокодозной химиотерапии (ВДХТ) с аутологичной трансплантацией периферических гемопоэтических стволовых клеток (ауто-ТГСК) осложняется развитием гематологической токсичности IV степени. Среди осложнений при проведении данного лечения наиболее частым являются инфекционные. Длительность нейтропении IV степени коррелирует с развитием тяжелых инфекционных осложнений, которые могут стать причиной летального исхода в раннем посттрансплантационном периоде. Применение колониестимулирующих факторов (КСФ) снижает длительность нейтропении и риск развития инфекционных осложнений, а также сокращает пребывание пациента в специализированном отделении стационара. Цель исследования оценить и сравнить эффективность и безопасность двух форм КСФ, филграстима и его пегилированной формы, для стимуляции лейкопоэза при проведении ВДХТ с последующей ауто-ТГСК у пациентов с лимфопролиферативными заболеваниями, а также определить наиболее предпочтительную с точки зрения фармакоэкономического анализа форму КСФ. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В исследование включено 100 больных: 39 – c лимфомой Ходжкина, 18 – с неходжкинскими лимфомами, 42 – с множественной миеломой, 1 – острый промиелоцитарный лейкоз; 51 – женщина, 49 – мужчин. Медиана возраста составила 43 года (18-72) (табл. 1). Кондиционирование проводилось по схемам алкеран 200 мг/м. кв., алкеран 140 мг/м.кв., BeEAC, CBV, BEAM, цитарабин+мелфалан. Пациенты были рандомизированы на группы: 1 группа – пациенты, получающие пегилированную форму КСФ (ПЕГ-КСФ) (n=52), 2 группа – пациенты, получающие непегилированную форму КСФ (n=48). Стимуляцию лейкопоэза начинали на Д+4. Г-КСФ вводили ежедневно в дозе 5 мкг /кг/день до выхода из агранулоцитоза (WBC=3,0х10 в 9 ст./л ). ПЕГ-КСФ вводили однократно в дозе 6 мг (на Д+4). Фармакоэкономический анализ включал сопоставление относительной экономической оценки ПЕГ-КСФ и непегилированной формы КСФ. Учитывались затраты на ПЕГ-КСФ или КСФ, которые вводились соответствующему пациенту в период после выполнения ауто-ТГСК. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Сравнительный клинический анализ использования КСФ и ПЕГ-КСФ проводился по следующим параметрам: возраст, число линий предтрансплантационной химиотерапии, количество трансплантированных CD34+ млн/кг, показатели восстановления гемопоэза, наличие инфекционных осложнений (нейтропеническая лихорадка), длительность госпитализации (табл. 2). Значимые отличия были получены по скорости восстановления уровня лейкоцитов (у пациентов из группы ПЕГ-КСФ выход из агранулоцитоза регистрировался значимо раньше). Но в группе КСФ угнетение эритроидного ростка было значимо меньше. Достоверных отличий по другим анализируемым параметрам получено не было.<br> Фармакоэкономический анализ показал, что медиана суммы денежных средств, использованных для приобретения ПЕГ-КСФ, вводимых для лечения одного больного, составила 49042,73 руб., а для КСФ 36180,63 руб. (p<0,05) (табл. 3). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> При клиническом анализе применения пегилированной и непегилированной форм колониестимулирующих факторов существенных отличий не выявлено. Фармакоэкономический анализ выявил преимущество непегилированной формы КСФ над ПЕГ-КСФ. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, аутологичная, колониестимулирующий фактор, пегилированный, эффективность, фармакоэкономика. </p> <h2>Таблица 1. Общая клиническая характеристика больных</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Число больных в группе </td> <td> 100 </td> </tr> <tr> <td> Возраст, медиана (интервал), лет </td> <td> 43 (18-72) </td> </tr> <tr> <td> Мужчины, абс. (%) </td> <td> 49 (49) </td> </tr> <tr> <td> Женщины, абс. (%) </td> <td> 51 (51) </td> </tr> <tr> <td> Неходжкинские лимфомы, абс. (%) </td> <td> 18 (18) </td> </tr> <tr> <td> Лимфома Ходжкина, абс. (%) </td> <td> 39 (39) </td> </tr> <tr> <td> Множественная миелома, абс. (%) </td> <td> 42 (42) </td> </tr> <tr> <td> Острый промиелоцитарный лейкоз, абс. (%) 1 </td> <td> 1 (1) </td> </tr> </tbody> </table> <h2>Таблица 2. Сравнительный анализ ПЕГ-КСФ и КСФ</h2> <table> <tbody> <tr> <td> </td> <td> Группа КСФ </td> <td> Группа ПЕГ-КСФ </td> <td> t-знач. </td> <td> p </td> </tr> <tr> <td> Возраст, годы (медиана) </td> <td> 43 </td> <td> 41,5 </td> <td> 0,12 </td> <td> 0,9 </td> </tr> <tr> <td> Количество трансплантированных CD34+ млн/кг, медиана </td> <td> 2,59 </td> <td> 2,65 </td> <td> 0,13 </td> <td> 0,86 </td> </tr> <tr> <td> Дни агранулоцитоза (медиана) </td> <td> 7 </td> <td> 8 </td> <td> -0,93 </td> <td> 0,35 </td> </tr> <tr> <td> День (после ТГСК) выхода из агранулоцитоза (медиана) </td> <td> 11 </td> <td> 10 </td> <td> 2,17 </td> <td> 0,03 </td> </tr> <tr> <td> День (после ТГСК) возникновения фебрильной нейтропении </td> <td> 4<br> </td> <td> 5 </td> <td> -1,18 </td> <td> 0,23 </td> </tr> <tr> <td> Пациенты с нейтропенической лихорадкой, абс. (%) </td> <td> 34 (34%) </td> <td> 40 (40%) </td> <td> 0,63 </td> <td> 0,52 </td> </tr> <tr> <td> Дни тромбоцитопении ниже 20х10^9/л (медиана) </td> <td> 4 </td> <td> 5 </td> <td> -1,42 </td> <td> 0,15 </td> </tr> <tr> <td> Уровень максимального снижения гемоглобина </td> <td> 95 </td> <td> 86 </td> <td> 3,34 </td> <td> 0,001 </td> </tr> <tr> <td> Число линий предтрансплантационной химиотерапии </td> <td> 2 </td> <td> 2 </td> <td> -1,3 </td> <td> 0,19 </td> </tr> <tr> <td> Длительность госпитализации </td> <td> 22 </td> <td> 22 </td> <td> -0,46 </td> <td> 0,64 </td> </tr> </tbody> </table> <h2>Таблица 3. Результаты анализа затрат на профилактику и лечение фебрильной нейтропении на 1 человека после ауто-ТГСК</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> ПЕГ-КСФ для лечения 1 пациента, руб. </td> <td> КСФ для лечения 1 пациента, руб. </td> <td> р </td> </tr> <tr> <td> 49042,73 </td> <td> 36180,63 </td> <td> <0,05 </td> </tr> </tbody> </table> <br>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(444) "Клинический и фармакоэкономический анализ использования пегилированной и непегилированной форм колониестимулирующих факторов для стимуляции лейкопоэза после аутологичной трансплантации периферических гемопоэтических стволовых клеток" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(444) "Клинический и фармакоэкономический анализ использования пегилированной и непегилированной форм колониестимулирующих факторов для стимуляции лейкопоэза после аутологичной трансплантации периферических гемопоэтических стволовых клеток" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(444) "Клинический и фармакоэкономический анализ использования пегилированной и непегилированной форм колониестимулирующих факторов для стимуляции лейкопоэза после аутологичной трансплантации периферических гемопоэтических стволовых клеток" ["SECTION_META_TITLE"]=> string(444) "Клинический и фармакоэкономический анализ использования пегилированной и непегилированной форм колониестимулирующих факторов для стимуляции лейкопоэза после аутологичной трансплантации периферических гемопоэтических стволовых клеток" ["SECTION_META_KEYWORDS"]=> string(444) "Клинический и фармакоэкономический анализ использования пегилированной и непегилированной форм колониестимулирующих факторов для стимуляции лейкопоэза после аутологичной трансплантации периферических гемопоэтических стволовых клеток" ["SECTION_META_DESCRIPTION"]=> string(444) "Клинический и фармакоэкономический анализ использования пегилированной и непегилированной форм колониестимулирующих факторов для стимуляции лейкопоэза после аутологичной трансплантации периферических гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_ALT"]=> string(444) "Клинический и фармакоэкономический анализ использования пегилированной и непегилированной форм колониестимулирующих факторов для стимуляции лейкопоэза после аутологичной трансплантации периферических гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_TITLE"]=> string(444) "Клинический и фармакоэкономический анализ использования пегилированной и непегилированной форм колониестимулирующих факторов для стимуляции лейкопоэза после аутологичной трансплантации периферических гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "klinicheskiy-i-farmakoekonomicheskiy-analiz-ispolzovaniya-pegilirovannoy-i-nepegilirovannoy-form-kol" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(444) "Клинический и фармакоэкономический анализ использования пегилированной и непегилированной форм колониестимулирующих факторов для стимуляции лейкопоэза после аутологичной трансплантации периферических гемопоэтических стволовых клеток" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(444) "Клинический и фармакоэкономический анализ использования пегилированной и непегилированной форм колониестимулирующих факторов для стимуляции лейкопоэза после аутологичной трансплантации периферических гемопоэтических стволовых клеток" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "klinicheskiy-i-farmakoekonomicheskiy-analiz-ispolzovaniya-pegilirovannoy-i-nepegilirovannoy-form-kol" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "klinicheskiy-i-farmakoekonomicheskiy-analiz-ispolzovaniya-pegilirovannoy-i-nepegilirovannoy-form-kol" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "klinicheskiy-i-farmakoekonomicheskiy-analiz-ispolzovaniya-pegilirovannoy-i-nepegilirovannoy-form-kol" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20475" ["VALUE"]=> array(2) { ["TEXT"]=> string(284) "Диана Д. Иванова, Владислав О. Саржевский, Владимир Я. Мельниченко, Никита Е. Мочкин, Юлия Н. Дубинина, Елена Г. Смирнова, Дина С. Колесникова, Анна Е. Банникова" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(284) "Диана Д. Иванова, Владислав О. Саржевский, Владимир Я. Мельниченко, Никита Е. Мочкин, Юлия Н. Дубинина, Елена Г. Смирнова, Дина С. Колесникова, Анна Е. Банникова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20476" ["VALUE"]=> array(2) { ["TEXT"]=> string(165) "ФГБУ «Национальный медико-хирургический центр им. Н. И. Пирогова» Минздрава России, Москва" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(165) "ФГБУ «Национальный медико-хирургический центр им. Н. И. Пирогова» Минздрава России, Москва" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20477" ["VALUE"]=> array(2) { ["TEXT"]=> string(12215) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Проведение высокодозной химиотерапии (ВДХТ) с аутологичной трансплантацией периферических гемопоэтических стволовых клеток (ауто-ТГСК) осложняется развитием гематологической токсичности IV степени. Среди осложнений при проведении данного лечения наиболее частым являются инфекционные. Длительность нейтропении IV степени коррелирует с развитием тяжелых инфекционных осложнений, которые могут стать причиной летального исхода в раннем посттрансплантационном периоде. Применение колониестимулирующих факторов (КСФ) снижает длительность нейтропении и риск развития инфекционных осложнений, а также сокращает пребывание пациента в специализированном отделении стационара. Цель исследования оценить и сравнить эффективность и безопасность двух форм КСФ, филграстима и его пегилированной формы, для стимуляции лейкопоэза при проведении ВДХТ с последующей ауто-ТГСК у пациентов с лимфопролиферативными заболеваниями, а также определить наиболее предпочтительную с точки зрения фармакоэкономического анализа форму КСФ. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В исследование включено 100 больных: 39 – c лимфомой Ходжкина, 18 – с неходжкинскими лимфомами, 42 – с множественной миеломой, 1 – острый промиелоцитарный лейкоз; 51 – женщина, 49 – мужчин. Медиана возраста составила 43 года (18-72) (табл. 1). Кондиционирование проводилось по схемам алкеран 200 мг/м. кв., алкеран 140 мг/м.кв., BeEAC, CBV, BEAM, цитарабин+мелфалан. Пациенты были рандомизированы на группы: 1 группа – пациенты, получающие пегилированную форму КСФ (ПЕГ-КСФ) (n=52), 2 группа – пациенты, получающие непегилированную форму КСФ (n=48). Стимуляцию лейкопоэза начинали на Д+4. Г-КСФ вводили ежедневно в дозе 5 мкг /кг/день до выхода из агранулоцитоза (WBC=3,0х10 в 9 ст./л ). ПЕГ-КСФ вводили однократно в дозе 6 мг (на Д+4). Фармакоэкономический анализ включал сопоставление относительной экономической оценки ПЕГ-КСФ и непегилированной формы КСФ. Учитывались затраты на ПЕГ-КСФ или КСФ, которые вводились соответствующему пациенту в период после выполнения ауто-ТГСК. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Сравнительный клинический анализ использования КСФ и ПЕГ-КСФ проводился по следующим параметрам: возраст, число линий предтрансплантационной химиотерапии, количество трансплантированных CD34+ млн/кг, показатели восстановления гемопоэза, наличие инфекционных осложнений (нейтропеническая лихорадка), длительность госпитализации (табл. 2). Значимые отличия были получены по скорости восстановления уровня лейкоцитов (у пациентов из группы ПЕГ-КСФ выход из агранулоцитоза регистрировался значимо раньше). Но в группе КСФ угнетение эритроидного ростка было значимо меньше. Достоверных отличий по другим анализируемым параметрам получено не было.<br> Фармакоэкономический анализ показал, что медиана суммы денежных средств, использованных для приобретения ПЕГ-КСФ, вводимых для лечения одного больного, составила 49042,73 руб., а для КСФ 36180,63 руб. (p<0,05) (табл. 3). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> При клиническом анализе применения пегилированной и непегилированной форм колониестимулирующих факторов существенных отличий не выявлено. Фармакоэкономический анализ выявил преимущество непегилированной формы КСФ над ПЕГ-КСФ. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, аутологичная, колониестимулирующий фактор, пегилированный, эффективность, фармакоэкономика. </p> <h2>Таблица 1. Общая клиническая характеристика больных</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Число больных в группе </td> <td> 100 </td> </tr> <tr> <td> Возраст, медиана (интервал), лет </td> <td> 43 (18-72) </td> </tr> <tr> <td> Мужчины, абс. (%) </td> <td> 49 (49) </td> </tr> <tr> <td> Женщины, абс. (%) </td> <td> 51 (51) </td> </tr> <tr> <td> Неходжкинские лимфомы, абс. (%) </td> <td> 18 (18) </td> </tr> <tr> <td> Лимфома Ходжкина, абс. (%) </td> <td> 39 (39) </td> </tr> <tr> <td> Множественная миелома, абс. (%) </td> <td> 42 (42) </td> </tr> <tr> <td> Острый промиелоцитарный лейкоз, абс. (%) 1 </td> <td> 1 (1) </td> </tr> </tbody> </table> <h2>Таблица 2. Сравнительный анализ ПЕГ-КСФ и КСФ</h2> <table> <tbody> <tr> <td> </td> <td> Группа КСФ </td> <td> Группа ПЕГ-КСФ </td> <td> t-знач. </td> <td> p </td> </tr> <tr> <td> Возраст, годы (медиана) </td> <td> 43 </td> <td> 41,5 </td> <td> 0,12 </td> <td> 0,9 </td> </tr> <tr> <td> Количество трансплантированных CD34+ млн/кг, медиана </td> <td> 2,59 </td> <td> 2,65 </td> <td> 0,13 </td> <td> 0,86 </td> </tr> <tr> <td> Дни агранулоцитоза (медиана) </td> <td> 7 </td> <td> 8 </td> <td> -0,93 </td> <td> 0,35 </td> </tr> <tr> <td> День (после ТГСК) выхода из агранулоцитоза (медиана) </td> <td> 11 </td> <td> 10 </td> <td> 2,17 </td> <td> 0,03 </td> </tr> <tr> <td> День (после ТГСК) возникновения фебрильной нейтропении </td> <td> 4<br> </td> <td> 5 </td> <td> -1,18 </td> <td> 0,23 </td> </tr> <tr> <td> Пациенты с нейтропенической лихорадкой, абс. (%) </td> <td> 34 (34%) </td> <td> 40 (40%) </td> <td> 0,63 </td> <td> 0,52 </td> </tr> <tr> <td> Дни тромбоцитопении ниже 20х10^9/л (медиана) </td> <td> 4 </td> <td> 5 </td> <td> -1,42 </td> <td> 0,15 </td> </tr> <tr> <td> Уровень максимального снижения гемоглобина </td> <td> 95 </td> <td> 86 </td> <td> 3,34 </td> <td> 0,001 </td> </tr> <tr> <td> Число линий предтрансплантационной химиотерапии </td> <td> 2 </td> <td> 2 </td> <td> -1,3 </td> <td> 0,19 </td> </tr> <tr> <td> Длительность госпитализации </td> <td> 22 </td> <td> 22 </td> <td> -0,46 </td> <td> 0,64 </td> </tr> </tbody> </table> <h2>Таблица 3. Результаты анализа затрат на профилактику и лечение фебрильной нейтропении на 1 человека после ауто-ТГСК</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> ПЕГ-КСФ для лечения 1 пациента, руб. </td> <td> КСФ для лечения 1 пациента, руб. </td> <td> р </td> </tr> <tr> <td> 49042,73 </td> <td> 36180,63 </td> <td> <0,05 </td> </tr> </tbody> </table> <br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(10613) "Введение
Проведение высокодозной химиотерапии (ВДХТ) с аутологичной трансплантацией периферических гемопоэтических стволовых клеток (ауто-ТГСК) осложняется развитием гематологической токсичности IV степени. Среди осложнений при проведении данного лечения наиболее частым являются инфекционные. Длительность нейтропении IV степени коррелирует с развитием тяжелых инфекционных осложнений, которые могут стать причиной летального исхода в раннем посттрансплантационном периоде. Применение колониестимулирующих факторов (КСФ) снижает длительность нейтропении и риск развития инфекционных осложнений, а также сокращает пребывание пациента в специализированном отделении стационара. Цель исследования оценить и сравнить эффективность и безопасность двух форм КСФ, филграстима и его пегилированной формы, для стимуляции лейкопоэза при проведении ВДХТ с последующей ауто-ТГСК у пациентов с лимфопролиферативными заболеваниями, а также определить наиболее предпочтительную с точки зрения фармакоэкономического анализа форму КСФ.
Материалы и методы
В исследование включено 100 больных: 39 – c лимфомой Ходжкина, 18 – с неходжкинскими лимфомами, 42 – с множественной миеломой, 1 – острый промиелоцитарный лейкоз; 51 – женщина, 49 – мужчин. Медиана возраста составила 43 года (18-72) (табл. 1). Кондиционирование проводилось по схемам алкеран 200 мг/м. кв., алкеран 140 мг/м.кв., BeEAC, CBV, BEAM, цитарабин+мелфалан. Пациенты были рандомизированы на группы: 1 группа – пациенты, получающие пегилированную форму КСФ (ПЕГ-КСФ) (n=52), 2 группа – пациенты, получающие непегилированную форму КСФ (n=48). Стимуляцию лейкопоэза начинали на Д+4. Г-КСФ вводили ежедневно в дозе 5 мкг /кг/день до выхода из агранулоцитоза (WBC=3,0х10 в 9 ст./л ). ПЕГ-КСФ вводили однократно в дозе 6 мг (на Д+4). Фармакоэкономический анализ включал сопоставление относительной экономической оценки ПЕГ-КСФ и непегилированной формы КСФ. Учитывались затраты на ПЕГ-КСФ или КСФ, которые вводились соответствующему пациенту в период после выполнения ауто-ТГСК.
Результаты
Сравнительный клинический анализ использования КСФ и ПЕГ-КСФ проводился по следующим параметрам: возраст, число линий предтрансплантационной химиотерапии, количество трансплантированных CD34+ млн/кг, показатели восстановления гемопоэза, наличие инфекционных осложнений (нейтропеническая лихорадка), длительность госпитализации (табл. 2). Значимые отличия были получены по скорости восстановления уровня лейкоцитов (у пациентов из группы ПЕГ-КСФ выход из агранулоцитоза регистрировался значимо раньше). Но в группе КСФ угнетение эритроидного ростка было значимо меньше. Достоверных отличий по другим анализируемым параметрам получено не было.
Фармакоэкономический анализ показал, что медиана суммы денежных средств, использованных для приобретения ПЕГ-КСФ, вводимых для лечения одного больного, составила 49042,73 руб., а для КСФ 36180,63 руб. (p<0,05) (табл. 3).
Выводы
При клиническом анализе применения пегилированной и непегилированной форм колониестимулирующих факторов существенных отличий не выявлено. Фармакоэкономический анализ выявил преимущество непегилированной формы КСФ над ПЕГ-КСФ.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, аутологичная, колониестимулирующий фактор, пегилированный, эффективность, фармакоэкономика.
Таблица 1. Общая клиническая характеристика больных
| Число больных в группе | 100 |
| Возраст, медиана (интервал), лет | 43 (18-72) |
| Мужчины, абс. (%) | 49 (49) |
| Женщины, абс. (%) | 51 (51) |
| Неходжкинские лимфомы, абс. (%) | 18 (18) |
| Лимфома Ходжкина, абс. (%) | 39 (39) |
| Множественная миелома, абс. (%) | 42 (42) |
| Острый промиелоцитарный лейкоз, абс. (%) 1 | 1 (1) |
Таблица 2. Сравнительный анализ ПЕГ-КСФ и КСФ
| Группа КСФ | Группа ПЕГ-КСФ | t-знач. | p | |
| Возраст, годы (медиана) | 43 | 41,5 | 0,12 | 0,9 |
| Количество трансплантированных CD34+ млн/кг, медиана | 2,59 | 2,65 | 0,13 | 0,86 |
| Дни агранулоцитоза (медиана) | 7 | 8 | -0,93 | 0,35 |
| День (после ТГСК) выхода из агранулоцитоза (медиана) | 11 | 10 | 2,17 | 0,03 |
| День (после ТГСК) возникновения фебрильной нейтропении |
4 |
5 | -1,18 | 0,23 |
| Пациенты с нейтропенической лихорадкой, абс. (%) | 34 (34%) | 40 (40%) | 0,63 | 0,52 |
| Дни тромбоцитопении ниже 20х10^9/л (медиана) | 4 | 5 | -1,42 | 0,15 |
| Уровень максимального снижения гемоглобина | 95 | 86 | 3,34 | 0,001 |
| Число линий предтрансплантационной химиотерапии | 2 | 2 | -1,3 | 0,19 |
| Длительность госпитализации | 22 | 22 | -0,46 | 0,64 |
Таблица 3. Результаты анализа затрат на профилактику и лечение фебрильной нейтропении на 1 человека после ауто-ТГСК
| ПЕГ-КСФ для лечения 1 пациента, руб. | КСФ для лечения 1 пациента, руб. | р |
| 49042,73 | 36180,63 | <0,05 |
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20478" ["VALUE"]=> array(2) { ["TEXT"]=> string(163) "Diana D. Ivanova, Vladislav O. Sarzhevsky, Vladimir Y. Melnichenko, Nikita E. Mochkin, Yulia N. Dubinina, Elena G. Smirnova, Dina S. Kolesnikova, Anna E. Bannikova" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(163) "Diana D. Ivanova, Vladislav O. Sarzhevsky, Vladimir Y. Melnichenko, Nikita E. Mochkin, Yulia N. Dubinina, Elena G. Smirnova, Dina S. Kolesnikova, Anna E. Bannikova" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20479" ["VALUE"]=> array(2) { ["TEXT"]=> string(82) "National N. I. Pirogov Medical Surgical Center, Russian Ministry of Health, Moscow" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(82) "National N. I. Pirogov Medical Surgical Center, Russian Ministry of Health, Moscow" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20480" ["VALUE"]=> array(2) { ["TEXT"]=> string(8690) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> High-dose chemotherapy (HDCT) with autologous transplantation of peripheral hematopoietic stem cells (auto-HSCT) is complicated by development of the grade IV hematologic toxicity. Among complications in this treatment, the most frequent are infectious conditions. The duration of grade IV neutropenia correlates with the development of severe infectious complications, which can cause death in the early posttransplant period. The use of colony-stimulating factors (CSF) reduces the duration of neutropenia as well as of developing infectious complications. The aim of the study is to evaluate and compare the efficacy, safety and pharmacoeconomic parameters of two forms of CSF, filgrastim and its pegylated form for stimulation leukopoiesis after auto-HSCT in the patients with lymphoproliferative diseases. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> The study included 100 patients: 39 with Hodgkin’s lymphoma, 18 with non-Hodgkin’s lymphomas, 42 with multiple myeloma, 1 acute promyelocytic leukemia; 51 women, 49 men. The median age was 43 years (18-72) (Table 1). The conditioning regimens were Melphalan 200 mg/m2, Melphalan 140 mg/m2, BeEAC, CBV, BEAM, Cytarabine + Melphalan. The patients were randomized into 2 groups: 1 group – patients who received pegylated form of CSF (PEG-CSF) (n=52), 2 group – patients with non- pegylated form of CSF (n=48). Stimulation of leukopoiesis was initiated on D+4. G-CSF was administered daily at dose of 5 μg/ kg/day until the release of agranulocytosis (WBC = 3.0x10 at 9 cells/L). PEG-CSF was administered once in dose of 6 mg (D+4). The pharmacoeconomic analysis included a comparison of economic evaluation of PEG-CSF treatment versus non-pegylated CSF therapy. Costs for PEG-CSF or CSF administered to the appropriate patient in the posttransplant period were taken into account. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Comparative clinical analysis of the use of CSF and PEGCSF was performed using the following parameters: age, number of pre-transplantation chemotherapy lines, number of transplanted CD34 + (mio cells/kg), hemopoiesis recovery, presence of infectious complications (neutropenic fever), duration of hospitalization (Table 2). </p> <p style="text-align: justify;"> Significant differences were obtained by the rate of recovery of leukocyte count (in 1st group, the yield from agranulocytosis was registered significantly earlier). But in the 2nd group, the inhibition of the erythroid line was significantly less. There were no significant differences in other analyzed parameters. Pharmacoeconomic analysis showed that the median amount of money used to purchase PEG-CSF, administered for the treatment of one patient, was 49,042.73 rubles, and for the CSF was 36180.63 rubles. (p <0, 05) (Table 3) . </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> There were no significant differences in the clinical analysis of the use of pegylated and non- pegylated forms of colony-stimulating factors. Pharmacoeconomic analysis revealed the advantage of non-pegylated form of CSF over PEG-CSF. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cell transplantation, autologous, colony stimulating factor, pegylated form, efficiency, pharmacoeconomics. </p> <h2 style="text-align: justify;">Table 1. General clinical characteristics of patients</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Number of patients in group </td> <td> 100 </td> </tr> <tr> <td> Age, median (interval), years </td> <td> 43 (18-72) </td> </tr> <tr> <td> Men, abs. (%) </td> <td> 49 (49) </td> </tr> <tr> <td> Women, abs. (%) </td> <td> 51 (51) </td> </tr> <tr> <td> Non-Hodgkin's lymphomas, abs. (%) </td> <td> 18 (18) </td> </tr> <tr> <td> Hodgkin Lymphoma, abs. (%) </td> <td> 39 (39) </td> </tr> <tr> <td> Multiple myeloma, abs. (%) </td> <td> 42 (42) </td> </tr> <tr> <td> Acute promyelocytic leukemia, abs. (%) </td> <td> 1 (1) </td> </tr> </tbody> </table> <h2>Table 2. Comparative analysis of PEG-CSF and CSF</h2> <table> <tbody> <tr> <td> </td> <td> Group CSF </td> <td> Group PEG-CSF </td> <td> t-value. </td> <td> p </td> </tr> <tr> <td> Age, years (median) </td> <td> 43 </td> <td> 41,5 </td> <td> 0,12 </td> <td> 0.9 </td> </tr> <tr> <td> The number of transplanted CD34 + million/kg, median </td> <td> 2.59 </td> <td> 2.65 </td> <td> 0.13 </td> <td> 0.86 </td> </tr> <tr> <td> Days of agranulocytosis (median) </td> <td> 7 </td> <td> 8 </td> <td> -0.93 </td> <td> 0.35 </td> </tr> <tr> <td> Day (after TSCC) of the marrow recovery agranulocytosis (median) </td> <td> 11 </td> <td> 10 </td> <td> 2.17 </td> <td> 0.03 </td> </tr> <tr> <td> Day (after TSCC) of febrile neutropenia </td> <td> 4 </td> <td> 5 </td> <td> -1.18 </td> <td> 0.23 </td> </tr> <tr> <td> Patients with neutropenic fever, abs. (%) </td> <td> 34 (34%) </td> <td> 40 (40%) </td> <td> 0.63 </td> <td> 0.52 </td> </tr> <tr> <td> Days of thrombocytopenia below 20х10^9/L (median) </td> <td> 4 </td> <td> 5 </td> <td> -1.42 </td> <td> 0.15 </td> </tr> <tr> <td> Level of maximum decrease in hemoglobin </td> <td> 95 </td> <td> 86 </td> <td> 3.34 </td> <td> 0.001 </td> </tr> <tr> <td> Number of pre-transplantation chemotherapy lines </td> <td> 2 </td> <td> 2 </td> <td> -1.3 </td> <td> 0.19 </td> </tr> <tr> <td> Duration of hospitalization </td> <td> 22 </td> <td> 22 </td> <td> -0.46 </td> <td> 0.64 </td> </tr> </tbody> </table> <h2>Table 3. Results of the cost analysis for the prevention and treatment of febrile neutropenia per 1 person after autograft</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> PEG-CSF<br> for treatment of 1 patient, Rub. </td> <td> CSF<br> for treatment of 1 patient, Rub. </td> <td> р </td> </tr> <tr> <td> 49042.73 </td> <td> 36180.63 </td> <td> <0.05 </td> </tr> </tbody> </table> <br> <h2></h2>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7044) "
Introduction
High-dose chemotherapy (HDCT) with autologous transplantation of peripheral hematopoietic stem cells (auto-HSCT) is complicated by development of the grade IV hematologic toxicity. Among complications in this treatment, the most frequent are infectious conditions. The duration of grade IV neutropenia correlates with the development of severe infectious complications, which can cause death in the early posttransplant period. The use of colony-stimulating factors (CSF) reduces the duration of neutropenia as well as of developing infectious complications. The aim of the study is to evaluate and compare the efficacy, safety and pharmacoeconomic parameters of two forms of CSF, filgrastim and its pegylated form for stimulation leukopoiesis after auto-HSCT in the patients with lymphoproliferative diseases.
Materials and methods
The study included 100 patients: 39 with Hodgkin’s lymphoma, 18 with non-Hodgkin’s lymphomas, 42 with multiple myeloma, 1 acute promyelocytic leukemia; 51 women, 49 men. The median age was 43 years (18-72) (Table 1). The conditioning regimens were Melphalan 200 mg/m2, Melphalan 140 mg/m2, BeEAC, CBV, BEAM, Cytarabine + Melphalan. The patients were randomized into 2 groups: 1 group – patients who received pegylated form of CSF (PEG-CSF) (n=52), 2 group – patients with non- pegylated form of CSF (n=48). Stimulation of leukopoiesis was initiated on D+4. G-CSF was administered daily at dose of 5 μg/ kg/day until the release of agranulocytosis (WBC = 3.0x10 at 9 cells/L). PEG-CSF was administered once in dose of 6 mg (D+4). The pharmacoeconomic analysis included a comparison of economic evaluation of PEG-CSF treatment versus non-pegylated CSF therapy. Costs for PEG-CSF or CSF administered to the appropriate patient in the posttransplant period were taken into account.
Results
Comparative clinical analysis of the use of CSF and PEGCSF was performed using the following parameters: age, number of pre-transplantation chemotherapy lines, number of transplanted CD34 + (mio cells/kg), hemopoiesis recovery, presence of infectious complications (neutropenic fever), duration of hospitalization (Table 2).
Significant differences were obtained by the rate of recovery of leukocyte count (in 1st group, the yield from agranulocytosis was registered significantly earlier). But in the 2nd group, the inhibition of the erythroid line was significantly less. There were no significant differences in other analyzed parameters. Pharmacoeconomic analysis showed that the median amount of money used to purchase PEG-CSF, administered for the treatment of one patient, was 49,042.73 rubles, and for the CSF was 36180.63 rubles. (p <0, 05) (Table 3) .
Conclusion
There were no significant differences in the clinical analysis of the use of pegylated and non- pegylated forms of colony-stimulating factors. Pharmacoeconomic analysis revealed the advantage of non-pegylated form of CSF over PEG-CSF.
Keywords
Hematopoietic stem cell transplantation, autologous, colony stimulating factor, pegylated form, efficiency, pharmacoeconomics.
Table 1. General clinical characteristics of patients
| Number of patients in group | 100 |
| Age, median (interval), years | 43 (18-72) |
| Men, abs. (%) | 49 (49) |
| Women, abs. (%) | 51 (51) |
| Non-Hodgkin's lymphomas, abs. (%) | 18 (18) |
| Hodgkin Lymphoma, abs. (%) | 39 (39) |
| Multiple myeloma, abs. (%) | 42 (42) |
| Acute promyelocytic leukemia, abs. (%) | 1 (1) |
Table 2. Comparative analysis of PEG-CSF and CSF
| Group CSF | Group PEG-CSF | t-value. | p | |
| Age, years (median) | 43 | 41,5 | 0,12 | 0.9 |
| The number of transplanted CD34 + million/kg, median | 2.59 | 2.65 | 0.13 | 0.86 |
| Days of agranulocytosis (median) | 7 | 8 | -0.93 | 0.35 |
| Day (after TSCC) of the marrow recovery agranulocytosis (median) | 11 | 10 | 2.17 | 0.03 |
| Day (after TSCC) of febrile neutropenia | 4 | 5 | -1.18 | 0.23 |
| Patients with neutropenic fever, abs. (%) | 34 (34%) | 40 (40%) | 0.63 | 0.52 |
| Days of thrombocytopenia below 20х10^9/L (median) | 4 | 5 | -1.42 | 0.15 |
| Level of maximum decrease in hemoglobin | 95 | 86 | 3.34 | 0.001 |
| Number of pre-transplantation chemotherapy lines | 2 | 2 | -1.3 | 0.19 |
| Duration of hospitalization | 22 | 22 | -0.46 | 0.64 |
Table 3. Results of the cost analysis for the prevention and treatment of febrile neutropenia per 1 person after autograft
|
PEG-CSF for treatment of 1 patient, Rub. |
CSF for treatment of 1 patient, Rub. |
р |
| 49042.73 | 36180.63 | <0.05 |
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20481" ["VALUE"]=> string(211) "Clinical and pharmacoeconomic analysis of pegylated and nonpegylated forms of colony-stimulating factors after autologous transplantation of hematopoietic stem cells in patients with lymphoproliferative diseases" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(211) "Clinical and pharmacoeconomic analysis of pegylated and nonpegylated forms of colony-stimulating factors after autologous transplantation of hematopoietic stem cells in patients with lymphoproliferative diseases" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20773" ["VALUE"]=> string(4) "1411" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1411" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20774" ["VALUE"]=> string(4) "1412" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1412" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20478" ["VALUE"]=> array(2) { ["TEXT"]=> string(163) "Diana D. Ivanova, Vladislav O. Sarzhevsky, Vladimir Y. Melnichenko, Nikita E. Mochkin, Yulia N. Dubinina, Elena G. Smirnova, Dina S. Kolesnikova, Anna E. Bannikova" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(163) "Diana D. Ivanova, Vladislav O. Sarzhevsky, Vladimir Y. Melnichenko, Nikita E. Mochkin, Yulia N. Dubinina, Elena G. Smirnova, Dina S. Kolesnikova, Anna E. Bannikova" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(163) "Diana D. Ivanova, Vladislav O. Sarzhevsky, Vladimir Y. Melnichenko, Nikita E. Mochkin, Yulia N. Dubinina, Elena G. Smirnova, Dina S. Kolesnikova, Anna E. Bannikova" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20480" ["VALUE"]=> array(2) { ["TEXT"]=> string(8690) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> High-dose chemotherapy (HDCT) with autologous transplantation of peripheral hematopoietic stem cells (auto-HSCT) is complicated by development of the grade IV hematologic toxicity. Among complications in this treatment, the most frequent are infectious conditions. The duration of grade IV neutropenia correlates with the development of severe infectious complications, which can cause death in the early posttransplant period. The use of colony-stimulating factors (CSF) reduces the duration of neutropenia as well as of developing infectious complications. The aim of the study is to evaluate and compare the efficacy, safety and pharmacoeconomic parameters of two forms of CSF, filgrastim and its pegylated form for stimulation leukopoiesis after auto-HSCT in the patients with lymphoproliferative diseases. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> The study included 100 patients: 39 with Hodgkin’s lymphoma, 18 with non-Hodgkin’s lymphomas, 42 with multiple myeloma, 1 acute promyelocytic leukemia; 51 women, 49 men. The median age was 43 years (18-72) (Table 1). The conditioning regimens were Melphalan 200 mg/m2, Melphalan 140 mg/m2, BeEAC, CBV, BEAM, Cytarabine + Melphalan. The patients were randomized into 2 groups: 1 group – patients who received pegylated form of CSF (PEG-CSF) (n=52), 2 group – patients with non- pegylated form of CSF (n=48). Stimulation of leukopoiesis was initiated on D+4. G-CSF was administered daily at dose of 5 μg/ kg/day until the release of agranulocytosis (WBC = 3.0x10 at 9 cells/L). PEG-CSF was administered once in dose of 6 mg (D+4). The pharmacoeconomic analysis included a comparison of economic evaluation of PEG-CSF treatment versus non-pegylated CSF therapy. Costs for PEG-CSF or CSF administered to the appropriate patient in the posttransplant period were taken into account. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Comparative clinical analysis of the use of CSF and PEGCSF was performed using the following parameters: age, number of pre-transplantation chemotherapy lines, number of transplanted CD34 + (mio cells/kg), hemopoiesis recovery, presence of infectious complications (neutropenic fever), duration of hospitalization (Table 2). </p> <p style="text-align: justify;"> Significant differences were obtained by the rate of recovery of leukocyte count (in 1st group, the yield from agranulocytosis was registered significantly earlier). But in the 2nd group, the inhibition of the erythroid line was significantly less. There were no significant differences in other analyzed parameters. Pharmacoeconomic analysis showed that the median amount of money used to purchase PEG-CSF, administered for the treatment of one patient, was 49,042.73 rubles, and for the CSF was 36180.63 rubles. (p <0, 05) (Table 3) . </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> There were no significant differences in the clinical analysis of the use of pegylated and non- pegylated forms of colony-stimulating factors. Pharmacoeconomic analysis revealed the advantage of non-pegylated form of CSF over PEG-CSF. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cell transplantation, autologous, colony stimulating factor, pegylated form, efficiency, pharmacoeconomics. </p> <h2 style="text-align: justify;">Table 1. General clinical characteristics of patients</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Number of patients in group </td> <td> 100 </td> </tr> <tr> <td> Age, median (interval), years </td> <td> 43 (18-72) </td> </tr> <tr> <td> Men, abs. (%) </td> <td> 49 (49) </td> </tr> <tr> <td> Women, abs. (%) </td> <td> 51 (51) </td> </tr> <tr> <td> Non-Hodgkin's lymphomas, abs. (%) </td> <td> 18 (18) </td> </tr> <tr> <td> Hodgkin Lymphoma, abs. (%) </td> <td> 39 (39) </td> </tr> <tr> <td> Multiple myeloma, abs. (%) </td> <td> 42 (42) </td> </tr> <tr> <td> Acute promyelocytic leukemia, abs. (%) </td> <td> 1 (1) </td> </tr> </tbody> </table> <h2>Table 2. Comparative analysis of PEG-CSF and CSF</h2> <table> <tbody> <tr> <td> </td> <td> Group CSF </td> <td> Group PEG-CSF </td> <td> t-value. </td> <td> p </td> </tr> <tr> <td> Age, years (median) </td> <td> 43 </td> <td> 41,5 </td> <td> 0,12 </td> <td> 0.9 </td> </tr> <tr> <td> The number of transplanted CD34 + million/kg, median </td> <td> 2.59 </td> <td> 2.65 </td> <td> 0.13 </td> <td> 0.86 </td> </tr> <tr> <td> Days of agranulocytosis (median) </td> <td> 7 </td> <td> 8 </td> <td> -0.93 </td> <td> 0.35 </td> </tr> <tr> <td> Day (after TSCC) of the marrow recovery agranulocytosis (median) </td> <td> 11 </td> <td> 10 </td> <td> 2.17 </td> <td> 0.03 </td> </tr> <tr> <td> Day (after TSCC) of febrile neutropenia </td> <td> 4 </td> <td> 5 </td> <td> -1.18 </td> <td> 0.23 </td> </tr> <tr> <td> Patients with neutropenic fever, abs. (%) </td> <td> 34 (34%) </td> <td> 40 (40%) </td> <td> 0.63 </td> <td> 0.52 </td> </tr> <tr> <td> Days of thrombocytopenia below 20х10^9/L (median) </td> <td> 4 </td> <td> 5 </td> <td> -1.42 </td> <td> 0.15 </td> </tr> <tr> <td> Level of maximum decrease in hemoglobin </td> <td> 95 </td> <td> 86 </td> <td> 3.34 </td> <td> 0.001 </td> </tr> <tr> <td> Number of pre-transplantation chemotherapy lines </td> <td> 2 </td> <td> 2 </td> <td> -1.3 </td> <td> 0.19 </td> </tr> <tr> <td> Duration of hospitalization </td> <td> 22 </td> <td> 22 </td> <td> -0.46 </td> <td> 0.64 </td> </tr> </tbody> </table> <h2>Table 3. Results of the cost analysis for the prevention and treatment of febrile neutropenia per 1 person after autograft</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> PEG-CSF<br> for treatment of 1 patient, Rub. </td> <td> CSF<br> for treatment of 1 patient, Rub. </td> <td> р </td> </tr> <tr> <td> 49042.73 </td> <td> 36180.63 </td> <td> <0.05 </td> </tr> </tbody> </table> <br> <h2></h2>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7044) "
Introduction
High-dose chemotherapy (HDCT) with autologous transplantation of peripheral hematopoietic stem cells (auto-HSCT) is complicated by development of the grade IV hematologic toxicity. Among complications in this treatment, the most frequent are infectious conditions. The duration of grade IV neutropenia correlates with the development of severe infectious complications, which can cause death in the early posttransplant period. The use of colony-stimulating factors (CSF) reduces the duration of neutropenia as well as of developing infectious complications. The aim of the study is to evaluate and compare the efficacy, safety and pharmacoeconomic parameters of two forms of CSF, filgrastim and its pegylated form for stimulation leukopoiesis after auto-HSCT in the patients with lymphoproliferative diseases.
Materials and methods
The study included 100 patients: 39 with Hodgkin’s lymphoma, 18 with non-Hodgkin’s lymphomas, 42 with multiple myeloma, 1 acute promyelocytic leukemia; 51 women, 49 men. The median age was 43 years (18-72) (Table 1). The conditioning regimens were Melphalan 200 mg/m2, Melphalan 140 mg/m2, BeEAC, CBV, BEAM, Cytarabine + Melphalan. The patients were randomized into 2 groups: 1 group – patients who received pegylated form of CSF (PEG-CSF) (n=52), 2 group – patients with non- pegylated form of CSF (n=48). Stimulation of leukopoiesis was initiated on D+4. G-CSF was administered daily at dose of 5 μg/ kg/day until the release of agranulocytosis (WBC = 3.0x10 at 9 cells/L). PEG-CSF was administered once in dose of 6 mg (D+4). The pharmacoeconomic analysis included a comparison of economic evaluation of PEG-CSF treatment versus non-pegylated CSF therapy. Costs for PEG-CSF or CSF administered to the appropriate patient in the posttransplant period were taken into account.
Results
Comparative clinical analysis of the use of CSF and PEGCSF was performed using the following parameters: age, number of pre-transplantation chemotherapy lines, number of transplanted CD34 + (mio cells/kg), hemopoiesis recovery, presence of infectious complications (neutropenic fever), duration of hospitalization (Table 2).
Significant differences were obtained by the rate of recovery of leukocyte count (in 1st group, the yield from agranulocytosis was registered significantly earlier). But in the 2nd group, the inhibition of the erythroid line was significantly less. There were no significant differences in other analyzed parameters. Pharmacoeconomic analysis showed that the median amount of money used to purchase PEG-CSF, administered for the treatment of one patient, was 49,042.73 rubles, and for the CSF was 36180.63 rubles. (p <0, 05) (Table 3) .
Conclusion
There were no significant differences in the clinical analysis of the use of pegylated and non- pegylated forms of colony-stimulating factors. Pharmacoeconomic analysis revealed the advantage of non-pegylated form of CSF over PEG-CSF.
Keywords
Hematopoietic stem cell transplantation, autologous, colony stimulating factor, pegylated form, efficiency, pharmacoeconomics.
Table 1. General clinical characteristics of patients
| Number of patients in group | 100 |
| Age, median (interval), years | 43 (18-72) |
| Men, abs. (%) | 49 (49) |
| Women, abs. (%) | 51 (51) |
| Non-Hodgkin's lymphomas, abs. (%) | 18 (18) |
| Hodgkin Lymphoma, abs. (%) | 39 (39) |
| Multiple myeloma, abs. (%) | 42 (42) |
| Acute promyelocytic leukemia, abs. (%) | 1 (1) |
Table 2. Comparative analysis of PEG-CSF and CSF
| Group CSF | Group PEG-CSF | t-value. | p | |
| Age, years (median) | 43 | 41,5 | 0,12 | 0.9 |
| The number of transplanted CD34 + million/kg, median | 2.59 | 2.65 | 0.13 | 0.86 |
| Days of agranulocytosis (median) | 7 | 8 | -0.93 | 0.35 |
| Day (after TSCC) of the marrow recovery agranulocytosis (median) | 11 | 10 | 2.17 | 0.03 |
| Day (after TSCC) of febrile neutropenia | 4 | 5 | -1.18 | 0.23 |
| Patients with neutropenic fever, abs. (%) | 34 (34%) | 40 (40%) | 0.63 | 0.52 |
| Days of thrombocytopenia below 20х10^9/L (median) | 4 | 5 | -1.42 | 0.15 |
| Level of maximum decrease in hemoglobin | 95 | 86 | 3.34 | 0.001 |
| Number of pre-transplantation chemotherapy lines | 2 | 2 | -1.3 | 0.19 |
| Duration of hospitalization | 22 | 22 | -0.46 | 0.64 |
Table 3. Results of the cost analysis for the prevention and treatment of febrile neutropenia per 1 person after autograft
|
PEG-CSF for treatment of 1 patient, Rub. |
CSF for treatment of 1 patient, Rub. |
р |
| 49042.73 | 36180.63 | <0.05 |
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(7044) "
Introduction
High-dose chemotherapy (HDCT) with autologous transplantation of peripheral hematopoietic stem cells (auto-HSCT) is complicated by development of the grade IV hematologic toxicity. Among complications in this treatment, the most frequent are infectious conditions. The duration of grade IV neutropenia correlates with the development of severe infectious complications, which can cause death in the early posttransplant period. The use of colony-stimulating factors (CSF) reduces the duration of neutropenia as well as of developing infectious complications. The aim of the study is to evaluate and compare the efficacy, safety and pharmacoeconomic parameters of two forms of CSF, filgrastim and its pegylated form for stimulation leukopoiesis after auto-HSCT in the patients with lymphoproliferative diseases.
Materials and methods
The study included 100 patients: 39 with Hodgkin’s lymphoma, 18 with non-Hodgkin’s lymphomas, 42 with multiple myeloma, 1 acute promyelocytic leukemia; 51 women, 49 men. The median age was 43 years (18-72) (Table 1). The conditioning regimens were Melphalan 200 mg/m2, Melphalan 140 mg/m2, BeEAC, CBV, BEAM, Cytarabine + Melphalan. The patients were randomized into 2 groups: 1 group – patients who received pegylated form of CSF (PEG-CSF) (n=52), 2 group – patients with non- pegylated form of CSF (n=48). Stimulation of leukopoiesis was initiated on D+4. G-CSF was administered daily at dose of 5 μg/ kg/day until the release of agranulocytosis (WBC = 3.0x10 at 9 cells/L). PEG-CSF was administered once in dose of 6 mg (D+4). The pharmacoeconomic analysis included a comparison of economic evaluation of PEG-CSF treatment versus non-pegylated CSF therapy. Costs for PEG-CSF or CSF administered to the appropriate patient in the posttransplant period were taken into account.
Results
Comparative clinical analysis of the use of CSF and PEGCSF was performed using the following parameters: age, number of pre-transplantation chemotherapy lines, number of transplanted CD34 + (mio cells/kg), hemopoiesis recovery, presence of infectious complications (neutropenic fever), duration of hospitalization (Table 2).
Significant differences were obtained by the rate of recovery of leukocyte count (in 1st group, the yield from agranulocytosis was registered significantly earlier). But in the 2nd group, the inhibition of the erythroid line was significantly less. There were no significant differences in other analyzed parameters. Pharmacoeconomic analysis showed that the median amount of money used to purchase PEG-CSF, administered for the treatment of one patient, was 49,042.73 rubles, and for the CSF was 36180.63 rubles. (p <0, 05) (Table 3) .
Conclusion
There were no significant differences in the clinical analysis of the use of pegylated and non- pegylated forms of colony-stimulating factors. Pharmacoeconomic analysis revealed the advantage of non-pegylated form of CSF over PEG-CSF.
Keywords
Hematopoietic stem cell transplantation, autologous, colony stimulating factor, pegylated form, efficiency, pharmacoeconomics.
Table 1. General clinical characteristics of patients
| Number of patients in group | 100 |
| Age, median (interval), years | 43 (18-72) |
| Men, abs. (%) | 49 (49) |
| Women, abs. (%) | 51 (51) |
| Non-Hodgkin's lymphomas, abs. (%) | 18 (18) |
| Hodgkin Lymphoma, abs. (%) | 39 (39) |
| Multiple myeloma, abs. (%) | 42 (42) |
| Acute promyelocytic leukemia, abs. (%) | 1 (1) |
Table 2. Comparative analysis of PEG-CSF and CSF
| Group CSF | Group PEG-CSF | t-value. | p | |
| Age, years (median) | 43 | 41,5 | 0,12 | 0.9 |
| The number of transplanted CD34 + million/kg, median | 2.59 | 2.65 | 0.13 | 0.86 |
| Days of agranulocytosis (median) | 7 | 8 | -0.93 | 0.35 |
| Day (after TSCC) of the marrow recovery agranulocytosis (median) | 11 | 10 | 2.17 | 0.03 |
| Day (after TSCC) of febrile neutropenia | 4 | 5 | -1.18 | 0.23 |
| Patients with neutropenic fever, abs. (%) | 34 (34%) | 40 (40%) | 0.63 | 0.52 |
| Days of thrombocytopenia below 20х10^9/L (median) | 4 | 5 | -1.42 | 0.15 |
| Level of maximum decrease in hemoglobin | 95 | 86 | 3.34 | 0.001 |
| Number of pre-transplantation chemotherapy lines | 2 | 2 | -1.3 | 0.19 |
| Duration of hospitalization | 22 | 22 | -0.46 | 0.64 |
Table 3. Results of the cost analysis for the prevention and treatment of febrile neutropenia per 1 person after autograft
|
PEG-CSF for treatment of 1 patient, Rub. |
CSF for treatment of 1 patient, Rub. |
р |
| 49042.73 | 36180.63 | <0.05 |
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20481" ["VALUE"]=> string(211) "Clinical and pharmacoeconomic analysis of pegylated and nonpegylated forms of colony-stimulating factors after autologous transplantation of hematopoietic stem cells in patients with lymphoproliferative diseases" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(211) "Clinical and pharmacoeconomic analysis of pegylated and nonpegylated forms of colony-stimulating factors after autologous transplantation of hematopoietic stem cells in patients with lymphoproliferative diseases" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(211) "Clinical and pharmacoeconomic analysis of pegylated and nonpegylated forms of colony-stimulating factors after autologous transplantation of hematopoietic stem cells in patients with lymphoproliferative diseases" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20479" ["VALUE"]=> array(2) { ["TEXT"]=> string(82) "National N. I. Pirogov Medical Surgical Center, Russian Ministry of Health, Moscow" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(82) "National N. I. Pirogov Medical Surgical Center, Russian Ministry of Health, Moscow" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(82) "National N. I. Pirogov Medical Surgical Center, Russian Ministry of Health, Moscow" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20475" ["VALUE"]=> array(2) { ["TEXT"]=> string(284) "Диана Д. Иванова, Владислав О. Саржевский, Владимир Я. Мельниченко, Никита Е. Мочкин, Юлия Н. Дубинина, Елена Г. Смирнова, Дина С. Колесникова, Анна Е. Банникова" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(284) "Диана Д. Иванова, Владислав О. Саржевский, Владимир Я. Мельниченко, Никита Е. Мочкин, Юлия Н. Дубинина, Елена Г. Смирнова, Дина С. Колесникова, Анна Е. Банникова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(284) "Диана Д. Иванова, Владислав О. Саржевский, Владимир Я. Мельниченко, Никита Е. Мочкин, Юлия Н. Дубинина, Елена Г. Смирнова, Дина С. Колесникова, Анна Е. Банникова" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20477" ["VALUE"]=> array(2) { ["TEXT"]=> string(12215) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Проведение высокодозной химиотерапии (ВДХТ) с аутологичной трансплантацией периферических гемопоэтических стволовых клеток (ауто-ТГСК) осложняется развитием гематологической токсичности IV степени. Среди осложнений при проведении данного лечения наиболее частым являются инфекционные. Длительность нейтропении IV степени коррелирует с развитием тяжелых инфекционных осложнений, которые могут стать причиной летального исхода в раннем посттрансплантационном периоде. Применение колониестимулирующих факторов (КСФ) снижает длительность нейтропении и риск развития инфекционных осложнений, а также сокращает пребывание пациента в специализированном отделении стационара. Цель исследования оценить и сравнить эффективность и безопасность двух форм КСФ, филграстима и его пегилированной формы, для стимуляции лейкопоэза при проведении ВДХТ с последующей ауто-ТГСК у пациентов с лимфопролиферативными заболеваниями, а также определить наиболее предпочтительную с точки зрения фармакоэкономического анализа форму КСФ. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В исследование включено 100 больных: 39 – c лимфомой Ходжкина, 18 – с неходжкинскими лимфомами, 42 – с множественной миеломой, 1 – острый промиелоцитарный лейкоз; 51 – женщина, 49 – мужчин. Медиана возраста составила 43 года (18-72) (табл. 1). Кондиционирование проводилось по схемам алкеран 200 мг/м. кв., алкеран 140 мг/м.кв., BeEAC, CBV, BEAM, цитарабин+мелфалан. Пациенты были рандомизированы на группы: 1 группа – пациенты, получающие пегилированную форму КСФ (ПЕГ-КСФ) (n=52), 2 группа – пациенты, получающие непегилированную форму КСФ (n=48). Стимуляцию лейкопоэза начинали на Д+4. Г-КСФ вводили ежедневно в дозе 5 мкг /кг/день до выхода из агранулоцитоза (WBC=3,0х10 в 9 ст./л ). ПЕГ-КСФ вводили однократно в дозе 6 мг (на Д+4). Фармакоэкономический анализ включал сопоставление относительной экономической оценки ПЕГ-КСФ и непегилированной формы КСФ. Учитывались затраты на ПЕГ-КСФ или КСФ, которые вводились соответствующему пациенту в период после выполнения ауто-ТГСК. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Сравнительный клинический анализ использования КСФ и ПЕГ-КСФ проводился по следующим параметрам: возраст, число линий предтрансплантационной химиотерапии, количество трансплантированных CD34+ млн/кг, показатели восстановления гемопоэза, наличие инфекционных осложнений (нейтропеническая лихорадка), длительность госпитализации (табл. 2). Значимые отличия были получены по скорости восстановления уровня лейкоцитов (у пациентов из группы ПЕГ-КСФ выход из агранулоцитоза регистрировался значимо раньше). Но в группе КСФ угнетение эритроидного ростка было значимо меньше. Достоверных отличий по другим анализируемым параметрам получено не было.<br> Фармакоэкономический анализ показал, что медиана суммы денежных средств, использованных для приобретения ПЕГ-КСФ, вводимых для лечения одного больного, составила 49042,73 руб., а для КСФ 36180,63 руб. (p<0,05) (табл. 3). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> При клиническом анализе применения пегилированной и непегилированной форм колониестимулирующих факторов существенных отличий не выявлено. Фармакоэкономический анализ выявил преимущество непегилированной формы КСФ над ПЕГ-КСФ. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, аутологичная, колониестимулирующий фактор, пегилированный, эффективность, фармакоэкономика. </p> <h2>Таблица 1. Общая клиническая характеристика больных</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Число больных в группе </td> <td> 100 </td> </tr> <tr> <td> Возраст, медиана (интервал), лет </td> <td> 43 (18-72) </td> </tr> <tr> <td> Мужчины, абс. (%) </td> <td> 49 (49) </td> </tr> <tr> <td> Женщины, абс. (%) </td> <td> 51 (51) </td> </tr> <tr> <td> Неходжкинские лимфомы, абс. (%) </td> <td> 18 (18) </td> </tr> <tr> <td> Лимфома Ходжкина, абс. (%) </td> <td> 39 (39) </td> </tr> <tr> <td> Множественная миелома, абс. (%) </td> <td> 42 (42) </td> </tr> <tr> <td> Острый промиелоцитарный лейкоз, абс. (%) 1 </td> <td> 1 (1) </td> </tr> </tbody> </table> <h2>Таблица 2. Сравнительный анализ ПЕГ-КСФ и КСФ</h2> <table> <tbody> <tr> <td> </td> <td> Группа КСФ </td> <td> Группа ПЕГ-КСФ </td> <td> t-знач. </td> <td> p </td> </tr> <tr> <td> Возраст, годы (медиана) </td> <td> 43 </td> <td> 41,5 </td> <td> 0,12 </td> <td> 0,9 </td> </tr> <tr> <td> Количество трансплантированных CD34+ млн/кг, медиана </td> <td> 2,59 </td> <td> 2,65 </td> <td> 0,13 </td> <td> 0,86 </td> </tr> <tr> <td> Дни агранулоцитоза (медиана) </td> <td> 7 </td> <td> 8 </td> <td> -0,93 </td> <td> 0,35 </td> </tr> <tr> <td> День (после ТГСК) выхода из агранулоцитоза (медиана) </td> <td> 11 </td> <td> 10 </td> <td> 2,17 </td> <td> 0,03 </td> </tr> <tr> <td> День (после ТГСК) возникновения фебрильной нейтропении </td> <td> 4<br> </td> <td> 5 </td> <td> -1,18 </td> <td> 0,23 </td> </tr> <tr> <td> Пациенты с нейтропенической лихорадкой, абс. (%) </td> <td> 34 (34%) </td> <td> 40 (40%) </td> <td> 0,63 </td> <td> 0,52 </td> </tr> <tr> <td> Дни тромбоцитопении ниже 20х10^9/л (медиана) </td> <td> 4 </td> <td> 5 </td> <td> -1,42 </td> <td> 0,15 </td> </tr> <tr> <td> Уровень максимального снижения гемоглобина </td> <td> 95 </td> <td> 86 </td> <td> 3,34 </td> <td> 0,001 </td> </tr> <tr> <td> Число линий предтрансплантационной химиотерапии </td> <td> 2 </td> <td> 2 </td> <td> -1,3 </td> <td> 0,19 </td> </tr> <tr> <td> Длительность госпитализации </td> <td> 22 </td> <td> 22 </td> <td> -0,46 </td> <td> 0,64 </td> </tr> </tbody> </table> <h2>Таблица 3. Результаты анализа затрат на профилактику и лечение фебрильной нейтропении на 1 человека после ауто-ТГСК</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> ПЕГ-КСФ для лечения 1 пациента, руб. </td> <td> КСФ для лечения 1 пациента, руб. </td> <td> р </td> </tr> <tr> <td> 49042,73 </td> <td> 36180,63 </td> <td> <0,05 </td> </tr> </tbody> </table> <br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(10613) "
Введение
Проведение высокодозной химиотерапии (ВДХТ) с аутологичной трансплантацией периферических гемопоэтических стволовых клеток (ауто-ТГСК) осложняется развитием гематологической токсичности IV степени. Среди осложнений при проведении данного лечения наиболее частым являются инфекционные. Длительность нейтропении IV степени коррелирует с развитием тяжелых инфекционных осложнений, которые могут стать причиной летального исхода в раннем посттрансплантационном периоде. Применение колониестимулирующих факторов (КСФ) снижает длительность нейтропении и риск развития инфекционных осложнений, а также сокращает пребывание пациента в специализированном отделении стационара. Цель исследования оценить и сравнить эффективность и безопасность двух форм КСФ, филграстима и его пегилированной формы, для стимуляции лейкопоэза при проведении ВДХТ с последующей ауто-ТГСК у пациентов с лимфопролиферативными заболеваниями, а также определить наиболее предпочтительную с точки зрения фармакоэкономического анализа форму КСФ.
Материалы и методы
В исследование включено 100 больных: 39 – c лимфомой Ходжкина, 18 – с неходжкинскими лимфомами, 42 – с множественной миеломой, 1 – острый промиелоцитарный лейкоз; 51 – женщина, 49 – мужчин. Медиана возраста составила 43 года (18-72) (табл. 1). Кондиционирование проводилось по схемам алкеран 200 мг/м. кв., алкеран 140 мг/м.кв., BeEAC, CBV, BEAM, цитарабин+мелфалан. Пациенты были рандомизированы на группы: 1 группа – пациенты, получающие пегилированную форму КСФ (ПЕГ-КСФ) (n=52), 2 группа – пациенты, получающие непегилированную форму КСФ (n=48). Стимуляцию лейкопоэза начинали на Д+4. Г-КСФ вводили ежедневно в дозе 5 мкг /кг/день до выхода из агранулоцитоза (WBC=3,0х10 в 9 ст./л ). ПЕГ-КСФ вводили однократно в дозе 6 мг (на Д+4). Фармакоэкономический анализ включал сопоставление относительной экономической оценки ПЕГ-КСФ и непегилированной формы КСФ. Учитывались затраты на ПЕГ-КСФ или КСФ, которые вводились соответствующему пациенту в период после выполнения ауто-ТГСК.
Результаты
Сравнительный клинический анализ использования КСФ и ПЕГ-КСФ проводился по следующим параметрам: возраст, число линий предтрансплантационной химиотерапии, количество трансплантированных CD34+ млн/кг, показатели восстановления гемопоэза, наличие инфекционных осложнений (нейтропеническая лихорадка), длительность госпитализации (табл. 2). Значимые отличия были получены по скорости восстановления уровня лейкоцитов (у пациентов из группы ПЕГ-КСФ выход из агранулоцитоза регистрировался значимо раньше). Но в группе КСФ угнетение эритроидного ростка было значимо меньше. Достоверных отличий по другим анализируемым параметрам получено не было.
Фармакоэкономический анализ показал, что медиана суммы денежных средств, использованных для приобретения ПЕГ-КСФ, вводимых для лечения одного больного, составила 49042,73 руб., а для КСФ 36180,63 руб. (p<0,05) (табл. 3).
Выводы
При клиническом анализе применения пегилированной и непегилированной форм колониестимулирующих факторов существенных отличий не выявлено. Фармакоэкономический анализ выявил преимущество непегилированной формы КСФ над ПЕГ-КСФ.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, аутологичная, колониестимулирующий фактор, пегилированный, эффективность, фармакоэкономика.
Таблица 1. Общая клиническая характеристика больных
| Число больных в группе | 100 |
| Возраст, медиана (интервал), лет | 43 (18-72) |
| Мужчины, абс. (%) | 49 (49) |
| Женщины, абс. (%) | 51 (51) |
| Неходжкинские лимфомы, абс. (%) | 18 (18) |
| Лимфома Ходжкина, абс. (%) | 39 (39) |
| Множественная миелома, абс. (%) | 42 (42) |
| Острый промиелоцитарный лейкоз, абс. (%) 1 | 1 (1) |
Таблица 2. Сравнительный анализ ПЕГ-КСФ и КСФ
| Группа КСФ | Группа ПЕГ-КСФ | t-знач. | p | |
| Возраст, годы (медиана) | 43 | 41,5 | 0,12 | 0,9 |
| Количество трансплантированных CD34+ млн/кг, медиана | 2,59 | 2,65 | 0,13 | 0,86 |
| Дни агранулоцитоза (медиана) | 7 | 8 | -0,93 | 0,35 |
| День (после ТГСК) выхода из агранулоцитоза (медиана) | 11 | 10 | 2,17 | 0,03 |
| День (после ТГСК) возникновения фебрильной нейтропении |
4 |
5 | -1,18 | 0,23 |
| Пациенты с нейтропенической лихорадкой, абс. (%) | 34 (34%) | 40 (40%) | 0,63 | 0,52 |
| Дни тромбоцитопении ниже 20х10^9/л (медиана) | 4 | 5 | -1,42 | 0,15 |
| Уровень максимального снижения гемоглобина | 95 | 86 | 3,34 | 0,001 |
| Число линий предтрансплантационной химиотерапии | 2 | 2 | -1,3 | 0,19 |
| Длительность госпитализации | 22 | 22 | -0,46 | 0,64 |
Таблица 3. Результаты анализа затрат на профилактику и лечение фебрильной нейтропении на 1 человека после ауто-ТГСК
| ПЕГ-КСФ для лечения 1 пациента, руб. | КСФ для лечения 1 пациента, руб. | р |
| 49042,73 | 36180,63 | <0,05 |
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(10613) "
Введение
Проведение высокодозной химиотерапии (ВДХТ) с аутологичной трансплантацией периферических гемопоэтических стволовых клеток (ауто-ТГСК) осложняется развитием гематологической токсичности IV степени. Среди осложнений при проведении данного лечения наиболее частым являются инфекционные. Длительность нейтропении IV степени коррелирует с развитием тяжелых инфекционных осложнений, которые могут стать причиной летального исхода в раннем посттрансплантационном периоде. Применение колониестимулирующих факторов (КСФ) снижает длительность нейтропении и риск развития инфекционных осложнений, а также сокращает пребывание пациента в специализированном отделении стационара. Цель исследования оценить и сравнить эффективность и безопасность двух форм КСФ, филграстима и его пегилированной формы, для стимуляции лейкопоэза при проведении ВДХТ с последующей ауто-ТГСК у пациентов с лимфопролиферативными заболеваниями, а также определить наиболее предпочтительную с точки зрения фармакоэкономического анализа форму КСФ.
Материалы и методы
В исследование включено 100 больных: 39 – c лимфомой Ходжкина, 18 – с неходжкинскими лимфомами, 42 – с множественной миеломой, 1 – острый промиелоцитарный лейкоз; 51 – женщина, 49 – мужчин. Медиана возраста составила 43 года (18-72) (табл. 1). Кондиционирование проводилось по схемам алкеран 200 мг/м. кв., алкеран 140 мг/м.кв., BeEAC, CBV, BEAM, цитарабин+мелфалан. Пациенты были рандомизированы на группы: 1 группа – пациенты, получающие пегилированную форму КСФ (ПЕГ-КСФ) (n=52), 2 группа – пациенты, получающие непегилированную форму КСФ (n=48). Стимуляцию лейкопоэза начинали на Д+4. Г-КСФ вводили ежедневно в дозе 5 мкг /кг/день до выхода из агранулоцитоза (WBC=3,0х10 в 9 ст./л ). ПЕГ-КСФ вводили однократно в дозе 6 мг (на Д+4). Фармакоэкономический анализ включал сопоставление относительной экономической оценки ПЕГ-КСФ и непегилированной формы КСФ. Учитывались затраты на ПЕГ-КСФ или КСФ, которые вводились соответствующему пациенту в период после выполнения ауто-ТГСК.
Результаты
Сравнительный клинический анализ использования КСФ и ПЕГ-КСФ проводился по следующим параметрам: возраст, число линий предтрансплантационной химиотерапии, количество трансплантированных CD34+ млн/кг, показатели восстановления гемопоэза, наличие инфекционных осложнений (нейтропеническая лихорадка), длительность госпитализации (табл. 2). Значимые отличия были получены по скорости восстановления уровня лейкоцитов (у пациентов из группы ПЕГ-КСФ выход из агранулоцитоза регистрировался значимо раньше). Но в группе КСФ угнетение эритроидного ростка было значимо меньше. Достоверных отличий по другим анализируемым параметрам получено не было.
Фармакоэкономический анализ показал, что медиана суммы денежных средств, использованных для приобретения ПЕГ-КСФ, вводимых для лечения одного больного, составила 49042,73 руб., а для КСФ 36180,63 руб. (p<0,05) (табл. 3).
Выводы
При клиническом анализе применения пегилированной и непегилированной форм колониестимулирующих факторов существенных отличий не выявлено. Фармакоэкономический анализ выявил преимущество непегилированной формы КСФ над ПЕГ-КСФ.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, аутологичная, колониестимулирующий фактор, пегилированный, эффективность, фармакоэкономика.
Таблица 1. Общая клиническая характеристика больных
| Число больных в группе | 100 |
| Возраст, медиана (интервал), лет | 43 (18-72) |
| Мужчины, абс. (%) | 49 (49) |
| Женщины, абс. (%) | 51 (51) |
| Неходжкинские лимфомы, абс. (%) | 18 (18) |
| Лимфома Ходжкина, абс. (%) | 39 (39) |
| Множественная миелома, абс. (%) | 42 (42) |
| Острый промиелоцитарный лейкоз, абс. (%) 1 | 1 (1) |
Таблица 2. Сравнительный анализ ПЕГ-КСФ и КСФ
| Группа КСФ | Группа ПЕГ-КСФ | t-знач. | p | |
| Возраст, годы (медиана) | 43 | 41,5 | 0,12 | 0,9 |
| Количество трансплантированных CD34+ млн/кг, медиана | 2,59 | 2,65 | 0,13 | 0,86 |
| Дни агранулоцитоза (медиана) | 7 | 8 | -0,93 | 0,35 |
| День (после ТГСК) выхода из агранулоцитоза (медиана) | 11 | 10 | 2,17 | 0,03 |
| День (после ТГСК) возникновения фебрильной нейтропении |
4 |
5 | -1,18 | 0,23 |
| Пациенты с нейтропенической лихорадкой, абс. (%) | 34 (34%) | 40 (40%) | 0,63 | 0,52 |
| Дни тромбоцитопении ниже 20х10^9/л (медиана) | 4 | 5 | -1,42 | 0,15 |
| Уровень максимального снижения гемоглобина | 95 | 86 | 3,34 | 0,001 |
| Число линий предтрансплантационной химиотерапии | 2 | 2 | -1,3 | 0,19 |
| Длительность госпитализации | 22 | 22 | -0,46 | 0,64 |
Таблица 3. Результаты анализа затрат на профилактику и лечение фебрильной нейтропении на 1 человека после ауто-ТГСК
| ПЕГ-КСФ для лечения 1 пациента, руб. | КСФ для лечения 1 пациента, руб. | р |
| 49042,73 | 36180,63 | <0,05 |
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20476" ["VALUE"]=> array(2) { ["TEXT"]=> string(165) "ФГБУ «Национальный медико-хирургический центр им. Н. И. Пирогова» Минздрава России, Москва" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(165) "ФГБУ «Национальный медико-хирургический центр им. Н. И. Пирогова» Минздрава России, Москва" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(165) "ФГБУ «Национальный медико-хирургический центр им. Н. И. Пирогова» Минздрава России, Москва" } } } [12]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1563" ["~ID"]=> string(4) "1563" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(368) "Влияние внутривенных ЦМВ-неспецифичных иммуноглобулинов на эффективность лечения ганцикловиром у больных после трансплантации аллогенных гемопоэтических стволовых клеток в период реактивации ЦМВ" ["~NAME"]=> string(368) "Влияние внутривенных ЦМВ-неспецифичных иммуноглобулинов на эффективность лечения ганцикловиром у больных после трансплантации аллогенных гемопоэтических стволовых клеток в период реактивации ЦМВ" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:29:57" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:29:57" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vliyanie-vnutrivennykh-tsmv-nespetsifichnykh-immunoglobulinov-na-effektivnost-lecheniya-gantsiklovir/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vliyanie-vnutrivennykh-tsmv-nespetsifichnykh-immunoglobulinov-na-effektivnost-lecheniya-gantsiklovir/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "vliyanie-vnutrivennykh-tsmv-nespetsifichnykh-immunoglobulinov-na-effektivnost-lecheniya-gantsiklovir" ["~CODE"]=> string(100) "vliyanie-vnutrivennykh-tsmv-nespetsifichnykh-immunoglobulinov-na-effektivnost-lecheniya-gantsiklovir" ["EXTERNAL_ID"]=> string(4) "1563" ["~EXTERNAL_ID"]=> string(4) "1563" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(368) "Влияние внутривенных ЦМВ-неспецифичных иммуноглобулинов на эффективность лечения ганцикловиром у больных после трансплантации аллогенных гемопоэтических стволовых клеток в период реактивации ЦМВ" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(537) "Влияние внутривенных ЦМВ-неспецифичных иммуноглобулинов на эффективность лечения ганцикловиром у больных после трансплантации аллогенных гемопоэтических стволовых клеток в период реактивации ЦМВInfluence of non-CMV specific intravenous immunoglobulin on intravenous ganciclovir effectiveness in patients after allogeneic stem cell transplantation with CMV-disease" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(6261) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Реактивация цитомегаловирусной инфекции (ЦМВ) остается одной из основных проблем трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Использование ЦМВ-неспецифичных внутривенных иммуноглобулинов (ИГ) до сих пор вызывает споры и определяется, в большей степени, внутренними протоколами трансплантационного центра без четкой доказательной базы. Стандартом же лечения ЦМВ до сих пор остается ганцикловир в дозе 10 мг/кг/сут в течение 14 дней с дальнейшим переходом на профилактическую дозу. Здесь мы приводим данные о влиянии ИГ в период лечения пациентов после алло-ТГСК ганцикловиром в период реактивации ЦМВ-инфекции </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Тридцать два пациента с гемобластозами после алло-ТГСК были включены в исследование. Детальные характеристики представлены в Таблице 1. Все пациенты на момент включения в исследования были ЦМВ-позитивны (по данным ПЦР, «АмплиСенс EBV/CMV/ HHV6-c-крин-FL», Интерлабсервис, Россия), а также требовали начала терапии ганцикловиром в дозе 10 мг/кг/сут. Часть пациентов получили в/в ИГ. Медиана суммарной дозы за время лечения составила 20 г. (7,5-90 г.). Метод Каплан-Мейера был использован для оценки вероятности достижения ЦМВ-негативности (по данным ПЦР). Логранк тест был использован для сравнения различий между двумя группами. Для анализа таблиц 2x2 был использован точный тест Фишера. Р-значение ниже 0.05 считалось значимым. </p> <h2 style="text-align: justify;"> Таблица 1. Характеристики пациентов<br> </h2> <img width="743" alt="14_Таблица 1. Характеристики пациентов.png" src="/upload/medialibrary/77f/14_tablitsa-1.-kharakteristiki-patsientov.png" height="508" title="14_Таблица 1. Характеристики пациентов.png"><br> <img width="740" alt="14_Таблица 1. Характеристики пациентов_2.png" src="/upload/medialibrary/097/14_tablitsa-1.-kharakteristiki-patsientov_2.png" height="272" title="14_Таблица 1. Характеристики пациентов_2.png"><br> <img width="717" alt="14_Рисунок 1. Время до достижения.png" src="/upload/medialibrary/1b2/14_risunok-1.-vremya-do-dostizheniya.png" height="431" title="14_Рисунок 1. Время до достижения.png"> <h2>Рисунок 1. Время до достижения ПЦР-негативности в зависимости от использования внутривенных ЦМВ-неспецифичных иммуноглобулинов</h2> <h2></h2> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Влияние ИГ на вероятность достижение ЦМВ-негативности (по данным ПЦР) у пациентов с алло-ТГСК показано на Рисунке 1. Как показано на рисунке различия между группами с/без введения ИГ в период терапии ганцикловиром были незначимы. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Использование внутривенных ЦМВ-неспецифичных иммуноглобулинов после алло-ТГСК до сих пор является спорной темой. Согласно нашим данным введение внутривенных ЦМВ-неспецифичных иммуноглобулинов в период терапии ганцикловиром не оказывает должного влияния на эффективность терапии ЦМВ. Однако требуется проведение большого рандомизированного исследования чтобы окончательно определить влияние ЦМВ-неспецифичных ИГ на эффективность лечения реактивации ЦМВ у больных после алло-ТГСК. </p> <h2 style="text-align: justify;">Конфликт интересов</h2> <p style="text-align: justify;"> Нет конфликта интересов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> ЦМВ, внутривенный иммуноглобулин, ганцикловир, алло-ТГСК, ПЦР. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(368) "Влияние внутривенных ЦМВ-неспецифичных иммуноглобулинов на эффективность лечения ганцикловиром у больных после трансплантации аллогенных гемопоэтических стволовых клеток в период реактивации ЦМВ" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(368) "Влияние внутривенных ЦМВ-неспецифичных иммуноглобулинов на эффективность лечения ганцикловиром у больных после трансплантации аллогенных гемопоэтических стволовых клеток в период реактивации ЦМВ" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(368) "Влияние внутривенных ЦМВ-неспецифичных иммуноглобулинов на эффективность лечения ганцикловиром у больных после трансплантации аллогенных гемопоэтических стволовых клеток в период реактивации ЦМВ" ["SECTION_META_TITLE"]=> string(368) "Влияние внутривенных ЦМВ-неспецифичных иммуноглобулинов на эффективность лечения ганцикловиром у больных после трансплантации аллогенных гемопоэтических стволовых клеток в период реактивации ЦМВ" ["SECTION_META_KEYWORDS"]=> string(368) "Влияние внутривенных ЦМВ-неспецифичных иммуноглобулинов на эффективность лечения ганцикловиром у больных после трансплантации аллогенных гемопоэтических стволовых клеток в период реактивации ЦМВ" ["SECTION_META_DESCRIPTION"]=> string(368) "Влияние внутривенных ЦМВ-неспецифичных иммуноглобулинов на эффективность лечения ганцикловиром у больных после трансплантации аллогенных гемопоэтических стволовых клеток в период реактивации ЦМВ" ["SECTION_PICTURE_FILE_ALT"]=> string(368) "Влияние внутривенных ЦМВ-неспецифичных иммуноглобулинов на эффективность лечения ганцикловиром у больных после трансплантации аллогенных гемопоэтических стволовых клеток в период реактивации ЦМВ" ["SECTION_PICTURE_FILE_TITLE"]=> string(368) "Влияние внутривенных ЦМВ-неспецифичных иммуноглобулинов на эффективность лечения ганцикловиром у больных после трансплантации аллогенных гемопоэтических стволовых клеток в период реактивации ЦМВ" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "vliyanie-vnutrivennykh-tsmv-nespetsifichnykh-immunoglobulinov-na-effektivnost-lecheniya-gantsiklovir" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(368) "Влияние внутривенных ЦМВ-неспецифичных иммуноглобулинов на эффективность лечения ганцикловиром у больных после трансплантации аллогенных гемопоэтических стволовых клеток в период реактивации ЦМВ" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(368) "Влияние внутривенных ЦМВ-неспецифичных иммуноглобулинов на эффективность лечения ганцикловиром у больных после трансплантации аллогенных гемопоэтических стволовых клеток в период реактивации ЦМВ" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vliyanie-vnutrivennykh-tsmv-nespetsifichnykh-immunoglobulinov-na-effektivnost-lecheniya-gantsiklovir" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "vliyanie-vnutrivennykh-tsmv-nespetsifichnykh-immunoglobulinov-na-effektivnost-lecheniya-gantsiklovir" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vliyanie-vnutrivennykh-tsmv-nespetsifichnykh-immunoglobulinov-na-effektivnost-lecheniya-gantsiklovir" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20398" ["VALUE"]=> array(2) { ["TEXT"]=> string(556) "Михаил Ю. Дроков, Дмитрий С. Тихомиров, Лариса А. Кузьмина, Татьяна А. Туполева, Наталья Н. Попова, Вера А. Васильева, Екатерина Д. Михальцова, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Татьяна В. Гапонова, Елена Н. Паровичникова, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(556) "Михаил Ю. Дроков, Дмитрий С. Тихомиров, Лариса А. Кузьмина, Татьяна А. Туполева, Наталья Н. Попова, Вера А. Васильева, Екатерина Д. Михальцова, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Татьяна В. Гапонова, Елена Н. Паровичникова, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20399" ["VALUE"]=> array(2) { ["TEXT"]=> string(127) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(127) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20400" ["VALUE"]=> array(2) { ["TEXT"]=> string(6261) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Реактивация цитомегаловирусной инфекции (ЦМВ) остается одной из основных проблем трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Использование ЦМВ-неспецифичных внутривенных иммуноглобулинов (ИГ) до сих пор вызывает споры и определяется, в большей степени, внутренними протоколами трансплантационного центра без четкой доказательной базы. Стандартом же лечения ЦМВ до сих пор остается ганцикловир в дозе 10 мг/кг/сут в течение 14 дней с дальнейшим переходом на профилактическую дозу. Здесь мы приводим данные о влиянии ИГ в период лечения пациентов после алло-ТГСК ганцикловиром в период реактивации ЦМВ-инфекции </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Тридцать два пациента с гемобластозами после алло-ТГСК были включены в исследование. Детальные характеристики представлены в Таблице 1. Все пациенты на момент включения в исследования были ЦМВ-позитивны (по данным ПЦР, «АмплиСенс EBV/CMV/ HHV6-c-крин-FL», Интерлабсервис, Россия), а также требовали начала терапии ганцикловиром в дозе 10 мг/кг/сут. Часть пациентов получили в/в ИГ. Медиана суммарной дозы за время лечения составила 20 г. (7,5-90 г.). Метод Каплан-Мейера был использован для оценки вероятности достижения ЦМВ-негативности (по данным ПЦР). Логранк тест был использован для сравнения различий между двумя группами. Для анализа таблиц 2x2 был использован точный тест Фишера. Р-значение ниже 0.05 считалось значимым. </p> <h2 style="text-align: justify;"> Таблица 1. Характеристики пациентов<br> </h2> <img width="743" alt="14_Таблица 1. Характеристики пациентов.png" src="/upload/medialibrary/77f/14_tablitsa-1.-kharakteristiki-patsientov.png" height="508" title="14_Таблица 1. Характеристики пациентов.png"><br> <img width="740" alt="14_Таблица 1. Характеристики пациентов_2.png" src="/upload/medialibrary/097/14_tablitsa-1.-kharakteristiki-patsientov_2.png" height="272" title="14_Таблица 1. Характеристики пациентов_2.png"><br> <img width="717" alt="14_Рисунок 1. Время до достижения.png" src="/upload/medialibrary/1b2/14_risunok-1.-vremya-do-dostizheniya.png" height="431" title="14_Рисунок 1. Время до достижения.png"> <h2>Рисунок 1. Время до достижения ПЦР-негативности в зависимости от использования внутривенных ЦМВ-неспецифичных иммуноглобулинов</h2> <h2></h2> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Влияние ИГ на вероятность достижение ЦМВ-негативности (по данным ПЦР) у пациентов с алло-ТГСК показано на Рисунке 1. Как показано на рисунке различия между группами с/без введения ИГ в период терапии ганцикловиром были незначимы. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Использование внутривенных ЦМВ-неспецифичных иммуноглобулинов после алло-ТГСК до сих пор является спорной темой. Согласно нашим данным введение внутривенных ЦМВ-неспецифичных иммуноглобулинов в период терапии ганцикловиром не оказывает должного влияния на эффективность терапии ЦМВ. Однако требуется проведение большого рандомизированного исследования чтобы окончательно определить влияние ЦМВ-неспецифичных ИГ на эффективность лечения реактивации ЦМВ у больных после алло-ТГСК. </p> <h2 style="text-align: justify;">Конфликт интересов</h2> <p style="text-align: justify;"> Нет конфликта интересов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> ЦМВ, внутривенный иммуноглобулин, ганцикловир, алло-ТГСК, ПЦР. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5753) "
Введение
Реактивация цитомегаловирусной инфекции (ЦМВ) остается одной из основных проблем трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Использование ЦМВ-неспецифичных внутривенных иммуноглобулинов (ИГ) до сих пор вызывает споры и определяется, в большей степени, внутренними протоколами трансплантационного центра без четкой доказательной базы. Стандартом же лечения ЦМВ до сих пор остается ганцикловир в дозе 10 мг/кг/сут в течение 14 дней с дальнейшим переходом на профилактическую дозу. Здесь мы приводим данные о влиянии ИГ в период лечения пациентов после алло-ТГСК ганцикловиром в период реактивации ЦМВ-инфекции
Пациенты и методы
Тридцать два пациента с гемобластозами после алло-ТГСК были включены в исследование. Детальные характеристики представлены в Таблице 1. Все пациенты на момент включения в исследования были ЦМВ-позитивны (по данным ПЦР, «АмплиСенс EBV/CMV/ HHV6-c-крин-FL», Интерлабсервис, Россия), а также требовали начала терапии ганцикловиром в дозе 10 мг/кг/сут. Часть пациентов получили в/в ИГ. Медиана суммарной дозы за время лечения составила 20 г. (7,5-90 г.). Метод Каплан-Мейера был использован для оценки вероятности достижения ЦМВ-негативности (по данным ПЦР). Логранк тест был использован для сравнения различий между двумя группами. Для анализа таблиц 2x2 был использован точный тест Фишера. Р-значение ниже 0.05 считалось значимым.
Таблица 1. Характеристики пациентов



Рисунок 1. Время до достижения ПЦР-негативности в зависимости от использования внутривенных ЦМВ-неспецифичных иммуноглобулинов
Результаты
Влияние ИГ на вероятность достижение ЦМВ-негативности (по данным ПЦР) у пациентов с алло-ТГСК показано на Рисунке 1. Как показано на рисунке различия между группами с/без введения ИГ в период терапии ганцикловиром были незначимы.
Заключение
Использование внутривенных ЦМВ-неспецифичных иммуноглобулинов после алло-ТГСК до сих пор является спорной темой. Согласно нашим данным введение внутривенных ЦМВ-неспецифичных иммуноглобулинов в период терапии ганцикловиром не оказывает должного влияния на эффективность терапии ЦМВ. Однако требуется проведение большого рандомизированного исследования чтобы окончательно определить влияние ЦМВ-неспецифичных ИГ на эффективность лечения реактивации ЦМВ у больных после алло-ТГСК.
Конфликт интересов
Нет конфликта интересов.
Ключевые слова
ЦМВ, внутривенный иммуноглобулин, ганцикловир, алло-ТГСК, ПЦР.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20401" ["VALUE"]=> array(2) { ["TEXT"]=> string(330) "Mikhail Y. Drokov, Dmitry S. Tikhomirov, Larisa A. Kuzmina, Tatyana A. Tupoleva, Natalia N. Popova, Vera A. Vasilyeva, Ekaterina D. Mikhaltsova, Olga M. Koroleva, Darya S. Dubnyak, Anna A. Sidorova, Ekaterina V. Usikova, Zoya V. Konova, Anna A. Dmitrova, Tatyana V. Gaponova, Elena N. Parovichnikova, Valery G. Savchenko<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(324) "Mikhail Y. Drokov, Dmitry S. Tikhomirov, Larisa A. Kuzmina, Tatyana A. Tupoleva, Natalia N. Popova, Vera A. Vasilyeva, Ekaterina D. Mikhaltsova, Olga M. Koroleva, Darya S. Dubnyak, Anna A. Sidorova, Ekaterina V. Usikova, Zoya V. Konova, Anna A. Dmitrova, Tatyana V. Gaponova, Elena N. Parovichnikova, Valery G. Savchenko" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20402" ["VALUE"]=> array(2) { ["TEXT"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20403" ["VALUE"]=> array(2) { ["TEXT"]=> string(4028) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Cytomegalovirus (CMV) reactivation is one of the main problems in allogenic hematopoietic stem cell transplantation (allo-HSCT). Use of non-CMV specific intravenous immunoglobulin (IVIG) is still controversial and mostly determined by protocols in every transplant center. Standard of care for CMV-disease is still ganciclovir at 10 mg/kg b.i.d. Here we report data about influence of non-CMV specific IVIG during ganciclovir treatment in allo-HSCT CMV+ patients. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Thirty two patients with hematological malignancies transplanted in NRCH were included in this study. Detailed patients characteristics are listed in Table 1. All patients were CMV-positive by PCR (Amplisens EBV/CMV/ HHV6-screen-FL”, InterLabService, Russia) and required to start therapy with ganciclovir 10 mg/kg. Patients in IVIG group also received non-CMV specific IVIG during ganciclovir treatment with a median total dose 20 g (7.5-90 g.). Kaplan-Meier estimator was used to determine probability of achievement of CMV-negativity from the time of ganciclovir was started to CMV-negativity (by PCR) or last contact. The log rank test was used to compare differences between the two groups. Fisher’s exact test was used for 2x2 tables. P-value less than 0.05 was considered statistically significant </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Impact of IVIG in allo-HSCT patients on probability of achievement of CMV-negativity (by PCR) are shown in the Figure 1. As we can see there is no significant differences on the achievement of CMV-negativity (by PCR) in patients with/without IVIG during ganciclovir therapy. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The use of non-CMV specific immunoglobulins after allo-HSCT is still controversial. According to our data there is no difference between IVIG/no-IVIG groups during ganciclovir treatment. For our opinion use of IVIG, for CMV-disease treatment has not been yet proved. Anyway a large randomized trial is required to determine indications for therapy with IVIG in CMV disease after allo-HSCT. </p> <h2 style="text-align: justify;">Disclosures</h2> <p style="text-align: justify;"> No relevant conflicts reported. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> CMV, intravenous immunoglobulin, ganciclovir, allo-HSCT, PCR. </p> <h2 style="text-align: justify;"> Table 1. Patients characteristics<br> </h2> <img width="741" alt="14_Table 1. Patients characteristics.png" src="/upload/medialibrary/94e/14_table-1.-patients-characteristics.png" height="324" title="14_Table 1. Patients characteristics.png"><br> <img width="743" alt="14_Table 1. Patients characteristics_2.png" src="/upload/medialibrary/e1b/14_table-1.-patients-characteristics_2.png" height="483" title="14_Table 1. Patients characteristics_2.png"><br> <br> <img width="717" alt="14_Figure 1. Time to CMV-negativity achievement depending on the therapy mode.png" src="/upload/medialibrary/ffe/14_figure-1.-time-to-cmv_negativity-achievement-depending-on-the-therapy-mode.png" height="431" title="14_Figure 1. Time to CMV-negativity achievement depending on the therapy mode.png"> <h2>Figure 1. Time to CMV-negativity achievement depending on the therapy mode</h2>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3526) "
Introduction
Cytomegalovirus (CMV) reactivation is one of the main problems in allogenic hematopoietic stem cell transplantation (allo-HSCT). Use of non-CMV specific intravenous immunoglobulin (IVIG) is still controversial and mostly determined by protocols in every transplant center. Standard of care for CMV-disease is still ganciclovir at 10 mg/kg b.i.d. Here we report data about influence of non-CMV specific IVIG during ganciclovir treatment in allo-HSCT CMV+ patients.
Patients and methods
Thirty two patients with hematological malignancies transplanted in NRCH were included in this study. Detailed patients characteristics are listed in Table 1. All patients were CMV-positive by PCR (Amplisens EBV/CMV/ HHV6-screen-FL”, InterLabService, Russia) and required to start therapy with ganciclovir 10 mg/kg. Patients in IVIG group also received non-CMV specific IVIG during ganciclovir treatment with a median total dose 20 g (7.5-90 g.). Kaplan-Meier estimator was used to determine probability of achievement of CMV-negativity from the time of ganciclovir was started to CMV-negativity (by PCR) or last contact. The log rank test was used to compare differences between the two groups. Fisher’s exact test was used for 2x2 tables. P-value less than 0.05 was considered statistically significant
Results
Impact of IVIG in allo-HSCT patients on probability of achievement of CMV-negativity (by PCR) are shown in the Figure 1. As we can see there is no significant differences on the achievement of CMV-negativity (by PCR) in patients with/without IVIG during ganciclovir therapy.
Conclusion
The use of non-CMV specific immunoglobulins after allo-HSCT is still controversial. According to our data there is no difference between IVIG/no-IVIG groups during ganciclovir treatment. For our opinion use of IVIG, for CMV-disease treatment has not been yet proved. Anyway a large randomized trial is required to determine indications for therapy with IVIG in CMV disease after allo-HSCT.
Disclosures
No relevant conflicts reported.
Keywords
CMV, intravenous immunoglobulin, ganciclovir, allo-HSCT, PCR.
Table 1. Patients characteristics



Figure 1. Time to CMV-negativity achievement depending on the therapy mode
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20404" ["VALUE"]=> string(169) "Influence of non-CMV specific intravenous immunoglobulin on intravenous ganciclovir effectiveness in patients after allogeneic stem cell transplantation with CMV-disease" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(169) "Influence of non-CMV specific intravenous immunoglobulin on intravenous ganciclovir effectiveness in patients after allogeneic stem cell transplantation with CMV-disease" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20759" ["VALUE"]=> string(4) "1395" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1395" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20760" ["VALUE"]=> string(4) "1396" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1396" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20401" ["VALUE"]=> array(2) { ["TEXT"]=> string(330) "Mikhail Y. Drokov, Dmitry S. Tikhomirov, Larisa A. Kuzmina, Tatyana A. Tupoleva, Natalia N. Popova, Vera A. Vasilyeva, Ekaterina D. Mikhaltsova, Olga M. Koroleva, Darya S. Dubnyak, Anna A. Sidorova, Ekaterina V. Usikova, Zoya V. Konova, Anna A. Dmitrova, Tatyana V. Gaponova, Elena N. Parovichnikova, Valery G. Savchenko<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(324) "Mikhail Y. Drokov, Dmitry S. Tikhomirov, Larisa A. Kuzmina, Tatyana A. Tupoleva, Natalia N. Popova, Vera A. Vasilyeva, Ekaterina D. Mikhaltsova, Olga M. Koroleva, Darya S. Dubnyak, Anna A. Sidorova, Ekaterina V. Usikova, Zoya V. Konova, Anna A. Dmitrova, Tatyana V. Gaponova, Elena N. Parovichnikova, Valery G. Savchenko" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(324) "Mikhail Y. Drokov, Dmitry S. Tikhomirov, Larisa A. Kuzmina, Tatyana A. Tupoleva, Natalia N. Popova, Vera A. Vasilyeva, Ekaterina D. Mikhaltsova, Olga M. Koroleva, Darya S. Dubnyak, Anna A. Sidorova, Ekaterina V. Usikova, Zoya V. Konova, Anna A. Dmitrova, Tatyana V. Gaponova, Elena N. Parovichnikova, Valery G. Savchenko
" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20403" ["VALUE"]=> array(2) { ["TEXT"]=> string(4028) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Cytomegalovirus (CMV) reactivation is one of the main problems in allogenic hematopoietic stem cell transplantation (allo-HSCT). Use of non-CMV specific intravenous immunoglobulin (IVIG) is still controversial and mostly determined by protocols in every transplant center. Standard of care for CMV-disease is still ganciclovir at 10 mg/kg b.i.d. Here we report data about influence of non-CMV specific IVIG during ganciclovir treatment in allo-HSCT CMV+ patients. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Thirty two patients with hematological malignancies transplanted in NRCH were included in this study. Detailed patients characteristics are listed in Table 1. All patients were CMV-positive by PCR (Amplisens EBV/CMV/ HHV6-screen-FL”, InterLabService, Russia) and required to start therapy with ganciclovir 10 mg/kg. Patients in IVIG group also received non-CMV specific IVIG during ganciclovir treatment with a median total dose 20 g (7.5-90 g.). Kaplan-Meier estimator was used to determine probability of achievement of CMV-negativity from the time of ganciclovir was started to CMV-negativity (by PCR) or last contact. The log rank test was used to compare differences between the two groups. Fisher’s exact test was used for 2x2 tables. P-value less than 0.05 was considered statistically significant </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Impact of IVIG in allo-HSCT patients on probability of achievement of CMV-negativity (by PCR) are shown in the Figure 1. As we can see there is no significant differences on the achievement of CMV-negativity (by PCR) in patients with/without IVIG during ganciclovir therapy. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The use of non-CMV specific immunoglobulins after allo-HSCT is still controversial. According to our data there is no difference between IVIG/no-IVIG groups during ganciclovir treatment. For our opinion use of IVIG, for CMV-disease treatment has not been yet proved. Anyway a large randomized trial is required to determine indications for therapy with IVIG in CMV disease after allo-HSCT. </p> <h2 style="text-align: justify;">Disclosures</h2> <p style="text-align: justify;"> No relevant conflicts reported. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> CMV, intravenous immunoglobulin, ganciclovir, allo-HSCT, PCR. </p> <h2 style="text-align: justify;"> Table 1. Patients characteristics<br> </h2> <img width="741" alt="14_Table 1. Patients characteristics.png" src="/upload/medialibrary/94e/14_table-1.-patients-characteristics.png" height="324" title="14_Table 1. Patients characteristics.png"><br> <img width="743" alt="14_Table 1. Patients characteristics_2.png" src="/upload/medialibrary/e1b/14_table-1.-patients-characteristics_2.png" height="483" title="14_Table 1. Patients characteristics_2.png"><br> <br> <img width="717" alt="14_Figure 1. Time to CMV-negativity achievement depending on the therapy mode.png" src="/upload/medialibrary/ffe/14_figure-1.-time-to-cmv_negativity-achievement-depending-on-the-therapy-mode.png" height="431" title="14_Figure 1. Time to CMV-negativity achievement depending on the therapy mode.png"> <h2>Figure 1. Time to CMV-negativity achievement depending on the therapy mode</h2>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3526) "
Introduction
Cytomegalovirus (CMV) reactivation is one of the main problems in allogenic hematopoietic stem cell transplantation (allo-HSCT). Use of non-CMV specific intravenous immunoglobulin (IVIG) is still controversial and mostly determined by protocols in every transplant center. Standard of care for CMV-disease is still ganciclovir at 10 mg/kg b.i.d. Here we report data about influence of non-CMV specific IVIG during ganciclovir treatment in allo-HSCT CMV+ patients.
Patients and methods
Thirty two patients with hematological malignancies transplanted in NRCH were included in this study. Detailed patients characteristics are listed in Table 1. All patients were CMV-positive by PCR (Amplisens EBV/CMV/ HHV6-screen-FL”, InterLabService, Russia) and required to start therapy with ganciclovir 10 mg/kg. Patients in IVIG group also received non-CMV specific IVIG during ganciclovir treatment with a median total dose 20 g (7.5-90 g.). Kaplan-Meier estimator was used to determine probability of achievement of CMV-negativity from the time of ganciclovir was started to CMV-negativity (by PCR) or last contact. The log rank test was used to compare differences between the two groups. Fisher’s exact test was used for 2x2 tables. P-value less than 0.05 was considered statistically significant
Results
Impact of IVIG in allo-HSCT patients on probability of achievement of CMV-negativity (by PCR) are shown in the Figure 1. As we can see there is no significant differences on the achievement of CMV-negativity (by PCR) in patients with/without IVIG during ganciclovir therapy.
Conclusion
The use of non-CMV specific immunoglobulins after allo-HSCT is still controversial. According to our data there is no difference between IVIG/no-IVIG groups during ganciclovir treatment. For our opinion use of IVIG, for CMV-disease treatment has not been yet proved. Anyway a large randomized trial is required to determine indications for therapy with IVIG in CMV disease after allo-HSCT.
Disclosures
No relevant conflicts reported.
Keywords
CMV, intravenous immunoglobulin, ganciclovir, allo-HSCT, PCR.
Table 1. Patients characteristics



Figure 1. Time to CMV-negativity achievement depending on the therapy mode
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3526) "Introduction
Cytomegalovirus (CMV) reactivation is one of the main problems in allogenic hematopoietic stem cell transplantation (allo-HSCT). Use of non-CMV specific intravenous immunoglobulin (IVIG) is still controversial and mostly determined by protocols in every transplant center. Standard of care for CMV-disease is still ganciclovir at 10 mg/kg b.i.d. Here we report data about influence of non-CMV specific IVIG during ganciclovir treatment in allo-HSCT CMV+ patients.
Patients and methods
Thirty two patients with hematological malignancies transplanted in NRCH were included in this study. Detailed patients characteristics are listed in Table 1. All patients were CMV-positive by PCR (Amplisens EBV/CMV/ HHV6-screen-FL”, InterLabService, Russia) and required to start therapy with ganciclovir 10 mg/kg. Patients in IVIG group also received non-CMV specific IVIG during ganciclovir treatment with a median total dose 20 g (7.5-90 g.). Kaplan-Meier estimator was used to determine probability of achievement of CMV-negativity from the time of ganciclovir was started to CMV-negativity (by PCR) or last contact. The log rank test was used to compare differences between the two groups. Fisher’s exact test was used for 2x2 tables. P-value less than 0.05 was considered statistically significant
Results
Impact of IVIG in allo-HSCT patients on probability of achievement of CMV-negativity (by PCR) are shown in the Figure 1. As we can see there is no significant differences on the achievement of CMV-negativity (by PCR) in patients with/without IVIG during ganciclovir therapy.
Conclusion
The use of non-CMV specific immunoglobulins after allo-HSCT is still controversial. According to our data there is no difference between IVIG/no-IVIG groups during ganciclovir treatment. For our opinion use of IVIG, for CMV-disease treatment has not been yet proved. Anyway a large randomized trial is required to determine indications for therapy with IVIG in CMV disease after allo-HSCT.
Disclosures
No relevant conflicts reported.
Keywords
CMV, intravenous immunoglobulin, ganciclovir, allo-HSCT, PCR.
Table 1. Patients characteristics



Figure 1. Time to CMV-negativity achievement depending on the therapy mode
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20404" ["VALUE"]=> string(169) "Influence of non-CMV specific intravenous immunoglobulin on intravenous ganciclovir effectiveness in patients after allogeneic stem cell transplantation with CMV-disease" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(169) "Influence of non-CMV specific intravenous immunoglobulin on intravenous ganciclovir effectiveness in patients after allogeneic stem cell transplantation with CMV-disease" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(169) "Influence of non-CMV specific intravenous immunoglobulin on intravenous ganciclovir effectiveness in patients after allogeneic stem cell transplantation with CMV-disease" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20402" ["VALUE"]=> array(2) { ["TEXT"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20398" ["VALUE"]=> array(2) { ["TEXT"]=> string(556) "Михаил Ю. Дроков, Дмитрий С. Тихомиров, Лариса А. Кузьмина, Татьяна А. Туполева, Наталья Н. Попова, Вера А. Васильева, Екатерина Д. Михальцова, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Татьяна В. Гапонова, Елена Н. Паровичникова, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(556) "Михаил Ю. Дроков, Дмитрий С. Тихомиров, Лариса А. Кузьмина, Татьяна А. Туполева, Наталья Н. Попова, Вера А. Васильева, Екатерина Д. Михальцова, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Татьяна В. Гапонова, Елена Н. Паровичникова, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(556) "Михаил Ю. Дроков, Дмитрий С. Тихомиров, Лариса А. Кузьмина, Татьяна А. Туполева, Наталья Н. Попова, Вера А. Васильева, Екатерина Д. Михальцова, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Татьяна В. Гапонова, Елена Н. Паровичникова, Валерий Г. Савченко" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20400" ["VALUE"]=> array(2) { ["TEXT"]=> string(6261) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Реактивация цитомегаловирусной инфекции (ЦМВ) остается одной из основных проблем трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Использование ЦМВ-неспецифичных внутривенных иммуноглобулинов (ИГ) до сих пор вызывает споры и определяется, в большей степени, внутренними протоколами трансплантационного центра без четкой доказательной базы. Стандартом же лечения ЦМВ до сих пор остается ганцикловир в дозе 10 мг/кг/сут в течение 14 дней с дальнейшим переходом на профилактическую дозу. Здесь мы приводим данные о влиянии ИГ в период лечения пациентов после алло-ТГСК ганцикловиром в период реактивации ЦМВ-инфекции </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Тридцать два пациента с гемобластозами после алло-ТГСК были включены в исследование. Детальные характеристики представлены в Таблице 1. Все пациенты на момент включения в исследования были ЦМВ-позитивны (по данным ПЦР, «АмплиСенс EBV/CMV/ HHV6-c-крин-FL», Интерлабсервис, Россия), а также требовали начала терапии ганцикловиром в дозе 10 мг/кг/сут. Часть пациентов получили в/в ИГ. Медиана суммарной дозы за время лечения составила 20 г. (7,5-90 г.). Метод Каплан-Мейера был использован для оценки вероятности достижения ЦМВ-негативности (по данным ПЦР). Логранк тест был использован для сравнения различий между двумя группами. Для анализа таблиц 2x2 был использован точный тест Фишера. Р-значение ниже 0.05 считалось значимым. </p> <h2 style="text-align: justify;"> Таблица 1. Характеристики пациентов<br> </h2> <img width="743" alt="14_Таблица 1. Характеристики пациентов.png" src="/upload/medialibrary/77f/14_tablitsa-1.-kharakteristiki-patsientov.png" height="508" title="14_Таблица 1. Характеристики пациентов.png"><br> <img width="740" alt="14_Таблица 1. Характеристики пациентов_2.png" src="/upload/medialibrary/097/14_tablitsa-1.-kharakteristiki-patsientov_2.png" height="272" title="14_Таблица 1. Характеристики пациентов_2.png"><br> <img width="717" alt="14_Рисунок 1. Время до достижения.png" src="/upload/medialibrary/1b2/14_risunok-1.-vremya-do-dostizheniya.png" height="431" title="14_Рисунок 1. Время до достижения.png"> <h2>Рисунок 1. Время до достижения ПЦР-негативности в зависимости от использования внутривенных ЦМВ-неспецифичных иммуноглобулинов</h2> <h2></h2> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Влияние ИГ на вероятность достижение ЦМВ-негативности (по данным ПЦР) у пациентов с алло-ТГСК показано на Рисунке 1. Как показано на рисунке различия между группами с/без введения ИГ в период терапии ганцикловиром были незначимы. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Использование внутривенных ЦМВ-неспецифичных иммуноглобулинов после алло-ТГСК до сих пор является спорной темой. Согласно нашим данным введение внутривенных ЦМВ-неспецифичных иммуноглобулинов в период терапии ганцикловиром не оказывает должного влияния на эффективность терапии ЦМВ. Однако требуется проведение большого рандомизированного исследования чтобы окончательно определить влияние ЦМВ-неспецифичных ИГ на эффективность лечения реактивации ЦМВ у больных после алло-ТГСК. </p> <h2 style="text-align: justify;">Конфликт интересов</h2> <p style="text-align: justify;"> Нет конфликта интересов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> ЦМВ, внутривенный иммуноглобулин, ганцикловир, алло-ТГСК, ПЦР. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5753) "Введение
Реактивация цитомегаловирусной инфекции (ЦМВ) остается одной из основных проблем трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Использование ЦМВ-неспецифичных внутривенных иммуноглобулинов (ИГ) до сих пор вызывает споры и определяется, в большей степени, внутренними протоколами трансплантационного центра без четкой доказательной базы. Стандартом же лечения ЦМВ до сих пор остается ганцикловир в дозе 10 мг/кг/сут в течение 14 дней с дальнейшим переходом на профилактическую дозу. Здесь мы приводим данные о влиянии ИГ в период лечения пациентов после алло-ТГСК ганцикловиром в период реактивации ЦМВ-инфекции
Пациенты и методы
Тридцать два пациента с гемобластозами после алло-ТГСК были включены в исследование. Детальные характеристики представлены в Таблице 1. Все пациенты на момент включения в исследования были ЦМВ-позитивны (по данным ПЦР, «АмплиСенс EBV/CMV/ HHV6-c-крин-FL», Интерлабсервис, Россия), а также требовали начала терапии ганцикловиром в дозе 10 мг/кг/сут. Часть пациентов получили в/в ИГ. Медиана суммарной дозы за время лечения составила 20 г. (7,5-90 г.). Метод Каплан-Мейера был использован для оценки вероятности достижения ЦМВ-негативности (по данным ПЦР). Логранк тест был использован для сравнения различий между двумя группами. Для анализа таблиц 2x2 был использован точный тест Фишера. Р-значение ниже 0.05 считалось значимым.
Таблица 1. Характеристики пациентов



Рисунок 1. Время до достижения ПЦР-негативности в зависимости от использования внутривенных ЦМВ-неспецифичных иммуноглобулинов
Результаты
Влияние ИГ на вероятность достижение ЦМВ-негативности (по данным ПЦР) у пациентов с алло-ТГСК показано на Рисунке 1. Как показано на рисунке различия между группами с/без введения ИГ в период терапии ганцикловиром были незначимы.
Заключение
Использование внутривенных ЦМВ-неспецифичных иммуноглобулинов после алло-ТГСК до сих пор является спорной темой. Согласно нашим данным введение внутривенных ЦМВ-неспецифичных иммуноглобулинов в период терапии ганцикловиром не оказывает должного влияния на эффективность терапии ЦМВ. Однако требуется проведение большого рандомизированного исследования чтобы окончательно определить влияние ЦМВ-неспецифичных ИГ на эффективность лечения реактивации ЦМВ у больных после алло-ТГСК.
Конфликт интересов
Нет конфликта интересов.
Ключевые слова
ЦМВ, внутривенный иммуноглобулин, ганцикловир, алло-ТГСК, ПЦР.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(5753) "Введение
Реактивация цитомегаловирусной инфекции (ЦМВ) остается одной из основных проблем трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Использование ЦМВ-неспецифичных внутривенных иммуноглобулинов (ИГ) до сих пор вызывает споры и определяется, в большей степени, внутренними протоколами трансплантационного центра без четкой доказательной базы. Стандартом же лечения ЦМВ до сих пор остается ганцикловир в дозе 10 мг/кг/сут в течение 14 дней с дальнейшим переходом на профилактическую дозу. Здесь мы приводим данные о влиянии ИГ в период лечения пациентов после алло-ТГСК ганцикловиром в период реактивации ЦМВ-инфекции
Пациенты и методы
Тридцать два пациента с гемобластозами после алло-ТГСК были включены в исследование. Детальные характеристики представлены в Таблице 1. Все пациенты на момент включения в исследования были ЦМВ-позитивны (по данным ПЦР, «АмплиСенс EBV/CMV/ HHV6-c-крин-FL», Интерлабсервис, Россия), а также требовали начала терапии ганцикловиром в дозе 10 мг/кг/сут. Часть пациентов получили в/в ИГ. Медиана суммарной дозы за время лечения составила 20 г. (7,5-90 г.). Метод Каплан-Мейера был использован для оценки вероятности достижения ЦМВ-негативности (по данным ПЦР). Логранк тест был использован для сравнения различий между двумя группами. Для анализа таблиц 2x2 был использован точный тест Фишера. Р-значение ниже 0.05 считалось значимым.
Таблица 1. Характеристики пациентов



Рисунок 1. Время до достижения ПЦР-негативности в зависимости от использования внутривенных ЦМВ-неспецифичных иммуноглобулинов
Результаты
Влияние ИГ на вероятность достижение ЦМВ-негативности (по данным ПЦР) у пациентов с алло-ТГСК показано на Рисунке 1. Как показано на рисунке различия между группами с/без введения ИГ в период терапии ганцикловиром были незначимы.
Заключение
Использование внутривенных ЦМВ-неспецифичных иммуноглобулинов после алло-ТГСК до сих пор является спорной темой. Согласно нашим данным введение внутривенных ЦМВ-неспецифичных иммуноглобулинов в период терапии ганцикловиром не оказывает должного влияния на эффективность терапии ЦМВ. Однако требуется проведение большого рандомизированного исследования чтобы окончательно определить влияние ЦМВ-неспецифичных ИГ на эффективность лечения реактивации ЦМВ у больных после алло-ТГСК.
Конфликт интересов
Нет конфликта интересов.
Ключевые слова
ЦМВ, внутривенный иммуноглобулин, ганцикловир, алло-ТГСК, ПЦР.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20399" ["VALUE"]=> array(2) { ["TEXT"]=> string(127) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(127) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(127) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва, Российская Федерация" } } } [13]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1562" ["~ID"]=> string(4) "1562" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(360) "Влияние возраста пациентов на частоту РТПХ и общую выживаемость при использовании посттрансплантационного циклофос- фамида (ПТ-ЦФ) и антитимоцитарного глобулина (АТГ) у больных острыми лейкозами" ["~NAME"]=> string(360) "Влияние возраста пациентов на частоту РТПХ и общую выживаемость при использовании посттрансплантационного циклофос- фамида (ПТ-ЦФ) и антитимоцитарного глобулина (АТГ) у больных острыми лейкозами" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:29:39" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:29:39" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vliyanie-vozrasta-patsientov-na-chastotu-rtpkh-i-obshchuyu-vyzhivaemost-pri-ispolzovanii-posttranspl/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vliyanie-vozrasta-patsientov-na-chastotu-rtpkh-i-obshchuyu-vyzhivaemost-pri-ispolzovanii-posttranspl/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "vliyanie-vozrasta-patsientov-na-chastotu-rtpkh-i-obshchuyu-vyzhivaemost-pri-ispolzovanii-posttranspl" ["~CODE"]=> string(100) "vliyanie-vozrasta-patsientov-na-chastotu-rtpkh-i-obshchuyu-vyzhivaemost-pri-ispolzovanii-posttranspl" ["EXTERNAL_ID"]=> string(4) "1562" ["~EXTERNAL_ID"]=> string(4) "1562" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(360) "Влияние возраста пациентов на частоту РТПХ и общую выживаемость при использовании посттрансплантационного циклофос- фамида (ПТ-ЦФ) и антитимоцитарного глобулина (АТГ) у больных острыми лейкозами" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(526) "Влияние возраста пациентов на частоту РТПХ и общую выживаемость при использовании посттрансплантационного циклофос- фамида (ПТ-ЦФ) и антитимоцитарного глобулина (АТГ) у больных острыми лейкозамиAge affects GVHD rate but not overall survival in leukemia patients with posttransplant cyclophosphamide (PT-CY) and anti-thymocyte globulin (ATG) as GVHD prophylaxis" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(8456) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Трансплантация аллогенного костного мозга (алло-ТГСК) с использованием высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) в качестве индуктора толерантности стала хорошей альтернативой стандартной иммуносупрессии. Часто необоснованные ожидания токсичности, особенно у пациентов старше 50, становятся препятствием для проведения алло-ТГСК у данных больных. Здесь нами представлены данные о влиянии возраста пациентов с острыми лейкозами в ПР на результаты алло-ТГСК с ПТ-ЦФ и АТГ в качестве профилактики РТПХ. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Сорок пациентов с острыми лейкозами были трансплантированы в ПР в НМИЦ гематологии МЗ РФ от неродственного частично-совместимого донора. Характеристика пациентов представлена в Таблице 1. Все пациенты в качестве профилактики РТПХ получали: АТГ в суммарной дозе 40 мг/кг с -4 по -1 день; ПТ-ЦФ в дозе 50 мг/кг/сут на +3, +4 день; Циклоспорин А в дозе 3 мг/кг/сут с -1 дня; Микофенолата мофетил 3000 мг/сут с +5 дня. Метод Каплан-Мейера был использован для оценки общей выживаемости, вероятности развития рецидива, острой РТПХ. Логранк тест был использован для сравнения различий между двумя группами. Р-значение ниже 0.05 считалось значимым. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Острая РТПХ в группе пациентов старше 50 лет была значимо выше, чем в группах в возрасте 40-49 и 20-39 лет (66,7% vs 25% vs 12,5%, p=0.0044) (Рис. 1). Вероятно, это может быть связано с резидуальной функцией тимуса, а также более частым использованием миелоаблативных режимов у молодых больных (младше 50 лет). Однако, несмотря на эти различия, высокая частота развития РТПХ свидетельствует о более низкой частоте развития рецидивов (Рис. 2), что, в свою очередь, ведет к отсутствию различий общей выживаемостью между группами (Рис. 3) – 56,1%, 66,7% и 65,6% для группы 20-39, 40-49 и 50+ соответственно. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Алло-ТГСК у пациентов в возрасте старше 50 лет имеет свои особенности, однако эффективность данной процедуры (общая выживаемость пациентов) ничуть не меньше, чем у более молодых пациентов. Таким образом, использование ПТ-ЦФ и АТГ у пациентов старше 50 лет вполне оправдано и достаточно эффективно. </p> <h2 style="text-align: justify;">Конфликт интересов</h2> <p style="text-align: justify;"> Отсутствует конфликт интересов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> РТПХ, посттрансплантационный циклофосфамид, возраст, острый лейкоз, АТГ. </p> <h2 style="text-align: justify;"> Таблица 1. Характеристика пациентов<br> </h2> <p style="text-align: justify;"> <img width="783" alt="13_Таблица 1. Характеристика пациентов.png" src="/upload/medialibrary/da0/13_tablitsa-1.-kharakteristika-patsientov.png" height="329" title="13_Таблица 1. Характеристика пациентов.png"><br> </p> <p style="text-align: justify;"> <img width="717" alt="13_Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами.png" src="/upload/medialibrary/87b/13_risunok-1.-veroyatnost-razvitiya-ostroy-rtpkh-v-razlichnykh-vozrastnykh-gruppakh-u-patsientov-s-ostrymi-leykozami.png" height="425" title="13_Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами.png"><br> </p> <h2 style="text-align: justify;"> Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ</h2> <p style="text-align: justify;"> <img width="717" alt="13_Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами.png" src="/upload/medialibrary/9d2/13_risunok-2.-veroyatnost-razvitiya-retsidiva-v-razlichnykh-vozrastnykh-gruppakh-u-patsientov-s-ostrymi-leykozami.png" height="426" title="13_Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами.png"><br> </p> <h2 style="text-align: justify;"> Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ</h2> <img width="717" alt="13_Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после.png" src="/upload/medialibrary/ea1/13_risunok-3.-obshchaya-vyzhivaemost-v-razlichnykh-vozrastnykh-gruppakh-u-patsientov-s-ostrymi-leykozami-posle.png" height="426" title="13_Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после.png"> <h2>Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ</h2>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(360) "Влияние возраста пациентов на частоту РТПХ и общую выживаемость при использовании посттрансплантационного циклофос- фамида (ПТ-ЦФ) и антитимоцитарного глобулина (АТГ) у больных острыми лейкозами" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(360) "Влияние возраста пациентов на частоту РТПХ и общую выживаемость при использовании посттрансплантационного циклофос- фамида (ПТ-ЦФ) и антитимоцитарного глобулина (АТГ) у больных острыми лейкозами" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(360) "Влияние возраста пациентов на частоту РТПХ и общую выживаемость при использовании посттрансплантационного циклофос- фамида (ПТ-ЦФ) и антитимоцитарного глобулина (АТГ) у больных острыми лейкозами" ["SECTION_META_TITLE"]=> string(360) "Влияние возраста пациентов на частоту РТПХ и общую выживаемость при использовании посттрансплантационного циклофос- фамида (ПТ-ЦФ) и антитимоцитарного глобулина (АТГ) у больных острыми лейкозами" ["SECTION_META_KEYWORDS"]=> string(360) "Влияние возраста пациентов на частоту РТПХ и общую выживаемость при использовании посттрансплантационного циклофос- фамида (ПТ-ЦФ) и антитимоцитарного глобулина (АТГ) у больных острыми лейкозами" ["SECTION_META_DESCRIPTION"]=> string(360) "Влияние возраста пациентов на частоту РТПХ и общую выживаемость при использовании посттрансплантационного циклофос- фамида (ПТ-ЦФ) и антитимоцитарного глобулина (АТГ) у больных острыми лейкозами" ["SECTION_PICTURE_FILE_ALT"]=> string(360) "Влияние возраста пациентов на частоту РТПХ и общую выживаемость при использовании посттрансплантационного циклофос- фамида (ПТ-ЦФ) и антитимоцитарного глобулина (АТГ) у больных острыми лейкозами" ["SECTION_PICTURE_FILE_TITLE"]=> string(360) "Влияние возраста пациентов на частоту РТПХ и общую выживаемость при использовании посттрансплантационного циклофос- фамида (ПТ-ЦФ) и антитимоцитарного глобулина (АТГ) у больных острыми лейкозами" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "vliyanie-vozrasta-patsientov-na-chastotu-rtpkh-i-obshchuyu-vyzhivaemost-pri-ispolzovanii-posttranspl" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(360) "Влияние возраста пациентов на частоту РТПХ и общую выживаемость при использовании посттрансплантационного циклофос- фамида (ПТ-ЦФ) и антитимоцитарного глобулина (АТГ) у больных острыми лейкозами" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(360) "Влияние возраста пациентов на частоту РТПХ и общую выживаемость при использовании посттрансплантационного циклофос- фамида (ПТ-ЦФ) и антитимоцитарного глобулина (АТГ) у больных острыми лейкозами" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vliyanie-vozrasta-patsientov-na-chastotu-rtpkh-i-obshchuyu-vyzhivaemost-pri-ispolzovanii-posttranspl" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "vliyanie-vozrasta-patsientov-na-chastotu-rtpkh-i-obshchuyu-vyzhivaemost-pri-ispolzovanii-posttranspl" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vliyanie-vozrasta-patsientov-na-chastotu-rtpkh-i-obshchuyu-vyzhivaemost-pri-ispolzovanii-posttranspl" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20389" ["VALUE"]=> array(2) { ["TEXT"]=> string(443) "Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Вера А. Васильева, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Елена Н. Паровичникова, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(443) "Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Вера А. Васильева, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Елена Н. Паровичникова, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20390" ["VALUE"]=> array(2) { ["TEXT"]=> string(86) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(86) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20391" ["VALUE"]=> array(2) { ["TEXT"]=> string(8456) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Трансплантация аллогенного костного мозга (алло-ТГСК) с использованием высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) в качестве индуктора толерантности стала хорошей альтернативой стандартной иммуносупрессии. Часто необоснованные ожидания токсичности, особенно у пациентов старше 50, становятся препятствием для проведения алло-ТГСК у данных больных. Здесь нами представлены данные о влиянии возраста пациентов с острыми лейкозами в ПР на результаты алло-ТГСК с ПТ-ЦФ и АТГ в качестве профилактики РТПХ. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Сорок пациентов с острыми лейкозами были трансплантированы в ПР в НМИЦ гематологии МЗ РФ от неродственного частично-совместимого донора. Характеристика пациентов представлена в Таблице 1. Все пациенты в качестве профилактики РТПХ получали: АТГ в суммарной дозе 40 мг/кг с -4 по -1 день; ПТ-ЦФ в дозе 50 мг/кг/сут на +3, +4 день; Циклоспорин А в дозе 3 мг/кг/сут с -1 дня; Микофенолата мофетил 3000 мг/сут с +5 дня. Метод Каплан-Мейера был использован для оценки общей выживаемости, вероятности развития рецидива, острой РТПХ. Логранк тест был использован для сравнения различий между двумя группами. Р-значение ниже 0.05 считалось значимым. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Острая РТПХ в группе пациентов старше 50 лет была значимо выше, чем в группах в возрасте 40-49 и 20-39 лет (66,7% vs 25% vs 12,5%, p=0.0044) (Рис. 1). Вероятно, это может быть связано с резидуальной функцией тимуса, а также более частым использованием миелоаблативных режимов у молодых больных (младше 50 лет). Однако, несмотря на эти различия, высокая частота развития РТПХ свидетельствует о более низкой частоте развития рецидивов (Рис. 2), что, в свою очередь, ведет к отсутствию различий общей выживаемостью между группами (Рис. 3) – 56,1%, 66,7% и 65,6% для группы 20-39, 40-49 и 50+ соответственно. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Алло-ТГСК у пациентов в возрасте старше 50 лет имеет свои особенности, однако эффективность данной процедуры (общая выживаемость пациентов) ничуть не меньше, чем у более молодых пациентов. Таким образом, использование ПТ-ЦФ и АТГ у пациентов старше 50 лет вполне оправдано и достаточно эффективно. </p> <h2 style="text-align: justify;">Конфликт интересов</h2> <p style="text-align: justify;"> Отсутствует конфликт интересов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> РТПХ, посттрансплантационный циклофосфамид, возраст, острый лейкоз, АТГ. </p> <h2 style="text-align: justify;"> Таблица 1. Характеристика пациентов<br> </h2> <p style="text-align: justify;"> <img width="783" alt="13_Таблица 1. Характеристика пациентов.png" src="/upload/medialibrary/da0/13_tablitsa-1.-kharakteristika-patsientov.png" height="329" title="13_Таблица 1. Характеристика пациентов.png"><br> </p> <p style="text-align: justify;"> <img width="717" alt="13_Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами.png" src="/upload/medialibrary/87b/13_risunok-1.-veroyatnost-razvitiya-ostroy-rtpkh-v-razlichnykh-vozrastnykh-gruppakh-u-patsientov-s-ostrymi-leykozami.png" height="425" title="13_Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами.png"><br> </p> <h2 style="text-align: justify;"> Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ</h2> <p style="text-align: justify;"> <img width="717" alt="13_Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами.png" src="/upload/medialibrary/9d2/13_risunok-2.-veroyatnost-razvitiya-retsidiva-v-razlichnykh-vozrastnykh-gruppakh-u-patsientov-s-ostrymi-leykozami.png" height="426" title="13_Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами.png"><br> </p> <h2 style="text-align: justify;"> Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ</h2> <img width="717" alt="13_Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после.png" src="/upload/medialibrary/ea1/13_risunok-3.-obshchaya-vyzhivaemost-v-razlichnykh-vozrastnykh-gruppakh-u-patsientov-s-ostrymi-leykozami-posle.png" height="426" title="13_Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после.png"> <h2>Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ</h2>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7788) "Введение
Трансплантация аллогенного костного мозга (алло-ТГСК) с использованием высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) в качестве индуктора толерантности стала хорошей альтернативой стандартной иммуносупрессии. Часто необоснованные ожидания токсичности, особенно у пациентов старше 50, становятся препятствием для проведения алло-ТГСК у данных больных. Здесь нами представлены данные о влиянии возраста пациентов с острыми лейкозами в ПР на результаты алло-ТГСК с ПТ-ЦФ и АТГ в качестве профилактики РТПХ.
Пациенты и методы
Сорок пациентов с острыми лейкозами были трансплантированы в ПР в НМИЦ гематологии МЗ РФ от неродственного частично-совместимого донора. Характеристика пациентов представлена в Таблице 1. Все пациенты в качестве профилактики РТПХ получали: АТГ в суммарной дозе 40 мг/кг с -4 по -1 день; ПТ-ЦФ в дозе 50 мг/кг/сут на +3, +4 день; Циклоспорин А в дозе 3 мг/кг/сут с -1 дня; Микофенолата мофетил 3000 мг/сут с +5 дня. Метод Каплан-Мейера был использован для оценки общей выживаемости, вероятности развития рецидива, острой РТПХ. Логранк тест был использован для сравнения различий между двумя группами. Р-значение ниже 0.05 считалось значимым.
Результаты
Острая РТПХ в группе пациентов старше 50 лет была значимо выше, чем в группах в возрасте 40-49 и 20-39 лет (66,7% vs 25% vs 12,5%, p=0.0044) (Рис. 1). Вероятно, это может быть связано с резидуальной функцией тимуса, а также более частым использованием миелоаблативных режимов у молодых больных (младше 50 лет). Однако, несмотря на эти различия, высокая частота развития РТПХ свидетельствует о более низкой частоте развития рецидивов (Рис. 2), что, в свою очередь, ведет к отсутствию различий общей выживаемостью между группами (Рис. 3) – 56,1%, 66,7% и 65,6% для группы 20-39, 40-49 и 50+ соответственно.
Заключение
Алло-ТГСК у пациентов в возрасте старше 50 лет имеет свои особенности, однако эффективность данной процедуры (общая выживаемость пациентов) ничуть не меньше, чем у более молодых пациентов. Таким образом, использование ПТ-ЦФ и АТГ у пациентов старше 50 лет вполне оправдано и достаточно эффективно.
Конфликт интересов
Отсутствует конфликт интересов.
Ключевые слова
РТПХ, посттрансплантационный циклофосфамид, возраст, острый лейкоз, АТГ.
Таблица 1. Характеристика пациентов


Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ

Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ

Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20392" ["VALUE"]=> array(2) { ["TEXT"]=> string(266) "Mikhail Y. Drokov, Larisa A. Kuzmina, Natalia N. Popova, Ekaterina D. Mikhaltsova, Vera A. Vasilyeva, Olga M. Koroleva, Darya S. Dubnyak, Anna A. Sidorova, Ekaterina V. Usikova, Zoya V. Konova, Anna A. Dmitrova, Elena N. Parovichnikova, Valery G. Savchenko<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(260) "Mikhail Y. Drokov, Larisa A. Kuzmina, Natalia N. Popova, Ekaterina D. Mikhaltsova, Vera A. Vasilyeva, Olga M. Koroleva, Darya S. Dubnyak, Anna A. Sidorova, Ekaterina V. Usikova, Zoya V. Konova, Anna A. Dmitrova, Elena N. Parovichnikova, Valery G. Savchenko" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20393" ["VALUE"]=> array(2) { ["TEXT"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20394" ["VALUE"]=> array(2) { ["TEXT"]=> string(4080) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic bone marrow transplantation (allo-BMT) with high-dose posttransplant cyclophosphamide (PT-CY) to promote graft-host tolerance has become an alternative for standard immunosuppression. But sometimes unjustified toxicity expectations in aged patients are the main limiting factor of allo-HSCT for this group. Here we report our data about an influence of age on allo-HSCT results in leukemia patients in CR with PT-CY and ATG as GVHD prophylaxis. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Forty patients with acute leukemia in CR transplanted in NRCH from mismatched unrelated donor were included in this study. All patient characteristics are listed in Table 1. All the patients received ATG at a dose 40 mg/kg from day -4 to day -1; PT-CY at dose 50 mg/kg daily at day +3,+4; Cyclosporine A 3 mg/kg from day -1 and MMF 3000 mg b.i.d from day +5. Kaplan-Meier estimator was used to determine overall survival, probability of aGVHD and relapse. The log-rank test was used to compare differences between the two groups. P-value less than 0.05 was considered statistically significant. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Acute GVHD rates in 50+ y.o. group are significantly higher (Fig. 1) than in younger patients (66.7% vs 25% vs 12.5%, p=0.0044). It can be explained by thymus function and use of MAC conditioning regimens in the last patient group. Despite that fact due to low relapse rate (Fig. 2) overall survival (Fig. 3) in 50+ y.o. patients looks comparable with younger patients (66.7% vs 65.6% vs 58.9% for 40-49 y.o., 50+ and 20-39 y.o. respectively). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Allo-HSCT still makes sense in 50+ y.o. patients, since the results are not worse than in younger patients. Usage of PT-CY and ATG as GVHD prophylaxis seems to be safe and effective approach even for aged leukemia patients. </p> <h2 style="text-align: justify;">Disclosures</h2> <p style="text-align: justify;"> No relevant conflicts of interest to declare. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> GVHD, PT-Cy, age, acute leukemia, ATG.<br> </p> <h2 style="text-align: justify;"> Table 1. Patients characteristics<br> </h2> <img width="787" alt="13_Table 1.png" src="/upload/medialibrary/f92/13_table-1.png" height="335" title="13_Table 1.png"><br> <img width="717" alt="13_Figure 1. Acute GVHD in different.png" src="/upload/medialibrary/50d/13_figure-1.-acute-gvhd-in-different.png" height="426" title="13_Figure 1. Acute GVHD in different.png"> <h2>Figure 1. Acute GVHD in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis</h2> <br> <img width="717" alt="13_Figure 2. Relapse rate.png" src="/upload/medialibrary/642/13_figure-2.-relapse-rate.png" height="431" title="13_Figure 2. Relapse rate.png"> <h2>Figure 2. Relapse rate in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis</h2> <img width="717" alt="13_Figure 3. Overall survival.png" src="/upload/medialibrary/b45/13_figure-3.-overall-survival.png" height="431" title="13_Figure 3. Overall survival.png"> <h2>Figure 3. Overall survival in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis</h2>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3498) "
Introduction
Allogeneic bone marrow transplantation (allo-BMT) with high-dose posttransplant cyclophosphamide (PT-CY) to promote graft-host tolerance has become an alternative for standard immunosuppression. But sometimes unjustified toxicity expectations in aged patients are the main limiting factor of allo-HSCT for this group. Here we report our data about an influence of age on allo-HSCT results in leukemia patients in CR with PT-CY and ATG as GVHD prophylaxis.
Patients and methods
Forty patients with acute leukemia in CR transplanted in NRCH from mismatched unrelated donor were included in this study. All patient characteristics are listed in Table 1. All the patients received ATG at a dose 40 mg/kg from day -4 to day -1; PT-CY at dose 50 mg/kg daily at day +3,+4; Cyclosporine A 3 mg/kg from day -1 and MMF 3000 mg b.i.d from day +5. Kaplan-Meier estimator was used to determine overall survival, probability of aGVHD and relapse. The log-rank test was used to compare differences between the two groups. P-value less than 0.05 was considered statistically significant.
Results
Acute GVHD rates in 50+ y.o. group are significantly higher (Fig. 1) than in younger patients (66.7% vs 25% vs 12.5%, p=0.0044). It can be explained by thymus function and use of MAC conditioning regimens in the last patient group. Despite that fact due to low relapse rate (Fig. 2) overall survival (Fig. 3) in 50+ y.o. patients looks comparable with younger patients (66.7% vs 65.6% vs 58.9% for 40-49 y.o., 50+ and 20-39 y.o. respectively).
Conclusion
Allo-HSCT still makes sense in 50+ y.o. patients, since the results are not worse than in younger patients. Usage of PT-CY and ATG as GVHD prophylaxis seems to be safe and effective approach even for aged leukemia patients.
Disclosures
No relevant conflicts of interest to declare.
Keywords
GVHD, PT-Cy, age, acute leukemia, ATG.
Table 1. Patients characteristics


Figure 1. Acute GVHD in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis

Figure 2. Relapse rate in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis

Figure 3. Overall survival in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20395" ["VALUE"]=> string(166) "Age affects GVHD rate but not overall survival in leukemia patients with posttransplant cyclophosphamide (PT-CY) and anti-thymocyte globulin (ATG) as GVHD prophylaxis" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(166) "Age affects GVHD rate but not overall survival in leukemia patients with posttransplant cyclophosphamide (PT-CY) and anti-thymocyte globulin (ATG) as GVHD prophylaxis" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20757" ["VALUE"]=> string(4) "1393" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1393" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20758" ["VALUE"]=> string(4) "1394" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1394" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20392" ["VALUE"]=> array(2) { ["TEXT"]=> string(266) "Mikhail Y. Drokov, Larisa A. Kuzmina, Natalia N. Popova, Ekaterina D. Mikhaltsova, Vera A. Vasilyeva, Olga M. Koroleva, Darya S. Dubnyak, Anna A. Sidorova, Ekaterina V. Usikova, Zoya V. Konova, Anna A. Dmitrova, Elena N. Parovichnikova, Valery G. Savchenko<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(260) "Mikhail Y. Drokov, Larisa A. Kuzmina, Natalia N. Popova, Ekaterina D. Mikhaltsova, Vera A. Vasilyeva, Olga M. Koroleva, Darya S. Dubnyak, Anna A. Sidorova, Ekaterina V. Usikova, Zoya V. Konova, Anna A. Dmitrova, Elena N. Parovichnikova, Valery G. Savchenko" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(260) "Mikhail Y. Drokov, Larisa A. Kuzmina, Natalia N. Popova, Ekaterina D. Mikhaltsova, Vera A. Vasilyeva, Olga M. Koroleva, Darya S. Dubnyak, Anna A. Sidorova, Ekaterina V. Usikova, Zoya V. Konova, Anna A. Dmitrova, Elena N. Parovichnikova, Valery G. Savchenko
" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20394" ["VALUE"]=> array(2) { ["TEXT"]=> string(4080) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic bone marrow transplantation (allo-BMT) with high-dose posttransplant cyclophosphamide (PT-CY) to promote graft-host tolerance has become an alternative for standard immunosuppression. But sometimes unjustified toxicity expectations in aged patients are the main limiting factor of allo-HSCT for this group. Here we report our data about an influence of age on allo-HSCT results in leukemia patients in CR with PT-CY and ATG as GVHD prophylaxis. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Forty patients with acute leukemia in CR transplanted in NRCH from mismatched unrelated donor were included in this study. All patient characteristics are listed in Table 1. All the patients received ATG at a dose 40 mg/kg from day -4 to day -1; PT-CY at dose 50 mg/kg daily at day +3,+4; Cyclosporine A 3 mg/kg from day -1 and MMF 3000 mg b.i.d from day +5. Kaplan-Meier estimator was used to determine overall survival, probability of aGVHD and relapse. The log-rank test was used to compare differences between the two groups. P-value less than 0.05 was considered statistically significant. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Acute GVHD rates in 50+ y.o. group are significantly higher (Fig. 1) than in younger patients (66.7% vs 25% vs 12.5%, p=0.0044). It can be explained by thymus function and use of MAC conditioning regimens in the last patient group. Despite that fact due to low relapse rate (Fig. 2) overall survival (Fig. 3) in 50+ y.o. patients looks comparable with younger patients (66.7% vs 65.6% vs 58.9% for 40-49 y.o., 50+ and 20-39 y.o. respectively). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Allo-HSCT still makes sense in 50+ y.o. patients, since the results are not worse than in younger patients. Usage of PT-CY and ATG as GVHD prophylaxis seems to be safe and effective approach even for aged leukemia patients. </p> <h2 style="text-align: justify;">Disclosures</h2> <p style="text-align: justify;"> No relevant conflicts of interest to declare. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> GVHD, PT-Cy, age, acute leukemia, ATG.<br> </p> <h2 style="text-align: justify;"> Table 1. Patients characteristics<br> </h2> <img width="787" alt="13_Table 1.png" src="/upload/medialibrary/f92/13_table-1.png" height="335" title="13_Table 1.png"><br> <img width="717" alt="13_Figure 1. Acute GVHD in different.png" src="/upload/medialibrary/50d/13_figure-1.-acute-gvhd-in-different.png" height="426" title="13_Figure 1. Acute GVHD in different.png"> <h2>Figure 1. Acute GVHD in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis</h2> <br> <img width="717" alt="13_Figure 2. Relapse rate.png" src="/upload/medialibrary/642/13_figure-2.-relapse-rate.png" height="431" title="13_Figure 2. Relapse rate.png"> <h2>Figure 2. Relapse rate in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis</h2> <img width="717" alt="13_Figure 3. Overall survival.png" src="/upload/medialibrary/b45/13_figure-3.-overall-survival.png" height="431" title="13_Figure 3. Overall survival.png"> <h2>Figure 3. Overall survival in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis</h2>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3498) "
Introduction
Allogeneic bone marrow transplantation (allo-BMT) with high-dose posttransplant cyclophosphamide (PT-CY) to promote graft-host tolerance has become an alternative for standard immunosuppression. But sometimes unjustified toxicity expectations in aged patients are the main limiting factor of allo-HSCT for this group. Here we report our data about an influence of age on allo-HSCT results in leukemia patients in CR with PT-CY and ATG as GVHD prophylaxis.
Patients and methods
Forty patients with acute leukemia in CR transplanted in NRCH from mismatched unrelated donor were included in this study. All patient characteristics are listed in Table 1. All the patients received ATG at a dose 40 mg/kg from day -4 to day -1; PT-CY at dose 50 mg/kg daily at day +3,+4; Cyclosporine A 3 mg/kg from day -1 and MMF 3000 mg b.i.d from day +5. Kaplan-Meier estimator was used to determine overall survival, probability of aGVHD and relapse. The log-rank test was used to compare differences between the two groups. P-value less than 0.05 was considered statistically significant.
Results
Acute GVHD rates in 50+ y.o. group are significantly higher (Fig. 1) than in younger patients (66.7% vs 25% vs 12.5%, p=0.0044). It can be explained by thymus function and use of MAC conditioning regimens in the last patient group. Despite that fact due to low relapse rate (Fig. 2) overall survival (Fig. 3) in 50+ y.o. patients looks comparable with younger patients (66.7% vs 65.6% vs 58.9% for 40-49 y.o., 50+ and 20-39 y.o. respectively).
Conclusion
Allo-HSCT still makes sense in 50+ y.o. patients, since the results are not worse than in younger patients. Usage of PT-CY and ATG as GVHD prophylaxis seems to be safe and effective approach even for aged leukemia patients.
Disclosures
No relevant conflicts of interest to declare.
Keywords
GVHD, PT-Cy, age, acute leukemia, ATG.
Table 1. Patients characteristics


Figure 1. Acute GVHD in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis

Figure 2. Relapse rate in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis

Figure 3. Overall survival in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3498) "Introduction
Allogeneic bone marrow transplantation (allo-BMT) with high-dose posttransplant cyclophosphamide (PT-CY) to promote graft-host tolerance has become an alternative for standard immunosuppression. But sometimes unjustified toxicity expectations in aged patients are the main limiting factor of allo-HSCT for this group. Here we report our data about an influence of age on allo-HSCT results in leukemia patients in CR with PT-CY and ATG as GVHD prophylaxis.
Patients and methods
Forty patients with acute leukemia in CR transplanted in NRCH from mismatched unrelated donor were included in this study. All patient characteristics are listed in Table 1. All the patients received ATG at a dose 40 mg/kg from day -4 to day -1; PT-CY at dose 50 mg/kg daily at day +3,+4; Cyclosporine A 3 mg/kg from day -1 and MMF 3000 mg b.i.d from day +5. Kaplan-Meier estimator was used to determine overall survival, probability of aGVHD and relapse. The log-rank test was used to compare differences between the two groups. P-value less than 0.05 was considered statistically significant.
Results
Acute GVHD rates in 50+ y.o. group are significantly higher (Fig. 1) than in younger patients (66.7% vs 25% vs 12.5%, p=0.0044). It can be explained by thymus function and use of MAC conditioning regimens in the last patient group. Despite that fact due to low relapse rate (Fig. 2) overall survival (Fig. 3) in 50+ y.o. patients looks comparable with younger patients (66.7% vs 65.6% vs 58.9% for 40-49 y.o., 50+ and 20-39 y.o. respectively).
Conclusion
Allo-HSCT still makes sense in 50+ y.o. patients, since the results are not worse than in younger patients. Usage of PT-CY and ATG as GVHD prophylaxis seems to be safe and effective approach even for aged leukemia patients.
Disclosures
No relevant conflicts of interest to declare.
Keywords
GVHD, PT-Cy, age, acute leukemia, ATG.
Table 1. Patients characteristics


Figure 1. Acute GVHD in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis

Figure 2. Relapse rate in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis

Figure 3. Overall survival in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20395" ["VALUE"]=> string(166) "Age affects GVHD rate but not overall survival in leukemia patients with posttransplant cyclophosphamide (PT-CY) and anti-thymocyte globulin (ATG) as GVHD prophylaxis" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(166) "Age affects GVHD rate but not overall survival in leukemia patients with posttransplant cyclophosphamide (PT-CY) and anti-thymocyte globulin (ATG) as GVHD prophylaxis" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(166) "Age affects GVHD rate but not overall survival in leukemia patients with posttransplant cyclophosphamide (PT-CY) and anti-thymocyte globulin (ATG) as GVHD prophylaxis" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20393" ["VALUE"]=> array(2) { ["TEXT"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20389" ["VALUE"]=> array(2) { ["TEXT"]=> string(443) "Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Вера А. Васильева, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Елена Н. Паровичникова, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(443) "Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Вера А. Васильева, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Елена Н. Паровичникова, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(443) "Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Вера А. Васильева, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Елена Н. Паровичникова, Валерий Г. Савченко" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20391" ["VALUE"]=> array(2) { ["TEXT"]=> string(8456) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Трансплантация аллогенного костного мозга (алло-ТГСК) с использованием высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) в качестве индуктора толерантности стала хорошей альтернативой стандартной иммуносупрессии. Часто необоснованные ожидания токсичности, особенно у пациентов старше 50, становятся препятствием для проведения алло-ТГСК у данных больных. Здесь нами представлены данные о влиянии возраста пациентов с острыми лейкозами в ПР на результаты алло-ТГСК с ПТ-ЦФ и АТГ в качестве профилактики РТПХ. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Сорок пациентов с острыми лейкозами были трансплантированы в ПР в НМИЦ гематологии МЗ РФ от неродственного частично-совместимого донора. Характеристика пациентов представлена в Таблице 1. Все пациенты в качестве профилактики РТПХ получали: АТГ в суммарной дозе 40 мг/кг с -4 по -1 день; ПТ-ЦФ в дозе 50 мг/кг/сут на +3, +4 день; Циклоспорин А в дозе 3 мг/кг/сут с -1 дня; Микофенолата мофетил 3000 мг/сут с +5 дня. Метод Каплан-Мейера был использован для оценки общей выживаемости, вероятности развития рецидива, острой РТПХ. Логранк тест был использован для сравнения различий между двумя группами. Р-значение ниже 0.05 считалось значимым. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Острая РТПХ в группе пациентов старше 50 лет была значимо выше, чем в группах в возрасте 40-49 и 20-39 лет (66,7% vs 25% vs 12,5%, p=0.0044) (Рис. 1). Вероятно, это может быть связано с резидуальной функцией тимуса, а также более частым использованием миелоаблативных режимов у молодых больных (младше 50 лет). Однако, несмотря на эти различия, высокая частота развития РТПХ свидетельствует о более низкой частоте развития рецидивов (Рис. 2), что, в свою очередь, ведет к отсутствию различий общей выживаемостью между группами (Рис. 3) – 56,1%, 66,7% и 65,6% для группы 20-39, 40-49 и 50+ соответственно. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Алло-ТГСК у пациентов в возрасте старше 50 лет имеет свои особенности, однако эффективность данной процедуры (общая выживаемость пациентов) ничуть не меньше, чем у более молодых пациентов. Таким образом, использование ПТ-ЦФ и АТГ у пациентов старше 50 лет вполне оправдано и достаточно эффективно. </p> <h2 style="text-align: justify;">Конфликт интересов</h2> <p style="text-align: justify;"> Отсутствует конфликт интересов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> РТПХ, посттрансплантационный циклофосфамид, возраст, острый лейкоз, АТГ. </p> <h2 style="text-align: justify;"> Таблица 1. Характеристика пациентов<br> </h2> <p style="text-align: justify;"> <img width="783" alt="13_Таблица 1. Характеристика пациентов.png" src="/upload/medialibrary/da0/13_tablitsa-1.-kharakteristika-patsientov.png" height="329" title="13_Таблица 1. Характеристика пациентов.png"><br> </p> <p style="text-align: justify;"> <img width="717" alt="13_Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами.png" src="/upload/medialibrary/87b/13_risunok-1.-veroyatnost-razvitiya-ostroy-rtpkh-v-razlichnykh-vozrastnykh-gruppakh-u-patsientov-s-ostrymi-leykozami.png" height="425" title="13_Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами.png"><br> </p> <h2 style="text-align: justify;"> Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ</h2> <p style="text-align: justify;"> <img width="717" alt="13_Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами.png" src="/upload/medialibrary/9d2/13_risunok-2.-veroyatnost-razvitiya-retsidiva-v-razlichnykh-vozrastnykh-gruppakh-u-patsientov-s-ostrymi-leykozami.png" height="426" title="13_Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами.png"><br> </p> <h2 style="text-align: justify;"> Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ</h2> <img width="717" alt="13_Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после.png" src="/upload/medialibrary/ea1/13_risunok-3.-obshchaya-vyzhivaemost-v-razlichnykh-vozrastnykh-gruppakh-u-patsientov-s-ostrymi-leykozami-posle.png" height="426" title="13_Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после.png"> <h2>Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ</h2>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7788) "Введение
Трансплантация аллогенного костного мозга (алло-ТГСК) с использованием высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) в качестве индуктора толерантности стала хорошей альтернативой стандартной иммуносупрессии. Часто необоснованные ожидания токсичности, особенно у пациентов старше 50, становятся препятствием для проведения алло-ТГСК у данных больных. Здесь нами представлены данные о влиянии возраста пациентов с острыми лейкозами в ПР на результаты алло-ТГСК с ПТ-ЦФ и АТГ в качестве профилактики РТПХ.
Пациенты и методы
Сорок пациентов с острыми лейкозами были трансплантированы в ПР в НМИЦ гематологии МЗ РФ от неродственного частично-совместимого донора. Характеристика пациентов представлена в Таблице 1. Все пациенты в качестве профилактики РТПХ получали: АТГ в суммарной дозе 40 мг/кг с -4 по -1 день; ПТ-ЦФ в дозе 50 мг/кг/сут на +3, +4 день; Циклоспорин А в дозе 3 мг/кг/сут с -1 дня; Микофенолата мофетил 3000 мг/сут с +5 дня. Метод Каплан-Мейера был использован для оценки общей выживаемости, вероятности развития рецидива, острой РТПХ. Логранк тест был использован для сравнения различий между двумя группами. Р-значение ниже 0.05 считалось значимым.
Результаты
Острая РТПХ в группе пациентов старше 50 лет была значимо выше, чем в группах в возрасте 40-49 и 20-39 лет (66,7% vs 25% vs 12,5%, p=0.0044) (Рис. 1). Вероятно, это может быть связано с резидуальной функцией тимуса, а также более частым использованием миелоаблативных режимов у молодых больных (младше 50 лет). Однако, несмотря на эти различия, высокая частота развития РТПХ свидетельствует о более низкой частоте развития рецидивов (Рис. 2), что, в свою очередь, ведет к отсутствию различий общей выживаемостью между группами (Рис. 3) – 56,1%, 66,7% и 65,6% для группы 20-39, 40-49 и 50+ соответственно.
Заключение
Алло-ТГСК у пациентов в возрасте старше 50 лет имеет свои особенности, однако эффективность данной процедуры (общая выживаемость пациентов) ничуть не меньше, чем у более молодых пациентов. Таким образом, использование ПТ-ЦФ и АТГ у пациентов старше 50 лет вполне оправдано и достаточно эффективно.
Конфликт интересов
Отсутствует конфликт интересов.
Ключевые слова
РТПХ, посттрансплантационный циклофосфамид, возраст, острый лейкоз, АТГ.
Таблица 1. Характеристика пациентов


Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ

Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ

Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(7788) "Введение
Трансплантация аллогенного костного мозга (алло-ТГСК) с использованием высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) в качестве индуктора толерантности стала хорошей альтернативой стандартной иммуносупрессии. Часто необоснованные ожидания токсичности, особенно у пациентов старше 50, становятся препятствием для проведения алло-ТГСК у данных больных. Здесь нами представлены данные о влиянии возраста пациентов с острыми лейкозами в ПР на результаты алло-ТГСК с ПТ-ЦФ и АТГ в качестве профилактики РТПХ.
Пациенты и методы
Сорок пациентов с острыми лейкозами были трансплантированы в ПР в НМИЦ гематологии МЗ РФ от неродственного частично-совместимого донора. Характеристика пациентов представлена в Таблице 1. Все пациенты в качестве профилактики РТПХ получали: АТГ в суммарной дозе 40 мг/кг с -4 по -1 день; ПТ-ЦФ в дозе 50 мг/кг/сут на +3, +4 день; Циклоспорин А в дозе 3 мг/кг/сут с -1 дня; Микофенолата мофетил 3000 мг/сут с +5 дня. Метод Каплан-Мейера был использован для оценки общей выживаемости, вероятности развития рецидива, острой РТПХ. Логранк тест был использован для сравнения различий между двумя группами. Р-значение ниже 0.05 считалось значимым.
Результаты
Острая РТПХ в группе пациентов старше 50 лет была значимо выше, чем в группах в возрасте 40-49 и 20-39 лет (66,7% vs 25% vs 12,5%, p=0.0044) (Рис. 1). Вероятно, это может быть связано с резидуальной функцией тимуса, а также более частым использованием миелоаблативных режимов у молодых больных (младше 50 лет). Однако, несмотря на эти различия, высокая частота развития РТПХ свидетельствует о более низкой частоте развития рецидивов (Рис. 2), что, в свою очередь, ведет к отсутствию различий общей выживаемостью между группами (Рис. 3) – 56,1%, 66,7% и 65,6% для группы 20-39, 40-49 и 50+ соответственно.
Заключение
Алло-ТГСК у пациентов в возрасте старше 50 лет имеет свои особенности, однако эффективность данной процедуры (общая выживаемость пациентов) ничуть не меньше, чем у более молодых пациентов. Таким образом, использование ПТ-ЦФ и АТГ у пациентов старше 50 лет вполне оправдано и достаточно эффективно.
Конфликт интересов
Отсутствует конфликт интересов.
Ключевые слова
РТПХ, посттрансплантационный циклофосфамид, возраст, острый лейкоз, АТГ.
Таблица 1. Характеристика пациентов


Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ

Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ

Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20390" ["VALUE"]=> array(2) { ["TEXT"]=> string(86) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(86) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(86) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва" } } } [14]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1553" ["~ID"]=> string(4) "1553" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(214) "Влияние показателей минимальной остаточной болезни перед аллогенной ТГСК на долгосрочные результаты пациентов ОМЛ" ["~NAME"]=> string(214) "Влияние показателей минимальной остаточной болезни перед аллогенной ТГСК на долгосрочные результаты пациентов ОМЛ" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:25:00" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:25:00" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vliyanie-pokazateley-minimalnoy-ostatochnoy-bolezni-pered-allogennoy-tgsk-na-dolgosrochnye-rezultaty/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vliyanie-pokazateley-minimalnoy-ostatochnoy-bolezni-pered-allogennoy-tgsk-na-dolgosrochnye-rezultaty/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "vliyanie-pokazateley-minimalnoy-ostatochnoy-bolezni-pered-allogennoy-tgsk-na-dolgosrochnye-rezultaty" ["~CODE"]=> string(100) "vliyanie-pokazateley-minimalnoy-ostatochnoy-bolezni-pered-allogennoy-tgsk-na-dolgosrochnye-rezultaty" ["EXTERNAL_ID"]=> string(4) "1553" ["~EXTERNAL_ID"]=> string(4) "1553" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(214) "Влияние показателей минимальной остаточной болезни перед аллогенной ТГСК на долгосрочные результаты пациентов ОМЛ" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(334) "Влияние показателей минимальной остаточной болезни перед аллогенной ТГСК на долгосрочные результаты пациентов ОМЛSignificance of minimal residual disease before allogeneic hematopoietic cell transplantation for acute myeloid leukemia" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(7752) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) является эффективным методом лечения острого миелобластного лейкоза (ОМЛ). Развитие рецидива после алло-ТГСК является наиболее частой причиной неудач лечения. Однако, проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания дает возможность определения минимальной остаточной болезни (МОБ) в ремиссии (ПР) ОМЛ с целью определения прогноза и выбора адекватной терапии. </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Оценить влияние наличия МОБ у пациентов ОМЛ перед алло-ТГСК на результаты лечения. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В исследование включено 195 пациентов за период 2012-16 гг. Медиана возраста составила 36 (18-70) лет. Медиана наблюдения составила 23 (23-467) мес. Статус заболевания перед алло-ТГСК: ПР1 – 148 (76%) пациентов, ПР2 – 47 (24%) пациентов. Согласно молекулярно-генетической классификации к группе низкого риска относились 31 (17%) пациент, среднего риска – 119 (59%), высокого риска – 45 (24%) пациентов. МОБ не определялась (МОБ-) у 155 (80%) пациентов. Положительный результат МОБ (МОБ+) перед алло-ТГСК был у 40 (20%) человек, из них мутации t(8;21)(q22;q22); RUNX1-RUNX1T1 – 3 пациента, inv(16)(p13.1q22); CBFB-MYH11 – 2, t(15;17) (q22;q21); PML-RARа – 1, t(9;11)(p22;q23); MLLT3-KTM2A – 2, NPM1 – 2, FLT3-ITD – 4; гиперэкспрессия: WT1 – 8 , EVI1 – 1 пациент; МОБ(+) методом проточной цитометрии у 18 пациентов, медиана 0,4% (0,13-3,9). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> При однофакторном анализе безрецидивная выживаемость (БРВ) после алло-ТГСК в ПР1 МОБ- составила 67% (95%ДИ 57-77), а при МОБ+ – 54% (95%ДИ 36-72) р=.03, тогда как у пациентов в ПР2 при МОБ- составила 57% (95%ДИ 41-73), и соответственно при МОБ(+) – 33% (95%ДИ 1-88) р=нд. Частота рецидивов (ЧР) в ПР1 МОБ- Д22%(95%ДИ 13-32), а при МОБ+ – 36%(95%ДИ 19-53), тогда как в ПР2 МОБ- 17% (95%ДИ 7-32), а при МОБ+ 66% (95%ДИ 15-91). При миелоаблативном кондиционировании БРВ и ЧР после алло-ТГСК в ПР1 не зависели от уровня МОБ: при МОБ- 70% (95%ДИ 59-81) и при МОБ+ 64% (95%ДИ 36-92) и соответственно 17% (95%ДИ 7-39) и 23% (95%ДИ 12-35). Тогда как при проведении кондиционирования редуцированной интенсивности, БРВ была выше, а ЧР ниже у пациентов МОБ-: 67% (95%ДИ 54-80) против 50% (95%ДИ 27-77) р=.03 и 50% (95%ДИ 25-70) и 23% (95%ДИ 12-35) р<.000. МОБ+ негативно влияла на БРВ и ЧР при использовании костного мозга в качестве трансплантата: МОБ- 76% (95%ДИ 57-87) по сравнению с МОБ+ 53% (95%ДИ 28-78) и 47% (95%ДИ 20-70) по сравнению с 24% (95%ДИ 8-44) р=.03,а при алло-ТГСК периферической крови разница БРВ и ЧР была не достоверна: 66% (95%ДИ 53-79) против 57% (95%ДИ 32-83) и 23% (95%ДИ 12-35) против 25% (95%ДИ 7-49). Цитогенетическая группа риска (средний и высокий) и донор (родственный и неродственный) не влияли на БРВ и ЧР: 74% (95%ДИ 61-87) против 63% (95%ДИ 39-85) и 47% (95%ДИ 22-72) против 38% (95%ДИ 5-71), 16% (95%ДИ 6-30) против 19% (95%ДИ 4-41) и 59% (95%ДИ 25-75) против 63% (95%ДИ 18-89); 68% (95%ДИ 56-80) против 57% (95%ДИ 46-78) и 65% (95%ДИ 45-84) против 42% (95%ДИ 5-79), 20% (95%ДИ 10-32) против 29% (95%ДИ 11-49) и 29% (95%ДИ 12-48) против 58% (95%ДИ 10-88). При отсутствии хронической РТПХ (хРТПХ) БРВ и ЧР были лучше у пациентов МОБ- 64% (95%ДИ 45-83) против 52% (95%ДИ 32-72) р=0.01 и 34% (95%ДИ 15-54) против 44% (95%ДИ 23-63) р=.03. У пациентов с хРТПХ разница в обеих группах была недостоверна: 70% (95%ДИ 57-83) против 80% (95%ДИ45-99) и 17% (95%ДИ 7-29) против 20% (95%ДИ1-62). При проведении многофакторного анализа влияние на ЧР оказал статус заболевания (МОБ+/МОБ-) (ОР, 2.3, 95%ДИ 1.1-4.9, р=.03) и наличие хРТПХ (да/нет) (ОР, 0.3, 95%ДИ 0.2-1.0, р=.05). БРВ была хуже при МОБ+ (ОР, 1.8, 95%ДИ 1.0-3.5, р=.05). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Необходимо проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания для возможности мониторинга МОБ в ремиссии ОМЛ. При ОМЛ наличие МОБ негативно влияет на БРВ и ЧР после алло-ТГСК. Статус МОБ+ перед алло-ТГСК является показанием для интенсификации режима кондиционирования. </p> <h2 style="text-align: justify;">Комментарии</h2> <p style="text-align: justify;"> Авторы заявляют об отсутствии скрытого конфликта интересов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый миелоидный лейкоз, минимальная остаточная болезнь, аллогенная трансплантация гемопоэтических стволовых клеток. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(214) "Влияние показателей минимальной остаточной болезни перед аллогенной ТГСК на долгосрочные результаты пациентов ОМЛ" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(214) "Влияние показателей минимальной остаточной болезни перед аллогенной ТГСК на долгосрочные результаты пациентов ОМЛ" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(214) "Влияние показателей минимальной остаточной болезни перед аллогенной ТГСК на долгосрочные результаты пациентов ОМЛ" ["SECTION_META_TITLE"]=> string(214) "Влияние показателей минимальной остаточной болезни перед аллогенной ТГСК на долгосрочные результаты пациентов ОМЛ" ["SECTION_META_KEYWORDS"]=> string(214) "Влияние показателей минимальной остаточной болезни перед аллогенной ТГСК на долгосрочные результаты пациентов ОМЛ" ["SECTION_META_DESCRIPTION"]=> string(214) "Влияние показателей минимальной остаточной болезни перед аллогенной ТГСК на долгосрочные результаты пациентов ОМЛ" ["SECTION_PICTURE_FILE_ALT"]=> string(214) "Влияние показателей минимальной остаточной болезни перед аллогенной ТГСК на долгосрочные результаты пациентов ОМЛ" ["SECTION_PICTURE_FILE_TITLE"]=> string(214) "Влияние показателей минимальной остаточной болезни перед аллогенной ТГСК на долгосрочные результаты пациентов ОМЛ" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "vliyanie-pokazateley-minimalnoy-ostatochnoy-bolezni-pered-allogennoy-tgsk-na-dolgosrochnye-rezultaty" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(214) "Влияние показателей минимальной остаточной болезни перед аллогенной ТГСК на долгосрочные результаты пациентов ОМЛ" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(214) "Влияние показателей минимальной остаточной болезни перед аллогенной ТГСК на долгосрочные результаты пациентов ОМЛ" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vliyanie-pokazateley-minimalnoy-ostatochnoy-bolezni-pered-allogennoy-tgsk-na-dolgosrochnye-rezultaty" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "vliyanie-pokazateley-minimalnoy-ostatochnoy-bolezni-pered-allogennoy-tgsk-na-dolgosrochnye-rezultaty" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vliyanie-pokazateley-minimalnoy-ostatochnoy-bolezni-pered-allogennoy-tgsk-na-dolgosrochnye-rezultaty" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20301" ["VALUE"]=> array(2) { ["TEXT"]=> string(717) "Сергей Н. Бондаренко <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Анна Г. Смирнова <sup>1</sup>, Ирина А. Самородова <sup>1</sup>, Ольга С. Успенская <sup>2</sup>, Елена В. Бабенко <sup>1</sup>, Ильдар М. Бархатов <sup>1</sup>, Татьяна Л. Гиндина <sup>1</sup>, Николай Н. Мамаев <sup>1</sup>, Александр Д. Кулагин <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(573) "Сергей Н. Бондаренко 1, Иван С. Моисеев 1, Елена И. Дарская 1, Анна Г. Смирнова 1, Ирина А. Самородова 1, Ольга С. Успенская 2, Елена В. Бабенко 1, Ильдар М. Бархатов 1, Татьяна Л. Гиндина 1, Николай Н. Мамаев 1, Александр Д. Кулагин 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20302" ["VALUE"]=> array(2) { ["TEXT"]=> string(316) "<sup>1</sup> НИИ ДОГиТ им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург<br> <sup>2</sup> Ленинградская областная клиническая больница, Санкт-Петербург<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(280) "1 НИИ ДОГиТ им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург2 Ленинградская областная клиническая больница, Санкт-Петербург
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20350" ["VALUE"]=> array(2) { ["TEXT"]=> string(7752) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) является эффективным методом лечения острого миелобластного лейкоза (ОМЛ). Развитие рецидива после алло-ТГСК является наиболее частой причиной неудач лечения. Однако, проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания дает возможность определения минимальной остаточной болезни (МОБ) в ремиссии (ПР) ОМЛ с целью определения прогноза и выбора адекватной терапии. </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Оценить влияние наличия МОБ у пациентов ОМЛ перед алло-ТГСК на результаты лечения. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В исследование включено 195 пациентов за период 2012-16 гг. Медиана возраста составила 36 (18-70) лет. Медиана наблюдения составила 23 (23-467) мес. Статус заболевания перед алло-ТГСК: ПР1 – 148 (76%) пациентов, ПР2 – 47 (24%) пациентов. Согласно молекулярно-генетической классификации к группе низкого риска относились 31 (17%) пациент, среднего риска – 119 (59%), высокого риска – 45 (24%) пациентов. МОБ не определялась (МОБ-) у 155 (80%) пациентов. Положительный результат МОБ (МОБ+) перед алло-ТГСК был у 40 (20%) человек, из них мутации t(8;21)(q22;q22); RUNX1-RUNX1T1 – 3 пациента, inv(16)(p13.1q22); CBFB-MYH11 – 2, t(15;17) (q22;q21); PML-RARа – 1, t(9;11)(p22;q23); MLLT3-KTM2A – 2, NPM1 – 2, FLT3-ITD – 4; гиперэкспрессия: WT1 – 8 , EVI1 – 1 пациент; МОБ(+) методом проточной цитометрии у 18 пациентов, медиана 0,4% (0,13-3,9). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> При однофакторном анализе безрецидивная выживаемость (БРВ) после алло-ТГСК в ПР1 МОБ- составила 67% (95%ДИ 57-77), а при МОБ+ – 54% (95%ДИ 36-72) р=.03, тогда как у пациентов в ПР2 при МОБ- составила 57% (95%ДИ 41-73), и соответственно при МОБ(+) – 33% (95%ДИ 1-88) р=нд. Частота рецидивов (ЧР) в ПР1 МОБ- Д22%(95%ДИ 13-32), а при МОБ+ – 36%(95%ДИ 19-53), тогда как в ПР2 МОБ- 17% (95%ДИ 7-32), а при МОБ+ 66% (95%ДИ 15-91). При миелоаблативном кондиционировании БРВ и ЧР после алло-ТГСК в ПР1 не зависели от уровня МОБ: при МОБ- 70% (95%ДИ 59-81) и при МОБ+ 64% (95%ДИ 36-92) и соответственно 17% (95%ДИ 7-39) и 23% (95%ДИ 12-35). Тогда как при проведении кондиционирования редуцированной интенсивности, БРВ была выше, а ЧР ниже у пациентов МОБ-: 67% (95%ДИ 54-80) против 50% (95%ДИ 27-77) р=.03 и 50% (95%ДИ 25-70) и 23% (95%ДИ 12-35) р<.000. МОБ+ негативно влияла на БРВ и ЧР при использовании костного мозга в качестве трансплантата: МОБ- 76% (95%ДИ 57-87) по сравнению с МОБ+ 53% (95%ДИ 28-78) и 47% (95%ДИ 20-70) по сравнению с 24% (95%ДИ 8-44) р=.03,а при алло-ТГСК периферической крови разница БРВ и ЧР была не достоверна: 66% (95%ДИ 53-79) против 57% (95%ДИ 32-83) и 23% (95%ДИ 12-35) против 25% (95%ДИ 7-49). Цитогенетическая группа риска (средний и высокий) и донор (родственный и неродственный) не влияли на БРВ и ЧР: 74% (95%ДИ 61-87) против 63% (95%ДИ 39-85) и 47% (95%ДИ 22-72) против 38% (95%ДИ 5-71), 16% (95%ДИ 6-30) против 19% (95%ДИ 4-41) и 59% (95%ДИ 25-75) против 63% (95%ДИ 18-89); 68% (95%ДИ 56-80) против 57% (95%ДИ 46-78) и 65% (95%ДИ 45-84) против 42% (95%ДИ 5-79), 20% (95%ДИ 10-32) против 29% (95%ДИ 11-49) и 29% (95%ДИ 12-48) против 58% (95%ДИ 10-88). При отсутствии хронической РТПХ (хРТПХ) БРВ и ЧР были лучше у пациентов МОБ- 64% (95%ДИ 45-83) против 52% (95%ДИ 32-72) р=0.01 и 34% (95%ДИ 15-54) против 44% (95%ДИ 23-63) р=.03. У пациентов с хРТПХ разница в обеих группах была недостоверна: 70% (95%ДИ 57-83) против 80% (95%ДИ45-99) и 17% (95%ДИ 7-29) против 20% (95%ДИ1-62). При проведении многофакторного анализа влияние на ЧР оказал статус заболевания (МОБ+/МОБ-) (ОР, 2.3, 95%ДИ 1.1-4.9, р=.03) и наличие хРТПХ (да/нет) (ОР, 0.3, 95%ДИ 0.2-1.0, р=.05). БРВ была хуже при МОБ+ (ОР, 1.8, 95%ДИ 1.0-3.5, р=.05). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Необходимо проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания для возможности мониторинга МОБ в ремиссии ОМЛ. При ОМЛ наличие МОБ негативно влияет на БРВ и ЧР после алло-ТГСК. Статус МОБ+ перед алло-ТГСК является показанием для интенсификации режима кондиционирования. </p> <h2 style="text-align: justify;">Комментарии</h2> <p style="text-align: justify;"> Авторы заявляют об отсутствии скрытого конфликта интересов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый миелоидный лейкоз, минимальная остаточная болезнь, аллогенная трансплантация гемопоэтических стволовых клеток. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7428) "
Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) является эффективным методом лечения острого миелобластного лейкоза (ОМЛ). Развитие рецидива после алло-ТГСК является наиболее частой причиной неудач лечения. Однако, проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания дает возможность определения минимальной остаточной болезни (МОБ) в ремиссии (ПР) ОМЛ с целью определения прогноза и выбора адекватной терапии.
Цель работы
Оценить влияние наличия МОБ у пациентов ОМЛ перед алло-ТГСК на результаты лечения.
Пациенты и методы
В исследование включено 195 пациентов за период 2012-16 гг. Медиана возраста составила 36 (18-70) лет. Медиана наблюдения составила 23 (23-467) мес. Статус заболевания перед алло-ТГСК: ПР1 – 148 (76%) пациентов, ПР2 – 47 (24%) пациентов. Согласно молекулярно-генетической классификации к группе низкого риска относились 31 (17%) пациент, среднего риска – 119 (59%), высокого риска – 45 (24%) пациентов. МОБ не определялась (МОБ-) у 155 (80%) пациентов. Положительный результат МОБ (МОБ+) перед алло-ТГСК был у 40 (20%) человек, из них мутации t(8;21)(q22;q22); RUNX1-RUNX1T1 – 3 пациента, inv(16)(p13.1q22); CBFB-MYH11 – 2, t(15;17) (q22;q21); PML-RARа – 1, t(9;11)(p22;q23); MLLT3-KTM2A – 2, NPM1 – 2, FLT3-ITD – 4; гиперэкспрессия: WT1 – 8 , EVI1 – 1 пациент; МОБ(+) методом проточной цитометрии у 18 пациентов, медиана 0,4% (0,13-3,9).
Результаты
При однофакторном анализе безрецидивная выживаемость (БРВ) после алло-ТГСК в ПР1 МОБ- составила 67% (95%ДИ 57-77), а при МОБ+ – 54% (95%ДИ 36-72) р=.03, тогда как у пациентов в ПР2 при МОБ- составила 57% (95%ДИ 41-73), и соответственно при МОБ(+) – 33% (95%ДИ 1-88) р=нд. Частота рецидивов (ЧР) в ПР1 МОБ- Д22%(95%ДИ 13-32), а при МОБ+ – 36%(95%ДИ 19-53), тогда как в ПР2 МОБ- 17% (95%ДИ 7-32), а при МОБ+ 66% (95%ДИ 15-91). При миелоаблативном кондиционировании БРВ и ЧР после алло-ТГСК в ПР1 не зависели от уровня МОБ: при МОБ- 70% (95%ДИ 59-81) и при МОБ+ 64% (95%ДИ 36-92) и соответственно 17% (95%ДИ 7-39) и 23% (95%ДИ 12-35). Тогда как при проведении кондиционирования редуцированной интенсивности, БРВ была выше, а ЧР ниже у пациентов МОБ-: 67% (95%ДИ 54-80) против 50% (95%ДИ 27-77) р=.03 и 50% (95%ДИ 25-70) и 23% (95%ДИ 12-35) р<.000. МОБ+ негативно влияла на БРВ и ЧР при использовании костного мозга в качестве трансплантата: МОБ- 76% (95%ДИ 57-87) по сравнению с МОБ+ 53% (95%ДИ 28-78) и 47% (95%ДИ 20-70) по сравнению с 24% (95%ДИ 8-44) р=.03,а при алло-ТГСК периферической крови разница БРВ и ЧР была не достоверна: 66% (95%ДИ 53-79) против 57% (95%ДИ 32-83) и 23% (95%ДИ 12-35) против 25% (95%ДИ 7-49). Цитогенетическая группа риска (средний и высокий) и донор (родственный и неродственный) не влияли на БРВ и ЧР: 74% (95%ДИ 61-87) против 63% (95%ДИ 39-85) и 47% (95%ДИ 22-72) против 38% (95%ДИ 5-71), 16% (95%ДИ 6-30) против 19% (95%ДИ 4-41) и 59% (95%ДИ 25-75) против 63% (95%ДИ 18-89); 68% (95%ДИ 56-80) против 57% (95%ДИ 46-78) и 65% (95%ДИ 45-84) против 42% (95%ДИ 5-79), 20% (95%ДИ 10-32) против 29% (95%ДИ 11-49) и 29% (95%ДИ 12-48) против 58% (95%ДИ 10-88). При отсутствии хронической РТПХ (хРТПХ) БРВ и ЧР были лучше у пациентов МОБ- 64% (95%ДИ 45-83) против 52% (95%ДИ 32-72) р=0.01 и 34% (95%ДИ 15-54) против 44% (95%ДИ 23-63) р=.03. У пациентов с хРТПХ разница в обеих группах была недостоверна: 70% (95%ДИ 57-83) против 80% (95%ДИ45-99) и 17% (95%ДИ 7-29) против 20% (95%ДИ1-62). При проведении многофакторного анализа влияние на ЧР оказал статус заболевания (МОБ+/МОБ-) (ОР, 2.3, 95%ДИ 1.1-4.9, р=.03) и наличие хРТПХ (да/нет) (ОР, 0.3, 95%ДИ 0.2-1.0, р=.05). БРВ была хуже при МОБ+ (ОР, 1.8, 95%ДИ 1.0-3.5, р=.05).
Заключение
Необходимо проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания для возможности мониторинга МОБ в ремиссии ОМЛ. При ОМЛ наличие МОБ негативно влияет на БРВ и ЧР после алло-ТГСК. Статус МОБ+ перед алло-ТГСК является показанием для интенсификации режима кондиционирования.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
Ключевые слова
Острый миелоидный лейкоз, минимальная остаточная болезнь, аллогенная трансплантация гемопоэтических стволовых клеток.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20303" ["VALUE"]=> array(2) { ["TEXT"]=> string(534) "Sergey N. Bondarenko <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Anna G. Smirnova <sup>1</sup>, Irina A. Samorodova <sup>1</sup>, Olga S. Uspenskaya <sup>2</sup>, Elena V. Babenko <sup>1</sup>, Ildar M. Barkhatov <sup>1</sup>, Tatyana L. Gindina <sup>1</sup>, Nikolay N. Mamaev <sup>1</sup>, Alexander D. Kulagin <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(390) "Sergey N. Bondarenko 1, Ivan S. Moiseev 1, Elena I. Darskaya 1, Anna G. Smirnova 1, Irina A. Samorodova 1, Olga S. Uspenskaya 2, Elena V. Babenko 1, Ildar M. Barkhatov 1, Tatyana L. Gindina 1, Nikolay N. Mamaev 1, Alexander D. Kulagin 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20304" ["VALUE"]=> array(2) { ["TEXT"]=> string(337) "<sup>1</sup> R. M. Gorbacheva Memorial Institute of Oncology, Hematology and Transplantation, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation<br> <sup>2</sup> Leningrad Regional Clinical Hospital, Hematology Department, St. Petersburg, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(301) "1 R. M. Gorbacheva Memorial Institute of Oncology, Hematology and Transplantation, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation2 Leningrad Regional Clinical Hospital, Hematology Department, St. Petersburg, Russian Federation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20351" ["VALUE"]=> array(2) { ["TEXT"]=> string(4172) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is an effective therapy for many patients with acute myeloid leukemia (AML). The relapse after allo-HSCT is the most common cause of treatment failure. However, multiparameter flow cytometry, cytogenetic and molecular studies in the onset of the disease makes it possible to detect the minimal residual disease (MRD) in AML remission in order to determine the prognosis and the therapy strategy. </p> <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> To evaluate the impact of MRD before allo-HSCT in patients with AML on the results of treatment. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> We analysed 195 consecutive patients with AML since 2012 to 2016. Median age was 36 (18-70) years. The median follow-up was 23 (23-467) months. Disease status before allo-HSCT: CR1 – 148 (76%), CR2 – 47 (24%) patients. Molecular and genetic low-risk group was defined in 31(17%), standard risk in 119 (59%) and 45 (24%) high-risk patients. MRD was not determined (MRD (-)) in 155 (80%) patients. A positive result of MRD (MRD (+)) before alloHSCT was in 40 (20%) patients, including mutations, gene overexpression and leukemia associated immunophenotypes. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Disease-free survival (DFS) after alloHSCT in CR1MRD(-) was 67% (95%CI 57-77), and in MRD(+) 54% (95%CI 36-72) (p=.03), whereas in patients with CR2MRD(-) 57% (95%CI 41-73) and CR2MRD(+) – 33% (95%CI 1-88) (p=ns). The relapse incidence (RI) in the CR1MRD(-) was 22% (95%CI 13-32), and in MRD(+) – 36% (95%CI 19-53), whereas in the CR2MRD(-) 17% (95%CI 7-32), and in MRD(+) 66% (95%CI 15-91). With myeloablative conditioning (MAC), the DFS and RI after allo-HSCT in CR1 did not depended on MRD: patients with MRD(-) 70% (95%CI 59-81) vs MRD(+) 64% (95%CI 36-92) and 17% (95%CI 7-39) vs 23% (95%CI 12-35) respectively. Whereas after reduced intensity conditioning (RIC), the DFC was higher, and the RI was lower in patients with MRD(-): 67% (95%CI 54-80) vs 50% (95%CI 27-77) (p=.03) and 50% (95%CI 25-70) vs 23% (95%CI 12-35) (p <.000). The cytogenetic risk group (intermediate and high) and the donor type (related and unrelated) had no effect on DFS and RI: 74% vs 63% and 47% vs 38%, 16% vs 19% and 59% vs 63 %; 68% vs 57% and 65% vs 42%, 20% vs 29% and 29% vs 58%. In the absence of chronic graft-versus-host disease (cGVHD), DFS and RI were better in patients with MRD(-) 64% (95%CI 45-83) vs 52% (95%CI 32-72) (p = 0.01) and 34% (95%CI 15-54) vs 44% (95%CI 23-63)(p =.03). In patients with cGVHD, the difference was insignificant: 70% vs 80% and 17% vs 20%. In multivariate analysis, the impact on the RI has had the status of the disease (MRD(+)/MRD(-)) (HR2.3, 95%CI, 1.1-4.9, p=.03) and the presence of cGVHD(yes/no) (HR0.3, 95%CI, 0.2-1.0, =.05). DFS was lower with MRD(+) (HR1.8, 95%CI, 1.0-3.5, p =.05). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Immunophenotypic, cytogenetic and molecular data in the onset of the disease is necessary for monitoring the MRD in AML remission. The presence of MRD has a negative effect on DFS and RI after allo-HSCT. MRD(+) status in front of the allo-HSCT is an indication for the intensification of the conditioning regimen. </p> <h2 style="text-align: justify;">Disclosure</h2> <p style="text-align: justify;"> The authors report no conflicts of interest in this work. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Acute myeloid leukemia, minimal residual disease, allogeneic hematopoietic stem cell transplantation. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3860) "
Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is an effective therapy for many patients with acute myeloid leukemia (AML). The relapse after allo-HSCT is the most common cause of treatment failure. However, multiparameter flow cytometry, cytogenetic and molecular studies in the onset of the disease makes it possible to detect the minimal residual disease (MRD) in AML remission in order to determine the prognosis and the therapy strategy.
Aim
To evaluate the impact of MRD before allo-HSCT in patients with AML on the results of treatment.
Patients and methods
We analysed 195 consecutive patients with AML since 2012 to 2016. Median age was 36 (18-70) years. The median follow-up was 23 (23-467) months. Disease status before allo-HSCT: CR1 – 148 (76%), CR2 – 47 (24%) patients. Molecular and genetic low-risk group was defined in 31(17%), standard risk in 119 (59%) and 45 (24%) high-risk patients. MRD was not determined (MRD (-)) in 155 (80%) patients. A positive result of MRD (MRD (+)) before alloHSCT was in 40 (20%) patients, including mutations, gene overexpression and leukemia associated immunophenotypes.
Results
Disease-free survival (DFS) after alloHSCT in CR1MRD(-) was 67% (95%CI 57-77), and in MRD(+) 54% (95%CI 36-72) (p=.03), whereas in patients with CR2MRD(-) 57% (95%CI 41-73) and CR2MRD(+) – 33% (95%CI 1-88) (p=ns). The relapse incidence (RI) in the CR1MRD(-) was 22% (95%CI 13-32), and in MRD(+) – 36% (95%CI 19-53), whereas in the CR2MRD(-) 17% (95%CI 7-32), and in MRD(+) 66% (95%CI 15-91). With myeloablative conditioning (MAC), the DFS and RI after allo-HSCT in CR1 did not depended on MRD: patients with MRD(-) 70% (95%CI 59-81) vs MRD(+) 64% (95%CI 36-92) and 17% (95%CI 7-39) vs 23% (95%CI 12-35) respectively. Whereas after reduced intensity conditioning (RIC), the DFC was higher, and the RI was lower in patients with MRD(-): 67% (95%CI 54-80) vs 50% (95%CI 27-77) (p=.03) and 50% (95%CI 25-70) vs 23% (95%CI 12-35) (p <.000). The cytogenetic risk group (intermediate and high) and the donor type (related and unrelated) had no effect on DFS and RI: 74% vs 63% and 47% vs 38%, 16% vs 19% and 59% vs 63 %; 68% vs 57% and 65% vs 42%, 20% vs 29% and 29% vs 58%. In the absence of chronic graft-versus-host disease (cGVHD), DFS and RI were better in patients with MRD(-) 64% (95%CI 45-83) vs 52% (95%CI 32-72) (p = 0.01) and 34% (95%CI 15-54) vs 44% (95%CI 23-63)(p =.03). In patients with cGVHD, the difference was insignificant: 70% vs 80% and 17% vs 20%. In multivariate analysis, the impact on the RI has had the status of the disease (MRD(+)/MRD(-)) (HR2.3, 95%CI, 1.1-4.9, p=.03) and the presence of cGVHD(yes/no) (HR0.3, 95%CI, 0.2-1.0, =.05). DFS was lower with MRD(+) (HR1.8, 95%CI, 1.0-3.5, p =.05).
Conclusion
Immunophenotypic, cytogenetic and molecular data in the onset of the disease is necessary for monitoring the MRD in AML remission. The presence of MRD has a negative effect on DFS and RI after allo-HSCT. MRD(+) status in front of the allo-HSCT is an indication for the intensification of the conditioning regimen.
Disclosure
The authors report no conflicts of interest in this work.
Keywords
Acute myeloid leukemia, minimal residual disease, allogeneic hematopoietic stem cell transplantation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20305" ["VALUE"]=> string(120) "Significance of minimal residual disease before allogeneic hematopoietic cell transplantation for acute myeloid leukemia" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(120) "Significance of minimal residual disease before allogeneic hematopoietic cell transplantation for acute myeloid leukemia" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20739" ["VALUE"]=> string(4) "1375" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1375" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20740" ["VALUE"]=> string(4) "1376" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1376" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20303" ["VALUE"]=> array(2) { ["TEXT"]=> string(534) "Sergey N. Bondarenko <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Anna G. Smirnova <sup>1</sup>, Irina A. Samorodova <sup>1</sup>, Olga S. Uspenskaya <sup>2</sup>, Elena V. Babenko <sup>1</sup>, Ildar M. Barkhatov <sup>1</sup>, Tatyana L. Gindina <sup>1</sup>, Nikolay N. Mamaev <sup>1</sup>, Alexander D. Kulagin <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(390) "Sergey N. Bondarenko 1, Ivan S. Moiseev 1, Elena I. Darskaya 1, Anna G. Smirnova 1, Irina A. Samorodova 1, Olga S. Uspenskaya 2, Elena V. Babenko 1, Ildar M. Barkhatov 1, Tatyana L. Gindina 1, Nikolay N. Mamaev 1, Alexander D. Kulagin 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(390) "Sergey N. Bondarenko 1, Ivan S. Moiseev 1, Elena I. Darskaya 1, Anna G. Smirnova 1, Irina A. Samorodova 1, Olga S. Uspenskaya 2, Elena V. Babenko 1, Ildar M. Barkhatov 1, Tatyana L. Gindina 1, Nikolay N. Mamaev 1, Alexander D. Kulagin 1, Boris V. Afanasyev 1" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20351" ["VALUE"]=> array(2) { ["TEXT"]=> string(4172) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is an effective therapy for many patients with acute myeloid leukemia (AML). The relapse after allo-HSCT is the most common cause of treatment failure. However, multiparameter flow cytometry, cytogenetic and molecular studies in the onset of the disease makes it possible to detect the minimal residual disease (MRD) in AML remission in order to determine the prognosis and the therapy strategy. </p> <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> To evaluate the impact of MRD before allo-HSCT in patients with AML on the results of treatment. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> We analysed 195 consecutive patients with AML since 2012 to 2016. Median age was 36 (18-70) years. The median follow-up was 23 (23-467) months. Disease status before allo-HSCT: CR1 – 148 (76%), CR2 – 47 (24%) patients. Molecular and genetic low-risk group was defined in 31(17%), standard risk in 119 (59%) and 45 (24%) high-risk patients. MRD was not determined (MRD (-)) in 155 (80%) patients. A positive result of MRD (MRD (+)) before alloHSCT was in 40 (20%) patients, including mutations, gene overexpression and leukemia associated immunophenotypes. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Disease-free survival (DFS) after alloHSCT in CR1MRD(-) was 67% (95%CI 57-77), and in MRD(+) 54% (95%CI 36-72) (p=.03), whereas in patients with CR2MRD(-) 57% (95%CI 41-73) and CR2MRD(+) – 33% (95%CI 1-88) (p=ns). The relapse incidence (RI) in the CR1MRD(-) was 22% (95%CI 13-32), and in MRD(+) – 36% (95%CI 19-53), whereas in the CR2MRD(-) 17% (95%CI 7-32), and in MRD(+) 66% (95%CI 15-91). With myeloablative conditioning (MAC), the DFS and RI after allo-HSCT in CR1 did not depended on MRD: patients with MRD(-) 70% (95%CI 59-81) vs MRD(+) 64% (95%CI 36-92) and 17% (95%CI 7-39) vs 23% (95%CI 12-35) respectively. Whereas after reduced intensity conditioning (RIC), the DFC was higher, and the RI was lower in patients with MRD(-): 67% (95%CI 54-80) vs 50% (95%CI 27-77) (p=.03) and 50% (95%CI 25-70) vs 23% (95%CI 12-35) (p <.000). The cytogenetic risk group (intermediate and high) and the donor type (related and unrelated) had no effect on DFS and RI: 74% vs 63% and 47% vs 38%, 16% vs 19% and 59% vs 63 %; 68% vs 57% and 65% vs 42%, 20% vs 29% and 29% vs 58%. In the absence of chronic graft-versus-host disease (cGVHD), DFS and RI were better in patients with MRD(-) 64% (95%CI 45-83) vs 52% (95%CI 32-72) (p = 0.01) and 34% (95%CI 15-54) vs 44% (95%CI 23-63)(p =.03). In patients with cGVHD, the difference was insignificant: 70% vs 80% and 17% vs 20%. In multivariate analysis, the impact on the RI has had the status of the disease (MRD(+)/MRD(-)) (HR2.3, 95%CI, 1.1-4.9, p=.03) and the presence of cGVHD(yes/no) (HR0.3, 95%CI, 0.2-1.0, =.05). DFS was lower with MRD(+) (HR1.8, 95%CI, 1.0-3.5, p =.05). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Immunophenotypic, cytogenetic and molecular data in the onset of the disease is necessary for monitoring the MRD in AML remission. The presence of MRD has a negative effect on DFS and RI after allo-HSCT. MRD(+) status in front of the allo-HSCT is an indication for the intensification of the conditioning regimen. </p> <h2 style="text-align: justify;">Disclosure</h2> <p style="text-align: justify;"> The authors report no conflicts of interest in this work. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Acute myeloid leukemia, minimal residual disease, allogeneic hematopoietic stem cell transplantation. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3860) "Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is an effective therapy for many patients with acute myeloid leukemia (AML). The relapse after allo-HSCT is the most common cause of treatment failure. However, multiparameter flow cytometry, cytogenetic and molecular studies in the onset of the disease makes it possible to detect the minimal residual disease (MRD) in AML remission in order to determine the prognosis and the therapy strategy.
Aim
To evaluate the impact of MRD before allo-HSCT in patients with AML on the results of treatment.
Patients and methods
We analysed 195 consecutive patients with AML since 2012 to 2016. Median age was 36 (18-70) years. The median follow-up was 23 (23-467) months. Disease status before allo-HSCT: CR1 – 148 (76%), CR2 – 47 (24%) patients. Molecular and genetic low-risk group was defined in 31(17%), standard risk in 119 (59%) and 45 (24%) high-risk patients. MRD was not determined (MRD (-)) in 155 (80%) patients. A positive result of MRD (MRD (+)) before alloHSCT was in 40 (20%) patients, including mutations, gene overexpression and leukemia associated immunophenotypes.
Results
Disease-free survival (DFS) after alloHSCT in CR1MRD(-) was 67% (95%CI 57-77), and in MRD(+) 54% (95%CI 36-72) (p=.03), whereas in patients with CR2MRD(-) 57% (95%CI 41-73) and CR2MRD(+) – 33% (95%CI 1-88) (p=ns). The relapse incidence (RI) in the CR1MRD(-) was 22% (95%CI 13-32), and in MRD(+) – 36% (95%CI 19-53), whereas in the CR2MRD(-) 17% (95%CI 7-32), and in MRD(+) 66% (95%CI 15-91). With myeloablative conditioning (MAC), the DFS and RI after allo-HSCT in CR1 did not depended on MRD: patients with MRD(-) 70% (95%CI 59-81) vs MRD(+) 64% (95%CI 36-92) and 17% (95%CI 7-39) vs 23% (95%CI 12-35) respectively. Whereas after reduced intensity conditioning (RIC), the DFC was higher, and the RI was lower in patients with MRD(-): 67% (95%CI 54-80) vs 50% (95%CI 27-77) (p=.03) and 50% (95%CI 25-70) vs 23% (95%CI 12-35) (p <.000). The cytogenetic risk group (intermediate and high) and the donor type (related and unrelated) had no effect on DFS and RI: 74% vs 63% and 47% vs 38%, 16% vs 19% and 59% vs 63 %; 68% vs 57% and 65% vs 42%, 20% vs 29% and 29% vs 58%. In the absence of chronic graft-versus-host disease (cGVHD), DFS and RI were better in patients with MRD(-) 64% (95%CI 45-83) vs 52% (95%CI 32-72) (p = 0.01) and 34% (95%CI 15-54) vs 44% (95%CI 23-63)(p =.03). In patients with cGVHD, the difference was insignificant: 70% vs 80% and 17% vs 20%. In multivariate analysis, the impact on the RI has had the status of the disease (MRD(+)/MRD(-)) (HR2.3, 95%CI, 1.1-4.9, p=.03) and the presence of cGVHD(yes/no) (HR0.3, 95%CI, 0.2-1.0, =.05). DFS was lower with MRD(+) (HR1.8, 95%CI, 1.0-3.5, p =.05).
Conclusion
Immunophenotypic, cytogenetic and molecular data in the onset of the disease is necessary for monitoring the MRD in AML remission. The presence of MRD has a negative effect on DFS and RI after allo-HSCT. MRD(+) status in front of the allo-HSCT is an indication for the intensification of the conditioning regimen.
Disclosure
The authors report no conflicts of interest in this work.
Keywords
Acute myeloid leukemia, minimal residual disease, allogeneic hematopoietic stem cell transplantation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3860) "Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is an effective therapy for many patients with acute myeloid leukemia (AML). The relapse after allo-HSCT is the most common cause of treatment failure. However, multiparameter flow cytometry, cytogenetic and molecular studies in the onset of the disease makes it possible to detect the minimal residual disease (MRD) in AML remission in order to determine the prognosis and the therapy strategy.
Aim
To evaluate the impact of MRD before allo-HSCT in patients with AML on the results of treatment.
Patients and methods
We analysed 195 consecutive patients with AML since 2012 to 2016. Median age was 36 (18-70) years. The median follow-up was 23 (23-467) months. Disease status before allo-HSCT: CR1 – 148 (76%), CR2 – 47 (24%) patients. Molecular and genetic low-risk group was defined in 31(17%), standard risk in 119 (59%) and 45 (24%) high-risk patients. MRD was not determined (MRD (-)) in 155 (80%) patients. A positive result of MRD (MRD (+)) before alloHSCT was in 40 (20%) patients, including mutations, gene overexpression and leukemia associated immunophenotypes.
Results
Disease-free survival (DFS) after alloHSCT in CR1MRD(-) was 67% (95%CI 57-77), and in MRD(+) 54% (95%CI 36-72) (p=.03), whereas in patients with CR2MRD(-) 57% (95%CI 41-73) and CR2MRD(+) – 33% (95%CI 1-88) (p=ns). The relapse incidence (RI) in the CR1MRD(-) was 22% (95%CI 13-32), and in MRD(+) – 36% (95%CI 19-53), whereas in the CR2MRD(-) 17% (95%CI 7-32), and in MRD(+) 66% (95%CI 15-91). With myeloablative conditioning (MAC), the DFS and RI after allo-HSCT in CR1 did not depended on MRD: patients with MRD(-) 70% (95%CI 59-81) vs MRD(+) 64% (95%CI 36-92) and 17% (95%CI 7-39) vs 23% (95%CI 12-35) respectively. Whereas after reduced intensity conditioning (RIC), the DFC was higher, and the RI was lower in patients with MRD(-): 67% (95%CI 54-80) vs 50% (95%CI 27-77) (p=.03) and 50% (95%CI 25-70) vs 23% (95%CI 12-35) (p <.000). The cytogenetic risk group (intermediate and high) and the donor type (related and unrelated) had no effect on DFS and RI: 74% vs 63% and 47% vs 38%, 16% vs 19% and 59% vs 63 %; 68% vs 57% and 65% vs 42%, 20% vs 29% and 29% vs 58%. In the absence of chronic graft-versus-host disease (cGVHD), DFS and RI were better in patients with MRD(-) 64% (95%CI 45-83) vs 52% (95%CI 32-72) (p = 0.01) and 34% (95%CI 15-54) vs 44% (95%CI 23-63)(p =.03). In patients with cGVHD, the difference was insignificant: 70% vs 80% and 17% vs 20%. In multivariate analysis, the impact on the RI has had the status of the disease (MRD(+)/MRD(-)) (HR2.3, 95%CI, 1.1-4.9, p=.03) and the presence of cGVHD(yes/no) (HR0.3, 95%CI, 0.2-1.0, =.05). DFS was lower with MRD(+) (HR1.8, 95%CI, 1.0-3.5, p =.05).
Conclusion
Immunophenotypic, cytogenetic and molecular data in the onset of the disease is necessary for monitoring the MRD in AML remission. The presence of MRD has a negative effect on DFS and RI after allo-HSCT. MRD(+) status in front of the allo-HSCT is an indication for the intensification of the conditioning regimen.
Disclosure
The authors report no conflicts of interest in this work.
Keywords
Acute myeloid leukemia, minimal residual disease, allogeneic hematopoietic stem cell transplantation.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20305" ["VALUE"]=> string(120) "Significance of minimal residual disease before allogeneic hematopoietic cell transplantation for acute myeloid leukemia" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(120) "Significance of minimal residual disease before allogeneic hematopoietic cell transplantation for acute myeloid leukemia" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(120) "Significance of minimal residual disease before allogeneic hematopoietic cell transplantation for acute myeloid leukemia" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20304" ["VALUE"]=> array(2) { ["TEXT"]=> string(337) "<sup>1</sup> R. M. Gorbacheva Memorial Institute of Oncology, Hematology and Transplantation, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation<br> <sup>2</sup> Leningrad Regional Clinical Hospital, Hematology Department, St. Petersburg, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(301) "1 R. M. Gorbacheva Memorial Institute of Oncology, Hematology and Transplantation, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation2 Leningrad Regional Clinical Hospital, Hematology Department, St. Petersburg, Russian Federation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(301) "1 R. M. Gorbacheva Memorial Institute of Oncology, Hematology and Transplantation, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation
2 Leningrad Regional Clinical Hospital, Hematology Department, St. Petersburg, Russian Federation
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20301" ["VALUE"]=> array(2) { ["TEXT"]=> string(717) "Сергей Н. Бондаренко <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Анна Г. Смирнова <sup>1</sup>, Ирина А. Самородова <sup>1</sup>, Ольга С. Успенская <sup>2</sup>, Елена В. Бабенко <sup>1</sup>, Ильдар М. Бархатов <sup>1</sup>, Татьяна Л. Гиндина <sup>1</sup>, Николай Н. Мамаев <sup>1</sup>, Александр Д. Кулагин <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(573) "Сергей Н. Бондаренко 1, Иван С. Моисеев 1, Елена И. Дарская 1, Анна Г. Смирнова 1, Ирина А. Самородова 1, Ольга С. Успенская 2, Елена В. Бабенко 1, Ильдар М. Бархатов 1, Татьяна Л. Гиндина 1, Николай Н. Мамаев 1, Александр Д. Кулагин 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(573) "Сергей Н. Бондаренко 1, Иван С. Моисеев 1, Елена И. Дарская 1, Анна Г. Смирнова 1, Ирина А. Самородова 1, Ольга С. Успенская 2, Елена В. Бабенко 1, Ильдар М. Бархатов 1, Татьяна Л. Гиндина 1, Николай Н. Мамаев 1, Александр Д. Кулагин 1, Борис В. Афанасьев 1" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20350" ["VALUE"]=> array(2) { ["TEXT"]=> string(7752) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) является эффективным методом лечения острого миелобластного лейкоза (ОМЛ). Развитие рецидива после алло-ТГСК является наиболее частой причиной неудач лечения. Однако, проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания дает возможность определения минимальной остаточной болезни (МОБ) в ремиссии (ПР) ОМЛ с целью определения прогноза и выбора адекватной терапии. </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Оценить влияние наличия МОБ у пациентов ОМЛ перед алло-ТГСК на результаты лечения. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В исследование включено 195 пациентов за период 2012-16 гг. Медиана возраста составила 36 (18-70) лет. Медиана наблюдения составила 23 (23-467) мес. Статус заболевания перед алло-ТГСК: ПР1 – 148 (76%) пациентов, ПР2 – 47 (24%) пациентов. Согласно молекулярно-генетической классификации к группе низкого риска относились 31 (17%) пациент, среднего риска – 119 (59%), высокого риска – 45 (24%) пациентов. МОБ не определялась (МОБ-) у 155 (80%) пациентов. Положительный результат МОБ (МОБ+) перед алло-ТГСК был у 40 (20%) человек, из них мутации t(8;21)(q22;q22); RUNX1-RUNX1T1 – 3 пациента, inv(16)(p13.1q22); CBFB-MYH11 – 2, t(15;17) (q22;q21); PML-RARа – 1, t(9;11)(p22;q23); MLLT3-KTM2A – 2, NPM1 – 2, FLT3-ITD – 4; гиперэкспрессия: WT1 – 8 , EVI1 – 1 пациент; МОБ(+) методом проточной цитометрии у 18 пациентов, медиана 0,4% (0,13-3,9). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> При однофакторном анализе безрецидивная выживаемость (БРВ) после алло-ТГСК в ПР1 МОБ- составила 67% (95%ДИ 57-77), а при МОБ+ – 54% (95%ДИ 36-72) р=.03, тогда как у пациентов в ПР2 при МОБ- составила 57% (95%ДИ 41-73), и соответственно при МОБ(+) – 33% (95%ДИ 1-88) р=нд. Частота рецидивов (ЧР) в ПР1 МОБ- Д22%(95%ДИ 13-32), а при МОБ+ – 36%(95%ДИ 19-53), тогда как в ПР2 МОБ- 17% (95%ДИ 7-32), а при МОБ+ 66% (95%ДИ 15-91). При миелоаблативном кондиционировании БРВ и ЧР после алло-ТГСК в ПР1 не зависели от уровня МОБ: при МОБ- 70% (95%ДИ 59-81) и при МОБ+ 64% (95%ДИ 36-92) и соответственно 17% (95%ДИ 7-39) и 23% (95%ДИ 12-35). Тогда как при проведении кондиционирования редуцированной интенсивности, БРВ была выше, а ЧР ниже у пациентов МОБ-: 67% (95%ДИ 54-80) против 50% (95%ДИ 27-77) р=.03 и 50% (95%ДИ 25-70) и 23% (95%ДИ 12-35) р<.000. МОБ+ негативно влияла на БРВ и ЧР при использовании костного мозга в качестве трансплантата: МОБ- 76% (95%ДИ 57-87) по сравнению с МОБ+ 53% (95%ДИ 28-78) и 47% (95%ДИ 20-70) по сравнению с 24% (95%ДИ 8-44) р=.03,а при алло-ТГСК периферической крови разница БРВ и ЧР была не достоверна: 66% (95%ДИ 53-79) против 57% (95%ДИ 32-83) и 23% (95%ДИ 12-35) против 25% (95%ДИ 7-49). Цитогенетическая группа риска (средний и высокий) и донор (родственный и неродственный) не влияли на БРВ и ЧР: 74% (95%ДИ 61-87) против 63% (95%ДИ 39-85) и 47% (95%ДИ 22-72) против 38% (95%ДИ 5-71), 16% (95%ДИ 6-30) против 19% (95%ДИ 4-41) и 59% (95%ДИ 25-75) против 63% (95%ДИ 18-89); 68% (95%ДИ 56-80) против 57% (95%ДИ 46-78) и 65% (95%ДИ 45-84) против 42% (95%ДИ 5-79), 20% (95%ДИ 10-32) против 29% (95%ДИ 11-49) и 29% (95%ДИ 12-48) против 58% (95%ДИ 10-88). При отсутствии хронической РТПХ (хРТПХ) БРВ и ЧР были лучше у пациентов МОБ- 64% (95%ДИ 45-83) против 52% (95%ДИ 32-72) р=0.01 и 34% (95%ДИ 15-54) против 44% (95%ДИ 23-63) р=.03. У пациентов с хРТПХ разница в обеих группах была недостоверна: 70% (95%ДИ 57-83) против 80% (95%ДИ45-99) и 17% (95%ДИ 7-29) против 20% (95%ДИ1-62). При проведении многофакторного анализа влияние на ЧР оказал статус заболевания (МОБ+/МОБ-) (ОР, 2.3, 95%ДИ 1.1-4.9, р=.03) и наличие хРТПХ (да/нет) (ОР, 0.3, 95%ДИ 0.2-1.0, р=.05). БРВ была хуже при МОБ+ (ОР, 1.8, 95%ДИ 1.0-3.5, р=.05). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Необходимо проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания для возможности мониторинга МОБ в ремиссии ОМЛ. При ОМЛ наличие МОБ негативно влияет на БРВ и ЧР после алло-ТГСК. Статус МОБ+ перед алло-ТГСК является показанием для интенсификации режима кондиционирования. </p> <h2 style="text-align: justify;">Комментарии</h2> <p style="text-align: justify;"> Авторы заявляют об отсутствии скрытого конфликта интересов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый миелоидный лейкоз, минимальная остаточная болезнь, аллогенная трансплантация гемопоэтических стволовых клеток. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7428) "
Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) является эффективным методом лечения острого миелобластного лейкоза (ОМЛ). Развитие рецидива после алло-ТГСК является наиболее частой причиной неудач лечения. Однако, проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания дает возможность определения минимальной остаточной болезни (МОБ) в ремиссии (ПР) ОМЛ с целью определения прогноза и выбора адекватной терапии.
Цель работы
Оценить влияние наличия МОБ у пациентов ОМЛ перед алло-ТГСК на результаты лечения.
Пациенты и методы
В исследование включено 195 пациентов за период 2012-16 гг. Медиана возраста составила 36 (18-70) лет. Медиана наблюдения составила 23 (23-467) мес. Статус заболевания перед алло-ТГСК: ПР1 – 148 (76%) пациентов, ПР2 – 47 (24%) пациентов. Согласно молекулярно-генетической классификации к группе низкого риска относились 31 (17%) пациент, среднего риска – 119 (59%), высокого риска – 45 (24%) пациентов. МОБ не определялась (МОБ-) у 155 (80%) пациентов. Положительный результат МОБ (МОБ+) перед алло-ТГСК был у 40 (20%) человек, из них мутации t(8;21)(q22;q22); RUNX1-RUNX1T1 – 3 пациента, inv(16)(p13.1q22); CBFB-MYH11 – 2, t(15;17) (q22;q21); PML-RARа – 1, t(9;11)(p22;q23); MLLT3-KTM2A – 2, NPM1 – 2, FLT3-ITD – 4; гиперэкспрессия: WT1 – 8 , EVI1 – 1 пациент; МОБ(+) методом проточной цитометрии у 18 пациентов, медиана 0,4% (0,13-3,9).
Результаты
При однофакторном анализе безрецидивная выживаемость (БРВ) после алло-ТГСК в ПР1 МОБ- составила 67% (95%ДИ 57-77), а при МОБ+ – 54% (95%ДИ 36-72) р=.03, тогда как у пациентов в ПР2 при МОБ- составила 57% (95%ДИ 41-73), и соответственно при МОБ(+) – 33% (95%ДИ 1-88) р=нд. Частота рецидивов (ЧР) в ПР1 МОБ- Д22%(95%ДИ 13-32), а при МОБ+ – 36%(95%ДИ 19-53), тогда как в ПР2 МОБ- 17% (95%ДИ 7-32), а при МОБ+ 66% (95%ДИ 15-91). При миелоаблативном кондиционировании БРВ и ЧР после алло-ТГСК в ПР1 не зависели от уровня МОБ: при МОБ- 70% (95%ДИ 59-81) и при МОБ+ 64% (95%ДИ 36-92) и соответственно 17% (95%ДИ 7-39) и 23% (95%ДИ 12-35). Тогда как при проведении кондиционирования редуцированной интенсивности, БРВ была выше, а ЧР ниже у пациентов МОБ-: 67% (95%ДИ 54-80) против 50% (95%ДИ 27-77) р=.03 и 50% (95%ДИ 25-70) и 23% (95%ДИ 12-35) р<.000. МОБ+ негативно влияла на БРВ и ЧР при использовании костного мозга в качестве трансплантата: МОБ- 76% (95%ДИ 57-87) по сравнению с МОБ+ 53% (95%ДИ 28-78) и 47% (95%ДИ 20-70) по сравнению с 24% (95%ДИ 8-44) р=.03,а при алло-ТГСК периферической крови разница БРВ и ЧР была не достоверна: 66% (95%ДИ 53-79) против 57% (95%ДИ 32-83) и 23% (95%ДИ 12-35) против 25% (95%ДИ 7-49). Цитогенетическая группа риска (средний и высокий) и донор (родственный и неродственный) не влияли на БРВ и ЧР: 74% (95%ДИ 61-87) против 63% (95%ДИ 39-85) и 47% (95%ДИ 22-72) против 38% (95%ДИ 5-71), 16% (95%ДИ 6-30) против 19% (95%ДИ 4-41) и 59% (95%ДИ 25-75) против 63% (95%ДИ 18-89); 68% (95%ДИ 56-80) против 57% (95%ДИ 46-78) и 65% (95%ДИ 45-84) против 42% (95%ДИ 5-79), 20% (95%ДИ 10-32) против 29% (95%ДИ 11-49) и 29% (95%ДИ 12-48) против 58% (95%ДИ 10-88). При отсутствии хронической РТПХ (хРТПХ) БРВ и ЧР были лучше у пациентов МОБ- 64% (95%ДИ 45-83) против 52% (95%ДИ 32-72) р=0.01 и 34% (95%ДИ 15-54) против 44% (95%ДИ 23-63) р=.03. У пациентов с хРТПХ разница в обеих группах была недостоверна: 70% (95%ДИ 57-83) против 80% (95%ДИ45-99) и 17% (95%ДИ 7-29) против 20% (95%ДИ1-62). При проведении многофакторного анализа влияние на ЧР оказал статус заболевания (МОБ+/МОБ-) (ОР, 2.3, 95%ДИ 1.1-4.9, р=.03) и наличие хРТПХ (да/нет) (ОР, 0.3, 95%ДИ 0.2-1.0, р=.05). БРВ была хуже при МОБ+ (ОР, 1.8, 95%ДИ 1.0-3.5, р=.05).
Заключение
Необходимо проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания для возможности мониторинга МОБ в ремиссии ОМЛ. При ОМЛ наличие МОБ негативно влияет на БРВ и ЧР после алло-ТГСК. Статус МОБ+ перед алло-ТГСК является показанием для интенсификации режима кондиционирования.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
Ключевые слова
Острый миелоидный лейкоз, минимальная остаточная болезнь, аллогенная трансплантация гемопоэтических стволовых клеток.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(7428) "Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) является эффективным методом лечения острого миелобластного лейкоза (ОМЛ). Развитие рецидива после алло-ТГСК является наиболее частой причиной неудач лечения. Однако, проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания дает возможность определения минимальной остаточной болезни (МОБ) в ремиссии (ПР) ОМЛ с целью определения прогноза и выбора адекватной терапии.
Цель работы
Оценить влияние наличия МОБ у пациентов ОМЛ перед алло-ТГСК на результаты лечения.
Пациенты и методы
В исследование включено 195 пациентов за период 2012-16 гг. Медиана возраста составила 36 (18-70) лет. Медиана наблюдения составила 23 (23-467) мес. Статус заболевания перед алло-ТГСК: ПР1 – 148 (76%) пациентов, ПР2 – 47 (24%) пациентов. Согласно молекулярно-генетической классификации к группе низкого риска относились 31 (17%) пациент, среднего риска – 119 (59%), высокого риска – 45 (24%) пациентов. МОБ не определялась (МОБ-) у 155 (80%) пациентов. Положительный результат МОБ (МОБ+) перед алло-ТГСК был у 40 (20%) человек, из них мутации t(8;21)(q22;q22); RUNX1-RUNX1T1 – 3 пациента, inv(16)(p13.1q22); CBFB-MYH11 – 2, t(15;17) (q22;q21); PML-RARа – 1, t(9;11)(p22;q23); MLLT3-KTM2A – 2, NPM1 – 2, FLT3-ITD – 4; гиперэкспрессия: WT1 – 8 , EVI1 – 1 пациент; МОБ(+) методом проточной цитометрии у 18 пациентов, медиана 0,4% (0,13-3,9).
Результаты
При однофакторном анализе безрецидивная выживаемость (БРВ) после алло-ТГСК в ПР1 МОБ- составила 67% (95%ДИ 57-77), а при МОБ+ – 54% (95%ДИ 36-72) р=.03, тогда как у пациентов в ПР2 при МОБ- составила 57% (95%ДИ 41-73), и соответственно при МОБ(+) – 33% (95%ДИ 1-88) р=нд. Частота рецидивов (ЧР) в ПР1 МОБ- Д22%(95%ДИ 13-32), а при МОБ+ – 36%(95%ДИ 19-53), тогда как в ПР2 МОБ- 17% (95%ДИ 7-32), а при МОБ+ 66% (95%ДИ 15-91). При миелоаблативном кондиционировании БРВ и ЧР после алло-ТГСК в ПР1 не зависели от уровня МОБ: при МОБ- 70% (95%ДИ 59-81) и при МОБ+ 64% (95%ДИ 36-92) и соответственно 17% (95%ДИ 7-39) и 23% (95%ДИ 12-35). Тогда как при проведении кондиционирования редуцированной интенсивности, БРВ была выше, а ЧР ниже у пациентов МОБ-: 67% (95%ДИ 54-80) против 50% (95%ДИ 27-77) р=.03 и 50% (95%ДИ 25-70) и 23% (95%ДИ 12-35) р<.000. МОБ+ негативно влияла на БРВ и ЧР при использовании костного мозга в качестве трансплантата: МОБ- 76% (95%ДИ 57-87) по сравнению с МОБ+ 53% (95%ДИ 28-78) и 47% (95%ДИ 20-70) по сравнению с 24% (95%ДИ 8-44) р=.03,а при алло-ТГСК периферической крови разница БРВ и ЧР была не достоверна: 66% (95%ДИ 53-79) против 57% (95%ДИ 32-83) и 23% (95%ДИ 12-35) против 25% (95%ДИ 7-49). Цитогенетическая группа риска (средний и высокий) и донор (родственный и неродственный) не влияли на БРВ и ЧР: 74% (95%ДИ 61-87) против 63% (95%ДИ 39-85) и 47% (95%ДИ 22-72) против 38% (95%ДИ 5-71), 16% (95%ДИ 6-30) против 19% (95%ДИ 4-41) и 59% (95%ДИ 25-75) против 63% (95%ДИ 18-89); 68% (95%ДИ 56-80) против 57% (95%ДИ 46-78) и 65% (95%ДИ 45-84) против 42% (95%ДИ 5-79), 20% (95%ДИ 10-32) против 29% (95%ДИ 11-49) и 29% (95%ДИ 12-48) против 58% (95%ДИ 10-88). При отсутствии хронической РТПХ (хРТПХ) БРВ и ЧР были лучше у пациентов МОБ- 64% (95%ДИ 45-83) против 52% (95%ДИ 32-72) р=0.01 и 34% (95%ДИ 15-54) против 44% (95%ДИ 23-63) р=.03. У пациентов с хРТПХ разница в обеих группах была недостоверна: 70% (95%ДИ 57-83) против 80% (95%ДИ45-99) и 17% (95%ДИ 7-29) против 20% (95%ДИ1-62). При проведении многофакторного анализа влияние на ЧР оказал статус заболевания (МОБ+/МОБ-) (ОР, 2.3, 95%ДИ 1.1-4.9, р=.03) и наличие хРТПХ (да/нет) (ОР, 0.3, 95%ДИ 0.2-1.0, р=.05). БРВ была хуже при МОБ+ (ОР, 1.8, 95%ДИ 1.0-3.5, р=.05).
Заключение
Необходимо проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания для возможности мониторинга МОБ в ремиссии ОМЛ. При ОМЛ наличие МОБ негативно влияет на БРВ и ЧР после алло-ТГСК. Статус МОБ+ перед алло-ТГСК является показанием для интенсификации режима кондиционирования.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
Ключевые слова
Острый миелоидный лейкоз, минимальная остаточная болезнь, аллогенная трансплантация гемопоэтических стволовых клеток.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20302" ["VALUE"]=> array(2) { ["TEXT"]=> string(316) "<sup>1</sup> НИИ ДОГиТ им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург<br> <sup>2</sup> Ленинградская областная клиническая больница, Санкт-Петербург<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(280) "1 НИИ ДОГиТ им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург2 Ленинградская областная клиническая больница, Санкт-Петербург
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(280) "1 НИИ ДОГиТ им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург
2 Ленинградская областная клиническая больница, Санкт-Петербург
" } } } [15]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1554" ["~ID"]=> string(4) "1554" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(144) "Эффективность и токсичность блинатумомаба при остром В-лимфобластном лейкозе" ["~NAME"]=> string(144) "Эффективность и токсичность блинатумомаба при остром В-лимфобластном лейкозе" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:25:30" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:25:30" ["DETAIL_PAGE_URL"]=> string(125) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/effektivnost-i-toksichnost-blinatumomaba-pri-ostrom-v-limfoblastnom-leykoze/" ["~DETAIL_PAGE_URL"]=> string(125) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/effektivnost-i-toksichnost-blinatumomaba-pri-ostrom-v-limfoblastnom-leykoze/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(75) "effektivnost-i-toksichnost-blinatumomaba-pri-ostrom-v-limfoblastnom-leykoze" ["~CODE"]=> string(75) "effektivnost-i-toksichnost-blinatumomaba-pri-ostrom-v-limfoblastnom-leykoze" ["EXTERNAL_ID"]=> string(4) "1554" ["~EXTERNAL_ID"]=> string(4) "1554" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(144) "Эффективность и токсичность блинатумомаба при остром В-лимфобластном лейкозе" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(215) "Эффективность и токсичность блинатумомаба при остром В-лимфобластном лейкозеEfficacy and toxicity of blinatumomab in acute B-lymphoblastic leukemia" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(6406) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Результаты терапии пациентов с положительной минимальной остаточной болезнью (МОБ+), рецидивами и рефрактерным течением острого В-лимфобластного лейкоза (Р/РОЛЛ), особенно после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), остаются неудовлетворительными. Возможности химиотерапии (ХТ) исчерпаны, что обуславливает необходимость использования новых методов терапии. Блинатумомаб (Б) является генно-инженерным антителом, активатором Т-клеток, биспецифичным по отношению к CD19 и CD3. Б помогает преодолеть резистентность к ХТ и может использоваться как до, так и после ТГСК за счет низкой токсичности. </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Оценить эффективность и безопасность Б при МОБ+ и Р/РОЛЛ. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В исследование включено 59 больных из 10 гематологических центров РФ с CD19+ОЛЛ. Медиана возраста составила 28 (18-62) лет. К B-I варианту относились 15 пациентов, B-II – 37, B-III – 18, и 1 больной имел ОЛ со смешанный фенотипом (В/миело). В рецидиве (Р) находилось 35 больных, из них 4 в комбинированном (костный мозг (КМ) и экстрамедуллярное поражение (ЭМ)) (РI – 14 , РII – 14 и РIII – 7), первично-рефрактерных – 2 и МОБ+ – 22. Число бластов КМ <50% выявлялось у 18 пациентов, а >50% у 19. Медиана уровня МОБ составила 0,35 (0,01-7,0)%. Б получили до ТГСК 42(71%) пациента, после ТГСК 17(29%). ТГСК (род-5, нерод-10, гапло-3, ауто-2) проведена после терапии Б 20 (34%) пациентам, из них 3 – повторная алло-ТГСК. У 9 больных после алло-ТГСК Б использовался в сочетании с инфузией донорских лимфоцитов (ИДЛ). Общее количество курсов Б составило от 1 до 7 (медиана 2). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> В группе МОБ+ негативный статус получен у 20 (91%) больных. Полная ремиссия (ПР) достигнута у 25 (68%)(в том числе 18 (72%) из них МОБ-): 13 (57%) пациентов при Р/РОЛЛ после ХТ, 12(86%) после алло-ТГСК. Частота достижения ПР была выше в группе больных с числом бластов <50% (78%(14/18) против 58%(11/19)). После терапии Б у 3 пациентов отмечалась ЭМ прогрессия ОЛЛ. РОЛЛ возник у 16(36%) больных: МОБ+ – 1, КМ – 11, ЭМ – 3, комбинированный – 1. В группах МОБ+ и Р/РОЛЛ 2хлетняя безрецидивная выживаемость (2БРВ) составили 62% (95%CI 35-89%) и 28%( 95%CI 6-50%), соответственно. В группах МОБ+ и Р/РОЛЛ 2хлетняя частота рецидивов (2ЧР) составили 38% (95%CI 4-60%) и 53% (95%CI 25-74%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии Б 2БРВ и 2ЧР составили 59% (95%CI 24-85%) против 30% (95%CI 7-53%) р=.08 и 27% (95%CI 7-52%) против 61% (95%CI 30-81%) р=.06, соответственно. Токсичность: гематологическая ≥3 степени (нейтропения, тромбоцитопения) наблюдалась у 15 (25%) больных, печеночная ≥3 степени – у 5(8%), неврологическая – у 11 (19%), синдром «высвобождения цитокин» наблюдался у 4 (7%). У 54 (92%) пациентов токсические явления были обратимы, и только у 5 (8%) больных терапия была прекращена досрочно. Только у 1 пациента после Б в сочетании с ИДЛ развилась оРТПХ (кожа 3 степени). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Б в лечении МОБ+ и Р/РОЛЛ показал высокую эффективность и приемлемую токсичность. Частота достижения ПР выше при лечении Б Р/РОЛЛ после алло-ТГСК. </p> <h2 style="text-align: justify;">Комментарии</h2> <p style="text-align: justify;"> Авторы заявляют об отсутствии скрытого конфликта интересов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый лимфобластный лейкоз, таргетная терапия, блинатумомаб. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(144) "Эффективность и токсичность блинатумомаба при остром В-лимфобластном лейкозе" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(144) "Эффективность и токсичность блинатумомаба при остром В-лимфобластном лейкозе" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(144) "Эффективность и токсичность блинатумомаба при остром В-лимфобластном лейкозе" ["SECTION_META_TITLE"]=> string(144) "Эффективность и токсичность блинатумомаба при остром В-лимфобластном лейкозе" ["SECTION_META_KEYWORDS"]=> string(144) "Эффективность и токсичность блинатумомаба при остром В-лимфобластном лейкозе" ["SECTION_META_DESCRIPTION"]=> string(144) "Эффективность и токсичность блинатумомаба при остром В-лимфобластном лейкозе" ["SECTION_PICTURE_FILE_ALT"]=> string(144) "Эффективность и токсичность блинатумомаба при остром В-лимфобластном лейкозе" ["SECTION_PICTURE_FILE_TITLE"]=> string(144) "Эффективность и токсичность блинатумомаба при остром В-лимфобластном лейкозе" ["SECTION_PICTURE_FILE_NAME"]=> string(79) "effektivnost-i-toksichnost-blinatumomaba-pri-ostrom-v-limfoblastnom-leykoze-img" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(144) "Эффективность и токсичность блинатумомаба при остром В-лимфобластном лейкозе" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(144) "Эффективность и токсичность блинатумомаба при остром В-лимфобластном лейкозе" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(79) "effektivnost-i-toksichnost-blinatumomaba-pri-ostrom-v-limfoblastnom-leykoze-img" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(79) "effektivnost-i-toksichnost-blinatumomaba-pri-ostrom-v-limfoblastnom-leykoze-img" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(79) "effektivnost-i-toksichnost-blinatumomaba-pri-ostrom-v-limfoblastnom-leykoze-img" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20309" ["VALUE"]=> array(2) { ["TEXT"]=> string(1310) "Сергей Н. Бондаренко <sup>1</sup>, Елена Н. Паровичникова <sup>2</sup>, Алексей А. Масчан <sup>3</sup>, Ольга Ю. Баранова <sup>4</sup>, Татьяна В. Шелехова <sup>5</sup>, Вадим А. Доронин <sup>6</sup>, Владимир Я. Мельниченко <sup>7</sup>, Камиль Д. Капланов <sup>8</sup>, Ольга С. Успенская <sup>9</sup>, Андрей Н. Соколов <sup>2</sup>, Наталья В. Мякова <sup>3</sup>, Иван С. Моисеев <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Анна Г. Смирнова <sup>1</sup>, Татьяна А. Быкова <sup>1</sup>, Белла И. Аюбова <sup>1</sup>, Ирина А. Самородова <sup>1</sup>, Елена В. Бабенко <sup>1</sup>, Ильдар М. Бархатов <sup>1</sup>, Татьяна Л. Гиндина <sup>1</sup>, Александр Д. Кулагин <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "TEXT" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1046) "Сергей Н. Бондаренко 1, Елена Н. Паровичникова 2, Алексей А. Масчан 3, Ольга Ю. Баранова 4, Татьяна В. Шелехова 5, Вадим А. Доронин 6, Владимир Я. Мельниченко 7, Камиль Д. Капланов 8, Ольга С. Успенская 9, Андрей Н. Соколов 2, Наталья В. Мякова 3, Иван С. Моисеев 1, Елена И. Дарская 1, Анна Г. Смирнова 1, Татьяна А. Быкова 1, Белла И. Аюбова 1, Ирина А. Самородова 1, Елена В. Бабенко 1, Ильдар М. Бархатов 1, Татьяна Л. Гиндина 1, Александр Д. Кулагин 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "TEXT" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20310" ["VALUE"]=> array(2) { ["TEXT"]=> string(1623) "<sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург<br> <sup>2</sup> Национальный медицинский исследовательский центр гематологии, Москва<br> <sup>3</sup> Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Д. Рогачева, Москва<br> <sup>4</sup> Национальный медицинский исследовательский центр онкологии им. Н. Н. Блохина, Москва<br> <sup>5</sup> Саратовский государственный медицинский университет им. В. И. Разумовского<br> <sup>6</sup> Городская клиническая больница №40 г. Москва<br> <sup>7</sup> Национальный медико-хирургический центр им. Н. И. Пирогова, Москва<br> <sup>8</sup> Волгоградский областной клинический онкологический диспансер<br> <sup>9</sup> Ленинградская областная клиническая больница, Санкт-Петербург<br>" ["TYPE"]=> string(4) "TEXT" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1461) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург
2 Национальный медицинский исследовательский центр гематологии, Москва
3 Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Д. Рогачева, Москва
4 Национальный медицинский исследовательский центр онкологии им. Н. Н. Блохина, Москва
5 Саратовский государственный медицинский университет им. В. И. Разумовского
6 Городская клиническая больница №40 г. Москва
7 Национальный медико-хирургический центр им. Н. И. Пирогова, Москва
8 Волгоградский областной клинический онкологический диспансер
9 Ленинградская областная клиническая больница, Санкт-Петербург
" ["TYPE"]=> string(4) "TEXT" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20348" ["VALUE"]=> array(2) { ["TEXT"]=> string(6406) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Результаты терапии пациентов с положительной минимальной остаточной болезнью (МОБ+), рецидивами и рефрактерным течением острого В-лимфобластного лейкоза (Р/РОЛЛ), особенно после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), остаются неудовлетворительными. Возможности химиотерапии (ХТ) исчерпаны, что обуславливает необходимость использования новых методов терапии. Блинатумомаб (Б) является генно-инженерным антителом, активатором Т-клеток, биспецифичным по отношению к CD19 и CD3. Б помогает преодолеть резистентность к ХТ и может использоваться как до, так и после ТГСК за счет низкой токсичности. </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Оценить эффективность и безопасность Б при МОБ+ и Р/РОЛЛ. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В исследование включено 59 больных из 10 гематологических центров РФ с CD19+ОЛЛ. Медиана возраста составила 28 (18-62) лет. К B-I варианту относились 15 пациентов, B-II – 37, B-III – 18, и 1 больной имел ОЛ со смешанный фенотипом (В/миело). В рецидиве (Р) находилось 35 больных, из них 4 в комбинированном (костный мозг (КМ) и экстрамедуллярное поражение (ЭМ)) (РI – 14 , РII – 14 и РIII – 7), первично-рефрактерных – 2 и МОБ+ – 22. Число бластов КМ <50% выявлялось у 18 пациентов, а >50% у 19. Медиана уровня МОБ составила 0,35 (0,01-7,0)%. Б получили до ТГСК 42(71%) пациента, после ТГСК 17(29%). ТГСК (род-5, нерод-10, гапло-3, ауто-2) проведена после терапии Б 20 (34%) пациентам, из них 3 – повторная алло-ТГСК. У 9 больных после алло-ТГСК Б использовался в сочетании с инфузией донорских лимфоцитов (ИДЛ). Общее количество курсов Б составило от 1 до 7 (медиана 2). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> В группе МОБ+ негативный статус получен у 20 (91%) больных. Полная ремиссия (ПР) достигнута у 25 (68%)(в том числе 18 (72%) из них МОБ-): 13 (57%) пациентов при Р/РОЛЛ после ХТ, 12(86%) после алло-ТГСК. Частота достижения ПР была выше в группе больных с числом бластов <50% (78%(14/18) против 58%(11/19)). После терапии Б у 3 пациентов отмечалась ЭМ прогрессия ОЛЛ. РОЛЛ возник у 16(36%) больных: МОБ+ – 1, КМ – 11, ЭМ – 3, комбинированный – 1. В группах МОБ+ и Р/РОЛЛ 2хлетняя безрецидивная выживаемость (2БРВ) составили 62% (95%CI 35-89%) и 28%( 95%CI 6-50%), соответственно. В группах МОБ+ и Р/РОЛЛ 2хлетняя частота рецидивов (2ЧР) составили 38% (95%CI 4-60%) и 53% (95%CI 25-74%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии Б 2БРВ и 2ЧР составили 59% (95%CI 24-85%) против 30% (95%CI 7-53%) р=.08 и 27% (95%CI 7-52%) против 61% (95%CI 30-81%) р=.06, соответственно. Токсичность: гематологическая ≥3 степени (нейтропения, тромбоцитопения) наблюдалась у 15 (25%) больных, печеночная ≥3 степени – у 5(8%), неврологическая – у 11 (19%), синдром «высвобождения цитокин» наблюдался у 4 (7%). У 54 (92%) пациентов токсические явления были обратимы, и только у 5 (8%) больных терапия была прекращена досрочно. Только у 1 пациента после Б в сочетании с ИДЛ развилась оРТПХ (кожа 3 степени). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Б в лечении МОБ+ и Р/РОЛЛ показал высокую эффективность и приемлемую токсичность. Частота достижения ПР выше при лечении Б Р/РОЛЛ после алло-ТГСК. </p> <h2 style="text-align: justify;">Комментарии</h2> <p style="text-align: justify;"> Авторы заявляют об отсутствии скрытого конфликта интересов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый лимфобластный лейкоз, таргетная терапия, блинатумомаб. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6086) "
Введение
Результаты терапии пациентов с положительной минимальной остаточной болезнью (МОБ+), рецидивами и рефрактерным течением острого В-лимфобластного лейкоза (Р/РОЛЛ), особенно после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), остаются неудовлетворительными. Возможности химиотерапии (ХТ) исчерпаны, что обуславливает необходимость использования новых методов терапии. Блинатумомаб (Б) является генно-инженерным антителом, активатором Т-клеток, биспецифичным по отношению к CD19 и CD3. Б помогает преодолеть резистентность к ХТ и может использоваться как до, так и после ТГСК за счет низкой токсичности.
Цель работы
Оценить эффективность и безопасность Б при МОБ+ и Р/РОЛЛ.
Пациенты и методы
В исследование включено 59 больных из 10 гематологических центров РФ с CD19+ОЛЛ. Медиана возраста составила 28 (18-62) лет. К B-I варианту относились 15 пациентов, B-II – 37, B-III – 18, и 1 больной имел ОЛ со смешанный фенотипом (В/миело). В рецидиве (Р) находилось 35 больных, из них 4 в комбинированном (костный мозг (КМ) и экстрамедуллярное поражение (ЭМ)) (РI – 14 , РII – 14 и РIII – 7), первично-рефрактерных – 2 и МОБ+ – 22. Число бластов КМ <50% выявлялось у 18 пациентов, а >50% у 19. Медиана уровня МОБ составила 0,35 (0,01-7,0)%. Б получили до ТГСК 42(71%) пациента, после ТГСК 17(29%). ТГСК (род-5, нерод-10, гапло-3, ауто-2) проведена после терапии Б 20 (34%) пациентам, из них 3 – повторная алло-ТГСК. У 9 больных после алло-ТГСК Б использовался в сочетании с инфузией донорских лимфоцитов (ИДЛ). Общее количество курсов Б составило от 1 до 7 (медиана 2).
Результаты
В группе МОБ+ негативный статус получен у 20 (91%) больных. Полная ремиссия (ПР) достигнута у 25 (68%)(в том числе 18 (72%) из них МОБ-): 13 (57%) пациентов при Р/РОЛЛ после ХТ, 12(86%) после алло-ТГСК. Частота достижения ПР была выше в группе больных с числом бластов <50% (78%(14/18) против 58%(11/19)). После терапии Б у 3 пациентов отмечалась ЭМ прогрессия ОЛЛ. РОЛЛ возник у 16(36%) больных: МОБ+ – 1, КМ – 11, ЭМ – 3, комбинированный – 1. В группах МОБ+ и Р/РОЛЛ 2хлетняя безрецидивная выживаемость (2БРВ) составили 62% (95%CI 35-89%) и 28%( 95%CI 6-50%), соответственно. В группах МОБ+ и Р/РОЛЛ 2хлетняя частота рецидивов (2ЧР) составили 38% (95%CI 4-60%) и 53% (95%CI 25-74%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии Б 2БРВ и 2ЧР составили 59% (95%CI 24-85%) против 30% (95%CI 7-53%) р=.08 и 27% (95%CI 7-52%) против 61% (95%CI 30-81%) р=.06, соответственно. Токсичность: гематологическая ≥3 степени (нейтропения, тромбоцитопения) наблюдалась у 15 (25%) больных, печеночная ≥3 степени – у 5(8%), неврологическая – у 11 (19%), синдром «высвобождения цитокин» наблюдался у 4 (7%). У 54 (92%) пациентов токсические явления были обратимы, и только у 5 (8%) больных терапия была прекращена досрочно. Только у 1 пациента после Б в сочетании с ИДЛ развилась оРТПХ (кожа 3 степени).
Заключение
Б в лечении МОБ+ и Р/РОЛЛ показал высокую эффективность и приемлемую токсичность. Частота достижения ПР выше при лечении Б Р/РОЛЛ после алло-ТГСК.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
Ключевые слова
Острый лимфобластный лейкоз, таргетная терапия, блинатумомаб.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20311" ["VALUE"]=> array(2) { ["TEXT"]=> string(988) "Sergey N. Bondarenko <sup>1</sup>, Elena N. Parovichnikova <sup>2</sup>, Alexey A. Maschan <sup>3</sup>, Olga Y. Baranova <sup>4</sup>, Tatyana V. Shelehova <sup>5</sup>, Vadim A. Doronin <sup>6</sup>, Vladimir Ya. Melnichenko <sup>7</sup>, Kamil D. Kaplanov <sup>8</sup>, Olga S. Uspenskaya <sup>9</sup>, Andrej N. Sokolov <sup>2</sup>, Natalya V. Myakova <sup>3</sup>, Ivan S. Moiseev <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Anna G. Smirnova <sup>1</sup>, Tatiana A. Bykova <sup>1</sup>, Bella I. Ayubova <sup>1</sup>, Irina A. Samorodova <sup>1</sup>, Elena V. Babenko <sup>1</sup>, Ildar M. Barkhatov <sup>1</sup>, Tatyana L. Gindina <sup>1</sup>, Alexander D. Kulagin <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "TEXT" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(724) "Sergey N. Bondarenko 1, Elena N. Parovichnikova 2, Alexey A. Maschan 3, Olga Y. Baranova 4, Tatyana V. Shelehova 5, Vadim A. Doronin 6, Vladimir Ya. Melnichenko 7, Kamil D. Kaplanov 8, Olga S. Uspenskaya 9, Andrej N. Sokolov 2, Natalya V. Myakova 3, Ivan S. Moiseev 1, Elena I. Darskaya 1, Anna G. Smirnova 1, Tatiana A. Bykova 1, Bella I. Ayubova 1, Irina A. Samorodova 1, Elena V. Babenko 1, Ildar M. Barkhatov 1, Tatyana L. Gindina 1, Alexander D. Kulagin 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "TEXT" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20312" ["VALUE"]=> array(2) { ["TEXT"]=> string(1137) "<sup>1</sup> Raisa Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, St. Petersburg First I. Pavlov State Medical University, St. Petersburg, Russian Federation<br> <sup>2</sup> National Research Center for Hematology, Russian Ministry of Healthcare, Moscow, Russian Federation<br> <sup>3</sup> National Medical D. Rogachev Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation;<br> <sup>4</sup> National Medical NN Blokhin Research Center of Oncology, Moscow, Russian Federation<br> <sup>5</sup> Saratov State Medical VI Razumovsky University<br> <sup>6 </sup>City Clinical Hospital №40, Moscow, Russian Federation<br> <sup>7</sup> National NI Pirogov Medical and Surgical Center, Moscow, Russian Federation<br> <sup>8</sup> Regional Clinical Oncology Center, Volgograd, Russian Federation<br> <sup>9</sup> Leningrad Regional Clinical Hospital, St. Petersburg, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(975) "1 Raisa Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, St. Petersburg First I. Pavlov State Medical University, St. Petersburg, Russian Federation2 National Research Center for Hematology, Russian Ministry of Healthcare, Moscow, Russian Federation
3 National Medical D. Rogachev Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation;
4 National Medical NN Blokhin Research Center of Oncology, Moscow, Russian Federation
5 Saratov State Medical VI Razumovsky University
6 City Clinical Hospital №40, Moscow, Russian Federation
7 National NI Pirogov Medical and Surgical Center, Moscow, Russian Federation
8 Regional Clinical Oncology Center, Volgograd, Russian Federation
9 Leningrad Regional Clinical Hospital, St. Petersburg, Russian Federation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20349" ["VALUE"]=> array(2) { ["TEXT"]=> string(3965) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> The results of therapy of patients with positive minimal residual disease (MRD+), relapses and refractory acute B-lymphoblastic leukemia (R/R ALL), especially after allogeneic hematopoietic stem cell transplantation (allo-HSCT), remain very poor. The possibilities of chemotherapy (CT) have been exhausted, new therapies is necessary. Blinatumomab (Btm) is a bispecific T-cell engager antibody construct with dual specificity for CD19 and CD3. Therapy with Btm may help to overcome the resistance to chemotherapy (CT) with minimal toxicity, and may be used both before and after HSCT because of low toxicity. Aim was to evaluate the efficacy and safety of Btm in MRD+ and R/R ALL. Patients and methods The study included 59 pts from 10 Russian hematological centers with CD19+ ALL. The median age was 28 (18-62) years. The diagnosis was ALL B-I (EGIL) subtype in 15 pts, B-II, in 37 cases; B-III, in 18 patients, and 1 patient had AL with a mixed phenotype (B/myelo). There were 35 pts in the relapse, 4 of them, with combined lesions bone marrow, i.e., bone marrow (BM) and extramedullary (EM) (RI-14, RII- 14 and RIII-7); primary-refractory disease was documented in 2 cases, and MRD+ was found in 22 pts. The number of BM blasts <50% was detected in 18 pts, and > 50%, in 19 cases. The median MRD level was 0.35 (0.01-7.0)%. Btm was administered to 42 pts (71%) before HSCT, and to 17 patients (29%) after HSCT. The HSCT (related-5, unrelated-10, haplo-3, auto-2) was performed after Btm therapy in 20 pts (34%), 3 of them underwent second allo-HSCT. In 9 pts after allo-HSCT, Btm was used in combination with donor lymphocyte infusion (DLI). The total number of Btm courses was 1 to 7 (median 2). Results In the MRD+ group, negative molecular status was obtained in 20 pts (91%). Complete remission (CR) was achieved in 25 cases (68%) including 18 MRD-negative cases (72%): 13(57%) pts with R/R ALL after CT, 12 (86%), after alloHSCT. Incidence of CR was higher in the group of pts with blasts <50% [78% (14/18) versus 58% (11/19)]. After Btm therapy, 3 pts experienced EM progression of ALL. Relapses developed in 16 pts (36%): MRD+, in 1; BM, in 11; EM, in 3; combined, in one case. In the MRD+ and R/R ALL groups, the 2-year disease-free survival rates (2DFS) were 62% (95% CI 35-89%) versus 28% (95% CI 6-50%), respectively. In MRD + and R/R ALL groups, the 2-year relapse rate (2RR) was 38% (95% CI 4-60%), and 53% (95% CI 25-74%), respectively. Depending on alloHSCT or no transplant after Btm therapy, the 2DFS and 2RR were 59% (95% CI 24-85%) versus 30% (95% CI 7-53%, p=.08), and 27% (95% CI 7-52%) versus 61% (95% CI 30-81%, p=.06), respectively. Hematological toxicity: grade 3 (neutropenia, thrombocytopenia) was observed in 15 pts (25%), hepatic toxicity grade ≥3 was documented in 5 pts (8%); neurotoxicity manifested in 11 pts (19%); the “cytokine release” syndrome was observed in 4 pts (7%). The toxic events in 54 pts (92%) were reversible, and only 5(8%) pts were terminated their treatment prematurely. Only 1 patient after B in combination with the DLI developed aGVHD (skin, grade 3). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Btm treatment in MRD+ and R/R ALL showed high efficacy and acceptable toxicity. Frequency of CR achievement is higher in Btm treatment for R/R ALL after allo-HSCT. </p> <h2 style="text-align: justify;">Disclosure</h2> <p style="text-align: justify;"> The authors report no conflicts of interest in this work. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Acute lymphoblastic leukemia, target therapy, blinatumomab. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3777) "
Introduction
The results of therapy of patients with positive minimal residual disease (MRD+), relapses and refractory acute B-lymphoblastic leukemia (R/R ALL), especially after allogeneic hematopoietic stem cell transplantation (allo-HSCT), remain very poor. The possibilities of chemotherapy (CT) have been exhausted, new therapies is necessary. Blinatumomab (Btm) is a bispecific T-cell engager antibody construct with dual specificity for CD19 and CD3. Therapy with Btm may help to overcome the resistance to chemotherapy (CT) with minimal toxicity, and may be used both before and after HSCT because of low toxicity. Aim was to evaluate the efficacy and safety of Btm in MRD+ and R/R ALL. Patients and methods The study included 59 pts from 10 Russian hematological centers with CD19+ ALL. The median age was 28 (18-62) years. The diagnosis was ALL B-I (EGIL) subtype in 15 pts, B-II, in 37 cases; B-III, in 18 patients, and 1 patient had AL with a mixed phenotype (B/myelo). There were 35 pts in the relapse, 4 of them, with combined lesions bone marrow, i.e., bone marrow (BM) and extramedullary (EM) (RI-14, RII- 14 and RIII-7); primary-refractory disease was documented in 2 cases, and MRD+ was found in 22 pts. The number of BM blasts <50% was detected in 18 pts, and > 50%, in 19 cases. The median MRD level was 0.35 (0.01-7.0)%. Btm was administered to 42 pts (71%) before HSCT, and to 17 patients (29%) after HSCT. The HSCT (related-5, unrelated-10, haplo-3, auto-2) was performed after Btm therapy in 20 pts (34%), 3 of them underwent second allo-HSCT. In 9 pts after allo-HSCT, Btm was used in combination with donor lymphocyte infusion (DLI). The total number of Btm courses was 1 to 7 (median 2). Results In the MRD+ group, negative molecular status was obtained in 20 pts (91%). Complete remission (CR) was achieved in 25 cases (68%) including 18 MRD-negative cases (72%): 13(57%) pts with R/R ALL after CT, 12 (86%), after alloHSCT. Incidence of CR was higher in the group of pts with blasts <50% [78% (14/18) versus 58% (11/19)]. After Btm therapy, 3 pts experienced EM progression of ALL. Relapses developed in 16 pts (36%): MRD+, in 1; BM, in 11; EM, in 3; combined, in one case. In the MRD+ and R/R ALL groups, the 2-year disease-free survival rates (2DFS) were 62% (95% CI 35-89%) versus 28% (95% CI 6-50%), respectively. In MRD + and R/R ALL groups, the 2-year relapse rate (2RR) was 38% (95% CI 4-60%), and 53% (95% CI 25-74%), respectively. Depending on alloHSCT or no transplant after Btm therapy, the 2DFS and 2RR were 59% (95% CI 24-85%) versus 30% (95% CI 7-53%, p=.08), and 27% (95% CI 7-52%) versus 61% (95% CI 30-81%, p=.06), respectively. Hematological toxicity: grade 3 (neutropenia, thrombocytopenia) was observed in 15 pts (25%), hepatic toxicity grade ≥3 was documented in 5 pts (8%); neurotoxicity manifested in 11 pts (19%); the “cytokine release” syndrome was observed in 4 pts (7%). The toxic events in 54 pts (92%) were reversible, and only 5(8%) pts were terminated their treatment prematurely. Only 1 patient after B in combination with the DLI developed aGVHD (skin, grade 3).
Conclusion
Btm treatment in MRD+ and R/R ALL showed high efficacy and acceptable toxicity. Frequency of CR achievement is higher in Btm treatment for R/R ALL after allo-HSCT.
Disclosure
The authors report no conflicts of interest in this work.
Keywords
Acute lymphoblastic leukemia, target therapy, blinatumomab.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20313" ["VALUE"]=> string(71) "Efficacy and toxicity of blinatumomab in acute B-lymphoblastic leukemia" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(71) "Efficacy and toxicity of blinatumomab in acute B-lymphoblastic leukemia" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20741" ["VALUE"]=> string(4) "1377" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1377" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20742" ["VALUE"]=> string(4) "1378" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1378" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20311" ["VALUE"]=> array(2) { ["TEXT"]=> string(988) "Sergey N. Bondarenko <sup>1</sup>, Elena N. Parovichnikova <sup>2</sup>, Alexey A. Maschan <sup>3</sup>, Olga Y. Baranova <sup>4</sup>, Tatyana V. Shelehova <sup>5</sup>, Vadim A. Doronin <sup>6</sup>, Vladimir Ya. Melnichenko <sup>7</sup>, Kamil D. Kaplanov <sup>8</sup>, Olga S. Uspenskaya <sup>9</sup>, Andrej N. Sokolov <sup>2</sup>, Natalya V. Myakova <sup>3</sup>, Ivan S. Moiseev <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Anna G. Smirnova <sup>1</sup>, Tatiana A. Bykova <sup>1</sup>, Bella I. Ayubova <sup>1</sup>, Irina A. Samorodova <sup>1</sup>, Elena V. Babenko <sup>1</sup>, Ildar M. Barkhatov <sup>1</sup>, Tatyana L. Gindina <sup>1</sup>, Alexander D. Kulagin <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "TEXT" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(724) "Sergey N. Bondarenko 1, Elena N. Parovichnikova 2, Alexey A. Maschan 3, Olga Y. Baranova 4, Tatyana V. Shelehova 5, Vadim A. Doronin 6, Vladimir Ya. Melnichenko 7, Kamil D. Kaplanov 8, Olga S. Uspenskaya 9, Andrej N. Sokolov 2, Natalya V. Myakova 3, Ivan S. Moiseev 1, Elena I. Darskaya 1, Anna G. Smirnova 1, Tatiana A. Bykova 1, Bella I. Ayubova 1, Irina A. Samorodova 1, Elena V. Babenko 1, Ildar M. Barkhatov 1, Tatyana L. Gindina 1, Alexander D. Kulagin 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "TEXT" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(988) "Sergey N. Bondarenko <sup>1</sup>, Elena N. Parovichnikova <sup>2</sup>, Alexey A. Maschan <sup>3</sup>, Olga Y. Baranova <sup>4</sup>, Tatyana V. Shelehova <sup>5</sup>, Vadim A. Doronin <sup>6</sup>, Vladimir Ya. Melnichenko <sup>7</sup>, Kamil D. Kaplanov <sup>8</sup>, Olga S. Uspenskaya <sup>9</sup>, Andrej N. Sokolov <sup>2</sup>, Natalya V. Myakova <sup>3</sup>, Ivan S. Moiseev <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Anna G. Smirnova <sup>1</sup>, Tatiana A. Bykova <sup>1</sup>, Bella I. Ayubova <sup>1</sup>, Irina A. Samorodova <sup>1</sup>, Elena V. Babenko <sup>1</sup>, Ildar M. Barkhatov <sup>1</sup>, Tatyana L. Gindina <sup>1</sup>, Alexander D. Kulagin <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20349" ["VALUE"]=> array(2) { ["TEXT"]=> string(3965) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> The results of therapy of patients with positive minimal residual disease (MRD+), relapses and refractory acute B-lymphoblastic leukemia (R/R ALL), especially after allogeneic hematopoietic stem cell transplantation (allo-HSCT), remain very poor. The possibilities of chemotherapy (CT) have been exhausted, new therapies is necessary. Blinatumomab (Btm) is a bispecific T-cell engager antibody construct with dual specificity for CD19 and CD3. Therapy with Btm may help to overcome the resistance to chemotherapy (CT) with minimal toxicity, and may be used both before and after HSCT because of low toxicity. Aim was to evaluate the efficacy and safety of Btm in MRD+ and R/R ALL. Patients and methods The study included 59 pts from 10 Russian hematological centers with CD19+ ALL. The median age was 28 (18-62) years. The diagnosis was ALL B-I (EGIL) subtype in 15 pts, B-II, in 37 cases; B-III, in 18 patients, and 1 patient had AL with a mixed phenotype (B/myelo). There were 35 pts in the relapse, 4 of them, with combined lesions bone marrow, i.e., bone marrow (BM) and extramedullary (EM) (RI-14, RII- 14 and RIII-7); primary-refractory disease was documented in 2 cases, and MRD+ was found in 22 pts. The number of BM blasts <50% was detected in 18 pts, and > 50%, in 19 cases. The median MRD level was 0.35 (0.01-7.0)%. Btm was administered to 42 pts (71%) before HSCT, and to 17 patients (29%) after HSCT. The HSCT (related-5, unrelated-10, haplo-3, auto-2) was performed after Btm therapy in 20 pts (34%), 3 of them underwent second allo-HSCT. In 9 pts after allo-HSCT, Btm was used in combination with donor lymphocyte infusion (DLI). The total number of Btm courses was 1 to 7 (median 2). Results In the MRD+ group, negative molecular status was obtained in 20 pts (91%). Complete remission (CR) was achieved in 25 cases (68%) including 18 MRD-negative cases (72%): 13(57%) pts with R/R ALL after CT, 12 (86%), after alloHSCT. Incidence of CR was higher in the group of pts with blasts <50% [78% (14/18) versus 58% (11/19)]. After Btm therapy, 3 pts experienced EM progression of ALL. Relapses developed in 16 pts (36%): MRD+, in 1; BM, in 11; EM, in 3; combined, in one case. In the MRD+ and R/R ALL groups, the 2-year disease-free survival rates (2DFS) were 62% (95% CI 35-89%) versus 28% (95% CI 6-50%), respectively. In MRD + and R/R ALL groups, the 2-year relapse rate (2RR) was 38% (95% CI 4-60%), and 53% (95% CI 25-74%), respectively. Depending on alloHSCT or no transplant after Btm therapy, the 2DFS and 2RR were 59% (95% CI 24-85%) versus 30% (95% CI 7-53%, p=.08), and 27% (95% CI 7-52%) versus 61% (95% CI 30-81%, p=.06), respectively. Hematological toxicity: grade 3 (neutropenia, thrombocytopenia) was observed in 15 pts (25%), hepatic toxicity grade ≥3 was documented in 5 pts (8%); neurotoxicity manifested in 11 pts (19%); the “cytokine release” syndrome was observed in 4 pts (7%). The toxic events in 54 pts (92%) were reversible, and only 5(8%) pts were terminated their treatment prematurely. Only 1 patient after B in combination with the DLI developed aGVHD (skin, grade 3). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Btm treatment in MRD+ and R/R ALL showed high efficacy and acceptable toxicity. Frequency of CR achievement is higher in Btm treatment for R/R ALL after allo-HSCT. </p> <h2 style="text-align: justify;">Disclosure</h2> <p style="text-align: justify;"> The authors report no conflicts of interest in this work. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Acute lymphoblastic leukemia, target therapy, blinatumomab. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3777) "Introduction
The results of therapy of patients with positive minimal residual disease (MRD+), relapses and refractory acute B-lymphoblastic leukemia (R/R ALL), especially after allogeneic hematopoietic stem cell transplantation (allo-HSCT), remain very poor. The possibilities of chemotherapy (CT) have been exhausted, new therapies is necessary. Blinatumomab (Btm) is a bispecific T-cell engager antibody construct with dual specificity for CD19 and CD3. Therapy with Btm may help to overcome the resistance to chemotherapy (CT) with minimal toxicity, and may be used both before and after HSCT because of low toxicity. Aim was to evaluate the efficacy and safety of Btm in MRD+ and R/R ALL. Patients and methods The study included 59 pts from 10 Russian hematological centers with CD19+ ALL. The median age was 28 (18-62) years. The diagnosis was ALL B-I (EGIL) subtype in 15 pts, B-II, in 37 cases; B-III, in 18 patients, and 1 patient had AL with a mixed phenotype (B/myelo). There were 35 pts in the relapse, 4 of them, with combined lesions bone marrow, i.e., bone marrow (BM) and extramedullary (EM) (RI-14, RII- 14 and RIII-7); primary-refractory disease was documented in 2 cases, and MRD+ was found in 22 pts. The number of BM blasts <50% was detected in 18 pts, and > 50%, in 19 cases. The median MRD level was 0.35 (0.01-7.0)%. Btm was administered to 42 pts (71%) before HSCT, and to 17 patients (29%) after HSCT. The HSCT (related-5, unrelated-10, haplo-3, auto-2) was performed after Btm therapy in 20 pts (34%), 3 of them underwent second allo-HSCT. In 9 pts after allo-HSCT, Btm was used in combination with donor lymphocyte infusion (DLI). The total number of Btm courses was 1 to 7 (median 2). Results In the MRD+ group, negative molecular status was obtained in 20 pts (91%). Complete remission (CR) was achieved in 25 cases (68%) including 18 MRD-negative cases (72%): 13(57%) pts with R/R ALL after CT, 12 (86%), after alloHSCT. Incidence of CR was higher in the group of pts with blasts <50% [78% (14/18) versus 58% (11/19)]. After Btm therapy, 3 pts experienced EM progression of ALL. Relapses developed in 16 pts (36%): MRD+, in 1; BM, in 11; EM, in 3; combined, in one case. In the MRD+ and R/R ALL groups, the 2-year disease-free survival rates (2DFS) were 62% (95% CI 35-89%) versus 28% (95% CI 6-50%), respectively. In MRD + and R/R ALL groups, the 2-year relapse rate (2RR) was 38% (95% CI 4-60%), and 53% (95% CI 25-74%), respectively. Depending on alloHSCT or no transplant after Btm therapy, the 2DFS and 2RR were 59% (95% CI 24-85%) versus 30% (95% CI 7-53%, p=.08), and 27% (95% CI 7-52%) versus 61% (95% CI 30-81%, p=.06), respectively. Hematological toxicity: grade 3 (neutropenia, thrombocytopenia) was observed in 15 pts (25%), hepatic toxicity grade ≥3 was documented in 5 pts (8%); neurotoxicity manifested in 11 pts (19%); the “cytokine release” syndrome was observed in 4 pts (7%). The toxic events in 54 pts (92%) were reversible, and only 5(8%) pts were terminated their treatment prematurely. Only 1 patient after B in combination with the DLI developed aGVHD (skin, grade 3).
Conclusion
Btm treatment in MRD+ and R/R ALL showed high efficacy and acceptable toxicity. Frequency of CR achievement is higher in Btm treatment for R/R ALL after allo-HSCT.
Disclosure
The authors report no conflicts of interest in this work.
Keywords
Acute lymphoblastic leukemia, target therapy, blinatumomab.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3777) "Introduction
The results of therapy of patients with positive minimal residual disease (MRD+), relapses and refractory acute B-lymphoblastic leukemia (R/R ALL), especially after allogeneic hematopoietic stem cell transplantation (allo-HSCT), remain very poor. The possibilities of chemotherapy (CT) have been exhausted, new therapies is necessary. Blinatumomab (Btm) is a bispecific T-cell engager antibody construct with dual specificity for CD19 and CD3. Therapy with Btm may help to overcome the resistance to chemotherapy (CT) with minimal toxicity, and may be used both before and after HSCT because of low toxicity. Aim was to evaluate the efficacy and safety of Btm in MRD+ and R/R ALL. Patients and methods The study included 59 pts from 10 Russian hematological centers with CD19+ ALL. The median age was 28 (18-62) years. The diagnosis was ALL B-I (EGIL) subtype in 15 pts, B-II, in 37 cases; B-III, in 18 patients, and 1 patient had AL with a mixed phenotype (B/myelo). There were 35 pts in the relapse, 4 of them, with combined lesions bone marrow, i.e., bone marrow (BM) and extramedullary (EM) (RI-14, RII- 14 and RIII-7); primary-refractory disease was documented in 2 cases, and MRD+ was found in 22 pts. The number of BM blasts <50% was detected in 18 pts, and > 50%, in 19 cases. The median MRD level was 0.35 (0.01-7.0)%. Btm was administered to 42 pts (71%) before HSCT, and to 17 patients (29%) after HSCT. The HSCT (related-5, unrelated-10, haplo-3, auto-2) was performed after Btm therapy in 20 pts (34%), 3 of them underwent second allo-HSCT. In 9 pts after allo-HSCT, Btm was used in combination with donor lymphocyte infusion (DLI). The total number of Btm courses was 1 to 7 (median 2). Results In the MRD+ group, negative molecular status was obtained in 20 pts (91%). Complete remission (CR) was achieved in 25 cases (68%) including 18 MRD-negative cases (72%): 13(57%) pts with R/R ALL after CT, 12 (86%), after alloHSCT. Incidence of CR was higher in the group of pts with blasts <50% [78% (14/18) versus 58% (11/19)]. After Btm therapy, 3 pts experienced EM progression of ALL. Relapses developed in 16 pts (36%): MRD+, in 1; BM, in 11; EM, in 3; combined, in one case. In the MRD+ and R/R ALL groups, the 2-year disease-free survival rates (2DFS) were 62% (95% CI 35-89%) versus 28% (95% CI 6-50%), respectively. In MRD + and R/R ALL groups, the 2-year relapse rate (2RR) was 38% (95% CI 4-60%), and 53% (95% CI 25-74%), respectively. Depending on alloHSCT or no transplant after Btm therapy, the 2DFS and 2RR were 59% (95% CI 24-85%) versus 30% (95% CI 7-53%, p=.08), and 27% (95% CI 7-52%) versus 61% (95% CI 30-81%, p=.06), respectively. Hematological toxicity: grade 3 (neutropenia, thrombocytopenia) was observed in 15 pts (25%), hepatic toxicity grade ≥3 was documented in 5 pts (8%); neurotoxicity manifested in 11 pts (19%); the “cytokine release” syndrome was observed in 4 pts (7%). The toxic events in 54 pts (92%) were reversible, and only 5(8%) pts were terminated their treatment prematurely. Only 1 patient after B in combination with the DLI developed aGVHD (skin, grade 3).
Conclusion
Btm treatment in MRD+ and R/R ALL showed high efficacy and acceptable toxicity. Frequency of CR achievement is higher in Btm treatment for R/R ALL after allo-HSCT.
Disclosure
The authors report no conflicts of interest in this work.
Keywords
Acute lymphoblastic leukemia, target therapy, blinatumomab.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20313" ["VALUE"]=> string(71) "Efficacy and toxicity of blinatumomab in acute B-lymphoblastic leukemia" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(71) "Efficacy and toxicity of blinatumomab in acute B-lymphoblastic leukemia" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(71) "Efficacy and toxicity of blinatumomab in acute B-lymphoblastic leukemia" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20312" ["VALUE"]=> array(2) { ["TEXT"]=> string(1137) "<sup>1</sup> Raisa Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, St. Petersburg First I. Pavlov State Medical University, St. Petersburg, Russian Federation<br> <sup>2</sup> National Research Center for Hematology, Russian Ministry of Healthcare, Moscow, Russian Federation<br> <sup>3</sup> National Medical D. Rogachev Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation;<br> <sup>4</sup> National Medical NN Blokhin Research Center of Oncology, Moscow, Russian Federation<br> <sup>5</sup> Saratov State Medical VI Razumovsky University<br> <sup>6 </sup>City Clinical Hospital №40, Moscow, Russian Federation<br> <sup>7</sup> National NI Pirogov Medical and Surgical Center, Moscow, Russian Federation<br> <sup>8</sup> Regional Clinical Oncology Center, Volgograd, Russian Federation<br> <sup>9</sup> Leningrad Regional Clinical Hospital, St. Petersburg, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(975) "1 Raisa Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, St. Petersburg First I. Pavlov State Medical University, St. Petersburg, Russian Federation2 National Research Center for Hematology, Russian Ministry of Healthcare, Moscow, Russian Federation
3 National Medical D. Rogachev Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation;
4 National Medical NN Blokhin Research Center of Oncology, Moscow, Russian Federation
5 Saratov State Medical VI Razumovsky University
6 City Clinical Hospital №40, Moscow, Russian Federation
7 National NI Pirogov Medical and Surgical Center, Moscow, Russian Federation
8 Regional Clinical Oncology Center, Volgograd, Russian Federation
9 Leningrad Regional Clinical Hospital, St. Petersburg, Russian Federation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(975) "1 Raisa Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, St. Petersburg First I. Pavlov State Medical University, St. Petersburg, Russian Federation
2 National Research Center for Hematology, Russian Ministry of Healthcare, Moscow, Russian Federation
3 National Medical D. Rogachev Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation;
4 National Medical NN Blokhin Research Center of Oncology, Moscow, Russian Federation
5 Saratov State Medical VI Razumovsky University
6 City Clinical Hospital №40, Moscow, Russian Federation
7 National NI Pirogov Medical and Surgical Center, Moscow, Russian Federation
8 Regional Clinical Oncology Center, Volgograd, Russian Federation
9 Leningrad Regional Clinical Hospital, St. Petersburg, Russian Federation
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20309" ["VALUE"]=> array(2) { ["TEXT"]=> string(1310) "Сергей Н. Бондаренко <sup>1</sup>, Елена Н. Паровичникова <sup>2</sup>, Алексей А. Масчан <sup>3</sup>, Ольга Ю. Баранова <sup>4</sup>, Татьяна В. Шелехова <sup>5</sup>, Вадим А. Доронин <sup>6</sup>, Владимир Я. Мельниченко <sup>7</sup>, Камиль Д. Капланов <sup>8</sup>, Ольга С. Успенская <sup>9</sup>, Андрей Н. Соколов <sup>2</sup>, Наталья В. Мякова <sup>3</sup>, Иван С. Моисеев <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Анна Г. Смирнова <sup>1</sup>, Татьяна А. Быкова <sup>1</sup>, Белла И. Аюбова <sup>1</sup>, Ирина А. Самородова <sup>1</sup>, Елена В. Бабенко <sup>1</sup>, Ильдар М. Бархатов <sup>1</sup>, Татьяна Л. Гиндина <sup>1</sup>, Александр Д. Кулагин <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "TEXT" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1046) "Сергей Н. Бондаренко 1, Елена Н. Паровичникова 2, Алексей А. Масчан 3, Ольга Ю. Баранова 4, Татьяна В. Шелехова 5, Вадим А. Доронин 6, Владимир Я. Мельниченко 7, Камиль Д. Капланов 8, Ольга С. Успенская 9, Андрей Н. Соколов 2, Наталья В. Мякова 3, Иван С. Моисеев 1, Елена И. Дарская 1, Анна Г. Смирнова 1, Татьяна А. Быкова 1, Белла И. Аюбова 1, Ирина А. Самородова 1, Елена В. Бабенко 1, Ильдар М. Бархатов 1, Татьяна Л. Гиндина 1, Александр Д. Кулагин 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "TEXT" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(1310) "Сергей Н. Бондаренко <sup>1</sup>, Елена Н. Паровичникова <sup>2</sup>, Алексей А. Масчан <sup>3</sup>, Ольга Ю. Баранова <sup>4</sup>, Татьяна В. Шелехова <sup>5</sup>, Вадим А. Доронин <sup>6</sup>, Владимир Я. Мельниченко <sup>7</sup>, Камиль Д. Капланов <sup>8</sup>, Ольга С. Успенская <sup>9</sup>, Андрей Н. Соколов <sup>2</sup>, Наталья В. Мякова <sup>3</sup>, Иван С. Моисеев <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Анна Г. Смирнова <sup>1</sup>, Татьяна А. Быкова <sup>1</sup>, Белла И. Аюбова <sup>1</sup>, Ирина А. Самородова <sup>1</sup>, Елена В. Бабенко <sup>1</sup>, Ильдар М. Бархатов <sup>1</sup>, Татьяна Л. Гиндина <sup>1</sup>, Александр Д. Кулагин <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20348" ["VALUE"]=> array(2) { ["TEXT"]=> string(6406) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Результаты терапии пациентов с положительной минимальной остаточной болезнью (МОБ+), рецидивами и рефрактерным течением острого В-лимфобластного лейкоза (Р/РОЛЛ), особенно после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), остаются неудовлетворительными. Возможности химиотерапии (ХТ) исчерпаны, что обуславливает необходимость использования новых методов терапии. Блинатумомаб (Б) является генно-инженерным антителом, активатором Т-клеток, биспецифичным по отношению к CD19 и CD3. Б помогает преодолеть резистентность к ХТ и может использоваться как до, так и после ТГСК за счет низкой токсичности. </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Оценить эффективность и безопасность Б при МОБ+ и Р/РОЛЛ. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В исследование включено 59 больных из 10 гематологических центров РФ с CD19+ОЛЛ. Медиана возраста составила 28 (18-62) лет. К B-I варианту относились 15 пациентов, B-II – 37, B-III – 18, и 1 больной имел ОЛ со смешанный фенотипом (В/миело). В рецидиве (Р) находилось 35 больных, из них 4 в комбинированном (костный мозг (КМ) и экстрамедуллярное поражение (ЭМ)) (РI – 14 , РII – 14 и РIII – 7), первично-рефрактерных – 2 и МОБ+ – 22. Число бластов КМ <50% выявлялось у 18 пациентов, а >50% у 19. Медиана уровня МОБ составила 0,35 (0,01-7,0)%. Б получили до ТГСК 42(71%) пациента, после ТГСК 17(29%). ТГСК (род-5, нерод-10, гапло-3, ауто-2) проведена после терапии Б 20 (34%) пациентам, из них 3 – повторная алло-ТГСК. У 9 больных после алло-ТГСК Б использовался в сочетании с инфузией донорских лимфоцитов (ИДЛ). Общее количество курсов Б составило от 1 до 7 (медиана 2). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> В группе МОБ+ негативный статус получен у 20 (91%) больных. Полная ремиссия (ПР) достигнута у 25 (68%)(в том числе 18 (72%) из них МОБ-): 13 (57%) пациентов при Р/РОЛЛ после ХТ, 12(86%) после алло-ТГСК. Частота достижения ПР была выше в группе больных с числом бластов <50% (78%(14/18) против 58%(11/19)). После терапии Б у 3 пациентов отмечалась ЭМ прогрессия ОЛЛ. РОЛЛ возник у 16(36%) больных: МОБ+ – 1, КМ – 11, ЭМ – 3, комбинированный – 1. В группах МОБ+ и Р/РОЛЛ 2хлетняя безрецидивная выживаемость (2БРВ) составили 62% (95%CI 35-89%) и 28%( 95%CI 6-50%), соответственно. В группах МОБ+ и Р/РОЛЛ 2хлетняя частота рецидивов (2ЧР) составили 38% (95%CI 4-60%) и 53% (95%CI 25-74%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии Б 2БРВ и 2ЧР составили 59% (95%CI 24-85%) против 30% (95%CI 7-53%) р=.08 и 27% (95%CI 7-52%) против 61% (95%CI 30-81%) р=.06, соответственно. Токсичность: гематологическая ≥3 степени (нейтропения, тромбоцитопения) наблюдалась у 15 (25%) больных, печеночная ≥3 степени – у 5(8%), неврологическая – у 11 (19%), синдром «высвобождения цитокин» наблюдался у 4 (7%). У 54 (92%) пациентов токсические явления были обратимы, и только у 5 (8%) больных терапия была прекращена досрочно. Только у 1 пациента после Б в сочетании с ИДЛ развилась оРТПХ (кожа 3 степени). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Б в лечении МОБ+ и Р/РОЛЛ показал высокую эффективность и приемлемую токсичность. Частота достижения ПР выше при лечении Б Р/РОЛЛ после алло-ТГСК. </p> <h2 style="text-align: justify;">Комментарии</h2> <p style="text-align: justify;"> Авторы заявляют об отсутствии скрытого конфликта интересов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый лимфобластный лейкоз, таргетная терапия, блинатумомаб. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6086) "
Введение
Результаты терапии пациентов с положительной минимальной остаточной болезнью (МОБ+), рецидивами и рефрактерным течением острого В-лимфобластного лейкоза (Р/РОЛЛ), особенно после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), остаются неудовлетворительными. Возможности химиотерапии (ХТ) исчерпаны, что обуславливает необходимость использования новых методов терапии. Блинатумомаб (Б) является генно-инженерным антителом, активатором Т-клеток, биспецифичным по отношению к CD19 и CD3. Б помогает преодолеть резистентность к ХТ и может использоваться как до, так и после ТГСК за счет низкой токсичности.
Цель работы
Оценить эффективность и безопасность Б при МОБ+ и Р/РОЛЛ.
Пациенты и методы
В исследование включено 59 больных из 10 гематологических центров РФ с CD19+ОЛЛ. Медиана возраста составила 28 (18-62) лет. К B-I варианту относились 15 пациентов, B-II – 37, B-III – 18, и 1 больной имел ОЛ со смешанный фенотипом (В/миело). В рецидиве (Р) находилось 35 больных, из них 4 в комбинированном (костный мозг (КМ) и экстрамедуллярное поражение (ЭМ)) (РI – 14 , РII – 14 и РIII – 7), первично-рефрактерных – 2 и МОБ+ – 22. Число бластов КМ <50% выявлялось у 18 пациентов, а >50% у 19. Медиана уровня МОБ составила 0,35 (0,01-7,0)%. Б получили до ТГСК 42(71%) пациента, после ТГСК 17(29%). ТГСК (род-5, нерод-10, гапло-3, ауто-2) проведена после терапии Б 20 (34%) пациентам, из них 3 – повторная алло-ТГСК. У 9 больных после алло-ТГСК Б использовался в сочетании с инфузией донорских лимфоцитов (ИДЛ). Общее количество курсов Б составило от 1 до 7 (медиана 2).
Результаты
В группе МОБ+ негативный статус получен у 20 (91%) больных. Полная ремиссия (ПР) достигнута у 25 (68%)(в том числе 18 (72%) из них МОБ-): 13 (57%) пациентов при Р/РОЛЛ после ХТ, 12(86%) после алло-ТГСК. Частота достижения ПР была выше в группе больных с числом бластов <50% (78%(14/18) против 58%(11/19)). После терапии Б у 3 пациентов отмечалась ЭМ прогрессия ОЛЛ. РОЛЛ возник у 16(36%) больных: МОБ+ – 1, КМ – 11, ЭМ – 3, комбинированный – 1. В группах МОБ+ и Р/РОЛЛ 2хлетняя безрецидивная выживаемость (2БРВ) составили 62% (95%CI 35-89%) и 28%( 95%CI 6-50%), соответственно. В группах МОБ+ и Р/РОЛЛ 2хлетняя частота рецидивов (2ЧР) составили 38% (95%CI 4-60%) и 53% (95%CI 25-74%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии Б 2БРВ и 2ЧР составили 59% (95%CI 24-85%) против 30% (95%CI 7-53%) р=.08 и 27% (95%CI 7-52%) против 61% (95%CI 30-81%) р=.06, соответственно. Токсичность: гематологическая ≥3 степени (нейтропения, тромбоцитопения) наблюдалась у 15 (25%) больных, печеночная ≥3 степени – у 5(8%), неврологическая – у 11 (19%), синдром «высвобождения цитокин» наблюдался у 4 (7%). У 54 (92%) пациентов токсические явления были обратимы, и только у 5 (8%) больных терапия была прекращена досрочно. Только у 1 пациента после Б в сочетании с ИДЛ развилась оРТПХ (кожа 3 степени).
Заключение
Б в лечении МОБ+ и Р/РОЛЛ показал высокую эффективность и приемлемую токсичность. Частота достижения ПР выше при лечении Б Р/РОЛЛ после алло-ТГСК.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
Ключевые слова
Острый лимфобластный лейкоз, таргетная терапия, блинатумомаб.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6086) "Введение
Результаты терапии пациентов с положительной минимальной остаточной болезнью (МОБ+), рецидивами и рефрактерным течением острого В-лимфобластного лейкоза (Р/РОЛЛ), особенно после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), остаются неудовлетворительными. Возможности химиотерапии (ХТ) исчерпаны, что обуславливает необходимость использования новых методов терапии. Блинатумомаб (Б) является генно-инженерным антителом, активатором Т-клеток, биспецифичным по отношению к CD19 и CD3. Б помогает преодолеть резистентность к ХТ и может использоваться как до, так и после ТГСК за счет низкой токсичности.
Цель работы
Оценить эффективность и безопасность Б при МОБ+ и Р/РОЛЛ.
Пациенты и методы
В исследование включено 59 больных из 10 гематологических центров РФ с CD19+ОЛЛ. Медиана возраста составила 28 (18-62) лет. К B-I варианту относились 15 пациентов, B-II – 37, B-III – 18, и 1 больной имел ОЛ со смешанный фенотипом (В/миело). В рецидиве (Р) находилось 35 больных, из них 4 в комбинированном (костный мозг (КМ) и экстрамедуллярное поражение (ЭМ)) (РI – 14 , РII – 14 и РIII – 7), первично-рефрактерных – 2 и МОБ+ – 22. Число бластов КМ <50% выявлялось у 18 пациентов, а >50% у 19. Медиана уровня МОБ составила 0,35 (0,01-7,0)%. Б получили до ТГСК 42(71%) пациента, после ТГСК 17(29%). ТГСК (род-5, нерод-10, гапло-3, ауто-2) проведена после терапии Б 20 (34%) пациентам, из них 3 – повторная алло-ТГСК. У 9 больных после алло-ТГСК Б использовался в сочетании с инфузией донорских лимфоцитов (ИДЛ). Общее количество курсов Б составило от 1 до 7 (медиана 2).
Результаты
В группе МОБ+ негативный статус получен у 20 (91%) больных. Полная ремиссия (ПР) достигнута у 25 (68%)(в том числе 18 (72%) из них МОБ-): 13 (57%) пациентов при Р/РОЛЛ после ХТ, 12(86%) после алло-ТГСК. Частота достижения ПР была выше в группе больных с числом бластов <50% (78%(14/18) против 58%(11/19)). После терапии Б у 3 пациентов отмечалась ЭМ прогрессия ОЛЛ. РОЛЛ возник у 16(36%) больных: МОБ+ – 1, КМ – 11, ЭМ – 3, комбинированный – 1. В группах МОБ+ и Р/РОЛЛ 2хлетняя безрецидивная выживаемость (2БРВ) составили 62% (95%CI 35-89%) и 28%( 95%CI 6-50%), соответственно. В группах МОБ+ и Р/РОЛЛ 2хлетняя частота рецидивов (2ЧР) составили 38% (95%CI 4-60%) и 53% (95%CI 25-74%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии Б 2БРВ и 2ЧР составили 59% (95%CI 24-85%) против 30% (95%CI 7-53%) р=.08 и 27% (95%CI 7-52%) против 61% (95%CI 30-81%) р=.06, соответственно. Токсичность: гематологическая ≥3 степени (нейтропения, тромбоцитопения) наблюдалась у 15 (25%) больных, печеночная ≥3 степени – у 5(8%), неврологическая – у 11 (19%), синдром «высвобождения цитокин» наблюдался у 4 (7%). У 54 (92%) пациентов токсические явления были обратимы, и только у 5 (8%) больных терапия была прекращена досрочно. Только у 1 пациента после Б в сочетании с ИДЛ развилась оРТПХ (кожа 3 степени).
Заключение
Б в лечении МОБ+ и Р/РОЛЛ показал высокую эффективность и приемлемую токсичность. Частота достижения ПР выше при лечении Б Р/РОЛЛ после алло-ТГСК.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
Ключевые слова
Острый лимфобластный лейкоз, таргетная терапия, блинатумомаб.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20310" ["VALUE"]=> array(2) { ["TEXT"]=> string(1623) "<sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург<br> <sup>2</sup> Национальный медицинский исследовательский центр гематологии, Москва<br> <sup>3</sup> Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Д. Рогачева, Москва<br> <sup>4</sup> Национальный медицинский исследовательский центр онкологии им. Н. Н. Блохина, Москва<br> <sup>5</sup> Саратовский государственный медицинский университет им. В. И. Разумовского<br> <sup>6</sup> Городская клиническая больница №40 г. Москва<br> <sup>7</sup> Национальный медико-хирургический центр им. Н. И. Пирогова, Москва<br> <sup>8</sup> Волгоградский областной клинический онкологический диспансер<br> <sup>9</sup> Ленинградская областная клиническая больница, Санкт-Петербург<br>" ["TYPE"]=> string(4) "TEXT" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1461) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург2 Национальный медицинский исследовательский центр гематологии, Москва
3 Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Д. Рогачева, Москва
4 Национальный медицинский исследовательский центр онкологии им. Н. Н. Блохина, Москва
5 Саратовский государственный медицинский университет им. В. И. Разумовского
6 Городская клиническая больница №40 г. Москва
7 Национальный медико-хирургический центр им. Н. И. Пирогова, Москва
8 Волгоградский областной клинический онкологический диспансер
9 Ленинградская областная клиническая больница, Санкт-Петербург
" ["TYPE"]=> string(4) "TEXT" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(1663) "<sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург<br>
<sup>2</sup> Национальный медицинский исследовательский центр гематологии, Москва<br>
<sup>3</sup> Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Д. Рогачева, Москва<br>
<sup>4</sup> Национальный медицинский исследовательский центр онкологии им. Н. Н. Блохина, Москва<br>
<sup>5</sup> Саратовский государственный медицинский университет им. В. И. Разумовского<br>
<sup>6</sup> Городская клиническая больница №40 г. Москва<br>
<sup>7</sup> Национальный медико-хирургический центр им. Н. И. Пирогова, Москва<br>
<sup>8</sup> Волгоградский областной клинический онкологический диспансер<br>
<sup>9</sup> Ленинградская областная клиническая больница, Санкт-Петербург<br>" } } } [16]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1552" ["~ID"]=> string(4) "1552" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(208) "Сравнительный анализ in vitro активности NK-клеточных линий человека, экспрессирующих химерные антигенные рецепторы" ["~NAME"]=> string(208) "Сравнительный анализ in vitro активности NK-клеточных линий человека, экспрессирующих химерные антигенные рецепторы" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:24:12" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:24:12" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/sravnitelnyy-analiz-in-vitro-aktivnosti-nk-kletochnykh-liniy-cheloveka-ekspressiruyushchikh-khimerny/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/sravnitelnyy-analiz-in-vitro-aktivnosti-nk-kletochnykh-liniy-cheloveka-ekspressiruyushchikh-khimerny/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "sravnitelnyy-analiz-in-vitro-aktivnosti-nk-kletochnykh-liniy-cheloveka-ekspressiruyushchikh-khimerny" ["~CODE"]=> string(100) "sravnitelnyy-analiz-in-vitro-aktivnosti-nk-kletochnykh-liniy-cheloveka-ekspressiruyushchikh-khimerny" ["EXTERNAL_ID"]=> string(4) "1552" ["~EXTERNAL_ID"]=> string(4) "1552" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(208) "Сравнительный анализ in vitro активности NK-клеточных линий человека, экспрессирующих химерные антигенные рецепторы" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(298) "Сравнительный анализ in vitro активности NK-клеточных линий человека, экспрессирующих химерные антигенные рецепторыComparative in vitro analysis of human NK-cell lines expressing chimeric antigen receptors" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(5889) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Терапия Т-клетками, экспрессирующими химерные антигенные рецепторы (CAR), была одобрена FDA к клиническому использованию в августе 2017 года для больных с r/rALL. Несмотря на значительную эффективность, у CAR T-клеточной терапии существуют серьезные ограничения, связанные с высокой стоимостью, сложной стандартизацией и невозможностью получить CAR Т-клетки для отдельных пациентов. В связи с этим крайне привлекательным выглядит создание универсальных аллогенных CAR T-клеток, однако на существующем уровне развития инструментов геномного редактирования и селекции субпопуляций Т-клеток этот подход сопровождается риском развития реакции «трансплантат против хозяина». Возможным решением этих проблем может быть переход к иммортализованным NK-клеточным линиям в качестве носителей CAR. Подобные линии недорогие в наработке, могут быть стандартизованы и не вызывают реакцию «трансплантат против хозяина». К настоящему моменту описано несколько NK-клеточных линий человека, однако систематического сравнения их свойств в качестве носителей CAR проведено не было. </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> В данное исследование были включены три NK-клеточные иммортализованные линии человека (А, В и NK-92). На основе каждой из трех линий методом лентивирусной трансдукции были получены сублинии, стабильно экспрессирующие CAR, специфичный к белку человека CD20. После этого был измерен уровень цитотоксичности CAR-NK клеточных линий по отношению к CD20-положительным клеткам линии Raji (клетки лимфомы Бёркитта) и клеткам линии HEK293Т, эктопически экспрессирующим CD20, либо изогенным контрольным клеткам. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Все три полученные CAR-NK-клеточные линии обнаруживали значимый уровень цитотоксичности против клеток линии Raji, однако клетки NK-92 дикого типа также лизировали мишени Raji. В связи с этим, для более корректного сравнения уровней цитотоксичности CAR-NK-клеточных линий в тестах <i>in vitro</i> были получены клетки линии HEK293Т, экспрессирующие CD20. Уровень неспецифической цитотоксичности немодифицированных NK клеток против таких мишеней не превышал 20% в диапазоне эффектор: мишень=1-5, при этом уровень специфической, CAR-опосредованной цитотоксичности составлял 73% (CAR-NK-92), 55% (CAR-B) и 34% (CAR-A) при соотношении эффектор:-мишень=5. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Все полученные CAR-NK-клеточные линии проявляют значимый уровень цитотоксичности по отношению к CD20-позитивным клеткам-мишеням в тестах <i>in vitro</i>, и клетки линии NK-92 проявляют самый высокий уровень как специфической, так и неспецифической цитотоксичности. Необходимы дополнительные исследования <i>in vivo</i>, чтобы определить профили безопасности и эффективности CAR-NK эффекторов. </p> <h2 style="text-align: justify;">Благодарности</h2> <p style="text-align: justify;"> Работа выполнена при финансовой поддержке Минобрнауки РФ, соглашение № 14.604.21.0169 (уникальный идентификатор проекта RFMEFI60417X0169). </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Химерный антигенный рецептор, NK-клеточные линии, цитотоксичность. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(208) "Сравнительный анализ in vitro активности NK-клеточных линий человека, экспрессирующих химерные антигенные рецепторы" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(208) "Сравнительный анализ in vitro активности NK-клеточных линий человека, экспрессирующих химерные антигенные рецепторы" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(208) "Сравнительный анализ in vitro активности NK-клеточных линий человека, экспрессирующих химерные антигенные рецепторы" ["SECTION_META_TITLE"]=> string(208) "Сравнительный анализ in vitro активности NK-клеточных линий человека, экспрессирующих химерные антигенные рецепторы" ["SECTION_META_KEYWORDS"]=> string(208) "Сравнительный анализ in vitro активности NK-клеточных линий человека, экспрессирующих химерные антигенные рецепторы" ["SECTION_META_DESCRIPTION"]=> string(208) "Сравнительный анализ in vitro активности NK-клеточных линий человека, экспрессирующих химерные антигенные рецепторы" ["SECTION_PICTURE_FILE_ALT"]=> string(208) "Сравнительный анализ in vitro активности NK-клеточных линий человека, экспрессирующих химерные антигенные рецепторы" ["SECTION_PICTURE_FILE_TITLE"]=> string(208) "Сравнительный анализ in vitro активности NK-клеточных линий человека, экспрессирующих химерные антигенные рецепторы" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "sravnitelnyy-analiz-in-vitro-aktivnosti-nk-kletochnykh-liniy-cheloveka-ekspressiruyushchikh-khimerny" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(208) "Сравнительный анализ in vitro активности NK-клеточных линий человека, экспрессирующих химерные антигенные рецепторы" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(208) "Сравнительный анализ in vitro активности NK-клеточных линий человека, экспрессирующих химерные антигенные рецепторы" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "sravnitelnyy-analiz-in-vitro-aktivnosti-nk-kletochnykh-liniy-cheloveka-ekspressiruyushchikh-khimerny" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "sravnitelnyy-analiz-in-vitro-aktivnosti-nk-kletochnykh-liniy-cheloveka-ekspressiruyushchikh-khimerny" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "sravnitelnyy-analiz-in-vitro-aktivnosti-nk-kletochnykh-liniy-cheloveka-ekspressiruyushchikh-khimerny" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20293" ["VALUE"]=> array(2) { ["TEXT"]=> string(512) "Татьяна Н. Беловежец <sup>1</sup>,<sup>2</sup>, Андрей А. Горчаков <sup>1</sup>,<sup>2</sup>, Сергей В. Кулемзин <sup>1</sup>, Антон Н. Чикаев <sup>1</sup>, Ольга А. Коваль <sup>1</sup>,<sup>3</sup>, Елена В. Кулигина <sup>2</sup>, Александр В. Таранин <sup>1</sup>,<sup>2</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(380) "Татьяна Н. Беловежец 1,2, Андрей А. Горчаков 1,2, Сергей В. Кулемзин 1, Антон Н. Чикаев 1, Ольга А. Коваль 1,3, Елена В. Кулигина 2, Александр В. Таранин 1,2" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20294" ["VALUE"]=> array(2) { ["TEXT"]=> string(514) "<sup>1</sup> Институт молекулярной и клеточной биологии СО РАН, Новосибирск, Россия<br> <sup>2</sup> Новосибирский государственный университет, Новосибирск, Россия<br> <sup>3</sup> Институт химической биологии и фундаментальной медицины СО РАН, Новосибирск, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(460) "1 Институт молекулярной и клеточной биологии СО РАН, Новосибирск, Россия
2 Новосибирский государственный университет, Новосибирск, Россия
3 Институт химической биологии и фундаментальной медицины СО РАН, Новосибирск, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20352" ["VALUE"]=> array(2) { ["TEXT"]=> string(5889) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Терапия Т-клетками, экспрессирующими химерные антигенные рецепторы (CAR), была одобрена FDA к клиническому использованию в августе 2017 года для больных с r/rALL. Несмотря на значительную эффективность, у CAR T-клеточной терапии существуют серьезные ограничения, связанные с высокой стоимостью, сложной стандартизацией и невозможностью получить CAR Т-клетки для отдельных пациентов. В связи с этим крайне привлекательным выглядит создание универсальных аллогенных CAR T-клеток, однако на существующем уровне развития инструментов геномного редактирования и селекции субпопуляций Т-клеток этот подход сопровождается риском развития реакции «трансплантат против хозяина». Возможным решением этих проблем может быть переход к иммортализованным NK-клеточным линиям в качестве носителей CAR. Подобные линии недорогие в наработке, могут быть стандартизованы и не вызывают реакцию «трансплантат против хозяина». К настоящему моменту описано несколько NK-клеточных линий человека, однако систематического сравнения их свойств в качестве носителей CAR проведено не было. </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> В данное исследование были включены три NK-клеточные иммортализованные линии человека (А, В и NK-92). На основе каждой из трех линий методом лентивирусной трансдукции были получены сублинии, стабильно экспрессирующие CAR, специфичный к белку человека CD20. После этого был измерен уровень цитотоксичности CAR-NK клеточных линий по отношению к CD20-положительным клеткам линии Raji (клетки лимфомы Бёркитта) и клеткам линии HEK293Т, эктопически экспрессирующим CD20, либо изогенным контрольным клеткам. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Все три полученные CAR-NK-клеточные линии обнаруживали значимый уровень цитотоксичности против клеток линии Raji, однако клетки NK-92 дикого типа также лизировали мишени Raji. В связи с этим, для более корректного сравнения уровней цитотоксичности CAR-NK-клеточных линий в тестах <i>in vitro</i> были получены клетки линии HEK293Т, экспрессирующие CD20. Уровень неспецифической цитотоксичности немодифицированных NK клеток против таких мишеней не превышал 20% в диапазоне эффектор: мишень=1-5, при этом уровень специфической, CAR-опосредованной цитотоксичности составлял 73% (CAR-NK-92), 55% (CAR-B) и 34% (CAR-A) при соотношении эффектор:-мишень=5. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Все полученные CAR-NK-клеточные линии проявляют значимый уровень цитотоксичности по отношению к CD20-позитивным клеткам-мишеням в тестах <i>in vitro</i>, и клетки линии NK-92 проявляют самый высокий уровень как специфической, так и неспецифической цитотоксичности. Необходимы дополнительные исследования <i>in vivo</i>, чтобы определить профили безопасности и эффективности CAR-NK эффекторов. </p> <h2 style="text-align: justify;">Благодарности</h2> <p style="text-align: justify;"> Работа выполнена при финансовой поддержке Минобрнауки РФ, соглашение № 14.604.21.0169 (уникальный идентификатор проекта RFMEFI60417X0169). </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Химерный антигенный рецептор, NK-клеточные линии, цитотоксичность. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5589) "
Введение
Терапия Т-клетками, экспрессирующими химерные антигенные рецепторы (CAR), была одобрена FDA к клиническому использованию в августе 2017 года для больных с r/rALL. Несмотря на значительную эффективность, у CAR T-клеточной терапии существуют серьезные ограничения, связанные с высокой стоимостью, сложной стандартизацией и невозможностью получить CAR Т-клетки для отдельных пациентов. В связи с этим крайне привлекательным выглядит создание универсальных аллогенных CAR T-клеток, однако на существующем уровне развития инструментов геномного редактирования и селекции субпопуляций Т-клеток этот подход сопровождается риском развития реакции «трансплантат против хозяина». Возможным решением этих проблем может быть переход к иммортализованным NK-клеточным линиям в качестве носителей CAR. Подобные линии недорогие в наработке, могут быть стандартизованы и не вызывают реакцию «трансплантат против хозяина». К настоящему моменту описано несколько NK-клеточных линий человека, однако систематического сравнения их свойств в качестве носителей CAR проведено не было.
Методы
В данное исследование были включены три NK-клеточные иммортализованные линии человека (А, В и NK-92). На основе каждой из трех линий методом лентивирусной трансдукции были получены сублинии, стабильно экспрессирующие CAR, специфичный к белку человека CD20. После этого был измерен уровень цитотоксичности CAR-NK клеточных линий по отношению к CD20-положительным клеткам линии Raji (клетки лимфомы Бёркитта) и клеткам линии HEK293Т, эктопически экспрессирующим CD20, либо изогенным контрольным клеткам.
Результаты
Все три полученные CAR-NK-клеточные линии обнаруживали значимый уровень цитотоксичности против клеток линии Raji, однако клетки NK-92 дикого типа также лизировали мишени Raji. В связи с этим, для более корректного сравнения уровней цитотоксичности CAR-NK-клеточных линий в тестах in vitro были получены клетки линии HEK293Т, экспрессирующие CD20. Уровень неспецифической цитотоксичности немодифицированных NK клеток против таких мишеней не превышал 20% в диапазоне эффектор: мишень=1-5, при этом уровень специфической, CAR-опосредованной цитотоксичности составлял 73% (CAR-NK-92), 55% (CAR-B) и 34% (CAR-A) при соотношении эффектор:-мишень=5.
Заключение
Все полученные CAR-NK-клеточные линии проявляют значимый уровень цитотоксичности по отношению к CD20-позитивным клеткам-мишеням в тестах in vitro, и клетки линии NK-92 проявляют самый высокий уровень как специфической, так и неспецифической цитотоксичности. Необходимы дополнительные исследования in vivo, чтобы определить профили безопасности и эффективности CAR-NK эффекторов.
Благодарности
Работа выполнена при финансовой поддержке Минобрнауки РФ, соглашение № 14.604.21.0169 (уникальный идентификатор проекта RFMEFI60417X0169).
Ключевые слова
Химерный антигенный рецептор, NK-клеточные линии, цитотоксичность.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20295" ["VALUE"]=> array(2) { ["TEXT"]=> string(418) "Tatyana N. Belovezhets <sup>1</sup>,<sup>2</sup>, Andrey A. Gorchakov <sup>1</sup>,<sup>2</sup>, Sergey V. Kulemzin <sup>1</sup>, Anton N. Chikaev <sup>1</sup>, Olga A. Koval <sup>1</sup>,<sup>3</sup>, Elena V. Kuligina <sup>3</sup>, Aleksander V. Taranin <sup>1</sup>,<sup>2</sup>" ["TYPE"]=> string(4) "TEXT" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(286) "Tatyana N. Belovezhets 1,2, Andrey A. Gorchakov 1,2, Sergey V. Kulemzin 1, Anton N. Chikaev 1, Olga A. Koval 1,3, Elena V. Kuligina 3, Aleksander V. Taranin 1,2" ["TYPE"]=> string(4) "TEXT" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20296" ["VALUE"]=> array(2) { ["TEXT"]=> string(303) "<sup>1</sup> Institute of Molecular and Cellular Biology SB RAS, Novosibirsk, Russia<br> <sup>2</sup> Novosibirsk State University, Novosibirsk, Russia<br> <sup>3</sup> Institute of Chemical Biology and Fundamental Medicine SB RAS, Novosibirsk, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(255) "1 Institute of Molecular and Cellular Biology SB RAS, Novosibirsk, Russia2 Novosibirsk State University, Novosibirsk, Russia
3 Institute of Chemical Biology and Fundamental Medicine SB RAS, Novosibirsk, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20353" ["VALUE"]=> array(2) { ["TEXT"]=> string(3360) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> CAR T cell therapy received regulatory approval for treatment of pediatric r/rALL patients in August, 2017. Despite impressive efficacy, widespread use of CAR T cell therapy is limited by prohibitively high costs, complex standardization procedures, as well as by inherent difficulties to produce CAR T cell products for certain groups of patients. Moving CAR T cell therapy from autologous to allogeneic format appears highly attractive, yet challenging, as current techniques of cell sorting and genome engineering may do not entirely eliminate the risk of GvHD. Choosing immortalized human NK-cell lines over T cells as CAR carriers offers a possible solution to this problem. Such cell lines are inexpensive to maintain, they do not cause GvHD, and are straightforward to standardize. Several human NK-cell lines have been described to date, however no side-by-side comparisons of activity of such cells engineered to express CARs have been performed. </p> <h2 style="text-align: justify;">Methods</h2> <p style="text-align: justify;"> In this study, three immortalized human NK-cell line backgrounds (A, B, and NK-92) were used to establish sublines expressing a CD20-specific CAR. In vitro cytotoxicity assays of parental and CAR-expressing cells against CD20-positive Burkitt lymphoma target cells (Raji) were performed. Alternative target cells (HEK293T(CD20+)) and non-target isogenic controls (HEK293T) were also included into cytotoxicity tests. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> All the three CAR-NK cell lines obtained displayed pronounced cytotoxicity against Raji target cells, however this cell line was also highly sensitive to killing by unmodified parental NK-92 cells. Thus, in order to perform side-by-side comparisons of CAR-NK cell activity in vitro, we established HEK293T cells overexpressing CD20, as the target cell line. The level of non-specific cytotoxicity of parental NK-cell lines against HEK293T(CD20+) cells was below 20% across the E:T ratios ranging from 1 to 5, whereas specific CAR-mediated cytotoxicity at E:T=5 constituted 73% (CAR-NK-92), 55% (CAR-B), and 34% (CAR-A). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> All the CAR-NK cell lines obtained in this study display significant cell killing activity towards target cells in vitro, with NK-92 cell line showing the highest level of both specific and non-specific cytotoxicity. Further studies in vivo are needed to explore the safety and efficacy profiles of CAR-NK cell lines. </p> <h2 style="text-align: justify;">Acknowledgements</h2> <p style="text-align: justify;"> This work was supported by the Ministry of Education and Science of the Russian Federation, grant agreement № 14.604.21.0169 (unique project identifier RFMEFI60417X0169). </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Chimeric antigen receptors, NK-cell lines, cytotoxicity. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3096) "
Introduction
CAR T cell therapy received regulatory approval for treatment of pediatric r/rALL patients in August, 2017. Despite impressive efficacy, widespread use of CAR T cell therapy is limited by prohibitively high costs, complex standardization procedures, as well as by inherent difficulties to produce CAR T cell products for certain groups of patients. Moving CAR T cell therapy from autologous to allogeneic format appears highly attractive, yet challenging, as current techniques of cell sorting and genome engineering may do not entirely eliminate the risk of GvHD. Choosing immortalized human NK-cell lines over T cells as CAR carriers offers a possible solution to this problem. Such cell lines are inexpensive to maintain, they do not cause GvHD, and are straightforward to standardize. Several human NK-cell lines have been described to date, however no side-by-side comparisons of activity of such cells engineered to express CARs have been performed.
Methods
In this study, three immortalized human NK-cell line backgrounds (A, B, and NK-92) were used to establish sublines expressing a CD20-specific CAR. In vitro cytotoxicity assays of parental and CAR-expressing cells against CD20-positive Burkitt lymphoma target cells (Raji) were performed. Alternative target cells (HEK293T(CD20+)) and non-target isogenic controls (HEK293T) were also included into cytotoxicity tests.
Results
All the three CAR-NK cell lines obtained displayed pronounced cytotoxicity against Raji target cells, however this cell line was also highly sensitive to killing by unmodified parental NK-92 cells. Thus, in order to perform side-by-side comparisons of CAR-NK cell activity in vitro, we established HEK293T cells overexpressing CD20, as the target cell line. The level of non-specific cytotoxicity of parental NK-cell lines against HEK293T(CD20+) cells was below 20% across the E:T ratios ranging from 1 to 5, whereas specific CAR-mediated cytotoxicity at E:T=5 constituted 73% (CAR-NK-92), 55% (CAR-B), and 34% (CAR-A).
Conclusion
All the CAR-NK cell lines obtained in this study display significant cell killing activity towards target cells in vitro, with NK-92 cell line showing the highest level of both specific and non-specific cytotoxicity. Further studies in vivo are needed to explore the safety and efficacy profiles of CAR-NK cell lines.
Acknowledgements
This work was supported by the Ministry of Education and Science of the Russian Federation, grant agreement № 14.604.21.0169 (unique project identifier RFMEFI60417X0169).
Keywords
Chimeric antigen receptors, NK-cell lines, cytotoxicity.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20297" ["VALUE"]=> string(90) "Comparative in vitro analysis of human NK-cell lines expressing chimeric antigen receptors" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(90) "Comparative in vitro analysis of human NK-cell lines expressing chimeric antigen receptors" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20737" ["VALUE"]=> string(4) "1373" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1373" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20738" ["VALUE"]=> string(4) "1374" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1374" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20295" ["VALUE"]=> array(2) { ["TEXT"]=> string(418) "Tatyana N. Belovezhets <sup>1</sup>,<sup>2</sup>, Andrey A. Gorchakov <sup>1</sup>,<sup>2</sup>, Sergey V. Kulemzin <sup>1</sup>, Anton N. Chikaev <sup>1</sup>, Olga A. Koval <sup>1</sup>,<sup>3</sup>, Elena V. Kuligina <sup>3</sup>, Aleksander V. Taranin <sup>1</sup>,<sup>2</sup>" ["TYPE"]=> string(4) "TEXT" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(286) "Tatyana N. Belovezhets 1,2, Andrey A. Gorchakov 1,2, Sergey V. Kulemzin 1, Anton N. Chikaev 1, Olga A. Koval 1,3, Elena V. Kuligina 3, Aleksander V. Taranin 1,2" ["TYPE"]=> string(4) "TEXT" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(468) "Tatyana N. Belovezhets <sup>1</sup>,<sup>2</sup>, Andrey A. Gorchakov <sup>1</sup>,<sup>2</sup>, Sergey V. Kulemzin <sup>1</sup>, Anton N. Chikaev <sup>1</sup>, Olga A. Koval <sup>1</sup>,<sup>3</sup>, Elena V. Kuligina <sup>3</sup>, Aleksander V. Taranin <sup>1</sup>,<sup>2</sup>" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20353" ["VALUE"]=> array(2) { ["TEXT"]=> string(3360) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> CAR T cell therapy received regulatory approval for treatment of pediatric r/rALL patients in August, 2017. Despite impressive efficacy, widespread use of CAR T cell therapy is limited by prohibitively high costs, complex standardization procedures, as well as by inherent difficulties to produce CAR T cell products for certain groups of patients. Moving CAR T cell therapy from autologous to allogeneic format appears highly attractive, yet challenging, as current techniques of cell sorting and genome engineering may do not entirely eliminate the risk of GvHD. Choosing immortalized human NK-cell lines over T cells as CAR carriers offers a possible solution to this problem. Such cell lines are inexpensive to maintain, they do not cause GvHD, and are straightforward to standardize. Several human NK-cell lines have been described to date, however no side-by-side comparisons of activity of such cells engineered to express CARs have been performed. </p> <h2 style="text-align: justify;">Methods</h2> <p style="text-align: justify;"> In this study, three immortalized human NK-cell line backgrounds (A, B, and NK-92) were used to establish sublines expressing a CD20-specific CAR. In vitro cytotoxicity assays of parental and CAR-expressing cells against CD20-positive Burkitt lymphoma target cells (Raji) were performed. Alternative target cells (HEK293T(CD20+)) and non-target isogenic controls (HEK293T) were also included into cytotoxicity tests. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> All the three CAR-NK cell lines obtained displayed pronounced cytotoxicity against Raji target cells, however this cell line was also highly sensitive to killing by unmodified parental NK-92 cells. Thus, in order to perform side-by-side comparisons of CAR-NK cell activity in vitro, we established HEK293T cells overexpressing CD20, as the target cell line. The level of non-specific cytotoxicity of parental NK-cell lines against HEK293T(CD20+) cells was below 20% across the E:T ratios ranging from 1 to 5, whereas specific CAR-mediated cytotoxicity at E:T=5 constituted 73% (CAR-NK-92), 55% (CAR-B), and 34% (CAR-A). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> All the CAR-NK cell lines obtained in this study display significant cell killing activity towards target cells in vitro, with NK-92 cell line showing the highest level of both specific and non-specific cytotoxicity. Further studies in vivo are needed to explore the safety and efficacy profiles of CAR-NK cell lines. </p> <h2 style="text-align: justify;">Acknowledgements</h2> <p style="text-align: justify;"> This work was supported by the Ministry of Education and Science of the Russian Federation, grant agreement № 14.604.21.0169 (unique project identifier RFMEFI60417X0169). </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Chimeric antigen receptors, NK-cell lines, cytotoxicity. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3096) "Introduction
CAR T cell therapy received regulatory approval for treatment of pediatric r/rALL patients in August, 2017. Despite impressive efficacy, widespread use of CAR T cell therapy is limited by prohibitively high costs, complex standardization procedures, as well as by inherent difficulties to produce CAR T cell products for certain groups of patients. Moving CAR T cell therapy from autologous to allogeneic format appears highly attractive, yet challenging, as current techniques of cell sorting and genome engineering may do not entirely eliminate the risk of GvHD. Choosing immortalized human NK-cell lines over T cells as CAR carriers offers a possible solution to this problem. Such cell lines are inexpensive to maintain, they do not cause GvHD, and are straightforward to standardize. Several human NK-cell lines have been described to date, however no side-by-side comparisons of activity of such cells engineered to express CARs have been performed.
Methods
In this study, three immortalized human NK-cell line backgrounds (A, B, and NK-92) were used to establish sublines expressing a CD20-specific CAR. In vitro cytotoxicity assays of parental and CAR-expressing cells against CD20-positive Burkitt lymphoma target cells (Raji) were performed. Alternative target cells (HEK293T(CD20+)) and non-target isogenic controls (HEK293T) were also included into cytotoxicity tests.
Results
All the three CAR-NK cell lines obtained displayed pronounced cytotoxicity against Raji target cells, however this cell line was also highly sensitive to killing by unmodified parental NK-92 cells. Thus, in order to perform side-by-side comparisons of CAR-NK cell activity in vitro, we established HEK293T cells overexpressing CD20, as the target cell line. The level of non-specific cytotoxicity of parental NK-cell lines against HEK293T(CD20+) cells was below 20% across the E:T ratios ranging from 1 to 5, whereas specific CAR-mediated cytotoxicity at E:T=5 constituted 73% (CAR-NK-92), 55% (CAR-B), and 34% (CAR-A).
Conclusion
All the CAR-NK cell lines obtained in this study display significant cell killing activity towards target cells in vitro, with NK-92 cell line showing the highest level of both specific and non-specific cytotoxicity. Further studies in vivo are needed to explore the safety and efficacy profiles of CAR-NK cell lines.
Acknowledgements
This work was supported by the Ministry of Education and Science of the Russian Federation, grant agreement № 14.604.21.0169 (unique project identifier RFMEFI60417X0169).
Keywords
Chimeric antigen receptors, NK-cell lines, cytotoxicity.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3096) "Introduction
CAR T cell therapy received regulatory approval for treatment of pediatric r/rALL patients in August, 2017. Despite impressive efficacy, widespread use of CAR T cell therapy is limited by prohibitively high costs, complex standardization procedures, as well as by inherent difficulties to produce CAR T cell products for certain groups of patients. Moving CAR T cell therapy from autologous to allogeneic format appears highly attractive, yet challenging, as current techniques of cell sorting and genome engineering may do not entirely eliminate the risk of GvHD. Choosing immortalized human NK-cell lines over T cells as CAR carriers offers a possible solution to this problem. Such cell lines are inexpensive to maintain, they do not cause GvHD, and are straightforward to standardize. Several human NK-cell lines have been described to date, however no side-by-side comparisons of activity of such cells engineered to express CARs have been performed.
Methods
In this study, three immortalized human NK-cell line backgrounds (A, B, and NK-92) were used to establish sublines expressing a CD20-specific CAR. In vitro cytotoxicity assays of parental and CAR-expressing cells against CD20-positive Burkitt lymphoma target cells (Raji) were performed. Alternative target cells (HEK293T(CD20+)) and non-target isogenic controls (HEK293T) were also included into cytotoxicity tests.
Results
All the three CAR-NK cell lines obtained displayed pronounced cytotoxicity against Raji target cells, however this cell line was also highly sensitive to killing by unmodified parental NK-92 cells. Thus, in order to perform side-by-side comparisons of CAR-NK cell activity in vitro, we established HEK293T cells overexpressing CD20, as the target cell line. The level of non-specific cytotoxicity of parental NK-cell lines against HEK293T(CD20+) cells was below 20% across the E:T ratios ranging from 1 to 5, whereas specific CAR-mediated cytotoxicity at E:T=5 constituted 73% (CAR-NK-92), 55% (CAR-B), and 34% (CAR-A).
Conclusion
All the CAR-NK cell lines obtained in this study display significant cell killing activity towards target cells in vitro, with NK-92 cell line showing the highest level of both specific and non-specific cytotoxicity. Further studies in vivo are needed to explore the safety and efficacy profiles of CAR-NK cell lines.
Acknowledgements
This work was supported by the Ministry of Education and Science of the Russian Federation, grant agreement № 14.604.21.0169 (unique project identifier RFMEFI60417X0169).
Keywords
Chimeric antigen receptors, NK-cell lines, cytotoxicity.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20297" ["VALUE"]=> string(90) "Comparative in vitro analysis of human NK-cell lines expressing chimeric antigen receptors" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(90) "Comparative in vitro analysis of human NK-cell lines expressing chimeric antigen receptors" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(90) "Comparative in vitro analysis of human NK-cell lines expressing chimeric antigen receptors" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20296" ["VALUE"]=> array(2) { ["TEXT"]=> string(303) "<sup>1</sup> Institute of Molecular and Cellular Biology SB RAS, Novosibirsk, Russia<br> <sup>2</sup> Novosibirsk State University, Novosibirsk, Russia<br> <sup>3</sup> Institute of Chemical Biology and Fundamental Medicine SB RAS, Novosibirsk, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(255) "1 Institute of Molecular and Cellular Biology SB RAS, Novosibirsk, Russia2 Novosibirsk State University, Novosibirsk, Russia
3 Institute of Chemical Biology and Fundamental Medicine SB RAS, Novosibirsk, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(255) "1 Institute of Molecular and Cellular Biology SB RAS, Novosibirsk, Russia
2 Novosibirsk State University, Novosibirsk, Russia
3 Institute of Chemical Biology and Fundamental Medicine SB RAS, Novosibirsk, Russia" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20293" ["VALUE"]=> array(2) { ["TEXT"]=> string(512) "Татьяна Н. Беловежец <sup>1</sup>,<sup>2</sup>, Андрей А. Горчаков <sup>1</sup>,<sup>2</sup>, Сергей В. Кулемзин <sup>1</sup>, Антон Н. Чикаев <sup>1</sup>, Ольга А. Коваль <sup>1</sup>,<sup>3</sup>, Елена В. Кулигина <sup>2</sup>, Александр В. Таранин <sup>1</sup>,<sup>2</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(380) "Татьяна Н. Беловежец 1,2, Андрей А. Горчаков 1,2, Сергей В. Кулемзин 1, Антон Н. Чикаев 1, Ольга А. Коваль 1,3, Елена В. Кулигина 2, Александр В. Таранин 1,2" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(380) "Татьяна Н. Беловежец 1,2, Андрей А. Горчаков 1,2, Сергей В. Кулемзин 1, Антон Н. Чикаев 1, Ольга А. Коваль 1,3, Елена В. Кулигина 2, Александр В. Таранин 1,2" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20352" ["VALUE"]=> array(2) { ["TEXT"]=> string(5889) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Терапия Т-клетками, экспрессирующими химерные антигенные рецепторы (CAR), была одобрена FDA к клиническому использованию в августе 2017 года для больных с r/rALL. Несмотря на значительную эффективность, у CAR T-клеточной терапии существуют серьезные ограничения, связанные с высокой стоимостью, сложной стандартизацией и невозможностью получить CAR Т-клетки для отдельных пациентов. В связи с этим крайне привлекательным выглядит создание универсальных аллогенных CAR T-клеток, однако на существующем уровне развития инструментов геномного редактирования и селекции субпопуляций Т-клеток этот подход сопровождается риском развития реакции «трансплантат против хозяина». Возможным решением этих проблем может быть переход к иммортализованным NK-клеточным линиям в качестве носителей CAR. Подобные линии недорогие в наработке, могут быть стандартизованы и не вызывают реакцию «трансплантат против хозяина». К настоящему моменту описано несколько NK-клеточных линий человека, однако систематического сравнения их свойств в качестве носителей CAR проведено не было. </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> В данное исследование были включены три NK-клеточные иммортализованные линии человека (А, В и NK-92). На основе каждой из трех линий методом лентивирусной трансдукции были получены сублинии, стабильно экспрессирующие CAR, специфичный к белку человека CD20. После этого был измерен уровень цитотоксичности CAR-NK клеточных линий по отношению к CD20-положительным клеткам линии Raji (клетки лимфомы Бёркитта) и клеткам линии HEK293Т, эктопически экспрессирующим CD20, либо изогенным контрольным клеткам. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Все три полученные CAR-NK-клеточные линии обнаруживали значимый уровень цитотоксичности против клеток линии Raji, однако клетки NK-92 дикого типа также лизировали мишени Raji. В связи с этим, для более корректного сравнения уровней цитотоксичности CAR-NK-клеточных линий в тестах <i>in vitro</i> были получены клетки линии HEK293Т, экспрессирующие CD20. Уровень неспецифической цитотоксичности немодифицированных NK клеток против таких мишеней не превышал 20% в диапазоне эффектор: мишень=1-5, при этом уровень специфической, CAR-опосредованной цитотоксичности составлял 73% (CAR-NK-92), 55% (CAR-B) и 34% (CAR-A) при соотношении эффектор:-мишень=5. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Все полученные CAR-NK-клеточные линии проявляют значимый уровень цитотоксичности по отношению к CD20-позитивным клеткам-мишеням в тестах <i>in vitro</i>, и клетки линии NK-92 проявляют самый высокий уровень как специфической, так и неспецифической цитотоксичности. Необходимы дополнительные исследования <i>in vivo</i>, чтобы определить профили безопасности и эффективности CAR-NK эффекторов. </p> <h2 style="text-align: justify;">Благодарности</h2> <p style="text-align: justify;"> Работа выполнена при финансовой поддержке Минобрнауки РФ, соглашение № 14.604.21.0169 (уникальный идентификатор проекта RFMEFI60417X0169). </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Химерный антигенный рецептор, NK-клеточные линии, цитотоксичность. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5589) "
Введение
Терапия Т-клетками, экспрессирующими химерные антигенные рецепторы (CAR), была одобрена FDA к клиническому использованию в августе 2017 года для больных с r/rALL. Несмотря на значительную эффективность, у CAR T-клеточной терапии существуют серьезные ограничения, связанные с высокой стоимостью, сложной стандартизацией и невозможностью получить CAR Т-клетки для отдельных пациентов. В связи с этим крайне привлекательным выглядит создание универсальных аллогенных CAR T-клеток, однако на существующем уровне развития инструментов геномного редактирования и селекции субпопуляций Т-клеток этот подход сопровождается риском развития реакции «трансплантат против хозяина». Возможным решением этих проблем может быть переход к иммортализованным NK-клеточным линиям в качестве носителей CAR. Подобные линии недорогие в наработке, могут быть стандартизованы и не вызывают реакцию «трансплантат против хозяина». К настоящему моменту описано несколько NK-клеточных линий человека, однако систематического сравнения их свойств в качестве носителей CAR проведено не было.
Методы
В данное исследование были включены три NK-клеточные иммортализованные линии человека (А, В и NK-92). На основе каждой из трех линий методом лентивирусной трансдукции были получены сублинии, стабильно экспрессирующие CAR, специфичный к белку человека CD20. После этого был измерен уровень цитотоксичности CAR-NK клеточных линий по отношению к CD20-положительным клеткам линии Raji (клетки лимфомы Бёркитта) и клеткам линии HEK293Т, эктопически экспрессирующим CD20, либо изогенным контрольным клеткам.
Результаты
Все три полученные CAR-NK-клеточные линии обнаруживали значимый уровень цитотоксичности против клеток линии Raji, однако клетки NK-92 дикого типа также лизировали мишени Raji. В связи с этим, для более корректного сравнения уровней цитотоксичности CAR-NK-клеточных линий в тестах in vitro были получены клетки линии HEK293Т, экспрессирующие CD20. Уровень неспецифической цитотоксичности немодифицированных NK клеток против таких мишеней не превышал 20% в диапазоне эффектор: мишень=1-5, при этом уровень специфической, CAR-опосредованной цитотоксичности составлял 73% (CAR-NK-92), 55% (CAR-B) и 34% (CAR-A) при соотношении эффектор:-мишень=5.
Заключение
Все полученные CAR-NK-клеточные линии проявляют значимый уровень цитотоксичности по отношению к CD20-позитивным клеткам-мишеням в тестах in vitro, и клетки линии NK-92 проявляют самый высокий уровень как специфической, так и неспецифической цитотоксичности. Необходимы дополнительные исследования in vivo, чтобы определить профили безопасности и эффективности CAR-NK эффекторов.
Благодарности
Работа выполнена при финансовой поддержке Минобрнауки РФ, соглашение № 14.604.21.0169 (уникальный идентификатор проекта RFMEFI60417X0169).
Ключевые слова
Химерный антигенный рецептор, NK-клеточные линии, цитотоксичность.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(5589) "Введение
Терапия Т-клетками, экспрессирующими химерные антигенные рецепторы (CAR), была одобрена FDA к клиническому использованию в августе 2017 года для больных с r/rALL. Несмотря на значительную эффективность, у CAR T-клеточной терапии существуют серьезные ограничения, связанные с высокой стоимостью, сложной стандартизацией и невозможностью получить CAR Т-клетки для отдельных пациентов. В связи с этим крайне привлекательным выглядит создание универсальных аллогенных CAR T-клеток, однако на существующем уровне развития инструментов геномного редактирования и селекции субпопуляций Т-клеток этот подход сопровождается риском развития реакции «трансплантат против хозяина». Возможным решением этих проблем может быть переход к иммортализованным NK-клеточным линиям в качестве носителей CAR. Подобные линии недорогие в наработке, могут быть стандартизованы и не вызывают реакцию «трансплантат против хозяина». К настоящему моменту описано несколько NK-клеточных линий человека, однако систематического сравнения их свойств в качестве носителей CAR проведено не было.
Методы
В данное исследование были включены три NK-клеточные иммортализованные линии человека (А, В и NK-92). На основе каждой из трех линий методом лентивирусной трансдукции были получены сублинии, стабильно экспрессирующие CAR, специфичный к белку человека CD20. После этого был измерен уровень цитотоксичности CAR-NK клеточных линий по отношению к CD20-положительным клеткам линии Raji (клетки лимфомы Бёркитта) и клеткам линии HEK293Т, эктопически экспрессирующим CD20, либо изогенным контрольным клеткам.
Результаты
Все три полученные CAR-NK-клеточные линии обнаруживали значимый уровень цитотоксичности против клеток линии Raji, однако клетки NK-92 дикого типа также лизировали мишени Raji. В связи с этим, для более корректного сравнения уровней цитотоксичности CAR-NK-клеточных линий в тестах in vitro были получены клетки линии HEK293Т, экспрессирующие CD20. Уровень неспецифической цитотоксичности немодифицированных NK клеток против таких мишеней не превышал 20% в диапазоне эффектор: мишень=1-5, при этом уровень специфической, CAR-опосредованной цитотоксичности составлял 73% (CAR-NK-92), 55% (CAR-B) и 34% (CAR-A) при соотношении эффектор:-мишень=5.
Заключение
Все полученные CAR-NK-клеточные линии проявляют значимый уровень цитотоксичности по отношению к CD20-позитивным клеткам-мишеням в тестах in vitro, и клетки линии NK-92 проявляют самый высокий уровень как специфической, так и неспецифической цитотоксичности. Необходимы дополнительные исследования in vivo, чтобы определить профили безопасности и эффективности CAR-NK эффекторов.
Благодарности
Работа выполнена при финансовой поддержке Минобрнауки РФ, соглашение № 14.604.21.0169 (уникальный идентификатор проекта RFMEFI60417X0169).
Ключевые слова
Химерный антигенный рецептор, NK-клеточные линии, цитотоксичность.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20294" ["VALUE"]=> array(2) { ["TEXT"]=> string(514) "<sup>1</sup> Институт молекулярной и клеточной биологии СО РАН, Новосибирск, Россия<br> <sup>2</sup> Новосибирский государственный университет, Новосибирск, Россия<br> <sup>3</sup> Институт химической биологии и фундаментальной медицины СО РАН, Новосибирск, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(460) "1 Институт молекулярной и клеточной биологии СО РАН, Новосибирск, Россия2 Новосибирский государственный университет, Новосибирск, Россия
3 Институт химической биологии и фундаментальной медицины СО РАН, Новосибирск, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(460) "1 Институт молекулярной и клеточной биологии СО РАН, Новосибирск, Россия
2 Новосибирский государственный университет, Новосибирск, Россия
3 Институт химической биологии и фундаментальной медицины СО РАН, Новосибирск, Россия
" } } } [17]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1551" ["~ID"]=> string(4) "1551" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(366) "Применение посттрансплантационного циклофосфамида и руксо- литиниба в качестве профилактики реакции трансплантат против хозяина и рецидива у пациентов с миелофиброзом: проспективное исследование" ["~NAME"]=> string(366) "Применение посттрансплантационного циклофосфамида и руксо- литиниба в качестве профилактики реакции трансплантат против хозяина и рецидива у пациентов с миелофиброзом: проспективное исследование" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:23:48" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:23:48" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/primenenie-posttransplantatsionnogo-tsiklofosfamida-i-rukso-litiniba-v-kachestve-profilaktiki-reakts/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/primenenie-posttransplantatsionnogo-tsiklofosfamida-i-rukso-litiniba-v-kachestve-profilaktiki-reakts/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "primenenie-posttransplantatsionnogo-tsiklofosfamida-i-rukso-litiniba-v-kachestve-profilaktiki-reakts" ["~CODE"]=> string(100) "primenenie-posttransplantatsionnogo-tsiklofosfamida-i-rukso-litiniba-v-kachestve-profilaktiki-reakts" ["EXTERNAL_ID"]=> string(4) "1551" ["~EXTERNAL_ID"]=> string(4) "1551" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(366) "Применение посттрансплантационного циклофосфамида и руксо- литиниба в качестве профилактики реакции трансплантат против хозяина и рецидива у пациентов с миелофиброзом: проспективное исследование" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(542) "Применение посттрансплантационного циклофосфамида и руксо- литиниба в качестве профилактики реакции трансплантат против хозяина и рецидива у пациентов с миелофиброзом: проспективное исследованиеA pilot study of ruxolitinib combined with cyclophosphamide for graft-versus-host disease prophylaxis and relapse prevention in patients with myelofibrosis: a prospective study" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(9561) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Миелофиброз относится к хроническим BCR-ABL-негативным миелопролиферативным неоплазиям и сопровождается, как правило, непрерывно прогрессирующим течением. Аллогенная трансплантация гемопоэтических стволовых клеток в настоящее время является единственным методом терапии, позволяющим добиться излечения от заболевания. Применение ингибитора JAK1/JAK2 руксолитиниба во многом позволяет изменить статус заболевания на момент алло-ТГСК – уменьшить спленомегалию, конституциональные симптомы, улучшить гематологические показатели, в ряде случаев привести к регрессу фиброза в костном мозге. В то же время руксолитиниб обладает иммуномодулирующим эффектом, благодаря чему широко используется для лечения острой и хронической РТПХ. В нашем исследовании мы использовали руксолитиниб в комбинации с посттрансплантационным циклофосфаном в качестве профилактики РТПХ и рецидива заболевания. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Мы проанализировали результаты алло-ТГСК у 20 пациентов в возрасте от 32 до 61 лет (медиана 51 год). У 14 пациентов был диагностирован первичный миелофиброз, у 2 пациентов – посттромбоцитемический миелофиброз, у 4 пациентов – постполицитемический миелофиброз. Одиннадцать пациентов относились к промежуточному-2 риску по шкале DIPSSplus, восемь – к высокой группе риска. Одному пациенту алло-ТГСК была выполнена в фазе бластного криза. У пятнадцати пациентов отмечалась мутация <i>JAK2V617F</i>, у двух – мутация в гене <i>MPL</i>, у трех – мутация в гене <i>CALR</i>. Все пациенты получали терапию руксолитинибом в качестве предтрансплантационной подготовки, медиана длительности терапии составила 6 месяцев (3-22) в дозе 30-45 мг. У восьми пациентов отмечалось клиническое улучшение, у 1 – прогрессирование заболевания, у 11 – стабилизации заболевания на момент алло-ТГСК. У семи пациентов была выполнена спленэктомия в связи с выраженной спленомегалией и недостаточным ответом со стороны селезенки. Во всех случаях применялся режим кондиционирования со сниженной интенсивностью доз (флударабин 180 мг/м<sup>2</sup>, бусульфан 10 мг/кг). Троим пациентам алло-ТГСК была выполнена от HLA-совместимого (10/10) родственного (3) и неродственного (10) донора, от частично-совместимого (9/10) неродственного донора (2) и гаплоидентичного (5) донора. В качестве профилактики РТПХ использовался циклофосфамид 100 мг/кг в день +3, +4 и руксолитиниб 5-7,5 мг х 2 раза в сутки с дня +5 по день +50(2) и день +100(18). Медиана количества CD34+-клеток составила 6,7x10<sup>6</sup> (1,4-12,0). Исследование зарегистрировано на clinicaltrials.gov, NCT02806375. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Приживление трансплантата было зарегистрировано у 18 больных. Медиана времени до приживления по лейкоцитам составила 32 дня (18-61), по тромбоцитам – 38 дней (15-219). Повторная алло-ТГСК была выполнена в одном случае в связи с первичным неприживлением. Однако пациент погиб из-за инфекционных осложнений во время цитопении. Тяжелая гипофункция трансплантата наблюдалась у 11 пациентов. Гипофункция разрешилась самостоятельно у семи больных в течение 79 дней (16-470), в остальных случаях было выполнено введение CD34+ клеток (3). Трое из 4 пациентов погибли до приживления: 1 – сепсис <i>Pseudomonas aeruginosa</i>, 1 – желудочно-кишечное кровотечение, 1 –первичное неприживление и сепсис. Одна пациентка погибла в результате тромботической микроангиопатии (ТМА) на Д+115. Острая РТПХ 2-4 степени отмечалась у 29% пациентов, острая РТПХ3-4 степени – 18%. Во всех случаях, кроме одного, острая РТПХ 3-4 степени разрешилась на фоне терапии ингибиторами кальциневрина. Один пациент получал терапию системными глюкокортикостероидами. Хроническая РТПХ средней степени тяжести наблюдалась у 29% пациентов. Переносимость режима кондиционирования и протокол профилактики была удовлетворительная. Токсичность 3-4 степени, в частности токсический гепатит и сепсис, отмечались у 4 и 5 пациентов соответственно. Веноокклюзионная болезнь средней степени тяжести наблюдалась у 1 пациента, ТМА – 1. Реактивация цитомегаловируса отмечалась у 6 пациентов, EBV – 1, HHV 1 и 2 типа – 1, HHV 6 типа – 2, ВК вируса – 1, геморрагический цистит – 2. Двухлетлетняя общая выживаемость составила 80%. Все пациенты достигли молекулярной, клинико-гематологической ремиссии, полного донорского химеризма. Практически полный регресс фиброза в костном мозге зарегистрирован зарегистрирован у 12 пациентов. Ни в одном случае не отмечалось развитие рецидива заболевания. Трансплантационная летальность составила 15% и 20% через 100 дней и 1 год после алло-ТГСК соответственно. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Алло-ТГСК является эффективной терапевтической опцией для пациентов с миелофиброзом. Применение в посттрансплантационном периоде циклофосфамида в комбинации с руксолитинибом представляется эффективной терапевтической опцией в качестве профилактики РТПХ и рецидива заболевания. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Миелофиброз, аллогенная трансплантация гемопоэтических стволовых клеток, руксолитиниб, реакция «трансплантат против хозяина», профилактика, циклофосфамид. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(366) "Применение посттрансплантационного циклофосфамида и руксо- литиниба в качестве профилактики реакции трансплантат против хозяина и рецидива у пациентов с миелофиброзом: проспективное исследование" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(366) "Применение посттрансплантационного циклофосфамида и руксо- литиниба в качестве профилактики реакции трансплантат против хозяина и рецидива у пациентов с миелофиброзом: проспективное исследование" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(366) "Применение посттрансплантационного циклофосфамида и руксо- литиниба в качестве профилактики реакции трансплантат против хозяина и рецидива у пациентов с миелофиброзом: проспективное исследование" ["SECTION_META_TITLE"]=> string(366) "Применение посттрансплантационного циклофосфамида и руксо- литиниба в качестве профилактики реакции трансплантат против хозяина и рецидива у пациентов с миелофиброзом: проспективное исследование" ["SECTION_META_KEYWORDS"]=> string(366) "Применение посттрансплантационного циклофосфамида и руксо- литиниба в качестве профилактики реакции трансплантат против хозяина и рецидива у пациентов с миелофиброзом: проспективное исследование" ["SECTION_META_DESCRIPTION"]=> string(366) "Применение посттрансплантационного циклофосфамида и руксо- литиниба в качестве профилактики реакции трансплантат против хозяина и рецидива у пациентов с миелофиброзом: проспективное исследование" ["SECTION_PICTURE_FILE_ALT"]=> string(366) "Применение посттрансплантационного циклофосфамида и руксо- литиниба в качестве профилактики реакции трансплантат против хозяина и рецидива у пациентов с миелофиброзом: проспективное исследование" ["SECTION_PICTURE_FILE_TITLE"]=> string(366) "Применение посттрансплантационного циклофосфамида и руксо- литиниба в качестве профилактики реакции трансплантат против хозяина и рецидива у пациентов с миелофиброзом: проспективное исследование" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "primenenie-posttransplantatsionnogo-tsiklofosfamida-i-rukso-litiniba-v-kachestve-profilaktiki-reakts" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(366) "Применение посттрансплантационного циклофосфамида и руксо- литиниба в качестве профилактики реакции трансплантат против хозяина и рецидива у пациентов с миелофиброзом: проспективное исследование" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(366) "Применение посттрансплантационного циклофосфамида и руксо- литиниба в качестве профилактики реакции трансплантат против хозяина и рецидива у пациентов с миелофиброзом: проспективное исследование" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "primenenie-posttransplantatsionnogo-tsiklofosfamida-i-rukso-litiniba-v-kachestve-profilaktiki-reakts" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "primenenie-posttransplantatsionnogo-tsiklofosfamida-i-rukso-litiniba-v-kachestve-profilaktiki-reakts" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "primenenie-posttransplantatsionnogo-tsiklofosfamida-i-rukso-litiniba-v-kachestve-profilaktiki-reakts" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20285" ["VALUE"]=> array(2) { ["TEXT"]=> string(231) "Мария В. Барабанщикова, Иван С. Моисеев, Елена В. Морозова, Юлия Ю. Власова, Вадим В. Байков, Ильдар М. Бархатов, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(231) "Мария В. Барабанщикова, Иван С. Моисеев, Елена В. Морозова, Юлия Ю. Власова, Вадим В. Байков, Ильдар М. Бархатов, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20286" ["VALUE"]=> array(2) { ["TEXT"]=> string(406) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(400) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20342" ["VALUE"]=> array(2) { ["TEXT"]=> string(9561) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Миелофиброз относится к хроническим BCR-ABL-негативным миелопролиферативным неоплазиям и сопровождается, как правило, непрерывно прогрессирующим течением. Аллогенная трансплантация гемопоэтических стволовых клеток в настоящее время является единственным методом терапии, позволяющим добиться излечения от заболевания. Применение ингибитора JAK1/JAK2 руксолитиниба во многом позволяет изменить статус заболевания на момент алло-ТГСК – уменьшить спленомегалию, конституциональные симптомы, улучшить гематологические показатели, в ряде случаев привести к регрессу фиброза в костном мозге. В то же время руксолитиниб обладает иммуномодулирующим эффектом, благодаря чему широко используется для лечения острой и хронической РТПХ. В нашем исследовании мы использовали руксолитиниб в комбинации с посттрансплантационным циклофосфаном в качестве профилактики РТПХ и рецидива заболевания. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Мы проанализировали результаты алло-ТГСК у 20 пациентов в возрасте от 32 до 61 лет (медиана 51 год). У 14 пациентов был диагностирован первичный миелофиброз, у 2 пациентов – посттромбоцитемический миелофиброз, у 4 пациентов – постполицитемический миелофиброз. Одиннадцать пациентов относились к промежуточному-2 риску по шкале DIPSSplus, восемь – к высокой группе риска. Одному пациенту алло-ТГСК была выполнена в фазе бластного криза. У пятнадцати пациентов отмечалась мутация <i>JAK2V617F</i>, у двух – мутация в гене <i>MPL</i>, у трех – мутация в гене <i>CALR</i>. Все пациенты получали терапию руксолитинибом в качестве предтрансплантационной подготовки, медиана длительности терапии составила 6 месяцев (3-22) в дозе 30-45 мг. У восьми пациентов отмечалось клиническое улучшение, у 1 – прогрессирование заболевания, у 11 – стабилизации заболевания на момент алло-ТГСК. У семи пациентов была выполнена спленэктомия в связи с выраженной спленомегалией и недостаточным ответом со стороны селезенки. Во всех случаях применялся режим кондиционирования со сниженной интенсивностью доз (флударабин 180 мг/м<sup>2</sup>, бусульфан 10 мг/кг). Троим пациентам алло-ТГСК была выполнена от HLA-совместимого (10/10) родственного (3) и неродственного (10) донора, от частично-совместимого (9/10) неродственного донора (2) и гаплоидентичного (5) донора. В качестве профилактики РТПХ использовался циклофосфамид 100 мг/кг в день +3, +4 и руксолитиниб 5-7,5 мг х 2 раза в сутки с дня +5 по день +50(2) и день +100(18). Медиана количества CD34+-клеток составила 6,7x10<sup>6</sup> (1,4-12,0). Исследование зарегистрировано на clinicaltrials.gov, NCT02806375. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Приживление трансплантата было зарегистрировано у 18 больных. Медиана времени до приживления по лейкоцитам составила 32 дня (18-61), по тромбоцитам – 38 дней (15-219). Повторная алло-ТГСК была выполнена в одном случае в связи с первичным неприживлением. Однако пациент погиб из-за инфекционных осложнений во время цитопении. Тяжелая гипофункция трансплантата наблюдалась у 11 пациентов. Гипофункция разрешилась самостоятельно у семи больных в течение 79 дней (16-470), в остальных случаях было выполнено введение CD34+ клеток (3). Трое из 4 пациентов погибли до приживления: 1 – сепсис <i>Pseudomonas aeruginosa</i>, 1 – желудочно-кишечное кровотечение, 1 –первичное неприживление и сепсис. Одна пациентка погибла в результате тромботической микроангиопатии (ТМА) на Д+115. Острая РТПХ 2-4 степени отмечалась у 29% пациентов, острая РТПХ3-4 степени – 18%. Во всех случаях, кроме одного, острая РТПХ 3-4 степени разрешилась на фоне терапии ингибиторами кальциневрина. Один пациент получал терапию системными глюкокортикостероидами. Хроническая РТПХ средней степени тяжести наблюдалась у 29% пациентов. Переносимость режима кондиционирования и протокол профилактики была удовлетворительная. Токсичность 3-4 степени, в частности токсический гепатит и сепсис, отмечались у 4 и 5 пациентов соответственно. Веноокклюзионная болезнь средней степени тяжести наблюдалась у 1 пациента, ТМА – 1. Реактивация цитомегаловируса отмечалась у 6 пациентов, EBV – 1, HHV 1 и 2 типа – 1, HHV 6 типа – 2, ВК вируса – 1, геморрагический цистит – 2. Двухлетлетняя общая выживаемость составила 80%. Все пациенты достигли молекулярной, клинико-гематологической ремиссии, полного донорского химеризма. Практически полный регресс фиброза в костном мозге зарегистрирован зарегистрирован у 12 пациентов. Ни в одном случае не отмечалось развитие рецидива заболевания. Трансплантационная летальность составила 15% и 20% через 100 дней и 1 год после алло-ТГСК соответственно. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Алло-ТГСК является эффективной терапевтической опцией для пациентов с миелофиброзом. Применение в посттрансплантационном периоде циклофосфамида в комбинации с руксолитинибом представляется эффективной терапевтической опцией в качестве профилактики РТПХ и рецидива заболевания. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Миелофиброз, аллогенная трансплантация гемопоэтических стволовых клеток, руксолитиниб, реакция «трансплантат против хозяина», профилактика, циклофосфамид. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(9269) "
Введение
Миелофиброз относится к хроническим BCR-ABL-негативным миелопролиферативным неоплазиям и сопровождается, как правило, непрерывно прогрессирующим течением. Аллогенная трансплантация гемопоэтических стволовых клеток в настоящее время является единственным методом терапии, позволяющим добиться излечения от заболевания. Применение ингибитора JAK1/JAK2 руксолитиниба во многом позволяет изменить статус заболевания на момент алло-ТГСК – уменьшить спленомегалию, конституциональные симптомы, улучшить гематологические показатели, в ряде случаев привести к регрессу фиброза в костном мозге. В то же время руксолитиниб обладает иммуномодулирующим эффектом, благодаря чему широко используется для лечения острой и хронической РТПХ. В нашем исследовании мы использовали руксолитиниб в комбинации с посттрансплантационным циклофосфаном в качестве профилактики РТПХ и рецидива заболевания.
Материалы и методы
Мы проанализировали результаты алло-ТГСК у 20 пациентов в возрасте от 32 до 61 лет (медиана 51 год). У 14 пациентов был диагностирован первичный миелофиброз, у 2 пациентов – посттромбоцитемический миелофиброз, у 4 пациентов – постполицитемический миелофиброз. Одиннадцать пациентов относились к промежуточному-2 риску по шкале DIPSSplus, восемь – к высокой группе риска. Одному пациенту алло-ТГСК была выполнена в фазе бластного криза. У пятнадцати пациентов отмечалась мутация JAK2V617F, у двух – мутация в гене MPL, у трех – мутация в гене CALR. Все пациенты получали терапию руксолитинибом в качестве предтрансплантационной подготовки, медиана длительности терапии составила 6 месяцев (3-22) в дозе 30-45 мг. У восьми пациентов отмечалось клиническое улучшение, у 1 – прогрессирование заболевания, у 11 – стабилизации заболевания на момент алло-ТГСК. У семи пациентов была выполнена спленэктомия в связи с выраженной спленомегалией и недостаточным ответом со стороны селезенки. Во всех случаях применялся режим кондиционирования со сниженной интенсивностью доз (флударабин 180 мг/м2, бусульфан 10 мг/кг). Троим пациентам алло-ТГСК была выполнена от HLA-совместимого (10/10) родственного (3) и неродственного (10) донора, от частично-совместимого (9/10) неродственного донора (2) и гаплоидентичного (5) донора. В качестве профилактики РТПХ использовался циклофосфамид 100 мг/кг в день +3, +4 и руксолитиниб 5-7,5 мг х 2 раза в сутки с дня +5 по день +50(2) и день +100(18). Медиана количества CD34+-клеток составила 6,7x106 (1,4-12,0). Исследование зарегистрировано на clinicaltrials.gov, NCT02806375.
Результаты
Приживление трансплантата было зарегистрировано у 18 больных. Медиана времени до приживления по лейкоцитам составила 32 дня (18-61), по тромбоцитам – 38 дней (15-219). Повторная алло-ТГСК была выполнена в одном случае в связи с первичным неприживлением. Однако пациент погиб из-за инфекционных осложнений во время цитопении. Тяжелая гипофункция трансплантата наблюдалась у 11 пациентов. Гипофункция разрешилась самостоятельно у семи больных в течение 79 дней (16-470), в остальных случаях было выполнено введение CD34+ клеток (3). Трое из 4 пациентов погибли до приживления: 1 – сепсис Pseudomonas aeruginosa, 1 – желудочно-кишечное кровотечение, 1 –первичное неприживление и сепсис. Одна пациентка погибла в результате тромботической микроангиопатии (ТМА) на Д+115. Острая РТПХ 2-4 степени отмечалась у 29% пациентов, острая РТПХ3-4 степени – 18%. Во всех случаях, кроме одного, острая РТПХ 3-4 степени разрешилась на фоне терапии ингибиторами кальциневрина. Один пациент получал терапию системными глюкокортикостероидами. Хроническая РТПХ средней степени тяжести наблюдалась у 29% пациентов. Переносимость режима кондиционирования и протокол профилактики была удовлетворительная. Токсичность 3-4 степени, в частности токсический гепатит и сепсис, отмечались у 4 и 5 пациентов соответственно. Веноокклюзионная болезнь средней степени тяжести наблюдалась у 1 пациента, ТМА – 1. Реактивация цитомегаловируса отмечалась у 6 пациентов, EBV – 1, HHV 1 и 2 типа – 1, HHV 6 типа – 2, ВК вируса – 1, геморрагический цистит – 2. Двухлетлетняя общая выживаемость составила 80%. Все пациенты достигли молекулярной, клинико-гематологической ремиссии, полного донорского химеризма. Практически полный регресс фиброза в костном мозге зарегистрирован зарегистрирован у 12 пациентов. Ни в одном случае не отмечалось развитие рецидива заболевания. Трансплантационная летальность составила 15% и 20% через 100 дней и 1 год после алло-ТГСК соответственно.
Заключение
Алло-ТГСК является эффективной терапевтической опцией для пациентов с миелофиброзом. Применение в посттрансплантационном периоде циклофосфамида в комбинации с руксолитинибом представляется эффективной терапевтической опцией в качестве профилактики РТПХ и рецидива заболевания.
Ключевые слова
Миелофиброз, аллогенная трансплантация гемопоэтических стволовых клеток, руксолитиниб, реакция «трансплантат против хозяина», профилактика, циклофосфамид.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20287" ["VALUE"]=> array(2) { ["TEXT"]=> string(134) "Maria V. Barabanshikova, Ivan S. Moiseev, Elena V. Morozova, Julia J. Vlasova, Vadim V. Baykov, Ildar M. Barkhatov, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(134) "Maria V. Barabanshikova, Ivan S. Moiseev, Elena V. Morozova, Julia J. Vlasova, Vadim V. Baykov, Ildar M. Barkhatov, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20288" ["VALUE"]=> array(2) { ["TEXT"]=> string(179) "Raisa Gorbacheva Memorial Institute of Children’s Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(179) "Raisa Gorbacheva Memorial Institute of Children’s Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20343" ["VALUE"]=> array(2) { ["TEXT"]=> string(5340) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic stem cell transplantation (allo-HSCT) is currently the only treatment modality with curative potential in patients with myelofibrosis (MF), although transplant-associated complications and relapses significantly reduce the application of this method. JAK1/JAK2 inhibitor ruxolitinib is effective in reducing symptomatic splenomegaly and myelofibrosis-related symptoms. At the same time it has significant immunomodulatory effect, and is used for the treatment of steroid-refractory acute and chronic graft-versus-host disease (GVHD). This study evaluated calcineurin inhibitor-free GVHD prophylaxis regimen with ruxolitinib in combination with posttransplant cyclophosphamide (PTCy). </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Twenty patients at a median age of 51 (32-61) years were enrolled in the study. Two patients were diagnosed with post-essential thrombocythemia myelofibrosis, 4, with postpolycythemia vera myelofibrosis; 14, with primary myelofibrosis. By the DIPSSplus scale, 11 patients had intermediate-2, 8 patients had high-risk disease and 1 patient was transplanted in blast crisis. Fifteen patients were positive for <i>JAK2V617F</i>; 3 were <i>CALR</i>-positive; and 2 were <i>MPL</i>-positive before alloHSCT. All patients were treated with JAK1/2 inhibitors before alloHSCT, with median treatment duration of 6 months (3-22) at a dose of 30-45 mg. The disease stabilization occurred in 11 patients; clinical improvement, in 8, and the disease progression was observed in 1 case. Splenectomy was performed in 7 patients, due to poor spleen response. Reduced-intensity conditioning (fludarabine 180 mg/m2 plus busulfan 8-10 mg/kg) followed by allo-HSCT performed from full-matched related (n=3) or unrelated donor (n=10), and mismatched HSCT (HLA 9/10) from unrelated (n=2) or haploidentical donor (n=5). Graft-versus-host disease (GVHD) prophylaxis consisted of posttransplant cyclophosphamide 100 mg/kg at day +3, +4 and ruxolitinib 5-7.5 mg bid from day+5 to day +50 (n=2), and day +100 (n=18). G-CSF-mobilized peripheral blood progenitor cells (n=19) and bone marrow (n=1) were used as stem cell sources. Median number of CD34+cells/kg was 6.7x10<sup>6</sup> (1.4-12.0). The trial is registered on clinicaltrials.gov, NCT02806375. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Median follow-up time was 18 (6.6–36.1) months. Primary engraftment was documented in 18 patients. Median time to leukocyte engraftment was 32 days (18-61), to platelet engraftment, 38 days (15-219). One patient received second transplantation from the same donor due to primary graft failure. He died in cytopenia accomplished by sepsis. Severe poor graft function was documented in 11 patients. In 7 of these cases, it resolved spontaneously with a median duration of 79 days (16-470). Three patients recovered after CD34+ boost administration. Dose reduction of ruxolitinib to 10 mg/day due to poor graft function was performed in 8 patients. Three out of four deaths occurred before engraftment: one patient was lost due to <i>Pseudomonas aeruginosa </i><i>sepsis</i>, one death was associated with gastrointestinal bleeding, and one patient deceased due to primary graft failure and sepsis. One patient died due to thrombotic microangiopathy and sepsis on D+115. Twenty-nine percent of patients developed acute GVHD (grade 2-4), 18%, aGVHD grade 3-4. In all cases except of one, aGVHD grade 3-4 was successfully treated with calcineurin inhibitors. One patient required systemic steroid therapy. Moderate chronic GVHD (NIH) was documented in 29% of patients. The regimen was well tolerated. Grade 3-4 toxicities included only toxic hepatitis in 4 and sepsis in 5 patients. Mild veno-occlusive disease was observed in one patient, TMA, in one case. Viral reactivation was documented in 47% of patients, CMV (n=6), EBV (n=1), HHV type 1,2 (n=1), HHV type 6 (n=2), BK virus (n=1). Moderate hemorrhagic cystitis developed in 2 patients. Non-relapse mortality on D+100 was 15% and 20%, at 1 year. The two-year overall survival was 80%. All the patients achieved hematological, molecular remission and full donor chimerism. Near-complete resolution of bone marrow fibrosis was documented in 12 patients. No molecular or hematological relapses were registered. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> AlloHSCT is an effective treatment modality for myelofibrosis. GVHD prophylaxis using a combination of PTCy and ruxolitinib is associated with good acute and chronic GVHD control, and it seems to be a promising modality, at least for MF patients. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Myelofibrosis, allogeneic hematopoietic stem cell transplantation, ruxolitinib, graft-versus-host disease, prophylaxis, cyclophosphamide. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5048) "Introduction
Allogeneic stem cell transplantation (allo-HSCT) is currently the only treatment modality with curative potential in patients with myelofibrosis (MF), although transplant-associated complications and relapses significantly reduce the application of this method. JAK1/JAK2 inhibitor ruxolitinib is effective in reducing symptomatic splenomegaly and myelofibrosis-related symptoms. At the same time it has significant immunomodulatory effect, and is used for the treatment of steroid-refractory acute and chronic graft-versus-host disease (GVHD). This study evaluated calcineurin inhibitor-free GVHD prophylaxis regimen with ruxolitinib in combination with posttransplant cyclophosphamide (PTCy).
Patients and methods
Twenty patients at a median age of 51 (32-61) years were enrolled in the study. Two patients were diagnosed with post-essential thrombocythemia myelofibrosis, 4, with postpolycythemia vera myelofibrosis; 14, with primary myelofibrosis. By the DIPSSplus scale, 11 patients had intermediate-2, 8 patients had high-risk disease and 1 patient was transplanted in blast crisis. Fifteen patients were positive for JAK2V617F; 3 were CALR-positive; and 2 were MPL-positive before alloHSCT. All patients were treated with JAK1/2 inhibitors before alloHSCT, with median treatment duration of 6 months (3-22) at a dose of 30-45 mg. The disease stabilization occurred in 11 patients; clinical improvement, in 8, and the disease progression was observed in 1 case. Splenectomy was performed in 7 patients, due to poor spleen response. Reduced-intensity conditioning (fludarabine 180 mg/m2 plus busulfan 8-10 mg/kg) followed by allo-HSCT performed from full-matched related (n=3) or unrelated donor (n=10), and mismatched HSCT (HLA 9/10) from unrelated (n=2) or haploidentical donor (n=5). Graft-versus-host disease (GVHD) prophylaxis consisted of posttransplant cyclophosphamide 100 mg/kg at day +3, +4 and ruxolitinib 5-7.5 mg bid from day+5 to day +50 (n=2), and day +100 (n=18). G-CSF-mobilized peripheral blood progenitor cells (n=19) and bone marrow (n=1) were used as stem cell sources. Median number of CD34+cells/kg was 6.7x106 (1.4-12.0). The trial is registered on clinicaltrials.gov, NCT02806375.
Results
Median follow-up time was 18 (6.6–36.1) months. Primary engraftment was documented in 18 patients. Median time to leukocyte engraftment was 32 days (18-61), to platelet engraftment, 38 days (15-219). One patient received second transplantation from the same donor due to primary graft failure. He died in cytopenia accomplished by sepsis. Severe poor graft function was documented in 11 patients. In 7 of these cases, it resolved spontaneously with a median duration of 79 days (16-470). Three patients recovered after CD34+ boost administration. Dose reduction of ruxolitinib to 10 mg/day due to poor graft function was performed in 8 patients. Three out of four deaths occurred before engraftment: one patient was lost due to Pseudomonas aeruginosa sepsis, one death was associated with gastrointestinal bleeding, and one patient deceased due to primary graft failure and sepsis. One patient died due to thrombotic microangiopathy and sepsis on D+115. Twenty-nine percent of patients developed acute GVHD (grade 2-4), 18%, aGVHD grade 3-4. In all cases except of one, aGVHD grade 3-4 was successfully treated with calcineurin inhibitors. One patient required systemic steroid therapy. Moderate chronic GVHD (NIH) was documented in 29% of patients. The regimen was well tolerated. Grade 3-4 toxicities included only toxic hepatitis in 4 and sepsis in 5 patients. Mild veno-occlusive disease was observed in one patient, TMA, in one case. Viral reactivation was documented in 47% of patients, CMV (n=6), EBV (n=1), HHV type 1,2 (n=1), HHV type 6 (n=2), BK virus (n=1). Moderate hemorrhagic cystitis developed in 2 patients. Non-relapse mortality on D+100 was 15% and 20%, at 1 year. The two-year overall survival was 80%. All the patients achieved hematological, molecular remission and full donor chimerism. Near-complete resolution of bone marrow fibrosis was documented in 12 patients. No molecular or hematological relapses were registered.
Conclusion
AlloHSCT is an effective treatment modality for myelofibrosis. GVHD prophylaxis using a combination of PTCy and ruxolitinib is associated with good acute and chronic GVHD control, and it seems to be a promising modality, at least for MF patients.
Keywords
Myelofibrosis, allogeneic hematopoietic stem cell transplantation, ruxolitinib, graft-versus-host disease, prophylaxis, cyclophosphamide.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20289" ["VALUE"]=> string(176) "A pilot study of ruxolitinib combined with cyclophosphamide for graft-versus-host disease prophylaxis and relapse prevention in patients with myelofibrosis: a prospective study" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(176) "A pilot study of ruxolitinib combined with cyclophosphamide for graft-versus-host disease prophylaxis and relapse prevention in patients with myelofibrosis: a prospective study" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20735" ["VALUE"]=> string(4) "1371" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1371" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20736" ["VALUE"]=> string(4) "1372" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1372" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20287" ["VALUE"]=> array(2) { ["TEXT"]=> string(134) "Maria V. Barabanshikova, Ivan S. Moiseev, Elena V. Morozova, Julia J. Vlasova, Vadim V. Baykov, Ildar M. Barkhatov, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(134) "Maria V. Barabanshikova, Ivan S. Moiseev, Elena V. Morozova, Julia J. Vlasova, Vadim V. Baykov, Ildar M. Barkhatov, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(134) "Maria V. Barabanshikova, Ivan S. Moiseev, Elena V. Morozova, Julia J. Vlasova, Vadim V. Baykov, Ildar M. Barkhatov, Boris V. Afanasyev" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20343" ["VALUE"]=> array(2) { ["TEXT"]=> string(5340) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic stem cell transplantation (allo-HSCT) is currently the only treatment modality with curative potential in patients with myelofibrosis (MF), although transplant-associated complications and relapses significantly reduce the application of this method. JAK1/JAK2 inhibitor ruxolitinib is effective in reducing symptomatic splenomegaly and myelofibrosis-related symptoms. At the same time it has significant immunomodulatory effect, and is used for the treatment of steroid-refractory acute and chronic graft-versus-host disease (GVHD). This study evaluated calcineurin inhibitor-free GVHD prophylaxis regimen with ruxolitinib in combination with posttransplant cyclophosphamide (PTCy). </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Twenty patients at a median age of 51 (32-61) years were enrolled in the study. Two patients were diagnosed with post-essential thrombocythemia myelofibrosis, 4, with postpolycythemia vera myelofibrosis; 14, with primary myelofibrosis. By the DIPSSplus scale, 11 patients had intermediate-2, 8 patients had high-risk disease and 1 patient was transplanted in blast crisis. Fifteen patients were positive for <i>JAK2V617F</i>; 3 were <i>CALR</i>-positive; and 2 were <i>MPL</i>-positive before alloHSCT. All patients were treated with JAK1/2 inhibitors before alloHSCT, with median treatment duration of 6 months (3-22) at a dose of 30-45 mg. The disease stabilization occurred in 11 patients; clinical improvement, in 8, and the disease progression was observed in 1 case. Splenectomy was performed in 7 patients, due to poor spleen response. Reduced-intensity conditioning (fludarabine 180 mg/m2 plus busulfan 8-10 mg/kg) followed by allo-HSCT performed from full-matched related (n=3) or unrelated donor (n=10), and mismatched HSCT (HLA 9/10) from unrelated (n=2) or haploidentical donor (n=5). Graft-versus-host disease (GVHD) prophylaxis consisted of posttransplant cyclophosphamide 100 mg/kg at day +3, +4 and ruxolitinib 5-7.5 mg bid from day+5 to day +50 (n=2), and day +100 (n=18). G-CSF-mobilized peripheral blood progenitor cells (n=19) and bone marrow (n=1) were used as stem cell sources. Median number of CD34+cells/kg was 6.7x10<sup>6</sup> (1.4-12.0). The trial is registered on clinicaltrials.gov, NCT02806375. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Median follow-up time was 18 (6.6–36.1) months. Primary engraftment was documented in 18 patients. Median time to leukocyte engraftment was 32 days (18-61), to platelet engraftment, 38 days (15-219). One patient received second transplantation from the same donor due to primary graft failure. He died in cytopenia accomplished by sepsis. Severe poor graft function was documented in 11 patients. In 7 of these cases, it resolved spontaneously with a median duration of 79 days (16-470). Three patients recovered after CD34+ boost administration. Dose reduction of ruxolitinib to 10 mg/day due to poor graft function was performed in 8 patients. Three out of four deaths occurred before engraftment: one patient was lost due to <i>Pseudomonas aeruginosa </i><i>sepsis</i>, one death was associated with gastrointestinal bleeding, and one patient deceased due to primary graft failure and sepsis. One patient died due to thrombotic microangiopathy and sepsis on D+115. Twenty-nine percent of patients developed acute GVHD (grade 2-4), 18%, aGVHD grade 3-4. In all cases except of one, aGVHD grade 3-4 was successfully treated with calcineurin inhibitors. One patient required systemic steroid therapy. Moderate chronic GVHD (NIH) was documented in 29% of patients. The regimen was well tolerated. Grade 3-4 toxicities included only toxic hepatitis in 4 and sepsis in 5 patients. Mild veno-occlusive disease was observed in one patient, TMA, in one case. Viral reactivation was documented in 47% of patients, CMV (n=6), EBV (n=1), HHV type 1,2 (n=1), HHV type 6 (n=2), BK virus (n=1). Moderate hemorrhagic cystitis developed in 2 patients. Non-relapse mortality on D+100 was 15% and 20%, at 1 year. The two-year overall survival was 80%. All the patients achieved hematological, molecular remission and full donor chimerism. Near-complete resolution of bone marrow fibrosis was documented in 12 patients. No molecular or hematological relapses were registered. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> AlloHSCT is an effective treatment modality for myelofibrosis. GVHD prophylaxis using a combination of PTCy and ruxolitinib is associated with good acute and chronic GVHD control, and it seems to be a promising modality, at least for MF patients. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Myelofibrosis, allogeneic hematopoietic stem cell transplantation, ruxolitinib, graft-versus-host disease, prophylaxis, cyclophosphamide. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5048) "Introduction
Allogeneic stem cell transplantation (allo-HSCT) is currently the only treatment modality with curative potential in patients with myelofibrosis (MF), although transplant-associated complications and relapses significantly reduce the application of this method. JAK1/JAK2 inhibitor ruxolitinib is effective in reducing symptomatic splenomegaly and myelofibrosis-related symptoms. At the same time it has significant immunomodulatory effect, and is used for the treatment of steroid-refractory acute and chronic graft-versus-host disease (GVHD). This study evaluated calcineurin inhibitor-free GVHD prophylaxis regimen with ruxolitinib in combination with posttransplant cyclophosphamide (PTCy).
Patients and methods
Twenty patients at a median age of 51 (32-61) years were enrolled in the study. Two patients were diagnosed with post-essential thrombocythemia myelofibrosis, 4, with postpolycythemia vera myelofibrosis; 14, with primary myelofibrosis. By the DIPSSplus scale, 11 patients had intermediate-2, 8 patients had high-risk disease and 1 patient was transplanted in blast crisis. Fifteen patients were positive for JAK2V617F; 3 were CALR-positive; and 2 were MPL-positive before alloHSCT. All patients were treated with JAK1/2 inhibitors before alloHSCT, with median treatment duration of 6 months (3-22) at a dose of 30-45 mg. The disease stabilization occurred in 11 patients; clinical improvement, in 8, and the disease progression was observed in 1 case. Splenectomy was performed in 7 patients, due to poor spleen response. Reduced-intensity conditioning (fludarabine 180 mg/m2 plus busulfan 8-10 mg/kg) followed by allo-HSCT performed from full-matched related (n=3) or unrelated donor (n=10), and mismatched HSCT (HLA 9/10) from unrelated (n=2) or haploidentical donor (n=5). Graft-versus-host disease (GVHD) prophylaxis consisted of posttransplant cyclophosphamide 100 mg/kg at day +3, +4 and ruxolitinib 5-7.5 mg bid from day+5 to day +50 (n=2), and day +100 (n=18). G-CSF-mobilized peripheral blood progenitor cells (n=19) and bone marrow (n=1) were used as stem cell sources. Median number of CD34+cells/kg was 6.7x106 (1.4-12.0). The trial is registered on clinicaltrials.gov, NCT02806375.
Results
Median follow-up time was 18 (6.6–36.1) months. Primary engraftment was documented in 18 patients. Median time to leukocyte engraftment was 32 days (18-61), to platelet engraftment, 38 days (15-219). One patient received second transplantation from the same donor due to primary graft failure. He died in cytopenia accomplished by sepsis. Severe poor graft function was documented in 11 patients. In 7 of these cases, it resolved spontaneously with a median duration of 79 days (16-470). Three patients recovered after CD34+ boost administration. Dose reduction of ruxolitinib to 10 mg/day due to poor graft function was performed in 8 patients. Three out of four deaths occurred before engraftment: one patient was lost due to Pseudomonas aeruginosa sepsis, one death was associated with gastrointestinal bleeding, and one patient deceased due to primary graft failure and sepsis. One patient died due to thrombotic microangiopathy and sepsis on D+115. Twenty-nine percent of patients developed acute GVHD (grade 2-4), 18%, aGVHD grade 3-4. In all cases except of one, aGVHD grade 3-4 was successfully treated with calcineurin inhibitors. One patient required systemic steroid therapy. Moderate chronic GVHD (NIH) was documented in 29% of patients. The regimen was well tolerated. Grade 3-4 toxicities included only toxic hepatitis in 4 and sepsis in 5 patients. Mild veno-occlusive disease was observed in one patient, TMA, in one case. Viral reactivation was documented in 47% of patients, CMV (n=6), EBV (n=1), HHV type 1,2 (n=1), HHV type 6 (n=2), BK virus (n=1). Moderate hemorrhagic cystitis developed in 2 patients. Non-relapse mortality on D+100 was 15% and 20%, at 1 year. The two-year overall survival was 80%. All the patients achieved hematological, molecular remission and full donor chimerism. Near-complete resolution of bone marrow fibrosis was documented in 12 patients. No molecular or hematological relapses were registered.
Conclusion
AlloHSCT is an effective treatment modality for myelofibrosis. GVHD prophylaxis using a combination of PTCy and ruxolitinib is associated with good acute and chronic GVHD control, and it seems to be a promising modality, at least for MF patients.
Keywords
Myelofibrosis, allogeneic hematopoietic stem cell transplantation, ruxolitinib, graft-versus-host disease, prophylaxis, cyclophosphamide.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(5048) "Introduction
Allogeneic stem cell transplantation (allo-HSCT) is currently the only treatment modality with curative potential in patients with myelofibrosis (MF), although transplant-associated complications and relapses significantly reduce the application of this method. JAK1/JAK2 inhibitor ruxolitinib is effective in reducing symptomatic splenomegaly and myelofibrosis-related symptoms. At the same time it has significant immunomodulatory effect, and is used for the treatment of steroid-refractory acute and chronic graft-versus-host disease (GVHD). This study evaluated calcineurin inhibitor-free GVHD prophylaxis regimen with ruxolitinib in combination with posttransplant cyclophosphamide (PTCy).
Patients and methods
Twenty patients at a median age of 51 (32-61) years were enrolled in the study. Two patients were diagnosed with post-essential thrombocythemia myelofibrosis, 4, with postpolycythemia vera myelofibrosis; 14, with primary myelofibrosis. By the DIPSSplus scale, 11 patients had intermediate-2, 8 patients had high-risk disease and 1 patient was transplanted in blast crisis. Fifteen patients were positive for JAK2V617F; 3 were CALR-positive; and 2 were MPL-positive before alloHSCT. All patients were treated with JAK1/2 inhibitors before alloHSCT, with median treatment duration of 6 months (3-22) at a dose of 30-45 mg. The disease stabilization occurred in 11 patients; clinical improvement, in 8, and the disease progression was observed in 1 case. Splenectomy was performed in 7 patients, due to poor spleen response. Reduced-intensity conditioning (fludarabine 180 mg/m2 plus busulfan 8-10 mg/kg) followed by allo-HSCT performed from full-matched related (n=3) or unrelated donor (n=10), and mismatched HSCT (HLA 9/10) from unrelated (n=2) or haploidentical donor (n=5). Graft-versus-host disease (GVHD) prophylaxis consisted of posttransplant cyclophosphamide 100 mg/kg at day +3, +4 and ruxolitinib 5-7.5 mg bid from day+5 to day +50 (n=2), and day +100 (n=18). G-CSF-mobilized peripheral blood progenitor cells (n=19) and bone marrow (n=1) were used as stem cell sources. Median number of CD34+cells/kg was 6.7x106 (1.4-12.0). The trial is registered on clinicaltrials.gov, NCT02806375.
Results
Median follow-up time was 18 (6.6–36.1) months. Primary engraftment was documented in 18 patients. Median time to leukocyte engraftment was 32 days (18-61), to platelet engraftment, 38 days (15-219). One patient received second transplantation from the same donor due to primary graft failure. He died in cytopenia accomplished by sepsis. Severe poor graft function was documented in 11 patients. In 7 of these cases, it resolved spontaneously with a median duration of 79 days (16-470). Three patients recovered after CD34+ boost administration. Dose reduction of ruxolitinib to 10 mg/day due to poor graft function was performed in 8 patients. Three out of four deaths occurred before engraftment: one patient was lost due to Pseudomonas aeruginosa sepsis, one death was associated with gastrointestinal bleeding, and one patient deceased due to primary graft failure and sepsis. One patient died due to thrombotic microangiopathy and sepsis on D+115. Twenty-nine percent of patients developed acute GVHD (grade 2-4), 18%, aGVHD grade 3-4. In all cases except of one, aGVHD grade 3-4 was successfully treated with calcineurin inhibitors. One patient required systemic steroid therapy. Moderate chronic GVHD (NIH) was documented in 29% of patients. The regimen was well tolerated. Grade 3-4 toxicities included only toxic hepatitis in 4 and sepsis in 5 patients. Mild veno-occlusive disease was observed in one patient, TMA, in one case. Viral reactivation was documented in 47% of patients, CMV (n=6), EBV (n=1), HHV type 1,2 (n=1), HHV type 6 (n=2), BK virus (n=1). Moderate hemorrhagic cystitis developed in 2 patients. Non-relapse mortality on D+100 was 15% and 20%, at 1 year. The two-year overall survival was 80%. All the patients achieved hematological, molecular remission and full donor chimerism. Near-complete resolution of bone marrow fibrosis was documented in 12 patients. No molecular or hematological relapses were registered.
Conclusion
AlloHSCT is an effective treatment modality for myelofibrosis. GVHD prophylaxis using a combination of PTCy and ruxolitinib is associated with good acute and chronic GVHD control, and it seems to be a promising modality, at least for MF patients.
Keywords
Myelofibrosis, allogeneic hematopoietic stem cell transplantation, ruxolitinib, graft-versus-host disease, prophylaxis, cyclophosphamide.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20289" ["VALUE"]=> string(176) "A pilot study of ruxolitinib combined with cyclophosphamide for graft-versus-host disease prophylaxis and relapse prevention in patients with myelofibrosis: a prospective study" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(176) "A pilot study of ruxolitinib combined with cyclophosphamide for graft-versus-host disease prophylaxis and relapse prevention in patients with myelofibrosis: a prospective study" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(176) "A pilot study of ruxolitinib combined with cyclophosphamide for graft-versus-host disease prophylaxis and relapse prevention in patients with myelofibrosis: a prospective study" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20288" ["VALUE"]=> array(2) { ["TEXT"]=> string(179) "Raisa Gorbacheva Memorial Institute of Children’s Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(179) "Raisa Gorbacheva Memorial Institute of Children’s Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(179) "Raisa Gorbacheva Memorial Institute of Children’s Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20285" ["VALUE"]=> array(2) { ["TEXT"]=> string(231) "Мария В. Барабанщикова, Иван С. Моисеев, Елена В. Морозова, Юлия Ю. Власова, Вадим В. Байков, Ильдар М. Бархатов, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(231) "Мария В. Барабанщикова, Иван С. Моисеев, Елена В. Морозова, Юлия Ю. Власова, Вадим В. Байков, Ильдар М. Бархатов, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(231) "Мария В. Барабанщикова, Иван С. Моисеев, Елена В. Морозова, Юлия Ю. Власова, Вадим В. Байков, Ильдар М. Бархатов, Борис В. Афанасьев" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20342" ["VALUE"]=> array(2) { ["TEXT"]=> string(9561) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Миелофиброз относится к хроническим BCR-ABL-негативным миелопролиферативным неоплазиям и сопровождается, как правило, непрерывно прогрессирующим течением. Аллогенная трансплантация гемопоэтических стволовых клеток в настоящее время является единственным методом терапии, позволяющим добиться излечения от заболевания. Применение ингибитора JAK1/JAK2 руксолитиниба во многом позволяет изменить статус заболевания на момент алло-ТГСК – уменьшить спленомегалию, конституциональные симптомы, улучшить гематологические показатели, в ряде случаев привести к регрессу фиброза в костном мозге. В то же время руксолитиниб обладает иммуномодулирующим эффектом, благодаря чему широко используется для лечения острой и хронической РТПХ. В нашем исследовании мы использовали руксолитиниб в комбинации с посттрансплантационным циклофосфаном в качестве профилактики РТПХ и рецидива заболевания. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Мы проанализировали результаты алло-ТГСК у 20 пациентов в возрасте от 32 до 61 лет (медиана 51 год). У 14 пациентов был диагностирован первичный миелофиброз, у 2 пациентов – посттромбоцитемический миелофиброз, у 4 пациентов – постполицитемический миелофиброз. Одиннадцать пациентов относились к промежуточному-2 риску по шкале DIPSSplus, восемь – к высокой группе риска. Одному пациенту алло-ТГСК была выполнена в фазе бластного криза. У пятнадцати пациентов отмечалась мутация <i>JAK2V617F</i>, у двух – мутация в гене <i>MPL</i>, у трех – мутация в гене <i>CALR</i>. Все пациенты получали терапию руксолитинибом в качестве предтрансплантационной подготовки, медиана длительности терапии составила 6 месяцев (3-22) в дозе 30-45 мг. У восьми пациентов отмечалось клиническое улучшение, у 1 – прогрессирование заболевания, у 11 – стабилизации заболевания на момент алло-ТГСК. У семи пациентов была выполнена спленэктомия в связи с выраженной спленомегалией и недостаточным ответом со стороны селезенки. Во всех случаях применялся режим кондиционирования со сниженной интенсивностью доз (флударабин 180 мг/м<sup>2</sup>, бусульфан 10 мг/кг). Троим пациентам алло-ТГСК была выполнена от HLA-совместимого (10/10) родственного (3) и неродственного (10) донора, от частично-совместимого (9/10) неродственного донора (2) и гаплоидентичного (5) донора. В качестве профилактики РТПХ использовался циклофосфамид 100 мг/кг в день +3, +4 и руксолитиниб 5-7,5 мг х 2 раза в сутки с дня +5 по день +50(2) и день +100(18). Медиана количества CD34+-клеток составила 6,7x10<sup>6</sup> (1,4-12,0). Исследование зарегистрировано на clinicaltrials.gov, NCT02806375. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Приживление трансплантата было зарегистрировано у 18 больных. Медиана времени до приживления по лейкоцитам составила 32 дня (18-61), по тромбоцитам – 38 дней (15-219). Повторная алло-ТГСК была выполнена в одном случае в связи с первичным неприживлением. Однако пациент погиб из-за инфекционных осложнений во время цитопении. Тяжелая гипофункция трансплантата наблюдалась у 11 пациентов. Гипофункция разрешилась самостоятельно у семи больных в течение 79 дней (16-470), в остальных случаях было выполнено введение CD34+ клеток (3). Трое из 4 пациентов погибли до приживления: 1 – сепсис <i>Pseudomonas aeruginosa</i>, 1 – желудочно-кишечное кровотечение, 1 –первичное неприживление и сепсис. Одна пациентка погибла в результате тромботической микроангиопатии (ТМА) на Д+115. Острая РТПХ 2-4 степени отмечалась у 29% пациентов, острая РТПХ3-4 степени – 18%. Во всех случаях, кроме одного, острая РТПХ 3-4 степени разрешилась на фоне терапии ингибиторами кальциневрина. Один пациент получал терапию системными глюкокортикостероидами. Хроническая РТПХ средней степени тяжести наблюдалась у 29% пациентов. Переносимость режима кондиционирования и протокол профилактики была удовлетворительная. Токсичность 3-4 степени, в частности токсический гепатит и сепсис, отмечались у 4 и 5 пациентов соответственно. Веноокклюзионная болезнь средней степени тяжести наблюдалась у 1 пациента, ТМА – 1. Реактивация цитомегаловируса отмечалась у 6 пациентов, EBV – 1, HHV 1 и 2 типа – 1, HHV 6 типа – 2, ВК вируса – 1, геморрагический цистит – 2. Двухлетлетняя общая выживаемость составила 80%. Все пациенты достигли молекулярной, клинико-гематологической ремиссии, полного донорского химеризма. Практически полный регресс фиброза в костном мозге зарегистрирован зарегистрирован у 12 пациентов. Ни в одном случае не отмечалось развитие рецидива заболевания. Трансплантационная летальность составила 15% и 20% через 100 дней и 1 год после алло-ТГСК соответственно. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Алло-ТГСК является эффективной терапевтической опцией для пациентов с миелофиброзом. Применение в посттрансплантационном периоде циклофосфамида в комбинации с руксолитинибом представляется эффективной терапевтической опцией в качестве профилактики РТПХ и рецидива заболевания. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Миелофиброз, аллогенная трансплантация гемопоэтических стволовых клеток, руксолитиниб, реакция «трансплантат против хозяина», профилактика, циклофосфамид. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(9269) "Введение
Миелофиброз относится к хроническим BCR-ABL-негативным миелопролиферативным неоплазиям и сопровождается, как правило, непрерывно прогрессирующим течением. Аллогенная трансплантация гемопоэтических стволовых клеток в настоящее время является единственным методом терапии, позволяющим добиться излечения от заболевания. Применение ингибитора JAK1/JAK2 руксолитиниба во многом позволяет изменить статус заболевания на момент алло-ТГСК – уменьшить спленомегалию, конституциональные симптомы, улучшить гематологические показатели, в ряде случаев привести к регрессу фиброза в костном мозге. В то же время руксолитиниб обладает иммуномодулирующим эффектом, благодаря чему широко используется для лечения острой и хронической РТПХ. В нашем исследовании мы использовали руксолитиниб в комбинации с посттрансплантационным циклофосфаном в качестве профилактики РТПХ и рецидива заболевания.
Материалы и методы
Мы проанализировали результаты алло-ТГСК у 20 пациентов в возрасте от 32 до 61 лет (медиана 51 год). У 14 пациентов был диагностирован первичный миелофиброз, у 2 пациентов – посттромбоцитемический миелофиброз, у 4 пациентов – постполицитемический миелофиброз. Одиннадцать пациентов относились к промежуточному-2 риску по шкале DIPSSplus, восемь – к высокой группе риска. Одному пациенту алло-ТГСК была выполнена в фазе бластного криза. У пятнадцати пациентов отмечалась мутация JAK2V617F, у двух – мутация в гене MPL, у трех – мутация в гене CALR. Все пациенты получали терапию руксолитинибом в качестве предтрансплантационной подготовки, медиана длительности терапии составила 6 месяцев (3-22) в дозе 30-45 мг. У восьми пациентов отмечалось клиническое улучшение, у 1 – прогрессирование заболевания, у 11 – стабилизации заболевания на момент алло-ТГСК. У семи пациентов была выполнена спленэктомия в связи с выраженной спленомегалией и недостаточным ответом со стороны селезенки. Во всех случаях применялся режим кондиционирования со сниженной интенсивностью доз (флударабин 180 мг/м2, бусульфан 10 мг/кг). Троим пациентам алло-ТГСК была выполнена от HLA-совместимого (10/10) родственного (3) и неродственного (10) донора, от частично-совместимого (9/10) неродственного донора (2) и гаплоидентичного (5) донора. В качестве профилактики РТПХ использовался циклофосфамид 100 мг/кг в день +3, +4 и руксолитиниб 5-7,5 мг х 2 раза в сутки с дня +5 по день +50(2) и день +100(18). Медиана количества CD34+-клеток составила 6,7x106 (1,4-12,0). Исследование зарегистрировано на clinicaltrials.gov, NCT02806375.
Результаты
Приживление трансплантата было зарегистрировано у 18 больных. Медиана времени до приживления по лейкоцитам составила 32 дня (18-61), по тромбоцитам – 38 дней (15-219). Повторная алло-ТГСК была выполнена в одном случае в связи с первичным неприживлением. Однако пациент погиб из-за инфекционных осложнений во время цитопении. Тяжелая гипофункция трансплантата наблюдалась у 11 пациентов. Гипофункция разрешилась самостоятельно у семи больных в течение 79 дней (16-470), в остальных случаях было выполнено введение CD34+ клеток (3). Трое из 4 пациентов погибли до приживления: 1 – сепсис Pseudomonas aeruginosa, 1 – желудочно-кишечное кровотечение, 1 –первичное неприживление и сепсис. Одна пациентка погибла в результате тромботической микроангиопатии (ТМА) на Д+115. Острая РТПХ 2-4 степени отмечалась у 29% пациентов, острая РТПХ3-4 степени – 18%. Во всех случаях, кроме одного, острая РТПХ 3-4 степени разрешилась на фоне терапии ингибиторами кальциневрина. Один пациент получал терапию системными глюкокортикостероидами. Хроническая РТПХ средней степени тяжести наблюдалась у 29% пациентов. Переносимость режима кондиционирования и протокол профилактики была удовлетворительная. Токсичность 3-4 степени, в частности токсический гепатит и сепсис, отмечались у 4 и 5 пациентов соответственно. Веноокклюзионная болезнь средней степени тяжести наблюдалась у 1 пациента, ТМА – 1. Реактивация цитомегаловируса отмечалась у 6 пациентов, EBV – 1, HHV 1 и 2 типа – 1, HHV 6 типа – 2, ВК вируса – 1, геморрагический цистит – 2. Двухлетлетняя общая выживаемость составила 80%. Все пациенты достигли молекулярной, клинико-гематологической ремиссии, полного донорского химеризма. Практически полный регресс фиброза в костном мозге зарегистрирован зарегистрирован у 12 пациентов. Ни в одном случае не отмечалось развитие рецидива заболевания. Трансплантационная летальность составила 15% и 20% через 100 дней и 1 год после алло-ТГСК соответственно.
Заключение
Алло-ТГСК является эффективной терапевтической опцией для пациентов с миелофиброзом. Применение в посттрансплантационном периоде циклофосфамида в комбинации с руксолитинибом представляется эффективной терапевтической опцией в качестве профилактики РТПХ и рецидива заболевания.
Ключевые слова
Миелофиброз, аллогенная трансплантация гемопоэтических стволовых клеток, руксолитиниб, реакция «трансплантат против хозяина», профилактика, циклофосфамид.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(9269) "Введение
Миелофиброз относится к хроническим BCR-ABL-негативным миелопролиферативным неоплазиям и сопровождается, как правило, непрерывно прогрессирующим течением. Аллогенная трансплантация гемопоэтических стволовых клеток в настоящее время является единственным методом терапии, позволяющим добиться излечения от заболевания. Применение ингибитора JAK1/JAK2 руксолитиниба во многом позволяет изменить статус заболевания на момент алло-ТГСК – уменьшить спленомегалию, конституциональные симптомы, улучшить гематологические показатели, в ряде случаев привести к регрессу фиброза в костном мозге. В то же время руксолитиниб обладает иммуномодулирующим эффектом, благодаря чему широко используется для лечения острой и хронической РТПХ. В нашем исследовании мы использовали руксолитиниб в комбинации с посттрансплантационным циклофосфаном в качестве профилактики РТПХ и рецидива заболевания.
Материалы и методы
Мы проанализировали результаты алло-ТГСК у 20 пациентов в возрасте от 32 до 61 лет (медиана 51 год). У 14 пациентов был диагностирован первичный миелофиброз, у 2 пациентов – посттромбоцитемический миелофиброз, у 4 пациентов – постполицитемический миелофиброз. Одиннадцать пациентов относились к промежуточному-2 риску по шкале DIPSSplus, восемь – к высокой группе риска. Одному пациенту алло-ТГСК была выполнена в фазе бластного криза. У пятнадцати пациентов отмечалась мутация JAK2V617F, у двух – мутация в гене MPL, у трех – мутация в гене CALR. Все пациенты получали терапию руксолитинибом в качестве предтрансплантационной подготовки, медиана длительности терапии составила 6 месяцев (3-22) в дозе 30-45 мг. У восьми пациентов отмечалось клиническое улучшение, у 1 – прогрессирование заболевания, у 11 – стабилизации заболевания на момент алло-ТГСК. У семи пациентов была выполнена спленэктомия в связи с выраженной спленомегалией и недостаточным ответом со стороны селезенки. Во всех случаях применялся режим кондиционирования со сниженной интенсивностью доз (флударабин 180 мг/м2, бусульфан 10 мг/кг). Троим пациентам алло-ТГСК была выполнена от HLA-совместимого (10/10) родственного (3) и неродственного (10) донора, от частично-совместимого (9/10) неродственного донора (2) и гаплоидентичного (5) донора. В качестве профилактики РТПХ использовался циклофосфамид 100 мг/кг в день +3, +4 и руксолитиниб 5-7,5 мг х 2 раза в сутки с дня +5 по день +50(2) и день +100(18). Медиана количества CD34+-клеток составила 6,7x106 (1,4-12,0). Исследование зарегистрировано на clinicaltrials.gov, NCT02806375.
Результаты
Приживление трансплантата было зарегистрировано у 18 больных. Медиана времени до приживления по лейкоцитам составила 32 дня (18-61), по тромбоцитам – 38 дней (15-219). Повторная алло-ТГСК была выполнена в одном случае в связи с первичным неприживлением. Однако пациент погиб из-за инфекционных осложнений во время цитопении. Тяжелая гипофункция трансплантата наблюдалась у 11 пациентов. Гипофункция разрешилась самостоятельно у семи больных в течение 79 дней (16-470), в остальных случаях было выполнено введение CD34+ клеток (3). Трое из 4 пациентов погибли до приживления: 1 – сепсис Pseudomonas aeruginosa, 1 – желудочно-кишечное кровотечение, 1 –первичное неприживление и сепсис. Одна пациентка погибла в результате тромботической микроангиопатии (ТМА) на Д+115. Острая РТПХ 2-4 степени отмечалась у 29% пациентов, острая РТПХ3-4 степени – 18%. Во всех случаях, кроме одного, острая РТПХ 3-4 степени разрешилась на фоне терапии ингибиторами кальциневрина. Один пациент получал терапию системными глюкокортикостероидами. Хроническая РТПХ средней степени тяжести наблюдалась у 29% пациентов. Переносимость режима кондиционирования и протокол профилактики была удовлетворительная. Токсичность 3-4 степени, в частности токсический гепатит и сепсис, отмечались у 4 и 5 пациентов соответственно. Веноокклюзионная болезнь средней степени тяжести наблюдалась у 1 пациента, ТМА – 1. Реактивация цитомегаловируса отмечалась у 6 пациентов, EBV – 1, HHV 1 и 2 типа – 1, HHV 6 типа – 2, ВК вируса – 1, геморрагический цистит – 2. Двухлетлетняя общая выживаемость составила 80%. Все пациенты достигли молекулярной, клинико-гематологической ремиссии, полного донорского химеризма. Практически полный регресс фиброза в костном мозге зарегистрирован зарегистрирован у 12 пациентов. Ни в одном случае не отмечалось развитие рецидива заболевания. Трансплантационная летальность составила 15% и 20% через 100 дней и 1 год после алло-ТГСК соответственно.
Заключение
Алло-ТГСК является эффективной терапевтической опцией для пациентов с миелофиброзом. Применение в посттрансплантационном периоде циклофосфамида в комбинации с руксолитинибом представляется эффективной терапевтической опцией в качестве профилактики РТПХ и рецидива заболевания.
Ключевые слова
Миелофиброз, аллогенная трансплантация гемопоэтических стволовых клеток, руксолитиниб, реакция «трансплантат против хозяина», профилактика, циклофосфамид.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20286" ["VALUE"]=> array(2) { ["TEXT"]=> string(406) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(400) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(400) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
" } } } [18]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1550" ["~ID"]=> string(4) "1550" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(148) "Сестринский уход за пациентами, получившими терапию моноклональными антителами" ["~NAME"]=> string(148) "Сестринский уход за пациентами, получившими терапию моноклональными антителами" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:23:12" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:23:12" ["DETAIL_PAGE_URL"]=> string(131) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/sestrinskiy-ukhod-za-patsientami-poluchivshimi-terapiyu-monoklonalnymi-antitelami/" ["~DETAIL_PAGE_URL"]=> string(131) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/sestrinskiy-ukhod-za-patsientami-poluchivshimi-terapiyu-monoklonalnymi-antitelami/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(81) "sestrinskiy-ukhod-za-patsientami-poluchivshimi-terapiyu-monoklonalnymi-antitelami" ["~CODE"]=> string(81) "sestrinskiy-ukhod-za-patsientami-poluchivshimi-terapiyu-monoklonalnymi-antitelami" ["EXTERNAL_ID"]=> string(4) "1550" ["~EXTERNAL_ID"]=> string(4) "1550" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(148) "Сестринский уход за пациентами, получившими терапию моноклональными антителами" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(221) "Сестринский уход за пациентами, получившими терапию моноклональными антителамиNursing care for patients who received therapy with monoclonal antibodies" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(3694) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Иммунотерапия моноклональными антителами – это новый вид лечения лейкозов, постепенно вводимый в практику российских гематологических клиник. Большинство препаратов входят в группу расширенного доступа, и не имеют инструкции на русском языке. </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Рассмотреть тактику ухода за пациентами, получившими терапию моноклональными антителами. Предложить рекомендации для медицинских сестер, работающих с моноклональными АТ. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В исследование было включено 45 человек, все они являлись пациентами отделения трасплантации костного мозга для детей №1 (ОТКМ №1) НИИ ДОГиТ им. Р. М. Горбачевой. Медиана возраста составила 8,7 лет (4 мес. – 17 лет). У 80% (n=36) диагностирован острый лимфобластный лейкоз (ОЛЛ), у 13,3% (n=6) острый миелобластный лейкоз (ОМЛ), а у 6,7% (n=3) был выявлен острый бифенотипический лейкоз (ОБЛ). Терапию Блинатумомабом получило 36 пациентов, Милотаргом – 6 человек, а Инотузумаб озогамицин получили 5 пациентов. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> У 62,2% (n=28) встречалась фебрильная лихорадка. После терапии моноклональными АТ 35,5% (n=16) была проведена родственная трансплантация гемопоэтических стволовых клеток (ТГСК), 26,7% (n=12) получили гаплоидентичную ТГСК, а 37,8 (n=17) не получали ТГСК. На август 2018 года живы 64,4% (n=29) пациентов. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Большинство пациентов получили терапию моноклональными АТ в качестве 3-й линии терапии. Лечение и уход за такими пациентами требуют особого внимания. Также, за неимением инструкции на русском языке, необходимо составить регламент приготовления раствора с моноклональным АТ. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Иммунотерапия, Милотарг, моноклональные антитела, Блинатумомаб, Инотузумаб. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(148) "Сестринский уход за пациентами, получившими терапию моноклональными антителами" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(148) "Сестринский уход за пациентами, получившими терапию моноклональными антителами" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(148) "Сестринский уход за пациентами, получившими терапию моноклональными антителами" ["SECTION_META_TITLE"]=> string(148) "Сестринский уход за пациентами, получившими терапию моноклональными антителами" ["SECTION_META_KEYWORDS"]=> string(148) "Сестринский уход за пациентами, получившими терапию моноклональными антителами" ["SECTION_META_DESCRIPTION"]=> string(148) "Сестринский уход за пациентами, получившими терапию моноклональными антителами" ["SECTION_PICTURE_FILE_ALT"]=> string(148) "Сестринский уход за пациентами, получившими терапию моноклональными антителами" ["SECTION_PICTURE_FILE_TITLE"]=> string(148) "Сестринский уход за пациентами, получившими терапию моноклональными антителами" ["SECTION_PICTURE_FILE_NAME"]=> string(85) "sestrinskiy-ukhod-za-patsientami-poluchivshimi-terapiyu-monoklonalnymi-antitelami-img" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(148) "Сестринский уход за пациентами, получившими терапию моноклональными антителами" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(148) "Сестринский уход за пациентами, получившими терапию моноклональными антителами" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(85) "sestrinskiy-ukhod-za-patsientami-poluchivshimi-terapiyu-monoklonalnymi-antitelami-img" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(85) "sestrinskiy-ukhod-za-patsientami-poluchivshimi-terapiyu-monoklonalnymi-antitelami-img" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(85) "sestrinskiy-ukhod-za-patsientami-poluchivshimi-terapiyu-monoklonalnymi-antitelami-img" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20277" ["VALUE"]=> array(2) { ["TEXT"]=> string(99) "Анна А. Апостолова, Олеся В. Паина, Юлия В. Богославская" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(99) "Анна А. Апостолова, Олеся В. Паина, Юлия В. Богославская" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20278" ["VALUE"]=> array(2) { ["TEXT"]=> string(416) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой (CIC 725), Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(410) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой (CIC 725), Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20354" ["VALUE"]=> array(2) { ["TEXT"]=> string(3694) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Иммунотерапия моноклональными антителами – это новый вид лечения лейкозов, постепенно вводимый в практику российских гематологических клиник. Большинство препаратов входят в группу расширенного доступа, и не имеют инструкции на русском языке. </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Рассмотреть тактику ухода за пациентами, получившими терапию моноклональными антителами. Предложить рекомендации для медицинских сестер, работающих с моноклональными АТ. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В исследование было включено 45 человек, все они являлись пациентами отделения трасплантации костного мозга для детей №1 (ОТКМ №1) НИИ ДОГиТ им. Р. М. Горбачевой. Медиана возраста составила 8,7 лет (4 мес. – 17 лет). У 80% (n=36) диагностирован острый лимфобластный лейкоз (ОЛЛ), у 13,3% (n=6) острый миелобластный лейкоз (ОМЛ), а у 6,7% (n=3) был выявлен острый бифенотипический лейкоз (ОБЛ). Терапию Блинатумомабом получило 36 пациентов, Милотаргом – 6 человек, а Инотузумаб озогамицин получили 5 пациентов. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> У 62,2% (n=28) встречалась фебрильная лихорадка. После терапии моноклональными АТ 35,5% (n=16) была проведена родственная трансплантация гемопоэтических стволовых клеток (ТГСК), 26,7% (n=12) получили гаплоидентичную ТГСК, а 37,8 (n=17) не получали ТГСК. На август 2018 года живы 64,4% (n=29) пациентов. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Большинство пациентов получили терапию моноклональными АТ в качестве 3-й линии терапии. Лечение и уход за такими пациентами требуют особого внимания. Также, за неимением инструкции на русском языке, необходимо составить регламент приготовления раствора с моноклональным АТ. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Иммунотерапия, Милотарг, моноклональные антитела, Блинатумомаб, Инотузумаб. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3430) "
Введение
Иммунотерапия моноклональными антителами – это новый вид лечения лейкозов, постепенно вводимый в практику российских гематологических клиник. Большинство препаратов входят в группу расширенного доступа, и не имеют инструкции на русском языке.
Цель работы
Рассмотреть тактику ухода за пациентами, получившими терапию моноклональными антителами. Предложить рекомендации для медицинских сестер, работающих с моноклональными АТ.
Материалы и методы
В исследование было включено 45 человек, все они являлись пациентами отделения трасплантации костного мозга для детей №1 (ОТКМ №1) НИИ ДОГиТ им. Р. М. Горбачевой. Медиана возраста составила 8,7 лет (4 мес. – 17 лет). У 80% (n=36) диагностирован острый лимфобластный лейкоз (ОЛЛ), у 13,3% (n=6) острый миелобластный лейкоз (ОМЛ), а у 6,7% (n=3) был выявлен острый бифенотипический лейкоз (ОБЛ). Терапию Блинатумомабом получило 36 пациентов, Милотаргом – 6 человек, а Инотузумаб озогамицин получили 5 пациентов.
Результаты
У 62,2% (n=28) встречалась фебрильная лихорадка. После терапии моноклональными АТ 35,5% (n=16) была проведена родственная трансплантация гемопоэтических стволовых клеток (ТГСК), 26,7% (n=12) получили гаплоидентичную ТГСК, а 37,8 (n=17) не получали ТГСК. На август 2018 года живы 64,4% (n=29) пациентов.
Выводы
Большинство пациентов получили терапию моноклональными АТ в качестве 3-й линии терапии. Лечение и уход за такими пациентами требуют особого внимания. Также, за неимением инструкции на русском языке, необходимо составить регламент приготовления раствора с моноклональным АТ.
Ключевые слова
Иммунотерапия, Милотарг, моноклональные антитела, Блинатумомаб, Инотузумаб.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20279" ["VALUE"]=> array(2) { ["TEXT"]=> string(61) "Anna A. Apostolova, Olesya V. Paina, Yulia V. Bogoslavskaya " ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(61) "Anna A. Apostolova, Olesya V. Paina, Yulia V. Bogoslavskaya " ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20280" ["VALUE"]=> array(2) { ["TEXT"]=> string(177) "R. Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation; First St. Petersburg I. Pavlov State Medical University, St. Petersburg, Russia (CIC 725)" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(177) "R. Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation; First St. Petersburg I. Pavlov State Medical University, St. Petersburg, Russia (CIC 725)" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20355" ["VALUE"]=> array(2) { ["TEXT"]=> string(2478) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Immunotherapy with monoclonal antibodies (Mabs) is a new type of leukemia treatment, being gradually introduced into the practice of Russian hematological clinics. Most drugs comprise a part of the extended access group, and do not have instructions in Russian. Aim of the present study was to consider the strategy of care for the patients who received therapy with monoclonal antibodies, and to suggest recommendations for the nurses working with monoclonal antibodies. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> The study included 45 patients. All the patients received treatment and medical care in the BMT Department No.1, at the R.Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation. Their median age was 8.7 years (4 months to 17 years old). Acute lymphoblastic leukemia (ALL) was diagnosed in 80% (n=36), acute myeloblastic leukemia (AML) was found in 13.3% (n=6), and acute biphenotypic leukemia was detected in 6.7% (n=3) (ABL). The therapy with Blinatumomab was applied to 36 patients, Mylotarg was administered in 6 cases, and 5 patients received Inotuzumab ozogamicin. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> 62.2% of the patients (n=28) exhibited febrile fever. After therapy with Mabs, a related hematopoietic stem cell transplantation (HSCT) was performed for 35.5% of patients (n=16), 26.7% of patients (n=12) received haploidentical HSCT, and 37.8% (n=17) did not underwent HSCT. Against the August 2018, 64.4% (n=29) of patients were alive. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Most patients were treated with monoclonal antibodies as the third-line therapy. Treatment and care for such patients require special attention. Also, in the absence of instructions in Russian language, it is necessary to compile an operation procedure for preparing a solution with monoclonal antibodies. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Immunotherapy, Mylotarg, monoclonal antibodies, Blinatumomab, Inotuzumab. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2258) "Introduction
Immunotherapy with monoclonal antibodies (Mabs) is a new type of leukemia treatment, being gradually introduced into the practice of Russian hematological clinics. Most drugs comprise a part of the extended access group, and do not have instructions in Russian. Aim of the present study was to consider the strategy of care for the patients who received therapy with monoclonal antibodies, and to suggest recommendations for the nurses working with monoclonal antibodies.
Materials and methods
The study included 45 patients. All the patients received treatment and medical care in the BMT Department No.1, at the R.Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation. Their median age was 8.7 years (4 months to 17 years old). Acute lymphoblastic leukemia (ALL) was diagnosed in 80% (n=36), acute myeloblastic leukemia (AML) was found in 13.3% (n=6), and acute biphenotypic leukemia was detected in 6.7% (n=3) (ABL). The therapy with Blinatumomab was applied to 36 patients, Mylotarg was administered in 6 cases, and 5 patients received Inotuzumab ozogamicin.
Results
62.2% of the patients (n=28) exhibited febrile fever. After therapy with Mabs, a related hematopoietic stem cell transplantation (HSCT) was performed for 35.5% of patients (n=16), 26.7% of patients (n=12) received haploidentical HSCT, and 37.8% (n=17) did not underwent HSCT. Against the August 2018, 64.4% (n=29) of patients were alive.
Conclusion
Most patients were treated with monoclonal antibodies as the third-line therapy. Treatment and care for such patients require special attention. Also, in the absence of instructions in Russian language, it is necessary to compile an operation procedure for preparing a solution with monoclonal antibodies.
Keywords
Immunotherapy, Mylotarg, monoclonal antibodies, Blinatumomab, Inotuzumab.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20281" ["VALUE"]=> string(73) "Nursing care for patients who received therapy with monoclonal antibodies" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(73) "Nursing care for patients who received therapy with monoclonal antibodies" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> &array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20733" ["VALUE"]=> string(4) "1369" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1369" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20734" ["VALUE"]=> string(4) "1370" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1370" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20279" ["VALUE"]=> array(2) { ["TEXT"]=> string(61) "Anna A. Apostolova, Olesya V. Paina, Yulia V. Bogoslavskaya " ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(61) "Anna A. Apostolova, Olesya V. Paina, Yulia V. Bogoslavskaya " ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(61) "Anna A. Apostolova, Olesya V. Paina, Yulia V. Bogoslavskaya " } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20355" ["VALUE"]=> array(2) { ["TEXT"]=> string(2478) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Immunotherapy with monoclonal antibodies (Mabs) is a new type of leukemia treatment, being gradually introduced into the practice of Russian hematological clinics. Most drugs comprise a part of the extended access group, and do not have instructions in Russian. Aim of the present study was to consider the strategy of care for the patients who received therapy with monoclonal antibodies, and to suggest recommendations for the nurses working with monoclonal antibodies. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> The study included 45 patients. All the patients received treatment and medical care in the BMT Department No.1, at the R.Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation. Their median age was 8.7 years (4 months to 17 years old). Acute lymphoblastic leukemia (ALL) was diagnosed in 80% (n=36), acute myeloblastic leukemia (AML) was found in 13.3% (n=6), and acute biphenotypic leukemia was detected in 6.7% (n=3) (ABL). The therapy with Blinatumomab was applied to 36 patients, Mylotarg was administered in 6 cases, and 5 patients received Inotuzumab ozogamicin. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> 62.2% of the patients (n=28) exhibited febrile fever. After therapy with Mabs, a related hematopoietic stem cell transplantation (HSCT) was performed for 35.5% of patients (n=16), 26.7% of patients (n=12) received haploidentical HSCT, and 37.8% (n=17) did not underwent HSCT. Against the August 2018, 64.4% (n=29) of patients were alive. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Most patients were treated with monoclonal antibodies as the third-line therapy. Treatment and care for such patients require special attention. Also, in the absence of instructions in Russian language, it is necessary to compile an operation procedure for preparing a solution with monoclonal antibodies. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Immunotherapy, Mylotarg, monoclonal antibodies, Blinatumomab, Inotuzumab. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2258) "Introduction
Immunotherapy with monoclonal antibodies (Mabs) is a new type of leukemia treatment, being gradually introduced into the practice of Russian hematological clinics. Most drugs comprise a part of the extended access group, and do not have instructions in Russian. Aim of the present study was to consider the strategy of care for the patients who received therapy with monoclonal antibodies, and to suggest recommendations for the nurses working with monoclonal antibodies.
Materials and methods
The study included 45 patients. All the patients received treatment and medical care in the BMT Department No.1, at the R.Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation. Their median age was 8.7 years (4 months to 17 years old). Acute lymphoblastic leukemia (ALL) was diagnosed in 80% (n=36), acute myeloblastic leukemia (AML) was found in 13.3% (n=6), and acute biphenotypic leukemia was detected in 6.7% (n=3) (ABL). The therapy with Blinatumomab was applied to 36 patients, Mylotarg was administered in 6 cases, and 5 patients received Inotuzumab ozogamicin.
Results
62.2% of the patients (n=28) exhibited febrile fever. After therapy with Mabs, a related hematopoietic stem cell transplantation (HSCT) was performed for 35.5% of patients (n=16), 26.7% of patients (n=12) received haploidentical HSCT, and 37.8% (n=17) did not underwent HSCT. Against the August 2018, 64.4% (n=29) of patients were alive.
Conclusion
Most patients were treated with monoclonal antibodies as the third-line therapy. Treatment and care for such patients require special attention. Also, in the absence of instructions in Russian language, it is necessary to compile an operation procedure for preparing a solution with monoclonal antibodies.
Keywords
Immunotherapy, Mylotarg, monoclonal antibodies, Blinatumomab, Inotuzumab.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2258) "Introduction
Immunotherapy with monoclonal antibodies (Mabs) is a new type of leukemia treatment, being gradually introduced into the practice of Russian hematological clinics. Most drugs comprise a part of the extended access group, and do not have instructions in Russian. Aim of the present study was to consider the strategy of care for the patients who received therapy with monoclonal antibodies, and to suggest recommendations for the nurses working with monoclonal antibodies.
Materials and methods
The study included 45 patients. All the patients received treatment and medical care in the BMT Department No.1, at the R.Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation. Their median age was 8.7 years (4 months to 17 years old). Acute lymphoblastic leukemia (ALL) was diagnosed in 80% (n=36), acute myeloblastic leukemia (AML) was found in 13.3% (n=6), and acute biphenotypic leukemia was detected in 6.7% (n=3) (ABL). The therapy with Blinatumomab was applied to 36 patients, Mylotarg was administered in 6 cases, and 5 patients received Inotuzumab ozogamicin.
Results
62.2% of the patients (n=28) exhibited febrile fever. After therapy with Mabs, a related hematopoietic stem cell transplantation (HSCT) was performed for 35.5% of patients (n=16), 26.7% of patients (n=12) received haploidentical HSCT, and 37.8% (n=17) did not underwent HSCT. Against the August 2018, 64.4% (n=29) of patients were alive.
Conclusion
Most patients were treated with monoclonal antibodies as the third-line therapy. Treatment and care for such patients require special attention. Also, in the absence of instructions in Russian language, it is necessary to compile an operation procedure for preparing a solution with monoclonal antibodies.
Keywords
Immunotherapy, Mylotarg, monoclonal antibodies, Blinatumomab, Inotuzumab.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20281" ["VALUE"]=> string(73) "Nursing care for patients who received therapy with monoclonal antibodies" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(73) "Nursing care for patients who received therapy with monoclonal antibodies" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(73) "Nursing care for patients who received therapy with monoclonal antibodies" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20280" ["VALUE"]=> array(2) { ["TEXT"]=> string(177) "R. Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation; First St. Petersburg I. Pavlov State Medical University, St. Petersburg, Russia (CIC 725)" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(177) "R. Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation; First St. Petersburg I. Pavlov State Medical University, St. Petersburg, Russia (CIC 725)" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(177) "R. Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation; First St. Petersburg I. Pavlov State Medical University, St. Petersburg, Russia (CIC 725)" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20277" ["VALUE"]=> array(2) { ["TEXT"]=> string(99) "Анна А. Апостолова, Олеся В. Паина, Юлия В. Богославская" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(99) "Анна А. Апостолова, Олеся В. Паина, Юлия В. Богославская" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(99) "Анна А. Апостолова, Олеся В. Паина, Юлия В. Богославская" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20354" ["VALUE"]=> array(2) { ["TEXT"]=> string(3694) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Иммунотерапия моноклональными антителами – это новый вид лечения лейкозов, постепенно вводимый в практику российских гематологических клиник. Большинство препаратов входят в группу расширенного доступа, и не имеют инструкции на русском языке. </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Рассмотреть тактику ухода за пациентами, получившими терапию моноклональными антителами. Предложить рекомендации для медицинских сестер, работающих с моноклональными АТ. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В исследование было включено 45 человек, все они являлись пациентами отделения трасплантации костного мозга для детей №1 (ОТКМ №1) НИИ ДОГиТ им. Р. М. Горбачевой. Медиана возраста составила 8,7 лет (4 мес. – 17 лет). У 80% (n=36) диагностирован острый лимфобластный лейкоз (ОЛЛ), у 13,3% (n=6) острый миелобластный лейкоз (ОМЛ), а у 6,7% (n=3) был выявлен острый бифенотипический лейкоз (ОБЛ). Терапию Блинатумомабом получило 36 пациентов, Милотаргом – 6 человек, а Инотузумаб озогамицин получили 5 пациентов. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> У 62,2% (n=28) встречалась фебрильная лихорадка. После терапии моноклональными АТ 35,5% (n=16) была проведена родственная трансплантация гемопоэтических стволовых клеток (ТГСК), 26,7% (n=12) получили гаплоидентичную ТГСК, а 37,8 (n=17) не получали ТГСК. На август 2018 года живы 64,4% (n=29) пациентов. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Большинство пациентов получили терапию моноклональными АТ в качестве 3-й линии терапии. Лечение и уход за такими пациентами требуют особого внимания. Также, за неимением инструкции на русском языке, необходимо составить регламент приготовления раствора с моноклональным АТ. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Иммунотерапия, Милотарг, моноклональные антитела, Блинатумомаб, Инотузумаб. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3430) "Введение
Иммунотерапия моноклональными антителами – это новый вид лечения лейкозов, постепенно вводимый в практику российских гематологических клиник. Большинство препаратов входят в группу расширенного доступа, и не имеют инструкции на русском языке.
Цель работы
Рассмотреть тактику ухода за пациентами, получившими терапию моноклональными антителами. Предложить рекомендации для медицинских сестер, работающих с моноклональными АТ.
Материалы и методы
В исследование было включено 45 человек, все они являлись пациентами отделения трасплантации костного мозга для детей №1 (ОТКМ №1) НИИ ДОГиТ им. Р. М. Горбачевой. Медиана возраста составила 8,7 лет (4 мес. – 17 лет). У 80% (n=36) диагностирован острый лимфобластный лейкоз (ОЛЛ), у 13,3% (n=6) острый миелобластный лейкоз (ОМЛ), а у 6,7% (n=3) был выявлен острый бифенотипический лейкоз (ОБЛ). Терапию Блинатумомабом получило 36 пациентов, Милотаргом – 6 человек, а Инотузумаб озогамицин получили 5 пациентов.
Результаты
У 62,2% (n=28) встречалась фебрильная лихорадка. После терапии моноклональными АТ 35,5% (n=16) была проведена родственная трансплантация гемопоэтических стволовых клеток (ТГСК), 26,7% (n=12) получили гаплоидентичную ТГСК, а 37,8 (n=17) не получали ТГСК. На август 2018 года живы 64,4% (n=29) пациентов.
Выводы
Большинство пациентов получили терапию моноклональными АТ в качестве 3-й линии терапии. Лечение и уход за такими пациентами требуют особого внимания. Также, за неимением инструкции на русском языке, необходимо составить регламент приготовления раствора с моноклональным АТ.
Ключевые слова
Иммунотерапия, Милотарг, моноклональные антитела, Блинатумомаб, Инотузумаб.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3430) "Введение
Иммунотерапия моноклональными антителами – это новый вид лечения лейкозов, постепенно вводимый в практику российских гематологических клиник. Большинство препаратов входят в группу расширенного доступа, и не имеют инструкции на русском языке.
Цель работы
Рассмотреть тактику ухода за пациентами, получившими терапию моноклональными антителами. Предложить рекомендации для медицинских сестер, работающих с моноклональными АТ.
Материалы и методы
В исследование было включено 45 человек, все они являлись пациентами отделения трасплантации костного мозга для детей №1 (ОТКМ №1) НИИ ДОГиТ им. Р. М. Горбачевой. Медиана возраста составила 8,7 лет (4 мес. – 17 лет). У 80% (n=36) диагностирован острый лимфобластный лейкоз (ОЛЛ), у 13,3% (n=6) острый миелобластный лейкоз (ОМЛ), а у 6,7% (n=3) был выявлен острый бифенотипический лейкоз (ОБЛ). Терапию Блинатумомабом получило 36 пациентов, Милотаргом – 6 человек, а Инотузумаб озогамицин получили 5 пациентов.
Результаты
У 62,2% (n=28) встречалась фебрильная лихорадка. После терапии моноклональными АТ 35,5% (n=16) была проведена родственная трансплантация гемопоэтических стволовых клеток (ТГСК), 26,7% (n=12) получили гаплоидентичную ТГСК, а 37,8 (n=17) не получали ТГСК. На август 2018 года живы 64,4% (n=29) пациентов.
Выводы
Большинство пациентов получили терапию моноклональными АТ в качестве 3-й линии терапии. Лечение и уход за такими пациентами требуют особого внимания. Также, за неимением инструкции на русском языке, необходимо составить регламент приготовления раствора с моноклональным АТ.
Ключевые слова
Иммунотерапия, Милотарг, моноклональные антитела, Блинатумомаб, Инотузумаб.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20278" ["VALUE"]=> array(2) { ["TEXT"]=> string(416) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой (CIC 725), Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(410) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой (CIC 725), Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(410) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой (CIC 725), Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
" } } } [19]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1555" ["~ID"]=> string(4) "1555" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(217) "Комбинация Гемтузумаб озогамицина и химиотерапии у пациентов при рецидиве и резистентным острым миелоидным лейкозом" ["~NAME"]=> string(217) "Комбинация Гемтузумаб озогамицина и химиотерапии у пациентов при рецидиве и резистентным острым миелоидным лейкозом" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:25:58" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:25:58" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/kombinatsiya-gemtuzumab-ozogamitsina-i-khimioterapii-u-patsientov-pri-retsidive-i-rezistentnym-ostry/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/kombinatsiya-gemtuzumab-ozogamitsina-i-khimioterapii-u-patsientov-pri-retsidive-i-rezistentnym-ostry/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "kombinatsiya-gemtuzumab-ozogamitsina-i-khimioterapii-u-patsientov-pri-retsidive-i-rezistentnym-ostry" ["~CODE"]=> string(100) "kombinatsiya-gemtuzumab-ozogamitsina-i-khimioterapii-u-patsientov-pri-retsidive-i-rezistentnym-ostry" ["EXTERNAL_ID"]=> string(4) "1555" ["~EXTERNAL_ID"]=> string(4) "1555" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(217) "Комбинация Гемтузумаб озогамицина и химиотерапии у пациентов при рецидиве и резистентным острым миелоидным лейкозом" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(319) "Комбинация Гемтузумаб озогамицина и химиотерапии у пациентов при рецидиве и резистентным острым миелоидным лейкозомGemtuzumab ozogamicin and chemotherapy in patients with relapses and refractory acute myeloid leukemia" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(6958) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> При развитии рецидива острого миелоидного лейкоза (ОМЛ) полную ремиссию (ПР) удается достичь в 25-50% случаев. Пятилетняя общая выживаемость составляет 11%. Прогноз для пациентов с химиорезистентным (ХР) ОМЛ остается неутешительным. Перспективы улучшить результаты терапии ОМЛ находятся в области таргетной терапии. Гемтузумаб озогамицин* (ГО) представляет собой конъюгированное моноклональное антиCD33 антитело, ковалентно связанное с цитотоксическим агентом – калихеамицином. Поскольку CD33 экспрессируется на бластах почти у всех пациентов с ОМЛ, использование ГО в сочетании с химиотерапией (ХТ) дает шанс на получение ПР и проведении аллогенной трансплантации костного мозга (алло-ТГСК). </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Оценить эффективность и токсичсность ГО в сочетании с ХТ у пациентов ХР ОМЛ. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В исследование включено 25 пациентов с ХР ОМЛ. Медиана возраста составила 36(18-68) лет. Согласно моекулярно-цитогенетической классификации (МЦК): низкий риск (НР) – 2, средний (СР) – 14, высокий (ВР) – 9 пациентов. Первично ХР (ПХР) были 13 пациентов, вторично ХР (ВХР) – 12. Изолированное поражение костного мозга было у 16 больных, комбинированное у 8 (ЦНС – 2, экстрамедуллярное поражение – 7; один пациент имел сочетанное поражение). Медиана уровня экспрессии CD33 составила 72 (9-95)%. ГО получили после алло-ТГСК 4 (16%) больных. ГО вводили в дозе 3 мг/м2 (максимально 5 мг) в сочетании с высокодозной ХТ (ВДХТ) (FLAG±Ida, HDAC, HAM) или низкодозной ХТ (НДХТ) (MEtA, LDARA-C) – 12 и 13 больных, соответственно. ГО вводился однократно (1ГО) у 13, двукратно (2ГО) – 4 и трехкратно (3ГО) – 8 пациентов, соответственно. ТГСК (нерод-3, гапло-3, ауто-1) проведена после терапии ГО 7(28%) пациентам, из них у 2 – повторная алло-ТГСК со сменой донора. Медиана сроков проведения ТГСК после терапии ГО 62 (17-138) дней. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> ПР достигнута у 3(12%), ПР без восстановления показателей периферической крови (нПР) у 6(24%) пациентов, соответственно, общий положительный ответ (ОПО) получен у 9(36%) больных. Медиана продолжительности ПР 56(6-341) дней. В зависимости от МЦК ОПО достигнут у 2 больных в НР, у 4 (29%) в СР, у 3 (33%) пациентов в ВР. ОПО был у 3 (23%) пациентов с ПХР, и у 6 (50%) с ВХР. При сочетании НДХТ+ГО ОПО получен у 3 (23%) пациентов, при ВДХТ+ГО – у 6 (50%). В зависимости от кратности введения ГО ОПО констатирован при 1ГО – у 4 (31%), 2ГО – 0, 3ГО – 5 (62%) пациентов. Однолетняя общая (1ОВ) и безрецидивная (1БРВ) выживаемость составили 26% (95%ДИ 6-46%) и 25% (95%ДИ 6-44%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии ГО 1ОБ и 1БРВ составила 21% (95%ДИ 4-38) против 8% (95%ДИ 1-15) р=.02 и 19% (95%ДИ 3-25) против 6% (95%ДИ 1-11) р=.01, соответственно. Из ответивших на терапию ГО умерло 3 пациента от прогрессии ОМЛ, 1 пациент от инфекции и 1 от геморрагического синдрома. Печеночная токсичность (трансфераземия) 1-2 степени у 3 пациентов и 3 степени – у 2; сепсис у 9 пациентов. Синусоидальный обструктивный синдром не отмечался ни у одного пациента.<br> <span style="font-family: Cuprum, sans-serif; font-size: 26px;">Заключение</span><br> Это исследование продемонстрировало значимую эффективность и приемлемый профиль токсичности при комбинации ГО и ХТ. Сочетанное применение ГО и ХТ может рассматриваться для пациентов с ХР ОМЛ, как этап подготовки к алло-ТГСК. </p> <h2 style="text-align: justify;">Комментарии</h2> <p style="text-align: justify;"> Авторы заявляют об отсутствии скрытого конфликта интересов.<br> * ГО предоставлялся в рамках программы расширенного доступа по жизненным показаниям </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый миелоидный лейкоз, таргетная терапия, гемтузумаб озогамицин. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(217) "Комбинация Гемтузумаб озогамицина и химиотерапии у пациентов при рецидиве и резистентным острым миелоидным лейкозом" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(217) "Комбинация Гемтузумаб озогамицина и химиотерапии у пациентов при рецидиве и резистентным острым миелоидным лейкозом" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(217) "Комбинация Гемтузумаб озогамицина и химиотерапии у пациентов при рецидиве и резистентным острым миелоидным лейкозом" ["SECTION_META_TITLE"]=> string(217) "Комбинация Гемтузумаб озогамицина и химиотерапии у пациентов при рецидиве и резистентным острым миелоидным лейкозом" ["SECTION_META_KEYWORDS"]=> string(217) "Комбинация Гемтузумаб озогамицина и химиотерапии у пациентов при рецидиве и резистентным острым миелоидным лейкозом" ["SECTION_META_DESCRIPTION"]=> string(217) "Комбинация Гемтузумаб озогамицина и химиотерапии у пациентов при рецидиве и резистентным острым миелоидным лейкозом" ["SECTION_PICTURE_FILE_ALT"]=> string(217) "Комбинация Гемтузумаб озогамицина и химиотерапии у пациентов при рецидиве и резистентным острым миелоидным лейкозом" ["SECTION_PICTURE_FILE_TITLE"]=> string(217) "Комбинация Гемтузумаб озогамицина и химиотерапии у пациентов при рецидиве и резистентным острым миелоидным лейкозом" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "kombinatsiya-gemtuzumab-ozogamitsina-i-khimioterapii-u-patsientov-pri-retsidive-i-rezistentnym-ostry" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(217) "Комбинация Гемтузумаб озогамицина и химиотерапии у пациентов при рецидиве и резистентным острым миелоидным лейкозом" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(217) "Комбинация Гемтузумаб озогамицина и химиотерапии у пациентов при рецидиве и резистентным острым миелоидным лейкозом" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "kombinatsiya-gemtuzumab-ozogamitsina-i-khimioterapii-u-patsientov-pri-retsidive-i-rezistentnym-ostry" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "kombinatsiya-gemtuzumab-ozogamitsina-i-khimioterapii-u-patsientov-pri-retsidive-i-rezistentnym-ostry" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "kombinatsiya-gemtuzumab-ozogamitsina-i-khimioterapii-u-patsientov-pri-retsidive-i-rezistentnym-ostry" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20317" ["VALUE"]=> array(2) { ["TEXT"]=> string(947) "Сергей Н. Бондаренко <sup>1</sup>, Ольга С. Успенская <sup>2</sup>, Елена В. Карягина <sup>3</sup>, Наталья В. Архипова <sup>4</sup>, Евгения И. Желнова <sup>4</sup>, Иван С. Моисеев <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Ирина А. Самородова <sup>1</sup>, Анна Г. Смирнова <sup>1</sup>, Татьяна А. Быкова <sup>1</sup>, Белла И. Аюбова <sup>1</sup>, Елена В. Бабенко <sup>1</sup>, Ильдар М. Бархатов <sup>1</sup>, Татьяна Л. Гиндина <sup>1</sup>, Александр Д. Кулагин <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(755) "Сергей Н. Бондаренко 1, Ольга С. Успенская 2, Елена В. Карягина 3, Наталья В. Архипова 4, Евгения И. Желнова 4, Иван С. Моисеев 1, Елена И. Дарская 1, Ирина А. Самородова 1, Анна Г. Смирнова 1, Татьяна А. Быкова 1, Белла И. Аюбова 1, Елена В. Бабенко 1, Ильдар М. Бархатов 1, Татьяна Л. Гиндина 1, Александр Д. Кулагин 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20318" ["VALUE"]=> array(2) { ["TEXT"]=> string(656) "<sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург<br> <sup>2</sup> Ленинградская областная клиническая больница, Санкт-Петербург<br> <sup>3</sup> Городская больница №15, Санкт-Петербург<br> <sup>4</sup> Городская клиническая больница №52, Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(590) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург
2 Ленинградская областная клиническая больница, Санкт-Петербург
3 Городская больница №15, Санкт-Петербург
4 Городская клиническая больница №52, Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20346" ["VALUE"]=> array(2) { ["TEXT"]=> string(6958) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> При развитии рецидива острого миелоидного лейкоза (ОМЛ) полную ремиссию (ПР) удается достичь в 25-50% случаев. Пятилетняя общая выживаемость составляет 11%. Прогноз для пациентов с химиорезистентным (ХР) ОМЛ остается неутешительным. Перспективы улучшить результаты терапии ОМЛ находятся в области таргетной терапии. Гемтузумаб озогамицин* (ГО) представляет собой конъюгированное моноклональное антиCD33 антитело, ковалентно связанное с цитотоксическим агентом – калихеамицином. Поскольку CD33 экспрессируется на бластах почти у всех пациентов с ОМЛ, использование ГО в сочетании с химиотерапией (ХТ) дает шанс на получение ПР и проведении аллогенной трансплантации костного мозга (алло-ТГСК). </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Оценить эффективность и токсичсность ГО в сочетании с ХТ у пациентов ХР ОМЛ. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В исследование включено 25 пациентов с ХР ОМЛ. Медиана возраста составила 36(18-68) лет. Согласно моекулярно-цитогенетической классификации (МЦК): низкий риск (НР) – 2, средний (СР) – 14, высокий (ВР) – 9 пациентов. Первично ХР (ПХР) были 13 пациентов, вторично ХР (ВХР) – 12. Изолированное поражение костного мозга было у 16 больных, комбинированное у 8 (ЦНС – 2, экстрамедуллярное поражение – 7; один пациент имел сочетанное поражение). Медиана уровня экспрессии CD33 составила 72 (9-95)%. ГО получили после алло-ТГСК 4 (16%) больных. ГО вводили в дозе 3 мг/м2 (максимально 5 мг) в сочетании с высокодозной ХТ (ВДХТ) (FLAG±Ida, HDAC, HAM) или низкодозной ХТ (НДХТ) (MEtA, LDARA-C) – 12 и 13 больных, соответственно. ГО вводился однократно (1ГО) у 13, двукратно (2ГО) – 4 и трехкратно (3ГО) – 8 пациентов, соответственно. ТГСК (нерод-3, гапло-3, ауто-1) проведена после терапии ГО 7(28%) пациентам, из них у 2 – повторная алло-ТГСК со сменой донора. Медиана сроков проведения ТГСК после терапии ГО 62 (17-138) дней. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> ПР достигнута у 3(12%), ПР без восстановления показателей периферической крови (нПР) у 6(24%) пациентов, соответственно, общий положительный ответ (ОПО) получен у 9(36%) больных. Медиана продолжительности ПР 56(6-341) дней. В зависимости от МЦК ОПО достигнут у 2 больных в НР, у 4 (29%) в СР, у 3 (33%) пациентов в ВР. ОПО был у 3 (23%) пациентов с ПХР, и у 6 (50%) с ВХР. При сочетании НДХТ+ГО ОПО получен у 3 (23%) пациентов, при ВДХТ+ГО – у 6 (50%). В зависимости от кратности введения ГО ОПО констатирован при 1ГО – у 4 (31%), 2ГО – 0, 3ГО – 5 (62%) пациентов. Однолетняя общая (1ОВ) и безрецидивная (1БРВ) выживаемость составили 26% (95%ДИ 6-46%) и 25% (95%ДИ 6-44%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии ГО 1ОБ и 1БРВ составила 21% (95%ДИ 4-38) против 8% (95%ДИ 1-15) р=.02 и 19% (95%ДИ 3-25) против 6% (95%ДИ 1-11) р=.01, соответственно. Из ответивших на терапию ГО умерло 3 пациента от прогрессии ОМЛ, 1 пациент от инфекции и 1 от геморрагического синдрома. Печеночная токсичность (трансфераземия) 1-2 степени у 3 пациентов и 3 степени – у 2; сепсис у 9 пациентов. Синусоидальный обструктивный синдром не отмечался ни у одного пациента.<br> <span style="font-family: Cuprum, sans-serif; font-size: 26px;">Заключение</span><br> Это исследование продемонстрировало значимую эффективность и приемлемый профиль токсичности при комбинации ГО и ХТ. Сочетанное применение ГО и ХТ может рассматриваться для пациентов с ХР ОМЛ, как этап подготовки к алло-ТГСК. </p> <h2 style="text-align: justify;">Комментарии</h2> <p style="text-align: justify;"> Авторы заявляют об отсутствии скрытого конфликта интересов.<br> * ГО предоставлялся в рамках программы расширенного доступа по жизненным показаниям </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый миелоидный лейкоз, таргетная терапия, гемтузумаб озогамицин. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6654) "
Введение
При развитии рецидива острого миелоидного лейкоза (ОМЛ) полную ремиссию (ПР) удается достичь в 25-50% случаев. Пятилетняя общая выживаемость составляет 11%. Прогноз для пациентов с химиорезистентным (ХР) ОМЛ остается неутешительным. Перспективы улучшить результаты терапии ОМЛ находятся в области таргетной терапии. Гемтузумаб озогамицин* (ГО) представляет собой конъюгированное моноклональное антиCD33 антитело, ковалентно связанное с цитотоксическим агентом – калихеамицином. Поскольку CD33 экспрессируется на бластах почти у всех пациентов с ОМЛ, использование ГО в сочетании с химиотерапией (ХТ) дает шанс на получение ПР и проведении аллогенной трансплантации костного мозга (алло-ТГСК).
Цель работы
Оценить эффективность и токсичсность ГО в сочетании с ХТ у пациентов ХР ОМЛ.
Пациенты и методы
В исследование включено 25 пациентов с ХР ОМЛ. Медиана возраста составила 36(18-68) лет. Согласно моекулярно-цитогенетической классификации (МЦК): низкий риск (НР) – 2, средний (СР) – 14, высокий (ВР) – 9 пациентов. Первично ХР (ПХР) были 13 пациентов, вторично ХР (ВХР) – 12. Изолированное поражение костного мозга было у 16 больных, комбинированное у 8 (ЦНС – 2, экстрамедуллярное поражение – 7; один пациент имел сочетанное поражение). Медиана уровня экспрессии CD33 составила 72 (9-95)%. ГО получили после алло-ТГСК 4 (16%) больных. ГО вводили в дозе 3 мг/м2 (максимально 5 мг) в сочетании с высокодозной ХТ (ВДХТ) (FLAG±Ida, HDAC, HAM) или низкодозной ХТ (НДХТ) (MEtA, LDARA-C) – 12 и 13 больных, соответственно. ГО вводился однократно (1ГО) у 13, двукратно (2ГО) – 4 и трехкратно (3ГО) – 8 пациентов, соответственно. ТГСК (нерод-3, гапло-3, ауто-1) проведена после терапии ГО 7(28%) пациентам, из них у 2 – повторная алло-ТГСК со сменой донора. Медиана сроков проведения ТГСК после терапии ГО 62 (17-138) дней.
Результаты
ПР достигнута у 3(12%), ПР без восстановления показателей периферической крови (нПР) у 6(24%) пациентов, соответственно, общий положительный ответ (ОПО) получен у 9(36%) больных. Медиана продолжительности ПР 56(6-341) дней. В зависимости от МЦК ОПО достигнут у 2 больных в НР, у 4 (29%) в СР, у 3 (33%) пациентов в ВР. ОПО был у 3 (23%) пациентов с ПХР, и у 6 (50%) с ВХР. При сочетании НДХТ+ГО ОПО получен у 3 (23%) пациентов, при ВДХТ+ГО – у 6 (50%). В зависимости от кратности введения ГО ОПО констатирован при 1ГО – у 4 (31%), 2ГО – 0, 3ГО – 5 (62%) пациентов. Однолетняя общая (1ОВ) и безрецидивная (1БРВ) выживаемость составили 26% (95%ДИ 6-46%) и 25% (95%ДИ 6-44%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии ГО 1ОБ и 1БРВ составила 21% (95%ДИ 4-38) против 8% (95%ДИ 1-15) р=.02 и 19% (95%ДИ 3-25) против 6% (95%ДИ 1-11) р=.01, соответственно. Из ответивших на терапию ГО умерло 3 пациента от прогрессии ОМЛ, 1 пациент от инфекции и 1 от геморрагического синдрома. Печеночная токсичность (трансфераземия) 1-2 степени у 3 пациентов и 3 степени – у 2; сепсис у 9 пациентов. Синусоидальный обструктивный синдром не отмечался ни у одного пациента.
Заключение
Это исследование продемонстрировало значимую эффективность и приемлемый профиль токсичности при комбинации ГО и ХТ. Сочетанное применение ГО и ХТ может рассматриваться для пациентов с ХР ОМЛ, как этап подготовки к алло-ТГСК.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
* ГО предоставлялся в рамках программы расширенного доступа по жизненным показаниям
Ключевые слова
Острый миелоидный лейкоз, таргетная терапия, гемтузумаб озогамицин.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20319" ["VALUE"]=> array(2) { ["TEXT"]=> string(715) "Sergey N. Bondarenko <sup>1</sup>, Olga S. Uspenskaya <sup>2</sup>, Elena V. Karyagina <sup>3</sup>, Natalya V. Arkhipova <sup>4</sup>, Evgenia I. Zhelnova <sup>4</sup>, Ivan S. Moiseev <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Irina A. Samorodova <sup>1</sup>, Anna G. Smirnova <sup>1</sup>, Tatyana A. Bykova <sup>1</sup>, Bella I. Ayubova <sup>1</sup>, Elena V. Babenko <sup>1</sup>, Ildar M. Barkhatov <sup>1</sup>, Tatyana L. Gindina <sup>1</sup>, Alexander D. Kulagin <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(523) "Sergey N. Bondarenko 1, Olga S. Uspenskaya 2, Elena V. Karyagina 3, Natalya V. Arkhipova 4, Evgenia I. Zhelnova 4, Ivan S. Moiseev 1, Elena I. Darskaya 1, Irina A. Samorodova 1, Anna G. Smirnova 1, Tatyana A. Bykova 1, Bella I. Ayubova 1, Elena V. Babenko 1, Ildar M. Barkhatov 1, Tatyana L. Gindina 1, Alexander D. Kulagin 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20320" ["VALUE"]=> array(2) { ["TEXT"]=> string(488) "<sup>1</sup> R. Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, The First State I. Pavlov Medical University, St. Petersburg, Russian Federation<br> <sup>2</sup> Leningrad Regional Clinical Hospital, St. Petersburg, Russian Federation<br> <sup>3</sup> City Hospital No.15, St. Petersburg, Russian Federation<br> <sup>4</sup> City Clinical Hospital №52, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(422) "1 R. Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, The First State I. Pavlov Medical University, St. Petersburg, Russian Federation2 Leningrad Regional Clinical Hospital, St. Petersburg, Russian Federation
3 City Hospital No.15, St. Petersburg, Russian Federation
4 City Clinical Hospital №52, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20347" ["VALUE"]=> array(2) { ["TEXT"]=> string(4613) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> In case of relapse and refractory course of acute myeloid leukemia (RAML), complete remission (CR) can be achieved in 25-50% pts. The five-year overall survival (OS) was 11%. The prognosis for patients with RAML remains disappointing. Prospects to improve the results of AML therapy are connected with implementation of target therapy. Gemtuzumab ozogamicin* (GO) is a conjugated monoclonal anti- CD33 antibody covalently bound to a cytotoxic agent-calicheamicin. Since CD33 is expressed on blast cells in almost all pts with AML, the use of GO in combination with chemotherapy (ChT) gives a chance to receive CR and perform allogeneic hematopoietic stem cell transplantation (allo-HSCT). </p> <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> Aim of the study was to assess efficacy and toxicity of GO in combination with ChT in patients with RAML. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> The study included 25 pts with RAML. The median age was 36 (18-68) years. According to the molecular cytogenetic classification (MCC): low risk (LR), in 2 cases; intermediate (IR), in 14; high risk (HR), in 9 pts. Primary resistance (PR) was documented in 13 pts, whereas 12 showed secondary resistance (SR). Isolated bone marrow involvement was registered in 16 pts, combined affection was found in 8 pts (CNS, 2 cases; other extramedullary lesions, in 7 patients, and one patient had multiple lesions). The median CD33 expression level was 72% (9-95%). Four patients (16%) received GO after allo-HSCT. GO was administered at a dose of 3 mg/m2 (max. 5 mg) in combination with high-dose ChT (HDCT) (FLAG ± Ida, HDAC, HAM) or low-dose CT (LDCT) (MEtA, LDARA-C) in 12 and 13 pts, respectively. GO was administered once (1 GO) in 13 cases; twice (2GO), in 4 patients, and it was applied 3 times (3GO) in 8 pts. HSCT (unrelated,3; haplo,3; auto, in 1case) was performed after therapy with GO in 7 pts (28%), two of them had a second allo-HSCT from another donor. Median time of HSCT after GO was 62(17-138) days. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Complete remission (CR) was achieved in 3 (12%), CR without peripheral blood recovery (NCR) in 6 (24%) pts, the overall positive response (OR) was obtained in 9 (36%) pts. The median CR duration was 56 (6-341) days. Depending on the MCC risk score, OR was achieved in 2 pts in LR, in 4 (29%) in IR, and in 3 (33%) pts in HR. OR was in 3 (23%) patients with PR, and in 6(50%) with SR. When combining LDCT and GO, the overall response (OR) was obtained in 3 (23%) patients, with HDCT + GO, it was achieved in 6 cases (50%). Depending on the number of the GO rounds, overall positive response (OR) was detected in 4 patients (31%) after 1GO; in none case, after 2GO; in 5 (62%) pts, after 3GO. The one-year overall survival (1OS) and disease-free survival (1DFS) were 26% (95% CI 6-46%), and 25% (95% CI 6-44%), respectively. Depending on allo-HSCT after GO therapy, the 1OS and 1DFS rates were 21% (95% CI 4-38) versus 8% (95% CI 1-15, p=.02), and 19% (95% CI 3-25) versus 6%(95% CI 1-11, p=.01), respectively. Among the responders to GO therapy, 3 pts died from AML progression, one patient was lost due to infection, and one died from hemorrhagic syndrome. Hepatic toxicity (ALT increase) of grade 1-2 was observed in 3 pts, and grade 3 was registered in 2 pts; sepsis was diagnosed in 9 pts. Sinusoidal obstruction syndrome was not observed in this group. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> This study demonstrated significant efficacy and acceptable toxicity profile for combination of GO and ChT. GO with ChT can be considered for patients with RAML, as a bridge to allo-HSCT. </p> <h2 style="text-align: justify;">Disclosure</h2> <p style="text-align: justify;"> The authors report no conflicts of interest in this work.<br> * GO was provided under program of extended access for vital indications. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Acute myeloid leukemia, target therapy, gemtuzumab ozogamicin. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4299) "
Introduction
In case of relapse and refractory course of acute myeloid leukemia (RAML), complete remission (CR) can be achieved in 25-50% pts. The five-year overall survival (OS) was 11%. The prognosis for patients with RAML remains disappointing. Prospects to improve the results of AML therapy are connected with implementation of target therapy. Gemtuzumab ozogamicin* (GO) is a conjugated monoclonal anti- CD33 antibody covalently bound to a cytotoxic agent-calicheamicin. Since CD33 is expressed on blast cells in almost all pts with AML, the use of GO in combination with chemotherapy (ChT) gives a chance to receive CR and perform allogeneic hematopoietic stem cell transplantation (allo-HSCT).
Aim
Aim of the study was to assess efficacy and toxicity of GO in combination with ChT in patients with RAML.
Patients and methods
The study included 25 pts with RAML. The median age was 36 (18-68) years. According to the molecular cytogenetic classification (MCC): low risk (LR), in 2 cases; intermediate (IR), in 14; high risk (HR), in 9 pts. Primary resistance (PR) was documented in 13 pts, whereas 12 showed secondary resistance (SR). Isolated bone marrow involvement was registered in 16 pts, combined affection was found in 8 pts (CNS, 2 cases; other extramedullary lesions, in 7 patients, and one patient had multiple lesions). The median CD33 expression level was 72% (9-95%). Four patients (16%) received GO after allo-HSCT. GO was administered at a dose of 3 mg/m2 (max. 5 mg) in combination with high-dose ChT (HDCT) (FLAG ± Ida, HDAC, HAM) or low-dose CT (LDCT) (MEtA, LDARA-C) in 12 and 13 pts, respectively. GO was administered once (1 GO) in 13 cases; twice (2GO), in 4 patients, and it was applied 3 times (3GO) in 8 pts. HSCT (unrelated,3; haplo,3; auto, in 1case) was performed after therapy with GO in 7 pts (28%), two of them had a second allo-HSCT from another donor. Median time of HSCT after GO was 62(17-138) days.
Results
Complete remission (CR) was achieved in 3 (12%), CR without peripheral blood recovery (NCR) in 6 (24%) pts, the overall positive response (OR) was obtained in 9 (36%) pts. The median CR duration was 56 (6-341) days. Depending on the MCC risk score, OR was achieved in 2 pts in LR, in 4 (29%) in IR, and in 3 (33%) pts in HR. OR was in 3 (23%) patients with PR, and in 6(50%) with SR. When combining LDCT and GO, the overall response (OR) was obtained in 3 (23%) patients, with HDCT + GO, it was achieved in 6 cases (50%). Depending on the number of the GO rounds, overall positive response (OR) was detected in 4 patients (31%) after 1GO; in none case, after 2GO; in 5 (62%) pts, after 3GO. The one-year overall survival (1OS) and disease-free survival (1DFS) were 26% (95% CI 6-46%), and 25% (95% CI 6-44%), respectively. Depending on allo-HSCT after GO therapy, the 1OS and 1DFS rates were 21% (95% CI 4-38) versus 8% (95% CI 1-15, p=.02), and 19% (95% CI 3-25) versus 6%(95% CI 1-11, p=.01), respectively. Among the responders to GO therapy, 3 pts died from AML progression, one patient was lost due to infection, and one died from hemorrhagic syndrome. Hepatic toxicity (ALT increase) of grade 1-2 was observed in 3 pts, and grade 3 was registered in 2 pts; sepsis was diagnosed in 9 pts. Sinusoidal obstruction syndrome was not observed in this group.
Conclusion
This study demonstrated significant efficacy and acceptable toxicity profile for combination of GO and ChT. GO with ChT can be considered for patients with RAML, as a bridge to allo-HSCT.
Disclosure
The authors report no conflicts of interest in this work.
* GO was provided under program of extended access for vital indications.
Keywords
Acute myeloid leukemia, target therapy, gemtuzumab ozogamicin.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20321" ["VALUE"]=> string(102) "Gemtuzumab ozogamicin and chemotherapy in patients with relapses and refractory acute myeloid leukemia" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(102) "Gemtuzumab ozogamicin and chemotherapy in patients with relapses and refractory acute myeloid leukemia" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20743" ["VALUE"]=> string(4) "1379" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1379" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20744" ["VALUE"]=> string(4) "1380" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1380" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20319" ["VALUE"]=> array(2) { ["TEXT"]=> string(715) "Sergey N. Bondarenko <sup>1</sup>, Olga S. Uspenskaya <sup>2</sup>, Elena V. Karyagina <sup>3</sup>, Natalya V. Arkhipova <sup>4</sup>, Evgenia I. Zhelnova <sup>4</sup>, Ivan S. Moiseev <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Irina A. Samorodova <sup>1</sup>, Anna G. Smirnova <sup>1</sup>, Tatyana A. Bykova <sup>1</sup>, Bella I. Ayubova <sup>1</sup>, Elena V. Babenko <sup>1</sup>, Ildar M. Barkhatov <sup>1</sup>, Tatyana L. Gindina <sup>1</sup>, Alexander D. Kulagin <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(523) "Sergey N. Bondarenko 1, Olga S. Uspenskaya 2, Elena V. Karyagina 3, Natalya V. Arkhipova 4, Evgenia I. Zhelnova 4, Ivan S. Moiseev 1, Elena I. Darskaya 1, Irina A. Samorodova 1, Anna G. Smirnova 1, Tatyana A. Bykova 1, Bella I. Ayubova 1, Elena V. Babenko 1, Ildar M. Barkhatov 1, Tatyana L. Gindina 1, Alexander D. Kulagin 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(523) "Sergey N. Bondarenko 1, Olga S. Uspenskaya 2, Elena V. Karyagina 3, Natalya V. Arkhipova 4, Evgenia I. Zhelnova 4, Ivan S. Moiseev 1, Elena I. Darskaya 1, Irina A. Samorodova 1, Anna G. Smirnova 1, Tatyana A. Bykova 1, Bella I. Ayubova 1, Elena V. Babenko 1, Ildar M. Barkhatov 1, Tatyana L. Gindina 1, Alexander D. Kulagin 1, Boris V. Afanasyev 1" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20347" ["VALUE"]=> array(2) { ["TEXT"]=> string(4613) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> In case of relapse and refractory course of acute myeloid leukemia (RAML), complete remission (CR) can be achieved in 25-50% pts. The five-year overall survival (OS) was 11%. The prognosis for patients with RAML remains disappointing. Prospects to improve the results of AML therapy are connected with implementation of target therapy. Gemtuzumab ozogamicin* (GO) is a conjugated monoclonal anti- CD33 antibody covalently bound to a cytotoxic agent-calicheamicin. Since CD33 is expressed on blast cells in almost all pts with AML, the use of GO in combination with chemotherapy (ChT) gives a chance to receive CR and perform allogeneic hematopoietic stem cell transplantation (allo-HSCT). </p> <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> Aim of the study was to assess efficacy and toxicity of GO in combination with ChT in patients with RAML. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> The study included 25 pts with RAML. The median age was 36 (18-68) years. According to the molecular cytogenetic classification (MCC): low risk (LR), in 2 cases; intermediate (IR), in 14; high risk (HR), in 9 pts. Primary resistance (PR) was documented in 13 pts, whereas 12 showed secondary resistance (SR). Isolated bone marrow involvement was registered in 16 pts, combined affection was found in 8 pts (CNS, 2 cases; other extramedullary lesions, in 7 patients, and one patient had multiple lesions). The median CD33 expression level was 72% (9-95%). Four patients (16%) received GO after allo-HSCT. GO was administered at a dose of 3 mg/m2 (max. 5 mg) in combination with high-dose ChT (HDCT) (FLAG ± Ida, HDAC, HAM) or low-dose CT (LDCT) (MEtA, LDARA-C) in 12 and 13 pts, respectively. GO was administered once (1 GO) in 13 cases; twice (2GO), in 4 patients, and it was applied 3 times (3GO) in 8 pts. HSCT (unrelated,3; haplo,3; auto, in 1case) was performed after therapy with GO in 7 pts (28%), two of them had a second allo-HSCT from another donor. Median time of HSCT after GO was 62(17-138) days. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Complete remission (CR) was achieved in 3 (12%), CR without peripheral blood recovery (NCR) in 6 (24%) pts, the overall positive response (OR) was obtained in 9 (36%) pts. The median CR duration was 56 (6-341) days. Depending on the MCC risk score, OR was achieved in 2 pts in LR, in 4 (29%) in IR, and in 3 (33%) pts in HR. OR was in 3 (23%) patients with PR, and in 6(50%) with SR. When combining LDCT and GO, the overall response (OR) was obtained in 3 (23%) patients, with HDCT + GO, it was achieved in 6 cases (50%). Depending on the number of the GO rounds, overall positive response (OR) was detected in 4 patients (31%) after 1GO; in none case, after 2GO; in 5 (62%) pts, after 3GO. The one-year overall survival (1OS) and disease-free survival (1DFS) were 26% (95% CI 6-46%), and 25% (95% CI 6-44%), respectively. Depending on allo-HSCT after GO therapy, the 1OS and 1DFS rates were 21% (95% CI 4-38) versus 8% (95% CI 1-15, p=.02), and 19% (95% CI 3-25) versus 6%(95% CI 1-11, p=.01), respectively. Among the responders to GO therapy, 3 pts died from AML progression, one patient was lost due to infection, and one died from hemorrhagic syndrome. Hepatic toxicity (ALT increase) of grade 1-2 was observed in 3 pts, and grade 3 was registered in 2 pts; sepsis was diagnosed in 9 pts. Sinusoidal obstruction syndrome was not observed in this group. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> This study demonstrated significant efficacy and acceptable toxicity profile for combination of GO and ChT. GO with ChT can be considered for patients with RAML, as a bridge to allo-HSCT. </p> <h2 style="text-align: justify;">Disclosure</h2> <p style="text-align: justify;"> The authors report no conflicts of interest in this work.<br> * GO was provided under program of extended access for vital indications. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Acute myeloid leukemia, target therapy, gemtuzumab ozogamicin. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4299) "Introduction
In case of relapse and refractory course of acute myeloid leukemia (RAML), complete remission (CR) can be achieved in 25-50% pts. The five-year overall survival (OS) was 11%. The prognosis for patients with RAML remains disappointing. Prospects to improve the results of AML therapy are connected with implementation of target therapy. Gemtuzumab ozogamicin* (GO) is a conjugated monoclonal anti- CD33 antibody covalently bound to a cytotoxic agent-calicheamicin. Since CD33 is expressed on blast cells in almost all pts with AML, the use of GO in combination with chemotherapy (ChT) gives a chance to receive CR and perform allogeneic hematopoietic stem cell transplantation (allo-HSCT).
Aim
Aim of the study was to assess efficacy and toxicity of GO in combination with ChT in patients with RAML.
Patients and methods
The study included 25 pts with RAML. The median age was 36 (18-68) years. According to the molecular cytogenetic classification (MCC): low risk (LR), in 2 cases; intermediate (IR), in 14; high risk (HR), in 9 pts. Primary resistance (PR) was documented in 13 pts, whereas 12 showed secondary resistance (SR). Isolated bone marrow involvement was registered in 16 pts, combined affection was found in 8 pts (CNS, 2 cases; other extramedullary lesions, in 7 patients, and one patient had multiple lesions). The median CD33 expression level was 72% (9-95%). Four patients (16%) received GO after allo-HSCT. GO was administered at a dose of 3 mg/m2 (max. 5 mg) in combination with high-dose ChT (HDCT) (FLAG ± Ida, HDAC, HAM) or low-dose CT (LDCT) (MEtA, LDARA-C) in 12 and 13 pts, respectively. GO was administered once (1 GO) in 13 cases; twice (2GO), in 4 patients, and it was applied 3 times (3GO) in 8 pts. HSCT (unrelated,3; haplo,3; auto, in 1case) was performed after therapy with GO in 7 pts (28%), two of them had a second allo-HSCT from another donor. Median time of HSCT after GO was 62(17-138) days.
Results
Complete remission (CR) was achieved in 3 (12%), CR without peripheral blood recovery (NCR) in 6 (24%) pts, the overall positive response (OR) was obtained in 9 (36%) pts. The median CR duration was 56 (6-341) days. Depending on the MCC risk score, OR was achieved in 2 pts in LR, in 4 (29%) in IR, and in 3 (33%) pts in HR. OR was in 3 (23%) patients with PR, and in 6(50%) with SR. When combining LDCT and GO, the overall response (OR) was obtained in 3 (23%) patients, with HDCT + GO, it was achieved in 6 cases (50%). Depending on the number of the GO rounds, overall positive response (OR) was detected in 4 patients (31%) after 1GO; in none case, after 2GO; in 5 (62%) pts, after 3GO. The one-year overall survival (1OS) and disease-free survival (1DFS) were 26% (95% CI 6-46%), and 25% (95% CI 6-44%), respectively. Depending on allo-HSCT after GO therapy, the 1OS and 1DFS rates were 21% (95% CI 4-38) versus 8% (95% CI 1-15, p=.02), and 19% (95% CI 3-25) versus 6%(95% CI 1-11, p=.01), respectively. Among the responders to GO therapy, 3 pts died from AML progression, one patient was lost due to infection, and one died from hemorrhagic syndrome. Hepatic toxicity (ALT increase) of grade 1-2 was observed in 3 pts, and grade 3 was registered in 2 pts; sepsis was diagnosed in 9 pts. Sinusoidal obstruction syndrome was not observed in this group.
Conclusion
This study demonstrated significant efficacy and acceptable toxicity profile for combination of GO and ChT. GO with ChT can be considered for patients with RAML, as a bridge to allo-HSCT.
Disclosure
The authors report no conflicts of interest in this work.
* GO was provided under program of extended access for vital indications.
Keywords
Acute myeloid leukemia, target therapy, gemtuzumab ozogamicin.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4299) "Introduction
In case of relapse and refractory course of acute myeloid leukemia (RAML), complete remission (CR) can be achieved in 25-50% pts. The five-year overall survival (OS) was 11%. The prognosis for patients with RAML remains disappointing. Prospects to improve the results of AML therapy are connected with implementation of target therapy. Gemtuzumab ozogamicin* (GO) is a conjugated monoclonal anti- CD33 antibody covalently bound to a cytotoxic agent-calicheamicin. Since CD33 is expressed on blast cells in almost all pts with AML, the use of GO in combination with chemotherapy (ChT) gives a chance to receive CR and perform allogeneic hematopoietic stem cell transplantation (allo-HSCT).
Aim
Aim of the study was to assess efficacy and toxicity of GO in combination with ChT in patients with RAML.
Patients and methods
The study included 25 pts with RAML. The median age was 36 (18-68) years. According to the molecular cytogenetic classification (MCC): low risk (LR), in 2 cases; intermediate (IR), in 14; high risk (HR), in 9 pts. Primary resistance (PR) was documented in 13 pts, whereas 12 showed secondary resistance (SR). Isolated bone marrow involvement was registered in 16 pts, combined affection was found in 8 pts (CNS, 2 cases; other extramedullary lesions, in 7 patients, and one patient had multiple lesions). The median CD33 expression level was 72% (9-95%). Four patients (16%) received GO after allo-HSCT. GO was administered at a dose of 3 mg/m2 (max. 5 mg) in combination with high-dose ChT (HDCT) (FLAG ± Ida, HDAC, HAM) or low-dose CT (LDCT) (MEtA, LDARA-C) in 12 and 13 pts, respectively. GO was administered once (1 GO) in 13 cases; twice (2GO), in 4 patients, and it was applied 3 times (3GO) in 8 pts. HSCT (unrelated,3; haplo,3; auto, in 1case) was performed after therapy with GO in 7 pts (28%), two of them had a second allo-HSCT from another donor. Median time of HSCT after GO was 62(17-138) days.
Results
Complete remission (CR) was achieved in 3 (12%), CR without peripheral blood recovery (NCR) in 6 (24%) pts, the overall positive response (OR) was obtained in 9 (36%) pts. The median CR duration was 56 (6-341) days. Depending on the MCC risk score, OR was achieved in 2 pts in LR, in 4 (29%) in IR, and in 3 (33%) pts in HR. OR was in 3 (23%) patients with PR, and in 6(50%) with SR. When combining LDCT and GO, the overall response (OR) was obtained in 3 (23%) patients, with HDCT + GO, it was achieved in 6 cases (50%). Depending on the number of the GO rounds, overall positive response (OR) was detected in 4 patients (31%) after 1GO; in none case, after 2GO; in 5 (62%) pts, after 3GO. The one-year overall survival (1OS) and disease-free survival (1DFS) were 26% (95% CI 6-46%), and 25% (95% CI 6-44%), respectively. Depending on allo-HSCT after GO therapy, the 1OS and 1DFS rates were 21% (95% CI 4-38) versus 8% (95% CI 1-15, p=.02), and 19% (95% CI 3-25) versus 6%(95% CI 1-11, p=.01), respectively. Among the responders to GO therapy, 3 pts died from AML progression, one patient was lost due to infection, and one died from hemorrhagic syndrome. Hepatic toxicity (ALT increase) of grade 1-2 was observed in 3 pts, and grade 3 was registered in 2 pts; sepsis was diagnosed in 9 pts. Sinusoidal obstruction syndrome was not observed in this group.
Conclusion
This study demonstrated significant efficacy and acceptable toxicity profile for combination of GO and ChT. GO with ChT can be considered for patients with RAML, as a bridge to allo-HSCT.
Disclosure
The authors report no conflicts of interest in this work.
* GO was provided under program of extended access for vital indications.
Keywords
Acute myeloid leukemia, target therapy, gemtuzumab ozogamicin.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20321" ["VALUE"]=> string(102) "Gemtuzumab ozogamicin and chemotherapy in patients with relapses and refractory acute myeloid leukemia" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(102) "Gemtuzumab ozogamicin and chemotherapy in patients with relapses and refractory acute myeloid leukemia" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(102) "Gemtuzumab ozogamicin and chemotherapy in patients with relapses and refractory acute myeloid leukemia" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20320" ["VALUE"]=> array(2) { ["TEXT"]=> string(488) "<sup>1</sup> R. Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, The First State I. Pavlov Medical University, St. Petersburg, Russian Federation<br> <sup>2</sup> Leningrad Regional Clinical Hospital, St. Petersburg, Russian Federation<br> <sup>3</sup> City Hospital No.15, St. Petersburg, Russian Federation<br> <sup>4</sup> City Clinical Hospital №52, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(422) "1 R. Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, The First State I. Pavlov Medical University, St. Petersburg, Russian Federation2 Leningrad Regional Clinical Hospital, St. Petersburg, Russian Federation
3 City Hospital No.15, St. Petersburg, Russian Federation
4 City Clinical Hospital №52, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(422) "1 R. Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, The First State I. Pavlov Medical University, St. Petersburg, Russian Federation
2 Leningrad Regional Clinical Hospital, St. Petersburg, Russian Federation
3 City Hospital No.15, St. Petersburg, Russian Federation
4 City Clinical Hospital №52, Moscow, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20317" ["VALUE"]=> array(2) { ["TEXT"]=> string(947) "Сергей Н. Бондаренко <sup>1</sup>, Ольга С. Успенская <sup>2</sup>, Елена В. Карягина <sup>3</sup>, Наталья В. Архипова <sup>4</sup>, Евгения И. Желнова <sup>4</sup>, Иван С. Моисеев <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Ирина А. Самородова <sup>1</sup>, Анна Г. Смирнова <sup>1</sup>, Татьяна А. Быкова <sup>1</sup>, Белла И. Аюбова <sup>1</sup>, Елена В. Бабенко <sup>1</sup>, Ильдар М. Бархатов <sup>1</sup>, Татьяна Л. Гиндина <sup>1</sup>, Александр Д. Кулагин <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(755) "Сергей Н. Бондаренко 1, Ольга С. Успенская 2, Елена В. Карягина 3, Наталья В. Архипова 4, Евгения И. Желнова 4, Иван С. Моисеев 1, Елена И. Дарская 1, Ирина А. Самородова 1, Анна Г. Смирнова 1, Татьяна А. Быкова 1, Белла И. Аюбова 1, Елена В. Бабенко 1, Ильдар М. Бархатов 1, Татьяна Л. Гиндина 1, Александр Д. Кулагин 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(755) "Сергей Н. Бондаренко 1, Ольга С. Успенская 2, Елена В. Карягина 3, Наталья В. Архипова 4, Евгения И. Желнова 4, Иван С. Моисеев 1, Елена И. Дарская 1, Ирина А. Самородова 1, Анна Г. Смирнова 1, Татьяна А. Быкова 1, Белла И. Аюбова 1, Елена В. Бабенко 1, Ильдар М. Бархатов 1, Татьяна Л. Гиндина 1, Александр Д. Кулагин 1, Борис В. Афанасьев 1" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20346" ["VALUE"]=> array(2) { ["TEXT"]=> string(6958) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> При развитии рецидива острого миелоидного лейкоза (ОМЛ) полную ремиссию (ПР) удается достичь в 25-50% случаев. Пятилетняя общая выживаемость составляет 11%. Прогноз для пациентов с химиорезистентным (ХР) ОМЛ остается неутешительным. Перспективы улучшить результаты терапии ОМЛ находятся в области таргетной терапии. Гемтузумаб озогамицин* (ГО) представляет собой конъюгированное моноклональное антиCD33 антитело, ковалентно связанное с цитотоксическим агентом – калихеамицином. Поскольку CD33 экспрессируется на бластах почти у всех пациентов с ОМЛ, использование ГО в сочетании с химиотерапией (ХТ) дает шанс на получение ПР и проведении аллогенной трансплантации костного мозга (алло-ТГСК). </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Оценить эффективность и токсичсность ГО в сочетании с ХТ у пациентов ХР ОМЛ. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В исследование включено 25 пациентов с ХР ОМЛ. Медиана возраста составила 36(18-68) лет. Согласно моекулярно-цитогенетической классификации (МЦК): низкий риск (НР) – 2, средний (СР) – 14, высокий (ВР) – 9 пациентов. Первично ХР (ПХР) были 13 пациентов, вторично ХР (ВХР) – 12. Изолированное поражение костного мозга было у 16 больных, комбинированное у 8 (ЦНС – 2, экстрамедуллярное поражение – 7; один пациент имел сочетанное поражение). Медиана уровня экспрессии CD33 составила 72 (9-95)%. ГО получили после алло-ТГСК 4 (16%) больных. ГО вводили в дозе 3 мг/м2 (максимально 5 мг) в сочетании с высокодозной ХТ (ВДХТ) (FLAG±Ida, HDAC, HAM) или низкодозной ХТ (НДХТ) (MEtA, LDARA-C) – 12 и 13 больных, соответственно. ГО вводился однократно (1ГО) у 13, двукратно (2ГО) – 4 и трехкратно (3ГО) – 8 пациентов, соответственно. ТГСК (нерод-3, гапло-3, ауто-1) проведена после терапии ГО 7(28%) пациентам, из них у 2 – повторная алло-ТГСК со сменой донора. Медиана сроков проведения ТГСК после терапии ГО 62 (17-138) дней. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> ПР достигнута у 3(12%), ПР без восстановления показателей периферической крови (нПР) у 6(24%) пациентов, соответственно, общий положительный ответ (ОПО) получен у 9(36%) больных. Медиана продолжительности ПР 56(6-341) дней. В зависимости от МЦК ОПО достигнут у 2 больных в НР, у 4 (29%) в СР, у 3 (33%) пациентов в ВР. ОПО был у 3 (23%) пациентов с ПХР, и у 6 (50%) с ВХР. При сочетании НДХТ+ГО ОПО получен у 3 (23%) пациентов, при ВДХТ+ГО – у 6 (50%). В зависимости от кратности введения ГО ОПО констатирован при 1ГО – у 4 (31%), 2ГО – 0, 3ГО – 5 (62%) пациентов. Однолетняя общая (1ОВ) и безрецидивная (1БРВ) выживаемость составили 26% (95%ДИ 6-46%) и 25% (95%ДИ 6-44%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии ГО 1ОБ и 1БРВ составила 21% (95%ДИ 4-38) против 8% (95%ДИ 1-15) р=.02 и 19% (95%ДИ 3-25) против 6% (95%ДИ 1-11) р=.01, соответственно. Из ответивших на терапию ГО умерло 3 пациента от прогрессии ОМЛ, 1 пациент от инфекции и 1 от геморрагического синдрома. Печеночная токсичность (трансфераземия) 1-2 степени у 3 пациентов и 3 степени – у 2; сепсис у 9 пациентов. Синусоидальный обструктивный синдром не отмечался ни у одного пациента.<br> <span style="font-family: Cuprum, sans-serif; font-size: 26px;">Заключение</span><br> Это исследование продемонстрировало значимую эффективность и приемлемый профиль токсичности при комбинации ГО и ХТ. Сочетанное применение ГО и ХТ может рассматриваться для пациентов с ХР ОМЛ, как этап подготовки к алло-ТГСК. </p> <h2 style="text-align: justify;">Комментарии</h2> <p style="text-align: justify;"> Авторы заявляют об отсутствии скрытого конфликта интересов.<br> * ГО предоставлялся в рамках программы расширенного доступа по жизненным показаниям </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый миелоидный лейкоз, таргетная терапия, гемтузумаб озогамицин. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6654) "
Введение
При развитии рецидива острого миелоидного лейкоза (ОМЛ) полную ремиссию (ПР) удается достичь в 25-50% случаев. Пятилетняя общая выживаемость составляет 11%. Прогноз для пациентов с химиорезистентным (ХР) ОМЛ остается неутешительным. Перспективы улучшить результаты терапии ОМЛ находятся в области таргетной терапии. Гемтузумаб озогамицин* (ГО) представляет собой конъюгированное моноклональное антиCD33 антитело, ковалентно связанное с цитотоксическим агентом – калихеамицином. Поскольку CD33 экспрессируется на бластах почти у всех пациентов с ОМЛ, использование ГО в сочетании с химиотерапией (ХТ) дает шанс на получение ПР и проведении аллогенной трансплантации костного мозга (алло-ТГСК).
Цель работы
Оценить эффективность и токсичсность ГО в сочетании с ХТ у пациентов ХР ОМЛ.
Пациенты и методы
В исследование включено 25 пациентов с ХР ОМЛ. Медиана возраста составила 36(18-68) лет. Согласно моекулярно-цитогенетической классификации (МЦК): низкий риск (НР) – 2, средний (СР) – 14, высокий (ВР) – 9 пациентов. Первично ХР (ПХР) были 13 пациентов, вторично ХР (ВХР) – 12. Изолированное поражение костного мозга было у 16 больных, комбинированное у 8 (ЦНС – 2, экстрамедуллярное поражение – 7; один пациент имел сочетанное поражение). Медиана уровня экспрессии CD33 составила 72 (9-95)%. ГО получили после алло-ТГСК 4 (16%) больных. ГО вводили в дозе 3 мг/м2 (максимально 5 мг) в сочетании с высокодозной ХТ (ВДХТ) (FLAG±Ida, HDAC, HAM) или низкодозной ХТ (НДХТ) (MEtA, LDARA-C) – 12 и 13 больных, соответственно. ГО вводился однократно (1ГО) у 13, двукратно (2ГО) – 4 и трехкратно (3ГО) – 8 пациентов, соответственно. ТГСК (нерод-3, гапло-3, ауто-1) проведена после терапии ГО 7(28%) пациентам, из них у 2 – повторная алло-ТГСК со сменой донора. Медиана сроков проведения ТГСК после терапии ГО 62 (17-138) дней.
Результаты
ПР достигнута у 3(12%), ПР без восстановления показателей периферической крови (нПР) у 6(24%) пациентов, соответственно, общий положительный ответ (ОПО) получен у 9(36%) больных. Медиана продолжительности ПР 56(6-341) дней. В зависимости от МЦК ОПО достигнут у 2 больных в НР, у 4 (29%) в СР, у 3 (33%) пациентов в ВР. ОПО был у 3 (23%) пациентов с ПХР, и у 6 (50%) с ВХР. При сочетании НДХТ+ГО ОПО получен у 3 (23%) пациентов, при ВДХТ+ГО – у 6 (50%). В зависимости от кратности введения ГО ОПО констатирован при 1ГО – у 4 (31%), 2ГО – 0, 3ГО – 5 (62%) пациентов. Однолетняя общая (1ОВ) и безрецидивная (1БРВ) выживаемость составили 26% (95%ДИ 6-46%) и 25% (95%ДИ 6-44%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии ГО 1ОБ и 1БРВ составила 21% (95%ДИ 4-38) против 8% (95%ДИ 1-15) р=.02 и 19% (95%ДИ 3-25) против 6% (95%ДИ 1-11) р=.01, соответственно. Из ответивших на терапию ГО умерло 3 пациента от прогрессии ОМЛ, 1 пациент от инфекции и 1 от геморрагического синдрома. Печеночная токсичность (трансфераземия) 1-2 степени у 3 пациентов и 3 степени – у 2; сепсис у 9 пациентов. Синусоидальный обструктивный синдром не отмечался ни у одного пациента.
Заключение
Это исследование продемонстрировало значимую эффективность и приемлемый профиль токсичности при комбинации ГО и ХТ. Сочетанное применение ГО и ХТ может рассматриваться для пациентов с ХР ОМЛ, как этап подготовки к алло-ТГСК.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
* ГО предоставлялся в рамках программы расширенного доступа по жизненным показаниям
Ключевые слова
Острый миелоидный лейкоз, таргетная терапия, гемтузумаб озогамицин.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6654) "Введение
При развитии рецидива острого миелоидного лейкоза (ОМЛ) полную ремиссию (ПР) удается достичь в 25-50% случаев. Пятилетняя общая выживаемость составляет 11%. Прогноз для пациентов с химиорезистентным (ХР) ОМЛ остается неутешительным. Перспективы улучшить результаты терапии ОМЛ находятся в области таргетной терапии. Гемтузумаб озогамицин* (ГО) представляет собой конъюгированное моноклональное антиCD33 антитело, ковалентно связанное с цитотоксическим агентом – калихеамицином. Поскольку CD33 экспрессируется на бластах почти у всех пациентов с ОМЛ, использование ГО в сочетании с химиотерапией (ХТ) дает шанс на получение ПР и проведении аллогенной трансплантации костного мозга (алло-ТГСК).
Цель работы
Оценить эффективность и токсичсность ГО в сочетании с ХТ у пациентов ХР ОМЛ.
Пациенты и методы
В исследование включено 25 пациентов с ХР ОМЛ. Медиана возраста составила 36(18-68) лет. Согласно моекулярно-цитогенетической классификации (МЦК): низкий риск (НР) – 2, средний (СР) – 14, высокий (ВР) – 9 пациентов. Первично ХР (ПХР) были 13 пациентов, вторично ХР (ВХР) – 12. Изолированное поражение костного мозга было у 16 больных, комбинированное у 8 (ЦНС – 2, экстрамедуллярное поражение – 7; один пациент имел сочетанное поражение). Медиана уровня экспрессии CD33 составила 72 (9-95)%. ГО получили после алло-ТГСК 4 (16%) больных. ГО вводили в дозе 3 мг/м2 (максимально 5 мг) в сочетании с высокодозной ХТ (ВДХТ) (FLAG±Ida, HDAC, HAM) или низкодозной ХТ (НДХТ) (MEtA, LDARA-C) – 12 и 13 больных, соответственно. ГО вводился однократно (1ГО) у 13, двукратно (2ГО) – 4 и трехкратно (3ГО) – 8 пациентов, соответственно. ТГСК (нерод-3, гапло-3, ауто-1) проведена после терапии ГО 7(28%) пациентам, из них у 2 – повторная алло-ТГСК со сменой донора. Медиана сроков проведения ТГСК после терапии ГО 62 (17-138) дней.
Результаты
ПР достигнута у 3(12%), ПР без восстановления показателей периферической крови (нПР) у 6(24%) пациентов, соответственно, общий положительный ответ (ОПО) получен у 9(36%) больных. Медиана продолжительности ПР 56(6-341) дней. В зависимости от МЦК ОПО достигнут у 2 больных в НР, у 4 (29%) в СР, у 3 (33%) пациентов в ВР. ОПО был у 3 (23%) пациентов с ПХР, и у 6 (50%) с ВХР. При сочетании НДХТ+ГО ОПО получен у 3 (23%) пациентов, при ВДХТ+ГО – у 6 (50%). В зависимости от кратности введения ГО ОПО констатирован при 1ГО – у 4 (31%), 2ГО – 0, 3ГО – 5 (62%) пациентов. Однолетняя общая (1ОВ) и безрецидивная (1БРВ) выживаемость составили 26% (95%ДИ 6-46%) и 25% (95%ДИ 6-44%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии ГО 1ОБ и 1БРВ составила 21% (95%ДИ 4-38) против 8% (95%ДИ 1-15) р=.02 и 19% (95%ДИ 3-25) против 6% (95%ДИ 1-11) р=.01, соответственно. Из ответивших на терапию ГО умерло 3 пациента от прогрессии ОМЛ, 1 пациент от инфекции и 1 от геморрагического синдрома. Печеночная токсичность (трансфераземия) 1-2 степени у 3 пациентов и 3 степени – у 2; сепсис у 9 пациентов. Синусоидальный обструктивный синдром не отмечался ни у одного пациента.
Заключение
Это исследование продемонстрировало значимую эффективность и приемлемый профиль токсичности при комбинации ГО и ХТ. Сочетанное применение ГО и ХТ может рассматриваться для пациентов с ХР ОМЛ, как этап подготовки к алло-ТГСК.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
* ГО предоставлялся в рамках программы расширенного доступа по жизненным показаниям
Ключевые слова
Острый миелоидный лейкоз, таргетная терапия, гемтузумаб озогамицин.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20318" ["VALUE"]=> array(2) { ["TEXT"]=> string(656) "<sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург<br> <sup>2</sup> Ленинградская областная клиническая больница, Санкт-Петербург<br> <sup>3</sup> Городская больница №15, Санкт-Петербург<br> <sup>4</sup> Городская клиническая больница №52, Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(590) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург2 Ленинградская областная клиническая больница, Санкт-Петербург
3 Городская больница №15, Санкт-Петербург
4 Городская клиническая больница №52, Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(590) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург
2 Ленинградская областная клиническая больница, Санкт-Петербург
3 Городская больница №15, Санкт-Петербург
4 Городская клиническая больница №52, Москва, Российская Федерация" } } } [20]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1556" ["~ID"]=> string(4) "1556" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(213) "Терапия рецидивов и прогрессии лимфомы Ходжкина после аллогенной трансплантации гемопоэтических стволовых клеток" ["~NAME"]=> string(213) "Терапия рецидивов и прогрессии лимфомы Ходжкина после аллогенной трансплантации гемопоэтических стволовых клеток" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:26:33" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:26:33" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/terapiya-retsidivov-i-progressii-limfomy-khodzhkina-posle-allogennoy-transplantatsii-gemopoeticheski/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/terapiya-retsidivov-i-progressii-limfomy-khodzhkina-posle-allogennoy-transplantatsii-gemopoeticheski/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "terapiya-retsidivov-i-progressii-limfomy-khodzhkina-posle-allogennoy-transplantatsii-gemopoeticheski" ["~CODE"]=> string(100) "terapiya-retsidivov-i-progressii-limfomy-khodzhkina-posle-allogennoy-transplantatsii-gemopoeticheski" ["EXTERNAL_ID"]=> string(4) "1556" ["~EXTERNAL_ID"]=> string(4) "1556" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(213) "Терапия рецидивов и прогрессии лимфомы Ходжкина после аллогенной трансплантации гемопоэтических стволовых клеток" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(333) "Терапия рецидивов и прогрессии лимфомы Ходжкина после аллогенной трансплантации гемопоэтических стволовых клетокTherapy of relapse and progression of classical Hodgkin lymphoma after allogeneic hematopoetic stem cell transplantation" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(8339) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) имеет высокий потенциал излечения классической лимфомы Ходжкина (ЛХ) у пациентов с рефрактерным или рецидивирующим течением (р/рЛХ). Тем не менее, опубликованных данных о терапии рецидива или прогрессирования ЛХ после алло-ТГСК крайне мало. В одноцентровом исследовании была проведена попытка выявить прогностические факторы в лечение подобных пациентов. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В этот ретроспективный анализ включены пациенты (n=27), прошедшие аллоТКМ в нашей клинике с 2002 по 2017 гг. Пациенты с подтвержденным прогрессиро-ванием заболевания после аллоТГСК составили 22,2% (n=6); пациенты с ПО, но c рецидивом или прогрессированием далее – 25,9% (n=7); пациенты с первым ответом хуже чем ПО (ЧО/СЗ) составили 51,8% (n=14), включая 7 пациентов c неподтвержденным 1-м статусом таким как ЧО/СЗ, основываясь на статусе заболевания перед аллоТКМ, при этом ПО и ПЗ также не подтверждены. При первом стадировании после алло-ТГСК у 7 пациентов зафиксирован ПО (25,0%), ЧО отмечен у 10 пациентов (37,0%), таким образом у 17 (62,9%) пациентов был общий ответ. За период наблюдения у 20 пациентов (74,0%) из 27 зафиксированы прогрессирование или рецидив ЛХ после аллоТКМ. 19 пациентов получили лечение: 6 пациентов получили только химиотерапию (х/т) после аллоТКМ (ChVPP, LABO, винбластин); 13 пациентов получили терапию новыми моноклональными антителами (МА): брентуксимаб ведотин (BV) и ниволумаб (Nivo), или сочетание их с химиотерапией. Остальные 8 пациентов были оставлены без терапии: 3 пациента (ЧО, СЗ, ПЗ) из-за осложнений алло-ТГСК и плохого соматического статуса; 5 пациентов из группы неподтвержденного статуса (ЧО-4, СЗ-1) – под динамическим наблюдением. 13 пациентов (48,1%). Терапию BV-содержащими схемами в качестве первой линии МА-терапии получили все 13 пациентов. 7 из них (53,8%; 25,9%) из-за продолжающегося прогрессирования ЛХ переведены на вторую линию терапии МА ниволумабом. До начала терапии MA (BV) 5 из 13 пациентов получили ХТ, и 4 пациента из 13 получили инфузии донорских лимфоцитов (ИЛД). Характеристики пациентов и методов представлены в таблице №1. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> На момент анализа время наблюдения за всеми пациентами (n=27) было 27 (1,4-3,7) мес. Для пациентов только с х/т (n=6) время наблюдения 25 (6,27-51) мес.; для 13 пациентов с МА-терапией – 45 мес. (23-73). Медиана наблюдения за пациентами без терапии (n=8) 11 мес. (1,47-39,37). Общая выживаемость для всех пациентов на момент анализа была 55% (n=15). Время от трансплантации до ПЗ/РЗ было 3,6 мес. (1,3-11,3 мес.). Среднее время от алло-ТГСК до начала терапии BV по поводу ПЗ/РЗ было 4,7 мес. (1,7-44 мес.). Среднее время от алло-ТГСК до начала терапии Nivo было 38,7 мес. (14,5-44,5). Среднее время между окончанием терапии BV и началом терапии Nivo было 2,83 (1,23-32,47) месяцев. На момент анализа 12 пациентов (44,4%) из 27 умерли: 6 из-за прогрессирования ЛХ и 6 пациентов из-за тяжелой хронической РТПХ (хрРТПХ) и инфекционных осложнений в посттрансплантационном периоде, включая 3 пациентов с МА-терапией и 1 пациента под динамическим наблюдением. 15 пациентов живы: у 4х пациентов в процессе наблюдения зафиксирован ПО; 6 пациентов в ПО после МА-терапии (5) и после ХТ (1); 5 пациентов продолжают лечение из-за стабилизации ли прогрессирования ЛХ. При сравнении результатов ХТ и терапии МА, прогностическим значением облада- ло лечение МА (76,9% против 16,7%, p=.003), также развитие хрРТПХ имело прогностическое значение (72,7% против 43,9%, p=.084). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> На небольшом клиническом материале было показано, что треть пациентов погибают от прогрессирования ЛХ и почти столько же от осложнений терапии. Несмотря на относительно благоприятный прогноз в этой тяжелой группе пациентов, требуются дальнейшие исследования для выбора оптимальной терапии посттрансплантационного рецидива и прогрессирования ЛХ. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфома Ходжкина, аллогенная трансплантация костного мозга, брентуксимаб ведотин, ниволумаб. </p> <h2 style="text-align: justify;"> Таблица 1. Характеристики пациентов и методы терапии (продолжение)<br> </h2> <p style="text-align: justify;"> <img width="780" alt="таблица 1 часть.png" src="/upload/medialibrary/94c/tablitsa-1-chast.png" height="407" title="таблица 1 часть.png"><br> </p> <p style="text-align: justify;"> <img width="781" alt="таблица 2 часть.png" src="/upload/medialibrary/664/tablitsa-2-chast.png" height="303" title="таблица 2 часть.png"><br> </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(213) "Терапия рецидивов и прогрессии лимфомы Ходжкина после аллогенной трансплантации гемопоэтических стволовых клеток" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(213) "Терапия рецидивов и прогрессии лимфомы Ходжкина после аллогенной трансплантации гемопоэтических стволовых клеток" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(213) "Терапия рецидивов и прогрессии лимфомы Ходжкина после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_META_TITLE"]=> string(213) "Терапия рецидивов и прогрессии лимфомы Ходжкина после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_META_KEYWORDS"]=> string(213) "Терапия рецидивов и прогрессии лимфомы Ходжкина после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_META_DESCRIPTION"]=> string(213) "Терапия рецидивов и прогрессии лимфомы Ходжкина после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_ALT"]=> string(213) "Терапия рецидивов и прогрессии лимфомы Ходжкина после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_TITLE"]=> string(213) "Терапия рецидивов и прогрессии лимфомы Ходжкина после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "terapiya-retsidivov-i-progressii-limfomy-khodzhkina-posle-allogennoy-transplantatsii-gemopoeticheski" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(213) "Терапия рецидивов и прогрессии лимфомы Ходжкина после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(213) "Терапия рецидивов и прогрессии лимфомы Ходжкина после аллогенной трансплантации гемопоэтических стволовых клеток" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "terapiya-retsidivov-i-progressii-limfomy-khodzhkina-posle-allogennoy-transplantatsii-gemopoeticheski" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "terapiya-retsidivov-i-progressii-limfomy-khodzhkina-posle-allogennoy-transplantatsii-gemopoeticheski" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "terapiya-retsidivov-i-progressii-limfomy-khodzhkina-posle-allogennoy-transplantatsii-gemopoeticheski" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20325" ["VALUE"]=> array(2) { ["TEXT"]=> string(387) "Евгения С. Борзенкова, Наталья Б. Михайлова, Кирилл В. Лепик, Лилия В. Стельмах, Анастасия В. Некрасова, Иван В. Цыганков, Иван С. Моисеев, Юрий Р. Залялов, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(381) "Евгения С. Борзенкова, Наталья Б. Михайлова, Кирилл В. Лепик, Лилия В. Стельмах, Анастасия В. Некрасова, Иван В. Цыганков, Иван С. Моисеев, Юрий Р. Залялов, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20326" ["VALUE"]=> array(2) { ["TEXT"]=> string(358) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(352) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20344" ["VALUE"]=> array(2) { ["TEXT"]=> string(8339) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) имеет высокий потенциал излечения классической лимфомы Ходжкина (ЛХ) у пациентов с рефрактерным или рецидивирующим течением (р/рЛХ). Тем не менее, опубликованных данных о терапии рецидива или прогрессирования ЛХ после алло-ТГСК крайне мало. В одноцентровом исследовании была проведена попытка выявить прогностические факторы в лечение подобных пациентов. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В этот ретроспективный анализ включены пациенты (n=27), прошедшие аллоТКМ в нашей клинике с 2002 по 2017 гг. Пациенты с подтвержденным прогрессиро-ванием заболевания после аллоТГСК составили 22,2% (n=6); пациенты с ПО, но c рецидивом или прогрессированием далее – 25,9% (n=7); пациенты с первым ответом хуже чем ПО (ЧО/СЗ) составили 51,8% (n=14), включая 7 пациентов c неподтвержденным 1-м статусом таким как ЧО/СЗ, основываясь на статусе заболевания перед аллоТКМ, при этом ПО и ПЗ также не подтверждены. При первом стадировании после алло-ТГСК у 7 пациентов зафиксирован ПО (25,0%), ЧО отмечен у 10 пациентов (37,0%), таким образом у 17 (62,9%) пациентов был общий ответ. За период наблюдения у 20 пациентов (74,0%) из 27 зафиксированы прогрессирование или рецидив ЛХ после аллоТКМ. 19 пациентов получили лечение: 6 пациентов получили только химиотерапию (х/т) после аллоТКМ (ChVPP, LABO, винбластин); 13 пациентов получили терапию новыми моноклональными антителами (МА): брентуксимаб ведотин (BV) и ниволумаб (Nivo), или сочетание их с химиотерапией. Остальные 8 пациентов были оставлены без терапии: 3 пациента (ЧО, СЗ, ПЗ) из-за осложнений алло-ТГСК и плохого соматического статуса; 5 пациентов из группы неподтвержденного статуса (ЧО-4, СЗ-1) – под динамическим наблюдением. 13 пациентов (48,1%). Терапию BV-содержащими схемами в качестве первой линии МА-терапии получили все 13 пациентов. 7 из них (53,8%; 25,9%) из-за продолжающегося прогрессирования ЛХ переведены на вторую линию терапии МА ниволумабом. До начала терапии MA (BV) 5 из 13 пациентов получили ХТ, и 4 пациента из 13 получили инфузии донорских лимфоцитов (ИЛД). Характеристики пациентов и методов представлены в таблице №1. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> На момент анализа время наблюдения за всеми пациентами (n=27) было 27 (1,4-3,7) мес. Для пациентов только с х/т (n=6) время наблюдения 25 (6,27-51) мес.; для 13 пациентов с МА-терапией – 45 мес. (23-73). Медиана наблюдения за пациентами без терапии (n=8) 11 мес. (1,47-39,37). Общая выживаемость для всех пациентов на момент анализа была 55% (n=15). Время от трансплантации до ПЗ/РЗ было 3,6 мес. (1,3-11,3 мес.). Среднее время от алло-ТГСК до начала терапии BV по поводу ПЗ/РЗ было 4,7 мес. (1,7-44 мес.). Среднее время от алло-ТГСК до начала терапии Nivo было 38,7 мес. (14,5-44,5). Среднее время между окончанием терапии BV и началом терапии Nivo было 2,83 (1,23-32,47) месяцев. На момент анализа 12 пациентов (44,4%) из 27 умерли: 6 из-за прогрессирования ЛХ и 6 пациентов из-за тяжелой хронической РТПХ (хрРТПХ) и инфекционных осложнений в посттрансплантационном периоде, включая 3 пациентов с МА-терапией и 1 пациента под динамическим наблюдением. 15 пациентов живы: у 4х пациентов в процессе наблюдения зафиксирован ПО; 6 пациентов в ПО после МА-терапии (5) и после ХТ (1); 5 пациентов продолжают лечение из-за стабилизации ли прогрессирования ЛХ. При сравнении результатов ХТ и терапии МА, прогностическим значением облада- ло лечение МА (76,9% против 16,7%, p=.003), также развитие хрРТПХ имело прогностическое значение (72,7% против 43,9%, p=.084). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> На небольшом клиническом материале было показано, что треть пациентов погибают от прогрессирования ЛХ и почти столько же от осложнений терапии. Несмотря на относительно благоприятный прогноз в этой тяжелой группе пациентов, требуются дальнейшие исследования для выбора оптимальной терапии посттрансплантационного рецидива и прогрессирования ЛХ. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфома Ходжкина, аллогенная трансплантация костного мозга, брентуксимаб ведотин, ниволумаб. </p> <h2 style="text-align: justify;"> Таблица 1. Характеристики пациентов и методы терапии (продолжение)<br> </h2> <p style="text-align: justify;"> <img width="780" alt="таблица 1 часть.png" src="/upload/medialibrary/94c/tablitsa-1-chast.png" height="407" title="таблица 1 часть.png"><br> </p> <p style="text-align: justify;"> <img width="781" alt="таблица 2 часть.png" src="/upload/medialibrary/664/tablitsa-2-chast.png" height="303" title="таблица 2 часть.png"><br> </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7923) "
Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) имеет высокий потенциал излечения классической лимфомы Ходжкина (ЛХ) у пациентов с рефрактерным или рецидивирующим течением (р/рЛХ). Тем не менее, опубликованных данных о терапии рецидива или прогрессирования ЛХ после алло-ТГСК крайне мало. В одноцентровом исследовании была проведена попытка выявить прогностические факторы в лечение подобных пациентов.
Пациенты и методы
В этот ретроспективный анализ включены пациенты (n=27), прошедшие аллоТКМ в нашей клинике с 2002 по 2017 гг. Пациенты с подтвержденным прогрессиро-ванием заболевания после аллоТГСК составили 22,2% (n=6); пациенты с ПО, но c рецидивом или прогрессированием далее – 25,9% (n=7); пациенты с первым ответом хуже чем ПО (ЧО/СЗ) составили 51,8% (n=14), включая 7 пациентов c неподтвержденным 1-м статусом таким как ЧО/СЗ, основываясь на статусе заболевания перед аллоТКМ, при этом ПО и ПЗ также не подтверждены. При первом стадировании после алло-ТГСК у 7 пациентов зафиксирован ПО (25,0%), ЧО отмечен у 10 пациентов (37,0%), таким образом у 17 (62,9%) пациентов был общий ответ. За период наблюдения у 20 пациентов (74,0%) из 27 зафиксированы прогрессирование или рецидив ЛХ после аллоТКМ. 19 пациентов получили лечение: 6 пациентов получили только химиотерапию (х/т) после аллоТКМ (ChVPP, LABO, винбластин); 13 пациентов получили терапию новыми моноклональными антителами (МА): брентуксимаб ведотин (BV) и ниволумаб (Nivo), или сочетание их с химиотерапией. Остальные 8 пациентов были оставлены без терапии: 3 пациента (ЧО, СЗ, ПЗ) из-за осложнений алло-ТГСК и плохого соматического статуса; 5 пациентов из группы неподтвержденного статуса (ЧО-4, СЗ-1) – под динамическим наблюдением. 13 пациентов (48,1%). Терапию BV-содержащими схемами в качестве первой линии МА-терапии получили все 13 пациентов. 7 из них (53,8%; 25,9%) из-за продолжающегося прогрессирования ЛХ переведены на вторую линию терапии МА ниволумабом. До начала терапии MA (BV) 5 из 13 пациентов получили ХТ, и 4 пациента из 13 получили инфузии донорских лимфоцитов (ИЛД). Характеристики пациентов и методов представлены в таблице №1.
Результаты
На момент анализа время наблюдения за всеми пациентами (n=27) было 27 (1,4-3,7) мес. Для пациентов только с х/т (n=6) время наблюдения 25 (6,27-51) мес.; для 13 пациентов с МА-терапией – 45 мес. (23-73). Медиана наблюдения за пациентами без терапии (n=8) 11 мес. (1,47-39,37). Общая выживаемость для всех пациентов на момент анализа была 55% (n=15). Время от трансплантации до ПЗ/РЗ было 3,6 мес. (1,3-11,3 мес.). Среднее время от алло-ТГСК до начала терапии BV по поводу ПЗ/РЗ было 4,7 мес. (1,7-44 мес.). Среднее время от алло-ТГСК до начала терапии Nivo было 38,7 мес. (14,5-44,5). Среднее время между окончанием терапии BV и началом терапии Nivo было 2,83 (1,23-32,47) месяцев. На момент анализа 12 пациентов (44,4%) из 27 умерли: 6 из-за прогрессирования ЛХ и 6 пациентов из-за тяжелой хронической РТПХ (хрРТПХ) и инфекционных осложнений в посттрансплантационном периоде, включая 3 пациентов с МА-терапией и 1 пациента под динамическим наблюдением. 15 пациентов живы: у 4х пациентов в процессе наблюдения зафиксирован ПО; 6 пациентов в ПО после МА-терапии (5) и после ХТ (1); 5 пациентов продолжают лечение из-за стабилизации ли прогрессирования ЛХ. При сравнении результатов ХТ и терапии МА, прогностическим значением облада- ло лечение МА (76,9% против 16,7%, p=.003), также развитие хрРТПХ имело прогностическое значение (72,7% против 43,9%, p=.084).
Выводы
На небольшом клиническом материале было показано, что треть пациентов погибают от прогрессирования ЛХ и почти столько же от осложнений терапии. Несмотря на относительно благоприятный прогноз в этой тяжелой группе пациентов, требуются дальнейшие исследования для выбора оптимальной терапии посттрансплантационного рецидива и прогрессирования ЛХ.
Ключевые слова
Лимфома Ходжкина, аллогенная трансплантация костного мозга, брентуксимаб ведотин, ниволумаб.
Таблица 1. Характеристики пациентов и методы терапии (продолжение)


" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20328" ["VALUE"]=> array(2) { ["TEXT"]=> string(179) "R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation; First St. Petersburg I. Pavlov State Medical University, St. Petersburg, Russia<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(173) "R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation; First St. Petersburg I. Pavlov State Medical University, St. Petersburg, Russia
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20345" ["VALUE"]=> array(2) { ["TEXT"]=> string(5037) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic hematopoetic stem cell transplantation (allo-HSCT) has the curative potential for patients with relapsed and/or refractory classical Hodgkin lymphoma (cHL). Nevertheless, published data about therapy of relapse or progression (r/r) of cHL after alloHSCT is limited. The aim of single-center retrospective study was to identify prognostic factors in treatment of r/r cHL patients after allo-HSCT. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> This retrospective analysis included patients with r/r cHL (n=27), who had undergone allo-HSCT in our center from 2002 to 2017. Patients with documented relapse or progression of cHL after allo-HSCT were represented by 22.2% (n=6); patients with documented CR after allo-HSCT, but had relapse further, were represented by 25.9% (n=7); patients with first disease status after alloHST worse than CR (PR/SD) comprised 51.8% (n=14), including 7 patients with non-documented 1st disease status, such as PR/SD, based on cHL status before allo-HSCT, herewith CR and PD also were no documented. At the first staging after alloHSCT, CR was achieved in 7 patients (25.0%), PR was achieved in 10 patients (37.0%), 17 (62.9%) patients had objective response. Further on, 20 patients (74.0%) of 27 had progression or disease relapse after allo-HSCT, 19 patients of them received treatment, i.e., six patients of 20 received only chemotherapy (c/t; chemo) after allo-HSCT (ChVPP, LABO, vinblastine); 13 patients of 20 received novel monoclonal antibodies (Mabs), including brentuximab vedotin (BV) and nivolumab (Nivo), or their combination with chemotherapy. 8 patients of 20 did not receive treatment of cHL: three patients, due to other complications and poor performance status, and 5 patients with no documented 1st disease status (PR-1, SD-1) were at dynamic observation. BV-based regimens were used as the first-line Mab-therapy in all 13 Mab-treated patients (48.1%). Seven of them (53.8%; 25.9%), due to continuous progression, were transferred to second Mab- therapy line (with Nivolumab). Before treatment by Mab (BV) 5 of 13 patients received chemotherapy and 4 patients from 13 had got donor lymphocyte infusion (DLI). The patients characteristics are presented in Table 1. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> At the time of analysis, the median follow-up period was 27 (1.4-3.7) months. For patients with chemotherapy only, (n=6) median follow-up was 25 (6.27-55) months, patients with Mab-therapy (including combination with chemo) (n=13), 45mo (range, 23-73), and for non-treated patients (n=8), the median follow-up was 11 months (1.47-39.37). The median interval to progression/relapse of disease was 3.6 mo (1.3-11.3mo). Overall survival (OS) at the moment of analysis was 55% (15/27). The median interval between alloSCT and first dose of BV due to PD/RD was 4.7 (1.7- 44) mo. The median interval between alloSCT and first dose of Nivo was 38.7 months (range, 14.5-44.5). The median interval between last dose of BV and first dose of Nivo was 2.83 (1.23-32.47) months. At the moment of analysis 12 patients (44.4%) died: six with Hodgkin lymphoma progression, and six other patients were lost due to severe chronic GVHD (chGVHD) and infectious complications over post-transplant period, including 3 patients with Mab therapy, and one patient from the group of dynamic observation. 15 patient are alive: four patients with dynamic observation had achieved CR; six patients had achieved CR after Mab-therapy (5) and chemotherapy (1); 5 patients are continuing treatment because of stable or progressing disease. When compared with chemotherapy, Mab-therapy had prognostic significance (76.9% vs 16.7%, p=.003). Development of chGVHD also had prognostic significance (72.7% vs 43.9%, p=.084). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> As based on a limited clinical material, we have demonstrated that the lymphoma progression was the cause of lethal outcomes in one third of patients, and therapy-related complications were fatal in almost the same number of patients. Despite relatively favorable outcome in heavily pretreated patients, further studies are required to determine optimal therapy for post-transplant relapse of cHL. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hodgkin lymphoma, allogeneic hematopoetic stem cell transplantation, brentuximab vedotin, nivolumab.<br> <img width="785" alt="table_1.png" src="/upload/medialibrary/ce5/table_1.png" height="757" title="table_1.png"> </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4755) "
Introduction
Allogeneic hematopoetic stem cell transplantation (allo-HSCT) has the curative potential for patients with relapsed and/or refractory classical Hodgkin lymphoma (cHL). Nevertheless, published data about therapy of relapse or progression (r/r) of cHL after alloHSCT is limited. The aim of single-center retrospective study was to identify prognostic factors in treatment of r/r cHL patients after allo-HSCT.
Patients and methods
This retrospective analysis included patients with r/r cHL (n=27), who had undergone allo-HSCT in our center from 2002 to 2017. Patients with documented relapse or progression of cHL after allo-HSCT were represented by 22.2% (n=6); patients with documented CR after allo-HSCT, but had relapse further, were represented by 25.9% (n=7); patients with first disease status after alloHST worse than CR (PR/SD) comprised 51.8% (n=14), including 7 patients with non-documented 1st disease status, such as PR/SD, based on cHL status before allo-HSCT, herewith CR and PD also were no documented. At the first staging after alloHSCT, CR was achieved in 7 patients (25.0%), PR was achieved in 10 patients (37.0%), 17 (62.9%) patients had objective response. Further on, 20 patients (74.0%) of 27 had progression or disease relapse after allo-HSCT, 19 patients of them received treatment, i.e., six patients of 20 received only chemotherapy (c/t; chemo) after allo-HSCT (ChVPP, LABO, vinblastine); 13 patients of 20 received novel monoclonal antibodies (Mabs), including brentuximab vedotin (BV) and nivolumab (Nivo), or their combination with chemotherapy. 8 patients of 20 did not receive treatment of cHL: three patients, due to other complications and poor performance status, and 5 patients with no documented 1st disease status (PR-1, SD-1) were at dynamic observation. BV-based regimens were used as the first-line Mab-therapy in all 13 Mab-treated patients (48.1%). Seven of them (53.8%; 25.9%), due to continuous progression, were transferred to second Mab- therapy line (with Nivolumab). Before treatment by Mab (BV) 5 of 13 patients received chemotherapy and 4 patients from 13 had got donor lymphocyte infusion (DLI). The patients characteristics are presented in Table 1.
Results
At the time of analysis, the median follow-up period was 27 (1.4-3.7) months. For patients with chemotherapy only, (n=6) median follow-up was 25 (6.27-55) months, patients with Mab-therapy (including combination with chemo) (n=13), 45mo (range, 23-73), and for non-treated patients (n=8), the median follow-up was 11 months (1.47-39.37). The median interval to progression/relapse of disease was 3.6 mo (1.3-11.3mo). Overall survival (OS) at the moment of analysis was 55% (15/27). The median interval between alloSCT and first dose of BV due to PD/RD was 4.7 (1.7- 44) mo. The median interval between alloSCT and first dose of Nivo was 38.7 months (range, 14.5-44.5). The median interval between last dose of BV and first dose of Nivo was 2.83 (1.23-32.47) months. At the moment of analysis 12 patients (44.4%) died: six with Hodgkin lymphoma progression, and six other patients were lost due to severe chronic GVHD (chGVHD) and infectious complications over post-transplant period, including 3 patients with Mab therapy, and one patient from the group of dynamic observation. 15 patient are alive: four patients with dynamic observation had achieved CR; six patients had achieved CR after Mab-therapy (5) and chemotherapy (1); 5 patients are continuing treatment because of stable or progressing disease. When compared with chemotherapy, Mab-therapy had prognostic significance (76.9% vs 16.7%, p=.003). Development of chGVHD also had prognostic significance (72.7% vs 43.9%, p=.084).
Conclusion
As based on a limited clinical material, we have demonstrated that the lymphoma progression was the cause of lethal outcomes in one third of patients, and therapy-related complications were fatal in almost the same number of patients. Despite relatively favorable outcome in heavily pretreated patients, further studies are required to determine optimal therapy for post-transplant relapse of cHL.
Keywords
Hodgkin lymphoma, allogeneic hematopoetic stem cell transplantation, brentuximab vedotin, nivolumab.

" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(224) "Evgeniya S. Borzenkova, Natalia B. Mikhailova, Kirill V. Lepik, Lilia V. Stelmakh, Anastasia V. Nekrasova, Ivan V. Tsygankov, Ivan S. Moiseev, Yuri R. Zalyalov, Elena I. Darskaya, Sergey N. Bondarenko, Boris V. Afanasyev
" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20345" ["VALUE"]=> array(2) { ["TEXT"]=> string(5037) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Allogeneic hematopoetic stem cell transplantation (allo-HSCT) has the curative potential for patients with relapsed and/or refractory classical Hodgkin lymphoma (cHL). Nevertheless, published data about therapy of relapse or progression (r/r) of cHL after alloHSCT is limited. The aim of single-center retrospective study was to identify prognostic factors in treatment of r/r cHL patients after allo-HSCT. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> This retrospective analysis included patients with r/r cHL (n=27), who had undergone allo-HSCT in our center from 2002 to 2017. Patients with documented relapse or progression of cHL after allo-HSCT were represented by 22.2% (n=6); patients with documented CR after allo-HSCT, but had relapse further, were represented by 25.9% (n=7); patients with first disease status after alloHST worse than CR (PR/SD) comprised 51.8% (n=14), including 7 patients with non-documented 1st disease status, such as PR/SD, based on cHL status before allo-HSCT, herewith CR and PD also were no documented. At the first staging after alloHSCT, CR was achieved in 7 patients (25.0%), PR was achieved in 10 patients (37.0%), 17 (62.9%) patients had objective response. Further on, 20 patients (74.0%) of 27 had progression or disease relapse after allo-HSCT, 19 patients of them received treatment, i.e., six patients of 20 received only chemotherapy (c/t; chemo) after allo-HSCT (ChVPP, LABO, vinblastine); 13 patients of 20 received novel monoclonal antibodies (Mabs), including brentuximab vedotin (BV) and nivolumab (Nivo), or their combination with chemotherapy. 8 patients of 20 did not receive treatment of cHL: three patients, due to other complications and poor performance status, and 5 patients with no documented 1st disease status (PR-1, SD-1) were at dynamic observation. BV-based regimens were used as the first-line Mab-therapy in all 13 Mab-treated patients (48.1%). Seven of them (53.8%; 25.9%), due to continuous progression, were transferred to second Mab- therapy line (with Nivolumab). Before treatment by Mab (BV) 5 of 13 patients received chemotherapy and 4 patients from 13 had got donor lymphocyte infusion (DLI). The patients characteristics are presented in Table 1. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> At the time of analysis, the median follow-up period was 27 (1.4-3.7) months. For patients with chemotherapy only, (n=6) median follow-up was 25 (6.27-55) months, patients with Mab-therapy (including combination with chemo) (n=13), 45mo (range, 23-73), and for non-treated patients (n=8), the median follow-up was 11 months (1.47-39.37). The median interval to progression/relapse of disease was 3.6 mo (1.3-11.3mo). Overall survival (OS) at the moment of analysis was 55% (15/27). The median interval between alloSCT and first dose of BV due to PD/RD was 4.7 (1.7- 44) mo. The median interval between alloSCT and first dose of Nivo was 38.7 months (range, 14.5-44.5). The median interval between last dose of BV and first dose of Nivo was 2.83 (1.23-32.47) months. At the moment of analysis 12 patients (44.4%) died: six with Hodgkin lymphoma progression, and six other patients were lost due to severe chronic GVHD (chGVHD) and infectious complications over post-transplant period, including 3 patients with Mab therapy, and one patient from the group of dynamic observation. 15 patient are alive: four patients with dynamic observation had achieved CR; six patients had achieved CR after Mab-therapy (5) and chemotherapy (1); 5 patients are continuing treatment because of stable or progressing disease. When compared with chemotherapy, Mab-therapy had prognostic significance (76.9% vs 16.7%, p=.003). Development of chGVHD also had prognostic significance (72.7% vs 43.9%, p=.084). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> As based on a limited clinical material, we have demonstrated that the lymphoma progression was the cause of lethal outcomes in one third of patients, and therapy-related complications were fatal in almost the same number of patients. Despite relatively favorable outcome in heavily pretreated patients, further studies are required to determine optimal therapy for post-transplant relapse of cHL. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hodgkin lymphoma, allogeneic hematopoetic stem cell transplantation, brentuximab vedotin, nivolumab.<br> <img width="785" alt="table_1.png" src="/upload/medialibrary/ce5/table_1.png" height="757" title="table_1.png"> </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4755) "
Introduction
Allogeneic hematopoetic stem cell transplantation (allo-HSCT) has the curative potential for patients with relapsed and/or refractory classical Hodgkin lymphoma (cHL). Nevertheless, published data about therapy of relapse or progression (r/r) of cHL after alloHSCT is limited. The aim of single-center retrospective study was to identify prognostic factors in treatment of r/r cHL patients after allo-HSCT.
Patients and methods
This retrospective analysis included patients with r/r cHL (n=27), who had undergone allo-HSCT in our center from 2002 to 2017. Patients with documented relapse or progression of cHL after allo-HSCT were represented by 22.2% (n=6); patients with documented CR after allo-HSCT, but had relapse further, were represented by 25.9% (n=7); patients with first disease status after alloHST worse than CR (PR/SD) comprised 51.8% (n=14), including 7 patients with non-documented 1st disease status, such as PR/SD, based on cHL status before allo-HSCT, herewith CR and PD also were no documented. At the first staging after alloHSCT, CR was achieved in 7 patients (25.0%), PR was achieved in 10 patients (37.0%), 17 (62.9%) patients had objective response. Further on, 20 patients (74.0%) of 27 had progression or disease relapse after allo-HSCT, 19 patients of them received treatment, i.e., six patients of 20 received only chemotherapy (c/t; chemo) after allo-HSCT (ChVPP, LABO, vinblastine); 13 patients of 20 received novel monoclonal antibodies (Mabs), including brentuximab vedotin (BV) and nivolumab (Nivo), or their combination with chemotherapy. 8 patients of 20 did not receive treatment of cHL: three patients, due to other complications and poor performance status, and 5 patients with no documented 1st disease status (PR-1, SD-1) were at dynamic observation. BV-based regimens were used as the first-line Mab-therapy in all 13 Mab-treated patients (48.1%). Seven of them (53.8%; 25.9%), due to continuous progression, were transferred to second Mab- therapy line (with Nivolumab). Before treatment by Mab (BV) 5 of 13 patients received chemotherapy and 4 patients from 13 had got donor lymphocyte infusion (DLI). The patients characteristics are presented in Table 1.
Results
At the time of analysis, the median follow-up period was 27 (1.4-3.7) months. For patients with chemotherapy only, (n=6) median follow-up was 25 (6.27-55) months, patients with Mab-therapy (including combination with chemo) (n=13), 45mo (range, 23-73), and for non-treated patients (n=8), the median follow-up was 11 months (1.47-39.37). The median interval to progression/relapse of disease was 3.6 mo (1.3-11.3mo). Overall survival (OS) at the moment of analysis was 55% (15/27). The median interval between alloSCT and first dose of BV due to PD/RD was 4.7 (1.7- 44) mo. The median interval between alloSCT and first dose of Nivo was 38.7 months (range, 14.5-44.5). The median interval between last dose of BV and first dose of Nivo was 2.83 (1.23-32.47) months. At the moment of analysis 12 patients (44.4%) died: six with Hodgkin lymphoma progression, and six other patients were lost due to severe chronic GVHD (chGVHD) and infectious complications over post-transplant period, including 3 patients with Mab therapy, and one patient from the group of dynamic observation. 15 patient are alive: four patients with dynamic observation had achieved CR; six patients had achieved CR after Mab-therapy (5) and chemotherapy (1); 5 patients are continuing treatment because of stable or progressing disease. When compared with chemotherapy, Mab-therapy had prognostic significance (76.9% vs 16.7%, p=.003). Development of chGVHD also had prognostic significance (72.7% vs 43.9%, p=.084).
Conclusion
As based on a limited clinical material, we have demonstrated that the lymphoma progression was the cause of lethal outcomes in one third of patients, and therapy-related complications were fatal in almost the same number of patients. Despite relatively favorable outcome in heavily pretreated patients, further studies are required to determine optimal therapy for post-transplant relapse of cHL.
Keywords
Hodgkin lymphoma, allogeneic hematopoetic stem cell transplantation, brentuximab vedotin, nivolumab.

Introduction
Allogeneic hematopoetic stem cell transplantation (allo-HSCT) has the curative potential for patients with relapsed and/or refractory classical Hodgkin lymphoma (cHL). Nevertheless, published data about therapy of relapse or progression (r/r) of cHL after alloHSCT is limited. The aim of single-center retrospective study was to identify prognostic factors in treatment of r/r cHL patients after allo-HSCT.
Patients and methods
This retrospective analysis included patients with r/r cHL (n=27), who had undergone allo-HSCT in our center from 2002 to 2017. Patients with documented relapse or progression of cHL after allo-HSCT were represented by 22.2% (n=6); patients with documented CR after allo-HSCT, but had relapse further, were represented by 25.9% (n=7); patients with first disease status after alloHST worse than CR (PR/SD) comprised 51.8% (n=14), including 7 patients with non-documented 1st disease status, such as PR/SD, based on cHL status before allo-HSCT, herewith CR and PD also were no documented. At the first staging after alloHSCT, CR was achieved in 7 patients (25.0%), PR was achieved in 10 patients (37.0%), 17 (62.9%) patients had objective response. Further on, 20 patients (74.0%) of 27 had progression or disease relapse after allo-HSCT, 19 patients of them received treatment, i.e., six patients of 20 received only chemotherapy (c/t; chemo) after allo-HSCT (ChVPP, LABO, vinblastine); 13 patients of 20 received novel monoclonal antibodies (Mabs), including brentuximab vedotin (BV) and nivolumab (Nivo), or their combination with chemotherapy. 8 patients of 20 did not receive treatment of cHL: three patients, due to other complications and poor performance status, and 5 patients with no documented 1st disease status (PR-1, SD-1) were at dynamic observation. BV-based regimens were used as the first-line Mab-therapy in all 13 Mab-treated patients (48.1%). Seven of them (53.8%; 25.9%), due to continuous progression, were transferred to second Mab- therapy line (with Nivolumab). Before treatment by Mab (BV) 5 of 13 patients received chemotherapy and 4 patients from 13 had got donor lymphocyte infusion (DLI). The patients characteristics are presented in Table 1.
Results
At the time of analysis, the median follow-up period was 27 (1.4-3.7) months. For patients with chemotherapy only, (n=6) median follow-up was 25 (6.27-55) months, patients with Mab-therapy (including combination with chemo) (n=13), 45mo (range, 23-73), and for non-treated patients (n=8), the median follow-up was 11 months (1.47-39.37). The median interval to progression/relapse of disease was 3.6 mo (1.3-11.3mo). Overall survival (OS) at the moment of analysis was 55% (15/27). The median interval between alloSCT and first dose of BV due to PD/RD was 4.7 (1.7- 44) mo. The median interval between alloSCT and first dose of Nivo was 38.7 months (range, 14.5-44.5). The median interval between last dose of BV and first dose of Nivo was 2.83 (1.23-32.47) months. At the moment of analysis 12 patients (44.4%) died: six with Hodgkin lymphoma progression, and six other patients were lost due to severe chronic GVHD (chGVHD) and infectious complications over post-transplant period, including 3 patients with Mab therapy, and one patient from the group of dynamic observation. 15 patient are alive: four patients with dynamic observation had achieved CR; six patients had achieved CR after Mab-therapy (5) and chemotherapy (1); 5 patients are continuing treatment because of stable or progressing disease. When compared with chemotherapy, Mab-therapy had prognostic significance (76.9% vs 16.7%, p=.003). Development of chGVHD also had prognostic significance (72.7% vs 43.9%, p=.084).
Conclusion
As based on a limited clinical material, we have demonstrated that the lymphoma progression was the cause of lethal outcomes in one third of patients, and therapy-related complications were fatal in almost the same number of patients. Despite relatively favorable outcome in heavily pretreated patients, further studies are required to determine optimal therapy for post-transplant relapse of cHL.
Keywords
Hodgkin lymphoma, allogeneic hematopoetic stem cell transplantation, brentuximab vedotin, nivolumab.

" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(173) "R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation; First St. Petersburg I. Pavlov State Medical University, St. Petersburg, Russia
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20325" ["VALUE"]=> array(2) { ["TEXT"]=> string(387) "Евгения С. Борзенкова, Наталья Б. Михайлова, Кирилл В. Лепик, Лилия В. Стельмах, Анастасия В. Некрасова, Иван В. Цыганков, Иван С. Моисеев, Юрий Р. Залялов, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(381) "Евгения С. Борзенкова, Наталья Б. Михайлова, Кирилл В. Лепик, Лилия В. Стельмах, Анастасия В. Некрасова, Иван В. Цыганков, Иван С. Моисеев, Юрий Р. Залялов, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(381) "Евгения С. Борзенкова, Наталья Б. Михайлова, Кирилл В. Лепик, Лилия В. Стельмах, Анастасия В. Некрасова, Иван В. Цыганков, Иван С. Моисеев, Юрий Р. Залялов, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев
" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20344" ["VALUE"]=> array(2) { ["TEXT"]=> string(8339) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) имеет высокий потенциал излечения классической лимфомы Ходжкина (ЛХ) у пациентов с рефрактерным или рецидивирующим течением (р/рЛХ). Тем не менее, опубликованных данных о терапии рецидива или прогрессирования ЛХ после алло-ТГСК крайне мало. В одноцентровом исследовании была проведена попытка выявить прогностические факторы в лечение подобных пациентов. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В этот ретроспективный анализ включены пациенты (n=27), прошедшие аллоТКМ в нашей клинике с 2002 по 2017 гг. Пациенты с подтвержденным прогрессиро-ванием заболевания после аллоТГСК составили 22,2% (n=6); пациенты с ПО, но c рецидивом или прогрессированием далее – 25,9% (n=7); пациенты с первым ответом хуже чем ПО (ЧО/СЗ) составили 51,8% (n=14), включая 7 пациентов c неподтвержденным 1-м статусом таким как ЧО/СЗ, основываясь на статусе заболевания перед аллоТКМ, при этом ПО и ПЗ также не подтверждены. При первом стадировании после алло-ТГСК у 7 пациентов зафиксирован ПО (25,0%), ЧО отмечен у 10 пациентов (37,0%), таким образом у 17 (62,9%) пациентов был общий ответ. За период наблюдения у 20 пациентов (74,0%) из 27 зафиксированы прогрессирование или рецидив ЛХ после аллоТКМ. 19 пациентов получили лечение: 6 пациентов получили только химиотерапию (х/т) после аллоТКМ (ChVPP, LABO, винбластин); 13 пациентов получили терапию новыми моноклональными антителами (МА): брентуксимаб ведотин (BV) и ниволумаб (Nivo), или сочетание их с химиотерапией. Остальные 8 пациентов были оставлены без терапии: 3 пациента (ЧО, СЗ, ПЗ) из-за осложнений алло-ТГСК и плохого соматического статуса; 5 пациентов из группы неподтвержденного статуса (ЧО-4, СЗ-1) – под динамическим наблюдением. 13 пациентов (48,1%). Терапию BV-содержащими схемами в качестве первой линии МА-терапии получили все 13 пациентов. 7 из них (53,8%; 25,9%) из-за продолжающегося прогрессирования ЛХ переведены на вторую линию терапии МА ниволумабом. До начала терапии MA (BV) 5 из 13 пациентов получили ХТ, и 4 пациента из 13 получили инфузии донорских лимфоцитов (ИЛД). Характеристики пациентов и методов представлены в таблице №1. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> На момент анализа время наблюдения за всеми пациентами (n=27) было 27 (1,4-3,7) мес. Для пациентов только с х/т (n=6) время наблюдения 25 (6,27-51) мес.; для 13 пациентов с МА-терапией – 45 мес. (23-73). Медиана наблюдения за пациентами без терапии (n=8) 11 мес. (1,47-39,37). Общая выживаемость для всех пациентов на момент анализа была 55% (n=15). Время от трансплантации до ПЗ/РЗ было 3,6 мес. (1,3-11,3 мес.). Среднее время от алло-ТГСК до начала терапии BV по поводу ПЗ/РЗ было 4,7 мес. (1,7-44 мес.). Среднее время от алло-ТГСК до начала терапии Nivo было 38,7 мес. (14,5-44,5). Среднее время между окончанием терапии BV и началом терапии Nivo было 2,83 (1,23-32,47) месяцев. На момент анализа 12 пациентов (44,4%) из 27 умерли: 6 из-за прогрессирования ЛХ и 6 пациентов из-за тяжелой хронической РТПХ (хрРТПХ) и инфекционных осложнений в посттрансплантационном периоде, включая 3 пациентов с МА-терапией и 1 пациента под динамическим наблюдением. 15 пациентов живы: у 4х пациентов в процессе наблюдения зафиксирован ПО; 6 пациентов в ПО после МА-терапии (5) и после ХТ (1); 5 пациентов продолжают лечение из-за стабилизации ли прогрессирования ЛХ. При сравнении результатов ХТ и терапии МА, прогностическим значением облада- ло лечение МА (76,9% против 16,7%, p=.003), также развитие хрРТПХ имело прогностическое значение (72,7% против 43,9%, p=.084). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> На небольшом клиническом материале было показано, что треть пациентов погибают от прогрессирования ЛХ и почти столько же от осложнений терапии. Несмотря на относительно благоприятный прогноз в этой тяжелой группе пациентов, требуются дальнейшие исследования для выбора оптимальной терапии посттрансплантационного рецидива и прогрессирования ЛХ. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфома Ходжкина, аллогенная трансплантация костного мозга, брентуксимаб ведотин, ниволумаб. </p> <h2 style="text-align: justify;"> Таблица 1. Характеристики пациентов и методы терапии (продолжение)<br> </h2> <p style="text-align: justify;"> <img width="780" alt="таблица 1 часть.png" src="/upload/medialibrary/94c/tablitsa-1-chast.png" height="407" title="таблица 1 часть.png"><br> </p> <p style="text-align: justify;"> <img width="781" alt="таблица 2 часть.png" src="/upload/medialibrary/664/tablitsa-2-chast.png" height="303" title="таблица 2 часть.png"><br> </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7923) "
Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) имеет высокий потенциал излечения классической лимфомы Ходжкина (ЛХ) у пациентов с рефрактерным или рецидивирующим течением (р/рЛХ). Тем не менее, опубликованных данных о терапии рецидива или прогрессирования ЛХ после алло-ТГСК крайне мало. В одноцентровом исследовании была проведена попытка выявить прогностические факторы в лечение подобных пациентов.
Пациенты и методы
В этот ретроспективный анализ включены пациенты (n=27), прошедшие аллоТКМ в нашей клинике с 2002 по 2017 гг. Пациенты с подтвержденным прогрессиро-ванием заболевания после аллоТГСК составили 22,2% (n=6); пациенты с ПО, но c рецидивом или прогрессированием далее – 25,9% (n=7); пациенты с первым ответом хуже чем ПО (ЧО/СЗ) составили 51,8% (n=14), включая 7 пациентов c неподтвержденным 1-м статусом таким как ЧО/СЗ, основываясь на статусе заболевания перед аллоТКМ, при этом ПО и ПЗ также не подтверждены. При первом стадировании после алло-ТГСК у 7 пациентов зафиксирован ПО (25,0%), ЧО отмечен у 10 пациентов (37,0%), таким образом у 17 (62,9%) пациентов был общий ответ. За период наблюдения у 20 пациентов (74,0%) из 27 зафиксированы прогрессирование или рецидив ЛХ после аллоТКМ. 19 пациентов получили лечение: 6 пациентов получили только химиотерапию (х/т) после аллоТКМ (ChVPP, LABO, винбластин); 13 пациентов получили терапию новыми моноклональными антителами (МА): брентуксимаб ведотин (BV) и ниволумаб (Nivo), или сочетание их с химиотерапией. Остальные 8 пациентов были оставлены без терапии: 3 пациента (ЧО, СЗ, ПЗ) из-за осложнений алло-ТГСК и плохого соматического статуса; 5 пациентов из группы неподтвержденного статуса (ЧО-4, СЗ-1) – под динамическим наблюдением. 13 пациентов (48,1%). Терапию BV-содержащими схемами в качестве первой линии МА-терапии получили все 13 пациентов. 7 из них (53,8%; 25,9%) из-за продолжающегося прогрессирования ЛХ переведены на вторую линию терапии МА ниволумабом. До начала терапии MA (BV) 5 из 13 пациентов получили ХТ, и 4 пациента из 13 получили инфузии донорских лимфоцитов (ИЛД). Характеристики пациентов и методов представлены в таблице №1.
Результаты
На момент анализа время наблюдения за всеми пациентами (n=27) было 27 (1,4-3,7) мес. Для пациентов только с х/т (n=6) время наблюдения 25 (6,27-51) мес.; для 13 пациентов с МА-терапией – 45 мес. (23-73). Медиана наблюдения за пациентами без терапии (n=8) 11 мес. (1,47-39,37). Общая выживаемость для всех пациентов на момент анализа была 55% (n=15). Время от трансплантации до ПЗ/РЗ было 3,6 мес. (1,3-11,3 мес.). Среднее время от алло-ТГСК до начала терапии BV по поводу ПЗ/РЗ было 4,7 мес. (1,7-44 мес.). Среднее время от алло-ТГСК до начала терапии Nivo было 38,7 мес. (14,5-44,5). Среднее время между окончанием терапии BV и началом терапии Nivo было 2,83 (1,23-32,47) месяцев. На момент анализа 12 пациентов (44,4%) из 27 умерли: 6 из-за прогрессирования ЛХ и 6 пациентов из-за тяжелой хронической РТПХ (хрРТПХ) и инфекционных осложнений в посттрансплантационном периоде, включая 3 пациентов с МА-терапией и 1 пациента под динамическим наблюдением. 15 пациентов живы: у 4х пациентов в процессе наблюдения зафиксирован ПО; 6 пациентов в ПО после МА-терапии (5) и после ХТ (1); 5 пациентов продолжают лечение из-за стабилизации ли прогрессирования ЛХ. При сравнении результатов ХТ и терапии МА, прогностическим значением облада- ло лечение МА (76,9% против 16,7%, p=.003), также развитие хрРТПХ имело прогностическое значение (72,7% против 43,9%, p=.084).
Выводы
На небольшом клиническом материале было показано, что треть пациентов погибают от прогрессирования ЛХ и почти столько же от осложнений терапии. Несмотря на относительно благоприятный прогноз в этой тяжелой группе пациентов, требуются дальнейшие исследования для выбора оптимальной терапии посттрансплантационного рецидива и прогрессирования ЛХ.
Ключевые слова
Лимфома Ходжкина, аллогенная трансплантация костного мозга, брентуксимаб ведотин, ниволумаб.
Таблица 1. Характеристики пациентов и методы терапии (продолжение)


Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) имеет высокий потенциал излечения классической лимфомы Ходжкина (ЛХ) у пациентов с рефрактерным или рецидивирующим течением (р/рЛХ). Тем не менее, опубликованных данных о терапии рецидива или прогрессирования ЛХ после алло-ТГСК крайне мало. В одноцентровом исследовании была проведена попытка выявить прогностические факторы в лечение подобных пациентов.
Пациенты и методы
В этот ретроспективный анализ включены пациенты (n=27), прошедшие аллоТКМ в нашей клинике с 2002 по 2017 гг. Пациенты с подтвержденным прогрессиро-ванием заболевания после аллоТГСК составили 22,2% (n=6); пациенты с ПО, но c рецидивом или прогрессированием далее – 25,9% (n=7); пациенты с первым ответом хуже чем ПО (ЧО/СЗ) составили 51,8% (n=14), включая 7 пациентов c неподтвержденным 1-м статусом таким как ЧО/СЗ, основываясь на статусе заболевания перед аллоТКМ, при этом ПО и ПЗ также не подтверждены. При первом стадировании после алло-ТГСК у 7 пациентов зафиксирован ПО (25,0%), ЧО отмечен у 10 пациентов (37,0%), таким образом у 17 (62,9%) пациентов был общий ответ. За период наблюдения у 20 пациентов (74,0%) из 27 зафиксированы прогрессирование или рецидив ЛХ после аллоТКМ. 19 пациентов получили лечение: 6 пациентов получили только химиотерапию (х/т) после аллоТКМ (ChVPP, LABO, винбластин); 13 пациентов получили терапию новыми моноклональными антителами (МА): брентуксимаб ведотин (BV) и ниволумаб (Nivo), или сочетание их с химиотерапией. Остальные 8 пациентов были оставлены без терапии: 3 пациента (ЧО, СЗ, ПЗ) из-за осложнений алло-ТГСК и плохого соматического статуса; 5 пациентов из группы неподтвержденного статуса (ЧО-4, СЗ-1) – под динамическим наблюдением. 13 пациентов (48,1%). Терапию BV-содержащими схемами в качестве первой линии МА-терапии получили все 13 пациентов. 7 из них (53,8%; 25,9%) из-за продолжающегося прогрессирования ЛХ переведены на вторую линию терапии МА ниволумабом. До начала терапии MA (BV) 5 из 13 пациентов получили ХТ, и 4 пациента из 13 получили инфузии донорских лимфоцитов (ИЛД). Характеристики пациентов и методов представлены в таблице №1.
Результаты
На момент анализа время наблюдения за всеми пациентами (n=27) было 27 (1,4-3,7) мес. Для пациентов только с х/т (n=6) время наблюдения 25 (6,27-51) мес.; для 13 пациентов с МА-терапией – 45 мес. (23-73). Медиана наблюдения за пациентами без терапии (n=8) 11 мес. (1,47-39,37). Общая выживаемость для всех пациентов на момент анализа была 55% (n=15). Время от трансплантации до ПЗ/РЗ было 3,6 мес. (1,3-11,3 мес.). Среднее время от алло-ТГСК до начала терапии BV по поводу ПЗ/РЗ было 4,7 мес. (1,7-44 мес.). Среднее время от алло-ТГСК до начала терапии Nivo было 38,7 мес. (14,5-44,5). Среднее время между окончанием терапии BV и началом терапии Nivo было 2,83 (1,23-32,47) месяцев. На момент анализа 12 пациентов (44,4%) из 27 умерли: 6 из-за прогрессирования ЛХ и 6 пациентов из-за тяжелой хронической РТПХ (хрРТПХ) и инфекционных осложнений в посттрансплантационном периоде, включая 3 пациентов с МА-терапией и 1 пациента под динамическим наблюдением. 15 пациентов живы: у 4х пациентов в процессе наблюдения зафиксирован ПО; 6 пациентов в ПО после МА-терапии (5) и после ХТ (1); 5 пациентов продолжают лечение из-за стабилизации ли прогрессирования ЛХ. При сравнении результатов ХТ и терапии МА, прогностическим значением облада- ло лечение МА (76,9% против 16,7%, p=.003), также развитие хрРТПХ имело прогностическое значение (72,7% против 43,9%, p=.084).
Выводы
На небольшом клиническом материале было показано, что треть пациентов погибают от прогрессирования ЛХ и почти столько же от осложнений терапии. Несмотря на относительно благоприятный прогноз в этой тяжелой группе пациентов, требуются дальнейшие исследования для выбора оптимальной терапии посттрансплантационного рецидива и прогрессирования ЛХ.
Ключевые слова
Лимфома Ходжкина, аллогенная трансплантация костного мозга, брентуксимаб ведотин, ниволумаб.
Таблица 1. Характеристики пациентов и методы терапии (продолжение)


" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(352) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
" } } } [21]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1560" ["~ID"]=> string(4) "1560" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(194) "Влияние циклофосфамида на длительность госпитализации у пациентов с острыми лейкозами в полной ремиссии" ["~NAME"]=> string(194) "Влияние циклофосфамида на длительность госпитализации у пациентов с острыми лейкозами в полной ремиссии" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:28:31" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:28:31" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vliyanie-tsiklofosfamida-na-dlitelnost-gospitalizatsii-u-patsientov-s-ostrymi-leykozami-v-polnoy-rem/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vliyanie-tsiklofosfamida-na-dlitelnost-gospitalizatsii-u-patsientov-s-ostrymi-leykozami-v-polnoy-rem/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "vliyanie-tsiklofosfamida-na-dlitelnost-gospitalizatsii-u-patsientov-s-ostrymi-leykozami-v-polnoy-rem" ["~CODE"]=> string(100) "vliyanie-tsiklofosfamida-na-dlitelnost-gospitalizatsii-u-patsientov-s-ostrymi-leykozami-v-polnoy-rem" ["EXTERNAL_ID"]=> string(4) "1560" ["~EXTERNAL_ID"]=> string(4) "1560" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(194) "Влияние циклофосфамида на длительность госпитализации у пациентов с острыми лейкозами в полной ремиссии" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(344) "Влияние циклофосфамида на длительность госпитализации у пациентов с острыми лейкозами в полной ремиссииImpact of using posttransplant high-dose cyclophosphamide (PT-CY) on the length of hospital stay in patients with acute leukemia in complete remission" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(4565) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Использование высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) является одной из наиболее актуальных методик профилактики РТПХ при выполнении трансплантации аллогенных гемопоэтических стволовых клеток крови (алло-ТГСК). Однако, влияние дополнительного введения ПТ-ЦФ на такой важный клинико-экономический параметр, как длительность пребывания в стационаре, и, соответственно, стоимость трансплантации остается не изученным. Здесь мы представляем анализ влияния введения высоких доз циклофосфамида с целью профилактики РТПХ после алло-ТГСК крови от неродственного донора на длительность госпитализации, связанной с проведением алло-ТГСК. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В исследование были включены больные в ремиссии острого лейкоза, которым была выполнена первая трансплантация алло-ТГСК от неродственного полностью совместимого или частично совместимого донора. Все больные на момент анализа были выписаны из стационара без признаков РТПХ и отторжения в течение всей госпитализации. Всего в исследование было включено 39 больных. Всем пациентам в качестве профилактики РТПХ был использован режим: антитимоцитарный глобулин (АТГ) 40 мг/кг (-4 по -1 день); циклоспорин А 3 мг/кг/сут (с +5 дня); микофенолата мофетил 3000 мг/сут (с +5 дня). При использовании в качестве источника трансплантата неродственного частично совместимого донора пациентам также вводился ПТ-ЦФ в дозе 50 мг/кг на +3, +4 день. Детальные характеристики представлены в таблице 1 (см. выше). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Данные по длительности госпитализации представлены на Рисунке 1 (см. выше). Согласно проведенному анализу, длительность госпитализации у пациентов в ремиссии острого лейкоза, которым была выполнена трансплантация алло-ТГСК с использованием ПТ-ЦФ и без ПТ-ЦФ составила 43 дня (14-126) и 48 дней (32-98) соответственно (p=0,48). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Таким образом, использование циклофосфамида на + 3, + 4 день с целью профилактики РТПХ не удлиняет период госпитализации при проведении алло-ТГСК у пациентов в ремиссии острого лейкоза. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация аллогенного костного мозга, иммуносупрессивная терапия, циклофосфамид, длительность госпитализации, неродственный донор. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(194) "Влияние циклофосфамида на длительность госпитализации у пациентов с острыми лейкозами в полной ремиссии" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(194) "Влияние циклофосфамида на длительность госпитализации у пациентов с острыми лейкозами в полной ремиссии" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(194) "Влияние циклофосфамида на длительность госпитализации у пациентов с острыми лейкозами в полной ремиссии" ["SECTION_META_TITLE"]=> string(194) "Влияние циклофосфамида на длительность госпитализации у пациентов с острыми лейкозами в полной ремиссии" ["SECTION_META_KEYWORDS"]=> string(194) "Влияние циклофосфамида на длительность госпитализации у пациентов с острыми лейкозами в полной ремиссии" ["SECTION_META_DESCRIPTION"]=> string(194) "Влияние циклофосфамида на длительность госпитализации у пациентов с острыми лейкозами в полной ремиссии" ["SECTION_PICTURE_FILE_ALT"]=> string(194) "Влияние циклофосфамида на длительность госпитализации у пациентов с острыми лейкозами в полной ремиссии" ["SECTION_PICTURE_FILE_TITLE"]=> string(194) "Влияние циклофосфамида на длительность госпитализации у пациентов с острыми лейкозами в полной ремиссии" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "vliyanie-tsiklofosfamida-na-dlitelnost-gospitalizatsii-u-patsientov-s-ostrymi-leykozami-v-polnoy-rem" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(194) "Влияние циклофосфамида на длительность госпитализации у пациентов с острыми лейкозами в полной ремиссии" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(194) "Влияние циклофосфамида на длительность госпитализации у пациентов с острыми лейкозами в полной ремиссии" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vliyanie-tsiklofosfamida-na-dlitelnost-gospitalizatsii-u-patsientov-s-ostrymi-leykozami-v-polnoy-rem" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "vliyanie-tsiklofosfamida-na-dlitelnost-gospitalizatsii-u-patsientov-s-ostrymi-leykozami-v-polnoy-rem" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vliyanie-tsiklofosfamida-na-dlitelnost-gospitalizatsii-u-patsientov-s-ostrymi-leykozami-v-polnoy-rem" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20373" ["VALUE"]=> array(2) { ["TEXT"]=> string(443) "Анна А. Дмитрова, Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Дарья С. Дубняк, Вера А. Васильева, Ольга М. Королева, Зоя В. Конова, Анна А. Сидорова, Екатерина В. Усикова, Елена Н. Паровичникова, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(443) "Анна А. Дмитрова, Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Дарья С. Дубняк, Вера А. Васильева, Ольга М. Королева, Зоя В. Конова, Анна А. Сидорова, Екатерина В. Усикова, Елена Н. Паровичникова, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20374" ["VALUE"]=> array(2) { ["TEXT"]=> string(234) "Отделение высокодозной химиотерапии и трансплантации костного мозга, ФГБУ «НМИЦ гематологии» МЗ РФ,<br> Москва, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(222) "Отделение высокодозной химиотерапии и трансплантации костного мозга, ФГБУ «НМИЦ гематологии» МЗ РФ,
Москва, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20375" ["VALUE"]=> array(2) { ["TEXT"]=> string(4565) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Использование высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) является одной из наиболее актуальных методик профилактики РТПХ при выполнении трансплантации аллогенных гемопоэтических стволовых клеток крови (алло-ТГСК). Однако, влияние дополнительного введения ПТ-ЦФ на такой важный клинико-экономический параметр, как длительность пребывания в стационаре, и, соответственно, стоимость трансплантации остается не изученным. Здесь мы представляем анализ влияния введения высоких доз циклофосфамида с целью профилактики РТПХ после алло-ТГСК крови от неродственного донора на длительность госпитализации, связанной с проведением алло-ТГСК. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В исследование были включены больные в ремиссии острого лейкоза, которым была выполнена первая трансплантация алло-ТГСК от неродственного полностью совместимого или частично совместимого донора. Все больные на момент анализа были выписаны из стационара без признаков РТПХ и отторжения в течение всей госпитализации. Всего в исследование было включено 39 больных. Всем пациентам в качестве профилактики РТПХ был использован режим: антитимоцитарный глобулин (АТГ) 40 мг/кг (-4 по -1 день); циклоспорин А 3 мг/кг/сут (с +5 дня); микофенолата мофетил 3000 мг/сут (с +5 дня). При использовании в качестве источника трансплантата неродственного частично совместимого донора пациентам также вводился ПТ-ЦФ в дозе 50 мг/кг на +3, +4 день. Детальные характеристики представлены в таблице 1 (см. выше). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Данные по длительности госпитализации представлены на Рисунке 1 (см. выше). Согласно проведенному анализу, длительность госпитализации у пациентов в ремиссии острого лейкоза, которым была выполнена трансплантация алло-ТГСК с использованием ПТ-ЦФ и без ПТ-ЦФ составила 43 дня (14-126) и 48 дней (32-98) соответственно (p=0,48). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Таким образом, использование циклофосфамида на + 3, + 4 день с целью профилактики РТПХ не удлиняет период госпитализации при проведении алло-ТГСК у пациентов в ремиссии острого лейкоза. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация аллогенного костного мозга, иммуносупрессивная терапия, циклофосфамид, длительность госпитализации, неродственный донор. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4333) "
Введение
Использование высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) является одной из наиболее актуальных методик профилактики РТПХ при выполнении трансплантации аллогенных гемопоэтических стволовых клеток крови (алло-ТГСК). Однако, влияние дополнительного введения ПТ-ЦФ на такой важный клинико-экономический параметр, как длительность пребывания в стационаре, и, соответственно, стоимость трансплантации остается не изученным. Здесь мы представляем анализ влияния введения высоких доз циклофосфамида с целью профилактики РТПХ после алло-ТГСК крови от неродственного донора на длительность госпитализации, связанной с проведением алло-ТГСК.
Пациенты и методы
В исследование были включены больные в ремиссии острого лейкоза, которым была выполнена первая трансплантация алло-ТГСК от неродственного полностью совместимого или частично совместимого донора. Все больные на момент анализа были выписаны из стационара без признаков РТПХ и отторжения в течение всей госпитализации. Всего в исследование было включено 39 больных. Всем пациентам в качестве профилактики РТПХ был использован режим: антитимоцитарный глобулин (АТГ) 40 мг/кг (-4 по -1 день); циклоспорин А 3 мг/кг/сут (с +5 дня); микофенолата мофетил 3000 мг/сут (с +5 дня). При использовании в качестве источника трансплантата неродственного частично совместимого донора пациентам также вводился ПТ-ЦФ в дозе 50 мг/кг на +3, +4 день. Детальные характеристики представлены в таблице 1 (см. выше).
Результаты
Данные по длительности госпитализации представлены на Рисунке 1 (см. выше). Согласно проведенному анализу, длительность госпитализации у пациентов в ремиссии острого лейкоза, которым была выполнена трансплантация алло-ТГСК с использованием ПТ-ЦФ и без ПТ-ЦФ составила 43 дня (14-126) и 48 дней (32-98) соответственно (p=0,48).
Заключение
Таким образом, использование циклофосфамида на + 3, + 4 день с целью профилактики РТПХ не удлиняет период госпитализации при проведении алло-ТГСК у пациентов в ремиссии острого лейкоза.
Ключевые слова
Трансплантация аллогенного костного мозга, иммуносупрессивная терапия, циклофосфамид, длительность госпитализации, неродственный донор.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20376" ["VALUE"]=> array(2) { ["TEXT"]=> string(257) "Anna A. Dmitrova, Mikhail Yu. Drokov, Larisa A. Kuzmina, Natalia N. Popova, Ekaterina D. Mikhaltsova, Darya S. Dubnyak, Vera A. Vasilyeva, Olga M. Koroleva, Zoya V. Konova, Anna A. Sidorova, Ekaterina V. Usikova, Elena N. Parovichnikova, Valery G. Savchenko" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(257) "Anna A. Dmitrova, Mikhail Yu. Drokov, Larisa A. Kuzmina, Natalia N. Popova, Ekaterina D. Mikhaltsova, Darya S. Dubnyak, Vera A. Vasilyeva, Olga M. Koroleva, Zoya V. Konova, Anna A. Sidorova, Ekaterina V. Usikova, Elena N. Parovichnikova, Valery G. Savchenko" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20377" ["VALUE"]=> array(2) { ["TEXT"]=> string(173) "Department of High-Dose Chemotherapy and BMT, National Research Center for Hematology, Ministry of Healthcare of the Russian Federation, Moscow, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(167) "Department of High-Dose Chemotherapy and BMT, National Research Center for Hematology, Ministry of Healthcare of the Russian Federation, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20464" ["VALUE"]=> array(2) { ["TEXT"]=> string(3411) "<h2>Introduction</h2> <p style="text-align: justify;"> Using posttransplant high-dose cyclophosphamide (PT-CY) as the graft versus host disease (GvHD) prophylaxis is an important option to prevent the GvHD in patients after allogeneic hematopoietic stem cell transplantation (allo-HCT) with a “high-grade” HLA-disparity (unrelated, haploidentical donor). However, the influence of PT-CY on the length ofhospital stay and the cost of hospitalization still remains unknown. Here we report data about impact of PT-CY on the length of hospital stay in leukemia patients after allo-HSCT from unrelated donor. </p> <p style="text-align: justify;"> <img width="385" alt="11_Figure 1. The duration of hospitalization.png" src="/upload/medialibrary/f83/11_figure-1.-the-duration-of-hospitalization.png" height="265" title="11_Figure 1. The duration of hospitalization.png"><br> </p> <p style="text-align: justify;"> Figure 1. The duration of hospitalization for the patients in complete remission of acute leukemia, who underwent allo-HSCT from unrelated donors using PT-CY and without using PT-CY </p> <h2 style="text-align: justify;"> Patients and methods </h2> <p style="text-align: justify;"> We included 39 patients in the complete remission of acute leukemia, whom allo-HSCT was performed from unrelated or mismatched unrelated donors. At the time of analysis, all patients were discharged from the hospital without any signs of GvHD or graft failure. Detailed characteristics of patients are presented in Table 1. To prevent the GvHD all patients recieve: anti-thymocyte globulin (ATG) 40 mg/kg (on days -4 to -1), cyclosporine A (CSA) 3 mg/kg/day (from +5 day), mycophenolate mofetil (MMF) 3000 mg/day (from + 5 day). After performing allo-HSCT from mismatched unrelated donor, the patients were also treated with PT-CY (50 mg/kg on +3, +4 day). </p> <h2 style="text-align: justify;"> Results </h2> <p style="text-align: justify;"> Length of hospital stay for all patients is presented in Figure 1. According to our analysis, length of hospital stay in patients after allo-HSCT with and without PT-CY was 43 days (14 to 126) versus 48 days (32 to 98) accordingly (p=0.48). </p> <h2 style="text-align: justify;"> Conclusion </h2> <p style="text-align: justify;"> Usage of PT-CY on day +3, +4 in prevention of GVHD does not extend the hospitalization period in leukemia patients transplanted in complete remission. </p> <h2 style="text-align: justify;"> Keywords </h2> <p style="text-align: justify;"> Allogeneic bone marrow transplantation, immunosuppressive therapy, posttransplant high-dose cyclophosphamide, hospital stay, unrelated donor. </p> <h2 style="text-align: justify;"> Table 1. Characteristics of the patients<br> </h2> <img width="783" alt="11_Table 1. Characteristics of the patients.png" src="/upload/medialibrary/67d/11_table-1.-characteristics-of-the-patients.png" height="363" title="11_Table 1. Characteristics of the patients.png"><br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3005) "
Introduction
Using posttransplant high-dose cyclophosphamide (PT-CY) as the graft versus host disease (GvHD) prophylaxis is an important option to prevent the GvHD in patients after allogeneic hematopoietic stem cell transplantation (allo-HCT) with a “high-grade” HLA-disparity (unrelated, haploidentical donor). However, the influence of PT-CY on the length ofhospital stay and the cost of hospitalization still remains unknown. Here we report data about impact of PT-CY on the length of hospital stay in leukemia patients after allo-HSCT from unrelated donor.

Figure 1. The duration of hospitalization for the patients in complete remission of acute leukemia, who underwent allo-HSCT from unrelated donors using PT-CY and without using PT-CY
Patients and methods
We included 39 patients in the complete remission of acute leukemia, whom allo-HSCT was performed from unrelated or mismatched unrelated donors. At the time of analysis, all patients were discharged from the hospital without any signs of GvHD or graft failure. Detailed characteristics of patients are presented in Table 1. To prevent the GvHD all patients recieve: anti-thymocyte globulin (ATG) 40 mg/kg (on days -4 to -1), cyclosporine A (CSA) 3 mg/kg/day (from +5 day), mycophenolate mofetil (MMF) 3000 mg/day (from + 5 day). After performing allo-HSCT from mismatched unrelated donor, the patients were also treated with PT-CY (50 mg/kg on +3, +4 day).
Results
Length of hospital stay for all patients is presented in Figure 1. According to our analysis, length of hospital stay in patients after allo-HSCT with and without PT-CY was 43 days (14 to 126) versus 48 days (32 to 98) accordingly (p=0.48).
Conclusion
Usage of PT-CY on day +3, +4 in prevention of GVHD does not extend the hospitalization period in leukemia patients transplanted in complete remission.
Keywords
Allogeneic bone marrow transplantation, immunosuppressive therapy, posttransplant high-dose cyclophosphamide, hospital stay, unrelated donor.
Table 1. Characteristics of the patients

" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20378" ["VALUE"]=> string(150) "Impact of using posttransplant high-dose cyclophosphamide (PT-CY) on the length of hospital stay in patients with acute leukemia in complete remission" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(150) "Impact of using posttransplant high-dose cyclophosphamide (PT-CY) on the length of hospital stay in patients with acute leukemia in complete remission" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20753" ["VALUE"]=> string(4) "1389" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1389" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20754" ["VALUE"]=> string(4) "1390" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1390" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20376" ["VALUE"]=> array(2) { ["TEXT"]=> string(257) "Anna A. Dmitrova, Mikhail Yu. Drokov, Larisa A. Kuzmina, Natalia N. Popova, Ekaterina D. Mikhaltsova, Darya S. Dubnyak, Vera A. Vasilyeva, Olga M. Koroleva, Zoya V. Konova, Anna A. Sidorova, Ekaterina V. Usikova, Elena N. Parovichnikova, Valery G. Savchenko" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(257) "Anna A. Dmitrova, Mikhail Yu. Drokov, Larisa A. Kuzmina, Natalia N. Popova, Ekaterina D. Mikhaltsova, Darya S. Dubnyak, Vera A. Vasilyeva, Olga M. Koroleva, Zoya V. Konova, Anna A. Sidorova, Ekaterina V. Usikova, Elena N. Parovichnikova, Valery G. Savchenko" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(257) "Anna A. Dmitrova, Mikhail Yu. Drokov, Larisa A. Kuzmina, Natalia N. Popova, Ekaterina D. Mikhaltsova, Darya S. Dubnyak, Vera A. Vasilyeva, Olga M. Koroleva, Zoya V. Konova, Anna A. Sidorova, Ekaterina V. Usikova, Elena N. Parovichnikova, Valery G. Savchenko" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20464" ["VALUE"]=> array(2) { ["TEXT"]=> string(3411) "<h2>Introduction</h2> <p style="text-align: justify;"> Using posttransplant high-dose cyclophosphamide (PT-CY) as the graft versus host disease (GvHD) prophylaxis is an important option to prevent the GvHD in patients after allogeneic hematopoietic stem cell transplantation (allo-HCT) with a “high-grade” HLA-disparity (unrelated, haploidentical donor). However, the influence of PT-CY on the length ofhospital stay and the cost of hospitalization still remains unknown. Here we report data about impact of PT-CY on the length of hospital stay in leukemia patients after allo-HSCT from unrelated donor. </p> <p style="text-align: justify;"> <img width="385" alt="11_Figure 1. The duration of hospitalization.png" src="/upload/medialibrary/f83/11_figure-1.-the-duration-of-hospitalization.png" height="265" title="11_Figure 1. The duration of hospitalization.png"><br> </p> <p style="text-align: justify;"> Figure 1. The duration of hospitalization for the patients in complete remission of acute leukemia, who underwent allo-HSCT from unrelated donors using PT-CY and without using PT-CY </p> <h2 style="text-align: justify;"> Patients and methods </h2> <p style="text-align: justify;"> We included 39 patients in the complete remission of acute leukemia, whom allo-HSCT was performed from unrelated or mismatched unrelated donors. At the time of analysis, all patients were discharged from the hospital without any signs of GvHD or graft failure. Detailed characteristics of patients are presented in Table 1. To prevent the GvHD all patients recieve: anti-thymocyte globulin (ATG) 40 mg/kg (on days -4 to -1), cyclosporine A (CSA) 3 mg/kg/day (from +5 day), mycophenolate mofetil (MMF) 3000 mg/day (from + 5 day). After performing allo-HSCT from mismatched unrelated donor, the patients were also treated with PT-CY (50 mg/kg on +3, +4 day). </p> <h2 style="text-align: justify;"> Results </h2> <p style="text-align: justify;"> Length of hospital stay for all patients is presented in Figure 1. According to our analysis, length of hospital stay in patients after allo-HSCT with and without PT-CY was 43 days (14 to 126) versus 48 days (32 to 98) accordingly (p=0.48). </p> <h2 style="text-align: justify;"> Conclusion </h2> <p style="text-align: justify;"> Usage of PT-CY on day +3, +4 in prevention of GVHD does not extend the hospitalization period in leukemia patients transplanted in complete remission. </p> <h2 style="text-align: justify;"> Keywords </h2> <p style="text-align: justify;"> Allogeneic bone marrow transplantation, immunosuppressive therapy, posttransplant high-dose cyclophosphamide, hospital stay, unrelated donor. </p> <h2 style="text-align: justify;"> Table 1. Characteristics of the patients<br> </h2> <img width="783" alt="11_Table 1. Characteristics of the patients.png" src="/upload/medialibrary/67d/11_table-1.-characteristics-of-the-patients.png" height="363" title="11_Table 1. Characteristics of the patients.png"><br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3005) "
Introduction
Using posttransplant high-dose cyclophosphamide (PT-CY) as the graft versus host disease (GvHD) prophylaxis is an important option to prevent the GvHD in patients after allogeneic hematopoietic stem cell transplantation (allo-HCT) with a “high-grade” HLA-disparity (unrelated, haploidentical donor). However, the influence of PT-CY on the length ofhospital stay and the cost of hospitalization still remains unknown. Here we report data about impact of PT-CY on the length of hospital stay in leukemia patients after allo-HSCT from unrelated donor.

Figure 1. The duration of hospitalization for the patients in complete remission of acute leukemia, who underwent allo-HSCT from unrelated donors using PT-CY and without using PT-CY
Patients and methods
We included 39 patients in the complete remission of acute leukemia, whom allo-HSCT was performed from unrelated or mismatched unrelated donors. At the time of analysis, all patients were discharged from the hospital without any signs of GvHD or graft failure. Detailed characteristics of patients are presented in Table 1. To prevent the GvHD all patients recieve: anti-thymocyte globulin (ATG) 40 mg/kg (on days -4 to -1), cyclosporine A (CSA) 3 mg/kg/day (from +5 day), mycophenolate mofetil (MMF) 3000 mg/day (from + 5 day). After performing allo-HSCT from mismatched unrelated donor, the patients were also treated with PT-CY (50 mg/kg on +3, +4 day).
Results
Length of hospital stay for all patients is presented in Figure 1. According to our analysis, length of hospital stay in patients after allo-HSCT with and without PT-CY was 43 days (14 to 126) versus 48 days (32 to 98) accordingly (p=0.48).
Conclusion
Usage of PT-CY on day +3, +4 in prevention of GVHD does not extend the hospitalization period in leukemia patients transplanted in complete remission.
Keywords
Allogeneic bone marrow transplantation, immunosuppressive therapy, posttransplant high-dose cyclophosphamide, hospital stay, unrelated donor.
Table 1. Characteristics of the patients

" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3005) "
Introduction
Using posttransplant high-dose cyclophosphamide (PT-CY) as the graft versus host disease (GvHD) prophylaxis is an important option to prevent the GvHD in patients after allogeneic hematopoietic stem cell transplantation (allo-HCT) with a “high-grade” HLA-disparity (unrelated, haploidentical donor). However, the influence of PT-CY on the length ofhospital stay and the cost of hospitalization still remains unknown. Here we report data about impact of PT-CY on the length of hospital stay in leukemia patients after allo-HSCT from unrelated donor.

Figure 1. The duration of hospitalization for the patients in complete remission of acute leukemia, who underwent allo-HSCT from unrelated donors using PT-CY and without using PT-CY
Patients and methods
We included 39 patients in the complete remission of acute leukemia, whom allo-HSCT was performed from unrelated or mismatched unrelated donors. At the time of analysis, all patients were discharged from the hospital without any signs of GvHD or graft failure. Detailed characteristics of patients are presented in Table 1. To prevent the GvHD all patients recieve: anti-thymocyte globulin (ATG) 40 mg/kg (on days -4 to -1), cyclosporine A (CSA) 3 mg/kg/day (from +5 day), mycophenolate mofetil (MMF) 3000 mg/day (from + 5 day). After performing allo-HSCT from mismatched unrelated donor, the patients were also treated with PT-CY (50 mg/kg on +3, +4 day).
Results
Length of hospital stay for all patients is presented in Figure 1. According to our analysis, length of hospital stay in patients after allo-HSCT with and without PT-CY was 43 days (14 to 126) versus 48 days (32 to 98) accordingly (p=0.48).
Conclusion
Usage of PT-CY on day +3, +4 in prevention of GVHD does not extend the hospitalization period in leukemia patients transplanted in complete remission.
Keywords
Allogeneic bone marrow transplantation, immunosuppressive therapy, posttransplant high-dose cyclophosphamide, hospital stay, unrelated donor.
Table 1. Characteristics of the patients

" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20378" ["VALUE"]=> string(150) "Impact of using posttransplant high-dose cyclophosphamide (PT-CY) on the length of hospital stay in patients with acute leukemia in complete remission" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(150) "Impact of using posttransplant high-dose cyclophosphamide (PT-CY) on the length of hospital stay in patients with acute leukemia in complete remission" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(150) "Impact of using posttransplant high-dose cyclophosphamide (PT-CY) on the length of hospital stay in patients with acute leukemia in complete remission" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20377" ["VALUE"]=> array(2) { ["TEXT"]=> string(173) "Department of High-Dose Chemotherapy and BMT, National Research Center for Hematology, Ministry of Healthcare of the Russian Federation, Moscow, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(167) "Department of High-Dose Chemotherapy and BMT, National Research Center for Hematology, Ministry of Healthcare of the Russian Federation, Moscow, Russian Federation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(167) "Department of High-Dose Chemotherapy and BMT, National Research Center for Hematology, Ministry of Healthcare of the Russian Federation, Moscow, Russian Federation
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20373" ["VALUE"]=> array(2) { ["TEXT"]=> string(443) "Анна А. Дмитрова, Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Дарья С. Дубняк, Вера А. Васильева, Ольга М. Королева, Зоя В. Конова, Анна А. Сидорова, Екатерина В. Усикова, Елена Н. Паровичникова, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(443) "Анна А. Дмитрова, Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Дарья С. Дубняк, Вера А. Васильева, Ольга М. Королева, Зоя В. Конова, Анна А. Сидорова, Екатерина В. Усикова, Елена Н. Паровичникова, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(443) "Анна А. Дмитрова, Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Дарья С. Дубняк, Вера А. Васильева, Ольга М. Королева, Зоя В. Конова, Анна А. Сидорова, Екатерина В. Усикова, Елена Н. Паровичникова, Валерий Г. Савченко" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20375" ["VALUE"]=> array(2) { ["TEXT"]=> string(4565) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Использование высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) является одной из наиболее актуальных методик профилактики РТПХ при выполнении трансплантации аллогенных гемопоэтических стволовых клеток крови (алло-ТГСК). Однако, влияние дополнительного введения ПТ-ЦФ на такой важный клинико-экономический параметр, как длительность пребывания в стационаре, и, соответственно, стоимость трансплантации остается не изученным. Здесь мы представляем анализ влияния введения высоких доз циклофосфамида с целью профилактики РТПХ после алло-ТГСК крови от неродственного донора на длительность госпитализации, связанной с проведением алло-ТГСК. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В исследование были включены больные в ремиссии острого лейкоза, которым была выполнена первая трансплантация алло-ТГСК от неродственного полностью совместимого или частично совместимого донора. Все больные на момент анализа были выписаны из стационара без признаков РТПХ и отторжения в течение всей госпитализации. Всего в исследование было включено 39 больных. Всем пациентам в качестве профилактики РТПХ был использован режим: антитимоцитарный глобулин (АТГ) 40 мг/кг (-4 по -1 день); циклоспорин А 3 мг/кг/сут (с +5 дня); микофенолата мофетил 3000 мг/сут (с +5 дня). При использовании в качестве источника трансплантата неродственного частично совместимого донора пациентам также вводился ПТ-ЦФ в дозе 50 мг/кг на +3, +4 день. Детальные характеристики представлены в таблице 1 (см. выше). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Данные по длительности госпитализации представлены на Рисунке 1 (см. выше). Согласно проведенному анализу, длительность госпитализации у пациентов в ремиссии острого лейкоза, которым была выполнена трансплантация алло-ТГСК с использованием ПТ-ЦФ и без ПТ-ЦФ составила 43 дня (14-126) и 48 дней (32-98) соответственно (p=0,48). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Таким образом, использование циклофосфамида на + 3, + 4 день с целью профилактики РТПХ не удлиняет период госпитализации при проведении алло-ТГСК у пациентов в ремиссии острого лейкоза. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация аллогенного костного мозга, иммуносупрессивная терапия, циклофосфамид, длительность госпитализации, неродственный донор. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4333) "
Введение
Использование высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) является одной из наиболее актуальных методик профилактики РТПХ при выполнении трансплантации аллогенных гемопоэтических стволовых клеток крови (алло-ТГСК). Однако, влияние дополнительного введения ПТ-ЦФ на такой важный клинико-экономический параметр, как длительность пребывания в стационаре, и, соответственно, стоимость трансплантации остается не изученным. Здесь мы представляем анализ влияния введения высоких доз циклофосфамида с целью профилактики РТПХ после алло-ТГСК крови от неродственного донора на длительность госпитализации, связанной с проведением алло-ТГСК.
Пациенты и методы
В исследование были включены больные в ремиссии острого лейкоза, которым была выполнена первая трансплантация алло-ТГСК от неродственного полностью совместимого или частично совместимого донора. Все больные на момент анализа были выписаны из стационара без признаков РТПХ и отторжения в течение всей госпитализации. Всего в исследование было включено 39 больных. Всем пациентам в качестве профилактики РТПХ был использован режим: антитимоцитарный глобулин (АТГ) 40 мг/кг (-4 по -1 день); циклоспорин А 3 мг/кг/сут (с +5 дня); микофенолата мофетил 3000 мг/сут (с +5 дня). При использовании в качестве источника трансплантата неродственного частично совместимого донора пациентам также вводился ПТ-ЦФ в дозе 50 мг/кг на +3, +4 день. Детальные характеристики представлены в таблице 1 (см. выше).
Результаты
Данные по длительности госпитализации представлены на Рисунке 1 (см. выше). Согласно проведенному анализу, длительность госпитализации у пациентов в ремиссии острого лейкоза, которым была выполнена трансплантация алло-ТГСК с использованием ПТ-ЦФ и без ПТ-ЦФ составила 43 дня (14-126) и 48 дней (32-98) соответственно (p=0,48).
Заключение
Таким образом, использование циклофосфамида на + 3, + 4 день с целью профилактики РТПХ не удлиняет период госпитализации при проведении алло-ТГСК у пациентов в ремиссии острого лейкоза.
Ключевые слова
Трансплантация аллогенного костного мозга, иммуносупрессивная терапия, циклофосфамид, длительность госпитализации, неродственный донор.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4333) "Введение
Использование высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) является одной из наиболее актуальных методик профилактики РТПХ при выполнении трансплантации аллогенных гемопоэтических стволовых клеток крови (алло-ТГСК). Однако, влияние дополнительного введения ПТ-ЦФ на такой важный клинико-экономический параметр, как длительность пребывания в стационаре, и, соответственно, стоимость трансплантации остается не изученным. Здесь мы представляем анализ влияния введения высоких доз циклофосфамида с целью профилактики РТПХ после алло-ТГСК крови от неродственного донора на длительность госпитализации, связанной с проведением алло-ТГСК.
Пациенты и методы
В исследование были включены больные в ремиссии острого лейкоза, которым была выполнена первая трансплантация алло-ТГСК от неродственного полностью совместимого или частично совместимого донора. Все больные на момент анализа были выписаны из стационара без признаков РТПХ и отторжения в течение всей госпитализации. Всего в исследование было включено 39 больных. Всем пациентам в качестве профилактики РТПХ был использован режим: антитимоцитарный глобулин (АТГ) 40 мг/кг (-4 по -1 день); циклоспорин А 3 мг/кг/сут (с +5 дня); микофенолата мофетил 3000 мг/сут (с +5 дня). При использовании в качестве источника трансплантата неродственного частично совместимого донора пациентам также вводился ПТ-ЦФ в дозе 50 мг/кг на +3, +4 день. Детальные характеристики представлены в таблице 1 (см. выше).
Результаты
Данные по длительности госпитализации представлены на Рисунке 1 (см. выше). Согласно проведенному анализу, длительность госпитализации у пациентов в ремиссии острого лейкоза, которым была выполнена трансплантация алло-ТГСК с использованием ПТ-ЦФ и без ПТ-ЦФ составила 43 дня (14-126) и 48 дней (32-98) соответственно (p=0,48).
Заключение
Таким образом, использование циклофосфамида на + 3, + 4 день с целью профилактики РТПХ не удлиняет период госпитализации при проведении алло-ТГСК у пациентов в ремиссии острого лейкоза.
Ключевые слова
Трансплантация аллогенного костного мозга, иммуносупрессивная терапия, циклофосфамид, длительность госпитализации, неродственный донор.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20374" ["VALUE"]=> array(2) { ["TEXT"]=> string(234) "Отделение высокодозной химиотерапии и трансплантации костного мозга, ФГБУ «НМИЦ гематологии» МЗ РФ,<br> Москва, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(222) "Отделение высокодозной химиотерапии и трансплантации костного мозга, ФГБУ «НМИЦ гематологии» МЗ РФ,Москва, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(222) "Отделение высокодозной химиотерапии и трансплантации костного мозга, ФГБУ «НМИЦ гематологии» МЗ РФ,
Москва, Россия
" } } } [22]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1561" ["~ID"]=> string(4) "1561" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(189) "Синдром выброса цитокинов после профилактики РТПХ с включением посттрансплантационного бендамустина" ["~NAME"]=> string(189) "Синдром выброса цитокинов после профилактики РТПХ с включением посттрансплантационного бендамустина" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:29:03" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:29:03" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/sindrom-vybrosa-tsitokinov-posle-profilaktiki-rtpkh-s-vklyucheniem-posttransplantatsionnogo-bendamus/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/sindrom-vybrosa-tsitokinov-posle-profilaktiki-rtpkh-s-vklyucheniem-posttransplantatsionnogo-bendamus/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "sindrom-vybrosa-tsitokinov-posle-profilaktiki-rtpkh-s-vklyucheniem-posttransplantatsionnogo-bendamus" ["~CODE"]=> string(100) "sindrom-vybrosa-tsitokinov-posle-profilaktiki-rtpkh-s-vklyucheniem-posttransplantatsionnogo-bendamus" ["EXTERNAL_ID"]=> string(4) "1561" ["~EXTERNAL_ID"]=> string(4) "1561" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(189) "Синдром выброса цитокинов после профилактики РТПХ с включением посттрансплантационного бендамустина" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(270) "Синдром выброса цитокинов после профилактики РТПХ с включением посттрансплантационного бендамустинаCytokine release syndrome after GVHD prophylaxis with posttransplant bendamustine" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(5312) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения многих онкологических заболеваний, а число трансплантаций растет во всем мире. На данный момент проводится множество клинических испытаний для усовершенствования и разработки более эффективных способов кондиционирования и профилактики РТПХ, главной задачей которых является уменьшение реакции трансплантатпротив хозяина и индуцирование реакции транплантат против лейкоза. С этой целью в НИИ ДОГиТ им. Р. М. Горбачевой в рамках клинического исследования был использован посттрансплантационный бендамустин (ПТБ). Одной из побочных реакций данного режима кондиционирования стало развитие синдрома выброса цитокинов (СВЦ). Понимание динамики цитокинов в развитии этого синдрома позволяет прогнозировать его развитие и проводить адекватную терапию. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В проспективное исследование (NCT02799147) вошли 12 пациентов: 8 с острым миелобастным лейкозом, 4 с острым лимфобластным лейкозом. Все пациенты имели химиорезистентное течение лейкоза и остутсвие ремиссии на момент трансплантата. Медиана возраста пациентов составила 38 лет (от 24 до 54 лет). Пациенты получали профилактику РТПХ бендамустином 100-140 мг/м2 в Д+3,+4. Всем пациентам был проведен миелоаблативный режим кондиционирования с использованием флударабина и бусульфана. Забор крови с последующим анализом уровня цитокинов (IFN-γ, IL-1, IL-10, IL-6, IL-17) осуществлялся в день -7, 0, +7, +14. У 8/12 развился синдром высвобождения цитокинов. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> У всех пациентов на момент первого забора крови уже определялся высокий уровень цитокинов. Тем не менее, после приживления выявлено дальнейшее повышение IFN-γ (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). Частота СВЦ составила 66,7% (n=8) в исследуемой группе, однако, достоверная связь с СВЦ была выявлена только для IL-6 (74 vs 8 ng/ml, p=0.036). Уровень IL-6 при этом не прогнозировал летальность от осложнений (76 vs 19 ng/ml, р=0.21). Частота СВЦ 1-2 степени тяжести составила 33,3% (n=4), 3-4 степени 33,3% (n=4). Наиболее частыми клиническими проявлениями цитокинового синдрома были лихорадка (100%), повышение уровня креатинина (90%), СРБ (100%), билирубина и трансаминаз (67%), острое повреждение почек (56%), гипотензия (50%), токсичность в отношении ЦНС (33%), ДВС-синдром (22%) и др. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Выявлено, что терапия ПТБ ассоциирована с повышением IFN-γ, IL-10, IL-6, однако только повышение IL-6 ассоциировано с СВЦ. Полученные результаты говорят о рациональности использования анти-IL6 терапии. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Реакция «трансплантат против хозяина», синдром выброса цитокинов, бендамустин после трансплантации. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(189) "Синдром выброса цитокинов после профилактики РТПХ с включением посттрансплантационного бендамустина" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(189) "Синдром выброса цитокинов после профилактики РТПХ с включением посттрансплантационного бендамустина" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(189) "Синдром выброса цитокинов после профилактики РТПХ с включением посттрансплантационного бендамустина" ["SECTION_META_TITLE"]=> string(189) "Синдром выброса цитокинов после профилактики РТПХ с включением посттрансплантационного бендамустина" ["SECTION_META_KEYWORDS"]=> string(189) "Синдром выброса цитокинов после профилактики РТПХ с включением посттрансплантационного бендамустина" ["SECTION_META_DESCRIPTION"]=> string(189) "Синдром выброса цитокинов после профилактики РТПХ с включением посттрансплантационного бендамустина" ["SECTION_PICTURE_FILE_ALT"]=> string(189) "Синдром выброса цитокинов после профилактики РТПХ с включением посттрансплантационного бендамустина" ["SECTION_PICTURE_FILE_TITLE"]=> string(189) "Синдром выброса цитокинов после профилактики РТПХ с включением посттрансплантационного бендамустина" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "sindrom-vybrosa-tsitokinov-posle-profilaktiki-rtpkh-s-vklyucheniem-posttransplantatsionnogo-bendamus" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(189) "Синдром выброса цитокинов после профилактики РТПХ с включением посттрансплантационного бендамустина" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(189) "Синдром выброса цитокинов после профилактики РТПХ с включением посттрансплантационного бендамустина" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "sindrom-vybrosa-tsitokinov-posle-profilaktiki-rtpkh-s-vklyucheniem-posttransplantatsionnogo-bendamus" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "sindrom-vybrosa-tsitokinov-posle-profilaktiki-rtpkh-s-vklyucheniem-posttransplantatsionnogo-bendamus" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "sindrom-vybrosa-tsitokinov-posle-profilaktiki-rtpkh-s-vklyucheniem-posttransplantatsionnogo-bendamus" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20381" ["VALUE"]=> array(2) { ["TEXT"]=> string(576) "Анна А. Доценко <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Елена А. Суркова <sup>1</sup>, Дарья А. Кузнецова <sup>2</sup>, Сергей В. Лапин <sup>2</sup>, Варвара Н. Овечкина <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Елена В. Морозова <sup>1</sup>, Сергей Н. Бондаренко <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(456) "Анна А. Доценко 1, Иван С. Моисеев 1, Елена А. Суркова 1, Дарья А. Кузнецова 2, Сергей В. Лапин 2, Варвара Н. Овечкина 1, Елена И. Дарская 1, Елена В. Морозова 1, Сергей Н. Бондаренко 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20461" ["VALUE"]=> array(2) { ["TEXT"]=> string(662) "<sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова<br> <sup>2</sup> Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова, Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(626) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова
2 Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20382" ["VALUE"]=> array(2) { ["TEXT"]=> string(5312) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения многих онкологических заболеваний, а число трансплантаций растет во всем мире. На данный момент проводится множество клинических испытаний для усовершенствования и разработки более эффективных способов кондиционирования и профилактики РТПХ, главной задачей которых является уменьшение реакции трансплантатпротив хозяина и индуцирование реакции транплантат против лейкоза. С этой целью в НИИ ДОГиТ им. Р. М. Горбачевой в рамках клинического исследования был использован посттрансплантационный бендамустин (ПТБ). Одной из побочных реакций данного режима кондиционирования стало развитие синдрома выброса цитокинов (СВЦ). Понимание динамики цитокинов в развитии этого синдрома позволяет прогнозировать его развитие и проводить адекватную терапию. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В проспективное исследование (NCT02799147) вошли 12 пациентов: 8 с острым миелобастным лейкозом, 4 с острым лимфобластным лейкозом. Все пациенты имели химиорезистентное течение лейкоза и остутсвие ремиссии на момент трансплантата. Медиана возраста пациентов составила 38 лет (от 24 до 54 лет). Пациенты получали профилактику РТПХ бендамустином 100-140 мг/м2 в Д+3,+4. Всем пациентам был проведен миелоаблативный режим кондиционирования с использованием флударабина и бусульфана. Забор крови с последующим анализом уровня цитокинов (IFN-γ, IL-1, IL-10, IL-6, IL-17) осуществлялся в день -7, 0, +7, +14. У 8/12 развился синдром высвобождения цитокинов. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> У всех пациентов на момент первого забора крови уже определялся высокий уровень цитокинов. Тем не менее, после приживления выявлено дальнейшее повышение IFN-γ (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). Частота СВЦ составила 66,7% (n=8) в исследуемой группе, однако, достоверная связь с СВЦ была выявлена только для IL-6 (74 vs 8 ng/ml, p=0.036). Уровень IL-6 при этом не прогнозировал летальность от осложнений (76 vs 19 ng/ml, р=0.21). Частота СВЦ 1-2 степени тяжести составила 33,3% (n=4), 3-4 степени 33,3% (n=4). Наиболее частыми клиническими проявлениями цитокинового синдрома были лихорадка (100%), повышение уровня креатинина (90%), СРБ (100%), билирубина и трансаминаз (67%), острое повреждение почек (56%), гипотензия (50%), токсичность в отношении ЦНС (33%), ДВС-синдром (22%) и др. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Выявлено, что терапия ПТБ ассоциирована с повышением IFN-γ, IL-10, IL-6, однако только повышение IL-6 ассоциировано с СВЦ. Полученные результаты говорят о рациональности использования анти-IL6 терапии. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Реакция «трансплантат против хозяина», синдром выброса цитокинов, бендамустин после трансплантации. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5092) "
Введение
Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения многих онкологических заболеваний, а число трансплантаций растет во всем мире. На данный момент проводится множество клинических испытаний для усовершенствования и разработки более эффективных способов кондиционирования и профилактики РТПХ, главной задачей которых является уменьшение реакции трансплантатпротив хозяина и индуцирование реакции транплантат против лейкоза. С этой целью в НИИ ДОГиТ им. Р. М. Горбачевой в рамках клинического исследования был использован посттрансплантационный бендамустин (ПТБ). Одной из побочных реакций данного режима кондиционирования стало развитие синдрома выброса цитокинов (СВЦ). Понимание динамики цитокинов в развитии этого синдрома позволяет прогнозировать его развитие и проводить адекватную терапию.
Материалы и методы
В проспективное исследование (NCT02799147) вошли 12 пациентов: 8 с острым миелобастным лейкозом, 4 с острым лимфобластным лейкозом. Все пациенты имели химиорезистентное течение лейкоза и остутсвие ремиссии на момент трансплантата. Медиана возраста пациентов составила 38 лет (от 24 до 54 лет). Пациенты получали профилактику РТПХ бендамустином 100-140 мг/м2 в Д+3,+4. Всем пациентам был проведен миелоаблативный режим кондиционирования с использованием флударабина и бусульфана. Забор крови с последующим анализом уровня цитокинов (IFN-γ, IL-1, IL-10, IL-6, IL-17) осуществлялся в день -7, 0, +7, +14. У 8/12 развился синдром высвобождения цитокинов.
Результаты
У всех пациентов на момент первого забора крови уже определялся высокий уровень цитокинов. Тем не менее, после приживления выявлено дальнейшее повышение IFN-γ (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). Частота СВЦ составила 66,7% (n=8) в исследуемой группе, однако, достоверная связь с СВЦ была выявлена только для IL-6 (74 vs 8 ng/ml, p=0.036). Уровень IL-6 при этом не прогнозировал летальность от осложнений (76 vs 19 ng/ml, р=0.21). Частота СВЦ 1-2 степени тяжести составила 33,3% (n=4), 3-4 степени 33,3% (n=4). Наиболее частыми клиническими проявлениями цитокинового синдрома были лихорадка (100%), повышение уровня креатинина (90%), СРБ (100%), билирубина и трансаминаз (67%), острое повреждение почек (56%), гипотензия (50%), токсичность в отношении ЦНС (33%), ДВС-синдром (22%) и др.
Заключение
Выявлено, что терапия ПТБ ассоциирована с повышением IFN-γ, IL-10, IL-6, однако только повышение IL-6 ассоциировано с СВЦ. Полученные результаты говорят о рациональности использования анти-IL6 терапии.
Ключевые слова
Реакция «трансплантат против хозяина», синдром выброса цитокинов, бендамустин после трансплантации.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20383" ["VALUE"]=> array(2) { ["TEXT"]=> string(441) "Anna A. Dotsenko <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Elena A. Surkova <sup>1</sup>, Daria A. Kuznetcova <sup>2</sup>, Sergey V. Lapin <sup>2</sup>, Varvara N. Ovechkina <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Elena V. Morozova <sup>1</sup>, Sergey N. Bondarenko <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(321) "Anna A. Dotsenko 1, Ivan S. Moiseev 1, Elena A. Surkova 1, Daria A. Kuznetcova 2, Sergey V. Lapin 2, Varvara N. Ovechkina 1, Elena I. Darskaya 1, Elena V. Morozova 1, Sergey N. Bondarenko 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20384" ["VALUE"]=> array(2) { ["TEXT"]=> string(368) "<sup>1</sup> R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation<br> <sup>2</sup> Laboratory of Autoimmune Diagnostics, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(332) "1 R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation2 Laboratory of Autoimmune Diagnostics, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20463" ["VALUE"]=> array(2) { ["TEXT"]=> string(3401) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Hematopoietic stem cells transplantation is an effective method of treatment of many cancer diseases and the number of transplants is increasing worldwide. There are many clinical trials under way to improve and develop more effective conditioning methods, the main task is to reduce graft-versushost disease and to induce graft versus leukemia response. For this goal posttransplant bendamustine (PTB) was used at the R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation in the setting of a clinical trial. One of the adverse reactions of this conditioning regimen was development of a life-threatening complication – cytokine release syndrome (CRS). Understanding dynamics of cytokines in the development of this syndrome allows to predict its development and to conduct relevant therapy. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> We carried out a prospective study (NCT02799147), which included 12 patients: 8 with acute myeloid leukemia, 4 with acute lymphoblastic leukemia. All patients had chemorefractory disease and absence of hematologic remission at the start of the conditioning. The median age was 38 years (from 24 to 54 years old). All patients received a prophylaxis of GVHD with bendamustine 100-140 mg/m2 per day +3, +4. Myeloablative conditioning regimen with fludarabine and busulfan was applied in all patients. Blood sampling with subsequent analysis of the level of cytokines (IFN-γ, IL-1, IL-10, IL-6, IL-17) was performed on day -7, 0, +7, +14. The cytokine release syndrome developed in 8/12 patients. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> High cytokine level was determined starting from the first blood sample in all patients. However, after engraftment, a further increase was detected in IFN-γ level (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). The frequency of CRS was 66.7% (n=8) in study group, but positive association with the CRS was detected only for IL-6 (74 vs 8 ng/ml, p=0.036). The level of IL-6 wasn’t a predictor of mortality from complications (76 vs 19 ng/ml, р=0.21). The frequency of CRS grades 1-2 was 33.3% (n=4), grades 3-4 was 33.3% (n=4). The most frequent clinical manifestations of CRS were fever (100%), increase in creatinine (90%), CRP (100%), bilirubin and transaminases (67%), acute kidney injury (56%), hypotension (50%), CNS toxicity (33%), disseminated intravascular coagulation syndrome (22%) and others. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The prophylaxis of GVHD with posttransplant bendamustine is associated with the increase of IFN-γ, IL-10, IL-6, however, only the increase of IL-6 was associated with CRS. These results confirmed the rationality of using anti-IL6 therapy. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Graft-versus-host disease, cytokine release syndrome (CRS), posttransplant bendamustine (PTB). </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3181) "
Introduction
Hematopoietic stem cells transplantation is an effective method of treatment of many cancer diseases and the number of transplants is increasing worldwide. There are many clinical trials under way to improve and develop more effective conditioning methods, the main task is to reduce graft-versushost disease and to induce graft versus leukemia response. For this goal posttransplant bendamustine (PTB) was used at the R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation in the setting of a clinical trial. One of the adverse reactions of this conditioning regimen was development of a life-threatening complication – cytokine release syndrome (CRS). Understanding dynamics of cytokines in the development of this syndrome allows to predict its development and to conduct relevant therapy.
Materials and methods
We carried out a prospective study (NCT02799147), which included 12 patients: 8 with acute myeloid leukemia, 4 with acute lymphoblastic leukemia. All patients had chemorefractory disease and absence of hematologic remission at the start of the conditioning. The median age was 38 years (from 24 to 54 years old). All patients received a prophylaxis of GVHD with bendamustine 100-140 mg/m2 per day +3, +4. Myeloablative conditioning regimen with fludarabine and busulfan was applied in all patients. Blood sampling with subsequent analysis of the level of cytokines (IFN-γ, IL-1, IL-10, IL-6, IL-17) was performed on day -7, 0, +7, +14. The cytokine release syndrome developed in 8/12 patients.
Results
High cytokine level was determined starting from the first blood sample in all patients. However, after engraftment, a further increase was detected in IFN-γ level (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). The frequency of CRS was 66.7% (n=8) in study group, but positive association with the CRS was detected only for IL-6 (74 vs 8 ng/ml, p=0.036). The level of IL-6 wasn’t a predictor of mortality from complications (76 vs 19 ng/ml, р=0.21). The frequency of CRS grades 1-2 was 33.3% (n=4), grades 3-4 was 33.3% (n=4). The most frequent clinical manifestations of CRS were fever (100%), increase in creatinine (90%), CRP (100%), bilirubin and transaminases (67%), acute kidney injury (56%), hypotension (50%), CNS toxicity (33%), disseminated intravascular coagulation syndrome (22%) and others.
Conclusion
The prophylaxis of GVHD with posttransplant bendamustine is associated with the increase of IFN-γ, IL-10, IL-6, however, only the increase of IL-6 was associated with CRS. These results confirmed the rationality of using anti-IL6 therapy.
Keywords
Graft-versus-host disease, cytokine release syndrome (CRS), posttransplant bendamustine (PTB).
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20385" ["VALUE"]=> string(81) "Cytokine release syndrome after GVHD prophylaxis with posttransplant bendamustine" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(81) "Cytokine release syndrome after GVHD prophylaxis with posttransplant bendamustine" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20755" ["VALUE"]=> string(4) "1391" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1391" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20756" ["VALUE"]=> string(4) "1392" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1392" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20383" ["VALUE"]=> array(2) { ["TEXT"]=> string(441) "Anna A. Dotsenko <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Elena A. Surkova <sup>1</sup>, Daria A. Kuznetcova <sup>2</sup>, Sergey V. Lapin <sup>2</sup>, Varvara N. Ovechkina <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Elena V. Morozova <sup>1</sup>, Sergey N. Bondarenko <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(321) "Anna A. Dotsenko 1, Ivan S. Moiseev 1, Elena A. Surkova 1, Daria A. Kuznetcova 2, Sergey V. Lapin 2, Varvara N. Ovechkina 1, Elena I. Darskaya 1, Elena V. Morozova 1, Sergey N. Bondarenko 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(321) "Anna A. Dotsenko 1, Ivan S. Moiseev 1, Elena A. Surkova 1, Daria A. Kuznetcova 2, Sergey V. Lapin 2, Varvara N. Ovechkina 1, Elena I. Darskaya 1, Elena V. Morozova 1, Sergey N. Bondarenko 1, Boris V. Afanasyev 1" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20463" ["VALUE"]=> array(2) { ["TEXT"]=> string(3401) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Hematopoietic stem cells transplantation is an effective method of treatment of many cancer diseases and the number of transplants is increasing worldwide. There are many clinical trials under way to improve and develop more effective conditioning methods, the main task is to reduce graft-versushost disease and to induce graft versus leukemia response. For this goal posttransplant bendamustine (PTB) was used at the R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation in the setting of a clinical trial. One of the adverse reactions of this conditioning regimen was development of a life-threatening complication – cytokine release syndrome (CRS). Understanding dynamics of cytokines in the development of this syndrome allows to predict its development and to conduct relevant therapy. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> We carried out a prospective study (NCT02799147), which included 12 patients: 8 with acute myeloid leukemia, 4 with acute lymphoblastic leukemia. All patients had chemorefractory disease and absence of hematologic remission at the start of the conditioning. The median age was 38 years (from 24 to 54 years old). All patients received a prophylaxis of GVHD with bendamustine 100-140 mg/m2 per day +3, +4. Myeloablative conditioning regimen with fludarabine and busulfan was applied in all patients. Blood sampling with subsequent analysis of the level of cytokines (IFN-γ, IL-1, IL-10, IL-6, IL-17) was performed on day -7, 0, +7, +14. The cytokine release syndrome developed in 8/12 patients. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> High cytokine level was determined starting from the first blood sample in all patients. However, after engraftment, a further increase was detected in IFN-γ level (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). The frequency of CRS was 66.7% (n=8) in study group, but positive association with the CRS was detected only for IL-6 (74 vs 8 ng/ml, p=0.036). The level of IL-6 wasn’t a predictor of mortality from complications (76 vs 19 ng/ml, р=0.21). The frequency of CRS grades 1-2 was 33.3% (n=4), grades 3-4 was 33.3% (n=4). The most frequent clinical manifestations of CRS were fever (100%), increase in creatinine (90%), CRP (100%), bilirubin and transaminases (67%), acute kidney injury (56%), hypotension (50%), CNS toxicity (33%), disseminated intravascular coagulation syndrome (22%) and others. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The prophylaxis of GVHD with posttransplant bendamustine is associated with the increase of IFN-γ, IL-10, IL-6, however, only the increase of IL-6 was associated with CRS. These results confirmed the rationality of using anti-IL6 therapy. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Graft-versus-host disease, cytokine release syndrome (CRS), posttransplant bendamustine (PTB). </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3181) "Introduction
Hematopoietic stem cells transplantation is an effective method of treatment of many cancer diseases and the number of transplants is increasing worldwide. There are many clinical trials under way to improve and develop more effective conditioning methods, the main task is to reduce graft-versushost disease and to induce graft versus leukemia response. For this goal posttransplant bendamustine (PTB) was used at the R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation in the setting of a clinical trial. One of the adverse reactions of this conditioning regimen was development of a life-threatening complication – cytokine release syndrome (CRS). Understanding dynamics of cytokines in the development of this syndrome allows to predict its development and to conduct relevant therapy.
Materials and methods
We carried out a prospective study (NCT02799147), which included 12 patients: 8 with acute myeloid leukemia, 4 with acute lymphoblastic leukemia. All patients had chemorefractory disease and absence of hematologic remission at the start of the conditioning. The median age was 38 years (from 24 to 54 years old). All patients received a prophylaxis of GVHD with bendamustine 100-140 mg/m2 per day +3, +4. Myeloablative conditioning regimen with fludarabine and busulfan was applied in all patients. Blood sampling with subsequent analysis of the level of cytokines (IFN-γ, IL-1, IL-10, IL-6, IL-17) was performed on day -7, 0, +7, +14. The cytokine release syndrome developed in 8/12 patients.
Results
High cytokine level was determined starting from the first blood sample in all patients. However, after engraftment, a further increase was detected in IFN-γ level (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). The frequency of CRS was 66.7% (n=8) in study group, but positive association with the CRS was detected only for IL-6 (74 vs 8 ng/ml, p=0.036). The level of IL-6 wasn’t a predictor of mortality from complications (76 vs 19 ng/ml, р=0.21). The frequency of CRS grades 1-2 was 33.3% (n=4), grades 3-4 was 33.3% (n=4). The most frequent clinical manifestations of CRS were fever (100%), increase in creatinine (90%), CRP (100%), bilirubin and transaminases (67%), acute kidney injury (56%), hypotension (50%), CNS toxicity (33%), disseminated intravascular coagulation syndrome (22%) and others.
Conclusion
The prophylaxis of GVHD with posttransplant bendamustine is associated with the increase of IFN-γ, IL-10, IL-6, however, only the increase of IL-6 was associated with CRS. These results confirmed the rationality of using anti-IL6 therapy.
Keywords
Graft-versus-host disease, cytokine release syndrome (CRS), posttransplant bendamustine (PTB).
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3181) "Introduction
Hematopoietic stem cells transplantation is an effective method of treatment of many cancer diseases and the number of transplants is increasing worldwide. There are many clinical trials under way to improve and develop more effective conditioning methods, the main task is to reduce graft-versushost disease and to induce graft versus leukemia response. For this goal posttransplant bendamustine (PTB) was used at the R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation in the setting of a clinical trial. One of the adverse reactions of this conditioning regimen was development of a life-threatening complication – cytokine release syndrome (CRS). Understanding dynamics of cytokines in the development of this syndrome allows to predict its development and to conduct relevant therapy.
Materials and methods
We carried out a prospective study (NCT02799147), which included 12 patients: 8 with acute myeloid leukemia, 4 with acute lymphoblastic leukemia. All patients had chemorefractory disease and absence of hematologic remission at the start of the conditioning. The median age was 38 years (from 24 to 54 years old). All patients received a prophylaxis of GVHD with bendamustine 100-140 mg/m2 per day +3, +4. Myeloablative conditioning regimen with fludarabine and busulfan was applied in all patients. Blood sampling with subsequent analysis of the level of cytokines (IFN-γ, IL-1, IL-10, IL-6, IL-17) was performed on day -7, 0, +7, +14. The cytokine release syndrome developed in 8/12 patients.
Results
High cytokine level was determined starting from the first blood sample in all patients. However, after engraftment, a further increase was detected in IFN-γ level (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). The frequency of CRS was 66.7% (n=8) in study group, but positive association with the CRS was detected only for IL-6 (74 vs 8 ng/ml, p=0.036). The level of IL-6 wasn’t a predictor of mortality from complications (76 vs 19 ng/ml, р=0.21). The frequency of CRS grades 1-2 was 33.3% (n=4), grades 3-4 was 33.3% (n=4). The most frequent clinical manifestations of CRS were fever (100%), increase in creatinine (90%), CRP (100%), bilirubin and transaminases (67%), acute kidney injury (56%), hypotension (50%), CNS toxicity (33%), disseminated intravascular coagulation syndrome (22%) and others.
Conclusion
The prophylaxis of GVHD with posttransplant bendamustine is associated with the increase of IFN-γ, IL-10, IL-6, however, only the increase of IL-6 was associated with CRS. These results confirmed the rationality of using anti-IL6 therapy.
Keywords
Graft-versus-host disease, cytokine release syndrome (CRS), posttransplant bendamustine (PTB).
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20385" ["VALUE"]=> string(81) "Cytokine release syndrome after GVHD prophylaxis with posttransplant bendamustine" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(81) "Cytokine release syndrome after GVHD prophylaxis with posttransplant bendamustine" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(81) "Cytokine release syndrome after GVHD prophylaxis with posttransplant bendamustine" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20384" ["VALUE"]=> array(2) { ["TEXT"]=> string(368) "<sup>1</sup> R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation<br> <sup>2</sup> Laboratory of Autoimmune Diagnostics, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(332) "1 R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation2 Laboratory of Autoimmune Diagnostics, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(332) "1 R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation
2 Laboratory of Autoimmune Diagnostics, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20381" ["VALUE"]=> array(2) { ["TEXT"]=> string(576) "Анна А. Доценко <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Елена А. Суркова <sup>1</sup>, Дарья А. Кузнецова <sup>2</sup>, Сергей В. Лапин <sup>2</sup>, Варвара Н. Овечкина <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Елена В. Морозова <sup>1</sup>, Сергей Н. Бондаренко <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(456) "Анна А. Доценко 1, Иван С. Моисеев 1, Елена А. Суркова 1, Дарья А. Кузнецова 2, Сергей В. Лапин 2, Варвара Н. Овечкина 1, Елена И. Дарская 1, Елена В. Морозова 1, Сергей Н. Бондаренко 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(456) "Анна А. Доценко 1, Иван С. Моисеев 1, Елена А. Суркова 1, Дарья А. Кузнецова 2, Сергей В. Лапин 2, Варвара Н. Овечкина 1, Елена И. Дарская 1, Елена В. Морозова 1, Сергей Н. Бондаренко 1, Борис В. Афанасьев 1" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20382" ["VALUE"]=> array(2) { ["TEXT"]=> string(5312) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения многих онкологических заболеваний, а число трансплантаций растет во всем мире. На данный момент проводится множество клинических испытаний для усовершенствования и разработки более эффективных способов кондиционирования и профилактики РТПХ, главной задачей которых является уменьшение реакции трансплантатпротив хозяина и индуцирование реакции транплантат против лейкоза. С этой целью в НИИ ДОГиТ им. Р. М. Горбачевой в рамках клинического исследования был использован посттрансплантационный бендамустин (ПТБ). Одной из побочных реакций данного режима кондиционирования стало развитие синдрома выброса цитокинов (СВЦ). Понимание динамики цитокинов в развитии этого синдрома позволяет прогнозировать его развитие и проводить адекватную терапию. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В проспективное исследование (NCT02799147) вошли 12 пациентов: 8 с острым миелобастным лейкозом, 4 с острым лимфобластным лейкозом. Все пациенты имели химиорезистентное течение лейкоза и остутсвие ремиссии на момент трансплантата. Медиана возраста пациентов составила 38 лет (от 24 до 54 лет). Пациенты получали профилактику РТПХ бендамустином 100-140 мг/м2 в Д+3,+4. Всем пациентам был проведен миелоаблативный режим кондиционирования с использованием флударабина и бусульфана. Забор крови с последующим анализом уровня цитокинов (IFN-γ, IL-1, IL-10, IL-6, IL-17) осуществлялся в день -7, 0, +7, +14. У 8/12 развился синдром высвобождения цитокинов. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> У всех пациентов на момент первого забора крови уже определялся высокий уровень цитокинов. Тем не менее, после приживления выявлено дальнейшее повышение IFN-γ (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). Частота СВЦ составила 66,7% (n=8) в исследуемой группе, однако, достоверная связь с СВЦ была выявлена только для IL-6 (74 vs 8 ng/ml, p=0.036). Уровень IL-6 при этом не прогнозировал летальность от осложнений (76 vs 19 ng/ml, р=0.21). Частота СВЦ 1-2 степени тяжести составила 33,3% (n=4), 3-4 степени 33,3% (n=4). Наиболее частыми клиническими проявлениями цитокинового синдрома были лихорадка (100%), повышение уровня креатинина (90%), СРБ (100%), билирубина и трансаминаз (67%), острое повреждение почек (56%), гипотензия (50%), токсичность в отношении ЦНС (33%), ДВС-синдром (22%) и др. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Выявлено, что терапия ПТБ ассоциирована с повышением IFN-γ, IL-10, IL-6, однако только повышение IL-6 ассоциировано с СВЦ. Полученные результаты говорят о рациональности использования анти-IL6 терапии. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Реакция «трансплантат против хозяина», синдром выброса цитокинов, бендамустин после трансплантации. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5092) "
Введение
Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения многих онкологических заболеваний, а число трансплантаций растет во всем мире. На данный момент проводится множество клинических испытаний для усовершенствования и разработки более эффективных способов кондиционирования и профилактики РТПХ, главной задачей которых является уменьшение реакции трансплантатпротив хозяина и индуцирование реакции транплантат против лейкоза. С этой целью в НИИ ДОГиТ им. Р. М. Горбачевой в рамках клинического исследования был использован посттрансплантационный бендамустин (ПТБ). Одной из побочных реакций данного режима кондиционирования стало развитие синдрома выброса цитокинов (СВЦ). Понимание динамики цитокинов в развитии этого синдрома позволяет прогнозировать его развитие и проводить адекватную терапию.
Материалы и методы
В проспективное исследование (NCT02799147) вошли 12 пациентов: 8 с острым миелобастным лейкозом, 4 с острым лимфобластным лейкозом. Все пациенты имели химиорезистентное течение лейкоза и остутсвие ремиссии на момент трансплантата. Медиана возраста пациентов составила 38 лет (от 24 до 54 лет). Пациенты получали профилактику РТПХ бендамустином 100-140 мг/м2 в Д+3,+4. Всем пациентам был проведен миелоаблативный режим кондиционирования с использованием флударабина и бусульфана. Забор крови с последующим анализом уровня цитокинов (IFN-γ, IL-1, IL-10, IL-6, IL-17) осуществлялся в день -7, 0, +7, +14. У 8/12 развился синдром высвобождения цитокинов.
Результаты
У всех пациентов на момент первого забора крови уже определялся высокий уровень цитокинов. Тем не менее, после приживления выявлено дальнейшее повышение IFN-γ (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). Частота СВЦ составила 66,7% (n=8) в исследуемой группе, однако, достоверная связь с СВЦ была выявлена только для IL-6 (74 vs 8 ng/ml, p=0.036). Уровень IL-6 при этом не прогнозировал летальность от осложнений (76 vs 19 ng/ml, р=0.21). Частота СВЦ 1-2 степени тяжести составила 33,3% (n=4), 3-4 степени 33,3% (n=4). Наиболее частыми клиническими проявлениями цитокинового синдрома были лихорадка (100%), повышение уровня креатинина (90%), СРБ (100%), билирубина и трансаминаз (67%), острое повреждение почек (56%), гипотензия (50%), токсичность в отношении ЦНС (33%), ДВС-синдром (22%) и др.
Заключение
Выявлено, что терапия ПТБ ассоциирована с повышением IFN-γ, IL-10, IL-6, однако только повышение IL-6 ассоциировано с СВЦ. Полученные результаты говорят о рациональности использования анти-IL6 терапии.
Ключевые слова
Реакция «трансплантат против хозяина», синдром выброса цитокинов, бендамустин после трансплантации.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(5092) "Введение
Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения многих онкологических заболеваний, а число трансплантаций растет во всем мире. На данный момент проводится множество клинических испытаний для усовершенствования и разработки более эффективных способов кондиционирования и профилактики РТПХ, главной задачей которых является уменьшение реакции трансплантатпротив хозяина и индуцирование реакции транплантат против лейкоза. С этой целью в НИИ ДОГиТ им. Р. М. Горбачевой в рамках клинического исследования был использован посттрансплантационный бендамустин (ПТБ). Одной из побочных реакций данного режима кондиционирования стало развитие синдрома выброса цитокинов (СВЦ). Понимание динамики цитокинов в развитии этого синдрома позволяет прогнозировать его развитие и проводить адекватную терапию.
Материалы и методы
В проспективное исследование (NCT02799147) вошли 12 пациентов: 8 с острым миелобастным лейкозом, 4 с острым лимфобластным лейкозом. Все пациенты имели химиорезистентное течение лейкоза и остутсвие ремиссии на момент трансплантата. Медиана возраста пациентов составила 38 лет (от 24 до 54 лет). Пациенты получали профилактику РТПХ бендамустином 100-140 мг/м2 в Д+3,+4. Всем пациентам был проведен миелоаблативный режим кондиционирования с использованием флударабина и бусульфана. Забор крови с последующим анализом уровня цитокинов (IFN-γ, IL-1, IL-10, IL-6, IL-17) осуществлялся в день -7, 0, +7, +14. У 8/12 развился синдром высвобождения цитокинов.
Результаты
У всех пациентов на момент первого забора крови уже определялся высокий уровень цитокинов. Тем не менее, после приживления выявлено дальнейшее повышение IFN-γ (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). Частота СВЦ составила 66,7% (n=8) в исследуемой группе, однако, достоверная связь с СВЦ была выявлена только для IL-6 (74 vs 8 ng/ml, p=0.036). Уровень IL-6 при этом не прогнозировал летальность от осложнений (76 vs 19 ng/ml, р=0.21). Частота СВЦ 1-2 степени тяжести составила 33,3% (n=4), 3-4 степени 33,3% (n=4). Наиболее частыми клиническими проявлениями цитокинового синдрома были лихорадка (100%), повышение уровня креатинина (90%), СРБ (100%), билирубина и трансаминаз (67%), острое повреждение почек (56%), гипотензия (50%), токсичность в отношении ЦНС (33%), ДВС-синдром (22%) и др.
Заключение
Выявлено, что терапия ПТБ ассоциирована с повышением IFN-γ, IL-10, IL-6, однако только повышение IL-6 ассоциировано с СВЦ. Полученные результаты говорят о рациональности использования анти-IL6 терапии.
Ключевые слова
Реакция «трансплантат против хозяина», синдром выброса цитокинов, бендамустин после трансплантации.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20461" ["VALUE"]=> array(2) { ["TEXT"]=> string(662) "<sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова<br> <sup>2</sup> Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова, Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(626) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова2 Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(626) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова
2 Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова, Санкт-Петербург, Россия
" } } } [23]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1559" ["~ID"]=> string(4) "1559" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(183) "Опыт применения терапии II линии рецидивов и резистентных форм лимфомы Ходжкина в Иркутской области" ["~NAME"]=> string(183) "Опыт применения терапии II линии рецидивов и резистентных форм лимфомы Ходжкина в Иркутской области" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:28:04" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:28:04" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/opyt-primeneniya-terapii-ii-linii-retsidivov-i-rezistentnykh-form-limfomy-khodzhkina-v-irkutskoy-obl/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/opyt-primeneniya-terapii-ii-linii-retsidivov-i-rezistentnykh-form-limfomy-khodzhkina-v-irkutskoy-obl/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "opyt-primeneniya-terapii-ii-linii-retsidivov-i-rezistentnykh-form-limfomy-khodzhkina-v-irkutskoy-obl" ["~CODE"]=> string(100) "opyt-primeneniya-terapii-ii-linii-retsidivov-i-rezistentnykh-form-limfomy-khodzhkina-v-irkutskoy-obl" ["EXTERNAL_ID"]=> string(4) "1559" ["~EXTERNAL_ID"]=> string(4) "1559" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(183) "Опыт применения терапии II линии рецидивов и резистентных форм лимфомы Ходжкина в Иркутской области" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(289) "Опыт применения терапии II линии рецидивов и резистентных форм лимфомы Ходжкина в Иркутской областиExperience with second-line therapy of relapsing and refractory Hodgkin’s lymphoma in the Irkutsk region" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(5757) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Ежегодно на базе Иркутского онкологического диспансера диагностируется 50 новых случаев лимфомы Ходжкина. Несмотря на достигнутые успехи в лечении лимфомы Ходжкина, проблемой терапии является развитие рецидивов заболевания и первичной/вторичной резистентности у 10-25% больных. Применение высокодозной химиотерапии (ВДХТ) с ауто-ТГСК является стандартом терапии при рецидивах и резистентных формах ЛХ. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Оценить эффективность и безопасность II линии терапии у больных с рецидивами и резистентными формами лимфомы Ходжина в Иркутском областном онкологическом диспансере за 2-х летний период (2016-2018). </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Проведен анализ течения заболевания 11 пациентов с ЛХ, госпитализированных в Иркутский онкологический диспансер с января 2016 по июнь 2018 г для проведения II линии терапии. Медиана возраста пациентов составила 34 года (22-46). Распределение по полу: мужчин – 6, женщин – 5. Преобладали пациенты с распространенными стадиями заболевания: 8 – III-IV стадия, и лишь у 3 – II стадия ЛХ. Среднее количество циклов терапии 1 линии – 15 (от 8 до 25 циклов). Все пациенты в качестве индукционной терапии получили ПХТ по схеме ABVD и BEACOPP, лучевая терапия проводилась 10 пациентам. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> На момент начала II линии терапии 5 человек имели рецидив ЛХ: ранний (n=2) и поздний (n=2), у 6 человек регистрировалась резистентность к проводимой терапии: первичная (n=2), вторичная (n=4). Медиана времени от момента диагностики ЛХ до проведения трансплантации составила 1 год (1 год – 10 лет 9 мес.). Все пациенты получили кондиционирование по протоколу BeEAM. Стволовые кроветворные клетки получали из костного мозга (n=1), периферической крови (n=10). Клеточность трансплантанта в среднем составляла 7,99х106/кг. В качестве подготовки к ВДХТ с ауто-ТГСК проводились курсы терапии по программе DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). Статус ЛХ на момент ауто-ТГСК: полная ремиссия (ПР) – 5 пациентов, частичная ремиссия (ЧР) – 5, нет ответа – 1 больной. Летальность, связанная с ВДХТ и ауто-ТГСК на «день 100» составила 0%. Оценка ответа по завершении терапии II линии проведена у 9 пациентов: полная ремиссия была достигнута у 6 пациентов (67%), у 3-х пациентов (33%) не получено ответа на проводимую терапию, что вероятно обусловлено отсутствием достижения полной ремиссии перед ауто-ТГСК (n=1) и длительным интервалом времени до ВДХТ. Общая выживаемость 100%, с медианой наблюдения 18 месяцев от начала II линии терапии. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Наш опыт подтверждает безопасность II линии терапии, включающей ВДХТ с ауто-ТГСК для лечения рефрактерных форм ЛХ. Эффективность II линии зависит от от достижения полной ремиссии до ауто-ТГКС и интервалом времени от момента диагностики ЛХ до проведения ВДХТ с ауто-ТГСК. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфома Ходжкина, рецидив, рефрактерность, высокодозная химиотерапия, ауто-ТГСК. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(183) "Опыт применения терапии II линии рецидивов и резистентных форм лимфомы Ходжкина в Иркутской области" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(183) "Опыт применения терапии II линии рецидивов и резистентных форм лимфомы Ходжкина в Иркутской области" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(183) "Опыт применения терапии II линии рецидивов и резистентных форм лимфомы Ходжкина в Иркутской области" ["SECTION_META_TITLE"]=> string(183) "Опыт применения терапии II линии рецидивов и резистентных форм лимфомы Ходжкина в Иркутской области" ["SECTION_META_KEYWORDS"]=> string(183) "Опыт применения терапии II линии рецидивов и резистентных форм лимфомы Ходжкина в Иркутской области" ["SECTION_META_DESCRIPTION"]=> string(183) "Опыт применения терапии II линии рецидивов и резистентных форм лимфомы Ходжкина в Иркутской области" ["SECTION_PICTURE_FILE_ALT"]=> string(183) "Опыт применения терапии II линии рецидивов и резистентных форм лимфомы Ходжкина в Иркутской области" ["SECTION_PICTURE_FILE_TITLE"]=> string(183) "Опыт применения терапии II линии рецидивов и резистентных форм лимфомы Ходжкина в Иркутской области" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "opyt-primeneniya-terapii-ii-linii-retsidivov-i-rezistentnykh-form-limfomy-khodzhkina-v-irkutskoy-obl" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(183) "Опыт применения терапии II линии рецидивов и резистентных форм лимфомы Ходжкина в Иркутской области" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(183) "Опыт применения терапии II линии рецидивов и резистентных форм лимфомы Ходжкина в Иркутской области" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "opyt-primeneniya-terapii-ii-linii-retsidivov-i-rezistentnykh-form-limfomy-khodzhkina-v-irkutskoy-obl" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "opyt-primeneniya-terapii-ii-linii-retsidivov-i-rezistentnykh-form-limfomy-khodzhkina-v-irkutskoy-obl" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "opyt-primeneniya-terapii-ii-linii-retsidivov-i-rezistentnykh-form-limfomy-khodzhkina-v-irkutskoy-obl" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20364" ["VALUE"]=> array(2) { ["TEXT"]=> string(280) "Марина В. Демченкова, Екатерина В. Зубкова, Дмитрий Д. Мориков, Людмила Е. Иванова, Анна В. Шевчук, Зоя В. Дьяконенко, Алена Л. Хороших, Александра Ю. Ефиркина" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(280) "Марина В. Демченкова, Екатерина В. Зубкова, Дмитрий Д. Мориков, Людмила Е. Иванова, Анна В. Шевчук, Зоя В. Дьяконенко, Алена Л. Хороших, Александра Ю. Ефиркина" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20365" ["VALUE"]=> array(2) { ["TEXT"]=> string(109) "ГБУЗ «Областной онкологический диспансер», Иркутск, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(109) "ГБУЗ «Областной онкологический диспансер», Иркутск, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20366" ["VALUE"]=> array(2) { ["TEXT"]=> string(5757) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Ежегодно на базе Иркутского онкологического диспансера диагностируется 50 новых случаев лимфомы Ходжкина. Несмотря на достигнутые успехи в лечении лимфомы Ходжкина, проблемой терапии является развитие рецидивов заболевания и первичной/вторичной резистентности у 10-25% больных. Применение высокодозной химиотерапии (ВДХТ) с ауто-ТГСК является стандартом терапии при рецидивах и резистентных формах ЛХ. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Оценить эффективность и безопасность II линии терапии у больных с рецидивами и резистентными формами лимфомы Ходжина в Иркутском областном онкологическом диспансере за 2-х летний период (2016-2018). </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Проведен анализ течения заболевания 11 пациентов с ЛХ, госпитализированных в Иркутский онкологический диспансер с января 2016 по июнь 2018 г для проведения II линии терапии. Медиана возраста пациентов составила 34 года (22-46). Распределение по полу: мужчин – 6, женщин – 5. Преобладали пациенты с распространенными стадиями заболевания: 8 – III-IV стадия, и лишь у 3 – II стадия ЛХ. Среднее количество циклов терапии 1 линии – 15 (от 8 до 25 циклов). Все пациенты в качестве индукционной терапии получили ПХТ по схеме ABVD и BEACOPP, лучевая терапия проводилась 10 пациентам. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> На момент начала II линии терапии 5 человек имели рецидив ЛХ: ранний (n=2) и поздний (n=2), у 6 человек регистрировалась резистентность к проводимой терапии: первичная (n=2), вторичная (n=4). Медиана времени от момента диагностики ЛХ до проведения трансплантации составила 1 год (1 год – 10 лет 9 мес.). Все пациенты получили кондиционирование по протоколу BeEAM. Стволовые кроветворные клетки получали из костного мозга (n=1), периферической крови (n=10). Клеточность трансплантанта в среднем составляла 7,99х106/кг. В качестве подготовки к ВДХТ с ауто-ТГСК проводились курсы терапии по программе DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). Статус ЛХ на момент ауто-ТГСК: полная ремиссия (ПР) – 5 пациентов, частичная ремиссия (ЧР) – 5, нет ответа – 1 больной. Летальность, связанная с ВДХТ и ауто-ТГСК на «день 100» составила 0%. Оценка ответа по завершении терапии II линии проведена у 9 пациентов: полная ремиссия была достигнута у 6 пациентов (67%), у 3-х пациентов (33%) не получено ответа на проводимую терапию, что вероятно обусловлено отсутствием достижения полной ремиссии перед ауто-ТГСК (n=1) и длительным интервалом времени до ВДХТ. Общая выживаемость 100%, с медианой наблюдения 18 месяцев от начала II линии терапии. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Наш опыт подтверждает безопасность II линии терапии, включающей ВДХТ с ауто-ТГСК для лечения рефрактерных форм ЛХ. Эффективность II линии зависит от от достижения полной ремиссии до ауто-ТГКС и интервалом времени от момента диагностики ЛХ до проведения ВДХТ с ауто-ТГСК. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфома Ходжкина, рецидив, рефрактерность, высокодозная химиотерапия, ауто-ТГСК. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5493) "
Введение
Ежегодно на базе Иркутского онкологического диспансера диагностируется 50 новых случаев лимфомы Ходжкина. Несмотря на достигнутые успехи в лечении лимфомы Ходжкина, проблемой терапии является развитие рецидивов заболевания и первичной/вторичной резистентности у 10-25% больных. Применение высокодозной химиотерапии (ВДХТ) с ауто-ТГСК является стандартом терапии при рецидивах и резистентных формах ЛХ.
Цель
Оценить эффективность и безопасность II линии терапии у больных с рецидивами и резистентными формами лимфомы Ходжина в Иркутском областном онкологическом диспансере за 2-х летний период (2016-2018).
Пациенты и методы
Проведен анализ течения заболевания 11 пациентов с ЛХ, госпитализированных в Иркутский онкологический диспансер с января 2016 по июнь 2018 г для проведения II линии терапии. Медиана возраста пациентов составила 34 года (22-46). Распределение по полу: мужчин – 6, женщин – 5. Преобладали пациенты с распространенными стадиями заболевания: 8 – III-IV стадия, и лишь у 3 – II стадия ЛХ. Среднее количество циклов терапии 1 линии – 15 (от 8 до 25 циклов). Все пациенты в качестве индукционной терапии получили ПХТ по схеме ABVD и BEACOPP, лучевая терапия проводилась 10 пациентам.
Результаты
На момент начала II линии терапии 5 человек имели рецидив ЛХ: ранний (n=2) и поздний (n=2), у 6 человек регистрировалась резистентность к проводимой терапии: первичная (n=2), вторичная (n=4). Медиана времени от момента диагностики ЛХ до проведения трансплантации составила 1 год (1 год – 10 лет 9 мес.). Все пациенты получили кондиционирование по протоколу BeEAM. Стволовые кроветворные клетки получали из костного мозга (n=1), периферической крови (n=10). Клеточность трансплантанта в среднем составляла 7,99х106/кг. В качестве подготовки к ВДХТ с ауто-ТГСК проводились курсы терапии по программе DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). Статус ЛХ на момент ауто-ТГСК: полная ремиссия (ПР) – 5 пациентов, частичная ремиссия (ЧР) – 5, нет ответа – 1 больной. Летальность, связанная с ВДХТ и ауто-ТГСК на «день 100» составила 0%. Оценка ответа по завершении терапии II линии проведена у 9 пациентов: полная ремиссия была достигнута у 6 пациентов (67%), у 3-х пациентов (33%) не получено ответа на проводимую терапию, что вероятно обусловлено отсутствием достижения полной ремиссии перед ауто-ТГСК (n=1) и длительным интервалом времени до ВДХТ. Общая выживаемость 100%, с медианой наблюдения 18 месяцев от начала II линии терапии.
Заключение
Наш опыт подтверждает безопасность II линии терапии, включающей ВДХТ с ауто-ТГСК для лечения рефрактерных форм ЛХ. Эффективность II линии зависит от от достижения полной ремиссии до ауто-ТГКС и интервалом времени от момента диагностики ЛХ до проведения ВДХТ с ауто-ТГСК.
Ключевые слова
Лимфома Ходжкина, рецидив, рефрактерность, высокодозная химиотерапия, ауто-ТГСК.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20367" ["VALUE"]=> array(2) { ["TEXT"]=> string(167) "Marina V. Demchenkova, Ekaterina V. Zubkova, Dmitriy D. Morikov, Lyudmila E. Ivanova, Anna V. Shevchuk, Zoya V. Dyakonenko, Alena L. Khoroshikh, Alexandra Yu. Efirkina" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(167) "Marina V. Demchenkova, Ekaterina V. Zubkova, Dmitriy D. Morikov, Lyudmila E. Ivanova, Anna V. Shevchuk, Zoya V. Dyakonenko, Alena L. Khoroshikh, Alexandra Yu. Efirkina" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20368" ["VALUE"]=> array(2) { ["TEXT"]=> string(80) "State Regional Clinical Hospital “Regional Oncology Center”, Irkutsk, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(80) "State Regional Clinical Hospital “Regional Oncology Center”, Irkutsk, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20369" ["VALUE"]=> array(2) { ["TEXT"]=> string(3328) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Fifty new cases of Hodgkin’s lymphoma (HL) are diagnosed annually in the Irkutsk Oncology Center. Despite the successes achieved in the treatment of HL from 10 to 25% of patients have refractory or relapse. The high-dose chemotherapy (HDCT) followed by auto-SCT is the standard therapy of relapsed/refractory HL. Purpose of our study was to estimate efficacy and safety of second line therapy in patients with relapsed/refractory HL in the Irkutsk Regional Oncology Center for a 2-year period (2016-2018). </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> The analysis of 11 case of relapsed/refractory HL have been performed, which have been treated with second line therapy in the Irkutsk Oncology Clinic from January 2016 till June 2018. The median age of the patients was 34 years (22-46). The distribution by sex: men – 6, women – 5. There was prevalence of patients with advanced stages of the disease: stage III-IV (n=8), and only in 3 patients – second stage. The average number of cycles of first line therapy was 15 (from 8 to 25 cycles). All patients received first line chemo with ABVD and BEACOPP, and 10 patients have undergone radiotherapy. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> At the time of second line initiation 5 patients had a relapse of HL: early (n=2), late (n=3), 6 patients had resistance to the therapy: primary (n=2), secondary (n=4). The median time from the diagnosis of HL till the SCT was 1 year (1 year – 10 years 9 months.). Conditioning regimen according to the BeEAM protocol have been used for all patients. Stem cells source was: bone marrow (n=1), peripheral blood (n=10). The mean of stem cells in graft was 7.99x106/kg. The remission re-induction chemotherapy included: DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). The effect of re-induction chemotherapy was: complete remission (n=5), partial remission (n=5), no response – 1 patient. The mortality rate at day 100 was 0%. Evaluation of the response after complete second line therapy was performed in 9 patients: complete remission was achieved in 6 patients (67%), 3 patients (33%) no response was received to the therapy, which is probably due to the lack of complete remission in front of auto-SCT (n=1) and a long time interval up to the HDCT. Overall survival was 100% with the medial follow up time – 18 months. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Our experience confirms the safety of the second line of therapy, including HDCT with auto-SCT for the treatment of relapsed/refractory HL, and also demonstrates that the efficacy depends on the time from the moment of diagnosis of HL to transplant and the status of the underlying disease at the moment of auto-SCT. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hodgkin’s lymphoma, relapse, refractoriness, high-dose chemotherapy, auto-SCT. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3108) "Introduction
Fifty new cases of Hodgkin’s lymphoma (HL) are diagnosed annually in the Irkutsk Oncology Center. Despite the successes achieved in the treatment of HL from 10 to 25% of patients have refractory or relapse. The high-dose chemotherapy (HDCT) followed by auto-SCT is the standard therapy of relapsed/refractory HL. Purpose of our study was to estimate efficacy and safety of second line therapy in patients with relapsed/refractory HL in the Irkutsk Regional Oncology Center for a 2-year period (2016-2018).
Patients and methods
The analysis of 11 case of relapsed/refractory HL have been performed, which have been treated with second line therapy in the Irkutsk Oncology Clinic from January 2016 till June 2018. The median age of the patients was 34 years (22-46). The distribution by sex: men – 6, women – 5. There was prevalence of patients with advanced stages of the disease: stage III-IV (n=8), and only in 3 patients – second stage. The average number of cycles of first line therapy was 15 (from 8 to 25 cycles). All patients received first line chemo with ABVD and BEACOPP, and 10 patients have undergone radiotherapy.
Results
At the time of second line initiation 5 patients had a relapse of HL: early (n=2), late (n=3), 6 patients had resistance to the therapy: primary (n=2), secondary (n=4). The median time from the diagnosis of HL till the SCT was 1 year (1 year – 10 years 9 months.). Conditioning regimen according to the BeEAM protocol have been used for all patients. Stem cells source was: bone marrow (n=1), peripheral blood (n=10). The mean of stem cells in graft was 7.99x106/kg. The remission re-induction chemotherapy included: DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). The effect of re-induction chemotherapy was: complete remission (n=5), partial remission (n=5), no response – 1 patient. The mortality rate at day 100 was 0%. Evaluation of the response after complete second line therapy was performed in 9 patients: complete remission was achieved in 6 patients (67%), 3 patients (33%) no response was received to the therapy, which is probably due to the lack of complete remission in front of auto-SCT (n=1) and a long time interval up to the HDCT. Overall survival was 100% with the medial follow up time – 18 months.
Conclusion
Our experience confirms the safety of the second line of therapy, including HDCT with auto-SCT for the treatment of relapsed/refractory HL, and also demonstrates that the efficacy depends on the time from the moment of diagnosis of HL to transplant and the status of the underlying disease at the moment of auto-SCT.
Keywords
Hodgkin’s lymphoma, relapse, refractoriness, high-dose chemotherapy, auto-SCT.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20370" ["VALUE"]=> string(106) "Experience with second-line therapy of relapsing and refractory Hodgkin’s lymphoma in the Irkutsk region" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(106) "Experience with second-line therapy of relapsing and refractory Hodgkin’s lymphoma in the Irkutsk region" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20751" ["VALUE"]=> string(4) "1387" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1387" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20752" ["VALUE"]=> string(4) "1388" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1388" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20367" ["VALUE"]=> array(2) { ["TEXT"]=> string(167) "Marina V. Demchenkova, Ekaterina V. Zubkova, Dmitriy D. Morikov, Lyudmila E. Ivanova, Anna V. Shevchuk, Zoya V. Dyakonenko, Alena L. Khoroshikh, Alexandra Yu. Efirkina" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(167) "Marina V. Demchenkova, Ekaterina V. Zubkova, Dmitriy D. Morikov, Lyudmila E. Ivanova, Anna V. Shevchuk, Zoya V. Dyakonenko, Alena L. Khoroshikh, Alexandra Yu. Efirkina" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(167) "Marina V. Demchenkova, Ekaterina V. Zubkova, Dmitriy D. Morikov, Lyudmila E. Ivanova, Anna V. Shevchuk, Zoya V. Dyakonenko, Alena L. Khoroshikh, Alexandra Yu. Efirkina" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20369" ["VALUE"]=> array(2) { ["TEXT"]=> string(3328) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Fifty new cases of Hodgkin’s lymphoma (HL) are diagnosed annually in the Irkutsk Oncology Center. Despite the successes achieved in the treatment of HL from 10 to 25% of patients have refractory or relapse. The high-dose chemotherapy (HDCT) followed by auto-SCT is the standard therapy of relapsed/refractory HL. Purpose of our study was to estimate efficacy and safety of second line therapy in patients with relapsed/refractory HL in the Irkutsk Regional Oncology Center for a 2-year period (2016-2018). </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> The analysis of 11 case of relapsed/refractory HL have been performed, which have been treated with second line therapy in the Irkutsk Oncology Clinic from January 2016 till June 2018. The median age of the patients was 34 years (22-46). The distribution by sex: men – 6, women – 5. There was prevalence of patients with advanced stages of the disease: stage III-IV (n=8), and only in 3 patients – second stage. The average number of cycles of first line therapy was 15 (from 8 to 25 cycles). All patients received first line chemo with ABVD and BEACOPP, and 10 patients have undergone radiotherapy. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> At the time of second line initiation 5 patients had a relapse of HL: early (n=2), late (n=3), 6 patients had resistance to the therapy: primary (n=2), secondary (n=4). The median time from the diagnosis of HL till the SCT was 1 year (1 year – 10 years 9 months.). Conditioning regimen according to the BeEAM protocol have been used for all patients. Stem cells source was: bone marrow (n=1), peripheral blood (n=10). The mean of stem cells in graft was 7.99x106/kg. The remission re-induction chemotherapy included: DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). The effect of re-induction chemotherapy was: complete remission (n=5), partial remission (n=5), no response – 1 patient. The mortality rate at day 100 was 0%. Evaluation of the response after complete second line therapy was performed in 9 patients: complete remission was achieved in 6 patients (67%), 3 patients (33%) no response was received to the therapy, which is probably due to the lack of complete remission in front of auto-SCT (n=1) and a long time interval up to the HDCT. Overall survival was 100% with the medial follow up time – 18 months. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Our experience confirms the safety of the second line of therapy, including HDCT with auto-SCT for the treatment of relapsed/refractory HL, and also demonstrates that the efficacy depends on the time from the moment of diagnosis of HL to transplant and the status of the underlying disease at the moment of auto-SCT. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hodgkin’s lymphoma, relapse, refractoriness, high-dose chemotherapy, auto-SCT. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3108) "Introduction
Fifty new cases of Hodgkin’s lymphoma (HL) are diagnosed annually in the Irkutsk Oncology Center. Despite the successes achieved in the treatment of HL from 10 to 25% of patients have refractory or relapse. The high-dose chemotherapy (HDCT) followed by auto-SCT is the standard therapy of relapsed/refractory HL. Purpose of our study was to estimate efficacy and safety of second line therapy in patients with relapsed/refractory HL in the Irkutsk Regional Oncology Center for a 2-year period (2016-2018).
Patients and methods
The analysis of 11 case of relapsed/refractory HL have been performed, which have been treated with second line therapy in the Irkutsk Oncology Clinic from January 2016 till June 2018. The median age of the patients was 34 years (22-46). The distribution by sex: men – 6, women – 5. There was prevalence of patients with advanced stages of the disease: stage III-IV (n=8), and only in 3 patients – second stage. The average number of cycles of first line therapy was 15 (from 8 to 25 cycles). All patients received first line chemo with ABVD and BEACOPP, and 10 patients have undergone radiotherapy.
Results
At the time of second line initiation 5 patients had a relapse of HL: early (n=2), late (n=3), 6 patients had resistance to the therapy: primary (n=2), secondary (n=4). The median time from the diagnosis of HL till the SCT was 1 year (1 year – 10 years 9 months.). Conditioning regimen according to the BeEAM protocol have been used for all patients. Stem cells source was: bone marrow (n=1), peripheral blood (n=10). The mean of stem cells in graft was 7.99x106/kg. The remission re-induction chemotherapy included: DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). The effect of re-induction chemotherapy was: complete remission (n=5), partial remission (n=5), no response – 1 patient. The mortality rate at day 100 was 0%. Evaluation of the response after complete second line therapy was performed in 9 patients: complete remission was achieved in 6 patients (67%), 3 patients (33%) no response was received to the therapy, which is probably due to the lack of complete remission in front of auto-SCT (n=1) and a long time interval up to the HDCT. Overall survival was 100% with the medial follow up time – 18 months.
Conclusion
Our experience confirms the safety of the second line of therapy, including HDCT with auto-SCT for the treatment of relapsed/refractory HL, and also demonstrates that the efficacy depends on the time from the moment of diagnosis of HL to transplant and the status of the underlying disease at the moment of auto-SCT.
Keywords
Hodgkin’s lymphoma, relapse, refractoriness, high-dose chemotherapy, auto-SCT.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3108) "Introduction
Fifty new cases of Hodgkin’s lymphoma (HL) are diagnosed annually in the Irkutsk Oncology Center. Despite the successes achieved in the treatment of HL from 10 to 25% of patients have refractory or relapse. The high-dose chemotherapy (HDCT) followed by auto-SCT is the standard therapy of relapsed/refractory HL. Purpose of our study was to estimate efficacy and safety of second line therapy in patients with relapsed/refractory HL in the Irkutsk Regional Oncology Center for a 2-year period (2016-2018).
Patients and methods
The analysis of 11 case of relapsed/refractory HL have been performed, which have been treated with second line therapy in the Irkutsk Oncology Clinic from January 2016 till June 2018. The median age of the patients was 34 years (22-46). The distribution by sex: men – 6, women – 5. There was prevalence of patients with advanced stages of the disease: stage III-IV (n=8), and only in 3 patients – second stage. The average number of cycles of first line therapy was 15 (from 8 to 25 cycles). All patients received first line chemo with ABVD and BEACOPP, and 10 patients have undergone radiotherapy.
Results
At the time of second line initiation 5 patients had a relapse of HL: early (n=2), late (n=3), 6 patients had resistance to the therapy: primary (n=2), secondary (n=4). The median time from the diagnosis of HL till the SCT was 1 year (1 year – 10 years 9 months.). Conditioning regimen according to the BeEAM protocol have been used for all patients. Stem cells source was: bone marrow (n=1), peripheral blood (n=10). The mean of stem cells in graft was 7.99x106/kg. The remission re-induction chemotherapy included: DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). The effect of re-induction chemotherapy was: complete remission (n=5), partial remission (n=5), no response – 1 patient. The mortality rate at day 100 was 0%. Evaluation of the response after complete second line therapy was performed in 9 patients: complete remission was achieved in 6 patients (67%), 3 patients (33%) no response was received to the therapy, which is probably due to the lack of complete remission in front of auto-SCT (n=1) and a long time interval up to the HDCT. Overall survival was 100% with the medial follow up time – 18 months.
Conclusion
Our experience confirms the safety of the second line of therapy, including HDCT with auto-SCT for the treatment of relapsed/refractory HL, and also demonstrates that the efficacy depends on the time from the moment of diagnosis of HL to transplant and the status of the underlying disease at the moment of auto-SCT.
Keywords
Hodgkin’s lymphoma, relapse, refractoriness, high-dose chemotherapy, auto-SCT.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20370" ["VALUE"]=> string(106) "Experience with second-line therapy of relapsing and refractory Hodgkin’s lymphoma in the Irkutsk region" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(106) "Experience with second-line therapy of relapsing and refractory Hodgkin’s lymphoma in the Irkutsk region" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(106) "Experience with second-line therapy of relapsing and refractory Hodgkin’s lymphoma in the Irkutsk region" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20368" ["VALUE"]=> array(2) { ["TEXT"]=> string(80) "State Regional Clinical Hospital “Regional Oncology Center”, Irkutsk, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(80) "State Regional Clinical Hospital “Regional Oncology Center”, Irkutsk, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(80) "State Regional Clinical Hospital “Regional Oncology Center”, Irkutsk, Russia" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20364" ["VALUE"]=> array(2) { ["TEXT"]=> string(280) "Марина В. Демченкова, Екатерина В. Зубкова, Дмитрий Д. Мориков, Людмила Е. Иванова, Анна В. Шевчук, Зоя В. Дьяконенко, Алена Л. Хороших, Александра Ю. Ефиркина" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(280) "Марина В. Демченкова, Екатерина В. Зубкова, Дмитрий Д. Мориков, Людмила Е. Иванова, Анна В. Шевчук, Зоя В. Дьяконенко, Алена Л. Хороших, Александра Ю. Ефиркина" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(280) "Марина В. Демченкова, Екатерина В. Зубкова, Дмитрий Д. Мориков, Людмила Е. Иванова, Анна В. Шевчук, Зоя В. Дьяконенко, Алена Л. Хороших, Александра Ю. Ефиркина" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20366" ["VALUE"]=> array(2) { ["TEXT"]=> string(5757) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Ежегодно на базе Иркутского онкологического диспансера диагностируется 50 новых случаев лимфомы Ходжкина. Несмотря на достигнутые успехи в лечении лимфомы Ходжкина, проблемой терапии является развитие рецидивов заболевания и первичной/вторичной резистентности у 10-25% больных. Применение высокодозной химиотерапии (ВДХТ) с ауто-ТГСК является стандартом терапии при рецидивах и резистентных формах ЛХ. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Оценить эффективность и безопасность II линии терапии у больных с рецидивами и резистентными формами лимфомы Ходжина в Иркутском областном онкологическом диспансере за 2-х летний период (2016-2018). </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Проведен анализ течения заболевания 11 пациентов с ЛХ, госпитализированных в Иркутский онкологический диспансер с января 2016 по июнь 2018 г для проведения II линии терапии. Медиана возраста пациентов составила 34 года (22-46). Распределение по полу: мужчин – 6, женщин – 5. Преобладали пациенты с распространенными стадиями заболевания: 8 – III-IV стадия, и лишь у 3 – II стадия ЛХ. Среднее количество циклов терапии 1 линии – 15 (от 8 до 25 циклов). Все пациенты в качестве индукционной терапии получили ПХТ по схеме ABVD и BEACOPP, лучевая терапия проводилась 10 пациентам. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> На момент начала II линии терапии 5 человек имели рецидив ЛХ: ранний (n=2) и поздний (n=2), у 6 человек регистрировалась резистентность к проводимой терапии: первичная (n=2), вторичная (n=4). Медиана времени от момента диагностики ЛХ до проведения трансплантации составила 1 год (1 год – 10 лет 9 мес.). Все пациенты получили кондиционирование по протоколу BeEAM. Стволовые кроветворные клетки получали из костного мозга (n=1), периферической крови (n=10). Клеточность трансплантанта в среднем составляла 7,99х106/кг. В качестве подготовки к ВДХТ с ауто-ТГСК проводились курсы терапии по программе DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). Статус ЛХ на момент ауто-ТГСК: полная ремиссия (ПР) – 5 пациентов, частичная ремиссия (ЧР) – 5, нет ответа – 1 больной. Летальность, связанная с ВДХТ и ауто-ТГСК на «день 100» составила 0%. Оценка ответа по завершении терапии II линии проведена у 9 пациентов: полная ремиссия была достигнута у 6 пациентов (67%), у 3-х пациентов (33%) не получено ответа на проводимую терапию, что вероятно обусловлено отсутствием достижения полной ремиссии перед ауто-ТГСК (n=1) и длительным интервалом времени до ВДХТ. Общая выживаемость 100%, с медианой наблюдения 18 месяцев от начала II линии терапии. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Наш опыт подтверждает безопасность II линии терапии, включающей ВДХТ с ауто-ТГСК для лечения рефрактерных форм ЛХ. Эффективность II линии зависит от от достижения полной ремиссии до ауто-ТГКС и интервалом времени от момента диагностики ЛХ до проведения ВДХТ с ауто-ТГСК. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфома Ходжкина, рецидив, рефрактерность, высокодозная химиотерапия, ауто-ТГСК. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5493) "Введение
Ежегодно на базе Иркутского онкологического диспансера диагностируется 50 новых случаев лимфомы Ходжкина. Несмотря на достигнутые успехи в лечении лимфомы Ходжкина, проблемой терапии является развитие рецидивов заболевания и первичной/вторичной резистентности у 10-25% больных. Применение высокодозной химиотерапии (ВДХТ) с ауто-ТГСК является стандартом терапии при рецидивах и резистентных формах ЛХ.
Цель
Оценить эффективность и безопасность II линии терапии у больных с рецидивами и резистентными формами лимфомы Ходжина в Иркутском областном онкологическом диспансере за 2-х летний период (2016-2018).
Пациенты и методы
Проведен анализ течения заболевания 11 пациентов с ЛХ, госпитализированных в Иркутский онкологический диспансер с января 2016 по июнь 2018 г для проведения II линии терапии. Медиана возраста пациентов составила 34 года (22-46). Распределение по полу: мужчин – 6, женщин – 5. Преобладали пациенты с распространенными стадиями заболевания: 8 – III-IV стадия, и лишь у 3 – II стадия ЛХ. Среднее количество циклов терапии 1 линии – 15 (от 8 до 25 циклов). Все пациенты в качестве индукционной терапии получили ПХТ по схеме ABVD и BEACOPP, лучевая терапия проводилась 10 пациентам.
Результаты
На момент начала II линии терапии 5 человек имели рецидив ЛХ: ранний (n=2) и поздний (n=2), у 6 человек регистрировалась резистентность к проводимой терапии: первичная (n=2), вторичная (n=4). Медиана времени от момента диагностики ЛХ до проведения трансплантации составила 1 год (1 год – 10 лет 9 мес.). Все пациенты получили кондиционирование по протоколу BeEAM. Стволовые кроветворные клетки получали из костного мозга (n=1), периферической крови (n=10). Клеточность трансплантанта в среднем составляла 7,99х106/кг. В качестве подготовки к ВДХТ с ауто-ТГСК проводились курсы терапии по программе DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). Статус ЛХ на момент ауто-ТГСК: полная ремиссия (ПР) – 5 пациентов, частичная ремиссия (ЧР) – 5, нет ответа – 1 больной. Летальность, связанная с ВДХТ и ауто-ТГСК на «день 100» составила 0%. Оценка ответа по завершении терапии II линии проведена у 9 пациентов: полная ремиссия была достигнута у 6 пациентов (67%), у 3-х пациентов (33%) не получено ответа на проводимую терапию, что вероятно обусловлено отсутствием достижения полной ремиссии перед ауто-ТГСК (n=1) и длительным интервалом времени до ВДХТ. Общая выживаемость 100%, с медианой наблюдения 18 месяцев от начала II линии терапии.
Заключение
Наш опыт подтверждает безопасность II линии терапии, включающей ВДХТ с ауто-ТГСК для лечения рефрактерных форм ЛХ. Эффективность II линии зависит от от достижения полной ремиссии до ауто-ТГКС и интервалом времени от момента диагностики ЛХ до проведения ВДХТ с ауто-ТГСК.
Ключевые слова
Лимфома Ходжкина, рецидив, рефрактерность, высокодозная химиотерапия, ауто-ТГСК.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(5493) "Введение
Ежегодно на базе Иркутского онкологического диспансера диагностируется 50 новых случаев лимфомы Ходжкина. Несмотря на достигнутые успехи в лечении лимфомы Ходжкина, проблемой терапии является развитие рецидивов заболевания и первичной/вторичной резистентности у 10-25% больных. Применение высокодозной химиотерапии (ВДХТ) с ауто-ТГСК является стандартом терапии при рецидивах и резистентных формах ЛХ.
Цель
Оценить эффективность и безопасность II линии терапии у больных с рецидивами и резистентными формами лимфомы Ходжина в Иркутском областном онкологическом диспансере за 2-х летний период (2016-2018).
Пациенты и методы
Проведен анализ течения заболевания 11 пациентов с ЛХ, госпитализированных в Иркутский онкологический диспансер с января 2016 по июнь 2018 г для проведения II линии терапии. Медиана возраста пациентов составила 34 года (22-46). Распределение по полу: мужчин – 6, женщин – 5. Преобладали пациенты с распространенными стадиями заболевания: 8 – III-IV стадия, и лишь у 3 – II стадия ЛХ. Среднее количество циклов терапии 1 линии – 15 (от 8 до 25 циклов). Все пациенты в качестве индукционной терапии получили ПХТ по схеме ABVD и BEACOPP, лучевая терапия проводилась 10 пациентам.
Результаты
На момент начала II линии терапии 5 человек имели рецидив ЛХ: ранний (n=2) и поздний (n=2), у 6 человек регистрировалась резистентность к проводимой терапии: первичная (n=2), вторичная (n=4). Медиана времени от момента диагностики ЛХ до проведения трансплантации составила 1 год (1 год – 10 лет 9 мес.). Все пациенты получили кондиционирование по протоколу BeEAM. Стволовые кроветворные клетки получали из костного мозга (n=1), периферической крови (n=10). Клеточность трансплантанта в среднем составляла 7,99х106/кг. В качестве подготовки к ВДХТ с ауто-ТГСК проводились курсы терапии по программе DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). Статус ЛХ на момент ауто-ТГСК: полная ремиссия (ПР) – 5 пациентов, частичная ремиссия (ЧР) – 5, нет ответа – 1 больной. Летальность, связанная с ВДХТ и ауто-ТГСК на «день 100» составила 0%. Оценка ответа по завершении терапии II линии проведена у 9 пациентов: полная ремиссия была достигнута у 6 пациентов (67%), у 3-х пациентов (33%) не получено ответа на проводимую терапию, что вероятно обусловлено отсутствием достижения полной ремиссии перед ауто-ТГСК (n=1) и длительным интервалом времени до ВДХТ. Общая выживаемость 100%, с медианой наблюдения 18 месяцев от начала II линии терапии.
Заключение
Наш опыт подтверждает безопасность II линии терапии, включающей ВДХТ с ауто-ТГСК для лечения рефрактерных форм ЛХ. Эффективность II линии зависит от от достижения полной ремиссии до ауто-ТГКС и интервалом времени от момента диагностики ЛХ до проведения ВДХТ с ауто-ТГСК.
Ключевые слова
Лимфома Ходжкина, рецидив, рефрактерность, высокодозная химиотерапия, ауто-ТГСК.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20365" ["VALUE"]=> array(2) { ["TEXT"]=> string(109) "ГБУЗ «Областной онкологический диспансер», Иркутск, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(109) "ГБУЗ «Областной онкологический диспансер», Иркутск, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(109) "ГБУЗ «Областной онкологический диспансер», Иркутск, Россия" } } } [24]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1558" ["~ID"]=> string(4) "1558" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(298) "Результаты гистологических и вирусологических исследований в диагностике острой реакции трансплантат против хозяина с повреждением желудочно-кишечного тракта" ["~NAME"]=> string(298) "Результаты гистологических и вирусологических исследований в диагностике острой реакции трансплантат против хозяина с повреждением желудочно-кишечного тракта" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:27:35" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:27:35" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/rezultaty-gistologicheskikh-i-virusologicheskikh-issledovaniy-v-diagnostike-ostroy-reaktsii-transpla/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/rezultaty-gistologicheskikh-i-virusologicheskikh-issledovaniy-v-diagnostike-ostroy-reaktsii-transpla/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "rezultaty-gistologicheskikh-i-virusologicheskikh-issledovaniy-v-diagnostike-ostroy-reaktsii-transpla" ["~CODE"]=> string(100) "rezultaty-gistologicheskikh-i-virusologicheskikh-issledovaniy-v-diagnostike-ostroy-reaktsii-transpla" ["EXTERNAL_ID"]=> string(4) "1558" ["~EXTERNAL_ID"]=> string(4) "1558" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(298) "Результаты гистологических и вирусологических исследований в диагностике острой реакции трансплантат против хозяина с повреждением желудочно-кишечного тракта" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(453) "Результаты гистологических и вирусологических исследований в диагностике острой реакции трансплантат против хозяина с повреждением желудочно-кишечного трактаThe role of histopathological, virological and bacteriological findings in the diagnostics of acute graft-versus-host disease of the gastrointestinal tract" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(7308) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Острая реакция трансплантат против хозяина (оРТПХ) с поражением желудочно-кишечного тракта (ЖКТ) – это одно из наиболее угрожающих осложнений у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). В настоящее время не существует стандартов по диагностике этого состояния. Клинические симптомы оРТПХ являются неспецифичными и могут мимикрировать под другие патологические состояния. Цель нашей работы заключается в анализе результатов гистологических исследований слизистых толстой кишки и верхнего отдела ЖКТ (желудка, двенадцатиперстной кишки, пищевода) у пациентов после алло-ТГСК, определении частоты выявления различных патологий ЖКТ после алло-ТГСК. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В ретроспективное исследование были включены 112 пациентов после алло-ТГСК. Большинство пациентов (68%) проходили лечение по поводу острого лейкоза. Медиана возраста в исследуемой группе составила 30 лет (2-67 лет). Всем пациентам была проведена фиброгастродуоденоскопия и/или фиброколоноскопия, выполнена биопсия и гистологическое исследование органов желудочно-кишечного тракта. Методом ПЦР в биоптатах выявляли вирус простого герпеса 1, 2, герпеса 6 типа и цитомегаловирус, а также проводили бактериологическое исследование кала на условно-патогенную флору и ИФА на C. difficile. Медиана времени выполнения биопсии после трансплантации составила 84 дня (15-413 дней). Исследования проводились по поводу различных симптомов поражения ЖКТ для верификации диагноза. В 56% случаев была выполнена биопсия толстой кишки, в 35% – биопсия верхних отделов ЖКТ (желудок, двенадцатиперстная кишка, пищевод), а также в 9% проводилось исследование обоих отделов. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> При биопсии толстой кишки признаки оРТПХ наблюдалась в 73,5% случаев и чаще, чем при биопсии верхнего отдела ЖКТ (36,5%, р=0,02). В нижних отделах ЖКТ легкая гистологическая степень оРТПХ определялась в 56% случаев, средней тяжести – в 28%, тяжелая – в 16%. В верхних отделах ЖКТ наблюдались легкие проявления РТПХ у 60% и средней тяжести – у 33%. Вирусная инфекция чаще наблюдалась при биопсии нижнего отдела ЖКТ (53% и 36%, р=0,046). Бактериальная инфекция встречалась у 38% и 19% пациентов, с биопсией нижнего и верхнего отделов ЖКТ соответственно (р=0,56). У пациентов, которым была выполнена биопсия толстой кишки, вирусная инфекция не влияла на 1-летнюю общую выживаемость (ОВ) (65,2% и 64,7%, р=0,67). Такая же картина наблюдалось при биопсии верхних отделов ЖКТ (85,7% и 86,4%, р=0,8). ОВ не зависела от наличия условно-патогенной бактериальной флоры, в группе пациентов с биопсией нижних отделов – 61,4% и 72,6% (р=0,4) и верхних отделов – 85,7% и 86,4%, соответственно (р=0,8). Основным фактором, оказавшим достоверное влияние на ОВ пациентов, которым проводилась биопсия толстой кишки, была гистологическая степень тяжести оРТПХ, так при легкой степени 1-летняя ОВ составила 88,2%, при средней степени тяжести – 47,6%, при тяжелой – 40,0%, а в случае отсутствия оРТПХ – 60,2% (р=0,01). При исследовании верхних отделов ОВ различалась, у пациентов с РТПХ составила 72,0%, без РТПХ – 95,2% (р=0,04). Однако степень выраженности РТПХ достоверно не изменяла ОВ, при 1 степени – 78,75%, при 2 – 60% (р=0,15), возможно, вследствие маленькой выборки (n=15). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Полученные данные демонстрируют неоднородность этиологии поражения различных отделов ЖКТ после алло-ТГСК, что подчеркивает необходимость гистологического и ПЦР исследования биоптатов ЖКТ. Возможно, из-за небольшой выборки пациентов, в исследовании не было показано влияния вирусного и бактериального поражения ЖКТ на выживаемость. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, острая реакция трансплантат против хозяина, желудочно-кишечный тракт, гистологическое исследование. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(298) "Результаты гистологических и вирусологических исследований в диагностике острой реакции трансплантат против хозяина с повреждением желудочно-кишечного тракта" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(298) "Результаты гистологических и вирусологических исследований в диагностике острой реакции трансплантат против хозяина с повреждением желудочно-кишечного тракта" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(298) "Результаты гистологических и вирусологических исследований в диагностике острой реакции трансплантат против хозяина с повреждением желудочно-кишечного тракта" ["SECTION_META_TITLE"]=> string(298) "Результаты гистологических и вирусологических исследований в диагностике острой реакции трансплантат против хозяина с повреждением желудочно-кишечного тракта" ["SECTION_META_KEYWORDS"]=> string(298) "Результаты гистологических и вирусологических исследований в диагностике острой реакции трансплантат против хозяина с повреждением желудочно-кишечного тракта" ["SECTION_META_DESCRIPTION"]=> string(298) "Результаты гистологических и вирусологических исследований в диагностике острой реакции трансплантат против хозяина с повреждением желудочно-кишечного тракта" ["SECTION_PICTURE_FILE_ALT"]=> string(298) "Результаты гистологических и вирусологических исследований в диагностике острой реакции трансплантат против хозяина с повреждением желудочно-кишечного тракта" ["SECTION_PICTURE_FILE_TITLE"]=> string(298) "Результаты гистологических и вирусологических исследований в диагностике острой реакции трансплантат против хозяина с повреждением желудочно-кишечного тракта" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "rezultaty-gistologicheskikh-i-virusologicheskikh-issledovaniy-v-diagnostike-ostroy-reaktsii-transpla" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(298) "Результаты гистологических и вирусологических исследований в диагностике острой реакции трансплантат против хозяина с повреждением желудочно-кишечного тракта" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(298) "Результаты гистологических и вирусологических исследований в диагностике острой реакции трансплантат против хозяина с повреждением желудочно-кишечного тракта" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "rezultaty-gistologicheskikh-i-virusologicheskikh-issledovaniy-v-diagnostike-ostroy-reaktsii-transpla" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "rezultaty-gistologicheskikh-i-virusologicheskikh-issledovaniy-v-diagnostike-ostroy-reaktsii-transpla" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "rezultaty-gistologicheskikh-i-virusologicheskikh-issledovaniy-v-diagnostike-ostroy-reaktsii-transpla" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20356" ["VALUE"]=> array(2) { ["TEXT"]=> string(868) "Дарья В. Чуракина <sup>1</sup>, Александр Н. Швецов <sup>1</sup>, Вадим Е. Карев <sup>2</sup>, Ирина А. Карабак <sup>2</sup>, Алексей Б. Чухловин <sup>1</sup>, Юрий А. Эйсмонт <sup>2</sup>, Ольга В. Пирогова <sup>1</sup>, Павел С. Жеребненко <sup>1</sup>, Олег В. Голощапов <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Татьяна А. Быкова <sup>1</sup>, Олеся В. Паина <sup>1</sup>, Людмила С. Зубаровская <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(688) "Дарья В. Чуракина 1, Александр Н. Швецов 1, Вадим Е. Карев 2, Ирина А. Карабак 2, Алексей Б. Чухловин 1, Юрий А. Эйсмонт 2, Ольга В. Пирогова 1, Павел С. Жеребненко 1, Олег В. Голощапов 1, Елена И. Дарская 1, Татьяна А. Быкова 1, Олеся В. Паина 1, Людмила С. Зубаровская 1, Иван С. Моисеев 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20357" ["VALUE"]=> array(2) { ["TEXT"]=> string(482) "<sup>1</sup> НИИ Детской Онкологии, Гематологии и Трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова<br> <sup>2</sup> ФГБУ «Детский научно-клинический центр инфекционных болезней»<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(446) "1 НИИ Детской Онкологии, Гематологии и Трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова2 ФГБУ «Детский научно-клинический центр инфекционных болезней»
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20462" ["VALUE"]=> array(2) { ["TEXT"]=> string(7308) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Острая реакция трансплантат против хозяина (оРТПХ) с поражением желудочно-кишечного тракта (ЖКТ) – это одно из наиболее угрожающих осложнений у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). В настоящее время не существует стандартов по диагностике этого состояния. Клинические симптомы оРТПХ являются неспецифичными и могут мимикрировать под другие патологические состояния. Цель нашей работы заключается в анализе результатов гистологических исследований слизистых толстой кишки и верхнего отдела ЖКТ (желудка, двенадцатиперстной кишки, пищевода) у пациентов после алло-ТГСК, определении частоты выявления различных патологий ЖКТ после алло-ТГСК. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В ретроспективное исследование были включены 112 пациентов после алло-ТГСК. Большинство пациентов (68%) проходили лечение по поводу острого лейкоза. Медиана возраста в исследуемой группе составила 30 лет (2-67 лет). Всем пациентам была проведена фиброгастродуоденоскопия и/или фиброколоноскопия, выполнена биопсия и гистологическое исследование органов желудочно-кишечного тракта. Методом ПЦР в биоптатах выявляли вирус простого герпеса 1, 2, герпеса 6 типа и цитомегаловирус, а также проводили бактериологическое исследование кала на условно-патогенную флору и ИФА на C. difficile. Медиана времени выполнения биопсии после трансплантации составила 84 дня (15-413 дней). Исследования проводились по поводу различных симптомов поражения ЖКТ для верификации диагноза. В 56% случаев была выполнена биопсия толстой кишки, в 35% – биопсия верхних отделов ЖКТ (желудок, двенадцатиперстная кишка, пищевод), а также в 9% проводилось исследование обоих отделов. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> При биопсии толстой кишки признаки оРТПХ наблюдалась в 73,5% случаев и чаще, чем при биопсии верхнего отдела ЖКТ (36,5%, р=0,02). В нижних отделах ЖКТ легкая гистологическая степень оРТПХ определялась в 56% случаев, средней тяжести – в 28%, тяжелая – в 16%. В верхних отделах ЖКТ наблюдались легкие проявления РТПХ у 60% и средней тяжести – у 33%. Вирусная инфекция чаще наблюдалась при биопсии нижнего отдела ЖКТ (53% и 36%, р=0,046). Бактериальная инфекция встречалась у 38% и 19% пациентов, с биопсией нижнего и верхнего отделов ЖКТ соответственно (р=0,56). У пациентов, которым была выполнена биопсия толстой кишки, вирусная инфекция не влияла на 1-летнюю общую выживаемость (ОВ) (65,2% и 64,7%, р=0,67). Такая же картина наблюдалось при биопсии верхних отделов ЖКТ (85,7% и 86,4%, р=0,8). ОВ не зависела от наличия условно-патогенной бактериальной флоры, в группе пациентов с биопсией нижних отделов – 61,4% и 72,6% (р=0,4) и верхних отделов – 85,7% и 86,4%, соответственно (р=0,8). Основным фактором, оказавшим достоверное влияние на ОВ пациентов, которым проводилась биопсия толстой кишки, была гистологическая степень тяжести оРТПХ, так при легкой степени 1-летняя ОВ составила 88,2%, при средней степени тяжести – 47,6%, при тяжелой – 40,0%, а в случае отсутствия оРТПХ – 60,2% (р=0,01). При исследовании верхних отделов ОВ различалась, у пациентов с РТПХ составила 72,0%, без РТПХ – 95,2% (р=0,04). Однако степень выраженности РТПХ достоверно не изменяла ОВ, при 1 степени – 78,75%, при 2 – 60% (р=0,15), возможно, вследствие маленькой выборки (n=15). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Полученные данные демонстрируют неоднородность этиологии поражения различных отделов ЖКТ после алло-ТГСК, что подчеркивает необходимость гистологического и ПЦР исследования биоптатов ЖКТ. Возможно, из-за небольшой выборки пациентов, в исследовании не было показано влияния вирусного и бактериального поражения ЖКТ на выживаемость. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, острая реакция трансплантат против хозяина, желудочно-кишечный тракт, гистологическое исследование. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7088) "
Введение
Острая реакция трансплантат против хозяина (оРТПХ) с поражением желудочно-кишечного тракта (ЖКТ) – это одно из наиболее угрожающих осложнений у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). В настоящее время не существует стандартов по диагностике этого состояния. Клинические симптомы оРТПХ являются неспецифичными и могут мимикрировать под другие патологические состояния. Цель нашей работы заключается в анализе результатов гистологических исследований слизистых толстой кишки и верхнего отдела ЖКТ (желудка, двенадцатиперстной кишки, пищевода) у пациентов после алло-ТГСК, определении частоты выявления различных патологий ЖКТ после алло-ТГСК.
Пациенты и методы
В ретроспективное исследование были включены 112 пациентов после алло-ТГСК. Большинство пациентов (68%) проходили лечение по поводу острого лейкоза. Медиана возраста в исследуемой группе составила 30 лет (2-67 лет). Всем пациентам была проведена фиброгастродуоденоскопия и/или фиброколоноскопия, выполнена биопсия и гистологическое исследование органов желудочно-кишечного тракта. Методом ПЦР в биоптатах выявляли вирус простого герпеса 1, 2, герпеса 6 типа и цитомегаловирус, а также проводили бактериологическое исследование кала на условно-патогенную флору и ИФА на C. difficile. Медиана времени выполнения биопсии после трансплантации составила 84 дня (15-413 дней). Исследования проводились по поводу различных симптомов поражения ЖКТ для верификации диагноза. В 56% случаев была выполнена биопсия толстой кишки, в 35% – биопсия верхних отделов ЖКТ (желудок, двенадцатиперстная кишка, пищевод), а также в 9% проводилось исследование обоих отделов.
Результаты
При биопсии толстой кишки признаки оРТПХ наблюдалась в 73,5% случаев и чаще, чем при биопсии верхнего отдела ЖКТ (36,5%, р=0,02). В нижних отделах ЖКТ легкая гистологическая степень оРТПХ определялась в 56% случаев, средней тяжести – в 28%, тяжелая – в 16%. В верхних отделах ЖКТ наблюдались легкие проявления РТПХ у 60% и средней тяжести – у 33%. Вирусная инфекция чаще наблюдалась при биопсии нижнего отдела ЖКТ (53% и 36%, р=0,046). Бактериальная инфекция встречалась у 38% и 19% пациентов, с биопсией нижнего и верхнего отделов ЖКТ соответственно (р=0,56). У пациентов, которым была выполнена биопсия толстой кишки, вирусная инфекция не влияла на 1-летнюю общую выживаемость (ОВ) (65,2% и 64,7%, р=0,67). Такая же картина наблюдалось при биопсии верхних отделов ЖКТ (85,7% и 86,4%, р=0,8). ОВ не зависела от наличия условно-патогенной бактериальной флоры, в группе пациентов с биопсией нижних отделов – 61,4% и 72,6% (р=0,4) и верхних отделов – 85,7% и 86,4%, соответственно (р=0,8). Основным фактором, оказавшим достоверное влияние на ОВ пациентов, которым проводилась биопсия толстой кишки, была гистологическая степень тяжести оРТПХ, так при легкой степени 1-летняя ОВ составила 88,2%, при средней степени тяжести – 47,6%, при тяжелой – 40,0%, а в случае отсутствия оРТПХ – 60,2% (р=0,01). При исследовании верхних отделов ОВ различалась, у пациентов с РТПХ составила 72,0%, без РТПХ – 95,2% (р=0,04). Однако степень выраженности РТПХ достоверно не изменяла ОВ, при 1 степени – 78,75%, при 2 – 60% (р=0,15), возможно, вследствие маленькой выборки (n=15).
Заключение
Полученные данные демонстрируют неоднородность этиологии поражения различных отделов ЖКТ после алло-ТГСК, что подчеркивает необходимость гистологического и ПЦР исследования биоптатов ЖКТ. Возможно, из-за небольшой выборки пациентов, в исследовании не было показано влияния вирусного и бактериального поражения ЖКТ на выживаемость.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, острая реакция трансплантат против хозяина, желудочно-кишечный тракт, гистологическое исследование.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20358" ["VALUE"]=> array(2) { ["TEXT"]=> string(669) "Darya V. Churakina <sup>1</sup>, Aleksander N. Shvetsov <sup>1</sup>, Vadim E. Karev <sup>2</sup>, Irina A. Karabak <sup>2</sup>, Alexey B. Chukhlovin <sup>1</sup>, Yurii A. Eismont <sup>2</sup>, Olga V. Pirogova <sup>1</sup>, Pavel S. Zherebenko <sup>1</sup>, Oleg V. Goloshchapov <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Tatiana A. Bykova <sup>1</sup>, Olesya V. Paina <sup>1</sup>, Ludmila S. Zubarovskaya <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "TEXT" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(489) "Darya V. Churakina 1, Aleksander N. Shvetsov 1, Vadim E. Karev 2, Irina A. Karabak 2, Alexey B. Chukhlovin 1, Yurii A. Eismont 2, Olga V. Pirogova 1, Pavel S. Zherebenko 1, Oleg V. Goloshchapov 1, Elena I. Darskaya 1, Tatiana A. Bykova 1, Olesya V. Paina 1, Ludmila S. Zubarovskaya 1, Ivan S. Moiseev 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "TEXT" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20359" ["VALUE"]=> array(2) { ["TEXT"]=> string(367) "<sup>1</sup> R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation<br> <sup>2</sup> Research Institute of Pediatric Infections, Federal Medico-Biological Agency of Russia, St. Petersburg, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(331) "1 R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation2 Research Institute of Pediatric Infections, Federal Medico-Biological Agency of Russia, St. Petersburg, Russian Federation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20465" ["VALUE"]=> array(2) { ["TEXT"]=> string(3839) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Acute graft-versus-host disease (aGVHD) of the gastrointestinal tract (GI tract) is one of the most dangerous complications after allogeneic hematopoietic stem cell transplantation (allo-HSCT). However, there is consensus now on the diagnostic workup in this complication. Clinical manifestations of aGVHD are nonspecific and can resemble other conditions. The goal of our research was to analyze the results of histological examination of mucous colon and upper digestive ways (esophagus, stomach, duodenum) of the patients after HSCT with suspected GVHD, and to determine the incidence of different findings. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Our retrospective research included 112 patients after allo-HSCT. Most of the patients received allo-HSCT as treatment for acute leukemia. Median age was 30 years (2-67). All these patients were studied by gastroduodenoscopy and/or colonoscopy, with biopsy and histopathology investigation of the GI sites. Herpes simplex virus, herpes virus type 6, cytomegalovirus were identified by PCR in the biopsies. Fecal samples were studied by ELISA for C. difficile, and seeded in cultures for antibiotic-resistant bacteria. Median timing for the biopsies was 85 days (15-413) post-HSCT. In 56% of cases, biopsy of upper GI compartments was performed, in 35% of cases, lower parts of GI-tract were sampled, and both compartments were subject to biopsies in 9% of cases. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Conventional histology revealed signs of aGVHD in 73.5% of colon biopsies, and only in 36.5% of upper GI biopsies, p=0.02. Mild histological signs of GVHD were present in 56% of biopsies from the lower GI mucosa, moderate pathology, in 28%, and severe changes, in 16%. In upper GI tract, mild histological signs were observed in 60% cases, moderate changes, in 33%. Viral infection revealed by PCR was more frequent in colon biopsies (53% and 36%, p=0.046). Bacterial infection was detected in 38% patients with lower GI biopsy sampling, and in 19%, from the upper GI biopsies, respectively, with no significant difference between these groups (p=0.56). Lower GI tract viral infection had no influence on the 1-year overall survival (OS) (65.2% and 64.7%, p=0.67). Similar effect was observed for the upper GI tract viral infections (85.7% and 84.4%, p=0.8). Overall survival (OS) was not influenced by bacterial infections in the biopsies of lower GI tract (61.4% and 72.6%, p=0.4), or upper GI tract samples (85.7% and 86.4%, p=0.8). Histological grade in lower GI biopsies was the main feature that affected OS (88.2%, 47.6, and 60.2%, for mild, moderate and severe histological grades, respectively, p=0.01). Presence of upper GI GVHD also adversely affected OS (72.0% and 95.2%, p=0.04). However, severity of upper GVHD had no influence on OS, possibly, as result of small sample size. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The study demonstrates different etiologies for upper and lower GI lesions after HSCT and confirms the necessity of biopsy and PCR assays of the samples. Although the study size was small, it did not identify the impact of viral and bacterial GI infections on survival. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Acute graft-versus-host disease, hematopoietic stem cell transplantation, gastrointestinal tract, histopathology. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3619) "
Introduction
Acute graft-versus-host disease (aGVHD) of the gastrointestinal tract (GI tract) is one of the most dangerous complications after allogeneic hematopoietic stem cell transplantation (allo-HSCT). However, there is consensus now on the diagnostic workup in this complication. Clinical manifestations of aGVHD are nonspecific and can resemble other conditions. The goal of our research was to analyze the results of histological examination of mucous colon and upper digestive ways (esophagus, stomach, duodenum) of the patients after HSCT with suspected GVHD, and to determine the incidence of different findings.
Patients and methods
Our retrospective research included 112 patients after allo-HSCT. Most of the patients received allo-HSCT as treatment for acute leukemia. Median age was 30 years (2-67). All these patients were studied by gastroduodenoscopy and/or colonoscopy, with biopsy and histopathology investigation of the GI sites. Herpes simplex virus, herpes virus type 6, cytomegalovirus were identified by PCR in the biopsies. Fecal samples were studied by ELISA for C. difficile, and seeded in cultures for antibiotic-resistant bacteria. Median timing for the biopsies was 85 days (15-413) post-HSCT. In 56% of cases, biopsy of upper GI compartments was performed, in 35% of cases, lower parts of GI-tract were sampled, and both compartments were subject to biopsies in 9% of cases.
Results
Conventional histology revealed signs of aGVHD in 73.5% of colon biopsies, and only in 36.5% of upper GI biopsies, p=0.02. Mild histological signs of GVHD were present in 56% of biopsies from the lower GI mucosa, moderate pathology, in 28%, and severe changes, in 16%. In upper GI tract, mild histological signs were observed in 60% cases, moderate changes, in 33%. Viral infection revealed by PCR was more frequent in colon biopsies (53% and 36%, p=0.046). Bacterial infection was detected in 38% patients with lower GI biopsy sampling, and in 19%, from the upper GI biopsies, respectively, with no significant difference between these groups (p=0.56). Lower GI tract viral infection had no influence on the 1-year overall survival (OS) (65.2% and 64.7%, p=0.67). Similar effect was observed for the upper GI tract viral infections (85.7% and 84.4%, p=0.8). Overall survival (OS) was not influenced by bacterial infections in the biopsies of lower GI tract (61.4% and 72.6%, p=0.4), or upper GI tract samples (85.7% and 86.4%, p=0.8). Histological grade in lower GI biopsies was the main feature that affected OS (88.2%, 47.6, and 60.2%, for mild, moderate and severe histological grades, respectively, p=0.01). Presence of upper GI GVHD also adversely affected OS (72.0% and 95.2%, p=0.04). However, severity of upper GVHD had no influence on OS, possibly, as result of small sample size.
Conclusion
The study demonstrates different etiologies for upper and lower GI lesions after HSCT and confirms the necessity of biopsy and PCR assays of the samples. Although the study size was small, it did not identify the impact of viral and bacterial GI infections on survival.
Keywords
Acute graft-versus-host disease, hematopoietic stem cell transplantation, gastrointestinal tract, histopathology.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20360" ["VALUE"]=> string(155) "The role of histopathological, virological and bacteriological findings in the diagnostics of acute graft-versus-host disease of the gastrointestinal tract" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(155) "The role of histopathological, virological and bacteriological findings in the diagnostics of acute graft-versus-host disease of the gastrointestinal tract" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20749" ["VALUE"]=> string(4) "1385" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1385" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20750" ["VALUE"]=> string(4) "1386" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1386" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20358" ["VALUE"]=> array(2) { ["TEXT"]=> string(669) "Darya V. Churakina <sup>1</sup>, Aleksander N. Shvetsov <sup>1</sup>, Vadim E. Karev <sup>2</sup>, Irina A. Karabak <sup>2</sup>, Alexey B. Chukhlovin <sup>1</sup>, Yurii A. Eismont <sup>2</sup>, Olga V. Pirogova <sup>1</sup>, Pavel S. Zherebenko <sup>1</sup>, Oleg V. Goloshchapov <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Tatiana A. Bykova <sup>1</sup>, Olesya V. Paina <sup>1</sup>, Ludmila S. Zubarovskaya <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "TEXT" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(489) "Darya V. Churakina 1, Aleksander N. Shvetsov 1, Vadim E. Karev 2, Irina A. Karabak 2, Alexey B. Chukhlovin 1, Yurii A. Eismont 2, Olga V. Pirogova 1, Pavel S. Zherebenko 1, Oleg V. Goloshchapov 1, Elena I. Darskaya 1, Tatiana A. Bykova 1, Olesya V. Paina 1, Ludmila S. Zubarovskaya 1, Ivan S. Moiseev 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "TEXT" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(669) "Darya V. Churakina <sup>1</sup>, Aleksander N. Shvetsov <sup>1</sup>, Vadim E. Karev <sup>2</sup>, Irina A. Karabak <sup>2</sup>, Alexey B. Chukhlovin <sup>1</sup>, Yurii A. Eismont <sup>2</sup>, Olga V. Pirogova <sup>1</sup>, Pavel S. Zherebenko <sup>1</sup>, Oleg V. Goloshchapov <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Tatiana A. Bykova <sup>1</sup>, Olesya V. Paina <sup>1</sup>, Ludmila S. Zubarovskaya <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20465" ["VALUE"]=> array(2) { ["TEXT"]=> string(3839) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Acute graft-versus-host disease (aGVHD) of the gastrointestinal tract (GI tract) is one of the most dangerous complications after allogeneic hematopoietic stem cell transplantation (allo-HSCT). However, there is consensus now on the diagnostic workup in this complication. Clinical manifestations of aGVHD are nonspecific and can resemble other conditions. The goal of our research was to analyze the results of histological examination of mucous colon and upper digestive ways (esophagus, stomach, duodenum) of the patients after HSCT with suspected GVHD, and to determine the incidence of different findings. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Our retrospective research included 112 patients after allo-HSCT. Most of the patients received allo-HSCT as treatment for acute leukemia. Median age was 30 years (2-67). All these patients were studied by gastroduodenoscopy and/or colonoscopy, with biopsy and histopathology investigation of the GI sites. Herpes simplex virus, herpes virus type 6, cytomegalovirus were identified by PCR in the biopsies. Fecal samples were studied by ELISA for C. difficile, and seeded in cultures for antibiotic-resistant bacteria. Median timing for the biopsies was 85 days (15-413) post-HSCT. In 56% of cases, biopsy of upper GI compartments was performed, in 35% of cases, lower parts of GI-tract were sampled, and both compartments were subject to biopsies in 9% of cases. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Conventional histology revealed signs of aGVHD in 73.5% of colon biopsies, and only in 36.5% of upper GI biopsies, p=0.02. Mild histological signs of GVHD were present in 56% of biopsies from the lower GI mucosa, moderate pathology, in 28%, and severe changes, in 16%. In upper GI tract, mild histological signs were observed in 60% cases, moderate changes, in 33%. Viral infection revealed by PCR was more frequent in colon biopsies (53% and 36%, p=0.046). Bacterial infection was detected in 38% patients with lower GI biopsy sampling, and in 19%, from the upper GI biopsies, respectively, with no significant difference between these groups (p=0.56). Lower GI tract viral infection had no influence on the 1-year overall survival (OS) (65.2% and 64.7%, p=0.67). Similar effect was observed for the upper GI tract viral infections (85.7% and 84.4%, p=0.8). Overall survival (OS) was not influenced by bacterial infections in the biopsies of lower GI tract (61.4% and 72.6%, p=0.4), or upper GI tract samples (85.7% and 86.4%, p=0.8). Histological grade in lower GI biopsies was the main feature that affected OS (88.2%, 47.6, and 60.2%, for mild, moderate and severe histological grades, respectively, p=0.01). Presence of upper GI GVHD also adversely affected OS (72.0% and 95.2%, p=0.04). However, severity of upper GVHD had no influence on OS, possibly, as result of small sample size. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The study demonstrates different etiologies for upper and lower GI lesions after HSCT and confirms the necessity of biopsy and PCR assays of the samples. Although the study size was small, it did not identify the impact of viral and bacterial GI infections on survival. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Acute graft-versus-host disease, hematopoietic stem cell transplantation, gastrointestinal tract, histopathology. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3619) "Introduction
Acute graft-versus-host disease (aGVHD) of the gastrointestinal tract (GI tract) is one of the most dangerous complications after allogeneic hematopoietic stem cell transplantation (allo-HSCT). However, there is consensus now on the diagnostic workup in this complication. Clinical manifestations of aGVHD are nonspecific and can resemble other conditions. The goal of our research was to analyze the results of histological examination of mucous colon and upper digestive ways (esophagus, stomach, duodenum) of the patients after HSCT with suspected GVHD, and to determine the incidence of different findings.
Patients and methods
Our retrospective research included 112 patients after allo-HSCT. Most of the patients received allo-HSCT as treatment for acute leukemia. Median age was 30 years (2-67). All these patients were studied by gastroduodenoscopy and/or colonoscopy, with biopsy and histopathology investigation of the GI sites. Herpes simplex virus, herpes virus type 6, cytomegalovirus were identified by PCR in the biopsies. Fecal samples were studied by ELISA for C. difficile, and seeded in cultures for antibiotic-resistant bacteria. Median timing for the biopsies was 85 days (15-413) post-HSCT. In 56% of cases, biopsy of upper GI compartments was performed, in 35% of cases, lower parts of GI-tract were sampled, and both compartments were subject to biopsies in 9% of cases.
Results
Conventional histology revealed signs of aGVHD in 73.5% of colon biopsies, and only in 36.5% of upper GI biopsies, p=0.02. Mild histological signs of GVHD were present in 56% of biopsies from the lower GI mucosa, moderate pathology, in 28%, and severe changes, in 16%. In upper GI tract, mild histological signs were observed in 60% cases, moderate changes, in 33%. Viral infection revealed by PCR was more frequent in colon biopsies (53% and 36%, p=0.046). Bacterial infection was detected in 38% patients with lower GI biopsy sampling, and in 19%, from the upper GI biopsies, respectively, with no significant difference between these groups (p=0.56). Lower GI tract viral infection had no influence on the 1-year overall survival (OS) (65.2% and 64.7%, p=0.67). Similar effect was observed for the upper GI tract viral infections (85.7% and 84.4%, p=0.8). Overall survival (OS) was not influenced by bacterial infections in the biopsies of lower GI tract (61.4% and 72.6%, p=0.4), or upper GI tract samples (85.7% and 86.4%, p=0.8). Histological grade in lower GI biopsies was the main feature that affected OS (88.2%, 47.6, and 60.2%, for mild, moderate and severe histological grades, respectively, p=0.01). Presence of upper GI GVHD also adversely affected OS (72.0% and 95.2%, p=0.04). However, severity of upper GVHD had no influence on OS, possibly, as result of small sample size.
Conclusion
The study demonstrates different etiologies for upper and lower GI lesions after HSCT and confirms the necessity of biopsy and PCR assays of the samples. Although the study size was small, it did not identify the impact of viral and bacterial GI infections on survival.
Keywords
Acute graft-versus-host disease, hematopoietic stem cell transplantation, gastrointestinal tract, histopathology.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3619) "Introduction
Acute graft-versus-host disease (aGVHD) of the gastrointestinal tract (GI tract) is one of the most dangerous complications after allogeneic hematopoietic stem cell transplantation (allo-HSCT). However, there is consensus now on the diagnostic workup in this complication. Clinical manifestations of aGVHD are nonspecific and can resemble other conditions. The goal of our research was to analyze the results of histological examination of mucous colon and upper digestive ways (esophagus, stomach, duodenum) of the patients after HSCT with suspected GVHD, and to determine the incidence of different findings.
Patients and methods
Our retrospective research included 112 patients after allo-HSCT. Most of the patients received allo-HSCT as treatment for acute leukemia. Median age was 30 years (2-67). All these patients were studied by gastroduodenoscopy and/or colonoscopy, with biopsy and histopathology investigation of the GI sites. Herpes simplex virus, herpes virus type 6, cytomegalovirus were identified by PCR in the biopsies. Fecal samples were studied by ELISA for C. difficile, and seeded in cultures for antibiotic-resistant bacteria. Median timing for the biopsies was 85 days (15-413) post-HSCT. In 56% of cases, biopsy of upper GI compartments was performed, in 35% of cases, lower parts of GI-tract were sampled, and both compartments were subject to biopsies in 9% of cases.
Results
Conventional histology revealed signs of aGVHD in 73.5% of colon biopsies, and only in 36.5% of upper GI biopsies, p=0.02. Mild histological signs of GVHD were present in 56% of biopsies from the lower GI mucosa, moderate pathology, in 28%, and severe changes, in 16%. In upper GI tract, mild histological signs were observed in 60% cases, moderate changes, in 33%. Viral infection revealed by PCR was more frequent in colon biopsies (53% and 36%, p=0.046). Bacterial infection was detected in 38% patients with lower GI biopsy sampling, and in 19%, from the upper GI biopsies, respectively, with no significant difference between these groups (p=0.56). Lower GI tract viral infection had no influence on the 1-year overall survival (OS) (65.2% and 64.7%, p=0.67). Similar effect was observed for the upper GI tract viral infections (85.7% and 84.4%, p=0.8). Overall survival (OS) was not influenced by bacterial infections in the biopsies of lower GI tract (61.4% and 72.6%, p=0.4), or upper GI tract samples (85.7% and 86.4%, p=0.8). Histological grade in lower GI biopsies was the main feature that affected OS (88.2%, 47.6, and 60.2%, for mild, moderate and severe histological grades, respectively, p=0.01). Presence of upper GI GVHD also adversely affected OS (72.0% and 95.2%, p=0.04). However, severity of upper GVHD had no influence on OS, possibly, as result of small sample size.
Conclusion
The study demonstrates different etiologies for upper and lower GI lesions after HSCT and confirms the necessity of biopsy and PCR assays of the samples. Although the study size was small, it did not identify the impact of viral and bacterial GI infections on survival.
Keywords
Acute graft-versus-host disease, hematopoietic stem cell transplantation, gastrointestinal tract, histopathology.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20360" ["VALUE"]=> string(155) "The role of histopathological, virological and bacteriological findings in the diagnostics of acute graft-versus-host disease of the gastrointestinal tract" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(155) "The role of histopathological, virological and bacteriological findings in the diagnostics of acute graft-versus-host disease of the gastrointestinal tract" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(155) "The role of histopathological, virological and bacteriological findings in the diagnostics of acute graft-versus-host disease of the gastrointestinal tract" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20359" ["VALUE"]=> array(2) { ["TEXT"]=> string(367) "<sup>1</sup> R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation<br> <sup>2</sup> Research Institute of Pediatric Infections, Federal Medico-Biological Agency of Russia, St. Petersburg, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(331) "1 R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation2 Research Institute of Pediatric Infections, Federal Medico-Biological Agency of Russia, St. Petersburg, Russian Federation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(331) "1 R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
2 Research Institute of Pediatric Infections, Federal Medico-Biological Agency of Russia, St. Petersburg, Russian Federation
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20356" ["VALUE"]=> array(2) { ["TEXT"]=> string(868) "Дарья В. Чуракина <sup>1</sup>, Александр Н. Швецов <sup>1</sup>, Вадим Е. Карев <sup>2</sup>, Ирина А. Карабак <sup>2</sup>, Алексей Б. Чухловин <sup>1</sup>, Юрий А. Эйсмонт <sup>2</sup>, Ольга В. Пирогова <sup>1</sup>, Павел С. Жеребненко <sup>1</sup>, Олег В. Голощапов <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Татьяна А. Быкова <sup>1</sup>, Олеся В. Паина <sup>1</sup>, Людмила С. Зубаровская <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(688) "Дарья В. Чуракина 1, Александр Н. Швецов 1, Вадим Е. Карев 2, Ирина А. Карабак 2, Алексей Б. Чухловин 1, Юрий А. Эйсмонт 2, Ольга В. Пирогова 1, Павел С. Жеребненко 1, Олег В. Голощапов 1, Елена И. Дарская 1, Татьяна А. Быкова 1, Олеся В. Паина 1, Людмила С. Зубаровская 1, Иван С. Моисеев 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(688) "Дарья В. Чуракина 1, Александр Н. Швецов 1, Вадим Е. Карев 2, Ирина А. Карабак 2, Алексей Б. Чухловин 1, Юрий А. Эйсмонт 2, Ольга В. Пирогова 1, Павел С. Жеребненко 1, Олег В. Голощапов 1, Елена И. Дарская 1, Татьяна А. Быкова 1, Олеся В. Паина 1, Людмила С. Зубаровская 1, Иван С. Моисеев 1, Борис В. Афанасьев 1" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20462" ["VALUE"]=> array(2) { ["TEXT"]=> string(7308) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Острая реакция трансплантат против хозяина (оРТПХ) с поражением желудочно-кишечного тракта (ЖКТ) – это одно из наиболее угрожающих осложнений у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). В настоящее время не существует стандартов по диагностике этого состояния. Клинические симптомы оРТПХ являются неспецифичными и могут мимикрировать под другие патологические состояния. Цель нашей работы заключается в анализе результатов гистологических исследований слизистых толстой кишки и верхнего отдела ЖКТ (желудка, двенадцатиперстной кишки, пищевода) у пациентов после алло-ТГСК, определении частоты выявления различных патологий ЖКТ после алло-ТГСК. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В ретроспективное исследование были включены 112 пациентов после алло-ТГСК. Большинство пациентов (68%) проходили лечение по поводу острого лейкоза. Медиана возраста в исследуемой группе составила 30 лет (2-67 лет). Всем пациентам была проведена фиброгастродуоденоскопия и/или фиброколоноскопия, выполнена биопсия и гистологическое исследование органов желудочно-кишечного тракта. Методом ПЦР в биоптатах выявляли вирус простого герпеса 1, 2, герпеса 6 типа и цитомегаловирус, а также проводили бактериологическое исследование кала на условно-патогенную флору и ИФА на C. difficile. Медиана времени выполнения биопсии после трансплантации составила 84 дня (15-413 дней). Исследования проводились по поводу различных симптомов поражения ЖКТ для верификации диагноза. В 56% случаев была выполнена биопсия толстой кишки, в 35% – биопсия верхних отделов ЖКТ (желудок, двенадцатиперстная кишка, пищевод), а также в 9% проводилось исследование обоих отделов. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> При биопсии толстой кишки признаки оРТПХ наблюдалась в 73,5% случаев и чаще, чем при биопсии верхнего отдела ЖКТ (36,5%, р=0,02). В нижних отделах ЖКТ легкая гистологическая степень оРТПХ определялась в 56% случаев, средней тяжести – в 28%, тяжелая – в 16%. В верхних отделах ЖКТ наблюдались легкие проявления РТПХ у 60% и средней тяжести – у 33%. Вирусная инфекция чаще наблюдалась при биопсии нижнего отдела ЖКТ (53% и 36%, р=0,046). Бактериальная инфекция встречалась у 38% и 19% пациентов, с биопсией нижнего и верхнего отделов ЖКТ соответственно (р=0,56). У пациентов, которым была выполнена биопсия толстой кишки, вирусная инфекция не влияла на 1-летнюю общую выживаемость (ОВ) (65,2% и 64,7%, р=0,67). Такая же картина наблюдалось при биопсии верхних отделов ЖКТ (85,7% и 86,4%, р=0,8). ОВ не зависела от наличия условно-патогенной бактериальной флоры, в группе пациентов с биопсией нижних отделов – 61,4% и 72,6% (р=0,4) и верхних отделов – 85,7% и 86,4%, соответственно (р=0,8). Основным фактором, оказавшим достоверное влияние на ОВ пациентов, которым проводилась биопсия толстой кишки, была гистологическая степень тяжести оРТПХ, так при легкой степени 1-летняя ОВ составила 88,2%, при средней степени тяжести – 47,6%, при тяжелой – 40,0%, а в случае отсутствия оРТПХ – 60,2% (р=0,01). При исследовании верхних отделов ОВ различалась, у пациентов с РТПХ составила 72,0%, без РТПХ – 95,2% (р=0,04). Однако степень выраженности РТПХ достоверно не изменяла ОВ, при 1 степени – 78,75%, при 2 – 60% (р=0,15), возможно, вследствие маленькой выборки (n=15). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Полученные данные демонстрируют неоднородность этиологии поражения различных отделов ЖКТ после алло-ТГСК, что подчеркивает необходимость гистологического и ПЦР исследования биоптатов ЖКТ. Возможно, из-за небольшой выборки пациентов, в исследовании не было показано влияния вирусного и бактериального поражения ЖКТ на выживаемость. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, острая реакция трансплантат против хозяина, желудочно-кишечный тракт, гистологическое исследование. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7088) "
Введение
Острая реакция трансплантат против хозяина (оРТПХ) с поражением желудочно-кишечного тракта (ЖКТ) – это одно из наиболее угрожающих осложнений у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). В настоящее время не существует стандартов по диагностике этого состояния. Клинические симптомы оРТПХ являются неспецифичными и могут мимикрировать под другие патологические состояния. Цель нашей работы заключается в анализе результатов гистологических исследований слизистых толстой кишки и верхнего отдела ЖКТ (желудка, двенадцатиперстной кишки, пищевода) у пациентов после алло-ТГСК, определении частоты выявления различных патологий ЖКТ после алло-ТГСК.
Пациенты и методы
В ретроспективное исследование были включены 112 пациентов после алло-ТГСК. Большинство пациентов (68%) проходили лечение по поводу острого лейкоза. Медиана возраста в исследуемой группе составила 30 лет (2-67 лет). Всем пациентам была проведена фиброгастродуоденоскопия и/или фиброколоноскопия, выполнена биопсия и гистологическое исследование органов желудочно-кишечного тракта. Методом ПЦР в биоптатах выявляли вирус простого герпеса 1, 2, герпеса 6 типа и цитомегаловирус, а также проводили бактериологическое исследование кала на условно-патогенную флору и ИФА на C. difficile. Медиана времени выполнения биопсии после трансплантации составила 84 дня (15-413 дней). Исследования проводились по поводу различных симптомов поражения ЖКТ для верификации диагноза. В 56% случаев была выполнена биопсия толстой кишки, в 35% – биопсия верхних отделов ЖКТ (желудок, двенадцатиперстная кишка, пищевод), а также в 9% проводилось исследование обоих отделов.
Результаты
При биопсии толстой кишки признаки оРТПХ наблюдалась в 73,5% случаев и чаще, чем при биопсии верхнего отдела ЖКТ (36,5%, р=0,02). В нижних отделах ЖКТ легкая гистологическая степень оРТПХ определялась в 56% случаев, средней тяжести – в 28%, тяжелая – в 16%. В верхних отделах ЖКТ наблюдались легкие проявления РТПХ у 60% и средней тяжести – у 33%. Вирусная инфекция чаще наблюдалась при биопсии нижнего отдела ЖКТ (53% и 36%, р=0,046). Бактериальная инфекция встречалась у 38% и 19% пациентов, с биопсией нижнего и верхнего отделов ЖКТ соответственно (р=0,56). У пациентов, которым была выполнена биопсия толстой кишки, вирусная инфекция не влияла на 1-летнюю общую выживаемость (ОВ) (65,2% и 64,7%, р=0,67). Такая же картина наблюдалось при биопсии верхних отделов ЖКТ (85,7% и 86,4%, р=0,8). ОВ не зависела от наличия условно-патогенной бактериальной флоры, в группе пациентов с биопсией нижних отделов – 61,4% и 72,6% (р=0,4) и верхних отделов – 85,7% и 86,4%, соответственно (р=0,8). Основным фактором, оказавшим достоверное влияние на ОВ пациентов, которым проводилась биопсия толстой кишки, была гистологическая степень тяжести оРТПХ, так при легкой степени 1-летняя ОВ составила 88,2%, при средней степени тяжести – 47,6%, при тяжелой – 40,0%, а в случае отсутствия оРТПХ – 60,2% (р=0,01). При исследовании верхних отделов ОВ различалась, у пациентов с РТПХ составила 72,0%, без РТПХ – 95,2% (р=0,04). Однако степень выраженности РТПХ достоверно не изменяла ОВ, при 1 степени – 78,75%, при 2 – 60% (р=0,15), возможно, вследствие маленькой выборки (n=15).
Заключение
Полученные данные демонстрируют неоднородность этиологии поражения различных отделов ЖКТ после алло-ТГСК, что подчеркивает необходимость гистологического и ПЦР исследования биоптатов ЖКТ. Возможно, из-за небольшой выборки пациентов, в исследовании не было показано влияния вирусного и бактериального поражения ЖКТ на выживаемость.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, острая реакция трансплантат против хозяина, желудочно-кишечный тракт, гистологическое исследование.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(7088) "Введение
Острая реакция трансплантат против хозяина (оРТПХ) с поражением желудочно-кишечного тракта (ЖКТ) – это одно из наиболее угрожающих осложнений у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). В настоящее время не существует стандартов по диагностике этого состояния. Клинические симптомы оРТПХ являются неспецифичными и могут мимикрировать под другие патологические состояния. Цель нашей работы заключается в анализе результатов гистологических исследований слизистых толстой кишки и верхнего отдела ЖКТ (желудка, двенадцатиперстной кишки, пищевода) у пациентов после алло-ТГСК, определении частоты выявления различных патологий ЖКТ после алло-ТГСК.
Пациенты и методы
В ретроспективное исследование были включены 112 пациентов после алло-ТГСК. Большинство пациентов (68%) проходили лечение по поводу острого лейкоза. Медиана возраста в исследуемой группе составила 30 лет (2-67 лет). Всем пациентам была проведена фиброгастродуоденоскопия и/или фиброколоноскопия, выполнена биопсия и гистологическое исследование органов желудочно-кишечного тракта. Методом ПЦР в биоптатах выявляли вирус простого герпеса 1, 2, герпеса 6 типа и цитомегаловирус, а также проводили бактериологическое исследование кала на условно-патогенную флору и ИФА на C. difficile. Медиана времени выполнения биопсии после трансплантации составила 84 дня (15-413 дней). Исследования проводились по поводу различных симптомов поражения ЖКТ для верификации диагноза. В 56% случаев была выполнена биопсия толстой кишки, в 35% – биопсия верхних отделов ЖКТ (желудок, двенадцатиперстная кишка, пищевод), а также в 9% проводилось исследование обоих отделов.
Результаты
При биопсии толстой кишки признаки оРТПХ наблюдалась в 73,5% случаев и чаще, чем при биопсии верхнего отдела ЖКТ (36,5%, р=0,02). В нижних отделах ЖКТ легкая гистологическая степень оРТПХ определялась в 56% случаев, средней тяжести – в 28%, тяжелая – в 16%. В верхних отделах ЖКТ наблюдались легкие проявления РТПХ у 60% и средней тяжести – у 33%. Вирусная инфекция чаще наблюдалась при биопсии нижнего отдела ЖКТ (53% и 36%, р=0,046). Бактериальная инфекция встречалась у 38% и 19% пациентов, с биопсией нижнего и верхнего отделов ЖКТ соответственно (р=0,56). У пациентов, которым была выполнена биопсия толстой кишки, вирусная инфекция не влияла на 1-летнюю общую выживаемость (ОВ) (65,2% и 64,7%, р=0,67). Такая же картина наблюдалось при биопсии верхних отделов ЖКТ (85,7% и 86,4%, р=0,8). ОВ не зависела от наличия условно-патогенной бактериальной флоры, в группе пациентов с биопсией нижних отделов – 61,4% и 72,6% (р=0,4) и верхних отделов – 85,7% и 86,4%, соответственно (р=0,8). Основным фактором, оказавшим достоверное влияние на ОВ пациентов, которым проводилась биопсия толстой кишки, была гистологическая степень тяжести оРТПХ, так при легкой степени 1-летняя ОВ составила 88,2%, при средней степени тяжести – 47,6%, при тяжелой – 40,0%, а в случае отсутствия оРТПХ – 60,2% (р=0,01). При исследовании верхних отделов ОВ различалась, у пациентов с РТПХ составила 72,0%, без РТПХ – 95,2% (р=0,04). Однако степень выраженности РТПХ достоверно не изменяла ОВ, при 1 степени – 78,75%, при 2 – 60% (р=0,15), возможно, вследствие маленькой выборки (n=15).
Заключение
Полученные данные демонстрируют неоднородность этиологии поражения различных отделов ЖКТ после алло-ТГСК, что подчеркивает необходимость гистологического и ПЦР исследования биоптатов ЖКТ. Возможно, из-за небольшой выборки пациентов, в исследовании не было показано влияния вирусного и бактериального поражения ЖКТ на выживаемость.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, острая реакция трансплантат против хозяина, желудочно-кишечный тракт, гистологическое исследование.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20357" ["VALUE"]=> array(2) { ["TEXT"]=> string(482) "<sup>1</sup> НИИ Детской Онкологии, Гематологии и Трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова<br> <sup>2</sup> ФГБУ «Детский научно-клинический центр инфекционных болезней»<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(446) "1 НИИ Детской Онкологии, Гематологии и Трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова2 ФГБУ «Детский научно-клинический центр инфекционных болезней»
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(446) "1 НИИ Детской Онкологии, Гематологии и Трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова
2 ФГБУ «Детский научно-клинический центр инфекционных болезней»
" } } } [25]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1557" ["~ID"]=> string(4) "1557" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(269) "Клинический случай эффективной трансплантации фекальной микробиоты в терапии острой реакции трансплантат против хозяина с поражением кишечника" ["~NAME"]=> string(269) "Клинический случай эффективной трансплантации фекальной микробиоты в терапии острой реакции трансплантат против хозяина с поражением кишечника" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:27:01" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:27:01" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/klinicheskiy-sluchay-effektivnoy-transplantatsii-fekalnoy-mikrobioty-v-terapii-ostroy-reaktsii-trans/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/klinicheskiy-sluchay-effektivnoy-transplantatsii-fekalnoy-mikrobioty-v-terapii-ostroy-reaktsii-trans/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "html" ["~DETAIL_TEXT_TYPE"]=> string(4) "html" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "klinicheskiy-sluchay-effektivnoy-transplantatsii-fekalnoy-mikrobioty-v-terapii-ostroy-reaktsii-trans" ["~CODE"]=> string(100) "klinicheskiy-sluchay-effektivnoy-transplantatsii-fekalnoy-mikrobioty-v-terapii-ostroy-reaktsii-trans" ["EXTERNAL_ID"]=> string(4) "1557" ["~EXTERNAL_ID"]=> string(4) "1557" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(269) "Клинический случай эффективной трансплантации фекальной микробиоты в терапии острой реакции трансплантат против хозяина с поражением кишечника" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(382) "Клинический случай эффективной трансплантации фекальной микробиоты в терапии острой реакции трансплантат против хозяина с поражением кишечникаCase report of effective fecal microbiota transplantation to alleviate acute intestinal graft-versus-host disease" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(8916) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> При проведении аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), вследствие применения цитостатических и антибактериальных препаратов, изменений в диете нарушается состав микробиоты желудочно-кишечного тракта (ЖКТ). Накапливаются данные о том, что микробиота влияет на работу иммунной системы человека, подавляет развитие патогенных микроорганизмов, способствует регенерации эпителия, что препятствует появлению иммунных и инфекционных осложнений после алло-ТГСК. Трансплантация фекальной микробиоты (ТФМ) направлена на восстановление микрофлоры ЖКТ реципиента. </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Цель работы состояла в демонстрации клинического случая стероид-резистентного течения острой реакции «трансплантат против хозяина» (оРТПХ) 3 степени тяжести, 4 стадия кишечных проявлений, в котором ТФМ в сочетании с иммуносупрессиной терапии, привела к разрешению оРТПХ кишечника. </p> <h2 style="text-align: justify;">Описание случая</h2> <p style="text-align: justify;"> Пациент, мужчина, 45 лет. Диагноз: острый миелобластный лейкоз с изменениями, связанными с миелодисплазией. Первые симптомы миелодиспластического синдрома с избытком бластов в марте 2016 года. Проведено 6 курсов 5-азацитидина. 20.02.17 – трансформация в ОМЛ. Терапия малыми дозами цитозара. 23.09.17 алло-ТГСК от неродственного донора с режимом кондиционирования флюдарабин + бусульфан (12 мг/кг). Профилактика РТПХ: тимоглобулин, такролимус, MMF. В связи с высоким риском развития рецидива, на Д+67 снижение дозы такролимуса, с полной отменой на Д+82. С Д+102 диарея до 3 л/сутки. Д+110 – госпитализация в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой. Cтул в объеме 5 л/сутки, сепсис (лихорадка 38°C, СРБ – 331 мг/л), начата эмпирическая антибактериальная терапия (дорипенем, ванкомицин). Биопсия слизистой толстой кишки (Д+114) – признаки умеренно выраженной РТПХ, вирусного поражения кишечника (ПЦР – HHV-6+, CMV+, EBV+). На Д+114 возобновлен такролимус, начат метилпреднизолон 2 мг/кг, ганцикловир 10 мг/кг. Д+118 – объем стула 13 л/сутки. С Д+117 из-за неэффективности терапии 1 линии начата терапия 2 линии – руксолитиниб 20 мг/сутки. Такролимус, в связи с развитием острого повреждения почек, заменен на сиролимус (Д+121). Д+133 – снижение объема стула до 3 л/сутки. При бактериологическом исследовании стула (Д+138) – обильный рост полирезистентной<i> K. Pneumoniae</i>. При 16S-секвенировании, 99% микробиоты ЖКТ составляло семейство <i>Staphylococcaceae</i>. Ответ по РТПХ кишки не достигнут, с Д +139 до Д+221 – продолжающееся кишечное кровотечение, геморрагический шок от Д+144 (Hb=39 г/л). Суммарно за весь период введено: эритроцитарная масса 29,8 л, тромбоцитарная масса 5,52 л, свежезамороженная плазма – 5,92 л. Получал терапию в отделении реанимации с Д+118 по Д+284. В этот период развились следующие осложнения: тяжелый сепсис, вызванный полирезистентными штаммами K. <i>pneumoniae </i>(Д+149) и <i>Acinetobacter spp</i>. (с Д+159 по Д+198) (уровень СРБ до 449 мг/л, пресепсина до 12839 пг/мл), двухсторонняя пневмония (<i>K. Pneumonia, Pseudomonas spp.</i>), полиорганная недостаточность (сердечно-сосудистая, печеночная, дыхательная, церебральная). Искусственная вентиляция легких в течение 83 дней. На Д+192 и +194 в связи с недостаточным эффектом от иммуносупрессивной терапии проведена ТФМ объемом 80 и 300 мл, через назоинтестинальный зонд, установленный под контролем эндоскопа. За 14 дней объем стула снизился до 1 л/сутки (Д+208), а на Д+280 до 500 мл/сутки, с Д+221 впервые отсутствие крови в стуле. В результате ТФМ, <i>K. pneumoniae</i>, ранее продуцирующая фермент металло-бета-лактамазу (NDM+), сменилась штаммом чувствительным к антибиотикам (NDM-). Это позволило назначить цефтазидим+авибактам с положительным эффектом (снижение прокальцитонина с 26,8 до 0,8 нг/мл). По данным ПЦР образцов стула после ТФМ значительно повысилась общая бактериальная масса (с пиком на Д+8 – Д+16 после ТФМ), за счет увеличения <i>Bacteroides fragilis, Bacteroides </i><i>thetaiataomicron, Lactobacillus spp., Bifidobacterium spp. </i>Полная отмена руксолитиниба на Д+284 и сиролимуса на Д+294. По результатам контрольной биопсии (Д+337) убедительных признаков РТПХ и вирусного поражения кишечника не выявлено (ПЦР – HHV-6 -, CMV -, EBV -). В настоящее время – стул с тенденцией к оформлению (около 300 г/сутки). Питание самостоятельное и дополнительное через гастростому. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> В представленном случае продемонстрировано эффективное применение ТФМ в сочетании с JAK2 ингибитором у пациента со стероид-резистентным течением оРТПХ и тяжелыми инфекционными осложнениями. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, стероид-резистентная реакция трансплантат против хозяина, трансплантация фекальной микробиоты, микробиота кишечника. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(269) "Клинический случай эффективной трансплантации фекальной микробиоты в терапии острой реакции трансплантат против хозяина с поражением кишечника" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(269) "Клинический случай эффективной трансплантации фекальной микробиоты в терапии острой реакции трансплантат против хозяина с поражением кишечника" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(269) "Клинический случай эффективной трансплантации фекальной микробиоты в терапии острой реакции трансплантат против хозяина с поражением кишечника" ["SECTION_META_TITLE"]=> string(269) "Клинический случай эффективной трансплантации фекальной микробиоты в терапии острой реакции трансплантат против хозяина с поражением кишечника" ["SECTION_META_KEYWORDS"]=> string(269) "Клинический случай эффективной трансплантации фекальной микробиоты в терапии острой реакции трансплантат против хозяина с поражением кишечника" ["SECTION_META_DESCRIPTION"]=> string(269) "Клинический случай эффективной трансплантации фекальной микробиоты в терапии острой реакции трансплантат против хозяина с поражением кишечника" ["SECTION_PICTURE_FILE_ALT"]=> string(269) "Клинический случай эффективной трансплантации фекальной микробиоты в терапии острой реакции трансплантат против хозяина с поражением кишечника" ["SECTION_PICTURE_FILE_TITLE"]=> string(269) "Клинический случай эффективной трансплантации фекальной микробиоты в терапии острой реакции трансплантат против хозяина с поражением кишечника" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "klinicheskiy-sluchay-effektivnoy-transplantatsii-fekalnoy-mikrobioty-v-terapii-ostroy-reaktsii-trans" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(269) "Клинический случай эффективной трансплантации фекальной микробиоты в терапии острой реакции трансплантат против хозяина с поражением кишечника" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(269) "Клинический случай эффективной трансплантации фекальной микробиоты в терапии острой реакции трансплантат против хозяина с поражением кишечника" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "klinicheskiy-sluchay-effektivnoy-transplantatsii-fekalnoy-mikrobioty-v-terapii-ostroy-reaktsii-trans" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "klinicheskiy-sluchay-effektivnoy-transplantatsii-fekalnoy-mikrobioty-v-terapii-ostroy-reaktsii-trans" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "klinicheskiy-sluchay-effektivnoy-transplantatsii-fekalnoy-mikrobioty-v-terapii-ostroy-reaktsii-trans" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20333" ["VALUE"]=> array(2) { ["TEXT"]=> string(660) "Дарья В. Чуракина <sup>1</sup>, Олег В. Голощапов <sup>1</sup>, Ольга В. Пирогова <sup>1</sup>, Александр Н. Швецов <sup>1</sup>, Руслана В. Клементьева <sup>1</sup>, Александр А. Щербаков <sup>1</sup>, Сергей В. Сидоренко <sup>2</sup>, Владимир А. Гостев <sup>2</sup>, Мария А. Суворова <sup>3</sup>, Юрий В. Лобзин <sup>2</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "TEXT" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(528) "Дарья В. Чуракина 1, Олег В. Голощапов 1, Ольга В. Пирогова 1, Александр Н. Швецов 1, Руслана В. Клементьева 1, Александр А. Щербаков 1, Сергей В. Сидоренко 2, Владимир А. Гостев 2, Мария А. Суворова 3, Юрий В. Лобзин 2, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "TEXT" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20334" ["VALUE"]=> array(2) { ["TEXT"]=> string(679) "<sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербург, Российская Федерация, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова<br> <sup>2</sup> ФГБУ ДНКЦИБ ФМБА России<br> <sup>3</sup> Научно-исследовательская лаборатория Explana, Санкт-Петербург, Российская Федерация<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(625) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербург, Российская Федерация, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова
2 ФГБУ ДНКЦИБ ФМБА России
3 Научно-исследовательская лаборатория Explana, Санкт-Петербург, Российская Федерация
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20732" ["VALUE"]=> array(2) { ["TEXT"]=> string(8916) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> При проведении аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), вследствие применения цитостатических и антибактериальных препаратов, изменений в диете нарушается состав микробиоты желудочно-кишечного тракта (ЖКТ). Накапливаются данные о том, что микробиота влияет на работу иммунной системы человека, подавляет развитие патогенных микроорганизмов, способствует регенерации эпителия, что препятствует появлению иммунных и инфекционных осложнений после алло-ТГСК. Трансплантация фекальной микробиоты (ТФМ) направлена на восстановление микрофлоры ЖКТ реципиента. </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Цель работы состояла в демонстрации клинического случая стероид-резистентного течения острой реакции «трансплантат против хозяина» (оРТПХ) 3 степени тяжести, 4 стадия кишечных проявлений, в котором ТФМ в сочетании с иммуносупрессиной терапии, привела к разрешению оРТПХ кишечника. </p> <h2 style="text-align: justify;">Описание случая</h2> <p style="text-align: justify;"> Пациент, мужчина, 45 лет. Диагноз: острый миелобластный лейкоз с изменениями, связанными с миелодисплазией. Первые симптомы миелодиспластического синдрома с избытком бластов в марте 2016 года. Проведено 6 курсов 5-азацитидина. 20.02.17 – трансформация в ОМЛ. Терапия малыми дозами цитозара. 23.09.17 алло-ТГСК от неродственного донора с режимом кондиционирования флюдарабин + бусульфан (12 мг/кг). Профилактика РТПХ: тимоглобулин, такролимус, MMF. В связи с высоким риском развития рецидива, на Д+67 снижение дозы такролимуса, с полной отменой на Д+82. С Д+102 диарея до 3 л/сутки. Д+110 – госпитализация в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой. Cтул в объеме 5 л/сутки, сепсис (лихорадка 38°C, СРБ – 331 мг/л), начата эмпирическая антибактериальная терапия (дорипенем, ванкомицин). Биопсия слизистой толстой кишки (Д+114) – признаки умеренно выраженной РТПХ, вирусного поражения кишечника (ПЦР – HHV-6+, CMV+, EBV+). На Д+114 возобновлен такролимус, начат метилпреднизолон 2 мг/кг, ганцикловир 10 мг/кг. Д+118 – объем стула 13 л/сутки. С Д+117 из-за неэффективности терапии 1 линии начата терапия 2 линии – руксолитиниб 20 мг/сутки. Такролимус, в связи с развитием острого повреждения почек, заменен на сиролимус (Д+121). Д+133 – снижение объема стула до 3 л/сутки. При бактериологическом исследовании стула (Д+138) – обильный рост полирезистентной<i> K. Pneumoniae</i>. При 16S-секвенировании, 99% микробиоты ЖКТ составляло семейство <i>Staphylococcaceae</i>. Ответ по РТПХ кишки не достигнут, с Д +139 до Д+221 – продолжающееся кишечное кровотечение, геморрагический шок от Д+144 (Hb=39 г/л). Суммарно за весь период введено: эритроцитарная масса 29,8 л, тромбоцитарная масса 5,52 л, свежезамороженная плазма – 5,92 л. Получал терапию в отделении реанимации с Д+118 по Д+284. В этот период развились следующие осложнения: тяжелый сепсис, вызванный полирезистентными штаммами K. <i>pneumoniae </i>(Д+149) и <i>Acinetobacter spp</i>. (с Д+159 по Д+198) (уровень СРБ до 449 мг/л, пресепсина до 12839 пг/мл), двухсторонняя пневмония (<i>K. Pneumonia, Pseudomonas spp.</i>), полиорганная недостаточность (сердечно-сосудистая, печеночная, дыхательная, церебральная). Искусственная вентиляция легких в течение 83 дней. На Д+192 и +194 в связи с недостаточным эффектом от иммуносупрессивной терапии проведена ТФМ объемом 80 и 300 мл, через назоинтестинальный зонд, установленный под контролем эндоскопа. За 14 дней объем стула снизился до 1 л/сутки (Д+208), а на Д+280 до 500 мл/сутки, с Д+221 впервые отсутствие крови в стуле. В результате ТФМ, <i>K. pneumoniae</i>, ранее продуцирующая фермент металло-бета-лактамазу (NDM+), сменилась штаммом чувствительным к антибиотикам (NDM-). Это позволило назначить цефтазидим+авибактам с положительным эффектом (снижение прокальцитонина с 26,8 до 0,8 нг/мл). По данным ПЦР образцов стула после ТФМ значительно повысилась общая бактериальная масса (с пиком на Д+8 – Д+16 после ТФМ), за счет увеличения <i>Bacteroides fragilis, Bacteroides </i><i>thetaiataomicron, Lactobacillus spp., Bifidobacterium spp. </i>Полная отмена руксолитиниба на Д+284 и сиролимуса на Д+294. По результатам контрольной биопсии (Д+337) убедительных признаков РТПХ и вирусного поражения кишечника не выявлено (ПЦР – HHV-6 -, CMV -, EBV -). В настоящее время – стул с тенденцией к оформлению (около 300 г/сутки). Питание самостоятельное и дополнительное через гастростому. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> В представленном случае продемонстрировано эффективное применение ТФМ в сочетании с JAK2 ингибитором у пациента со стероид-резистентным течением оРТПХ и тяжелыми инфекционными осложнениями. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, стероид-резистентная реакция трансплантат против хозяина, трансплантация фекальной микробиоты, микробиота кишечника. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(8588) "
Введение
При проведении аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), вследствие применения цитостатических и антибактериальных препаратов, изменений в диете нарушается состав микробиоты желудочно-кишечного тракта (ЖКТ). Накапливаются данные о том, что микробиота влияет на работу иммунной системы человека, подавляет развитие патогенных микроорганизмов, способствует регенерации эпителия, что препятствует появлению иммунных и инфекционных осложнений после алло-ТГСК. Трансплантация фекальной микробиоты (ТФМ) направлена на восстановление микрофлоры ЖКТ реципиента.
Цель работы
Цель работы состояла в демонстрации клинического случая стероид-резистентного течения острой реакции «трансплантат против хозяина» (оРТПХ) 3 степени тяжести, 4 стадия кишечных проявлений, в котором ТФМ в сочетании с иммуносупрессиной терапии, привела к разрешению оРТПХ кишечника.
Описание случая
Пациент, мужчина, 45 лет. Диагноз: острый миелобластный лейкоз с изменениями, связанными с миелодисплазией. Первые симптомы миелодиспластического синдрома с избытком бластов в марте 2016 года. Проведено 6 курсов 5-азацитидина. 20.02.17 – трансформация в ОМЛ. Терапия малыми дозами цитозара. 23.09.17 алло-ТГСК от неродственного донора с режимом кондиционирования флюдарабин + бусульфан (12 мг/кг). Профилактика РТПХ: тимоглобулин, такролимус, MMF. В связи с высоким риском развития рецидива, на Д+67 снижение дозы такролимуса, с полной отменой на Д+82. С Д+102 диарея до 3 л/сутки. Д+110 – госпитализация в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой. Cтул в объеме 5 л/сутки, сепсис (лихорадка 38°C, СРБ – 331 мг/л), начата эмпирическая антибактериальная терапия (дорипенем, ванкомицин). Биопсия слизистой толстой кишки (Д+114) – признаки умеренно выраженной РТПХ, вирусного поражения кишечника (ПЦР – HHV-6+, CMV+, EBV+). На Д+114 возобновлен такролимус, начат метилпреднизолон 2 мг/кг, ганцикловир 10 мг/кг. Д+118 – объем стула 13 л/сутки. С Д+117 из-за неэффективности терапии 1 линии начата терапия 2 линии – руксолитиниб 20 мг/сутки. Такролимус, в связи с развитием острого повреждения почек, заменен на сиролимус (Д+121). Д+133 – снижение объема стула до 3 л/сутки. При бактериологическом исследовании стула (Д+138) – обильный рост полирезистентной K. Pneumoniae. При 16S-секвенировании, 99% микробиоты ЖКТ составляло семейство Staphylococcaceae. Ответ по РТПХ кишки не достигнут, с Д +139 до Д+221 – продолжающееся кишечное кровотечение, геморрагический шок от Д+144 (Hb=39 г/л). Суммарно за весь период введено: эритроцитарная масса 29,8 л, тромбоцитарная масса 5,52 л, свежезамороженная плазма – 5,92 л. Получал терапию в отделении реанимации с Д+118 по Д+284. В этот период развились следующие осложнения: тяжелый сепсис, вызванный полирезистентными штаммами K. pneumoniae (Д+149) и Acinetobacter spp. (с Д+159 по Д+198) (уровень СРБ до 449 мг/л, пресепсина до 12839 пг/мл), двухсторонняя пневмония (K. Pneumonia, Pseudomonas spp.), полиорганная недостаточность (сердечно-сосудистая, печеночная, дыхательная, церебральная). Искусственная вентиляция легких в течение 83 дней. На Д+192 и +194 в связи с недостаточным эффектом от иммуносупрессивной терапии проведена ТФМ объемом 80 и 300 мл, через назоинтестинальный зонд, установленный под контролем эндоскопа. За 14 дней объем стула снизился до 1 л/сутки (Д+208), а на Д+280 до 500 мл/сутки, с Д+221 впервые отсутствие крови в стуле. В результате ТФМ, K. pneumoniae, ранее продуцирующая фермент металло-бета-лактамазу (NDM+), сменилась штаммом чувствительным к антибиотикам (NDM-). Это позволило назначить цефтазидим+авибактам с положительным эффектом (снижение прокальцитонина с 26,8 до 0,8 нг/мл). По данным ПЦР образцов стула после ТФМ значительно повысилась общая бактериальная масса (с пиком на Д+8 – Д+16 после ТФМ), за счет увеличения Bacteroides fragilis, Bacteroides thetaiataomicron, Lactobacillus spp., Bifidobacterium spp. Полная отмена руксолитиниба на Д+284 и сиролимуса на Д+294. По результатам контрольной биопсии (Д+337) убедительных признаков РТПХ и вирусного поражения кишечника не выявлено (ПЦР – HHV-6 -, CMV -, EBV -). В настоящее время – стул с тенденцией к оформлению (около 300 г/сутки). Питание самостоятельное и дополнительное через гастростому.
Заключение
В представленном случае продемонстрировано эффективное применение ТФМ в сочетании с JAK2 ингибитором у пациента со стероид-резистентным течением оРТПХ и тяжелыми инфекционными осложнениями.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, стероид-резистентная реакция трансплантат против хозяина, трансплантация фекальной микробиоты, микробиота кишечника.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20335" ["VALUE"]=> array(2) { ["TEXT"]=> string(503) "Darya V. Churakina <sup>1</sup>, Oleg V. Goloshchapov <sup>1</sup>, Olga V. Pirogova <sup>1</sup>, Aleksander N. Shvetsov <sup>1</sup>, Ruslana V. Klementeva <sup>1</sup>, Aleksandr A. Shcherbakov <sup>1</sup>, Sergey V. Sidorenko <sup>2</sup>, Vladimir A. Gostev <sup>2</sup>, Maria A. Suvorova <sup>3</sup>, Yuri V. Lobzin <sup>2</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(371) "Darya V. Churakina 1, Oleg V. Goloshchapov 1, Olga V. Pirogova 1, Aleksander N. Shvetsov 1, Ruslana V. Klementeva 1, Aleksandr A. Shcherbakov 1, Sergey V. Sidorenko 2, Vladimir A. Gostev 2, Maria A. Suvorova 3, Yuri V. Lobzin 2, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20336" ["VALUE"]=> array(2) { ["TEXT"]=> string(429) "<sup>1</sup> R. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation<br> <sup>2</sup> Research Scientific Institute of Children’s Infections, St. Petersburg, Russian Federation<br> <sup>3</sup> The Explana Research Laboratory, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(381) "1 R. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation2 Research Scientific Institute of Children’s Infections, St. Petersburg, Russian Federation
3 The Explana Research Laboratory, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20341" ["VALUE"]=> array(2) { ["TEXT"]=> string(4846) "<p style="text-align: justify;"> In allogeneic hematopoietic stem cell transplantation (HSCT), the recipients have altered composition of gastrointestinal (GI) microbiota, due to the use of cytostatic and antibacterial drugs, changes in diet. There is a growing evidence that microbiota influences the immune system, suppresses pathogenic bacteria, promotes regeneration of the GI mucosa. It may prevent immune and infectious complications after HSCT. Transplantation of fecal microbiota (FMT) is directed to recovery of recipient microflora. Our aim was to present a clinical case of a patient with steroid-resistant intestinal graft-versus-host disease (GVHD), stage 4, grade 3, therefore treated by FMT. </p> <h2 style="text-align: justify;">Case description</h2> <p style="text-align: justify;"> A forty-five year old patient underwent HSCT in Sep 2017, for secondary acute myeloid leukemia (AML) evolving from myelodysplastic syndrome. Hematopoietic graft was from unrelated donor, conditioning regimen included fludarabin+ busulphan (12 mg/kg). Prevention of GVHD was performed with thymoglobulin, tacrolimus, MMF. Since D+67, tacrolimus was tapered and stopped at D+82 due to high relapse risk. From D+102, persistent diarrhea syndrome developed, with up to 3 L/d. The patient was admitted to the R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation. The diarrhea volume reached 5 L/d, and the patient has became septic (fever of 38oC, serum CRP, 331mg/L). Empirical antibiotic therapy consisted of doripenem, vancomycin. Colon biopsy (D+114) identified histological grade 2 of GVHD and multiple viral infection (PCR-positive for HHV-6, CMV, EBV). Tacrolimus was restarted, methylprednisolone at 2 mg/kg, and ganciclovir 10 mg/kg were administered. After 7 days of therapy, the diarrhea volume was 13 L/d. After failure of the first-line treatment, ruxolitimib (20 mg/d) was administered. Due to acute kidney injury, tacrolimus was replaced by sirolimus. At D+133, the diarrhea decreased to 3 L/d. Meanwhile, the stool samples became positive for antibiotic-resistant K. Pneumonia (D+138). The 16S rRNA gene sequencing showed the Staphylococcaceae family to represent 99% of intestinal microbiota. Despite reduced stool volume, no clinical response was achieved. GI bleeding continued from D+139 to D+221 followed by hemorrhagic shock observed at D+144, with blood hemoglobin levels of 39 g/L. In total, the patient was transfused with 29.8 L of RBCs, 5.5 L of platelet concentrate, and 5.9 L of fresh-frozen plasma.<br> The patient was treated at the ICU from D+118 to D+284 posttransplant. Over this time period, the patient suffered with severe polyresistant K. pneumoniae sepsis (D+149), Acinetobacter spp. infection (D+159 to D+198). СRP levels reached 449 mg/L, presepsin was increased to 12839 pg/ml, along with features of multiple organ failure (cardiovascular, hepatic, respiratory, cerebral affection), bilateral pneumonia (K. Pneumonia, Pseudomonas spp.). Artificial lung ventilation was performed for 83 days.<br> Considering persistent GI bleeding and multiple antibiotic- resistant bacterial complications the patient received TFM via naso-intestinal tube installed under endoscopical control, at the doses of, 80 and 300 mL on D+192 and D+194, respectively. Fourteen days later (D+208), the diarrhea decreased to 1 L/d, and to <500 mL/d by D+280 where GI bleeding was undetectable since D+221. Following the TFM procedure, the beta-lactamase-positive K. pneumoniae (NDM+), was replaced by a more sensitive strain (NDM-), thus enabling ceftazidim+avibactam treatment with a positive effect. Multiple PCR of stool sample has shown an increased bacterial mass, with a maximum at D+8 to D+16 after FMT, with increase in Bacteroides fragilis, Bacteroides thetaiataomicron, Lactobacillus and Bifidobacterium microbial species. Ruxolitimib and Sirolimus were discontinued at D+284 and D+294, respectively. No signs of GVHD were revealed at control GI biopsy, and viral infections (HHV-6, CMV, EBV) were not detectable. The feeding is fully enteral now, with supplementation via gastrostoma. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The present case report suggests an effective curation of the patient with steroid-resistant GVHD and severe infectious complications observed under combined treatment with JAK2 inhibitor and TFM. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cell transplantation, steroid-resistant graft-versus-host disease, fecal microbiota transplantation, microbiota. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4676) "
In allogeneic hematopoietic stem cell transplantation (HSCT), the recipients have altered composition of gastrointestinal (GI) microbiota, due to the use of cytostatic and antibacterial drugs, changes in diet. There is a growing evidence that microbiota influences the immune system, suppresses pathogenic bacteria, promotes regeneration of the GI mucosa. It may prevent immune and infectious complications after HSCT. Transplantation of fecal microbiota (FMT) is directed to recovery of recipient microflora. Our aim was to present a clinical case of a patient with steroid-resistant intestinal graft-versus-host disease (GVHD), stage 4, grade 3, therefore treated by FMT.
Case description
A forty-five year old patient underwent HSCT in Sep 2017, for secondary acute myeloid leukemia (AML) evolving from myelodysplastic syndrome. Hematopoietic graft was from unrelated donor, conditioning regimen included fludarabin+ busulphan (12 mg/kg). Prevention of GVHD was performed with thymoglobulin, tacrolimus, MMF. Since D+67, tacrolimus was tapered and stopped at D+82 due to high relapse risk. From D+102, persistent diarrhea syndrome developed, with up to 3 L/d. The patient was admitted to the R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation. The diarrhea volume reached 5 L/d, and the patient has became septic (fever of 38oC, serum CRP, 331mg/L). Empirical antibiotic therapy consisted of doripenem, vancomycin. Colon biopsy (D+114) identified histological grade 2 of GVHD and multiple viral infection (PCR-positive for HHV-6, CMV, EBV). Tacrolimus was restarted, methylprednisolone at 2 mg/kg, and ganciclovir 10 mg/kg were administered. After 7 days of therapy, the diarrhea volume was 13 L/d. After failure of the first-line treatment, ruxolitimib (20 mg/d) was administered. Due to acute kidney injury, tacrolimus was replaced by sirolimus. At D+133, the diarrhea decreased to 3 L/d. Meanwhile, the stool samples became positive for antibiotic-resistant K. Pneumonia (D+138). The 16S rRNA gene sequencing showed the Staphylococcaceae family to represent 99% of intestinal microbiota. Despite reduced stool volume, no clinical response was achieved. GI bleeding continued from D+139 to D+221 followed by hemorrhagic shock observed at D+144, with blood hemoglobin levels of 39 g/L. In total, the patient was transfused with 29.8 L of RBCs, 5.5 L of platelet concentrate, and 5.9 L of fresh-frozen plasma.
The patient was treated at the ICU from D+118 to D+284 posttransplant. Over this time period, the patient suffered with severe polyresistant K. pneumoniae sepsis (D+149), Acinetobacter spp. infection (D+159 to D+198). СRP levels reached 449 mg/L, presepsin was increased to 12839 pg/ml, along with features of multiple organ failure (cardiovascular, hepatic, respiratory, cerebral affection), bilateral pneumonia (K. Pneumonia, Pseudomonas spp.). Artificial lung ventilation was performed for 83 days.
Considering persistent GI bleeding and multiple antibiotic- resistant bacterial complications the patient received TFM via naso-intestinal tube installed under endoscopical control, at the doses of, 80 and 300 mL on D+192 and D+194, respectively. Fourteen days later (D+208), the diarrhea decreased to 1 L/d, and to <500 mL/d by D+280 where GI bleeding was undetectable since D+221. Following the TFM procedure, the beta-lactamase-positive K. pneumoniae (NDM+), was replaced by a more sensitive strain (NDM-), thus enabling ceftazidim+avibactam treatment with a positive effect. Multiple PCR of stool sample has shown an increased bacterial mass, with a maximum at D+8 to D+16 after FMT, with increase in Bacteroides fragilis, Bacteroides thetaiataomicron, Lactobacillus and Bifidobacterium microbial species. Ruxolitimib and Sirolimus were discontinued at D+284 and D+294, respectively. No signs of GVHD were revealed at control GI biopsy, and viral infections (HHV-6, CMV, EBV) were not detectable. The feeding is fully enteral now, with supplementation via gastrostoma.
Conclusion
The present case report suggests an effective curation of the patient with steroid-resistant GVHD and severe infectious complications observed under combined treatment with JAK2 inhibitor and TFM.
Keywords
Hematopoietic stem cell transplantation, steroid-resistant graft-versus-host disease, fecal microbiota transplantation, microbiota.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20337" ["VALUE"]=> string(113) "Case report of effective fecal microbiota transplantation to alleviate acute intestinal graft-versus-host disease" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(113) "Case report of effective fecal microbiota transplantation to alleviate acute intestinal graft-versus-host disease" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20747" ["VALUE"]=> string(4) "1383" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1383" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20748" ["VALUE"]=> string(4) "1384" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1384" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20335" ["VALUE"]=> array(2) { ["TEXT"]=> string(503) "Darya V. Churakina <sup>1</sup>, Oleg V. Goloshchapov <sup>1</sup>, Olga V. Pirogova <sup>1</sup>, Aleksander N. Shvetsov <sup>1</sup>, Ruslana V. Klementeva <sup>1</sup>, Aleksandr A. Shcherbakov <sup>1</sup>, Sergey V. Sidorenko <sup>2</sup>, Vladimir A. Gostev <sup>2</sup>, Maria A. Suvorova <sup>3</sup>, Yuri V. Lobzin <sup>2</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(371) "Darya V. Churakina 1, Oleg V. Goloshchapov 1, Olga V. Pirogova 1, Aleksander N. Shvetsov 1, Ruslana V. Klementeva 1, Aleksandr A. Shcherbakov 1, Sergey V. Sidorenko 2, Vladimir A. Gostev 2, Maria A. Suvorova 3, Yuri V. Lobzin 2, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(371) "Darya V. Churakina 1, Oleg V. Goloshchapov 1, Olga V. Pirogova 1, Aleksander N. Shvetsov 1, Ruslana V. Klementeva 1, Aleksandr A. Shcherbakov 1, Sergey V. Sidorenko 2, Vladimir A. Gostev 2, Maria A. Suvorova 3, Yuri V. Lobzin 2, Boris V. Afanasyev 1" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20341" ["VALUE"]=> array(2) { ["TEXT"]=> string(4846) "<p style="text-align: justify;"> In allogeneic hematopoietic stem cell transplantation (HSCT), the recipients have altered composition of gastrointestinal (GI) microbiota, due to the use of cytostatic and antibacterial drugs, changes in diet. There is a growing evidence that microbiota influences the immune system, suppresses pathogenic bacteria, promotes regeneration of the GI mucosa. It may prevent immune and infectious complications after HSCT. Transplantation of fecal microbiota (FMT) is directed to recovery of recipient microflora. Our aim was to present a clinical case of a patient with steroid-resistant intestinal graft-versus-host disease (GVHD), stage 4, grade 3, therefore treated by FMT. </p> <h2 style="text-align: justify;">Case description</h2> <p style="text-align: justify;"> A forty-five year old patient underwent HSCT in Sep 2017, for secondary acute myeloid leukemia (AML) evolving from myelodysplastic syndrome. Hematopoietic graft was from unrelated donor, conditioning regimen included fludarabin+ busulphan (12 mg/kg). Prevention of GVHD was performed with thymoglobulin, tacrolimus, MMF. Since D+67, tacrolimus was tapered and stopped at D+82 due to high relapse risk. From D+102, persistent diarrhea syndrome developed, with up to 3 L/d. The patient was admitted to the R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation. The diarrhea volume reached 5 L/d, and the patient has became septic (fever of 38oC, serum CRP, 331mg/L). Empirical antibiotic therapy consisted of doripenem, vancomycin. Colon biopsy (D+114) identified histological grade 2 of GVHD and multiple viral infection (PCR-positive for HHV-6, CMV, EBV). Tacrolimus was restarted, methylprednisolone at 2 mg/kg, and ganciclovir 10 mg/kg were administered. After 7 days of therapy, the diarrhea volume was 13 L/d. After failure of the first-line treatment, ruxolitimib (20 mg/d) was administered. Due to acute kidney injury, tacrolimus was replaced by sirolimus. At D+133, the diarrhea decreased to 3 L/d. Meanwhile, the stool samples became positive for antibiotic-resistant K. Pneumonia (D+138). The 16S rRNA gene sequencing showed the Staphylococcaceae family to represent 99% of intestinal microbiota. Despite reduced stool volume, no clinical response was achieved. GI bleeding continued from D+139 to D+221 followed by hemorrhagic shock observed at D+144, with blood hemoglobin levels of 39 g/L. In total, the patient was transfused with 29.8 L of RBCs, 5.5 L of platelet concentrate, and 5.9 L of fresh-frozen plasma.<br> The patient was treated at the ICU from D+118 to D+284 posttransplant. Over this time period, the patient suffered with severe polyresistant K. pneumoniae sepsis (D+149), Acinetobacter spp. infection (D+159 to D+198). СRP levels reached 449 mg/L, presepsin was increased to 12839 pg/ml, along with features of multiple organ failure (cardiovascular, hepatic, respiratory, cerebral affection), bilateral pneumonia (K. Pneumonia, Pseudomonas spp.). Artificial lung ventilation was performed for 83 days.<br> Considering persistent GI bleeding and multiple antibiotic- resistant bacterial complications the patient received TFM via naso-intestinal tube installed under endoscopical control, at the doses of, 80 and 300 mL on D+192 and D+194, respectively. Fourteen days later (D+208), the diarrhea decreased to 1 L/d, and to <500 mL/d by D+280 where GI bleeding was undetectable since D+221. Following the TFM procedure, the beta-lactamase-positive K. pneumoniae (NDM+), was replaced by a more sensitive strain (NDM-), thus enabling ceftazidim+avibactam treatment with a positive effect. Multiple PCR of stool sample has shown an increased bacterial mass, with a maximum at D+8 to D+16 after FMT, with increase in Bacteroides fragilis, Bacteroides thetaiataomicron, Lactobacillus and Bifidobacterium microbial species. Ruxolitimib and Sirolimus were discontinued at D+284 and D+294, respectively. No signs of GVHD were revealed at control GI biopsy, and viral infections (HHV-6, CMV, EBV) were not detectable. The feeding is fully enteral now, with supplementation via gastrostoma. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The present case report suggests an effective curation of the patient with steroid-resistant GVHD and severe infectious complications observed under combined treatment with JAK2 inhibitor and TFM. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cell transplantation, steroid-resistant graft-versus-host disease, fecal microbiota transplantation, microbiota. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4676) "In allogeneic hematopoietic stem cell transplantation (HSCT), the recipients have altered composition of gastrointestinal (GI) microbiota, due to the use of cytostatic and antibacterial drugs, changes in diet. There is a growing evidence that microbiota influences the immune system, suppresses pathogenic bacteria, promotes regeneration of the GI mucosa. It may prevent immune and infectious complications after HSCT. Transplantation of fecal microbiota (FMT) is directed to recovery of recipient microflora. Our aim was to present a clinical case of a patient with steroid-resistant intestinal graft-versus-host disease (GVHD), stage 4, grade 3, therefore treated by FMT.
Case description
A forty-five year old patient underwent HSCT in Sep 2017, for secondary acute myeloid leukemia (AML) evolving from myelodysplastic syndrome. Hematopoietic graft was from unrelated donor, conditioning regimen included fludarabin+ busulphan (12 mg/kg). Prevention of GVHD was performed with thymoglobulin, tacrolimus, MMF. Since D+67, tacrolimus was tapered and stopped at D+82 due to high relapse risk. From D+102, persistent diarrhea syndrome developed, with up to 3 L/d. The patient was admitted to the R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation. The diarrhea volume reached 5 L/d, and the patient has became septic (fever of 38oC, serum CRP, 331mg/L). Empirical antibiotic therapy consisted of doripenem, vancomycin. Colon biopsy (D+114) identified histological grade 2 of GVHD and multiple viral infection (PCR-positive for HHV-6, CMV, EBV). Tacrolimus was restarted, methylprednisolone at 2 mg/kg, and ganciclovir 10 mg/kg were administered. After 7 days of therapy, the diarrhea volume was 13 L/d. After failure of the first-line treatment, ruxolitimib (20 mg/d) was administered. Due to acute kidney injury, tacrolimus was replaced by sirolimus. At D+133, the diarrhea decreased to 3 L/d. Meanwhile, the stool samples became positive for antibiotic-resistant K. Pneumonia (D+138). The 16S rRNA gene sequencing showed the Staphylococcaceae family to represent 99% of intestinal microbiota. Despite reduced stool volume, no clinical response was achieved. GI bleeding continued from D+139 to D+221 followed by hemorrhagic shock observed at D+144, with blood hemoglobin levels of 39 g/L. In total, the patient was transfused with 29.8 L of RBCs, 5.5 L of platelet concentrate, and 5.9 L of fresh-frozen plasma.
The patient was treated at the ICU from D+118 to D+284 posttransplant. Over this time period, the patient suffered with severe polyresistant K. pneumoniae sepsis (D+149), Acinetobacter spp. infection (D+159 to D+198). СRP levels reached 449 mg/L, presepsin was increased to 12839 pg/ml, along with features of multiple organ failure (cardiovascular, hepatic, respiratory, cerebral affection), bilateral pneumonia (K. Pneumonia, Pseudomonas spp.). Artificial lung ventilation was performed for 83 days.
Considering persistent GI bleeding and multiple antibiotic- resistant bacterial complications the patient received TFM via naso-intestinal tube installed under endoscopical control, at the doses of, 80 and 300 mL on D+192 and D+194, respectively. Fourteen days later (D+208), the diarrhea decreased to 1 L/d, and to <500 mL/d by D+280 where GI bleeding was undetectable since D+221. Following the TFM procedure, the beta-lactamase-positive K. pneumoniae (NDM+), was replaced by a more sensitive strain (NDM-), thus enabling ceftazidim+avibactam treatment with a positive effect. Multiple PCR of stool sample has shown an increased bacterial mass, with a maximum at D+8 to D+16 after FMT, with increase in Bacteroides fragilis, Bacteroides thetaiataomicron, Lactobacillus and Bifidobacterium microbial species. Ruxolitimib and Sirolimus were discontinued at D+284 and D+294, respectively. No signs of GVHD were revealed at control GI biopsy, and viral infections (HHV-6, CMV, EBV) were not detectable. The feeding is fully enteral now, with supplementation via gastrostoma.
Conclusion
The present case report suggests an effective curation of the patient with steroid-resistant GVHD and severe infectious complications observed under combined treatment with JAK2 inhibitor and TFM.
Keywords
Hematopoietic stem cell transplantation, steroid-resistant graft-versus-host disease, fecal microbiota transplantation, microbiota.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4676) "In allogeneic hematopoietic stem cell transplantation (HSCT), the recipients have altered composition of gastrointestinal (GI) microbiota, due to the use of cytostatic and antibacterial drugs, changes in diet. There is a growing evidence that microbiota influences the immune system, suppresses pathogenic bacteria, promotes regeneration of the GI mucosa. It may prevent immune and infectious complications after HSCT. Transplantation of fecal microbiota (FMT) is directed to recovery of recipient microflora. Our aim was to present a clinical case of a patient with steroid-resistant intestinal graft-versus-host disease (GVHD), stage 4, grade 3, therefore treated by FMT.
Case description
A forty-five year old patient underwent HSCT in Sep 2017, for secondary acute myeloid leukemia (AML) evolving from myelodysplastic syndrome. Hematopoietic graft was from unrelated donor, conditioning regimen included fludarabin+ busulphan (12 mg/kg). Prevention of GVHD was performed with thymoglobulin, tacrolimus, MMF. Since D+67, tacrolimus was tapered and stopped at D+82 due to high relapse risk. From D+102, persistent diarrhea syndrome developed, with up to 3 L/d. The patient was admitted to the R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation. The diarrhea volume reached 5 L/d, and the patient has became septic (fever of 38oC, serum CRP, 331mg/L). Empirical antibiotic therapy consisted of doripenem, vancomycin. Colon biopsy (D+114) identified histological grade 2 of GVHD and multiple viral infection (PCR-positive for HHV-6, CMV, EBV). Tacrolimus was restarted, methylprednisolone at 2 mg/kg, and ganciclovir 10 mg/kg were administered. After 7 days of therapy, the diarrhea volume was 13 L/d. After failure of the first-line treatment, ruxolitimib (20 mg/d) was administered. Due to acute kidney injury, tacrolimus was replaced by sirolimus. At D+133, the diarrhea decreased to 3 L/d. Meanwhile, the stool samples became positive for antibiotic-resistant K. Pneumonia (D+138). The 16S rRNA gene sequencing showed the Staphylococcaceae family to represent 99% of intestinal microbiota. Despite reduced stool volume, no clinical response was achieved. GI bleeding continued from D+139 to D+221 followed by hemorrhagic shock observed at D+144, with blood hemoglobin levels of 39 g/L. In total, the patient was transfused with 29.8 L of RBCs, 5.5 L of platelet concentrate, and 5.9 L of fresh-frozen plasma.
The patient was treated at the ICU from D+118 to D+284 posttransplant. Over this time period, the patient suffered with severe polyresistant K. pneumoniae sepsis (D+149), Acinetobacter spp. infection (D+159 to D+198). СRP levels reached 449 mg/L, presepsin was increased to 12839 pg/ml, along with features of multiple organ failure (cardiovascular, hepatic, respiratory, cerebral affection), bilateral pneumonia (K. Pneumonia, Pseudomonas spp.). Artificial lung ventilation was performed for 83 days.
Considering persistent GI bleeding and multiple antibiotic- resistant bacterial complications the patient received TFM via naso-intestinal tube installed under endoscopical control, at the doses of, 80 and 300 mL on D+192 and D+194, respectively. Fourteen days later (D+208), the diarrhea decreased to 1 L/d, and to <500 mL/d by D+280 where GI bleeding was undetectable since D+221. Following the TFM procedure, the beta-lactamase-positive K. pneumoniae (NDM+), was replaced by a more sensitive strain (NDM-), thus enabling ceftazidim+avibactam treatment with a positive effect. Multiple PCR of stool sample has shown an increased bacterial mass, with a maximum at D+8 to D+16 after FMT, with increase in Bacteroides fragilis, Bacteroides thetaiataomicron, Lactobacillus and Bifidobacterium microbial species. Ruxolitimib and Sirolimus were discontinued at D+284 and D+294, respectively. No signs of GVHD were revealed at control GI biopsy, and viral infections (HHV-6, CMV, EBV) were not detectable. The feeding is fully enteral now, with supplementation via gastrostoma.
Conclusion
The present case report suggests an effective curation of the patient with steroid-resistant GVHD and severe infectious complications observed under combined treatment with JAK2 inhibitor and TFM.
Keywords
Hematopoietic stem cell transplantation, steroid-resistant graft-versus-host disease, fecal microbiota transplantation, microbiota.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20337" ["VALUE"]=> string(113) "Case report of effective fecal microbiota transplantation to alleviate acute intestinal graft-versus-host disease" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(113) "Case report of effective fecal microbiota transplantation to alleviate acute intestinal graft-versus-host disease" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(113) "Case report of effective fecal microbiota transplantation to alleviate acute intestinal graft-versus-host disease" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20336" ["VALUE"]=> array(2) { ["TEXT"]=> string(429) "<sup>1</sup> R. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation<br> <sup>2</sup> Research Scientific Institute of Children’s Infections, St. Petersburg, Russian Federation<br> <sup>3</sup> The Explana Research Laboratory, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(381) "1 R. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation2 Research Scientific Institute of Children’s Infections, St. Petersburg, Russian Federation
3 The Explana Research Laboratory, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(381) "1 R. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
2 Research Scientific Institute of Children’s Infections, St. Petersburg, Russian Federation
3 The Explana Research Laboratory, St. Petersburg, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20333" ["VALUE"]=> array(2) { ["TEXT"]=> string(660) "Дарья В. Чуракина <sup>1</sup>, Олег В. Голощапов <sup>1</sup>, Ольга В. Пирогова <sup>1</sup>, Александр Н. Швецов <sup>1</sup>, Руслана В. Клементьева <sup>1</sup>, Александр А. Щербаков <sup>1</sup>, Сергей В. Сидоренко <sup>2</sup>, Владимир А. Гостев <sup>2</sup>, Мария А. Суворова <sup>3</sup>, Юрий В. Лобзин <sup>2</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "TEXT" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(528) "Дарья В. Чуракина 1, Олег В. Голощапов 1, Ольга В. Пирогова 1, Александр Н. Швецов 1, Руслана В. Клементьева 1, Александр А. Щербаков 1, Сергей В. Сидоренко 2, Владимир А. Гостев 2, Мария А. Суворова 3, Юрий В. Лобзин 2, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "TEXT" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(660) "Дарья В. Чуракина <sup>1</sup>, Олег В. Голощапов <sup>1</sup>, Ольга В. Пирогова <sup>1</sup>, Александр Н. Швецов <sup>1</sup>, Руслана В. Клементьева <sup>1</sup>, Александр А. Щербаков <sup>1</sup>, Сергей В. Сидоренко <sup>2</sup>, Владимир А. Гостев <sup>2</sup>, Мария А. Суворова <sup>3</sup>, Юрий В. Лобзин <sup>2</sup>, Борис В. Афанасьев <sup>1</sup>" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20732" ["VALUE"]=> array(2) { ["TEXT"]=> string(8916) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> При проведении аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), вследствие применения цитостатических и антибактериальных препаратов, изменений в диете нарушается состав микробиоты желудочно-кишечного тракта (ЖКТ). Накапливаются данные о том, что микробиота влияет на работу иммунной системы человека, подавляет развитие патогенных микроорганизмов, способствует регенерации эпителия, что препятствует появлению иммунных и инфекционных осложнений после алло-ТГСК. Трансплантация фекальной микробиоты (ТФМ) направлена на восстановление микрофлоры ЖКТ реципиента. </p> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Цель работы состояла в демонстрации клинического случая стероид-резистентного течения острой реакции «трансплантат против хозяина» (оРТПХ) 3 степени тяжести, 4 стадия кишечных проявлений, в котором ТФМ в сочетании с иммуносупрессиной терапии, привела к разрешению оРТПХ кишечника. </p> <h2 style="text-align: justify;">Описание случая</h2> <p style="text-align: justify;"> Пациент, мужчина, 45 лет. Диагноз: острый миелобластный лейкоз с изменениями, связанными с миелодисплазией. Первые симптомы миелодиспластического синдрома с избытком бластов в марте 2016 года. Проведено 6 курсов 5-азацитидина. 20.02.17 – трансформация в ОМЛ. Терапия малыми дозами цитозара. 23.09.17 алло-ТГСК от неродственного донора с режимом кондиционирования флюдарабин + бусульфан (12 мг/кг). Профилактика РТПХ: тимоглобулин, такролимус, MMF. В связи с высоким риском развития рецидива, на Д+67 снижение дозы такролимуса, с полной отменой на Д+82. С Д+102 диарея до 3 л/сутки. Д+110 – госпитализация в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой. Cтул в объеме 5 л/сутки, сепсис (лихорадка 38°C, СРБ – 331 мг/л), начата эмпирическая антибактериальная терапия (дорипенем, ванкомицин). Биопсия слизистой толстой кишки (Д+114) – признаки умеренно выраженной РТПХ, вирусного поражения кишечника (ПЦР – HHV-6+, CMV+, EBV+). На Д+114 возобновлен такролимус, начат метилпреднизолон 2 мг/кг, ганцикловир 10 мг/кг. Д+118 – объем стула 13 л/сутки. С Д+117 из-за неэффективности терапии 1 линии начата терапия 2 линии – руксолитиниб 20 мг/сутки. Такролимус, в связи с развитием острого повреждения почек, заменен на сиролимус (Д+121). Д+133 – снижение объема стула до 3 л/сутки. При бактериологическом исследовании стула (Д+138) – обильный рост полирезистентной<i> K. Pneumoniae</i>. При 16S-секвенировании, 99% микробиоты ЖКТ составляло семейство <i>Staphylococcaceae</i>. Ответ по РТПХ кишки не достигнут, с Д +139 до Д+221 – продолжающееся кишечное кровотечение, геморрагический шок от Д+144 (Hb=39 г/л). Суммарно за весь период введено: эритроцитарная масса 29,8 л, тромбоцитарная масса 5,52 л, свежезамороженная плазма – 5,92 л. Получал терапию в отделении реанимации с Д+118 по Д+284. В этот период развились следующие осложнения: тяжелый сепсис, вызванный полирезистентными штаммами K. <i>pneumoniae </i>(Д+149) и <i>Acinetobacter spp</i>. (с Д+159 по Д+198) (уровень СРБ до 449 мг/л, пресепсина до 12839 пг/мл), двухсторонняя пневмония (<i>K. Pneumonia, Pseudomonas spp.</i>), полиорганная недостаточность (сердечно-сосудистая, печеночная, дыхательная, церебральная). Искусственная вентиляция легких в течение 83 дней. На Д+192 и +194 в связи с недостаточным эффектом от иммуносупрессивной терапии проведена ТФМ объемом 80 и 300 мл, через назоинтестинальный зонд, установленный под контролем эндоскопа. За 14 дней объем стула снизился до 1 л/сутки (Д+208), а на Д+280 до 500 мл/сутки, с Д+221 впервые отсутствие крови в стуле. В результате ТФМ, <i>K. pneumoniae</i>, ранее продуцирующая фермент металло-бета-лактамазу (NDM+), сменилась штаммом чувствительным к антибиотикам (NDM-). Это позволило назначить цефтазидим+авибактам с положительным эффектом (снижение прокальцитонина с 26,8 до 0,8 нг/мл). По данным ПЦР образцов стула после ТФМ значительно повысилась общая бактериальная масса (с пиком на Д+8 – Д+16 после ТФМ), за счет увеличения <i>Bacteroides fragilis, Bacteroides </i><i>thetaiataomicron, Lactobacillus spp., Bifidobacterium spp. </i>Полная отмена руксолитиниба на Д+284 и сиролимуса на Д+294. По результатам контрольной биопсии (Д+337) убедительных признаков РТПХ и вирусного поражения кишечника не выявлено (ПЦР – HHV-6 -, CMV -, EBV -). В настоящее время – стул с тенденцией к оформлению (около 300 г/сутки). Питание самостоятельное и дополнительное через гастростому. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> В представленном случае продемонстрировано эффективное применение ТФМ в сочетании с JAK2 ингибитором у пациента со стероид-резистентным течением оРТПХ и тяжелыми инфекционными осложнениями. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, стероид-резистентная реакция трансплантат против хозяина, трансплантация фекальной микробиоты, микробиота кишечника. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(8588) "
Введение
При проведении аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), вследствие применения цитостатических и антибактериальных препаратов, изменений в диете нарушается состав микробиоты желудочно-кишечного тракта (ЖКТ). Накапливаются данные о том, что микробиота влияет на работу иммунной системы человека, подавляет развитие патогенных микроорганизмов, способствует регенерации эпителия, что препятствует появлению иммунных и инфекционных осложнений после алло-ТГСК. Трансплантация фекальной микробиоты (ТФМ) направлена на восстановление микрофлоры ЖКТ реципиента.
Цель работы
Цель работы состояла в демонстрации клинического случая стероид-резистентного течения острой реакции «трансплантат против хозяина» (оРТПХ) 3 степени тяжести, 4 стадия кишечных проявлений, в котором ТФМ в сочетании с иммуносупрессиной терапии, привела к разрешению оРТПХ кишечника.
Описание случая
Пациент, мужчина, 45 лет. Диагноз: острый миелобластный лейкоз с изменениями, связанными с миелодисплазией. Первые симптомы миелодиспластического синдрома с избытком бластов в марте 2016 года. Проведено 6 курсов 5-азацитидина. 20.02.17 – трансформация в ОМЛ. Терапия малыми дозами цитозара. 23.09.17 алло-ТГСК от неродственного донора с режимом кондиционирования флюдарабин + бусульфан (12 мг/кг). Профилактика РТПХ: тимоглобулин, такролимус, MMF. В связи с высоким риском развития рецидива, на Д+67 снижение дозы такролимуса, с полной отменой на Д+82. С Д+102 диарея до 3 л/сутки. Д+110 – госпитализация в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой. Cтул в объеме 5 л/сутки, сепсис (лихорадка 38°C, СРБ – 331 мг/л), начата эмпирическая антибактериальная терапия (дорипенем, ванкомицин). Биопсия слизистой толстой кишки (Д+114) – признаки умеренно выраженной РТПХ, вирусного поражения кишечника (ПЦР – HHV-6+, CMV+, EBV+). На Д+114 возобновлен такролимус, начат метилпреднизолон 2 мг/кг, ганцикловир 10 мг/кг. Д+118 – объем стула 13 л/сутки. С Д+117 из-за неэффективности терапии 1 линии начата терапия 2 линии – руксолитиниб 20 мг/сутки. Такролимус, в связи с развитием острого повреждения почек, заменен на сиролимус (Д+121). Д+133 – снижение объема стула до 3 л/сутки. При бактериологическом исследовании стула (Д+138) – обильный рост полирезистентной K. Pneumoniae. При 16S-секвенировании, 99% микробиоты ЖКТ составляло семейство Staphylococcaceae. Ответ по РТПХ кишки не достигнут, с Д +139 до Д+221 – продолжающееся кишечное кровотечение, геморрагический шок от Д+144 (Hb=39 г/л). Суммарно за весь период введено: эритроцитарная масса 29,8 л, тромбоцитарная масса 5,52 л, свежезамороженная плазма – 5,92 л. Получал терапию в отделении реанимации с Д+118 по Д+284. В этот период развились следующие осложнения: тяжелый сепсис, вызванный полирезистентными штаммами K. pneumoniae (Д+149) и Acinetobacter spp. (с Д+159 по Д+198) (уровень СРБ до 449 мг/л, пресепсина до 12839 пг/мл), двухсторонняя пневмония (K. Pneumonia, Pseudomonas spp.), полиорганная недостаточность (сердечно-сосудистая, печеночная, дыхательная, церебральная). Искусственная вентиляция легких в течение 83 дней. На Д+192 и +194 в связи с недостаточным эффектом от иммуносупрессивной терапии проведена ТФМ объемом 80 и 300 мл, через назоинтестинальный зонд, установленный под контролем эндоскопа. За 14 дней объем стула снизился до 1 л/сутки (Д+208), а на Д+280 до 500 мл/сутки, с Д+221 впервые отсутствие крови в стуле. В результате ТФМ, K. pneumoniae, ранее продуцирующая фермент металло-бета-лактамазу (NDM+), сменилась штаммом чувствительным к антибиотикам (NDM-). Это позволило назначить цефтазидим+авибактам с положительным эффектом (снижение прокальцитонина с 26,8 до 0,8 нг/мл). По данным ПЦР образцов стула после ТФМ значительно повысилась общая бактериальная масса (с пиком на Д+8 – Д+16 после ТФМ), за счет увеличения Bacteroides fragilis, Bacteroides thetaiataomicron, Lactobacillus spp., Bifidobacterium spp. Полная отмена руксолитиниба на Д+284 и сиролимуса на Д+294. По результатам контрольной биопсии (Д+337) убедительных признаков РТПХ и вирусного поражения кишечника не выявлено (ПЦР – HHV-6 -, CMV -, EBV -). В настоящее время – стул с тенденцией к оформлению (около 300 г/сутки). Питание самостоятельное и дополнительное через гастростому.
Заключение
В представленном случае продемонстрировано эффективное применение ТФМ в сочетании с JAK2 ингибитором у пациента со стероид-резистентным течением оРТПХ и тяжелыми инфекционными осложнениями.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, стероид-резистентная реакция трансплантат против хозяина, трансплантация фекальной микробиоты, микробиота кишечника.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(8588) "Введение
При проведении аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), вследствие применения цитостатических и антибактериальных препаратов, изменений в диете нарушается состав микробиоты желудочно-кишечного тракта (ЖКТ). Накапливаются данные о том, что микробиота влияет на работу иммунной системы человека, подавляет развитие патогенных микроорганизмов, способствует регенерации эпителия, что препятствует появлению иммунных и инфекционных осложнений после алло-ТГСК. Трансплантация фекальной микробиоты (ТФМ) направлена на восстановление микрофлоры ЖКТ реципиента.
Цель работы
Цель работы состояла в демонстрации клинического случая стероид-резистентного течения острой реакции «трансплантат против хозяина» (оРТПХ) 3 степени тяжести, 4 стадия кишечных проявлений, в котором ТФМ в сочетании с иммуносупрессиной терапии, привела к разрешению оРТПХ кишечника.
Описание случая
Пациент, мужчина, 45 лет. Диагноз: острый миелобластный лейкоз с изменениями, связанными с миелодисплазией. Первые симптомы миелодиспластического синдрома с избытком бластов в марте 2016 года. Проведено 6 курсов 5-азацитидина. 20.02.17 – трансформация в ОМЛ. Терапия малыми дозами цитозара. 23.09.17 алло-ТГСК от неродственного донора с режимом кондиционирования флюдарабин + бусульфан (12 мг/кг). Профилактика РТПХ: тимоглобулин, такролимус, MMF. В связи с высоким риском развития рецидива, на Д+67 снижение дозы такролимуса, с полной отменой на Д+82. С Д+102 диарея до 3 л/сутки. Д+110 – госпитализация в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой. Cтул в объеме 5 л/сутки, сепсис (лихорадка 38°C, СРБ – 331 мг/л), начата эмпирическая антибактериальная терапия (дорипенем, ванкомицин). Биопсия слизистой толстой кишки (Д+114) – признаки умеренно выраженной РТПХ, вирусного поражения кишечника (ПЦР – HHV-6+, CMV+, EBV+). На Д+114 возобновлен такролимус, начат метилпреднизолон 2 мг/кг, ганцикловир 10 мг/кг. Д+118 – объем стула 13 л/сутки. С Д+117 из-за неэффективности терапии 1 линии начата терапия 2 линии – руксолитиниб 20 мг/сутки. Такролимус, в связи с развитием острого повреждения почек, заменен на сиролимус (Д+121). Д+133 – снижение объема стула до 3 л/сутки. При бактериологическом исследовании стула (Д+138) – обильный рост полирезистентной K. Pneumoniae. При 16S-секвенировании, 99% микробиоты ЖКТ составляло семейство Staphylococcaceae. Ответ по РТПХ кишки не достигнут, с Д +139 до Д+221 – продолжающееся кишечное кровотечение, геморрагический шок от Д+144 (Hb=39 г/л). Суммарно за весь период введено: эритроцитарная масса 29,8 л, тромбоцитарная масса 5,52 л, свежезамороженная плазма – 5,92 л. Получал терапию в отделении реанимации с Д+118 по Д+284. В этот период развились следующие осложнения: тяжелый сепсис, вызванный полирезистентными штаммами K. pneumoniae (Д+149) и Acinetobacter spp. (с Д+159 по Д+198) (уровень СРБ до 449 мг/л, пресепсина до 12839 пг/мл), двухсторонняя пневмония (K. Pneumonia, Pseudomonas spp.), полиорганная недостаточность (сердечно-сосудистая, печеночная, дыхательная, церебральная). Искусственная вентиляция легких в течение 83 дней. На Д+192 и +194 в связи с недостаточным эффектом от иммуносупрессивной терапии проведена ТФМ объемом 80 и 300 мл, через назоинтестинальный зонд, установленный под контролем эндоскопа. За 14 дней объем стула снизился до 1 л/сутки (Д+208), а на Д+280 до 500 мл/сутки, с Д+221 впервые отсутствие крови в стуле. В результате ТФМ, K. pneumoniae, ранее продуцирующая фермент металло-бета-лактамазу (NDM+), сменилась штаммом чувствительным к антибиотикам (NDM-). Это позволило назначить цефтазидим+авибактам с положительным эффектом (снижение прокальцитонина с 26,8 до 0,8 нг/мл). По данным ПЦР образцов стула после ТФМ значительно повысилась общая бактериальная масса (с пиком на Д+8 – Д+16 после ТФМ), за счет увеличения Bacteroides fragilis, Bacteroides thetaiataomicron, Lactobacillus spp., Bifidobacterium spp. Полная отмена руксолитиниба на Д+284 и сиролимуса на Д+294. По результатам контрольной биопсии (Д+337) убедительных признаков РТПХ и вирусного поражения кишечника не выявлено (ПЦР – HHV-6 -, CMV -, EBV -). В настоящее время – стул с тенденцией к оформлению (около 300 г/сутки). Питание самостоятельное и дополнительное через гастростому.
Заключение
В представленном случае продемонстрировано эффективное применение ТФМ в сочетании с JAK2 ингибитором у пациента со стероид-резистентным течением оРТПХ и тяжелыми инфекционными осложнениями.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, стероид-резистентная реакция трансплантат против хозяина, трансплантация фекальной микробиоты, микробиота кишечника.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20334" ["VALUE"]=> array(2) { ["TEXT"]=> string(679) "<sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербург, Российская Федерация, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова<br> <sup>2</sup> ФГБУ ДНКЦИБ ФМБА России<br> <sup>3</sup> Научно-исследовательская лаборатория Explana, Санкт-Петербург, Российская Федерация<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(625) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербург, Российская Федерация, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова2 ФГБУ ДНКЦИБ ФМБА России
3 Научно-исследовательская лаборатория Explana, Санкт-Петербург, Российская Федерация
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(625) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербург, Российская Федерация, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова
2 ФГБУ ДНКЦИБ ФМБА России
3 Научно-исследовательская лаборатория Explana, Санкт-Петербург, Российская Федерация
" } } } [26]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1576" ["~ID"]=> string(4) "1576" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(304) "Опыт трансплантации гемопоэтических стволовых клеток с TCRαβ+/CD19+ деплецией без посттрансплантационной профилак- тики РТПХ у пациентов с первичными иммунодефицитами" ["~NAME"]=> string(304) "Опыт трансплантации гемопоэтических стволовых клеток с TCRαβ+/CD19+ деплецией без посттрансплантационной профилак- тики РТПХ у пациентов с первичными иммунодефицитами" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:36:58" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:36:58" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/opyt-transplantatsii-gemopoeticheskikh-stvolovykh-kletok-s-tcr-cd19-depletsiey-bez-posttransplantats/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/opyt-transplantatsii-gemopoeticheskikh-stvolovykh-kletok-s-tcr-cd19-depletsiey-bez-posttransplantats/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "opyt-transplantatsii-gemopoeticheskikh-stvolovykh-kletok-s-tcr-cd19-depletsiey-bez-posttransplantats" ["~CODE"]=> string(100) "opyt-transplantatsii-gemopoeticheskikh-stvolovykh-kletok-s-tcr-cd19-depletsiey-bez-posttransplantats" ["EXTERNAL_ID"]=> string(4) "1576" ["~EXTERNAL_ID"]=> string(4) "1576" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(304) "Опыт трансплантации гемопоэтических стволовых клеток с TCRαβ+/CD19+ деплецией без посттрансплантационной профилак- тики РТПХ у пациентов с первичными иммунодефицитами" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(490) "Опыт трансплантации гемопоэтических стволовых клеток с TCRαβ+/CD19+ деплецией без посттрансплантационной профилак- тики РТПХ у пациентов с первичными иммунодефицитамиThe experience of hematopoietic stem cells transplantation with TCRαβ+/CD19+ depletion without posttransplantation prophylaxis of GVHD in patients with primary immunodeficiencies (PID)" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(4856) "<h2></h2> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Оценка выполнимости и безопасности аллогенной ТГСК с TCRαβ+/CD19+ деплецией у пациентов с первичными иммунодефицитами (ПИД) без использования посттрансплантационной иммуносупрессивной терапии. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> С октября 2017 по май 2018 проведено 10 аллогенных ТГСК от неродственного(n=8) и гаплоидентичного(n=2) доноров с TCRαβ+/CD19+ деплецией трансплантата у пациентов с ПИД (сидром Ниймеген – 1, хроническая гранулематозная болезнь – 2, гипер IgM синдром – 3, ПИД с дефицитом PI3K-дельта – 1, Х-сцепленный лимфопролиферативный синдром I типа – 1, ПИД с дефектом адгезии лейкоцитов I типа – 1, тяжелая врожденная нейтропения – 1). У 9 пациентов проведен режим кондиционирования – треосульфан 42 гр/м2, флударабин 150 мг/м2, мельфалан 140 мг/м2; одному пациенту (синдром Ниймеген) – треосульфан 30 гр/м2, флударабин 150 мг/м2, циклофосфамид 40 мг/кг. В качестве серотерапии во всех случаях использовался антитимоцитарный иммуноглобулин – Тимоглобулин® (“Genzyme Europe B.V.”, Нидерланды) в дозах 5-7,5 мг/кг. Посттрансплантационная иммуносупрессивная терапия для профилактика РТПХ не проводилась. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Приживление трансплантата было зарегистрировано у всех пациентов. Острая РТПХ верифицирована в 3 из 10 случаях, в 2 из которых РТПХ была ограничена исключительно поражением кожи 2 степени. Только у одного пациента (с синдромом Ниймеген) отмечалось развитие острой РТПХ 3 стадии с поражением печени, потребовавшей комбинированной иммуносупрессивной терапии. Все пациенты живы на сроках от 2 до 10 месяцев после ТГСК с хорошими функциональными характеристиками трансплантата. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Исключение иммуносупрессивной терапии из протокола ТГСК с TCRαβ+/CD19+ деплецией у пациентов ПИД продемонстрировало свою безопасность в отношении риска развития РТПХ. Тяжелая висцеральная форма РТПХ была зарегистрирована только у пациента с высоким риском развития данного осложнения, обусловленного особенностями основного заболевания (синдром Ниймеген). В настоящее время набор пациентов продолжается. Поэтому оценка темпов иммунореконституции, частоты реактивации вирусных инфекций и ряд других факторов будут оценены позднее. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, TCRαβ+/CD19+ деплеция, реакция трансплантат против хозяина, посттрансплантационная иммуносупрессивная терапия, первичный иммунодефицит. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(304) "Опыт трансплантации гемопоэтических стволовых клеток с TCRαβ+/CD19+ деплецией без посттрансплантационной профилак- тики РТПХ у пациентов с первичными иммунодефицитами" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(304) "Опыт трансплантации гемопоэтических стволовых клеток с TCRαβ+/CD19+ деплецией без посттрансплантационной профилак- тики РТПХ у пациентов с первичными иммунодефицитами" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(304) "Опыт трансплантации гемопоэтических стволовых клеток с TCRαβ+/CD19+ деплецией без посттрансплантационной профилак- тики РТПХ у пациентов с первичными иммунодефицитами" ["SECTION_META_TITLE"]=> string(304) "Опыт трансплантации гемопоэтических стволовых клеток с TCRαβ+/CD19+ деплецией без посттрансплантационной профилак- тики РТПХ у пациентов с первичными иммунодефицитами" ["SECTION_META_KEYWORDS"]=> string(304) "Опыт трансплантации гемопоэтических стволовых клеток с TCRαβ+/CD19+ деплецией без посттрансплантационной профилак- тики РТПХ у пациентов с первичными иммунодефицитами" ["SECTION_META_DESCRIPTION"]=> string(304) "Опыт трансплантации гемопоэтических стволовых клеток с TCRαβ+/CD19+ деплецией без посттрансплантационной профилак- тики РТПХ у пациентов с первичными иммунодефицитами" ["SECTION_PICTURE_FILE_ALT"]=> string(304) "Опыт трансплантации гемопоэтических стволовых клеток с TCRαβ+/CD19+ деплецией без посттрансплантационной профилак- тики РТПХ у пациентов с первичными иммунодефицитами" ["SECTION_PICTURE_FILE_TITLE"]=> string(304) "Опыт трансплантации гемопоэтических стволовых клеток с TCRαβ+/CD19+ деплецией без посттрансплантационной профилак- тики РТПХ у пациентов с первичными иммунодефицитами" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "opyt-transplantatsii-gemopoeticheskikh-stvolovykh-kletok-s-tcr-cd19-depletsiey-bez-posttransplantats" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(304) "Опыт трансплантации гемопоэтических стволовых клеток с TCRαβ+/CD19+ деплецией без посттрансплантационной профилак- тики РТПХ у пациентов с первичными иммунодефицитами" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(304) "Опыт трансплантации гемопоэтических стволовых клеток с TCRαβ+/CD19+ деплецией без посттрансплантационной профилак- тики РТПХ у пациентов с первичными иммунодефицитами" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "opyt-transplantatsii-gemopoeticheskikh-stvolovykh-kletok-s-tcr-cd19-depletsiey-bez-posttransplantats" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "opyt-transplantatsii-gemopoeticheskikh-stvolovykh-kletok-s-tcr-cd19-depletsiey-bez-posttransplantats" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "opyt-transplantatsii-gemopoeticheskikh-stvolovykh-kletok-s-tcr-cd19-depletsiey-bez-posttransplantats" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20520" ["VALUE"]=> array(2) { ["TEXT"]=> string(226) "Светлана Н. Козловская, Светлана А. Радыгина, Ирина П. Шипицына, Елена И. Гутовская, Константин В. Митраков, Дмитрий Н. Балашов" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(226) "Светлана Н. Козловская, Светлана А. Радыгина, Ирина П. Шипицына, Елена И. Гутовская, Константин В. Митраков, Дмитрий Н. Балашов" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20521" ["VALUE"]=> array(2) { ["TEXT"]=> string(469) "Федеральное государственное бюджетное учреждение «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Министерства здравоохранения Российской Федерации, Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(469) "Федеральное государственное бюджетное учреждение «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Министерства здравоохранения Российской Федерации, Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20522" ["VALUE"]=> array(2) { ["TEXT"]=> string(4856) "<h2></h2> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Оценка выполнимости и безопасности аллогенной ТГСК с TCRαβ+/CD19+ деплецией у пациентов с первичными иммунодефицитами (ПИД) без использования посттрансплантационной иммуносупрессивной терапии. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> С октября 2017 по май 2018 проведено 10 аллогенных ТГСК от неродственного(n=8) и гаплоидентичного(n=2) доноров с TCRαβ+/CD19+ деплецией трансплантата у пациентов с ПИД (сидром Ниймеген – 1, хроническая гранулематозная болезнь – 2, гипер IgM синдром – 3, ПИД с дефицитом PI3K-дельта – 1, Х-сцепленный лимфопролиферативный синдром I типа – 1, ПИД с дефектом адгезии лейкоцитов I типа – 1, тяжелая врожденная нейтропения – 1). У 9 пациентов проведен режим кондиционирования – треосульфан 42 гр/м2, флударабин 150 мг/м2, мельфалан 140 мг/м2; одному пациенту (синдром Ниймеген) – треосульфан 30 гр/м2, флударабин 150 мг/м2, циклофосфамид 40 мг/кг. В качестве серотерапии во всех случаях использовался антитимоцитарный иммуноглобулин – Тимоглобулин® (“Genzyme Europe B.V.”, Нидерланды) в дозах 5-7,5 мг/кг. Посттрансплантационная иммуносупрессивная терапия для профилактика РТПХ не проводилась. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Приживление трансплантата было зарегистрировано у всех пациентов. Острая РТПХ верифицирована в 3 из 10 случаях, в 2 из которых РТПХ была ограничена исключительно поражением кожи 2 степени. Только у одного пациента (с синдромом Ниймеген) отмечалось развитие острой РТПХ 3 стадии с поражением печени, потребовавшей комбинированной иммуносупрессивной терапии. Все пациенты живы на сроках от 2 до 10 месяцев после ТГСК с хорошими функциональными характеристиками трансплантата. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Исключение иммуносупрессивной терапии из протокола ТГСК с TCRαβ+/CD19+ деплецией у пациентов ПИД продемонстрировало свою безопасность в отношении риска развития РТПХ. Тяжелая висцеральная форма РТПХ была зарегистрирована только у пациента с высоким риском развития данного осложнения, обусловленного особенностями основного заболевания (синдром Ниймеген). В настоящее время набор пациентов продолжается. Поэтому оценка темпов иммунореконституции, частоты реактивации вирусных инфекций и ряд других факторов будут оценены позднее. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, TCRαβ+/CD19+ деплеция, реакция трансплантат против хозяина, посттрансплантационная иммуносупрессивная терапия, первичный иммунодефицит. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4624) "
Цель
Оценка выполнимости и безопасности аллогенной ТГСК с TCRαβ+/CD19+ деплецией у пациентов с первичными иммунодефицитами (ПИД) без использования посттрансплантационной иммуносупрессивной терапии.
Пациенты и методы
С октября 2017 по май 2018 проведено 10 аллогенных ТГСК от неродственного(n=8) и гаплоидентичного(n=2) доноров с TCRαβ+/CD19+ деплецией трансплантата у пациентов с ПИД (сидром Ниймеген – 1, хроническая гранулематозная болезнь – 2, гипер IgM синдром – 3, ПИД с дефицитом PI3K-дельта – 1, Х-сцепленный лимфопролиферативный синдром I типа – 1, ПИД с дефектом адгезии лейкоцитов I типа – 1, тяжелая врожденная нейтропения – 1). У 9 пациентов проведен режим кондиционирования – треосульфан 42 гр/м2, флударабин 150 мг/м2, мельфалан 140 мг/м2; одному пациенту (синдром Ниймеген) – треосульфан 30 гр/м2, флударабин 150 мг/м2, циклофосфамид 40 мг/кг. В качестве серотерапии во всех случаях использовался антитимоцитарный иммуноглобулин – Тимоглобулин® (“Genzyme Europe B.V.”, Нидерланды) в дозах 5-7,5 мг/кг. Посттрансплантационная иммуносупрессивная терапия для профилактика РТПХ не проводилась.
Результаты
Приживление трансплантата было зарегистрировано у всех пациентов. Острая РТПХ верифицирована в 3 из 10 случаях, в 2 из которых РТПХ была ограничена исключительно поражением кожи 2 степени. Только у одного пациента (с синдромом Ниймеген) отмечалось развитие острой РТПХ 3 стадии с поражением печени, потребовавшей комбинированной иммуносупрессивной терапии. Все пациенты живы на сроках от 2 до 10 месяцев после ТГСК с хорошими функциональными характеристиками трансплантата.
Заключение
Исключение иммуносупрессивной терапии из протокола ТГСК с TCRαβ+/CD19+ деплецией у пациентов ПИД продемонстрировало свою безопасность в отношении риска развития РТПХ. Тяжелая висцеральная форма РТПХ была зарегистрирована только у пациента с высоким риском развития данного осложнения, обусловленного особенностями основного заболевания (синдром Ниймеген). В настоящее время набор пациентов продолжается. Поэтому оценка темпов иммунореконституции, частоты реактивации вирусных инфекций и ряд других факторов будут оценены позднее.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, TCRαβ+/CD19+ деплеция, реакция трансплантат против хозяина, посттрансплантационная иммуносупрессивная терапия, первичный иммунодефицит.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20523" ["VALUE"]=> array(2) { ["TEXT"]=> string(131) "Svetlana N. Kozlovskaya, Svetlana A. Radygina, Irina P. Shypitsyna, Elena I. Gutovskaya, Konstantin V. Mitrakov, Dmitry N. Balashov" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(131) "Svetlana N. Kozlovskaya, Svetlana A. Radygina, Irina P. Shypitsyna, Elena I. Gutovskaya, Konstantin V. Mitrakov, Dmitry N. Balashov" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20524" ["VALUE"]=> array(2) { ["TEXT"]=> string(126) "Dmitriy Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(126) "Dmitriy Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20525" ["VALUE"]=> array(2) { ["TEXT"]=> string(2912) "<h2 style="text-align: justify;">Objective</h2> <p style="text-align: justify;"> Estimation of feasibility and safety of allogeneic hematopoietic stem cell transplantation (HSCT) with TCRαβ +/CD19+ cell depletion in patients with primary immunodeficiency (PID) without usage of posttransplant immunosuppressive therapy. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Ten allogeneic HSCTs were performed from October 2017 to May 2018 to the patients with PID (Nijmegen breakage syndrome, 1; Chronic granulomatous disease, 2; CID with CD40L deficiency, 3; PID with PI3K-delta deficiency, 1; X-linked lymphoproliferative syndrome type I, 1; leukocyte adhesion deficiency; 1; severe congenital neutropenia, 1). We carried out trans plants from unrelated (n=8) or haploidentical donors (n=2) using TCRαβ+/CD19 + depletion. Nine patients were conditioned for HSCT with treosulfan 42 g/m2, fludarabine 150 mg/m2, melphalan 140 mg/m2; one patient (Nijmegen’s syndrome) – treosulfan 30 g/m2, fludarabine 150 mg/m2, cyclophosphamide 40 mg/kg. Antithymocyte immunoglobulin – Thymoglobulin® (“Genzyme Europe B.V.”, The Netherlands) was used as a serotherapy at the doses of 5 to 7.5 mg/kg in all cases. Posttransplant GVHD prophylaxis was not performed. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Transplant engraftment was recorded in all the patients. Acute GVHD was verified in 3 out of 10 cases, in 2 of which GVHD of 2nd degree was limited to skin. Only one patient (with Nijmegen syndrome) had acute liver GVHD stage 3 and combined immunosuppressive therapy was required. All the patients are alive at 2 to 10 months after HSCT, with good functional characteristics of the transplants. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Exclusion of posttransplant immunosuppressive therapy after HSCT with TCRαβ+/CD19+ depletion in patients with PID has demonstrated safety in relation to the risk of GVHD development. Severe visceral form of GVHD was recorded only in a patient being at high risk of developing this complication, due to characteristics of the disease (Nijmegen syndrome). Currently, the recruitment of patients is underway, and estimation of immune reconstitution rates reactivation of viral infections, and other factors should be evaluated later. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cell transplantation, TCRαβ+/CD19+ depletion, graft-versus-host disease, posttransplant immunosuppressive therapy, primary immunodeficiency. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2692) "Objective
Estimation of feasibility and safety of allogeneic hematopoietic stem cell transplantation (HSCT) with TCRαβ +/CD19+ cell depletion in patients with primary immunodeficiency (PID) without usage of posttransplant immunosuppressive therapy.
Patients and methods
Ten allogeneic HSCTs were performed from October 2017 to May 2018 to the patients with PID (Nijmegen breakage syndrome, 1; Chronic granulomatous disease, 2; CID with CD40L deficiency, 3; PID with PI3K-delta deficiency, 1; X-linked lymphoproliferative syndrome type I, 1; leukocyte adhesion deficiency; 1; severe congenital neutropenia, 1). We carried out trans plants from unrelated (n=8) or haploidentical donors (n=2) using TCRαβ+/CD19 + depletion. Nine patients were conditioned for HSCT with treosulfan 42 g/m2, fludarabine 150 mg/m2, melphalan 140 mg/m2; one patient (Nijmegen’s syndrome) – treosulfan 30 g/m2, fludarabine 150 mg/m2, cyclophosphamide 40 mg/kg. Antithymocyte immunoglobulin – Thymoglobulin® (“Genzyme Europe B.V.”, The Netherlands) was used as a serotherapy at the doses of 5 to 7.5 mg/kg in all cases. Posttransplant GVHD prophylaxis was not performed.
Results
Transplant engraftment was recorded in all the patients. Acute GVHD was verified in 3 out of 10 cases, in 2 of which GVHD of 2nd degree was limited to skin. Only one patient (with Nijmegen syndrome) had acute liver GVHD stage 3 and combined immunosuppressive therapy was required. All the patients are alive at 2 to 10 months after HSCT, with good functional characteristics of the transplants.
Conclusion
Exclusion of posttransplant immunosuppressive therapy after HSCT with TCRαβ+/CD19+ depletion in patients with PID has demonstrated safety in relation to the risk of GVHD development. Severe visceral form of GVHD was recorded only in a patient being at high risk of developing this complication, due to characteristics of the disease (Nijmegen syndrome). Currently, the recruitment of patients is underway, and estimation of immune reconstitution rates reactivation of viral infections, and other factors should be evaluated later.
Keywords
Hematopoietic stem cell transplantation, TCRαβ+/CD19+ depletion, graft-versus-host disease, posttransplant immunosuppressive therapy, primary immunodeficiency.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20526" ["VALUE"]=> string(186) "The experience of hematopoietic stem cells transplantation with TCRαβ+/CD19+ depletion without posttransplantation prophylaxis of GVHD in patients with primary immunodeficiencies (PID)" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(186) "The experience of hematopoietic stem cells transplantation with TCRαβ+/CD19+ depletion without posttransplantation prophylaxis of GVHD in patients with primary immunodeficiencies (PID)" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20783" ["VALUE"]=> string(4) "1421" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1421" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20784" ["VALUE"]=> string(4) "1422" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1422" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20523" ["VALUE"]=> array(2) { ["TEXT"]=> string(131) "Svetlana N. Kozlovskaya, Svetlana A. Radygina, Irina P. Shypitsyna, Elena I. Gutovskaya, Konstantin V. Mitrakov, Dmitry N. Balashov" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(131) "Svetlana N. Kozlovskaya, Svetlana A. Radygina, Irina P. Shypitsyna, Elena I. Gutovskaya, Konstantin V. Mitrakov, Dmitry N. Balashov" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(131) "Svetlana N. Kozlovskaya, Svetlana A. Radygina, Irina P. Shypitsyna, Elena I. Gutovskaya, Konstantin V. Mitrakov, Dmitry N. Balashov" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20525" ["VALUE"]=> array(2) { ["TEXT"]=> string(2912) "<h2 style="text-align: justify;">Objective</h2> <p style="text-align: justify;"> Estimation of feasibility and safety of allogeneic hematopoietic stem cell transplantation (HSCT) with TCRαβ +/CD19+ cell depletion in patients with primary immunodeficiency (PID) without usage of posttransplant immunosuppressive therapy. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Ten allogeneic HSCTs were performed from October 2017 to May 2018 to the patients with PID (Nijmegen breakage syndrome, 1; Chronic granulomatous disease, 2; CID with CD40L deficiency, 3; PID with PI3K-delta deficiency, 1; X-linked lymphoproliferative syndrome type I, 1; leukocyte adhesion deficiency; 1; severe congenital neutropenia, 1). We carried out trans plants from unrelated (n=8) or haploidentical donors (n=2) using TCRαβ+/CD19 + depletion. Nine patients were conditioned for HSCT with treosulfan 42 g/m2, fludarabine 150 mg/m2, melphalan 140 mg/m2; one patient (Nijmegen’s syndrome) – treosulfan 30 g/m2, fludarabine 150 mg/m2, cyclophosphamide 40 mg/kg. Antithymocyte immunoglobulin – Thymoglobulin® (“Genzyme Europe B.V.”, The Netherlands) was used as a serotherapy at the doses of 5 to 7.5 mg/kg in all cases. Posttransplant GVHD prophylaxis was not performed. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Transplant engraftment was recorded in all the patients. Acute GVHD was verified in 3 out of 10 cases, in 2 of which GVHD of 2nd degree was limited to skin. Only one patient (with Nijmegen syndrome) had acute liver GVHD stage 3 and combined immunosuppressive therapy was required. All the patients are alive at 2 to 10 months after HSCT, with good functional characteristics of the transplants. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Exclusion of posttransplant immunosuppressive therapy after HSCT with TCRαβ+/CD19+ depletion in patients with PID has demonstrated safety in relation to the risk of GVHD development. Severe visceral form of GVHD was recorded only in a patient being at high risk of developing this complication, due to characteristics of the disease (Nijmegen syndrome). Currently, the recruitment of patients is underway, and estimation of immune reconstitution rates reactivation of viral infections, and other factors should be evaluated later. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cell transplantation, TCRαβ+/CD19+ depletion, graft-versus-host disease, posttransplant immunosuppressive therapy, primary immunodeficiency. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2692) "Objective
Estimation of feasibility and safety of allogeneic hematopoietic stem cell transplantation (HSCT) with TCRαβ +/CD19+ cell depletion in patients with primary immunodeficiency (PID) without usage of posttransplant immunosuppressive therapy.
Patients and methods
Ten allogeneic HSCTs were performed from October 2017 to May 2018 to the patients with PID (Nijmegen breakage syndrome, 1; Chronic granulomatous disease, 2; CID with CD40L deficiency, 3; PID with PI3K-delta deficiency, 1; X-linked lymphoproliferative syndrome type I, 1; leukocyte adhesion deficiency; 1; severe congenital neutropenia, 1). We carried out trans plants from unrelated (n=8) or haploidentical donors (n=2) using TCRαβ+/CD19 + depletion. Nine patients were conditioned for HSCT with treosulfan 42 g/m2, fludarabine 150 mg/m2, melphalan 140 mg/m2; one patient (Nijmegen’s syndrome) – treosulfan 30 g/m2, fludarabine 150 mg/m2, cyclophosphamide 40 mg/kg. Antithymocyte immunoglobulin – Thymoglobulin® (“Genzyme Europe B.V.”, The Netherlands) was used as a serotherapy at the doses of 5 to 7.5 mg/kg in all cases. Posttransplant GVHD prophylaxis was not performed.
Results
Transplant engraftment was recorded in all the patients. Acute GVHD was verified in 3 out of 10 cases, in 2 of which GVHD of 2nd degree was limited to skin. Only one patient (with Nijmegen syndrome) had acute liver GVHD stage 3 and combined immunosuppressive therapy was required. All the patients are alive at 2 to 10 months after HSCT, with good functional characteristics of the transplants.
Conclusion
Exclusion of posttransplant immunosuppressive therapy after HSCT with TCRαβ+/CD19+ depletion in patients with PID has demonstrated safety in relation to the risk of GVHD development. Severe visceral form of GVHD was recorded only in a patient being at high risk of developing this complication, due to characteristics of the disease (Nijmegen syndrome). Currently, the recruitment of patients is underway, and estimation of immune reconstitution rates reactivation of viral infections, and other factors should be evaluated later.
Keywords
Hematopoietic stem cell transplantation, TCRαβ+/CD19+ depletion, graft-versus-host disease, posttransplant immunosuppressive therapy, primary immunodeficiency.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2692) "Objective
Estimation of feasibility and safety of allogeneic hematopoietic stem cell transplantation (HSCT) with TCRαβ +/CD19+ cell depletion in patients with primary immunodeficiency (PID) without usage of posttransplant immunosuppressive therapy.
Patients and methods
Ten allogeneic HSCTs were performed from October 2017 to May 2018 to the patients with PID (Nijmegen breakage syndrome, 1; Chronic granulomatous disease, 2; CID with CD40L deficiency, 3; PID with PI3K-delta deficiency, 1; X-linked lymphoproliferative syndrome type I, 1; leukocyte adhesion deficiency; 1; severe congenital neutropenia, 1). We carried out trans plants from unrelated (n=8) or haploidentical donors (n=2) using TCRαβ+/CD19 + depletion. Nine patients were conditioned for HSCT with treosulfan 42 g/m2, fludarabine 150 mg/m2, melphalan 140 mg/m2; one patient (Nijmegen’s syndrome) – treosulfan 30 g/m2, fludarabine 150 mg/m2, cyclophosphamide 40 mg/kg. Antithymocyte immunoglobulin – Thymoglobulin® (“Genzyme Europe B.V.”, The Netherlands) was used as a serotherapy at the doses of 5 to 7.5 mg/kg in all cases. Posttransplant GVHD prophylaxis was not performed.
Results
Transplant engraftment was recorded in all the patients. Acute GVHD was verified in 3 out of 10 cases, in 2 of which GVHD of 2nd degree was limited to skin. Only one patient (with Nijmegen syndrome) had acute liver GVHD stage 3 and combined immunosuppressive therapy was required. All the patients are alive at 2 to 10 months after HSCT, with good functional characteristics of the transplants.
Conclusion
Exclusion of posttransplant immunosuppressive therapy after HSCT with TCRαβ+/CD19+ depletion in patients with PID has demonstrated safety in relation to the risk of GVHD development. Severe visceral form of GVHD was recorded only in a patient being at high risk of developing this complication, due to characteristics of the disease (Nijmegen syndrome). Currently, the recruitment of patients is underway, and estimation of immune reconstitution rates reactivation of viral infections, and other factors should be evaluated later.
Keywords
Hematopoietic stem cell transplantation, TCRαβ+/CD19+ depletion, graft-versus-host disease, posttransplant immunosuppressive therapy, primary immunodeficiency.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20526" ["VALUE"]=> string(186) "The experience of hematopoietic stem cells transplantation with TCRαβ+/CD19+ depletion without posttransplantation prophylaxis of GVHD in patients with primary immunodeficiencies (PID)" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(186) "The experience of hematopoietic stem cells transplantation with TCRαβ+/CD19+ depletion without posttransplantation prophylaxis of GVHD in patients with primary immunodeficiencies (PID)" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(186) "The experience of hematopoietic stem cells transplantation with TCRαβ+/CD19+ depletion without posttransplantation prophylaxis of GVHD in patients with primary immunodeficiencies (PID)" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20524" ["VALUE"]=> array(2) { ["TEXT"]=> string(126) "Dmitriy Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(126) "Dmitriy Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(126) "Dmitriy Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20520" ["VALUE"]=> array(2) { ["TEXT"]=> string(226) "Светлана Н. Козловская, Светлана А. Радыгина, Ирина П. Шипицына, Елена И. Гутовская, Константин В. Митраков, Дмитрий Н. Балашов" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(226) "Светлана Н. Козловская, Светлана А. Радыгина, Ирина П. Шипицына, Елена И. Гутовская, Константин В. Митраков, Дмитрий Н. Балашов" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(226) "Светлана Н. Козловская, Светлана А. Радыгина, Ирина П. Шипицына, Елена И. Гутовская, Константин В. Митраков, Дмитрий Н. Балашов" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20522" ["VALUE"]=> array(2) { ["TEXT"]=> string(4856) "<h2></h2> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Оценка выполнимости и безопасности аллогенной ТГСК с TCRαβ+/CD19+ деплецией у пациентов с первичными иммунодефицитами (ПИД) без использования посттрансплантационной иммуносупрессивной терапии. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> С октября 2017 по май 2018 проведено 10 аллогенных ТГСК от неродственного(n=8) и гаплоидентичного(n=2) доноров с TCRαβ+/CD19+ деплецией трансплантата у пациентов с ПИД (сидром Ниймеген – 1, хроническая гранулематозная болезнь – 2, гипер IgM синдром – 3, ПИД с дефицитом PI3K-дельта – 1, Х-сцепленный лимфопролиферативный синдром I типа – 1, ПИД с дефектом адгезии лейкоцитов I типа – 1, тяжелая врожденная нейтропения – 1). У 9 пациентов проведен режим кондиционирования – треосульфан 42 гр/м2, флударабин 150 мг/м2, мельфалан 140 мг/м2; одному пациенту (синдром Ниймеген) – треосульфан 30 гр/м2, флударабин 150 мг/м2, циклофосфамид 40 мг/кг. В качестве серотерапии во всех случаях использовался антитимоцитарный иммуноглобулин – Тимоглобулин® (“Genzyme Europe B.V.”, Нидерланды) в дозах 5-7,5 мг/кг. Посттрансплантационная иммуносупрессивная терапия для профилактика РТПХ не проводилась. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Приживление трансплантата было зарегистрировано у всех пациентов. Острая РТПХ верифицирована в 3 из 10 случаях, в 2 из которых РТПХ была ограничена исключительно поражением кожи 2 степени. Только у одного пациента (с синдромом Ниймеген) отмечалось развитие острой РТПХ 3 стадии с поражением печени, потребовавшей комбинированной иммуносупрессивной терапии. Все пациенты живы на сроках от 2 до 10 месяцев после ТГСК с хорошими функциональными характеристиками трансплантата. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Исключение иммуносупрессивной терапии из протокола ТГСК с TCRαβ+/CD19+ деплецией у пациентов ПИД продемонстрировало свою безопасность в отношении риска развития РТПХ. Тяжелая висцеральная форма РТПХ была зарегистрирована только у пациента с высоким риском развития данного осложнения, обусловленного особенностями основного заболевания (синдром Ниймеген). В настоящее время набор пациентов продолжается. Поэтому оценка темпов иммунореконституции, частоты реактивации вирусных инфекций и ряд других факторов будут оценены позднее. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток, TCRαβ+/CD19+ деплеция, реакция трансплантат против хозяина, посттрансплантационная иммуносупрессивная терапия, первичный иммунодефицит. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4624) "Цель
Оценка выполнимости и безопасности аллогенной ТГСК с TCRαβ+/CD19+ деплецией у пациентов с первичными иммунодефицитами (ПИД) без использования посттрансплантационной иммуносупрессивной терапии.
Пациенты и методы
С октября 2017 по май 2018 проведено 10 аллогенных ТГСК от неродственного(n=8) и гаплоидентичного(n=2) доноров с TCRαβ+/CD19+ деплецией трансплантата у пациентов с ПИД (сидром Ниймеген – 1, хроническая гранулематозная болезнь – 2, гипер IgM синдром – 3, ПИД с дефицитом PI3K-дельта – 1, Х-сцепленный лимфопролиферативный синдром I типа – 1, ПИД с дефектом адгезии лейкоцитов I типа – 1, тяжелая врожденная нейтропения – 1). У 9 пациентов проведен режим кондиционирования – треосульфан 42 гр/м2, флударабин 150 мг/м2, мельфалан 140 мг/м2; одному пациенту (синдром Ниймеген) – треосульфан 30 гр/м2, флударабин 150 мг/м2, циклофосфамид 40 мг/кг. В качестве серотерапии во всех случаях использовался антитимоцитарный иммуноглобулин – Тимоглобулин® (“Genzyme Europe B.V.”, Нидерланды) в дозах 5-7,5 мг/кг. Посттрансплантационная иммуносупрессивная терапия для профилактика РТПХ не проводилась.
Результаты
Приживление трансплантата было зарегистрировано у всех пациентов. Острая РТПХ верифицирована в 3 из 10 случаях, в 2 из которых РТПХ была ограничена исключительно поражением кожи 2 степени. Только у одного пациента (с синдромом Ниймеген) отмечалось развитие острой РТПХ 3 стадии с поражением печени, потребовавшей комбинированной иммуносупрессивной терапии. Все пациенты живы на сроках от 2 до 10 месяцев после ТГСК с хорошими функциональными характеристиками трансплантата.
Заключение
Исключение иммуносупрессивной терапии из протокола ТГСК с TCRαβ+/CD19+ деплецией у пациентов ПИД продемонстрировало свою безопасность в отношении риска развития РТПХ. Тяжелая висцеральная форма РТПХ была зарегистрирована только у пациента с высоким риском развития данного осложнения, обусловленного особенностями основного заболевания (синдром Ниймеген). В настоящее время набор пациентов продолжается. Поэтому оценка темпов иммунореконституции, частоты реактивации вирусных инфекций и ряд других факторов будут оценены позднее.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, TCRαβ+/CD19+ деплеция, реакция трансплантат против хозяина, посттрансплантационная иммуносупрессивная терапия, первичный иммунодефицит.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4624) "Цель
Оценка выполнимости и безопасности аллогенной ТГСК с TCRαβ+/CD19+ деплецией у пациентов с первичными иммунодефицитами (ПИД) без использования посттрансплантационной иммуносупрессивной терапии.
Пациенты и методы
С октября 2017 по май 2018 проведено 10 аллогенных ТГСК от неродственного(n=8) и гаплоидентичного(n=2) доноров с TCRαβ+/CD19+ деплецией трансплантата у пациентов с ПИД (сидром Ниймеген – 1, хроническая гранулематозная болезнь – 2, гипер IgM синдром – 3, ПИД с дефицитом PI3K-дельта – 1, Х-сцепленный лимфопролиферативный синдром I типа – 1, ПИД с дефектом адгезии лейкоцитов I типа – 1, тяжелая врожденная нейтропения – 1). У 9 пациентов проведен режим кондиционирования – треосульфан 42 гр/м2, флударабин 150 мг/м2, мельфалан 140 мг/м2; одному пациенту (синдром Ниймеген) – треосульфан 30 гр/м2, флударабин 150 мг/м2, циклофосфамид 40 мг/кг. В качестве серотерапии во всех случаях использовался антитимоцитарный иммуноглобулин – Тимоглобулин® (“Genzyme Europe B.V.”, Нидерланды) в дозах 5-7,5 мг/кг. Посттрансплантационная иммуносупрессивная терапия для профилактика РТПХ не проводилась.
Результаты
Приживление трансплантата было зарегистрировано у всех пациентов. Острая РТПХ верифицирована в 3 из 10 случаях, в 2 из которых РТПХ была ограничена исключительно поражением кожи 2 степени. Только у одного пациента (с синдромом Ниймеген) отмечалось развитие острой РТПХ 3 стадии с поражением печени, потребовавшей комбинированной иммуносупрессивной терапии. Все пациенты живы на сроках от 2 до 10 месяцев после ТГСК с хорошими функциональными характеристиками трансплантата.
Заключение
Исключение иммуносупрессивной терапии из протокола ТГСК с TCRαβ+/CD19+ деплецией у пациентов ПИД продемонстрировало свою безопасность в отношении риска развития РТПХ. Тяжелая висцеральная форма РТПХ была зарегистрирована только у пациента с высоким риском развития данного осложнения, обусловленного особенностями основного заболевания (синдром Ниймеген). В настоящее время набор пациентов продолжается. Поэтому оценка темпов иммунореконституции, частоты реактивации вирусных инфекций и ряд других факторов будут оценены позднее.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, TCRαβ+/CD19+ деплеция, реакция трансплантат против хозяина, посттрансплантационная иммуносупрессивная терапия, первичный иммунодефицит.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20521" ["VALUE"]=> array(2) { ["TEXT"]=> string(469) "Федеральное государственное бюджетное учреждение «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Министерства здравоохранения Российской Федерации, Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(469) "Федеральное государственное бюджетное учреждение «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Министерства здравоохранения Российской Федерации, Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(469) "Федеральное государственное бюджетное учреждение «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Министерства здравоохранения Российской Федерации, Москва, Российская Федерация" } } } [27]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1577" ["~ID"]=> string(4) "1577" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(109) "Химиотерапия, инфузионная терапия: роль медицинской сестры" ["~NAME"]=> string(109) "Химиотерапия, инфузионная терапия: роль медицинской сестры" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:37:54" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:37:54" ["DETAIL_PAGE_URL"]=> string(110) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/khimioterapiya-infuzionnaya-terapiya-rol-meditsinskoy-sestry/" ["~DETAIL_PAGE_URL"]=> string(110) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/khimioterapiya-infuzionnaya-terapiya-rol-meditsinskoy-sestry/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(60) "khimioterapiya-infuzionnaya-terapiya-rol-meditsinskoy-sestry" ["~CODE"]=> string(60) "khimioterapiya-infuzionnaya-terapiya-rol-meditsinskoy-sestry" ["EXTERNAL_ID"]=> string(4) "1577" ["~EXTERNAL_ID"]=> string(4) "1577" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(109) "Химиотерапия, инфузионная терапия: роль медицинской сестры" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(160) "Химиотерапия, инфузионная терапия: роль медицинской сестрыChemotherapy, infusion therapy: the role of a nurse" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(10691) "<h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель работы – изучить роль медицинской сестры и особенности сестринского ухода за пациентами при проведении химиотерапии, инфузионной терапии, трансплантации гемопоэтических стволовых клеток (ТГСК); изучить сестринский процесс подготовки донора к сдаче концентрата периферических мононуклеаров. </p> <h2 style="text-align: justify;">Методы исследования</h2> <p style="text-align: justify;"> За основу исследования был взят протокол ТГСК при остром миелоидном лейкозе (ОМЛ). Стандартные процедуры: 1. Химиотерапия (кондиционирование). 2. Инфузионная терапия. 3. Подготовка донора. 4. ТГСК. </p> <h3 style="text-align: justify;">1. Химиотерапия</h3> <p style="text-align: justify;"> В данный протокол кондиционирования входят следующие препараты: Флударабин, Треосульфан, Тиотепа, Актемра, Оренсия. При введении препаратов на этапе кондиционирования роль медицинской сестры заключается в правильности введения (дозировка и разведение препарата, скорость введения, при необходимости оказание экстренной помощи), знать об возможных осложнениях, применять разработанные рекомендации для профилактики осложнений, обучить родителей и контролировать их выполнение. Профилактика возможных осложнений: а) Кожные покровы. Применение топических стероидов по уходу за кожей, увлажняющих и смягчающих кремов. Ежедневное обтирание моющим лосьоном с применением одноразовых рукавиц для мытья. в) Слизистые оболочки. Использование для полоскания и орошения ротовой полости антисептических растворов; с) Желудочно-кишечный тракт. Предотвращение тошноты и рвоты (рекомендации по питанию, введение противорвотных препаратов). d) Мочеполовая система. Применение антисептических растворов для подмывания наружных половых органов для дезинфицирующего действия. e) Нервная система. По назначению врача выдача лекарственных препаратов, действие которых направлено на устранение тревожности, симптомов периферической нейропатии (мышечная слабость, нарушение мышечного тонуса, дрожание в мышцах, судороги в мышцах). </p> <h3 style="text-align: justify;">2. Инфузионная терапия</h3> <p style="text-align: justify;"> Для эффективной и безопасной инфузионной терапии (ИТ) необходимо владеть полной информацией: продолжительность внутривенных вливаний, правила проведение вливаний, уход за устройством и местом венозного доступа. При проведении инфузионной терапии медицинская сестра должна оценить состояние пациента (подсчет водного баланса, мониторинг жизненно важных функций); провести разъяснительную и просветительную беседу о планируемом лечении. </p> <h3 style="text-align: justify;">3. Подготовка донора</h3> <p style="text-align: justify;"> Важным этапом в проведении ТГСК стоит в подготовке донора стволовых клеток к сдаче материала путем цитафереза. Для получения концентрата периферических мононуклеаров, обогащенного стволовыми гемопоэтическими стволовыми клетками необходима предварительная мобилизация лейкоцитов гранулоцитарным колониестимулирующим фактором (Г-КСФ). Г-КСФ повышает количество лейкоцитов и стимулирует выход стволовых клеток из костного мозга в периферическую кровь. Медицинская сестра в течении 5 дней вводит подкожно препараты Г-КСФ и регистрирует возможные редкие побочные явления. По назначению врача медицинская сестра вводит обезболивающие, осуществляет забор крови для анализов и постановку инфузионной терапии. </p> <h3 style="text-align: justify;">4. Трансплантация гемопоэтических стволовых клеток</h3> <p style="text-align: justify;"> При лечении пациентов по протоколу с диагнозом ОМЛ проводится гаплоидентичная трансплантация гемопоэтических стволовых клеток с TCR альфа/бета и деплецией CD19+ клеток. Преимущества метода: Удалением из трансплантата TCR альфа/бета клеток осуществляется профилактика РТПХ; оставшийся небольшой процент гамма/дельта Т-клеток запускает процесс реконституции иммунной системы и, как следствие – ее более быстрое восстановление. При проведении процедуры трансплантации роль медицинской сестры заключается в следующем: проводить мониторинг жизненно важных функций; обеспечение доступности лекарственных препаратов при побочных осложнениях: для предотвращения реакций или аллоиммунизации использовать фильтры при процедуре трансплантации; медицинская сестра должна знать о возможных осложнениях и уметь оказывать необходимую помощь. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Роль медицинской сестры на протяжении всех стандартных процедур, включенных в протоколы лечения в нашем Центре, имеет огромную значимость. Медицинская сестра должна ознакомить пациента с отделением, объяснить план лечения, назначенный лечащим врачом. Она должна уметь отвечать на вопросы пациента о подготовке к проведению химиотерапии, ТГСК, объяснить, почему химиотерапия может вызывать осложнения и как можно их предотвратить или уменьшить. Развитие побочных реакций при использовании противоопухолевых препаратов и проведении ТГСК создает определенные проблемы для пациента и медицинского персонала, осуществляющего уход, требует от медицинских сестер внимания и индивидуального подхода к каждому из пациентов. </p> <h2 style="text-align: justify;">Список литературы</h2> <p style="text-align: justify;"> 1. М. А. Масчан Деплеция альфа/бета-Т-лимфоцитов – надежная платформа для развития трансплантации гемопоэтических стволовых клеток от гаплоидентичных доноров//Российский журнал детской гематологии и онкологии НОДГО. 2015. №3. С. 34-38.<br> 2. Е. В. Самочатова, А. Г. Румянцев Сестринский уход в детской гематологии и онкологии // М.: Издательство «Литтерра», 2011.-220c. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Химиотерапия, кондиционирование, инфузионная терапия, роль медицинской сестры, донор, трансплантация гемопоэтических стволовых клеток. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(109) "Химиотерапия, инфузионная терапия: роль медицинской сестры" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(109) "Химиотерапия, инфузионная терапия: роль медицинской сестры" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(109) "Химиотерапия, инфузионная терапия: роль медицинской сестры" ["SECTION_META_TITLE"]=> string(109) "Химиотерапия, инфузионная терапия: роль медицинской сестры" ["SECTION_META_KEYWORDS"]=> string(109) "Химиотерапия, инфузионная терапия: роль медицинской сестры" ["SECTION_META_DESCRIPTION"]=> string(109) "Химиотерапия, инфузионная терапия: роль медицинской сестры" ["SECTION_PICTURE_FILE_ALT"]=> string(109) "Химиотерапия, инфузионная терапия: роль медицинской сестры" ["SECTION_PICTURE_FILE_TITLE"]=> string(109) "Химиотерапия, инфузионная терапия: роль медицинской сестры" ["SECTION_PICTURE_FILE_NAME"]=> string(64) "khimioterapiya-infuzionnaya-terapiya-rol-meditsinskoy-sestry-img" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(109) "Химиотерапия, инфузионная терапия: роль медицинской сестры" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(109) "Химиотерапия, инфузионная терапия: роль медицинской сестры" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(64) "khimioterapiya-infuzionnaya-terapiya-rol-meditsinskoy-sestry-img" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(64) "khimioterapiya-infuzionnaya-terapiya-rol-meditsinskoy-sestry-img" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(64) "khimioterapiya-infuzionnaya-terapiya-rol-meditsinskoy-sestry-img" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20529" ["VALUE"]=> array(2) { ["TEXT"]=> string(101) "Наталья П. Лещук, Андрей Б. Абросимов, Лариса Н. Шелихова" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(101) "Наталья П. Лещук, Андрей Б. Абросимов, Лариса Н. Шелихова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20530" ["VALUE"]=> array(2) { ["TEXT"]=> string(128) "ФГБУ «НМИЦ ДГОИ имени Дмитрия Рогачева», Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(128) "ФГБУ «НМИЦ ДГОИ имени Дмитрия Рогачева», Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20531" ["VALUE"]=> array(2) { ["TEXT"]=> string(10691) "<h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель работы – изучить роль медицинской сестры и особенности сестринского ухода за пациентами при проведении химиотерапии, инфузионной терапии, трансплантации гемопоэтических стволовых клеток (ТГСК); изучить сестринский процесс подготовки донора к сдаче концентрата периферических мононуклеаров. </p> <h2 style="text-align: justify;">Методы исследования</h2> <p style="text-align: justify;"> За основу исследования был взят протокол ТГСК при остром миелоидном лейкозе (ОМЛ). Стандартные процедуры: 1. Химиотерапия (кондиционирование). 2. Инфузионная терапия. 3. Подготовка донора. 4. ТГСК. </p> <h3 style="text-align: justify;">1. Химиотерапия</h3> <p style="text-align: justify;"> В данный протокол кондиционирования входят следующие препараты: Флударабин, Треосульфан, Тиотепа, Актемра, Оренсия. При введении препаратов на этапе кондиционирования роль медицинской сестры заключается в правильности введения (дозировка и разведение препарата, скорость введения, при необходимости оказание экстренной помощи), знать об возможных осложнениях, применять разработанные рекомендации для профилактики осложнений, обучить родителей и контролировать их выполнение. Профилактика возможных осложнений: а) Кожные покровы. Применение топических стероидов по уходу за кожей, увлажняющих и смягчающих кремов. Ежедневное обтирание моющим лосьоном с применением одноразовых рукавиц для мытья. в) Слизистые оболочки. Использование для полоскания и орошения ротовой полости антисептических растворов; с) Желудочно-кишечный тракт. Предотвращение тошноты и рвоты (рекомендации по питанию, введение противорвотных препаратов). d) Мочеполовая система. Применение антисептических растворов для подмывания наружных половых органов для дезинфицирующего действия. e) Нервная система. По назначению врача выдача лекарственных препаратов, действие которых направлено на устранение тревожности, симптомов периферической нейропатии (мышечная слабость, нарушение мышечного тонуса, дрожание в мышцах, судороги в мышцах). </p> <h3 style="text-align: justify;">2. Инфузионная терапия</h3> <p style="text-align: justify;"> Для эффективной и безопасной инфузионной терапии (ИТ) необходимо владеть полной информацией: продолжительность внутривенных вливаний, правила проведение вливаний, уход за устройством и местом венозного доступа. При проведении инфузионной терапии медицинская сестра должна оценить состояние пациента (подсчет водного баланса, мониторинг жизненно важных функций); провести разъяснительную и просветительную беседу о планируемом лечении. </p> <h3 style="text-align: justify;">3. Подготовка донора</h3> <p style="text-align: justify;"> Важным этапом в проведении ТГСК стоит в подготовке донора стволовых клеток к сдаче материала путем цитафереза. Для получения концентрата периферических мононуклеаров, обогащенного стволовыми гемопоэтическими стволовыми клетками необходима предварительная мобилизация лейкоцитов гранулоцитарным колониестимулирующим фактором (Г-КСФ). Г-КСФ повышает количество лейкоцитов и стимулирует выход стволовых клеток из костного мозга в периферическую кровь. Медицинская сестра в течении 5 дней вводит подкожно препараты Г-КСФ и регистрирует возможные редкие побочные явления. По назначению врача медицинская сестра вводит обезболивающие, осуществляет забор крови для анализов и постановку инфузионной терапии. </p> <h3 style="text-align: justify;">4. Трансплантация гемопоэтических стволовых клеток</h3> <p style="text-align: justify;"> При лечении пациентов по протоколу с диагнозом ОМЛ проводится гаплоидентичная трансплантация гемопоэтических стволовых клеток с TCR альфа/бета и деплецией CD19+ клеток. Преимущества метода: Удалением из трансплантата TCR альфа/бета клеток осуществляется профилактика РТПХ; оставшийся небольшой процент гамма/дельта Т-клеток запускает процесс реконституции иммунной системы и, как следствие – ее более быстрое восстановление. При проведении процедуры трансплантации роль медицинской сестры заключается в следующем: проводить мониторинг жизненно важных функций; обеспечение доступности лекарственных препаратов при побочных осложнениях: для предотвращения реакций или аллоиммунизации использовать фильтры при процедуре трансплантации; медицинская сестра должна знать о возможных осложнениях и уметь оказывать необходимую помощь. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Роль медицинской сестры на протяжении всех стандартных процедур, включенных в протоколы лечения в нашем Центре, имеет огромную значимость. Медицинская сестра должна ознакомить пациента с отделением, объяснить план лечения, назначенный лечащим врачом. Она должна уметь отвечать на вопросы пациента о подготовке к проведению химиотерапии, ТГСК, объяснить, почему химиотерапия может вызывать осложнения и как можно их предотвратить или уменьшить. Развитие побочных реакций при использовании противоопухолевых препаратов и проведении ТГСК создает определенные проблемы для пациента и медицинского персонала, осуществляющего уход, требует от медицинских сестер внимания и индивидуального подхода к каждому из пациентов. </p> <h2 style="text-align: justify;">Список литературы</h2> <p style="text-align: justify;"> 1. М. А. Масчан Деплеция альфа/бета-Т-лимфоцитов – надежная платформа для развития трансплантации гемопоэтических стволовых клеток от гаплоидентичных доноров//Российский журнал детской гематологии и онкологии НОДГО. 2015. №3. С. 34-38.<br> 2. Е. В. Самочатова, А. Г. Румянцев Сестринский уход в детской гематологии и онкологии // М.: Издательство «Литтерра», 2011.-220c. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Химиотерапия, кондиционирование, инфузионная терапия, роль медицинской сестры, донор, трансплантация гемопоэтических стволовых клеток. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(10289) "Цель
Цель работы – изучить роль медицинской сестры и особенности сестринского ухода за пациентами при проведении химиотерапии, инфузионной терапии, трансплантации гемопоэтических стволовых клеток (ТГСК); изучить сестринский процесс подготовки донора к сдаче концентрата периферических мононуклеаров.
Методы исследования
За основу исследования был взят протокол ТГСК при остром миелоидном лейкозе (ОМЛ). Стандартные процедуры: 1. Химиотерапия (кондиционирование). 2. Инфузионная терапия. 3. Подготовка донора. 4. ТГСК.
1. Химиотерапия
В данный протокол кондиционирования входят следующие препараты: Флударабин, Треосульфан, Тиотепа, Актемра, Оренсия. При введении препаратов на этапе кондиционирования роль медицинской сестры заключается в правильности введения (дозировка и разведение препарата, скорость введения, при необходимости оказание экстренной помощи), знать об возможных осложнениях, применять разработанные рекомендации для профилактики осложнений, обучить родителей и контролировать их выполнение. Профилактика возможных осложнений: а) Кожные покровы. Применение топических стероидов по уходу за кожей, увлажняющих и смягчающих кремов. Ежедневное обтирание моющим лосьоном с применением одноразовых рукавиц для мытья. в) Слизистые оболочки. Использование для полоскания и орошения ротовой полости антисептических растворов; с) Желудочно-кишечный тракт. Предотвращение тошноты и рвоты (рекомендации по питанию, введение противорвотных препаратов). d) Мочеполовая система. Применение антисептических растворов для подмывания наружных половых органов для дезинфицирующего действия. e) Нервная система. По назначению врача выдача лекарственных препаратов, действие которых направлено на устранение тревожности, симптомов периферической нейропатии (мышечная слабость, нарушение мышечного тонуса, дрожание в мышцах, судороги в мышцах).
2. Инфузионная терапия
Для эффективной и безопасной инфузионной терапии (ИТ) необходимо владеть полной информацией: продолжительность внутривенных вливаний, правила проведение вливаний, уход за устройством и местом венозного доступа. При проведении инфузионной терапии медицинская сестра должна оценить состояние пациента (подсчет водного баланса, мониторинг жизненно важных функций); провести разъяснительную и просветительную беседу о планируемом лечении.
3. Подготовка донора
Важным этапом в проведении ТГСК стоит в подготовке донора стволовых клеток к сдаче материала путем цитафереза. Для получения концентрата периферических мононуклеаров, обогащенного стволовыми гемопоэтическими стволовыми клетками необходима предварительная мобилизация лейкоцитов гранулоцитарным колониестимулирующим фактором (Г-КСФ). Г-КСФ повышает количество лейкоцитов и стимулирует выход стволовых клеток из костного мозга в периферическую кровь. Медицинская сестра в течении 5 дней вводит подкожно препараты Г-КСФ и регистрирует возможные редкие побочные явления. По назначению врача медицинская сестра вводит обезболивающие, осуществляет забор крови для анализов и постановку инфузионной терапии.
4. Трансплантация гемопоэтических стволовых клеток
При лечении пациентов по протоколу с диагнозом ОМЛ проводится гаплоидентичная трансплантация гемопоэтических стволовых клеток с TCR альфа/бета и деплецией CD19+ клеток. Преимущества метода: Удалением из трансплантата TCR альфа/бета клеток осуществляется профилактика РТПХ; оставшийся небольшой процент гамма/дельта Т-клеток запускает процесс реконституции иммунной системы и, как следствие – ее более быстрое восстановление. При проведении процедуры трансплантации роль медицинской сестры заключается в следующем: проводить мониторинг жизненно важных функций; обеспечение доступности лекарственных препаратов при побочных осложнениях: для предотвращения реакций или аллоиммунизации использовать фильтры при процедуре трансплантации; медицинская сестра должна знать о возможных осложнениях и уметь оказывать необходимую помощь.
Заключение
Роль медицинской сестры на протяжении всех стандартных процедур, включенных в протоколы лечения в нашем Центре, имеет огромную значимость. Медицинская сестра должна ознакомить пациента с отделением, объяснить план лечения, назначенный лечащим врачом. Она должна уметь отвечать на вопросы пациента о подготовке к проведению химиотерапии, ТГСК, объяснить, почему химиотерапия может вызывать осложнения и как можно их предотвратить или уменьшить. Развитие побочных реакций при использовании противоопухолевых препаратов и проведении ТГСК создает определенные проблемы для пациента и медицинского персонала, осуществляющего уход, требует от медицинских сестер внимания и индивидуального подхода к каждому из пациентов.
Список литературы
1. М. А. Масчан Деплеция альфа/бета-Т-лимфоцитов – надежная платформа для развития трансплантации гемопоэтических стволовых клеток от гаплоидентичных доноров//Российский журнал детской гематологии и онкологии НОДГО. 2015. №3. С. 34-38.
2. Е. В. Самочатова, А. Г. Румянцев Сестринский уход в детской гематологии и онкологии // М.: Издательство «Литтерра», 2011.-220c.
Ключевые слова
Химиотерапия, кондиционирование, инфузионная терапия, роль медицинской сестры, донор, трансплантация гемопоэтических стволовых клеток.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20532" ["VALUE"]=> array(2) { ["TEXT"]=> string(62) "Natalia P. Leshchuk, Andrei B. Abrosimov, Larisa N. Shelikhova" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(62) "Natalia P. Leshchuk, Andrei B. Abrosimov, Larisa N. Shelikhova" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20533" ["VALUE"]=> array(2) { ["TEXT"]=> string(121) "D. Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(121) "D. Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20534" ["VALUE"]=> array(2) { ["TEXT"]=> string(5527) "<h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> The aim of this study is to explore the role of a nurse and the specifics of nursing care during chemotherapy, infusion therapy, hematopoietic stem cell transplantation (HSCT) and study the process of a donor preparation for the donation of a peripheral blood mononuclear cell (PMBC) concentrate. </p> <h2 style="text-align: justify;">Methods of investigation</h2> <p style="text-align: justify;"> The study is based on the HSCT protocol in acute myeloid leukemia (AML). The standard procedures included: 1. Chemotherapy (conditioning). 2. Infusion therapy. 3. Preparation of a donor. 4. HSCT. </p> <h3 style="text-align: justify;">1. Chemotherapy stage</h3> <p style="text-align: justify;"> This conditioning treatment protocol includes the following chemotherapy agents: Fludarabine, Treosulfan, Thiotepa, Actemra, Orencia. When using drugs within the conditioning treatment, the role of a nurse is to ensure the prescribed injection regimen (drug dosage and dilution, speed of injection, first aid, if necessary). A nurse should be aware of any possible complications, apply recommendations for the prevention of complications, educate patient’s parents on these recommendations. Prevention of potential complications: a) Skin: use of topical corticosteroids, moisturizing and softening creams for skin care. Daily application of cleansing lotion using disposable wash gloves. b) Mucous membranes. Use of oral antiseptic solution (gargling and irrigation); c) Gastrointestinal system: prevention of nausea and vomiting (dietary recommendations, use of antiemetics). d) Urogenital system: application of an antiseptic solution to the external genitalia for purposes of disinfection. e) Nervous system: distribution of prescribed medications which are aimed for management of anxiety, peripheral neuropathy symptoms (muscle weakness, muscle tone impairment, tremor, muscle spasm). </p> <h3 style="text-align: justify;">2. Infusion therapy</h3> <p style="text-align: justify;"> In order to provide effective and safe infusion therapy (IT) delivery it is necessary to have a detailed information on the following aspects: duration of intravenous infusions, guidelines of infusions, venous access site care and equipment maintenance. Before starting the infusion therapy, a nurse must perform an assessment of a patient (fluid balance measurement, patient’s vital signs monitoring); educate and inform a patient and her/his parents about the planned treatment. </p> <h3 style="text-align: justify;">3. Preparation of a donor</h3> <p style="text-align: justify;"> An important stage in HSCT is to prepare a donor for stem cell donation by means of cytapheresis. To obtain a peripheral blood mononuclear cell concentrate enriched in hematopoietic stem cells, a preliminary G-CSF-induced leukocyte mobilization is required. G-CSF increases WBC count and stimulates stem cell release from the bone marrow into the peripheral blood. A nurse performs subcutaneous injections of G-CSF for 5 days and registers possible uncommon side effects. At doctor’s instruction a nurse performs an injection of anesthesia, collects blood for testing and places a catheter for the infusion therapy. </p> <h3 style="text-align: justify;">4. Hematopoietic stem cell transplantation</h3> <p style="text-align: justify;"> During the treatment on the AML protocol, TCR-Alpha/Beta and CD19 depleted haploidentical stem cell transplantation is performed. The advantages of the method: TCR aplha/beta cells are removed from the graft to perform a GVHD prophylaxis. The remaining small percentage of gamma/delta T-cells induces a faster immune system recovery and, as a consequence, leads to more rapid immune reconstitution. During the procedure of transplantation, a nurse is responsible for: monitoring of patient’s vital signs; ensuring the availability of drugs for side effect management; using filters to prevent transfusion reactions and alloimmunization during transplantation. A nurse should be aware of potential complications and provide an appropriate assistance. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Nursing staff plays an important role in implementation of all standard procedures of treatment protocols at our Center. A nurse must guide the patient through the department and inform her/him of the treatment plan prescribed by the treating physician. She should be able to answer the patient’s questions relating to the preparation for the chemotherapy and HSCT, explain the cause of the chemotherapy-induced complications and inform the patient on how to prevent or reduce them. Side effects induced by anti-cancer drugs and HSCT creates certain problems for a patient and medical staff involved in care, management of which require the assistance of nursing staff and personalized approach to each patient. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Chemotherapy, conditioning, infusion therapy, role of nurse, donor, hematopoietic stem cell transplantation. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5175) "Aim
The aim of this study is to explore the role of a nurse and the specifics of nursing care during chemotherapy, infusion therapy, hematopoietic stem cell transplantation (HSCT) and study the process of a donor preparation for the donation of a peripheral blood mononuclear cell (PMBC) concentrate.
Methods of investigation
The study is based on the HSCT protocol in acute myeloid leukemia (AML). The standard procedures included: 1. Chemotherapy (conditioning). 2. Infusion therapy. 3. Preparation of a donor. 4. HSCT.
1. Chemotherapy stage
This conditioning treatment protocol includes the following chemotherapy agents: Fludarabine, Treosulfan, Thiotepa, Actemra, Orencia. When using drugs within the conditioning treatment, the role of a nurse is to ensure the prescribed injection regimen (drug dosage and dilution, speed of injection, first aid, if necessary). A nurse should be aware of any possible complications, apply recommendations for the prevention of complications, educate patient’s parents on these recommendations. Prevention of potential complications: a) Skin: use of topical corticosteroids, moisturizing and softening creams for skin care. Daily application of cleansing lotion using disposable wash gloves. b) Mucous membranes. Use of oral antiseptic solution (gargling and irrigation); c) Gastrointestinal system: prevention of nausea and vomiting (dietary recommendations, use of antiemetics). d) Urogenital system: application of an antiseptic solution to the external genitalia for purposes of disinfection. e) Nervous system: distribution of prescribed medications which are aimed for management of anxiety, peripheral neuropathy symptoms (muscle weakness, muscle tone impairment, tremor, muscle spasm).
2. Infusion therapy
In order to provide effective and safe infusion therapy (IT) delivery it is necessary to have a detailed information on the following aspects: duration of intravenous infusions, guidelines of infusions, venous access site care and equipment maintenance. Before starting the infusion therapy, a nurse must perform an assessment of a patient (fluid balance measurement, patient’s vital signs monitoring); educate and inform a patient and her/his parents about the planned treatment.
3. Preparation of a donor
An important stage in HSCT is to prepare a donor for stem cell donation by means of cytapheresis. To obtain a peripheral blood mononuclear cell concentrate enriched in hematopoietic stem cells, a preliminary G-CSF-induced leukocyte mobilization is required. G-CSF increases WBC count and stimulates stem cell release from the bone marrow into the peripheral blood. A nurse performs subcutaneous injections of G-CSF for 5 days and registers possible uncommon side effects. At doctor’s instruction a nurse performs an injection of anesthesia, collects blood for testing and places a catheter for the infusion therapy.
4. Hematopoietic stem cell transplantation
During the treatment on the AML protocol, TCR-Alpha/Beta and CD19 depleted haploidentical stem cell transplantation is performed. The advantages of the method: TCR aplha/beta cells are removed from the graft to perform a GVHD prophylaxis. The remaining small percentage of gamma/delta T-cells induces a faster immune system recovery and, as a consequence, leads to more rapid immune reconstitution. During the procedure of transplantation, a nurse is responsible for: monitoring of patient’s vital signs; ensuring the availability of drugs for side effect management; using filters to prevent transfusion reactions and alloimmunization during transplantation. A nurse should be aware of potential complications and provide an appropriate assistance.
Conclusion
Nursing staff plays an important role in implementation of all standard procedures of treatment protocols at our Center. A nurse must guide the patient through the department and inform her/him of the treatment plan prescribed by the treating physician. She should be able to answer the patient’s questions relating to the preparation for the chemotherapy and HSCT, explain the cause of the chemotherapy-induced complications and inform the patient on how to prevent or reduce them. Side effects induced by anti-cancer drugs and HSCT creates certain problems for a patient and medical staff involved in care, management of which require the assistance of nursing staff and personalized approach to each patient.
Keywords
Chemotherapy, conditioning, infusion therapy, role of nurse, donor, hematopoietic stem cell transplantation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20535" ["VALUE"]=> string(51) "Chemotherapy, infusion therapy: the role of a nurse" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(51) "Chemotherapy, infusion therapy: the role of a nurse" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20787" ["VALUE"]=> string(4) "1425" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1425" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20788" ["VALUE"]=> string(4) "1426" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1426" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20532" ["VALUE"]=> array(2) { ["TEXT"]=> string(62) "Natalia P. Leshchuk, Andrei B. Abrosimov, Larisa N. Shelikhova" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(62) "Natalia P. Leshchuk, Andrei B. Abrosimov, Larisa N. Shelikhova" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(62) "Natalia P. Leshchuk, Andrei B. Abrosimov, Larisa N. Shelikhova" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20534" ["VALUE"]=> array(2) { ["TEXT"]=> string(5527) "<h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> The aim of this study is to explore the role of a nurse and the specifics of nursing care during chemotherapy, infusion therapy, hematopoietic stem cell transplantation (HSCT) and study the process of a donor preparation for the donation of a peripheral blood mononuclear cell (PMBC) concentrate. </p> <h2 style="text-align: justify;">Methods of investigation</h2> <p style="text-align: justify;"> The study is based on the HSCT protocol in acute myeloid leukemia (AML). The standard procedures included: 1. Chemotherapy (conditioning). 2. Infusion therapy. 3. Preparation of a donor. 4. HSCT. </p> <h3 style="text-align: justify;">1. Chemotherapy stage</h3> <p style="text-align: justify;"> This conditioning treatment protocol includes the following chemotherapy agents: Fludarabine, Treosulfan, Thiotepa, Actemra, Orencia. When using drugs within the conditioning treatment, the role of a nurse is to ensure the prescribed injection regimen (drug dosage and dilution, speed of injection, first aid, if necessary). A nurse should be aware of any possible complications, apply recommendations for the prevention of complications, educate patient’s parents on these recommendations. Prevention of potential complications: a) Skin: use of topical corticosteroids, moisturizing and softening creams for skin care. Daily application of cleansing lotion using disposable wash gloves. b) Mucous membranes. Use of oral antiseptic solution (gargling and irrigation); c) Gastrointestinal system: prevention of nausea and vomiting (dietary recommendations, use of antiemetics). d) Urogenital system: application of an antiseptic solution to the external genitalia for purposes of disinfection. e) Nervous system: distribution of prescribed medications which are aimed for management of anxiety, peripheral neuropathy symptoms (muscle weakness, muscle tone impairment, tremor, muscle spasm). </p> <h3 style="text-align: justify;">2. Infusion therapy</h3> <p style="text-align: justify;"> In order to provide effective and safe infusion therapy (IT) delivery it is necessary to have a detailed information on the following aspects: duration of intravenous infusions, guidelines of infusions, venous access site care and equipment maintenance. Before starting the infusion therapy, a nurse must perform an assessment of a patient (fluid balance measurement, patient’s vital signs monitoring); educate and inform a patient and her/his parents about the planned treatment. </p> <h3 style="text-align: justify;">3. Preparation of a donor</h3> <p style="text-align: justify;"> An important stage in HSCT is to prepare a donor for stem cell donation by means of cytapheresis. To obtain a peripheral blood mononuclear cell concentrate enriched in hematopoietic stem cells, a preliminary G-CSF-induced leukocyte mobilization is required. G-CSF increases WBC count and stimulates stem cell release from the bone marrow into the peripheral blood. A nurse performs subcutaneous injections of G-CSF for 5 days and registers possible uncommon side effects. At doctor’s instruction a nurse performs an injection of anesthesia, collects blood for testing and places a catheter for the infusion therapy. </p> <h3 style="text-align: justify;">4. Hematopoietic stem cell transplantation</h3> <p style="text-align: justify;"> During the treatment on the AML protocol, TCR-Alpha/Beta and CD19 depleted haploidentical stem cell transplantation is performed. The advantages of the method: TCR aplha/beta cells are removed from the graft to perform a GVHD prophylaxis. The remaining small percentage of gamma/delta T-cells induces a faster immune system recovery and, as a consequence, leads to more rapid immune reconstitution. During the procedure of transplantation, a nurse is responsible for: monitoring of patient’s vital signs; ensuring the availability of drugs for side effect management; using filters to prevent transfusion reactions and alloimmunization during transplantation. A nurse should be aware of potential complications and provide an appropriate assistance. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Nursing staff plays an important role in implementation of all standard procedures of treatment protocols at our Center. A nurse must guide the patient through the department and inform her/him of the treatment plan prescribed by the treating physician. She should be able to answer the patient’s questions relating to the preparation for the chemotherapy and HSCT, explain the cause of the chemotherapy-induced complications and inform the patient on how to prevent or reduce them. Side effects induced by anti-cancer drugs and HSCT creates certain problems for a patient and medical staff involved in care, management of which require the assistance of nursing staff and personalized approach to each patient. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Chemotherapy, conditioning, infusion therapy, role of nurse, donor, hematopoietic stem cell transplantation. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5175) "Aim
The aim of this study is to explore the role of a nurse and the specifics of nursing care during chemotherapy, infusion therapy, hematopoietic stem cell transplantation (HSCT) and study the process of a donor preparation for the donation of a peripheral blood mononuclear cell (PMBC) concentrate.
Methods of investigation
The study is based on the HSCT protocol in acute myeloid leukemia (AML). The standard procedures included: 1. Chemotherapy (conditioning). 2. Infusion therapy. 3. Preparation of a donor. 4. HSCT.
1. Chemotherapy stage
This conditioning treatment protocol includes the following chemotherapy agents: Fludarabine, Treosulfan, Thiotepa, Actemra, Orencia. When using drugs within the conditioning treatment, the role of a nurse is to ensure the prescribed injection regimen (drug dosage and dilution, speed of injection, first aid, if necessary). A nurse should be aware of any possible complications, apply recommendations for the prevention of complications, educate patient’s parents on these recommendations. Prevention of potential complications: a) Skin: use of topical corticosteroids, moisturizing and softening creams for skin care. Daily application of cleansing lotion using disposable wash gloves. b) Mucous membranes. Use of oral antiseptic solution (gargling and irrigation); c) Gastrointestinal system: prevention of nausea and vomiting (dietary recommendations, use of antiemetics). d) Urogenital system: application of an antiseptic solution to the external genitalia for purposes of disinfection. e) Nervous system: distribution of prescribed medications which are aimed for management of anxiety, peripheral neuropathy symptoms (muscle weakness, muscle tone impairment, tremor, muscle spasm).
2. Infusion therapy
In order to provide effective and safe infusion therapy (IT) delivery it is necessary to have a detailed information on the following aspects: duration of intravenous infusions, guidelines of infusions, venous access site care and equipment maintenance. Before starting the infusion therapy, a nurse must perform an assessment of a patient (fluid balance measurement, patient’s vital signs monitoring); educate and inform a patient and her/his parents about the planned treatment.
3. Preparation of a donor
An important stage in HSCT is to prepare a donor for stem cell donation by means of cytapheresis. To obtain a peripheral blood mononuclear cell concentrate enriched in hematopoietic stem cells, a preliminary G-CSF-induced leukocyte mobilization is required. G-CSF increases WBC count and stimulates stem cell release from the bone marrow into the peripheral blood. A nurse performs subcutaneous injections of G-CSF for 5 days and registers possible uncommon side effects. At doctor’s instruction a nurse performs an injection of anesthesia, collects blood for testing and places a catheter for the infusion therapy.
4. Hematopoietic stem cell transplantation
During the treatment on the AML protocol, TCR-Alpha/Beta and CD19 depleted haploidentical stem cell transplantation is performed. The advantages of the method: TCR aplha/beta cells are removed from the graft to perform a GVHD prophylaxis. The remaining small percentage of gamma/delta T-cells induces a faster immune system recovery and, as a consequence, leads to more rapid immune reconstitution. During the procedure of transplantation, a nurse is responsible for: monitoring of patient’s vital signs; ensuring the availability of drugs for side effect management; using filters to prevent transfusion reactions and alloimmunization during transplantation. A nurse should be aware of potential complications and provide an appropriate assistance.
Conclusion
Nursing staff plays an important role in implementation of all standard procedures of treatment protocols at our Center. A nurse must guide the patient through the department and inform her/him of the treatment plan prescribed by the treating physician. She should be able to answer the patient’s questions relating to the preparation for the chemotherapy and HSCT, explain the cause of the chemotherapy-induced complications and inform the patient on how to prevent or reduce them. Side effects induced by anti-cancer drugs and HSCT creates certain problems for a patient and medical staff involved in care, management of which require the assistance of nursing staff and personalized approach to each patient.
Keywords
Chemotherapy, conditioning, infusion therapy, role of nurse, donor, hematopoietic stem cell transplantation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(5175) "Aim
The aim of this study is to explore the role of a nurse and the specifics of nursing care during chemotherapy, infusion therapy, hematopoietic stem cell transplantation (HSCT) and study the process of a donor preparation for the donation of a peripheral blood mononuclear cell (PMBC) concentrate.
Methods of investigation
The study is based on the HSCT protocol in acute myeloid leukemia (AML). The standard procedures included: 1. Chemotherapy (conditioning). 2. Infusion therapy. 3. Preparation of a donor. 4. HSCT.
1. Chemotherapy stage
This conditioning treatment protocol includes the following chemotherapy agents: Fludarabine, Treosulfan, Thiotepa, Actemra, Orencia. When using drugs within the conditioning treatment, the role of a nurse is to ensure the prescribed injection regimen (drug dosage and dilution, speed of injection, first aid, if necessary). A nurse should be aware of any possible complications, apply recommendations for the prevention of complications, educate patient’s parents on these recommendations. Prevention of potential complications: a) Skin: use of topical corticosteroids, moisturizing and softening creams for skin care. Daily application of cleansing lotion using disposable wash gloves. b) Mucous membranes. Use of oral antiseptic solution (gargling and irrigation); c) Gastrointestinal system: prevention of nausea and vomiting (dietary recommendations, use of antiemetics). d) Urogenital system: application of an antiseptic solution to the external genitalia for purposes of disinfection. e) Nervous system: distribution of prescribed medications which are aimed for management of anxiety, peripheral neuropathy symptoms (muscle weakness, muscle tone impairment, tremor, muscle spasm).
2. Infusion therapy
In order to provide effective and safe infusion therapy (IT) delivery it is necessary to have a detailed information on the following aspects: duration of intravenous infusions, guidelines of infusions, venous access site care and equipment maintenance. Before starting the infusion therapy, a nurse must perform an assessment of a patient (fluid balance measurement, patient’s vital signs monitoring); educate and inform a patient and her/his parents about the planned treatment.
3. Preparation of a donor
An important stage in HSCT is to prepare a donor for stem cell donation by means of cytapheresis. To obtain a peripheral blood mononuclear cell concentrate enriched in hematopoietic stem cells, a preliminary G-CSF-induced leukocyte mobilization is required. G-CSF increases WBC count and stimulates stem cell release from the bone marrow into the peripheral blood. A nurse performs subcutaneous injections of G-CSF for 5 days and registers possible uncommon side effects. At doctor’s instruction a nurse performs an injection of anesthesia, collects blood for testing and places a catheter for the infusion therapy.
4. Hematopoietic stem cell transplantation
During the treatment on the AML protocol, TCR-Alpha/Beta and CD19 depleted haploidentical stem cell transplantation is performed. The advantages of the method: TCR aplha/beta cells are removed from the graft to perform a GVHD prophylaxis. The remaining small percentage of gamma/delta T-cells induces a faster immune system recovery and, as a consequence, leads to more rapid immune reconstitution. During the procedure of transplantation, a nurse is responsible for: monitoring of patient’s vital signs; ensuring the availability of drugs for side effect management; using filters to prevent transfusion reactions and alloimmunization during transplantation. A nurse should be aware of potential complications and provide an appropriate assistance.
Conclusion
Nursing staff plays an important role in implementation of all standard procedures of treatment protocols at our Center. A nurse must guide the patient through the department and inform her/him of the treatment plan prescribed by the treating physician. She should be able to answer the patient’s questions relating to the preparation for the chemotherapy and HSCT, explain the cause of the chemotherapy-induced complications and inform the patient on how to prevent or reduce them. Side effects induced by anti-cancer drugs and HSCT creates certain problems for a patient and medical staff involved in care, management of which require the assistance of nursing staff and personalized approach to each patient.
Keywords
Chemotherapy, conditioning, infusion therapy, role of nurse, donor, hematopoietic stem cell transplantation.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20535" ["VALUE"]=> string(51) "Chemotherapy, infusion therapy: the role of a nurse" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(51) "Chemotherapy, infusion therapy: the role of a nurse" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(51) "Chemotherapy, infusion therapy: the role of a nurse" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20533" ["VALUE"]=> array(2) { ["TEXT"]=> string(121) "D. Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(121) "D. Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(121) "D. Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20529" ["VALUE"]=> array(2) { ["TEXT"]=> string(101) "Наталья П. Лещук, Андрей Б. Абросимов, Лариса Н. Шелихова" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(101) "Наталья П. Лещук, Андрей Б. Абросимов, Лариса Н. Шелихова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(101) "Наталья П. Лещук, Андрей Б. Абросимов, Лариса Н. Шелихова" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20531" ["VALUE"]=> array(2) { ["TEXT"]=> string(10691) "<h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель работы – изучить роль медицинской сестры и особенности сестринского ухода за пациентами при проведении химиотерапии, инфузионной терапии, трансплантации гемопоэтических стволовых клеток (ТГСК); изучить сестринский процесс подготовки донора к сдаче концентрата периферических мононуклеаров. </p> <h2 style="text-align: justify;">Методы исследования</h2> <p style="text-align: justify;"> За основу исследования был взят протокол ТГСК при остром миелоидном лейкозе (ОМЛ). Стандартные процедуры: 1. Химиотерапия (кондиционирование). 2. Инфузионная терапия. 3. Подготовка донора. 4. ТГСК. </p> <h3 style="text-align: justify;">1. Химиотерапия</h3> <p style="text-align: justify;"> В данный протокол кондиционирования входят следующие препараты: Флударабин, Треосульфан, Тиотепа, Актемра, Оренсия. При введении препаратов на этапе кондиционирования роль медицинской сестры заключается в правильности введения (дозировка и разведение препарата, скорость введения, при необходимости оказание экстренной помощи), знать об возможных осложнениях, применять разработанные рекомендации для профилактики осложнений, обучить родителей и контролировать их выполнение. Профилактика возможных осложнений: а) Кожные покровы. Применение топических стероидов по уходу за кожей, увлажняющих и смягчающих кремов. Ежедневное обтирание моющим лосьоном с применением одноразовых рукавиц для мытья. в) Слизистые оболочки. Использование для полоскания и орошения ротовой полости антисептических растворов; с) Желудочно-кишечный тракт. Предотвращение тошноты и рвоты (рекомендации по питанию, введение противорвотных препаратов). d) Мочеполовая система. Применение антисептических растворов для подмывания наружных половых органов для дезинфицирующего действия. e) Нервная система. По назначению врача выдача лекарственных препаратов, действие которых направлено на устранение тревожности, симптомов периферической нейропатии (мышечная слабость, нарушение мышечного тонуса, дрожание в мышцах, судороги в мышцах). </p> <h3 style="text-align: justify;">2. Инфузионная терапия</h3> <p style="text-align: justify;"> Для эффективной и безопасной инфузионной терапии (ИТ) необходимо владеть полной информацией: продолжительность внутривенных вливаний, правила проведение вливаний, уход за устройством и местом венозного доступа. При проведении инфузионной терапии медицинская сестра должна оценить состояние пациента (подсчет водного баланса, мониторинг жизненно важных функций); провести разъяснительную и просветительную беседу о планируемом лечении. </p> <h3 style="text-align: justify;">3. Подготовка донора</h3> <p style="text-align: justify;"> Важным этапом в проведении ТГСК стоит в подготовке донора стволовых клеток к сдаче материала путем цитафереза. Для получения концентрата периферических мононуклеаров, обогащенного стволовыми гемопоэтическими стволовыми клетками необходима предварительная мобилизация лейкоцитов гранулоцитарным колониестимулирующим фактором (Г-КСФ). Г-КСФ повышает количество лейкоцитов и стимулирует выход стволовых клеток из костного мозга в периферическую кровь. Медицинская сестра в течении 5 дней вводит подкожно препараты Г-КСФ и регистрирует возможные редкие побочные явления. По назначению врача медицинская сестра вводит обезболивающие, осуществляет забор крови для анализов и постановку инфузионной терапии. </p> <h3 style="text-align: justify;">4. Трансплантация гемопоэтических стволовых клеток</h3> <p style="text-align: justify;"> При лечении пациентов по протоколу с диагнозом ОМЛ проводится гаплоидентичная трансплантация гемопоэтических стволовых клеток с TCR альфа/бета и деплецией CD19+ клеток. Преимущества метода: Удалением из трансплантата TCR альфа/бета клеток осуществляется профилактика РТПХ; оставшийся небольшой процент гамма/дельта Т-клеток запускает процесс реконституции иммунной системы и, как следствие – ее более быстрое восстановление. При проведении процедуры трансплантации роль медицинской сестры заключается в следующем: проводить мониторинг жизненно важных функций; обеспечение доступности лекарственных препаратов при побочных осложнениях: для предотвращения реакций или аллоиммунизации использовать фильтры при процедуре трансплантации; медицинская сестра должна знать о возможных осложнениях и уметь оказывать необходимую помощь. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Роль медицинской сестры на протяжении всех стандартных процедур, включенных в протоколы лечения в нашем Центре, имеет огромную значимость. Медицинская сестра должна ознакомить пациента с отделением, объяснить план лечения, назначенный лечащим врачом. Она должна уметь отвечать на вопросы пациента о подготовке к проведению химиотерапии, ТГСК, объяснить, почему химиотерапия может вызывать осложнения и как можно их предотвратить или уменьшить. Развитие побочных реакций при использовании противоопухолевых препаратов и проведении ТГСК создает определенные проблемы для пациента и медицинского персонала, осуществляющего уход, требует от медицинских сестер внимания и индивидуального подхода к каждому из пациентов. </p> <h2 style="text-align: justify;">Список литературы</h2> <p style="text-align: justify;"> 1. М. А. Масчан Деплеция альфа/бета-Т-лимфоцитов – надежная платформа для развития трансплантации гемопоэтических стволовых клеток от гаплоидентичных доноров//Российский журнал детской гематологии и онкологии НОДГО. 2015. №3. С. 34-38.<br> 2. Е. В. Самочатова, А. Г. Румянцев Сестринский уход в детской гематологии и онкологии // М.: Издательство «Литтерра», 2011.-220c. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Химиотерапия, кондиционирование, инфузионная терапия, роль медицинской сестры, донор, трансплантация гемопоэтических стволовых клеток. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(10289) "Цель
Цель работы – изучить роль медицинской сестры и особенности сестринского ухода за пациентами при проведении химиотерапии, инфузионной терапии, трансплантации гемопоэтических стволовых клеток (ТГСК); изучить сестринский процесс подготовки донора к сдаче концентрата периферических мононуклеаров.
Методы исследования
За основу исследования был взят протокол ТГСК при остром миелоидном лейкозе (ОМЛ). Стандартные процедуры: 1. Химиотерапия (кондиционирование). 2. Инфузионная терапия. 3. Подготовка донора. 4. ТГСК.
1. Химиотерапия
В данный протокол кондиционирования входят следующие препараты: Флударабин, Треосульфан, Тиотепа, Актемра, Оренсия. При введении препаратов на этапе кондиционирования роль медицинской сестры заключается в правильности введения (дозировка и разведение препарата, скорость введения, при необходимости оказание экстренной помощи), знать об возможных осложнениях, применять разработанные рекомендации для профилактики осложнений, обучить родителей и контролировать их выполнение. Профилактика возможных осложнений: а) Кожные покровы. Применение топических стероидов по уходу за кожей, увлажняющих и смягчающих кремов. Ежедневное обтирание моющим лосьоном с применением одноразовых рукавиц для мытья. в) Слизистые оболочки. Использование для полоскания и орошения ротовой полости антисептических растворов; с) Желудочно-кишечный тракт. Предотвращение тошноты и рвоты (рекомендации по питанию, введение противорвотных препаратов). d) Мочеполовая система. Применение антисептических растворов для подмывания наружных половых органов для дезинфицирующего действия. e) Нервная система. По назначению врача выдача лекарственных препаратов, действие которых направлено на устранение тревожности, симптомов периферической нейропатии (мышечная слабость, нарушение мышечного тонуса, дрожание в мышцах, судороги в мышцах).
2. Инфузионная терапия
Для эффективной и безопасной инфузионной терапии (ИТ) необходимо владеть полной информацией: продолжительность внутривенных вливаний, правила проведение вливаний, уход за устройством и местом венозного доступа. При проведении инфузионной терапии медицинская сестра должна оценить состояние пациента (подсчет водного баланса, мониторинг жизненно важных функций); провести разъяснительную и просветительную беседу о планируемом лечении.
3. Подготовка донора
Важным этапом в проведении ТГСК стоит в подготовке донора стволовых клеток к сдаче материала путем цитафереза. Для получения концентрата периферических мононуклеаров, обогащенного стволовыми гемопоэтическими стволовыми клетками необходима предварительная мобилизация лейкоцитов гранулоцитарным колониестимулирующим фактором (Г-КСФ). Г-КСФ повышает количество лейкоцитов и стимулирует выход стволовых клеток из костного мозга в периферическую кровь. Медицинская сестра в течении 5 дней вводит подкожно препараты Г-КСФ и регистрирует возможные редкие побочные явления. По назначению врача медицинская сестра вводит обезболивающие, осуществляет забор крови для анализов и постановку инфузионной терапии.
4. Трансплантация гемопоэтических стволовых клеток
При лечении пациентов по протоколу с диагнозом ОМЛ проводится гаплоидентичная трансплантация гемопоэтических стволовых клеток с TCR альфа/бета и деплецией CD19+ клеток. Преимущества метода: Удалением из трансплантата TCR альфа/бета клеток осуществляется профилактика РТПХ; оставшийся небольшой процент гамма/дельта Т-клеток запускает процесс реконституции иммунной системы и, как следствие – ее более быстрое восстановление. При проведении процедуры трансплантации роль медицинской сестры заключается в следующем: проводить мониторинг жизненно важных функций; обеспечение доступности лекарственных препаратов при побочных осложнениях: для предотвращения реакций или аллоиммунизации использовать фильтры при процедуре трансплантации; медицинская сестра должна знать о возможных осложнениях и уметь оказывать необходимую помощь.
Заключение
Роль медицинской сестры на протяжении всех стандартных процедур, включенных в протоколы лечения в нашем Центре, имеет огромную значимость. Медицинская сестра должна ознакомить пациента с отделением, объяснить план лечения, назначенный лечащим врачом. Она должна уметь отвечать на вопросы пациента о подготовке к проведению химиотерапии, ТГСК, объяснить, почему химиотерапия может вызывать осложнения и как можно их предотвратить или уменьшить. Развитие побочных реакций при использовании противоопухолевых препаратов и проведении ТГСК создает определенные проблемы для пациента и медицинского персонала, осуществляющего уход, требует от медицинских сестер внимания и индивидуального подхода к каждому из пациентов.
Список литературы
1. М. А. Масчан Деплеция альфа/бета-Т-лимфоцитов – надежная платформа для развития трансплантации гемопоэтических стволовых клеток от гаплоидентичных доноров//Российский журнал детской гематологии и онкологии НОДГО. 2015. №3. С. 34-38.
2. Е. В. Самочатова, А. Г. Румянцев Сестринский уход в детской гематологии и онкологии // М.: Издательство «Литтерра», 2011.-220c.
Ключевые слова
Химиотерапия, кондиционирование, инфузионная терапия, роль медицинской сестры, донор, трансплантация гемопоэтических стволовых клеток.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(10289) "Цель
Цель работы – изучить роль медицинской сестры и особенности сестринского ухода за пациентами при проведении химиотерапии, инфузионной терапии, трансплантации гемопоэтических стволовых клеток (ТГСК); изучить сестринский процесс подготовки донора к сдаче концентрата периферических мононуклеаров.
Методы исследования
За основу исследования был взят протокол ТГСК при остром миелоидном лейкозе (ОМЛ). Стандартные процедуры: 1. Химиотерапия (кондиционирование). 2. Инфузионная терапия. 3. Подготовка донора. 4. ТГСК.
1. Химиотерапия
В данный протокол кондиционирования входят следующие препараты: Флударабин, Треосульфан, Тиотепа, Актемра, Оренсия. При введении препаратов на этапе кондиционирования роль медицинской сестры заключается в правильности введения (дозировка и разведение препарата, скорость введения, при необходимости оказание экстренной помощи), знать об возможных осложнениях, применять разработанные рекомендации для профилактики осложнений, обучить родителей и контролировать их выполнение. Профилактика возможных осложнений: а) Кожные покровы. Применение топических стероидов по уходу за кожей, увлажняющих и смягчающих кремов. Ежедневное обтирание моющим лосьоном с применением одноразовых рукавиц для мытья. в) Слизистые оболочки. Использование для полоскания и орошения ротовой полости антисептических растворов; с) Желудочно-кишечный тракт. Предотвращение тошноты и рвоты (рекомендации по питанию, введение противорвотных препаратов). d) Мочеполовая система. Применение антисептических растворов для подмывания наружных половых органов для дезинфицирующего действия. e) Нервная система. По назначению врача выдача лекарственных препаратов, действие которых направлено на устранение тревожности, симптомов периферической нейропатии (мышечная слабость, нарушение мышечного тонуса, дрожание в мышцах, судороги в мышцах).
2. Инфузионная терапия
Для эффективной и безопасной инфузионной терапии (ИТ) необходимо владеть полной информацией: продолжительность внутривенных вливаний, правила проведение вливаний, уход за устройством и местом венозного доступа. При проведении инфузионной терапии медицинская сестра должна оценить состояние пациента (подсчет водного баланса, мониторинг жизненно важных функций); провести разъяснительную и просветительную беседу о планируемом лечении.
3. Подготовка донора
Важным этапом в проведении ТГСК стоит в подготовке донора стволовых клеток к сдаче материала путем цитафереза. Для получения концентрата периферических мононуклеаров, обогащенного стволовыми гемопоэтическими стволовыми клетками необходима предварительная мобилизация лейкоцитов гранулоцитарным колониестимулирующим фактором (Г-КСФ). Г-КСФ повышает количество лейкоцитов и стимулирует выход стволовых клеток из костного мозга в периферическую кровь. Медицинская сестра в течении 5 дней вводит подкожно препараты Г-КСФ и регистрирует возможные редкие побочные явления. По назначению врача медицинская сестра вводит обезболивающие, осуществляет забор крови для анализов и постановку инфузионной терапии.
4. Трансплантация гемопоэтических стволовых клеток
При лечении пациентов по протоколу с диагнозом ОМЛ проводится гаплоидентичная трансплантация гемопоэтических стволовых клеток с TCR альфа/бета и деплецией CD19+ клеток. Преимущества метода: Удалением из трансплантата TCR альфа/бета клеток осуществляется профилактика РТПХ; оставшийся небольшой процент гамма/дельта Т-клеток запускает процесс реконституции иммунной системы и, как следствие – ее более быстрое восстановление. При проведении процедуры трансплантации роль медицинской сестры заключается в следующем: проводить мониторинг жизненно важных функций; обеспечение доступности лекарственных препаратов при побочных осложнениях: для предотвращения реакций или аллоиммунизации использовать фильтры при процедуре трансплантации; медицинская сестра должна знать о возможных осложнениях и уметь оказывать необходимую помощь.
Заключение
Роль медицинской сестры на протяжении всех стандартных процедур, включенных в протоколы лечения в нашем Центре, имеет огромную значимость. Медицинская сестра должна ознакомить пациента с отделением, объяснить план лечения, назначенный лечащим врачом. Она должна уметь отвечать на вопросы пациента о подготовке к проведению химиотерапии, ТГСК, объяснить, почему химиотерапия может вызывать осложнения и как можно их предотвратить или уменьшить. Развитие побочных реакций при использовании противоопухолевых препаратов и проведении ТГСК создает определенные проблемы для пациента и медицинского персонала, осуществляющего уход, требует от медицинских сестер внимания и индивидуального подхода к каждому из пациентов.
Список литературы
1. М. А. Масчан Деплеция альфа/бета-Т-лимфоцитов – надежная платформа для развития трансплантации гемопоэтических стволовых клеток от гаплоидентичных доноров//Российский журнал детской гематологии и онкологии НОДГО. 2015. №3. С. 34-38.
2. Е. В. Самочатова, А. Г. Румянцев Сестринский уход в детской гематологии и онкологии // М.: Издательство «Литтерра», 2011.-220c.
Ключевые слова
Химиотерапия, кондиционирование, инфузионная терапия, роль медицинской сестры, донор, трансплантация гемопоэтических стволовых клеток.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20530" ["VALUE"]=> array(2) { ["TEXT"]=> string(128) "ФГБУ «НМИЦ ДГОИ имени Дмитрия Рогачева», Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(128) "ФГБУ «НМИЦ ДГОИ имени Дмитрия Рогачева», Москва, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(128) "ФГБУ «НМИЦ ДГОИ имени Дмитрия Рогачева», Москва, Российская Федерация" } } } [28]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1594" ["~ID"]=> string(4) "1594" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(338) "Сравнение поздних осложнений треосульфан- и бусульфан-содержащих миелоаблативных режимов кондиционирования при аллогенных трансплантациях гемопоэтических стволовых клеток у детей" ["~NAME"]=> string(338) "Сравнение поздних осложнений треосульфан- и бусульфан-содержащих миелоаблативных режимов кондиционирования при аллогенных трансплантациях гемопоэтических стволовых клеток у детей" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:46:01" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:46:01" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/sravnenie-pozdnikh-oslozhneniy-treosulfan-i-busulfan-soderzhashchikh-mieloablativnykh-rezhimov-kondi/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/sravnenie-pozdnikh-oslozhneniy-treosulfan-i-busulfan-soderzhashchikh-mieloablativnykh-rezhimov-kondi/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "sravnenie-pozdnikh-oslozhneniy-treosulfan-i-busulfan-soderzhashchikh-mieloablativnykh-rezhimov-kondi" ["~CODE"]=> string(100) "sravnenie-pozdnikh-oslozhneniy-treosulfan-i-busulfan-soderzhashchikh-mieloablativnykh-rezhimov-kondi" ["EXTERNAL_ID"]=> string(4) "1594" ["~EXTERNAL_ID"]=> string(4) "1594" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(338) "Сравнение поздних осложнений треосульфан- и бусульфан-содержащих миелоаблативных режимов кондиционирования при аллогенных трансплантациях гемопоэтических стволовых клеток у детей" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(514) "Сравнение поздних осложнений треосульфан- и бусульфан-содержащих миелоаблативных режимов кондиционирования при аллогенных трансплантациях гемопоэтических стволовых клеток у детейComparative analysis of late effects after treosulfan- and busulfan-based myeloablative conditioning regimens for allogeneic hematopoietic stem cell transplantation in children" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(6906) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Треосульфан активно используется в качестве миелоаблативного и иммуносупрессивного компонента современных режимов кондиционирования, что позволяет снизить раннюю токсичность аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Однако, отсутствуют данные о его поздних эффектах. Целью исследования явилось ретроспективное изучение поздних осложнений при проведении треосульфани бусульфан-содержащих миелоаблативных режимов кондиционирования у детей. </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> Проведен сравнительный анализ поздних осложнений у детей, получивших алло-ТГСК на базе отделения трансплантации костного мозга Российской детской клинической больницы (РДКБ)/Национального медицинского исследовательского центра детской гематологии, онкологии и иммунологии им. Дм. Рогачева (НМИЦ ДГОИ) (г. Москва, Россия) с 1994 по 2011 гг., имевших бусульфан- (группа 1, n=110, медиана наблюдения 7,4 г.) или треосульфан-содержащее (группа 2, n=38, медиана наблюдения 5,7 г.) кондиционирование и проживших минимум 1 г. от момента ТГСК. Учитывая различие в медианах наблюдения, статистический анализ проводили на сроке 5 лет от момента алло-ТГСК для обеих групп. Оценивали развитие хронической РТПХ, патологии эндокринной, нервной, сердечно-сосудистой систем, снижение костной минеральной плотности, развитие вторичных злокачественных заболеваний. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Пациенты с гемобластозами (105 в группе с бусульфаном и 30 в группе с треосульфаном) имели схожие показатели 5-летней выживаемости: общая выживаемость в 1-й и 2-й группах составила 79,3% и 66,1%, а безрецидивная выживаемость – 82,5% и 74,1%, соответственно. Частота хронической РТПХ – 57% в группе с треосульфаном и 50% в группе с бусульфаном. Кумулятивный риск развития экстенсивной хронической РТПХ составил 27,6% в 1-й группе и 43,3% во 2-й группе. При анализе других поздних осложнений обнаружено снижение частоты развития эндокринных нарушений в группе с треосульфаном – 27% против 43% в 1-й группе, при этом не зарегистрировано ни одного случая развития гипергонадотропного гипогонадизма (кумулятивный риск развития 32,8% в 1-й группе против 0% во 2-й, р = 0,012). Патология щитовидной железы в структуре эндокринных нарушений также преобладала в 1-й группе детей – 29% против 13%. Патология центральной нервной системы в группе с треосульфаном носила в большей степени функциональный характер в отличие от преобладания органических нарушений в 1-й группе: не зарегистрировано ни одного случая энцефалопатии, вторичной эпилепсии. Также отмечались качественные различия в развитии кардиоваскулярной патологии – 16% в 1-й группе с преобладанием вторичной кардиомиопатии против 10% во 2-й группе. В обеих группах зарегистрировано по одному случаю вторичных неоплазий на поздних сроках после ТГСК. Cреди детей с незлокачественными заболеваниями (первичными иммунодефицитами) 5 получили бусульфан-содержащее кондиционирование, а 8 – треосульфан-содержащее. Общая 5-летняя выживаемость составила 87,5% в 1-й группе против 60% во 2-й. Существенных различий в частоте поздних осложнений алло-ТГСК не выявлено. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Треосульфан-содержащее миелоаблативное кондиционирование позволяет снизить риск развития поздних осложнений со стороны эндокринной системы (особенно гипогонадизма), центральной нервной системы и кардиоваскулярных нарушений после алло-ТГСК у детей по сравнению с классическими бусульфан-содержащими режимами. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Алло-ТГСК, кондиционирование, треосульфан, поздние осложнения, дети. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(338) "Сравнение поздних осложнений треосульфан- и бусульфан-содержащих миелоаблативных режимов кондиционирования при аллогенных трансплантациях гемопоэтических стволовых клеток у детей" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(338) "Сравнение поздних осложнений треосульфан- и бусульфан-содержащих миелоаблативных режимов кондиционирования при аллогенных трансплантациях гемопоэтических стволовых клеток у детей" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(338) "Сравнение поздних осложнений треосульфан- и бусульфан-содержащих миелоаблативных режимов кондиционирования при аллогенных трансплантациях гемопоэтических стволовых клеток у детей" ["SECTION_META_TITLE"]=> string(338) "Сравнение поздних осложнений треосульфан- и бусульфан-содержащих миелоаблативных режимов кондиционирования при аллогенных трансплантациях гемопоэтических стволовых клеток у детей" ["SECTION_META_KEYWORDS"]=> string(338) "Сравнение поздних осложнений треосульфан- и бусульфан-содержащих миелоаблативных режимов кондиционирования при аллогенных трансплантациях гемопоэтических стволовых клеток у детей" ["SECTION_META_DESCRIPTION"]=> string(338) "Сравнение поздних осложнений треосульфан- и бусульфан-содержащих миелоаблативных режимов кондиционирования при аллогенных трансплантациях гемопоэтических стволовых клеток у детей" ["SECTION_PICTURE_FILE_ALT"]=> string(338) "Сравнение поздних осложнений треосульфан- и бусульфан-содержащих миелоаблативных режимов кондиционирования при аллогенных трансплантациях гемопоэтических стволовых клеток у детей" ["SECTION_PICTURE_FILE_TITLE"]=> string(338) "Сравнение поздних осложнений треосульфан- и бусульфан-содержащих миелоаблативных режимов кондиционирования при аллогенных трансплантациях гемопоэтических стволовых клеток у детей" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "sravnenie-pozdnikh-oslozhneniy-treosulfan-i-busulfan-soderzhashchikh-mieloablativnykh-rezhimov-kondi" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(338) "Сравнение поздних осложнений треосульфан- и бусульфан-содержащих миелоаблативных режимов кондиционирования при аллогенных трансплантациях гемопоэтических стволовых клеток у детей" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(338) "Сравнение поздних осложнений треосульфан- и бусульфан-содержащих миелоаблативных режимов кондиционирования при аллогенных трансплантациях гемопоэтических стволовых клеток у детей" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "sravnenie-pozdnikh-oslozhneniy-treosulfan-i-busulfan-soderzhashchikh-mieloablativnykh-rezhimov-kondi" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "sravnenie-pozdnikh-oslozhneniy-treosulfan-i-busulfan-soderzhashchikh-mieloablativnykh-rezhimov-kondi" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "sravnenie-pozdnikh-oslozhneniy-treosulfan-i-busulfan-soderzhashchikh-mieloablativnykh-rezhimov-kondi" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20662" ["VALUE"]=> array(2) { ["TEXT"]=> string(710) "Юлия В. Скворцова <sup>1</sup>, Ирина П. Шипицына <sup>1</sup>, Дмитрий Н. Балашов <sup>1</sup>, Павел Е. Трахтман <sup>1</sup>, Елена В. Скоробогатова <sup>2</sup>, Людмила И. Папуша <sup>1</sup>, Елена И. Гутовская <sup>1</sup>, Лариса Н. Шелихова <sup>1</sup>, Елена Е. Курникова <sup>1</sup>, Кирилл А. Воронин <sup>1</sup>, Михаил А. Масчан <sup>1</sup>, Алексей А. Масчан <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(566) "Юлия В. Скворцова 1, Ирина П. Шипицына 1, Дмитрий Н. Балашов 1, Павел Е. Трахтман 1, Елена В. Скоробогатова 2, Людмила И. Папуша 1, Елена И. Гутовская 1, Лариса Н. Шелихова 1, Елена Е. Курникова 1, Кирилл А. Воронин 1, Михаил А. Масчан 1, Алексей А. Масчан 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20663" ["VALUE"]=> array(2) { ["TEXT"]=> string(393) "<sup>1</sup> ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» МЗ РФ <sup>2</sup> ФГБУ «Российская детская клиническая больница» МЗ РФ" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(369) "1 ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» МЗ РФ 2 ФГБУ «Российская детская клиническая больница» МЗ РФ" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20664" ["VALUE"]=> array(2) { ["TEXT"]=> string(6906) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Треосульфан активно используется в качестве миелоаблативного и иммуносупрессивного компонента современных режимов кондиционирования, что позволяет снизить раннюю токсичность аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Однако, отсутствуют данные о его поздних эффектах. Целью исследования явилось ретроспективное изучение поздних осложнений при проведении треосульфани бусульфан-содержащих миелоаблативных режимов кондиционирования у детей. </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> Проведен сравнительный анализ поздних осложнений у детей, получивших алло-ТГСК на базе отделения трансплантации костного мозга Российской детской клинической больницы (РДКБ)/Национального медицинского исследовательского центра детской гематологии, онкологии и иммунологии им. Дм. Рогачева (НМИЦ ДГОИ) (г. Москва, Россия) с 1994 по 2011 гг., имевших бусульфан- (группа 1, n=110, медиана наблюдения 7,4 г.) или треосульфан-содержащее (группа 2, n=38, медиана наблюдения 5,7 г.) кондиционирование и проживших минимум 1 г. от момента ТГСК. Учитывая различие в медианах наблюдения, статистический анализ проводили на сроке 5 лет от момента алло-ТГСК для обеих групп. Оценивали развитие хронической РТПХ, патологии эндокринной, нервной, сердечно-сосудистой систем, снижение костной минеральной плотности, развитие вторичных злокачественных заболеваний. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Пациенты с гемобластозами (105 в группе с бусульфаном и 30 в группе с треосульфаном) имели схожие показатели 5-летней выживаемости: общая выживаемость в 1-й и 2-й группах составила 79,3% и 66,1%, а безрецидивная выживаемость – 82,5% и 74,1%, соответственно. Частота хронической РТПХ – 57% в группе с треосульфаном и 50% в группе с бусульфаном. Кумулятивный риск развития экстенсивной хронической РТПХ составил 27,6% в 1-й группе и 43,3% во 2-й группе. При анализе других поздних осложнений обнаружено снижение частоты развития эндокринных нарушений в группе с треосульфаном – 27% против 43% в 1-й группе, при этом не зарегистрировано ни одного случая развития гипергонадотропного гипогонадизма (кумулятивный риск развития 32,8% в 1-й группе против 0% во 2-й, р = 0,012). Патология щитовидной железы в структуре эндокринных нарушений также преобладала в 1-й группе детей – 29% против 13%. Патология центральной нервной системы в группе с треосульфаном носила в большей степени функциональный характер в отличие от преобладания органических нарушений в 1-й группе: не зарегистрировано ни одного случая энцефалопатии, вторичной эпилепсии. Также отмечались качественные различия в развитии кардиоваскулярной патологии – 16% в 1-й группе с преобладанием вторичной кардиомиопатии против 10% во 2-й группе. В обеих группах зарегистрировано по одному случаю вторичных неоплазий на поздних сроках после ТГСК. Cреди детей с незлокачественными заболеваниями (первичными иммунодефицитами) 5 получили бусульфан-содержащее кондиционирование, а 8 – треосульфан-содержащее. Общая 5-летняя выживаемость составила 87,5% в 1-й группе против 60% во 2-й. Существенных различий в частоте поздних осложнений алло-ТГСК не выявлено. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Треосульфан-содержащее миелоаблативное кондиционирование позволяет снизить риск развития поздних осложнений со стороны эндокринной системы (особенно гипогонадизма), центральной нервной системы и кардиоваскулярных нарушений после алло-ТГСК у детей по сравнению с классическими бусульфан-содержащими режимами. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Алло-ТГСК, кондиционирование, треосульфан, поздние осложнения, дети. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6674) "Введение
Треосульфан активно используется в качестве миелоаблативного и иммуносупрессивного компонента современных режимов кондиционирования, что позволяет снизить раннюю токсичность аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Однако, отсутствуют данные о его поздних эффектах. Целью исследования явилось ретроспективное изучение поздних осложнений при проведении треосульфани бусульфан-содержащих миелоаблативных режимов кондиционирования у детей.
Методы
Проведен сравнительный анализ поздних осложнений у детей, получивших алло-ТГСК на базе отделения трансплантации костного мозга Российской детской клинической больницы (РДКБ)/Национального медицинского исследовательского центра детской гематологии, онкологии и иммунологии им. Дм. Рогачева (НМИЦ ДГОИ) (г. Москва, Россия) с 1994 по 2011 гг., имевших бусульфан- (группа 1, n=110, медиана наблюдения 7,4 г.) или треосульфан-содержащее (группа 2, n=38, медиана наблюдения 5,7 г.) кондиционирование и проживших минимум 1 г. от момента ТГСК. Учитывая различие в медианах наблюдения, статистический анализ проводили на сроке 5 лет от момента алло-ТГСК для обеих групп. Оценивали развитие хронической РТПХ, патологии эндокринной, нервной, сердечно-сосудистой систем, снижение костной минеральной плотности, развитие вторичных злокачественных заболеваний.
Результаты
Пациенты с гемобластозами (105 в группе с бусульфаном и 30 в группе с треосульфаном) имели схожие показатели 5-летней выживаемости: общая выживаемость в 1-й и 2-й группах составила 79,3% и 66,1%, а безрецидивная выживаемость – 82,5% и 74,1%, соответственно. Частота хронической РТПХ – 57% в группе с треосульфаном и 50% в группе с бусульфаном. Кумулятивный риск развития экстенсивной хронической РТПХ составил 27,6% в 1-й группе и 43,3% во 2-й группе. При анализе других поздних осложнений обнаружено снижение частоты развития эндокринных нарушений в группе с треосульфаном – 27% против 43% в 1-й группе, при этом не зарегистрировано ни одного случая развития гипергонадотропного гипогонадизма (кумулятивный риск развития 32,8% в 1-й группе против 0% во 2-й, р = 0,012). Патология щитовидной железы в структуре эндокринных нарушений также преобладала в 1-й группе детей – 29% против 13%. Патология центральной нервной системы в группе с треосульфаном носила в большей степени функциональный характер в отличие от преобладания органических нарушений в 1-й группе: не зарегистрировано ни одного случая энцефалопатии, вторичной эпилепсии. Также отмечались качественные различия в развитии кардиоваскулярной патологии – 16% в 1-й группе с преобладанием вторичной кардиомиопатии против 10% во 2-й группе. В обеих группах зарегистрировано по одному случаю вторичных неоплазий на поздних сроках после ТГСК. Cреди детей с незлокачественными заболеваниями (первичными иммунодефицитами) 5 получили бусульфан-содержащее кондиционирование, а 8 – треосульфан-содержащее. Общая 5-летняя выживаемость составила 87,5% в 1-й группе против 60% во 2-й. Существенных различий в частоте поздних осложнений алло-ТГСК не выявлено.
Заключение
Треосульфан-содержащее миелоаблативное кондиционирование позволяет снизить риск развития поздних осложнений со стороны эндокринной системы (особенно гипогонадизма), центральной нервной системы и кардиоваскулярных нарушений после алло-ТГСК у детей по сравнению с классическими бусульфан-содержащими режимами.
Ключевые слова
Алло-ТГСК, кондиционирование, треосульфан, поздние осложнения, дети.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20665" ["VALUE"]=> array(2) { ["TEXT"]=> string(546) "Yulia V. Skvortsova <sup>1</sup>, Irina P. Shipitsina <sup>1</sup>, Dmitrij N. Balashov <sup>1</sup>, Pavel E. Trakhtman <sup>1</sup>, Elena V. Skorobogatova <sup>2</sup>, Ludmila I. Papusha <sup>1</sup>, Elena I. Gutovskaya <sup>1</sup>, Larisa N. Shelikhova <sup>1</sup>, Elena E. Kurnikova <sup>1</sup>, Kirill A. Voronin <sup>1</sup>, Michael A. Maschan <sup>1</sup>, Alexei A. Maschan <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(402) "Yulia V. Skvortsova 1, Irina P. Shipitsina 1, Dmitrij N. Balashov 1, Pavel E. Trakhtman 1, Elena V. Skorobogatova 2, Ludmila I. Papusha 1, Elena I. Gutovskaya 1, Larisa N. Shelikhova 1, Elena E. Kurnikova 1, Kirill A. Voronin 1, Michael A. Maschan 1, Alexei A. Maschan 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20666" ["VALUE"]=> array(2) { ["TEXT"]=> string(227) "<sup>1</sup> Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology (Moscow, Russian Federation) <sup>2</sup> Russian Children’s Hospital, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(203) "1 Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology (Moscow, Russian Federation) 2 Russian Children’s Hospital, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20667" ["VALUE"]=> array(2) { ["TEXT"]=> string(3647) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Treosulfan is actively used as myeloablative and immunosuppressive agent in modern conditioning regimens, while exhibiting a reduced early toxicity in the setting of allogeneic hematopoietic stem cell transplantation (allo-HSCT). But there are no data about long-term effects. The aim of this study was retrospective analysis of late effects after treosulfan-and busulfan-based myeloablative conditioning regimens in children. </p> <h2 style="text-align: justify;">Methods</h2> <p style="text-align: justify;"> We propose a comparative analysis of late effects in children, who got allo-HSCT at BMT Department of Russian Children’s Hospital/Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology (Moscow, Russia) between 2004 and 2011 with busulfan- (group 1, n=110, median follow-up 7.4 yrs) or treosulfan-based (group 2, n=38, median follow-up 5.7 yrs) and survived at least 1 year after HSCT. The statistical analysis was carried out for the median period of 5 years after allo-HSCT for both groups. Chronic graft-versus-host disease (GVHD), pathology of endocrine, nervous, cardiovascular systems, bone mineral turnover and secondary malignancies were studied. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Patients with malignant diseases (105 in busulfan group and 30 in treosulfan group) had similar 5-year survival results: overall survival in 1st and 2nd groups were 79.3% and 66.1%, relapse-free survival – 82.5% and 74.1%, respectively. Chronic GVHD incidence was 57% in treosulfan group and 50% in busulfan group. Cumulative incidence (CI) of chronic extensive GVHD was 27.6% in group 1 and 43.3% in group 2. The analysis of other late effects revealed the reduction of endocrine complications in treosulfan group, 27% against 43% in the 1st group, none had hypergonadotropic hypogonadism (CI 32.8% in group 1 opposite to 0% in group 2, р = 0.012). Thyroid gland pathology dominated in group 1 – 29% opposite to 13% in group 2. Central nervous system pathology in treosulfan group was functional unlike predominance of organic impairment in group 1: no cases of encephalopathy or secondary epilepsy were registered. Differences in cardiovascular complications incidence were revealed, i.e., 16% in group 1 with secondary cardiomyopathy predominance in contrast with 10% in group 2. Both groups demonstrated one case of secondary neoplasms after a long follow-up period. Among patients with nonmalignant disorders (primary immunodeficiencies), 5 got busulfan-based conditioning and 8 received treosulfan-based treatment. Overall 5-year survival was 87.5% in group 1 and 60% in group 2. No significant differences in late effects after allo-HSCT were revealed. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Treosulfan-based myeloablative conditioning allows to reduce incidence of late endocrine complications (especially, hypogonadism), central nervous system and cardiovascular system pathology after allogeneic HSCT in children when compared with classical busulfan-based conditioning regimens. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Allogeneic HSCT, conditioning, treosulfan, late complications, children. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3415) "Introduction
Treosulfan is actively used as myeloablative and immunosuppressive agent in modern conditioning regimens, while exhibiting a reduced early toxicity in the setting of allogeneic hematopoietic stem cell transplantation (allo-HSCT). But there are no data about long-term effects. The aim of this study was retrospective analysis of late effects after treosulfan-and busulfan-based myeloablative conditioning regimens in children.
Methods
We propose a comparative analysis of late effects in children, who got allo-HSCT at BMT Department of Russian Children’s Hospital/Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology (Moscow, Russia) between 2004 and 2011 with busulfan- (group 1, n=110, median follow-up 7.4 yrs) or treosulfan-based (group 2, n=38, median follow-up 5.7 yrs) and survived at least 1 year after HSCT. The statistical analysis was carried out for the median period of 5 years after allo-HSCT for both groups. Chronic graft-versus-host disease (GVHD), pathology of endocrine, nervous, cardiovascular systems, bone mineral turnover and secondary malignancies were studied.
Results
Patients with malignant diseases (105 in busulfan group and 30 in treosulfan group) had similar 5-year survival results: overall survival in 1st and 2nd groups were 79.3% and 66.1%, relapse-free survival – 82.5% and 74.1%, respectively. Chronic GVHD incidence was 57% in treosulfan group and 50% in busulfan group. Cumulative incidence (CI) of chronic extensive GVHD was 27.6% in group 1 and 43.3% in group 2. The analysis of other late effects revealed the reduction of endocrine complications in treosulfan group, 27% against 43% in the 1st group, none had hypergonadotropic hypogonadism (CI 32.8% in group 1 opposite to 0% in group 2, р = 0.012). Thyroid gland pathology dominated in group 1 – 29% opposite to 13% in group 2. Central nervous system pathology in treosulfan group was functional unlike predominance of organic impairment in group 1: no cases of encephalopathy or secondary epilepsy were registered. Differences in cardiovascular complications incidence were revealed, i.e., 16% in group 1 with secondary cardiomyopathy predominance in contrast with 10% in group 2. Both groups demonstrated one case of secondary neoplasms after a long follow-up period. Among patients with nonmalignant disorders (primary immunodeficiencies), 5 got busulfan-based conditioning and 8 received treosulfan-based treatment. Overall 5-year survival was 87.5% in group 1 and 60% in group 2. No significant differences in late effects after allo-HSCT were revealed.
Conclusion
Treosulfan-based myeloablative conditioning allows to reduce incidence of late endocrine complications (especially, hypogonadism), central nervous system and cardiovascular system pathology after allogeneic HSCT in children when compared with classical busulfan-based conditioning regimens.
Keywords
Allogeneic HSCT, conditioning, treosulfan, late complications, children.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20668" ["VALUE"]=> string(176) "Comparative analysis of late effects after treosulfan- and busulfan-based myeloablative conditioning regimens for allogeneic hematopoietic stem cell transplantation in children" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(176) "Comparative analysis of late effects after treosulfan- and busulfan-based myeloablative conditioning regimens for allogeneic hematopoietic stem cell transplantation in children" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20823" ["VALUE"]=> string(4) "1461" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1461" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20824" ["VALUE"]=> string(4) "1462" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1462" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20665" ["VALUE"]=> array(2) { ["TEXT"]=> string(546) "Yulia V. Skvortsova <sup>1</sup>, Irina P. Shipitsina <sup>1</sup>, Dmitrij N. Balashov <sup>1</sup>, Pavel E. Trakhtman <sup>1</sup>, Elena V. Skorobogatova <sup>2</sup>, Ludmila I. Papusha <sup>1</sup>, Elena I. Gutovskaya <sup>1</sup>, Larisa N. Shelikhova <sup>1</sup>, Elena E. Kurnikova <sup>1</sup>, Kirill A. Voronin <sup>1</sup>, Michael A. Maschan <sup>1</sup>, Alexei A. Maschan <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(402) "Yulia V. Skvortsova 1, Irina P. Shipitsina 1, Dmitrij N. Balashov 1, Pavel E. Trakhtman 1, Elena V. Skorobogatova 2, Ludmila I. Papusha 1, Elena I. Gutovskaya 1, Larisa N. Shelikhova 1, Elena E. Kurnikova 1, Kirill A. Voronin 1, Michael A. Maschan 1, Alexei A. Maschan 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(402) "Yulia V. Skvortsova 1, Irina P. Shipitsina 1, Dmitrij N. Balashov 1, Pavel E. Trakhtman 1, Elena V. Skorobogatova 2, Ludmila I. Papusha 1, Elena I. Gutovskaya 1, Larisa N. Shelikhova 1, Elena E. Kurnikova 1, Kirill A. Voronin 1, Michael A. Maschan 1, Alexei A. Maschan 1" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20667" ["VALUE"]=> array(2) { ["TEXT"]=> string(3647) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Treosulfan is actively used as myeloablative and immunosuppressive agent in modern conditioning regimens, while exhibiting a reduced early toxicity in the setting of allogeneic hematopoietic stem cell transplantation (allo-HSCT). But there are no data about long-term effects. The aim of this study was retrospective analysis of late effects after treosulfan-and busulfan-based myeloablative conditioning regimens in children. </p> <h2 style="text-align: justify;">Methods</h2> <p style="text-align: justify;"> We propose a comparative analysis of late effects in children, who got allo-HSCT at BMT Department of Russian Children’s Hospital/Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology (Moscow, Russia) between 2004 and 2011 with busulfan- (group 1, n=110, median follow-up 7.4 yrs) or treosulfan-based (group 2, n=38, median follow-up 5.7 yrs) and survived at least 1 year after HSCT. The statistical analysis was carried out for the median period of 5 years after allo-HSCT for both groups. Chronic graft-versus-host disease (GVHD), pathology of endocrine, nervous, cardiovascular systems, bone mineral turnover and secondary malignancies were studied. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Patients with malignant diseases (105 in busulfan group and 30 in treosulfan group) had similar 5-year survival results: overall survival in 1st and 2nd groups were 79.3% and 66.1%, relapse-free survival – 82.5% and 74.1%, respectively. Chronic GVHD incidence was 57% in treosulfan group and 50% in busulfan group. Cumulative incidence (CI) of chronic extensive GVHD was 27.6% in group 1 and 43.3% in group 2. The analysis of other late effects revealed the reduction of endocrine complications in treosulfan group, 27% against 43% in the 1st group, none had hypergonadotropic hypogonadism (CI 32.8% in group 1 opposite to 0% in group 2, р = 0.012). Thyroid gland pathology dominated in group 1 – 29% opposite to 13% in group 2. Central nervous system pathology in treosulfan group was functional unlike predominance of organic impairment in group 1: no cases of encephalopathy or secondary epilepsy were registered. Differences in cardiovascular complications incidence were revealed, i.e., 16% in group 1 with secondary cardiomyopathy predominance in contrast with 10% in group 2. Both groups demonstrated one case of secondary neoplasms after a long follow-up period. Among patients with nonmalignant disorders (primary immunodeficiencies), 5 got busulfan-based conditioning and 8 received treosulfan-based treatment. Overall 5-year survival was 87.5% in group 1 and 60% in group 2. No significant differences in late effects after allo-HSCT were revealed. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Treosulfan-based myeloablative conditioning allows to reduce incidence of late endocrine complications (especially, hypogonadism), central nervous system and cardiovascular system pathology after allogeneic HSCT in children when compared with classical busulfan-based conditioning regimens. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Allogeneic HSCT, conditioning, treosulfan, late complications, children. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3415) "Introduction
Treosulfan is actively used as myeloablative and immunosuppressive agent in modern conditioning regimens, while exhibiting a reduced early toxicity in the setting of allogeneic hematopoietic stem cell transplantation (allo-HSCT). But there are no data about long-term effects. The aim of this study was retrospective analysis of late effects after treosulfan-and busulfan-based myeloablative conditioning regimens in children.
Methods
We propose a comparative analysis of late effects in children, who got allo-HSCT at BMT Department of Russian Children’s Hospital/Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology (Moscow, Russia) between 2004 and 2011 with busulfan- (group 1, n=110, median follow-up 7.4 yrs) or treosulfan-based (group 2, n=38, median follow-up 5.7 yrs) and survived at least 1 year after HSCT. The statistical analysis was carried out for the median period of 5 years after allo-HSCT for both groups. Chronic graft-versus-host disease (GVHD), pathology of endocrine, nervous, cardiovascular systems, bone mineral turnover and secondary malignancies were studied.
Results
Patients with malignant diseases (105 in busulfan group and 30 in treosulfan group) had similar 5-year survival results: overall survival in 1st and 2nd groups were 79.3% and 66.1%, relapse-free survival – 82.5% and 74.1%, respectively. Chronic GVHD incidence was 57% in treosulfan group and 50% in busulfan group. Cumulative incidence (CI) of chronic extensive GVHD was 27.6% in group 1 and 43.3% in group 2. The analysis of other late effects revealed the reduction of endocrine complications in treosulfan group, 27% against 43% in the 1st group, none had hypergonadotropic hypogonadism (CI 32.8% in group 1 opposite to 0% in group 2, р = 0.012). Thyroid gland pathology dominated in group 1 – 29% opposite to 13% in group 2. Central nervous system pathology in treosulfan group was functional unlike predominance of organic impairment in group 1: no cases of encephalopathy or secondary epilepsy were registered. Differences in cardiovascular complications incidence were revealed, i.e., 16% in group 1 with secondary cardiomyopathy predominance in contrast with 10% in group 2. Both groups demonstrated one case of secondary neoplasms after a long follow-up period. Among patients with nonmalignant disorders (primary immunodeficiencies), 5 got busulfan-based conditioning and 8 received treosulfan-based treatment. Overall 5-year survival was 87.5% in group 1 and 60% in group 2. No significant differences in late effects after allo-HSCT were revealed.
Conclusion
Treosulfan-based myeloablative conditioning allows to reduce incidence of late endocrine complications (especially, hypogonadism), central nervous system and cardiovascular system pathology after allogeneic HSCT in children when compared with classical busulfan-based conditioning regimens.
Keywords
Allogeneic HSCT, conditioning, treosulfan, late complications, children.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3415) "Introduction
Treosulfan is actively used as myeloablative and immunosuppressive agent in modern conditioning regimens, while exhibiting a reduced early toxicity in the setting of allogeneic hematopoietic stem cell transplantation (allo-HSCT). But there are no data about long-term effects. The aim of this study was retrospective analysis of late effects after treosulfan-and busulfan-based myeloablative conditioning regimens in children.
Methods
We propose a comparative analysis of late effects in children, who got allo-HSCT at BMT Department of Russian Children’s Hospital/Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology (Moscow, Russia) between 2004 and 2011 with busulfan- (group 1, n=110, median follow-up 7.4 yrs) or treosulfan-based (group 2, n=38, median follow-up 5.7 yrs) and survived at least 1 year after HSCT. The statistical analysis was carried out for the median period of 5 years after allo-HSCT for both groups. Chronic graft-versus-host disease (GVHD), pathology of endocrine, nervous, cardiovascular systems, bone mineral turnover and secondary malignancies were studied.
Results
Patients with malignant diseases (105 in busulfan group and 30 in treosulfan group) had similar 5-year survival results: overall survival in 1st and 2nd groups were 79.3% and 66.1%, relapse-free survival – 82.5% and 74.1%, respectively. Chronic GVHD incidence was 57% in treosulfan group and 50% in busulfan group. Cumulative incidence (CI) of chronic extensive GVHD was 27.6% in group 1 and 43.3% in group 2. The analysis of other late effects revealed the reduction of endocrine complications in treosulfan group, 27% against 43% in the 1st group, none had hypergonadotropic hypogonadism (CI 32.8% in group 1 opposite to 0% in group 2, р = 0.012). Thyroid gland pathology dominated in group 1 – 29% opposite to 13% in group 2. Central nervous system pathology in treosulfan group was functional unlike predominance of organic impairment in group 1: no cases of encephalopathy or secondary epilepsy were registered. Differences in cardiovascular complications incidence were revealed, i.e., 16% in group 1 with secondary cardiomyopathy predominance in contrast with 10% in group 2. Both groups demonstrated one case of secondary neoplasms after a long follow-up period. Among patients with nonmalignant disorders (primary immunodeficiencies), 5 got busulfan-based conditioning and 8 received treosulfan-based treatment. Overall 5-year survival was 87.5% in group 1 and 60% in group 2. No significant differences in late effects after allo-HSCT were revealed.
Conclusion
Treosulfan-based myeloablative conditioning allows to reduce incidence of late endocrine complications (especially, hypogonadism), central nervous system and cardiovascular system pathology after allogeneic HSCT in children when compared with classical busulfan-based conditioning regimens.
Keywords
Allogeneic HSCT, conditioning, treosulfan, late complications, children.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20668" ["VALUE"]=> string(176) "Comparative analysis of late effects after treosulfan- and busulfan-based myeloablative conditioning regimens for allogeneic hematopoietic stem cell transplantation in children" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(176) "Comparative analysis of late effects after treosulfan- and busulfan-based myeloablative conditioning regimens for allogeneic hematopoietic stem cell transplantation in children" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(176) "Comparative analysis of late effects after treosulfan- and busulfan-based myeloablative conditioning regimens for allogeneic hematopoietic stem cell transplantation in children" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20666" ["VALUE"]=> array(2) { ["TEXT"]=> string(227) "<sup>1</sup> Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology (Moscow, Russian Federation) <sup>2</sup> Russian Children’s Hospital, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(203) "1 Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology (Moscow, Russian Federation) 2 Russian Children’s Hospital, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(203) "1 Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology (Moscow, Russian Federation) 2 Russian Children’s Hospital, Moscow, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20662" ["VALUE"]=> array(2) { ["TEXT"]=> string(710) "Юлия В. Скворцова <sup>1</sup>, Ирина П. Шипицына <sup>1</sup>, Дмитрий Н. Балашов <sup>1</sup>, Павел Е. Трахтман <sup>1</sup>, Елена В. Скоробогатова <sup>2</sup>, Людмила И. Папуша <sup>1</sup>, Елена И. Гутовская <sup>1</sup>, Лариса Н. Шелихова <sup>1</sup>, Елена Е. Курникова <sup>1</sup>, Кирилл А. Воронин <sup>1</sup>, Михаил А. Масчан <sup>1</sup>, Алексей А. Масчан <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(566) "Юлия В. Скворцова 1, Ирина П. Шипицына 1, Дмитрий Н. Балашов 1, Павел Е. Трахтман 1, Елена В. Скоробогатова 2, Людмила И. Папуша 1, Елена И. Гутовская 1, Лариса Н. Шелихова 1, Елена Е. Курникова 1, Кирилл А. Воронин 1, Михаил А. Масчан 1, Алексей А. Масчан 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(566) "Юлия В. Скворцова 1, Ирина П. Шипицына 1, Дмитрий Н. Балашов 1, Павел Е. Трахтман 1, Елена В. Скоробогатова 2, Людмила И. Папуша 1, Елена И. Гутовская 1, Лариса Н. Шелихова 1, Елена Е. Курникова 1, Кирилл А. Воронин 1, Михаил А. Масчан 1, Алексей А. Масчан 1" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20664" ["VALUE"]=> array(2) { ["TEXT"]=> string(6906) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Треосульфан активно используется в качестве миелоаблативного и иммуносупрессивного компонента современных режимов кондиционирования, что позволяет снизить раннюю токсичность аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Однако, отсутствуют данные о его поздних эффектах. Целью исследования явилось ретроспективное изучение поздних осложнений при проведении треосульфани бусульфан-содержащих миелоаблативных режимов кондиционирования у детей. </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> Проведен сравнительный анализ поздних осложнений у детей, получивших алло-ТГСК на базе отделения трансплантации костного мозга Российской детской клинической больницы (РДКБ)/Национального медицинского исследовательского центра детской гематологии, онкологии и иммунологии им. Дм. Рогачева (НМИЦ ДГОИ) (г. Москва, Россия) с 1994 по 2011 гг., имевших бусульфан- (группа 1, n=110, медиана наблюдения 7,4 г.) или треосульфан-содержащее (группа 2, n=38, медиана наблюдения 5,7 г.) кондиционирование и проживших минимум 1 г. от момента ТГСК. Учитывая различие в медианах наблюдения, статистический анализ проводили на сроке 5 лет от момента алло-ТГСК для обеих групп. Оценивали развитие хронической РТПХ, патологии эндокринной, нервной, сердечно-сосудистой систем, снижение костной минеральной плотности, развитие вторичных злокачественных заболеваний. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Пациенты с гемобластозами (105 в группе с бусульфаном и 30 в группе с треосульфаном) имели схожие показатели 5-летней выживаемости: общая выживаемость в 1-й и 2-й группах составила 79,3% и 66,1%, а безрецидивная выживаемость – 82,5% и 74,1%, соответственно. Частота хронической РТПХ – 57% в группе с треосульфаном и 50% в группе с бусульфаном. Кумулятивный риск развития экстенсивной хронической РТПХ составил 27,6% в 1-й группе и 43,3% во 2-й группе. При анализе других поздних осложнений обнаружено снижение частоты развития эндокринных нарушений в группе с треосульфаном – 27% против 43% в 1-й группе, при этом не зарегистрировано ни одного случая развития гипергонадотропного гипогонадизма (кумулятивный риск развития 32,8% в 1-й группе против 0% во 2-й, р = 0,012). Патология щитовидной железы в структуре эндокринных нарушений также преобладала в 1-й группе детей – 29% против 13%. Патология центральной нервной системы в группе с треосульфаном носила в большей степени функциональный характер в отличие от преобладания органических нарушений в 1-й группе: не зарегистрировано ни одного случая энцефалопатии, вторичной эпилепсии. Также отмечались качественные различия в развитии кардиоваскулярной патологии – 16% в 1-й группе с преобладанием вторичной кардиомиопатии против 10% во 2-й группе. В обеих группах зарегистрировано по одному случаю вторичных неоплазий на поздних сроках после ТГСК. Cреди детей с незлокачественными заболеваниями (первичными иммунодефицитами) 5 получили бусульфан-содержащее кондиционирование, а 8 – треосульфан-содержащее. Общая 5-летняя выживаемость составила 87,5% в 1-й группе против 60% во 2-й. Существенных различий в частоте поздних осложнений алло-ТГСК не выявлено. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Треосульфан-содержащее миелоаблативное кондиционирование позволяет снизить риск развития поздних осложнений со стороны эндокринной системы (особенно гипогонадизма), центральной нервной системы и кардиоваскулярных нарушений после алло-ТГСК у детей по сравнению с классическими бусульфан-содержащими режимами. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Алло-ТГСК, кондиционирование, треосульфан, поздние осложнения, дети. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6674) "Введение
Треосульфан активно используется в качестве миелоаблативного и иммуносупрессивного компонента современных режимов кондиционирования, что позволяет снизить раннюю токсичность аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Однако, отсутствуют данные о его поздних эффектах. Целью исследования явилось ретроспективное изучение поздних осложнений при проведении треосульфани бусульфан-содержащих миелоаблативных режимов кондиционирования у детей.
Методы
Проведен сравнительный анализ поздних осложнений у детей, получивших алло-ТГСК на базе отделения трансплантации костного мозга Российской детской клинической больницы (РДКБ)/Национального медицинского исследовательского центра детской гематологии, онкологии и иммунологии им. Дм. Рогачева (НМИЦ ДГОИ) (г. Москва, Россия) с 1994 по 2011 гг., имевших бусульфан- (группа 1, n=110, медиана наблюдения 7,4 г.) или треосульфан-содержащее (группа 2, n=38, медиана наблюдения 5,7 г.) кондиционирование и проживших минимум 1 г. от момента ТГСК. Учитывая различие в медианах наблюдения, статистический анализ проводили на сроке 5 лет от момента алло-ТГСК для обеих групп. Оценивали развитие хронической РТПХ, патологии эндокринной, нервной, сердечно-сосудистой систем, снижение костной минеральной плотности, развитие вторичных злокачественных заболеваний.
Результаты
Пациенты с гемобластозами (105 в группе с бусульфаном и 30 в группе с треосульфаном) имели схожие показатели 5-летней выживаемости: общая выживаемость в 1-й и 2-й группах составила 79,3% и 66,1%, а безрецидивная выживаемость – 82,5% и 74,1%, соответственно. Частота хронической РТПХ – 57% в группе с треосульфаном и 50% в группе с бусульфаном. Кумулятивный риск развития экстенсивной хронической РТПХ составил 27,6% в 1-й группе и 43,3% во 2-й группе. При анализе других поздних осложнений обнаружено снижение частоты развития эндокринных нарушений в группе с треосульфаном – 27% против 43% в 1-й группе, при этом не зарегистрировано ни одного случая развития гипергонадотропного гипогонадизма (кумулятивный риск развития 32,8% в 1-й группе против 0% во 2-й, р = 0,012). Патология щитовидной железы в структуре эндокринных нарушений также преобладала в 1-й группе детей – 29% против 13%. Патология центральной нервной системы в группе с треосульфаном носила в большей степени функциональный характер в отличие от преобладания органических нарушений в 1-й группе: не зарегистрировано ни одного случая энцефалопатии, вторичной эпилепсии. Также отмечались качественные различия в развитии кардиоваскулярной патологии – 16% в 1-й группе с преобладанием вторичной кардиомиопатии против 10% во 2-й группе. В обеих группах зарегистрировано по одному случаю вторичных неоплазий на поздних сроках после ТГСК. Cреди детей с незлокачественными заболеваниями (первичными иммунодефицитами) 5 получили бусульфан-содержащее кондиционирование, а 8 – треосульфан-содержащее. Общая 5-летняя выживаемость составила 87,5% в 1-й группе против 60% во 2-й. Существенных различий в частоте поздних осложнений алло-ТГСК не выявлено.
Заключение
Треосульфан-содержащее миелоаблативное кондиционирование позволяет снизить риск развития поздних осложнений со стороны эндокринной системы (особенно гипогонадизма), центральной нервной системы и кардиоваскулярных нарушений после алло-ТГСК у детей по сравнению с классическими бусульфан-содержащими режимами.
Ключевые слова
Алло-ТГСК, кондиционирование, треосульфан, поздние осложнения, дети.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6674) "Введение
Треосульфан активно используется в качестве миелоаблативного и иммуносупрессивного компонента современных режимов кондиционирования, что позволяет снизить раннюю токсичность аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Однако, отсутствуют данные о его поздних эффектах. Целью исследования явилось ретроспективное изучение поздних осложнений при проведении треосульфани бусульфан-содержащих миелоаблативных режимов кондиционирования у детей.
Методы
Проведен сравнительный анализ поздних осложнений у детей, получивших алло-ТГСК на базе отделения трансплантации костного мозга Российской детской клинической больницы (РДКБ)/Национального медицинского исследовательского центра детской гематологии, онкологии и иммунологии им. Дм. Рогачева (НМИЦ ДГОИ) (г. Москва, Россия) с 1994 по 2011 гг., имевших бусульфан- (группа 1, n=110, медиана наблюдения 7,4 г.) или треосульфан-содержащее (группа 2, n=38, медиана наблюдения 5,7 г.) кондиционирование и проживших минимум 1 г. от момента ТГСК. Учитывая различие в медианах наблюдения, статистический анализ проводили на сроке 5 лет от момента алло-ТГСК для обеих групп. Оценивали развитие хронической РТПХ, патологии эндокринной, нервной, сердечно-сосудистой систем, снижение костной минеральной плотности, развитие вторичных злокачественных заболеваний.
Результаты
Пациенты с гемобластозами (105 в группе с бусульфаном и 30 в группе с треосульфаном) имели схожие показатели 5-летней выживаемости: общая выживаемость в 1-й и 2-й группах составила 79,3% и 66,1%, а безрецидивная выживаемость – 82,5% и 74,1%, соответственно. Частота хронической РТПХ – 57% в группе с треосульфаном и 50% в группе с бусульфаном. Кумулятивный риск развития экстенсивной хронической РТПХ составил 27,6% в 1-й группе и 43,3% во 2-й группе. При анализе других поздних осложнений обнаружено снижение частоты развития эндокринных нарушений в группе с треосульфаном – 27% против 43% в 1-й группе, при этом не зарегистрировано ни одного случая развития гипергонадотропного гипогонадизма (кумулятивный риск развития 32,8% в 1-й группе против 0% во 2-й, р = 0,012). Патология щитовидной железы в структуре эндокринных нарушений также преобладала в 1-й группе детей – 29% против 13%. Патология центральной нервной системы в группе с треосульфаном носила в большей степени функциональный характер в отличие от преобладания органических нарушений в 1-й группе: не зарегистрировано ни одного случая энцефалопатии, вторичной эпилепсии. Также отмечались качественные различия в развитии кардиоваскулярной патологии – 16% в 1-й группе с преобладанием вторичной кардиомиопатии против 10% во 2-й группе. В обеих группах зарегистрировано по одному случаю вторичных неоплазий на поздних сроках после ТГСК. Cреди детей с незлокачественными заболеваниями (первичными иммунодефицитами) 5 получили бусульфан-содержащее кондиционирование, а 8 – треосульфан-содержащее. Общая 5-летняя выживаемость составила 87,5% в 1-й группе против 60% во 2-й. Существенных различий в частоте поздних осложнений алло-ТГСК не выявлено.
Заключение
Треосульфан-содержащее миелоаблативное кондиционирование позволяет снизить риск развития поздних осложнений со стороны эндокринной системы (особенно гипогонадизма), центральной нервной системы и кардиоваскулярных нарушений после алло-ТГСК у детей по сравнению с классическими бусульфан-содержащими режимами.
Ключевые слова
Алло-ТГСК, кондиционирование, треосульфан, поздние осложнения, дети.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20663" ["VALUE"]=> array(2) { ["TEXT"]=> string(393) "<sup>1</sup> ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» МЗ РФ <sup>2</sup> ФГБУ «Российская детская клиническая больница» МЗ РФ" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(369) "1 ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» МЗ РФ 2 ФГБУ «Российская детская клиническая больница» МЗ РФ" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(369) "1 ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» МЗ РФ 2 ФГБУ «Российская детская клиническая больница» МЗ РФ" } } } [29]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1595" ["~ID"]=> string(4) "1595" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(280) "Определение гемопоэтических стволовых клеток в периферической крови и продукте афереза на гематологическом анализаторе Sysmex XN (XN-HPC): клинический случай" ["~NAME"]=> string(280) "Определение гемопоэтических стволовых клеток в периферической крови и продукте афереза на гематологическом анализаторе Sysmex XN (XN-HPC): клинический случай" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:45:42" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:45:42" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/opredelenie-gemopoeticheskikh-stvolovykh-kletok-v-perifericheskoy-krovi-i-produkte-afereza-na-gemato/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/opredelenie-gemopoeticheskikh-stvolovykh-kletok-v-perifericheskoy-krovi-i-produkte-afereza-na-gemato/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "opredelenie-gemopoeticheskikh-stvolovykh-kletok-v-perifericheskoy-krovi-i-produkte-afereza-na-gemato" ["~CODE"]=> string(100) "opredelenie-gemopoeticheskikh-stvolovykh-kletok-v-perifericheskoy-krovi-i-produkte-afereza-na-gemato" ["EXTERNAL_ID"]=> string(4) "1595" ["~EXTERNAL_ID"]=> string(4) "1595" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(280) "Определение гемопоэтических стволовых клеток в периферической крови и продукте афереза на гематологическом анализаторе Sysmex XN (XN-HPC): клинический случай" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(426) "Определение гемопоэтических стволовых клеток в периферической крови и продукте афереза на гематологическом анализаторе Sysmex XN (XN-HPC): клинический случайEvaluation of hematopoietic stem cells in peripheral blood and apheresis product on the hematological analyzer Sysmex XN (XN-HPC): a clinical case" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(8028) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Рутинным методом определения количества гемопоэтических стволовых клеток (ГСК) является проточная цитофлуориметрия с использованием меченых антител и витального красителя. К серьезным недостаткам данного метода можно отнести сложность стандартизации, отсутствие автоматизации, большие трудозатраты квалифицированного персонала, а также относительная дороговизна расходных материалов. В связи с высокой потребностью частого определения ГСК в периферической крови (ПК) и продуктах афереза существует необходимость разработки стандартизированных, автоматизированных методов. Sysmex-XN является использующимся в клинической практике гематологическом анализатором, имеющим все необходимые возможности для стандартизации проводящихся на нем исследований. В настоящее время разработана возможность определения количества ГСК на Sysmex-XN в канале WPC в режиме XN-HPC. Определение ГСК данным методом является исследовательским, но в перспективе может быть внедрено в клиническую практику в дополнение к рутинному методу в случае получения сопоставимых данных. Целью работы было сравнение данных по количественному определению ГСК в ПК и продукте афереза после мобилизации с помощью Г-КСФ двумя методами, а также трудовых и финансовых затрат. </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> В качестве стандарта использовался метод подсчета ГСК: подсчет лейкоцитов в камере Горяева и проточная цитофлуориметрия с маркерами CD45/CD34/7AAD (BD; San Jose, USA) на аппарате BD FacsCalibur по протоколу ISHAGE. Исследуемый метод – автоматизированный метод подсчета ГСК, доступный на анализаторах Sysmex XN (XN-HPC) в канале WPC, основанный на измерении размера, структуры и интенсивности флуоресценции клеток. Пробы ПК и продукта афереза забирались для исследований из одних образцов. Заготовка ГСК проводилась на сепараторе COBE Spectra. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Представляется клинический случай пациентки Г., 2 г. 4 мес., рост 85,5 см., вес 15 кг, с диагнозом медуллобластома. Для лечения рецидива планируется высокодозная химиотерапии с аутотрансплантацией ГСК. Заготовка ГСК ПК проводилась после стимуляции Г-КСФ в дозе 10 мкг/кг однократно в течение 5-ти дней. На пятый день выполнен аферез. Объем перфузии составил 2900.0 мл, получено 230.0 мл концентрата. Результаты исследований представлены в таблицах: (1) количественное определение ГСК в ПК, (2) оценка количества ГСК в аферезном концентрате, (3) оценка финансовых и трудозатрат (без учета амортизации оборудования и коммунальных затрат). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Представленный клинический случай демонстрирует, что результаты количественного определения ГСК на анализаторе Sysmex-XN сопоставимы с результатами рутинного метода, в то время как трудовые и финансовые затраты по меньшей мере в 3 раза ниже. Быстрота получения результата и относительно низкая стоимость позволяет предложить использование количественного определения ГСК на анализаторе Sysmex-XN в качестве дополнительного скринингового метода, результаты которого в дальнейшем будут валидироваться стандартным методом исследования. Внедрение нового скринингового метода определения ГСК приведет к оптимизации алгоритмов проведения афереза и, как следствие, получению трансплантатов ГСК лучшего качества. Тем не менее, для использования нового метода в клинической практике необходимо проведение сравнительных исследований по количественному определению ГСК в ПК и продуктах афереза от широкой когорты доноров/пациентов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Гемопоэтические стволовые клетки, заготовка ГСК, периферическая кровь, продукт афереза, проточная цитометрия, Sysmex-XN, скрининг количества ГСК. </p> <h2 style="text-align: justify;"> Таблица 1. Результаты исследований ПК<br> </h2> <img width="781" alt="46_таблица 1.png" src="/upload/medialibrary/3db/46_tablitsa-1.png" height="179" title="46_таблица 1.png"> <h2>Таблица 2. Результаты исследований аферезного концентрата</h2> <img width="783" alt="46_таблица 2.png" src="/upload/medialibrary/176/46_tablitsa-2.png" height="89" title="46_таблица 2.png"> <h2>Таблица 3. Оценка финансовых и трудозатрат</h2> <img width="783" alt="46_таблица 3.png" src="/upload/medialibrary/7f9/46_tablitsa-3.png" height="289" title="46_таблица 3.png"><br>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(280) "Определение гемопоэтических стволовых клеток в периферической крови и продукте афереза на гематологическом анализаторе Sysmex XN (XN-HPC): клинический случай" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(280) "Определение гемопоэтических стволовых клеток в периферической крови и продукте афереза на гематологическом анализаторе Sysmex XN (XN-HPC): клинический случай" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(280) "Определение гемопоэтических стволовых клеток в периферической крови и продукте афереза на гематологическом анализаторе Sysmex XN (XN-HPC): клинический случай" ["SECTION_META_TITLE"]=> string(280) "Определение гемопоэтических стволовых клеток в периферической крови и продукте афереза на гематологическом анализаторе Sysmex XN (XN-HPC): клинический случай" ["SECTION_META_KEYWORDS"]=> string(280) "Определение гемопоэтических стволовых клеток в периферической крови и продукте афереза на гематологическом анализаторе Sysmex XN (XN-HPC): клинический случай" ["SECTION_META_DESCRIPTION"]=> string(280) "Определение гемопоэтических стволовых клеток в периферической крови и продукте афереза на гематологическом анализаторе Sysmex XN (XN-HPC): клинический случай" ["SECTION_PICTURE_FILE_ALT"]=> string(280) "Определение гемопоэтических стволовых клеток в периферической крови и продукте афереза на гематологическом анализаторе Sysmex XN (XN-HPC): клинический случай" ["SECTION_PICTURE_FILE_TITLE"]=> string(280) "Определение гемопоэтических стволовых клеток в периферической крови и продукте афереза на гематологическом анализаторе Sysmex XN (XN-HPC): клинический случай" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "opredelenie-gemopoeticheskikh-stvolovykh-kletok-v-perifericheskoy-krovi-i-produkte-afereza-na-gemato" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(280) "Определение гемопоэтических стволовых клеток в периферической крови и продукте афереза на гематологическом анализаторе Sysmex XN (XN-HPC): клинический случай" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(280) "Определение гемопоэтических стволовых клеток в периферической крови и продукте афереза на гематологическом анализаторе Sysmex XN (XN-HPC): клинический случай" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "opredelenie-gemopoeticheskikh-stvolovykh-kletok-v-perifericheskoy-krovi-i-produkte-afereza-na-gemato" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "opredelenie-gemopoeticheskikh-stvolovykh-kletok-v-perifericheskoy-krovi-i-produkte-afereza-na-gemato" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "opredelenie-gemopoeticheskikh-stvolovykh-kletok-v-perifericheskoy-krovi-i-produkte-afereza-na-gemato" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20669" ["VALUE"]=> array(2) { ["TEXT"]=> string(453) "Татьяна С. Щеголева, Марина А. Городнова, Валентина М. Кравцова, Владислав С. Сергеев, Елена В. Бабенко, Мария А. Эстрина, Полина С. Куга, Ирина И. Кулагина, Марина О. Попова, Татьяна В. Андреева, Асмик Г. Геворгян, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(453) "Татьяна С. Щеголева, Марина А. Городнова, Валентина М. Кравцова, Владислав С. Сергеев, Елена В. Бабенко, Мария А. Эстрина, Полина С. Куга, Ирина И. Кулагина, Марина О. Попова, Татьяна В. Андреева, Асмик Г. Геворгян, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20670" ["VALUE"]=> array(2) { ["TEXT"]=> string(303) "Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(303) "Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20671" ["VALUE"]=> array(2) { ["TEXT"]=> string(8028) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Рутинным методом определения количества гемопоэтических стволовых клеток (ГСК) является проточная цитофлуориметрия с использованием меченых антител и витального красителя. К серьезным недостаткам данного метода можно отнести сложность стандартизации, отсутствие автоматизации, большие трудозатраты квалифицированного персонала, а также относительная дороговизна расходных материалов. В связи с высокой потребностью частого определения ГСК в периферической крови (ПК) и продуктах афереза существует необходимость разработки стандартизированных, автоматизированных методов. Sysmex-XN является использующимся в клинической практике гематологическом анализатором, имеющим все необходимые возможности для стандартизации проводящихся на нем исследований. В настоящее время разработана возможность определения количества ГСК на Sysmex-XN в канале WPC в режиме XN-HPC. Определение ГСК данным методом является исследовательским, но в перспективе может быть внедрено в клиническую практику в дополнение к рутинному методу в случае получения сопоставимых данных. Целью работы было сравнение данных по количественному определению ГСК в ПК и продукте афереза после мобилизации с помощью Г-КСФ двумя методами, а также трудовых и финансовых затрат. </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> В качестве стандарта использовался метод подсчета ГСК: подсчет лейкоцитов в камере Горяева и проточная цитофлуориметрия с маркерами CD45/CD34/7AAD (BD; San Jose, USA) на аппарате BD FacsCalibur по протоколу ISHAGE. Исследуемый метод – автоматизированный метод подсчета ГСК, доступный на анализаторах Sysmex XN (XN-HPC) в канале WPC, основанный на измерении размера, структуры и интенсивности флуоресценции клеток. Пробы ПК и продукта афереза забирались для исследований из одних образцов. Заготовка ГСК проводилась на сепараторе COBE Spectra. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Представляется клинический случай пациентки Г., 2 г. 4 мес., рост 85,5 см., вес 15 кг, с диагнозом медуллобластома. Для лечения рецидива планируется высокодозная химиотерапии с аутотрансплантацией ГСК. Заготовка ГСК ПК проводилась после стимуляции Г-КСФ в дозе 10 мкг/кг однократно в течение 5-ти дней. На пятый день выполнен аферез. Объем перфузии составил 2900.0 мл, получено 230.0 мл концентрата. Результаты исследований представлены в таблицах: (1) количественное определение ГСК в ПК, (2) оценка количества ГСК в аферезном концентрате, (3) оценка финансовых и трудозатрат (без учета амортизации оборудования и коммунальных затрат). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Представленный клинический случай демонстрирует, что результаты количественного определения ГСК на анализаторе Sysmex-XN сопоставимы с результатами рутинного метода, в то время как трудовые и финансовые затраты по меньшей мере в 3 раза ниже. Быстрота получения результата и относительно низкая стоимость позволяет предложить использование количественного определения ГСК на анализаторе Sysmex-XN в качестве дополнительного скринингового метода, результаты которого в дальнейшем будут валидироваться стандартным методом исследования. Внедрение нового скринингового метода определения ГСК приведет к оптимизации алгоритмов проведения афереза и, как следствие, получению трансплантатов ГСК лучшего качества. Тем не менее, для использования нового метода в клинической практике необходимо проведение сравнительных исследований по количественному определению ГСК в ПК и продуктах афереза от широкой когорты доноров/пациентов. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Гемопоэтические стволовые клетки, заготовка ГСК, периферическая кровь, продукт афереза, проточная цитометрия, Sysmex-XN, скрининг количества ГСК. </p> <h2 style="text-align: justify;"> Таблица 1. Результаты исследований ПК<br> </h2> <img width="781" alt="46_таблица 1.png" src="/upload/medialibrary/3db/46_tablitsa-1.png" height="179" title="46_таблица 1.png"> <h2>Таблица 2. Результаты исследований аферезного концентрата</h2> <img width="783" alt="46_таблица 2.png" src="/upload/medialibrary/176/46_tablitsa-2.png" height="89" title="46_таблица 2.png"> <h2>Таблица 3. Оценка финансовых и трудозатрат</h2> <img width="783" alt="46_таблица 3.png" src="/upload/medialibrary/7f9/46_tablitsa-3.png" height="289" title="46_таблица 3.png"><br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7570) "Введение
Рутинным методом определения количества гемопоэтических стволовых клеток (ГСК) является проточная цитофлуориметрия с использованием меченых антител и витального красителя. К серьезным недостаткам данного метода можно отнести сложность стандартизации, отсутствие автоматизации, большие трудозатраты квалифицированного персонала, а также относительная дороговизна расходных материалов. В связи с высокой потребностью частого определения ГСК в периферической крови (ПК) и продуктах афереза существует необходимость разработки стандартизированных, автоматизированных методов. Sysmex-XN является использующимся в клинической практике гематологическом анализатором, имеющим все необходимые возможности для стандартизации проводящихся на нем исследований. В настоящее время разработана возможность определения количества ГСК на Sysmex-XN в канале WPC в режиме XN-HPC. Определение ГСК данным методом является исследовательским, но в перспективе может быть внедрено в клиническую практику в дополнение к рутинному методу в случае получения сопоставимых данных. Целью работы было сравнение данных по количественному определению ГСК в ПК и продукте афереза после мобилизации с помощью Г-КСФ двумя методами, а также трудовых и финансовых затрат.
Методы
В качестве стандарта использовался метод подсчета ГСК: подсчет лейкоцитов в камере Горяева и проточная цитофлуориметрия с маркерами CD45/CD34/7AAD (BD; San Jose, USA) на аппарате BD FacsCalibur по протоколу ISHAGE. Исследуемый метод – автоматизированный метод подсчета ГСК, доступный на анализаторах Sysmex XN (XN-HPC) в канале WPC, основанный на измерении размера, структуры и интенсивности флуоресценции клеток. Пробы ПК и продукта афереза забирались для исследований из одних образцов. Заготовка ГСК проводилась на сепараторе COBE Spectra.
Результаты
Представляется клинический случай пациентки Г., 2 г. 4 мес., рост 85,5 см., вес 15 кг, с диагнозом медуллобластома. Для лечения рецидива планируется высокодозная химиотерапии с аутотрансплантацией ГСК. Заготовка ГСК ПК проводилась после стимуляции Г-КСФ в дозе 10 мкг/кг однократно в течение 5-ти дней. На пятый день выполнен аферез. Объем перфузии составил 2900.0 мл, получено 230.0 мл концентрата. Результаты исследований представлены в таблицах: (1) количественное определение ГСК в ПК, (2) оценка количества ГСК в аферезном концентрате, (3) оценка финансовых и трудозатрат (без учета амортизации оборудования и коммунальных затрат).
Выводы
Представленный клинический случай демонстрирует, что результаты количественного определения ГСК на анализаторе Sysmex-XN сопоставимы с результатами рутинного метода, в то время как трудовые и финансовые затраты по меньшей мере в 3 раза ниже. Быстрота получения результата и относительно низкая стоимость позволяет предложить использование количественного определения ГСК на анализаторе Sysmex-XN в качестве дополнительного скринингового метода, результаты которого в дальнейшем будут валидироваться стандартным методом исследования. Внедрение нового скринингового метода определения ГСК приведет к оптимизации алгоритмов проведения афереза и, как следствие, получению трансплантатов ГСК лучшего качества. Тем не менее, для использования нового метода в клинической практике необходимо проведение сравнительных исследований по количественному определению ГСК в ПК и продуктах афереза от широкой когорты доноров/пациентов.
Ключевые слова
Гемопоэтические стволовые клетки, заготовка ГСК, периферическая кровь, продукт афереза, проточная цитометрия, Sysmex-XN, скрининг количества ГСК.
Таблица 1. Результаты исследований ПК

Таблица 2. Результаты исследований аферезного концентрата

Таблица 3. Оценка финансовых и трудозатрат

" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20672" ["VALUE"]=> array(2) { ["TEXT"]=> string(264) "Tatiana S. Shchegoleva, Marina A. Gorodnova, Valentina M. Kravtsova, Vladislav S. Sergeev, Elena V. Babenko, Maria A. Estrina, Polina S. Kuga, Irina I. Kulagina, Marina O. Popova, Tatyana V. Andreeva, Asmik G. Gevorgyan, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(264) "Tatiana S. Shchegoleva, Marina A. Gorodnova, Valentina M. Kravtsova, Vladislav S. Sergeev, Elena V. Babenko, Maria A. Estrina, Polina S. Kuga, Irina I. Kulagina, Marina O. Popova, Tatyana V. Andreeva, Asmik G. Gevorgyan, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20673" ["VALUE"]=> array(2) { ["TEXT"]=> string(186) "Raisa Gorbacheva Memorial Research Institute of Children’s Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St.Peterburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(186) "Raisa Gorbacheva Memorial Research Institute of Children’s Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St.Peterburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20674" ["VALUE"]=> array(2) { ["TEXT"]=> string(5380) "<h2></h2> <h2 style="text-align: justify;">Background</h2> <p style="text-align: justify;"> The routine method for evaluation of hematopoietic stem cells (HSC) is flow cytometry using labeled antibodies and vital dye. Serious disadvantages of this method include the difficulty of standardization, the lack of automation, the high labor costs of qualified personnel, and the relative high cost of consumables. Frequent evaluation of HSC in peripheral blood (PB) and apheresis products are a high clinical need test. The development of standardized, automated methods of HSC evaluation is an actual challenge. Sysmex-XN is a clinical hematological analyzer which has already had all the necessary facilities for standardizing the evaluations conducted on it. Currently, the ability to evaluate the number of HSCs on Sysmex-XN in a WPC channel in the XNHPC mode has been developed. The evaluation of HSC by<br> this method is at research stage, but in the future it can be introduced into clinical practice in addition to the routine method in the case of obtaining comparable data. Aim of this study was to compare the data of the quantitative evaluation of HSC in peripheral blood and apheresis product after mobilization with G-CSF by two methods, as well as labor and financial costs. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> As a standard, the HSC counting method was used: counting of leukocytes in the Goryaev’ chamber and flow cytometry with markers CD45/CD34/7AAD (BD, San Jose, USA) using BD FacsCalibur and the ISHAGE protocol. A new method is an automated method for calculating HSC, available on Sysmex XN analyzers (XN-HPC) in the WPC channel, based on measuring the size, structure, and fluorescence intensity of cells. Samples of PB and apheresis product were taken for research from same specimens. The HSCs were collected on a COBE Spectra separator. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> We report a clinical case of the patient G., 2 years 4 months, height 85.5 cm, weight 15 kg, with the diagnosis of medulloblastoma. The treatment of relapse has to include highdose chemotherapy with autologous hematopoietic stem cell transplantation. Harvesting HSCs of PB was performed after stimulation of G-CSF in a dose of 10 μg/kg once for 5 days. Apheresis was performed on the fifth day of mobilization. The volume of perfusion was 2900.0 ml, 230.0 ml of concentrate was obtained. The comparative results of the studies are presented in the tables: (1) the quantitative evaluation of HSC in the PB, (2) the estimation of the amount of HSC in the apheresis concentrate, (3) the financial and labor costs evaluation (without depreciation of equipment and utility costs). </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> The presented clinical case demonstrates that the results of quantitative evaluation of HSC on the Sysmex-XN analyzer are comparable with the results of the routine method, while labor and financial costs are at least 3 times lower. The speed of obtaining the result and the relatively low cost make it possible to propose the use of quantitative evaluation of HSC on the Sysmex-XN analyzer as an additional screening method, the results of which will subsequently be validated by the standard method of investigation. The introduction of a new screening method for evaluation of HSCs will lead to optimization of the peripheral blood HSC harvesting protocols and, as a consequence, to obtaining HSC transplants of better quality. Nevertheless, to use the new method in clinical practice, it is necessary to conduct comparative studies on the evaluation of HSC in the PB and apheresis products from a broad cohort of donors/patients. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cells, peripheral blood, HSC harvesting, apheresis concentrate, flow cytometry, Sysmex-XN, quantitative HSC screening. </p> <h2 style="text-align: justify;">Table 1. Evaluation of HSCs in peripheral blood</h2> <p style="text-align: justify;"> <img width="783" alt="46_table 1.png" src="/upload/medialibrary/984/46_table-1.png" height="203" title="46_table 1.png"> </p> <h2 style="text-align: justify;">Table 2. The evaluation of HSCs in apheresis concentrate</h2> <p style="text-align: justify;"> <img width="783" alt="46_table 2.png" src="/upload/medialibrary/f12/46_table-2.png" height="105" title="46_table 2.png"> </p> <h2 style="text-align: justify;">Table 3. Evaluation of time expenses and financial costs</h2> <p style="text-align: justify;"> <img width="783" alt="46_table 3.png" src="/upload/medialibrary/ef6/46_table-3.png" height="321" title="46_table 3.png"> </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4842) "
Background
The routine method for evaluation of hematopoietic stem cells (HSC) is flow cytometry using labeled antibodies and vital dye. Serious disadvantages of this method include the difficulty of standardization, the lack of automation, the high labor costs of qualified personnel, and the relative high cost of consumables. Frequent evaluation of HSC in peripheral blood (PB) and apheresis products are a high clinical need test. The development of standardized, automated methods of HSC evaluation is an actual challenge. Sysmex-XN is a clinical hematological analyzer which has already had all the necessary facilities for standardizing the evaluations conducted on it. Currently, the ability to evaluate the number of HSCs on Sysmex-XN in a WPC channel in the XNHPC mode has been developed. The evaluation of HSC by
this method is at research stage, but in the future it can be introduced into clinical practice in addition to the routine method in the case of obtaining comparable data. Aim of this study was to compare the data of the quantitative evaluation of HSC in peripheral blood and apheresis product after mobilization with G-CSF by two methods, as well as labor and financial costs.
Materials and methods
As a standard, the HSC counting method was used: counting of leukocytes in the Goryaev’ chamber and flow cytometry with markers CD45/CD34/7AAD (BD, San Jose, USA) using BD FacsCalibur and the ISHAGE protocol. A new method is an automated method for calculating HSC, available on Sysmex XN analyzers (XN-HPC) in the WPC channel, based on measuring the size, structure, and fluorescence intensity of cells. Samples of PB and apheresis product were taken for research from same specimens. The HSCs were collected on a COBE Spectra separator.
Results
We report a clinical case of the patient G., 2 years 4 months, height 85.5 cm, weight 15 kg, with the diagnosis of medulloblastoma. The treatment of relapse has to include highdose chemotherapy with autologous hematopoietic stem cell transplantation. Harvesting HSCs of PB was performed after stimulation of G-CSF in a dose of 10 μg/kg once for 5 days. Apheresis was performed on the fifth day of mobilization. The volume of perfusion was 2900.0 ml, 230.0 ml of concentrate was obtained. The comparative results of the studies are presented in the tables: (1) the quantitative evaluation of HSC in the PB, (2) the estimation of the amount of HSC in the apheresis concentrate, (3) the financial and labor costs evaluation (without depreciation of equipment and utility costs).
Conclusions
The presented clinical case demonstrates that the results of quantitative evaluation of HSC on the Sysmex-XN analyzer are comparable with the results of the routine method, while labor and financial costs are at least 3 times lower. The speed of obtaining the result and the relatively low cost make it possible to propose the use of quantitative evaluation of HSC on the Sysmex-XN analyzer as an additional screening method, the results of which will subsequently be validated by the standard method of investigation. The introduction of a new screening method for evaluation of HSCs will lead to optimization of the peripheral blood HSC harvesting protocols and, as a consequence, to obtaining HSC transplants of better quality. Nevertheless, to use the new method in clinical practice, it is necessary to conduct comparative studies on the evaluation of HSC in the PB and apheresis products from a broad cohort of donors/patients.
Keywords
Hematopoietic stem cells, peripheral blood, HSC harvesting, apheresis concentrate, flow cytometry, Sysmex-XN, quantitative HSC screening.
Table 1. Evaluation of HSCs in peripheral blood

Table 2. The evaluation of HSCs in apheresis concentrate

Table 3. Evaluation of time expenses and financial costs

Background
The routine method for evaluation of hematopoietic stem cells (HSC) is flow cytometry using labeled antibodies and vital dye. Serious disadvantages of this method include the difficulty of standardization, the lack of automation, the high labor costs of qualified personnel, and the relative high cost of consumables. Frequent evaluation of HSC in peripheral blood (PB) and apheresis products are a high clinical need test. The development of standardized, automated methods of HSC evaluation is an actual challenge. Sysmex-XN is a clinical hematological analyzer which has already had all the necessary facilities for standardizing the evaluations conducted on it. Currently, the ability to evaluate the number of HSCs on Sysmex-XN in a WPC channel in the XNHPC mode has been developed. The evaluation of HSC by
this method is at research stage, but in the future it can be introduced into clinical practice in addition to the routine method in the case of obtaining comparable data. Aim of this study was to compare the data of the quantitative evaluation of HSC in peripheral blood and apheresis product after mobilization with G-CSF by two methods, as well as labor and financial costs.
Materials and methods
As a standard, the HSC counting method was used: counting of leukocytes in the Goryaev’ chamber and flow cytometry with markers CD45/CD34/7AAD (BD, San Jose, USA) using BD FacsCalibur and the ISHAGE protocol. A new method is an automated method for calculating HSC, available on Sysmex XN analyzers (XN-HPC) in the WPC channel, based on measuring the size, structure, and fluorescence intensity of cells. Samples of PB and apheresis product were taken for research from same specimens. The HSCs were collected on a COBE Spectra separator.
Results
We report a clinical case of the patient G., 2 years 4 months, height 85.5 cm, weight 15 kg, with the diagnosis of medulloblastoma. The treatment of relapse has to include highdose chemotherapy with autologous hematopoietic stem cell transplantation. Harvesting HSCs of PB was performed after stimulation of G-CSF in a dose of 10 μg/kg once for 5 days. Apheresis was performed on the fifth day of mobilization. The volume of perfusion was 2900.0 ml, 230.0 ml of concentrate was obtained. The comparative results of the studies are presented in the tables: (1) the quantitative evaluation of HSC in the PB, (2) the estimation of the amount of HSC in the apheresis concentrate, (3) the financial and labor costs evaluation (without depreciation of equipment and utility costs).
Conclusions
The presented clinical case demonstrates that the results of quantitative evaluation of HSC on the Sysmex-XN analyzer are comparable with the results of the routine method, while labor and financial costs are at least 3 times lower. The speed of obtaining the result and the relatively low cost make it possible to propose the use of quantitative evaluation of HSC on the Sysmex-XN analyzer as an additional screening method, the results of which will subsequently be validated by the standard method of investigation. The introduction of a new screening method for evaluation of HSCs will lead to optimization of the peripheral blood HSC harvesting protocols and, as a consequence, to obtaining HSC transplants of better quality. Nevertheless, to use the new method in clinical practice, it is necessary to conduct comparative studies on the evaluation of HSC in the PB and apheresis products from a broad cohort of donors/patients.
Keywords
Hematopoietic stem cells, peripheral blood, HSC harvesting, apheresis concentrate, flow cytometry, Sysmex-XN, quantitative HSC screening.
Table 1. Evaluation of HSCs in peripheral blood

Table 2. The evaluation of HSCs in apheresis concentrate

Table 3. Evaluation of time expenses and financial costs

Background
The routine method for evaluation of hematopoietic stem cells (HSC) is flow cytometry using labeled antibodies and vital dye. Serious disadvantages of this method include the difficulty of standardization, the lack of automation, the high labor costs of qualified personnel, and the relative high cost of consumables. Frequent evaluation of HSC in peripheral blood (PB) and apheresis products are a high clinical need test. The development of standardized, automated methods of HSC evaluation is an actual challenge. Sysmex-XN is a clinical hematological analyzer which has already had all the necessary facilities for standardizing the evaluations conducted on it. Currently, the ability to evaluate the number of HSCs on Sysmex-XN in a WPC channel in the XNHPC mode has been developed. The evaluation of HSC by
this method is at research stage, but in the future it can be introduced into clinical practice in addition to the routine method in the case of obtaining comparable data. Aim of this study was to compare the data of the quantitative evaluation of HSC in peripheral blood and apheresis product after mobilization with G-CSF by two methods, as well as labor and financial costs.
Materials and methods
As a standard, the HSC counting method was used: counting of leukocytes in the Goryaev’ chamber and flow cytometry with markers CD45/CD34/7AAD (BD, San Jose, USA) using BD FacsCalibur and the ISHAGE protocol. A new method is an automated method for calculating HSC, available on Sysmex XN analyzers (XN-HPC) in the WPC channel, based on measuring the size, structure, and fluorescence intensity of cells. Samples of PB and apheresis product were taken for research from same specimens. The HSCs were collected on a COBE Spectra separator.
Results
We report a clinical case of the patient G., 2 years 4 months, height 85.5 cm, weight 15 kg, with the diagnosis of medulloblastoma. The treatment of relapse has to include highdose chemotherapy with autologous hematopoietic stem cell transplantation. Harvesting HSCs of PB was performed after stimulation of G-CSF in a dose of 10 μg/kg once for 5 days. Apheresis was performed on the fifth day of mobilization. The volume of perfusion was 2900.0 ml, 230.0 ml of concentrate was obtained. The comparative results of the studies are presented in the tables: (1) the quantitative evaluation of HSC in the PB, (2) the estimation of the amount of HSC in the apheresis concentrate, (3) the financial and labor costs evaluation (without depreciation of equipment and utility costs).
Conclusions
The presented clinical case demonstrates that the results of quantitative evaluation of HSC on the Sysmex-XN analyzer are comparable with the results of the routine method, while labor and financial costs are at least 3 times lower. The speed of obtaining the result and the relatively low cost make it possible to propose the use of quantitative evaluation of HSC on the Sysmex-XN analyzer as an additional screening method, the results of which will subsequently be validated by the standard method of investigation. The introduction of a new screening method for evaluation of HSCs will lead to optimization of the peripheral blood HSC harvesting protocols and, as a consequence, to obtaining HSC transplants of better quality. Nevertheless, to use the new method in clinical practice, it is necessary to conduct comparative studies on the evaluation of HSC in the PB and apheresis products from a broad cohort of donors/patients.
Keywords
Hematopoietic stem cells, peripheral blood, HSC harvesting, apheresis concentrate, flow cytometry, Sysmex-XN, quantitative HSC screening.
Table 1. Evaluation of HSCs in peripheral blood

Table 2. The evaluation of HSCs in apheresis concentrate

Table 3. Evaluation of time expenses and financial costs

Введение
Рутинным методом определения количества гемопоэтических стволовых клеток (ГСК) является проточная цитофлуориметрия с использованием меченых антител и витального красителя. К серьезным недостаткам данного метода можно отнести сложность стандартизации, отсутствие автоматизации, большие трудозатраты квалифицированного персонала, а также относительная дороговизна расходных материалов. В связи с высокой потребностью частого определения ГСК в периферической крови (ПК) и продуктах афереза существует необходимость разработки стандартизированных, автоматизированных методов. Sysmex-XN является использующимся в клинической практике гематологическом анализатором, имеющим все необходимые возможности для стандартизации проводящихся на нем исследований. В настоящее время разработана возможность определения количества ГСК на Sysmex-XN в канале WPC в режиме XN-HPC. Определение ГСК данным методом является исследовательским, но в перспективе может быть внедрено в клиническую практику в дополнение к рутинному методу в случае получения сопоставимых данных. Целью работы было сравнение данных по количественному определению ГСК в ПК и продукте афереза после мобилизации с помощью Г-КСФ двумя методами, а также трудовых и финансовых затрат.
Методы
В качестве стандарта использовался метод подсчета ГСК: подсчет лейкоцитов в камере Горяева и проточная цитофлуориметрия с маркерами CD45/CD34/7AAD (BD; San Jose, USA) на аппарате BD FacsCalibur по протоколу ISHAGE. Исследуемый метод – автоматизированный метод подсчета ГСК, доступный на анализаторах Sysmex XN (XN-HPC) в канале WPC, основанный на измерении размера, структуры и интенсивности флуоресценции клеток. Пробы ПК и продукта афереза забирались для исследований из одних образцов. Заготовка ГСК проводилась на сепараторе COBE Spectra.
Результаты
Представляется клинический случай пациентки Г., 2 г. 4 мес., рост 85,5 см., вес 15 кг, с диагнозом медуллобластома. Для лечения рецидива планируется высокодозная химиотерапии с аутотрансплантацией ГСК. Заготовка ГСК ПК проводилась после стимуляции Г-КСФ в дозе 10 мкг/кг однократно в течение 5-ти дней. На пятый день выполнен аферез. Объем перфузии составил 2900.0 мл, получено 230.0 мл концентрата. Результаты исследований представлены в таблицах: (1) количественное определение ГСК в ПК, (2) оценка количества ГСК в аферезном концентрате, (3) оценка финансовых и трудозатрат (без учета амортизации оборудования и коммунальных затрат).
Выводы
Представленный клинический случай демонстрирует, что результаты количественного определения ГСК на анализаторе Sysmex-XN сопоставимы с результатами рутинного метода, в то время как трудовые и финансовые затраты по меньшей мере в 3 раза ниже. Быстрота получения результата и относительно низкая стоимость позволяет предложить использование количественного определения ГСК на анализаторе Sysmex-XN в качестве дополнительного скринингового метода, результаты которого в дальнейшем будут валидироваться стандартным методом исследования. Внедрение нового скринингового метода определения ГСК приведет к оптимизации алгоритмов проведения афереза и, как следствие, получению трансплантатов ГСК лучшего качества. Тем не менее, для использования нового метода в клинической практике необходимо проведение сравнительных исследований по количественному определению ГСК в ПК и продуктах афереза от широкой когорты доноров/пациентов.
Ключевые слова
Гемопоэтические стволовые клетки, заготовка ГСК, периферическая кровь, продукт афереза, проточная цитометрия, Sysmex-XN, скрининг количества ГСК.
Таблица 1. Результаты исследований ПК

Таблица 2. Результаты исследований аферезного концентрата

Таблица 3. Оценка финансовых и трудозатрат

" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(7570) "
Введение
Рутинным методом определения количества гемопоэтических стволовых клеток (ГСК) является проточная цитофлуориметрия с использованием меченых антител и витального красителя. К серьезным недостаткам данного метода можно отнести сложность стандартизации, отсутствие автоматизации, большие трудозатраты квалифицированного персонала, а также относительная дороговизна расходных материалов. В связи с высокой потребностью частого определения ГСК в периферической крови (ПК) и продуктах афереза существует необходимость разработки стандартизированных, автоматизированных методов. Sysmex-XN является использующимся в клинической практике гематологическом анализатором, имеющим все необходимые возможности для стандартизации проводящихся на нем исследований. В настоящее время разработана возможность определения количества ГСК на Sysmex-XN в канале WPC в режиме XN-HPC. Определение ГСК данным методом является исследовательским, но в перспективе может быть внедрено в клиническую практику в дополнение к рутинному методу в случае получения сопоставимых данных. Целью работы было сравнение данных по количественному определению ГСК в ПК и продукте афереза после мобилизации с помощью Г-КСФ двумя методами, а также трудовых и финансовых затрат.
Методы
В качестве стандарта использовался метод подсчета ГСК: подсчет лейкоцитов в камере Горяева и проточная цитофлуориметрия с маркерами CD45/CD34/7AAD (BD; San Jose, USA) на аппарате BD FacsCalibur по протоколу ISHAGE. Исследуемый метод – автоматизированный метод подсчета ГСК, доступный на анализаторах Sysmex XN (XN-HPC) в канале WPC, основанный на измерении размера, структуры и интенсивности флуоресценции клеток. Пробы ПК и продукта афереза забирались для исследований из одних образцов. Заготовка ГСК проводилась на сепараторе COBE Spectra.
Результаты
Представляется клинический случай пациентки Г., 2 г. 4 мес., рост 85,5 см., вес 15 кг, с диагнозом медуллобластома. Для лечения рецидива планируется высокодозная химиотерапии с аутотрансплантацией ГСК. Заготовка ГСК ПК проводилась после стимуляции Г-КСФ в дозе 10 мкг/кг однократно в течение 5-ти дней. На пятый день выполнен аферез. Объем перфузии составил 2900.0 мл, получено 230.0 мл концентрата. Результаты исследований представлены в таблицах: (1) количественное определение ГСК в ПК, (2) оценка количества ГСК в аферезном концентрате, (3) оценка финансовых и трудозатрат (без учета амортизации оборудования и коммунальных затрат).
Выводы
Представленный клинический случай демонстрирует, что результаты количественного определения ГСК на анализаторе Sysmex-XN сопоставимы с результатами рутинного метода, в то время как трудовые и финансовые затраты по меньшей мере в 3 раза ниже. Быстрота получения результата и относительно низкая стоимость позволяет предложить использование количественного определения ГСК на анализаторе Sysmex-XN в качестве дополнительного скринингового метода, результаты которого в дальнейшем будут валидироваться стандартным методом исследования. Внедрение нового скринингового метода определения ГСК приведет к оптимизации алгоритмов проведения афереза и, как следствие, получению трансплантатов ГСК лучшего качества. Тем не менее, для использования нового метода в клинической практике необходимо проведение сравнительных исследований по количественному определению ГСК в ПК и продуктах афереза от широкой когорты доноров/пациентов.
Ключевые слова
Гемопоэтические стволовые клетки, заготовка ГСК, периферическая кровь, продукт афереза, проточная цитометрия, Sysmex-XN, скрининг количества ГСК.
Таблица 1. Результаты исследований ПК

Таблица 2. Результаты исследований аферезного концентрата

Таблица 3. Оценка финансовых и трудозатрат

" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20670" ["VALUE"]=> array(2) { ["TEXT"]=> string(303) "Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(303) "Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(303) "Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова" } } } [30]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1593" ["~ID"]=> string(4) "1593" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(251) "Случай ЭБВ-ассоциированного лимфопролиферативного заболевания у пациента с тяжелой комбинированной иммунной недостаточностью до ТГСК" ["~NAME"]=> string(251) "Случай ЭБВ-ассоциированного лимфопролиферативного заболевания у пациента с тяжелой комбинированной иммунной недостаточностью до ТГСК" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:47:25" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:47:25" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/sluchay-ebv-assotsiirovannogo-limfoproliferativnogo-zabolevaniya-u-patsienta-s-tyazheloy-kombinirova/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/sluchay-ebv-assotsiirovannogo-limfoproliferativnogo-zabolevaniya-u-patsienta-s-tyazheloy-kombinirova/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "sluchay-ebv-assotsiirovannogo-limfoproliferativnogo-zabolevaniya-u-patsienta-s-tyazheloy-kombinirova" ["~CODE"]=> string(100) "sluchay-ebv-assotsiirovannogo-limfoproliferativnogo-zabolevaniya-u-patsienta-s-tyazheloy-kombinirova" ["EXTERNAL_ID"]=> string(4) "1593" ["~EXTERNAL_ID"]=> string(4) "1593" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(251) "Случай ЭБВ-ассоциированного лимфопролиферативного заболевания у пациента с тяжелой комбинированной иммунной недостаточностью до ТГСК" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(333) "Случай ЭБВ-ассоциированного лимфопролиферативного заболевания у пациента с тяжелой комбинированной иммунной недостаточностью до ТГСКEBV-associated lymphoproliferative (PTLD-like) disease in SCID patient before HSCT" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(4825) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Цель работы: демонстрация клинического случая развития Эпштейн-Барр вирус (ЭБВ)-ассоциированного лимфопролиферативного заболевания (ЛПЗ) у пациента с тяжелой комбинированной иммунной недостаточностью (ТКИН) до трансплантации гемопоэтических стволовых клеток (ТГСК). </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> Пациент, поступил в клинику в возрасте трех месяцев; было проведено обследование, детальный анализ лабораторных и клинических данных, установлен диагноз; терапия была направлена не только на основное заболевание, но и диагностированные осложнения. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Проведенные исследования подтвердили диагноз ТКИН и выявили (КТ, биопсия) ЭБВ-ассоциированное ЛПЗ с поражением средостения. Терапия до ТГСК включала дексаметазон для снижения опухолевого объема и ритуксимаб. На КТ через 2 недели отмечалась положительная динамика. Учитывая основное заболевание далее была проведена трансплантация периферических стволовых кроветворных клеток. Также, в качестве экспериментальной противовирусной терапии, основанной на инфузии ЭБВ-специфических клеток после ТГСК у пациентов с посттрансплантационным ЛПЗ (ПТЛПЗ), на +5 сутки выполнена инфузия CD45-RA деплетированных лимфоцитов. Полное нивелирование очагов в легких (КТ) – на +180 день после ТГСК, что совпало с иммунореконституцией. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Данный случай демонстрирует редкое развитие ЭБВ-ассоциированного ЛПЗ у пациента с ТКИН на первых месяцах жизни до проведения ТГСК. ЛПЗ у пациентов с ТКИН и ПТЛПЗ имеют схожий механизм развития – потеря Т-клеточного контроля. Терапевтические опции в обоих случаях включают применение ритуксимаба и, основанную на передаче активного клеточного иммунитета от донора к реципиенту, клеточную терапию. ЛПЗ регистрируется у ТКИН реже, чем у других первичных иммунодефицитов ввиду их высокой смертности или проведения ТГСК в первые месяцы жизни, что подводит нас к важности правильного диагностического и дифференциально-диагностического поиска у пациента с комбинированным иммунодефицитом, готовящегося к ТГСК, независимо от возраста и комплекса иных клинических проблем. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфопролиферативное заболевание, тяжелая комбинированная иммунная недостаточность, трансплантация гемопоэтических стволовых клеток, вирус Эпштейна-Барр, инфузия донорских лимфоцитов, иммунная реконституция. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(251) "Случай ЭБВ-ассоциированного лимфопролиферативного заболевания у пациента с тяжелой комбинированной иммунной недостаточностью до ТГСК" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(251) "Случай ЭБВ-ассоциированного лимфопролиферативного заболевания у пациента с тяжелой комбинированной иммунной недостаточностью до ТГСК" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(251) "Случай ЭБВ-ассоциированного лимфопролиферативного заболевания у пациента с тяжелой комбинированной иммунной недостаточностью до ТГСК" ["SECTION_META_TITLE"]=> string(251) "Случай ЭБВ-ассоциированного лимфопролиферативного заболевания у пациента с тяжелой комбинированной иммунной недостаточностью до ТГСК" ["SECTION_META_KEYWORDS"]=> string(251) "Случай ЭБВ-ассоциированного лимфопролиферативного заболевания у пациента с тяжелой комбинированной иммунной недостаточностью до ТГСК" ["SECTION_META_DESCRIPTION"]=> string(251) "Случай ЭБВ-ассоциированного лимфопролиферативного заболевания у пациента с тяжелой комбинированной иммунной недостаточностью до ТГСК" ["SECTION_PICTURE_FILE_ALT"]=> string(251) "Случай ЭБВ-ассоциированного лимфопролиферативного заболевания у пациента с тяжелой комбинированной иммунной недостаточностью до ТГСК" ["SECTION_PICTURE_FILE_TITLE"]=> string(251) "Случай ЭБВ-ассоциированного лимфопролиферативного заболевания у пациента с тяжелой комбинированной иммунной недостаточностью до ТГСК" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "sluchay-ebv-assotsiirovannogo-limfoproliferativnogo-zabolevaniya-u-patsienta-s-tyazheloy-kombinirova" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(251) "Случай ЭБВ-ассоциированного лимфопролиферативного заболевания у пациента с тяжелой комбинированной иммунной недостаточностью до ТГСК" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(251) "Случай ЭБВ-ассоциированного лимфопролиферативного заболевания у пациента с тяжелой комбинированной иммунной недостаточностью до ТГСК" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "sluchay-ebv-assotsiirovannogo-limfoproliferativnogo-zabolevaniya-u-patsienta-s-tyazheloy-kombinirova" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "sluchay-ebv-assotsiirovannogo-limfoproliferativnogo-zabolevaniya-u-patsienta-s-tyazheloy-kombinirova" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "sluchay-ebv-assotsiirovannogo-limfoproliferativnogo-zabolevaniya-u-patsienta-s-tyazheloy-kombinirova" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20655" ["VALUE"]=> array(2) { ["TEXT"]=> string(220) "Эльвира Р. Султанова, Александра Л. Лаберко, Анна А. Богоявленская, Сергей Л. Благов, Лариса Н. Шелихова, Дмитрий Н. Балашов" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(220) "Эльвира Р. Султанова, Александра Л. Лаберко, Анна А. Богоявленская, Сергей Л. Благов, Лариса Н. Шелихова, Дмитрий Н. Балашов" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20656" ["VALUE"]=> array(2) { ["TEXT"]=> string(128) "ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России, Москва, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(128) "ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России, Москва, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20657" ["VALUE"]=> array(2) { ["TEXT"]=> string(4825) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Цель работы: демонстрация клинического случая развития Эпштейн-Барр вирус (ЭБВ)-ассоциированного лимфопролиферативного заболевания (ЛПЗ) у пациента с тяжелой комбинированной иммунной недостаточностью (ТКИН) до трансплантации гемопоэтических стволовых клеток (ТГСК). </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> Пациент, поступил в клинику в возрасте трех месяцев; было проведено обследование, детальный анализ лабораторных и клинических данных, установлен диагноз; терапия была направлена не только на основное заболевание, но и диагностированные осложнения. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Проведенные исследования подтвердили диагноз ТКИН и выявили (КТ, биопсия) ЭБВ-ассоциированное ЛПЗ с поражением средостения. Терапия до ТГСК включала дексаметазон для снижения опухолевого объема и ритуксимаб. На КТ через 2 недели отмечалась положительная динамика. Учитывая основное заболевание далее была проведена трансплантация периферических стволовых кроветворных клеток. Также, в качестве экспериментальной противовирусной терапии, основанной на инфузии ЭБВ-специфических клеток после ТГСК у пациентов с посттрансплантационным ЛПЗ (ПТЛПЗ), на +5 сутки выполнена инфузия CD45-RA деплетированных лимфоцитов. Полное нивелирование очагов в легких (КТ) – на +180 день после ТГСК, что совпало с иммунореконституцией. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Данный случай демонстрирует редкое развитие ЭБВ-ассоциированного ЛПЗ у пациента с ТКИН на первых месяцах жизни до проведения ТГСК. ЛПЗ у пациентов с ТКИН и ПТЛПЗ имеют схожий механизм развития – потеря Т-клеточного контроля. Терапевтические опции в обоих случаях включают применение ритуксимаба и, основанную на передаче активного клеточного иммунитета от донора к реципиенту, клеточную терапию. ЛПЗ регистрируется у ТКИН реже, чем у других первичных иммунодефицитов ввиду их высокой смертности или проведения ТГСК в первые месяцы жизни, что подводит нас к важности правильного диагностического и дифференциально-диагностического поиска у пациента с комбинированным иммунодефицитом, готовящегося к ТГСК, независимо от возраста и комплекса иных клинических проблем. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфопролиферативное заболевание, тяжелая комбинированная иммунная недостаточность, трансплантация гемопоэтических стволовых клеток, вирус Эпштейна-Барр, инфузия донорских лимфоцитов, иммунная реконституция. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4593) "
Введение
Цель работы: демонстрация клинического случая развития Эпштейн-Барр вирус (ЭБВ)-ассоциированного лимфопролиферативного заболевания (ЛПЗ) у пациента с тяжелой комбинированной иммунной недостаточностью (ТКИН) до трансплантации гемопоэтических стволовых клеток (ТГСК).
Методы
Пациент, поступил в клинику в возрасте трех месяцев; было проведено обследование, детальный анализ лабораторных и клинических данных, установлен диагноз; терапия была направлена не только на основное заболевание, но и диагностированные осложнения.
Результаты
Проведенные исследования подтвердили диагноз ТКИН и выявили (КТ, биопсия) ЭБВ-ассоциированное ЛПЗ с поражением средостения. Терапия до ТГСК включала дексаметазон для снижения опухолевого объема и ритуксимаб. На КТ через 2 недели отмечалась положительная динамика. Учитывая основное заболевание далее была проведена трансплантация периферических стволовых кроветворных клеток. Также, в качестве экспериментальной противовирусной терапии, основанной на инфузии ЭБВ-специфических клеток после ТГСК у пациентов с посттрансплантационным ЛПЗ (ПТЛПЗ), на +5 сутки выполнена инфузия CD45-RA деплетированных лимфоцитов. Полное нивелирование очагов в легких (КТ) – на +180 день после ТГСК, что совпало с иммунореконституцией.
Заключение
Данный случай демонстрирует редкое развитие ЭБВ-ассоциированного ЛПЗ у пациента с ТКИН на первых месяцах жизни до проведения ТГСК. ЛПЗ у пациентов с ТКИН и ПТЛПЗ имеют схожий механизм развития – потеря Т-клеточного контроля. Терапевтические опции в обоих случаях включают применение ритуксимаба и, основанную на передаче активного клеточного иммунитета от донора к реципиенту, клеточную терапию. ЛПЗ регистрируется у ТКИН реже, чем у других первичных иммунодефицитов ввиду их высокой смертности или проведения ТГСК в первые месяцы жизни, что подводит нас к важности правильного диагностического и дифференциально-диагностического поиска у пациента с комбинированным иммунодефицитом, готовящегося к ТГСК, независимо от возраста и комплекса иных клинических проблем.
Ключевые слова
Лимфопролиферативное заболевание, тяжелая комбинированная иммунная недостаточность, трансплантация гемопоэтических стволовых клеток, вирус Эпштейна-Барр, инфузия донорских лимфоцитов, иммунная реконституция.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20658" ["VALUE"]=> array(2) { ["TEXT"]=> string(126) "Elvira R. Sultanova, Alexandra L. Laberko, Anna A. Bogoyavlenskaya, Sergey L. Blagov, Larisa N. Shelikhova, Dmitry N. Balashov" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(126) "Elvira R. Sultanova, Alexandra L. Laberko, Anna A. Bogoyavlenskaya, Sergey L. Blagov, Larisa N. Shelikhova, Dmitry N. Balashov" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20659" ["VALUE"]=> array(2) { ["TEXT"]=> string(105) "Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(105) "Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20660" ["VALUE"]=> array(2) { ["TEXT"]=> string(2891) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Objective of this work was to demonstrate a case report of Epstein-Barr virus (EBV)-associated lymphoproliferative disease (LPD) in a patient with severe combined immune deficiency (SCID) before hematopoietic stem cell transplantation (HSCT). </p> <h2 style="text-align: justify;">Methods</h2> <p style="text-align: justify;"> The patient at the age of 3 months has been admitted to our hospital and was clinically examined. Detailed analysis of the data was carried out, and diagnosis made. Appropriate treatment targeted at underlying disease as well as the complications diagnosed. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The diagnosis of SCID was confirmed at our clinic. CT scan and lung biopsy showed EBV-associated LPD of the lung. Treatment before HSCT included dexamethasone for cytoreduction, and rituximab administration. CT scan 2 weeks after starting the therapy showed partial reduction in size of the tumor mass. Transplantation of peripheral blood stem cells was the next therapeutic step. Moreover, infusion of CD45-RA depleted lymphocytes was performed on D+5 post-transplant, as an experimental antiviral therapy based on infusion of EBV-specific cells after HSCT in patients with posttransplant LPD (PTLD). At the day +180, a CT scan showed complete resolution of the pulmonary mass, along with immune reconstitution achieved by this time. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The present case demonstrates a rare opportunity for EBV-associated LPD (PTLD-like) developing in a SCID patient within first months of life before HSCT. LPD in SCID patient and PTLD may have similar mechanism, i.e., loss of T-cell control. Treatment options included rituximab, as well as cell therapy, i.e., transfer of active cellular immunity from donor to the recipient. Incidence of LPD in SCID patients is less common than LPD in patient with other primary immune deficiencies, due to high mortality rates among SCID patients before HSCT, or at following months. This case shows importance of correct diagnosis and differential diagnosis in a patient with combined immunodeficiency during his preparation for HSCT, despite of age and other multiple clinical problems. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Lymphoproliferative disease, severe combined immunodeficiency, hematopoietic stem cell transplantation, Epstein-Barr virus, donor lymphocytes infusion, immune reconstitution. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2659) "Introduction
Objective of this work was to demonstrate a case report of Epstein-Barr virus (EBV)-associated lymphoproliferative disease (LPD) in a patient with severe combined immune deficiency (SCID) before hematopoietic stem cell transplantation (HSCT).
Methods
The patient at the age of 3 months has been admitted to our hospital and was clinically examined. Detailed analysis of the data was carried out, and diagnosis made. Appropriate treatment targeted at underlying disease as well as the complications diagnosed.
Results
The diagnosis of SCID was confirmed at our clinic. CT scan and lung biopsy showed EBV-associated LPD of the lung. Treatment before HSCT included dexamethasone for cytoreduction, and rituximab administration. CT scan 2 weeks after starting the therapy showed partial reduction in size of the tumor mass. Transplantation of peripheral blood stem cells was the next therapeutic step. Moreover, infusion of CD45-RA depleted lymphocytes was performed on D+5 post-transplant, as an experimental antiviral therapy based on infusion of EBV-specific cells after HSCT in patients with posttransplant LPD (PTLD). At the day +180, a CT scan showed complete resolution of the pulmonary mass, along with immune reconstitution achieved by this time.
Conclusion
The present case demonstrates a rare opportunity for EBV-associated LPD (PTLD-like) developing in a SCID patient within first months of life before HSCT. LPD in SCID patient and PTLD may have similar mechanism, i.e., loss of T-cell control. Treatment options included rituximab, as well as cell therapy, i.e., transfer of active cellular immunity from donor to the recipient. Incidence of LPD in SCID patients is less common than LPD in patient with other primary immune deficiencies, due to high mortality rates among SCID patients before HSCT, or at following months. This case shows importance of correct diagnosis and differential diagnosis in a patient with combined immunodeficiency during his preparation for HSCT, despite of age and other multiple clinical problems.
Keywords
Lymphoproliferative disease, severe combined immunodeficiency, hematopoietic stem cell transplantation, Epstein-Barr virus, donor lymphocytes infusion, immune reconstitution.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20661" ["VALUE"]=> string(82) "EBV-associated lymphoproliferative (PTLD-like) disease in SCID patient before HSCT" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(82) "EBV-associated lymphoproliferative (PTLD-like) disease in SCID patient before HSCT" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20825" ["VALUE"]=> string(4) "1465" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1465" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20826" ["VALUE"]=> string(4) "1464" ["DESCRIPTION"]=> NULL ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1464" ["~DESCRIPTION"]=> NULL ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20658" ["VALUE"]=> array(2) { ["TEXT"]=> string(126) "Elvira R. Sultanova, Alexandra L. Laberko, Anna A. Bogoyavlenskaya, Sergey L. Blagov, Larisa N. Shelikhova, Dmitry N. Balashov" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(126) "Elvira R. Sultanova, Alexandra L. Laberko, Anna A. Bogoyavlenskaya, Sergey L. Blagov, Larisa N. Shelikhova, Dmitry N. Balashov" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(126) "Elvira R. Sultanova, Alexandra L. Laberko, Anna A. Bogoyavlenskaya, Sergey L. Blagov, Larisa N. Shelikhova, Dmitry N. Balashov" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20660" ["VALUE"]=> array(2) { ["TEXT"]=> string(2891) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Objective of this work was to demonstrate a case report of Epstein-Barr virus (EBV)-associated lymphoproliferative disease (LPD) in a patient with severe combined immune deficiency (SCID) before hematopoietic stem cell transplantation (HSCT). </p> <h2 style="text-align: justify;">Methods</h2> <p style="text-align: justify;"> The patient at the age of 3 months has been admitted to our hospital and was clinically examined. Detailed analysis of the data was carried out, and diagnosis made. Appropriate treatment targeted at underlying disease as well as the complications diagnosed. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The diagnosis of SCID was confirmed at our clinic. CT scan and lung biopsy showed EBV-associated LPD of the lung. Treatment before HSCT included dexamethasone for cytoreduction, and rituximab administration. CT scan 2 weeks after starting the therapy showed partial reduction in size of the tumor mass. Transplantation of peripheral blood stem cells was the next therapeutic step. Moreover, infusion of CD45-RA depleted lymphocytes was performed on D+5 post-transplant, as an experimental antiviral therapy based on infusion of EBV-specific cells after HSCT in patients with posttransplant LPD (PTLD). At the day +180, a CT scan showed complete resolution of the pulmonary mass, along with immune reconstitution achieved by this time. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The present case demonstrates a rare opportunity for EBV-associated LPD (PTLD-like) developing in a SCID patient within first months of life before HSCT. LPD in SCID patient and PTLD may have similar mechanism, i.e., loss of T-cell control. Treatment options included rituximab, as well as cell therapy, i.e., transfer of active cellular immunity from donor to the recipient. Incidence of LPD in SCID patients is less common than LPD in patient with other primary immune deficiencies, due to high mortality rates among SCID patients before HSCT, or at following months. This case shows importance of correct diagnosis and differential diagnosis in a patient with combined immunodeficiency during his preparation for HSCT, despite of age and other multiple clinical problems. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Lymphoproliferative disease, severe combined immunodeficiency, hematopoietic stem cell transplantation, Epstein-Barr virus, donor lymphocytes infusion, immune reconstitution. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2659) "Introduction
Objective of this work was to demonstrate a case report of Epstein-Barr virus (EBV)-associated lymphoproliferative disease (LPD) in a patient with severe combined immune deficiency (SCID) before hematopoietic stem cell transplantation (HSCT).
Methods
The patient at the age of 3 months has been admitted to our hospital and was clinically examined. Detailed analysis of the data was carried out, and diagnosis made. Appropriate treatment targeted at underlying disease as well as the complications diagnosed.
Results
The diagnosis of SCID was confirmed at our clinic. CT scan and lung biopsy showed EBV-associated LPD of the lung. Treatment before HSCT included dexamethasone for cytoreduction, and rituximab administration. CT scan 2 weeks after starting the therapy showed partial reduction in size of the tumor mass. Transplantation of peripheral blood stem cells was the next therapeutic step. Moreover, infusion of CD45-RA depleted lymphocytes was performed on D+5 post-transplant, as an experimental antiviral therapy based on infusion of EBV-specific cells after HSCT in patients with posttransplant LPD (PTLD). At the day +180, a CT scan showed complete resolution of the pulmonary mass, along with immune reconstitution achieved by this time.
Conclusion
The present case demonstrates a rare opportunity for EBV-associated LPD (PTLD-like) developing in a SCID patient within first months of life before HSCT. LPD in SCID patient and PTLD may have similar mechanism, i.e., loss of T-cell control. Treatment options included rituximab, as well as cell therapy, i.e., transfer of active cellular immunity from donor to the recipient. Incidence of LPD in SCID patients is less common than LPD in patient with other primary immune deficiencies, due to high mortality rates among SCID patients before HSCT, or at following months. This case shows importance of correct diagnosis and differential diagnosis in a patient with combined immunodeficiency during his preparation for HSCT, despite of age and other multiple clinical problems.
Keywords
Lymphoproliferative disease, severe combined immunodeficiency, hematopoietic stem cell transplantation, Epstein-Barr virus, donor lymphocytes infusion, immune reconstitution.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2659) "Introduction
Objective of this work was to demonstrate a case report of Epstein-Barr virus (EBV)-associated lymphoproliferative disease (LPD) in a patient with severe combined immune deficiency (SCID) before hematopoietic stem cell transplantation (HSCT).
Methods
The patient at the age of 3 months has been admitted to our hospital and was clinically examined. Detailed analysis of the data was carried out, and diagnosis made. Appropriate treatment targeted at underlying disease as well as the complications diagnosed.
Results
The diagnosis of SCID was confirmed at our clinic. CT scan and lung biopsy showed EBV-associated LPD of the lung. Treatment before HSCT included dexamethasone for cytoreduction, and rituximab administration. CT scan 2 weeks after starting the therapy showed partial reduction in size of the tumor mass. Transplantation of peripheral blood stem cells was the next therapeutic step. Moreover, infusion of CD45-RA depleted lymphocytes was performed on D+5 post-transplant, as an experimental antiviral therapy based on infusion of EBV-specific cells after HSCT in patients with posttransplant LPD (PTLD). At the day +180, a CT scan showed complete resolution of the pulmonary mass, along with immune reconstitution achieved by this time.
Conclusion
The present case demonstrates a rare opportunity for EBV-associated LPD (PTLD-like) developing in a SCID patient within first months of life before HSCT. LPD in SCID patient and PTLD may have similar mechanism, i.e., loss of T-cell control. Treatment options included rituximab, as well as cell therapy, i.e., transfer of active cellular immunity from donor to the recipient. Incidence of LPD in SCID patients is less common than LPD in patient with other primary immune deficiencies, due to high mortality rates among SCID patients before HSCT, or at following months. This case shows importance of correct diagnosis and differential diagnosis in a patient with combined immunodeficiency during his preparation for HSCT, despite of age and other multiple clinical problems.
Keywords
Lymphoproliferative disease, severe combined immunodeficiency, hematopoietic stem cell transplantation, Epstein-Barr virus, donor lymphocytes infusion, immune reconstitution.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20661" ["VALUE"]=> string(82) "EBV-associated lymphoproliferative (PTLD-like) disease in SCID patient before HSCT" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(82) "EBV-associated lymphoproliferative (PTLD-like) disease in SCID patient before HSCT" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(82) "EBV-associated lymphoproliferative (PTLD-like) disease in SCID patient before HSCT" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20659" ["VALUE"]=> array(2) { ["TEXT"]=> string(105) "Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(105) "Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(105) "Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russia" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20655" ["VALUE"]=> array(2) { ["TEXT"]=> string(220) "Эльвира Р. Султанова, Александра Л. Лаберко, Анна А. Богоявленская, Сергей Л. Благов, Лариса Н. Шелихова, Дмитрий Н. Балашов" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(220) "Эльвира Р. Султанова, Александра Л. Лаберко, Анна А. Богоявленская, Сергей Л. Благов, Лариса Н. Шелихова, Дмитрий Н. Балашов" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(220) "Эльвира Р. Султанова, Александра Л. Лаберко, Анна А. Богоявленская, Сергей Л. Благов, Лариса Н. Шелихова, Дмитрий Н. Балашов" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20657" ["VALUE"]=> array(2) { ["TEXT"]=> string(4825) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Цель работы: демонстрация клинического случая развития Эпштейн-Барр вирус (ЭБВ)-ассоциированного лимфопролиферативного заболевания (ЛПЗ) у пациента с тяжелой комбинированной иммунной недостаточностью (ТКИН) до трансплантации гемопоэтических стволовых клеток (ТГСК). </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> Пациент, поступил в клинику в возрасте трех месяцев; было проведено обследование, детальный анализ лабораторных и клинических данных, установлен диагноз; терапия была направлена не только на основное заболевание, но и диагностированные осложнения. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Проведенные исследования подтвердили диагноз ТКИН и выявили (КТ, биопсия) ЭБВ-ассоциированное ЛПЗ с поражением средостения. Терапия до ТГСК включала дексаметазон для снижения опухолевого объема и ритуксимаб. На КТ через 2 недели отмечалась положительная динамика. Учитывая основное заболевание далее была проведена трансплантация периферических стволовых кроветворных клеток. Также, в качестве экспериментальной противовирусной терапии, основанной на инфузии ЭБВ-специфических клеток после ТГСК у пациентов с посттрансплантационным ЛПЗ (ПТЛПЗ), на +5 сутки выполнена инфузия CD45-RA деплетированных лимфоцитов. Полное нивелирование очагов в легких (КТ) – на +180 день после ТГСК, что совпало с иммунореконституцией. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Данный случай демонстрирует редкое развитие ЭБВ-ассоциированного ЛПЗ у пациента с ТКИН на первых месяцах жизни до проведения ТГСК. ЛПЗ у пациентов с ТКИН и ПТЛПЗ имеют схожий механизм развития – потеря Т-клеточного контроля. Терапевтические опции в обоих случаях включают применение ритуксимаба и, основанную на передаче активного клеточного иммунитета от донора к реципиенту, клеточную терапию. ЛПЗ регистрируется у ТКИН реже, чем у других первичных иммунодефицитов ввиду их высокой смертности или проведения ТГСК в первые месяцы жизни, что подводит нас к важности правильного диагностического и дифференциально-диагностического поиска у пациента с комбинированным иммунодефицитом, готовящегося к ТГСК, независимо от возраста и комплекса иных клинических проблем. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфопролиферативное заболевание, тяжелая комбинированная иммунная недостаточность, трансплантация гемопоэтических стволовых клеток, вирус Эпштейна-Барр, инфузия донорских лимфоцитов, иммунная реконституция. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4593) "Введение
Цель работы: демонстрация клинического случая развития Эпштейн-Барр вирус (ЭБВ)-ассоциированного лимфопролиферативного заболевания (ЛПЗ) у пациента с тяжелой комбинированной иммунной недостаточностью (ТКИН) до трансплантации гемопоэтических стволовых клеток (ТГСК).
Методы
Пациент, поступил в клинику в возрасте трех месяцев; было проведено обследование, детальный анализ лабораторных и клинических данных, установлен диагноз; терапия была направлена не только на основное заболевание, но и диагностированные осложнения.
Результаты
Проведенные исследования подтвердили диагноз ТКИН и выявили (КТ, биопсия) ЭБВ-ассоциированное ЛПЗ с поражением средостения. Терапия до ТГСК включала дексаметазон для снижения опухолевого объема и ритуксимаб. На КТ через 2 недели отмечалась положительная динамика. Учитывая основное заболевание далее была проведена трансплантация периферических стволовых кроветворных клеток. Также, в качестве экспериментальной противовирусной терапии, основанной на инфузии ЭБВ-специфических клеток после ТГСК у пациентов с посттрансплантационным ЛПЗ (ПТЛПЗ), на +5 сутки выполнена инфузия CD45-RA деплетированных лимфоцитов. Полное нивелирование очагов в легких (КТ) – на +180 день после ТГСК, что совпало с иммунореконституцией.
Заключение
Данный случай демонстрирует редкое развитие ЭБВ-ассоциированного ЛПЗ у пациента с ТКИН на первых месяцах жизни до проведения ТГСК. ЛПЗ у пациентов с ТКИН и ПТЛПЗ имеют схожий механизм развития – потеря Т-клеточного контроля. Терапевтические опции в обоих случаях включают применение ритуксимаба и, основанную на передаче активного клеточного иммунитета от донора к реципиенту, клеточную терапию. ЛПЗ регистрируется у ТКИН реже, чем у других первичных иммунодефицитов ввиду их высокой смертности или проведения ТГСК в первые месяцы жизни, что подводит нас к важности правильного диагностического и дифференциально-диагностического поиска у пациента с комбинированным иммунодефицитом, готовящегося к ТГСК, независимо от возраста и комплекса иных клинических проблем.
Ключевые слова
Лимфопролиферативное заболевание, тяжелая комбинированная иммунная недостаточность, трансплантация гемопоэтических стволовых клеток, вирус Эпштейна-Барр, инфузия донорских лимфоцитов, иммунная реконституция.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4593) "Введение
Цель работы: демонстрация клинического случая развития Эпштейн-Барр вирус (ЭБВ)-ассоциированного лимфопролиферативного заболевания (ЛПЗ) у пациента с тяжелой комбинированной иммунной недостаточностью (ТКИН) до трансплантации гемопоэтических стволовых клеток (ТГСК).
Методы
Пациент, поступил в клинику в возрасте трех месяцев; было проведено обследование, детальный анализ лабораторных и клинических данных, установлен диагноз; терапия была направлена не только на основное заболевание, но и диагностированные осложнения.
Результаты
Проведенные исследования подтвердили диагноз ТКИН и выявили (КТ, биопсия) ЭБВ-ассоциированное ЛПЗ с поражением средостения. Терапия до ТГСК включала дексаметазон для снижения опухолевого объема и ритуксимаб. На КТ через 2 недели отмечалась положительная динамика. Учитывая основное заболевание далее была проведена трансплантация периферических стволовых кроветворных клеток. Также, в качестве экспериментальной противовирусной терапии, основанной на инфузии ЭБВ-специфических клеток после ТГСК у пациентов с посттрансплантационным ЛПЗ (ПТЛПЗ), на +5 сутки выполнена инфузия CD45-RA деплетированных лимфоцитов. Полное нивелирование очагов в легких (КТ) – на +180 день после ТГСК, что совпало с иммунореконституцией.
Заключение
Данный случай демонстрирует редкое развитие ЭБВ-ассоциированного ЛПЗ у пациента с ТКИН на первых месяцах жизни до проведения ТГСК. ЛПЗ у пациентов с ТКИН и ПТЛПЗ имеют схожий механизм развития – потеря Т-клеточного контроля. Терапевтические опции в обоих случаях включают применение ритуксимаба и, основанную на передаче активного клеточного иммунитета от донора к реципиенту, клеточную терапию. ЛПЗ регистрируется у ТКИН реже, чем у других первичных иммунодефицитов ввиду их высокой смертности или проведения ТГСК в первые месяцы жизни, что подводит нас к важности правильного диагностического и дифференциально-диагностического поиска у пациента с комбинированным иммунодефицитом, готовящегося к ТГСК, независимо от возраста и комплекса иных клинических проблем.
Ключевые слова
Лимфопролиферативное заболевание, тяжелая комбинированная иммунная недостаточность, трансплантация гемопоэтических стволовых клеток, вирус Эпштейна-Барр, инфузия донорских лимфоцитов, иммунная реконституция.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20656" ["VALUE"]=> array(2) { ["TEXT"]=> string(128) "ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России, Москва, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(128) "ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России, Москва, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(128) "ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России, Москва, Россия" } } } [31]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1592" ["~ID"]=> string(4) "1592" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(137) "Идентификация нового аллеля HLA-B*44:02:17 у трех членов афро-американской семьи" ["~NAME"]=> string(137) "Идентификация нового аллеля HLA-B*44:02:17 у трех членов афро-американской семьи" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:44:21" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:44:21" ["DETAIL_PAGE_URL"]=> string(134) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/identifikatsiya-novogo-allelya-hla-b-44-02-17-u-trekh-chlenov-afro-amerikanskoy-semi/" ["~DETAIL_PAGE_URL"]=> string(134) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/identifikatsiya-novogo-allelya-hla-b-44-02-17-u-trekh-chlenov-afro-amerikanskoy-semi/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(84) "identifikatsiya-novogo-allelya-hla-b-44-02-17-u-trekh-chlenov-afro-amerikanskoy-semi" ["~CODE"]=> string(84) "identifikatsiya-novogo-allelya-hla-b-44-02-17-u-trekh-chlenov-afro-amerikanskoy-semi" ["EXTERNAL_ID"]=> string(4) "1592" ["~EXTERNAL_ID"]=> string(4) "1592" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(137) "Идентификация нового аллеля HLA-B*44:02:17 у трех членов афро-американской семьи" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(237) "Идентификация нового аллеля HLA-B*44:02:17 у трех членов афро-американской семьиThe identification of a new HLA-B*44:02:17 allele of the three members of an African-American family" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(1649) "<p style="text-align: justify;"> Была описана идентификация нового аллеля HLA-B* 44:02:17, который был обнаружен в семье афроамериканских индивидуумов во время типирования HLA пациента и доноров для трансплантации костного мозга. Новый аллель HLA-B*44:02:17 отличается от HLA-B* 44: 02:01:01 одним синонимным нуклеотидным изменением в положении 606 bp, кодоном 178, экзон 3 (ACG> ACC, Thr – Silent change). Кроме того, расширенные последовательности HLA-B*44:02:17, за пределами экзонов 2 и 3, были описаны путем клонирования и полноразмерного SBT 3,5 kb фрагмента, простирающегося от 5’-нетранслируемой области до 3’-нетранслируемой области. Название B*44:02:17 было официально присвоено Комитетом номенклатуры ВОЗ. Нуклеотидная последовательность доступна в базе данных IMGT/HLA с номером присоединения HWS100122239. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> HLA-B*44:02, HLA-B*44:02:17, полногеномное секвенирование, ген HLA-B. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(137) "Идентификация нового аллеля HLA-B*44:02:17 у трех членов афро-американской семьи" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(137) "Идентификация нового аллеля HLA-B*44:02:17 у трех членов афро-американской семьи" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(137) "Идентификация нового аллеля HLA-B*44:02:17 у трех членов афро-американской семьи" ["SECTION_META_TITLE"]=> string(137) "Идентификация нового аллеля HLA-B*44:02:17 у трех членов афро-американской семьи" ["SECTION_META_KEYWORDS"]=> string(137) "Идентификация нового аллеля HLA-B*44:02:17 у трех членов афро-американской семьи" ["SECTION_META_DESCRIPTION"]=> string(137) "Идентификация нового аллеля HLA-B*44:02:17 у трех членов афро-американской семьи" ["SECTION_PICTURE_FILE_ALT"]=> string(137) "Идентификация нового аллеля HLA-B*44:02:17 у трех членов афро-американской семьи" ["SECTION_PICTURE_FILE_TITLE"]=> string(137) "Идентификация нового аллеля HLA-B*44:02:17 у трех членов афро-американской семьи" ["SECTION_PICTURE_FILE_NAME"]=> string(88) "identifikatsiya-novogo-allelya-hla-b-44-02-17-u-trekh-chlenov-afro-amerikanskoy-semi-img" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(137) "Идентификация нового аллеля HLA-B*44:02:17 у трех членов афро-американской семьи" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(137) "Идентификация нового аллеля HLA-B*44:02:17 у трех членов афро-американской семьи" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(88) "identifikatsiya-novogo-allelya-hla-b-44-02-17-u-trekh-chlenov-afro-amerikanskoy-semi-img" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(88) "identifikatsiya-novogo-allelya-hla-b-44-02-17-u-trekh-chlenov-afro-amerikanskoy-semi-img" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(88) "identifikatsiya-novogo-allelya-hla-b-44-02-17-u-trekh-chlenov-afro-amerikanskoy-semi-img" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20648" ["VALUE"]=> array(2) { ["TEXT"]=> string(73) "Юрий А. Серов <sup>1</sup>,<sup>2</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(49) "Юрий А. Серов 1,2" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20649" ["VALUE"]=> array(2) { ["TEXT"]=> string(582) "<sup>1</sup> Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация <sup>2</sup> Лаборатория HLA, Медицинский факультет, Университет Индианы, Индианаполис, Индиана, США" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(558) "1 Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация 2 Лаборатория HLA, Медицинский факультет, Университет Индианы, Индианаполис, Индиана, США" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20650" ["VALUE"]=> array(2) { ["TEXT"]=> string(1649) "<p style="text-align: justify;"> Была описана идентификация нового аллеля HLA-B* 44:02:17, который был обнаружен в семье афроамериканских индивидуумов во время типирования HLA пациента и доноров для трансплантации костного мозга. Новый аллель HLA-B*44:02:17 отличается от HLA-B* 44: 02:01:01 одним синонимным нуклеотидным изменением в положении 606 bp, кодоном 178, экзон 3 (ACG> ACC, Thr – Silent change). Кроме того, расширенные последовательности HLA-B*44:02:17, за пределами экзонов 2 и 3, были описаны путем клонирования и полноразмерного SBT 3,5 kb фрагмента, простирающегося от 5’-нетранслируемой области до 3’-нетранслируемой области. Название B*44:02:17 было официально присвоено Комитетом номенклатуры ВОЗ. Нуклеотидная последовательность доступна в базе данных IMGT/HLA с номером присоединения HWS100122239. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> HLA-B*44:02, HLA-B*44:02:17, полногеномное секвенирование, ген HLA-B. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1579) "Была описана идентификация нового аллеля HLA-B* 44:02:17, который был обнаружен в семье афроамериканских индивидуумов во время типирования HLA пациента и доноров для трансплантации костного мозга. Новый аллель HLA-B*44:02:17 отличается от HLA-B* 44: 02:01:01 одним синонимным нуклеотидным изменением в положении 606 bp, кодоном 178, экзон 3 (ACG> ACC, Thr – Silent change). Кроме того, расширенные последовательности HLA-B*44:02:17, за пределами экзонов 2 и 3, были описаны путем клонирования и полноразмерного SBT 3,5 kb фрагмента, простирающегося от 5’-нетранслируемой области до 3’-нетранслируемой области. Название B*44:02:17 было официально присвоено Комитетом номенклатуры ВОЗ. Нуклеотидная последовательность доступна в базе данных IMGT/HLA с номером присоединения HWS100122239.
Ключевые слова
HLA-B*44:02, HLA-B*44:02:17, полногеномное секвенирование, ген HLA-B.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20651" ["VALUE"]=> array(2) { ["TEXT"]=> string(63) "Yury A. Serov <sup>1</sup>,<sup>2</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(39) "Yury A. Serov 1,2" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20652" ["VALUE"]=> array(2) { ["TEXT"]=> string(305) "<sup>1</sup> Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, The First I. P. Pavlov State Medical University, St. Petersburg, Russia. <sup>2</sup> HLA Laboratory, Department of Medicine, Indiana University, Indianapolis, Indiana, USA" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(281) "1 Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, The First I. P. Pavlov State Medical University, St. Petersburg, Russia. 2 HLA Laboratory, Department of Medicine, Indiana University, Indianapolis, Indiana, USA" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20653" ["VALUE"]=> array(2) { ["TEXT"]=> string(1037) "<p style="text-align: justify;"> The identification of the new allele HLA-B*44:02:17 was described, which was found in a family of African American individuals during the HLA typing of a patient for a bone marrow transplant. The new HLA-B*44:02:17 allele differs from HLA-B*44:02:01:01 by one synonymous nucleotide change at position 606 b.p., codon 178, Exon 3 (ACG > ACC, Thr – Silent change). In addition, extended sequences of HLA-B*44:02:17, beyond exons 2 and 3 was reported by cloning and full-length SBT 3.5 kb fragment extending from the 5’ untranslated region to the 3’ untranslated region. The name B*44:02:17 has been officially assigned by the WHO Nomenclature Committee. The nucleotide sequence is available in IMGT/HLA Database with the accession number HWS100122239. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> HLA-B*44:02, HLA-B*44:02:17, full-length sequence-based typing, HLA-B gene. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(967) "The identification of the new allele HLA-B*44:02:17 was described, which was found in a family of African American individuals during the HLA typing of a patient for a bone marrow transplant. The new HLA-B*44:02:17 allele differs from HLA-B*44:02:01:01 by one synonymous nucleotide change at position 606 b.p., codon 178, Exon 3 (ACG > ACC, Thr – Silent change). In addition, extended sequences of HLA-B*44:02:17, beyond exons 2 and 3 was reported by cloning and full-length SBT 3.5 kb fragment extending from the 5’ untranslated region to the 3’ untranslated region. The name B*44:02:17 has been officially assigned by the WHO Nomenclature Committee. The nucleotide sequence is available in IMGT/HLA Database with the accession number HWS100122239.
Keywords
HLA-B*44:02, HLA-B*44:02:17, full-length sequence-based typing, HLA-B gene.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20654" ["VALUE"]=> string(100) "The identification of a new HLA-B*44:02:17 allele of the three members of an African-American family" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(100) "The identification of a new HLA-B*44:02:17 allele of the three members of an African-American family" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20815" ["VALUE"]=> string(4) "1453" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1453" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20816" ["VALUE"]=> string(4) "1454" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1454" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20651" ["VALUE"]=> array(2) { ["TEXT"]=> string(63) "Yury A. Serov <sup>1</sup>,<sup>2</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(39) "Yury A. Serov 1,2" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(39) "Yury A. Serov 1,2" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20653" ["VALUE"]=> array(2) { ["TEXT"]=> string(1037) "<p style="text-align: justify;"> The identification of the new allele HLA-B*44:02:17 was described, which was found in a family of African American individuals during the HLA typing of a patient for a bone marrow transplant. The new HLA-B*44:02:17 allele differs from HLA-B*44:02:01:01 by one synonymous nucleotide change at position 606 b.p., codon 178, Exon 3 (ACG > ACC, Thr – Silent change). In addition, extended sequences of HLA-B*44:02:17, beyond exons 2 and 3 was reported by cloning and full-length SBT 3.5 kb fragment extending from the 5’ untranslated region to the 3’ untranslated region. The name B*44:02:17 has been officially assigned by the WHO Nomenclature Committee. The nucleotide sequence is available in IMGT/HLA Database with the accession number HWS100122239. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> HLA-B*44:02, HLA-B*44:02:17, full-length sequence-based typing, HLA-B gene. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(967) "The identification of the new allele HLA-B*44:02:17 was described, which was found in a family of African American individuals during the HLA typing of a patient for a bone marrow transplant. The new HLA-B*44:02:17 allele differs from HLA-B*44:02:01:01 by one synonymous nucleotide change at position 606 b.p., codon 178, Exon 3 (ACG > ACC, Thr – Silent change). In addition, extended sequences of HLA-B*44:02:17, beyond exons 2 and 3 was reported by cloning and full-length SBT 3.5 kb fragment extending from the 5’ untranslated region to the 3’ untranslated region. The name B*44:02:17 has been officially assigned by the WHO Nomenclature Committee. The nucleotide sequence is available in IMGT/HLA Database with the accession number HWS100122239.
Keywords
HLA-B*44:02, HLA-B*44:02:17, full-length sequence-based typing, HLA-B gene.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(967) "The identification of the new allele HLA-B*44:02:17 was described, which was found in a family of African American individuals during the HLA typing of a patient for a bone marrow transplant. The new HLA-B*44:02:17 allele differs from HLA-B*44:02:01:01 by one synonymous nucleotide change at position 606 b.p., codon 178, Exon 3 (ACG > ACC, Thr – Silent change). In addition, extended sequences of HLA-B*44:02:17, beyond exons 2 and 3 was reported by cloning and full-length SBT 3.5 kb fragment extending from the 5’ untranslated region to the 3’ untranslated region. The name B*44:02:17 has been officially assigned by the WHO Nomenclature Committee. The nucleotide sequence is available in IMGT/HLA Database with the accession number HWS100122239.
Keywords
HLA-B*44:02, HLA-B*44:02:17, full-length sequence-based typing, HLA-B gene.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20654" ["VALUE"]=> string(100) "The identification of a new HLA-B*44:02:17 allele of the three members of an African-American family" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(100) "The identification of a new HLA-B*44:02:17 allele of the three members of an African-American family" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(100) "The identification of a new HLA-B*44:02:17 allele of the three members of an African-American family" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20652" ["VALUE"]=> array(2) { ["TEXT"]=> string(305) "<sup>1</sup> Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, The First I. P. Pavlov State Medical University, St. Petersburg, Russia. <sup>2</sup> HLA Laboratory, Department of Medicine, Indiana University, Indianapolis, Indiana, USA" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(281) "1 Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, The First I. P. Pavlov State Medical University, St. Petersburg, Russia. 2 HLA Laboratory, Department of Medicine, Indiana University, Indianapolis, Indiana, USA" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(281) "1 Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, The First I. P. Pavlov State Medical University, St. Petersburg, Russia. 2 HLA Laboratory, Department of Medicine, Indiana University, Indianapolis, Indiana, USA" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20648" ["VALUE"]=> array(2) { ["TEXT"]=> string(73) "Юрий А. Серов <sup>1</sup>,<sup>2</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(49) "Юрий А. Серов 1,2" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(49) "Юрий А. Серов 1,2" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20650" ["VALUE"]=> array(2) { ["TEXT"]=> string(1649) "<p style="text-align: justify;"> Была описана идентификация нового аллеля HLA-B* 44:02:17, который был обнаружен в семье афроамериканских индивидуумов во время типирования HLA пациента и доноров для трансплантации костного мозга. Новый аллель HLA-B*44:02:17 отличается от HLA-B* 44: 02:01:01 одним синонимным нуклеотидным изменением в положении 606 bp, кодоном 178, экзон 3 (ACG> ACC, Thr – Silent change). Кроме того, расширенные последовательности HLA-B*44:02:17, за пределами экзонов 2 и 3, были описаны путем клонирования и полноразмерного SBT 3,5 kb фрагмента, простирающегося от 5’-нетранслируемой области до 3’-нетранслируемой области. Название B*44:02:17 было официально присвоено Комитетом номенклатуры ВОЗ. Нуклеотидная последовательность доступна в базе данных IMGT/HLA с номером присоединения HWS100122239. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> HLA-B*44:02, HLA-B*44:02:17, полногеномное секвенирование, ген HLA-B. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1579) "Была описана идентификация нового аллеля HLA-B* 44:02:17, который был обнаружен в семье афроамериканских индивидуумов во время типирования HLA пациента и доноров для трансплантации костного мозга. Новый аллель HLA-B*44:02:17 отличается от HLA-B* 44: 02:01:01 одним синонимным нуклеотидным изменением в положении 606 bp, кодоном 178, экзон 3 (ACG> ACC, Thr – Silent change). Кроме того, расширенные последовательности HLA-B*44:02:17, за пределами экзонов 2 и 3, были описаны путем клонирования и полноразмерного SBT 3,5 kb фрагмента, простирающегося от 5’-нетранслируемой области до 3’-нетранслируемой области. Название B*44:02:17 было официально присвоено Комитетом номенклатуры ВОЗ. Нуклеотидная последовательность доступна в базе данных IMGT/HLA с номером присоединения HWS100122239.
Ключевые слова
HLA-B*44:02, HLA-B*44:02:17, полногеномное секвенирование, ген HLA-B.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(1579) "Была описана идентификация нового аллеля HLA-B* 44:02:17, который был обнаружен в семье афроамериканских индивидуумов во время типирования HLA пациента и доноров для трансплантации костного мозга. Новый аллель HLA-B*44:02:17 отличается от HLA-B* 44: 02:01:01 одним синонимным нуклеотидным изменением в положении 606 bp, кодоном 178, экзон 3 (ACG> ACC, Thr – Silent change). Кроме того, расширенные последовательности HLA-B*44:02:17, за пределами экзонов 2 и 3, были описаны путем клонирования и полноразмерного SBT 3,5 kb фрагмента, простирающегося от 5’-нетранслируемой области до 3’-нетранслируемой области. Название B*44:02:17 было официально присвоено Комитетом номенклатуры ВОЗ. Нуклеотидная последовательность доступна в базе данных IMGT/HLA с номером присоединения HWS100122239.
Ключевые слова
HLA-B*44:02, HLA-B*44:02:17, полногеномное секвенирование, ген HLA-B.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20649" ["VALUE"]=> array(2) { ["TEXT"]=> string(582) "<sup>1</sup> Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация <sup>2</sup> Лаборатория HLA, Медицинский факультет, Университет Индианы, Индианаполис, Индиана, США" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(558) "1 Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация 2 Лаборатория HLA, Медицинский факультет, Университет Индианы, Индианаполис, Индиана, США" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(558) "1 Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация 2 Лаборатория HLA, Медицинский факультет, Университет Индианы, Индианаполис, Индиана, США" } } } [32]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1591" ["~ID"]=> string(4) "1591" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(152) "Новый HLA аллель – HLA DQB1*03:31, идентифицированный путем клонирования и секвенирования" ["~NAME"]=> string(152) "Новый HLA аллель – HLA DQB1*03:31, идентифицированный путем клонирования и секвенирования" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:43:33" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:43:33" ["DETAIL_PAGE_URL"]=> string(138) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/novyy-hla-allel-hla-dqb1-03-31-identifitsirovannyy-putem-klonirovaniya-i-sekvenirovaniya/" ["~DETAIL_PAGE_URL"]=> string(138) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/novyy-hla-allel-hla-dqb1-03-31-identifitsirovannyy-putem-klonirovaniya-i-sekvenirovaniya/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(88) "novyy-hla-allel-hla-dqb1-03-31-identifitsirovannyy-putem-klonirovaniya-i-sekvenirovaniya" ["~CODE"]=> string(88) "novyy-hla-allel-hla-dqb1-03-31-identifitsirovannyy-putem-klonirovaniya-i-sekvenirovaniya" ["EXTERNAL_ID"]=> string(4) "1591" ["~EXTERNAL_ID"]=> string(4) "1591" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(152) "Новый HLA аллель – HLA DQB1*03:31, идентифицированный путем клонирования и секвенирования" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(216) "Новый HLA аллель – HLA DQB1*03:31, идентифицированный путем клонирования и секвенированияA new DQB1*03:31 identified by cloning and sequence-based typing" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(2627) "<p style="text-align: justify;"> В процессе HLA типирования пациента для предстоящей пересадки костного мозга и его потенциальных доноров, мы идентифицировали новую аллель HLA DQB1*03:31, в образце ДНК мужчины, потомка американских индейцев. Эта аллель присутствует в гаплотипе HLA A*02:01, B*57:01, C *06:02, DRB1*07:01, DRB4*01:01, DQA1 *02:01, DQB1*03:31. Его другим гаплотипом являются HLA A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3 * 02:02, DQA1*01:01, DQB1*05:03, что так же было обнаружено у донора. Этот новый аллель идентичен HLA DQB1*03:03:02:01-03:03:02:05 в экзоне 2, за исключением кодона 116 (позиция 346 п.н.), где нуклеотидное замещение (GTC> ATC) приводит к мутантной мутации – изменение аминокислоты – Валин на Изолейцин. Название новой аллели – HLA DQB1*03:31 было официально присвоено Комитетом номенклатуры ВОЗ. Это следует за согласованной политикой, которая подчиняется условиям, указанным в последнем отчете о номенклатуре, имена будут назначены новым последовательностям по мере их идентификации. Списки таких новых имен были опубликованы в отчете о номенклатуре ВОЗ. Номер доступа GenBank – HM998989.1. Остаток 116 находится в β1-спирали молекулы HLA класса II, которая является частью кармана F, участвующего в связывании пептидов. Новый аллель содержит изменение аминокислоты в сайте связывания белка HLA антигена, который может изменить его пространственные представляющие свойства. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> HLA DQB1, HLA DQB1*03:31, ген HLA, клонирование, секвенирование. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(152) "Новый HLA аллель – HLA DQB1*03:31, идентифицированный путем клонирования и секвенирования" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(152) "Новый HLA аллель – HLA DQB1*03:31, идентифицированный путем клонирования и секвенирования" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(152) "Новый HLA аллель – HLA DQB1*03:31, идентифицированный путем клонирования и секвенирования" ["SECTION_META_TITLE"]=> string(152) "Новый HLA аллель – HLA DQB1*03:31, идентифицированный путем клонирования и секвенирования" ["SECTION_META_KEYWORDS"]=> string(152) "Новый HLA аллель – HLA DQB1*03:31, идентифицированный путем клонирования и секвенирования" ["SECTION_META_DESCRIPTION"]=> string(152) "Новый HLA аллель – HLA DQB1*03:31, идентифицированный путем клонирования и секвенирования" ["SECTION_PICTURE_FILE_ALT"]=> string(152) "Новый HLA аллель – HLA DQB1*03:31, идентифицированный путем клонирования и секвенирования" ["SECTION_PICTURE_FILE_TITLE"]=> string(152) "Новый HLA аллель – HLA DQB1*03:31, идентифицированный путем клонирования и секвенирования" ["SECTION_PICTURE_FILE_NAME"]=> string(92) "novyy-hla-allel-hla-dqb1-03-31-identifitsirovannyy-putem-klonirovaniya-i-sekvenirovaniya-img" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(152) "Новый HLA аллель – HLA DQB1*03:31, идентифицированный путем клонирования и секвенирования" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(152) "Новый HLA аллель – HLA DQB1*03:31, идентифицированный путем клонирования и секвенирования" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(92) "novyy-hla-allel-hla-dqb1-03-31-identifitsirovannyy-putem-klonirovaniya-i-sekvenirovaniya-img" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(92) "novyy-hla-allel-hla-dqb1-03-31-identifitsirovannyy-putem-klonirovaniya-i-sekvenirovaniya-img" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(92) "novyy-hla-allel-hla-dqb1-03-31-identifitsirovannyy-putem-klonirovaniya-i-sekvenirovaniya-img" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20641" ["VALUE"]=> array(2) { ["TEXT"]=> string(73) "Юрий А. Серов <sup>1</sup>,<sup>2</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(49) "Юрий А. Серов 1,2" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20642" ["VALUE"]=> array(2) { ["TEXT"]=> string(510) "<sup>1</sup> Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский Университет им. акад. И. П. Павлова <sup>2</sup> Лаборатория HLA, Медицинский факультет, Университет Индианы, Индианаполис, Индиана, США" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(486) "1 Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский Университет им. акад. И. П. Павлова 2 Лаборатория HLA, Медицинский факультет, Университет Индианы, Индианаполис, Индиана, США" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20643" ["VALUE"]=> array(2) { ["TEXT"]=> string(2627) "<p style="text-align: justify;"> В процессе HLA типирования пациента для предстоящей пересадки костного мозга и его потенциальных доноров, мы идентифицировали новую аллель HLA DQB1*03:31, в образце ДНК мужчины, потомка американских индейцев. Эта аллель присутствует в гаплотипе HLA A*02:01, B*57:01, C *06:02, DRB1*07:01, DRB4*01:01, DQA1 *02:01, DQB1*03:31. Его другим гаплотипом являются HLA A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3 * 02:02, DQA1*01:01, DQB1*05:03, что так же было обнаружено у донора. Этот новый аллель идентичен HLA DQB1*03:03:02:01-03:03:02:05 в экзоне 2, за исключением кодона 116 (позиция 346 п.н.), где нуклеотидное замещение (GTC> ATC) приводит к мутантной мутации – изменение аминокислоты – Валин на Изолейцин. Название новой аллели – HLA DQB1*03:31 было официально присвоено Комитетом номенклатуры ВОЗ. Это следует за согласованной политикой, которая подчиняется условиям, указанным в последнем отчете о номенклатуре, имена будут назначены новым последовательностям по мере их идентификации. Списки таких новых имен были опубликованы в отчете о номенклатуре ВОЗ. Номер доступа GenBank – HM998989.1. Остаток 116 находится в β1-спирали молекулы HLA класса II, которая является частью кармана F, участвующего в связывании пептидов. Новый аллель содержит изменение аминокислоты в сайте связывания белка HLA антигена, который может изменить его пространственные представляющие свойства. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> HLA DQB1, HLA DQB1*03:31, ген HLA, клонирование, секвенирование. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2557) "В процессе HLA типирования пациента для предстоящей пересадки костного мозга и его потенциальных доноров, мы идентифицировали новую аллель HLA DQB1*03:31, в образце ДНК мужчины, потомка американских индейцев. Эта аллель присутствует в гаплотипе HLA A*02:01, B*57:01, C *06:02, DRB1*07:01, DRB4*01:01, DQA1 *02:01, DQB1*03:31. Его другим гаплотипом являются HLA A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3 * 02:02, DQA1*01:01, DQB1*05:03, что так же было обнаружено у донора. Этот новый аллель идентичен HLA DQB1*03:03:02:01-03:03:02:05 в экзоне 2, за исключением кодона 116 (позиция 346 п.н.), где нуклеотидное замещение (GTC> ATC) приводит к мутантной мутации – изменение аминокислоты – Валин на Изолейцин. Название новой аллели – HLA DQB1*03:31 было официально присвоено Комитетом номенклатуры ВОЗ. Это следует за согласованной политикой, которая подчиняется условиям, указанным в последнем отчете о номенклатуре, имена будут назначены новым последовательностям по мере их идентификации. Списки таких новых имен были опубликованы в отчете о номенклатуре ВОЗ. Номер доступа GenBank – HM998989.1. Остаток 116 находится в β1-спирали молекулы HLA класса II, которая является частью кармана F, участвующего в связывании пептидов. Новый аллель содержит изменение аминокислоты в сайте связывания белка HLA антигена, который может изменить его пространственные представляющие свойства.
Ключевые слова
HLA DQB1, HLA DQB1*03:31, ген HLA, клонирование, секвенирование.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20644" ["VALUE"]=> array(2) { ["TEXT"]=> string(63) "Yury A. Serov <sup>1</sup>,<sup>2</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(39) "Yury A. Serov 1,2" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20645" ["VALUE"]=> array(2) { ["TEXT"]=> string(323) "<sup>1</sup> Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, First I. P. Pavlov State Medical University of St. Petersburg, Russia <sup>2</sup> Histocompatibility Laboratory, Department of Medicine, Indiana University, Indianapolis, Indiana 46202, USA" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(299) "1 Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, First I. P. Pavlov State Medical University of St. Petersburg, Russia 2 Histocompatibility Laboratory, Department of Medicine, Indiana University, Indianapolis, Indiana 46202, USA" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20646" ["VALUE"]=> array(2) { ["TEXT"]=> string(1631) "<p style="text-align: justify;"> In the process of HLA typing bone marrow patient and his potential donors, we have identified the novel DRQB1 allele, DQB1*03:31, in the DNA sample of a male, Native American (American Indian) descendant. This allele is present on the haplotype A* 02:01, B* 57:01, C* 06:02, DRB1* 07:01, DRB4* 01:01, DQA1*02:01, DQB1* 03:31. His other haplotype is A*30:02, is A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3*02:02, DQA1*01:01, DQB1*05:03, which also occurs on the donor. This new allele is identical to DQB1*03:03:02:01-03:03:02:05 in exon 2 except at codon 116 (position 346 b.p. ) where a nucleotide substitution (GTC >ATC) gives rise to a missense mutation – an amino acid change from Valine to Isoleucine.<br> The name of the new allele – DQB1*03:31 has been officially assigned by the WHO Nomenclature Committee. This follows the agreed policy that subjects to the conditions stated in the most recent Nomenclature report, names will be assigned to the new sequences as they are identified. Lists of such new names were published in the following WHO Nomenclature report. The GenBank accession number is HM998989.1.<br> Residue 116 is located in the β1-helix of the HLA class II molecule, which is part of the pocket F involved in peptide binding. The new allele contains an amino acid change in the antigen binding site of the HLA protein, which may alter its presenting properties. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> HLA DQB1, HLA DQ </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1549) "
In the process of HLA typing bone marrow patient and his potential donors, we have identified the novel DRQB1 allele, DQB1*03:31, in the DNA sample of a male, Native American (American Indian) descendant. This allele is present on the haplotype A* 02:01, B* 57:01, C* 06:02, DRB1* 07:01, DRB4* 01:01, DQA1*02:01, DQB1* 03:31. His other haplotype is A*30:02, is A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3*02:02, DQA1*01:01, DQB1*05:03, which also occurs on the donor. This new allele is identical to DQB1*03:03:02:01-03:03:02:05 in exon 2 except at codon 116 (position 346 b.p. ) where a nucleotide substitution (GTC >ATC) gives rise to a missense mutation – an amino acid change from Valine to Isoleucine.
The name of the new allele – DQB1*03:31 has been officially assigned by the WHO Nomenclature Committee. This follows the agreed policy that subjects to the conditions stated in the most recent Nomenclature report, names will be assigned to the new sequences as they are identified. Lists of such new names were published in the following WHO Nomenclature report. The GenBank accession number is HM998989.1.
Residue 116 is located in the β1-helix of the HLA class II molecule, which is part of the pocket F involved in peptide binding. The new allele contains an amino acid change in the antigen binding site of the HLA protein, which may alter its presenting properties.
Keywords
HLA DQB1, HLA DQ
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20647" ["VALUE"]=> string(64) "A new DQB1*03:31 identified by cloning and sequence-based typing" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(64) "A new DQB1*03:31 identified by cloning and sequence-based typing" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20813" ["VALUE"]=> string(4) "1451" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1451" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20814" ["VALUE"]=> string(4) "1452" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1452" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20644" ["VALUE"]=> array(2) { ["TEXT"]=> string(63) "Yury A. Serov <sup>1</sup>,<sup>2</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(39) "Yury A. Serov 1,2" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(39) "Yury A. Serov 1,2" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20646" ["VALUE"]=> array(2) { ["TEXT"]=> string(1631) "<p style="text-align: justify;"> In the process of HLA typing bone marrow patient and his potential donors, we have identified the novel DRQB1 allele, DQB1*03:31, in the DNA sample of a male, Native American (American Indian) descendant. This allele is present on the haplotype A* 02:01, B* 57:01, C* 06:02, DRB1* 07:01, DRB4* 01:01, DQA1*02:01, DQB1* 03:31. His other haplotype is A*30:02, is A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3*02:02, DQA1*01:01, DQB1*05:03, which also occurs on the donor. This new allele is identical to DQB1*03:03:02:01-03:03:02:05 in exon 2 except at codon 116 (position 346 b.p. ) where a nucleotide substitution (GTC >ATC) gives rise to a missense mutation – an amino acid change from Valine to Isoleucine.<br> The name of the new allele – DQB1*03:31 has been officially assigned by the WHO Nomenclature Committee. This follows the agreed policy that subjects to the conditions stated in the most recent Nomenclature report, names will be assigned to the new sequences as they are identified. Lists of such new names were published in the following WHO Nomenclature report. The GenBank accession number is HM998989.1.<br> Residue 116 is located in the β1-helix of the HLA class II molecule, which is part of the pocket F involved in peptide binding. The new allele contains an amino acid change in the antigen binding site of the HLA protein, which may alter its presenting properties. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> HLA DQB1, HLA DQ </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(1549) "
In the process of HLA typing bone marrow patient and his potential donors, we have identified the novel DRQB1 allele, DQB1*03:31, in the DNA sample of a male, Native American (American Indian) descendant. This allele is present on the haplotype A* 02:01, B* 57:01, C* 06:02, DRB1* 07:01, DRB4* 01:01, DQA1*02:01, DQB1* 03:31. His other haplotype is A*30:02, is A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3*02:02, DQA1*01:01, DQB1*05:03, which also occurs on the donor. This new allele is identical to DQB1*03:03:02:01-03:03:02:05 in exon 2 except at codon 116 (position 346 b.p. ) where a nucleotide substitution (GTC >ATC) gives rise to a missense mutation – an amino acid change from Valine to Isoleucine.
The name of the new allele – DQB1*03:31 has been officially assigned by the WHO Nomenclature Committee. This follows the agreed policy that subjects to the conditions stated in the most recent Nomenclature report, names will be assigned to the new sequences as they are identified. Lists of such new names were published in the following WHO Nomenclature report. The GenBank accession number is HM998989.1.
Residue 116 is located in the β1-helix of the HLA class II molecule, which is part of the pocket F involved in peptide binding. The new allele contains an amino acid change in the antigen binding site of the HLA protein, which may alter its presenting properties.
Keywords
HLA DQB1, HLA DQ
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(1549) "
In the process of HLA typing bone marrow patient and his potential donors, we have identified the novel DRQB1 allele, DQB1*03:31, in the DNA sample of a male, Native American (American Indian) descendant. This allele is present on the haplotype A* 02:01, B* 57:01, C* 06:02, DRB1* 07:01, DRB4* 01:01, DQA1*02:01, DQB1* 03:31. His other haplotype is A*30:02, is A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3*02:02, DQA1*01:01, DQB1*05:03, which also occurs on the donor. This new allele is identical to DQB1*03:03:02:01-03:03:02:05 in exon 2 except at codon 116 (position 346 b.p. ) where a nucleotide substitution (GTC >ATC) gives rise to a missense mutation – an amino acid change from Valine to Isoleucine.
The name of the new allele – DQB1*03:31 has been officially assigned by the WHO Nomenclature Committee. This follows the agreed policy that subjects to the conditions stated in the most recent Nomenclature report, names will be assigned to the new sequences as they are identified. Lists of such new names were published in the following WHO Nomenclature report. The GenBank accession number is HM998989.1.
Residue 116 is located in the β1-helix of the HLA class II molecule, which is part of the pocket F involved in peptide binding. The new allele contains an amino acid change in the antigen binding site of the HLA protein, which may alter its presenting properties.
Keywords
HLA DQB1, HLA DQ
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20647" ["VALUE"]=> string(64) "A new DQB1*03:31 identified by cloning and sequence-based typing" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(64) "A new DQB1*03:31 identified by cloning and sequence-based typing" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(64) "A new DQB1*03:31 identified by cloning and sequence-based typing" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20645" ["VALUE"]=> array(2) { ["TEXT"]=> string(323) "<sup>1</sup> Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, First I. P. Pavlov State Medical University of St. Petersburg, Russia <sup>2</sup> Histocompatibility Laboratory, Department of Medicine, Indiana University, Indianapolis, Indiana 46202, USA" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(299) "1 Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, First I. P. Pavlov State Medical University of St. Petersburg, Russia 2 Histocompatibility Laboratory, Department of Medicine, Indiana University, Indianapolis, Indiana 46202, USA" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(299) "1 Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, First I. P. Pavlov State Medical University of St. Petersburg, Russia 2 Histocompatibility Laboratory, Department of Medicine, Indiana University, Indianapolis, Indiana 46202, USA" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20641" ["VALUE"]=> array(2) { ["TEXT"]=> string(73) "Юрий А. Серов <sup>1</sup>,<sup>2</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(49) "Юрий А. Серов 1,2" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(49) "Юрий А. Серов 1,2" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20643" ["VALUE"]=> array(2) { ["TEXT"]=> string(2627) "<p style="text-align: justify;"> В процессе HLA типирования пациента для предстоящей пересадки костного мозга и его потенциальных доноров, мы идентифицировали новую аллель HLA DQB1*03:31, в образце ДНК мужчины, потомка американских индейцев. Эта аллель присутствует в гаплотипе HLA A*02:01, B*57:01, C *06:02, DRB1*07:01, DRB4*01:01, DQA1 *02:01, DQB1*03:31. Его другим гаплотипом являются HLA A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3 * 02:02, DQA1*01:01, DQB1*05:03, что так же было обнаружено у донора. Этот новый аллель идентичен HLA DQB1*03:03:02:01-03:03:02:05 в экзоне 2, за исключением кодона 116 (позиция 346 п.н.), где нуклеотидное замещение (GTC> ATC) приводит к мутантной мутации – изменение аминокислоты – Валин на Изолейцин. Название новой аллели – HLA DQB1*03:31 было официально присвоено Комитетом номенклатуры ВОЗ. Это следует за согласованной политикой, которая подчиняется условиям, указанным в последнем отчете о номенклатуре, имена будут назначены новым последовательностям по мере их идентификации. Списки таких новых имен были опубликованы в отчете о номенклатуре ВОЗ. Номер доступа GenBank – HM998989.1. Остаток 116 находится в β1-спирали молекулы HLA класса II, которая является частью кармана F, участвующего в связывании пептидов. Новый аллель содержит изменение аминокислоты в сайте связывания белка HLA антигена, который может изменить его пространственные представляющие свойства. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> HLA DQB1, HLA DQB1*03:31, ген HLA, клонирование, секвенирование. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2557) "В процессе HLA типирования пациента для предстоящей пересадки костного мозга и его потенциальных доноров, мы идентифицировали новую аллель HLA DQB1*03:31, в образце ДНК мужчины, потомка американских индейцев. Эта аллель присутствует в гаплотипе HLA A*02:01, B*57:01, C *06:02, DRB1*07:01, DRB4*01:01, DQA1 *02:01, DQB1*03:31. Его другим гаплотипом являются HLA A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3 * 02:02, DQA1*01:01, DQB1*05:03, что так же было обнаружено у донора. Этот новый аллель идентичен HLA DQB1*03:03:02:01-03:03:02:05 в экзоне 2, за исключением кодона 116 (позиция 346 п.н.), где нуклеотидное замещение (GTC> ATC) приводит к мутантной мутации – изменение аминокислоты – Валин на Изолейцин. Название новой аллели – HLA DQB1*03:31 было официально присвоено Комитетом номенклатуры ВОЗ. Это следует за согласованной политикой, которая подчиняется условиям, указанным в последнем отчете о номенклатуре, имена будут назначены новым последовательностям по мере их идентификации. Списки таких новых имен были опубликованы в отчете о номенклатуре ВОЗ. Номер доступа GenBank – HM998989.1. Остаток 116 находится в β1-спирали молекулы HLA класса II, которая является частью кармана F, участвующего в связывании пептидов. Новый аллель содержит изменение аминокислоты в сайте связывания белка HLA антигена, который может изменить его пространственные представляющие свойства.
Ключевые слова
HLA DQB1, HLA DQB1*03:31, ген HLA, клонирование, секвенирование.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2557) "В процессе HLA типирования пациента для предстоящей пересадки костного мозга и его потенциальных доноров, мы идентифицировали новую аллель HLA DQB1*03:31, в образце ДНК мужчины, потомка американских индейцев. Эта аллель присутствует в гаплотипе HLA A*02:01, B*57:01, C *06:02, DRB1*07:01, DRB4*01:01, DQA1 *02:01, DQB1*03:31. Его другим гаплотипом являются HLA A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3 * 02:02, DQA1*01:01, DQB1*05:03, что так же было обнаружено у донора. Этот новый аллель идентичен HLA DQB1*03:03:02:01-03:03:02:05 в экзоне 2, за исключением кодона 116 (позиция 346 п.н.), где нуклеотидное замещение (GTC> ATC) приводит к мутантной мутации – изменение аминокислоты – Валин на Изолейцин. Название новой аллели – HLA DQB1*03:31 было официально присвоено Комитетом номенклатуры ВОЗ. Это следует за согласованной политикой, которая подчиняется условиям, указанным в последнем отчете о номенклатуре, имена будут назначены новым последовательностям по мере их идентификации. Списки таких новых имен были опубликованы в отчете о номенклатуре ВОЗ. Номер доступа GenBank – HM998989.1. Остаток 116 находится в β1-спирали молекулы HLA класса II, которая является частью кармана F, участвующего в связывании пептидов. Новый аллель содержит изменение аминокислоты в сайте связывания белка HLA антигена, который может изменить его пространственные представляющие свойства.
Ключевые слова
HLA DQB1, HLA DQB1*03:31, ген HLA, клонирование, секвенирование.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20642" ["VALUE"]=> array(2) { ["TEXT"]=> string(510) "<sup>1</sup> Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский Университет им. акад. И. П. Павлова <sup>2</sup> Лаборатория HLA, Медицинский факультет, Университет Индианы, Индианаполис, Индиана, США" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(486) "1 Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский Университет им. акад. И. П. Павлова 2 Лаборатория HLA, Медицинский факультет, Университет Индианы, Индианаполис, Индиана, США" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(486) "1 Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский Университет им. акад. И. П. Павлова 2 Лаборатория HLA, Медицинский факультет, Университет Индианы, Индианаполис, Индиана, США" } } } [33]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1596" ["~ID"]=> string(4) "1596" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(214) "Ретроспективный анализ использования иксазомиба у пациентов с рецидивирующей/рефрактерной множественной миеломой" ["~NAME"]=> string(214) "Ретроспективный анализ использования иксазомиба у пациентов с рецидивирующей/рефрактерной множественной миеломой" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:45:20" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:45:20" ["DETAIL_PAGE_URL"]=> string(151) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/retrospektivnyy-analiz-ispolzovaniya-iksazomiba-u-patsientov-s-retsidiviruyushchey-refrakternoy-mnozh/" ["~DETAIL_PAGE_URL"]=> string(151) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/retrospektivnyy-analiz-ispolzovaniya-iksazomiba-u-patsientov-s-retsidiviruyushchey-refrakternoy-mnozh/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(101) "retrospektivnyy-analiz-ispolzovaniya-iksazomiba-u-patsientov-s-retsidiviruyushchey-refrakternoy-mnozh" ["~CODE"]=> string(101) "retrospektivnyy-analiz-ispolzovaniya-iksazomiba-u-patsientov-s-retsidiviruyushchey-refrakternoy-mnozh" ["EXTERNAL_ID"]=> string(4) "1596" ["~EXTERNAL_ID"]=> string(4) "1596" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(214) "Ретроспективный анализ использования иксазомиба у пациентов с рецидивирующей/рефрактерной множественной миеломой" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(308) "Ретроспективный анализ использования иксазомиба у пациентов с рецидивирующей/рефрактерной множественной миеломойRetrospective analysis of using ixazomib in patients with relapsed/refractory multiple myeloma" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(7236) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Множественная миелома остается неизлечимым рецидивирующим заболеванием, и новые лекарственные средства являются мишенью исследований, направленных на увеличение беспрогрессивной и общей выживаемости пациентов с множественной миеломой (ММ). Иксазомиб – первый пероральный ингибитор протеасом, показавший свою эффективность в лечении пациентов с рецидивирующей/рефрактерной множественной миеломой. Как недавно появившееся лекарственное средство, иксазомиб нуждается в дальнейших исследованиях. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Был проведен ретроспективный анализ опыта применения препарата у 12 пациентов с ММ. Были оценены эффективность и переносимость режима терапии, основанного на иксазомибе. Пациенты получали терапию в период с декабря 2016 по июль 2018 в научно-исследовательском институте детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой. Каждый пациент имел как минимум одну предшествующую линию терапии и рецидивирующее или рефрактерное течение заболевания. Ответ на терапию оценивался согласно критериям ответа International Myeloma Working Group (Kumar et al., 2016). 11 пациентов (92%) получали режим IRd (иксазомиб+леналидомид+дексаметазон), 1 пациент получал преднизолон вместо дексаметазона. Медиана возраста составляла 65,5 (44-75) лет на момент постановки диагноза и 70 (48-76) на момент начала терапии иксазомибом, 67% (n=8) были мужчинами. Для оценки влияния предшествующей терапии леналидомидом и количества предшествующих линий терапии на частоту общего ответа и частоту очень хорошего частичного ответа (ОХЧО) и полного ответа (ПО) был проведен однофакторный анализ с использованием критерия Хи-квадрат для качественных переменных. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Медиана времени наблюдения составила 10 месяцев. Медиана количества (диапазон) линий терапии составила 8 (2-17) месяцев. Частота общего ответа составила 58% (n=7), из которых 8% (n=1) имели ПО, 17% (n=2) имели ОХЧО и 33% (n=4) имели частичный ответ, как лучший ответ. У 3 пациентов (25%) была отмечена стабилизация заболевания и у 2 пациентов (17%) наблюдалось прогрессирование заболевания. Медиана (диапазон) времени до ответа составила 3 (1-8) месяцев и медиана (диапазон) длительности ответа составила 7 (2-13) месяцев. 11 (92%) пациентов имели как минимум 1 нежелательное явление. У 5 (42%) пациентов наблюдалась анемия (у 2 (17%) – 3 степени)), у 6 (50%) – тромбоцитопения (2 пациента имели 4 степень), у 4 (33%) – нейтропения (у 2 (17%) – 3-4 степени), у 1 (8%) развилась диарея 1 степени, и у 3 (25%) пациентов были отмечены инфекции верхних дыхательных путей. 33% пациентов (n=4) имели нежелательные явления ≥3 степени. До IRd 6 пациентов имели множественные линии терапии, в том числе леналидомид-содержащие, и 6 пациентов были леналидомид-наивными и получили только 1 линию терапии перед IRd. Различия в частоте общего ответа между пациентами с множественными предшествующими линиями терапии (частота общего ответа=33%, n=2) и пациентами, получившими 1 линию терапии перед режимом IRd (частота общего ответа=87%, n=5), не были статистически значимыми (p=0,079). Однако частота ПО и ОХЧО была значительно выше в группе, которая получала IRd, как терапию второй линии (0% против 50%, p=0,046). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Терапия, основанная на иксазомибе, показала хорошую эффективность (частота общего ответа 58%) и приемлемую токсичность. Пациенты, не получавшие ранее леналидомид и имевшие только 1 предшествующую линию терапии, имеют статистически значимо более высокую частоту ПО и ОЧХО. На основе этого, можно предположить, что использование режима IRd в качестве терапии второй линии может улучшить глубину ответа пациентов с ММ, включая резистентные формы. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Миеломная болезнь, рефрактерная форма, рецидивы, иксазомиб, эффективность. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(214) "Ретроспективный анализ использования иксазомиба у пациентов с рецидивирующей/рефрактерной множественной миеломой" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(214) "Ретроспективный анализ использования иксазомиба у пациентов с рецидивирующей/рефрактерной множественной миеломой" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(214) "Ретроспективный анализ использования иксазомиба у пациентов с рецидивирующей/рефрактерной множественной миеломой" ["SECTION_META_TITLE"]=> string(214) "Ретроспективный анализ использования иксазомиба у пациентов с рецидивирующей/рефрактерной множественной миеломой" ["SECTION_META_KEYWORDS"]=> string(214) "Ретроспективный анализ использования иксазомиба у пациентов с рецидивирующей/рефрактерной множественной миеломой" ["SECTION_META_DESCRIPTION"]=> string(214) "Ретроспективный анализ использования иксазомиба у пациентов с рецидивирующей/рефрактерной множественной миеломой" ["SECTION_PICTURE_FILE_ALT"]=> string(214) "Ретроспективный анализ использования иксазомиба у пациентов с рецидивирующей/рефрактерной множественной миеломой" ["SECTION_PICTURE_FILE_TITLE"]=> string(214) "Ретроспективный анализ использования иксазомиба у пациентов с рецидивирующей/рефрактерной множественной миеломой" ["SECTION_PICTURE_FILE_NAME"]=> string(101) "retrospektivnyy-analiz-ispolzovaniya-iksazomiba-u-patsientov-s-retsidiviruyushchey-refrakternoy-mnozh" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(214) "Ретроспективный анализ использования иксазомиба у пациентов с рецидивирующей/рефрактерной множественной миеломой" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(214) "Ретроспективный анализ использования иксазомиба у пациентов с рецидивирующей/рефрактерной множественной миеломой" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(101) "retrospektivnyy-analiz-ispolzovaniya-iksazomiba-u-patsientov-s-retsidiviruyushchey-refrakternoy-mnozh" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(101) "retrospektivnyy-analiz-ispolzovaniya-iksazomiba-u-patsientov-s-retsidiviruyushchey-refrakternoy-mnozh" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(101) "retrospektivnyy-analiz-ispolzovaniya-iksazomiba-u-patsientov-s-retsidiviruyushchey-refrakternoy-mnozh" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20676" ["VALUE"]=> array(2) { ["TEXT"]=> string(239) "Даниил И. Шмидт, Ольга В. Пирогова, Валентина В. Порунова, Ольга В. Кудяшева, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(239) "Даниил И. Шмидт, Ольга В. Пирогова, Валентина В. Порунова, Ольга В. Кудяшева, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20677" ["VALUE"]=> array(2) { ["TEXT"]=> string(484) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(484) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20678" ["VALUE"]=> array(2) { ["TEXT"]=> string(7236) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Множественная миелома остается неизлечимым рецидивирующим заболеванием, и новые лекарственные средства являются мишенью исследований, направленных на увеличение беспрогрессивной и общей выживаемости пациентов с множественной миеломой (ММ). Иксазомиб – первый пероральный ингибитор протеасом, показавший свою эффективность в лечении пациентов с рецидивирующей/рефрактерной множественной миеломой. Как недавно появившееся лекарственное средство, иксазомиб нуждается в дальнейших исследованиях. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Был проведен ретроспективный анализ опыта применения препарата у 12 пациентов с ММ. Были оценены эффективность и переносимость режима терапии, основанного на иксазомибе. Пациенты получали терапию в период с декабря 2016 по июль 2018 в научно-исследовательском институте детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой. Каждый пациент имел как минимум одну предшествующую линию терапии и рецидивирующее или рефрактерное течение заболевания. Ответ на терапию оценивался согласно критериям ответа International Myeloma Working Group (Kumar et al., 2016). 11 пациентов (92%) получали режим IRd (иксазомиб+леналидомид+дексаметазон), 1 пациент получал преднизолон вместо дексаметазона. Медиана возраста составляла 65,5 (44-75) лет на момент постановки диагноза и 70 (48-76) на момент начала терапии иксазомибом, 67% (n=8) были мужчинами. Для оценки влияния предшествующей терапии леналидомидом и количества предшествующих линий терапии на частоту общего ответа и частоту очень хорошего частичного ответа (ОХЧО) и полного ответа (ПО) был проведен однофакторный анализ с использованием критерия Хи-квадрат для качественных переменных. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Медиана времени наблюдения составила 10 месяцев. Медиана количества (диапазон) линий терапии составила 8 (2-17) месяцев. Частота общего ответа составила 58% (n=7), из которых 8% (n=1) имели ПО, 17% (n=2) имели ОХЧО и 33% (n=4) имели частичный ответ, как лучший ответ. У 3 пациентов (25%) была отмечена стабилизация заболевания и у 2 пациентов (17%) наблюдалось прогрессирование заболевания. Медиана (диапазон) времени до ответа составила 3 (1-8) месяцев и медиана (диапазон) длительности ответа составила 7 (2-13) месяцев. 11 (92%) пациентов имели как минимум 1 нежелательное явление. У 5 (42%) пациентов наблюдалась анемия (у 2 (17%) – 3 степени)), у 6 (50%) – тромбоцитопения (2 пациента имели 4 степень), у 4 (33%) – нейтропения (у 2 (17%) – 3-4 степени), у 1 (8%) развилась диарея 1 степени, и у 3 (25%) пациентов были отмечены инфекции верхних дыхательных путей. 33% пациентов (n=4) имели нежелательные явления ≥3 степени. До IRd 6 пациентов имели множественные линии терапии, в том числе леналидомид-содержащие, и 6 пациентов были леналидомид-наивными и получили только 1 линию терапии перед IRd. Различия в частоте общего ответа между пациентами с множественными предшествующими линиями терапии (частота общего ответа=33%, n=2) и пациентами, получившими 1 линию терапии перед режимом IRd (частота общего ответа=87%, n=5), не были статистически значимыми (p=0,079). Однако частота ПО и ОХЧО была значительно выше в группе, которая получала IRd, как терапию второй линии (0% против 50%, p=0,046). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Терапия, основанная на иксазомибе, показала хорошую эффективность (частота общего ответа 58%) и приемлемую токсичность. Пациенты, не получавшие ранее леналидомид и имевшие только 1 предшествующую линию терапии, имеют статистически значимо более высокую частоту ПО и ОЧХО. На основе этого, можно предположить, что использование режима IRd в качестве терапии второй линии может улучшить глубину ответа пациентов с ММ, включая резистентные формы. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Миеломная болезнь, рефрактерная форма, рецидивы, иксазомиб, эффективность. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7004) "Введение
Множественная миелома остается неизлечимым рецидивирующим заболеванием, и новые лекарственные средства являются мишенью исследований, направленных на увеличение беспрогрессивной и общей выживаемости пациентов с множественной миеломой (ММ). Иксазомиб – первый пероральный ингибитор протеасом, показавший свою эффективность в лечении пациентов с рецидивирующей/рефрактерной множественной миеломой. Как недавно появившееся лекарственное средство, иксазомиб нуждается в дальнейших исследованиях.
Пациенты и методы
Был проведен ретроспективный анализ опыта применения препарата у 12 пациентов с ММ. Были оценены эффективность и переносимость режима терапии, основанного на иксазомибе. Пациенты получали терапию в период с декабря 2016 по июль 2018 в научно-исследовательском институте детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой. Каждый пациент имел как минимум одну предшествующую линию терапии и рецидивирующее или рефрактерное течение заболевания. Ответ на терапию оценивался согласно критериям ответа International Myeloma Working Group (Kumar et al., 2016). 11 пациентов (92%) получали режим IRd (иксазомиб+леналидомид+дексаметазон), 1 пациент получал преднизолон вместо дексаметазона. Медиана возраста составляла 65,5 (44-75) лет на момент постановки диагноза и 70 (48-76) на момент начала терапии иксазомибом, 67% (n=8) были мужчинами. Для оценки влияния предшествующей терапии леналидомидом и количества предшествующих линий терапии на частоту общего ответа и частоту очень хорошего частичного ответа (ОХЧО) и полного ответа (ПО) был проведен однофакторный анализ с использованием критерия Хи-квадрат для качественных переменных.
Результаты
Медиана времени наблюдения составила 10 месяцев. Медиана количества (диапазон) линий терапии составила 8 (2-17) месяцев. Частота общего ответа составила 58% (n=7), из которых 8% (n=1) имели ПО, 17% (n=2) имели ОХЧО и 33% (n=4) имели частичный ответ, как лучший ответ. У 3 пациентов (25%) была отмечена стабилизация заболевания и у 2 пациентов (17%) наблюдалось прогрессирование заболевания. Медиана (диапазон) времени до ответа составила 3 (1-8) месяцев и медиана (диапазон) длительности ответа составила 7 (2-13) месяцев. 11 (92%) пациентов имели как минимум 1 нежелательное явление. У 5 (42%) пациентов наблюдалась анемия (у 2 (17%) – 3 степени)), у 6 (50%) – тромбоцитопения (2 пациента имели 4 степень), у 4 (33%) – нейтропения (у 2 (17%) – 3-4 степени), у 1 (8%) развилась диарея 1 степени, и у 3 (25%) пациентов были отмечены инфекции верхних дыхательных путей. 33% пациентов (n=4) имели нежелательные явления ≥3 степени. До IRd 6 пациентов имели множественные линии терапии, в том числе леналидомид-содержащие, и 6 пациентов были леналидомид-наивными и получили только 1 линию терапии перед IRd. Различия в частоте общего ответа между пациентами с множественными предшествующими линиями терапии (частота общего ответа=33%, n=2) и пациентами, получившими 1 линию терапии перед режимом IRd (частота общего ответа=87%, n=5), не были статистически значимыми (p=0,079). Однако частота ПО и ОХЧО была значительно выше в группе, которая получала IRd, как терапию второй линии (0% против 50%, p=0,046).
Заключение
Терапия, основанная на иксазомибе, показала хорошую эффективность (частота общего ответа 58%) и приемлемую токсичность. Пациенты, не получавшие ранее леналидомид и имевшие только 1 предшествующую линию терапии, имеют статистически значимо более высокую частоту ПО и ОЧХО. На основе этого, можно предположить, что использование режима IRd в качестве терапии второй линии может улучшить глубину ответа пациентов с ММ, включая резистентные формы.
Ключевые слова
Миеломная болезнь, рефрактерная форма, рецидивы, иксазомиб, эффективность.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20679" ["VALUE"]=> array(2) { ["TEXT"]=> string(138) "Daniil I. Shmidt, Olga V. Pirogova, Valentina V. Porunova, Olga V. Kudyasheva, Elena I. Darskaya, Sergey N. Bondarenko, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(138) "Daniil I. Shmidt, Olga V. Pirogova, Valentina V. Porunova, Olga V. Kudyasheva, Elena I. Darskaya, Sergey N. Bondarenko, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20680" ["VALUE"]=> array(2) { ["TEXT"]=> string(230) "R. M. Gorbacheva Memorial Institute of Oncology, Hematology and Transplantation; Chair of Hematology, Transfusiology and Transplantology, Pavlov First Saint Petersburg State Medical University, Saint Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(230) "R. M. Gorbacheva Memorial Institute of Oncology, Hematology and Transplantation; Chair of Hematology, Transfusiology and Transplantology, Pavlov First Saint Petersburg State Medical University, Saint Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20681" ["VALUE"]=> array(2) { ["TEXT"]=> string(4032) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Multiple myeloma (MM) remains incurable relapsing disease and novel agents are under investigation in order to prolong progression-free and overall survival of MM patients (pts). Ixazomib is the first oral proteasome inhibitor that showed effectiveness in relapsed/refractory MM. Patients (pts) refractory to prior bortezomib therapy are often responsive to ixazomib treatment. As newly introduced agent, ixazomib requires further investigation. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Retrospective analysis of a single-center experience was performed in 12 pts with MM. Efficacy and tolerability of ixazomibe-based regimen was assessed. These patients were treated with ixazomib between December 2016 and July 2018 in Raisa Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation. All of them had at list one prior line therapy and relapsed or refractory disease. Response to treatment was assessed according to International Myeloma Working Group consensus criteria for response and minimal residual disease assessment in multiple myeloma (Kumar et al., 2016). 11 pts (92%) received IRd treatment regimen (ixazomib+ lenalidomide+ dexamethasone) and 1 patient was treated with prednisolone instead of dexamethasone. Median age was 65.5 (44-75) years at the time of diagnosis, and 70 (48-76) at the start of IRd treatment. 67% (n=8) were males. To assess impact of prior lenalidomide therapy and number of prior treatments on overall response rate (ORR) and rate of complete response (CR) and very good partial response (VGPR) univariate analysis was performed using Chi-square tests for categorical variables. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The median follow-up was 10 months. Median treatment cycles (range) was 8 (2-17). Overall response rate was 58% (n=7), of which 8% (n=1) had CR, 17% (n=2) had VGPR, 33% (n=4) had partial response (PR) as best response. 3 pts (25%) were considered to have stable disease and 2 pts (17%) showed the disease progression. Median (range) time to response was 3 (1-8) months and median (range) response duration was 7 (2-13) months. Eleven patients (92%) had, at least, one adverse event. 5 (42%) developed anemia: 2 (17%) had grade 3 anemia), 6 (50%) had thrombocytopenia (2 pts with grade 4); 4 (33%) had neutropenia: 2 (17%), with grade 3-4; 1 patient (8%) exhibited grade 1 diarrhea, and 3 patients (25%) had upper respiratory tract infections. 33% (n=4) of the patients had adverse events (grade ≥3). Before IRd, 6 pts had multiple lines of treatment including lenalidomide and 6 pts were lenalidomide-naïve and received only one line of treatment. Difference in ORR was not statistically significant between patients with multiple lines of previous treatment (ORR=33%, n=2), and cases with one line of prior therapy (ORR=87%, n=5) (p=0.079), but CR and VGPR rate were significantly higher in the group who received IRd as second-line treatment (0% vs 50%, p=0.046). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Ixazomib-based treatment showed good efficacy (ORR=58%) and acceptable toxicity. Patients without prior lenalidomide and one prior line of treatment had statistically significant improvement in VGPR and CR rate. From this basis, it can be assumed that use of IRd regimen as the second-line therapy may improve depth of response in relapsed/refractory multiple myeloma patients. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Multiple myeloma, relapsed, refractory, ixazomib, efficiency. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3800) "Introduction
Multiple myeloma (MM) remains incurable relapsing disease and novel agents are under investigation in order to prolong progression-free and overall survival of MM patients (pts). Ixazomib is the first oral proteasome inhibitor that showed effectiveness in relapsed/refractory MM. Patients (pts) refractory to prior bortezomib therapy are often responsive to ixazomib treatment. As newly introduced agent, ixazomib requires further investigation.
Patients and methods
Retrospective analysis of a single-center experience was performed in 12 pts with MM. Efficacy and tolerability of ixazomibe-based regimen was assessed. These patients were treated with ixazomib between December 2016 and July 2018 in Raisa Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation. All of them had at list one prior line therapy and relapsed or refractory disease. Response to treatment was assessed according to International Myeloma Working Group consensus criteria for response and minimal residual disease assessment in multiple myeloma (Kumar et al., 2016). 11 pts (92%) received IRd treatment regimen (ixazomib+ lenalidomide+ dexamethasone) and 1 patient was treated with prednisolone instead of dexamethasone. Median age was 65.5 (44-75) years at the time of diagnosis, and 70 (48-76) at the start of IRd treatment. 67% (n=8) were males. To assess impact of prior lenalidomide therapy and number of prior treatments on overall response rate (ORR) and rate of complete response (CR) and very good partial response (VGPR) univariate analysis was performed using Chi-square tests for categorical variables.
Results
The median follow-up was 10 months. Median treatment cycles (range) was 8 (2-17). Overall response rate was 58% (n=7), of which 8% (n=1) had CR, 17% (n=2) had VGPR, 33% (n=4) had partial response (PR) as best response. 3 pts (25%) were considered to have stable disease and 2 pts (17%) showed the disease progression. Median (range) time to response was 3 (1-8) months and median (range) response duration was 7 (2-13) months. Eleven patients (92%) had, at least, one adverse event. 5 (42%) developed anemia: 2 (17%) had grade 3 anemia), 6 (50%) had thrombocytopenia (2 pts with grade 4); 4 (33%) had neutropenia: 2 (17%), with grade 3-4; 1 patient (8%) exhibited grade 1 diarrhea, and 3 patients (25%) had upper respiratory tract infections. 33% (n=4) of the patients had adverse events (grade ≥3). Before IRd, 6 pts had multiple lines of treatment including lenalidomide and 6 pts were lenalidomide-naïve and received only one line of treatment. Difference in ORR was not statistically significant between patients with multiple lines of previous treatment (ORR=33%, n=2), and cases with one line of prior therapy (ORR=87%, n=5) (p=0.079), but CR and VGPR rate were significantly higher in the group who received IRd as second-line treatment (0% vs 50%, p=0.046).
Conclusion
Ixazomib-based treatment showed good efficacy (ORR=58%) and acceptable toxicity. Patients without prior lenalidomide and one prior line of treatment had statistically significant improvement in VGPR and CR rate. From this basis, it can be assumed that use of IRd regimen as the second-line therapy may improve depth of response in relapsed/refractory multiple myeloma patients.
Keywords
Multiple myeloma, relapsed, refractory, ixazomib, efficiency.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20682" ["VALUE"]=> string(94) "Retrospective analysis of using ixazomib in patients with relapsed/refractory multiple myeloma" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(94) "Retrospective analysis of using ixazomib in patients with relapsed/refractory multiple myeloma" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20819" ["VALUE"]=> string(4) "1457" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1457" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20820" ["VALUE"]=> string(4) "1458" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1458" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20679" ["VALUE"]=> array(2) { ["TEXT"]=> string(138) "Daniil I. Shmidt, Olga V. Pirogova, Valentina V. Porunova, Olga V. Kudyasheva, Elena I. Darskaya, Sergey N. Bondarenko, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(138) "Daniil I. Shmidt, Olga V. Pirogova, Valentina V. Porunova, Olga V. Kudyasheva, Elena I. Darskaya, Sergey N. Bondarenko, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(138) "Daniil I. Shmidt, Olga V. Pirogova, Valentina V. Porunova, Olga V. Kudyasheva, Elena I. Darskaya, Sergey N. Bondarenko, Boris V. Afanasyev" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20681" ["VALUE"]=> array(2) { ["TEXT"]=> string(4032) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Multiple myeloma (MM) remains incurable relapsing disease and novel agents are under investigation in order to prolong progression-free and overall survival of MM patients (pts). Ixazomib is the first oral proteasome inhibitor that showed effectiveness in relapsed/refractory MM. Patients (pts) refractory to prior bortezomib therapy are often responsive to ixazomib treatment. As newly introduced agent, ixazomib requires further investigation. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Retrospective analysis of a single-center experience was performed in 12 pts with MM. Efficacy and tolerability of ixazomibe-based regimen was assessed. These patients were treated with ixazomib between December 2016 and July 2018 in Raisa Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation. All of them had at list one prior line therapy and relapsed or refractory disease. Response to treatment was assessed according to International Myeloma Working Group consensus criteria for response and minimal residual disease assessment in multiple myeloma (Kumar et al., 2016). 11 pts (92%) received IRd treatment regimen (ixazomib+ lenalidomide+ dexamethasone) and 1 patient was treated with prednisolone instead of dexamethasone. Median age was 65.5 (44-75) years at the time of diagnosis, and 70 (48-76) at the start of IRd treatment. 67% (n=8) were males. To assess impact of prior lenalidomide therapy and number of prior treatments on overall response rate (ORR) and rate of complete response (CR) and very good partial response (VGPR) univariate analysis was performed using Chi-square tests for categorical variables. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The median follow-up was 10 months. Median treatment cycles (range) was 8 (2-17). Overall response rate was 58% (n=7), of which 8% (n=1) had CR, 17% (n=2) had VGPR, 33% (n=4) had partial response (PR) as best response. 3 pts (25%) were considered to have stable disease and 2 pts (17%) showed the disease progression. Median (range) time to response was 3 (1-8) months and median (range) response duration was 7 (2-13) months. Eleven patients (92%) had, at least, one adverse event. 5 (42%) developed anemia: 2 (17%) had grade 3 anemia), 6 (50%) had thrombocytopenia (2 pts with grade 4); 4 (33%) had neutropenia: 2 (17%), with grade 3-4; 1 patient (8%) exhibited grade 1 diarrhea, and 3 patients (25%) had upper respiratory tract infections. 33% (n=4) of the patients had adverse events (grade ≥3). Before IRd, 6 pts had multiple lines of treatment including lenalidomide and 6 pts were lenalidomide-naïve and received only one line of treatment. Difference in ORR was not statistically significant between patients with multiple lines of previous treatment (ORR=33%, n=2), and cases with one line of prior therapy (ORR=87%, n=5) (p=0.079), but CR and VGPR rate were significantly higher in the group who received IRd as second-line treatment (0% vs 50%, p=0.046). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Ixazomib-based treatment showed good efficacy (ORR=58%) and acceptable toxicity. Patients without prior lenalidomide and one prior line of treatment had statistically significant improvement in VGPR and CR rate. From this basis, it can be assumed that use of IRd regimen as the second-line therapy may improve depth of response in relapsed/refractory multiple myeloma patients. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Multiple myeloma, relapsed, refractory, ixazomib, efficiency. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3800) "Introduction
Multiple myeloma (MM) remains incurable relapsing disease and novel agents are under investigation in order to prolong progression-free and overall survival of MM patients (pts). Ixazomib is the first oral proteasome inhibitor that showed effectiveness in relapsed/refractory MM. Patients (pts) refractory to prior bortezomib therapy are often responsive to ixazomib treatment. As newly introduced agent, ixazomib requires further investigation.
Patients and methods
Retrospective analysis of a single-center experience was performed in 12 pts with MM. Efficacy and tolerability of ixazomibe-based regimen was assessed. These patients were treated with ixazomib between December 2016 and July 2018 in Raisa Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation. All of them had at list one prior line therapy and relapsed or refractory disease. Response to treatment was assessed according to International Myeloma Working Group consensus criteria for response and minimal residual disease assessment in multiple myeloma (Kumar et al., 2016). 11 pts (92%) received IRd treatment regimen (ixazomib+ lenalidomide+ dexamethasone) and 1 patient was treated with prednisolone instead of dexamethasone. Median age was 65.5 (44-75) years at the time of diagnosis, and 70 (48-76) at the start of IRd treatment. 67% (n=8) were males. To assess impact of prior lenalidomide therapy and number of prior treatments on overall response rate (ORR) and rate of complete response (CR) and very good partial response (VGPR) univariate analysis was performed using Chi-square tests for categorical variables.
Results
The median follow-up was 10 months. Median treatment cycles (range) was 8 (2-17). Overall response rate was 58% (n=7), of which 8% (n=1) had CR, 17% (n=2) had VGPR, 33% (n=4) had partial response (PR) as best response. 3 pts (25%) were considered to have stable disease and 2 pts (17%) showed the disease progression. Median (range) time to response was 3 (1-8) months and median (range) response duration was 7 (2-13) months. Eleven patients (92%) had, at least, one adverse event. 5 (42%) developed anemia: 2 (17%) had grade 3 anemia), 6 (50%) had thrombocytopenia (2 pts with grade 4); 4 (33%) had neutropenia: 2 (17%), with grade 3-4; 1 patient (8%) exhibited grade 1 diarrhea, and 3 patients (25%) had upper respiratory tract infections. 33% (n=4) of the patients had adverse events (grade ≥3). Before IRd, 6 pts had multiple lines of treatment including lenalidomide and 6 pts were lenalidomide-naïve and received only one line of treatment. Difference in ORR was not statistically significant between patients with multiple lines of previous treatment (ORR=33%, n=2), and cases with one line of prior therapy (ORR=87%, n=5) (p=0.079), but CR and VGPR rate were significantly higher in the group who received IRd as second-line treatment (0% vs 50%, p=0.046).
Conclusion
Ixazomib-based treatment showed good efficacy (ORR=58%) and acceptable toxicity. Patients without prior lenalidomide and one prior line of treatment had statistically significant improvement in VGPR and CR rate. From this basis, it can be assumed that use of IRd regimen as the second-line therapy may improve depth of response in relapsed/refractory multiple myeloma patients.
Keywords
Multiple myeloma, relapsed, refractory, ixazomib, efficiency.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3800) "Introduction
Multiple myeloma (MM) remains incurable relapsing disease and novel agents are under investigation in order to prolong progression-free and overall survival of MM patients (pts). Ixazomib is the first oral proteasome inhibitor that showed effectiveness in relapsed/refractory MM. Patients (pts) refractory to prior bortezomib therapy are often responsive to ixazomib treatment. As newly introduced agent, ixazomib requires further investigation.
Patients and methods
Retrospective analysis of a single-center experience was performed in 12 pts with MM. Efficacy and tolerability of ixazomibe-based regimen was assessed. These patients were treated with ixazomib between December 2016 and July 2018 in Raisa Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation. All of them had at list one prior line therapy and relapsed or refractory disease. Response to treatment was assessed according to International Myeloma Working Group consensus criteria for response and minimal residual disease assessment in multiple myeloma (Kumar et al., 2016). 11 pts (92%) received IRd treatment regimen (ixazomib+ lenalidomide+ dexamethasone) and 1 patient was treated with prednisolone instead of dexamethasone. Median age was 65.5 (44-75) years at the time of diagnosis, and 70 (48-76) at the start of IRd treatment. 67% (n=8) were males. To assess impact of prior lenalidomide therapy and number of prior treatments on overall response rate (ORR) and rate of complete response (CR) and very good partial response (VGPR) univariate analysis was performed using Chi-square tests for categorical variables.
Results
The median follow-up was 10 months. Median treatment cycles (range) was 8 (2-17). Overall response rate was 58% (n=7), of which 8% (n=1) had CR, 17% (n=2) had VGPR, 33% (n=4) had partial response (PR) as best response. 3 pts (25%) were considered to have stable disease and 2 pts (17%) showed the disease progression. Median (range) time to response was 3 (1-8) months and median (range) response duration was 7 (2-13) months. Eleven patients (92%) had, at least, one adverse event. 5 (42%) developed anemia: 2 (17%) had grade 3 anemia), 6 (50%) had thrombocytopenia (2 pts with grade 4); 4 (33%) had neutropenia: 2 (17%), with grade 3-4; 1 patient (8%) exhibited grade 1 diarrhea, and 3 patients (25%) had upper respiratory tract infections. 33% (n=4) of the patients had adverse events (grade ≥3). Before IRd, 6 pts had multiple lines of treatment including lenalidomide and 6 pts were lenalidomide-naïve and received only one line of treatment. Difference in ORR was not statistically significant between patients with multiple lines of previous treatment (ORR=33%, n=2), and cases with one line of prior therapy (ORR=87%, n=5) (p=0.079), but CR and VGPR rate were significantly higher in the group who received IRd as second-line treatment (0% vs 50%, p=0.046).
Conclusion
Ixazomib-based treatment showed good efficacy (ORR=58%) and acceptable toxicity. Patients without prior lenalidomide and one prior line of treatment had statistically significant improvement in VGPR and CR rate. From this basis, it can be assumed that use of IRd regimen as the second-line therapy may improve depth of response in relapsed/refractory multiple myeloma patients.
Keywords
Multiple myeloma, relapsed, refractory, ixazomib, efficiency.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20682" ["VALUE"]=> string(94) "Retrospective analysis of using ixazomib in patients with relapsed/refractory multiple myeloma" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(94) "Retrospective analysis of using ixazomib in patients with relapsed/refractory multiple myeloma" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(94) "Retrospective analysis of using ixazomib in patients with relapsed/refractory multiple myeloma" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20680" ["VALUE"]=> array(2) { ["TEXT"]=> string(230) "R. M. Gorbacheva Memorial Institute of Oncology, Hematology and Transplantation; Chair of Hematology, Transfusiology and Transplantology, Pavlov First Saint Petersburg State Medical University, Saint Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(230) "R. M. Gorbacheva Memorial Institute of Oncology, Hematology and Transplantation; Chair of Hematology, Transfusiology and Transplantology, Pavlov First Saint Petersburg State Medical University, Saint Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(230) "R. M. Gorbacheva Memorial Institute of Oncology, Hematology and Transplantation; Chair of Hematology, Transfusiology and Transplantology, Pavlov First Saint Petersburg State Medical University, Saint Petersburg, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20676" ["VALUE"]=> array(2) { ["TEXT"]=> string(239) "Даниил И. Шмидт, Ольга В. Пирогова, Валентина В. Порунова, Ольга В. Кудяшева, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(239) "Даниил И. Шмидт, Ольга В. Пирогова, Валентина В. Порунова, Ольга В. Кудяшева, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(239) "Даниил И. Шмидт, Ольга В. Пирогова, Валентина В. Порунова, Ольга В. Кудяшева, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20678" ["VALUE"]=> array(2) { ["TEXT"]=> string(7236) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Множественная миелома остается неизлечимым рецидивирующим заболеванием, и новые лекарственные средства являются мишенью исследований, направленных на увеличение беспрогрессивной и общей выживаемости пациентов с множественной миеломой (ММ). Иксазомиб – первый пероральный ингибитор протеасом, показавший свою эффективность в лечении пациентов с рецидивирующей/рефрактерной множественной миеломой. Как недавно появившееся лекарственное средство, иксазомиб нуждается в дальнейших исследованиях. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Был проведен ретроспективный анализ опыта применения препарата у 12 пациентов с ММ. Были оценены эффективность и переносимость режима терапии, основанного на иксазомибе. Пациенты получали терапию в период с декабря 2016 по июль 2018 в научно-исследовательском институте детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой. Каждый пациент имел как минимум одну предшествующую линию терапии и рецидивирующее или рефрактерное течение заболевания. Ответ на терапию оценивался согласно критериям ответа International Myeloma Working Group (Kumar et al., 2016). 11 пациентов (92%) получали режим IRd (иксазомиб+леналидомид+дексаметазон), 1 пациент получал преднизолон вместо дексаметазона. Медиана возраста составляла 65,5 (44-75) лет на момент постановки диагноза и 70 (48-76) на момент начала терапии иксазомибом, 67% (n=8) были мужчинами. Для оценки влияния предшествующей терапии леналидомидом и количества предшествующих линий терапии на частоту общего ответа и частоту очень хорошего частичного ответа (ОХЧО) и полного ответа (ПО) был проведен однофакторный анализ с использованием критерия Хи-квадрат для качественных переменных. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Медиана времени наблюдения составила 10 месяцев. Медиана количества (диапазон) линий терапии составила 8 (2-17) месяцев. Частота общего ответа составила 58% (n=7), из которых 8% (n=1) имели ПО, 17% (n=2) имели ОХЧО и 33% (n=4) имели частичный ответ, как лучший ответ. У 3 пациентов (25%) была отмечена стабилизация заболевания и у 2 пациентов (17%) наблюдалось прогрессирование заболевания. Медиана (диапазон) времени до ответа составила 3 (1-8) месяцев и медиана (диапазон) длительности ответа составила 7 (2-13) месяцев. 11 (92%) пациентов имели как минимум 1 нежелательное явление. У 5 (42%) пациентов наблюдалась анемия (у 2 (17%) – 3 степени)), у 6 (50%) – тромбоцитопения (2 пациента имели 4 степень), у 4 (33%) – нейтропения (у 2 (17%) – 3-4 степени), у 1 (8%) развилась диарея 1 степени, и у 3 (25%) пациентов были отмечены инфекции верхних дыхательных путей. 33% пациентов (n=4) имели нежелательные явления ≥3 степени. До IRd 6 пациентов имели множественные линии терапии, в том числе леналидомид-содержащие, и 6 пациентов были леналидомид-наивными и получили только 1 линию терапии перед IRd. Различия в частоте общего ответа между пациентами с множественными предшествующими линиями терапии (частота общего ответа=33%, n=2) и пациентами, получившими 1 линию терапии перед режимом IRd (частота общего ответа=87%, n=5), не были статистически значимыми (p=0,079). Однако частота ПО и ОХЧО была значительно выше в группе, которая получала IRd, как терапию второй линии (0% против 50%, p=0,046). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Терапия, основанная на иксазомибе, показала хорошую эффективность (частота общего ответа 58%) и приемлемую токсичность. Пациенты, не получавшие ранее леналидомид и имевшие только 1 предшествующую линию терапии, имеют статистически значимо более высокую частоту ПО и ОЧХО. На основе этого, можно предположить, что использование режима IRd в качестве терапии второй линии может улучшить глубину ответа пациентов с ММ, включая резистентные формы. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Миеломная болезнь, рефрактерная форма, рецидивы, иксазомиб, эффективность. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7004) "Введение
Множественная миелома остается неизлечимым рецидивирующим заболеванием, и новые лекарственные средства являются мишенью исследований, направленных на увеличение беспрогрессивной и общей выживаемости пациентов с множественной миеломой (ММ). Иксазомиб – первый пероральный ингибитор протеасом, показавший свою эффективность в лечении пациентов с рецидивирующей/рефрактерной множественной миеломой. Как недавно появившееся лекарственное средство, иксазомиб нуждается в дальнейших исследованиях.
Пациенты и методы
Был проведен ретроспективный анализ опыта применения препарата у 12 пациентов с ММ. Были оценены эффективность и переносимость режима терапии, основанного на иксазомибе. Пациенты получали терапию в период с декабря 2016 по июль 2018 в научно-исследовательском институте детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой. Каждый пациент имел как минимум одну предшествующую линию терапии и рецидивирующее или рефрактерное течение заболевания. Ответ на терапию оценивался согласно критериям ответа International Myeloma Working Group (Kumar et al., 2016). 11 пациентов (92%) получали режим IRd (иксазомиб+леналидомид+дексаметазон), 1 пациент получал преднизолон вместо дексаметазона. Медиана возраста составляла 65,5 (44-75) лет на момент постановки диагноза и 70 (48-76) на момент начала терапии иксазомибом, 67% (n=8) были мужчинами. Для оценки влияния предшествующей терапии леналидомидом и количества предшествующих линий терапии на частоту общего ответа и частоту очень хорошего частичного ответа (ОХЧО) и полного ответа (ПО) был проведен однофакторный анализ с использованием критерия Хи-квадрат для качественных переменных.
Результаты
Медиана времени наблюдения составила 10 месяцев. Медиана количества (диапазон) линий терапии составила 8 (2-17) месяцев. Частота общего ответа составила 58% (n=7), из которых 8% (n=1) имели ПО, 17% (n=2) имели ОХЧО и 33% (n=4) имели частичный ответ, как лучший ответ. У 3 пациентов (25%) была отмечена стабилизация заболевания и у 2 пациентов (17%) наблюдалось прогрессирование заболевания. Медиана (диапазон) времени до ответа составила 3 (1-8) месяцев и медиана (диапазон) длительности ответа составила 7 (2-13) месяцев. 11 (92%) пациентов имели как минимум 1 нежелательное явление. У 5 (42%) пациентов наблюдалась анемия (у 2 (17%) – 3 степени)), у 6 (50%) – тромбоцитопения (2 пациента имели 4 степень), у 4 (33%) – нейтропения (у 2 (17%) – 3-4 степени), у 1 (8%) развилась диарея 1 степени, и у 3 (25%) пациентов были отмечены инфекции верхних дыхательных путей. 33% пациентов (n=4) имели нежелательные явления ≥3 степени. До IRd 6 пациентов имели множественные линии терапии, в том числе леналидомид-содержащие, и 6 пациентов были леналидомид-наивными и получили только 1 линию терапии перед IRd. Различия в частоте общего ответа между пациентами с множественными предшествующими линиями терапии (частота общего ответа=33%, n=2) и пациентами, получившими 1 линию терапии перед режимом IRd (частота общего ответа=87%, n=5), не были статистически значимыми (p=0,079). Однако частота ПО и ОХЧО была значительно выше в группе, которая получала IRd, как терапию второй линии (0% против 50%, p=0,046).
Заключение
Терапия, основанная на иксазомибе, показала хорошую эффективность (частота общего ответа 58%) и приемлемую токсичность. Пациенты, не получавшие ранее леналидомид и имевшие только 1 предшествующую линию терапии, имеют статистически значимо более высокую частоту ПО и ОЧХО. На основе этого, можно предположить, что использование режима IRd в качестве терапии второй линии может улучшить глубину ответа пациентов с ММ, включая резистентные формы.
Ключевые слова
Миеломная болезнь, рефрактерная форма, рецидивы, иксазомиб, эффективность.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(7004) "Введение
Множественная миелома остается неизлечимым рецидивирующим заболеванием, и новые лекарственные средства являются мишенью исследований, направленных на увеличение беспрогрессивной и общей выживаемости пациентов с множественной миеломой (ММ). Иксазомиб – первый пероральный ингибитор протеасом, показавший свою эффективность в лечении пациентов с рецидивирующей/рефрактерной множественной миеломой. Как недавно появившееся лекарственное средство, иксазомиб нуждается в дальнейших исследованиях.
Пациенты и методы
Был проведен ретроспективный анализ опыта применения препарата у 12 пациентов с ММ. Были оценены эффективность и переносимость режима терапии, основанного на иксазомибе. Пациенты получали терапию в период с декабря 2016 по июль 2018 в научно-исследовательском институте детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой. Каждый пациент имел как минимум одну предшествующую линию терапии и рецидивирующее или рефрактерное течение заболевания. Ответ на терапию оценивался согласно критериям ответа International Myeloma Working Group (Kumar et al., 2016). 11 пациентов (92%) получали режим IRd (иксазомиб+леналидомид+дексаметазон), 1 пациент получал преднизолон вместо дексаметазона. Медиана возраста составляла 65,5 (44-75) лет на момент постановки диагноза и 70 (48-76) на момент начала терапии иксазомибом, 67% (n=8) были мужчинами. Для оценки влияния предшествующей терапии леналидомидом и количества предшествующих линий терапии на частоту общего ответа и частоту очень хорошего частичного ответа (ОХЧО) и полного ответа (ПО) был проведен однофакторный анализ с использованием критерия Хи-квадрат для качественных переменных.
Результаты
Медиана времени наблюдения составила 10 месяцев. Медиана количества (диапазон) линий терапии составила 8 (2-17) месяцев. Частота общего ответа составила 58% (n=7), из которых 8% (n=1) имели ПО, 17% (n=2) имели ОХЧО и 33% (n=4) имели частичный ответ, как лучший ответ. У 3 пациентов (25%) была отмечена стабилизация заболевания и у 2 пациентов (17%) наблюдалось прогрессирование заболевания. Медиана (диапазон) времени до ответа составила 3 (1-8) месяцев и медиана (диапазон) длительности ответа составила 7 (2-13) месяцев. 11 (92%) пациентов имели как минимум 1 нежелательное явление. У 5 (42%) пациентов наблюдалась анемия (у 2 (17%) – 3 степени)), у 6 (50%) – тромбоцитопения (2 пациента имели 4 степень), у 4 (33%) – нейтропения (у 2 (17%) – 3-4 степени), у 1 (8%) развилась диарея 1 степени, и у 3 (25%) пациентов были отмечены инфекции верхних дыхательных путей. 33% пациентов (n=4) имели нежелательные явления ≥3 степени. До IRd 6 пациентов имели множественные линии терапии, в том числе леналидомид-содержащие, и 6 пациентов были леналидомид-наивными и получили только 1 линию терапии перед IRd. Различия в частоте общего ответа между пациентами с множественными предшествующими линиями терапии (частота общего ответа=33%, n=2) и пациентами, получившими 1 линию терапии перед режимом IRd (частота общего ответа=87%, n=5), не были статистически значимыми (p=0,079). Однако частота ПО и ОХЧО была значительно выше в группе, которая получала IRd, как терапию второй линии (0% против 50%, p=0,046).
Заключение
Терапия, основанная на иксазомибе, показала хорошую эффективность (частота общего ответа 58%) и приемлемую токсичность. Пациенты, не получавшие ранее леналидомид и имевшие только 1 предшествующую линию терапии, имеют статистически значимо более высокую частоту ПО и ОЧХО. На основе этого, можно предположить, что использование режима IRd в качестве терапии второй линии может улучшить глубину ответа пациентов с ММ, включая резистентные формы.
Ключевые слова
Миеломная болезнь, рефрактерная форма, рецидивы, иксазомиб, эффективность.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20677" ["VALUE"]=> array(2) { ["TEXT"]=> string(484) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(484) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(484) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" } } } [34]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1597" ["~ID"]=> string(4) "1597" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(315) "Трансплантация гемопоэтических стволовых клеток с деплецией альфа/бета Т-лимфоцитов и CD19-клеток у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией" ["~NAME"]=> string(315) "Трансплантация гемопоэтических стволовых клеток с деплецией альфа/бета Т-лимфоцитов и CD19-клеток у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:45:03" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:45:03" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-s-depletsiey-alfa-beta-t-limfotsitov-i-cd19-kle/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-s-depletsiey-alfa-beta-t-limfotsitov-i-cd19-kle/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-s-depletsiey-alfa-beta-t-limfotsitov-i-cd19-kle" ["~CODE"]=> string(100) "transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-s-depletsiey-alfa-beta-t-limfotsitov-i-cd19-kle" ["EXTERNAL_ID"]=> string(4) "1597" ["~EXTERNAL_ID"]=> string(4) "1597" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(315) "Трансплантация гемопоэтических стволовых клеток с деплецией альфа/бета Т-лимфоцитов и CD19-клеток у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(568) "Трансплантация гемопоэтических стволовых клеток с деплецией альфа/бета Т-лимфоцитов и CD19-клеток у подростков и молодых взрослых с пароксизмальной ночной гемоглобинуриейHematopoietic stem cell transplantation with alpha/beta T lymphocyte and CD19 cell depletion in adolescents and young adults with paroxysmal nocturnal hemoglobinuria using the immune-ablative conditioning and “peritransplant” therapy with eculizumab" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(9783) "<h2></h2> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Оптимизировать подходы к трансплантации гемопоэтических стволовых клеток (ТГСК) у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией (ПНГ) путем снижения риска реакции «трансплантат против хозяина» (РТПХ) и посттрансплантационных осложнений. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Мы описываем опыт ТГСК от HLA-совместимых неродственных доноров с использованием деплеции альфа/бета Т-лимфоцитов и CD19-клеток у 5 пациентов (1 мужчина, 4 женщины) с ПНГ, развившейся в результате эволюции приобретенной апластической анемии (АА) после успешной иммуносупрессивной терапии (ИСТ) – см. Табл. 1. Медиана возраста пациентов на момент трансплантации составила 17,8 года (14,5-22,7 года), медиана интервала до диагностики ПНГ – 4 года (5 мес.-6,5 лет) от проведения ИСТ. У всех пациентов присутствовали признаки нетяжелой костномозговой недостаточности: гранулоциты 0,8·109/л (0,8-1,8·109/л), тромбоциты 106·109/л (27-143·109/л), гемоглобин – 78 г/л, медиана размера ПНГ-клона во фракции гранулоцитов составила 94% (75-99%). У одной пациентки в анамнезе был тромбоз мозговых венозных синусов. Кондиционирование состояло из торакоабдоминального облучения (ТАО) 4-6 Гр, циклофосфамида 100 мг/кг, флударабина 150 мг/м2 и лошадиного антитимоцитарного глобулина/алемтузумаба (Табл. 2). Экулизумаб вводили со дня (–7) до дня (+14) 1 раз в 7 дней, всего 4 введения, профилактика РТПХ/отторжения состояла из такролимуса ± метотрексат. Клеточные характеристики трансплантата были следующими: CD34+/кг 8,1·106/кг, альфа/бета Т-лимфоциты/кг 150·103/кг, гамма/дельта Т-лимфоциты/кг 7,3·106/кг, СD19+/кг 221·103/кг, NK/кг 6,4·108/кг (Табл. 3). Медиана продолжительности приема такролимуса после ТГСК составила 117 (27-365) сут. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Первичное приживление лейкоцитарного и тромбоцитарного ростков было достигнуто у всех пятерых пациентов с медианой 15 (12-18) и 13 (10-18) дней соответственно, ни одного отторжения не зафиксировано. Острую РТПХ наблюдали у одного пациента – I стадия (поражение кожи 2-й степени), которая потребовала системного назначения глюкокортикостероидов с быстрым ответом и быстрой отменой терапии. Хроническая РТПХ не развилась ни у одного пациента. Реактивация ЦМВ оказалась у 1 пациента, на (-1) сутки, проводилась упреждающая терапия фоскавиром в течение 2 нед., реактивации вируса Эпштейна-Барр (ЭБВ) и аденовируса не наблюдалось. Ни в одном случае не зарегистрировано проявлений эндотелиальной токсичности. У всех пациентов ко дню +30 достигнут полный донорский химеризм в миелоидном ростке. При этом во фракции Т-лимфоцитов памяти (фракция CD45RO+) у 1 пациента длительно сохранялся собственный химеризм, в то время как во фракции наивных Т-лимфоцитов (CD45RА+) химеризм был стабильно донорским с момента их появления в периферической крови. Ни у одного пациента не развилось гемолитического криза и исчезновение ПНГ-клона документировано у всех пациентов к +60 дню (см. рис. 1). Иммунореконституция (СD 3+/4+ > 200/мкл, СD19 + > 50/мкл) оказалась замедленной и наступала с медианой 6 мес после ТГСК (от 4 до 10 мес после ТГСК), однако клинически значимых инфекций, связанных c Т-клеточным дефицитом, не отмечено. В настоящее время все пять пациентов живы с нормальным гемопоэзом, полным количественным восстановлением показателей иммунитета, не имеют посттрансплантационных осложнений, клинически здоровы и хорошо социально адаптированы. Медиана посттрансплантационного наблюдения составляет 4 года (1,7–5,5 лет). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Таким образом, выполнение ТГСК с деплецией альфа/бета Т-лимфоцитов и CD19-клеток от полностью совместимого неродственного донора после мощного иммуносупрессивного кондиционирования с минимальной органной токсичностью показало более чем обнадеживающие результаты в группе подростков и молодых взрослых с ПНГ. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Пароксизмальная ночная гемоглобинурия, трансплантация, деплеция альфа/бета Т-лимфоциты и CD19-клеток, неродственные доноры, подростки, молодые взрослые. </p> <h2 style="text-align: justify;">Таблица 1. Характеристика пациентов</h2> <p style="text-align: justify;"> <img width="787" alt="44_таблица 1.png" src="/upload/medialibrary/614/44_tablitsa-1.png" height="516" title="44_таблица 1.png"><br> Примечания. CsA – циклоспорин А, ПО – полный ответ, ЧО – частичный ответ, гран. – гранулоциты, тромб. – тромбоциты, ретик. – ретикулоциты </p> <h2 style="text-align: justify;">Таблица 2. Режим кондиционирования и лечение экулизумабом (дни)</h2> <p style="text-align: justify;"> <img width="783" alt="44_таблица 2.png" src="/upload/medialibrary/9d9/44_tablitsa-2.png" height="325" title="44_таблица 2.png"><br> </p> <h2 style="text-align: justify;">Таблица 3. Характеристики трансплантата и режимов профилактики отторжения/РТПХ</h2> <p style="text-align: justify;"> <img width="784" alt="44_таблица 3.png" src="/upload/medialibrary/240/44_tablitsa-3.png" height="232" title="44_таблица 3.png"><br> Примечание. А/б Т/кг – альфа/бета Т-лифоциты/кг, Г/д T/кг – гамма/дельта Т-лимфоциты/кг. </p> <h2 style="text-align: justify;">Рисунок 1. Эволюция ПНГ-клона после ТГСК</h2> <p style="text-align: justify;"> <img width="448" alt="44_рисунок 1.png" src="/upload/medialibrary/d25/44_risunok-1.png" height="403" title="44_рисунок 1.png"> </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(315) "Трансплантация гемопоэтических стволовых клеток с деплецией альфа/бета Т-лимфоцитов и CD19-клеток у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(315) "Трансплантация гемопоэтических стволовых клеток с деплецией альфа/бета Т-лимфоцитов и CD19-клеток у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(315) "Трансплантация гемопоэтических стволовых клеток с деплецией альфа/бета Т-лимфоцитов и CD19-клеток у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией" ["SECTION_META_TITLE"]=> string(315) "Трансплантация гемопоэтических стволовых клеток с деплецией альфа/бета Т-лимфоцитов и CD19-клеток у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией" ["SECTION_META_KEYWORDS"]=> string(315) "Трансплантация гемопоэтических стволовых клеток с деплецией альфа/бета Т-лимфоцитов и CD19-клеток у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией" ["SECTION_META_DESCRIPTION"]=> string(315) "Трансплантация гемопоэтических стволовых клеток с деплецией альфа/бета Т-лимфоцитов и CD19-клеток у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией" ["SECTION_PICTURE_FILE_ALT"]=> string(315) "Трансплантация гемопоэтических стволовых клеток с деплецией альфа/бета Т-лимфоцитов и CD19-клеток у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией" ["SECTION_PICTURE_FILE_TITLE"]=> string(315) "Трансплантация гемопоэтических стволовых клеток с деплецией альфа/бета Т-лимфоцитов и CD19-клеток у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-s-depletsiey-alfa-beta-t-limfotsitov-i-cd19-kle" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(315) "Трансплантация гемопоэтических стволовых клеток с деплецией альфа/бета Т-лимфоцитов и CD19-клеток у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(315) "Трансплантация гемопоэтических стволовых клеток с деплецией альфа/бета Т-лимфоцитов и CD19-клеток у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-s-depletsiey-alfa-beta-t-limfotsitov-i-cd19-kle" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-s-depletsiey-alfa-beta-t-limfotsitov-i-cd19-kle" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "transplantatsiya-gemopoeticheskikh-stvolovykh-kletok-s-depletsiey-alfa-beta-t-limfotsitov-i-cd19-kle" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20683" ["VALUE"]=> array(2) { ["TEXT"]=> string(474) "Дарья А. Шашелева, Алексей А. Масчан, Лариса Н. Шелихова, Ульяна Н. Петрова, Мария А. Илюшина, Жанна Б. Шеховцова, Сергей Л. Благов, Андрей Б. Абросимов, Елена И. Гутовская, Елена Е. Курникова, Ольга И. Илларионова, Елена В. Боякова, Галина А. Новичкова, Михаил А. Масчан" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(474) "Дарья А. Шашелева, Алексей А. Масчан, Лариса Н. Шелихова, Ульяна Н. Петрова, Мария А. Илюшина, Жанна Б. Шеховцова, Сергей Л. Благов, Андрей Б. Абросимов, Елена И. Гутовская, Елена Е. Курникова, Ольга И. Илларионова, Елена В. Боякова, Галина А. Новичкова, Михаил А. Масчан" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20684" ["VALUE"]=> array(2) { ["TEXT"]=> string(484) "ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Минздрава России, отдел оптимизации лечения и профилактики осложнений трансплантации гемопоэтических стволовых клеток, Москва, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(484) "ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Минздрава России, отдел оптимизации лечения и профилактики осложнений трансплантации гемопоэтических стволовых клеток, Москва, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20685" ["VALUE"]=> array(2) { ["TEXT"]=> string(9783) "<h2></h2> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Оптимизировать подходы к трансплантации гемопоэтических стволовых клеток (ТГСК) у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией (ПНГ) путем снижения риска реакции «трансплантат против хозяина» (РТПХ) и посттрансплантационных осложнений. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Мы описываем опыт ТГСК от HLA-совместимых неродственных доноров с использованием деплеции альфа/бета Т-лимфоцитов и CD19-клеток у 5 пациентов (1 мужчина, 4 женщины) с ПНГ, развившейся в результате эволюции приобретенной апластической анемии (АА) после успешной иммуносупрессивной терапии (ИСТ) – см. Табл. 1. Медиана возраста пациентов на момент трансплантации составила 17,8 года (14,5-22,7 года), медиана интервала до диагностики ПНГ – 4 года (5 мес.-6,5 лет) от проведения ИСТ. У всех пациентов присутствовали признаки нетяжелой костномозговой недостаточности: гранулоциты 0,8·109/л (0,8-1,8·109/л), тромбоциты 106·109/л (27-143·109/л), гемоглобин – 78 г/л, медиана размера ПНГ-клона во фракции гранулоцитов составила 94% (75-99%). У одной пациентки в анамнезе был тромбоз мозговых венозных синусов. Кондиционирование состояло из торакоабдоминального облучения (ТАО) 4-6 Гр, циклофосфамида 100 мг/кг, флударабина 150 мг/м2 и лошадиного антитимоцитарного глобулина/алемтузумаба (Табл. 2). Экулизумаб вводили со дня (–7) до дня (+14) 1 раз в 7 дней, всего 4 введения, профилактика РТПХ/отторжения состояла из такролимуса ± метотрексат. Клеточные характеристики трансплантата были следующими: CD34+/кг 8,1·106/кг, альфа/бета Т-лимфоциты/кг 150·103/кг, гамма/дельта Т-лимфоциты/кг 7,3·106/кг, СD19+/кг 221·103/кг, NK/кг 6,4·108/кг (Табл. 3). Медиана продолжительности приема такролимуса после ТГСК составила 117 (27-365) сут. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Первичное приживление лейкоцитарного и тромбоцитарного ростков было достигнуто у всех пятерых пациентов с медианой 15 (12-18) и 13 (10-18) дней соответственно, ни одного отторжения не зафиксировано. Острую РТПХ наблюдали у одного пациента – I стадия (поражение кожи 2-й степени), которая потребовала системного назначения глюкокортикостероидов с быстрым ответом и быстрой отменой терапии. Хроническая РТПХ не развилась ни у одного пациента. Реактивация ЦМВ оказалась у 1 пациента, на (-1) сутки, проводилась упреждающая терапия фоскавиром в течение 2 нед., реактивации вируса Эпштейна-Барр (ЭБВ) и аденовируса не наблюдалось. Ни в одном случае не зарегистрировано проявлений эндотелиальной токсичности. У всех пациентов ко дню +30 достигнут полный донорский химеризм в миелоидном ростке. При этом во фракции Т-лимфоцитов памяти (фракция CD45RO+) у 1 пациента длительно сохранялся собственный химеризм, в то время как во фракции наивных Т-лимфоцитов (CD45RА+) химеризм был стабильно донорским с момента их появления в периферической крови. Ни у одного пациента не развилось гемолитического криза и исчезновение ПНГ-клона документировано у всех пациентов к +60 дню (см. рис. 1). Иммунореконституция (СD 3+/4+ > 200/мкл, СD19 + > 50/мкл) оказалась замедленной и наступала с медианой 6 мес после ТГСК (от 4 до 10 мес после ТГСК), однако клинически значимых инфекций, связанных c Т-клеточным дефицитом, не отмечено. В настоящее время все пять пациентов живы с нормальным гемопоэзом, полным количественным восстановлением показателей иммунитета, не имеют посттрансплантационных осложнений, клинически здоровы и хорошо социально адаптированы. Медиана посттрансплантационного наблюдения составляет 4 года (1,7–5,5 лет). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Таким образом, выполнение ТГСК с деплецией альфа/бета Т-лимфоцитов и CD19-клеток от полностью совместимого неродственного донора после мощного иммуносупрессивного кондиционирования с минимальной органной токсичностью показало более чем обнадеживающие результаты в группе подростков и молодых взрослых с ПНГ. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Пароксизмальная ночная гемоглобинурия, трансплантация, деплеция альфа/бета Т-лимфоциты и CD19-клеток, неродственные доноры, подростки, молодые взрослые. </p> <h2 style="text-align: justify;">Таблица 1. Характеристика пациентов</h2> <p style="text-align: justify;"> <img width="787" alt="44_таблица 1.png" src="/upload/medialibrary/614/44_tablitsa-1.png" height="516" title="44_таблица 1.png"><br> Примечания. CsA – циклоспорин А, ПО – полный ответ, ЧО – частичный ответ, гран. – гранулоциты, тромб. – тромбоциты, ретик. – ретикулоциты </p> <h2 style="text-align: justify;">Таблица 2. Режим кондиционирования и лечение экулизумабом (дни)</h2> <p style="text-align: justify;"> <img width="783" alt="44_таблица 2.png" src="/upload/medialibrary/9d9/44_tablitsa-2.png" height="325" title="44_таблица 2.png"><br> </p> <h2 style="text-align: justify;">Таблица 3. Характеристики трансплантата и режимов профилактики отторжения/РТПХ</h2> <p style="text-align: justify;"> <img width="784" alt="44_таблица 3.png" src="/upload/medialibrary/240/44_tablitsa-3.png" height="232" title="44_таблица 3.png"><br> Примечание. А/б Т/кг – альфа/бета Т-лифоциты/кг, Г/д T/кг – гамма/дельта Т-лимфоциты/кг. </p> <h2 style="text-align: justify;">Рисунок 1. Эволюция ПНГ-клона после ТГСК</h2> <p style="text-align: justify;"> <img width="448" alt="44_рисунок 1.png" src="/upload/medialibrary/d25/44_risunok-1.png" height="403" title="44_рисунок 1.png"> </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(9125) "Цель работы
Оптимизировать подходы к трансплантации гемопоэтических стволовых клеток (ТГСК) у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией (ПНГ) путем снижения риска реакции «трансплантат против хозяина» (РТПХ) и посттрансплантационных осложнений.
Материалы и методы
Мы описываем опыт ТГСК от HLA-совместимых неродственных доноров с использованием деплеции альфа/бета Т-лимфоцитов и CD19-клеток у 5 пациентов (1 мужчина, 4 женщины) с ПНГ, развившейся в результате эволюции приобретенной апластической анемии (АА) после успешной иммуносупрессивной терапии (ИСТ) – см. Табл. 1. Медиана возраста пациентов на момент трансплантации составила 17,8 года (14,5-22,7 года), медиана интервала до диагностики ПНГ – 4 года (5 мес.-6,5 лет) от проведения ИСТ. У всех пациентов присутствовали признаки нетяжелой костномозговой недостаточности: гранулоциты 0,8·109/л (0,8-1,8·109/л), тромбоциты 106·109/л (27-143·109/л), гемоглобин – 78 г/л, медиана размера ПНГ-клона во фракции гранулоцитов составила 94% (75-99%). У одной пациентки в анамнезе был тромбоз мозговых венозных синусов. Кондиционирование состояло из торакоабдоминального облучения (ТАО) 4-6 Гр, циклофосфамида 100 мг/кг, флударабина 150 мг/м2 и лошадиного антитимоцитарного глобулина/алемтузумаба (Табл. 2). Экулизумаб вводили со дня (–7) до дня (+14) 1 раз в 7 дней, всего 4 введения, профилактика РТПХ/отторжения состояла из такролимуса ± метотрексат. Клеточные характеристики трансплантата были следующими: CD34+/кг 8,1·106/кг, альфа/бета Т-лимфоциты/кг 150·103/кг, гамма/дельта Т-лимфоциты/кг 7,3·106/кг, СD19+/кг 221·103/кг, NK/кг 6,4·108/кг (Табл. 3). Медиана продолжительности приема такролимуса после ТГСК составила 117 (27-365) сут.
Результаты
Первичное приживление лейкоцитарного и тромбоцитарного ростков было достигнуто у всех пятерых пациентов с медианой 15 (12-18) и 13 (10-18) дней соответственно, ни одного отторжения не зафиксировано. Острую РТПХ наблюдали у одного пациента – I стадия (поражение кожи 2-й степени), которая потребовала системного назначения глюкокортикостероидов с быстрым ответом и быстрой отменой терапии. Хроническая РТПХ не развилась ни у одного пациента. Реактивация ЦМВ оказалась у 1 пациента, на (-1) сутки, проводилась упреждающая терапия фоскавиром в течение 2 нед., реактивации вируса Эпштейна-Барр (ЭБВ) и аденовируса не наблюдалось. Ни в одном случае не зарегистрировано проявлений эндотелиальной токсичности. У всех пациентов ко дню +30 достигнут полный донорский химеризм в миелоидном ростке. При этом во фракции Т-лимфоцитов памяти (фракция CD45RO+) у 1 пациента длительно сохранялся собственный химеризм, в то время как во фракции наивных Т-лимфоцитов (CD45RА+) химеризм был стабильно донорским с момента их появления в периферической крови. Ни у одного пациента не развилось гемолитического криза и исчезновение ПНГ-клона документировано у всех пациентов к +60 дню (см. рис. 1). Иммунореконституция (СD 3+/4+ > 200/мкл, СD19 + > 50/мкл) оказалась замедленной и наступала с медианой 6 мес после ТГСК (от 4 до 10 мес после ТГСК), однако клинически значимых инфекций, связанных c Т-клеточным дефицитом, не отмечено. В настоящее время все пять пациентов живы с нормальным гемопоэзом, полным количественным восстановлением показателей иммунитета, не имеют посттрансплантационных осложнений, клинически здоровы и хорошо социально адаптированы. Медиана посттрансплантационного наблюдения составляет 4 года (1,7–5,5 лет).
Заключение
Таким образом, выполнение ТГСК с деплецией альфа/бета Т-лимфоцитов и CD19-клеток от полностью совместимого неродственного донора после мощного иммуносупрессивного кондиционирования с минимальной органной токсичностью показало более чем обнадеживающие результаты в группе подростков и молодых взрослых с ПНГ.
Ключевые слова
Пароксизмальная ночная гемоглобинурия, трансплантация, деплеция альфа/бета Т-лимфоциты и CD19-клеток, неродственные доноры, подростки, молодые взрослые.
Таблица 1. Характеристика пациентов

Примечания. CsA – циклоспорин А, ПО – полный ответ, ЧО – частичный ответ, гран. – гранулоциты, тромб. – тромбоциты, ретик. – ретикулоциты
Таблица 2. Режим кондиционирования и лечение экулизумабом (дни)

Таблица 3. Характеристики трансплантата и режимов профилактики отторжения/РТПХ

Примечание. А/б Т/кг – альфа/бета Т-лифоциты/кг, Г/д T/кг – гамма/дельта Т-лимфоциты/кг.
Рисунок 1. Эволюция ПНГ-клона после ТГСК

Introduction
The main goal was to optimize hematopoietic stem cell transplantation (HSCT) approach among adolescents and young adults with paroxysmal nocturnal hemoglobinuria (PNH) by means of Graft-versus-host disease (GVHD) and posttransplant complications risk lowering.
Materials and methods
We report our experience of HSCT from HLA-matched unrelated donors using TCR alfa/beta and CD19 depletion in 5 pts (1M/4F) with PNH, developed after successful immunosuppressive therapy (IST) of acquired aplastic anemia (AA). Median age of pts at the moment of transplantation was 17.8 years (range 14.5-22.7), median interval from IST to PNH was 4 years (5mo – 6.5 y). In all patients non-severe pancytopenia was present: granulocytes 0.8х109/l (0.8-1.8х109/l) platelets 106х109/l (27-143х109/l) and Hb -78 g/l, median PNH clone size in granulocytes was 94 (range 75-99)%. One pts previously developed sinus thrombosis. Conditioning consisted of thoraco-abdominal irradiation 4-6 Gy, cyclophosphamide 100 mg/kg, fludarabine 150 mg/m2 and antithymocyte globulin (ATG) or alemtuzumab. Eculizumab was given from day (-7) till day (+14) (every 7 days, only 4 times). GVHD prophylaxis was tacrolimus +/- methotrexate. Infusedgraft characteristics were: CD34+ – 8.1х106/kg, CD3TCRab+ – 150х103/kg, CD3gd+ – 7.3х106/kg, СD19+ – 221х103/kg, NK – 6.4х108/kg.
Results
Engraftment was achieved in all 5 pts with a median of 15 (12-18) и 13 (10-18) days for granulocytes and platelets, respectively. Skin acute GVHD grade I developed in only 1 pt, and subsided with short course of glucocorticoids. CMV reactivation occurred in 1 pt; there were no episodes of Epstein- Barr Virus (EBV) or Adenovirus (AdV) reactivation. Full donor myeloid chimerism was established in all cases by day +30. Immune reconstitution was delayed until 6 months after transplant but no severe infections occurred. All pts are alive for 1.7-5.5 years (med 4 years) after HSCT with normal hematopoiesis and immune function, full donor chimerism and no late sequelae.
Conclusions
Transplantation of TCRalfa/beta and CD19 depleted hematopoietic cells from matched unrelated donor after immunoablative conditioning and supported with short course of eculizumab is perfectly safe and efficient technology leading to cure in young patients with PNH.
Keywords
Paroxysmal nocturnal hemoglobinuria, TCR alfa/beta and CD19 depletion, transplantation, adolescents, young adults.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20689" ["VALUE"]=> string(253) "Hematopoietic stem cell transplantation with alpha/beta T lymphocyte and CD19 cell depletion in adolescents and young adults with paroxysmal nocturnal hemoglobinuria using the immune-ablative conditioning and “peritransplant” therapy with eculizumab" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(253) "Hematopoietic stem cell transplantation with alpha/beta T lymphocyte and CD19 cell depletion in adolescents and young adults with paroxysmal nocturnal hemoglobinuria using the immune-ablative conditioning and “peritransplant” therapy with eculizumab" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20817" ["VALUE"]=> string(4) "1455" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1455" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20818" ["VALUE"]=> string(4) "1456" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1456" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20686" ["VALUE"]=> array(2) { ["TEXT"]=> string(285) "Daria A. Shasheleva, Alexei A. Maschan, Larisa N. Shelikhova, Ulyana N. Petrova, Maria A. Ilyushina, Zhanna B. Shekhovtsova, Sergey L. Blagov, Andrei B. Abrosimov, Elena I. Gutovskaya, Elena E. Kurnikova, Olga I. Illarionova, Elena V. Boyakova, Galina A. Novichkova, Michael A. Maschan" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(285) "Daria A. Shasheleva, Alexei A. Maschan, Larisa N. Shelikhova, Ulyana N. Petrova, Maria A. Ilyushina, Zhanna B. Shekhovtsova, Sergey L. Blagov, Andrei B. Abrosimov, Elena I. Gutovskaya, Elena E. Kurnikova, Olga I. Illarionova, Elena V. Boyakova, Galina A. Novichkova, Michael A. Maschan" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(285) "Daria A. Shasheleva, Alexei A. Maschan, Larisa N. Shelikhova, Ulyana N. Petrova, Maria A. Ilyushina, Zhanna B. Shekhovtsova, Sergey L. Blagov, Andrei B. Abrosimov, Elena I. Gutovskaya, Elena E. Kurnikova, Olga I. Illarionova, Elena V. Boyakova, Galina A. Novichkova, Michael A. Maschan" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20688" ["VALUE"]=> array(2) { ["TEXT"]=> string(3103) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> The main goal was to optimize hematopoietic stem cell transplantation (HSCT) approach among adolescents and young adults with paroxysmal nocturnal hemoglobinuria (PNH) by means of Graft-versus-host disease (GVHD) and posttransplant complications risk lowering. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> We report our experience of HSCT from HLA-matched unrelated donors using TCR alfa/beta and CD19 depletion in 5 pts (1M/4F) with PNH, developed after successful immunosuppressive therapy (IST) of acquired aplastic anemia (AA). Median age of pts at the moment of transplantation was 17.8 years (range 14.5-22.7), median interval from IST to PNH was 4 years (5mo – 6.5 y). In all patients non-severe pancytopenia was present: granulocytes 0.8х109/l (0.8-1.8х109/l) platelets 106х109/l (27-143х109/l) and Hb -78 g/l, median PNH clone size in granulocytes was 94 (range 75-99)%. One pts previously developed sinus thrombosis. Conditioning consisted of thoraco-abdominal irradiation 4-6 Gy, cyclophosphamide 100 mg/kg, fludarabine 150 mg/m2 and antithymocyte globulin (ATG) or alemtuzumab. Eculizumab was given from day (-7) till day (+14) (every 7 days, only 4 times). GVHD prophylaxis was tacrolimus +/- methotrexate. Infusedgraft characteristics were: CD34+ – 8.1х106/kg, CD3TCRab+ – 150х103/kg, CD3gd+ – 7.3х106/kg, СD19+ – 221х103/kg, NK – 6.4х108/kg. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Engraftment was achieved in all 5 pts with a median of 15 (12-18) и 13 (10-18) days for granulocytes and platelets, respectively. Skin acute GVHD grade I developed in only 1 pt, and subsided with short course of glucocorticoids. CMV reactivation occurred in 1 pt; there were no episodes of Epstein- Barr Virus (EBV) or Adenovirus (AdV) reactivation. Full donor myeloid chimerism was established in all cases by day +30. Immune reconstitution was delayed until 6 months after transplant but no severe infections occurred. All pts are alive for 1.7-5.5 years (med 4 years) after HSCT with normal hematopoiesis and immune function, full donor chimerism and no late sequelae. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> Transplantation of TCRalfa/beta and CD19 depleted hematopoietic cells from matched unrelated donor after immunoablative conditioning and supported with short course of eculizumab is perfectly safe and efficient technology leading to cure in young patients with PNH. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Paroxysmal nocturnal hemoglobinuria, TCR alfa/beta and CD19 depletion, transplantation, adolescents, young adults. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2871) "Introduction
The main goal was to optimize hematopoietic stem cell transplantation (HSCT) approach among adolescents and young adults with paroxysmal nocturnal hemoglobinuria (PNH) by means of Graft-versus-host disease (GVHD) and posttransplant complications risk lowering.
Materials and methods
We report our experience of HSCT from HLA-matched unrelated donors using TCR alfa/beta and CD19 depletion in 5 pts (1M/4F) with PNH, developed after successful immunosuppressive therapy (IST) of acquired aplastic anemia (AA). Median age of pts at the moment of transplantation was 17.8 years (range 14.5-22.7), median interval from IST to PNH was 4 years (5mo – 6.5 y). In all patients non-severe pancytopenia was present: granulocytes 0.8х109/l (0.8-1.8х109/l) platelets 106х109/l (27-143х109/l) and Hb -78 g/l, median PNH clone size in granulocytes was 94 (range 75-99)%. One pts previously developed sinus thrombosis. Conditioning consisted of thoraco-abdominal irradiation 4-6 Gy, cyclophosphamide 100 mg/kg, fludarabine 150 mg/m2 and antithymocyte globulin (ATG) or alemtuzumab. Eculizumab was given from day (-7) till day (+14) (every 7 days, only 4 times). GVHD prophylaxis was tacrolimus +/- methotrexate. Infusedgraft characteristics were: CD34+ – 8.1х106/kg, CD3TCRab+ – 150х103/kg, CD3gd+ – 7.3х106/kg, СD19+ – 221х103/kg, NK – 6.4х108/kg.
Results
Engraftment was achieved in all 5 pts with a median of 15 (12-18) и 13 (10-18) days for granulocytes and platelets, respectively. Skin acute GVHD grade I developed in only 1 pt, and subsided with short course of glucocorticoids. CMV reactivation occurred in 1 pt; there were no episodes of Epstein- Barr Virus (EBV) or Adenovirus (AdV) reactivation. Full donor myeloid chimerism was established in all cases by day +30. Immune reconstitution was delayed until 6 months after transplant but no severe infections occurred. All pts are alive for 1.7-5.5 years (med 4 years) after HSCT with normal hematopoiesis and immune function, full donor chimerism and no late sequelae.
Conclusions
Transplantation of TCRalfa/beta and CD19 depleted hematopoietic cells from matched unrelated donor after immunoablative conditioning and supported with short course of eculizumab is perfectly safe and efficient technology leading to cure in young patients with PNH.
Keywords
Paroxysmal nocturnal hemoglobinuria, TCR alfa/beta and CD19 depletion, transplantation, adolescents, young adults.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2871) "Introduction
The main goal was to optimize hematopoietic stem cell transplantation (HSCT) approach among adolescents and young adults with paroxysmal nocturnal hemoglobinuria (PNH) by means of Graft-versus-host disease (GVHD) and posttransplant complications risk lowering.
Materials and methods
We report our experience of HSCT from HLA-matched unrelated donors using TCR alfa/beta and CD19 depletion in 5 pts (1M/4F) with PNH, developed after successful immunosuppressive therapy (IST) of acquired aplastic anemia (AA). Median age of pts at the moment of transplantation was 17.8 years (range 14.5-22.7), median interval from IST to PNH was 4 years (5mo – 6.5 y). In all patients non-severe pancytopenia was present: granulocytes 0.8х109/l (0.8-1.8х109/l) platelets 106х109/l (27-143х109/l) and Hb -78 g/l, median PNH clone size in granulocytes was 94 (range 75-99)%. One pts previously developed sinus thrombosis. Conditioning consisted of thoraco-abdominal irradiation 4-6 Gy, cyclophosphamide 100 mg/kg, fludarabine 150 mg/m2 and antithymocyte globulin (ATG) or alemtuzumab. Eculizumab was given from day (-7) till day (+14) (every 7 days, only 4 times). GVHD prophylaxis was tacrolimus +/- methotrexate. Infusedgraft characteristics were: CD34+ – 8.1х106/kg, CD3TCRab+ – 150х103/kg, CD3gd+ – 7.3х106/kg, СD19+ – 221х103/kg, NK – 6.4х108/kg.
Results
Engraftment was achieved in all 5 pts with a median of 15 (12-18) и 13 (10-18) days for granulocytes and platelets, respectively. Skin acute GVHD grade I developed in only 1 pt, and subsided with short course of glucocorticoids. CMV reactivation occurred in 1 pt; there were no episodes of Epstein- Barr Virus (EBV) or Adenovirus (AdV) reactivation. Full donor myeloid chimerism was established in all cases by day +30. Immune reconstitution was delayed until 6 months after transplant but no severe infections occurred. All pts are alive for 1.7-5.5 years (med 4 years) after HSCT with normal hematopoiesis and immune function, full donor chimerism and no late sequelae.
Conclusions
Transplantation of TCRalfa/beta and CD19 depleted hematopoietic cells from matched unrelated donor after immunoablative conditioning and supported with short course of eculizumab is perfectly safe and efficient technology leading to cure in young patients with PNH.
Keywords
Paroxysmal nocturnal hemoglobinuria, TCR alfa/beta and CD19 depletion, transplantation, adolescents, young adults.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20689" ["VALUE"]=> string(253) "Hematopoietic stem cell transplantation with alpha/beta T lymphocyte and CD19 cell depletion in adolescents and young adults with paroxysmal nocturnal hemoglobinuria using the immune-ablative conditioning and “peritransplant” therapy with eculizumab" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(253) "Hematopoietic stem cell transplantation with alpha/beta T lymphocyte and CD19 cell depletion in adolescents and young adults with paroxysmal nocturnal hemoglobinuria using the immune-ablative conditioning and “peritransplant” therapy with eculizumab" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(253) "Hematopoietic stem cell transplantation with alpha/beta T lymphocyte and CD19 cell depletion in adolescents and young adults with paroxysmal nocturnal hemoglobinuria using the immune-ablative conditioning and “peritransplant” therapy with eculizumab" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20687" ["VALUE"]=> array(2) { ["TEXT"]=> string(127) "Dmitriy Rogachev National Medical Research Center for Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(127) "Dmitriy Rogachev National Medical Research Center for Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(127) "Dmitriy Rogachev National Medical Research Center for Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20683" ["VALUE"]=> array(2) { ["TEXT"]=> string(474) "Дарья А. Шашелева, Алексей А. Масчан, Лариса Н. Шелихова, Ульяна Н. Петрова, Мария А. Илюшина, Жанна Б. Шеховцова, Сергей Л. Благов, Андрей Б. Абросимов, Елена И. Гутовская, Елена Е. Курникова, Ольга И. Илларионова, Елена В. Боякова, Галина А. Новичкова, Михаил А. Масчан" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(474) "Дарья А. Шашелева, Алексей А. Масчан, Лариса Н. Шелихова, Ульяна Н. Петрова, Мария А. Илюшина, Жанна Б. Шеховцова, Сергей Л. Благов, Андрей Б. Абросимов, Елена И. Гутовская, Елена Е. Курникова, Ольга И. Илларионова, Елена В. Боякова, Галина А. Новичкова, Михаил А. Масчан" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(474) "Дарья А. Шашелева, Алексей А. Масчан, Лариса Н. Шелихова, Ульяна Н. Петрова, Мария А. Илюшина, Жанна Б. Шеховцова, Сергей Л. Благов, Андрей Б. Абросимов, Елена И. Гутовская, Елена Е. Курникова, Ольга И. Илларионова, Елена В. Боякова, Галина А. Новичкова, Михаил А. Масчан" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20685" ["VALUE"]=> array(2) { ["TEXT"]=> string(9783) "<h2></h2> <h2 style="text-align: justify;">Цель работы</h2> <p style="text-align: justify;"> Оптимизировать подходы к трансплантации гемопоэтических стволовых клеток (ТГСК) у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией (ПНГ) путем снижения риска реакции «трансплантат против хозяина» (РТПХ) и посттрансплантационных осложнений. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Мы описываем опыт ТГСК от HLA-совместимых неродственных доноров с использованием деплеции альфа/бета Т-лимфоцитов и CD19-клеток у 5 пациентов (1 мужчина, 4 женщины) с ПНГ, развившейся в результате эволюции приобретенной апластической анемии (АА) после успешной иммуносупрессивной терапии (ИСТ) – см. Табл. 1. Медиана возраста пациентов на момент трансплантации составила 17,8 года (14,5-22,7 года), медиана интервала до диагностики ПНГ – 4 года (5 мес.-6,5 лет) от проведения ИСТ. У всех пациентов присутствовали признаки нетяжелой костномозговой недостаточности: гранулоциты 0,8·109/л (0,8-1,8·109/л), тромбоциты 106·109/л (27-143·109/л), гемоглобин – 78 г/л, медиана размера ПНГ-клона во фракции гранулоцитов составила 94% (75-99%). У одной пациентки в анамнезе был тромбоз мозговых венозных синусов. Кондиционирование состояло из торакоабдоминального облучения (ТАО) 4-6 Гр, циклофосфамида 100 мг/кг, флударабина 150 мг/м2 и лошадиного антитимоцитарного глобулина/алемтузумаба (Табл. 2). Экулизумаб вводили со дня (–7) до дня (+14) 1 раз в 7 дней, всего 4 введения, профилактика РТПХ/отторжения состояла из такролимуса ± метотрексат. Клеточные характеристики трансплантата были следующими: CD34+/кг 8,1·106/кг, альфа/бета Т-лимфоциты/кг 150·103/кг, гамма/дельта Т-лимфоциты/кг 7,3·106/кг, СD19+/кг 221·103/кг, NK/кг 6,4·108/кг (Табл. 3). Медиана продолжительности приема такролимуса после ТГСК составила 117 (27-365) сут. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Первичное приживление лейкоцитарного и тромбоцитарного ростков было достигнуто у всех пятерых пациентов с медианой 15 (12-18) и 13 (10-18) дней соответственно, ни одного отторжения не зафиксировано. Острую РТПХ наблюдали у одного пациента – I стадия (поражение кожи 2-й степени), которая потребовала системного назначения глюкокортикостероидов с быстрым ответом и быстрой отменой терапии. Хроническая РТПХ не развилась ни у одного пациента. Реактивация ЦМВ оказалась у 1 пациента, на (-1) сутки, проводилась упреждающая терапия фоскавиром в течение 2 нед., реактивации вируса Эпштейна-Барр (ЭБВ) и аденовируса не наблюдалось. Ни в одном случае не зарегистрировано проявлений эндотелиальной токсичности. У всех пациентов ко дню +30 достигнут полный донорский химеризм в миелоидном ростке. При этом во фракции Т-лимфоцитов памяти (фракция CD45RO+) у 1 пациента длительно сохранялся собственный химеризм, в то время как во фракции наивных Т-лимфоцитов (CD45RА+) химеризм был стабильно донорским с момента их появления в периферической крови. Ни у одного пациента не развилось гемолитического криза и исчезновение ПНГ-клона документировано у всех пациентов к +60 дню (см. рис. 1). Иммунореконституция (СD 3+/4+ > 200/мкл, СD19 + > 50/мкл) оказалась замедленной и наступала с медианой 6 мес после ТГСК (от 4 до 10 мес после ТГСК), однако клинически значимых инфекций, связанных c Т-клеточным дефицитом, не отмечено. В настоящее время все пять пациентов живы с нормальным гемопоэзом, полным количественным восстановлением показателей иммунитета, не имеют посттрансплантационных осложнений, клинически здоровы и хорошо социально адаптированы. Медиана посттрансплантационного наблюдения составляет 4 года (1,7–5,5 лет). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Таким образом, выполнение ТГСК с деплецией альфа/бета Т-лимфоцитов и CD19-клеток от полностью совместимого неродственного донора после мощного иммуносупрессивного кондиционирования с минимальной органной токсичностью показало более чем обнадеживающие результаты в группе подростков и молодых взрослых с ПНГ. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Пароксизмальная ночная гемоглобинурия, трансплантация, деплеция альфа/бета Т-лимфоциты и CD19-клеток, неродственные доноры, подростки, молодые взрослые. </p> <h2 style="text-align: justify;">Таблица 1. Характеристика пациентов</h2> <p style="text-align: justify;"> <img width="787" alt="44_таблица 1.png" src="/upload/medialibrary/614/44_tablitsa-1.png" height="516" title="44_таблица 1.png"><br> Примечания. CsA – циклоспорин А, ПО – полный ответ, ЧО – частичный ответ, гран. – гранулоциты, тромб. – тромбоциты, ретик. – ретикулоциты </p> <h2 style="text-align: justify;">Таблица 2. Режим кондиционирования и лечение экулизумабом (дни)</h2> <p style="text-align: justify;"> <img width="783" alt="44_таблица 2.png" src="/upload/medialibrary/9d9/44_tablitsa-2.png" height="325" title="44_таблица 2.png"><br> </p> <h2 style="text-align: justify;">Таблица 3. Характеристики трансплантата и режимов профилактики отторжения/РТПХ</h2> <p style="text-align: justify;"> <img width="784" alt="44_таблица 3.png" src="/upload/medialibrary/240/44_tablitsa-3.png" height="232" title="44_таблица 3.png"><br> Примечание. А/б Т/кг – альфа/бета Т-лифоциты/кг, Г/д T/кг – гамма/дельта Т-лимфоциты/кг. </p> <h2 style="text-align: justify;">Рисунок 1. Эволюция ПНГ-клона после ТГСК</h2> <p style="text-align: justify;"> <img width="448" alt="44_рисунок 1.png" src="/upload/medialibrary/d25/44_risunok-1.png" height="403" title="44_рисунок 1.png"> </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(9125) "Цель работы
Оптимизировать подходы к трансплантации гемопоэтических стволовых клеток (ТГСК) у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией (ПНГ) путем снижения риска реакции «трансплантат против хозяина» (РТПХ) и посттрансплантационных осложнений.
Материалы и методы
Мы описываем опыт ТГСК от HLA-совместимых неродственных доноров с использованием деплеции альфа/бета Т-лимфоцитов и CD19-клеток у 5 пациентов (1 мужчина, 4 женщины) с ПНГ, развившейся в результате эволюции приобретенной апластической анемии (АА) после успешной иммуносупрессивной терапии (ИСТ) – см. Табл. 1. Медиана возраста пациентов на момент трансплантации составила 17,8 года (14,5-22,7 года), медиана интервала до диагностики ПНГ – 4 года (5 мес.-6,5 лет) от проведения ИСТ. У всех пациентов присутствовали признаки нетяжелой костномозговой недостаточности: гранулоциты 0,8·109/л (0,8-1,8·109/л), тромбоциты 106·109/л (27-143·109/л), гемоглобин – 78 г/л, медиана размера ПНГ-клона во фракции гранулоцитов составила 94% (75-99%). У одной пациентки в анамнезе был тромбоз мозговых венозных синусов. Кондиционирование состояло из торакоабдоминального облучения (ТАО) 4-6 Гр, циклофосфамида 100 мг/кг, флударабина 150 мг/м2 и лошадиного антитимоцитарного глобулина/алемтузумаба (Табл. 2). Экулизумаб вводили со дня (–7) до дня (+14) 1 раз в 7 дней, всего 4 введения, профилактика РТПХ/отторжения состояла из такролимуса ± метотрексат. Клеточные характеристики трансплантата были следующими: CD34+/кг 8,1·106/кг, альфа/бета Т-лимфоциты/кг 150·103/кг, гамма/дельта Т-лимфоциты/кг 7,3·106/кг, СD19+/кг 221·103/кг, NK/кг 6,4·108/кг (Табл. 3). Медиана продолжительности приема такролимуса после ТГСК составила 117 (27-365) сут.
Результаты
Первичное приживление лейкоцитарного и тромбоцитарного ростков было достигнуто у всех пятерых пациентов с медианой 15 (12-18) и 13 (10-18) дней соответственно, ни одного отторжения не зафиксировано. Острую РТПХ наблюдали у одного пациента – I стадия (поражение кожи 2-й степени), которая потребовала системного назначения глюкокортикостероидов с быстрым ответом и быстрой отменой терапии. Хроническая РТПХ не развилась ни у одного пациента. Реактивация ЦМВ оказалась у 1 пациента, на (-1) сутки, проводилась упреждающая терапия фоскавиром в течение 2 нед., реактивации вируса Эпштейна-Барр (ЭБВ) и аденовируса не наблюдалось. Ни в одном случае не зарегистрировано проявлений эндотелиальной токсичности. У всех пациентов ко дню +30 достигнут полный донорский химеризм в миелоидном ростке. При этом во фракции Т-лимфоцитов памяти (фракция CD45RO+) у 1 пациента длительно сохранялся собственный химеризм, в то время как во фракции наивных Т-лимфоцитов (CD45RА+) химеризм был стабильно донорским с момента их появления в периферической крови. Ни у одного пациента не развилось гемолитического криза и исчезновение ПНГ-клона документировано у всех пациентов к +60 дню (см. рис. 1). Иммунореконституция (СD 3+/4+ > 200/мкл, СD19 + > 50/мкл) оказалась замедленной и наступала с медианой 6 мес после ТГСК (от 4 до 10 мес после ТГСК), однако клинически значимых инфекций, связанных c Т-клеточным дефицитом, не отмечено. В настоящее время все пять пациентов живы с нормальным гемопоэзом, полным количественным восстановлением показателей иммунитета, не имеют посттрансплантационных осложнений, клинически здоровы и хорошо социально адаптированы. Медиана посттрансплантационного наблюдения составляет 4 года (1,7–5,5 лет).
Заключение
Таким образом, выполнение ТГСК с деплецией альфа/бета Т-лимфоцитов и CD19-клеток от полностью совместимого неродственного донора после мощного иммуносупрессивного кондиционирования с минимальной органной токсичностью показало более чем обнадеживающие результаты в группе подростков и молодых взрослых с ПНГ.
Ключевые слова
Пароксизмальная ночная гемоглобинурия, трансплантация, деплеция альфа/бета Т-лимфоциты и CD19-клеток, неродственные доноры, подростки, молодые взрослые.
Таблица 1. Характеристика пациентов

Примечания. CsA – циклоспорин А, ПО – полный ответ, ЧО – частичный ответ, гран. – гранулоциты, тромб. – тромбоциты, ретик. – ретикулоциты
Таблица 2. Режим кондиционирования и лечение экулизумабом (дни)

Таблица 3. Характеристики трансплантата и режимов профилактики отторжения/РТПХ

Примечание. А/б Т/кг – альфа/бета Т-лифоциты/кг, Г/д T/кг – гамма/дельта Т-лимфоциты/кг.
Рисунок 1. Эволюция ПНГ-клона после ТГСК

Цель работы
Оптимизировать подходы к трансплантации гемопоэтических стволовых клеток (ТГСК) у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией (ПНГ) путем снижения риска реакции «трансплантат против хозяина» (РТПХ) и посттрансплантационных осложнений.
Материалы и методы
Мы описываем опыт ТГСК от HLA-совместимых неродственных доноров с использованием деплеции альфа/бета Т-лимфоцитов и CD19-клеток у 5 пациентов (1 мужчина, 4 женщины) с ПНГ, развившейся в результате эволюции приобретенной апластической анемии (АА) после успешной иммуносупрессивной терапии (ИСТ) – см. Табл. 1. Медиана возраста пациентов на момент трансплантации составила 17,8 года (14,5-22,7 года), медиана интервала до диагностики ПНГ – 4 года (5 мес.-6,5 лет) от проведения ИСТ. У всех пациентов присутствовали признаки нетяжелой костномозговой недостаточности: гранулоциты 0,8·109/л (0,8-1,8·109/л), тромбоциты 106·109/л (27-143·109/л), гемоглобин – 78 г/л, медиана размера ПНГ-клона во фракции гранулоцитов составила 94% (75-99%). У одной пациентки в анамнезе был тромбоз мозговых венозных синусов. Кондиционирование состояло из торакоабдоминального облучения (ТАО) 4-6 Гр, циклофосфамида 100 мг/кг, флударабина 150 мг/м2 и лошадиного антитимоцитарного глобулина/алемтузумаба (Табл. 2). Экулизумаб вводили со дня (–7) до дня (+14) 1 раз в 7 дней, всего 4 введения, профилактика РТПХ/отторжения состояла из такролимуса ± метотрексат. Клеточные характеристики трансплантата были следующими: CD34+/кг 8,1·106/кг, альфа/бета Т-лимфоциты/кг 150·103/кг, гамма/дельта Т-лимфоциты/кг 7,3·106/кг, СD19+/кг 221·103/кг, NK/кг 6,4·108/кг (Табл. 3). Медиана продолжительности приема такролимуса после ТГСК составила 117 (27-365) сут.
Результаты
Первичное приживление лейкоцитарного и тромбоцитарного ростков было достигнуто у всех пятерых пациентов с медианой 15 (12-18) и 13 (10-18) дней соответственно, ни одного отторжения не зафиксировано. Острую РТПХ наблюдали у одного пациента – I стадия (поражение кожи 2-й степени), которая потребовала системного назначения глюкокортикостероидов с быстрым ответом и быстрой отменой терапии. Хроническая РТПХ не развилась ни у одного пациента. Реактивация ЦМВ оказалась у 1 пациента, на (-1) сутки, проводилась упреждающая терапия фоскавиром в течение 2 нед., реактивации вируса Эпштейна-Барр (ЭБВ) и аденовируса не наблюдалось. Ни в одном случае не зарегистрировано проявлений эндотелиальной токсичности. У всех пациентов ко дню +30 достигнут полный донорский химеризм в миелоидном ростке. При этом во фракции Т-лимфоцитов памяти (фракция CD45RO+) у 1 пациента длительно сохранялся собственный химеризм, в то время как во фракции наивных Т-лимфоцитов (CD45RА+) химеризм был стабильно донорским с момента их появления в периферической крови. Ни у одного пациента не развилось гемолитического криза и исчезновение ПНГ-клона документировано у всех пациентов к +60 дню (см. рис. 1). Иммунореконституция (СD 3+/4+ > 200/мкл, СD19 + > 50/мкл) оказалась замедленной и наступала с медианой 6 мес после ТГСК (от 4 до 10 мес после ТГСК), однако клинически значимых инфекций, связанных c Т-клеточным дефицитом, не отмечено. В настоящее время все пять пациентов живы с нормальным гемопоэзом, полным количественным восстановлением показателей иммунитета, не имеют посттрансплантационных осложнений, клинически здоровы и хорошо социально адаптированы. Медиана посттрансплантационного наблюдения составляет 4 года (1,7–5,5 лет).
Заключение
Таким образом, выполнение ТГСК с деплецией альфа/бета Т-лимфоцитов и CD19-клеток от полностью совместимого неродственного донора после мощного иммуносупрессивного кондиционирования с минимальной органной токсичностью показало более чем обнадеживающие результаты в группе подростков и молодых взрослых с ПНГ.
Ключевые слова
Пароксизмальная ночная гемоглобинурия, трансплантация, деплеция альфа/бета Т-лимфоциты и CD19-клеток, неродственные доноры, подростки, молодые взрослые.
Таблица 1. Характеристика пациентов

Примечания. CsA – циклоспорин А, ПО – полный ответ, ЧО – частичный ответ, гран. – гранулоциты, тромб. – тромбоциты, ретик. – ретикулоциты
Таблица 2. Режим кондиционирования и лечение экулизумабом (дни)

Таблица 3. Характеристики трансплантата и режимов профилактики отторжения/РТПХ

Примечание. А/б Т/кг – альфа/бета Т-лифоциты/кг, Г/д T/кг – гамма/дельта Т-лимфоциты/кг.
Рисунок 1. Эволюция ПНГ-клона после ТГСК

Введение
Лечение ХМЛ основано на применении ингибиторов тирозинкиназ (ИТК). Несмотря на высокую эффективность ИТК, некоторые пациенты в ХФ и значительно большее количество пациентов в ФА и БК оказываются к нему резистентными. Наиболее важный из обсуждаемых механизмов резистентности к ИТК – возникновение точечных мутаций в киназном домене АВL-тирозинкиназы. На сегодня T315I считается единственной мутацией, вызывающей резистентность лейкозных клеток ко всем известным ИТК I и II поколения, кроме Понатиниба.
Цель
Цель работы состояла в оценке результатов различных методов лечения у пациентов с мутацией T315I ХМЛ.
Материалы и методы
Приведены результаты ретроспективного анализа 79 BCR-ABLT315I-позитивных пациентов. 22 аллогенных трансплантаций костного мозга (алло-ТГСК) выполнены 20 пациентам, фармакологическую терапию получили 59 пациентов (41 больной получал ИТК в качестве монотерапии или в комбинации с другими препаратами, 10 пациентов получали α-интерферон в комбинации с другими препаратами, 8 – получали только гидроксикарбамид/химиотерапию). К моменту алло-ТГСК 6 пациентов находились в хронической фазе (ХФ1); 7– в ХФ≥2; 6 – в фазе акселерации и 3 пациента – в бластном кризе (БК). Медиана (Ме) возраста в момент выявления мутации была 47 лет (15-76), и 38 лет – в группе алло-ТГСК. В группе алло-ТГСК в 7 случаях донорами были HLA – идентичные сиблинги, в 13 – неродственные доноры, 13 пациентов (65%) получили более 2 линий ИТК перед алло-ТГСК. Количество баллов по шкале EBMT: 3-4 балла – 16 пациентов, 5-7 баллов – 6 пациента. Режим кондиционирования в 13 случаях (70%) был со сниженной интенсивностью доз. Ме времени от выявления мутации до алло-ТГСК 10 месяцев (2-38). Анализ выживаемости проводили с использованием мето- да Каплан-Майера, сравнение в группах проводили с применением лог-рангового критерия. Регрессионный анализ выживаемости выполнен с применением модели пропорциональных интенсивностей Кокса. Многофакторный регрессионный анализ включал следующие факторы и ковариаты: возраст на дату диагноза, пол, фаза на начало терапии, фаза на дату выявления мутации, терапия после выявления мутации (без алло-ТГСК и с алло-ТГСК), время до выявления мутации от начала терапии.
Результаты
Ме времени наблюдения после выявления мутации T315I 21 месяц (1-100). 5-летняя ОВ в группе в целом составила 42%. При проведении многофакторного анализа только фаза ХМЛ во время обнаружения мутации значительно влияет на ОВ всей группы. Всего в фазе БК на момент выявления мутации было 7 человек, 3-м из них была выполнена алло-ТГСК. Все больные умерли в течение 1-го года после индикации T315I с Ме выживаемости 1.3 месяца. 5-летняя ОВ в группе фармакологической терапии (n=59) 42% с Ме выживаемости 2.8 года. ОВ в группе алло-ТГСК (n=20) 37% после 1-го года, Ме выживаемости 5 месяцев. Oднaкo, 7 пaциентoв пpoжили бoлее 2 лет пocле aллo-ТГCК, 2 – бoлее 6 лет. У всех пациентов после алло-ТГСК получен глубокий молекулярный ответ. У пaциентoв вo 2-й ХФ ОВ 47% (ДИ 95% 29-53%), p = 0,46. В группе фармакологической терапии без ИТК (N=18), включая ИТК (N=41) не было достоверных различий в 5-летней ОВ (42% и 47% соответственно, р=05,3). В гpуппе, пoлучaвшей α-интерферон в кoмбинaции c дpугими пpепapaтaми (n=10), 5-летняя OВ выше, чем в гpуппе, не пoлучaвшей интеpфеpoнo-теpaпию (n=49), и cocтaвляет 72 и 45% cooтветcтвеннo(p=0,21).
Выводы
Появление клона с мутацией T315I у больных ХМЛ с резистентностью изменяет прогноз для данной категории пациентов, особенно в продвинутых фазах. Алло-ТГСК являетcя эффективным метoдoм лечения, пpивoдящим к выздopoвлению. Фaктopoм pиcкa, уxудшaющим pезультaты тpaнcплaнтaции являетcя фaзa БКнa мoмент aллo-ТГCК. Пpoведение фapмaкoлoгичеcкoй теpaпии в 1-й xpoничеcкoй фaзе являетcя эффективным метoдoм лечения, пoзвoляющим кoнтpoлиpoвaть зaбoлевaние в течение длительнoгo вpемени. У пaциентoв вo 2-й ХФ пpoведение aллo-ТГCК пoзвoляет дocтигнуть 47% (ДИ 95% 29–53%) веpoятнocти 5-летней oбщей выживaемocти.
Ключевые слова
Хронический миелоидный лейкоз, мутация T315I, алло-ТГСК, лекарственная резистентность." ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20714" ["VALUE"]=> array(2) { ["TEXT"]=> string(181) "Julia Yu. Vlasova, Elena V. Morozova, Maria V. Barabanshchikova, Tatyana L. Gindina, Ildar M. Barhatov, Alexandr L. Alyanskiy, Elena I. Darskaya, Ivan S. Moiseev, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(181) "Julia Yu. Vlasova, Elena V. Morozova, Maria V. Barabanshchikova, Tatyana L. Gindina, Ildar M. Barhatov, Alexandr L. Alyanskiy, Elena I. Darskaya, Ivan S. Moiseev, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20715" ["VALUE"]=> array(2) { ["TEXT"]=> string(213) "R. M. Gorbacheva Institute of Pediatric Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, First St. Petersburg State I. P. Pavlov Medical University, St. Petersburg" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(213) "R. M. Gorbacheva Institute of Pediatric Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, First St. Petersburg State I. P. Pavlov Medical University, St. Petersburg" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20716" ["VALUE"]=> array(2) { ["TEXT"]=> string(4290) "<h2></h2> <h2 style="text-align: justify;">Background</h2> <p style="text-align: justify;"> Resistance to tyrosine kinase inhibitors (TKI) in patients with chronic myeloid leukemia (CML) is frequently caused by point mutations in the BCR-ABL kinase domain, including the gatekeeper mutant T315I, which confers a high degree of resistance to all currently approved tyrosine kinase inhibitors except ponatinib. </p> <h2 style="text-align: justify;">Aims</h2> <p style="text-align: justify;"> To evaluate the results of different treatment modalities in CML patients with T315I mutation. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> A retrospective analysis of 79 BCR-ABLT315I –positive CML patients (pts) was done. Allogeneic bone marrow transplantation (allo-HSCT) was made in 20 pts, 59 pts received only pharmacological therapy (41 pts received TKI as monotherapy or in combination with other drugs, 10- α-IF, other 8 pts received hydroxyurea or chemotherapy). At the time of allo-HSCT 6 pts were in CP 1, 7- CP≥2, 6 pts had AP and 3 pts were in BC. Median age at the time of mutation detected was 42 years (13-75) (38 years in HSCT-group). In allo-HSCT group 13 pts had unrelated donors, 13(65%) pts received more than 2 lines TKIs before HSCT. The EBMT scores were as follows: 3-4 points, 16 pts; 5-7 points, 6 pts. Conditioning regimen in 13 (70%) pts had reduced intensity. Median time to HSCT after T315I detection was 7 months (0-72). The BCR-ABL mutation analysis was performed by Sanger sequencing. Overall survival (OS) was estimated by Kaplan-Meier method with log-rank test for comparison between groups. Cox regression was used for multivariate survival analysis that included next covariates: age, phase on the time of mutation detection, performance of allo-HSCT, time to T315I detection from TKI start. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Median follow-up time after T315I detection was 21 months (1-100). 5-years OS in whole group was 42%. According to multivariate analysis, only CML phase at the time of mutation detection did significantly affect survival in the entire group. All the pts in BC (n=7), 3 in HSCT group, and 4, in non-HSCT group, died within first year after the T315I detection, whereas the median survival time was 1.3 months. The 5-year OS in non-HSCT group (n=59) comprised 42%, with median survival time of 2.8 years. The 5-year OS after allo-HSCT (n=20) was 37%, with median survival time of 5 months. However, 7 pts lived for more than 2 years after allo-HSCT; 2 patients survived for more than 6 years. All living patients after allo-HSCT are in deep molecular response. The patients in 2nd chronic phase have OS rate of 47% (CI 95% 29-53%), p = 0.46. There was no significant difference in 5-year OS between the non-HSCT groups with TKI (n=41) and non-TKI (n=18) therapy (42% and 47%, respectively, p=0.53). the The 5-year overall survival (OS) among the patients who received α-interferon combined with other drugs (n=10) was higher than in the group that was not treated with interferon (n = 49), 72% vs 45%, respectively (p = 0.21). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Presence of T315I mutation in TKI-resistant patients is extremely unfavorable factor for survival, and it is a major reason for switching to ponatinib or other new potentially available drugs, if possible. Allo-HSCT is an effective method of treatment for this group of patients in case of good selection, however, taking transplant risks into consideration, especially for patients in CP ≥2 . Administration of pharmacological therapy in the 1st CP is an effective method of treatment, which allows to control the disease for a long time. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Chronic myeloid leukemia, T315I mutation, allo-BMT, drug resistance. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4014) "Background
Resistance to tyrosine kinase inhibitors (TKI) in patients with chronic myeloid leukemia (CML) is frequently caused by point mutations in the BCR-ABL kinase domain, including the gatekeeper mutant T315I, which confers a high degree of resistance to all currently approved tyrosine kinase inhibitors except ponatinib.
Aims
To evaluate the results of different treatment modalities in CML patients with T315I mutation.
Patients and methods
A retrospective analysis of 79 BCR-ABLT315I –positive CML patients (pts) was done. Allogeneic bone marrow transplantation (allo-HSCT) was made in 20 pts, 59 pts received only pharmacological therapy (41 pts received TKI as monotherapy or in combination with other drugs, 10- α-IF, other 8 pts received hydroxyurea or chemotherapy). At the time of allo-HSCT 6 pts were in CP 1, 7- CP≥2, 6 pts had AP and 3 pts were in BC. Median age at the time of mutation detected was 42 years (13-75) (38 years in HSCT-group). In allo-HSCT group 13 pts had unrelated donors, 13(65%) pts received more than 2 lines TKIs before HSCT. The EBMT scores were as follows: 3-4 points, 16 pts; 5-7 points, 6 pts. Conditioning regimen in 13 (70%) pts had reduced intensity. Median time to HSCT after T315I detection was 7 months (0-72). The BCR-ABL mutation analysis was performed by Sanger sequencing. Overall survival (OS) was estimated by Kaplan-Meier method with log-rank test for comparison between groups. Cox regression was used for multivariate survival analysis that included next covariates: age, phase on the time of mutation detection, performance of allo-HSCT, time to T315I detection from TKI start.
Results
Median follow-up time after T315I detection was 21 months (1-100). 5-years OS in whole group was 42%. According to multivariate analysis, only CML phase at the time of mutation detection did significantly affect survival in the entire group. All the pts in BC (n=7), 3 in HSCT group, and 4, in non-HSCT group, died within first year after the T315I detection, whereas the median survival time was 1.3 months. The 5-year OS in non-HSCT group (n=59) comprised 42%, with median survival time of 2.8 years. The 5-year OS after allo-HSCT (n=20) was 37%, with median survival time of 5 months. However, 7 pts lived for more than 2 years after allo-HSCT; 2 patients survived for more than 6 years. All living patients after allo-HSCT are in deep molecular response. The patients in 2nd chronic phase have OS rate of 47% (CI 95% 29-53%), p = 0.46. There was no significant difference in 5-year OS between the non-HSCT groups with TKI (n=41) and non-TKI (n=18) therapy (42% and 47%, respectively, p=0.53). the The 5-year overall survival (OS) among the patients who received α-interferon combined with other drugs (n=10) was higher than in the group that was not treated with interferon (n = 49), 72% vs 45%, respectively (p = 0.21).
Conclusion
Presence of T315I mutation in TKI-resistant patients is extremely unfavorable factor for survival, and it is a major reason for switching to ponatinib or other new potentially available drugs, if possible. Allo-HSCT is an effective method of treatment for this group of patients in case of good selection, however, taking transplant risks into consideration, especially for patients in CP ≥2 . Administration of pharmacological therapy in the 1st CP is an effective method of treatment, which allows to control the disease for a long time.
Keywords
Chronic myeloid leukemia, T315I mutation, allo-BMT, drug resistance.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20717" ["VALUE"]=> string(79) "CML patients with T315I mutation: characteristics and outcomes of the treatment" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(79) "CML patients with T315I mutation: characteristics and outcomes of the treatment" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20833" ["VALUE"]=> string(4) "1472" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1472" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20834" ["VALUE"]=> string(4) "1473" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1473" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20714" ["VALUE"]=> array(2) { ["TEXT"]=> string(181) "Julia Yu. Vlasova, Elena V. Morozova, Maria V. Barabanshchikova, Tatyana L. Gindina, Ildar M. Barhatov, Alexandr L. Alyanskiy, Elena I. Darskaya, Ivan S. Moiseev, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(181) "Julia Yu. Vlasova, Elena V. Morozova, Maria V. Barabanshchikova, Tatyana L. Gindina, Ildar M. Barhatov, Alexandr L. Alyanskiy, Elena I. Darskaya, Ivan S. Moiseev, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(181) "Julia Yu. Vlasova, Elena V. Morozova, Maria V. Barabanshchikova, Tatyana L. Gindina, Ildar M. Barhatov, Alexandr L. Alyanskiy, Elena I. Darskaya, Ivan S. Moiseev, Boris V. Afanasyev" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20716" ["VALUE"]=> array(2) { ["TEXT"]=> string(4290) "<h2></h2> <h2 style="text-align: justify;">Background</h2> <p style="text-align: justify;"> Resistance to tyrosine kinase inhibitors (TKI) in patients with chronic myeloid leukemia (CML) is frequently caused by point mutations in the BCR-ABL kinase domain, including the gatekeeper mutant T315I, which confers a high degree of resistance to all currently approved tyrosine kinase inhibitors except ponatinib. </p> <h2 style="text-align: justify;">Aims</h2> <p style="text-align: justify;"> To evaluate the results of different treatment modalities in CML patients with T315I mutation. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> A retrospective analysis of 79 BCR-ABLT315I –positive CML patients (pts) was done. Allogeneic bone marrow transplantation (allo-HSCT) was made in 20 pts, 59 pts received only pharmacological therapy (41 pts received TKI as monotherapy or in combination with other drugs, 10- α-IF, other 8 pts received hydroxyurea or chemotherapy). At the time of allo-HSCT 6 pts were in CP 1, 7- CP≥2, 6 pts had AP and 3 pts were in BC. Median age at the time of mutation detected was 42 years (13-75) (38 years in HSCT-group). In allo-HSCT group 13 pts had unrelated donors, 13(65%) pts received more than 2 lines TKIs before HSCT. The EBMT scores were as follows: 3-4 points, 16 pts; 5-7 points, 6 pts. Conditioning regimen in 13 (70%) pts had reduced intensity. Median time to HSCT after T315I detection was 7 months (0-72). The BCR-ABL mutation analysis was performed by Sanger sequencing. Overall survival (OS) was estimated by Kaplan-Meier method with log-rank test for comparison between groups. Cox regression was used for multivariate survival analysis that included next covariates: age, phase on the time of mutation detection, performance of allo-HSCT, time to T315I detection from TKI start. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Median follow-up time after T315I detection was 21 months (1-100). 5-years OS in whole group was 42%. According to multivariate analysis, only CML phase at the time of mutation detection did significantly affect survival in the entire group. All the pts in BC (n=7), 3 in HSCT group, and 4, in non-HSCT group, died within first year after the T315I detection, whereas the median survival time was 1.3 months. The 5-year OS in non-HSCT group (n=59) comprised 42%, with median survival time of 2.8 years. The 5-year OS after allo-HSCT (n=20) was 37%, with median survival time of 5 months. However, 7 pts lived for more than 2 years after allo-HSCT; 2 patients survived for more than 6 years. All living patients after allo-HSCT are in deep molecular response. The patients in 2nd chronic phase have OS rate of 47% (CI 95% 29-53%), p = 0.46. There was no significant difference in 5-year OS between the non-HSCT groups with TKI (n=41) and non-TKI (n=18) therapy (42% and 47%, respectively, p=0.53). the The 5-year overall survival (OS) among the patients who received α-interferon combined with other drugs (n=10) was higher than in the group that was not treated with interferon (n = 49), 72% vs 45%, respectively (p = 0.21). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Presence of T315I mutation in TKI-resistant patients is extremely unfavorable factor for survival, and it is a major reason for switching to ponatinib or other new potentially available drugs, if possible. Allo-HSCT is an effective method of treatment for this group of patients in case of good selection, however, taking transplant risks into consideration, especially for patients in CP ≥2 . Administration of pharmacological therapy in the 1st CP is an effective method of treatment, which allows to control the disease for a long time. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Chronic myeloid leukemia, T315I mutation, allo-BMT, drug resistance. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4014) "Background
Resistance to tyrosine kinase inhibitors (TKI) in patients with chronic myeloid leukemia (CML) is frequently caused by point mutations in the BCR-ABL kinase domain, including the gatekeeper mutant T315I, which confers a high degree of resistance to all currently approved tyrosine kinase inhibitors except ponatinib.
Aims
To evaluate the results of different treatment modalities in CML patients with T315I mutation.
Patients and methods
A retrospective analysis of 79 BCR-ABLT315I –positive CML patients (pts) was done. Allogeneic bone marrow transplantation (allo-HSCT) was made in 20 pts, 59 pts received only pharmacological therapy (41 pts received TKI as monotherapy or in combination with other drugs, 10- α-IF, other 8 pts received hydroxyurea or chemotherapy). At the time of allo-HSCT 6 pts were in CP 1, 7- CP≥2, 6 pts had AP and 3 pts were in BC. Median age at the time of mutation detected was 42 years (13-75) (38 years in HSCT-group). In allo-HSCT group 13 pts had unrelated donors, 13(65%) pts received more than 2 lines TKIs before HSCT. The EBMT scores were as follows: 3-4 points, 16 pts; 5-7 points, 6 pts. Conditioning regimen in 13 (70%) pts had reduced intensity. Median time to HSCT after T315I detection was 7 months (0-72). The BCR-ABL mutation analysis was performed by Sanger sequencing. Overall survival (OS) was estimated by Kaplan-Meier method with log-rank test for comparison between groups. Cox regression was used for multivariate survival analysis that included next covariates: age, phase on the time of mutation detection, performance of allo-HSCT, time to T315I detection from TKI start.
Results
Median follow-up time after T315I detection was 21 months (1-100). 5-years OS in whole group was 42%. According to multivariate analysis, only CML phase at the time of mutation detection did significantly affect survival in the entire group. All the pts in BC (n=7), 3 in HSCT group, and 4, in non-HSCT group, died within first year after the T315I detection, whereas the median survival time was 1.3 months. The 5-year OS in non-HSCT group (n=59) comprised 42%, with median survival time of 2.8 years. The 5-year OS after allo-HSCT (n=20) was 37%, with median survival time of 5 months. However, 7 pts lived for more than 2 years after allo-HSCT; 2 patients survived for more than 6 years. All living patients after allo-HSCT are in deep molecular response. The patients in 2nd chronic phase have OS rate of 47% (CI 95% 29-53%), p = 0.46. There was no significant difference in 5-year OS between the non-HSCT groups with TKI (n=41) and non-TKI (n=18) therapy (42% and 47%, respectively, p=0.53). the The 5-year overall survival (OS) among the patients who received α-interferon combined with other drugs (n=10) was higher than in the group that was not treated with interferon (n = 49), 72% vs 45%, respectively (p = 0.21).
Conclusion
Presence of T315I mutation in TKI-resistant patients is extremely unfavorable factor for survival, and it is a major reason for switching to ponatinib or other new potentially available drugs, if possible. Allo-HSCT is an effective method of treatment for this group of patients in case of good selection, however, taking transplant risks into consideration, especially for patients in CP ≥2 . Administration of pharmacological therapy in the 1st CP is an effective method of treatment, which allows to control the disease for a long time.
Keywords
Chronic myeloid leukemia, T315I mutation, allo-BMT, drug resistance.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4014) "Background
Resistance to tyrosine kinase inhibitors (TKI) in patients with chronic myeloid leukemia (CML) is frequently caused by point mutations in the BCR-ABL kinase domain, including the gatekeeper mutant T315I, which confers a high degree of resistance to all currently approved tyrosine kinase inhibitors except ponatinib.
Aims
To evaluate the results of different treatment modalities in CML patients with T315I mutation.
Patients and methods
A retrospective analysis of 79 BCR-ABLT315I –positive CML patients (pts) was done. Allogeneic bone marrow transplantation (allo-HSCT) was made in 20 pts, 59 pts received only pharmacological therapy (41 pts received TKI as monotherapy or in combination with other drugs, 10- α-IF, other 8 pts received hydroxyurea or chemotherapy). At the time of allo-HSCT 6 pts were in CP 1, 7- CP≥2, 6 pts had AP and 3 pts were in BC. Median age at the time of mutation detected was 42 years (13-75) (38 years in HSCT-group). In allo-HSCT group 13 pts had unrelated donors, 13(65%) pts received more than 2 lines TKIs before HSCT. The EBMT scores were as follows: 3-4 points, 16 pts; 5-7 points, 6 pts. Conditioning regimen in 13 (70%) pts had reduced intensity. Median time to HSCT after T315I detection was 7 months (0-72). The BCR-ABL mutation analysis was performed by Sanger sequencing. Overall survival (OS) was estimated by Kaplan-Meier method with log-rank test for comparison between groups. Cox regression was used for multivariate survival analysis that included next covariates: age, phase on the time of mutation detection, performance of allo-HSCT, time to T315I detection from TKI start.
Results
Median follow-up time after T315I detection was 21 months (1-100). 5-years OS in whole group was 42%. According to multivariate analysis, only CML phase at the time of mutation detection did significantly affect survival in the entire group. All the pts in BC (n=7), 3 in HSCT group, and 4, in non-HSCT group, died within first year after the T315I detection, whereas the median survival time was 1.3 months. The 5-year OS in non-HSCT group (n=59) comprised 42%, with median survival time of 2.8 years. The 5-year OS after allo-HSCT (n=20) was 37%, with median survival time of 5 months. However, 7 pts lived for more than 2 years after allo-HSCT; 2 patients survived for more than 6 years. All living patients after allo-HSCT are in deep molecular response. The patients in 2nd chronic phase have OS rate of 47% (CI 95% 29-53%), p = 0.46. There was no significant difference in 5-year OS between the non-HSCT groups with TKI (n=41) and non-TKI (n=18) therapy (42% and 47%, respectively, p=0.53). the The 5-year overall survival (OS) among the patients who received α-interferon combined with other drugs (n=10) was higher than in the group that was not treated with interferon (n = 49), 72% vs 45%, respectively (p = 0.21).
Conclusion
Presence of T315I mutation in TKI-resistant patients is extremely unfavorable factor for survival, and it is a major reason for switching to ponatinib or other new potentially available drugs, if possible. Allo-HSCT is an effective method of treatment for this group of patients in case of good selection, however, taking transplant risks into consideration, especially for patients in CP ≥2 . Administration of pharmacological therapy in the 1st CP is an effective method of treatment, which allows to control the disease for a long time.
Keywords
Chronic myeloid leukemia, T315I mutation, allo-BMT, drug resistance.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20717" ["VALUE"]=> string(79) "CML patients with T315I mutation: characteristics and outcomes of the treatment" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(79) "CML patients with T315I mutation: characteristics and outcomes of the treatment" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(79) "CML patients with T315I mutation: characteristics and outcomes of the treatment" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20715" ["VALUE"]=> array(2) { ["TEXT"]=> string(213) "R. M. Gorbacheva Institute of Pediatric Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, First St. Petersburg State I. P. Pavlov Medical University, St. Petersburg" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(213) "R. M. Gorbacheva Institute of Pediatric Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, First St. Petersburg State I. P. Pavlov Medical University, St. Petersburg" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(213) "R. M. Gorbacheva Institute of Pediatric Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, First St. Petersburg State I. P. Pavlov Medical University, St. Petersburg" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20711" ["VALUE"]=> array(2) { ["TEXT"]=> string(309) "Юлия Ю. Власова, Елена В. Морозова, Мария В. Барабанщикова, Татьяна Л. Гиндина, Ильдар М. Бархатов, Александр Л. Алянский, Елена И. Дарская, Иван С. Моисеев, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(309) "Юлия Ю. Власова, Елена В. Морозова, Мария В. Барабанщикова, Татьяна Л. Гиндина, Ильдар М. Бархатов, Александр Л. Алянский, Елена И. Дарская, Иван С. Моисеев, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(309) "Юлия Ю. Власова, Елена В. Морозова, Мария В. Барабанщикова, Татьяна Л. Гиндина, Ильдар М. Бархатов, Александр Л. Алянский, Елена И. Дарская, Иван С. Моисеев, Борис В. Афанасьев" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20713" ["VALUE"]=> array(2) { ["TEXT"]=> string(8065) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Лечение ХМЛ основано на применении ингибиторов тирозинкиназ (ИТК). Несмотря на высокую эффективность ИТК, некоторые пациенты в ХФ и значительно большее количество пациентов в ФА и БК оказываются к нему резистентными. Наиболее важный из обсуждаемых механизмов резистентности к ИТК – возникновение точечных мутаций в киназном домене АВL-тирозинкиназы. На сегодня T315I считается единственной мутацией, вызывающей резистентность лейкозных клеток ко всем известным ИТК I и II поколения, кроме Понатиниба. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель работы состояла в оценке результатов различных методов лечения у пациентов с мутацией T315I ХМЛ. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Приведены результаты ретроспективного анализа 79 BCR-ABLT315I-позитивных пациентов. 22 аллогенных трансплантаций костного мозга (алло-ТГСК) выполнены 20 пациентам, фармакологическую терапию получили 59 пациентов (41 больной получал ИТК в качестве монотерапии или в комбинации с другими препаратами, 10 пациентов получали α-интерферон в комбинации с другими препаратами, 8 – получали только гидроксикарбамид/химиотерапию). К моменту алло-ТГСК 6 пациентов находились в хронической фазе (ХФ1); 7– в ХФ≥2; 6 – в фазе акселерации и 3 пациента – в бластном кризе (БК). Медиана (Ме) возраста в момент выявления мутации была 47 лет (15-76), и 38 лет – в группе алло-ТГСК. В группе алло-ТГСК в 7 случаях донорами были HLA – идентичные сиблинги, в 13 – неродственные доноры, 13 пациентов (65%) получили более 2 линий ИТК перед алло-ТГСК. Количество баллов по шкале EBMT: 3-4 балла – 16 пациентов, 5-7 баллов – 6 пациента. Режим кондиционирования в 13 случаях (70%) был со сниженной интенсивностью доз. Ме времени от выявления мутации до алло-ТГСК 10 месяцев (2-38). Анализ выживаемости проводили с использованием мето- да Каплан-Майера, сравнение в группах проводили с применением лог-рангового критерия. Регрессионный анализ выживаемости выполнен с применением модели пропорциональных интенсивностей Кокса. Многофакторный регрессионный анализ включал следующие факторы и ковариаты: возраст на дату диагноза, пол, фаза на начало терапии, фаза на дату выявления мутации, терапия после выявления мутации (без алло-ТГСК и с алло-ТГСК), время до выявления мутации от начала терапии. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Ме времени наблюдения после выявления мутации T315I 21 месяц (1-100). 5-летняя ОВ в группе в целом составила 42%. При проведении многофакторного анализа только фаза ХМЛ во время обнаружения мутации значительно влияет на ОВ всей группы. Всего в фазе БК на момент выявления мутации было 7 человек, 3-м из них была выполнена алло-ТГСК. Все больные умерли в течение 1-го года после индикации T315I с Ме выживаемости 1.3 месяца. 5-летняя ОВ в группе фармакологической терапии (n=59) 42% с Ме выживаемости 2.8 года. ОВ в группе алло-ТГСК (n=20) 37% после 1-го года, Ме выживаемости 5 месяцев. Oднaкo, 7 пaциентoв пpoжили бoлее 2 лет пocле aллo-ТГCК, 2 – бoлее 6 лет. У всех пациентов после алло-ТГСК получен глубокий молекулярный ответ. У пaциентoв вo 2-й ХФ ОВ 47% (ДИ 95% 29-53%), p = 0,46. В группе фармакологической терапии без ИТК (N=18), включая ИТК (N=41) не было достоверных различий в 5-летней ОВ (42% и 47% соответственно, р=05,3). В гpуппе, пoлучaвшей α-интерферон в кoмбинaции c дpугими пpепapaтaми (n=10), 5-летняя OВ выше, чем в гpуппе, не пoлучaвшей интеpфеpoнo-теpaпию (n=49), и cocтaвляет 72 и 45% cooтветcтвеннo(p=0,21). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Появление клона с мутацией T315I у больных ХМЛ с резистентностью изменяет прогноз для данной категории пациентов, особенно в продвинутых фазах. Алло-ТГСК являетcя эффективным метoдoм лечения, пpивoдящим к выздopoвлению. Фaктopoм pиcкa, уxудшaющим pезультaты тpaнcплaнтaции являетcя фaзa БКнa мoмент aллo-ТГCК. Пpoведение фapмaкoлoгичеcкoй теpaпии в 1-й xpoничеcкoй фaзе являетcя эффективным метoдoм лечения, пoзвoляющим кoнтpoлиpoвaть зaбoлевaние в течение длительнoгo вpемени. У пaциентoв вo 2-й ХФ пpoведение aллo-ТГCК пoзвoляет дocтигнуть 47% (ДИ 95% 29–53%) веpoятнocти 5-летней oбщей выживaемocти. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <span style="font-family: "Minion Pro", georgia, serif; font-size: 17px; text-align: justify;">Хронический миелоидный лейкоз, мутация T315I, </span><span style="font-family: "Minion Pro", georgia, serif; font-size: 17px; text-align: justify;">алло-ТГСК, лекарственная резистентность.</span>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7751) "Введение
Лечение ХМЛ основано на применении ингибиторов тирозинкиназ (ИТК). Несмотря на высокую эффективность ИТК, некоторые пациенты в ХФ и значительно большее количество пациентов в ФА и БК оказываются к нему резистентными. Наиболее важный из обсуждаемых механизмов резистентности к ИТК – возникновение точечных мутаций в киназном домене АВL-тирозинкиназы. На сегодня T315I считается единственной мутацией, вызывающей резистентность лейкозных клеток ко всем известным ИТК I и II поколения, кроме Понатиниба.
Цель
Цель работы состояла в оценке результатов различных методов лечения у пациентов с мутацией T315I ХМЛ.
Материалы и методы
Приведены результаты ретроспективного анализа 79 BCR-ABLT315I-позитивных пациентов. 22 аллогенных трансплантаций костного мозга (алло-ТГСК) выполнены 20 пациентам, фармакологическую терапию получили 59 пациентов (41 больной получал ИТК в качестве монотерапии или в комбинации с другими препаратами, 10 пациентов получали α-интерферон в комбинации с другими препаратами, 8 – получали только гидроксикарбамид/химиотерапию). К моменту алло-ТГСК 6 пациентов находились в хронической фазе (ХФ1); 7– в ХФ≥2; 6 – в фазе акселерации и 3 пациента – в бластном кризе (БК). Медиана (Ме) возраста в момент выявления мутации была 47 лет (15-76), и 38 лет – в группе алло-ТГСК. В группе алло-ТГСК в 7 случаях донорами были HLA – идентичные сиблинги, в 13 – неродственные доноры, 13 пациентов (65%) получили более 2 линий ИТК перед алло-ТГСК. Количество баллов по шкале EBMT: 3-4 балла – 16 пациентов, 5-7 баллов – 6 пациента. Режим кондиционирования в 13 случаях (70%) был со сниженной интенсивностью доз. Ме времени от выявления мутации до алло-ТГСК 10 месяцев (2-38). Анализ выживаемости проводили с использованием мето- да Каплан-Майера, сравнение в группах проводили с применением лог-рангового критерия. Регрессионный анализ выживаемости выполнен с применением модели пропорциональных интенсивностей Кокса. Многофакторный регрессионный анализ включал следующие факторы и ковариаты: возраст на дату диагноза, пол, фаза на начало терапии, фаза на дату выявления мутации, терапия после выявления мутации (без алло-ТГСК и с алло-ТГСК), время до выявления мутации от начала терапии.
Результаты
Ме времени наблюдения после выявления мутации T315I 21 месяц (1-100). 5-летняя ОВ в группе в целом составила 42%. При проведении многофакторного анализа только фаза ХМЛ во время обнаружения мутации значительно влияет на ОВ всей группы. Всего в фазе БК на момент выявления мутации было 7 человек, 3-м из них была выполнена алло-ТГСК. Все больные умерли в течение 1-го года после индикации T315I с Ме выживаемости 1.3 месяца. 5-летняя ОВ в группе фармакологической терапии (n=59) 42% с Ме выживаемости 2.8 года. ОВ в группе алло-ТГСК (n=20) 37% после 1-го года, Ме выживаемости 5 месяцев. Oднaкo, 7 пaциентoв пpoжили бoлее 2 лет пocле aллo-ТГCК, 2 – бoлее 6 лет. У всех пациентов после алло-ТГСК получен глубокий молекулярный ответ. У пaциентoв вo 2-й ХФ ОВ 47% (ДИ 95% 29-53%), p = 0,46. В группе фармакологической терапии без ИТК (N=18), включая ИТК (N=41) не было достоверных различий в 5-летней ОВ (42% и 47% соответственно, р=05,3). В гpуппе, пoлучaвшей α-интерферон в кoмбинaции c дpугими пpепapaтaми (n=10), 5-летняя OВ выше, чем в гpуппе, не пoлучaвшей интеpфеpoнo-теpaпию (n=49), и cocтaвляет 72 и 45% cooтветcтвеннo(p=0,21).
Выводы
Появление клона с мутацией T315I у больных ХМЛ с резистентностью изменяет прогноз для данной категории пациентов, особенно в продвинутых фазах. Алло-ТГСК являетcя эффективным метoдoм лечения, пpивoдящим к выздopoвлению. Фaктopoм pиcкa, уxудшaющим pезультaты тpaнcплaнтaции являетcя фaзa БКнa мoмент aллo-ТГCК. Пpoведение фapмaкoлoгичеcкoй теpaпии в 1-й xpoничеcкoй фaзе являетcя эффективным метoдoм лечения, пoзвoляющим кoнтpoлиpoвaть зaбoлевaние в течение длительнoгo вpемени. У пaциентoв вo 2-й ХФ пpoведение aллo-ТГCК пoзвoляет дocтигнуть 47% (ДИ 95% 29–53%) веpoятнocти 5-летней oбщей выживaемocти.
Ключевые слова
Хронический миелоидный лейкоз, мутация T315I, алло-ТГСК, лекарственная резистентность." ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(7751) "Введение
Лечение ХМЛ основано на применении ингибиторов тирозинкиназ (ИТК). Несмотря на высокую эффективность ИТК, некоторые пациенты в ХФ и значительно большее количество пациентов в ФА и БК оказываются к нему резистентными. Наиболее важный из обсуждаемых механизмов резистентности к ИТК – возникновение точечных мутаций в киназном домене АВL-тирозинкиназы. На сегодня T315I считается единственной мутацией, вызывающей резистентность лейкозных клеток ко всем известным ИТК I и II поколения, кроме Понатиниба.
Цель
Цель работы состояла в оценке результатов различных методов лечения у пациентов с мутацией T315I ХМЛ.
Материалы и методы
Приведены результаты ретроспективного анализа 79 BCR-ABLT315I-позитивных пациентов. 22 аллогенных трансплантаций костного мозга (алло-ТГСК) выполнены 20 пациентам, фармакологическую терапию получили 59 пациентов (41 больной получал ИТК в качестве монотерапии или в комбинации с другими препаратами, 10 пациентов получали α-интерферон в комбинации с другими препаратами, 8 – получали только гидроксикарбамид/химиотерапию). К моменту алло-ТГСК 6 пациентов находились в хронической фазе (ХФ1); 7– в ХФ≥2; 6 – в фазе акселерации и 3 пациента – в бластном кризе (БК). Медиана (Ме) возраста в момент выявления мутации была 47 лет (15-76), и 38 лет – в группе алло-ТГСК. В группе алло-ТГСК в 7 случаях донорами были HLA – идентичные сиблинги, в 13 – неродственные доноры, 13 пациентов (65%) получили более 2 линий ИТК перед алло-ТГСК. Количество баллов по шкале EBMT: 3-4 балла – 16 пациентов, 5-7 баллов – 6 пациента. Режим кондиционирования в 13 случаях (70%) был со сниженной интенсивностью доз. Ме времени от выявления мутации до алло-ТГСК 10 месяцев (2-38). Анализ выживаемости проводили с использованием мето- да Каплан-Майера, сравнение в группах проводили с применением лог-рангового критерия. Регрессионный анализ выживаемости выполнен с применением модели пропорциональных интенсивностей Кокса. Многофакторный регрессионный анализ включал следующие факторы и ковариаты: возраст на дату диагноза, пол, фаза на начало терапии, фаза на дату выявления мутации, терапия после выявления мутации (без алло-ТГСК и с алло-ТГСК), время до выявления мутации от начала терапии.
Результаты
Ме времени наблюдения после выявления мутации T315I 21 месяц (1-100). 5-летняя ОВ в группе в целом составила 42%. При проведении многофакторного анализа только фаза ХМЛ во время обнаружения мутации значительно влияет на ОВ всей группы. Всего в фазе БК на момент выявления мутации было 7 человек, 3-м из них была выполнена алло-ТГСК. Все больные умерли в течение 1-го года после индикации T315I с Ме выживаемости 1.3 месяца. 5-летняя ОВ в группе фармакологической терапии (n=59) 42% с Ме выживаемости 2.8 года. ОВ в группе алло-ТГСК (n=20) 37% после 1-го года, Ме выживаемости 5 месяцев. Oднaкo, 7 пaциентoв пpoжили бoлее 2 лет пocле aллo-ТГCК, 2 – бoлее 6 лет. У всех пациентов после алло-ТГСК получен глубокий молекулярный ответ. У пaциентoв вo 2-й ХФ ОВ 47% (ДИ 95% 29-53%), p = 0,46. В группе фармакологической терапии без ИТК (N=18), включая ИТК (N=41) не было достоверных различий в 5-летней ОВ (42% и 47% соответственно, р=05,3). В гpуппе, пoлучaвшей α-интерферон в кoмбинaции c дpугими пpепapaтaми (n=10), 5-летняя OВ выше, чем в гpуппе, не пoлучaвшей интеpфеpoнo-теpaпию (n=49), и cocтaвляет 72 и 45% cooтветcтвеннo(p=0,21).
Выводы
Появление клона с мутацией T315I у больных ХМЛ с резистентностью изменяет прогноз для данной категории пациентов, особенно в продвинутых фазах. Алло-ТГСК являетcя эффективным метoдoм лечения, пpивoдящим к выздopoвлению. Фaктopoм pиcкa, уxудшaющим pезультaты тpaнcплaнтaции являетcя фaзa БКнa мoмент aллo-ТГCК. Пpoведение фapмaкoлoгичеcкoй теpaпии в 1-й xpoничеcкoй фaзе являетcя эффективным метoдoм лечения, пoзвoляющим кoнтpoлиpoвaть зaбoлевaние в течение длительнoгo вpемени. У пaциентoв вo 2-й ХФ пpoведение aллo-ТГCК пoзвoляет дocтигнуть 47% (ДИ 95% 29–53%) веpoятнocти 5-летней oбщей выживaемocти.
Ключевые слова
Хронический миелоидный лейкоз, мутация T315I, алло-ТГСК, лекарственная резистентность." } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20712" ["VALUE"]=> array(2) { ["TEXT"]=> string(442) "НИИ детской онкологии гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(442) "НИИ детской онкологии гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(442) "НИИ детской онкологии гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург" } } } [36]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1602" ["~ID"]=> string(4) "1602" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(358) "Высокодозная химиотерапия с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ-инфекции: результаты проспективного сравнительного исследования" ["~NAME"]=> string(358) "Высокодозная химиотерапия с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ-инфекции: результаты проспективного сравнительного исследования" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:48:18" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:48:18" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vysokodoznaya-khimioterapiya-s-autologichnoy-transplantatsiey-gemopoeticheskikh-stvolovykh-kletok-u-/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vysokodoznaya-khimioterapiya-s-autologichnoy-transplantatsiey-gemopoeticheskikh-stvolovykh-kletok-u-/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "vysokodoznaya-khimioterapiya-s-autologichnoy-transplantatsiey-gemopoeticheskikh-stvolovykh-kletok-u-" ["~CODE"]=> string(100) "vysokodoznaya-khimioterapiya-s-autologichnoy-transplantatsiey-gemopoeticheskikh-stvolovykh-kletok-u-" ["EXTERNAL_ID"]=> string(4) "1602" ["~EXTERNAL_ID"]=> string(4) "1602" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(358) "Высокодозная химиотерапия с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ-инфекции: результаты проспективного сравнительного исследования" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(518) "Высокодозная химиотерапия с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ-инфекции: результаты проспективного сравнительного исследованияHigh-dose chemotherapy followed by autologous hematopoietic stem cell transplantation for HIV-related lymphomas: the results of a prospective case-control study" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(8790) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Вирус иммунодефицита человека (ВИЧ) связан с высоким риском развития злокачественных новообразований, таких как – лимфома Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на успешное применение антиретровирусной терапии (АРВТ) [1]. Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать агрессивную терапию, включающую высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [2]. Результаты ауто-ТГСК для лечения ВИЧ-ассоциированных лимфом все еще являются предметом споров. Количество проспективных сравнительных исследований эффективности и безопасности ВДХТ с последующей ауто-ТГСК ограничено. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В проспективное исследование включены 10 пациентов с лимфомами на фоне ВИЧ (группа исследования), которым была проведена ВДХТ с последующей ауто-ТГСК в клинике НИИ ДОГиТ в период с 2016 по 2018 год. Для сравнения эффективности и безопасности процедуры использован метод «случай-контроль» (1:4) и, в качестве группы сравнения, в исследование включены 40 пациентов без ВИЧ-инфекции, сопоставимые по основным характеристикам (контрольная группа), которым была выполнена ауто-ТГСК в тот же промежуток времени. Медиана наблюдения составила 8 (1-28) месяцев в обеих группах. Проводилась оценка острой токсичности по шкале Common Terminology Criteria for Adverse Events 4.0 (CTCAE), скорости восстановления кроветворения, а так же общей выживаемости (ОВ), выживаемости без прогрессирования (ВБП) и времени до прогрессирования (ВДП) в течение 18 месяцев после ауто-ТГСК. При исследовании ВБП и ВДП из анализа исключены 4 пациента контрольной группы с ЛХ, которые получали посттрансплантационную терапию брентуксимаб ведотином. Основными заболеваниями в группе исследования были: ЛХ п=6 (60%) и НХЛ п=4 (40%), в контрольной группе – ЛХ п=29 (72,5%) и НХЛ п=11 (27,5%). ВИЧ-статус на момент трансплантации в группе исследования: вирусная нагрузка (ПЦР-РНК ВИЧ) – <50 копий/мл; медиана уровня CD4+ клеток составила 484 (210-715) клеток/ мкл; все пациенты получали АРВТ. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Общая выживаемость в течение 18 месяцев от ауто-ТГСК составила 88% (n=50): в группе пациентов с ВИЧ – 90%, в группе сравнения – 87,5% (р=0,605). Медиана дня восстановления лейкоцитов, нейтрофилов и тромбоцитов в группе исследования составила Д+14, Д+17, Д+20, в группе сравнения – Д+14, Д+16, Д+19, соответственно. В результате анализа токсичности по шкале СТСАЕ, частота развития энтеро-, гепато-, нефро- токсичности в обеих группах не различалась (таблица 1). Частота рецидива основного заболевания в течение 18 месяцев у пациентов с ВИЧ инфекцией составила 20%, медиана ВДП – 3 мес. (2-4), в контрольной группе – 11,1%, медиана ВДП – 8,5 мес. (3-11) (р=0,645). Выживаемость без прогрессирования в течение 18 месяцев после ауто-ТГСК составила 76,1% (n=46): в группе пациентов с ВИЧ – 70%, в группе сравнения – 77,8% (р=0,892). При анализе в подгруппах ЛХ и НХЛ различий в ОВ, ВБП и ВДП различий не обнаружено. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Общая выживаемость в течение 18 месяцев после высокодозной химиотерапии с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ составила 90%, и не отличалась от контрольной группы. Показатели выживаемости без прогрессирования у пациентов с ВИЧ и частоты рецидивов составили 70% и 20% соответственно, и не отличались от группы пациентов без ВИЧ. Восстановление кроветворения и спектр токсичности не различались в группах сравнения. Полученные данные подтверждают, что высокодозная химиотерапия с ауто-ТГСК такая же эффективная и безопасная процедура у пациентов с ВИЧ-ассоциированными лимфомами, как и у пациентов с лимфомами без ВИЧ. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> ВИЧ-ассоциированные лимфомы, ВИЧ, аутологичная трансплантация гемопоэтическх стволовых клеток, высокодозная химиотерапия, общая выживаемость, токсичность, восстановление гемопоэза, ВИЧ-статус, выживаемость без прогрессирования. </p> <h2 style="text-align: justify;">Литература</h2> <p style="text-align: justify;"> 1. Yanik EL, Napravnik S, Cole SR, Achenbach CJ, Gopal S, Olshan A, et al. Incidence and timing of cancer in HIV-infected individuals following initiation of combination antiretroviral therapy. Clin Infect Dis. 2013;57:756–764.<br> 2. Krishnan A, Palmer JM, Zaia JA, Tsai NC, Alvarnas J, Forman SJ. HIV status does not affect the outcome of autologous stem cell transplantation (ASCT) for non-Hodgkin lymphoma (NHL). Biol Blood Marrow Transplantation. 2010;16(9):1302-1308. </p> <h2 style="text-align: justify;">Таблица 1. Клинические характеристики ВИЧ-инфицированной и контрольной групп пациентов</h2> <p style="text-align: justify;"> <img width="787" alt="52_таблица 1.png" src="/upload/medialibrary/328/52_tablitsa-1.png" height="209" title="52_таблица 1.png"> </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(358) "Высокодозная химиотерапия с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ-инфекции: результаты проспективного сравнительного исследования" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(358) "Высокодозная химиотерапия с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ-инфекции: результаты проспективного сравнительного исследования" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(358) "Высокодозная химиотерапия с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ-инфекции: результаты проспективного сравнительного исследования" ["SECTION_META_TITLE"]=> string(358) "Высокодозная химиотерапия с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ-инфекции: результаты проспективного сравнительного исследования" ["SECTION_META_KEYWORDS"]=> string(358) "Высокодозная химиотерапия с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ-инфекции: результаты проспективного сравнительного исследования" ["SECTION_META_DESCRIPTION"]=> string(358) "Высокодозная химиотерапия с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ-инфекции: результаты проспективного сравнительного исследования" ["SECTION_PICTURE_FILE_ALT"]=> string(358) "Высокодозная химиотерапия с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ-инфекции: результаты проспективного сравнительного исследования" ["SECTION_PICTURE_FILE_TITLE"]=> string(358) "Высокодозная химиотерапия с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ-инфекции: результаты проспективного сравнительного исследования" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "vysokodoznaya-khimioterapiya-s-autologichnoy-transplantatsiey-gemopoeticheskikh-stvolovykh-kletok-u-" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(358) "Высокодозная химиотерапия с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ-инфекции: результаты проспективного сравнительного исследования" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(358) "Высокодозная химиотерапия с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ-инфекции: результаты проспективного сравнительного исследования" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vysokodoznaya-khimioterapiya-s-autologichnoy-transplantatsiey-gemopoeticheskikh-stvolovykh-kletok-u-" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "vysokodoznaya-khimioterapiya-s-autologichnoy-transplantatsiey-gemopoeticheskikh-stvolovykh-kletok-u-" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vysokodoznaya-khimioterapiya-s-autologichnoy-transplantatsiey-gemopoeticheskikh-stvolovykh-kletok-u-" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20718" ["VALUE"]=> array(2) { ["TEXT"]=> string(394) "Иван В. Цыганков, Марина О. Попова, Анастасия В. Некрасова, Юлия А. Рогачева, Кирилл В. Лепик, Елена В. Кондакова, Елена И. Дарская, Лилия В. Стельмах, Юрий Р. Залялов, Вадим В. Байков, Наталья Б. Михайлова, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(394) "Иван В. Цыганков, Марина О. Попова, Анастасия В. Некрасова, Юлия А. Рогачева, Кирилл В. Лепик, Елена В. Кондакова, Елена И. Дарская, Лилия В. Стельмах, Юрий Р. Залялов, Вадим В. Байков, Наталья Б. Михайлова, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20719" ["VALUE"]=> array(2) { ["TEXT"]=> string(456) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(456) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20720" ["VALUE"]=> array(2) { ["TEXT"]=> string(8790) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Вирус иммунодефицита человека (ВИЧ) связан с высоким риском развития злокачественных новообразований, таких как – лимфома Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на успешное применение антиретровирусной терапии (АРВТ) [1]. Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать агрессивную терапию, включающую высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [2]. Результаты ауто-ТГСК для лечения ВИЧ-ассоциированных лимфом все еще являются предметом споров. Количество проспективных сравнительных исследований эффективности и безопасности ВДХТ с последующей ауто-ТГСК ограничено. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В проспективное исследование включены 10 пациентов с лимфомами на фоне ВИЧ (группа исследования), которым была проведена ВДХТ с последующей ауто-ТГСК в клинике НИИ ДОГиТ в период с 2016 по 2018 год. Для сравнения эффективности и безопасности процедуры использован метод «случай-контроль» (1:4) и, в качестве группы сравнения, в исследование включены 40 пациентов без ВИЧ-инфекции, сопоставимые по основным характеристикам (контрольная группа), которым была выполнена ауто-ТГСК в тот же промежуток времени. Медиана наблюдения составила 8 (1-28) месяцев в обеих группах. Проводилась оценка острой токсичности по шкале Common Terminology Criteria for Adverse Events 4.0 (CTCAE), скорости восстановления кроветворения, а так же общей выживаемости (ОВ), выживаемости без прогрессирования (ВБП) и времени до прогрессирования (ВДП) в течение 18 месяцев после ауто-ТГСК. При исследовании ВБП и ВДП из анализа исключены 4 пациента контрольной группы с ЛХ, которые получали посттрансплантационную терапию брентуксимаб ведотином. Основными заболеваниями в группе исследования были: ЛХ п=6 (60%) и НХЛ п=4 (40%), в контрольной группе – ЛХ п=29 (72,5%) и НХЛ п=11 (27,5%). ВИЧ-статус на момент трансплантации в группе исследования: вирусная нагрузка (ПЦР-РНК ВИЧ) – <50 копий/мл; медиана уровня CD4+ клеток составила 484 (210-715) клеток/ мкл; все пациенты получали АРВТ. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Общая выживаемость в течение 18 месяцев от ауто-ТГСК составила 88% (n=50): в группе пациентов с ВИЧ – 90%, в группе сравнения – 87,5% (р=0,605). Медиана дня восстановления лейкоцитов, нейтрофилов и тромбоцитов в группе исследования составила Д+14, Д+17, Д+20, в группе сравнения – Д+14, Д+16, Д+19, соответственно. В результате анализа токсичности по шкале СТСАЕ, частота развития энтеро-, гепато-, нефро- токсичности в обеих группах не различалась (таблица 1). Частота рецидива основного заболевания в течение 18 месяцев у пациентов с ВИЧ инфекцией составила 20%, медиана ВДП – 3 мес. (2-4), в контрольной группе – 11,1%, медиана ВДП – 8,5 мес. (3-11) (р=0,645). Выживаемость без прогрессирования в течение 18 месяцев после ауто-ТГСК составила 76,1% (n=46): в группе пациентов с ВИЧ – 70%, в группе сравнения – 77,8% (р=0,892). При анализе в подгруппах ЛХ и НХЛ различий в ОВ, ВБП и ВДП различий не обнаружено. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Общая выживаемость в течение 18 месяцев после высокодозной химиотерапии с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ составила 90%, и не отличалась от контрольной группы. Показатели выживаемости без прогрессирования у пациентов с ВИЧ и частоты рецидивов составили 70% и 20% соответственно, и не отличались от группы пациентов без ВИЧ. Восстановление кроветворения и спектр токсичности не различались в группах сравнения. Полученные данные подтверждают, что высокодозная химиотерапия с ауто-ТГСК такая же эффективная и безопасная процедура у пациентов с ВИЧ-ассоциированными лимфомами, как и у пациентов с лимфомами без ВИЧ. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> ВИЧ-ассоциированные лимфомы, ВИЧ, аутологичная трансплантация гемопоэтическх стволовых клеток, высокодозная химиотерапия, общая выживаемость, токсичность, восстановление гемопоэза, ВИЧ-статус, выживаемость без прогрессирования. </p> <h2 style="text-align: justify;">Литература</h2> <p style="text-align: justify;"> 1. Yanik EL, Napravnik S, Cole SR, Achenbach CJ, Gopal S, Olshan A, et al. Incidence and timing of cancer in HIV-infected individuals following initiation of combination antiretroviral therapy. Clin Infect Dis. 2013;57:756–764.<br> 2. Krishnan A, Palmer JM, Zaia JA, Tsai NC, Alvarnas J, Forman SJ. HIV status does not affect the outcome of autologous stem cell transplantation (ASCT) for non-Hodgkin lymphoma (NHL). Biol Blood Marrow Transplantation. 2010;16(9):1302-1308. </p> <h2 style="text-align: justify;">Таблица 1. Клинические характеристики ВИЧ-инфицированной и контрольной групп пациентов</h2> <p style="text-align: justify;"> <img width="787" alt="52_таблица 1.png" src="/upload/medialibrary/328/52_tablitsa-1.png" height="209" title="52_таблица 1.png"> </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(8404) "Введение
Вирус иммунодефицита человека (ВИЧ) связан с высоким риском развития злокачественных новообразований, таких как – лимфома Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на успешное применение антиретровирусной терапии (АРВТ) [1]. Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать агрессивную терапию, включающую высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [2]. Результаты ауто-ТГСК для лечения ВИЧ-ассоциированных лимфом все еще являются предметом споров. Количество проспективных сравнительных исследований эффективности и безопасности ВДХТ с последующей ауто-ТГСК ограничено.
Пациенты и методы
В проспективное исследование включены 10 пациентов с лимфомами на фоне ВИЧ (группа исследования), которым была проведена ВДХТ с последующей ауто-ТГСК в клинике НИИ ДОГиТ в период с 2016 по 2018 год. Для сравнения эффективности и безопасности процедуры использован метод «случай-контроль» (1:4) и, в качестве группы сравнения, в исследование включены 40 пациентов без ВИЧ-инфекции, сопоставимые по основным характеристикам (контрольная группа), которым была выполнена ауто-ТГСК в тот же промежуток времени. Медиана наблюдения составила 8 (1-28) месяцев в обеих группах. Проводилась оценка острой токсичности по шкале Common Terminology Criteria for Adverse Events 4.0 (CTCAE), скорости восстановления кроветворения, а так же общей выживаемости (ОВ), выживаемости без прогрессирования (ВБП) и времени до прогрессирования (ВДП) в течение 18 месяцев после ауто-ТГСК. При исследовании ВБП и ВДП из анализа исключены 4 пациента контрольной группы с ЛХ, которые получали посттрансплантационную терапию брентуксимаб ведотином. Основными заболеваниями в группе исследования были: ЛХ п=6 (60%) и НХЛ п=4 (40%), в контрольной группе – ЛХ п=29 (72,5%) и НХЛ п=11 (27,5%). ВИЧ-статус на момент трансплантации в группе исследования: вирусная нагрузка (ПЦР-РНК ВИЧ) – <50 копий/мл; медиана уровня CD4+ клеток составила 484 (210-715) клеток/ мкл; все пациенты получали АРВТ.
Результаты
Общая выживаемость в течение 18 месяцев от ауто-ТГСК составила 88% (n=50): в группе пациентов с ВИЧ – 90%, в группе сравнения – 87,5% (р=0,605). Медиана дня восстановления лейкоцитов, нейтрофилов и тромбоцитов в группе исследования составила Д+14, Д+17, Д+20, в группе сравнения – Д+14, Д+16, Д+19, соответственно. В результате анализа токсичности по шкале СТСАЕ, частота развития энтеро-, гепато-, нефро- токсичности в обеих группах не различалась (таблица 1). Частота рецидива основного заболевания в течение 18 месяцев у пациентов с ВИЧ инфекцией составила 20%, медиана ВДП – 3 мес. (2-4), в контрольной группе – 11,1%, медиана ВДП – 8,5 мес. (3-11) (р=0,645). Выживаемость без прогрессирования в течение 18 месяцев после ауто-ТГСК составила 76,1% (n=46): в группе пациентов с ВИЧ – 70%, в группе сравнения – 77,8% (р=0,892). При анализе в подгруппах ЛХ и НХЛ различий в ОВ, ВБП и ВДП различий не обнаружено.
Заключение
Общая выживаемость в течение 18 месяцев после высокодозной химиотерапии с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ составила 90%, и не отличалась от контрольной группы. Показатели выживаемости без прогрессирования у пациентов с ВИЧ и частоты рецидивов составили 70% и 20% соответственно, и не отличались от группы пациентов без ВИЧ. Восстановление кроветворения и спектр токсичности не различались в группах сравнения. Полученные данные подтверждают, что высокодозная химиотерапия с ауто-ТГСК такая же эффективная и безопасная процедура у пациентов с ВИЧ-ассоциированными лимфомами, как и у пациентов с лимфомами без ВИЧ.
Ключевые слова
ВИЧ-ассоциированные лимфомы, ВИЧ, аутологичная трансплантация гемопоэтическх стволовых клеток, высокодозная химиотерапия, общая выживаемость, токсичность, восстановление гемопоэза, ВИЧ-статус, выживаемость без прогрессирования.
Литература
1. Yanik EL, Napravnik S, Cole SR, Achenbach CJ, Gopal S, Olshan A, et al. Incidence and timing of cancer in HIV-infected individuals following initiation of combination antiretroviral therapy. Clin Infect Dis. 2013;57:756–764.
2. Krishnan A, Palmer JM, Zaia JA, Tsai NC, Alvarnas J, Forman SJ. HIV status does not affect the outcome of autologous stem cell transplantation (ASCT) for non-Hodgkin lymphoma (NHL). Biol Blood Marrow Transplantation. 2010;16(9):1302-1308.
Таблица 1. Клинические характеристики ВИЧ-инфицированной и контрольной групп пациентов

Introduction
Infection with human immunodeficiency virus (HIV) is associated with a significantly increased risk of cancer, including Hodgkin lymphoma (HL) and non-Hodgkin lymphoma (NHL), even when patients are treated successfully with contemporary antiretroviral therapy [1]. Widespread use of the antiretroviral therapy (ART) has changed the approach to treatment of the HIV-related lymphomas, allowing the use of aggressive therapy including high-dose chemotherapy (HDC) followed by autologous hematopoietic stem cell transplantation (ASCT) [2]. The outcome of ASCT for HIV-related lymphomas is still a subject for controversy. The number of a prospective case-control studies where estimated safety and efficiency of ASCT procedure is limited.
Patients and methods
From January 2016 to March 2018, ten patients with HIV-related lymphoma who underwent HDC followed by ASCT were included into a prospective study (study HIV-infected group, n=10). To compare the efficacy and safety of the procedure, a “case-control” method (1:4) have been applied. The comparison group consisted of non-HIV-infected patients with lymphoma comparable for basic characteristics patients, who have undergone ASCT at the same period of time (control group, n=40). Median follow-up time was 8 (1- 28) months for both groups. The primary endpoint of the study was to estimate overall survival (OS) at 18 months after ASCT, time of hematopoietic recovery and toxicity according to Common Terminology Criteria for Adverse Events 4.0 (CTCAE). Secondary endpoints included relapse rate calculated by time to progression (TTP) and progression free survival (PFS) at 18 months after ASCT. Four patients of control group with HL who was treated with brentuximab vedotin after ASCT were excluded from the TTP and PFS analyses. The underlying diseases in HIV-group were: HL (n=6; 60%), NHL (n=4; 40%); in control group: HL (n=29; 72.5 %), and NHL (n=11; 27.5%). HIV status in study group at the moment of transplantation showed undetectable HIV viral load (<50 copies/mL) in all patients; the median CD4+ cell number was 473 (210-715) cells/μL, and all the patients received ART.
Results
Overall survival (OS) at 18 months after ASCT for the entire patient group (n=50) was 88%: in the HIV-group, 90% versus 87.5% in control group (p=0.605). The median terms for recovery of leukocytes, neutrophils, and platelets were D+14, D+17, D+20 in HIV-group and D+14, D+16, D+19 in control group, respectively. Toxicity rates, according to CTCAE are shown in Table 1. Relapse incidence of the underlying disease at 18 months after ASCT was 20%, with the median TTP of 3 months (2-4) in HIV-group, and 11.1% with median TTP value of 8.5 months (3-11) in control group (р=0.645). Progression-free survival at 18 months after ASCT was 76.1% (n=46): in HIV-group, 70% versus 77.8% in control group (p=0.892). There were no differences revealed in the subgroup analysis for separate HL and NHL cases.
Table 1. Clinical characteristics of HIV-positive and HIV-negative groups

Conclusion
Overall survival at 18 months after HDC followed by ASCT in patients with HIV-related lymphomas was 90%, whereas progression-free survival was 70%, the relapse incidence was 20% with median time to progression 3 months (2-4) and did not differ from the group of patients without HIV infection. We have not found any statistically significant differences between the two groups for hematopoietic recovery
and toxicity rates. The obtained data confirm that ASCT is a safe and efficient procedure for HIV-related lymphomas, as well as for lymphoma patients without HIV.
Keywords
HIV-related lymphoma, HIV, autologous hematopoietic stem cell transplantation, high-dose chemotherapy, overall survival, toxicity, hematopoiesis recovery, HIV status, progression free survival.
References
1. Yanik EL, Napravnik S, Cole SR, Achenbach CJ, Gopal S, Olshan A, et al. Incidence and timing of cancer in HIV-infected individuals following initiation of combination antiretroviral therapy. Clin Infect Dis. 2013; 57: 756–764.
2. Krishnan A, Palmer JM, Zaia JA, Tsai NC, Alvarnas J, Forman SJ. HIV status does not affect the outcome of autologous stem cell transplantation (ASCT) for non-Hodgkin lymphoma (NHL). Biol Blood Marrow Transplantation. 2010; 16(9):1302-1308.
Introduction
Infection with human immunodeficiency virus (HIV) is associated with a significantly increased risk of cancer, including Hodgkin lymphoma (HL) and non-Hodgkin lymphoma (NHL), even when patients are treated successfully with contemporary antiretroviral therapy [1]. Widespread use of the antiretroviral therapy (ART) has changed the approach to treatment of the HIV-related lymphomas, allowing the use of aggressive therapy including high-dose chemotherapy (HDC) followed by autologous hematopoietic stem cell transplantation (ASCT) [2]. The outcome of ASCT for HIV-related lymphomas is still a subject for controversy. The number of a prospective case-control studies where estimated safety and efficiency of ASCT procedure is limited.
Patients and methods
From January 2016 to March 2018, ten patients with HIV-related lymphoma who underwent HDC followed by ASCT were included into a prospective study (study HIV-infected group, n=10). To compare the efficacy and safety of the procedure, a “case-control” method (1:4) have been applied. The comparison group consisted of non-HIV-infected patients with lymphoma comparable for basic characteristics patients, who have undergone ASCT at the same period of time (control group, n=40). Median follow-up time was 8 (1- 28) months for both groups. The primary endpoint of the study was to estimate overall survival (OS) at 18 months after ASCT, time of hematopoietic recovery and toxicity according to Common Terminology Criteria for Adverse Events 4.0 (CTCAE). Secondary endpoints included relapse rate calculated by time to progression (TTP) and progression free survival (PFS) at 18 months after ASCT. Four patients of control group with HL who was treated with brentuximab vedotin after ASCT were excluded from the TTP and PFS analyses. The underlying diseases in HIV-group were: HL (n=6; 60%), NHL (n=4; 40%); in control group: HL (n=29; 72.5 %), and NHL (n=11; 27.5%). HIV status in study group at the moment of transplantation showed undetectable HIV viral load (<50 copies/mL) in all patients; the median CD4+ cell number was 473 (210-715) cells/μL, and all the patients received ART.
Results
Overall survival (OS) at 18 months after ASCT for the entire patient group (n=50) was 88%: in the HIV-group, 90% versus 87.5% in control group (p=0.605). The median terms for recovery of leukocytes, neutrophils, and platelets were D+14, D+17, D+20 in HIV-group and D+14, D+16, D+19 in control group, respectively. Toxicity rates, according to CTCAE are shown in Table 1. Relapse incidence of the underlying disease at 18 months after ASCT was 20%, with the median TTP of 3 months (2-4) in HIV-group, and 11.1% with median TTP value of 8.5 months (3-11) in control group (р=0.645). Progression-free survival at 18 months after ASCT was 76.1% (n=46): in HIV-group, 70% versus 77.8% in control group (p=0.892). There were no differences revealed in the subgroup analysis for separate HL and NHL cases.
Table 1. Clinical characteristics of HIV-positive and HIV-negative groups

Conclusion
Overall survival at 18 months after HDC followed by ASCT in patients with HIV-related lymphomas was 90%, whereas progression-free survival was 70%, the relapse incidence was 20% with median time to progression 3 months (2-4) and did not differ from the group of patients without HIV infection. We have not found any statistically significant differences between the two groups for hematopoietic recovery
and toxicity rates. The obtained data confirm that ASCT is a safe and efficient procedure for HIV-related lymphomas, as well as for lymphoma patients without HIV.
Keywords
HIV-related lymphoma, HIV, autologous hematopoietic stem cell transplantation, high-dose chemotherapy, overall survival, toxicity, hematopoiesis recovery, HIV status, progression free survival.
References
1. Yanik EL, Napravnik S, Cole SR, Achenbach CJ, Gopal S, Olshan A, et al. Incidence and timing of cancer in HIV-infected individuals following initiation of combination antiretroviral therapy. Clin Infect Dis. 2013; 57: 756–764.
2. Krishnan A, Palmer JM, Zaia JA, Tsai NC, Alvarnas J, Forman SJ. HIV status does not affect the outcome of autologous stem cell transplantation (ASCT) for non-Hodgkin lymphoma (NHL). Biol Blood Marrow Transplantation. 2010; 16(9):1302-1308.
Introduction
Infection with human immunodeficiency virus (HIV) is associated with a significantly increased risk of cancer, including Hodgkin lymphoma (HL) and non-Hodgkin lymphoma (NHL), even when patients are treated successfully with contemporary antiretroviral therapy [1]. Widespread use of the antiretroviral therapy (ART) has changed the approach to treatment of the HIV-related lymphomas, allowing the use of aggressive therapy including high-dose chemotherapy (HDC) followed by autologous hematopoietic stem cell transplantation (ASCT) [2]. The outcome of ASCT for HIV-related lymphomas is still a subject for controversy. The number of a prospective case-control studies where estimated safety and efficiency of ASCT procedure is limited.
Patients and methods
From January 2016 to March 2018, ten patients with HIV-related lymphoma who underwent HDC followed by ASCT were included into a prospective study (study HIV-infected group, n=10). To compare the efficacy and safety of the procedure, a “case-control” method (1:4) have been applied. The comparison group consisted of non-HIV-infected patients with lymphoma comparable for basic characteristics patients, who have undergone ASCT at the same period of time (control group, n=40). Median follow-up time was 8 (1- 28) months for both groups. The primary endpoint of the study was to estimate overall survival (OS) at 18 months after ASCT, time of hematopoietic recovery and toxicity according to Common Terminology Criteria for Adverse Events 4.0 (CTCAE). Secondary endpoints included relapse rate calculated by time to progression (TTP) and progression free survival (PFS) at 18 months after ASCT. Four patients of control group with HL who was treated with brentuximab vedotin after ASCT were excluded from the TTP and PFS analyses. The underlying diseases in HIV-group were: HL (n=6; 60%), NHL (n=4; 40%); in control group: HL (n=29; 72.5 %), and NHL (n=11; 27.5%). HIV status in study group at the moment of transplantation showed undetectable HIV viral load (<50 copies/mL) in all patients; the median CD4+ cell number was 473 (210-715) cells/μL, and all the patients received ART.
Results
Overall survival (OS) at 18 months after ASCT for the entire patient group (n=50) was 88%: in the HIV-group, 90% versus 87.5% in control group (p=0.605). The median terms for recovery of leukocytes, neutrophils, and platelets were D+14, D+17, D+20 in HIV-group and D+14, D+16, D+19 in control group, respectively. Toxicity rates, according to CTCAE are shown in Table 1. Relapse incidence of the underlying disease at 18 months after ASCT was 20%, with the median TTP of 3 months (2-4) in HIV-group, and 11.1% with median TTP value of 8.5 months (3-11) in control group (р=0.645). Progression-free survival at 18 months after ASCT was 76.1% (n=46): in HIV-group, 70% versus 77.8% in control group (p=0.892). There were no differences revealed in the subgroup analysis for separate HL and NHL cases.
Table 1. Clinical characteristics of HIV-positive and HIV-negative groups

Conclusion
Overall survival at 18 months after HDC followed by ASCT in patients with HIV-related lymphomas was 90%, whereas progression-free survival was 70%, the relapse incidence was 20% with median time to progression 3 months (2-4) and did not differ from the group of patients without HIV infection. We have not found any statistically significant differences between the two groups for hematopoietic recovery
and toxicity rates. The obtained data confirm that ASCT is a safe and efficient procedure for HIV-related lymphomas, as well as for lymphoma patients without HIV.
Keywords
HIV-related lymphoma, HIV, autologous hematopoietic stem cell transplantation, high-dose chemotherapy, overall survival, toxicity, hematopoiesis recovery, HIV status, progression free survival.
References
1. Yanik EL, Napravnik S, Cole SR, Achenbach CJ, Gopal S, Olshan A, et al. Incidence and timing of cancer in HIV-infected individuals following initiation of combination antiretroviral therapy. Clin Infect Dis. 2013; 57: 756–764.
2. Krishnan A, Palmer JM, Zaia JA, Tsai NC, Alvarnas J, Forman SJ. HIV status does not affect the outcome of autologous stem cell transplantation (ASCT) for non-Hodgkin lymphoma (NHL). Biol Blood Marrow Transplantation. 2010; 16(9):1302-1308.
Введение
Вирус иммунодефицита человека (ВИЧ) связан с высоким риском развития злокачественных новообразований, таких как – лимфома Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на успешное применение антиретровирусной терапии (АРВТ) [1]. Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать агрессивную терапию, включающую высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [2]. Результаты ауто-ТГСК для лечения ВИЧ-ассоциированных лимфом все еще являются предметом споров. Количество проспективных сравнительных исследований эффективности и безопасности ВДХТ с последующей ауто-ТГСК ограничено.
Пациенты и методы
В проспективное исследование включены 10 пациентов с лимфомами на фоне ВИЧ (группа исследования), которым была проведена ВДХТ с последующей ауто-ТГСК в клинике НИИ ДОГиТ в период с 2016 по 2018 год. Для сравнения эффективности и безопасности процедуры использован метод «случай-контроль» (1:4) и, в качестве группы сравнения, в исследование включены 40 пациентов без ВИЧ-инфекции, сопоставимые по основным характеристикам (контрольная группа), которым была выполнена ауто-ТГСК в тот же промежуток времени. Медиана наблюдения составила 8 (1-28) месяцев в обеих группах. Проводилась оценка острой токсичности по шкале Common Terminology Criteria for Adverse Events 4.0 (CTCAE), скорости восстановления кроветворения, а так же общей выживаемости (ОВ), выживаемости без прогрессирования (ВБП) и времени до прогрессирования (ВДП) в течение 18 месяцев после ауто-ТГСК. При исследовании ВБП и ВДП из анализа исключены 4 пациента контрольной группы с ЛХ, которые получали посттрансплантационную терапию брентуксимаб ведотином. Основными заболеваниями в группе исследования были: ЛХ п=6 (60%) и НХЛ п=4 (40%), в контрольной группе – ЛХ п=29 (72,5%) и НХЛ п=11 (27,5%). ВИЧ-статус на момент трансплантации в группе исследования: вирусная нагрузка (ПЦР-РНК ВИЧ) – <50 копий/мл; медиана уровня CD4+ клеток составила 484 (210-715) клеток/ мкл; все пациенты получали АРВТ.
Результаты
Общая выживаемость в течение 18 месяцев от ауто-ТГСК составила 88% (n=50): в группе пациентов с ВИЧ – 90%, в группе сравнения – 87,5% (р=0,605). Медиана дня восстановления лейкоцитов, нейтрофилов и тромбоцитов в группе исследования составила Д+14, Д+17, Д+20, в группе сравнения – Д+14, Д+16, Д+19, соответственно. В результате анализа токсичности по шкале СТСАЕ, частота развития энтеро-, гепато-, нефро- токсичности в обеих группах не различалась (таблица 1). Частота рецидива основного заболевания в течение 18 месяцев у пациентов с ВИЧ инфекцией составила 20%, медиана ВДП – 3 мес. (2-4), в контрольной группе – 11,1%, медиана ВДП – 8,5 мес. (3-11) (р=0,645). Выживаемость без прогрессирования в течение 18 месяцев после ауто-ТГСК составила 76,1% (n=46): в группе пациентов с ВИЧ – 70%, в группе сравнения – 77,8% (р=0,892). При анализе в подгруппах ЛХ и НХЛ различий в ОВ, ВБП и ВДП различий не обнаружено.
Заключение
Общая выживаемость в течение 18 месяцев после высокодозной химиотерапии с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ составила 90%, и не отличалась от контрольной группы. Показатели выживаемости без прогрессирования у пациентов с ВИЧ и частоты рецидивов составили 70% и 20% соответственно, и не отличались от группы пациентов без ВИЧ. Восстановление кроветворения и спектр токсичности не различались в группах сравнения. Полученные данные подтверждают, что высокодозная химиотерапия с ауто-ТГСК такая же эффективная и безопасная процедура у пациентов с ВИЧ-ассоциированными лимфомами, как и у пациентов с лимфомами без ВИЧ.
Ключевые слова
ВИЧ-ассоциированные лимфомы, ВИЧ, аутологичная трансплантация гемопоэтическх стволовых клеток, высокодозная химиотерапия, общая выживаемость, токсичность, восстановление гемопоэза, ВИЧ-статус, выживаемость без прогрессирования.
Литература
1. Yanik EL, Napravnik S, Cole SR, Achenbach CJ, Gopal S, Olshan A, et al. Incidence and timing of cancer in HIV-infected individuals following initiation of combination antiretroviral therapy. Clin Infect Dis. 2013;57:756–764.
2. Krishnan A, Palmer JM, Zaia JA, Tsai NC, Alvarnas J, Forman SJ. HIV status does not affect the outcome of autologous stem cell transplantation (ASCT) for non-Hodgkin lymphoma (NHL). Biol Blood Marrow Transplantation. 2010;16(9):1302-1308.
Таблица 1. Клинические характеристики ВИЧ-инфицированной и контрольной групп пациентов

Введение
Вирус иммунодефицита человека (ВИЧ) связан с высоким риском развития злокачественных новообразований, таких как – лимфома Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на успешное применение антиретровирусной терапии (АРВТ) [1]. Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать агрессивную терапию, включающую высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [2]. Результаты ауто-ТГСК для лечения ВИЧ-ассоциированных лимфом все еще являются предметом споров. Количество проспективных сравнительных исследований эффективности и безопасности ВДХТ с последующей ауто-ТГСК ограничено.
Пациенты и методы
В проспективное исследование включены 10 пациентов с лимфомами на фоне ВИЧ (группа исследования), которым была проведена ВДХТ с последующей ауто-ТГСК в клинике НИИ ДОГиТ в период с 2016 по 2018 год. Для сравнения эффективности и безопасности процедуры использован метод «случай-контроль» (1:4) и, в качестве группы сравнения, в исследование включены 40 пациентов без ВИЧ-инфекции, сопоставимые по основным характеристикам (контрольная группа), которым была выполнена ауто-ТГСК в тот же промежуток времени. Медиана наблюдения составила 8 (1-28) месяцев в обеих группах. Проводилась оценка острой токсичности по шкале Common Terminology Criteria for Adverse Events 4.0 (CTCAE), скорости восстановления кроветворения, а так же общей выживаемости (ОВ), выживаемости без прогрессирования (ВБП) и времени до прогрессирования (ВДП) в течение 18 месяцев после ауто-ТГСК. При исследовании ВБП и ВДП из анализа исключены 4 пациента контрольной группы с ЛХ, которые получали посттрансплантационную терапию брентуксимаб ведотином. Основными заболеваниями в группе исследования были: ЛХ п=6 (60%) и НХЛ п=4 (40%), в контрольной группе – ЛХ п=29 (72,5%) и НХЛ п=11 (27,5%). ВИЧ-статус на момент трансплантации в группе исследования: вирусная нагрузка (ПЦР-РНК ВИЧ) – <50 копий/мл; медиана уровня CD4+ клеток составила 484 (210-715) клеток/ мкл; все пациенты получали АРВТ.
Результаты
Общая выживаемость в течение 18 месяцев от ауто-ТГСК составила 88% (n=50): в группе пациентов с ВИЧ – 90%, в группе сравнения – 87,5% (р=0,605). Медиана дня восстановления лейкоцитов, нейтрофилов и тромбоцитов в группе исследования составила Д+14, Д+17, Д+20, в группе сравнения – Д+14, Д+16, Д+19, соответственно. В результате анализа токсичности по шкале СТСАЕ, частота развития энтеро-, гепато-, нефро- токсичности в обеих группах не различалась (таблица 1). Частота рецидива основного заболевания в течение 18 месяцев у пациентов с ВИЧ инфекцией составила 20%, медиана ВДП – 3 мес. (2-4), в контрольной группе – 11,1%, медиана ВДП – 8,5 мес. (3-11) (р=0,645). Выживаемость без прогрессирования в течение 18 месяцев после ауто-ТГСК составила 76,1% (n=46): в группе пациентов с ВИЧ – 70%, в группе сравнения – 77,8% (р=0,892). При анализе в подгруппах ЛХ и НХЛ различий в ОВ, ВБП и ВДП различий не обнаружено.
Заключение
Общая выживаемость в течение 18 месяцев после высокодозной химиотерапии с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ составила 90%, и не отличалась от контрольной группы. Показатели выживаемости без прогрессирования у пациентов с ВИЧ и частоты рецидивов составили 70% и 20% соответственно, и не отличались от группы пациентов без ВИЧ. Восстановление кроветворения и спектр токсичности не различались в группах сравнения. Полученные данные подтверждают, что высокодозная химиотерапия с ауто-ТГСК такая же эффективная и безопасная процедура у пациентов с ВИЧ-ассоциированными лимфомами, как и у пациентов с лимфомами без ВИЧ.
Ключевые слова
ВИЧ-ассоциированные лимфомы, ВИЧ, аутологичная трансплантация гемопоэтическх стволовых клеток, высокодозная химиотерапия, общая выживаемость, токсичность, восстановление гемопоэза, ВИЧ-статус, выживаемость без прогрессирования.
Литература
1. Yanik EL, Napravnik S, Cole SR, Achenbach CJ, Gopal S, Olshan A, et al. Incidence and timing of cancer in HIV-infected individuals following initiation of combination antiretroviral therapy. Clin Infect Dis. 2013;57:756–764.
2. Krishnan A, Palmer JM, Zaia JA, Tsai NC, Alvarnas J, Forman SJ. HIV status does not affect the outcome of autologous stem cell transplantation (ASCT) for non-Hodgkin lymphoma (NHL). Biol Blood Marrow Transplantation. 2010;16(9):1302-1308.
Таблица 1. Клинические характеристики ВИЧ-инфицированной и контрольной групп пациентов

Введение
Аллогенная трансплантация гемопоэтических столовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелоидным лейкозом группы высокого риска (ОМЛ). Возникновение рецидива после алло-ТГСК происходит примерно у 20-50% пациентов в зависимости от стадии заболевания на момент трансплантации и отрицательных прогностических факторов. Одним из предикторов рецидива при ОМЛ может быть минимальная остаточная болезнь (МОБ), определяемая с помощью проточной цитофлюорометрии или полимеразной цепной реакции. Опубликованные исследования демонстрируют высокую прогностическую значимость определения МОБ непосредственно перед проведением алло-ТГСК у взрослых пациентов. Однако у детей с ОМЛ данные о влиянии МОБ перед алло-ТГСК на эффективность лечения ограничены. Целью данного исследования стала оценка влияния МОБ перед алло-ТГСК на общую выживаемость (ОВ), бессобытийную выживаемость (БСВ), безрецидивную выживаемость (БРВ), трансплантационную летальность, кумулятивную частоту рецидива (ЧР) и частоту первичного неприживления у детей и подростков с ОМЛ.
Материалы и методы
С 2008-2018 гг. в клинике НИИ ДОГиТ им. Р. М. Горбачевой алло-ТГСК проведена 95 детям с ОМЛ в клинико-гематологической ремиссии заболевания заболевания. Большинство пациентов получили первичную химиотерапию по протоколу AML-BFM 2004. Для установления группы цитогенетического риска были использованы WHO критерии 2008 г. (пересмотр 2016 г.). Перед алло-ТГСК всем пациентам выполнялась аспирация/биопсия костного мозга для рестадирования. Среди этих пациентов у 79 проводилось определение МОБ с помощью молекулярно-генетического/цитогенетического исследований и/или метода иммунофенотипирования. Таким образом, 79 пациентов с медианой возраста 10 лет (1-18) на момент алло-ТГСК были включены в данное ретроспективное исследование. Все пациенты были поделены на 2 группы: 1 гр. – МОБ+ n=33 (42%), 2 гр. – МОБ– n=46 (58%). В первой ремиссии алло-ТГСК была выполнена 23 (70%) МОБ+ пациентам и 35 (76%) МОБ– пациентам. Высокий цитогенетический риск инициально наблюдался у 14/30 (46%) МОБ+ пациентов и у 16/40 (40%) МОБ– пациентов (p=0,7). В каждой группе наблюдалось равное число вторичных ОМЛ (n=4; 12% и n=4; 8% соответственно, p=0,7), а также ОМЛ с экстрамедуллярным поражением (n=6; 18% и n=6; 13% соответственно, p=0,5). В той и другой группе применялись различные по интенсивности режимы кондиционирования в равных пропорциях (РИК/МАК): в 1 гр. – 18/15 (1,2), во 2 гр. – 25/21 (1,2). ОВ, БСВ, БРВ, а также летальность, обусловленная терапией, были рассчитаны, используя метод Каплана-Майера. При определении БСВ за событие был принят рецидив лейкоза или смерть. Кумулятивная частота рецидива и первичного отторжения трансплантата установлены с помощью критерия Манна-Уитни.
Результаты
Приживление ГСК было зафиксировано у 71 (90%) пациента. Частота первичного неприживления в обеих группах была одинаковая (n=4; 12% и n=4; 8% соответственно, р=0,6). При медиане наблюдения 3 года ОВ составила 63,6% в группе МОБ+ и 69,6% в группе МОБ–(p=0,7). БСВ при данной медиане равна 45,5% у МОБ+ пациентов, 65,2% у МОБ– (p=0,1). Трехгодичная частота рецидива была достоверно выше у МОБ+ пациентов (n=14), чем у МОБ– (n=8) пациентов (42% и 17% соответственно, p=0,01). БРВ также достоверно различалась у пациентов с различным МОБ статусом (57,6% у МОБ+, 82,6% у МОБ–, р=0,02). Трансплантационная летальность составила 15,2% и 17,4% в 1-й и 2-й группах соответственно (p=0,6). Резистентный рецидив ОМЛ после алло-ТГСК был причиной смерти у 13/26 (50%) пациентов, среди них 7 МОБ+ пациентов, 6 МОБ– пациентов. Профилактическая/превентивная терапия гипометилирующими агентами ± инфузия донорских лимфоцитов (ИДЛ) была проведена 9 (27%) МОБ+ пациентам и 5 МОБ– (10%) пациентам. Рецидив после проведенной терапии произошел только у одного пациента из группы МОБ+.
Заключение
Данное исследование демонстрирует, что наличие предтрансплантационной МОБ у детей и подростков с ОМЛ ассоциировано с повышенным риском возникновения рецидива после алло-ТГСК (различие в ЧР, p= 0,01 и БРВ, р=0,02). При этом БСВ и ОВ достоверно не различались в обеих группах (р=0,7 и р=0,1, соответственно), так как рецидив не оказал решающего значения на данные показатели.
Ключевые слова
Острый миелоидный лейкоз, минимальная остаточная болезнь, алло-ТГСК,
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20707" ["VALUE"]=> array(2) { ["TEXT"]=> string(263) "Liubov A. Tsvetkova, Olesya V. Paina, Inna V. Markova, Polina V. Kozhokar’, Sergey N. Bondarenko, Ildar M. Barkhatov, Elena V. Babenko, Alexander L. Alyanskiy, Kirill A. Ekushev, Tatyana L. Gindina, Elena V. Semenova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(263) "Liubov A. Tsvetkova, Olesya V. Paina, Inna V. Markova, Polina V. Kozhokar’, Sergey N. Bondarenko, Ildar M. Barkhatov, Elena V. Babenko, Alexander L. Alyanskiy, Kirill A. Ekushev, Tatyana L. Gindina, Elena V. Semenova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20708" ["VALUE"]=> array(2) { ["TEXT"]=> string(176) "R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, I. P. Pavlov First Saint-Petersburg State Medical University, Saint-Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(176) "R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, I. P. Pavlov First Saint-Petersburg State Medical University, Saint-Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20709" ["VALUE"]=> array(2) { ["TEXT"]=> string(4612) "<h2></h2> <h2 style="text-align: justify;">Background</h2> <p style="text-align: justify;"> Allogeneic haemopoietic stem cell transplantation (allo-HSCT) – is an effective option in the treatment of high risk patients with acute myeloid leukemia (AML). The relapse after allo-HSCT occurs in about 20-50% of patients, depending on status of the disease and negative prognostic factors. Minimal residual disease (MRD) is a powerful and independent predictor of subsequent relapse, which is detected using polymerase chain reactions or multiparametric flow cytometry. Presented clinical data demonstrated the high prognostic significance of the measured MRD in adults before allo-HSCT. However, impact of pre-transplantation MRD status in children and adolescents with AML is not well elucidated. The goal of this study was to evaluate the impact of pre-transplantation MRD on overall survival (OS), event-free survival (EFS), transplant-related mortality (TRM), relapse-free survival (RFS), relapse incidence (RI) and primary graft failure in transplantation in children and adolescents with AML. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> From 2008 to 2018 a total of 95 AML pediatric patients of R. M. Gorbacheva Memorial Institute received allo-HSCT in complete clinical-hematological remission. Most of the patients received AML-BFM 2004 as primary treatment. We used WHO 2008 criteria (review 2016) to assign cytogenetic risk. All subsequent patients eligible for this study underwent bone marrow (BM) aspiration or biopsy prior to allo-HSCT. Among these patients, 79 were assessed for MRD before HSCT and were considered in this retrospective analysis. MRD was examined with immunophenotyping or polymerase chain reaction/ cytogenetic. The median age was 10 years (1-18). Patients were divided into 2 groups: 1 group – MRD-positive n=33 (42%), 2 group – MRD-negative n=46 (58%). Allo-HSCT was performed in first remission in 23 (70%) MRD-positive patients and 35 (76%) MRD-negative patients. High cytogenetic risk accounted for 14/30 (46%) MRD-positive and 16/40 (40%) MRD-negative patients (p=0.7). Equal number of secondary (n=4; 12% and n=4; 8%, respectively, p=0.7) AML, and also extramedullary (n=6; 18% and n=6; 13%, respectively, p=0.5) disease were observed in both groups. Different in intensity regimes of conditioning were used in equal proportions in both groups (RIC/MAC): 18/15 (1.2) in MRD-positive patients, 25/21 (1.2) in MRD-negative patients. Probabilities of OS, EFS, RFS, TRM were estimated by using the Kaplan-Meier method. Relapse of leukemia and death was accepted as event in EFS. Cumulative RI and primary graft failure – by using Mann-Whitney U-test. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Transplant engraftment was identified in 71 (90%) of patients. Graft failure occurs in the 4 patients of each group (12% for MRD-positive и 8% for MRD-negative. P=0.6). At the median follow up 3 years OS were 63,6% for MRD-positive and 69,6% for MRD-negative patients (p=0,7); the 3-year EFS were 45,5% and 65,2% respectively (p=0,1). The cumulative RI was higher for MRD-positive (n=14) than for patients MRD-negative (n=8) patients (42% and 17% respectively; p=0,01). RFS were also different in the both groups (57,6% and 82.6%; р=0.02). TRM were similar for MRD-positive patients compared with MRD-negative patients (15.2% and 17.4% respectively; p=0.6). Resistant relapse was the reason of death in 13/26 (50%) patients. Nine (27%) MRD-positive and 5 MRD-negative (10%) patient were treated with prophylactic/preventive hypomethylating agent ± IDL in posttransplantation period. One MRD-positive patient experienced a relapse after epigenetic therapy. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> These data demonstrated, that pre-transplantation MRD is associated with increased risk of relapse in children and adolescents with AML (RI-p=0.01; RFS- p=0.02). MRD-positive patients had similar OS (p=0.7), EFS (p=0.1) to patients with MRD-negative status, because relapse had not decisive role for survival. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Acute myeloid leukemia, minimal residual disease, allo-HSCT, children. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4380) "Background
Allogeneic haemopoietic stem cell transplantation (allo-HSCT) – is an effective option in the treatment of high risk patients with acute myeloid leukemia (AML). The relapse after allo-HSCT occurs in about 20-50% of patients, depending on status of the disease and negative prognostic factors. Minimal residual disease (MRD) is a powerful and independent predictor of subsequent relapse, which is detected using polymerase chain reactions or multiparametric flow cytometry. Presented clinical data demonstrated the high prognostic significance of the measured MRD in adults before allo-HSCT. However, impact of pre-transplantation MRD status in children and adolescents with AML is not well elucidated. The goal of this study was to evaluate the impact of pre-transplantation MRD on overall survival (OS), event-free survival (EFS), transplant-related mortality (TRM), relapse-free survival (RFS), relapse incidence (RI) and primary graft failure in transplantation in children and adolescents with AML.
Materials and methods
From 2008 to 2018 a total of 95 AML pediatric patients of R. M. Gorbacheva Memorial Institute received allo-HSCT in complete clinical-hematological remission. Most of the patients received AML-BFM 2004 as primary treatment. We used WHO 2008 criteria (review 2016) to assign cytogenetic risk. All subsequent patients eligible for this study underwent bone marrow (BM) aspiration or biopsy prior to allo-HSCT. Among these patients, 79 were assessed for MRD before HSCT and were considered in this retrospective analysis. MRD was examined with immunophenotyping or polymerase chain reaction/ cytogenetic. The median age was 10 years (1-18). Patients were divided into 2 groups: 1 group – MRD-positive n=33 (42%), 2 group – MRD-negative n=46 (58%). Allo-HSCT was performed in first remission in 23 (70%) MRD-positive patients and 35 (76%) MRD-negative patients. High cytogenetic risk accounted for 14/30 (46%) MRD-positive and 16/40 (40%) MRD-negative patients (p=0.7). Equal number of secondary (n=4; 12% and n=4; 8%, respectively, p=0.7) AML, and also extramedullary (n=6; 18% and n=6; 13%, respectively, p=0.5) disease were observed in both groups. Different in intensity regimes of conditioning were used in equal proportions in both groups (RIC/MAC): 18/15 (1.2) in MRD-positive patients, 25/21 (1.2) in MRD-negative patients. Probabilities of OS, EFS, RFS, TRM were estimated by using the Kaplan-Meier method. Relapse of leukemia and death was accepted as event in EFS. Cumulative RI and primary graft failure – by using Mann-Whitney U-test.
Results
Transplant engraftment was identified in 71 (90%) of patients. Graft failure occurs in the 4 patients of each group (12% for MRD-positive и 8% for MRD-negative. P=0.6). At the median follow up 3 years OS were 63,6% for MRD-positive and 69,6% for MRD-negative patients (p=0,7); the 3-year EFS were 45,5% and 65,2% respectively (p=0,1). The cumulative RI was higher for MRD-positive (n=14) than for patients MRD-negative (n=8) patients (42% and 17% respectively; p=0,01). RFS were also different in the both groups (57,6% and 82.6%; р=0.02). TRM were similar for MRD-positive patients compared with MRD-negative patients (15.2% and 17.4% respectively; p=0.6). Resistant relapse was the reason of death in 13/26 (50%) patients. Nine (27%) MRD-positive and 5 MRD-negative (10%) patient were treated with prophylactic/preventive hypomethylating agent ± IDL in posttransplantation period. One MRD-positive patient experienced a relapse after epigenetic therapy.
Conclusion
These data demonstrated, that pre-transplantation MRD is associated with increased risk of relapse in children and adolescents with AML (RI-p=0.01; RFS- p=0.02). MRD-positive patients had similar OS (p=0.7), EFS (p=0.1) to patients with MRD-negative status, because relapse had not decisive role for survival.
Keywords
Acute myeloid leukemia, minimal residual disease, allo-HSCT, children.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20710" ["VALUE"]=> string(126) "Predictive value of minimal residual disease befor allo-HSCT in children and adolescents with high-risk acute myeloid leukemia" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(126) "Predictive value of minimal residual disease befor allo-HSCT in children and adolescents with high-risk acute myeloid leukemia" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20829" ["VALUE"]=> string(4) "1468" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1468" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20830" ["VALUE"]=> string(4) "1469" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1469" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20707" ["VALUE"]=> array(2) { ["TEXT"]=> string(263) "Liubov A. Tsvetkova, Olesya V. Paina, Inna V. Markova, Polina V. Kozhokar’, Sergey N. Bondarenko, Ildar M. Barkhatov, Elena V. Babenko, Alexander L. Alyanskiy, Kirill A. Ekushev, Tatyana L. Gindina, Elena V. Semenova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(263) "Liubov A. Tsvetkova, Olesya V. Paina, Inna V. Markova, Polina V. Kozhokar’, Sergey N. Bondarenko, Ildar M. Barkhatov, Elena V. Babenko, Alexander L. Alyanskiy, Kirill A. Ekushev, Tatyana L. Gindina, Elena V. Semenova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(263) "Liubov A. Tsvetkova, Olesya V. Paina, Inna V. Markova, Polina V. Kozhokar’, Sergey N. Bondarenko, Ildar M. Barkhatov, Elena V. Babenko, Alexander L. Alyanskiy, Kirill A. Ekushev, Tatyana L. Gindina, Elena V. Semenova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20709" ["VALUE"]=> array(2) { ["TEXT"]=> string(4612) "<h2></h2> <h2 style="text-align: justify;">Background</h2> <p style="text-align: justify;"> Allogeneic haemopoietic stem cell transplantation (allo-HSCT) – is an effective option in the treatment of high risk patients with acute myeloid leukemia (AML). The relapse after allo-HSCT occurs in about 20-50% of patients, depending on status of the disease and negative prognostic factors. Minimal residual disease (MRD) is a powerful and independent predictor of subsequent relapse, which is detected using polymerase chain reactions or multiparametric flow cytometry. Presented clinical data demonstrated the high prognostic significance of the measured MRD in adults before allo-HSCT. However, impact of pre-transplantation MRD status in children and adolescents with AML is not well elucidated. The goal of this study was to evaluate the impact of pre-transplantation MRD on overall survival (OS), event-free survival (EFS), transplant-related mortality (TRM), relapse-free survival (RFS), relapse incidence (RI) and primary graft failure in transplantation in children and adolescents with AML. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> From 2008 to 2018 a total of 95 AML pediatric patients of R. M. Gorbacheva Memorial Institute received allo-HSCT in complete clinical-hematological remission. Most of the patients received AML-BFM 2004 as primary treatment. We used WHO 2008 criteria (review 2016) to assign cytogenetic risk. All subsequent patients eligible for this study underwent bone marrow (BM) aspiration or biopsy prior to allo-HSCT. Among these patients, 79 were assessed for MRD before HSCT and were considered in this retrospective analysis. MRD was examined with immunophenotyping or polymerase chain reaction/ cytogenetic. The median age was 10 years (1-18). Patients were divided into 2 groups: 1 group – MRD-positive n=33 (42%), 2 group – MRD-negative n=46 (58%). Allo-HSCT was performed in first remission in 23 (70%) MRD-positive patients and 35 (76%) MRD-negative patients. High cytogenetic risk accounted for 14/30 (46%) MRD-positive and 16/40 (40%) MRD-negative patients (p=0.7). Equal number of secondary (n=4; 12% and n=4; 8%, respectively, p=0.7) AML, and also extramedullary (n=6; 18% and n=6; 13%, respectively, p=0.5) disease were observed in both groups. Different in intensity regimes of conditioning were used in equal proportions in both groups (RIC/MAC): 18/15 (1.2) in MRD-positive patients, 25/21 (1.2) in MRD-negative patients. Probabilities of OS, EFS, RFS, TRM were estimated by using the Kaplan-Meier method. Relapse of leukemia and death was accepted as event in EFS. Cumulative RI and primary graft failure – by using Mann-Whitney U-test. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Transplant engraftment was identified in 71 (90%) of patients. Graft failure occurs in the 4 patients of each group (12% for MRD-positive и 8% for MRD-negative. P=0.6). At the median follow up 3 years OS were 63,6% for MRD-positive and 69,6% for MRD-negative patients (p=0,7); the 3-year EFS were 45,5% and 65,2% respectively (p=0,1). The cumulative RI was higher for MRD-positive (n=14) than for patients MRD-negative (n=8) patients (42% and 17% respectively; p=0,01). RFS were also different in the both groups (57,6% and 82.6%; р=0.02). TRM were similar for MRD-positive patients compared with MRD-negative patients (15.2% and 17.4% respectively; p=0.6). Resistant relapse was the reason of death in 13/26 (50%) patients. Nine (27%) MRD-positive and 5 MRD-negative (10%) patient were treated with prophylactic/preventive hypomethylating agent ± IDL in posttransplantation period. One MRD-positive patient experienced a relapse after epigenetic therapy. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> These data demonstrated, that pre-transplantation MRD is associated with increased risk of relapse in children and adolescents with AML (RI-p=0.01; RFS- p=0.02). MRD-positive patients had similar OS (p=0.7), EFS (p=0.1) to patients with MRD-negative status, because relapse had not decisive role for survival. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Acute myeloid leukemia, minimal residual disease, allo-HSCT, children. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4380) "Background
Allogeneic haemopoietic stem cell transplantation (allo-HSCT) – is an effective option in the treatment of high risk patients with acute myeloid leukemia (AML). The relapse after allo-HSCT occurs in about 20-50% of patients, depending on status of the disease and negative prognostic factors. Minimal residual disease (MRD) is a powerful and independent predictor of subsequent relapse, which is detected using polymerase chain reactions or multiparametric flow cytometry. Presented clinical data demonstrated the high prognostic significance of the measured MRD in adults before allo-HSCT. However, impact of pre-transplantation MRD status in children and adolescents with AML is not well elucidated. The goal of this study was to evaluate the impact of pre-transplantation MRD on overall survival (OS), event-free survival (EFS), transplant-related mortality (TRM), relapse-free survival (RFS), relapse incidence (RI) and primary graft failure in transplantation in children and adolescents with AML.
Materials and methods
From 2008 to 2018 a total of 95 AML pediatric patients of R. M. Gorbacheva Memorial Institute received allo-HSCT in complete clinical-hematological remission. Most of the patients received AML-BFM 2004 as primary treatment. We used WHO 2008 criteria (review 2016) to assign cytogenetic risk. All subsequent patients eligible for this study underwent bone marrow (BM) aspiration or biopsy prior to allo-HSCT. Among these patients, 79 were assessed for MRD before HSCT and were considered in this retrospective analysis. MRD was examined with immunophenotyping or polymerase chain reaction/ cytogenetic. The median age was 10 years (1-18). Patients were divided into 2 groups: 1 group – MRD-positive n=33 (42%), 2 group – MRD-negative n=46 (58%). Allo-HSCT was performed in first remission in 23 (70%) MRD-positive patients and 35 (76%) MRD-negative patients. High cytogenetic risk accounted for 14/30 (46%) MRD-positive and 16/40 (40%) MRD-negative patients (p=0.7). Equal number of secondary (n=4; 12% and n=4; 8%, respectively, p=0.7) AML, and also extramedullary (n=6; 18% and n=6; 13%, respectively, p=0.5) disease were observed in both groups. Different in intensity regimes of conditioning were used in equal proportions in both groups (RIC/MAC): 18/15 (1.2) in MRD-positive patients, 25/21 (1.2) in MRD-negative patients. Probabilities of OS, EFS, RFS, TRM were estimated by using the Kaplan-Meier method. Relapse of leukemia and death was accepted as event in EFS. Cumulative RI and primary graft failure – by using Mann-Whitney U-test.
Results
Transplant engraftment was identified in 71 (90%) of patients. Graft failure occurs in the 4 patients of each group (12% for MRD-positive и 8% for MRD-negative. P=0.6). At the median follow up 3 years OS were 63,6% for MRD-positive and 69,6% for MRD-negative patients (p=0,7); the 3-year EFS were 45,5% and 65,2% respectively (p=0,1). The cumulative RI was higher for MRD-positive (n=14) than for patients MRD-negative (n=8) patients (42% and 17% respectively; p=0,01). RFS were also different in the both groups (57,6% and 82.6%; р=0.02). TRM were similar for MRD-positive patients compared with MRD-negative patients (15.2% and 17.4% respectively; p=0.6). Resistant relapse was the reason of death in 13/26 (50%) patients. Nine (27%) MRD-positive and 5 MRD-negative (10%) patient were treated with prophylactic/preventive hypomethylating agent ± IDL in posttransplantation period. One MRD-positive patient experienced a relapse after epigenetic therapy.
Conclusion
These data demonstrated, that pre-transplantation MRD is associated with increased risk of relapse in children and adolescents with AML (RI-p=0.01; RFS- p=0.02). MRD-positive patients had similar OS (p=0.7), EFS (p=0.1) to patients with MRD-negative status, because relapse had not decisive role for survival.
Keywords
Acute myeloid leukemia, minimal residual disease, allo-HSCT, children.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4380) "Background
Allogeneic haemopoietic stem cell transplantation (allo-HSCT) – is an effective option in the treatment of high risk patients with acute myeloid leukemia (AML). The relapse after allo-HSCT occurs in about 20-50% of patients, depending on status of the disease and negative prognostic factors. Minimal residual disease (MRD) is a powerful and independent predictor of subsequent relapse, which is detected using polymerase chain reactions or multiparametric flow cytometry. Presented clinical data demonstrated the high prognostic significance of the measured MRD in adults before allo-HSCT. However, impact of pre-transplantation MRD status in children and adolescents with AML is not well elucidated. The goal of this study was to evaluate the impact of pre-transplantation MRD on overall survival (OS), event-free survival (EFS), transplant-related mortality (TRM), relapse-free survival (RFS), relapse incidence (RI) and primary graft failure in transplantation in children and adolescents with AML.
Materials and methods
From 2008 to 2018 a total of 95 AML pediatric patients of R. M. Gorbacheva Memorial Institute received allo-HSCT in complete clinical-hematological remission. Most of the patients received AML-BFM 2004 as primary treatment. We used WHO 2008 criteria (review 2016) to assign cytogenetic risk. All subsequent patients eligible for this study underwent bone marrow (BM) aspiration or biopsy prior to allo-HSCT. Among these patients, 79 were assessed for MRD before HSCT and were considered in this retrospective analysis. MRD was examined with immunophenotyping or polymerase chain reaction/ cytogenetic. The median age was 10 years (1-18). Patients were divided into 2 groups: 1 group – MRD-positive n=33 (42%), 2 group – MRD-negative n=46 (58%). Allo-HSCT was performed in first remission in 23 (70%) MRD-positive patients and 35 (76%) MRD-negative patients. High cytogenetic risk accounted for 14/30 (46%) MRD-positive and 16/40 (40%) MRD-negative patients (p=0.7). Equal number of secondary (n=4; 12% and n=4; 8%, respectively, p=0.7) AML, and also extramedullary (n=6; 18% and n=6; 13%, respectively, p=0.5) disease were observed in both groups. Different in intensity regimes of conditioning were used in equal proportions in both groups (RIC/MAC): 18/15 (1.2) in MRD-positive patients, 25/21 (1.2) in MRD-negative patients. Probabilities of OS, EFS, RFS, TRM were estimated by using the Kaplan-Meier method. Relapse of leukemia and death was accepted as event in EFS. Cumulative RI and primary graft failure – by using Mann-Whitney U-test.
Results
Transplant engraftment was identified in 71 (90%) of patients. Graft failure occurs in the 4 patients of each group (12% for MRD-positive и 8% for MRD-negative. P=0.6). At the median follow up 3 years OS were 63,6% for MRD-positive and 69,6% for MRD-negative patients (p=0,7); the 3-year EFS were 45,5% and 65,2% respectively (p=0,1). The cumulative RI was higher for MRD-positive (n=14) than for patients MRD-negative (n=8) patients (42% and 17% respectively; p=0,01). RFS were also different in the both groups (57,6% and 82.6%; р=0.02). TRM were similar for MRD-positive patients compared with MRD-negative patients (15.2% and 17.4% respectively; p=0.6). Resistant relapse was the reason of death in 13/26 (50%) patients. Nine (27%) MRD-positive and 5 MRD-negative (10%) patient were treated with prophylactic/preventive hypomethylating agent ± IDL in posttransplantation period. One MRD-positive patient experienced a relapse after epigenetic therapy.
Conclusion
These data demonstrated, that pre-transplantation MRD is associated with increased risk of relapse in children and adolescents with AML (RI-p=0.01; RFS- p=0.02). MRD-positive patients had similar OS (p=0.7), EFS (p=0.1) to patients with MRD-negative status, because relapse had not decisive role for survival.
Keywords
Acute myeloid leukemia, minimal residual disease, allo-HSCT, children.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20710" ["VALUE"]=> string(126) "Predictive value of minimal residual disease befor allo-HSCT in children and adolescents with high-risk acute myeloid leukemia" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(126) "Predictive value of minimal residual disease befor allo-HSCT in children and adolescents with high-risk acute myeloid leukemia" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(126) "Predictive value of minimal residual disease befor allo-HSCT in children and adolescents with high-risk acute myeloid leukemia" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20708" ["VALUE"]=> array(2) { ["TEXT"]=> string(176) "R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, I. P. Pavlov First Saint-Petersburg State Medical University, Saint-Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(176) "R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, I. P. Pavlov First Saint-Petersburg State Medical University, Saint-Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(176) "R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, I. P. Pavlov First Saint-Petersburg State Medical University, Saint-Petersburg, Russia" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20704" ["VALUE"]=> array(2) { ["TEXT"]=> string(447) "Любовь А. Цветкова, Олеся В. Паина, Инна В. Маркова, Полина В. Кожокарь, Сергей Н. Бондаренко, Ильдар М. Бархатов, Елена В. Бабенко, Александр Л. Алянский, Кирилл А. Екушев, Татьяна Л. Гиндина, Елена В. Семенова, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(447) "Любовь А. Цветкова, Олеся В. Паина, Инна В. Маркова, Полина В. Кожокарь, Сергей Н. Бондаренко, Ильдар М. Бархатов, Елена В. Бабенко, Александр Л. Алянский, Кирилл А. Екушев, Татьяна Л. Гиндина, Елена В. Семенова, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(447) "Любовь А. Цветкова, Олеся В. Паина, Инна В. Маркова, Полина В. Кожокарь, Сергей Н. Бондаренко, Ильдар М. Бархатов, Елена В. Бабенко, Александр Л. Алянский, Кирилл А. Екушев, Татьяна Л. Гиндина, Елена В. Семенова, Людмила С. Зубаровская, Борис В. Афанасьев" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20706" ["VALUE"]=> array(2) { ["TEXT"]=> string(8232) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Аллогенная трансплантация гемопоэтических столовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелоидным лейкозом группы высокого риска (ОМЛ). Возникновение рецидива после алло-ТГСК происходит примерно у 20-50% пациентов в зависимости от стадии заболевания на момент трансплантации и отрицательных прогностических факторов. Одним из предикторов рецидива при ОМЛ может быть минимальная остаточная болезнь (МОБ), определяемая с помощью проточной цитофлюорометрии или полимеразной цепной реакции. Опубликованные исследования демонстрируют высокую прогностическую значимость определения МОБ непосредственно перед проведением алло-ТГСК у взрослых пациентов. Однако у детей с ОМЛ данные о влиянии МОБ перед алло-ТГСК на эффективность лечения ограничены. Целью данного исследования стала оценка влияния МОБ перед алло-ТГСК на общую выживаемость (ОВ), бессобытийную выживаемость (БСВ), безрецидивную выживаемость (БРВ), трансплантационную летальность, кумулятивную частоту рецидива (ЧР) и частоту первичного неприживления у детей и подростков с ОМЛ. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> С 2008-2018 гг. в клинике НИИ ДОГиТ им. Р. М. Горбачевой алло-ТГСК проведена 95 детям с ОМЛ в клинико-гематологической ремиссии заболевания заболевания. Большинство пациентов получили первичную химиотерапию по протоколу AML-BFM 2004. Для установления группы цитогенетического риска были использованы WHO критерии 2008 г. (пересмотр 2016 г.). Перед алло-ТГСК всем пациентам выполнялась аспирация/биопсия костного мозга для рестадирования. Среди этих пациентов у 79 проводилось определение МОБ с помощью молекулярно-генетического/цитогенетического исследований и/или метода иммунофенотипирования. Таким образом, 79 пациентов с медианой возраста 10 лет (1-18) на момент алло-ТГСК были включены в данное ретроспективное исследование. Все пациенты были поделены на 2 группы: 1 гр. – МОБ+ n=33 (42%), 2 гр. – МОБ– n=46 (58%). В первой ремиссии алло-ТГСК была выполнена 23 (70%) МОБ+ пациентам и 35 (76%) МОБ– пациентам. Высокий цитогенетический риск инициально наблюдался у 14/30 (46%) МОБ+ пациентов и у 16/40 (40%) МОБ– пациентов (p=0,7). В каждой группе наблюдалось равное число вторичных ОМЛ (n=4; 12% и n=4; 8% соответственно, p=0,7), а также ОМЛ с экстрамедуллярным поражением (n=6; 18% и n=6; 13% соответственно, p=0,5). В той и другой группе применялись различные по интенсивности режимы кондиционирования в равных пропорциях (РИК/МАК): в 1 гр. – 18/15 (1,2), во 2 гр. – 25/21 (1,2). ОВ, БСВ, БРВ, а также летальность, обусловленная терапией, были рассчитаны, используя метод Каплана-Майера. При определении БСВ за событие был принят рецидив лейкоза или смерть. Кумулятивная частота рецидива и первичного отторжения трансплантата установлены с помощью критерия Манна-Уитни. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Приживление ГСК было зафиксировано у 71 (90%) пациента. Частота первичного неприживления в обеих группах была одинаковая (n=4; 12% и n=4; 8% соответственно, р=0,6). При медиане наблюдения 3 года ОВ составила 63,6% в группе МОБ+ и 69,6% в группе МОБ–(p=0,7). БСВ при данной медиане равна 45,5% у МОБ+ пациентов, 65,2% у МОБ– (p=0,1). Трехгодичная частота рецидива была достоверно выше у МОБ+ пациентов (n=14), чем у МОБ– (n=8) пациентов (42% и 17% соответственно, p=0,01). БРВ также достоверно различалась у пациентов с различным МОБ статусом (57,6% у МОБ+, 82,6% у МОБ–, р=0,02). Трансплантационная летальность составила 15,2% и 17,4% в 1-й и 2-й группах соответственно (p=0,6). Резистентный рецидив ОМЛ после алло-ТГСК был причиной смерти у 13/26 (50%) пациентов, среди них 7 МОБ+ пациентов, 6 МОБ– пациентов. Профилактическая/превентивная терапия гипометилирующими агентами ± инфузия донорских лимфоцитов (ИДЛ) была проведена 9 (27%) МОБ+ пациентам и 5 МОБ– (10%) пациентам. Рецидив после проведенной терапии произошел только у одного пациента из группы МОБ+. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Данное исследование демонстрирует, что наличие предтрансплантационной МОБ у детей и подростков с ОМЛ ассоциировано с повышенным риском возникновения рецидива после алло-ТГСК (различие в ЧР, p= 0,01 и БРВ, р=0,02). При этом БСВ и ОВ достоверно не различались в обеих группах (р=0,7 и р=0,1, соответственно), так как рецидив не оказал решающего значения на данные показатели. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Острый миелоидный лейкоз, минимальная остаточная болезнь, алло-ТГСК, </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(8000) "Введение
Аллогенная трансплантация гемопоэтических столовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелоидным лейкозом группы высокого риска (ОМЛ). Возникновение рецидива после алло-ТГСК происходит примерно у 20-50% пациентов в зависимости от стадии заболевания на момент трансплантации и отрицательных прогностических факторов. Одним из предикторов рецидива при ОМЛ может быть минимальная остаточная болезнь (МОБ), определяемая с помощью проточной цитофлюорометрии или полимеразной цепной реакции. Опубликованные исследования демонстрируют высокую прогностическую значимость определения МОБ непосредственно перед проведением алло-ТГСК у взрослых пациентов. Однако у детей с ОМЛ данные о влиянии МОБ перед алло-ТГСК на эффективность лечения ограничены. Целью данного исследования стала оценка влияния МОБ перед алло-ТГСК на общую выживаемость (ОВ), бессобытийную выживаемость (БСВ), безрецидивную выживаемость (БРВ), трансплантационную летальность, кумулятивную частоту рецидива (ЧР) и частоту первичного неприживления у детей и подростков с ОМЛ.
Материалы и методы
С 2008-2018 гг. в клинике НИИ ДОГиТ им. Р. М. Горбачевой алло-ТГСК проведена 95 детям с ОМЛ в клинико-гематологической ремиссии заболевания заболевания. Большинство пациентов получили первичную химиотерапию по протоколу AML-BFM 2004. Для установления группы цитогенетического риска были использованы WHO критерии 2008 г. (пересмотр 2016 г.). Перед алло-ТГСК всем пациентам выполнялась аспирация/биопсия костного мозга для рестадирования. Среди этих пациентов у 79 проводилось определение МОБ с помощью молекулярно-генетического/цитогенетического исследований и/или метода иммунофенотипирования. Таким образом, 79 пациентов с медианой возраста 10 лет (1-18) на момент алло-ТГСК были включены в данное ретроспективное исследование. Все пациенты были поделены на 2 группы: 1 гр. – МОБ+ n=33 (42%), 2 гр. – МОБ– n=46 (58%). В первой ремиссии алло-ТГСК была выполнена 23 (70%) МОБ+ пациентам и 35 (76%) МОБ– пациентам. Высокий цитогенетический риск инициально наблюдался у 14/30 (46%) МОБ+ пациентов и у 16/40 (40%) МОБ– пациентов (p=0,7). В каждой группе наблюдалось равное число вторичных ОМЛ (n=4; 12% и n=4; 8% соответственно, p=0,7), а также ОМЛ с экстрамедуллярным поражением (n=6; 18% и n=6; 13% соответственно, p=0,5). В той и другой группе применялись различные по интенсивности режимы кондиционирования в равных пропорциях (РИК/МАК): в 1 гр. – 18/15 (1,2), во 2 гр. – 25/21 (1,2). ОВ, БСВ, БРВ, а также летальность, обусловленная терапией, были рассчитаны, используя метод Каплана-Майера. При определении БСВ за событие был принят рецидив лейкоза или смерть. Кумулятивная частота рецидива и первичного отторжения трансплантата установлены с помощью критерия Манна-Уитни.
Результаты
Приживление ГСК было зафиксировано у 71 (90%) пациента. Частота первичного неприживления в обеих группах была одинаковая (n=4; 12% и n=4; 8% соответственно, р=0,6). При медиане наблюдения 3 года ОВ составила 63,6% в группе МОБ+ и 69,6% в группе МОБ–(p=0,7). БСВ при данной медиане равна 45,5% у МОБ+ пациентов, 65,2% у МОБ– (p=0,1). Трехгодичная частота рецидива была достоверно выше у МОБ+ пациентов (n=14), чем у МОБ– (n=8) пациентов (42% и 17% соответственно, p=0,01). БРВ также достоверно различалась у пациентов с различным МОБ статусом (57,6% у МОБ+, 82,6% у МОБ–, р=0,02). Трансплантационная летальность составила 15,2% и 17,4% в 1-й и 2-й группах соответственно (p=0,6). Резистентный рецидив ОМЛ после алло-ТГСК был причиной смерти у 13/26 (50%) пациентов, среди них 7 МОБ+ пациентов, 6 МОБ– пациентов. Профилактическая/превентивная терапия гипометилирующими агентами ± инфузия донорских лимфоцитов (ИДЛ) была проведена 9 (27%) МОБ+ пациентам и 5 МОБ– (10%) пациентам. Рецидив после проведенной терапии произошел только у одного пациента из группы МОБ+.
Заключение
Данное исследование демонстрирует, что наличие предтрансплантационной МОБ у детей и подростков с ОМЛ ассоциировано с повышенным риском возникновения рецидива после алло-ТГСК (различие в ЧР, p= 0,01 и БРВ, р=0,02). При этом БСВ и ОВ достоверно не различались в обеих группах (р=0,7 и р=0,1, соответственно), так как рецидив не оказал решающего значения на данные показатели.
Ключевые слова
Острый миелоидный лейкоз, минимальная остаточная болезнь, алло-ТГСК,
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(8000) "Введение
Аллогенная трансплантация гемопоэтических столовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелоидным лейкозом группы высокого риска (ОМЛ). Возникновение рецидива после алло-ТГСК происходит примерно у 20-50% пациентов в зависимости от стадии заболевания на момент трансплантации и отрицательных прогностических факторов. Одним из предикторов рецидива при ОМЛ может быть минимальная остаточная болезнь (МОБ), определяемая с помощью проточной цитофлюорометрии или полимеразной цепной реакции. Опубликованные исследования демонстрируют высокую прогностическую значимость определения МОБ непосредственно перед проведением алло-ТГСК у взрослых пациентов. Однако у детей с ОМЛ данные о влиянии МОБ перед алло-ТГСК на эффективность лечения ограничены. Целью данного исследования стала оценка влияния МОБ перед алло-ТГСК на общую выживаемость (ОВ), бессобытийную выживаемость (БСВ), безрецидивную выживаемость (БРВ), трансплантационную летальность, кумулятивную частоту рецидива (ЧР) и частоту первичного неприживления у детей и подростков с ОМЛ.
Материалы и методы
С 2008-2018 гг. в клинике НИИ ДОГиТ им. Р. М. Горбачевой алло-ТГСК проведена 95 детям с ОМЛ в клинико-гематологической ремиссии заболевания заболевания. Большинство пациентов получили первичную химиотерапию по протоколу AML-BFM 2004. Для установления группы цитогенетического риска были использованы WHO критерии 2008 г. (пересмотр 2016 г.). Перед алло-ТГСК всем пациентам выполнялась аспирация/биопсия костного мозга для рестадирования. Среди этих пациентов у 79 проводилось определение МОБ с помощью молекулярно-генетического/цитогенетического исследований и/или метода иммунофенотипирования. Таким образом, 79 пациентов с медианой возраста 10 лет (1-18) на момент алло-ТГСК были включены в данное ретроспективное исследование. Все пациенты были поделены на 2 группы: 1 гр. – МОБ+ n=33 (42%), 2 гр. – МОБ– n=46 (58%). В первой ремиссии алло-ТГСК была выполнена 23 (70%) МОБ+ пациентам и 35 (76%) МОБ– пациентам. Высокий цитогенетический риск инициально наблюдался у 14/30 (46%) МОБ+ пациентов и у 16/40 (40%) МОБ– пациентов (p=0,7). В каждой группе наблюдалось равное число вторичных ОМЛ (n=4; 12% и n=4; 8% соответственно, p=0,7), а также ОМЛ с экстрамедуллярным поражением (n=6; 18% и n=6; 13% соответственно, p=0,5). В той и другой группе применялись различные по интенсивности режимы кондиционирования в равных пропорциях (РИК/МАК): в 1 гр. – 18/15 (1,2), во 2 гр. – 25/21 (1,2). ОВ, БСВ, БРВ, а также летальность, обусловленная терапией, были рассчитаны, используя метод Каплана-Майера. При определении БСВ за событие был принят рецидив лейкоза или смерть. Кумулятивная частота рецидива и первичного отторжения трансплантата установлены с помощью критерия Манна-Уитни.
Результаты
Приживление ГСК было зафиксировано у 71 (90%) пациента. Частота первичного неприживления в обеих группах была одинаковая (n=4; 12% и n=4; 8% соответственно, р=0,6). При медиане наблюдения 3 года ОВ составила 63,6% в группе МОБ+ и 69,6% в группе МОБ–(p=0,7). БСВ при данной медиане равна 45,5% у МОБ+ пациентов, 65,2% у МОБ– (p=0,1). Трехгодичная частота рецидива была достоверно выше у МОБ+ пациентов (n=14), чем у МОБ– (n=8) пациентов (42% и 17% соответственно, p=0,01). БРВ также достоверно различалась у пациентов с различным МОБ статусом (57,6% у МОБ+, 82,6% у МОБ–, р=0,02). Трансплантационная летальность составила 15,2% и 17,4% в 1-й и 2-й группах соответственно (p=0,6). Резистентный рецидив ОМЛ после алло-ТГСК был причиной смерти у 13/26 (50%) пациентов, среди них 7 МОБ+ пациентов, 6 МОБ– пациентов. Профилактическая/превентивная терапия гипометилирующими агентами ± инфузия донорских лимфоцитов (ИДЛ) была проведена 9 (27%) МОБ+ пациентам и 5 МОБ– (10%) пациентам. Рецидив после проведенной терапии произошел только у одного пациента из группы МОБ+.
Заключение
Данное исследование демонстрирует, что наличие предтрансплантационной МОБ у детей и подростков с ОМЛ ассоциировано с повышенным риском возникновения рецидива после алло-ТГСК (различие в ЧР, p= 0,01 и БРВ, р=0,02). При этом БСВ и ОВ достоверно не различались в обеих группах (р=0,7 и р=0,1, соответственно), так как рецидив не оказал решающего значения на данные показатели.
Ключевые слова
Острый миелоидный лейкоз, минимальная остаточная болезнь, алло-ТГСК,
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20705" ["VALUE"]=> array(2) { ["TEXT"]=> string(425) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой; Первый Санкт-Петербургский государственный медицинский университет имени академика И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(425) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой; Первый Санкт-Петербургский государственный медицинский университет имени академика И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(425) "Научно-исследовательский институт детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой; Первый Санкт-Петербургский государственный медицинский университет имени академика И. П. Павлова, Санкт-Петербург, Россия" } } } [38]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1599" ["~ID"]=> string(4) "1599" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(292) "Модификация мезенхимных стромальных клеток костного мозга с использованием мультифункциональных микрокапсул для целевой доставки лекарственных соединений" ["~NAME"]=> string(292) "Модификация мезенхимных стромальных клеток костного мозга с использованием мультифункциональных микрокапсул для целевой доставки лекарственных соединений" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:47:41" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:47:41" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/modifikatsiya-mezenkhimnykh-stromalnykh-kletok-kostnogo-mozga-s-ispolzovaniem-multifunktsionalnykh-m/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/modifikatsiya-mezenkhimnykh-stromalnykh-kletok-kostnogo-mozga-s-ispolzovaniem-multifunktsionalnykh-m/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "modifikatsiya-mezenkhimnykh-stromalnykh-kletok-kostnogo-mozga-s-ispolzovaniem-multifunktsionalnykh-m" ["~CODE"]=> string(100) "modifikatsiya-mezenkhimnykh-stromalnykh-kletok-kostnogo-mozga-s-ispolzovaniem-multifunktsionalnykh-m" ["EXTERNAL_ID"]=> string(4) "1599" ["~EXTERNAL_ID"]=> string(4) "1599" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(292) "Модификация мезенхимных стромальных клеток костного мозга с использованием мультифункциональных микрокапсул для целевой доставки лекарственных соединений" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(405) "Модификация мезенхимных стромальных клеток костного мозга с использованием мультифункциональных микрокапсул для целевой доставки лекарственных соединенийFunctionalization of bone marrow mesenchymal stromal cells by multifunctional capsules for targeted drug delivery" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(6473) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Цель данной работы состояла в исследовании возможностей применения мультипотентных мезенхимальных стромальных клеток (ММСК) в качестве платформы для доставки препаратов, заключенных в гибридные полимерные микрокапсулы. ММСК являются высокопотенциальной клеточной популяцией, которая за счет феномена патотропизма может решить проблему таргетной доставки препарата, выступая в качестве носителя. Таким образом, объединение биологического феномена миграции клеток и высокой загружающей способности полимерных капсул обеспечит возможность контролировать направленность действия и позволит выполнить таргетную доставку вещества без внешнего и внутреннего воздействия для клеток-носителей. Для отработки методики, доксорубицин и винкристин были отобраны, в качестве противоопухолевых препаратов с дозозависимым эффектом, которые включены в состав многих схем полихимиотерапии. </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> В ходе данного исследования был произведен синтез гибридных микрокапсул различных размеров (5 мкм, 1 мкм, 0,5 мкм) при помощи технологии Layer-by- Layer (Polyarginine/Dextran sulfate) и золь-гель синтеза (Tetraethyl orthosilicate). Данные микроконтейнеры обладают низкой токсичностью, высокой биосовместимостью, а также способны защитить клетку от инкапсулированных препаратов. На следующем этапе была выполнена оценка ассоциации клеток с капсулами различных размеров при помощи проточной цитометрии и лазерной сканирующей конфокальной микроскопии для определения оптимального соотношения капсул и клеток. Спонтанная миграция МСК, и влияние на нее ассоциированных с клетками капсул различных размеров была исследована при помощи системы наблюдения за живыми клетками в культуре Cell-IQ. На завершающем этапе работы была изучена способность ММСК к направленной миграции по градиенту концентрации SDF-1. Для качественной и количественной оценки миграции были использованы Transwell, μ-Slide Chemotaxis, а также была исследована способность ММСК к миграции в коллагеновом геле в сторону сфероидов из раковых клеток, синтезирующих SDF-1, и их способность проникать внутрь конгломерата клеток. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Полученные результаты показывают, что МСК клетки способны захватывать более 10 капсул, содержащие противоопухолевые препараты – доксорубицин, винкристин. По экспериментальным данным проточной цитометрии показано, что 90 % клеток способны интернализировать капсулы с высокой эффективностью. Уникальная структура капсул предотвращает высвобождение противоопухолевых препаратов в течение 72 часов. Показано, что большая часть клеток способны направлено переносить капсулы по SDF-1 градиенту и в очаг опухолевого сфероида. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Таким образом, показано, что МСК с включенными капсулами, содержащие противоопухолевые препараты, могут выступать в качестве новой лекарственной формы для направленной доставки противоопухолевых препаратов в очаг опухолей.</p> <h2>Благодарности</h2> <p style="text-align: justify;"> Работа выполнена при поддержке Российского Фонда Фундаментальных исследований (грант № 18-015-00100). </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Таргетная доставка, микро- и нанокапсулы, противоо пухолевые препараты, интернализация, мезенхимные стромальные клетки, миграция, фармакокинетика, синтез, культивирование, клетки-носители. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(292) "Модификация мезенхимных стромальных клеток костного мозга с использованием мультифункциональных микрокапсул для целевой доставки лекарственных соединений" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(292) "Модификация мезенхимных стромальных клеток костного мозга с использованием мультифункциональных микрокапсул для целевой доставки лекарственных соединений" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(292) "Модификация мезенхимных стромальных клеток костного мозга с использованием мультифункциональных микрокапсул для целевой доставки лекарственных соединений" ["SECTION_META_TITLE"]=> string(292) "Модификация мезенхимных стромальных клеток костного мозга с использованием мультифункциональных микрокапсул для целевой доставки лекарственных соединений" ["SECTION_META_KEYWORDS"]=> string(292) "Модификация мезенхимных стромальных клеток костного мозга с использованием мультифункциональных микрокапсул для целевой доставки лекарственных соединений" ["SECTION_META_DESCRIPTION"]=> string(292) "Модификация мезенхимных стромальных клеток костного мозга с использованием мультифункциональных микрокапсул для целевой доставки лекарственных соединений" ["SECTION_PICTURE_FILE_ALT"]=> string(292) "Модификация мезенхимных стромальных клеток костного мозга с использованием мультифункциональных микрокапсул для целевой доставки лекарственных соединений" ["SECTION_PICTURE_FILE_TITLE"]=> string(292) "Модификация мезенхимных стромальных клеток костного мозга с использованием мультифункциональных микрокапсул для целевой доставки лекарственных соединений" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "modifikatsiya-mezenkhimnykh-stromalnykh-kletok-kostnogo-mozga-s-ispolzovaniem-multifunktsionalnykh-m" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(292) "Модификация мезенхимных стромальных клеток костного мозга с использованием мультифункциональных микрокапсул для целевой доставки лекарственных соединений" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(292) "Модификация мезенхимных стромальных клеток костного мозга с использованием мультифункциональных микрокапсул для целевой доставки лекарственных соединений" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "modifikatsiya-mezenkhimnykh-stromalnykh-kletok-kostnogo-mozga-s-ispolzovaniem-multifunktsionalnykh-m" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "modifikatsiya-mezenkhimnykh-stromalnykh-kletok-kostnogo-mozga-s-ispolzovaniem-multifunktsionalnykh-m" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "modifikatsiya-mezenkhimnykh-stromalnykh-kletok-kostnogo-mozga-s-ispolzovaniem-multifunktsionalnykh-m" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20697" ["VALUE"]=> array(2) { ["TEXT"]=> string(863) "Александр С. Тимин <sup>1</sup>,<sup>2</sup>, Альберт Р. Муслимов <sup>1</sup>, Алексей А. Пельтек <sup>3</sup>, Михаил В. Зюзин <sup>4</sup>, Ольга С. Епифановская <sup>1</sup>, Владислав С. Сергеев <sup>1</sup>, Анна А. Доценко <sup>1</sup>, Тимофей Е. Карпов <sup>3</sup>, Игорь С. Сергеев <sup>3</sup>, Александр А. Гончаренко <sup>3</sup>, Яна В. Тараканчикова <sup>5</sup>, Кирилл В. Лепик <sup>1</sup>, Глеб Б. Сухоруков <sup>3</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(683) "Александр С. Тимин 1,2, Альберт Р. Муслимов 1, Алексей А. Пельтек 3, Михаил В. Зюзин 4, Ольга С. Епифановская 1, Владислав С. Сергеев 1, Анна А. Доценко 1, Тимофей Е. Карпов 3, Игорь С. Сергеев 3, Александр А. Гончаренко 3, Яна В. Тараканчикова 5, Кирилл В. Лепик 1, Глеб Б. Сухоруков 3, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20698" ["VALUE"]=> array(2) { ["TEXT"]=> string(958) "<sup>1</sup> Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия <sup>2</sup> Томский политехнический университет, Томск, Россия <sup>3</sup> Санкт-Петербургский Политехнический Университет Петра Великого, Санкт-Петербург, Россия <sup>4</sup> Санкт-Петербургский Национальный Исследовательский Университет ИТМО, Санкт-Петербург, Россия <sup>5</sup> Санкт-Петербургский Национальный Исследовательский Академический Университет, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(898) "1 Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия 2 Томский политехнический университет, Томск, Россия 3 Санкт-Петербургский Политехнический Университет Петра Великого, Санкт-Петербург, Россия 4 Санкт-Петербургский Национальный Исследовательский Университет ИТМО, Санкт-Петербург, Россия 5 Санкт-Петербургский Национальный Исследовательский Академический Университет, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20699" ["VALUE"]=> array(2) { ["TEXT"]=> string(6473) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Цель данной работы состояла в исследовании возможностей применения мультипотентных мезенхимальных стромальных клеток (ММСК) в качестве платформы для доставки препаратов, заключенных в гибридные полимерные микрокапсулы. ММСК являются высокопотенциальной клеточной популяцией, которая за счет феномена патотропизма может решить проблему таргетной доставки препарата, выступая в качестве носителя. Таким образом, объединение биологического феномена миграции клеток и высокой загружающей способности полимерных капсул обеспечит возможность контролировать направленность действия и позволит выполнить таргетную доставку вещества без внешнего и внутреннего воздействия для клеток-носителей. Для отработки методики, доксорубицин и винкристин были отобраны, в качестве противоопухолевых препаратов с дозозависимым эффектом, которые включены в состав многих схем полихимиотерапии. </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> В ходе данного исследования был произведен синтез гибридных микрокапсул различных размеров (5 мкм, 1 мкм, 0,5 мкм) при помощи технологии Layer-by- Layer (Polyarginine/Dextran sulfate) и золь-гель синтеза (Tetraethyl orthosilicate). Данные микроконтейнеры обладают низкой токсичностью, высокой биосовместимостью, а также способны защитить клетку от инкапсулированных препаратов. На следующем этапе была выполнена оценка ассоциации клеток с капсулами различных размеров при помощи проточной цитометрии и лазерной сканирующей конфокальной микроскопии для определения оптимального соотношения капсул и клеток. Спонтанная миграция МСК, и влияние на нее ассоциированных с клетками капсул различных размеров была исследована при помощи системы наблюдения за живыми клетками в культуре Cell-IQ. На завершающем этапе работы была изучена способность ММСК к направленной миграции по градиенту концентрации SDF-1. Для качественной и количественной оценки миграции были использованы Transwell, μ-Slide Chemotaxis, а также была исследована способность ММСК к миграции в коллагеновом геле в сторону сфероидов из раковых клеток, синтезирующих SDF-1, и их способность проникать внутрь конгломерата клеток. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Полученные результаты показывают, что МСК клетки способны захватывать более 10 капсул, содержащие противоопухолевые препараты – доксорубицин, винкристин. По экспериментальным данным проточной цитометрии показано, что 90 % клеток способны интернализировать капсулы с высокой эффективностью. Уникальная структура капсул предотвращает высвобождение противоопухолевых препаратов в течение 72 часов. Показано, что большая часть клеток способны направлено переносить капсулы по SDF-1 градиенту и в очаг опухолевого сфероида. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Таким образом, показано, что МСК с включенными капсулами, содержащие противоопухолевые препараты, могут выступать в качестве новой лекарственной формы для направленной доставки противоопухолевых препаратов в очаг опухолей.</p> <h2>Благодарности</h2> <p style="text-align: justify;"> Работа выполнена при поддержке Российского Фонда Фундаментальных исследований (грант № 18-015-00100). </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Таргетная доставка, микро- и нанокапсулы, противоо пухолевые препараты, интернализация, мезенхимные стромальные клетки, миграция, фармакокинетика, синтез, культивирование, клетки-носители. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6219) "Введение
Цель данной работы состояла в исследовании возможностей применения мультипотентных мезенхимальных стромальных клеток (ММСК) в качестве платформы для доставки препаратов, заключенных в гибридные полимерные микрокапсулы. ММСК являются высокопотенциальной клеточной популяцией, которая за счет феномена патотропизма может решить проблему таргетной доставки препарата, выступая в качестве носителя. Таким образом, объединение биологического феномена миграции клеток и высокой загружающей способности полимерных капсул обеспечит возможность контролировать направленность действия и позволит выполнить таргетную доставку вещества без внешнего и внутреннего воздействия для клеток-носителей. Для отработки методики, доксорубицин и винкристин были отобраны, в качестве противоопухолевых препаратов с дозозависимым эффектом, которые включены в состав многих схем полихимиотерапии.
Методы
В ходе данного исследования был произведен синтез гибридных микрокапсул различных размеров (5 мкм, 1 мкм, 0,5 мкм) при помощи технологии Layer-by- Layer (Polyarginine/Dextran sulfate) и золь-гель синтеза (Tetraethyl orthosilicate). Данные микроконтейнеры обладают низкой токсичностью, высокой биосовместимостью, а также способны защитить клетку от инкапсулированных препаратов. На следующем этапе была выполнена оценка ассоциации клеток с капсулами различных размеров при помощи проточной цитометрии и лазерной сканирующей конфокальной микроскопии для определения оптимального соотношения капсул и клеток. Спонтанная миграция МСК, и влияние на нее ассоциированных с клетками капсул различных размеров была исследована при помощи системы наблюдения за живыми клетками в культуре Cell-IQ. На завершающем этапе работы была изучена способность ММСК к направленной миграции по градиенту концентрации SDF-1. Для качественной и количественной оценки миграции были использованы Transwell, μ-Slide Chemotaxis, а также была исследована способность ММСК к миграции в коллагеновом геле в сторону сфероидов из раковых клеток, синтезирующих SDF-1, и их способность проникать внутрь конгломерата клеток.
Результаты
Полученные результаты показывают, что МСК клетки способны захватывать более 10 капсул, содержащие противоопухолевые препараты – доксорубицин, винкристин. По экспериментальным данным проточной цитометрии показано, что 90 % клеток способны интернализировать капсулы с высокой эффективностью. Уникальная структура капсул предотвращает высвобождение противоопухолевых препаратов в течение 72 часов. Показано, что большая часть клеток способны направлено переносить капсулы по SDF-1 градиенту и в очаг опухолевого сфероида.
Заключение
Таким образом, показано, что МСК с включенными капсулами, содержащие противоопухолевые препараты, могут выступать в качестве новой лекарственной формы для направленной доставки противоопухолевых препаратов в очаг опухолей.
Благодарности
Работа выполнена при поддержке Российского Фонда Фундаментальных исследований (грант № 18-015-00100).
Ключевые слова
Таргетная доставка, микро- и нанокапсулы, противоо пухолевые препараты, интернализация, мезенхимные стромальные клетки, миграция, фармакокинетика, синтез, культивирование, клетки-носители.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20700" ["VALUE"]=> array(2) { ["TEXT"]=> string(657) "Alexander S. Timin <sup>1</sup>,<sup>2</sup>, Albert R. Muslimov <sup>1</sup>, Oleksii O. Peltek <sup>3</sup>, Mikhail V. Zyuzin <sup>4</sup>, Olga S. Epifanovskaya <sup>1</sup>, Vladislav S. Sergeev <sup>1</sup>, Anna A. Dotsenko <sup>1</sup>, Timofey E. Karpov <sup>3</sup>, Igor S. Sergeev <sup>3</sup>, Alexander A. Goncharenko <sup>3</sup>, Yana V. Tarakanchikova <sup>5</sup>, Kirill V. Lepik <sup>1</sup>, Gleb B. Sukhorukov <sup>3</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(477) "Alexander S. Timin 1,2, Albert R. Muslimov 1, Oleksii O. Peltek 3, Mikhail V. Zyuzin 4, Olga S. Epifanovskaya 1, Vladislav S. Sergeev 1, Anna A. Dotsenko 1, Timofey E. Karpov 3, Igor S. Sergeev 3, Alexander A. Goncharenko 3, Yana V. Tarakanchikova 5, Kirill V. Lepik 1, Gleb B. Sukhorukov 3, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20701" ["VALUE"]=> array(2) { ["TEXT"]=> string(536) "<sup>1</sup> First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation <sup>2</sup> Tomsk Polytechnic University, Tomsk, Russian Federation <sup>3</sup> Peter The Great St. Petersburg Polytechnic University, St. Petersburg, Russian Federation <sup>4</sup> Department of Nanophotonics and Metamaterials, ITMO University, St. Petersburg, Russian Federation <sup>5</sup> St. Petersburg Academic University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(476) "1 First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation 2 Tomsk Polytechnic University, Tomsk, Russian Federation 3 Peter The Great St. Petersburg Polytechnic University, St. Petersburg, Russian Federation 4 Department of Nanophotonics and Metamaterials, ITMO University, St. Petersburg, Russian Federation 5 St. Petersburg Academic University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20702" ["VALUE"]=> array(2) { ["TEXT"]=> string(3611) "<h2></h2> <h2 style="text-align: justify;">Introduction and goals</h2> <p style="text-align: justify;"> The aim of this work is to investigate the possibilities of usage of multipotent mesenchymal stromal cells (MMSC) as a platform for delivering drugs which are contained in hybrid polymeric microcapsules. MMSCs are a cell population with high potential which due to the phenomenon of pathotropism can solve the problem of target drug delivery by acting as a carrier. Thus, combination of the biological phenomenon of cell migration and the high loading capacity of polymer capsules will allow targeted delivery of a substance without external and internal effect on carrier cells. To test the technique, doxorubicin and vincristine were selected as antitumor drugs with a dose-dependent effect, which are included in many polychemotherapy regimens. </p> <h2 style="text-align: justify;">Methods</h2> <p style="text-align: justify;"> In this study, hybrid microcapsules of various sizes (5 μm, 1 μm, 0.5 μm) were synthesized using Layer-by-Layer technique (Polyarginine/Dextran sulfate) and sol-gel synthesis (Tetraethyl orthosilicate). These micro containers have low toxicity, high biocompatibility, and are also capable of protecting the cell from encapsulated drugs. The association of cells with capsules of various sizes was evaluated using flow cytometry and laser scanning confocal microscopy in order to determine the optimal ratio of capsules and cells. The effect of capsules of various sizes associated with cells on spontaneous migration of MSCs, was examined using a cell-IQ cell culture monitoring system. The ability of MMSC to direct migration through the concentration gradient of SDF-1 was studied. For qualitative and quantitative assessment of migration, Transwell, μ-Slide Chemotaxis were used, and the ability of MMSC to migrate in the collagen gel towards spheroids of cancer cells synthesizing SDF-1 and their ability to penetrate the conglomerate of cells was investigated. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The results show that MSC cells are able to capture more than 10 capsules containing antitumor drugs – doxorubicin, vincristine. According to the experimental data of flow cytometry, it has been shown that about 90% of the cells are able to internalize the capsules with high efficiency. The unique structure of capsules prevents the release of antitumor drugs within 72 hours. It is shown that most of the cells are able to transfer capsules along the SDF-1 gradient and into the tumor spheroid focus. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Thus, it is shown that MSCs with capsules containing antitumor drugs can serve as a new dosage form for the targeted delivery of antitumor drugs to the tumor site. </p> <h2 style="text-align: justify;">Acknowledgments</h2> <p style="text-align: justify;"> This work was supported by the Russian Foundation for Basic Research (grant No. 18-015-00100). </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Targeted delivery, micro and nanocapsules, antitumor drugs, internalization, mesenchymal stromal cells, migration, pharmacokinetics, synthesis, cultivation, carrier cells. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3335) "Introduction and goals
The aim of this work is to investigate the possibilities of usage of multipotent mesenchymal stromal cells (MMSC) as a platform for delivering drugs which are contained in hybrid polymeric microcapsules. MMSCs are a cell population with high potential which due to the phenomenon of pathotropism can solve the problem of target drug delivery by acting as a carrier. Thus, combination of the biological phenomenon of cell migration and the high loading capacity of polymer capsules will allow targeted delivery of a substance without external and internal effect on carrier cells. To test the technique, doxorubicin and vincristine were selected as antitumor drugs with a dose-dependent effect, which are included in many polychemotherapy regimens.
Methods
In this study, hybrid microcapsules of various sizes (5 μm, 1 μm, 0.5 μm) were synthesized using Layer-by-Layer technique (Polyarginine/Dextran sulfate) and sol-gel synthesis (Tetraethyl orthosilicate). These micro containers have low toxicity, high biocompatibility, and are also capable of protecting the cell from encapsulated drugs. The association of cells with capsules of various sizes was evaluated using flow cytometry and laser scanning confocal microscopy in order to determine the optimal ratio of capsules and cells. The effect of capsules of various sizes associated with cells on spontaneous migration of MSCs, was examined using a cell-IQ cell culture monitoring system. The ability of MMSC to direct migration through the concentration gradient of SDF-1 was studied. For qualitative and quantitative assessment of migration, Transwell, μ-Slide Chemotaxis were used, and the ability of MMSC to migrate in the collagen gel towards spheroids of cancer cells synthesizing SDF-1 and their ability to penetrate the conglomerate of cells was investigated.
Results
The results show that MSC cells are able to capture more than 10 capsules containing antitumor drugs – doxorubicin, vincristine. According to the experimental data of flow cytometry, it has been shown that about 90% of the cells are able to internalize the capsules with high efficiency. The unique structure of capsules prevents the release of antitumor drugs within 72 hours. It is shown that most of the cells are able to transfer capsules along the SDF-1 gradient and into the tumor spheroid focus.
Conclusion
Thus, it is shown that MSCs with capsules containing antitumor drugs can serve as a new dosage form for the targeted delivery of antitumor drugs to the tumor site.
Acknowledgments
This work was supported by the Russian Foundation for Basic Research (grant No. 18-015-00100).
Keywords
Targeted delivery, micro and nanocapsules, antitumor drugs, internalization, mesenchymal stromal cells, migration, pharmacokinetics, synthesis, cultivation, carrier cells.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20703" ["VALUE"]=> string(113) "Functionalization of bone marrow mesenchymal stromal cells by multifunctional capsules for targeted drug delivery" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(113) "Functionalization of bone marrow mesenchymal stromal cells by multifunctional capsules for targeted drug delivery" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20827" ["VALUE"]=> string(4) "1466" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1466" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20828" ["VALUE"]=> string(4) "1467" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1467" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20700" ["VALUE"]=> array(2) { ["TEXT"]=> string(657) "Alexander S. Timin <sup>1</sup>,<sup>2</sup>, Albert R. Muslimov <sup>1</sup>, Oleksii O. Peltek <sup>3</sup>, Mikhail V. Zyuzin <sup>4</sup>, Olga S. Epifanovskaya <sup>1</sup>, Vladislav S. Sergeev <sup>1</sup>, Anna A. Dotsenko <sup>1</sup>, Timofey E. Karpov <sup>3</sup>, Igor S. Sergeev <sup>3</sup>, Alexander A. Goncharenko <sup>3</sup>, Yana V. Tarakanchikova <sup>5</sup>, Kirill V. Lepik <sup>1</sup>, Gleb B. Sukhorukov <sup>3</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(477) "Alexander S. Timin 1,2, Albert R. Muslimov 1, Oleksii O. Peltek 3, Mikhail V. Zyuzin 4, Olga S. Epifanovskaya 1, Vladislav S. Sergeev 1, Anna A. Dotsenko 1, Timofey E. Karpov 3, Igor S. Sergeev 3, Alexander A. Goncharenko 3, Yana V. Tarakanchikova 5, Kirill V. Lepik 1, Gleb B. Sukhorukov 3, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(477) "Alexander S. Timin 1,2, Albert R. Muslimov 1, Oleksii O. Peltek 3, Mikhail V. Zyuzin 4, Olga S. Epifanovskaya 1, Vladislav S. Sergeev 1, Anna A. Dotsenko 1, Timofey E. Karpov 3, Igor S. Sergeev 3, Alexander A. Goncharenko 3, Yana V. Tarakanchikova 5, Kirill V. Lepik 1, Gleb B. Sukhorukov 3, Boris V. Afanasyev 1" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20702" ["VALUE"]=> array(2) { ["TEXT"]=> string(3611) "<h2></h2> <h2 style="text-align: justify;">Introduction and goals</h2> <p style="text-align: justify;"> The aim of this work is to investigate the possibilities of usage of multipotent mesenchymal stromal cells (MMSC) as a platform for delivering drugs which are contained in hybrid polymeric microcapsules. MMSCs are a cell population with high potential which due to the phenomenon of pathotropism can solve the problem of target drug delivery by acting as a carrier. Thus, combination of the biological phenomenon of cell migration and the high loading capacity of polymer capsules will allow targeted delivery of a substance without external and internal effect on carrier cells. To test the technique, doxorubicin and vincristine were selected as antitumor drugs with a dose-dependent effect, which are included in many polychemotherapy regimens. </p> <h2 style="text-align: justify;">Methods</h2> <p style="text-align: justify;"> In this study, hybrid microcapsules of various sizes (5 μm, 1 μm, 0.5 μm) were synthesized using Layer-by-Layer technique (Polyarginine/Dextran sulfate) and sol-gel synthesis (Tetraethyl orthosilicate). These micro containers have low toxicity, high biocompatibility, and are also capable of protecting the cell from encapsulated drugs. The association of cells with capsules of various sizes was evaluated using flow cytometry and laser scanning confocal microscopy in order to determine the optimal ratio of capsules and cells. The effect of capsules of various sizes associated with cells on spontaneous migration of MSCs, was examined using a cell-IQ cell culture monitoring system. The ability of MMSC to direct migration through the concentration gradient of SDF-1 was studied. For qualitative and quantitative assessment of migration, Transwell, μ-Slide Chemotaxis were used, and the ability of MMSC to migrate in the collagen gel towards spheroids of cancer cells synthesizing SDF-1 and their ability to penetrate the conglomerate of cells was investigated. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The results show that MSC cells are able to capture more than 10 capsules containing antitumor drugs – doxorubicin, vincristine. According to the experimental data of flow cytometry, it has been shown that about 90% of the cells are able to internalize the capsules with high efficiency. The unique structure of capsules prevents the release of antitumor drugs within 72 hours. It is shown that most of the cells are able to transfer capsules along the SDF-1 gradient and into the tumor spheroid focus. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Thus, it is shown that MSCs with capsules containing antitumor drugs can serve as a new dosage form for the targeted delivery of antitumor drugs to the tumor site. </p> <h2 style="text-align: justify;">Acknowledgments</h2> <p style="text-align: justify;"> This work was supported by the Russian Foundation for Basic Research (grant No. 18-015-00100). </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Targeted delivery, micro and nanocapsules, antitumor drugs, internalization, mesenchymal stromal cells, migration, pharmacokinetics, synthesis, cultivation, carrier cells. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3335) "Introduction and goals
The aim of this work is to investigate the possibilities of usage of multipotent mesenchymal stromal cells (MMSC) as a platform for delivering drugs which are contained in hybrid polymeric microcapsules. MMSCs are a cell population with high potential which due to the phenomenon of pathotropism can solve the problem of target drug delivery by acting as a carrier. Thus, combination of the biological phenomenon of cell migration and the high loading capacity of polymer capsules will allow targeted delivery of a substance without external and internal effect on carrier cells. To test the technique, doxorubicin and vincristine were selected as antitumor drugs with a dose-dependent effect, which are included in many polychemotherapy regimens.
Methods
In this study, hybrid microcapsules of various sizes (5 μm, 1 μm, 0.5 μm) were synthesized using Layer-by-Layer technique (Polyarginine/Dextran sulfate) and sol-gel synthesis (Tetraethyl orthosilicate). These micro containers have low toxicity, high biocompatibility, and are also capable of protecting the cell from encapsulated drugs. The association of cells with capsules of various sizes was evaluated using flow cytometry and laser scanning confocal microscopy in order to determine the optimal ratio of capsules and cells. The effect of capsules of various sizes associated with cells on spontaneous migration of MSCs, was examined using a cell-IQ cell culture monitoring system. The ability of MMSC to direct migration through the concentration gradient of SDF-1 was studied. For qualitative and quantitative assessment of migration, Transwell, μ-Slide Chemotaxis were used, and the ability of MMSC to migrate in the collagen gel towards spheroids of cancer cells synthesizing SDF-1 and their ability to penetrate the conglomerate of cells was investigated.
Results
The results show that MSC cells are able to capture more than 10 capsules containing antitumor drugs – doxorubicin, vincristine. According to the experimental data of flow cytometry, it has been shown that about 90% of the cells are able to internalize the capsules with high efficiency. The unique structure of capsules prevents the release of antitumor drugs within 72 hours. It is shown that most of the cells are able to transfer capsules along the SDF-1 gradient and into the tumor spheroid focus.
Conclusion
Thus, it is shown that MSCs with capsules containing antitumor drugs can serve as a new dosage form for the targeted delivery of antitumor drugs to the tumor site.
Acknowledgments
This work was supported by the Russian Foundation for Basic Research (grant No. 18-015-00100).
Keywords
Targeted delivery, micro and nanocapsules, antitumor drugs, internalization, mesenchymal stromal cells, migration, pharmacokinetics, synthesis, cultivation, carrier cells.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3335) "Introduction and goals
The aim of this work is to investigate the possibilities of usage of multipotent mesenchymal stromal cells (MMSC) as a platform for delivering drugs which are contained in hybrid polymeric microcapsules. MMSCs are a cell population with high potential which due to the phenomenon of pathotropism can solve the problem of target drug delivery by acting as a carrier. Thus, combination of the biological phenomenon of cell migration and the high loading capacity of polymer capsules will allow targeted delivery of a substance without external and internal effect on carrier cells. To test the technique, doxorubicin and vincristine were selected as antitumor drugs with a dose-dependent effect, which are included in many polychemotherapy regimens.
Methods
In this study, hybrid microcapsules of various sizes (5 μm, 1 μm, 0.5 μm) were synthesized using Layer-by-Layer technique (Polyarginine/Dextran sulfate) and sol-gel synthesis (Tetraethyl orthosilicate). These micro containers have low toxicity, high biocompatibility, and are also capable of protecting the cell from encapsulated drugs. The association of cells with capsules of various sizes was evaluated using flow cytometry and laser scanning confocal microscopy in order to determine the optimal ratio of capsules and cells. The effect of capsules of various sizes associated with cells on spontaneous migration of MSCs, was examined using a cell-IQ cell culture monitoring system. The ability of MMSC to direct migration through the concentration gradient of SDF-1 was studied. For qualitative and quantitative assessment of migration, Transwell, μ-Slide Chemotaxis were used, and the ability of MMSC to migrate in the collagen gel towards spheroids of cancer cells synthesizing SDF-1 and their ability to penetrate the conglomerate of cells was investigated.
Results
The results show that MSC cells are able to capture more than 10 capsules containing antitumor drugs – doxorubicin, vincristine. According to the experimental data of flow cytometry, it has been shown that about 90% of the cells are able to internalize the capsules with high efficiency. The unique structure of capsules prevents the release of antitumor drugs within 72 hours. It is shown that most of the cells are able to transfer capsules along the SDF-1 gradient and into the tumor spheroid focus.
Conclusion
Thus, it is shown that MSCs with capsules containing antitumor drugs can serve as a new dosage form for the targeted delivery of antitumor drugs to the tumor site.
Acknowledgments
This work was supported by the Russian Foundation for Basic Research (grant No. 18-015-00100).
Keywords
Targeted delivery, micro and nanocapsules, antitumor drugs, internalization, mesenchymal stromal cells, migration, pharmacokinetics, synthesis, cultivation, carrier cells.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20703" ["VALUE"]=> string(113) "Functionalization of bone marrow mesenchymal stromal cells by multifunctional capsules for targeted drug delivery" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(113) "Functionalization of bone marrow mesenchymal stromal cells by multifunctional capsules for targeted drug delivery" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(113) "Functionalization of bone marrow mesenchymal stromal cells by multifunctional capsules for targeted drug delivery" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20701" ["VALUE"]=> array(2) { ["TEXT"]=> string(536) "<sup>1</sup> First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation <sup>2</sup> Tomsk Polytechnic University, Tomsk, Russian Federation <sup>3</sup> Peter The Great St. Petersburg Polytechnic University, St. Petersburg, Russian Federation <sup>4</sup> Department of Nanophotonics and Metamaterials, ITMO University, St. Petersburg, Russian Federation <sup>5</sup> St. Petersburg Academic University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(476) "1 First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation 2 Tomsk Polytechnic University, Tomsk, Russian Federation 3 Peter The Great St. Petersburg Polytechnic University, St. Petersburg, Russian Federation 4 Department of Nanophotonics and Metamaterials, ITMO University, St. Petersburg, Russian Federation 5 St. Petersburg Academic University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(476) "1 First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation 2 Tomsk Polytechnic University, Tomsk, Russian Federation 3 Peter The Great St. Petersburg Polytechnic University, St. Petersburg, Russian Federation 4 Department of Nanophotonics and Metamaterials, ITMO University, St. Petersburg, Russian Federation 5 St. Petersburg Academic University, St. Petersburg, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20697" ["VALUE"]=> array(2) { ["TEXT"]=> string(863) "Александр С. Тимин <sup>1</sup>,<sup>2</sup>, Альберт Р. Муслимов <sup>1</sup>, Алексей А. Пельтек <sup>3</sup>, Михаил В. Зюзин <sup>4</sup>, Ольга С. Епифановская <sup>1</sup>, Владислав С. Сергеев <sup>1</sup>, Анна А. Доценко <sup>1</sup>, Тимофей Е. Карпов <sup>3</sup>, Игорь С. Сергеев <sup>3</sup>, Александр А. Гончаренко <sup>3</sup>, Яна В. Тараканчикова <sup>5</sup>, Кирилл В. Лепик <sup>1</sup>, Глеб Б. Сухоруков <sup>3</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(683) "Александр С. Тимин 1,2, Альберт Р. Муслимов 1, Алексей А. Пельтек 3, Михаил В. Зюзин 4, Ольга С. Епифановская 1, Владислав С. Сергеев 1, Анна А. Доценко 1, Тимофей Е. Карпов 3, Игорь С. Сергеев 3, Александр А. Гончаренко 3, Яна В. Тараканчикова 5, Кирилл В. Лепик 1, Глеб Б. Сухоруков 3, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(683) "Александр С. Тимин 1,2, Альберт Р. Муслимов 1, Алексей А. Пельтек 3, Михаил В. Зюзин 4, Ольга С. Епифановская 1, Владислав С. Сергеев 1, Анна А. Доценко 1, Тимофей Е. Карпов 3, Игорь С. Сергеев 3, Александр А. Гончаренко 3, Яна В. Тараканчикова 5, Кирилл В. Лепик 1, Глеб Б. Сухоруков 3, Борис В. Афанасьев 1" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20699" ["VALUE"]=> array(2) { ["TEXT"]=> string(6473) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Цель данной работы состояла в исследовании возможностей применения мультипотентных мезенхимальных стромальных клеток (ММСК) в качестве платформы для доставки препаратов, заключенных в гибридные полимерные микрокапсулы. ММСК являются высокопотенциальной клеточной популяцией, которая за счет феномена патотропизма может решить проблему таргетной доставки препарата, выступая в качестве носителя. Таким образом, объединение биологического феномена миграции клеток и высокой загружающей способности полимерных капсул обеспечит возможность контролировать направленность действия и позволит выполнить таргетную доставку вещества без внешнего и внутреннего воздействия для клеток-носителей. Для отработки методики, доксорубицин и винкристин были отобраны, в качестве противоопухолевых препаратов с дозозависимым эффектом, которые включены в состав многих схем полихимиотерапии. </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> В ходе данного исследования был произведен синтез гибридных микрокапсул различных размеров (5 мкм, 1 мкм, 0,5 мкм) при помощи технологии Layer-by- Layer (Polyarginine/Dextran sulfate) и золь-гель синтеза (Tetraethyl orthosilicate). Данные микроконтейнеры обладают низкой токсичностью, высокой биосовместимостью, а также способны защитить клетку от инкапсулированных препаратов. На следующем этапе была выполнена оценка ассоциации клеток с капсулами различных размеров при помощи проточной цитометрии и лазерной сканирующей конфокальной микроскопии для определения оптимального соотношения капсул и клеток. Спонтанная миграция МСК, и влияние на нее ассоциированных с клетками капсул различных размеров была исследована при помощи системы наблюдения за живыми клетками в культуре Cell-IQ. На завершающем этапе работы была изучена способность ММСК к направленной миграции по градиенту концентрации SDF-1. Для качественной и количественной оценки миграции были использованы Transwell, μ-Slide Chemotaxis, а также была исследована способность ММСК к миграции в коллагеновом геле в сторону сфероидов из раковых клеток, синтезирующих SDF-1, и их способность проникать внутрь конгломерата клеток. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Полученные результаты показывают, что МСК клетки способны захватывать более 10 капсул, содержащие противоопухолевые препараты – доксорубицин, винкристин. По экспериментальным данным проточной цитометрии показано, что 90 % клеток способны интернализировать капсулы с высокой эффективностью. Уникальная структура капсул предотвращает высвобождение противоопухолевых препаратов в течение 72 часов. Показано, что большая часть клеток способны направлено переносить капсулы по SDF-1 градиенту и в очаг опухолевого сфероида. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Таким образом, показано, что МСК с включенными капсулами, содержащие противоопухолевые препараты, могут выступать в качестве новой лекарственной формы для направленной доставки противоопухолевых препаратов в очаг опухолей.</p> <h2>Благодарности</h2> <p style="text-align: justify;"> Работа выполнена при поддержке Российского Фонда Фундаментальных исследований (грант № 18-015-00100). </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Таргетная доставка, микро- и нанокапсулы, противоо пухолевые препараты, интернализация, мезенхимные стромальные клетки, миграция, фармакокинетика, синтез, культивирование, клетки-носители. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6219) "Введение
Цель данной работы состояла в исследовании возможностей применения мультипотентных мезенхимальных стромальных клеток (ММСК) в качестве платформы для доставки препаратов, заключенных в гибридные полимерные микрокапсулы. ММСК являются высокопотенциальной клеточной популяцией, которая за счет феномена патотропизма может решить проблему таргетной доставки препарата, выступая в качестве носителя. Таким образом, объединение биологического феномена миграции клеток и высокой загружающей способности полимерных капсул обеспечит возможность контролировать направленность действия и позволит выполнить таргетную доставку вещества без внешнего и внутреннего воздействия для клеток-носителей. Для отработки методики, доксорубицин и винкристин были отобраны, в качестве противоопухолевых препаратов с дозозависимым эффектом, которые включены в состав многих схем полихимиотерапии.
Методы
В ходе данного исследования был произведен синтез гибридных микрокапсул различных размеров (5 мкм, 1 мкм, 0,5 мкм) при помощи технологии Layer-by- Layer (Polyarginine/Dextran sulfate) и золь-гель синтеза (Tetraethyl orthosilicate). Данные микроконтейнеры обладают низкой токсичностью, высокой биосовместимостью, а также способны защитить клетку от инкапсулированных препаратов. На следующем этапе была выполнена оценка ассоциации клеток с капсулами различных размеров при помощи проточной цитометрии и лазерной сканирующей конфокальной микроскопии для определения оптимального соотношения капсул и клеток. Спонтанная миграция МСК, и влияние на нее ассоциированных с клетками капсул различных размеров была исследована при помощи системы наблюдения за живыми клетками в культуре Cell-IQ. На завершающем этапе работы была изучена способность ММСК к направленной миграции по градиенту концентрации SDF-1. Для качественной и количественной оценки миграции были использованы Transwell, μ-Slide Chemotaxis, а также была исследована способность ММСК к миграции в коллагеновом геле в сторону сфероидов из раковых клеток, синтезирующих SDF-1, и их способность проникать внутрь конгломерата клеток.
Результаты
Полученные результаты показывают, что МСК клетки способны захватывать более 10 капсул, содержащие противоопухолевые препараты – доксорубицин, винкристин. По экспериментальным данным проточной цитометрии показано, что 90 % клеток способны интернализировать капсулы с высокой эффективностью. Уникальная структура капсул предотвращает высвобождение противоопухолевых препаратов в течение 72 часов. Показано, что большая часть клеток способны направлено переносить капсулы по SDF-1 градиенту и в очаг опухолевого сфероида.
Заключение
Таким образом, показано, что МСК с включенными капсулами, содержащие противоопухолевые препараты, могут выступать в качестве новой лекарственной формы для направленной доставки противоопухолевых препаратов в очаг опухолей.
Благодарности
Работа выполнена при поддержке Российского Фонда Фундаментальных исследований (грант № 18-015-00100).
Ключевые слова
Таргетная доставка, микро- и нанокапсулы, противоо пухолевые препараты, интернализация, мезенхимные стромальные клетки, миграция, фармакокинетика, синтез, культивирование, клетки-носители.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6219) "Введение
Цель данной работы состояла в исследовании возможностей применения мультипотентных мезенхимальных стромальных клеток (ММСК) в качестве платформы для доставки препаратов, заключенных в гибридные полимерные микрокапсулы. ММСК являются высокопотенциальной клеточной популяцией, которая за счет феномена патотропизма может решить проблему таргетной доставки препарата, выступая в качестве носителя. Таким образом, объединение биологического феномена миграции клеток и высокой загружающей способности полимерных капсул обеспечит возможность контролировать направленность действия и позволит выполнить таргетную доставку вещества без внешнего и внутреннего воздействия для клеток-носителей. Для отработки методики, доксорубицин и винкристин были отобраны, в качестве противоопухолевых препаратов с дозозависимым эффектом, которые включены в состав многих схем полихимиотерапии.
Методы
В ходе данного исследования был произведен синтез гибридных микрокапсул различных размеров (5 мкм, 1 мкм, 0,5 мкм) при помощи технологии Layer-by- Layer (Polyarginine/Dextran sulfate) и золь-гель синтеза (Tetraethyl orthosilicate). Данные микроконтейнеры обладают низкой токсичностью, высокой биосовместимостью, а также способны защитить клетку от инкапсулированных препаратов. На следующем этапе была выполнена оценка ассоциации клеток с капсулами различных размеров при помощи проточной цитометрии и лазерной сканирующей конфокальной микроскопии для определения оптимального соотношения капсул и клеток. Спонтанная миграция МСК, и влияние на нее ассоциированных с клетками капсул различных размеров была исследована при помощи системы наблюдения за живыми клетками в культуре Cell-IQ. На завершающем этапе работы была изучена способность ММСК к направленной миграции по градиенту концентрации SDF-1. Для качественной и количественной оценки миграции были использованы Transwell, μ-Slide Chemotaxis, а также была исследована способность ММСК к миграции в коллагеновом геле в сторону сфероидов из раковых клеток, синтезирующих SDF-1, и их способность проникать внутрь конгломерата клеток.
Результаты
Полученные результаты показывают, что МСК клетки способны захватывать более 10 капсул, содержащие противоопухолевые препараты – доксорубицин, винкристин. По экспериментальным данным проточной цитометрии показано, что 90 % клеток способны интернализировать капсулы с высокой эффективностью. Уникальная структура капсул предотвращает высвобождение противоопухолевых препаратов в течение 72 часов. Показано, что большая часть клеток способны направлено переносить капсулы по SDF-1 градиенту и в очаг опухолевого сфероида.
Заключение
Таким образом, показано, что МСК с включенными капсулами, содержащие противоопухолевые препараты, могут выступать в качестве новой лекарственной формы для направленной доставки противоопухолевых препаратов в очаг опухолей.
Благодарности
Работа выполнена при поддержке Российского Фонда Фундаментальных исследований (грант № 18-015-00100).
Ключевые слова
Таргетная доставка, микро- и нанокапсулы, противоо пухолевые препараты, интернализация, мезенхимные стромальные клетки, миграция, фармакокинетика, синтез, культивирование, клетки-носители.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20698" ["VALUE"]=> array(2) { ["TEXT"]=> string(958) "<sup>1</sup> Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия <sup>2</sup> Томский политехнический университет, Томск, Россия <sup>3</sup> Санкт-Петербургский Политехнический Университет Петра Великого, Санкт-Петербург, Россия <sup>4</sup> Санкт-Петербургский Национальный Исследовательский Университет ИТМО, Санкт-Петербург, Россия <sup>5</sup> Санкт-Петербургский Национальный Исследовательский Академический Университет, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(898) "1 Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия 2 Томский политехнический университет, Томск, Россия 3 Санкт-Петербургский Политехнический Университет Петра Великого, Санкт-Петербург, Россия 4 Санкт-Петербургский Национальный Исследовательский Университет ИТМО, Санкт-Петербург, Россия 5 Санкт-Петербургский Национальный Исследовательский Академический Университет, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(898) "1 Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия 2 Томский политехнический университет, Томск, Россия 3 Санкт-Петербургский Политехнический Университет Петра Великого, Санкт-Петербург, Россия 4 Санкт-Петербургский Национальный Исследовательский Университет ИТМО, Санкт-Петербург, Россия 5 Санкт-Петербургский Национальный Исследовательский Академический Университет, Санкт-Петербург, Россия" } } } [39]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1598" ["~ID"]=> string(4) "1598" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(172) "Опыт приготовления парэнтерального питания методом компаундинга у пациентов после алло-ТГСК" ["~NAME"]=> string(172) "Опыт приготовления парэнтерального питания методом компаундинга у пациентов после алло-ТГСК" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "12.12.2018 22:15:55" ["~TIMESTAMP_X"]=> string(19) "12.12.2018 22:15:55" ["DETAIL_PAGE_URL"]=> string(143) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/opyt-prigotovleniya-parenteralnogo-pitaniya-metodom-kompaundinga-u-patsientov-posle-allo-tgsk/" ["~DETAIL_PAGE_URL"]=> string(143) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/opyt-prigotovleniya-parenteralnogo-pitaniya-metodom-kompaundinga-u-patsientov-posle-allo-tgsk/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(93) "opyt-prigotovleniya-parenteralnogo-pitaniya-metodom-kompaundinga-u-patsientov-posle-allo-tgsk" ["~CODE"]=> string(93) "opyt-prigotovleniya-parenteralnogo-pitaniya-metodom-kompaundinga-u-patsientov-posle-allo-tgsk" ["EXTERNAL_ID"]=> string(4) "1598" ["~EXTERNAL_ID"]=> string(4) "1598" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(172) "Опыт приготовления парэнтерального питания методом компаундинга у пациентов после алло-ТГСК" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(255) "Опыт приготовления парэнтерального питания методом компаундинга у пациентов после алло-ТГСКOur experience in compounding the parenteral nutrition for patients after allo-HSCT" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(5289) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Нутриционная поддержка онкологических больных заняла прочную позицию в ряду лечебных мероприятий. По данным отчета Европейского общества парентерального и энтерального питания, частота недостаточности питания у онкологических больных колеблется от 46 до 88%. С 2011 г. для приготовления парэнтерального питания (ПП), дозирования антибиотиков и разведения препаратов для химиотерапии используется технология компаундинга. Целью работы было сравнение аппаратного приготовления парэнтерального питания методом компаундинга с «флаконной» методикой – использование нескольких флаконов с нутриентами, и заполнением мешков вручную. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В 2018 году на базе НИИ «Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой» для приготовления парэнтерального питания 13 пациентам использован метод – компаундинга. Характеристика пациентов. Медиана возраста – 10 лет (от 11 мес. до 45 лет), 7 женщин и 6 мужчин. Основной диагноз: ОЛЛ – 38,5% (n=5), ОМЛ – 30,8%(n=4), МДС – 23,1%(n=3), ХМЛ – 7,7%(n=1). Было приготовлено 13 мешков с питанием с помощью медицинского компаундера, 4 мешка заполнялись вручную, «флаконный» метод парэнтерального питания применяли у 9 пациентов. Проведен подсчет затрачиваемого времени на три способа приготовления парэнтерального питания: технология компаундинга, «флаконная методика» и заполнение мешка вручную. Для исследования стерильности приготавливаемой смеси проводились бактериологические исследования готового раствора. В конце эксперимента проведен опрос медсестер отделения об удобстве использования парэнтерального питания (ПП) приготовленного по технологии компаундинга. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Методика компаундинга: на приготовления ПП до 1 л требовалось в среднем 6,5 мин., от 1-1,5 л в 9 мин., на пакет объемом от 1,5 до 2 л требовалось 11 мин., от 2-3 л – 15 мин. На заполнение мешка вручную ушло не менее 25 мин. На приготовление ПП «флаконным» методом затрачивали не менее 15 мин. Все бактериологические тесты смеси для парэнтерального питания приготовленного методом компаундинга были отрицательны. Опрос медсестер отделения показал, что применения готового индивидуального питания – удобно, экономит время и безопасно для пациента. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> На приготовление парэнтерального питания с помощью медицинского компаундера затрачивается меньше времени, чем на «флаконный» метод или заполнения мешка вручную. ПП, приготовленное методом компаундинга, стерильно и удобно в применении. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Парэнтеральное питание, медицинский смеситель, компаундинг, асептика, нозокомиальная инфекция. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(172) "Опыт приготовления парэнтерального питания методом компаундинга у пациентов после алло-ТГСК" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(172) "Опыт приготовления парэнтерального питания методом компаундинга у пациентов после алло-ТГСК" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(172) "Опыт приготовления парэнтерального питания методом компаундинга у пациентов после алло-ТГСК" ["SECTION_META_TITLE"]=> string(172) "Опыт приготовления парэнтерального питания методом компаундинга у пациентов после алло-ТГСК" ["SECTION_META_KEYWORDS"]=> string(172) "Опыт приготовления парэнтерального питания методом компаундинга у пациентов после алло-ТГСК" ["SECTION_META_DESCRIPTION"]=> string(172) "Опыт приготовления парэнтерального питания методом компаундинга у пациентов после алло-ТГСК" ["SECTION_PICTURE_FILE_ALT"]=> string(172) "Опыт приготовления парэнтерального питания методом компаундинга у пациентов после алло-ТГСК" ["SECTION_PICTURE_FILE_TITLE"]=> string(172) "Опыт приготовления парэнтерального питания методом компаундинга у пациентов после алло-ТГСК" ["SECTION_PICTURE_FILE_NAME"]=> string(97) "opyt-prigotovleniya-parenteralnogo-pitaniya-metodom-kompaundinga-u-patsientov-posle-allo-tgsk-img" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(172) "Опыт приготовления парэнтерального питания методом компаундинга у пациентов после алло-ТГСК" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(172) "Опыт приготовления парэнтерального питания методом компаундинга у пациентов после алло-ТГСК" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(97) "opyt-prigotovleniya-parenteralnogo-pitaniya-metodom-kompaundinga-u-patsientov-posle-allo-tgsk-img" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(97) "opyt-prigotovleniya-parenteralnogo-pitaniya-metodom-kompaundinga-u-patsientov-posle-allo-tgsk-img" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(97) "opyt-prigotovleniya-parenteralnogo-pitaniya-metodom-kompaundinga-u-patsientov-posle-allo-tgsk-img" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20690" ["VALUE"]=> array(2) { ["TEXT"]=> string(169) "Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Олег В. Голощапов, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(169) "Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Олег В. Голощапов, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20691" ["VALUE"]=> array(2) { ["TEXT"]=> string(375) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(375) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20692" ["VALUE"]=> array(2) { ["TEXT"]=> string(5289) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Нутриционная поддержка онкологических больных заняла прочную позицию в ряду лечебных мероприятий. По данным отчета Европейского общества парентерального и энтерального питания, частота недостаточности питания у онкологических больных колеблется от 46 до 88%. С 2011 г. для приготовления парэнтерального питания (ПП), дозирования антибиотиков и разведения препаратов для химиотерапии используется технология компаундинга. Целью работы было сравнение аппаратного приготовления парэнтерального питания методом компаундинга с «флаконной» методикой – использование нескольких флаконов с нутриентами, и заполнением мешков вручную. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В 2018 году на базе НИИ «Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой» для приготовления парэнтерального питания 13 пациентам использован метод – компаундинга. Характеристика пациентов. Медиана возраста – 10 лет (от 11 мес. до 45 лет), 7 женщин и 6 мужчин. Основной диагноз: ОЛЛ – 38,5% (n=5), ОМЛ – 30,8%(n=4), МДС – 23,1%(n=3), ХМЛ – 7,7%(n=1). Было приготовлено 13 мешков с питанием с помощью медицинского компаундера, 4 мешка заполнялись вручную, «флаконный» метод парэнтерального питания применяли у 9 пациентов. Проведен подсчет затрачиваемого времени на три способа приготовления парэнтерального питания: технология компаундинга, «флаконная методика» и заполнение мешка вручную. Для исследования стерильности приготавливаемой смеси проводились бактериологические исследования готового раствора. В конце эксперимента проведен опрос медсестер отделения об удобстве использования парэнтерального питания (ПП) приготовленного по технологии компаундинга. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Методика компаундинга: на приготовления ПП до 1 л требовалось в среднем 6,5 мин., от 1-1,5 л в 9 мин., на пакет объемом от 1,5 до 2 л требовалось 11 мин., от 2-3 л – 15 мин. На заполнение мешка вручную ушло не менее 25 мин. На приготовление ПП «флаконным» методом затрачивали не менее 15 мин. Все бактериологические тесты смеси для парэнтерального питания приготовленного методом компаундинга были отрицательны. Опрос медсестер отделения показал, что применения готового индивидуального питания – удобно, экономит время и безопасно для пациента. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> На приготовление парэнтерального питания с помощью медицинского компаундера затрачивается меньше времени, чем на «флаконный» метод или заполнения мешка вручную. ПП, приготовленное методом компаундинга, стерильно и удобно в применении. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Парэнтеральное питание, медицинский смеситель, компаундинг, асептика, нозокомиальная инфекция. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5057) "Введение
Нутриционная поддержка онкологических больных заняла прочную позицию в ряду лечебных мероприятий. По данным отчета Европейского общества парентерального и энтерального питания, частота недостаточности питания у онкологических больных колеблется от 46 до 88%. С 2011 г. для приготовления парэнтерального питания (ПП), дозирования антибиотиков и разведения препаратов для химиотерапии используется технология компаундинга. Целью работы было сравнение аппаратного приготовления парэнтерального питания методом компаундинга с «флаконной» методикой – использование нескольких флаконов с нутриентами, и заполнением мешков вручную.
Пациенты и методы
В 2018 году на базе НИИ «Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой» для приготовления парэнтерального питания 13 пациентам использован метод – компаундинга. Характеристика пациентов. Медиана возраста – 10 лет (от 11 мес. до 45 лет), 7 женщин и 6 мужчин. Основной диагноз: ОЛЛ – 38,5% (n=5), ОМЛ – 30,8%(n=4), МДС – 23,1%(n=3), ХМЛ – 7,7%(n=1). Было приготовлено 13 мешков с питанием с помощью медицинского компаундера, 4 мешка заполнялись вручную, «флаконный» метод парэнтерального питания применяли у 9 пациентов. Проведен подсчет затрачиваемого времени на три способа приготовления парэнтерального питания: технология компаундинга, «флаконная методика» и заполнение мешка вручную. Для исследования стерильности приготавливаемой смеси проводились бактериологические исследования готового раствора. В конце эксперимента проведен опрос медсестер отделения об удобстве использования парэнтерального питания (ПП) приготовленного по технологии компаундинга.
Результаты
Методика компаундинга: на приготовления ПП до 1 л требовалось в среднем 6,5 мин., от 1-1,5 л в 9 мин., на пакет объемом от 1,5 до 2 л требовалось 11 мин., от 2-3 л – 15 мин. На заполнение мешка вручную ушло не менее 25 мин. На приготовление ПП «флаконным» методом затрачивали не менее 15 мин. Все бактериологические тесты смеси для парэнтерального питания приготовленного методом компаундинга были отрицательны. Опрос медсестер отделения показал, что применения готового индивидуального питания – удобно, экономит время и безопасно для пациента.
Выводы
На приготовление парэнтерального питания с помощью медицинского компаундера затрачивается меньше времени, чем на «флаконный» метод или заполнения мешка вручную. ПП, приготовленное методом компаундинга, стерильно и удобно в применении.
Ключевые слова
Парэнтеральное питание, медицинский смеситель, компаундинг, асептика, нозокомиальная инфекция.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20693" ["VALUE"]=> array(2) { ["TEXT"]=> string(100) "Aschot A. Tadevosian, Olga A. Prokofieva, Olga E. Pigareva, Oleg V. Goloshchapov, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(100) "Aschot A. Tadevosian, Olga A. Prokofieva, Olga E. Pigareva, Oleg V. Goloshchapov, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20694" ["VALUE"]=> array(2) { ["TEXT"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20695" ["VALUE"]=> array(2) { ["TEXT"]=> string(2995) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Nutritional support is an established approach, along with other treatment procedures for patients with malignancies. According to the ESPEN’s report, incidence of nutritional deficiency among oncology patients varies from 46% to 88%. Since 2011, automatic compounding technology is used to prepare parenteral nutrition, antibiotics, and chemotherapy medications. Objective of the study was to compare automatic compounding of parenteral nutrition (PN) with “the flask method” providing separate infusions of distinct nutrients, and with manual PN mixing. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> In 2018, an automatic compounding technology was used to prepare parenteral nutrition for 13 patients treated at the R. Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation. The patient group included 7 women and 6 men at a median age of 10 years (11 months to 45 years old) with following primary disorders: ALL, 38.5% (n=5); AML, 30.8% (n=4); MDS, 23.1% (n=3); CML, 7.7% (n=1). Thirteen bags of parenteral nutrition were prepared using a medical compounder, and 4 bags were filled manually. Nine patients received PN by “the flask method”. In each case, time spent for preparing the nutrition was evaluated, and the prepared solutions were bacteriologically tested. As a part of the experiment, nurses at the unit were interviewed about convenience of PN usage when prepared by automatic compounding. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> At an average, it took 6.5 minutes to prepare one liter of PN by automatic compounding. It took 9 minutes to prepare 1 to 1.5-liter bag, 11 minutes to prepare 1.5 to 2.0-liter bag, and 15 minutes for a 2 to 3-liter bag. Meanwhile, it took at least 25 minutes to fill a bag manually, and 15 minutes to prepare PN using a “flask method”. All the bacteriological tests performed on the compounder-made PN mixtures were negative. Interviews with medical nurses at the unit showed that the compounder-made PN was easy to use, safe for patients, and helped to save time. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> It takes less time to prepare parenteral nutrition by using a medical compounder as compared to “the flask method” or by filling bags manually. The automatically prepared PN is sterile and easy to use. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Parenteral nutrition, nutritional support, medical compounder, compounding, aseptic, nosocomial infection. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2763) "Introduction
Nutritional support is an established approach, along with other treatment procedures for patients with malignancies. According to the ESPEN’s report, incidence of nutritional deficiency among oncology patients varies from 46% to 88%. Since 2011, automatic compounding technology is used to prepare parenteral nutrition, antibiotics, and chemotherapy medications. Objective of the study was to compare automatic compounding of parenteral nutrition (PN) with “the flask method” providing separate infusions of distinct nutrients, and with manual PN mixing.
Patients and methods
In 2018, an automatic compounding technology was used to prepare parenteral nutrition for 13 patients treated at the R. Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation. The patient group included 7 women and 6 men at a median age of 10 years (11 months to 45 years old) with following primary disorders: ALL, 38.5% (n=5); AML, 30.8% (n=4); MDS, 23.1% (n=3); CML, 7.7% (n=1). Thirteen bags of parenteral nutrition were prepared using a medical compounder, and 4 bags were filled manually. Nine patients received PN by “the flask method”. In each case, time spent for preparing the nutrition was evaluated, and the prepared solutions were bacteriologically tested. As a part of the experiment, nurses at the unit were interviewed about convenience of PN usage when prepared by automatic compounding.
Results
At an average, it took 6.5 minutes to prepare one liter of PN by automatic compounding. It took 9 minutes to prepare 1 to 1.5-liter bag, 11 minutes to prepare 1.5 to 2.0-liter bag, and 15 minutes for a 2 to 3-liter bag. Meanwhile, it took at least 25 minutes to fill a bag manually, and 15 minutes to prepare PN using a “flask method”. All the bacteriological tests performed on the compounder-made PN mixtures were negative. Interviews with medical nurses at the unit showed that the compounder-made PN was easy to use, safe for patients, and helped to save time.
Conclusion
It takes less time to prepare parenteral nutrition by using a medical compounder as compared to “the flask method” or by filling bags manually. The automatically prepared PN is sterile and easy to use.
Keywords
Parenteral nutrition, nutritional support, medical compounder, compounding, aseptic, nosocomial infection.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20696" ["VALUE"]=> string(83) "Our experience in compounding the parenteral nutrition for patients after allo-HSCT" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(83) "Our experience in compounding the parenteral nutrition for patients after allo-HSCT" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20837" ["VALUE"]=> string(4) "1476" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1476" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20838" ["VALUE"]=> string(4) "1477" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1477" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20693" ["VALUE"]=> array(2) { ["TEXT"]=> string(100) "Aschot A. Tadevosian, Olga A. Prokofieva, Olga E. Pigareva, Oleg V. Goloshchapov, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(100) "Aschot A. Tadevosian, Olga A. Prokofieva, Olga E. Pigareva, Oleg V. Goloshchapov, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(100) "Aschot A. Tadevosian, Olga A. Prokofieva, Olga E. Pigareva, Oleg V. Goloshchapov, Boris V. Afanasyev" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20695" ["VALUE"]=> array(2) { ["TEXT"]=> string(2995) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Nutritional support is an established approach, along with other treatment procedures for patients with malignancies. According to the ESPEN’s report, incidence of nutritional deficiency among oncology patients varies from 46% to 88%. Since 2011, automatic compounding technology is used to prepare parenteral nutrition, antibiotics, and chemotherapy medications. Objective of the study was to compare automatic compounding of parenteral nutrition (PN) with “the flask method” providing separate infusions of distinct nutrients, and with manual PN mixing. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> In 2018, an automatic compounding technology was used to prepare parenteral nutrition for 13 patients treated at the R. Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation. The patient group included 7 women and 6 men at a median age of 10 years (11 months to 45 years old) with following primary disorders: ALL, 38.5% (n=5); AML, 30.8% (n=4); MDS, 23.1% (n=3); CML, 7.7% (n=1). Thirteen bags of parenteral nutrition were prepared using a medical compounder, and 4 bags were filled manually. Nine patients received PN by “the flask method”. In each case, time spent for preparing the nutrition was evaluated, and the prepared solutions were bacteriologically tested. As a part of the experiment, nurses at the unit were interviewed about convenience of PN usage when prepared by automatic compounding. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> At an average, it took 6.5 minutes to prepare one liter of PN by automatic compounding. It took 9 minutes to prepare 1 to 1.5-liter bag, 11 minutes to prepare 1.5 to 2.0-liter bag, and 15 minutes for a 2 to 3-liter bag. Meanwhile, it took at least 25 minutes to fill a bag manually, and 15 minutes to prepare PN using a “flask method”. All the bacteriological tests performed on the compounder-made PN mixtures were negative. Interviews with medical nurses at the unit showed that the compounder-made PN was easy to use, safe for patients, and helped to save time. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> It takes less time to prepare parenteral nutrition by using a medical compounder as compared to “the flask method” or by filling bags manually. The automatically prepared PN is sterile and easy to use. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Parenteral nutrition, nutritional support, medical compounder, compounding, aseptic, nosocomial infection. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2763) "Introduction
Nutritional support is an established approach, along with other treatment procedures for patients with malignancies. According to the ESPEN’s report, incidence of nutritional deficiency among oncology patients varies from 46% to 88%. Since 2011, automatic compounding technology is used to prepare parenteral nutrition, antibiotics, and chemotherapy medications. Objective of the study was to compare automatic compounding of parenteral nutrition (PN) with “the flask method” providing separate infusions of distinct nutrients, and with manual PN mixing.
Patients and methods
In 2018, an automatic compounding technology was used to prepare parenteral nutrition for 13 patients treated at the R. Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation. The patient group included 7 women and 6 men at a median age of 10 years (11 months to 45 years old) with following primary disorders: ALL, 38.5% (n=5); AML, 30.8% (n=4); MDS, 23.1% (n=3); CML, 7.7% (n=1). Thirteen bags of parenteral nutrition were prepared using a medical compounder, and 4 bags were filled manually. Nine patients received PN by “the flask method”. In each case, time spent for preparing the nutrition was evaluated, and the prepared solutions were bacteriologically tested. As a part of the experiment, nurses at the unit were interviewed about convenience of PN usage when prepared by automatic compounding.
Results
At an average, it took 6.5 minutes to prepare one liter of PN by automatic compounding. It took 9 minutes to prepare 1 to 1.5-liter bag, 11 minutes to prepare 1.5 to 2.0-liter bag, and 15 minutes for a 2 to 3-liter bag. Meanwhile, it took at least 25 minutes to fill a bag manually, and 15 minutes to prepare PN using a “flask method”. All the bacteriological tests performed on the compounder-made PN mixtures were negative. Interviews with medical nurses at the unit showed that the compounder-made PN was easy to use, safe for patients, and helped to save time.
Conclusion
It takes less time to prepare parenteral nutrition by using a medical compounder as compared to “the flask method” or by filling bags manually. The automatically prepared PN is sterile and easy to use.
Keywords
Parenteral nutrition, nutritional support, medical compounder, compounding, aseptic, nosocomial infection.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2763) "Introduction
Nutritional support is an established approach, along with other treatment procedures for patients with malignancies. According to the ESPEN’s report, incidence of nutritional deficiency among oncology patients varies from 46% to 88%. Since 2011, automatic compounding technology is used to prepare parenteral nutrition, antibiotics, and chemotherapy medications. Objective of the study was to compare automatic compounding of parenteral nutrition (PN) with “the flask method” providing separate infusions of distinct nutrients, and with manual PN mixing.
Patients and methods
In 2018, an automatic compounding technology was used to prepare parenteral nutrition for 13 patients treated at the R. Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation. The patient group included 7 women and 6 men at a median age of 10 years (11 months to 45 years old) with following primary disorders: ALL, 38.5% (n=5); AML, 30.8% (n=4); MDS, 23.1% (n=3); CML, 7.7% (n=1). Thirteen bags of parenteral nutrition were prepared using a medical compounder, and 4 bags were filled manually. Nine patients received PN by “the flask method”. In each case, time spent for preparing the nutrition was evaluated, and the prepared solutions were bacteriologically tested. As a part of the experiment, nurses at the unit were interviewed about convenience of PN usage when prepared by automatic compounding.
Results
At an average, it took 6.5 minutes to prepare one liter of PN by automatic compounding. It took 9 minutes to prepare 1 to 1.5-liter bag, 11 minutes to prepare 1.5 to 2.0-liter bag, and 15 minutes for a 2 to 3-liter bag. Meanwhile, it took at least 25 minutes to fill a bag manually, and 15 minutes to prepare PN using a “flask method”. All the bacteriological tests performed on the compounder-made PN mixtures were negative. Interviews with medical nurses at the unit showed that the compounder-made PN was easy to use, safe for patients, and helped to save time.
Conclusion
It takes less time to prepare parenteral nutrition by using a medical compounder as compared to “the flask method” or by filling bags manually. The automatically prepared PN is sterile and easy to use.
Keywords
Parenteral nutrition, nutritional support, medical compounder, compounding, aseptic, nosocomial infection.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20696" ["VALUE"]=> string(83) "Our experience in compounding the parenteral nutrition for patients after allo-HSCT" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(83) "Our experience in compounding the parenteral nutrition for patients after allo-HSCT" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(83) "Our experience in compounding the parenteral nutrition for patients after allo-HSCT" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20694" ["VALUE"]=> array(2) { ["TEXT"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20690" ["VALUE"]=> array(2) { ["TEXT"]=> string(169) "Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Олег В. Голощапов, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(169) "Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Олег В. Голощапов, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(169) "Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Олег В. Голощапов, Борис В. Афанасьев" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20692" ["VALUE"]=> array(2) { ["TEXT"]=> string(5289) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Нутриционная поддержка онкологических больных заняла прочную позицию в ряду лечебных мероприятий. По данным отчета Европейского общества парентерального и энтерального питания, частота недостаточности питания у онкологических больных колеблется от 46 до 88%. С 2011 г. для приготовления парэнтерального питания (ПП), дозирования антибиотиков и разведения препаратов для химиотерапии используется технология компаундинга. Целью работы было сравнение аппаратного приготовления парэнтерального питания методом компаундинга с «флаконной» методикой – использование нескольких флаконов с нутриентами, и заполнением мешков вручную. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> В 2018 году на базе НИИ «Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой» для приготовления парэнтерального питания 13 пациентам использован метод – компаундинга. Характеристика пациентов. Медиана возраста – 10 лет (от 11 мес. до 45 лет), 7 женщин и 6 мужчин. Основной диагноз: ОЛЛ – 38,5% (n=5), ОМЛ – 30,8%(n=4), МДС – 23,1%(n=3), ХМЛ – 7,7%(n=1). Было приготовлено 13 мешков с питанием с помощью медицинского компаундера, 4 мешка заполнялись вручную, «флаконный» метод парэнтерального питания применяли у 9 пациентов. Проведен подсчет затрачиваемого времени на три способа приготовления парэнтерального питания: технология компаундинга, «флаконная методика» и заполнение мешка вручную. Для исследования стерильности приготавливаемой смеси проводились бактериологические исследования готового раствора. В конце эксперимента проведен опрос медсестер отделения об удобстве использования парэнтерального питания (ПП) приготовленного по технологии компаундинга. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Методика компаундинга: на приготовления ПП до 1 л требовалось в среднем 6,5 мин., от 1-1,5 л в 9 мин., на пакет объемом от 1,5 до 2 л требовалось 11 мин., от 2-3 л – 15 мин. На заполнение мешка вручную ушло не менее 25 мин. На приготовление ПП «флаконным» методом затрачивали не менее 15 мин. Все бактериологические тесты смеси для парэнтерального питания приготовленного методом компаундинга были отрицательны. Опрос медсестер отделения показал, что применения готового индивидуального питания – удобно, экономит время и безопасно для пациента. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> На приготовление парэнтерального питания с помощью медицинского компаундера затрачивается меньше времени, чем на «флаконный» метод или заполнения мешка вручную. ПП, приготовленное методом компаундинга, стерильно и удобно в применении. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Парэнтеральное питание, медицинский смеситель, компаундинг, асептика, нозокомиальная инфекция. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5057) "Введение
Нутриционная поддержка онкологических больных заняла прочную позицию в ряду лечебных мероприятий. По данным отчета Европейского общества парентерального и энтерального питания, частота недостаточности питания у онкологических больных колеблется от 46 до 88%. С 2011 г. для приготовления парэнтерального питания (ПП), дозирования антибиотиков и разведения препаратов для химиотерапии используется технология компаундинга. Целью работы было сравнение аппаратного приготовления парэнтерального питания методом компаундинга с «флаконной» методикой – использование нескольких флаконов с нутриентами, и заполнением мешков вручную.
Пациенты и методы
В 2018 году на базе НИИ «Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой» для приготовления парэнтерального питания 13 пациентам использован метод – компаундинга. Характеристика пациентов. Медиана возраста – 10 лет (от 11 мес. до 45 лет), 7 женщин и 6 мужчин. Основной диагноз: ОЛЛ – 38,5% (n=5), ОМЛ – 30,8%(n=4), МДС – 23,1%(n=3), ХМЛ – 7,7%(n=1). Было приготовлено 13 мешков с питанием с помощью медицинского компаундера, 4 мешка заполнялись вручную, «флаконный» метод парэнтерального питания применяли у 9 пациентов. Проведен подсчет затрачиваемого времени на три способа приготовления парэнтерального питания: технология компаундинга, «флаконная методика» и заполнение мешка вручную. Для исследования стерильности приготавливаемой смеси проводились бактериологические исследования готового раствора. В конце эксперимента проведен опрос медсестер отделения об удобстве использования парэнтерального питания (ПП) приготовленного по технологии компаундинга.
Результаты
Методика компаундинга: на приготовления ПП до 1 л требовалось в среднем 6,5 мин., от 1-1,5 л в 9 мин., на пакет объемом от 1,5 до 2 л требовалось 11 мин., от 2-3 л – 15 мин. На заполнение мешка вручную ушло не менее 25 мин. На приготовление ПП «флаконным» методом затрачивали не менее 15 мин. Все бактериологические тесты смеси для парэнтерального питания приготовленного методом компаундинга были отрицательны. Опрос медсестер отделения показал, что применения готового индивидуального питания – удобно, экономит время и безопасно для пациента.
Выводы
На приготовление парэнтерального питания с помощью медицинского компаундера затрачивается меньше времени, чем на «флаконный» метод или заполнения мешка вручную. ПП, приготовленное методом компаундинга, стерильно и удобно в применении.
Ключевые слова
Парэнтеральное питание, медицинский смеситель, компаундинг, асептика, нозокомиальная инфекция.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(5057) "Введение
Нутриционная поддержка онкологических больных заняла прочную позицию в ряду лечебных мероприятий. По данным отчета Европейского общества парентерального и энтерального питания, частота недостаточности питания у онкологических больных колеблется от 46 до 88%. С 2011 г. для приготовления парэнтерального питания (ПП), дозирования антибиотиков и разведения препаратов для химиотерапии используется технология компаундинга. Целью работы было сравнение аппаратного приготовления парэнтерального питания методом компаундинга с «флаконной» методикой – использование нескольких флаконов с нутриентами, и заполнением мешков вручную.
Пациенты и методы
В 2018 году на базе НИИ «Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой» для приготовления парэнтерального питания 13 пациентам использован метод – компаундинга. Характеристика пациентов. Медиана возраста – 10 лет (от 11 мес. до 45 лет), 7 женщин и 6 мужчин. Основной диагноз: ОЛЛ – 38,5% (n=5), ОМЛ – 30,8%(n=4), МДС – 23,1%(n=3), ХМЛ – 7,7%(n=1). Было приготовлено 13 мешков с питанием с помощью медицинского компаундера, 4 мешка заполнялись вручную, «флаконный» метод парэнтерального питания применяли у 9 пациентов. Проведен подсчет затрачиваемого времени на три способа приготовления парэнтерального питания: технология компаундинга, «флаконная методика» и заполнение мешка вручную. Для исследования стерильности приготавливаемой смеси проводились бактериологические исследования готового раствора. В конце эксперимента проведен опрос медсестер отделения об удобстве использования парэнтерального питания (ПП) приготовленного по технологии компаундинга.
Результаты
Методика компаундинга: на приготовления ПП до 1 л требовалось в среднем 6,5 мин., от 1-1,5 л в 9 мин., на пакет объемом от 1,5 до 2 л требовалось 11 мин., от 2-3 л – 15 мин. На заполнение мешка вручную ушло не менее 25 мин. На приготовление ПП «флаконным» методом затрачивали не менее 15 мин. Все бактериологические тесты смеси для парэнтерального питания приготовленного методом компаундинга были отрицательны. Опрос медсестер отделения показал, что применения готового индивидуального питания – удобно, экономит время и безопасно для пациента.
Выводы
На приготовление парэнтерального питания с помощью медицинского компаундера затрачивается меньше времени, чем на «флаконный» метод или заполнения мешка вручную. ПП, приготовленное методом компаундинга, стерильно и удобно в применении.
Ключевые слова
Парэнтеральное питание, медицинский смеситель, компаундинг, асептика, нозокомиальная инфекция.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20691" ["VALUE"]=> array(2) { ["TEXT"]=> string(375) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(375) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(375) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" } } } [40]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1590" ["~ID"]=> string(4) "1590" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(163) "Ниволумаб для лечения ВИЧ-ассоциированных лимфом с рецидивирущим/рефрактерным течением" ["~NAME"]=> string(163) "Ниволумаб для лечения ВИЧ-ассоциированных лимфом с рецидивирущим/рефрактерным течением" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:42:55" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:42:55" ["DETAIL_PAGE_URL"]=> string(147) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/nivolumab-dlya-lecheniya-vich-assotsiirovannykh-limfom-s-retsidivirushchim-refrakternym-techeniem/" ["~DETAIL_PAGE_URL"]=> string(147) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/nivolumab-dlya-lecheniya-vich-assotsiirovannykh-limfom-s-retsidivirushchim-refrakternym-techeniem/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(97) "nivolumab-dlya-lecheniya-vich-assotsiirovannykh-limfom-s-retsidivirushchim-refrakternym-techeniem" ["~CODE"]=> string(97) "nivolumab-dlya-lecheniya-vich-assotsiirovannykh-limfom-s-retsidivirushchim-refrakternym-techeniem" ["EXTERNAL_ID"]=> string(4) "1590" ["~EXTERNAL_ID"]=> string(4) "1590" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(163) "Ниволумаб для лечения ВИЧ-ассоциированных лимфом с рецидивирущим/рефрактерным течением" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(241) "Ниволумаб для лечения ВИЧ-ассоциированных лимфом с рецидивирущим/рефрактерным течениемNivolumab treatment in patients with relapsed/refractory HIV-related lymphomas" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(9283) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> ВИЧ-инфекция ассоциирована с увеличением риска развития опухолей, включая лимфому Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на применение современной антиретровирусной терапии (АРВТ). Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать стандартную терапию, включая высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [1]. Ниволумаб это новая опция для терапии спасения у пациентов с рецидивирующими/рефрактерными (р/р) течением ЛХ и НХЛ, но эффективность и безопасность использования этого препарата у ВИЧ-инфицированных пациентов остается неизвестным. Известно, что ниволумаб обладает не только противоопухолевой активностью, но и способствует снижению вирусной нагрузки при ВИЧ-инфекции [2]. Описано несколько случаев использования ниволумаба для лечения ВИЧ-ассоциированных лимфом [3,4]. В НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой терапия ниволумабом была проведена у 6 пациентов с ВИЧ-ассоциированными ЛХ и НХЛ. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В исследование включены шесть пациентов мужского пола с р/р лимфомами, которые получили терапию ниволумабом в 2017 году. Первичной конечной точкой была оценка ответа на терапию. Вторичные точки – оценка токсичности, частота рецидива и общая выживаемость (ОВ) в течение 12 месяцев от терапии ниволумабом. Common Terminology Criteria for Adverce Events (CTCAE 4.0) были использованы для оценки токсичности и иммуноопосредованных эффектов. Критерии LYRIC использовались для оценки ответа по ПЭТ-КТ. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Основные заболевания в группе исследования были: ЛХ n=4 (66%) и НХЛ, диффузная В-крупноклеточная лимфома (ДБККЛ) n=2 (34%). Медиана количества предшествующих линий терапия – 2 (2-3). Три пациента получали ниволумаб в качестве bridge-терапии перед ауто-ТГСК. После трансплантации ниволумаб был использован у одного пациента, двум пациентам ауто-ТГСК не выполнялась. Два пациента с ЛХ получали ниволумаб в качестве монотерапии, 4 пациента в комбинации с бендамустином и гемцитабином, у одного пациента в комбинацию был добавлен ритуксимаб. Медиана дозы ниволумаба составила 1 мг/кг (0,5-1,5 мг/кг). Медиана количества введений составила 8,5 (2-12). Медиана количества CD4+ клеток – 382 кл/мкл (45-490); 83,3% пациентов получали АРВТ. Один пациент не получал АРВТ из-за острой почечной недостаточности (креатинин 680 мкмоль/л). Только у пяти пациентов можно было объективно оценить ответ на терапию, один пациент умер до проведения ПЭТ-КТ, после 2 курсов терапии ниволумаб. Общий ответ был зарегистрирован в 83,3% случаев. Два – частичная ремиссия у пациентов с лимфомой Ходжкина и три (50%) пациентов с ЛХ и НХЛ имели полный метаболический ответ, один пациент с НХЛ – прогрессирование заболевания (оценен клинически). Значимой токсичности, согласно критериям CTCAE, и иммуноопосредованных эффектов выявлено не было. Рецидив основного заболевания был диагностирован у двух пациентов, время до прогрессирования у пациента с ЛХ составило 485 дней и 266 у пациента с ДБККЛ. ОВ 12 месяцев для ВИЧ-инфицированных пациентов от первого введения ниволумаба составила 83,3%. Пациент с острой почечной недостаточностью, не получавший АРВТ, умер от прогрессирования лимфомы. Основные характеристики пациентов представлены в таблице 1. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> У пациентов с ВИЧ-ассоциированными лимфомами общий ответ на терапию ниволумабом составил 83,3%. Токсичность и иммуноопосредованные эффекты не были зарегистрированы. ОВ в течение 1 года составила 83,3%. Предварительные результаты показывают, что терапия р/р ВИЧ-ассоциированных лимфом ниволумабом – эффективна и безопасна, но необходимо подтверждение в исследованиях в большей популяцией. </p> <h2 style="text-align: justify;">Литература</h2> <p style="text-align: justify;"> 1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cellular Therapy and Transplantation (CTT). Vol. 6, No. 4(21), 2017,-P.42-51<br> 2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. -2018.-Vol. 29.-P.517-518<br> 3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. Journal of Immunotherapy. -2018-Vol.41.-P.379–383<br> 4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIVrelated relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. Journal for ImmunoTherapy of Cancer. -2017-Vol.20.-P.49 </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Иммунотерапия, ВИЧ-ассоциированные лимфомы, ниволумаб, ВИЧ, рецидивирущее/рефрактерное течение лимфомы Ходжкина, неходжкинская лимфома, ответ на терапию, частота рецидивов, токсичность, высокодозная химиотерапия, аутологичная трансплантация гемопоэтических стволовых клеток, общая выживаемость. </p> <h2>Таблица 1. Характеристика пациентов, леченных ниволумабом</h2> <img width="783" alt="41_таблица1.png" src="/upload/medialibrary/86d/41_tablitsa1.png" height="367" title="41_таблица1.png"><br>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(163) "Ниволумаб для лечения ВИЧ-ассоциированных лимфом с рецидивирущим/рефрактерным течением" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(163) "Ниволумаб для лечения ВИЧ-ассоциированных лимфом с рецидивирущим/рефрактерным течением" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(163) "Ниволумаб для лечения ВИЧ-ассоциированных лимфом с рецидивирущим/рефрактерным течением" ["SECTION_META_TITLE"]=> string(163) "Ниволумаб для лечения ВИЧ-ассоциированных лимфом с рецидивирущим/рефрактерным течением" ["SECTION_META_KEYWORDS"]=> string(163) "Ниволумаб для лечения ВИЧ-ассоциированных лимфом с рецидивирущим/рефрактерным течением" ["SECTION_META_DESCRIPTION"]=> string(163) "Ниволумаб для лечения ВИЧ-ассоциированных лимфом с рецидивирущим/рефрактерным течением" ["SECTION_PICTURE_FILE_ALT"]=> string(163) "Ниволумаб для лечения ВИЧ-ассоциированных лимфом с рецидивирущим/рефрактерным течением" ["SECTION_PICTURE_FILE_TITLE"]=> string(163) "Ниволумаб для лечения ВИЧ-ассоциированных лимфом с рецидивирущим/рефрактерным течением" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "nivolumab-dlya-lecheniya-vich-assotsiirovannykh-limfom-s-retsidivirushchim-refrakternym-techeniem-im" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(163) "Ниволумаб для лечения ВИЧ-ассоциированных лимфом с рецидивирущим/рефрактерным течением" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(163) "Ниволумаб для лечения ВИЧ-ассоциированных лимфом с рецидивирущим/рефрактерным течением" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "nivolumab-dlya-lecheniya-vich-assotsiirovannykh-limfom-s-retsidivirushchim-refrakternym-techeniem-im" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "nivolumab-dlya-lecheniya-vich-assotsiirovannykh-limfom-s-retsidivirushchim-refrakternym-techeniem-im" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "nivolumab-dlya-lecheniya-vich-assotsiirovannykh-limfom-s-retsidivirushchim-refrakternym-techeniem-im" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20634" ["VALUE"]=> array(2) { ["TEXT"]=> string(367) "Юлия А. Рогачева, Марина О. Попова, Анастасия В. Некрасова, Иван В. Цыганков, Кирилл В. Лепик, Лилия В. Стельмах, Иван С. Моисеев, Сергей Н. Бондаренко, Наталья Б. Михайлова, Вадим В. Байков, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(367) "Юлия А. Рогачева, Марина О. Попова, Анастасия В. Некрасова, Иван В. Цыганков, Кирилл В. Лепик, Лилия В. Стельмах, Иван С. Моисеев, Сергей Н. Бондаренко, Наталья Б. Михайлова, Вадим В. Байков, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20635" ["VALUE"]=> array(2) { ["TEXT"]=> string(491) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; кафедра гематологии, транcфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(485) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; кафедра гематологии, транcфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20636" ["VALUE"]=> array(2) { ["TEXT"]=> string(9283) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> ВИЧ-инфекция ассоциирована с увеличением риска развития опухолей, включая лимфому Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на применение современной антиретровирусной терапии (АРВТ). Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать стандартную терапию, включая высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [1]. Ниволумаб это новая опция для терапии спасения у пациентов с рецидивирующими/рефрактерными (р/р) течением ЛХ и НХЛ, но эффективность и безопасность использования этого препарата у ВИЧ-инфицированных пациентов остается неизвестным. Известно, что ниволумаб обладает не только противоопухолевой активностью, но и способствует снижению вирусной нагрузки при ВИЧ-инфекции [2]. Описано несколько случаев использования ниволумаба для лечения ВИЧ-ассоциированных лимфом [3,4]. В НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой терапия ниволумабом была проведена у 6 пациентов с ВИЧ-ассоциированными ЛХ и НХЛ. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В исследование включены шесть пациентов мужского пола с р/р лимфомами, которые получили терапию ниволумабом в 2017 году. Первичной конечной точкой была оценка ответа на терапию. Вторичные точки – оценка токсичности, частота рецидива и общая выживаемость (ОВ) в течение 12 месяцев от терапии ниволумабом. Common Terminology Criteria for Adverce Events (CTCAE 4.0) были использованы для оценки токсичности и иммуноопосредованных эффектов. Критерии LYRIC использовались для оценки ответа по ПЭТ-КТ. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Основные заболевания в группе исследования были: ЛХ n=4 (66%) и НХЛ, диффузная В-крупноклеточная лимфома (ДБККЛ) n=2 (34%). Медиана количества предшествующих линий терапия – 2 (2-3). Три пациента получали ниволумаб в качестве bridge-терапии перед ауто-ТГСК. После трансплантации ниволумаб был использован у одного пациента, двум пациентам ауто-ТГСК не выполнялась. Два пациента с ЛХ получали ниволумаб в качестве монотерапии, 4 пациента в комбинации с бендамустином и гемцитабином, у одного пациента в комбинацию был добавлен ритуксимаб. Медиана дозы ниволумаба составила 1 мг/кг (0,5-1,5 мг/кг). Медиана количества введений составила 8,5 (2-12). Медиана количества CD4+ клеток – 382 кл/мкл (45-490); 83,3% пациентов получали АРВТ. Один пациент не получал АРВТ из-за острой почечной недостаточности (креатинин 680 мкмоль/л). Только у пяти пациентов можно было объективно оценить ответ на терапию, один пациент умер до проведения ПЭТ-КТ, после 2 курсов терапии ниволумаб. Общий ответ был зарегистрирован в 83,3% случаев. Два – частичная ремиссия у пациентов с лимфомой Ходжкина и три (50%) пациентов с ЛХ и НХЛ имели полный метаболический ответ, один пациент с НХЛ – прогрессирование заболевания (оценен клинически). Значимой токсичности, согласно критериям CTCAE, и иммуноопосредованных эффектов выявлено не было. Рецидив основного заболевания был диагностирован у двух пациентов, время до прогрессирования у пациента с ЛХ составило 485 дней и 266 у пациента с ДБККЛ. ОВ 12 месяцев для ВИЧ-инфицированных пациентов от первого введения ниволумаба составила 83,3%. Пациент с острой почечной недостаточностью, не получавший АРВТ, умер от прогрессирования лимфомы. Основные характеристики пациентов представлены в таблице 1. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> У пациентов с ВИЧ-ассоциированными лимфомами общий ответ на терапию ниволумабом составил 83,3%. Токсичность и иммуноопосредованные эффекты не были зарегистрированы. ОВ в течение 1 года составила 83,3%. Предварительные результаты показывают, что терапия р/р ВИЧ-ассоциированных лимфом ниволумабом – эффективна и безопасна, но необходимо подтверждение в исследованиях в большей популяцией. </p> <h2 style="text-align: justify;">Литература</h2> <p style="text-align: justify;"> 1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cellular Therapy and Transplantation (CTT). Vol. 6, No. 4(21), 2017,-P.42-51<br> 2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. -2018.-Vol. 29.-P.517-518<br> 3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. Journal of Immunotherapy. -2018-Vol.41.-P.379–383<br> 4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIVrelated relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. Journal for ImmunoTherapy of Cancer. -2017-Vol.20.-P.49 </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Иммунотерапия, ВИЧ-ассоциированные лимфомы, ниволумаб, ВИЧ, рецидивирущее/рефрактерное течение лимфомы Ходжкина, неходжкинская лимфома, ответ на терапию, частота рецидивов, токсичность, высокодозная химиотерапия, аутологичная трансплантация гемопоэтических стволовых клеток, общая выживаемость. </p> <h2>Таблица 1. Характеристика пациентов, леченных ниволумабом</h2> <img width="783" alt="41_таблица1.png" src="/upload/medialibrary/86d/41_tablitsa1.png" height="367" title="41_таблица1.png"><br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(8915) "
Введение
ВИЧ-инфекция ассоциирована с увеличением риска развития опухолей, включая лимфому Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на применение современной антиретровирусной терапии (АРВТ). Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать стандартную терапию, включая высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [1]. Ниволумаб это новая опция для терапии спасения у пациентов с рецидивирующими/рефрактерными (р/р) течением ЛХ и НХЛ, но эффективность и безопасность использования этого препарата у ВИЧ-инфицированных пациентов остается неизвестным. Известно, что ниволумаб обладает не только противоопухолевой активностью, но и способствует снижению вирусной нагрузки при ВИЧ-инфекции [2]. Описано несколько случаев использования ниволумаба для лечения ВИЧ-ассоциированных лимфом [3,4]. В НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой терапия ниволумабом была проведена у 6 пациентов с ВИЧ-ассоциированными ЛХ и НХЛ.
Материалы и методы
В исследование включены шесть пациентов мужского пола с р/р лимфомами, которые получили терапию ниволумабом в 2017 году. Первичной конечной точкой была оценка ответа на терапию. Вторичные точки – оценка токсичности, частота рецидива и общая выживаемость (ОВ) в течение 12 месяцев от терапии ниволумабом. Common Terminology Criteria for Adverce Events (CTCAE 4.0) были использованы для оценки токсичности и иммуноопосредованных эффектов. Критерии LYRIC использовались для оценки ответа по ПЭТ-КТ.
Результаты
Основные заболевания в группе исследования были: ЛХ n=4 (66%) и НХЛ, диффузная В-крупноклеточная лимфома (ДБККЛ) n=2 (34%). Медиана количества предшествующих линий терапия – 2 (2-3). Три пациента получали ниволумаб в качестве bridge-терапии перед ауто-ТГСК. После трансплантации ниволумаб был использован у одного пациента, двум пациентам ауто-ТГСК не выполнялась. Два пациента с ЛХ получали ниволумаб в качестве монотерапии, 4 пациента в комбинации с бендамустином и гемцитабином, у одного пациента в комбинацию был добавлен ритуксимаб. Медиана дозы ниволумаба составила 1 мг/кг (0,5-1,5 мг/кг). Медиана количества введений составила 8,5 (2-12). Медиана количества CD4+ клеток – 382 кл/мкл (45-490); 83,3% пациентов получали АРВТ. Один пациент не получал АРВТ из-за острой почечной недостаточности (креатинин 680 мкмоль/л). Только у пяти пациентов можно было объективно оценить ответ на терапию, один пациент умер до проведения ПЭТ-КТ, после 2 курсов терапии ниволумаб. Общий ответ был зарегистрирован в 83,3% случаев. Два – частичная ремиссия у пациентов с лимфомой Ходжкина и три (50%) пациентов с ЛХ и НХЛ имели полный метаболический ответ, один пациент с НХЛ – прогрессирование заболевания (оценен клинически). Значимой токсичности, согласно критериям CTCAE, и иммуноопосредованных эффектов выявлено не было. Рецидив основного заболевания был диагностирован у двух пациентов, время до прогрессирования у пациента с ЛХ составило 485 дней и 266 у пациента с ДБККЛ. ОВ 12 месяцев для ВИЧ-инфицированных пациентов от первого введения ниволумаба составила 83,3%. Пациент с острой почечной недостаточностью, не получавший АРВТ, умер от прогрессирования лимфомы. Основные характеристики пациентов представлены в таблице 1.
Выводы
У пациентов с ВИЧ-ассоциированными лимфомами общий ответ на терапию ниволумабом составил 83,3%. Токсичность и иммуноопосредованные эффекты не были зарегистрированы. ОВ в течение 1 года составила 83,3%. Предварительные результаты показывают, что терапия р/р ВИЧ-ассоциированных лимфом ниволумабом – эффективна и безопасна, но необходимо подтверждение в исследованиях в большей популяцией.
Литература
1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cellular Therapy and Transplantation (CTT). Vol. 6, No. 4(21), 2017,-P.42-51
2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. -2018.-Vol. 29.-P.517-518
3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. Journal of Immunotherapy. -2018-Vol.41.-P.379–383
4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIVrelated relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. Journal for ImmunoTherapy of Cancer. -2017-Vol.20.-P.49
Ключевые слова
Иммунотерапия, ВИЧ-ассоциированные лимфомы, ниволумаб, ВИЧ, рецидивирущее/рефрактерное течение лимфомы Ходжкина, неходжкинская лимфома, ответ на терапию, частота рецидивов, токсичность, высокодозная химиотерапия, аутологичная трансплантация гемопоэтических стволовых клеток, общая выживаемость.
Таблица 1. Характеристика пациентов, леченных ниволумабом

" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20637" ["VALUE"]=> array(2) { ["TEXT"]=> string(214) "Yulia A. Rogacheva, Marina O. Popova, Anastasia V. Nekrasova, Ivan V. Tsygankov, Kirill V. Lepik, Lilia V. Stelmakh, Ivan S. Moiseev, Sergey N. Bondarenko, Natalia B. Mikhaylova, Vadim V. Baykov, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(214) "Yulia A. Rogacheva, Marina O. Popova, Anastasia V. Nekrasova, Ivan V. Tsygankov, Kirill V. Lepik, Lilia V. Stelmakh, Ivan S. Moiseev, Sergey N. Bondarenko, Natalia B. Mikhaylova, Vadim V. Baykov, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20638" ["VALUE"]=> array(2) { ["TEXT"]=> string(240) "Raisa Gorbacheva Research Institute of Children Oncology, Hematology and Transplantation; Chair of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(234) "Raisa Gorbacheva Research Institute of Children Oncology, Hematology and Transplantation; Chair of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20639" ["VALUE"]=> array(2) { ["TEXT"]=> string(6015) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Infection with HIV is associated with a significantly increased risk of cancer, including Hodgkin lymphoma (HL) and non-Hodgkin lymphoma (NHL) even when patients are treated successfully with modern combination anti-retroviral therapy (cART). Immune preservation with cART has changed the therapeutic approach to HIV-related lymphoma, allowing the use standard chemotherapy, including high dose chemotherapy with autologous hematopoietic stem cell transplantation (ASCT) [1]. Nivolumab is a salvage option in relapsed/refractory (r/r) HL and NHL, but efficacy and safety in patients with HIV infection are still unknown. Patients with HIV-related lymphoma may benefit not only anticancer activity of nivolumab, but also from its potential anti-HIV effect [2]. Just a few cases of HIV-related lymphoma treated with nivolumab were reported [3, 4]. We describe a case series of r/r HIV-related lymphoma receiving nivolumab in Raisa Gorbacheva Institute of Children Oncology, Haematology and Transplantation, First Pavlov State Medical University of Saint-Petersburg. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Six male patients with r/r HIV-related lymphoma were treated with nivolumab in 2017. Clinical response to therapy was the primary endpoint. Secondary endpoints were determined by toxicity, relapse incidence and overall survival (OS) at 12 months after first nivolumab infusion. Common Terminology Criteria for Adverse Events (CTCAE v4.03) for the toxicity analysis and immune-related adverse effects have been used. LYRIC criteria for assessing FDG-PET/CT were applied. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The underlying diseases in the patients observed were as follows: HL was registered in four cases (66%), whereas NHL and diffuse large B-cell lymphoma (DLBCL) were diagnosed in two remaining patients (34%). Median number of prior lines of therapy was 2 (range, 2-3). Three patients received nivolumab as a bridge to ASCT. Relapse after ASCT was treated in one patient, two patients didn’t proceed to ASCT. Two patients with HL received nivolumab as monotherapy, 4 patients were subject to nivolumab in combination with bendamustine and gemcitabine, including one patient receiving supplemental treatment with rituximab. The median dose of nivolumab was 1 mg/kg (range, 0.5-1.5 mg/kg). The median number of nivolumab doses received was 8.5 (range, 2-12). The median number of CD4+ cells was 382 cells/μl (range, 45-490); 83.3% patients were on cART. One patient didn’t received cART due acute renal failure (creatinine 680 mcM). Only 5 patients were available for objective response estimation, one of them died before PET/CT study was performed. Overall response rate was 83.3%. Of those, partial remission was shown in two HL patients; three patients with HL and NHL (50% of total) had complete metabolic responses, and one patient with NHL developed the disease progression, as clinically assessed. Toxicity according to CTCAE and any immune-related adverse effects were not registered. Relapse of the underlying disease was diagnosed in 2 patients, time to progression for those patients were 485 days (HL) and 266 days (DLBCL). Overall survival (OS) at 12 months for the patients with HIV (n=6) from the time of nivolumab therapy was 83.3%. The patient who didn’t receive cART and developed acute renal failure died from the progression of lymphoma. Summary of patients are outlined on table 1. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Overall response rate in patients with HIV-related lymphomas was 83.3%. Toxicity and immune-related adverse effects were not registered. One-year overall survival in patients with HIV-related lymphoma was 83.3%. Preliminary data suggest that nivolumab is an effective and safe treatment option for r/r HIV-related lymphoma, but needs to be confirmed in larger studies. </p> <h2 style="text-align: justify;">References</h2> <p style="text-align: justify;"> 1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cell Ther Transplant (CTT). 2017; 6(4):42-51.<br> 2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. 2018; 29:517-518.<br> 3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. J Immunother. 2018; 41:379–383.<br> 4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIV-related relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. J Immunother Cancer. 2017;20:49. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Immunotherapy, HIV-related lymphoma, nivolumab, HIV, relapsed/refractory Hodgkin lymphoma, non-Hodgkin lymphoma, response to therapy, relapse incidence, toxicity, high-dose chemotherapy, autologous hematopoietic stem cell transplantation, overall survival. </p> <h2 style="text-align: justify;">Table 1. Some clinical characteristics of HIV patients treated with Nivolumab</h2> <p style="text-align: justify;"> <img width="780" alt="41_table_1.png" src="/upload/medialibrary/15b/41_table_1.png" height="404" title="41_table_1.png"> </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(5621) "
Introduction
Infection with HIV is associated with a significantly increased risk of cancer, including Hodgkin lymphoma (HL) and non-Hodgkin lymphoma (NHL) even when patients are treated successfully with modern combination anti-retroviral therapy (cART). Immune preservation with cART has changed the therapeutic approach to HIV-related lymphoma, allowing the use standard chemotherapy, including high dose chemotherapy with autologous hematopoietic stem cell transplantation (ASCT) [1]. Nivolumab is a salvage option in relapsed/refractory (r/r) HL and NHL, but efficacy and safety in patients with HIV infection are still unknown. Patients with HIV-related lymphoma may benefit not only anticancer activity of nivolumab, but also from its potential anti-HIV effect [2]. Just a few cases of HIV-related lymphoma treated with nivolumab were reported [3, 4]. We describe a case series of r/r HIV-related lymphoma receiving nivolumab in Raisa Gorbacheva Institute of Children Oncology, Haematology and Transplantation, First Pavlov State Medical University of Saint-Petersburg.
Patients and methods
Six male patients with r/r HIV-related lymphoma were treated with nivolumab in 2017. Clinical response to therapy was the primary endpoint. Secondary endpoints were determined by toxicity, relapse incidence and overall survival (OS) at 12 months after first nivolumab infusion. Common Terminology Criteria for Adverse Events (CTCAE v4.03) for the toxicity analysis and immune-related adverse effects have been used. LYRIC criteria for assessing FDG-PET/CT were applied.
Results
The underlying diseases in the patients observed were as follows: HL was registered in four cases (66%), whereas NHL and diffuse large B-cell lymphoma (DLBCL) were diagnosed in two remaining patients (34%). Median number of prior lines of therapy was 2 (range, 2-3). Three patients received nivolumab as a bridge to ASCT. Relapse after ASCT was treated in one patient, two patients didn’t proceed to ASCT. Two patients with HL received nivolumab as monotherapy, 4 patients were subject to nivolumab in combination with bendamustine and gemcitabine, including one patient receiving supplemental treatment with rituximab. The median dose of nivolumab was 1 mg/kg (range, 0.5-1.5 mg/kg). The median number of nivolumab doses received was 8.5 (range, 2-12). The median number of CD4+ cells was 382 cells/μl (range, 45-490); 83.3% patients were on cART. One patient didn’t received cART due acute renal failure (creatinine 680 mcM). Only 5 patients were available for objective response estimation, one of them died before PET/CT study was performed. Overall response rate was 83.3%. Of those, partial remission was shown in two HL patients; three patients with HL and NHL (50% of total) had complete metabolic responses, and one patient with NHL developed the disease progression, as clinically assessed. Toxicity according to CTCAE and any immune-related adverse effects were not registered. Relapse of the underlying disease was diagnosed in 2 patients, time to progression for those patients were 485 days (HL) and 266 days (DLBCL). Overall survival (OS) at 12 months for the patients with HIV (n=6) from the time of nivolumab therapy was 83.3%. The patient who didn’t receive cART and developed acute renal failure died from the progression of lymphoma. Summary of patients are outlined on table 1.
Conclusion
Overall response rate in patients with HIV-related lymphomas was 83.3%. Toxicity and immune-related adverse effects were not registered. One-year overall survival in patients with HIV-related lymphoma was 83.3%. Preliminary data suggest that nivolumab is an effective and safe treatment option for r/r HIV-related lymphoma, but needs to be confirmed in larger studies.
References
1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cell Ther Transplant (CTT). 2017; 6(4):42-51.
2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. 2018; 29:517-518.
3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. J Immunother. 2018; 41:379–383.
4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIV-related relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. J Immunother Cancer. 2017;20:49.
Keywords
Immunotherapy, HIV-related lymphoma, nivolumab, HIV, relapsed/refractory Hodgkin lymphoma, non-Hodgkin lymphoma, response to therapy, relapse incidence, toxicity, high-dose chemotherapy, autologous hematopoietic stem cell transplantation, overall survival.
Table 1. Some clinical characteristics of HIV patients treated with Nivolumab

Introduction
Infection with HIV is associated with a significantly increased risk of cancer, including Hodgkin lymphoma (HL) and non-Hodgkin lymphoma (NHL) even when patients are treated successfully with modern combination anti-retroviral therapy (cART). Immune preservation with cART has changed the therapeutic approach to HIV-related lymphoma, allowing the use standard chemotherapy, including high dose chemotherapy with autologous hematopoietic stem cell transplantation (ASCT) [1]. Nivolumab is a salvage option in relapsed/refractory (r/r) HL and NHL, but efficacy and safety in patients with HIV infection are still unknown. Patients with HIV-related lymphoma may benefit not only anticancer activity of nivolumab, but also from its potential anti-HIV effect [2]. Just a few cases of HIV-related lymphoma treated with nivolumab were reported [3, 4]. We describe a case series of r/r HIV-related lymphoma receiving nivolumab in Raisa Gorbacheva Institute of Children Oncology, Haematology and Transplantation, First Pavlov State Medical University of Saint-Petersburg.
Patients and methods
Six male patients with r/r HIV-related lymphoma were treated with nivolumab in 2017. Clinical response to therapy was the primary endpoint. Secondary endpoints were determined by toxicity, relapse incidence and overall survival (OS) at 12 months after first nivolumab infusion. Common Terminology Criteria for Adverse Events (CTCAE v4.03) for the toxicity analysis and immune-related adverse effects have been used. LYRIC criteria for assessing FDG-PET/CT were applied.
Results
The underlying diseases in the patients observed were as follows: HL was registered in four cases (66%), whereas NHL and diffuse large B-cell lymphoma (DLBCL) were diagnosed in two remaining patients (34%). Median number of prior lines of therapy was 2 (range, 2-3). Three patients received nivolumab as a bridge to ASCT. Relapse after ASCT was treated in one patient, two patients didn’t proceed to ASCT. Two patients with HL received nivolumab as monotherapy, 4 patients were subject to nivolumab in combination with bendamustine and gemcitabine, including one patient receiving supplemental treatment with rituximab. The median dose of nivolumab was 1 mg/kg (range, 0.5-1.5 mg/kg). The median number of nivolumab doses received was 8.5 (range, 2-12). The median number of CD4+ cells was 382 cells/μl (range, 45-490); 83.3% patients were on cART. One patient didn’t received cART due acute renal failure (creatinine 680 mcM). Only 5 patients were available for objective response estimation, one of them died before PET/CT study was performed. Overall response rate was 83.3%. Of those, partial remission was shown in two HL patients; three patients with HL and NHL (50% of total) had complete metabolic responses, and one patient with NHL developed the disease progression, as clinically assessed. Toxicity according to CTCAE and any immune-related adverse effects were not registered. Relapse of the underlying disease was diagnosed in 2 patients, time to progression for those patients were 485 days (HL) and 266 days (DLBCL). Overall survival (OS) at 12 months for the patients with HIV (n=6) from the time of nivolumab therapy was 83.3%. The patient who didn’t receive cART and developed acute renal failure died from the progression of lymphoma. Summary of patients are outlined on table 1.
Conclusion
Overall response rate in patients with HIV-related lymphomas was 83.3%. Toxicity and immune-related adverse effects were not registered. One-year overall survival in patients with HIV-related lymphoma was 83.3%. Preliminary data suggest that nivolumab is an effective and safe treatment option for r/r HIV-related lymphoma, but needs to be confirmed in larger studies.
References
1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cell Ther Transplant (CTT). 2017; 6(4):42-51.
2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. 2018; 29:517-518.
3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. J Immunother. 2018; 41:379–383.
4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIV-related relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. J Immunother Cancer. 2017;20:49.
Keywords
Immunotherapy, HIV-related lymphoma, nivolumab, HIV, relapsed/refractory Hodgkin lymphoma, non-Hodgkin lymphoma, response to therapy, relapse incidence, toxicity, high-dose chemotherapy, autologous hematopoietic stem cell transplantation, overall survival.
Table 1. Some clinical characteristics of HIV patients treated with Nivolumab

Introduction
Infection with HIV is associated with a significantly increased risk of cancer, including Hodgkin lymphoma (HL) and non-Hodgkin lymphoma (NHL) even when patients are treated successfully with modern combination anti-retroviral therapy (cART). Immune preservation with cART has changed the therapeutic approach to HIV-related lymphoma, allowing the use standard chemotherapy, including high dose chemotherapy with autologous hematopoietic stem cell transplantation (ASCT) [1]. Nivolumab is a salvage option in relapsed/refractory (r/r) HL and NHL, but efficacy and safety in patients with HIV infection are still unknown. Patients with HIV-related lymphoma may benefit not only anticancer activity of nivolumab, but also from its potential anti-HIV effect [2]. Just a few cases of HIV-related lymphoma treated with nivolumab were reported [3, 4]. We describe a case series of r/r HIV-related lymphoma receiving nivolumab in Raisa Gorbacheva Institute of Children Oncology, Haematology and Transplantation, First Pavlov State Medical University of Saint-Petersburg.
Patients and methods
Six male patients with r/r HIV-related lymphoma were treated with nivolumab in 2017. Clinical response to therapy was the primary endpoint. Secondary endpoints were determined by toxicity, relapse incidence and overall survival (OS) at 12 months after first nivolumab infusion. Common Terminology Criteria for Adverse Events (CTCAE v4.03) for the toxicity analysis and immune-related adverse effects have been used. LYRIC criteria for assessing FDG-PET/CT were applied.
Results
The underlying diseases in the patients observed were as follows: HL was registered in four cases (66%), whereas NHL and diffuse large B-cell lymphoma (DLBCL) were diagnosed in two remaining patients (34%). Median number of prior lines of therapy was 2 (range, 2-3). Three patients received nivolumab as a bridge to ASCT. Relapse after ASCT was treated in one patient, two patients didn’t proceed to ASCT. Two patients with HL received nivolumab as monotherapy, 4 patients were subject to nivolumab in combination with bendamustine and gemcitabine, including one patient receiving supplemental treatment with rituximab. The median dose of nivolumab was 1 mg/kg (range, 0.5-1.5 mg/kg). The median number of nivolumab doses received was 8.5 (range, 2-12). The median number of CD4+ cells was 382 cells/μl (range, 45-490); 83.3% patients were on cART. One patient didn’t received cART due acute renal failure (creatinine 680 mcM). Only 5 patients were available for objective response estimation, one of them died before PET/CT study was performed. Overall response rate was 83.3%. Of those, partial remission was shown in two HL patients; three patients with HL and NHL (50% of total) had complete metabolic responses, and one patient with NHL developed the disease progression, as clinically assessed. Toxicity according to CTCAE and any immune-related adverse effects were not registered. Relapse of the underlying disease was diagnosed in 2 patients, time to progression for those patients were 485 days (HL) and 266 days (DLBCL). Overall survival (OS) at 12 months for the patients with HIV (n=6) from the time of nivolumab therapy was 83.3%. The patient who didn’t receive cART and developed acute renal failure died from the progression of lymphoma. Summary of patients are outlined on table 1.
Conclusion
Overall response rate in patients with HIV-related lymphomas was 83.3%. Toxicity and immune-related adverse effects were not registered. One-year overall survival in patients with HIV-related lymphoma was 83.3%. Preliminary data suggest that nivolumab is an effective and safe treatment option for r/r HIV-related lymphoma, but needs to be confirmed in larger studies.
References
1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cell Ther Transplant (CTT). 2017; 6(4):42-51.
2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. 2018; 29:517-518.
3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. J Immunother. 2018; 41:379–383.
4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIV-related relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. J Immunother Cancer. 2017;20:49.
Keywords
Immunotherapy, HIV-related lymphoma, nivolumab, HIV, relapsed/refractory Hodgkin lymphoma, non-Hodgkin lymphoma, response to therapy, relapse incidence, toxicity, high-dose chemotherapy, autologous hematopoietic stem cell transplantation, overall survival.
Table 1. Some clinical characteristics of HIV patients treated with Nivolumab

" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(234) "Raisa Gorbacheva Research Institute of Children Oncology, Hematology and Transplantation; Chair of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20634" ["VALUE"]=> array(2) { ["TEXT"]=> string(367) "Юлия А. Рогачева, Марина О. Попова, Анастасия В. Некрасова, Иван В. Цыганков, Кирилл В. Лепик, Лилия В. Стельмах, Иван С. Моисеев, Сергей Н. Бондаренко, Наталья Б. Михайлова, Вадим В. Байков, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(367) "Юлия А. Рогачева, Марина О. Попова, Анастасия В. Некрасова, Иван В. Цыганков, Кирилл В. Лепик, Лилия В. Стельмах, Иван С. Моисеев, Сергей Н. Бондаренко, Наталья Б. Михайлова, Вадим В. Байков, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(367) "Юлия А. Рогачева, Марина О. Попова, Анастасия В. Некрасова, Иван В. Цыганков, Кирилл В. Лепик, Лилия В. Стельмах, Иван С. Моисеев, Сергей Н. Бондаренко, Наталья Б. Михайлова, Вадим В. Байков, Борис В. Афанасьев" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20636" ["VALUE"]=> array(2) { ["TEXT"]=> string(9283) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> ВИЧ-инфекция ассоциирована с увеличением риска развития опухолей, включая лимфому Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на применение современной антиретровирусной терапии (АРВТ). Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать стандартную терапию, включая высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [1]. Ниволумаб это новая опция для терапии спасения у пациентов с рецидивирующими/рефрактерными (р/р) течением ЛХ и НХЛ, но эффективность и безопасность использования этого препарата у ВИЧ-инфицированных пациентов остается неизвестным. Известно, что ниволумаб обладает не только противоопухолевой активностью, но и способствует снижению вирусной нагрузки при ВИЧ-инфекции [2]. Описано несколько случаев использования ниволумаба для лечения ВИЧ-ассоциированных лимфом [3,4]. В НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой терапия ниволумабом была проведена у 6 пациентов с ВИЧ-ассоциированными ЛХ и НХЛ. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В исследование включены шесть пациентов мужского пола с р/р лимфомами, которые получили терапию ниволумабом в 2017 году. Первичной конечной точкой была оценка ответа на терапию. Вторичные точки – оценка токсичности, частота рецидива и общая выживаемость (ОВ) в течение 12 месяцев от терапии ниволумабом. Common Terminology Criteria for Adverce Events (CTCAE 4.0) были использованы для оценки токсичности и иммуноопосредованных эффектов. Критерии LYRIC использовались для оценки ответа по ПЭТ-КТ. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Основные заболевания в группе исследования были: ЛХ n=4 (66%) и НХЛ, диффузная В-крупноклеточная лимфома (ДБККЛ) n=2 (34%). Медиана количества предшествующих линий терапия – 2 (2-3). Три пациента получали ниволумаб в качестве bridge-терапии перед ауто-ТГСК. После трансплантации ниволумаб был использован у одного пациента, двум пациентам ауто-ТГСК не выполнялась. Два пациента с ЛХ получали ниволумаб в качестве монотерапии, 4 пациента в комбинации с бендамустином и гемцитабином, у одного пациента в комбинацию был добавлен ритуксимаб. Медиана дозы ниволумаба составила 1 мг/кг (0,5-1,5 мг/кг). Медиана количества введений составила 8,5 (2-12). Медиана количества CD4+ клеток – 382 кл/мкл (45-490); 83,3% пациентов получали АРВТ. Один пациент не получал АРВТ из-за острой почечной недостаточности (креатинин 680 мкмоль/л). Только у пяти пациентов можно было объективно оценить ответ на терапию, один пациент умер до проведения ПЭТ-КТ, после 2 курсов терапии ниволумаб. Общий ответ был зарегистрирован в 83,3% случаев. Два – частичная ремиссия у пациентов с лимфомой Ходжкина и три (50%) пациентов с ЛХ и НХЛ имели полный метаболический ответ, один пациент с НХЛ – прогрессирование заболевания (оценен клинически). Значимой токсичности, согласно критериям CTCAE, и иммуноопосредованных эффектов выявлено не было. Рецидив основного заболевания был диагностирован у двух пациентов, время до прогрессирования у пациента с ЛХ составило 485 дней и 266 у пациента с ДБККЛ. ОВ 12 месяцев для ВИЧ-инфицированных пациентов от первого введения ниволумаба составила 83,3%. Пациент с острой почечной недостаточностью, не получавший АРВТ, умер от прогрессирования лимфомы. Основные характеристики пациентов представлены в таблице 1. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> У пациентов с ВИЧ-ассоциированными лимфомами общий ответ на терапию ниволумабом составил 83,3%. Токсичность и иммуноопосредованные эффекты не были зарегистрированы. ОВ в течение 1 года составила 83,3%. Предварительные результаты показывают, что терапия р/р ВИЧ-ассоциированных лимфом ниволумабом – эффективна и безопасна, но необходимо подтверждение в исследованиях в большей популяцией. </p> <h2 style="text-align: justify;">Литература</h2> <p style="text-align: justify;"> 1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cellular Therapy and Transplantation (CTT). Vol. 6, No. 4(21), 2017,-P.42-51<br> 2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. -2018.-Vol. 29.-P.517-518<br> 3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. Journal of Immunotherapy. -2018-Vol.41.-P.379–383<br> 4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIVrelated relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. Journal for ImmunoTherapy of Cancer. -2017-Vol.20.-P.49 </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Иммунотерапия, ВИЧ-ассоциированные лимфомы, ниволумаб, ВИЧ, рецидивирущее/рефрактерное течение лимфомы Ходжкина, неходжкинская лимфома, ответ на терапию, частота рецидивов, токсичность, высокодозная химиотерапия, аутологичная трансплантация гемопоэтических стволовых клеток, общая выживаемость. </p> <h2>Таблица 1. Характеристика пациентов, леченных ниволумабом</h2> <img width="783" alt="41_таблица1.png" src="/upload/medialibrary/86d/41_tablitsa1.png" height="367" title="41_таблица1.png"><br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(8915) "
Введение
ВИЧ-инфекция ассоциирована с увеличением риска развития опухолей, включая лимфому Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на применение современной антиретровирусной терапии (АРВТ). Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать стандартную терапию, включая высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [1]. Ниволумаб это новая опция для терапии спасения у пациентов с рецидивирующими/рефрактерными (р/р) течением ЛХ и НХЛ, но эффективность и безопасность использования этого препарата у ВИЧ-инфицированных пациентов остается неизвестным. Известно, что ниволумаб обладает не только противоопухолевой активностью, но и способствует снижению вирусной нагрузки при ВИЧ-инфекции [2]. Описано несколько случаев использования ниволумаба для лечения ВИЧ-ассоциированных лимфом [3,4]. В НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой терапия ниволумабом была проведена у 6 пациентов с ВИЧ-ассоциированными ЛХ и НХЛ.
Материалы и методы
В исследование включены шесть пациентов мужского пола с р/р лимфомами, которые получили терапию ниволумабом в 2017 году. Первичной конечной точкой была оценка ответа на терапию. Вторичные точки – оценка токсичности, частота рецидива и общая выживаемость (ОВ) в течение 12 месяцев от терапии ниволумабом. Common Terminology Criteria for Adverce Events (CTCAE 4.0) были использованы для оценки токсичности и иммуноопосредованных эффектов. Критерии LYRIC использовались для оценки ответа по ПЭТ-КТ.
Результаты
Основные заболевания в группе исследования были: ЛХ n=4 (66%) и НХЛ, диффузная В-крупноклеточная лимфома (ДБККЛ) n=2 (34%). Медиана количества предшествующих линий терапия – 2 (2-3). Три пациента получали ниволумаб в качестве bridge-терапии перед ауто-ТГСК. После трансплантации ниволумаб был использован у одного пациента, двум пациентам ауто-ТГСК не выполнялась. Два пациента с ЛХ получали ниволумаб в качестве монотерапии, 4 пациента в комбинации с бендамустином и гемцитабином, у одного пациента в комбинацию был добавлен ритуксимаб. Медиана дозы ниволумаба составила 1 мг/кг (0,5-1,5 мг/кг). Медиана количества введений составила 8,5 (2-12). Медиана количества CD4+ клеток – 382 кл/мкл (45-490); 83,3% пациентов получали АРВТ. Один пациент не получал АРВТ из-за острой почечной недостаточности (креатинин 680 мкмоль/л). Только у пяти пациентов можно было объективно оценить ответ на терапию, один пациент умер до проведения ПЭТ-КТ, после 2 курсов терапии ниволумаб. Общий ответ был зарегистрирован в 83,3% случаев. Два – частичная ремиссия у пациентов с лимфомой Ходжкина и три (50%) пациентов с ЛХ и НХЛ имели полный метаболический ответ, один пациент с НХЛ – прогрессирование заболевания (оценен клинически). Значимой токсичности, согласно критериям CTCAE, и иммуноопосредованных эффектов выявлено не было. Рецидив основного заболевания был диагностирован у двух пациентов, время до прогрессирования у пациента с ЛХ составило 485 дней и 266 у пациента с ДБККЛ. ОВ 12 месяцев для ВИЧ-инфицированных пациентов от первого введения ниволумаба составила 83,3%. Пациент с острой почечной недостаточностью, не получавший АРВТ, умер от прогрессирования лимфомы. Основные характеристики пациентов представлены в таблице 1.
Выводы
У пациентов с ВИЧ-ассоциированными лимфомами общий ответ на терапию ниволумабом составил 83,3%. Токсичность и иммуноопосредованные эффекты не были зарегистрированы. ОВ в течение 1 года составила 83,3%. Предварительные результаты показывают, что терапия р/р ВИЧ-ассоциированных лимфом ниволумабом – эффективна и безопасна, но необходимо подтверждение в исследованиях в большей популяцией.
Литература
1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cellular Therapy and Transplantation (CTT). Vol. 6, No. 4(21), 2017,-P.42-51
2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. -2018.-Vol. 29.-P.517-518
3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. Journal of Immunotherapy. -2018-Vol.41.-P.379–383
4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIVrelated relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. Journal for ImmunoTherapy of Cancer. -2017-Vol.20.-P.49
Ключевые слова
Иммунотерапия, ВИЧ-ассоциированные лимфомы, ниволумаб, ВИЧ, рецидивирущее/рефрактерное течение лимфомы Ходжкина, неходжкинская лимфома, ответ на терапию, частота рецидивов, токсичность, высокодозная химиотерапия, аутологичная трансплантация гемопоэтических стволовых клеток, общая выживаемость.
Таблица 1. Характеристика пациентов, леченных ниволумабом

" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(8915) "
Введение
ВИЧ-инфекция ассоциирована с увеличением риска развития опухолей, включая лимфому Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на применение современной антиретровирусной терапии (АРВТ). Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать стандартную терапию, включая высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [1]. Ниволумаб это новая опция для терапии спасения у пациентов с рецидивирующими/рефрактерными (р/р) течением ЛХ и НХЛ, но эффективность и безопасность использования этого препарата у ВИЧ-инфицированных пациентов остается неизвестным. Известно, что ниволумаб обладает не только противоопухолевой активностью, но и способствует снижению вирусной нагрузки при ВИЧ-инфекции [2]. Описано несколько случаев использования ниволумаба для лечения ВИЧ-ассоциированных лимфом [3,4]. В НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой терапия ниволумабом была проведена у 6 пациентов с ВИЧ-ассоциированными ЛХ и НХЛ.
Материалы и методы
В исследование включены шесть пациентов мужского пола с р/р лимфомами, которые получили терапию ниволумабом в 2017 году. Первичной конечной точкой была оценка ответа на терапию. Вторичные точки – оценка токсичности, частота рецидива и общая выживаемость (ОВ) в течение 12 месяцев от терапии ниволумабом. Common Terminology Criteria for Adverce Events (CTCAE 4.0) были использованы для оценки токсичности и иммуноопосредованных эффектов. Критерии LYRIC использовались для оценки ответа по ПЭТ-КТ.
Результаты
Основные заболевания в группе исследования были: ЛХ n=4 (66%) и НХЛ, диффузная В-крупноклеточная лимфома (ДБККЛ) n=2 (34%). Медиана количества предшествующих линий терапия – 2 (2-3). Три пациента получали ниволумаб в качестве bridge-терапии перед ауто-ТГСК. После трансплантации ниволумаб был использован у одного пациента, двум пациентам ауто-ТГСК не выполнялась. Два пациента с ЛХ получали ниволумаб в качестве монотерапии, 4 пациента в комбинации с бендамустином и гемцитабином, у одного пациента в комбинацию был добавлен ритуксимаб. Медиана дозы ниволумаба составила 1 мг/кг (0,5-1,5 мг/кг). Медиана количества введений составила 8,5 (2-12). Медиана количества CD4+ клеток – 382 кл/мкл (45-490); 83,3% пациентов получали АРВТ. Один пациент не получал АРВТ из-за острой почечной недостаточности (креатинин 680 мкмоль/л). Только у пяти пациентов можно было объективно оценить ответ на терапию, один пациент умер до проведения ПЭТ-КТ, после 2 курсов терапии ниволумаб. Общий ответ был зарегистрирован в 83,3% случаев. Два – частичная ремиссия у пациентов с лимфомой Ходжкина и три (50%) пациентов с ЛХ и НХЛ имели полный метаболический ответ, один пациент с НХЛ – прогрессирование заболевания (оценен клинически). Значимой токсичности, согласно критериям CTCAE, и иммуноопосредованных эффектов выявлено не было. Рецидив основного заболевания был диагностирован у двух пациентов, время до прогрессирования у пациента с ЛХ составило 485 дней и 266 у пациента с ДБККЛ. ОВ 12 месяцев для ВИЧ-инфицированных пациентов от первого введения ниволумаба составила 83,3%. Пациент с острой почечной недостаточностью, не получавший АРВТ, умер от прогрессирования лимфомы. Основные характеристики пациентов представлены в таблице 1.
Выводы
У пациентов с ВИЧ-ассоциированными лимфомами общий ответ на терапию ниволумабом составил 83,3%. Токсичность и иммуноопосредованные эффекты не были зарегистрированы. ОВ в течение 1 года составила 83,3%. Предварительные результаты показывают, что терапия р/р ВИЧ-ассоциированных лимфом ниволумабом – эффективна и безопасна, но необходимо подтверждение в исследованиях в большей популяцией.
Литература
1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cellular Therapy and Transplantation (CTT). Vol. 6, No. 4(21), 2017,-P.42-51
2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. -2018.-Vol. 29.-P.517-518
3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. Journal of Immunotherapy. -2018-Vol.41.-P.379–383
4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIVrelated relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. Journal for ImmunoTherapy of Cancer. -2017-Vol.20.-P.49
Ключевые слова
Иммунотерапия, ВИЧ-ассоциированные лимфомы, ниволумаб, ВИЧ, рецидивирущее/рефрактерное течение лимфомы Ходжкина, неходжкинская лимфома, ответ на терапию, частота рецидивов, токсичность, высокодозная химиотерапия, аутологичная трансплантация гемопоэтических стволовых клеток, общая выживаемость.
Таблица 1. Характеристика пациентов, леченных ниволумабом

" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20635" ["VALUE"]=> array(2) { ["TEXT"]=> string(491) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; кафедра гематологии, транcфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(485) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; кафедра гематологии, транcфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(485) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; кафедра гематологии, транcфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
" } } } [41]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1589" ["~ID"]=> string(4) "1589" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(178) "Кандидемия у гематологических пациентов после трансплантации гемопоэтических стволовых клеток" ["~NAME"]=> string(178) "Кандидемия у гематологических пациентов после трансплантации гемопоэтических стволовых клеток" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:42:24" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:42:24" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/kandidemiya-u-gematologicheskikh-patsientov-posle-transplantatsii-gemopoeticheskikh-stvolovykh-kleto/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/kandidemiya-u-gematologicheskikh-patsientov-posle-transplantatsii-gemopoeticheskikh-stvolovykh-kleto/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "kandidemiya-u-gematologicheskikh-patsientov-posle-transplantatsii-gemopoeticheskikh-stvolovykh-kleto" ["~CODE"]=> string(100) "kandidemiya-u-gematologicheskikh-patsientov-posle-transplantatsii-gemopoeticheskikh-stvolovykh-kleto" ["EXTERNAL_ID"]=> string(4) "1589" ["~EXTERNAL_ID"]=> string(4) "1589" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(178) "Кандидемия у гематологических пациентов после трансплантации гемопоэтических стволовых клеток" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(260) "Кандидемия у гематологических пациентов после трансплантации гемопоэтических стволовых клетокCandidemia in hematological patients after hematopoietic stem cell transplantation" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(6295) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Инвазивный кандизоз/кандидемия – редкий инвазивный микоз, при этом связан с высоким уровнем летальности у пациентов с гематологическими заболеваниями. Кандидемия особенно часто наблюдается у пациентов, которые госпитализируются на долгий период, получающих химиотерапию (ХТ), трансплантацию гемопоэтических стволовых клеток (ТГСК). Целью нашего исследования было изучить эпидемиологию кандидемии у большой когорты реципиентов гемопоэтических стволовых клеток в течение десятилетнего периода высокой трансплантационной активности НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> 2430 трансплантаций гемопоэтических стволовых клеток выполнены в клинике CIC725 в период с 2008 по 2017 год: 1647 аллогенных ТГСК (алло-ТГСК) и 783 аутологичных ТГСК (ауто-ТГСК). Ретроспективное исследование включает 26 случаев кандидемии у пациентов с гематологическими заболеваниями реципиентов ТГСК. Критерии EORTC/MSG 2008 были использованы для постановки диагноза кандидемии также, как и для оценки ответа на терапию. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Частота кандидемии за 10-летний период у реципиентов ТГСК составила 1%: у пациентов после алло-ТГСК частота составила 1,2%, при ауто-ТГСК – 0,7%. Основным заболеванием у реципиентов ТГСК с кандидемией был острый лейкоз у 65% (n=17) пациентов. Медиана возраста – 10 лет (1 месяц-59 лет). В исследуемой популяции алло-ТГСК была выполнена от неродственного донора у 50% (n=13) пациентов, гапло-ТГСК – 26% (n=6) и ауто-ТГСК – 24% (n=6). Полная ремиссия на момент трансплантации не была достигнута у 27% (n=7) пациентов. Первичная противогрибковая профилактика включала назначение флуконазола – 35% (n=9), эхинокандинов – 15% (n=4), без профилактики ув 23% (n=6) пациентов; в качестве вторичной профилактики был использован вориконазол у 27% (n=7) пациентов. Медиана дня возникновения кандидемии оставила 109 дней после алло-ТГСК (3-1337) и 20 дней (8-33) после ауто-ТГСК. Наиболее частым возбудителем были грибы Candida parapsilosis (38%). Этиология кандидемий представлена на рисунке 1. Фебрильная лихорадка была главным клиническим симптомом. Септический синдром развился в 60% случаев. Общая выживаемость (ОВ) в течение 30 дней от диагностики кандидемии составила 65%. При использовании эхинокандинов в качестве стартовой терапии ОВ в течение 30 дней составила 100%, и 65% у пациентов с применением других противогрибковых препаратов (p=0,09). Удаление центрального венозного катетера (ЦВК) при диагностике кандидемии – единственный фактор, достоверно, улучшающий общую 30-дневную выживаемость (91% vs 17%; р =0,001). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Частота кандидемий у реципиентов ТГСК в течение 10-летнего периода наблюдения составила 1%: 1,2% у пациентов после алло-ТГСК и 0,7% после ауто-ТГСК. Общая 30-дневная выживаемость с момента постановки диагноза составила 65%. Удаление ЦВК улучшает общую выживаемость гематологических пациентов с кандидемией. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Кандидемия, гематологические больные, трансплантация гемопоэтических стволовых клеток, высокодозная химиотерапия, частота, общая выживаемость, эхинокандины, центральный венозный катетер. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(178) "Кандидемия у гематологических пациентов после трансплантации гемопоэтических стволовых клеток" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(178) "Кандидемия у гематологических пациентов после трансплантации гемопоэтических стволовых клеток" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(178) "Кандидемия у гематологических пациентов после трансплантации гемопоэтических стволовых клеток" ["SECTION_META_TITLE"]=> string(178) "Кандидемия у гематологических пациентов после трансплантации гемопоэтических стволовых клеток" ["SECTION_META_KEYWORDS"]=> string(178) "Кандидемия у гематологических пациентов после трансплантации гемопоэтических стволовых клеток" ["SECTION_META_DESCRIPTION"]=> string(178) "Кандидемия у гематологических пациентов после трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_ALT"]=> string(178) "Кандидемия у гематологических пациентов после трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_TITLE"]=> string(178) "Кандидемия у гематологических пациентов после трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "kandidemiya-u-gematologicheskikh-patsientov-posle-transplantatsii-gemopoeticheskikh-stvolovykh-kleto" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(178) "Кандидемия у гематологических пациентов после трансплантации гемопоэтических стволовых клеток" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(178) "Кандидемия у гематологических пациентов после трансплантации гемопоэтических стволовых клеток" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "kandidemiya-u-gematologicheskikh-patsientov-posle-transplantatsii-gemopoeticheskikh-stvolovykh-kleto" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "kandidemiya-u-gematologicheskikh-patsientov-posle-transplantatsii-gemopoeticheskikh-stvolovykh-kleto" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "kandidemiya-u-gematologicheskikh-patsientov-posle-transplantatsii-gemopoeticheskikh-stvolovykh-kleto" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20627" ["VALUE"]=> array(2) { ["TEXT"]=> string(986) "Юлия А. Рогачева <sup>1</sup>, Марина О. Попова <sup>1</sup>, Анастасия С. Фролова <sup>1</sup>, Инна В. Маркова <sup>1</sup>, Алиса Г. Волкова <sup>1</sup>, Кирилл А. Екушев <sup>1</sup>, Ольга Н. Пинегина <sup>1</sup>, Олеся В. Паина <sup>1</sup>, Татьяна А. Быкова <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Мария Д. Владовская <sup>1</sup>, Борис И. Смирнов <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Сергей Н. Бондаренко <sup>1</sup>, Людмила С. Зубаровская <sup>1</sup>, Николай Н. Климко <sup>2</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(782) "Юлия А. Рогачева 1, Марина О. Попова 1, Анастасия С. Фролова 1, Инна В. Маркова 1, Алиса Г. Волкова 1, Кирилл А. Екушев 1, Ольга Н. Пинегина 1, Олеся В. Паина 1, Татьяна А. Быкова 1, Елена И. Дарская 1, Мария Д. Владовская 1, Борис И. Смирнов 1, Иван С. Моисеев 1, Сергей Н. Бондаренко 1, Людмила С. Зубаровская 1, Николай Н. Климко 2, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20628" ["VALUE"]=> array(2) { ["TEXT"]=> string(734) "<sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия<br> <sup>2</sup> ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И. И. Мечникова», Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(698) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
2 ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И. И. Мечникова», Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20629" ["VALUE"]=> array(2) { ["TEXT"]=> string(6295) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Инвазивный кандизоз/кандидемия – редкий инвазивный микоз, при этом связан с высоким уровнем летальности у пациентов с гематологическими заболеваниями. Кандидемия особенно часто наблюдается у пациентов, которые госпитализируются на долгий период, получающих химиотерапию (ХТ), трансплантацию гемопоэтических стволовых клеток (ТГСК). Целью нашего исследования было изучить эпидемиологию кандидемии у большой когорты реципиентов гемопоэтических стволовых клеток в течение десятилетнего периода высокой трансплантационной активности НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> 2430 трансплантаций гемопоэтических стволовых клеток выполнены в клинике CIC725 в период с 2008 по 2017 год: 1647 аллогенных ТГСК (алло-ТГСК) и 783 аутологичных ТГСК (ауто-ТГСК). Ретроспективное исследование включает 26 случаев кандидемии у пациентов с гематологическими заболеваниями реципиентов ТГСК. Критерии EORTC/MSG 2008 были использованы для постановки диагноза кандидемии также, как и для оценки ответа на терапию. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Частота кандидемии за 10-летний период у реципиентов ТГСК составила 1%: у пациентов после алло-ТГСК частота составила 1,2%, при ауто-ТГСК – 0,7%. Основным заболеванием у реципиентов ТГСК с кандидемией был острый лейкоз у 65% (n=17) пациентов. Медиана возраста – 10 лет (1 месяц-59 лет). В исследуемой популяции алло-ТГСК была выполнена от неродственного донора у 50% (n=13) пациентов, гапло-ТГСК – 26% (n=6) и ауто-ТГСК – 24% (n=6). Полная ремиссия на момент трансплантации не была достигнута у 27% (n=7) пациентов. Первичная противогрибковая профилактика включала назначение флуконазола – 35% (n=9), эхинокандинов – 15% (n=4), без профилактики ув 23% (n=6) пациентов; в качестве вторичной профилактики был использован вориконазол у 27% (n=7) пациентов. Медиана дня возникновения кандидемии оставила 109 дней после алло-ТГСК (3-1337) и 20 дней (8-33) после ауто-ТГСК. Наиболее частым возбудителем были грибы Candida parapsilosis (38%). Этиология кандидемий представлена на рисунке 1. Фебрильная лихорадка была главным клиническим симптомом. Септический синдром развился в 60% случаев. Общая выживаемость (ОВ) в течение 30 дней от диагностики кандидемии составила 65%. При использовании эхинокандинов в качестве стартовой терапии ОВ в течение 30 дней составила 100%, и 65% у пациентов с применением других противогрибковых препаратов (p=0,09). Удаление центрального венозного катетера (ЦВК) при диагностике кандидемии – единственный фактор, достоверно, улучшающий общую 30-дневную выживаемость (91% vs 17%; р =0,001). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Частота кандидемий у реципиентов ТГСК в течение 10-летнего периода наблюдения составила 1%: 1,2% у пациентов после алло-ТГСК и 0,7% после ауто-ТГСК. Общая 30-дневная выживаемость с момента постановки диагноза составила 65%. Удаление ЦВК улучшает общую выживаемость гематологических пациентов с кандидемией. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Кандидемия, гематологические больные, трансплантация гемопоэтических стволовых клеток, высокодозная химиотерапия, частота, общая выживаемость, эхинокандины, центральный венозный катетер. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6063) "
Введение
Инвазивный кандизоз/кандидемия – редкий инвазивный микоз, при этом связан с высоким уровнем летальности у пациентов с гематологическими заболеваниями. Кандидемия особенно часто наблюдается у пациентов, которые госпитализируются на долгий период, получающих химиотерапию (ХТ), трансплантацию гемопоэтических стволовых клеток (ТГСК). Целью нашего исследования было изучить эпидемиологию кандидемии у большой когорты реципиентов гемопоэтических стволовых клеток в течение десятилетнего периода высокой трансплантационной активности НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета.
Материалы и методы
2430 трансплантаций гемопоэтических стволовых клеток выполнены в клинике CIC725 в период с 2008 по 2017 год: 1647 аллогенных ТГСК (алло-ТГСК) и 783 аутологичных ТГСК (ауто-ТГСК). Ретроспективное исследование включает 26 случаев кандидемии у пациентов с гематологическими заболеваниями реципиентов ТГСК. Критерии EORTC/MSG 2008 были использованы для постановки диагноза кандидемии также, как и для оценки ответа на терапию.
Результаты
Частота кандидемии за 10-летний период у реципиентов ТГСК составила 1%: у пациентов после алло-ТГСК частота составила 1,2%, при ауто-ТГСК – 0,7%. Основным заболеванием у реципиентов ТГСК с кандидемией был острый лейкоз у 65% (n=17) пациентов. Медиана возраста – 10 лет (1 месяц-59 лет). В исследуемой популяции алло-ТГСК была выполнена от неродственного донора у 50% (n=13) пациентов, гапло-ТГСК – 26% (n=6) и ауто-ТГСК – 24% (n=6). Полная ремиссия на момент трансплантации не была достигнута у 27% (n=7) пациентов. Первичная противогрибковая профилактика включала назначение флуконазола – 35% (n=9), эхинокандинов – 15% (n=4), без профилактики ув 23% (n=6) пациентов; в качестве вторичной профилактики был использован вориконазол у 27% (n=7) пациентов. Медиана дня возникновения кандидемии оставила 109 дней после алло-ТГСК (3-1337) и 20 дней (8-33) после ауто-ТГСК. Наиболее частым возбудителем были грибы Candida parapsilosis (38%). Этиология кандидемий представлена на рисунке 1. Фебрильная лихорадка была главным клиническим симптомом. Септический синдром развился в 60% случаев. Общая выживаемость (ОВ) в течение 30 дней от диагностики кандидемии составила 65%. При использовании эхинокандинов в качестве стартовой терапии ОВ в течение 30 дней составила 100%, и 65% у пациентов с применением других противогрибковых препаратов (p=0,09). Удаление центрального венозного катетера (ЦВК) при диагностике кандидемии – единственный фактор, достоверно, улучшающий общую 30-дневную выживаемость (91% vs 17%; р =0,001).
Заключение
Частота кандидемий у реципиентов ТГСК в течение 10-летнего периода наблюдения составила 1%: 1,2% у пациентов после алло-ТГСК и 0,7% после ауто-ТГСК. Общая 30-дневная выживаемость с момента постановки диагноза составила 65%. Удаление ЦВК улучшает общую выживаемость гематологических пациентов с кандидемией.
Ключевые слова
Кандидемия, гематологические больные, трансплантация гемопоэтических стволовых клеток, высокодозная химиотерапия, частота, общая выживаемость, эхинокандины, центральный венозный катетер.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20630" ["VALUE"]=> array(2) { ["TEXT"]=> string(752) "Yulia A. Rogacheva <sup>1</sup>, Marina O. Popova <sup>1</sup>, Anastasia S. Frolova <sup>1</sup>, Inna V. Markova <sup>1</sup>, Alisa G. Volkova <sup>1</sup>, Kirill A. Ekushev <sup>1</sup>, Olga N. Pinegina <sup>1</sup>, Olesya V. Paina <sup>1</sup>,Tatyana A. Bykova <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Maria D. Vladovskaya <sup>1</sup>, Boris I. Smirnov <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Sergey N. Bondarenko <sup>1</sup>, Ludmila S. Zubarovskaya <sup>1</sup>, Nikolay N. Klimko <sup>2</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(548) "Yulia A. Rogacheva 1, Marina O. Popova 1, Anastasia S. Frolova 1, Inna V. Markova 1, Alisa G. Volkova 1, Kirill A. Ekushev 1, Olga N. Pinegina 1, Olesya V. Paina 1,Tatyana A. Bykova 1, Elena I. Darskaya 1, Maria D. Vladovskaya 1, Boris I. Smirnov 1, Ivan S. Moiseev 1, Sergey N. Bondarenko 1, Ludmila S. Zubarovskaya 1, Nikolay N. Klimko 2, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20631" ["VALUE"]=> array(2) { ["TEXT"]=> string(376) "<sup>1</sup> Raisa Gorbacheva Institute of Children Oncology, Hematology and Transplantation, and Chair of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia<br> <sup>2</sup> I. I. Mechnikov North-Western State Medical University, St. Petersburg, Russia<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(340) "1 Raisa Gorbacheva Institute of Children Oncology, Hematology and Transplantation, and Chair of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia2 I. I. Mechnikov North-Western State Medical University, St. Petersburg, Russia
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20632" ["VALUE"]=> array(2) { ["TEXT"]=> string(4298) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Invasive candidiasis/candidemia is a rare invasive fungal disease, however, associated with high mortality rates in hematological patients. Candidemia has been observed particularly among patients hospitalized for a long periods who have been on chemotherapy, including hematopoietic stem cell transplantation (HSCT). The aim of our study was to estimate epidemiology of candidemia in large HSCT recipients’ cohort for the 10-year period transplant activity in R. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation of First Pavlov State Medical University of St. Petersburg. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> 2430 stem cell transplantations have been performed at our BMT center (CIC 725) between 2008 and 2017 including 1647 allogeneic and 783 autologous HSCTs. A retrospective study included 26 cases of candidemia in the period of time in patients with hematological malignances and non-malignant hematological diseases after HSCT. EORTC/MSG 2008 criteria were used for the diagnosis of proven candidemia as well as to evaluate response to therapy. </p> <h3 style="text-align: justify;">Candida etiology</h3> <p style="text-align: justify;"> <img width="500" alt="40_figure 1.png" src="/upload/medialibrary/e13/40_figure-1.png" title="40_figure 1.png"><br> <span style="font-family: Cuprum, sans-serif; font-size: 26px;">Figure 1. Etiology of candidemia in patients following</span><span style="font-family: Cuprum, sans-serif; font-size: 26px;"> hematopoietic transplantation<br> </span> </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Incidence of candidemia for the 10-year period of high transplant activity was 1%: 1.2% in allo-HSCT recipients (n=20/1647), 0.7%, in auto-HSCTs (6/783). The most frequent underlying diseases were acute leukemias (65%, n=17). The median age was 10 y.o. (range, 1 month to 59 years). In the study population, allo-HSCT from unrelated donors was performed in 50% (n=13); haplo-HSCT, in 26% (n=7), and auto-HSCT, in 24% (n=6). Patients had no complete remission at the moment of HSCT in 27% (n=7). As a primary antifungal prophylaxis, the patients received fluconazole (35%, n=9); echinocandins (15%, n=4). 6 patients (23%) were without specific prophylaxis, and voriconazole was applied as secondary prophylaxis in 27% (n=7). The median term for candidemia registration was 109 days after allo-HSCT (range, 3 to 1337) versus 20 days after auto-HSCT (range, 8-33). Candida parapsilosis was the main pathogen revealed (38% of the cases). Spectrum of different Candida species found is shown in Fig. 1. Febrile fever was the main clinical symptom, whereas septic syndrome developed in 60% of cases. Overall survival (OS) at 30 days from the diagnosis of candidemia was 65%. OS at 30 days in patients with echinocandins as antifungal therapy in first line was 100%, versus 65% in cases with other therapies (p=0.09). Removal of central venous catheter (CVC) was the only factor that significantly improved OS at 30 days after candidemia diagnosis (91% vs 17%, p=0.001). </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> Incidence of candidemia over 10 years of observation was 1%: 1.2% in allo-HSCT recipients, 0.7% after auto-HSCT. Overall survival at 30 days from the diagnosis of candidemia was 65%. Removing the central venous catheter caused OS improvement in hematological patients with candidemia. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Candidemia, hematological patients, hematopoietic stem cell transplantation, high-dose chemotherapy, incidence, overall survival, echinocandins, central venous catheter (CVC). </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3920) "
Introduction
Invasive candidiasis/candidemia is a rare invasive fungal disease, however, associated with high mortality rates in hematological patients. Candidemia has been observed particularly among patients hospitalized for a long periods who have been on chemotherapy, including hematopoietic stem cell transplantation (HSCT). The aim of our study was to estimate epidemiology of candidemia in large HSCT recipients’ cohort for the 10-year period transplant activity in R. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation of First Pavlov State Medical University of St. Petersburg.
Patients and methods
2430 stem cell transplantations have been performed at our BMT center (CIC 725) between 2008 and 2017 including 1647 allogeneic and 783 autologous HSCTs. A retrospective study included 26 cases of candidemia in the period of time in patients with hematological malignances and non-malignant hematological diseases after HSCT. EORTC/MSG 2008 criteria were used for the diagnosis of proven candidemia as well as to evaluate response to therapy.
Candida etiology

Figure 1. Etiology of candidemia in patients following
hematopoietic transplantation
Results
Incidence of candidemia for the 10-year period of high transplant activity was 1%: 1.2% in allo-HSCT recipients (n=20/1647), 0.7%, in auto-HSCTs (6/783). The most frequent underlying diseases were acute leukemias (65%, n=17). The median age was 10 y.o. (range, 1 month to 59 years). In the study population, allo-HSCT from unrelated donors was performed in 50% (n=13); haplo-HSCT, in 26% (n=7), and auto-HSCT, in 24% (n=6). Patients had no complete remission at the moment of HSCT in 27% (n=7). As a primary antifungal prophylaxis, the patients received fluconazole (35%, n=9); echinocandins (15%, n=4). 6 patients (23%) were without specific prophylaxis, and voriconazole was applied as secondary prophylaxis in 27% (n=7). The median term for candidemia registration was 109 days after allo-HSCT (range, 3 to 1337) versus 20 days after auto-HSCT (range, 8-33). Candida parapsilosis was the main pathogen revealed (38% of the cases). Spectrum of different Candida species found is shown in Fig. 1. Febrile fever was the main clinical symptom, whereas septic syndrome developed in 60% of cases. Overall survival (OS) at 30 days from the diagnosis of candidemia was 65%. OS at 30 days in patients with echinocandins as antifungal therapy in first line was 100%, versus 65% in cases with other therapies (p=0.09). Removal of central venous catheter (CVC) was the only factor that significantly improved OS at 30 days after candidemia diagnosis (91% vs 17%, p=0.001).
Conclusions
Incidence of candidemia over 10 years of observation was 1%: 1.2% in allo-HSCT recipients, 0.7% after auto-HSCT. Overall survival at 30 days from the diagnosis of candidemia was 65%. Removing the central venous catheter caused OS improvement in hematological patients with candidemia.
Keywords
Candidemia, hematological patients, hematopoietic stem cell transplantation, high-dose chemotherapy, incidence, overall survival, echinocandins, central venous catheter (CVC).
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20633" ["VALUE"]=> string(82) "Candidemia in hematological patients after hematopoietic stem cell transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(82) "Candidemia in hematological patients after hematopoietic stem cell transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20809" ["VALUE"]=> string(4) "1447" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1447" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20810" ["VALUE"]=> string(4) "1448" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1448" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20630" ["VALUE"]=> array(2) { ["TEXT"]=> string(752) "Yulia A. Rogacheva <sup>1</sup>, Marina O. Popova <sup>1</sup>, Anastasia S. Frolova <sup>1</sup>, Inna V. Markova <sup>1</sup>, Alisa G. Volkova <sup>1</sup>, Kirill A. Ekushev <sup>1</sup>, Olga N. Pinegina <sup>1</sup>, Olesya V. Paina <sup>1</sup>,Tatyana A. Bykova <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Maria D. Vladovskaya <sup>1</sup>, Boris I. Smirnov <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Sergey N. Bondarenko <sup>1</sup>, Ludmila S. Zubarovskaya <sup>1</sup>, Nikolay N. Klimko <sup>2</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(548) "Yulia A. Rogacheva 1, Marina O. Popova 1, Anastasia S. Frolova 1, Inna V. Markova 1, Alisa G. Volkova 1, Kirill A. Ekushev 1, Olga N. Pinegina 1, Olesya V. Paina 1,Tatyana A. Bykova 1, Elena I. Darskaya 1, Maria D. Vladovskaya 1, Boris I. Smirnov 1, Ivan S. Moiseev 1, Sergey N. Bondarenko 1, Ludmila S. Zubarovskaya 1, Nikolay N. Klimko 2, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(548) "Yulia A. Rogacheva 1, Marina O. Popova 1, Anastasia S. Frolova 1, Inna V. Markova 1, Alisa G. Volkova 1, Kirill A. Ekushev 1, Olga N. Pinegina 1, Olesya V. Paina 1,Tatyana A. Bykova 1, Elena I. Darskaya 1, Maria D. Vladovskaya 1, Boris I. Smirnov 1, Ivan S. Moiseev 1, Sergey N. Bondarenko 1, Ludmila S. Zubarovskaya 1, Nikolay N. Klimko 2, Boris V. Afanasyev 1" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20632" ["VALUE"]=> array(2) { ["TEXT"]=> string(4298) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Invasive candidiasis/candidemia is a rare invasive fungal disease, however, associated with high mortality rates in hematological patients. Candidemia has been observed particularly among patients hospitalized for a long periods who have been on chemotherapy, including hematopoietic stem cell transplantation (HSCT). The aim of our study was to estimate epidemiology of candidemia in large HSCT recipients’ cohort for the 10-year period transplant activity in R. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation of First Pavlov State Medical University of St. Petersburg. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> 2430 stem cell transplantations have been performed at our BMT center (CIC 725) between 2008 and 2017 including 1647 allogeneic and 783 autologous HSCTs. A retrospective study included 26 cases of candidemia in the period of time in patients with hematological malignances and non-malignant hematological diseases after HSCT. EORTC/MSG 2008 criteria were used for the diagnosis of proven candidemia as well as to evaluate response to therapy. </p> <h3 style="text-align: justify;">Candida etiology</h3> <p style="text-align: justify;"> <img width="500" alt="40_figure 1.png" src="/upload/medialibrary/e13/40_figure-1.png" title="40_figure 1.png"><br> <span style="font-family: Cuprum, sans-serif; font-size: 26px;">Figure 1. Etiology of candidemia in patients following</span><span style="font-family: Cuprum, sans-serif; font-size: 26px;"> hematopoietic transplantation<br> </span> </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Incidence of candidemia for the 10-year period of high transplant activity was 1%: 1.2% in allo-HSCT recipients (n=20/1647), 0.7%, in auto-HSCTs (6/783). The most frequent underlying diseases were acute leukemias (65%, n=17). The median age was 10 y.o. (range, 1 month to 59 years). In the study population, allo-HSCT from unrelated donors was performed in 50% (n=13); haplo-HSCT, in 26% (n=7), and auto-HSCT, in 24% (n=6). Patients had no complete remission at the moment of HSCT in 27% (n=7). As a primary antifungal prophylaxis, the patients received fluconazole (35%, n=9); echinocandins (15%, n=4). 6 patients (23%) were without specific prophylaxis, and voriconazole was applied as secondary prophylaxis in 27% (n=7). The median term for candidemia registration was 109 days after allo-HSCT (range, 3 to 1337) versus 20 days after auto-HSCT (range, 8-33). Candida parapsilosis was the main pathogen revealed (38% of the cases). Spectrum of different Candida species found is shown in Fig. 1. Febrile fever was the main clinical symptom, whereas septic syndrome developed in 60% of cases. Overall survival (OS) at 30 days from the diagnosis of candidemia was 65%. OS at 30 days in patients with echinocandins as antifungal therapy in first line was 100%, versus 65% in cases with other therapies (p=0.09). Removal of central venous catheter (CVC) was the only factor that significantly improved OS at 30 days after candidemia diagnosis (91% vs 17%, p=0.001). </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> Incidence of candidemia over 10 years of observation was 1%: 1.2% in allo-HSCT recipients, 0.7% after auto-HSCT. Overall survival at 30 days from the diagnosis of candidemia was 65%. Removing the central venous catheter caused OS improvement in hematological patients with candidemia. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Candidemia, hematological patients, hematopoietic stem cell transplantation, high-dose chemotherapy, incidence, overall survival, echinocandins, central venous catheter (CVC). </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3920) "Introduction
Invasive candidiasis/candidemia is a rare invasive fungal disease, however, associated with high mortality rates in hematological patients. Candidemia has been observed particularly among patients hospitalized for a long periods who have been on chemotherapy, including hematopoietic stem cell transplantation (HSCT). The aim of our study was to estimate epidemiology of candidemia in large HSCT recipients’ cohort for the 10-year period transplant activity in R. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation of First Pavlov State Medical University of St. Petersburg.
Patients and methods
2430 stem cell transplantations have been performed at our BMT center (CIC 725) between 2008 and 2017 including 1647 allogeneic and 783 autologous HSCTs. A retrospective study included 26 cases of candidemia in the period of time in patients with hematological malignances and non-malignant hematological diseases after HSCT. EORTC/MSG 2008 criteria were used for the diagnosis of proven candidemia as well as to evaluate response to therapy.
Candida etiology

Figure 1. Etiology of candidemia in patients following
hematopoietic transplantation
Results
Incidence of candidemia for the 10-year period of high transplant activity was 1%: 1.2% in allo-HSCT recipients (n=20/1647), 0.7%, in auto-HSCTs (6/783). The most frequent underlying diseases were acute leukemias (65%, n=17). The median age was 10 y.o. (range, 1 month to 59 years). In the study population, allo-HSCT from unrelated donors was performed in 50% (n=13); haplo-HSCT, in 26% (n=7), and auto-HSCT, in 24% (n=6). Patients had no complete remission at the moment of HSCT in 27% (n=7). As a primary antifungal prophylaxis, the patients received fluconazole (35%, n=9); echinocandins (15%, n=4). 6 patients (23%) were without specific prophylaxis, and voriconazole was applied as secondary prophylaxis in 27% (n=7). The median term for candidemia registration was 109 days after allo-HSCT (range, 3 to 1337) versus 20 days after auto-HSCT (range, 8-33). Candida parapsilosis was the main pathogen revealed (38% of the cases). Spectrum of different Candida species found is shown in Fig. 1. Febrile fever was the main clinical symptom, whereas septic syndrome developed in 60% of cases. Overall survival (OS) at 30 days from the diagnosis of candidemia was 65%. OS at 30 days in patients with echinocandins as antifungal therapy in first line was 100%, versus 65% in cases with other therapies (p=0.09). Removal of central venous catheter (CVC) was the only factor that significantly improved OS at 30 days after candidemia diagnosis (91% vs 17%, p=0.001).
Conclusions
Incidence of candidemia over 10 years of observation was 1%: 1.2% in allo-HSCT recipients, 0.7% after auto-HSCT. Overall survival at 30 days from the diagnosis of candidemia was 65%. Removing the central venous catheter caused OS improvement in hematological patients with candidemia.
Keywords
Candidemia, hematological patients, hematopoietic stem cell transplantation, high-dose chemotherapy, incidence, overall survival, echinocandins, central venous catheter (CVC).
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3920) "Introduction
Invasive candidiasis/candidemia is a rare invasive fungal disease, however, associated with high mortality rates in hematological patients. Candidemia has been observed particularly among patients hospitalized for a long periods who have been on chemotherapy, including hematopoietic stem cell transplantation (HSCT). The aim of our study was to estimate epidemiology of candidemia in large HSCT recipients’ cohort for the 10-year period transplant activity in R. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation of First Pavlov State Medical University of St. Petersburg.
Patients and methods
2430 stem cell transplantations have been performed at our BMT center (CIC 725) between 2008 and 2017 including 1647 allogeneic and 783 autologous HSCTs. A retrospective study included 26 cases of candidemia in the period of time in patients with hematological malignances and non-malignant hematological diseases after HSCT. EORTC/MSG 2008 criteria were used for the diagnosis of proven candidemia as well as to evaluate response to therapy.
Candida etiology

Figure 1. Etiology of candidemia in patients following
hematopoietic transplantation
Results
Incidence of candidemia for the 10-year period of high transplant activity was 1%: 1.2% in allo-HSCT recipients (n=20/1647), 0.7%, in auto-HSCTs (6/783). The most frequent underlying diseases were acute leukemias (65%, n=17). The median age was 10 y.o. (range, 1 month to 59 years). In the study population, allo-HSCT from unrelated donors was performed in 50% (n=13); haplo-HSCT, in 26% (n=7), and auto-HSCT, in 24% (n=6). Patients had no complete remission at the moment of HSCT in 27% (n=7). As a primary antifungal prophylaxis, the patients received fluconazole (35%, n=9); echinocandins (15%, n=4). 6 patients (23%) were without specific prophylaxis, and voriconazole was applied as secondary prophylaxis in 27% (n=7). The median term for candidemia registration was 109 days after allo-HSCT (range, 3 to 1337) versus 20 days after auto-HSCT (range, 8-33). Candida parapsilosis was the main pathogen revealed (38% of the cases). Spectrum of different Candida species found is shown in Fig. 1. Febrile fever was the main clinical symptom, whereas septic syndrome developed in 60% of cases. Overall survival (OS) at 30 days from the diagnosis of candidemia was 65%. OS at 30 days in patients with echinocandins as antifungal therapy in first line was 100%, versus 65% in cases with other therapies (p=0.09). Removal of central venous catheter (CVC) was the only factor that significantly improved OS at 30 days after candidemia diagnosis (91% vs 17%, p=0.001).
Conclusions
Incidence of candidemia over 10 years of observation was 1%: 1.2% in allo-HSCT recipients, 0.7% after auto-HSCT. Overall survival at 30 days from the diagnosis of candidemia was 65%. Removing the central venous catheter caused OS improvement in hematological patients with candidemia.
Keywords
Candidemia, hematological patients, hematopoietic stem cell transplantation, high-dose chemotherapy, incidence, overall survival, echinocandins, central venous catheter (CVC).
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20633" ["VALUE"]=> string(82) "Candidemia in hematological patients after hematopoietic stem cell transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(82) "Candidemia in hematological patients after hematopoietic stem cell transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(82) "Candidemia in hematological patients after hematopoietic stem cell transplantation" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20631" ["VALUE"]=> array(2) { ["TEXT"]=> string(376) "<sup>1</sup> Raisa Gorbacheva Institute of Children Oncology, Hematology and Transplantation, and Chair of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia<br> <sup>2</sup> I. I. Mechnikov North-Western State Medical University, St. Petersburg, Russia<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(340) "1 Raisa Gorbacheva Institute of Children Oncology, Hematology and Transplantation, and Chair of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia2 I. I. Mechnikov North-Western State Medical University, St. Petersburg, Russia
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(340) "1 Raisa Gorbacheva Institute of Children Oncology, Hematology and Transplantation, and Chair of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
2 I. I. Mechnikov North-Western State Medical University, St. Petersburg, Russia
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20627" ["VALUE"]=> array(2) { ["TEXT"]=> string(986) "Юлия А. Рогачева <sup>1</sup>, Марина О. Попова <sup>1</sup>, Анастасия С. Фролова <sup>1</sup>, Инна В. Маркова <sup>1</sup>, Алиса Г. Волкова <sup>1</sup>, Кирилл А. Екушев <sup>1</sup>, Ольга Н. Пинегина <sup>1</sup>, Олеся В. Паина <sup>1</sup>, Татьяна А. Быкова <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Мария Д. Владовская <sup>1</sup>, Борис И. Смирнов <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Сергей Н. Бондаренко <sup>1</sup>, Людмила С. Зубаровская <sup>1</sup>, Николай Н. Климко <sup>2</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(782) "Юлия А. Рогачева 1, Марина О. Попова 1, Анастасия С. Фролова 1, Инна В. Маркова 1, Алиса Г. Волкова 1, Кирилл А. Екушев 1, Ольга Н. Пинегина 1, Олеся В. Паина 1, Татьяна А. Быкова 1, Елена И. Дарская 1, Мария Д. Владовская 1, Борис И. Смирнов 1, Иван С. Моисеев 1, Сергей Н. Бондаренко 1, Людмила С. Зубаровская 1, Николай Н. Климко 2, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(782) "Юлия А. Рогачева 1, Марина О. Попова 1, Анастасия С. Фролова 1, Инна В. Маркова 1, Алиса Г. Волкова 1, Кирилл А. Екушев 1, Ольга Н. Пинегина 1, Олеся В. Паина 1, Татьяна А. Быкова 1, Елена И. Дарская 1, Мария Д. Владовская 1, Борис И. Смирнов 1, Иван С. Моисеев 1, Сергей Н. Бондаренко 1, Людмила С. Зубаровская 1, Николай Н. Климко 2, Борис В. Афанасьев 1" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20629" ["VALUE"]=> array(2) { ["TEXT"]=> string(6295) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Инвазивный кандизоз/кандидемия – редкий инвазивный микоз, при этом связан с высоким уровнем летальности у пациентов с гематологическими заболеваниями. Кандидемия особенно часто наблюдается у пациентов, которые госпитализируются на долгий период, получающих химиотерапию (ХТ), трансплантацию гемопоэтических стволовых клеток (ТГСК). Целью нашего исследования было изучить эпидемиологию кандидемии у большой когорты реципиентов гемопоэтических стволовых клеток в течение десятилетнего периода высокой трансплантационной активности НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> 2430 трансплантаций гемопоэтических стволовых клеток выполнены в клинике CIC725 в период с 2008 по 2017 год: 1647 аллогенных ТГСК (алло-ТГСК) и 783 аутологичных ТГСК (ауто-ТГСК). Ретроспективное исследование включает 26 случаев кандидемии у пациентов с гематологическими заболеваниями реципиентов ТГСК. Критерии EORTC/MSG 2008 были использованы для постановки диагноза кандидемии также, как и для оценки ответа на терапию. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Частота кандидемии за 10-летний период у реципиентов ТГСК составила 1%: у пациентов после алло-ТГСК частота составила 1,2%, при ауто-ТГСК – 0,7%. Основным заболеванием у реципиентов ТГСК с кандидемией был острый лейкоз у 65% (n=17) пациентов. Медиана возраста – 10 лет (1 месяц-59 лет). В исследуемой популяции алло-ТГСК была выполнена от неродственного донора у 50% (n=13) пациентов, гапло-ТГСК – 26% (n=6) и ауто-ТГСК – 24% (n=6). Полная ремиссия на момент трансплантации не была достигнута у 27% (n=7) пациентов. Первичная противогрибковая профилактика включала назначение флуконазола – 35% (n=9), эхинокандинов – 15% (n=4), без профилактики ув 23% (n=6) пациентов; в качестве вторичной профилактики был использован вориконазол у 27% (n=7) пациентов. Медиана дня возникновения кандидемии оставила 109 дней после алло-ТГСК (3-1337) и 20 дней (8-33) после ауто-ТГСК. Наиболее частым возбудителем были грибы Candida parapsilosis (38%). Этиология кандидемий представлена на рисунке 1. Фебрильная лихорадка была главным клиническим симптомом. Септический синдром развился в 60% случаев. Общая выживаемость (ОВ) в течение 30 дней от диагностики кандидемии составила 65%. При использовании эхинокандинов в качестве стартовой терапии ОВ в течение 30 дней составила 100%, и 65% у пациентов с применением других противогрибковых препаратов (p=0,09). Удаление центрального венозного катетера (ЦВК) при диагностике кандидемии – единственный фактор, достоверно, улучшающий общую 30-дневную выживаемость (91% vs 17%; р =0,001). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Частота кандидемий у реципиентов ТГСК в течение 10-летнего периода наблюдения составила 1%: 1,2% у пациентов после алло-ТГСК и 0,7% после ауто-ТГСК. Общая 30-дневная выживаемость с момента постановки диагноза составила 65%. Удаление ЦВК улучшает общую выживаемость гематологических пациентов с кандидемией. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Кандидемия, гематологические больные, трансплантация гемопоэтических стволовых клеток, высокодозная химиотерапия, частота, общая выживаемость, эхинокандины, центральный венозный катетер. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6063) "
Введение
Инвазивный кандизоз/кандидемия – редкий инвазивный микоз, при этом связан с высоким уровнем летальности у пациентов с гематологическими заболеваниями. Кандидемия особенно часто наблюдается у пациентов, которые госпитализируются на долгий период, получающих химиотерапию (ХТ), трансплантацию гемопоэтических стволовых клеток (ТГСК). Целью нашего исследования было изучить эпидемиологию кандидемии у большой когорты реципиентов гемопоэтических стволовых клеток в течение десятилетнего периода высокой трансплантационной активности НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета.
Материалы и методы
2430 трансплантаций гемопоэтических стволовых клеток выполнены в клинике CIC725 в период с 2008 по 2017 год: 1647 аллогенных ТГСК (алло-ТГСК) и 783 аутологичных ТГСК (ауто-ТГСК). Ретроспективное исследование включает 26 случаев кандидемии у пациентов с гематологическими заболеваниями реципиентов ТГСК. Критерии EORTC/MSG 2008 были использованы для постановки диагноза кандидемии также, как и для оценки ответа на терапию.
Результаты
Частота кандидемии за 10-летний период у реципиентов ТГСК составила 1%: у пациентов после алло-ТГСК частота составила 1,2%, при ауто-ТГСК – 0,7%. Основным заболеванием у реципиентов ТГСК с кандидемией был острый лейкоз у 65% (n=17) пациентов. Медиана возраста – 10 лет (1 месяц-59 лет). В исследуемой популяции алло-ТГСК была выполнена от неродственного донора у 50% (n=13) пациентов, гапло-ТГСК – 26% (n=6) и ауто-ТГСК – 24% (n=6). Полная ремиссия на момент трансплантации не была достигнута у 27% (n=7) пациентов. Первичная противогрибковая профилактика включала назначение флуконазола – 35% (n=9), эхинокандинов – 15% (n=4), без профилактики ув 23% (n=6) пациентов; в качестве вторичной профилактики был использован вориконазол у 27% (n=7) пациентов. Медиана дня возникновения кандидемии оставила 109 дней после алло-ТГСК (3-1337) и 20 дней (8-33) после ауто-ТГСК. Наиболее частым возбудителем были грибы Candida parapsilosis (38%). Этиология кандидемий представлена на рисунке 1. Фебрильная лихорадка была главным клиническим симптомом. Септический синдром развился в 60% случаев. Общая выживаемость (ОВ) в течение 30 дней от диагностики кандидемии составила 65%. При использовании эхинокандинов в качестве стартовой терапии ОВ в течение 30 дней составила 100%, и 65% у пациентов с применением других противогрибковых препаратов (p=0,09). Удаление центрального венозного катетера (ЦВК) при диагностике кандидемии – единственный фактор, достоверно, улучшающий общую 30-дневную выживаемость (91% vs 17%; р =0,001).
Заключение
Частота кандидемий у реципиентов ТГСК в течение 10-летнего периода наблюдения составила 1%: 1,2% у пациентов после алло-ТГСК и 0,7% после ауто-ТГСК. Общая 30-дневная выживаемость с момента постановки диагноза составила 65%. Удаление ЦВК улучшает общую выживаемость гематологических пациентов с кандидемией.
Ключевые слова
Кандидемия, гематологические больные, трансплантация гемопоэтических стволовых клеток, высокодозная химиотерапия, частота, общая выживаемость, эхинокандины, центральный венозный катетер.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6063) "Введение
Инвазивный кандизоз/кандидемия – редкий инвазивный микоз, при этом связан с высоким уровнем летальности у пациентов с гематологическими заболеваниями. Кандидемия особенно часто наблюдается у пациентов, которые госпитализируются на долгий период, получающих химиотерапию (ХТ), трансплантацию гемопоэтических стволовых клеток (ТГСК). Целью нашего исследования было изучить эпидемиологию кандидемии у большой когорты реципиентов гемопоэтических стволовых клеток в течение десятилетнего периода высокой трансплантационной активности НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета.
Материалы и методы
2430 трансплантаций гемопоэтических стволовых клеток выполнены в клинике CIC725 в период с 2008 по 2017 год: 1647 аллогенных ТГСК (алло-ТГСК) и 783 аутологичных ТГСК (ауто-ТГСК). Ретроспективное исследование включает 26 случаев кандидемии у пациентов с гематологическими заболеваниями реципиентов ТГСК. Критерии EORTC/MSG 2008 были использованы для постановки диагноза кандидемии также, как и для оценки ответа на терапию.
Результаты
Частота кандидемии за 10-летний период у реципиентов ТГСК составила 1%: у пациентов после алло-ТГСК частота составила 1,2%, при ауто-ТГСК – 0,7%. Основным заболеванием у реципиентов ТГСК с кандидемией был острый лейкоз у 65% (n=17) пациентов. Медиана возраста – 10 лет (1 месяц-59 лет). В исследуемой популяции алло-ТГСК была выполнена от неродственного донора у 50% (n=13) пациентов, гапло-ТГСК – 26% (n=6) и ауто-ТГСК – 24% (n=6). Полная ремиссия на момент трансплантации не была достигнута у 27% (n=7) пациентов. Первичная противогрибковая профилактика включала назначение флуконазола – 35% (n=9), эхинокандинов – 15% (n=4), без профилактики ув 23% (n=6) пациентов; в качестве вторичной профилактики был использован вориконазол у 27% (n=7) пациентов. Медиана дня возникновения кандидемии оставила 109 дней после алло-ТГСК (3-1337) и 20 дней (8-33) после ауто-ТГСК. Наиболее частым возбудителем были грибы Candida parapsilosis (38%). Этиология кандидемий представлена на рисунке 1. Фебрильная лихорадка была главным клиническим симптомом. Септический синдром развился в 60% случаев. Общая выживаемость (ОВ) в течение 30 дней от диагностики кандидемии составила 65%. При использовании эхинокандинов в качестве стартовой терапии ОВ в течение 30 дней составила 100%, и 65% у пациентов с применением других противогрибковых препаратов (p=0,09). Удаление центрального венозного катетера (ЦВК) при диагностике кандидемии – единственный фактор, достоверно, улучшающий общую 30-дневную выживаемость (91% vs 17%; р =0,001).
Заключение
Частота кандидемий у реципиентов ТГСК в течение 10-летнего периода наблюдения составила 1%: 1,2% у пациентов после алло-ТГСК и 0,7% после ауто-ТГСК. Общая 30-дневная выживаемость с момента постановки диагноза составила 65%. Удаление ЦВК улучшает общую выживаемость гематологических пациентов с кандидемией.
Ключевые слова
Кандидемия, гематологические больные, трансплантация гемопоэтических стволовых клеток, высокодозная химиотерапия, частота, общая выживаемость, эхинокандины, центральный венозный катетер.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20628" ["VALUE"]=> array(2) { ["TEXT"]=> string(734) "<sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия<br> <sup>2</sup> ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И. И. Мечникова», Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(698) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия2 ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И. И. Мечникова», Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(698) "1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
2 ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И. И. Мечникова», Санкт-Петербург, Россия
" } } } [42]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1581" ["~ID"]=> string(4) "1581" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(332) "Поиск прогностических биомаркеров у взрослых пациентов при родственных и неродственных трансплантациях гемопоэтических стволовых клеток с посттрансплантационным циклофосфаном" ["~NAME"]=> string(332) "Поиск прогностических биомаркеров у взрослых пациентов при родственных и неродственных трансплантациях гемопоэтических стволовых клеток с посттрансплантационным циклофосфаном" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:38:54" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:38:54" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/poisk-prognosticheskikh-biomarkerov-u-vzroslykh-patsientov-pri-rodstvennykh-i-nerodstvennykh-transpl/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/poisk-prognosticheskikh-biomarkerov-u-vzroslykh-patsientov-pri-rodstvennykh-i-nerodstvennykh-transpl/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "poisk-prognosticheskikh-biomarkerov-u-vzroslykh-patsientov-pri-rodstvennykh-i-nerodstvennykh-transpl" ["~CODE"]=> string(100) "poisk-prognosticheskikh-biomarkerov-u-vzroslykh-patsientov-pri-rodstvennykh-i-nerodstvennykh-transpl" ["EXTERNAL_ID"]=> string(4) "1581" ["~EXTERNAL_ID"]=> string(4) "1581" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(332) "Поиск прогностических биомаркеров у взрослых пациентов при родственных и неродственных трансплантациях гемопоэтических стволовых клеток с посттрансплантационным циклофосфаном" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(462) "Поиск прогностических биомаркеров у взрослых пациентов при родственных и неродственных трансплантациях гемопоэтических стволовых клеток с посттрансплантационным циклофосфаномScreening for predictive biomarkers after related and unrelated grafts with posttransplantation cyclophosphamide in adult patients" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(8260) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> В настоящий момент существует ряд биомаркеров, которые обладают прогностическим значением в отношении реакции «трансплантат против хозяина» (РТПХ), трансплантационной летальности (ТЛ) и рецидивов основного заболевания. Однако, валидация этих биомаркеров преимущественно выполнялась после классической профилактики РТПХ, включающий ингибитор кальциневрина, метотрексат/микофенолат и антитимоцитарный глобулин при неродственных трансплантациях. Число исследований прогностического значения биомаркеров после посттрансплантационного циклофосфана (ПТЦф) крайне ограничено. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> С 2015 по 2016 было проведено проспективное исследование с включением 79 реципиентов аллогенной трансплантации гемопоэтических стволовых клеток (ТГСК). В исследование были включены только пациенты в ремиссии острого лейкоза, 34% с острым лимфобластным лейкозом, 66% с острым миелобластным. В первой ремиссии ТГСК выполнялась 68% пациентов, во второй – 27%, в третьей – 5%. Двадцати шести пациентам выполнена ТГСК от родственного донора с источником трансплантата – костный мозг, 53 – выполнена неродственная ТГСК с источником трансплантата – стволовые клетки периферической крови. Профилактика РТПХ при родственных включала только ПТЦф 50 мг/кг в Д+3,+4 без дальнейшей иммуносупрессии, при неродственных – комбинацию ПТЦф, такролимуса и микофенолата мофетила. Медиана возраста составила 35 лет (диапазон 18-59). Было проведено расширенное исследование трансплантата методом проточной цитометрии (цитометр FACS ARIA II, моноклональные антитела Miltenyi biotec). Исследовалось наличие следующих популяций лимфоцитов: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Т-регуляторы, дубль-позитивные Т-клетки, дубль-негативные Т-клетки, TCRalpha/beta, Т-клетки памяти TCR v11. Также исследовались замороженные образцы плазмы методом ИФА: VEGF A в Д0, растворимый рецептор к ФНОальфа, ИЛ-8, ИЛL-6, растворимый рецептор к ИЛ-2 (ИЛ-2Р) в Д+7, и ST2, ИЛ-17, растворимый рецептор к ФНОальфа в Д+21-30 (образец после приживления). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> При медиане наблюдения 15 месяцев общая выживаемость (ОВ) в исследуемой группе составила 79%, трансплантационная летальность – 6%, частота рецидивов – 20%, бессобытийная выживаемость – 75%, острая РТПХ II-IV степени – 13%, III-IV степени – 5%, хроническая РТПХ средней и тяжелой степени – 22%. Трансплантационная летальность в группе пациентов с РТПХ составила 0%. Несмотря на то, что в ROC анализе содержание Трег (AUC 0.608), CD4 (0.628) и iNKT (0.630) в трансплантате имели предиктивное значение, различия были не значимы из-за низкой частоты РТПХ (р>0.07). Прогностическим значением в отношении хронической РТПХ обладал ИЛ-17 при измерении на Д+30 (AUC 0.615, 57% против 29%, р=0.017). Наиболее прогностическими популяциями в трансплантате в отшении ОВ были CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613дубль-позитивные T-клетки (AUC 0.657). Прогностическая значимость цитокинов в отношении ОВ была ограничена, за исключением ИЛ-2Р (AUC 0.610). Различия в ОВ в основном были связаны с рецидивом основного заболевания. Например, содержание CD8 клеток в трансплантате >18% достоверно повышало вероятность рецидива (53% vs 12%, p<0.001). Такой же тренд наблюдался и для других популяций. Наблюдаемый фенотип со сниженной реакцией трансплантат-против-лейкоза наблюдался независимо от источника трансплантата (р=0.57), развития острой (р=0.37) или хронической РТПХ (р=0.50). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Исследованные биомаркеры РТПХ обладали ограниченным прогностическим значением после родственных и неродственных ТГСК с ПТЦф, что связано с низкой частотой развития этого осложнения и нулевой РТПХ-ассоциированной летальностью. Тем не менее, было выявлено, что пацинты, которым выполнена трансфузия трансплантата с высоким содержанием эффекторных популяций лимфоцитов, имели повышенный риск рецидива после трансплантации. Биологическое обоснование этому феномену может быть получено в дальнейших исследованиях иммунной реконституции этих популяций. </p> <h2 style="text-align: justify;">Конфликт интересов</h2> <p style="text-align: justify;"> Данное исследование проведено при поддержке РФФИ, грант № 16-34-60142 мол_а_дк. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических клеток, реакция «трансплантат против хозяина», циклофосфамид, профилактика, биомаркеры, эффективность. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(332) "Поиск прогностических биомаркеров у взрослых пациентов при родственных и неродственных трансплантациях гемопоэтических стволовых клеток с посттрансплантационным циклофосфаном" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(332) "Поиск прогностических биомаркеров у взрослых пациентов при родственных и неродственных трансплантациях гемопоэтических стволовых клеток с посттрансплантационным циклофосфаном" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(332) "Поиск прогностических биомаркеров у взрослых пациентов при родственных и неродственных трансплантациях гемопоэтических стволовых клеток с посттрансплантационным циклофосфаном" ["SECTION_META_TITLE"]=> string(332) "Поиск прогностических биомаркеров у взрослых пациентов при родственных и неродственных трансплантациях гемопоэтических стволовых клеток с посттрансплантационным циклофосфаном" ["SECTION_META_KEYWORDS"]=> string(332) "Поиск прогностических биомаркеров у взрослых пациентов при родственных и неродственных трансплантациях гемопоэтических стволовых клеток с посттрансплантационным циклофосфаном" ["SECTION_META_DESCRIPTION"]=> string(332) "Поиск прогностических биомаркеров у взрослых пациентов при родственных и неродственных трансплантациях гемопоэтических стволовых клеток с посттрансплантационным циклофосфаном" ["SECTION_PICTURE_FILE_ALT"]=> string(332) "Поиск прогностических биомаркеров у взрослых пациентов при родственных и неродственных трансплантациях гемопоэтических стволовых клеток с посттрансплантационным циклофосфаном" ["SECTION_PICTURE_FILE_TITLE"]=> string(332) "Поиск прогностических биомаркеров у взрослых пациентов при родственных и неродственных трансплантациях гемопоэтических стволовых клеток с посттрансплантационным циклофосфаном" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "poisk-prognosticheskikh-biomarkerov-u-vzroslykh-patsientov-pri-rodstvennykh-i-nerodstvennykh-transpl" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(332) "Поиск прогностических биомаркеров у взрослых пациентов при родственных и неродственных трансплантациях гемопоэтических стволовых клеток с посттрансплантационным циклофосфаном" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(332) "Поиск прогностических биомаркеров у взрослых пациентов при родственных и неродственных трансплантациях гемопоэтических стволовых клеток с посттрансплантационным циклофосфаном" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "poisk-prognosticheskikh-biomarkerov-u-vzroslykh-patsientov-pri-rodstvennykh-i-nerodstvennykh-transpl" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "poisk-prognosticheskikh-biomarkerov-u-vzroslykh-patsientov-pri-rodstvennykh-i-nerodstvennykh-transpl" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "poisk-prognosticheskikh-biomarkerov-u-vzroslykh-patsientov-pri-rodstvennykh-i-nerodstvennykh-transpl" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20565" ["VALUE"]=> array(2) { ["TEXT"]=> string(700) "Иван С. Моисеев <sup>1</sup>, Елена В. Бабенко <sup>1</sup>, Ольга С. Епифановская <sup>1</sup>, Анна А. Доценко <sup>1</sup>, Владислав С. Сергеев <sup>1</sup>, Елена А. Суркова <sup>2</sup>, Дарья А. Кузнецова <sup>2</sup>, Сергей В. Лапин <sup>2</sup>, Елена И. Дарская <sup>1</sup>, Елена В. Морозова <sup>1</sup>, Серегй Н. Бондаренко <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(556) "Иван С. Моисеев 1, Елена В. Бабенко 1, Ольга С. Епифановская 1, Анна А. Доценко 1, Владислав С. Сергеев 1, Елена А. Суркова 2, Дарья А. Кузнецова 2, Сергей В. Лапин 2, Елена И. Дарская 1, Елена В. Морозова 1, Серегй Н. Бондаренко 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20566" ["VALUE"]=> array(2) { ["TEXT"]=> string(607) "<sup>1</sup> НИИ Детской Онкологии, Гематологии и Трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова<br> <sup>2</sup> Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(577) "1 НИИ Детской Онкологии, Гематологии и Трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова
2 Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20567" ["VALUE"]=> array(2) { ["TEXT"]=> string(8260) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> В настоящий момент существует ряд биомаркеров, которые обладают прогностическим значением в отношении реакции «трансплантат против хозяина» (РТПХ), трансплантационной летальности (ТЛ) и рецидивов основного заболевания. Однако, валидация этих биомаркеров преимущественно выполнялась после классической профилактики РТПХ, включающий ингибитор кальциневрина, метотрексат/микофенолат и антитимоцитарный глобулин при неродственных трансплантациях. Число исследований прогностического значения биомаркеров после посттрансплантационного циклофосфана (ПТЦф) крайне ограничено. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> С 2015 по 2016 было проведено проспективное исследование с включением 79 реципиентов аллогенной трансплантации гемопоэтических стволовых клеток (ТГСК). В исследование были включены только пациенты в ремиссии острого лейкоза, 34% с острым лимфобластным лейкозом, 66% с острым миелобластным. В первой ремиссии ТГСК выполнялась 68% пациентов, во второй – 27%, в третьей – 5%. Двадцати шести пациентам выполнена ТГСК от родственного донора с источником трансплантата – костный мозг, 53 – выполнена неродственная ТГСК с источником трансплантата – стволовые клетки периферической крови. Профилактика РТПХ при родственных включала только ПТЦф 50 мг/кг в Д+3,+4 без дальнейшей иммуносупрессии, при неродственных – комбинацию ПТЦф, такролимуса и микофенолата мофетила. Медиана возраста составила 35 лет (диапазон 18-59). Было проведено расширенное исследование трансплантата методом проточной цитометрии (цитометр FACS ARIA II, моноклональные антитела Miltenyi biotec). Исследовалось наличие следующих популяций лимфоцитов: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Т-регуляторы, дубль-позитивные Т-клетки, дубль-негативные Т-клетки, TCRalpha/beta, Т-клетки памяти TCR v11. Также исследовались замороженные образцы плазмы методом ИФА: VEGF A в Д0, растворимый рецептор к ФНОальфа, ИЛ-8, ИЛL-6, растворимый рецептор к ИЛ-2 (ИЛ-2Р) в Д+7, и ST2, ИЛ-17, растворимый рецептор к ФНОальфа в Д+21-30 (образец после приживления). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> При медиане наблюдения 15 месяцев общая выживаемость (ОВ) в исследуемой группе составила 79%, трансплантационная летальность – 6%, частота рецидивов – 20%, бессобытийная выживаемость – 75%, острая РТПХ II-IV степени – 13%, III-IV степени – 5%, хроническая РТПХ средней и тяжелой степени – 22%. Трансплантационная летальность в группе пациентов с РТПХ составила 0%. Несмотря на то, что в ROC анализе содержание Трег (AUC 0.608), CD4 (0.628) и iNKT (0.630) в трансплантате имели предиктивное значение, различия были не значимы из-за низкой частоты РТПХ (р>0.07). Прогностическим значением в отношении хронической РТПХ обладал ИЛ-17 при измерении на Д+30 (AUC 0.615, 57% против 29%, р=0.017). Наиболее прогностическими популяциями в трансплантате в отшении ОВ были CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613дубль-позитивные T-клетки (AUC 0.657). Прогностическая значимость цитокинов в отношении ОВ была ограничена, за исключением ИЛ-2Р (AUC 0.610). Различия в ОВ в основном были связаны с рецидивом основного заболевания. Например, содержание CD8 клеток в трансплантате >18% достоверно повышало вероятность рецидива (53% vs 12%, p<0.001). Такой же тренд наблюдался и для других популяций. Наблюдаемый фенотип со сниженной реакцией трансплантат-против-лейкоза наблюдался независимо от источника трансплантата (р=0.57), развития острой (р=0.37) или хронической РТПХ (р=0.50). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Исследованные биомаркеры РТПХ обладали ограниченным прогностическим значением после родственных и неродственных ТГСК с ПТЦф, что связано с низкой частотой развития этого осложнения и нулевой РТПХ-ассоциированной летальностью. Тем не менее, было выявлено, что пацинты, которым выполнена трансфузия трансплантата с высоким содержанием эффекторных популяций лимфоцитов, имели повышенный риск рецидива после трансплантации. Биологическое обоснование этому феномену может быть получено в дальнейших исследованиях иммунной реконституции этих популяций. </p> <h2 style="text-align: justify;">Конфликт интересов</h2> <p style="text-align: justify;"> Данное исследование проведено при поддержке РФФИ, грант № 16-34-60142 мол_а_дк. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических клеток, реакция «трансплантат против хозяина», циклофосфамид, профилактика, биомаркеры, эффективность. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7984) "
Введение
В настоящий момент существует ряд биомаркеров, которые обладают прогностическим значением в отношении реакции «трансплантат против хозяина» (РТПХ), трансплантационной летальности (ТЛ) и рецидивов основного заболевания. Однако, валидация этих биомаркеров преимущественно выполнялась после классической профилактики РТПХ, включающий ингибитор кальциневрина, метотрексат/микофенолат и антитимоцитарный глобулин при неродственных трансплантациях. Число исследований прогностического значения биомаркеров после посттрансплантационного циклофосфана (ПТЦф) крайне ограничено.
Пациенты и методы
С 2015 по 2016 было проведено проспективное исследование с включением 79 реципиентов аллогенной трансплантации гемопоэтических стволовых клеток (ТГСК). В исследование были включены только пациенты в ремиссии острого лейкоза, 34% с острым лимфобластным лейкозом, 66% с острым миелобластным. В первой ремиссии ТГСК выполнялась 68% пациентов, во второй – 27%, в третьей – 5%. Двадцати шести пациентам выполнена ТГСК от родственного донора с источником трансплантата – костный мозг, 53 – выполнена неродственная ТГСК с источником трансплантата – стволовые клетки периферической крови. Профилактика РТПХ при родственных включала только ПТЦф 50 мг/кг в Д+3,+4 без дальнейшей иммуносупрессии, при неродственных – комбинацию ПТЦф, такролимуса и микофенолата мофетила. Медиана возраста составила 35 лет (диапазон 18-59). Было проведено расширенное исследование трансплантата методом проточной цитометрии (цитометр FACS ARIA II, моноклональные антитела Miltenyi biotec). Исследовалось наличие следующих популяций лимфоцитов: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Т-регуляторы, дубль-позитивные Т-клетки, дубль-негативные Т-клетки, TCRalpha/beta, Т-клетки памяти TCR v11. Также исследовались замороженные образцы плазмы методом ИФА: VEGF A в Д0, растворимый рецептор к ФНОальфа, ИЛ-8, ИЛL-6, растворимый рецептор к ИЛ-2 (ИЛ-2Р) в Д+7, и ST2, ИЛ-17, растворимый рецептор к ФНОальфа в Д+21-30 (образец после приживления).
Результаты
При медиане наблюдения 15 месяцев общая выживаемость (ОВ) в исследуемой группе составила 79%, трансплантационная летальность – 6%, частота рецидивов – 20%, бессобытийная выживаемость – 75%, острая РТПХ II-IV степени – 13%, III-IV степени – 5%, хроническая РТПХ средней и тяжелой степени – 22%. Трансплантационная летальность в группе пациентов с РТПХ составила 0%. Несмотря на то, что в ROC анализе содержание Трег (AUC 0.608), CD4 (0.628) и iNKT (0.630) в трансплантате имели предиктивное значение, различия были не значимы из-за низкой частоты РТПХ (р>0.07). Прогностическим значением в отношении хронической РТПХ обладал ИЛ-17 при измерении на Д+30 (AUC 0.615, 57% против 29%, р=0.017). Наиболее прогностическими популяциями в трансплантате в отшении ОВ были CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613дубль-позитивные T-клетки (AUC 0.657). Прогностическая значимость цитокинов в отношении ОВ была ограничена, за исключением ИЛ-2Р (AUC 0.610). Различия в ОВ в основном были связаны с рецидивом основного заболевания. Например, содержание CD8 клеток в трансплантате >18% достоверно повышало вероятность рецидива (53% vs 12%, p<0.001). Такой же тренд наблюдался и для других популяций. Наблюдаемый фенотип со сниженной реакцией трансплантат-против-лейкоза наблюдался независимо от источника трансплантата (р=0.57), развития острой (р=0.37) или хронической РТПХ (р=0.50).
Заключение
Исследованные биомаркеры РТПХ обладали ограниченным прогностическим значением после родственных и неродственных ТГСК с ПТЦф, что связано с низкой частотой развития этого осложнения и нулевой РТПХ-ассоциированной летальностью. Тем не менее, было выявлено, что пацинты, которым выполнена трансфузия трансплантата с высоким содержанием эффекторных популяций лимфоцитов, имели повышенный риск рецидива после трансплантации. Биологическое обоснование этому феномену может быть получено в дальнейших исследованиях иммунной реконституции этих популяций.
Конфликт интересов
Данное исследование проведено при поддержке РФФИ, грант № 16-34-60142 мол_а_дк.
Ключевые слова
Трансплантация гемопоэтических клеток, реакция «трансплантат против хозяина», циклофосфамид, профилактика, биомаркеры, эффективность.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20568" ["VALUE"]=> array(2) { ["TEXT"]=> string(531) "Ivan S. Moiseev <sup>1</sup>, Elena V. Babenko <sup>1</sup>, Olga S. Epifanovskaya <sup>1</sup>, Anna A. Dotsenko <sup>1</sup>, Vladislav S. Sergeev <sup>1</sup>, Elena A. Surkova <sup>2</sup>, Daria A. Kuznetcova <sup>2</sup>, Sergey V. Lapin <sup>2</sup>, Elena I. Darskaya <sup>1</sup>, Elena V. Morozova <sup>1</sup>,Sergey N. Bondarenko <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(387) "Ivan S. Moiseev 1, Elena V. Babenko 1, Olga S. Epifanovskaya 1, Anna A. Dotsenko 1, Vladislav S. Sergeev 1, Elena A. Surkova 2, Daria A. Kuznetcova 2, Sergey V. Lapin 2, Elena I. Darskaya 1, Elena V. Morozova 1,Sergey N. Bondarenko 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20569" ["VALUE"]=> array(2) { ["TEXT"]=> string(268) "<sup>1</sup> R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation<br> <sup>2</sup> Laboratory of Autoimmune Diagnostics, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(238) "1 R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation2 Laboratory of Autoimmune Diagnostics, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20570" ["VALUE"]=> array(2) { ["TEXT"]=> string(4477) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> There are a number of biomarkers that predict non-relapse mortality (NRM), graft-versus-host disease (GVHD) and relapse incidence (RI) after conventional GVHD prophylaxis based on calcineurin inhibitors with or without antithymocyte globulin. The biologic mechanisms behind the prophylaxis with posttransplantation cyclophosphamide (PTCy) might be different. Currently there is limited data whether the conventional predictive biomarkers work with this type of prophylaxis. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> We conducted a prospective single-center study between 2015 and 2016 in 79 patients. 34% of patients had acute lymphoblastic leukemia, 66% – acute myeloblastic. 68% of patients were in the first complete remission, 27% – in the 2nd and 5% – in the 3rd. 26 received matched related bone marrow (BM) graft with single-agent PTCy GVHD prophylaxis and 53 received unrelated peripheral blood stem cell graft (PBSC) with PTCy, tacrolimus and MMF prophylaxis. Median age was 35 years (range 18-59). The graft was studies extensively studied by flow cytometry (cytometer FACS Aria II, antibodies by Miltenyi biotec). The following populations were analysed: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Treg, double-positive T-cells, double-negative T-cells, TCRalpha/beta, TCR v11 memory cells. The frozen plasma from day +0 was analysed by ELISA (commercial kits by eBioscience) for VEGF A, from day +7 for soluble TNF receptor, IL-8, IL-6, soluble IL-2 receptor, from day+21-30 (after engraftment sample) for ST2, IL-17, soluble TNF receptor. The above mentioned biomarkers were tested in logisted regression for predictive value regarding GVHD and overall survival (OS). </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> With median follow-up of 15 months overall survival in the study group was 79%, NRM 6%, RI 20%, event-free-survival 75%, acute GVHD grade II-IV 13%, grade III-IV 5%, moderate and severe chronic GVHD 22%. NRM in patients with GVHD was 0%. Despite some predictive value in ROC analysis for acute GVHD of Treg (AUC 0.608), % of CD4 (0.628) and iNKT (0.630), the difference in the GVHD rate was not significant due to small number of events (p>0.07). The predictive biomarker of chronic GVHD was IL-17 measured on day +30 (AUC 0.615), with increased incidence of 57% vs 29%, p=0.017 in patients with elevated level. The most predictive populations for OS were CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613), double-positive T-cells (AUC 0.657). Measured cytokines had lower predictive value for OS than graft composition, except IL-2 receptor (AUC 0.610). The differences in OS was predominantly due to RI. For example, presence of CD8 cells >18% significantly increased the risk of relapse (53% vs 12%, p<0.001). The same trend was observed for other populations. This phenotype with reduced graft-versus-leukemia was independent of the graft source (p=0.57) and occurrence of acute (p=0.37) and chronic GVHD (p=0.50). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The current biomarkers of acute GVHD has limited predictive value after related and unrelated grafts with PTCy, because of the low incidence of this complication and low GVHD-associated mortality. On the contrary we have observed that patients with high prevalence of effector cell populations in the graft have increased RI after transplantation. The explanation of this phenomenon could be elucidated during further studies that evaluate reconstitution of these populations. </p> <h2 style="text-align: justify;">Disclosure</h2> <p style="text-align: justify;"> The reported study was funded by RFBR, according to the research project No. 16-34-60142 mol_а_dk. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cell transplantation, graft-versus-host disease, cyclophosphamide prophylaxis, biomarkers, efficiency. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4201) "
Introduction
There are a number of biomarkers that predict non-relapse mortality (NRM), graft-versus-host disease (GVHD) and relapse incidence (RI) after conventional GVHD prophylaxis based on calcineurin inhibitors with or without antithymocyte globulin. The biologic mechanisms behind the prophylaxis with posttransplantation cyclophosphamide (PTCy) might be different. Currently there is limited data whether the conventional predictive biomarkers work with this type of prophylaxis.
Patients and methods
We conducted a prospective single-center study between 2015 and 2016 in 79 patients. 34% of patients had acute lymphoblastic leukemia, 66% – acute myeloblastic. 68% of patients were in the first complete remission, 27% – in the 2nd and 5% – in the 3rd. 26 received matched related bone marrow (BM) graft with single-agent PTCy GVHD prophylaxis and 53 received unrelated peripheral blood stem cell graft (PBSC) with PTCy, tacrolimus and MMF prophylaxis. Median age was 35 years (range 18-59). The graft was studies extensively studied by flow cytometry (cytometer FACS Aria II, antibodies by Miltenyi biotec). The following populations were analysed: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Treg, double-positive T-cells, double-negative T-cells, TCRalpha/beta, TCR v11 memory cells. The frozen plasma from day +0 was analysed by ELISA (commercial kits by eBioscience) for VEGF A, from day +7 for soluble TNF receptor, IL-8, IL-6, soluble IL-2 receptor, from day+21-30 (after engraftment sample) for ST2, IL-17, soluble TNF receptor. The above mentioned biomarkers were tested in logisted regression for predictive value regarding GVHD and overall survival (OS).
Results
With median follow-up of 15 months overall survival in the study group was 79%, NRM 6%, RI 20%, event-free-survival 75%, acute GVHD grade II-IV 13%, grade III-IV 5%, moderate and severe chronic GVHD 22%. NRM in patients with GVHD was 0%. Despite some predictive value in ROC analysis for acute GVHD of Treg (AUC 0.608), % of CD4 (0.628) and iNKT (0.630), the difference in the GVHD rate was not significant due to small number of events (p>0.07). The predictive biomarker of chronic GVHD was IL-17 measured on day +30 (AUC 0.615), with increased incidence of 57% vs 29%, p=0.017 in patients with elevated level. The most predictive populations for OS were CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613), double-positive T-cells (AUC 0.657). Measured cytokines had lower predictive value for OS than graft composition, except IL-2 receptor (AUC 0.610). The differences in OS was predominantly due to RI. For example, presence of CD8 cells >18% significantly increased the risk of relapse (53% vs 12%, p<0.001). The same trend was observed for other populations. This phenotype with reduced graft-versus-leukemia was independent of the graft source (p=0.57) and occurrence of acute (p=0.37) and chronic GVHD (p=0.50).
Conclusion
The current biomarkers of acute GVHD has limited predictive value after related and unrelated grafts with PTCy, because of the low incidence of this complication and low GVHD-associated mortality. On the contrary we have observed that patients with high prevalence of effector cell populations in the graft have increased RI after transplantation. The explanation of this phenomenon could be elucidated during further studies that evaluate reconstitution of these populations.
Disclosure
The reported study was funded by RFBR, according to the research project No. 16-34-60142 mol_а_dk.
Keywords
Hematopoietic stem cell transplantation, graft-versus-host disease, cyclophosphamide prophylaxis, biomarkers, efficiency.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20571" ["VALUE"]=> string(130) "Screening for predictive biomarkers after related and unrelated grafts with posttransplantation cyclophosphamide in adult patients" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(130) "Screening for predictive biomarkers after related and unrelated grafts with posttransplantation cyclophosphamide in adult patients" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20793" ["VALUE"]=> string(4) "1431" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1431" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20794" ["VALUE"]=> string(4) "1432" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1432" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20568" ["VALUE"]=> array(2) { ["TEXT"]=> string(531) "Ivan S. Moiseev <sup>1</sup>, Elena V. Babenko <sup>1</sup>, Olga S. Epifanovskaya <sup>1</sup>, Anna A. Dotsenko <sup>1</sup>, Vladislav S. Sergeev <sup>1</sup>, Elena A. Surkova <sup>2</sup>, Daria A. Kuznetcova <sup>2</sup>, Sergey V. Lapin <sup>2</sup>, Elena I. Darskaya <sup>1</sup>, Elena V. Morozova <sup>1</sup>,Sergey N. Bondarenko <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(387) "Ivan S. Moiseev 1, Elena V. Babenko 1, Olga S. Epifanovskaya 1, Anna A. Dotsenko 1, Vladislav S. Sergeev 1, Elena A. Surkova 2, Daria A. Kuznetcova 2, Sergey V. Lapin 2, Elena I. Darskaya 1, Elena V. Morozova 1,Sergey N. Bondarenko 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(387) "Ivan S. Moiseev 1, Elena V. Babenko 1, Olga S. Epifanovskaya 1, Anna A. Dotsenko 1, Vladislav S. Sergeev 1, Elena A. Surkova 2, Daria A. Kuznetcova 2, Sergey V. Lapin 2, Elena I. Darskaya 1, Elena V. Morozova 1,Sergey N. Bondarenko 1, Boris V. Afanasyev 1" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20570" ["VALUE"]=> array(2) { ["TEXT"]=> string(4477) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> There are a number of biomarkers that predict non-relapse mortality (NRM), graft-versus-host disease (GVHD) and relapse incidence (RI) after conventional GVHD prophylaxis based on calcineurin inhibitors with or without antithymocyte globulin. The biologic mechanisms behind the prophylaxis with posttransplantation cyclophosphamide (PTCy) might be different. Currently there is limited data whether the conventional predictive biomarkers work with this type of prophylaxis. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> We conducted a prospective single-center study between 2015 and 2016 in 79 patients. 34% of patients had acute lymphoblastic leukemia, 66% – acute myeloblastic. 68% of patients were in the first complete remission, 27% – in the 2nd and 5% – in the 3rd. 26 received matched related bone marrow (BM) graft with single-agent PTCy GVHD prophylaxis and 53 received unrelated peripheral blood stem cell graft (PBSC) with PTCy, tacrolimus and MMF prophylaxis. Median age was 35 years (range 18-59). The graft was studies extensively studied by flow cytometry (cytometer FACS Aria II, antibodies by Miltenyi biotec). The following populations were analysed: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Treg, double-positive T-cells, double-negative T-cells, TCRalpha/beta, TCR v11 memory cells. The frozen plasma from day +0 was analysed by ELISA (commercial kits by eBioscience) for VEGF A, from day +7 for soluble TNF receptor, IL-8, IL-6, soluble IL-2 receptor, from day+21-30 (after engraftment sample) for ST2, IL-17, soluble TNF receptor. The above mentioned biomarkers were tested in logisted regression for predictive value regarding GVHD and overall survival (OS). </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> With median follow-up of 15 months overall survival in the study group was 79%, NRM 6%, RI 20%, event-free-survival 75%, acute GVHD grade II-IV 13%, grade III-IV 5%, moderate and severe chronic GVHD 22%. NRM in patients with GVHD was 0%. Despite some predictive value in ROC analysis for acute GVHD of Treg (AUC 0.608), % of CD4 (0.628) and iNKT (0.630), the difference in the GVHD rate was not significant due to small number of events (p>0.07). The predictive biomarker of chronic GVHD was IL-17 measured on day +30 (AUC 0.615), with increased incidence of 57% vs 29%, p=0.017 in patients with elevated level. The most predictive populations for OS were CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613), double-positive T-cells (AUC 0.657). Measured cytokines had lower predictive value for OS than graft composition, except IL-2 receptor (AUC 0.610). The differences in OS was predominantly due to RI. For example, presence of CD8 cells >18% significantly increased the risk of relapse (53% vs 12%, p<0.001). The same trend was observed for other populations. This phenotype with reduced graft-versus-leukemia was independent of the graft source (p=0.57) and occurrence of acute (p=0.37) and chronic GVHD (p=0.50). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The current biomarkers of acute GVHD has limited predictive value after related and unrelated grafts with PTCy, because of the low incidence of this complication and low GVHD-associated mortality. On the contrary we have observed that patients with high prevalence of effector cell populations in the graft have increased RI after transplantation. The explanation of this phenomenon could be elucidated during further studies that evaluate reconstitution of these populations. </p> <h2 style="text-align: justify;">Disclosure</h2> <p style="text-align: justify;"> The reported study was funded by RFBR, according to the research project No. 16-34-60142 mol_а_dk. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cell transplantation, graft-versus-host disease, cyclophosphamide prophylaxis, biomarkers, efficiency. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4201) "Introduction
There are a number of biomarkers that predict non-relapse mortality (NRM), graft-versus-host disease (GVHD) and relapse incidence (RI) after conventional GVHD prophylaxis based on calcineurin inhibitors with or without antithymocyte globulin. The biologic mechanisms behind the prophylaxis with posttransplantation cyclophosphamide (PTCy) might be different. Currently there is limited data whether the conventional predictive biomarkers work with this type of prophylaxis.
Patients and methods
We conducted a prospective single-center study between 2015 and 2016 in 79 patients. 34% of patients had acute lymphoblastic leukemia, 66% – acute myeloblastic. 68% of patients were in the first complete remission, 27% – in the 2nd and 5% – in the 3rd. 26 received matched related bone marrow (BM) graft with single-agent PTCy GVHD prophylaxis and 53 received unrelated peripheral blood stem cell graft (PBSC) with PTCy, tacrolimus and MMF prophylaxis. Median age was 35 years (range 18-59). The graft was studies extensively studied by flow cytometry (cytometer FACS Aria II, antibodies by Miltenyi biotec). The following populations were analysed: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Treg, double-positive T-cells, double-negative T-cells, TCRalpha/beta, TCR v11 memory cells. The frozen plasma from day +0 was analysed by ELISA (commercial kits by eBioscience) for VEGF A, from day +7 for soluble TNF receptor, IL-8, IL-6, soluble IL-2 receptor, from day+21-30 (after engraftment sample) for ST2, IL-17, soluble TNF receptor. The above mentioned biomarkers were tested in logisted regression for predictive value regarding GVHD and overall survival (OS).
Results
With median follow-up of 15 months overall survival in the study group was 79%, NRM 6%, RI 20%, event-free-survival 75%, acute GVHD grade II-IV 13%, grade III-IV 5%, moderate and severe chronic GVHD 22%. NRM in patients with GVHD was 0%. Despite some predictive value in ROC analysis for acute GVHD of Treg (AUC 0.608), % of CD4 (0.628) and iNKT (0.630), the difference in the GVHD rate was not significant due to small number of events (p>0.07). The predictive biomarker of chronic GVHD was IL-17 measured on day +30 (AUC 0.615), with increased incidence of 57% vs 29%, p=0.017 in patients with elevated level. The most predictive populations for OS were CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613), double-positive T-cells (AUC 0.657). Measured cytokines had lower predictive value for OS than graft composition, except IL-2 receptor (AUC 0.610). The differences in OS was predominantly due to RI. For example, presence of CD8 cells >18% significantly increased the risk of relapse (53% vs 12%, p<0.001). The same trend was observed for other populations. This phenotype with reduced graft-versus-leukemia was independent of the graft source (p=0.57) and occurrence of acute (p=0.37) and chronic GVHD (p=0.50).
Conclusion
The current biomarkers of acute GVHD has limited predictive value after related and unrelated grafts with PTCy, because of the low incidence of this complication and low GVHD-associated mortality. On the contrary we have observed that patients with high prevalence of effector cell populations in the graft have increased RI after transplantation. The explanation of this phenomenon could be elucidated during further studies that evaluate reconstitution of these populations.
Disclosure
The reported study was funded by RFBR, according to the research project No. 16-34-60142 mol_а_dk.
Keywords
Hematopoietic stem cell transplantation, graft-versus-host disease, cyclophosphamide prophylaxis, biomarkers, efficiency.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4201) "Introduction
There are a number of biomarkers that predict non-relapse mortality (NRM), graft-versus-host disease (GVHD) and relapse incidence (RI) after conventional GVHD prophylaxis based on calcineurin inhibitors with or without antithymocyte globulin. The biologic mechanisms behind the prophylaxis with posttransplantation cyclophosphamide (PTCy) might be different. Currently there is limited data whether the conventional predictive biomarkers work with this type of prophylaxis.
Patients and methods
We conducted a prospective single-center study between 2015 and 2016 in 79 patients. 34% of patients had acute lymphoblastic leukemia, 66% – acute myeloblastic. 68% of patients were in the first complete remission, 27% – in the 2nd and 5% – in the 3rd. 26 received matched related bone marrow (BM) graft with single-agent PTCy GVHD prophylaxis and 53 received unrelated peripheral blood stem cell graft (PBSC) with PTCy, tacrolimus and MMF prophylaxis. Median age was 35 years (range 18-59). The graft was studies extensively studied by flow cytometry (cytometer FACS Aria II, antibodies by Miltenyi biotec). The following populations were analysed: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Treg, double-positive T-cells, double-negative T-cells, TCRalpha/beta, TCR v11 memory cells. The frozen plasma from day +0 was analysed by ELISA (commercial kits by eBioscience) for VEGF A, from day +7 for soluble TNF receptor, IL-8, IL-6, soluble IL-2 receptor, from day+21-30 (after engraftment sample) for ST2, IL-17, soluble TNF receptor. The above mentioned biomarkers were tested in logisted regression for predictive value regarding GVHD and overall survival (OS).
Results
With median follow-up of 15 months overall survival in the study group was 79%, NRM 6%, RI 20%, event-free-survival 75%, acute GVHD grade II-IV 13%, grade III-IV 5%, moderate and severe chronic GVHD 22%. NRM in patients with GVHD was 0%. Despite some predictive value in ROC analysis for acute GVHD of Treg (AUC 0.608), % of CD4 (0.628) and iNKT (0.630), the difference in the GVHD rate was not significant due to small number of events (p>0.07). The predictive biomarker of chronic GVHD was IL-17 measured on day +30 (AUC 0.615), with increased incidence of 57% vs 29%, p=0.017 in patients with elevated level. The most predictive populations for OS were CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613), double-positive T-cells (AUC 0.657). Measured cytokines had lower predictive value for OS than graft composition, except IL-2 receptor (AUC 0.610). The differences in OS was predominantly due to RI. For example, presence of CD8 cells >18% significantly increased the risk of relapse (53% vs 12%, p<0.001). The same trend was observed for other populations. This phenotype with reduced graft-versus-leukemia was independent of the graft source (p=0.57) and occurrence of acute (p=0.37) and chronic GVHD (p=0.50).
Conclusion
The current biomarkers of acute GVHD has limited predictive value after related and unrelated grafts with PTCy, because of the low incidence of this complication and low GVHD-associated mortality. On the contrary we have observed that patients with high prevalence of effector cell populations in the graft have increased RI after transplantation. The explanation of this phenomenon could be elucidated during further studies that evaluate reconstitution of these populations.
Disclosure
The reported study was funded by RFBR, according to the research project No. 16-34-60142 mol_а_dk.
Keywords
Hematopoietic stem cell transplantation, graft-versus-host disease, cyclophosphamide prophylaxis, biomarkers, efficiency.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20571" ["VALUE"]=> string(130) "Screening for predictive biomarkers after related and unrelated grafts with posttransplantation cyclophosphamide in adult patients" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(130) "Screening for predictive biomarkers after related and unrelated grafts with posttransplantation cyclophosphamide in adult patients" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(130) "Screening for predictive biomarkers after related and unrelated grafts with posttransplantation cyclophosphamide in adult patients" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20569" ["VALUE"]=> array(2) { ["TEXT"]=> string(268) "<sup>1</sup> R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation<br> <sup>2</sup> Laboratory of Autoimmune Diagnostics, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(238) "1 R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation2 Laboratory of Autoimmune Diagnostics, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(238) "1 R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation
2 Laboratory of Autoimmune Diagnostics, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20565" ["VALUE"]=> array(2) { ["TEXT"]=> string(700) "Иван С. Моисеев <sup>1</sup>, Елена В. Бабенко <sup>1</sup>, Ольга С. Епифановская <sup>1</sup>, Анна А. Доценко <sup>1</sup>, Владислав С. Сергеев <sup>1</sup>, Елена А. Суркова <sup>2</sup>, Дарья А. Кузнецова <sup>2</sup>, Сергей В. Лапин <sup>2</sup>, Елена И. Дарская <sup>1</sup>, Елена В. Морозова <sup>1</sup>, Серегй Н. Бондаренко <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(556) "Иван С. Моисеев 1, Елена В. Бабенко 1, Ольга С. Епифановская 1, Анна А. Доценко 1, Владислав С. Сергеев 1, Елена А. Суркова 2, Дарья А. Кузнецова 2, Сергей В. Лапин 2, Елена И. Дарская 1, Елена В. Морозова 1, Серегй Н. Бондаренко 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(556) "Иван С. Моисеев 1, Елена В. Бабенко 1, Ольга С. Епифановская 1, Анна А. Доценко 1, Владислав С. Сергеев 1, Елена А. Суркова 2, Дарья А. Кузнецова 2, Сергей В. Лапин 2, Елена И. Дарская 1, Елена В. Морозова 1, Серегй Н. Бондаренко 1, Борис В. Афанасьев 1" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20567" ["VALUE"]=> array(2) { ["TEXT"]=> string(8260) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> В настоящий момент существует ряд биомаркеров, которые обладают прогностическим значением в отношении реакции «трансплантат против хозяина» (РТПХ), трансплантационной летальности (ТЛ) и рецидивов основного заболевания. Однако, валидация этих биомаркеров преимущественно выполнялась после классической профилактики РТПХ, включающий ингибитор кальциневрина, метотрексат/микофенолат и антитимоцитарный глобулин при неродственных трансплантациях. Число исследований прогностического значения биомаркеров после посттрансплантационного циклофосфана (ПТЦф) крайне ограничено. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> С 2015 по 2016 было проведено проспективное исследование с включением 79 реципиентов аллогенной трансплантации гемопоэтических стволовых клеток (ТГСК). В исследование были включены только пациенты в ремиссии острого лейкоза, 34% с острым лимфобластным лейкозом, 66% с острым миелобластным. В первой ремиссии ТГСК выполнялась 68% пациентов, во второй – 27%, в третьей – 5%. Двадцати шести пациентам выполнена ТГСК от родственного донора с источником трансплантата – костный мозг, 53 – выполнена неродственная ТГСК с источником трансплантата – стволовые клетки периферической крови. Профилактика РТПХ при родственных включала только ПТЦф 50 мг/кг в Д+3,+4 без дальнейшей иммуносупрессии, при неродственных – комбинацию ПТЦф, такролимуса и микофенолата мофетила. Медиана возраста составила 35 лет (диапазон 18-59). Было проведено расширенное исследование трансплантата методом проточной цитометрии (цитометр FACS ARIA II, моноклональные антитела Miltenyi biotec). Исследовалось наличие следующих популяций лимфоцитов: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Т-регуляторы, дубль-позитивные Т-клетки, дубль-негативные Т-клетки, TCRalpha/beta, Т-клетки памяти TCR v11. Также исследовались замороженные образцы плазмы методом ИФА: VEGF A в Д0, растворимый рецептор к ФНОальфа, ИЛ-8, ИЛL-6, растворимый рецептор к ИЛ-2 (ИЛ-2Р) в Д+7, и ST2, ИЛ-17, растворимый рецептор к ФНОальфа в Д+21-30 (образец после приживления). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> При медиане наблюдения 15 месяцев общая выживаемость (ОВ) в исследуемой группе составила 79%, трансплантационная летальность – 6%, частота рецидивов – 20%, бессобытийная выживаемость – 75%, острая РТПХ II-IV степени – 13%, III-IV степени – 5%, хроническая РТПХ средней и тяжелой степени – 22%. Трансплантационная летальность в группе пациентов с РТПХ составила 0%. Несмотря на то, что в ROC анализе содержание Трег (AUC 0.608), CD4 (0.628) и iNKT (0.630) в трансплантате имели предиктивное значение, различия были не значимы из-за низкой частоты РТПХ (р>0.07). Прогностическим значением в отношении хронической РТПХ обладал ИЛ-17 при измерении на Д+30 (AUC 0.615, 57% против 29%, р=0.017). Наиболее прогностическими популяциями в трансплантате в отшении ОВ были CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613дубль-позитивные T-клетки (AUC 0.657). Прогностическая значимость цитокинов в отношении ОВ была ограничена, за исключением ИЛ-2Р (AUC 0.610). Различия в ОВ в основном были связаны с рецидивом основного заболевания. Например, содержание CD8 клеток в трансплантате >18% достоверно повышало вероятность рецидива (53% vs 12%, p<0.001). Такой же тренд наблюдался и для других популяций. Наблюдаемый фенотип со сниженной реакцией трансплантат-против-лейкоза наблюдался независимо от источника трансплантата (р=0.57), развития острой (р=0.37) или хронической РТПХ (р=0.50). </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Исследованные биомаркеры РТПХ обладали ограниченным прогностическим значением после родственных и неродственных ТГСК с ПТЦф, что связано с низкой частотой развития этого осложнения и нулевой РТПХ-ассоциированной летальностью. Тем не менее, было выявлено, что пацинты, которым выполнена трансфузия трансплантата с высоким содержанием эффекторных популяций лимфоцитов, имели повышенный риск рецидива после трансплантации. Биологическое обоснование этому феномену может быть получено в дальнейших исследованиях иммунной реконституции этих популяций. </p> <h2 style="text-align: justify;">Конфликт интересов</h2> <p style="text-align: justify;"> Данное исследование проведено при поддержке РФФИ, грант № 16-34-60142 мол_а_дк. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических клеток, реакция «трансплантат против хозяина», циклофосфамид, профилактика, биомаркеры, эффективность. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7984) "
Введение
В настоящий момент существует ряд биомаркеров, которые обладают прогностическим значением в отношении реакции «трансплантат против хозяина» (РТПХ), трансплантационной летальности (ТЛ) и рецидивов основного заболевания. Однако, валидация этих биомаркеров преимущественно выполнялась после классической профилактики РТПХ, включающий ингибитор кальциневрина, метотрексат/микофенолат и антитимоцитарный глобулин при неродственных трансплантациях. Число исследований прогностического значения биомаркеров после посттрансплантационного циклофосфана (ПТЦф) крайне ограничено.
Пациенты и методы
С 2015 по 2016 было проведено проспективное исследование с включением 79 реципиентов аллогенной трансплантации гемопоэтических стволовых клеток (ТГСК). В исследование были включены только пациенты в ремиссии острого лейкоза, 34% с острым лимфобластным лейкозом, 66% с острым миелобластным. В первой ремиссии ТГСК выполнялась 68% пациентов, во второй – 27%, в третьей – 5%. Двадцати шести пациентам выполнена ТГСК от родственного донора с источником трансплантата – костный мозг, 53 – выполнена неродственная ТГСК с источником трансплантата – стволовые клетки периферической крови. Профилактика РТПХ при родственных включала только ПТЦф 50 мг/кг в Д+3,+4 без дальнейшей иммуносупрессии, при неродственных – комбинацию ПТЦф, такролимуса и микофенолата мофетила. Медиана возраста составила 35 лет (диапазон 18-59). Было проведено расширенное исследование трансплантата методом проточной цитометрии (цитометр FACS ARIA II, моноклональные антитела Miltenyi biotec). Исследовалось наличие следующих популяций лимфоцитов: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Т-регуляторы, дубль-позитивные Т-клетки, дубль-негативные Т-клетки, TCRalpha/beta, Т-клетки памяти TCR v11. Также исследовались замороженные образцы плазмы методом ИФА: VEGF A в Д0, растворимый рецептор к ФНОальфа, ИЛ-8, ИЛL-6, растворимый рецептор к ИЛ-2 (ИЛ-2Р) в Д+7, и ST2, ИЛ-17, растворимый рецептор к ФНОальфа в Д+21-30 (образец после приживления).
Результаты
При медиане наблюдения 15 месяцев общая выживаемость (ОВ) в исследуемой группе составила 79%, трансплантационная летальность – 6%, частота рецидивов – 20%, бессобытийная выживаемость – 75%, острая РТПХ II-IV степени – 13%, III-IV степени – 5%, хроническая РТПХ средней и тяжелой степени – 22%. Трансплантационная летальность в группе пациентов с РТПХ составила 0%. Несмотря на то, что в ROC анализе содержание Трег (AUC 0.608), CD4 (0.628) и iNKT (0.630) в трансплантате имели предиктивное значение, различия были не значимы из-за низкой частоты РТПХ (р>0.07). Прогностическим значением в отношении хронической РТПХ обладал ИЛ-17 при измерении на Д+30 (AUC 0.615, 57% против 29%, р=0.017). Наиболее прогностическими популяциями в трансплантате в отшении ОВ были CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613дубль-позитивные T-клетки (AUC 0.657). Прогностическая значимость цитокинов в отношении ОВ была ограничена, за исключением ИЛ-2Р (AUC 0.610). Различия в ОВ в основном были связаны с рецидивом основного заболевания. Например, содержание CD8 клеток в трансплантате >18% достоверно повышало вероятность рецидива (53% vs 12%, p<0.001). Такой же тренд наблюдался и для других популяций. Наблюдаемый фенотип со сниженной реакцией трансплантат-против-лейкоза наблюдался независимо от источника трансплантата (р=0.57), развития острой (р=0.37) или хронической РТПХ (р=0.50).
Заключение
Исследованные биомаркеры РТПХ обладали ограниченным прогностическим значением после родственных и неродственных ТГСК с ПТЦф, что связано с низкой частотой развития этого осложнения и нулевой РТПХ-ассоциированной летальностью. Тем не менее, было выявлено, что пацинты, которым выполнена трансфузия трансплантата с высоким содержанием эффекторных популяций лимфоцитов, имели повышенный риск рецидива после трансплантации. Биологическое обоснование этому феномену может быть получено в дальнейших исследованиях иммунной реконституции этих популяций.
Конфликт интересов
Данное исследование проведено при поддержке РФФИ, грант № 16-34-60142 мол_а_дк.
Ключевые слова
Трансплантация гемопоэтических клеток, реакция «трансплантат против хозяина», циклофосфамид, профилактика, биомаркеры, эффективность.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(7984) "Введение
В настоящий момент существует ряд биомаркеров, которые обладают прогностическим значением в отношении реакции «трансплантат против хозяина» (РТПХ), трансплантационной летальности (ТЛ) и рецидивов основного заболевания. Однако, валидация этих биомаркеров преимущественно выполнялась после классической профилактики РТПХ, включающий ингибитор кальциневрина, метотрексат/микофенолат и антитимоцитарный глобулин при неродственных трансплантациях. Число исследований прогностического значения биомаркеров после посттрансплантационного циклофосфана (ПТЦф) крайне ограничено.
Пациенты и методы
С 2015 по 2016 было проведено проспективное исследование с включением 79 реципиентов аллогенной трансплантации гемопоэтических стволовых клеток (ТГСК). В исследование были включены только пациенты в ремиссии острого лейкоза, 34% с острым лимфобластным лейкозом, 66% с острым миелобластным. В первой ремиссии ТГСК выполнялась 68% пациентов, во второй – 27%, в третьей – 5%. Двадцати шести пациентам выполнена ТГСК от родственного донора с источником трансплантата – костный мозг, 53 – выполнена неродственная ТГСК с источником трансплантата – стволовые клетки периферической крови. Профилактика РТПХ при родственных включала только ПТЦф 50 мг/кг в Д+3,+4 без дальнейшей иммуносупрессии, при неродственных – комбинацию ПТЦф, такролимуса и микофенолата мофетила. Медиана возраста составила 35 лет (диапазон 18-59). Было проведено расширенное исследование трансплантата методом проточной цитометрии (цитометр FACS ARIA II, моноклональные антитела Miltenyi biotec). Исследовалось наличие следующих популяций лимфоцитов: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Т-регуляторы, дубль-позитивные Т-клетки, дубль-негативные Т-клетки, TCRalpha/beta, Т-клетки памяти TCR v11. Также исследовались замороженные образцы плазмы методом ИФА: VEGF A в Д0, растворимый рецептор к ФНОальфа, ИЛ-8, ИЛL-6, растворимый рецептор к ИЛ-2 (ИЛ-2Р) в Д+7, и ST2, ИЛ-17, растворимый рецептор к ФНОальфа в Д+21-30 (образец после приживления).
Результаты
При медиане наблюдения 15 месяцев общая выживаемость (ОВ) в исследуемой группе составила 79%, трансплантационная летальность – 6%, частота рецидивов – 20%, бессобытийная выживаемость – 75%, острая РТПХ II-IV степени – 13%, III-IV степени – 5%, хроническая РТПХ средней и тяжелой степени – 22%. Трансплантационная летальность в группе пациентов с РТПХ составила 0%. Несмотря на то, что в ROC анализе содержание Трег (AUC 0.608), CD4 (0.628) и iNKT (0.630) в трансплантате имели предиктивное значение, различия были не значимы из-за низкой частоты РТПХ (р>0.07). Прогностическим значением в отношении хронической РТПХ обладал ИЛ-17 при измерении на Д+30 (AUC 0.615, 57% против 29%, р=0.017). Наиболее прогностическими популяциями в трансплантате в отшении ОВ были CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613дубль-позитивные T-клетки (AUC 0.657). Прогностическая значимость цитокинов в отношении ОВ была ограничена, за исключением ИЛ-2Р (AUC 0.610). Различия в ОВ в основном были связаны с рецидивом основного заболевания. Например, содержание CD8 клеток в трансплантате >18% достоверно повышало вероятность рецидива (53% vs 12%, p<0.001). Такой же тренд наблюдался и для других популяций. Наблюдаемый фенотип со сниженной реакцией трансплантат-против-лейкоза наблюдался независимо от источника трансплантата (р=0.57), развития острой (р=0.37) или хронической РТПХ (р=0.50).
Заключение
Исследованные биомаркеры РТПХ обладали ограниченным прогностическим значением после родственных и неродственных ТГСК с ПТЦф, что связано с низкой частотой развития этого осложнения и нулевой РТПХ-ассоциированной летальностью. Тем не менее, было выявлено, что пацинты, которым выполнена трансфузия трансплантата с высоким содержанием эффекторных популяций лимфоцитов, имели повышенный риск рецидива после трансплантации. Биологическое обоснование этому феномену может быть получено в дальнейших исследованиях иммунной реконституции этих популяций.
Конфликт интересов
Данное исследование проведено при поддержке РФФИ, грант № 16-34-60142 мол_а_дк.
Ключевые слова
Трансплантация гемопоэтических клеток, реакция «трансплантат против хозяина», циклофосфамид, профилактика, биомаркеры, эффективность.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20566" ["VALUE"]=> array(2) { ["TEXT"]=> string(607) "<sup>1</sup> НИИ Детской Онкологии, Гематологии и Трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова<br> <sup>2</sup> Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(577) "1 НИИ Детской Онкологии, Гематологии и Трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова2 Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(577) "1 НИИ Детской Онкологии, Гематологии и Трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова
2 Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова" } } } [43]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1582" ["~ID"]=> string(4) "1582" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(235) "Эффективность и безопасность терапии ниволумабом у детей с рецидивами онкогематологических заболеваний после аллогенной ТГСК" ["~NAME"]=> string(235) "Эффективность и безопасность терапии ниволумабом у детей с рецидивами онкогематологических заболеваний после аллогенной ТГСК" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:39:19" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:39:19" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/effektivnost-i-bezopasnost-terapii-nivolumabom-u-detey-s-retsidivami-onkogematologicheskikh-zaboleva/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/effektivnost-i-bezopasnost-terapii-nivolumabom-u-detey-s-retsidivami-onkogematologicheskikh-zaboleva/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "effektivnost-i-bezopasnost-terapii-nivolumabom-u-detey-s-retsidivami-onkogematologicheskikh-zaboleva" ["~CODE"]=> string(100) "effektivnost-i-bezopasnost-terapii-nivolumabom-u-detey-s-retsidivami-onkogematologicheskikh-zaboleva" ["EXTERNAL_ID"]=> string(4) "1582" ["~EXTERNAL_ID"]=> string(4) "1582" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(235) "Эффективность и безопасность терапии ниволумабом у детей с рецидивами онкогематологических заболеваний после аллогенной ТГСК" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(355) "Эффективность и безопасность терапии ниволумабом у детей с рецидивами онкогематологических заболеваний после аллогенной ТГСКEfficacy and safety of nivolumab-based therapy in children with relapse of hematologic malignancies after allogenic HSCT" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(7440) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Рецидивы острых лейкозов и лимфом у реципиентов алло-ТГСК трудно поддаются лечению и прогноз пациентов крайне неутешителен. Основными проблемами остаются краткосрочные ремиссии после стандартной химиотерапии, «взрывное» развитие рецидива, сочетанная токсичность химиотерапии и первой ТГСК, отсутствие донора для повторной трансплантации. Возможная альтернатива стандартной химиотерапии – применение блокаторов PD-1, потенциирующих иммуный ответ, что позволяет рассчитывать на усиление эффекта «трансплантат против лейкемии» у пациентов с рецидивами онкогематологических заболеваний после аллогенной ТГСК. Целью наблюдения было оценить эффективность и безопасность применения ниволумаба у данной когорты пациентов. </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> Мы ретроспективно проанализировали истории болезни 8 пациентов в возрасте от 3 до 14 лет, получивших терапию ингибиторами PD1 после ТГСК. 6 из них имели диагноз ОМЛ, 1 пациент – диагноз ОЛЛ, 1 пациент – диагноз гепатоспленическая γδ-Т-клеточная лимфома. На момент ТГСК 5 пациентов имели продвинутую стадию заболевания, 2 были в полной ремиссии, и 1 находился в MRD-позитивной ремиссии. Все пациенты получали аллогенную ТГСК (5 пациентов от гаплоидентичного донора, 3 пациента от HLA-идентичного сиблинга). На +30 сутки от ТГСК все пациенты находились в клинико-гематологической и молекулярной ремиссии. У 50% пациентов развилась острая РТПХ 1-2 степени с поражением кожи и ЖКТ. Среднее время до развития рецидива составило 180 (97-420) дней. Развернутый костно-мозговой рецидив был зафиксирован у 6 пациентов, у 2 пациентов был отмечен молекулярный рецидив. Все пациенты получили 1 инъекцию ниволумаба в дозе 3 мг/кг. Один пациент с ОМЛ получил инъекцию ниволумаба, уже находясь в ремиссии после повторной ТГСК, в связи с высоким риском повторного рецидива. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Нежелательные явления были зарегистрированы у 6 (75%) пациентов. У двух пациентов развился иммунный менингоэнцефалит, у 1 пациента – иммунный гепатит 4 степени, у 2 пациентов была отмечена РТПХ кожи 3й степени, у 4 пациентов развилась иммунная лихорадка. Четырем пациентам потребовалось назначение системной иммуносупрессивной терапии для борьбы с иммуноопосредованными реакциями. Связанной с токсичностью летальности отмечено не было. Для оценки эффективности терапии после первой инъекции ниволумаба всем пациентам были выполнены костномозговые пункции. Шесть из семи пациентов не ответили на терапию. Среднее время до прогрессирования заболевания составляло 21 день. У пациента 7 лет с ОМЛ, находящегося в ремиссии на момент введения ниволумаба, спустя 2 недели после введения развилась иммунная лихорадка и иммунный менингоэнцефалит с явлениями когнитивных расстройств, дизартрии, мышечной слабости, полностью разрешившийся на фоне пульс-терапии солу-медролом. В настоящее время спустя 1 год 10 месяцев после введения ниволумаба у пациента сохраняется морфологическая MRD негативная ремиссия, выраженной патологии со стороны органов и систем нет. Пациентка 7 лет, находившаяся в развернутом рецидиве ОЛЛ на момент введения ниволумаба, достигла стойкой ремиссии. Однако спустя 14 дней от введения препарата у ребенка развился аутоиммунный гепатит 4 степени, рефрактерный ко всем видам терапии, включая ТАО в СОД 6 Гр. В связи с прогрессирующим фатальным повреждением печени произведена успешная трансплантация печени от родственного донора, на сроке 1 год 3 месяца после введения ниволумаба сохраняется полная ремиссия. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Наш небольшой опыт показывает, что применение ингибиторов PD-1 после аллогенной ТГСК связано со значительной токсичностью. Для обеспечения безопасности и эффективности этого подхода требуются дальнейшие проспективные исследования. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Аллогенная ТГСК, ингибиторы PD1, рецидив, ОЛЛ, ОМЛ. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(235) "Эффективность и безопасность терапии ниволумабом у детей с рецидивами онкогематологических заболеваний после аллогенной ТГСК" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(235) "Эффективность и безопасность терапии ниволумабом у детей с рецидивами онкогематологических заболеваний после аллогенной ТГСК" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(235) "Эффективность и безопасность терапии ниволумабом у детей с рецидивами онкогематологических заболеваний после аллогенной ТГСК" ["SECTION_META_TITLE"]=> string(235) "Эффективность и безопасность терапии ниволумабом у детей с рецидивами онкогематологических заболеваний после аллогенной ТГСК" ["SECTION_META_KEYWORDS"]=> string(235) "Эффективность и безопасность терапии ниволумабом у детей с рецидивами онкогематологических заболеваний после аллогенной ТГСК" ["SECTION_META_DESCRIPTION"]=> string(235) "Эффективность и безопасность терапии ниволумабом у детей с рецидивами онкогематологических заболеваний после аллогенной ТГСК" ["SECTION_PICTURE_FILE_ALT"]=> string(235) "Эффективность и безопасность терапии ниволумабом у детей с рецидивами онкогематологических заболеваний после аллогенной ТГСК" ["SECTION_PICTURE_FILE_TITLE"]=> string(235) "Эффективность и безопасность терапии ниволумабом у детей с рецидивами онкогематологических заболеваний после аллогенной ТГСК" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "effektivnost-i-bezopasnost-terapii-nivolumabom-u-detey-s-retsidivami-onkogematologicheskikh-zaboleva" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(235) "Эффективность и безопасность терапии ниволумабом у детей с рецидивами онкогематологических заболеваний после аллогенной ТГСК" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(235) "Эффективность и безопасность терапии ниволумабом у детей с рецидивами онкогематологических заболеваний после аллогенной ТГСК" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "effektivnost-i-bezopasnost-terapii-nivolumabom-u-detey-s-retsidivami-onkogematologicheskikh-zaboleva" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "effektivnost-i-bezopasnost-terapii-nivolumabom-u-detey-s-retsidivami-onkogematologicheskikh-zaboleva" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "effektivnost-i-bezopasnost-terapii-nivolumabom-u-detey-s-retsidivami-onkogematologicheskikh-zaboleva" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20574" ["VALUE"]=> array(2) { ["TEXT"]=> string(272) "Ольга О. Молостова, Лариса Н. Шелихова, Мария А. Алябьева, Дмитрий Н. Балашов, Светлана А. Радыгина, Ирина И. Калинина, Михаил А. Масчан, Алексей А. Масчан" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(272) "Ольга О. Молостова, Лариса Н. Шелихова, Мария А. Алябьева, Дмитрий Н. Балашов, Светлана А. Радыгина, Ирина И. Калинина, Михаил А. Масчан, Алексей А. Масчан" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20575" ["VALUE"]=> array(2) { ["TEXT"]=> string(271) "ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева», Москва, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(265) "ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева», Москва, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20576" ["VALUE"]=> array(2) { ["TEXT"]=> string(7440) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Рецидивы острых лейкозов и лимфом у реципиентов алло-ТГСК трудно поддаются лечению и прогноз пациентов крайне неутешителен. Основными проблемами остаются краткосрочные ремиссии после стандартной химиотерапии, «взрывное» развитие рецидива, сочетанная токсичность химиотерапии и первой ТГСК, отсутствие донора для повторной трансплантации. Возможная альтернатива стандартной химиотерапии – применение блокаторов PD-1, потенциирующих иммуный ответ, что позволяет рассчитывать на усиление эффекта «трансплантат против лейкемии» у пациентов с рецидивами онкогематологических заболеваний после аллогенной ТГСК. Целью наблюдения было оценить эффективность и безопасность применения ниволумаба у данной когорты пациентов. </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> Мы ретроспективно проанализировали истории болезни 8 пациентов в возрасте от 3 до 14 лет, получивших терапию ингибиторами PD1 после ТГСК. 6 из них имели диагноз ОМЛ, 1 пациент – диагноз ОЛЛ, 1 пациент – диагноз гепатоспленическая γδ-Т-клеточная лимфома. На момент ТГСК 5 пациентов имели продвинутую стадию заболевания, 2 были в полной ремиссии, и 1 находился в MRD-позитивной ремиссии. Все пациенты получали аллогенную ТГСК (5 пациентов от гаплоидентичного донора, 3 пациента от HLA-идентичного сиблинга). На +30 сутки от ТГСК все пациенты находились в клинико-гематологической и молекулярной ремиссии. У 50% пациентов развилась острая РТПХ 1-2 степени с поражением кожи и ЖКТ. Среднее время до развития рецидива составило 180 (97-420) дней. Развернутый костно-мозговой рецидив был зафиксирован у 6 пациентов, у 2 пациентов был отмечен молекулярный рецидив. Все пациенты получили 1 инъекцию ниволумаба в дозе 3 мг/кг. Один пациент с ОМЛ получил инъекцию ниволумаба, уже находясь в ремиссии после повторной ТГСК, в связи с высоким риском повторного рецидива. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Нежелательные явления были зарегистрированы у 6 (75%) пациентов. У двух пациентов развился иммунный менингоэнцефалит, у 1 пациента – иммунный гепатит 4 степени, у 2 пациентов была отмечена РТПХ кожи 3й степени, у 4 пациентов развилась иммунная лихорадка. Четырем пациентам потребовалось назначение системной иммуносупрессивной терапии для борьбы с иммуноопосредованными реакциями. Связанной с токсичностью летальности отмечено не было. Для оценки эффективности терапии после первой инъекции ниволумаба всем пациентам были выполнены костномозговые пункции. Шесть из семи пациентов не ответили на терапию. Среднее время до прогрессирования заболевания составляло 21 день. У пациента 7 лет с ОМЛ, находящегося в ремиссии на момент введения ниволумаба, спустя 2 недели после введения развилась иммунная лихорадка и иммунный менингоэнцефалит с явлениями когнитивных расстройств, дизартрии, мышечной слабости, полностью разрешившийся на фоне пульс-терапии солу-медролом. В настоящее время спустя 1 год 10 месяцев после введения ниволумаба у пациента сохраняется морфологическая MRD негативная ремиссия, выраженной патологии со стороны органов и систем нет. Пациентка 7 лет, находившаяся в развернутом рецидиве ОЛЛ на момент введения ниволумаба, достигла стойкой ремиссии. Однако спустя 14 дней от введения препарата у ребенка развился аутоиммунный гепатит 4 степени, рефрактерный ко всем видам терапии, включая ТАО в СОД 6 Гр. В связи с прогрессирующим фатальным повреждением печени произведена успешная трансплантация печени от родственного донора, на сроке 1 год 3 месяца после введения ниволумаба сохраняется полная ремиссия. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Наш небольшой опыт показывает, что применение ингибиторов PD-1 после аллогенной ТГСК связано со значительной токсичностью. Для обеспечения безопасности и эффективности этого подхода требуются дальнейшие проспективные исследования. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Аллогенная ТГСК, ингибиторы PD1, рецидив, ОЛЛ, ОМЛ. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7220) "
Введение
Рецидивы острых лейкозов и лимфом у реципиентов алло-ТГСК трудно поддаются лечению и прогноз пациентов крайне неутешителен. Основными проблемами остаются краткосрочные ремиссии после стандартной химиотерапии, «взрывное» развитие рецидива, сочетанная токсичность химиотерапии и первой ТГСК, отсутствие донора для повторной трансплантации. Возможная альтернатива стандартной химиотерапии – применение блокаторов PD-1, потенциирующих иммуный ответ, что позволяет рассчитывать на усиление эффекта «трансплантат против лейкемии» у пациентов с рецидивами онкогематологических заболеваний после аллогенной ТГСК. Целью наблюдения было оценить эффективность и безопасность применения ниволумаба у данной когорты пациентов.
Методы
Мы ретроспективно проанализировали истории болезни 8 пациентов в возрасте от 3 до 14 лет, получивших терапию ингибиторами PD1 после ТГСК. 6 из них имели диагноз ОМЛ, 1 пациент – диагноз ОЛЛ, 1 пациент – диагноз гепатоспленическая γδ-Т-клеточная лимфома. На момент ТГСК 5 пациентов имели продвинутую стадию заболевания, 2 были в полной ремиссии, и 1 находился в MRD-позитивной ремиссии. Все пациенты получали аллогенную ТГСК (5 пациентов от гаплоидентичного донора, 3 пациента от HLA-идентичного сиблинга). На +30 сутки от ТГСК все пациенты находились в клинико-гематологической и молекулярной ремиссии. У 50% пациентов развилась острая РТПХ 1-2 степени с поражением кожи и ЖКТ. Среднее время до развития рецидива составило 180 (97-420) дней. Развернутый костно-мозговой рецидив был зафиксирован у 6 пациентов, у 2 пациентов был отмечен молекулярный рецидив. Все пациенты получили 1 инъекцию ниволумаба в дозе 3 мг/кг. Один пациент с ОМЛ получил инъекцию ниволумаба, уже находясь в ремиссии после повторной ТГСК, в связи с высоким риском повторного рецидива.
Результаты
Нежелательные явления были зарегистрированы у 6 (75%) пациентов. У двух пациентов развился иммунный менингоэнцефалит, у 1 пациента – иммунный гепатит 4 степени, у 2 пациентов была отмечена РТПХ кожи 3й степени, у 4 пациентов развилась иммунная лихорадка. Четырем пациентам потребовалось назначение системной иммуносупрессивной терапии для борьбы с иммуноопосредованными реакциями. Связанной с токсичностью летальности отмечено не было. Для оценки эффективности терапии после первой инъекции ниволумаба всем пациентам были выполнены костномозговые пункции. Шесть из семи пациентов не ответили на терапию. Среднее время до прогрессирования заболевания составляло 21 день. У пациента 7 лет с ОМЛ, находящегося в ремиссии на момент введения ниволумаба, спустя 2 недели после введения развилась иммунная лихорадка и иммунный менингоэнцефалит с явлениями когнитивных расстройств, дизартрии, мышечной слабости, полностью разрешившийся на фоне пульс-терапии солу-медролом. В настоящее время спустя 1 год 10 месяцев после введения ниволумаба у пациента сохраняется морфологическая MRD негативная ремиссия, выраженной патологии со стороны органов и систем нет. Пациентка 7 лет, находившаяся в развернутом рецидиве ОЛЛ на момент введения ниволумаба, достигла стойкой ремиссии. Однако спустя 14 дней от введения препарата у ребенка развился аутоиммунный гепатит 4 степени, рефрактерный ко всем видам терапии, включая ТАО в СОД 6 Гр. В связи с прогрессирующим фатальным повреждением печени произведена успешная трансплантация печени от родственного донора, на сроке 1 год 3 месяца после введения ниволумаба сохраняется полная ремиссия.
Выводы
Наш небольшой опыт показывает, что применение ингибиторов PD-1 после аллогенной ТГСК связано со значительной токсичностью. Для обеспечения безопасности и эффективности этого подхода требуются дальнейшие проспективные исследования.
Ключевые слова
Аллогенная ТГСК, ингибиторы PD1, рецидив, ОЛЛ, ОМЛ.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20577" ["VALUE"]=> array(2) { ["TEXT"]=> string(160) "Olga O. Molostova, Larisa N. Shelikhova, Mariya A. Alyabieva, Dmitry N. Balashov, Svetlana A. Radygina, Irina I. Kalinina, Michael A. Maschan, Alexei A. Maschan" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(160) "Olga O. Molostova, Larisa N. Shelikhova, Mariya A. Alyabieva, Dmitry N. Balashov, Svetlana A. Radygina, Irina I. Kalinina, Michael A. Maschan, Alexei A. Maschan" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20578" ["VALUE"]=> array(2) { ["TEXT"]=> string(137) "Dmitriy Rogachev National Medical Research Center for Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(131) "Dmitriy Rogachev National Medical Research Center for Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20579" ["VALUE"]=> array(2) { ["TEXT"]=> string(3558) "<h2 style="text-align: justify;">Background</h2> <p style="text-align: justify;"> Patients with posttransplant acute leukemia relapse are hardly curable and the outcome is extremely poor. The effectiveness of standard chemotherapy and donor lymphocyte infusions is limited. A possible alternative to standard chemotherapy and DLI is use of PD-1 inhibitors, which may potentiate the allogeneic immune response in order to harness graft-versus-leukemia effect. </p> <h2 style="text-align: justify;">Methods</h2> <p style="text-align: justify;"> We analyzed retrospectively 8 patients, age 3 to 14 years, who had received therapy with PD-1-inhibitor after HSCT. The cohort included 6 patients with acute myeloid leukemia, 1 pt with acute lymphoblastic leukemia and 1 pt with hepatosplenic gamma/delta T cell lymphoma. At the moment of HSCT 5 patients had an advanced stage of their disease, 2 were in complete remission and 1 had positive minimal residual disease. All patients received allo-HSCT (5 patients from haploidentical donors, 3 patients from HLA-identical siblings). At day +30 after HSCT all patients were in clinical and molecular remission, 50% of the patients developed grade 1-2 acute GVHD with skin and GI impairment. The average time to relapse was 180 (97-420) days. Bone marrow relapse was detected in 6 patients while 2 patients had molecular relapse. All patients received 1 injection of nivolumab at a dose of 3 mg/kg. One patient with AML received the injection of nivolumab already being in the remission after second HSCT because of high risk of relapse. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Adverse events were registered in 6 (75%) patients. Two patients developed immune meningoencephalitis, 1 pt had grade 4 immune-mediated liver toxicity, 2 pt had grade 3 skin GVHD flare and immune fever was registered in 4 pts. Four patients required prolonged systemic immunosuppressive therapy to control immune-mediated adverse effects. No mortality related to checkpoint-inhibitor toxicity was registered. One patient developed progressive liver disease. Bone marrow aspiration was done to evaluate efficiency of therapy after the first injection of nivolumab. Seven patients were evaluable for response. Six of 7 patients did not respond to therapy. Average time to disease progression was 21 days. Stable remission was achieved in 1 patient with ALL who received injection of nivolumab being in the full-blown relapse after HSCT. One year and 3 months later this patient remains in clinical and molecular remission, although immune-mediated liver damage progressed to end-stage liver disease and patient received a successful liver transplantation. Patient with AML received the injection of nivolumab already being in the remission and 22 months after therapy remains in clinical and molecular remission. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> Our limited experience suggests that use of PD-1 inhibitors after allo-HSCT is associated with significant toxicity. Further prospective study is required to establish the safety and efficiency of this approach. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> PD-1 inhibitors, allo-HSCT, relapse, ALL, AML. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3338) "
Background
Patients with posttransplant acute leukemia relapse are hardly curable and the outcome is extremely poor. The effectiveness of standard chemotherapy and donor lymphocyte infusions is limited. A possible alternative to standard chemotherapy and DLI is use of PD-1 inhibitors, which may potentiate the allogeneic immune response in order to harness graft-versus-leukemia effect.
Methods
We analyzed retrospectively 8 patients, age 3 to 14 years, who had received therapy with PD-1-inhibitor after HSCT. The cohort included 6 patients with acute myeloid leukemia, 1 pt with acute lymphoblastic leukemia and 1 pt with hepatosplenic gamma/delta T cell lymphoma. At the moment of HSCT 5 patients had an advanced stage of their disease, 2 were in complete remission and 1 had positive minimal residual disease. All patients received allo-HSCT (5 patients from haploidentical donors, 3 patients from HLA-identical siblings). At day +30 after HSCT all patients were in clinical and molecular remission, 50% of the patients developed grade 1-2 acute GVHD with skin and GI impairment. The average time to relapse was 180 (97-420) days. Bone marrow relapse was detected in 6 patients while 2 patients had molecular relapse. All patients received 1 injection of nivolumab at a dose of 3 mg/kg. One patient with AML received the injection of nivolumab already being in the remission after second HSCT because of high risk of relapse.
Results
Adverse events were registered in 6 (75%) patients. Two patients developed immune meningoencephalitis, 1 pt had grade 4 immune-mediated liver toxicity, 2 pt had grade 3 skin GVHD flare and immune fever was registered in 4 pts. Four patients required prolonged systemic immunosuppressive therapy to control immune-mediated adverse effects. No mortality related to checkpoint-inhibitor toxicity was registered. One patient developed progressive liver disease. Bone marrow aspiration was done to evaluate efficiency of therapy after the first injection of nivolumab. Seven patients were evaluable for response. Six of 7 patients did not respond to therapy. Average time to disease progression was 21 days. Stable remission was achieved in 1 patient with ALL who received injection of nivolumab being in the full-blown relapse after HSCT. One year and 3 months later this patient remains in clinical and molecular remission, although immune-mediated liver damage progressed to end-stage liver disease and patient received a successful liver transplantation. Patient with AML received the injection of nivolumab already being in the remission and 22 months after therapy remains in clinical and molecular remission.
Conclusions
Our limited experience suggests that use of PD-1 inhibitors after allo-HSCT is associated with significant toxicity. Further prospective study is required to establish the safety and efficiency of this approach.
Keywords
PD-1 inhibitors, allo-HSCT, relapse, ALL, AML.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20580" ["VALUE"]=> string(120) "Efficacy and safety of nivolumab-based therapy in children with relapse of hematologic malignancies after allogenic HSCT" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(120) "Efficacy and safety of nivolumab-based therapy in children with relapse of hematologic malignancies after allogenic HSCT" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20795" ["VALUE"]=> string(4) "1433" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1433" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20796" ["VALUE"]=> string(4) "1434" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1434" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20577" ["VALUE"]=> array(2) { ["TEXT"]=> string(160) "Olga O. Molostova, Larisa N. Shelikhova, Mariya A. Alyabieva, Dmitry N. Balashov, Svetlana A. Radygina, Irina I. Kalinina, Michael A. Maschan, Alexei A. Maschan" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(160) "Olga O. Molostova, Larisa N. Shelikhova, Mariya A. Alyabieva, Dmitry N. Balashov, Svetlana A. Radygina, Irina I. Kalinina, Michael A. Maschan, Alexei A. Maschan" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(160) "Olga O. Molostova, Larisa N. Shelikhova, Mariya A. Alyabieva, Dmitry N. Balashov, Svetlana A. Radygina, Irina I. Kalinina, Michael A. Maschan, Alexei A. Maschan" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20579" ["VALUE"]=> array(2) { ["TEXT"]=> string(3558) "<h2 style="text-align: justify;">Background</h2> <p style="text-align: justify;"> Patients with posttransplant acute leukemia relapse are hardly curable and the outcome is extremely poor. The effectiveness of standard chemotherapy and donor lymphocyte infusions is limited. A possible alternative to standard chemotherapy and DLI is use of PD-1 inhibitors, which may potentiate the allogeneic immune response in order to harness graft-versus-leukemia effect. </p> <h2 style="text-align: justify;">Methods</h2> <p style="text-align: justify;"> We analyzed retrospectively 8 patients, age 3 to 14 years, who had received therapy with PD-1-inhibitor after HSCT. The cohort included 6 patients with acute myeloid leukemia, 1 pt with acute lymphoblastic leukemia and 1 pt with hepatosplenic gamma/delta T cell lymphoma. At the moment of HSCT 5 patients had an advanced stage of their disease, 2 were in complete remission and 1 had positive minimal residual disease. All patients received allo-HSCT (5 patients from haploidentical donors, 3 patients from HLA-identical siblings). At day +30 after HSCT all patients were in clinical and molecular remission, 50% of the patients developed grade 1-2 acute GVHD with skin and GI impairment. The average time to relapse was 180 (97-420) days. Bone marrow relapse was detected in 6 patients while 2 patients had molecular relapse. All patients received 1 injection of nivolumab at a dose of 3 mg/kg. One patient with AML received the injection of nivolumab already being in the remission after second HSCT because of high risk of relapse. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Adverse events were registered in 6 (75%) patients. Two patients developed immune meningoencephalitis, 1 pt had grade 4 immune-mediated liver toxicity, 2 pt had grade 3 skin GVHD flare and immune fever was registered in 4 pts. Four patients required prolonged systemic immunosuppressive therapy to control immune-mediated adverse effects. No mortality related to checkpoint-inhibitor toxicity was registered. One patient developed progressive liver disease. Bone marrow aspiration was done to evaluate efficiency of therapy after the first injection of nivolumab. Seven patients were evaluable for response. Six of 7 patients did not respond to therapy. Average time to disease progression was 21 days. Stable remission was achieved in 1 patient with ALL who received injection of nivolumab being in the full-blown relapse after HSCT. One year and 3 months later this patient remains in clinical and molecular remission, although immune-mediated liver damage progressed to end-stage liver disease and patient received a successful liver transplantation. Patient with AML received the injection of nivolumab already being in the remission and 22 months after therapy remains in clinical and molecular remission. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> Our limited experience suggests that use of PD-1 inhibitors after allo-HSCT is associated with significant toxicity. Further prospective study is required to establish the safety and efficiency of this approach. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> PD-1 inhibitors, allo-HSCT, relapse, ALL, AML. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3338) "Background
Patients with posttransplant acute leukemia relapse are hardly curable and the outcome is extremely poor. The effectiveness of standard chemotherapy and donor lymphocyte infusions is limited. A possible alternative to standard chemotherapy and DLI is use of PD-1 inhibitors, which may potentiate the allogeneic immune response in order to harness graft-versus-leukemia effect.
Methods
We analyzed retrospectively 8 patients, age 3 to 14 years, who had received therapy with PD-1-inhibitor after HSCT. The cohort included 6 patients with acute myeloid leukemia, 1 pt with acute lymphoblastic leukemia and 1 pt with hepatosplenic gamma/delta T cell lymphoma. At the moment of HSCT 5 patients had an advanced stage of their disease, 2 were in complete remission and 1 had positive minimal residual disease. All patients received allo-HSCT (5 patients from haploidentical donors, 3 patients from HLA-identical siblings). At day +30 after HSCT all patients were in clinical and molecular remission, 50% of the patients developed grade 1-2 acute GVHD with skin and GI impairment. The average time to relapse was 180 (97-420) days. Bone marrow relapse was detected in 6 patients while 2 patients had molecular relapse. All patients received 1 injection of nivolumab at a dose of 3 mg/kg. One patient with AML received the injection of nivolumab already being in the remission after second HSCT because of high risk of relapse.
Results
Adverse events were registered in 6 (75%) patients. Two patients developed immune meningoencephalitis, 1 pt had grade 4 immune-mediated liver toxicity, 2 pt had grade 3 skin GVHD flare and immune fever was registered in 4 pts. Four patients required prolonged systemic immunosuppressive therapy to control immune-mediated adverse effects. No mortality related to checkpoint-inhibitor toxicity was registered. One patient developed progressive liver disease. Bone marrow aspiration was done to evaluate efficiency of therapy after the first injection of nivolumab. Seven patients were evaluable for response. Six of 7 patients did not respond to therapy. Average time to disease progression was 21 days. Stable remission was achieved in 1 patient with ALL who received injection of nivolumab being in the full-blown relapse after HSCT. One year and 3 months later this patient remains in clinical and molecular remission, although immune-mediated liver damage progressed to end-stage liver disease and patient received a successful liver transplantation. Patient with AML received the injection of nivolumab already being in the remission and 22 months after therapy remains in clinical and molecular remission.
Conclusions
Our limited experience suggests that use of PD-1 inhibitors after allo-HSCT is associated with significant toxicity. Further prospective study is required to establish the safety and efficiency of this approach.
Keywords
PD-1 inhibitors, allo-HSCT, relapse, ALL, AML.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3338) "Background
Patients with posttransplant acute leukemia relapse are hardly curable and the outcome is extremely poor. The effectiveness of standard chemotherapy and donor lymphocyte infusions is limited. A possible alternative to standard chemotherapy and DLI is use of PD-1 inhibitors, which may potentiate the allogeneic immune response in order to harness graft-versus-leukemia effect.
Methods
We analyzed retrospectively 8 patients, age 3 to 14 years, who had received therapy with PD-1-inhibitor after HSCT. The cohort included 6 patients with acute myeloid leukemia, 1 pt with acute lymphoblastic leukemia and 1 pt with hepatosplenic gamma/delta T cell lymphoma. At the moment of HSCT 5 patients had an advanced stage of their disease, 2 were in complete remission and 1 had positive minimal residual disease. All patients received allo-HSCT (5 patients from haploidentical donors, 3 patients from HLA-identical siblings). At day +30 after HSCT all patients were in clinical and molecular remission, 50% of the patients developed grade 1-2 acute GVHD with skin and GI impairment. The average time to relapse was 180 (97-420) days. Bone marrow relapse was detected in 6 patients while 2 patients had molecular relapse. All patients received 1 injection of nivolumab at a dose of 3 mg/kg. One patient with AML received the injection of nivolumab already being in the remission after second HSCT because of high risk of relapse.
Results
Adverse events were registered in 6 (75%) patients. Two patients developed immune meningoencephalitis, 1 pt had grade 4 immune-mediated liver toxicity, 2 pt had grade 3 skin GVHD flare and immune fever was registered in 4 pts. Four patients required prolonged systemic immunosuppressive therapy to control immune-mediated adverse effects. No mortality related to checkpoint-inhibitor toxicity was registered. One patient developed progressive liver disease. Bone marrow aspiration was done to evaluate efficiency of therapy after the first injection of nivolumab. Seven patients were evaluable for response. Six of 7 patients did not respond to therapy. Average time to disease progression was 21 days. Stable remission was achieved in 1 patient with ALL who received injection of nivolumab being in the full-blown relapse after HSCT. One year and 3 months later this patient remains in clinical and molecular remission, although immune-mediated liver damage progressed to end-stage liver disease and patient received a successful liver transplantation. Patient with AML received the injection of nivolumab already being in the remission and 22 months after therapy remains in clinical and molecular remission.
Conclusions
Our limited experience suggests that use of PD-1 inhibitors after allo-HSCT is associated with significant toxicity. Further prospective study is required to establish the safety and efficiency of this approach.
Keywords
PD-1 inhibitors, allo-HSCT, relapse, ALL, AML.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20580" ["VALUE"]=> string(120) "Efficacy and safety of nivolumab-based therapy in children with relapse of hematologic malignancies after allogenic HSCT" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(120) "Efficacy and safety of nivolumab-based therapy in children with relapse of hematologic malignancies after allogenic HSCT" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(120) "Efficacy and safety of nivolumab-based therapy in children with relapse of hematologic malignancies after allogenic HSCT" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20578" ["VALUE"]=> array(2) { ["TEXT"]=> string(137) "Dmitriy Rogachev National Medical Research Center for Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(131) "Dmitriy Rogachev National Medical Research Center for Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(131) "Dmitriy Rogachev National Medical Research Center for Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20574" ["VALUE"]=> array(2) { ["TEXT"]=> string(272) "Ольга О. Молостова, Лариса Н. Шелихова, Мария А. Алябьева, Дмитрий Н. Балашов, Светлана А. Радыгина, Ирина И. Калинина, Михаил А. Масчан, Алексей А. Масчан" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(272) "Ольга О. Молостова, Лариса Н. Шелихова, Мария А. Алябьева, Дмитрий Н. Балашов, Светлана А. Радыгина, Ирина И. Калинина, Михаил А. Масчан, Алексей А. Масчан" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(272) "Ольга О. Молостова, Лариса Н. Шелихова, Мария А. Алябьева, Дмитрий Н. Балашов, Светлана А. Радыгина, Ирина И. Калинина, Михаил А. Масчан, Алексей А. Масчан" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20576" ["VALUE"]=> array(2) { ["TEXT"]=> string(7440) "<h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Рецидивы острых лейкозов и лимфом у реципиентов алло-ТГСК трудно поддаются лечению и прогноз пациентов крайне неутешителен. Основными проблемами остаются краткосрочные ремиссии после стандартной химиотерапии, «взрывное» развитие рецидива, сочетанная токсичность химиотерапии и первой ТГСК, отсутствие донора для повторной трансплантации. Возможная альтернатива стандартной химиотерапии – применение блокаторов PD-1, потенциирующих иммуный ответ, что позволяет рассчитывать на усиление эффекта «трансплантат против лейкемии» у пациентов с рецидивами онкогематологических заболеваний после аллогенной ТГСК. Целью наблюдения было оценить эффективность и безопасность применения ниволумаба у данной когорты пациентов. </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> Мы ретроспективно проанализировали истории болезни 8 пациентов в возрасте от 3 до 14 лет, получивших терапию ингибиторами PD1 после ТГСК. 6 из них имели диагноз ОМЛ, 1 пациент – диагноз ОЛЛ, 1 пациент – диагноз гепатоспленическая γδ-Т-клеточная лимфома. На момент ТГСК 5 пациентов имели продвинутую стадию заболевания, 2 были в полной ремиссии, и 1 находился в MRD-позитивной ремиссии. Все пациенты получали аллогенную ТГСК (5 пациентов от гаплоидентичного донора, 3 пациента от HLA-идентичного сиблинга). На +30 сутки от ТГСК все пациенты находились в клинико-гематологической и молекулярной ремиссии. У 50% пациентов развилась острая РТПХ 1-2 степени с поражением кожи и ЖКТ. Среднее время до развития рецидива составило 180 (97-420) дней. Развернутый костно-мозговой рецидив был зафиксирован у 6 пациентов, у 2 пациентов был отмечен молекулярный рецидив. Все пациенты получили 1 инъекцию ниволумаба в дозе 3 мг/кг. Один пациент с ОМЛ получил инъекцию ниволумаба, уже находясь в ремиссии после повторной ТГСК, в связи с высоким риском повторного рецидива. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Нежелательные явления были зарегистрированы у 6 (75%) пациентов. У двух пациентов развился иммунный менингоэнцефалит, у 1 пациента – иммунный гепатит 4 степени, у 2 пациентов была отмечена РТПХ кожи 3й степени, у 4 пациентов развилась иммунная лихорадка. Четырем пациентам потребовалось назначение системной иммуносупрессивной терапии для борьбы с иммуноопосредованными реакциями. Связанной с токсичностью летальности отмечено не было. Для оценки эффективности терапии после первой инъекции ниволумаба всем пациентам были выполнены костномозговые пункции. Шесть из семи пациентов не ответили на терапию. Среднее время до прогрессирования заболевания составляло 21 день. У пациента 7 лет с ОМЛ, находящегося в ремиссии на момент введения ниволумаба, спустя 2 недели после введения развилась иммунная лихорадка и иммунный менингоэнцефалит с явлениями когнитивных расстройств, дизартрии, мышечной слабости, полностью разрешившийся на фоне пульс-терапии солу-медролом. В настоящее время спустя 1 год 10 месяцев после введения ниволумаба у пациента сохраняется морфологическая MRD негативная ремиссия, выраженной патологии со стороны органов и систем нет. Пациентка 7 лет, находившаяся в развернутом рецидиве ОЛЛ на момент введения ниволумаба, достигла стойкой ремиссии. Однако спустя 14 дней от введения препарата у ребенка развился аутоиммунный гепатит 4 степени, рефрактерный ко всем видам терапии, включая ТАО в СОД 6 Гр. В связи с прогрессирующим фатальным повреждением печени произведена успешная трансплантация печени от родственного донора, на сроке 1 год 3 месяца после введения ниволумаба сохраняется полная ремиссия. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Наш небольшой опыт показывает, что применение ингибиторов PD-1 после аллогенной ТГСК связано со значительной токсичностью. Для обеспечения безопасности и эффективности этого подхода требуются дальнейшие проспективные исследования. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Аллогенная ТГСК, ингибиторы PD1, рецидив, ОЛЛ, ОМЛ. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7220) "
Введение
Рецидивы острых лейкозов и лимфом у реципиентов алло-ТГСК трудно поддаются лечению и прогноз пациентов крайне неутешителен. Основными проблемами остаются краткосрочные ремиссии после стандартной химиотерапии, «взрывное» развитие рецидива, сочетанная токсичность химиотерапии и первой ТГСК, отсутствие донора для повторной трансплантации. Возможная альтернатива стандартной химиотерапии – применение блокаторов PD-1, потенциирующих иммуный ответ, что позволяет рассчитывать на усиление эффекта «трансплантат против лейкемии» у пациентов с рецидивами онкогематологических заболеваний после аллогенной ТГСК. Целью наблюдения было оценить эффективность и безопасность применения ниволумаба у данной когорты пациентов.
Методы
Мы ретроспективно проанализировали истории болезни 8 пациентов в возрасте от 3 до 14 лет, получивших терапию ингибиторами PD1 после ТГСК. 6 из них имели диагноз ОМЛ, 1 пациент – диагноз ОЛЛ, 1 пациент – диагноз гепатоспленическая γδ-Т-клеточная лимфома. На момент ТГСК 5 пациентов имели продвинутую стадию заболевания, 2 были в полной ремиссии, и 1 находился в MRD-позитивной ремиссии. Все пациенты получали аллогенную ТГСК (5 пациентов от гаплоидентичного донора, 3 пациента от HLA-идентичного сиблинга). На +30 сутки от ТГСК все пациенты находились в клинико-гематологической и молекулярной ремиссии. У 50% пациентов развилась острая РТПХ 1-2 степени с поражением кожи и ЖКТ. Среднее время до развития рецидива составило 180 (97-420) дней. Развернутый костно-мозговой рецидив был зафиксирован у 6 пациентов, у 2 пациентов был отмечен молекулярный рецидив. Все пациенты получили 1 инъекцию ниволумаба в дозе 3 мг/кг. Один пациент с ОМЛ получил инъекцию ниволумаба, уже находясь в ремиссии после повторной ТГСК, в связи с высоким риском повторного рецидива.
Результаты
Нежелательные явления были зарегистрированы у 6 (75%) пациентов. У двух пациентов развился иммунный менингоэнцефалит, у 1 пациента – иммунный гепатит 4 степени, у 2 пациентов была отмечена РТПХ кожи 3й степени, у 4 пациентов развилась иммунная лихорадка. Четырем пациентам потребовалось назначение системной иммуносупрессивной терапии для борьбы с иммуноопосредованными реакциями. Связанной с токсичностью летальности отмечено не было. Для оценки эффективности терапии после первой инъекции ниволумаба всем пациентам были выполнены костномозговые пункции. Шесть из семи пациентов не ответили на терапию. Среднее время до прогрессирования заболевания составляло 21 день. У пациента 7 лет с ОМЛ, находящегося в ремиссии на момент введения ниволумаба, спустя 2 недели после введения развилась иммунная лихорадка и иммунный менингоэнцефалит с явлениями когнитивных расстройств, дизартрии, мышечной слабости, полностью разрешившийся на фоне пульс-терапии солу-медролом. В настоящее время спустя 1 год 10 месяцев после введения ниволумаба у пациента сохраняется морфологическая MRD негативная ремиссия, выраженной патологии со стороны органов и систем нет. Пациентка 7 лет, находившаяся в развернутом рецидиве ОЛЛ на момент введения ниволумаба, достигла стойкой ремиссии. Однако спустя 14 дней от введения препарата у ребенка развился аутоиммунный гепатит 4 степени, рефрактерный ко всем видам терапии, включая ТАО в СОД 6 Гр. В связи с прогрессирующим фатальным повреждением печени произведена успешная трансплантация печени от родственного донора, на сроке 1 год 3 месяца после введения ниволумаба сохраняется полная ремиссия.
Выводы
Наш небольшой опыт показывает, что применение ингибиторов PD-1 после аллогенной ТГСК связано со значительной токсичностью. Для обеспечения безопасности и эффективности этого подхода требуются дальнейшие проспективные исследования.
Ключевые слова
Аллогенная ТГСК, ингибиторы PD1, рецидив, ОЛЛ, ОМЛ.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(7220) "Введение
Рецидивы острых лейкозов и лимфом у реципиентов алло-ТГСК трудно поддаются лечению и прогноз пациентов крайне неутешителен. Основными проблемами остаются краткосрочные ремиссии после стандартной химиотерапии, «взрывное» развитие рецидива, сочетанная токсичность химиотерапии и первой ТГСК, отсутствие донора для повторной трансплантации. Возможная альтернатива стандартной химиотерапии – применение блокаторов PD-1, потенциирующих иммуный ответ, что позволяет рассчитывать на усиление эффекта «трансплантат против лейкемии» у пациентов с рецидивами онкогематологических заболеваний после аллогенной ТГСК. Целью наблюдения было оценить эффективность и безопасность применения ниволумаба у данной когорты пациентов.
Методы
Мы ретроспективно проанализировали истории болезни 8 пациентов в возрасте от 3 до 14 лет, получивших терапию ингибиторами PD1 после ТГСК. 6 из них имели диагноз ОМЛ, 1 пациент – диагноз ОЛЛ, 1 пациент – диагноз гепатоспленическая γδ-Т-клеточная лимфома. На момент ТГСК 5 пациентов имели продвинутую стадию заболевания, 2 были в полной ремиссии, и 1 находился в MRD-позитивной ремиссии. Все пациенты получали аллогенную ТГСК (5 пациентов от гаплоидентичного донора, 3 пациента от HLA-идентичного сиблинга). На +30 сутки от ТГСК все пациенты находились в клинико-гематологической и молекулярной ремиссии. У 50% пациентов развилась острая РТПХ 1-2 степени с поражением кожи и ЖКТ. Среднее время до развития рецидива составило 180 (97-420) дней. Развернутый костно-мозговой рецидив был зафиксирован у 6 пациентов, у 2 пациентов был отмечен молекулярный рецидив. Все пациенты получили 1 инъекцию ниволумаба в дозе 3 мг/кг. Один пациент с ОМЛ получил инъекцию ниволумаба, уже находясь в ремиссии после повторной ТГСК, в связи с высоким риском повторного рецидива.
Результаты
Нежелательные явления были зарегистрированы у 6 (75%) пациентов. У двух пациентов развился иммунный менингоэнцефалит, у 1 пациента – иммунный гепатит 4 степени, у 2 пациентов была отмечена РТПХ кожи 3й степени, у 4 пациентов развилась иммунная лихорадка. Четырем пациентам потребовалось назначение системной иммуносупрессивной терапии для борьбы с иммуноопосредованными реакциями. Связанной с токсичностью летальности отмечено не было. Для оценки эффективности терапии после первой инъекции ниволумаба всем пациентам были выполнены костномозговые пункции. Шесть из семи пациентов не ответили на терапию. Среднее время до прогрессирования заболевания составляло 21 день. У пациента 7 лет с ОМЛ, находящегося в ремиссии на момент введения ниволумаба, спустя 2 недели после введения развилась иммунная лихорадка и иммунный менингоэнцефалит с явлениями когнитивных расстройств, дизартрии, мышечной слабости, полностью разрешившийся на фоне пульс-терапии солу-медролом. В настоящее время спустя 1 год 10 месяцев после введения ниволумаба у пациента сохраняется морфологическая MRD негативная ремиссия, выраженной патологии со стороны органов и систем нет. Пациентка 7 лет, находившаяся в развернутом рецидиве ОЛЛ на момент введения ниволумаба, достигла стойкой ремиссии. Однако спустя 14 дней от введения препарата у ребенка развился аутоиммунный гепатит 4 степени, рефрактерный ко всем видам терапии, включая ТАО в СОД 6 Гр. В связи с прогрессирующим фатальным повреждением печени произведена успешная трансплантация печени от родственного донора, на сроке 1 год 3 месяца после введения ниволумаба сохраняется полная ремиссия.
Выводы
Наш небольшой опыт показывает, что применение ингибиторов PD-1 после аллогенной ТГСК связано со значительной токсичностью. Для обеспечения безопасности и эффективности этого подхода требуются дальнейшие проспективные исследования.
Ключевые слова
Аллогенная ТГСК, ингибиторы PD1, рецидив, ОЛЛ, ОМЛ.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20575" ["VALUE"]=> array(2) { ["TEXT"]=> string(271) "ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева», Москва, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(265) "ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева», Москва, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(265) "ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева», Москва, Россия
" } } } [44]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1580" ["~ID"]=> string(4) "1580" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(342) "Модель взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток и центра заготовки трансплантационного материала: опыт ФГБУН КНИИ ГПК ФМБА России" ["~NAME"]=> string(342) "Модель взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток и центра заготовки трансплантационного материала: опыт ФГБУН КНИИ ГПК ФМБА России" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:38:35" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:38:35" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/model-vzaimodeystviya-regionalnogo-registra-potentsialnykh-donorov-gemopoeticheskikh-stvolovykh-klet/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/model-vzaimodeystviya-regionalnogo-registra-potentsialnykh-donorov-gemopoeticheskikh-stvolovykh-klet/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "model-vzaimodeystviya-regionalnogo-registra-potentsialnykh-donorov-gemopoeticheskikh-stvolovykh-klet" ["~CODE"]=> string(100) "model-vzaimodeystviya-regionalnogo-registra-potentsialnykh-donorov-gemopoeticheskikh-stvolovykh-klet" ["EXTERNAL_ID"]=> string(4) "1580" ["~EXTERNAL_ID"]=> string(4) "1580" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(342) "Модель взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток и центра заготовки трансплантационного материала: опыт ФГБУН КНИИ ГПК ФМБА России" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(554) "Модель взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток и центра заготовки трансплантационного материала: опыт ФГБУН КНИИ ГПК ФМБА РоссииA model for interaction between hematopoietic stem cells potential donor’s regional registry and transplant material harvesting center: experience of Kirov Research Institute of Hematology and Blood Transfusion" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(8875) "<h2></h2> <h2 style="text-align: justify;">Актуальность</h2> <p style="text-align: justify;"> В настоящее время потребность отечественного здравоохранения в аллогенных трансплантациях костного мозга удовлетворяются в недостаточном объеме. Необходимым условием выполнения алло-ТГСК является наличие HLA-совместимого донора. В случае отсутствия такового среди родственников, осуществляется поиск неродственного донора и преимущественно в зарубежных регистрах. Практика привлечения российских доноров крайне незначительна, что обусловлено малочисленностью локальных регистров, отсутствием научно-обоснованных подходов к их наполнению, учитывающих генетическое разнообразие доноров и обеспечиваемых контингентов, отсутствием отлаженного механизма обследования совместимых доноров, получения, хранения, транспортировки гемопоэтического материала, с учетом территориальной разобщенности трансплантационного центра и места проживания донора. Учитывая это, требуется создать собственную систему, соответствующую принципам отечественного здравоохранения. В настоящей работе представлен 5 летний опыт взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России. </p> <h2 style="text-align: justify;">Цель исследования</h2> <p style="text-align: justify;"> Анализ эффективности взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России в рамках организации обеспечения трансплантационных центров РФ клеточным материалом от российскихнеродственных доноров. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Общая численность регистра потенциальных доноров ГСК на 1.07.18 составила 35649 человек. Это 43,3% от всех протипированных в РФ неродственных доноров. За период 2013-2018 гг. нами произведено 118 заготовок клеточного материала для 10 трансплантационных центров РФ и ближнего зарубежья, что составляет 51,9% от общего числа донаций ГСК от российских неродственных доноров. В 37,1% для получения трансплантата использовалась миелоэксфузия, в остальных 62,9% применялся аппаратный цитаферез. Выбор метода заготовки ГСК определяли, исходя из решения потенциального донора и наличия медицинских противопоказаний, с учетом предпочтений трансплантационного центра. Перед заготовкой трансплантата все доноры ГСК подвергались обследованию на значимые для безопасности реципиента гемотрансмиссивные инфекции. При передаче клеточного материала производилась оценка соответствия количественных и качественных характеристик утвержденной спецификации. При получении ГСК методом аппаратного цитафереза содержание CD34+/кг в трансплантационном материале составило в среднем 6,3x106/кг, при заготовке методом миелоэксфузии – 3,6x106/кг реципиента. Время транспортировки клеточного материала от центра заготовки до трансплантационной клиники составило в среднем 16,3 часа. Согласно представленных трансплантационными клиниками отчетов отклонения количественных показателей от исходных данных были минимальные, составив 1-2% и не зависели от сроков транспортировки. Период от момента активации донора до получения трансплантата занимал не более 8 недель. Все процессы осуществлялись в соответствии с требованиями системы менеджмента качества и комплексом разработанных в учреждении стандартных операционных процедур. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> В результате взаимодействия двух учреждений, подведомственных ФМБА России, реализована российская модель обеспечения трансплантационных центров РФ клеточным материалом для неродственных трансплантаций. Модель подразумевает весь комплекс необходимых мероприятий: от привлечения потенциальных доноров ГСК до оценки качества заготовленного клеточного материала, его транспортировки и порядка передачи в трансплантирующую клинику. Полученные данные свидетельствуют о высокой эффективности созданной системы. Опыт может быть распространен на деятельность других локальных регистров ГСК в РФ и взят за основу при формировании национальной системы обеспечения трансплантационных центров гемопоэтическим материалом от российских неродственных доноров. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Регистр доноров костного мозга, аллогенная трансплантация гемопоэтических стволовых клеток, неродственный донор гемопоэтических стволовых клеток. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(342) "Модель взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток и центра заготовки трансплантационного материала: опыт ФГБУН КНИИ ГПК ФМБА России" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(342) "Модель взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток и центра заготовки трансплантационного материала: опыт ФГБУН КНИИ ГПК ФМБА России" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(342) "Модель взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток и центра заготовки трансплантационного материала: опыт ФГБУН КНИИ ГПК ФМБА России" ["SECTION_META_TITLE"]=> string(342) "Модель взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток и центра заготовки трансплантационного материала: опыт ФГБУН КНИИ ГПК ФМБА России" ["SECTION_META_KEYWORDS"]=> string(342) "Модель взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток и центра заготовки трансплантационного материала: опыт ФГБУН КНИИ ГПК ФМБА России" ["SECTION_META_DESCRIPTION"]=> string(342) "Модель взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток и центра заготовки трансплантационного материала: опыт ФГБУН КНИИ ГПК ФМБА России" ["SECTION_PICTURE_FILE_ALT"]=> string(342) "Модель взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток и центра заготовки трансплантационного материала: опыт ФГБУН КНИИ ГПК ФМБА России" ["SECTION_PICTURE_FILE_TITLE"]=> string(342) "Модель взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток и центра заготовки трансплантационного материала: опыт ФГБУН КНИИ ГПК ФМБА России" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "model-vzaimodeystviya-regionalnogo-registra-potentsialnykh-donorov-gemopoeticheskikh-stvolovykh-klet" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(342) "Модель взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток и центра заготовки трансплантационного материала: опыт ФГБУН КНИИ ГПК ФМБА России" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(342) "Модель взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток и центра заготовки трансплантационного материала: опыт ФГБУН КНИИ ГПК ФМБА России" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "model-vzaimodeystviya-regionalnogo-registra-potentsialnykh-donorov-gemopoeticheskikh-stvolovykh-klet" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "model-vzaimodeystviya-regionalnogo-registra-potentsialnykh-donorov-gemopoeticheskikh-stvolovykh-klet" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "model-vzaimodeystviya-regionalnogo-registra-potentsialnykh-donorov-gemopoeticheskikh-stvolovykh-klet" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20556" ["VALUE"]=> array(2) { ["TEXT"]=> string(404) "Наталья В. Минаева, Мария А. Логинова, Наталья А. Малышева, Наталья А. Зорина, Марина Н. Хоробрых, Филипп С. Шерстнев, Наталья В. Исаева, Елена Н. Калинина, Елена Л. Назарова, Николай М. Поздеев, Андрей В. Рылов, Игорь В. Парамонов" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(404) "Наталья В. Минаева, Мария А. Логинова, Наталья А. Малышева, Наталья А. Зорина, Марина Н. Хоробрых, Филипп С. Шерстнев, Наталья В. Исаева, Елена Н. Калинина, Елена Л. Назарова, Николай М. Поздеев, Андрей В. Рылов, Игорь В. Парамонов" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20557" ["VALUE"]=> array(2) { ["TEXT"]=> string(364) "Федеральное государственное бюджетное учреждение науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства», Киров, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(364) "Федеральное государственное бюджетное учреждение науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства», Киров, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20558" ["VALUE"]=> array(2) { ["TEXT"]=> string(8875) "<h2></h2> <h2 style="text-align: justify;">Актуальность</h2> <p style="text-align: justify;"> В настоящее время потребность отечественного здравоохранения в аллогенных трансплантациях костного мозга удовлетворяются в недостаточном объеме. Необходимым условием выполнения алло-ТГСК является наличие HLA-совместимого донора. В случае отсутствия такового среди родственников, осуществляется поиск неродственного донора и преимущественно в зарубежных регистрах. Практика привлечения российских доноров крайне незначительна, что обусловлено малочисленностью локальных регистров, отсутствием научно-обоснованных подходов к их наполнению, учитывающих генетическое разнообразие доноров и обеспечиваемых контингентов, отсутствием отлаженного механизма обследования совместимых доноров, получения, хранения, транспортировки гемопоэтического материала, с учетом территориальной разобщенности трансплантационного центра и места проживания донора. Учитывая это, требуется создать собственную систему, соответствующую принципам отечественного здравоохранения. В настоящей работе представлен 5 летний опыт взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России. </p> <h2 style="text-align: justify;">Цель исследования</h2> <p style="text-align: justify;"> Анализ эффективности взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России в рамках организации обеспечения трансплантационных центров РФ клеточным материалом от российскихнеродственных доноров. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Общая численность регистра потенциальных доноров ГСК на 1.07.18 составила 35649 человек. Это 43,3% от всех протипированных в РФ неродственных доноров. За период 2013-2018 гг. нами произведено 118 заготовок клеточного материала для 10 трансплантационных центров РФ и ближнего зарубежья, что составляет 51,9% от общего числа донаций ГСК от российских неродственных доноров. В 37,1% для получения трансплантата использовалась миелоэксфузия, в остальных 62,9% применялся аппаратный цитаферез. Выбор метода заготовки ГСК определяли, исходя из решения потенциального донора и наличия медицинских противопоказаний, с учетом предпочтений трансплантационного центра. Перед заготовкой трансплантата все доноры ГСК подвергались обследованию на значимые для безопасности реципиента гемотрансмиссивные инфекции. При передаче клеточного материала производилась оценка соответствия количественных и качественных характеристик утвержденной спецификации. При получении ГСК методом аппаратного цитафереза содержание CD34+/кг в трансплантационном материале составило в среднем 6,3x106/кг, при заготовке методом миелоэксфузии – 3,6x106/кг реципиента. Время транспортировки клеточного материала от центра заготовки до трансплантационной клиники составило в среднем 16,3 часа. Согласно представленных трансплантационными клиниками отчетов отклонения количественных показателей от исходных данных были минимальные, составив 1-2% и не зависели от сроков транспортировки. Период от момента активации донора до получения трансплантата занимал не более 8 недель. Все процессы осуществлялись в соответствии с требованиями системы менеджмента качества и комплексом разработанных в учреждении стандартных операционных процедур. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> В результате взаимодействия двух учреждений, подведомственных ФМБА России, реализована российская модель обеспечения трансплантационных центров РФ клеточным материалом для неродственных трансплантаций. Модель подразумевает весь комплекс необходимых мероприятий: от привлечения потенциальных доноров ГСК до оценки качества заготовленного клеточного материала, его транспортировки и порядка передачи в трансплантирующую клинику. Полученные данные свидетельствуют о высокой эффективности созданной системы. Опыт может быть распространен на деятельность других локальных регистров ГСК в РФ и взят за основу при формировании национальной системы обеспечения трансплантационных центров гемопоэтическим материалом от российских неродственных доноров. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Регистр доноров костного мозга, аллогенная трансплантация гемопоэтических стволовых клеток, неродственный донор гемопоэтических стволовых клеток. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(8643) "
Актуальность
В настоящее время потребность отечественного здравоохранения в аллогенных трансплантациях костного мозга удовлетворяются в недостаточном объеме. Необходимым условием выполнения алло-ТГСК является наличие HLA-совместимого донора. В случае отсутствия такового среди родственников, осуществляется поиск неродственного донора и преимущественно в зарубежных регистрах. Практика привлечения российских доноров крайне незначительна, что обусловлено малочисленностью локальных регистров, отсутствием научно-обоснованных подходов к их наполнению, учитывающих генетическое разнообразие доноров и обеспечиваемых контингентов, отсутствием отлаженного механизма обследования совместимых доноров, получения, хранения, транспортировки гемопоэтического материала, с учетом территориальной разобщенности трансплантационного центра и места проживания донора. Учитывая это, требуется создать собственную систему, соответствующую принципам отечественного здравоохранения. В настоящей работе представлен 5 летний опыт взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России.
Цель исследования
Анализ эффективности взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России в рамках организации обеспечения трансплантационных центров РФ клеточным материалом от российскихнеродственных доноров.
Результаты
Общая численность регистра потенциальных доноров ГСК на 1.07.18 составила 35649 человек. Это 43,3% от всех протипированных в РФ неродственных доноров. За период 2013-2018 гг. нами произведено 118 заготовок клеточного материала для 10 трансплантационных центров РФ и ближнего зарубежья, что составляет 51,9% от общего числа донаций ГСК от российских неродственных доноров. В 37,1% для получения трансплантата использовалась миелоэксфузия, в остальных 62,9% применялся аппаратный цитаферез. Выбор метода заготовки ГСК определяли, исходя из решения потенциального донора и наличия медицинских противопоказаний, с учетом предпочтений трансплантационного центра. Перед заготовкой трансплантата все доноры ГСК подвергались обследованию на значимые для безопасности реципиента гемотрансмиссивные инфекции. При передаче клеточного материала производилась оценка соответствия количественных и качественных характеристик утвержденной спецификации. При получении ГСК методом аппаратного цитафереза содержание CD34+/кг в трансплантационном материале составило в среднем 6,3x106/кг, при заготовке методом миелоэксфузии – 3,6x106/кг реципиента. Время транспортировки клеточного материала от центра заготовки до трансплантационной клиники составило в среднем 16,3 часа. Согласно представленных трансплантационными клиниками отчетов отклонения количественных показателей от исходных данных были минимальные, составив 1-2% и не зависели от сроков транспортировки. Период от момента активации донора до получения трансплантата занимал не более 8 недель. Все процессы осуществлялись в соответствии с требованиями системы менеджмента качества и комплексом разработанных в учреждении стандартных операционных процедур.
Заключение
В результате взаимодействия двух учреждений, подведомственных ФМБА России, реализована российская модель обеспечения трансплантационных центров РФ клеточным материалом для неродственных трансплантаций. Модель подразумевает весь комплекс необходимых мероприятий: от привлечения потенциальных доноров ГСК до оценки качества заготовленного клеточного материала, его транспортировки и порядка передачи в трансплантирующую клинику. Полученные данные свидетельствуют о высокой эффективности созданной системы. Опыт может быть распространен на деятельность других локальных регистров ГСК в РФ и взят за основу при формировании национальной системы обеспечения трансплантационных центров гемопоэтическим материалом от российских неродственных доноров.
Ключевые слова
Регистр доноров костного мозга, аллогенная трансплантация гемопоэтических стволовых клеток, неродственный донор гемопоэтических стволовых клеток.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20559" ["VALUE"]=> array(2) { ["TEXT"]=> string(235) "Natalia V. Minaeva, Maria A. Loginova, Natalia A. Malysheva, Natalia A. Zorina, Marina N. Khorobrykh, Philipp S. Sherstnev, Natalia V. Isaeva, Elena N. Kalinina, Elena L. Nazarova, Nikolay M. Pozdeev, Andrey V. Rylov, Igor V. Paramonov" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(235) "Natalia V. Minaeva, Maria A. Loginova, Natalia A. Malysheva, Natalia A. Zorina, Marina N. Khorobrykh, Philipp S. Sherstnev, Natalia V. Isaeva, Elena N. Kalinina, Elena L. Nazarova, Nikolay M. Pozdeev, Andrey V. Rylov, Igor V. Paramonov" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20560" ["VALUE"]=> array(2) { ["TEXT"]=> string(87) "Kirov Research Institute of Hematology and Blood Transfusion, Kirov, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(87) "Kirov Research Institute of Hematology and Blood Transfusion, Kirov, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20561" ["VALUE"]=> array(2) { ["TEXT"]=> string(4863) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> At present, the need for national health care in allogeneic bone marrow transplantation is insufficiently met. A necessary condition for performing of allogeneic hematopoietic stem cell transplantation (allo-HSCT) is the presence of an HLA-matched donor. In the absence of such among relatives, an unrelated donor is sought and mainly in foreign registries. The practice of attracting Russian donors is extremely low, due to the small number of local registries, the lack of scientifically based approaches to filling them, taking into account the genetic diversity of donors and provided contingents, the lack of a well-functioning mechanism for examining matched donors, obtaining, storing, transporting the hemopoietic material, taking into account the territorial disconnection of the transplantation center and place of donor residence. Considering this, it is required to create system that meets the national healthcare principles. This paper represents 5-year experience of hematopoietic stem cells (HSC) potential donors regional registry of the Federal State Facility “Russian Medical Research and Production Center “Rosplasma” in Kirov and the center for the transplant material harvesting on the basis of the Federal State Institute of Science “Kirov Research Institute of Hematology and Blood Transfusion” subordinating to the Federal Medical and Biological Agency of Russia. The aim of the research is analysis of the effectiveness of interaction between HSC donor regional registry and the center for the transplant material harvesting in providing of russian transplant centers with cellular material from russian unrelated donors, based on the 5-year experience. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The total number of potential donors in the HSC regional registry on July 1, 2018 was 35,649 persons. This is 43.3% of all HLA-genotyped unrelated potential donors in Russia. From 2013 to 2018 we performed 118 cellular material harvests for 10 transplant centers in Russia and the near abroad countries, this represents 51.9% of the total number of HSC donations from Russian unrelated donors. In 37.1% for the graft preparation bone marrow was collected, in the remaining 62.9% – apheresis was used. Selection of the HSC harvesting method was based upon decision of the potential donor with consideration of medical contraindications, and the transplantation center preferences. Before the graft preparation, all HSC donors were screened for significant bloodborne infections. Before issuing of cellular material consistency with approved specification of the quantitative and qualitative characteristics were assessed. In apheresis collection the CD34+-cells content in the transplantation material averaged 5.3x106/kg, in marrow collection – 3.6x106/kg of the patient’s weight. The duration of transport of the cellular material from the harvesting center to the transplant clinic was 16.3 hours on average. According to the reports, submitted by the transplant clinics, the deviations of the quantitative indicators from the initial data were minimal, amounting to 1-2% and did not depend on the transportation period. The time span from the donor activation to transplant delivery was less than 8 weeks. All processes were carried out in accordance with requirements of the quality management system and a set of standard operating procedures developed in the institution. </p> <p style="text-align: justify;"> <span style="font-family: Cuprum, sans-serif; font-size: 26px;">Conclusion</span> </p> <p style="text-align: justify;"> Interaction pattern between two institutions, subordinating to the Federal Medical and Biological Agency of Russia, is the basis of Russian model of cellular material providing for unrelated transplantations for clinics in Russian Federation. This model implies the whole complex of necessary measures: recruitment of potential donors, assessing the quality of harvested cellular material, its distribution and shipment to transplant clinic. The received data testify to high efficiency of the created system. Experience could be extended to the practice of other local HSC registers in Russia and taken as a basis for the national hematopoietic material providing system formation. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Donor’s bone marrow registry, allogeneic hematopoietic stem cell transplantation, unrelated donor hematopoietic stem cells. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4653) "Introduction
At present, the need for national health care in allogeneic bone marrow transplantation is insufficiently met. A necessary condition for performing of allogeneic hematopoietic stem cell transplantation (allo-HSCT) is the presence of an HLA-matched donor. In the absence of such among relatives, an unrelated donor is sought and mainly in foreign registries. The practice of attracting Russian donors is extremely low, due to the small number of local registries, the lack of scientifically based approaches to filling them, taking into account the genetic diversity of donors and provided contingents, the lack of a well-functioning mechanism for examining matched donors, obtaining, storing, transporting the hemopoietic material, taking into account the territorial disconnection of the transplantation center and place of donor residence. Considering this, it is required to create system that meets the national healthcare principles. This paper represents 5-year experience of hematopoietic stem cells (HSC) potential donors regional registry of the Federal State Facility “Russian Medical Research and Production Center “Rosplasma” in Kirov and the center for the transplant material harvesting on the basis of the Federal State Institute of Science “Kirov Research Institute of Hematology and Blood Transfusion” subordinating to the Federal Medical and Biological Agency of Russia. The aim of the research is analysis of the effectiveness of interaction between HSC donor regional registry and the center for the transplant material harvesting in providing of russian transplant centers with cellular material from russian unrelated donors, based on the 5-year experience.
Results
The total number of potential donors in the HSC regional registry on July 1, 2018 was 35,649 persons. This is 43.3% of all HLA-genotyped unrelated potential donors in Russia. From 2013 to 2018 we performed 118 cellular material harvests for 10 transplant centers in Russia and the near abroad countries, this represents 51.9% of the total number of HSC donations from Russian unrelated donors. In 37.1% for the graft preparation bone marrow was collected, in the remaining 62.9% – apheresis was used. Selection of the HSC harvesting method was based upon decision of the potential donor with consideration of medical contraindications, and the transplantation center preferences. Before the graft preparation, all HSC donors were screened for significant bloodborne infections. Before issuing of cellular material consistency with approved specification of the quantitative and qualitative characteristics were assessed. In apheresis collection the CD34+-cells content in the transplantation material averaged 5.3x106/kg, in marrow collection – 3.6x106/kg of the patient’s weight. The duration of transport of the cellular material from the harvesting center to the transplant clinic was 16.3 hours on average. According to the reports, submitted by the transplant clinics, the deviations of the quantitative indicators from the initial data were minimal, amounting to 1-2% and did not depend on the transportation period. The time span from the donor activation to transplant delivery was less than 8 weeks. All processes were carried out in accordance with requirements of the quality management system and a set of standard operating procedures developed in the institution.
Conclusion
Interaction pattern between two institutions, subordinating to the Federal Medical and Biological Agency of Russia, is the basis of Russian model of cellular material providing for unrelated transplantations for clinics in Russian Federation. This model implies the whole complex of necessary measures: recruitment of potential donors, assessing the quality of harvested cellular material, its distribution and shipment to transplant clinic. The received data testify to high efficiency of the created system. Experience could be extended to the practice of other local HSC registers in Russia and taken as a basis for the national hematopoietic material providing system formation.
Keywords
Donor’s bone marrow registry, allogeneic hematopoietic stem cell transplantation, unrelated donor hematopoietic stem cells.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20562" ["VALUE"]=> string(212) "A model for interaction between hematopoietic stem cells potential donor’s regional registry and transplant material harvesting center: experience of Kirov Research Institute of Hematology and Blood Transfusion" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(212) "A model for interaction between hematopoietic stem cells potential donor’s regional registry and transplant material harvesting center: experience of Kirov Research Institute of Hematology and Blood Transfusion" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20791" ["VALUE"]=> string(4) "1429" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1429" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20792" ["VALUE"]=> string(4) "1430" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1430" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20559" ["VALUE"]=> array(2) { ["TEXT"]=> string(235) "Natalia V. Minaeva, Maria A. Loginova, Natalia A. Malysheva, Natalia A. Zorina, Marina N. Khorobrykh, Philipp S. Sherstnev, Natalia V. Isaeva, Elena N. Kalinina, Elena L. Nazarova, Nikolay M. Pozdeev, Andrey V. Rylov, Igor V. Paramonov" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(235) "Natalia V. Minaeva, Maria A. Loginova, Natalia A. Malysheva, Natalia A. Zorina, Marina N. Khorobrykh, Philipp S. Sherstnev, Natalia V. Isaeva, Elena N. Kalinina, Elena L. Nazarova, Nikolay M. Pozdeev, Andrey V. Rylov, Igor V. Paramonov" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(235) "Natalia V. Minaeva, Maria A. Loginova, Natalia A. Malysheva, Natalia A. Zorina, Marina N. Khorobrykh, Philipp S. Sherstnev, Natalia V. Isaeva, Elena N. Kalinina, Elena L. Nazarova, Nikolay M. Pozdeev, Andrey V. Rylov, Igor V. Paramonov" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20561" ["VALUE"]=> array(2) { ["TEXT"]=> string(4863) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> At present, the need for national health care in allogeneic bone marrow transplantation is insufficiently met. A necessary condition for performing of allogeneic hematopoietic stem cell transplantation (allo-HSCT) is the presence of an HLA-matched donor. In the absence of such among relatives, an unrelated donor is sought and mainly in foreign registries. The practice of attracting Russian donors is extremely low, due to the small number of local registries, the lack of scientifically based approaches to filling them, taking into account the genetic diversity of donors and provided contingents, the lack of a well-functioning mechanism for examining matched donors, obtaining, storing, transporting the hemopoietic material, taking into account the territorial disconnection of the transplantation center and place of donor residence. Considering this, it is required to create system that meets the national healthcare principles. This paper represents 5-year experience of hematopoietic stem cells (HSC) potential donors regional registry of the Federal State Facility “Russian Medical Research and Production Center “Rosplasma” in Kirov and the center for the transplant material harvesting on the basis of the Federal State Institute of Science “Kirov Research Institute of Hematology and Blood Transfusion” subordinating to the Federal Medical and Biological Agency of Russia. The aim of the research is analysis of the effectiveness of interaction between HSC donor regional registry and the center for the transplant material harvesting in providing of russian transplant centers with cellular material from russian unrelated donors, based on the 5-year experience. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The total number of potential donors in the HSC regional registry on July 1, 2018 was 35,649 persons. This is 43.3% of all HLA-genotyped unrelated potential donors in Russia. From 2013 to 2018 we performed 118 cellular material harvests for 10 transplant centers in Russia and the near abroad countries, this represents 51.9% of the total number of HSC donations from Russian unrelated donors. In 37.1% for the graft preparation bone marrow was collected, in the remaining 62.9% – apheresis was used. Selection of the HSC harvesting method was based upon decision of the potential donor with consideration of medical contraindications, and the transplantation center preferences. Before the graft preparation, all HSC donors were screened for significant bloodborne infections. Before issuing of cellular material consistency with approved specification of the quantitative and qualitative characteristics were assessed. In apheresis collection the CD34+-cells content in the transplantation material averaged 5.3x106/kg, in marrow collection – 3.6x106/kg of the patient’s weight. The duration of transport of the cellular material from the harvesting center to the transplant clinic was 16.3 hours on average. According to the reports, submitted by the transplant clinics, the deviations of the quantitative indicators from the initial data were minimal, amounting to 1-2% and did not depend on the transportation period. The time span from the donor activation to transplant delivery was less than 8 weeks. All processes were carried out in accordance with requirements of the quality management system and a set of standard operating procedures developed in the institution. </p> <p style="text-align: justify;"> <span style="font-family: Cuprum, sans-serif; font-size: 26px;">Conclusion</span> </p> <p style="text-align: justify;"> Interaction pattern between two institutions, subordinating to the Federal Medical and Biological Agency of Russia, is the basis of Russian model of cellular material providing for unrelated transplantations for clinics in Russian Federation. This model implies the whole complex of necessary measures: recruitment of potential donors, assessing the quality of harvested cellular material, its distribution and shipment to transplant clinic. The received data testify to high efficiency of the created system. Experience could be extended to the practice of other local HSC registers in Russia and taken as a basis for the national hematopoietic material providing system formation. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Donor’s bone marrow registry, allogeneic hematopoietic stem cell transplantation, unrelated donor hematopoietic stem cells. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4653) "Introduction
At present, the need for national health care in allogeneic bone marrow transplantation is insufficiently met. A necessary condition for performing of allogeneic hematopoietic stem cell transplantation (allo-HSCT) is the presence of an HLA-matched donor. In the absence of such among relatives, an unrelated donor is sought and mainly in foreign registries. The practice of attracting Russian donors is extremely low, due to the small number of local registries, the lack of scientifically based approaches to filling them, taking into account the genetic diversity of donors and provided contingents, the lack of a well-functioning mechanism for examining matched donors, obtaining, storing, transporting the hemopoietic material, taking into account the territorial disconnection of the transplantation center and place of donor residence. Considering this, it is required to create system that meets the national healthcare principles. This paper represents 5-year experience of hematopoietic stem cells (HSC) potential donors regional registry of the Federal State Facility “Russian Medical Research and Production Center “Rosplasma” in Kirov and the center for the transplant material harvesting on the basis of the Federal State Institute of Science “Kirov Research Institute of Hematology and Blood Transfusion” subordinating to the Federal Medical and Biological Agency of Russia. The aim of the research is analysis of the effectiveness of interaction between HSC donor regional registry and the center for the transplant material harvesting in providing of russian transplant centers with cellular material from russian unrelated donors, based on the 5-year experience.
Results
The total number of potential donors in the HSC regional registry on July 1, 2018 was 35,649 persons. This is 43.3% of all HLA-genotyped unrelated potential donors in Russia. From 2013 to 2018 we performed 118 cellular material harvests for 10 transplant centers in Russia and the near abroad countries, this represents 51.9% of the total number of HSC donations from Russian unrelated donors. In 37.1% for the graft preparation bone marrow was collected, in the remaining 62.9% – apheresis was used. Selection of the HSC harvesting method was based upon decision of the potential donor with consideration of medical contraindications, and the transplantation center preferences. Before the graft preparation, all HSC donors were screened for significant bloodborne infections. Before issuing of cellular material consistency with approved specification of the quantitative and qualitative characteristics were assessed. In apheresis collection the CD34+-cells content in the transplantation material averaged 5.3x106/kg, in marrow collection – 3.6x106/kg of the patient’s weight. The duration of transport of the cellular material from the harvesting center to the transplant clinic was 16.3 hours on average. According to the reports, submitted by the transplant clinics, the deviations of the quantitative indicators from the initial data were minimal, amounting to 1-2% and did not depend on the transportation period. The time span from the donor activation to transplant delivery was less than 8 weeks. All processes were carried out in accordance with requirements of the quality management system and a set of standard operating procedures developed in the institution.
Conclusion
Interaction pattern between two institutions, subordinating to the Federal Medical and Biological Agency of Russia, is the basis of Russian model of cellular material providing for unrelated transplantations for clinics in Russian Federation. This model implies the whole complex of necessary measures: recruitment of potential donors, assessing the quality of harvested cellular material, its distribution and shipment to transplant clinic. The received data testify to high efficiency of the created system. Experience could be extended to the practice of other local HSC registers in Russia and taken as a basis for the national hematopoietic material providing system formation.
Keywords
Donor’s bone marrow registry, allogeneic hematopoietic stem cell transplantation, unrelated donor hematopoietic stem cells.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4653) "Introduction
At present, the need for national health care in allogeneic bone marrow transplantation is insufficiently met. A necessary condition for performing of allogeneic hematopoietic stem cell transplantation (allo-HSCT) is the presence of an HLA-matched donor. In the absence of such among relatives, an unrelated donor is sought and mainly in foreign registries. The practice of attracting Russian donors is extremely low, due to the small number of local registries, the lack of scientifically based approaches to filling them, taking into account the genetic diversity of donors and provided contingents, the lack of a well-functioning mechanism for examining matched donors, obtaining, storing, transporting the hemopoietic material, taking into account the territorial disconnection of the transplantation center and place of donor residence. Considering this, it is required to create system that meets the national healthcare principles. This paper represents 5-year experience of hematopoietic stem cells (HSC) potential donors regional registry of the Federal State Facility “Russian Medical Research and Production Center “Rosplasma” in Kirov and the center for the transplant material harvesting on the basis of the Federal State Institute of Science “Kirov Research Institute of Hematology and Blood Transfusion” subordinating to the Federal Medical and Biological Agency of Russia. The aim of the research is analysis of the effectiveness of interaction between HSC donor regional registry and the center for the transplant material harvesting in providing of russian transplant centers with cellular material from russian unrelated donors, based on the 5-year experience.
Results
The total number of potential donors in the HSC regional registry on July 1, 2018 was 35,649 persons. This is 43.3% of all HLA-genotyped unrelated potential donors in Russia. From 2013 to 2018 we performed 118 cellular material harvests for 10 transplant centers in Russia and the near abroad countries, this represents 51.9% of the total number of HSC donations from Russian unrelated donors. In 37.1% for the graft preparation bone marrow was collected, in the remaining 62.9% – apheresis was used. Selection of the HSC harvesting method was based upon decision of the potential donor with consideration of medical contraindications, and the transplantation center preferences. Before the graft preparation, all HSC donors were screened for significant bloodborne infections. Before issuing of cellular material consistency with approved specification of the quantitative and qualitative characteristics were assessed. In apheresis collection the CD34+-cells content in the transplantation material averaged 5.3x106/kg, in marrow collection – 3.6x106/kg of the patient’s weight. The duration of transport of the cellular material from the harvesting center to the transplant clinic was 16.3 hours on average. According to the reports, submitted by the transplant clinics, the deviations of the quantitative indicators from the initial data were minimal, amounting to 1-2% and did not depend on the transportation period. The time span from the donor activation to transplant delivery was less than 8 weeks. All processes were carried out in accordance with requirements of the quality management system and a set of standard operating procedures developed in the institution.
Conclusion
Interaction pattern between two institutions, subordinating to the Federal Medical and Biological Agency of Russia, is the basis of Russian model of cellular material providing for unrelated transplantations for clinics in Russian Federation. This model implies the whole complex of necessary measures: recruitment of potential donors, assessing the quality of harvested cellular material, its distribution and shipment to transplant clinic. The received data testify to high efficiency of the created system. Experience could be extended to the practice of other local HSC registers in Russia and taken as a basis for the national hematopoietic material providing system formation.
Keywords
Donor’s bone marrow registry, allogeneic hematopoietic stem cell transplantation, unrelated donor hematopoietic stem cells.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20562" ["VALUE"]=> string(212) "A model for interaction between hematopoietic stem cells potential donor’s regional registry and transplant material harvesting center: experience of Kirov Research Institute of Hematology and Blood Transfusion" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(212) "A model for interaction between hematopoietic stem cells potential donor’s regional registry and transplant material harvesting center: experience of Kirov Research Institute of Hematology and Blood Transfusion" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(212) "A model for interaction between hematopoietic stem cells potential donor’s regional registry and transplant material harvesting center: experience of Kirov Research Institute of Hematology and Blood Transfusion" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20560" ["VALUE"]=> array(2) { ["TEXT"]=> string(87) "Kirov Research Institute of Hematology and Blood Transfusion, Kirov, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(87) "Kirov Research Institute of Hematology and Blood Transfusion, Kirov, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(87) "Kirov Research Institute of Hematology and Blood Transfusion, Kirov, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20556" ["VALUE"]=> array(2) { ["TEXT"]=> string(404) "Наталья В. Минаева, Мария А. Логинова, Наталья А. Малышева, Наталья А. Зорина, Марина Н. Хоробрых, Филипп С. Шерстнев, Наталья В. Исаева, Елена Н. Калинина, Елена Л. Назарова, Николай М. Поздеев, Андрей В. Рылов, Игорь В. Парамонов" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(404) "Наталья В. Минаева, Мария А. Логинова, Наталья А. Малышева, Наталья А. Зорина, Марина Н. Хоробрых, Филипп С. Шерстнев, Наталья В. Исаева, Елена Н. Калинина, Елена Л. Назарова, Николай М. Поздеев, Андрей В. Рылов, Игорь В. Парамонов" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(404) "Наталья В. Минаева, Мария А. Логинова, Наталья А. Малышева, Наталья А. Зорина, Марина Н. Хоробрых, Филипп С. Шерстнев, Наталья В. Исаева, Елена Н. Калинина, Елена Л. Назарова, Николай М. Поздеев, Андрей В. Рылов, Игорь В. Парамонов" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20558" ["VALUE"]=> array(2) { ["TEXT"]=> string(8875) "<h2></h2> <h2 style="text-align: justify;">Актуальность</h2> <p style="text-align: justify;"> В настоящее время потребность отечественного здравоохранения в аллогенных трансплантациях костного мозга удовлетворяются в недостаточном объеме. Необходимым условием выполнения алло-ТГСК является наличие HLA-совместимого донора. В случае отсутствия такового среди родственников, осуществляется поиск неродственного донора и преимущественно в зарубежных регистрах. Практика привлечения российских доноров крайне незначительна, что обусловлено малочисленностью локальных регистров, отсутствием научно-обоснованных подходов к их наполнению, учитывающих генетическое разнообразие доноров и обеспечиваемых контингентов, отсутствием отлаженного механизма обследования совместимых доноров, получения, хранения, транспортировки гемопоэтического материала, с учетом территориальной разобщенности трансплантационного центра и места проживания донора. Учитывая это, требуется создать собственную систему, соответствующую принципам отечественного здравоохранения. В настоящей работе представлен 5 летний опыт взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России. </p> <h2 style="text-align: justify;">Цель исследования</h2> <p style="text-align: justify;"> Анализ эффективности взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России в рамках организации обеспечения трансплантационных центров РФ клеточным материалом от российскихнеродственных доноров. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Общая численность регистра потенциальных доноров ГСК на 1.07.18 составила 35649 человек. Это 43,3% от всех протипированных в РФ неродственных доноров. За период 2013-2018 гг. нами произведено 118 заготовок клеточного материала для 10 трансплантационных центров РФ и ближнего зарубежья, что составляет 51,9% от общего числа донаций ГСК от российских неродственных доноров. В 37,1% для получения трансплантата использовалась миелоэксфузия, в остальных 62,9% применялся аппаратный цитаферез. Выбор метода заготовки ГСК определяли, исходя из решения потенциального донора и наличия медицинских противопоказаний, с учетом предпочтений трансплантационного центра. Перед заготовкой трансплантата все доноры ГСК подвергались обследованию на значимые для безопасности реципиента гемотрансмиссивные инфекции. При передаче клеточного материала производилась оценка соответствия количественных и качественных характеристик утвержденной спецификации. При получении ГСК методом аппаратного цитафереза содержание CD34+/кг в трансплантационном материале составило в среднем 6,3x106/кг, при заготовке методом миелоэксфузии – 3,6x106/кг реципиента. Время транспортировки клеточного материала от центра заготовки до трансплантационной клиники составило в среднем 16,3 часа. Согласно представленных трансплантационными клиниками отчетов отклонения количественных показателей от исходных данных были минимальные, составив 1-2% и не зависели от сроков транспортировки. Период от момента активации донора до получения трансплантата занимал не более 8 недель. Все процессы осуществлялись в соответствии с требованиями системы менеджмента качества и комплексом разработанных в учреждении стандартных операционных процедур. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> В результате взаимодействия двух учреждений, подведомственных ФМБА России, реализована российская модель обеспечения трансплантационных центров РФ клеточным материалом для неродственных трансплантаций. Модель подразумевает весь комплекс необходимых мероприятий: от привлечения потенциальных доноров ГСК до оценки качества заготовленного клеточного материала, его транспортировки и порядка передачи в трансплантирующую клинику. Полученные данные свидетельствуют о высокой эффективности созданной системы. Опыт может быть распространен на деятельность других локальных регистров ГСК в РФ и взят за основу при формировании национальной системы обеспечения трансплантационных центров гемопоэтическим материалом от российских неродственных доноров. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Регистр доноров костного мозга, аллогенная трансплантация гемопоэтических стволовых клеток, неродственный донор гемопоэтических стволовых клеток. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(8643) "Актуальность
В настоящее время потребность отечественного здравоохранения в аллогенных трансплантациях костного мозга удовлетворяются в недостаточном объеме. Необходимым условием выполнения алло-ТГСК является наличие HLA-совместимого донора. В случае отсутствия такового среди родственников, осуществляется поиск неродственного донора и преимущественно в зарубежных регистрах. Практика привлечения российских доноров крайне незначительна, что обусловлено малочисленностью локальных регистров, отсутствием научно-обоснованных подходов к их наполнению, учитывающих генетическое разнообразие доноров и обеспечиваемых контингентов, отсутствием отлаженного механизма обследования совместимых доноров, получения, хранения, транспортировки гемопоэтического материала, с учетом территориальной разобщенности трансплантационного центра и места проживания донора. Учитывая это, требуется создать собственную систему, соответствующую принципам отечественного здравоохранения. В настоящей работе представлен 5 летний опыт взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России.
Цель исследования
Анализ эффективности взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России в рамках организации обеспечения трансплантационных центров РФ клеточным материалом от российскихнеродственных доноров.
Результаты
Общая численность регистра потенциальных доноров ГСК на 1.07.18 составила 35649 человек. Это 43,3% от всех протипированных в РФ неродственных доноров. За период 2013-2018 гг. нами произведено 118 заготовок клеточного материала для 10 трансплантационных центров РФ и ближнего зарубежья, что составляет 51,9% от общего числа донаций ГСК от российских неродственных доноров. В 37,1% для получения трансплантата использовалась миелоэксфузия, в остальных 62,9% применялся аппаратный цитаферез. Выбор метода заготовки ГСК определяли, исходя из решения потенциального донора и наличия медицинских противопоказаний, с учетом предпочтений трансплантационного центра. Перед заготовкой трансплантата все доноры ГСК подвергались обследованию на значимые для безопасности реципиента гемотрансмиссивные инфекции. При передаче клеточного материала производилась оценка соответствия количественных и качественных характеристик утвержденной спецификации. При получении ГСК методом аппаратного цитафереза содержание CD34+/кг в трансплантационном материале составило в среднем 6,3x106/кг, при заготовке методом миелоэксфузии – 3,6x106/кг реципиента. Время транспортировки клеточного материала от центра заготовки до трансплантационной клиники составило в среднем 16,3 часа. Согласно представленных трансплантационными клиниками отчетов отклонения количественных показателей от исходных данных были минимальные, составив 1-2% и не зависели от сроков транспортировки. Период от момента активации донора до получения трансплантата занимал не более 8 недель. Все процессы осуществлялись в соответствии с требованиями системы менеджмента качества и комплексом разработанных в учреждении стандартных операционных процедур.
Заключение
В результате взаимодействия двух учреждений, подведомственных ФМБА России, реализована российская модель обеспечения трансплантационных центров РФ клеточным материалом для неродственных трансплантаций. Модель подразумевает весь комплекс необходимых мероприятий: от привлечения потенциальных доноров ГСК до оценки качества заготовленного клеточного материала, его транспортировки и порядка передачи в трансплантирующую клинику. Полученные данные свидетельствуют о высокой эффективности созданной системы. Опыт может быть распространен на деятельность других локальных регистров ГСК в РФ и взят за основу при формировании национальной системы обеспечения трансплантационных центров гемопоэтическим материалом от российских неродственных доноров.
Ключевые слова
Регистр доноров костного мозга, аллогенная трансплантация гемопоэтических стволовых клеток, неродственный донор гемопоэтических стволовых клеток.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(8643) "Актуальность
В настоящее время потребность отечественного здравоохранения в аллогенных трансплантациях костного мозга удовлетворяются в недостаточном объеме. Необходимым условием выполнения алло-ТГСК является наличие HLA-совместимого донора. В случае отсутствия такового среди родственников, осуществляется поиск неродственного донора и преимущественно в зарубежных регистрах. Практика привлечения российских доноров крайне незначительна, что обусловлено малочисленностью локальных регистров, отсутствием научно-обоснованных подходов к их наполнению, учитывающих генетическое разнообразие доноров и обеспечиваемых контингентов, отсутствием отлаженного механизма обследования совместимых доноров, получения, хранения, транспортировки гемопоэтического материала, с учетом территориальной разобщенности трансплантационного центра и места проживания донора. Учитывая это, требуется создать собственную систему, соответствующую принципам отечественного здравоохранения. В настоящей работе представлен 5 летний опыт взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России.
Цель исследования
Анализ эффективности взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России в рамках организации обеспечения трансплантационных центров РФ клеточным материалом от российскихнеродственных доноров.
Результаты
Общая численность регистра потенциальных доноров ГСК на 1.07.18 составила 35649 человек. Это 43,3% от всех протипированных в РФ неродственных доноров. За период 2013-2018 гг. нами произведено 118 заготовок клеточного материала для 10 трансплантационных центров РФ и ближнего зарубежья, что составляет 51,9% от общего числа донаций ГСК от российских неродственных доноров. В 37,1% для получения трансплантата использовалась миелоэксфузия, в остальных 62,9% применялся аппаратный цитаферез. Выбор метода заготовки ГСК определяли, исходя из решения потенциального донора и наличия медицинских противопоказаний, с учетом предпочтений трансплантационного центра. Перед заготовкой трансплантата все доноры ГСК подвергались обследованию на значимые для безопасности реципиента гемотрансмиссивные инфекции. При передаче клеточного материала производилась оценка соответствия количественных и качественных характеристик утвержденной спецификации. При получении ГСК методом аппаратного цитафереза содержание CD34+/кг в трансплантационном материале составило в среднем 6,3x106/кг, при заготовке методом миелоэксфузии – 3,6x106/кг реципиента. Время транспортировки клеточного материала от центра заготовки до трансплантационной клиники составило в среднем 16,3 часа. Согласно представленных трансплантационными клиниками отчетов отклонения количественных показателей от исходных данных были минимальные, составив 1-2% и не зависели от сроков транспортировки. Период от момента активации донора до получения трансплантата занимал не более 8 недель. Все процессы осуществлялись в соответствии с требованиями системы менеджмента качества и комплексом разработанных в учреждении стандартных операционных процедур.
Заключение
В результате взаимодействия двух учреждений, подведомственных ФМБА России, реализована российская модель обеспечения трансплантационных центров РФ клеточным материалом для неродственных трансплантаций. Модель подразумевает весь комплекс необходимых мероприятий: от привлечения потенциальных доноров ГСК до оценки качества заготовленного клеточного материала, его транспортировки и порядка передачи в трансплантирующую клинику. Полученные данные свидетельствуют о высокой эффективности созданной системы. Опыт может быть распространен на деятельность других локальных регистров ГСК в РФ и взят за основу при формировании национальной системы обеспечения трансплантационных центров гемопоэтическим материалом от российских неродственных доноров.
Ключевые слова
Регистр доноров костного мозга, аллогенная трансплантация гемопоэтических стволовых клеток, неродственный донор гемопоэтических стволовых клеток.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20557" ["VALUE"]=> array(2) { ["TEXT"]=> string(364) "Федеральное государственное бюджетное учреждение науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства», Киров, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(364) "Федеральное государственное бюджетное учреждение науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства», Киров, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(364) "Федеральное государственное бюджетное учреждение науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства», Киров, Россия" } } } [45]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1579" ["~ID"]=> string(4) "1579" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(101) "Дезинфекция медицинских помещений с помощью аэрозолей" ["~NAME"]=> string(101) "Дезинфекция медицинских помещений с помощью аэрозолей" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:37:39" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:37:39" ["DETAIL_PAGE_URL"]=> string(113) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/dezinfektsiya-meditsinskikh-pomeshcheniy-s-pomoshchyu-aerozoley/" ["~DETAIL_PAGE_URL"]=> string(113) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/dezinfektsiya-meditsinskikh-pomeshcheniy-s-pomoshchyu-aerozoley/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(63) "dezinfektsiya-meditsinskikh-pomeshcheniy-s-pomoshchyu-aerozoley" ["~CODE"]=> string(63) "dezinfektsiya-meditsinskikh-pomeshcheniy-s-pomoshchyu-aerozoley" ["EXTERNAL_ID"]=> string(4) "1579" ["~EXTERNAL_ID"]=> string(4) "1579" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(101) "Дезинфекция медицинских помещений с помощью аэрозолей" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(159) "Дезинфекция медицинских помещений с помощью аэрозолейUsage of aerosol sprays for disinfection of hospital rooms" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(6970) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Качество и эффективность дезинфекции объектов окружающей (госпитальной) среды при применении растворов химических дезинфицирующих средств зависит от контакта действующего агента с условно-патогенными микроорганизмами, находящимися на обрабатываемых поверхностях; обсемененности объекта, подлежащего дезинфекции; состава дезинфицирующего средства, его концентрации, времени экспозиции. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Сравнение качества заключительной дезинфекции с использованием генератора аэрозолей («аппаратный метод») и ранцевого распылителя жидкостей («ручной метод»). </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> В НИИ ДОГИТ им. Р. М. Горбачевой с 06.2018 по 08.2018 для распыления химических дезинфицирующих средств применяли две методики. Для аппаратно-аэрозольной дезинфекции использовали генератор аэрозолей с дезинфицирующим средством «Nocolyse» (Состав: перекись водорода 6%, неионогенное ПАВ 1%, ионы серебра), ручной, ранцевого типа распылитель жидкостей снаряжали дезсредством «Амиксан» (Состав: N,N-бис(3-аминопропил) додециламин 3%, алкилдиметилбензиламмоний хлорид + алкилдиметилэтилбензиламмоний хлорид 25 %). При использовании аппаратной обработки был протестированы режим: 1:1 (1мл «Nocolyse» на 1 м3), 1:3, 1:6. Смывы с объектов окружающей среды проводили до проведения заключительной дезинфекции (с целью определения общего микробного числа) и после прове- дения заключительной дезинфекции аппаратным методом (контроль качества проведенной дезинфекции). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Заключительная дезинфекция с применением аппарата аэрозольной обработки в режиме 1:1 (5 случаев). Результаты санитарно-бактериологических исследований помещений выявили следующий бактериологический пейзаж объектов окружающей среды, соответственно, до и после антибактериальной обработки: Escherichia coli – 3 (15%) – E.coli – 0, Pseudomonas spp. – 3 (15%), – Pseudomonas sp. – 1 (8,33%), Klebsiella pneumoniae – 3 (15%) – K. pneumoniae – 0, Acinetobacter spр. – 1 (5%) – Acinetobacter spр. – 1 (8,3%), Staphylococcus epidermidis – 7 (35%) – S. epidermidis – 9 (75%), Enterococcus faecium – 1 (5%), E. faecium – 0, Bacillus – 2 (10%) – Bacillus – 1 (8,3%). При режиме 1:3 (3 обработки): Pseudomonas spp. – 1 (6,7%) – Pseudomonas spp. – 0, Staphylococcus epidermidis – 8 (53,3%) – S. epidermidis – 8 (88,9%), Klebsiella pneumoniae – 2 (13,3), K. pneumoniae – 0, Bacillus – 3 (20%) – Bacillus – 1 (11,1%), Staphylococcus aureus – 1 (6,7%) – S.aureus – 0.<br> Режим 1:6 (2 обработки): Staphylococcus epidermidis – 2 (40%) – S. epidermidis – 1 (100%), Acinetobacter spр. – 1 (20%) – Acinetobacter spр. – 0, Klebsiella pneumoniae – 2 (40%) – K.pneumoniae – 0. «Ручная» обработка (4 обработки): Klebsiella pneumoniae – 1 (20%) – K. pneumoniae – 0, Acinetobacter spр. – 2 (40%) – Acinetobacter spр. – 0, Pseudomonas spp. – 1 (20%) – Pseudomonas spp. – 1 (33,3%), Enterobacter spр. – 1 (20%) – Enterobacter spр. – 2 (66,7%). Во всех случаях при положительных бактериологических тестах дезинфекция проводилась повторно до подтверждения отрицательных результатов. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> 1. На основании полученных данных нельзя однозначно утверждать, что «аппаратная» обработка эффективнее «ручной». </p> <p style="text-align: justify;"> 2. В режиме 1:1 аппаратная обработка может стать хорошим дополнением к текущей дезинфекции. </p> <p style="text-align: justify;"> 3. В режиме 1:3 и 1:6 «аппаратная» обработка дает удовлетворительные результаты в борьбе с главными возбудителями нозокомиальной инфекции и может составить альтернативу «ручной». </p> <h2 style="text-align: justify;">Благодарность</h2> <p style="text-align: justify;"> Выражаем особую благодарность сотрудникам отделения реанимации и интенсивной терапии №3 Жаравиной С. В., Журавлевой Н. И. за помощь в организацииработы. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Дезинфекция, больничные палаты, ручной режим, автоматический режим, бактерии, загрязнение. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(101) "Дезинфекция медицинских помещений с помощью аэрозолей" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(101) "Дезинфекция медицинских помещений с помощью аэрозолей" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(101) "Дезинфекция медицинских помещений с помощью аэрозолей" ["SECTION_META_TITLE"]=> string(101) "Дезинфекция медицинских помещений с помощью аэрозолей" ["SECTION_META_KEYWORDS"]=> string(101) "Дезинфекция медицинских помещений с помощью аэрозолей" ["SECTION_META_DESCRIPTION"]=> string(101) "Дезинфекция медицинских помещений с помощью аэрозолей" ["SECTION_PICTURE_FILE_ALT"]=> string(101) "Дезинфекция медицинских помещений с помощью аэрозолей" ["SECTION_PICTURE_FILE_TITLE"]=> string(101) "Дезинфекция медицинских помещений с помощью аэрозолей" ["SECTION_PICTURE_FILE_NAME"]=> string(67) "dezinfektsiya-meditsinskikh-pomeshcheniy-s-pomoshchyu-aerozoley-img" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(101) "Дезинфекция медицинских помещений с помощью аэрозолей" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(101) "Дезинфекция медицинских помещений с помощью аэрозолей" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(67) "dezinfektsiya-meditsinskikh-pomeshcheniy-s-pomoshchyu-aerozoley-img" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(67) "dezinfektsiya-meditsinskikh-pomeshcheniy-s-pomoshchyu-aerozoley-img" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(67) "dezinfektsiya-meditsinskikh-pomeshcheniy-s-pomoshchyu-aerozoley-img" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20547" ["VALUE"]=> array(2) { ["TEXT"]=> string(338) "Алексей К. Кравченко, Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Анна А. Галкина, Ольга Я. Кулагина, Жанна Г. Якимова, Анна А. Спиридонова, Олег В. Голощапов, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(338) "Алексей К. Кравченко, Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Анна А. Галкина, Ольга Я. Кулагина, Жанна Г. Якимова, Анна А. Спиридонова, Олег В. Голощапов, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20548" ["VALUE"]=> array(2) { ["TEXT"]=> string(375) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(375) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20549" ["VALUE"]=> array(2) { ["TEXT"]=> string(6970) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Качество и эффективность дезинфекции объектов окружающей (госпитальной) среды при применении растворов химических дезинфицирующих средств зависит от контакта действующего агента с условно-патогенными микроорганизмами, находящимися на обрабатываемых поверхностях; обсемененности объекта, подлежащего дезинфекции; состава дезинфицирующего средства, его концентрации, времени экспозиции. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Сравнение качества заключительной дезинфекции с использованием генератора аэрозолей («аппаратный метод») и ранцевого распылителя жидкостей («ручной метод»). </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> В НИИ ДОГИТ им. Р. М. Горбачевой с 06.2018 по 08.2018 для распыления химических дезинфицирующих средств применяли две методики. Для аппаратно-аэрозольной дезинфекции использовали генератор аэрозолей с дезинфицирующим средством «Nocolyse» (Состав: перекись водорода 6%, неионогенное ПАВ 1%, ионы серебра), ручной, ранцевого типа распылитель жидкостей снаряжали дезсредством «Амиксан» (Состав: N,N-бис(3-аминопропил) додециламин 3%, алкилдиметилбензиламмоний хлорид + алкилдиметилэтилбензиламмоний хлорид 25 %). При использовании аппаратной обработки был протестированы режим: 1:1 (1мл «Nocolyse» на 1 м3), 1:3, 1:6. Смывы с объектов окружающей среды проводили до проведения заключительной дезинфекции (с целью определения общего микробного числа) и после прове- дения заключительной дезинфекции аппаратным методом (контроль качества проведенной дезинфекции). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Заключительная дезинфекция с применением аппарата аэрозольной обработки в режиме 1:1 (5 случаев). Результаты санитарно-бактериологических исследований помещений выявили следующий бактериологический пейзаж объектов окружающей среды, соответственно, до и после антибактериальной обработки: Escherichia coli – 3 (15%) – E.coli – 0, Pseudomonas spp. – 3 (15%), – Pseudomonas sp. – 1 (8,33%), Klebsiella pneumoniae – 3 (15%) – K. pneumoniae – 0, Acinetobacter spр. – 1 (5%) – Acinetobacter spр. – 1 (8,3%), Staphylococcus epidermidis – 7 (35%) – S. epidermidis – 9 (75%), Enterococcus faecium – 1 (5%), E. faecium – 0, Bacillus – 2 (10%) – Bacillus – 1 (8,3%). При режиме 1:3 (3 обработки): Pseudomonas spp. – 1 (6,7%) – Pseudomonas spp. – 0, Staphylococcus epidermidis – 8 (53,3%) – S. epidermidis – 8 (88,9%), Klebsiella pneumoniae – 2 (13,3), K. pneumoniae – 0, Bacillus – 3 (20%) – Bacillus – 1 (11,1%), Staphylococcus aureus – 1 (6,7%) – S.aureus – 0.<br> Режим 1:6 (2 обработки): Staphylococcus epidermidis – 2 (40%) – S. epidermidis – 1 (100%), Acinetobacter spр. – 1 (20%) – Acinetobacter spр. – 0, Klebsiella pneumoniae – 2 (40%) – K.pneumoniae – 0. «Ручная» обработка (4 обработки): Klebsiella pneumoniae – 1 (20%) – K. pneumoniae – 0, Acinetobacter spр. – 2 (40%) – Acinetobacter spр. – 0, Pseudomonas spp. – 1 (20%) – Pseudomonas spp. – 1 (33,3%), Enterobacter spр. – 1 (20%) – Enterobacter spр. – 2 (66,7%). Во всех случаях при положительных бактериологических тестах дезинфекция проводилась повторно до подтверждения отрицательных результатов. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> 1. На основании полученных данных нельзя однозначно утверждать, что «аппаратная» обработка эффективнее «ручной». </p> <p style="text-align: justify;"> 2. В режиме 1:1 аппаратная обработка может стать хорошим дополнением к текущей дезинфекции. </p> <p style="text-align: justify;"> 3. В режиме 1:3 и 1:6 «аппаратная» обработка дает удовлетворительные результаты в борьбе с главными возбудителями нозокомиальной инфекции и может составить альтернативу «ручной». </p> <h2 style="text-align: justify;">Благодарность</h2> <p style="text-align: justify;"> Выражаем особую благодарность сотрудникам отделения реанимации и интенсивной терапии №3 Жаравиной С. В., Журавлевой Н. И. за помощь в организацииработы. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Дезинфекция, больничные палаты, ручной режим, автоматический режим, бактерии, загрязнение. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6600) "Введение
Качество и эффективность дезинфекции объектов окружающей (госпитальной) среды при применении растворов химических дезинфицирующих средств зависит от контакта действующего агента с условно-патогенными микроорганизмами, находящимися на обрабатываемых поверхностях; обсемененности объекта, подлежащего дезинфекции; состава дезинфицирующего средства, его концентрации, времени экспозиции.
Цель
Сравнение качества заключительной дезинфекции с использованием генератора аэрозолей («аппаратный метод») и ранцевого распылителя жидкостей («ручной метод»).
Методы
В НИИ ДОГИТ им. Р. М. Горбачевой с 06.2018 по 08.2018 для распыления химических дезинфицирующих средств применяли две методики. Для аппаратно-аэрозольной дезинфекции использовали генератор аэрозолей с дезинфицирующим средством «Nocolyse» (Состав: перекись водорода 6%, неионогенное ПАВ 1%, ионы серебра), ручной, ранцевого типа распылитель жидкостей снаряжали дезсредством «Амиксан» (Состав: N,N-бис(3-аминопропил) додециламин 3%, алкилдиметилбензиламмоний хлорид + алкилдиметилэтилбензиламмоний хлорид 25 %). При использовании аппаратной обработки был протестированы режим: 1:1 (1мл «Nocolyse» на 1 м3), 1:3, 1:6. Смывы с объектов окружающей среды проводили до проведения заключительной дезинфекции (с целью определения общего микробного числа) и после прове- дения заключительной дезинфекции аппаратным методом (контроль качества проведенной дезинфекции).
Результаты
Заключительная дезинфекция с применением аппарата аэрозольной обработки в режиме 1:1 (5 случаев). Результаты санитарно-бактериологических исследований помещений выявили следующий бактериологический пейзаж объектов окружающей среды, соответственно, до и после антибактериальной обработки: Escherichia coli – 3 (15%) – E.coli – 0, Pseudomonas spp. – 3 (15%), – Pseudomonas sp. – 1 (8,33%), Klebsiella pneumoniae – 3 (15%) – K. pneumoniae – 0, Acinetobacter spр. – 1 (5%) – Acinetobacter spр. – 1 (8,3%), Staphylococcus epidermidis – 7 (35%) – S. epidermidis – 9 (75%), Enterococcus faecium – 1 (5%), E. faecium – 0, Bacillus – 2 (10%) – Bacillus – 1 (8,3%). При режиме 1:3 (3 обработки): Pseudomonas spp. – 1 (6,7%) – Pseudomonas spp. – 0, Staphylococcus epidermidis – 8 (53,3%) – S. epidermidis – 8 (88,9%), Klebsiella pneumoniae – 2 (13,3), K. pneumoniae – 0, Bacillus – 3 (20%) – Bacillus – 1 (11,1%), Staphylococcus aureus – 1 (6,7%) – S.aureus – 0.
Режим 1:6 (2 обработки): Staphylococcus epidermidis – 2 (40%) – S. epidermidis – 1 (100%), Acinetobacter spр. – 1 (20%) – Acinetobacter spр. – 0, Klebsiella pneumoniae – 2 (40%) – K.pneumoniae – 0. «Ручная» обработка (4 обработки): Klebsiella pneumoniae – 1 (20%) – K. pneumoniae – 0, Acinetobacter spр. – 2 (40%) – Acinetobacter spр. – 0, Pseudomonas spp. – 1 (20%) – Pseudomonas spp. – 1 (33,3%), Enterobacter spр. – 1 (20%) – Enterobacter spр. – 2 (66,7%). Во всех случаях при положительных бактериологических тестах дезинфекция проводилась повторно до подтверждения отрицательных результатов.
Выводы
1. На основании полученных данных нельзя однозначно утверждать, что «аппаратная» обработка эффективнее «ручной».
2. В режиме 1:1 аппаратная обработка может стать хорошим дополнением к текущей дезинфекции.
3. В режиме 1:3 и 1:6 «аппаратная» обработка дает удовлетворительные результаты в борьбе с главными возбудителями нозокомиальной инфекции и может составить альтернативу «ручной».
Благодарность
Выражаем особую благодарность сотрудникам отделения реанимации и интенсивной терапии №3 Жаравиной С. В., Журавлевой Н. И. за помощь в организацииработы.
Ключевые слова
Дезинфекция, больничные палаты, ручной режим, автоматический режим, бактерии, загрязнение.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20550" ["VALUE"]=> array(2) { ["TEXT"]=> string(197) "Alexey K. Kravchenko, Ashot A. Tadevosian, Olga A. Prokofieva, Olga E. Pigareva, Anna A. Galkina, Olga Y. Kulagina, Zhanna G. Yakimova, Anna A. Spiridonova, Oleg V. Goloshchapov, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(197) "Alexey K. Kravchenko, Ashot A. Tadevosian, Olga A. Prokofieva, Olga E. Pigareva, Anna A. Galkina, Olga Y. Kulagina, Zhanna G. Yakimova, Anna A. Spiridonova, Oleg V. Goloshchapov, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20551" ["VALUE"]=> array(2) { ["TEXT"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20552" ["VALUE"]=> array(2) { ["TEXT"]=> string(4757) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Quality and efficacy of environmental (hospital) object disinfection performed using chemical disinfectant solutions depend on contact between the active agent and the opportunistic microorganisms on the contaminated surfaces, severity of contamination, and also composition of the disinfectant, its concentration, and time of exposure. </p> <h2 style="text-align: justify;">Objectives</h2> <p style="text-align: justify;"> To compare results of terminal disinfection performed by using an aerosol generator (“an automated method”), or applying a backpack sprayer (“a manual method”). </p> <h2 style="text-align: justify;">Methods</h2> <p style="text-align: justify;"> From 06.2018 to 08.2018, the two aforementioned methods were used to spray disinfecting agents in the rooms of Raisa Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation. An aerosol generator and disinfectant “Nocolyse” composed of hydrogen peroxide (6%), nonionic surfactant (1%), and containing silver ions, were used to perform automated aerosol disinfection. A backpack sprayer filled with disinfectant “Amixan” containing nn-bis(3-aminopropyl) dodecylamine (3%), alkyldimethylbenzylammonium chloride plus alkyldimethylbenzylammonium chloride (25%) was used for manual disinfection. While using automated method, three operation modes were tested: 1:1 (1 ml of “Nocolyse” per 1 cubic meter), as well as 1 per 3, and 1 per 6 cubic meters. Test swabs from enviromental objects were taken before treatment (to determine total microbial counts), and after terminal disinfection (to evaluate efficacy of the procedure). </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> (1) Terminal disinfection by aerosol generator, 1:1 mode (5 cases). Sanitary and bacteriological tests showed presence of the following microflora (before and after the procedure respectably): E. coli, 3 (15%) vs E.coli, 0; Pseudomonas spp., 3 (15%) vs Pseudomonas spp., 1 (8.3%); Klebsiella pneumonia, 3 (15%) versus K.pneumoniae, 0; Acinetobacter spр., 1 (5%) vs – Acinetobacter spр., 1 (8.3%); Staphylococcus epidermidis, 7 (35%) vs S.epidermidis, 9 (75%); Enterococcus faecium, 1 (5%) vs E. faecium, 0; Bacillus, 2 (10%) vs Bacillus, 1 (8.3%). Microbiology with 1 to 3 mode (3 cases) has shown: Pseudomonas spp., 1 (6.7%) vs Pseudomonas spp., 0; Staphylococcus epidermidis, 8 (53.3%) vs S. epidermidis, 8 (88.9%); Klebsiella pneumonia, 2 (13.3%) vs K. pneumonia, 0; Bacillus, 3 (20%) vs Bacillus, 1 (11.1%); Staphylococcus aureus, 1 (6.7%); S. aureus, 0.<br> 1:6 mode (2 cases). Microbiological findings were as follows: Staphylococcus epidermidis, 2 (40%) vs S.epidermidis, 1 (100%), Acinetobacter spр., 1 (20%) vs Acinetobacter spр., 0; Klebsiella pneumonia, 2(40%) vs. K. pneumoniae – 0. Meanwhile, manual disinfection (4 cases) yielded the following results: Klebsiella pneumonia, 1 (20%) vs K.pneumonia, 0; Acinetobacter spр., 2 (40%) vs Acinetobacter spр., 0; Pseudomonas spp., 1 (20%) vs Pseudomonas spp., 1 (33.3%); Enterobacter spр., 1 (20%); Enterobacter spp., 2 (66,7%). In cases of positive bacteriological tests, the disinfection procedure was repeated until the negative bacteriology results. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> 1. Automated method was not clearly confirmed to be more effective than the manual method. </p> <p style="text-align: justify;"> 2. Automated disinfection done at the 1:1 mode can be a good addition to routine disinfection. </p> <p style="text-align: justify;"> 3. Automated disinfection done at the 1:3 and 1:6 modes shows satisfactory results against the main disease-causing nosocomial pathogens, and it can be used as an alternative to the manual method. </p> <h2 style="text-align: justify;">Credits</h2> <p style="text-align: justify;"> We gratefully aknowledge Jaravina S. V. and Juravleva N. I., members of ICU №3 staff who helped us to organize our work. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Disinfection, hospital rooms, manual regimen, automatic regimen, bacteria, contamination. </p> <span id="bx-cursor-node"></span><br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4371) "Introduction
Quality and efficacy of environmental (hospital) object disinfection performed using chemical disinfectant solutions depend on contact between the active agent and the opportunistic microorganisms on the contaminated surfaces, severity of contamination, and also composition of the disinfectant, its concentration, and time of exposure.
Objectives
To compare results of terminal disinfection performed by using an aerosol generator (“an automated method”), or applying a backpack sprayer (“a manual method”).
Methods
From 06.2018 to 08.2018, the two aforementioned methods were used to spray disinfecting agents in the rooms of Raisa Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation. An aerosol generator and disinfectant “Nocolyse” composed of hydrogen peroxide (6%), nonionic surfactant (1%), and containing silver ions, were used to perform automated aerosol disinfection. A backpack sprayer filled with disinfectant “Amixan” containing nn-bis(3-aminopropyl) dodecylamine (3%), alkyldimethylbenzylammonium chloride plus alkyldimethylbenzylammonium chloride (25%) was used for manual disinfection. While using automated method, three operation modes were tested: 1:1 (1 ml of “Nocolyse” per 1 cubic meter), as well as 1 per 3, and 1 per 6 cubic meters. Test swabs from enviromental objects were taken before treatment (to determine total microbial counts), and after terminal disinfection (to evaluate efficacy of the procedure).
Results
(1) Terminal disinfection by aerosol generator, 1:1 mode (5 cases). Sanitary and bacteriological tests showed presence of the following microflora (before and after the procedure respectably): E. coli, 3 (15%) vs E.coli, 0; Pseudomonas spp., 3 (15%) vs Pseudomonas spp., 1 (8.3%); Klebsiella pneumonia, 3 (15%) versus K.pneumoniae, 0; Acinetobacter spр., 1 (5%) vs – Acinetobacter spр., 1 (8.3%); Staphylococcus epidermidis, 7 (35%) vs S.epidermidis, 9 (75%); Enterococcus faecium, 1 (5%) vs E. faecium, 0; Bacillus, 2 (10%) vs Bacillus, 1 (8.3%). Microbiology with 1 to 3 mode (3 cases) has shown: Pseudomonas spp., 1 (6.7%) vs Pseudomonas spp., 0; Staphylococcus epidermidis, 8 (53.3%) vs S. epidermidis, 8 (88.9%); Klebsiella pneumonia, 2 (13.3%) vs K. pneumonia, 0; Bacillus, 3 (20%) vs Bacillus, 1 (11.1%); Staphylococcus aureus, 1 (6.7%); S. aureus, 0.
1:6 mode (2 cases). Microbiological findings were as follows: Staphylococcus epidermidis, 2 (40%) vs S.epidermidis, 1 (100%), Acinetobacter spр., 1 (20%) vs Acinetobacter spр., 0; Klebsiella pneumonia, 2(40%) vs. K. pneumoniae – 0. Meanwhile, manual disinfection (4 cases) yielded the following results: Klebsiella pneumonia, 1 (20%) vs K.pneumonia, 0; Acinetobacter spр., 2 (40%) vs Acinetobacter spр., 0; Pseudomonas spp., 1 (20%) vs Pseudomonas spp., 1 (33.3%); Enterobacter spр., 1 (20%); Enterobacter spp., 2 (66,7%). In cases of positive bacteriological tests, the disinfection procedure was repeated until the negative bacteriology results.
Conclusions
1. Automated method was not clearly confirmed to be more effective than the manual method.
2. Automated disinfection done at the 1:1 mode can be a good addition to routine disinfection.
3. Automated disinfection done at the 1:3 and 1:6 modes shows satisfactory results against the main disease-causing nosocomial pathogens, and it can be used as an alternative to the manual method.
Credits
We gratefully aknowledge Jaravina S. V. and Juravleva N. I., members of ICU №3 staff who helped us to organize our work.
Keywords
Disinfection, hospital rooms, manual regimen, automatic regimen, bacteria, contamination.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20553" ["VALUE"]=> string(58) "Usage of aerosol sprays for disinfection of hospital rooms" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(58) "Usage of aerosol sprays for disinfection of hospital rooms" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20785" ["VALUE"]=> string(4) "1423" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1423" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20786" ["VALUE"]=> string(4) "1424" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1424" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20550" ["VALUE"]=> array(2) { ["TEXT"]=> string(197) "Alexey K. Kravchenko, Ashot A. Tadevosian, Olga A. Prokofieva, Olga E. Pigareva, Anna A. Galkina, Olga Y. Kulagina, Zhanna G. Yakimova, Anna A. Spiridonova, Oleg V. Goloshchapov, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(197) "Alexey K. Kravchenko, Ashot A. Tadevosian, Olga A. Prokofieva, Olga E. Pigareva, Anna A. Galkina, Olga Y. Kulagina, Zhanna G. Yakimova, Anna A. Spiridonova, Oleg V. Goloshchapov, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(197) "Alexey K. Kravchenko, Ashot A. Tadevosian, Olga A. Prokofieva, Olga E. Pigareva, Anna A. Galkina, Olga Y. Kulagina, Zhanna G. Yakimova, Anna A. Spiridonova, Oleg V. Goloshchapov, Boris V. Afanasyev" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20552" ["VALUE"]=> array(2) { ["TEXT"]=> string(4757) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Quality and efficacy of environmental (hospital) object disinfection performed using chemical disinfectant solutions depend on contact between the active agent and the opportunistic microorganisms on the contaminated surfaces, severity of contamination, and also composition of the disinfectant, its concentration, and time of exposure. </p> <h2 style="text-align: justify;">Objectives</h2> <p style="text-align: justify;"> To compare results of terminal disinfection performed by using an aerosol generator (“an automated method”), or applying a backpack sprayer (“a manual method”). </p> <h2 style="text-align: justify;">Methods</h2> <p style="text-align: justify;"> From 06.2018 to 08.2018, the two aforementioned methods were used to spray disinfecting agents in the rooms of Raisa Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation. An aerosol generator and disinfectant “Nocolyse” composed of hydrogen peroxide (6%), nonionic surfactant (1%), and containing silver ions, were used to perform automated aerosol disinfection. A backpack sprayer filled with disinfectant “Amixan” containing nn-bis(3-aminopropyl) dodecylamine (3%), alkyldimethylbenzylammonium chloride plus alkyldimethylbenzylammonium chloride (25%) was used for manual disinfection. While using automated method, three operation modes were tested: 1:1 (1 ml of “Nocolyse” per 1 cubic meter), as well as 1 per 3, and 1 per 6 cubic meters. Test swabs from enviromental objects were taken before treatment (to determine total microbial counts), and after terminal disinfection (to evaluate efficacy of the procedure). </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> (1) Terminal disinfection by aerosol generator, 1:1 mode (5 cases). Sanitary and bacteriological tests showed presence of the following microflora (before and after the procedure respectably): E. coli, 3 (15%) vs E.coli, 0; Pseudomonas spp., 3 (15%) vs Pseudomonas spp., 1 (8.3%); Klebsiella pneumonia, 3 (15%) versus K.pneumoniae, 0; Acinetobacter spр., 1 (5%) vs – Acinetobacter spр., 1 (8.3%); Staphylococcus epidermidis, 7 (35%) vs S.epidermidis, 9 (75%); Enterococcus faecium, 1 (5%) vs E. faecium, 0; Bacillus, 2 (10%) vs Bacillus, 1 (8.3%). Microbiology with 1 to 3 mode (3 cases) has shown: Pseudomonas spp., 1 (6.7%) vs Pseudomonas spp., 0; Staphylococcus epidermidis, 8 (53.3%) vs S. epidermidis, 8 (88.9%); Klebsiella pneumonia, 2 (13.3%) vs K. pneumonia, 0; Bacillus, 3 (20%) vs Bacillus, 1 (11.1%); Staphylococcus aureus, 1 (6.7%); S. aureus, 0.<br> 1:6 mode (2 cases). Microbiological findings were as follows: Staphylococcus epidermidis, 2 (40%) vs S.epidermidis, 1 (100%), Acinetobacter spр., 1 (20%) vs Acinetobacter spр., 0; Klebsiella pneumonia, 2(40%) vs. K. pneumoniae – 0. Meanwhile, manual disinfection (4 cases) yielded the following results: Klebsiella pneumonia, 1 (20%) vs K.pneumonia, 0; Acinetobacter spр., 2 (40%) vs Acinetobacter spр., 0; Pseudomonas spp., 1 (20%) vs Pseudomonas spp., 1 (33.3%); Enterobacter spр., 1 (20%); Enterobacter spp., 2 (66,7%). In cases of positive bacteriological tests, the disinfection procedure was repeated until the negative bacteriology results. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> 1. Automated method was not clearly confirmed to be more effective than the manual method. </p> <p style="text-align: justify;"> 2. Automated disinfection done at the 1:1 mode can be a good addition to routine disinfection. </p> <p style="text-align: justify;"> 3. Automated disinfection done at the 1:3 and 1:6 modes shows satisfactory results against the main disease-causing nosocomial pathogens, and it can be used as an alternative to the manual method. </p> <h2 style="text-align: justify;">Credits</h2> <p style="text-align: justify;"> We gratefully aknowledge Jaravina S. V. and Juravleva N. I., members of ICU №3 staff who helped us to organize our work. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Disinfection, hospital rooms, manual regimen, automatic regimen, bacteria, contamination. </p> <span id="bx-cursor-node"></span><br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4371) "
Introduction
Quality and efficacy of environmental (hospital) object disinfection performed using chemical disinfectant solutions depend on contact between the active agent and the opportunistic microorganisms on the contaminated surfaces, severity of contamination, and also composition of the disinfectant, its concentration, and time of exposure.
Objectives
To compare results of terminal disinfection performed by using an aerosol generator (“an automated method”), or applying a backpack sprayer (“a manual method”).
Methods
From 06.2018 to 08.2018, the two aforementioned methods were used to spray disinfecting agents in the rooms of Raisa Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation. An aerosol generator and disinfectant “Nocolyse” composed of hydrogen peroxide (6%), nonionic surfactant (1%), and containing silver ions, were used to perform automated aerosol disinfection. A backpack sprayer filled with disinfectant “Amixan” containing nn-bis(3-aminopropyl) dodecylamine (3%), alkyldimethylbenzylammonium chloride plus alkyldimethylbenzylammonium chloride (25%) was used for manual disinfection. While using automated method, three operation modes were tested: 1:1 (1 ml of “Nocolyse” per 1 cubic meter), as well as 1 per 3, and 1 per 6 cubic meters. Test swabs from enviromental objects were taken before treatment (to determine total microbial counts), and after terminal disinfection (to evaluate efficacy of the procedure).
Results
(1) Terminal disinfection by aerosol generator, 1:1 mode (5 cases). Sanitary and bacteriological tests showed presence of the following microflora (before and after the procedure respectably): E. coli, 3 (15%) vs E.coli, 0; Pseudomonas spp., 3 (15%) vs Pseudomonas spp., 1 (8.3%); Klebsiella pneumonia, 3 (15%) versus K.pneumoniae, 0; Acinetobacter spр., 1 (5%) vs – Acinetobacter spр., 1 (8.3%); Staphylococcus epidermidis, 7 (35%) vs S.epidermidis, 9 (75%); Enterococcus faecium, 1 (5%) vs E. faecium, 0; Bacillus, 2 (10%) vs Bacillus, 1 (8.3%). Microbiology with 1 to 3 mode (3 cases) has shown: Pseudomonas spp., 1 (6.7%) vs Pseudomonas spp., 0; Staphylococcus epidermidis, 8 (53.3%) vs S. epidermidis, 8 (88.9%); Klebsiella pneumonia, 2 (13.3%) vs K. pneumonia, 0; Bacillus, 3 (20%) vs Bacillus, 1 (11.1%); Staphylococcus aureus, 1 (6.7%); S. aureus, 0.
1:6 mode (2 cases). Microbiological findings were as follows: Staphylococcus epidermidis, 2 (40%) vs S.epidermidis, 1 (100%), Acinetobacter spр., 1 (20%) vs Acinetobacter spр., 0; Klebsiella pneumonia, 2(40%) vs. K. pneumoniae – 0. Meanwhile, manual disinfection (4 cases) yielded the following results: Klebsiella pneumonia, 1 (20%) vs K.pneumonia, 0; Acinetobacter spр., 2 (40%) vs Acinetobacter spр., 0; Pseudomonas spp., 1 (20%) vs Pseudomonas spp., 1 (33.3%); Enterobacter spр., 1 (20%); Enterobacter spp., 2 (66,7%). In cases of positive bacteriological tests, the disinfection procedure was repeated until the negative bacteriology results.
Conclusions
1. Automated method was not clearly confirmed to be more effective than the manual method.
2. Automated disinfection done at the 1:1 mode can be a good addition to routine disinfection.
3. Automated disinfection done at the 1:3 and 1:6 modes shows satisfactory results against the main disease-causing nosocomial pathogens, and it can be used as an alternative to the manual method.
Credits
We gratefully aknowledge Jaravina S. V. and Juravleva N. I., members of ICU №3 staff who helped us to organize our work.
Keywords
Disinfection, hospital rooms, manual regimen, automatic regimen, bacteria, contamination.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4371) "
Introduction
Quality and efficacy of environmental (hospital) object disinfection performed using chemical disinfectant solutions depend on contact between the active agent and the opportunistic microorganisms on the contaminated surfaces, severity of contamination, and also composition of the disinfectant, its concentration, and time of exposure.
Objectives
To compare results of terminal disinfection performed by using an aerosol generator (“an automated method”), or applying a backpack sprayer (“a manual method”).
Methods
From 06.2018 to 08.2018, the two aforementioned methods were used to spray disinfecting agents in the rooms of Raisa Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation. An aerosol generator and disinfectant “Nocolyse” composed of hydrogen peroxide (6%), nonionic surfactant (1%), and containing silver ions, were used to perform automated aerosol disinfection. A backpack sprayer filled with disinfectant “Amixan” containing nn-bis(3-aminopropyl) dodecylamine (3%), alkyldimethylbenzylammonium chloride plus alkyldimethylbenzylammonium chloride (25%) was used for manual disinfection. While using automated method, three operation modes were tested: 1:1 (1 ml of “Nocolyse” per 1 cubic meter), as well as 1 per 3, and 1 per 6 cubic meters. Test swabs from enviromental objects were taken before treatment (to determine total microbial counts), and after terminal disinfection (to evaluate efficacy of the procedure).
Results
(1) Terminal disinfection by aerosol generator, 1:1 mode (5 cases). Sanitary and bacteriological tests showed presence of the following microflora (before and after the procedure respectably): E. coli, 3 (15%) vs E.coli, 0; Pseudomonas spp., 3 (15%) vs Pseudomonas spp., 1 (8.3%); Klebsiella pneumonia, 3 (15%) versus K.pneumoniae, 0; Acinetobacter spр., 1 (5%) vs – Acinetobacter spр., 1 (8.3%); Staphylococcus epidermidis, 7 (35%) vs S.epidermidis, 9 (75%); Enterococcus faecium, 1 (5%) vs E. faecium, 0; Bacillus, 2 (10%) vs Bacillus, 1 (8.3%). Microbiology with 1 to 3 mode (3 cases) has shown: Pseudomonas spp., 1 (6.7%) vs Pseudomonas spp., 0; Staphylococcus epidermidis, 8 (53.3%) vs S. epidermidis, 8 (88.9%); Klebsiella pneumonia, 2 (13.3%) vs K. pneumonia, 0; Bacillus, 3 (20%) vs Bacillus, 1 (11.1%); Staphylococcus aureus, 1 (6.7%); S. aureus, 0.
1:6 mode (2 cases). Microbiological findings were as follows: Staphylococcus epidermidis, 2 (40%) vs S.epidermidis, 1 (100%), Acinetobacter spр., 1 (20%) vs Acinetobacter spр., 0; Klebsiella pneumonia, 2(40%) vs. K. pneumoniae – 0. Meanwhile, manual disinfection (4 cases) yielded the following results: Klebsiella pneumonia, 1 (20%) vs K.pneumonia, 0; Acinetobacter spр., 2 (40%) vs Acinetobacter spр., 0; Pseudomonas spp., 1 (20%) vs Pseudomonas spp., 1 (33.3%); Enterobacter spр., 1 (20%); Enterobacter spp., 2 (66,7%). In cases of positive bacteriological tests, the disinfection procedure was repeated until the negative bacteriology results.
Conclusions
1. Automated method was not clearly confirmed to be more effective than the manual method.
2. Automated disinfection done at the 1:1 mode can be a good addition to routine disinfection.
3. Automated disinfection done at the 1:3 and 1:6 modes shows satisfactory results against the main disease-causing nosocomial pathogens, and it can be used as an alternative to the manual method.
Credits
We gratefully aknowledge Jaravina S. V. and Juravleva N. I., members of ICU №3 staff who helped us to organize our work.
Keywords
Disinfection, hospital rooms, manual regimen, automatic regimen, bacteria, contamination.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20553" ["VALUE"]=> string(58) "Usage of aerosol sprays for disinfection of hospital rooms" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(58) "Usage of aerosol sprays for disinfection of hospital rooms" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(58) "Usage of aerosol sprays for disinfection of hospital rooms" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20551" ["VALUE"]=> array(2) { ["TEXT"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(176) "Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20547" ["VALUE"]=> array(2) { ["TEXT"]=> string(338) "Алексей К. Кравченко, Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Анна А. Галкина, Ольга Я. Кулагина, Жанна Г. Якимова, Анна А. Спиридонова, Олег В. Голощапов, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(338) "Алексей К. Кравченко, Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Анна А. Галкина, Ольга Я. Кулагина, Жанна Г. Якимова, Анна А. Спиридонова, Олег В. Голощапов, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(338) "Алексей К. Кравченко, Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Анна А. Галкина, Ольга Я. Кулагина, Жанна Г. Якимова, Анна А. Спиридонова, Олег В. Голощапов, Борис В. Афанасьев" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20549" ["VALUE"]=> array(2) { ["TEXT"]=> string(6970) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Качество и эффективность дезинфекции объектов окружающей (госпитальной) среды при применении растворов химических дезинфицирующих средств зависит от контакта действующего агента с условно-патогенными микроорганизмами, находящимися на обрабатываемых поверхностях; обсемененности объекта, подлежащего дезинфекции; состава дезинфицирующего средства, его концентрации, времени экспозиции. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Сравнение качества заключительной дезинфекции с использованием генератора аэрозолей («аппаратный метод») и ранцевого распылителя жидкостей («ручной метод»). </p> <h2 style="text-align: justify;">Методы</h2> <p style="text-align: justify;"> В НИИ ДОГИТ им. Р. М. Горбачевой с 06.2018 по 08.2018 для распыления химических дезинфицирующих средств применяли две методики. Для аппаратно-аэрозольной дезинфекции использовали генератор аэрозолей с дезинфицирующим средством «Nocolyse» (Состав: перекись водорода 6%, неионогенное ПАВ 1%, ионы серебра), ручной, ранцевого типа распылитель жидкостей снаряжали дезсредством «Амиксан» (Состав: N,N-бис(3-аминопропил) додециламин 3%, алкилдиметилбензиламмоний хлорид + алкилдиметилэтилбензиламмоний хлорид 25 %). При использовании аппаратной обработки был протестированы режим: 1:1 (1мл «Nocolyse» на 1 м3), 1:3, 1:6. Смывы с объектов окружающей среды проводили до проведения заключительной дезинфекции (с целью определения общего микробного числа) и после прове- дения заключительной дезинфекции аппаратным методом (контроль качества проведенной дезинфекции). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Заключительная дезинфекция с применением аппарата аэрозольной обработки в режиме 1:1 (5 случаев). Результаты санитарно-бактериологических исследований помещений выявили следующий бактериологический пейзаж объектов окружающей среды, соответственно, до и после антибактериальной обработки: Escherichia coli – 3 (15%) – E.coli – 0, Pseudomonas spp. – 3 (15%), – Pseudomonas sp. – 1 (8,33%), Klebsiella pneumoniae – 3 (15%) – K. pneumoniae – 0, Acinetobacter spр. – 1 (5%) – Acinetobacter spр. – 1 (8,3%), Staphylococcus epidermidis – 7 (35%) – S. epidermidis – 9 (75%), Enterococcus faecium – 1 (5%), E. faecium – 0, Bacillus – 2 (10%) – Bacillus – 1 (8,3%). При режиме 1:3 (3 обработки): Pseudomonas spp. – 1 (6,7%) – Pseudomonas spp. – 0, Staphylococcus epidermidis – 8 (53,3%) – S. epidermidis – 8 (88,9%), Klebsiella pneumoniae – 2 (13,3), K. pneumoniae – 0, Bacillus – 3 (20%) – Bacillus – 1 (11,1%), Staphylococcus aureus – 1 (6,7%) – S.aureus – 0.<br> Режим 1:6 (2 обработки): Staphylococcus epidermidis – 2 (40%) – S. epidermidis – 1 (100%), Acinetobacter spр. – 1 (20%) – Acinetobacter spр. – 0, Klebsiella pneumoniae – 2 (40%) – K.pneumoniae – 0. «Ручная» обработка (4 обработки): Klebsiella pneumoniae – 1 (20%) – K. pneumoniae – 0, Acinetobacter spр. – 2 (40%) – Acinetobacter spр. – 0, Pseudomonas spp. – 1 (20%) – Pseudomonas spp. – 1 (33,3%), Enterobacter spр. – 1 (20%) – Enterobacter spр. – 2 (66,7%). Во всех случаях при положительных бактериологических тестах дезинфекция проводилась повторно до подтверждения отрицательных результатов. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> 1. На основании полученных данных нельзя однозначно утверждать, что «аппаратная» обработка эффективнее «ручной». </p> <p style="text-align: justify;"> 2. В режиме 1:1 аппаратная обработка может стать хорошим дополнением к текущей дезинфекции. </p> <p style="text-align: justify;"> 3. В режиме 1:3 и 1:6 «аппаратная» обработка дает удовлетворительные результаты в борьбе с главными возбудителями нозокомиальной инфекции и может составить альтернативу «ручной». </p> <h2 style="text-align: justify;">Благодарность</h2> <p style="text-align: justify;"> Выражаем особую благодарность сотрудникам отделения реанимации и интенсивной терапии №3 Жаравиной С. В., Журавлевой Н. И. за помощь в организацииработы. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Дезинфекция, больничные палаты, ручной режим, автоматический режим, бактерии, загрязнение. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6600) "
Введение
Качество и эффективность дезинфекции объектов окружающей (госпитальной) среды при применении растворов химических дезинфицирующих средств зависит от контакта действующего агента с условно-патогенными микроорганизмами, находящимися на обрабатываемых поверхностях; обсемененности объекта, подлежащего дезинфекции; состава дезинфицирующего средства, его концентрации, времени экспозиции.
Цель
Сравнение качества заключительной дезинфекции с использованием генератора аэрозолей («аппаратный метод») и ранцевого распылителя жидкостей («ручной метод»).
Методы
В НИИ ДОГИТ им. Р. М. Горбачевой с 06.2018 по 08.2018 для распыления химических дезинфицирующих средств применяли две методики. Для аппаратно-аэрозольной дезинфекции использовали генератор аэрозолей с дезинфицирующим средством «Nocolyse» (Состав: перекись водорода 6%, неионогенное ПАВ 1%, ионы серебра), ручной, ранцевого типа распылитель жидкостей снаряжали дезсредством «Амиксан» (Состав: N,N-бис(3-аминопропил) додециламин 3%, алкилдиметилбензиламмоний хлорид + алкилдиметилэтилбензиламмоний хлорид 25 %). При использовании аппаратной обработки был протестированы режим: 1:1 (1мл «Nocolyse» на 1 м3), 1:3, 1:6. Смывы с объектов окружающей среды проводили до проведения заключительной дезинфекции (с целью определения общего микробного числа) и после прове- дения заключительной дезинфекции аппаратным методом (контроль качества проведенной дезинфекции).
Результаты
Заключительная дезинфекция с применением аппарата аэрозольной обработки в режиме 1:1 (5 случаев). Результаты санитарно-бактериологических исследований помещений выявили следующий бактериологический пейзаж объектов окружающей среды, соответственно, до и после антибактериальной обработки: Escherichia coli – 3 (15%) – E.coli – 0, Pseudomonas spp. – 3 (15%), – Pseudomonas sp. – 1 (8,33%), Klebsiella pneumoniae – 3 (15%) – K. pneumoniae – 0, Acinetobacter spр. – 1 (5%) – Acinetobacter spр. – 1 (8,3%), Staphylococcus epidermidis – 7 (35%) – S. epidermidis – 9 (75%), Enterococcus faecium – 1 (5%), E. faecium – 0, Bacillus – 2 (10%) – Bacillus – 1 (8,3%). При режиме 1:3 (3 обработки): Pseudomonas spp. – 1 (6,7%) – Pseudomonas spp. – 0, Staphylococcus epidermidis – 8 (53,3%) – S. epidermidis – 8 (88,9%), Klebsiella pneumoniae – 2 (13,3), K. pneumoniae – 0, Bacillus – 3 (20%) – Bacillus – 1 (11,1%), Staphylococcus aureus – 1 (6,7%) – S.aureus – 0.
Режим 1:6 (2 обработки): Staphylococcus epidermidis – 2 (40%) – S. epidermidis – 1 (100%), Acinetobacter spр. – 1 (20%) – Acinetobacter spр. – 0, Klebsiella pneumoniae – 2 (40%) – K.pneumoniae – 0. «Ручная» обработка (4 обработки): Klebsiella pneumoniae – 1 (20%) – K. pneumoniae – 0, Acinetobacter spр. – 2 (40%) – Acinetobacter spр. – 0, Pseudomonas spp. – 1 (20%) – Pseudomonas spp. – 1 (33,3%), Enterobacter spр. – 1 (20%) – Enterobacter spр. – 2 (66,7%). Во всех случаях при положительных бактериологических тестах дезинфекция проводилась повторно до подтверждения отрицательных результатов.
Выводы
1. На основании полученных данных нельзя однозначно утверждать, что «аппаратная» обработка эффективнее «ручной».
2. В режиме 1:1 аппаратная обработка может стать хорошим дополнением к текущей дезинфекции.
3. В режиме 1:3 и 1:6 «аппаратная» обработка дает удовлетворительные результаты в борьбе с главными возбудителями нозокомиальной инфекции и может составить альтернативу «ручной».
Благодарность
Выражаем особую благодарность сотрудникам отделения реанимации и интенсивной терапии №3 Жаравиной С. В., Журавлевой Н. И. за помощь в организацииработы.
Ключевые слова
Дезинфекция, больничные палаты, ручной режим, автоматический режим, бактерии, загрязнение.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6600) "Введение
Качество и эффективность дезинфекции объектов окружающей (госпитальной) среды при применении растворов химических дезинфицирующих средств зависит от контакта действующего агента с условно-патогенными микроорганизмами, находящимися на обрабатываемых поверхностях; обсемененности объекта, подлежащего дезинфекции; состава дезинфицирующего средства, его концентрации, времени экспозиции.
Цель
Сравнение качества заключительной дезинфекции с использованием генератора аэрозолей («аппаратный метод») и ранцевого распылителя жидкостей («ручной метод»).
Методы
В НИИ ДОГИТ им. Р. М. Горбачевой с 06.2018 по 08.2018 для распыления химических дезинфицирующих средств применяли две методики. Для аппаратно-аэрозольной дезинфекции использовали генератор аэрозолей с дезинфицирующим средством «Nocolyse» (Состав: перекись водорода 6%, неионогенное ПАВ 1%, ионы серебра), ручной, ранцевого типа распылитель жидкостей снаряжали дезсредством «Амиксан» (Состав: N,N-бис(3-аминопропил) додециламин 3%, алкилдиметилбензиламмоний хлорид + алкилдиметилэтилбензиламмоний хлорид 25 %). При использовании аппаратной обработки был протестированы режим: 1:1 (1мл «Nocolyse» на 1 м3), 1:3, 1:6. Смывы с объектов окружающей среды проводили до проведения заключительной дезинфекции (с целью определения общего микробного числа) и после прове- дения заключительной дезинфекции аппаратным методом (контроль качества проведенной дезинфекции).
Результаты
Заключительная дезинфекция с применением аппарата аэрозольной обработки в режиме 1:1 (5 случаев). Результаты санитарно-бактериологических исследований помещений выявили следующий бактериологический пейзаж объектов окружающей среды, соответственно, до и после антибактериальной обработки: Escherichia coli – 3 (15%) – E.coli – 0, Pseudomonas spp. – 3 (15%), – Pseudomonas sp. – 1 (8,33%), Klebsiella pneumoniae – 3 (15%) – K. pneumoniae – 0, Acinetobacter spр. – 1 (5%) – Acinetobacter spр. – 1 (8,3%), Staphylococcus epidermidis – 7 (35%) – S. epidermidis – 9 (75%), Enterococcus faecium – 1 (5%), E. faecium – 0, Bacillus – 2 (10%) – Bacillus – 1 (8,3%). При режиме 1:3 (3 обработки): Pseudomonas spp. – 1 (6,7%) – Pseudomonas spp. – 0, Staphylococcus epidermidis – 8 (53,3%) – S. epidermidis – 8 (88,9%), Klebsiella pneumoniae – 2 (13,3), K. pneumoniae – 0, Bacillus – 3 (20%) – Bacillus – 1 (11,1%), Staphylococcus aureus – 1 (6,7%) – S.aureus – 0.
Режим 1:6 (2 обработки): Staphylococcus epidermidis – 2 (40%) – S. epidermidis – 1 (100%), Acinetobacter spр. – 1 (20%) – Acinetobacter spр. – 0, Klebsiella pneumoniae – 2 (40%) – K.pneumoniae – 0. «Ручная» обработка (4 обработки): Klebsiella pneumoniae – 1 (20%) – K. pneumoniae – 0, Acinetobacter spр. – 2 (40%) – Acinetobacter spр. – 0, Pseudomonas spp. – 1 (20%) – Pseudomonas spp. – 1 (33,3%), Enterobacter spр. – 1 (20%) – Enterobacter spр. – 2 (66,7%). Во всех случаях при положительных бактериологических тестах дезинфекция проводилась повторно до подтверждения отрицательных результатов.
Выводы
1. На основании полученных данных нельзя однозначно утверждать, что «аппаратная» обработка эффективнее «ручной».
2. В режиме 1:1 аппаратная обработка может стать хорошим дополнением к текущей дезинфекции.
3. В режиме 1:3 и 1:6 «аппаратная» обработка дает удовлетворительные результаты в борьбе с главными возбудителями нозокомиальной инфекции и может составить альтернативу «ручной».
Благодарность
Выражаем особую благодарность сотрудникам отделения реанимации и интенсивной терапии №3 Жаравиной С. В., Журавлевой Н. И. за помощь в организацииработы.
Ключевые слова
Дезинфекция, больничные палаты, ручной режим, автоматический режим, бактерии, загрязнение.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20548" ["VALUE"]=> array(2) { ["TEXT"]=> string(375) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(375) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(375) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" } } } [46]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1578" ["~ID"]=> string(4) "1578" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(161) "Гендерные аспекты коморбидной патологии у пациентов на фоне хронического лимфолейкоза" ["~NAME"]=> string(161) "Гендерные аспекты коморбидной патологии у пациентов на фоне хронического лимфолейкоза" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:38:11" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:38:11" ["DETAIL_PAGE_URL"]=> string(138) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/gendernye-aspekty-komorbidnoy-patologii-u-patsientov-na-fone-khronicheskogo-limfoleykoza/" ["~DETAIL_PAGE_URL"]=> string(138) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/gendernye-aspekty-komorbidnoy-patologii-u-patsientov-na-fone-khronicheskogo-limfoleykoza/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(88) "gendernye-aspekty-komorbidnoy-patologii-u-patsientov-na-fone-khronicheskogo-limfoleykoza" ["~CODE"]=> string(88) "gendernye-aspekty-komorbidnoy-patologii-u-patsientov-na-fone-khronicheskogo-limfoleykoza" ["EXTERNAL_ID"]=> string(4) "1578" ["~EXTERNAL_ID"]=> string(4) "1578" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(161) "Гендерные аспекты коморбидной патологии у пациентов на фоне хронического лимфолейкоза" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(243) "Гендерные аспекты коморбидной патологии у пациентов на фоне хронического лимфолейкозаGender aspects of comorbid pathology in patients with chronic lymphocytic leukemia" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(6294) "<h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель исследования – изучить гендерные особенности коморбидной патологии у пациентов с хроническим лимфолейкозом (ХЛЛ). </p> <h2>Материалы и методы</h2> <p style="text-align: justify;"> Обследовано 70 пациентов (35 мужчин и 35 женщин) в возрасте от 42 до 80 лет. В момент постановки диагноза ХЛЛ пациентам рассчитывали индекс коморбидности Charlson (ИК Charlson) и скорость клубочковй фильтрации (СКФ) по формуле MDRD. ИК Charlson представляет собой бальную систему оценки возраста и наличия определенных сопутствующих заболеваний и используется для оценки прогноза больных с длительными сроками наблюдения. Снижение СКФ также служит маркером для прогноза многих заболеваний. Установлено, что это один из факторов риска появления сердечно-сосудистых осложнений, которые приводят к повышению уровня смертности людей. Для статистической оценки полученных данных вычисляли среднее значение показателя и его стандартное отклонение. Для сравнения групп применялся t-критерий Стьюдента. Корреляционный анализ проводился по Пирсону. Достоверным считался уровень значимости при р <0,05. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Средний возраст мужчин и женщин при постановки диагноза ХЛЛ был сопоставим и составлял 66,4±7,9 лет и 67,7±9,6 лет соответственно (р≥0,05). Так же не получили достоверных различий по уровню ИК Charlson в группах: 6,5±1,5 у мужчин и 6,8±1,6 у женщин (р≥0,05). Структура коморбидной патологии включала в себя наличие хронической сердечной недостаточности (87% – муж., 82% – жен.), хронических неспецифических заболеваний легких (43% – муж., 37% – жен.), нарушение мозгового кровообращения в анамнезе (23% – муж., 26% – жен.), сахарный диабет (14% – муж., 17% – жен.), заболевания почек и мочевыводящих путей (11% – муж., 43% – жен.), постинфарктный кардиосклероз (11% – муж., 8% – жен.), коллагенозы (0% – муж., 3% – жен.). </p> <h2>Расчет</h2> <p style="text-align: justify;"> СКФ по MDRD показал значимые различия в группах исследования. Этот параметр у женщин был достоверно ниже – 58,7±12,4 мл/мин/1,73м2 по сравнению с группой мужчин – 68,8±9,1 мл/мин/1,73м2 (р<0,05). Одновременно с этим в группе женщин получена обратная корреляционная связь средней степени между показателем ИК Charlson и СКФ (r=0,58, р=0,02). </p> <h2 style="text-align: justify;">Обсуждение и выводы</h2> <p style="text-align: justify;"> Полученные результаты свидетельствуют о богатой коморбидной патологии, имеющейся у пациентов с ХЛЛ на момент постановки диагноза. По ИК Charlson в обеих группах исследования в среднем диагностировали низкую общую 10-летнюю выживаемость (15%). Тем не менее, имеются гендерные отличия в структуре сопутствующих заболеваний. Так, среди женщин достоверно чаще встречается патология почек и мочевыводящих путей, что отражено снижением СКФ в этой группе по сравнению с мужчинами. Данный факт не рассматривается нами как особенность пациентов с ХЛЛ. Ранее установлено, что патология почек и мочевыводящих путей встречается в женской популяции чаще, чем в мужской, ввиду анатомических особенностей этого отдела тела. Беря этот факт во внимание, при назначении химиолечения у пациенток с ХЛЛ и ИК Charlson более 6 следует внимательно исследовать показатель СКФ. </p> <p style="text-align: justify;"> <span style="font-family: Cuprum, sans-serif; font-size: 26px;">Ключевые слова</span> </p> <p style="text-align: justify;"> Хронический лимфолейкоз, индекс коморбидности Charlson, скорость клубочковой фильтрации, гендерные различия. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(161) "Гендерные аспекты коморбидной патологии у пациентов на фоне хронического лимфолейкоза" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(161) "Гендерные аспекты коморбидной патологии у пациентов на фоне хронического лимфолейкоза" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(161) "Гендерные аспекты коморбидной патологии у пациентов на фоне хронического лимфолейкоза" ["SECTION_META_TITLE"]=> string(161) "Гендерные аспекты коморбидной патологии у пациентов на фоне хронического лимфолейкоза" ["SECTION_META_KEYWORDS"]=> string(161) "Гендерные аспекты коморбидной патологии у пациентов на фоне хронического лимфолейкоза" ["SECTION_META_DESCRIPTION"]=> string(161) "Гендерные аспекты коморбидной патологии у пациентов на фоне хронического лимфолейкоза" ["SECTION_PICTURE_FILE_ALT"]=> string(161) "Гендерные аспекты коморбидной патологии у пациентов на фоне хронического лимфолейкоза" ["SECTION_PICTURE_FILE_TITLE"]=> string(161) "Гендерные аспекты коморбидной патологии у пациентов на фоне хронического лимфолейкоза" ["SECTION_PICTURE_FILE_NAME"]=> string(92) "gendernye-aspekty-komorbidnoy-patologii-u-patsientov-na-fone-khronicheskogo-limfoleykoza-img" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(161) "Гендерные аспекты коморбидной патологии у пациентов на фоне хронического лимфолейкоза" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(161) "Гендерные аспекты коморбидной патологии у пациентов на фоне хронического лимфолейкоза" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(92) "gendernye-aspekty-komorbidnoy-patologii-u-patsientov-na-fone-khronicheskogo-limfoleykoza-img" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(92) "gendernye-aspekty-komorbidnoy-patologii-u-patsientov-na-fone-khronicheskogo-limfoleykoza-img" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(92) "gendernye-aspekty-komorbidnoy-patologii-u-patsientov-na-fone-khronicheskogo-limfoleykoza-img" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20538" ["VALUE"]=> array(2) { ["TEXT"]=> string(35) "Мария В. Марковцева" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(35) "Мария В. Марковцева" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20539" ["VALUE"]=> array(2) { ["TEXT"]=> string(114) "Ульяновский государственный университет, г. Ульяновск, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(114) "Ульяновский государственный университет, г. Ульяновск, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20540" ["VALUE"]=> array(2) { ["TEXT"]=> string(6294) "<h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель исследования – изучить гендерные особенности коморбидной патологии у пациентов с хроническим лимфолейкозом (ХЛЛ). </p> <h2>Материалы и методы</h2> <p style="text-align: justify;"> Обследовано 70 пациентов (35 мужчин и 35 женщин) в возрасте от 42 до 80 лет. В момент постановки диагноза ХЛЛ пациентам рассчитывали индекс коморбидности Charlson (ИК Charlson) и скорость клубочковй фильтрации (СКФ) по формуле MDRD. ИК Charlson представляет собой бальную систему оценки возраста и наличия определенных сопутствующих заболеваний и используется для оценки прогноза больных с длительными сроками наблюдения. Снижение СКФ также служит маркером для прогноза многих заболеваний. Установлено, что это один из факторов риска появления сердечно-сосудистых осложнений, которые приводят к повышению уровня смертности людей. Для статистической оценки полученных данных вычисляли среднее значение показателя и его стандартное отклонение. Для сравнения групп применялся t-критерий Стьюдента. Корреляционный анализ проводился по Пирсону. Достоверным считался уровень значимости при р <0,05. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Средний возраст мужчин и женщин при постановки диагноза ХЛЛ был сопоставим и составлял 66,4±7,9 лет и 67,7±9,6 лет соответственно (р≥0,05). Так же не получили достоверных различий по уровню ИК Charlson в группах: 6,5±1,5 у мужчин и 6,8±1,6 у женщин (р≥0,05). Структура коморбидной патологии включала в себя наличие хронической сердечной недостаточности (87% – муж., 82% – жен.), хронических неспецифических заболеваний легких (43% – муж., 37% – жен.), нарушение мозгового кровообращения в анамнезе (23% – муж., 26% – жен.), сахарный диабет (14% – муж., 17% – жен.), заболевания почек и мочевыводящих путей (11% – муж., 43% – жен.), постинфарктный кардиосклероз (11% – муж., 8% – жен.), коллагенозы (0% – муж., 3% – жен.). </p> <h2>Расчет</h2> <p style="text-align: justify;"> СКФ по MDRD показал значимые различия в группах исследования. Этот параметр у женщин был достоверно ниже – 58,7±12,4 мл/мин/1,73м2 по сравнению с группой мужчин – 68,8±9,1 мл/мин/1,73м2 (р<0,05). Одновременно с этим в группе женщин получена обратная корреляционная связь средней степени между показателем ИК Charlson и СКФ (r=0,58, р=0,02). </p> <h2 style="text-align: justify;">Обсуждение и выводы</h2> <p style="text-align: justify;"> Полученные результаты свидетельствуют о богатой коморбидной патологии, имеющейся у пациентов с ХЛЛ на момент постановки диагноза. По ИК Charlson в обеих группах исследования в среднем диагностировали низкую общую 10-летнюю выживаемость (15%). Тем не менее, имеются гендерные отличия в структуре сопутствующих заболеваний. Так, среди женщин достоверно чаще встречается патология почек и мочевыводящих путей, что отражено снижением СКФ в этой группе по сравнению с мужчинами. Данный факт не рассматривается нами как особенность пациентов с ХЛЛ. Ранее установлено, что патология почек и мочевыводящих путей встречается в женской популяции чаще, чем в мужской, ввиду анатомических особенностей этого отдела тела. Беря этот факт во внимание, при назначении химиолечения у пациенток с ХЛЛ и ИК Charlson более 6 следует внимательно исследовать показатель СКФ. </p> <p style="text-align: justify;"> <span style="font-family: Cuprum, sans-serif; font-size: 26px;">Ключевые слова</span> </p> <p style="text-align: justify;"> Хронический лимфолейкоз, индекс коморбидности Charlson, скорость клубочковой фильтрации, гендерные различия. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6020) "Цель
Цель исследования – изучить гендерные особенности коморбидной патологии у пациентов с хроническим лимфолейкозом (ХЛЛ).
Материалы и методы
Обследовано 70 пациентов (35 мужчин и 35 женщин) в возрасте от 42 до 80 лет. В момент постановки диагноза ХЛЛ пациентам рассчитывали индекс коморбидности Charlson (ИК Charlson) и скорость клубочковй фильтрации (СКФ) по формуле MDRD. ИК Charlson представляет собой бальную систему оценки возраста и наличия определенных сопутствующих заболеваний и используется для оценки прогноза больных с длительными сроками наблюдения. Снижение СКФ также служит маркером для прогноза многих заболеваний. Установлено, что это один из факторов риска появления сердечно-сосудистых осложнений, которые приводят к повышению уровня смертности людей. Для статистической оценки полученных данных вычисляли среднее значение показателя и его стандартное отклонение. Для сравнения групп применялся t-критерий Стьюдента. Корреляционный анализ проводился по Пирсону. Достоверным считался уровень значимости при р <0,05.
Результаты
Средний возраст мужчин и женщин при постановки диагноза ХЛЛ был сопоставим и составлял 66,4±7,9 лет и 67,7±9,6 лет соответственно (р≥0,05). Так же не получили достоверных различий по уровню ИК Charlson в группах: 6,5±1,5 у мужчин и 6,8±1,6 у женщин (р≥0,05). Структура коморбидной патологии включала в себя наличие хронической сердечной недостаточности (87% – муж., 82% – жен.), хронических неспецифических заболеваний легких (43% – муж., 37% – жен.), нарушение мозгового кровообращения в анамнезе (23% – муж., 26% – жен.), сахарный диабет (14% – муж., 17% – жен.), заболевания почек и мочевыводящих путей (11% – муж., 43% – жен.), постинфарктный кардиосклероз (11% – муж., 8% – жен.), коллагенозы (0% – муж., 3% – жен.).
Расчет
СКФ по MDRD показал значимые различия в группах исследования. Этот параметр у женщин был достоверно ниже – 58,7±12,4 мл/мин/1,73м2 по сравнению с группой мужчин – 68,8±9,1 мл/мин/1,73м2 (р<0,05). Одновременно с этим в группе женщин получена обратная корреляционная связь средней степени между показателем ИК Charlson и СКФ (r=0,58, р=0,02).
Обсуждение и выводы
Полученные результаты свидетельствуют о богатой коморбидной патологии, имеющейся у пациентов с ХЛЛ на момент постановки диагноза. По ИК Charlson в обеих группах исследования в среднем диагностировали низкую общую 10-летнюю выживаемость (15%). Тем не менее, имеются гендерные отличия в структуре сопутствующих заболеваний. Так, среди женщин достоверно чаще встречается патология почек и мочевыводящих путей, что отражено снижением СКФ в этой группе по сравнению с мужчинами. Данный факт не рассматривается нами как особенность пациентов с ХЛЛ. Ранее установлено, что патология почек и мочевыводящих путей встречается в женской популяции чаще, чем в мужской, ввиду анатомических особенностей этого отдела тела. Беря этот факт во внимание, при назначении химиолечения у пациенток с ХЛЛ и ИК Charlson более 6 следует внимательно исследовать показатель СКФ.
Ключевые слова
Хронический лимфолейкоз, индекс коморбидности Charlson, скорость клубочковой фильтрации, гендерные различия.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20541" ["VALUE"]=> array(2) { ["TEXT"]=> string(20) "Maria V. Markovtseva" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(20) "Maria V. Markovtseva" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20542" ["VALUE"]=> array(2) { ["TEXT"]=> string(45) "Ulyanovsk State University, Ulyanovsk, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(45) "Ulyanovsk State University, Ulyanovsk, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20543" ["VALUE"]=> array(2) { ["TEXT"]=> string(3842) "<h2></h2> <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> The aim of the study was to study the gender characteristics of comorbid pathology in patients with chronic lymphocytic leukemia (CLL). </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> We examined 70 patients (35 men and 35 women) aged from 42 to 80 years. At the time of diagnosis of CLL patients were calculated Charlson comorbidity index (Charlson CI) and glomerular filtration rate (GFR) by the MDRD formula. Charlson CI is a point system for assessing the age and presence of certain comorbidities and is used to assess the prognosis of patients with long-term follow-up. Decline in GFR also serves as a marker for the prognosis of many diseases. It is established that this is one of the risk factors for cardiovascular complications, which lead to an increase in mortality. For statistical evaluation of the obtained data, the average value of the indicator and its standard deviation were calculated. Student t-test was used to compare groups. Correlation analysis was carried out on Pearson. The significance level at p < 0.05 was considered reliable. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The mean age of men and women at diagnosis of CLL was comparable and was 66.4±7.9 years and 67.7±9.6 years, respectively (p ≥ 0.05). Similarly, there were no significant differences in the level of Charlson CI in the groups: 6.5±1.5 in men and 6.8±1.6 in women (p ≥ 0.05). The structure of comorbid pathology included the presence of chronic heart failure (87% – men, 82% – women), chronic non-specific lung diseases (43% – men, 37% – women), violation of cerebral circulation in the history (23% – men, 26% – women), diabetes (14% – men, 17% – women ), kidney and urinary tract diseases (11% – men, 43% – women ), postinfarction cardiosclerosis (11% – men, 8% – women ), connective tissue diseases (0% – men, 3% – women). The calculation of GFR by MDRD showed significant differences in the studing groups. This parameter was significantly lower in the women – 58.7±12.4 ml/min/1,73 m2 compared to the group of the men – 68.8±9.1 ml/min/1,73m2 (p<0.05). At the same time, in the group of women, the inverse correlation between the mean degree of the Charlson CI and GFR was obtained (r=0.58, p=0.02). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The results indicate to different comorbidities in the CLL patients at the time of diagnosis. According to Charlson CI, both groups of the study were diagnosed with low overall 10- year survival (15%). However, there are gender differences in the structure of comorbidities. Thus, among women, kidney and urinary tract pathology is significantly more common, which is reflected by a decrease in GFR in this group compared to men. This fact is not considered by us as a specific feature of CLL patients. It was previously established that the pathology of kidneys and urinary tract occurs in the female population more often than in the male, due to the anatomical features of this part of the body. Taking this fact into account, in the appointment of chemotherapy in women with CLL and Charlson CI more than 6 the rate of GFR should be carefully examined. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Chronic lymphocytic leukemia, Charlson comorbidity index, glomerular filtration rate, gender difference. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3602) "Aim
The aim of the study was to study the gender characteristics of comorbid pathology in patients with chronic lymphocytic leukemia (CLL).
Materials and methods
We examined 70 patients (35 men and 35 women) aged from 42 to 80 years. At the time of diagnosis of CLL patients were calculated Charlson comorbidity index (Charlson CI) and glomerular filtration rate (GFR) by the MDRD formula. Charlson CI is a point system for assessing the age and presence of certain comorbidities and is used to assess the prognosis of patients with long-term follow-up. Decline in GFR also serves as a marker for the prognosis of many diseases. It is established that this is one of the risk factors for cardiovascular complications, which lead to an increase in mortality. For statistical evaluation of the obtained data, the average value of the indicator and its standard deviation were calculated. Student t-test was used to compare groups. Correlation analysis was carried out on Pearson. The significance level at p < 0.05 was considered reliable.
Results
The mean age of men and women at diagnosis of CLL was comparable and was 66.4±7.9 years and 67.7±9.6 years, respectively (p ≥ 0.05). Similarly, there were no significant differences in the level of Charlson CI in the groups: 6.5±1.5 in men and 6.8±1.6 in women (p ≥ 0.05). The structure of comorbid pathology included the presence of chronic heart failure (87% – men, 82% – women), chronic non-specific lung diseases (43% – men, 37% – women), violation of cerebral circulation in the history (23% – men, 26% – women), diabetes (14% – men, 17% – women ), kidney and urinary tract diseases (11% – men, 43% – women ), postinfarction cardiosclerosis (11% – men, 8% – women ), connective tissue diseases (0% – men, 3% – women). The calculation of GFR by MDRD showed significant differences in the studing groups. This parameter was significantly lower in the women – 58.7±12.4 ml/min/1,73 m2 compared to the group of the men – 68.8±9.1 ml/min/1,73m2 (p<0.05). At the same time, in the group of women, the inverse correlation between the mean degree of the Charlson CI and GFR was obtained (r=0.58, p=0.02).
Conclusion
The results indicate to different comorbidities in the CLL patients at the time of diagnosis. According to Charlson CI, both groups of the study were diagnosed with low overall 10- year survival (15%). However, there are gender differences in the structure of comorbidities. Thus, among women, kidney and urinary tract pathology is significantly more common, which is reflected by a decrease in GFR in this group compared to men. This fact is not considered by us as a specific feature of CLL patients. It was previously established that the pathology of kidneys and urinary tract occurs in the female population more often than in the male, due to the anatomical features of this part of the body. Taking this fact into account, in the appointment of chemotherapy in women with CLL and Charlson CI more than 6 the rate of GFR should be carefully examined.
Keywords
Chronic lymphocytic leukemia, Charlson comorbidity index, glomerular filtration rate, gender difference.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20544" ["VALUE"]=> string(82) "Gender aspects of comorbid pathology in patients with chronic lymphocytic leukemia" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(82) "Gender aspects of comorbid pathology in patients with chronic lymphocytic leukemia" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20789" ["VALUE"]=> string(4) "1427" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1427" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20790" ["VALUE"]=> string(4) "1428" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1428" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20541" ["VALUE"]=> array(2) { ["TEXT"]=> string(20) "Maria V. Markovtseva" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(20) "Maria V. Markovtseva" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(20) "Maria V. Markovtseva" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20543" ["VALUE"]=> array(2) { ["TEXT"]=> string(3842) "<h2></h2> <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> The aim of the study was to study the gender characteristics of comorbid pathology in patients with chronic lymphocytic leukemia (CLL). </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> We examined 70 patients (35 men and 35 women) aged from 42 to 80 years. At the time of diagnosis of CLL patients were calculated Charlson comorbidity index (Charlson CI) and glomerular filtration rate (GFR) by the MDRD formula. Charlson CI is a point system for assessing the age and presence of certain comorbidities and is used to assess the prognosis of patients with long-term follow-up. Decline in GFR also serves as a marker for the prognosis of many diseases. It is established that this is one of the risk factors for cardiovascular complications, which lead to an increase in mortality. For statistical evaluation of the obtained data, the average value of the indicator and its standard deviation were calculated. Student t-test was used to compare groups. Correlation analysis was carried out on Pearson. The significance level at p < 0.05 was considered reliable. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The mean age of men and women at diagnosis of CLL was comparable and was 66.4±7.9 years and 67.7±9.6 years, respectively (p ≥ 0.05). Similarly, there were no significant differences in the level of Charlson CI in the groups: 6.5±1.5 in men and 6.8±1.6 in women (p ≥ 0.05). The structure of comorbid pathology included the presence of chronic heart failure (87% – men, 82% – women), chronic non-specific lung diseases (43% – men, 37% – women), violation of cerebral circulation in the history (23% – men, 26% – women), diabetes (14% – men, 17% – women ), kidney and urinary tract diseases (11% – men, 43% – women ), postinfarction cardiosclerosis (11% – men, 8% – women ), connective tissue diseases (0% – men, 3% – women). The calculation of GFR by MDRD showed significant differences in the studing groups. This parameter was significantly lower in the women – 58.7±12.4 ml/min/1,73 m2 compared to the group of the men – 68.8±9.1 ml/min/1,73m2 (p<0.05). At the same time, in the group of women, the inverse correlation between the mean degree of the Charlson CI and GFR was obtained (r=0.58, p=0.02). </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> The results indicate to different comorbidities in the CLL patients at the time of diagnosis. According to Charlson CI, both groups of the study were diagnosed with low overall 10- year survival (15%). However, there are gender differences in the structure of comorbidities. Thus, among women, kidney and urinary tract pathology is significantly more common, which is reflected by a decrease in GFR in this group compared to men. This fact is not considered by us as a specific feature of CLL patients. It was previously established that the pathology of kidneys and urinary tract occurs in the female population more often than in the male, due to the anatomical features of this part of the body. Taking this fact into account, in the appointment of chemotherapy in women with CLL and Charlson CI more than 6 the rate of GFR should be carefully examined. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Chronic lymphocytic leukemia, Charlson comorbidity index, glomerular filtration rate, gender difference. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3602) "Aim
The aim of the study was to study the gender characteristics of comorbid pathology in patients with chronic lymphocytic leukemia (CLL).
Materials and methods
We examined 70 patients (35 men and 35 women) aged from 42 to 80 years. At the time of diagnosis of CLL patients were calculated Charlson comorbidity index (Charlson CI) and glomerular filtration rate (GFR) by the MDRD formula. Charlson CI is a point system for assessing the age and presence of certain comorbidities and is used to assess the prognosis of patients with long-term follow-up. Decline in GFR also serves as a marker for the prognosis of many diseases. It is established that this is one of the risk factors for cardiovascular complications, which lead to an increase in mortality. For statistical evaluation of the obtained data, the average value of the indicator and its standard deviation were calculated. Student t-test was used to compare groups. Correlation analysis was carried out on Pearson. The significance level at p < 0.05 was considered reliable.
Results
The mean age of men and women at diagnosis of CLL was comparable and was 66.4±7.9 years and 67.7±9.6 years, respectively (p ≥ 0.05). Similarly, there were no significant differences in the level of Charlson CI in the groups: 6.5±1.5 in men and 6.8±1.6 in women (p ≥ 0.05). The structure of comorbid pathology included the presence of chronic heart failure (87% – men, 82% – women), chronic non-specific lung diseases (43% – men, 37% – women), violation of cerebral circulation in the history (23% – men, 26% – women), diabetes (14% – men, 17% – women ), kidney and urinary tract diseases (11% – men, 43% – women ), postinfarction cardiosclerosis (11% – men, 8% – women ), connective tissue diseases (0% – men, 3% – women). The calculation of GFR by MDRD showed significant differences in the studing groups. This parameter was significantly lower in the women – 58.7±12.4 ml/min/1,73 m2 compared to the group of the men – 68.8±9.1 ml/min/1,73m2 (p<0.05). At the same time, in the group of women, the inverse correlation between the mean degree of the Charlson CI and GFR was obtained (r=0.58, p=0.02).
Conclusion
The results indicate to different comorbidities in the CLL patients at the time of diagnosis. According to Charlson CI, both groups of the study were diagnosed with low overall 10- year survival (15%). However, there are gender differences in the structure of comorbidities. Thus, among women, kidney and urinary tract pathology is significantly more common, which is reflected by a decrease in GFR in this group compared to men. This fact is not considered by us as a specific feature of CLL patients. It was previously established that the pathology of kidneys and urinary tract occurs in the female population more often than in the male, due to the anatomical features of this part of the body. Taking this fact into account, in the appointment of chemotherapy in women with CLL and Charlson CI more than 6 the rate of GFR should be carefully examined.
Keywords
Chronic lymphocytic leukemia, Charlson comorbidity index, glomerular filtration rate, gender difference.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3602) "Aim
The aim of the study was to study the gender characteristics of comorbid pathology in patients with chronic lymphocytic leukemia (CLL).
Materials and methods
We examined 70 patients (35 men and 35 women) aged from 42 to 80 years. At the time of diagnosis of CLL patients were calculated Charlson comorbidity index (Charlson CI) and glomerular filtration rate (GFR) by the MDRD formula. Charlson CI is a point system for assessing the age and presence of certain comorbidities and is used to assess the prognosis of patients with long-term follow-up. Decline in GFR also serves as a marker for the prognosis of many diseases. It is established that this is one of the risk factors for cardiovascular complications, which lead to an increase in mortality. For statistical evaluation of the obtained data, the average value of the indicator and its standard deviation were calculated. Student t-test was used to compare groups. Correlation analysis was carried out on Pearson. The significance level at p < 0.05 was considered reliable.
Results
The mean age of men and women at diagnosis of CLL was comparable and was 66.4±7.9 years and 67.7±9.6 years, respectively (p ≥ 0.05). Similarly, there were no significant differences in the level of Charlson CI in the groups: 6.5±1.5 in men and 6.8±1.6 in women (p ≥ 0.05). The structure of comorbid pathology included the presence of chronic heart failure (87% – men, 82% – women), chronic non-specific lung diseases (43% – men, 37% – women), violation of cerebral circulation in the history (23% – men, 26% – women), diabetes (14% – men, 17% – women ), kidney and urinary tract diseases (11% – men, 43% – women ), postinfarction cardiosclerosis (11% – men, 8% – women ), connective tissue diseases (0% – men, 3% – women). The calculation of GFR by MDRD showed significant differences in the studing groups. This parameter was significantly lower in the women – 58.7±12.4 ml/min/1,73 m2 compared to the group of the men – 68.8±9.1 ml/min/1,73m2 (p<0.05). At the same time, in the group of women, the inverse correlation between the mean degree of the Charlson CI and GFR was obtained (r=0.58, p=0.02).
Conclusion
The results indicate to different comorbidities in the CLL patients at the time of diagnosis. According to Charlson CI, both groups of the study were diagnosed with low overall 10- year survival (15%). However, there are gender differences in the structure of comorbidities. Thus, among women, kidney and urinary tract pathology is significantly more common, which is reflected by a decrease in GFR in this group compared to men. This fact is not considered by us as a specific feature of CLL patients. It was previously established that the pathology of kidneys and urinary tract occurs in the female population more often than in the male, due to the anatomical features of this part of the body. Taking this fact into account, in the appointment of chemotherapy in women with CLL and Charlson CI more than 6 the rate of GFR should be carefully examined.
Keywords
Chronic lymphocytic leukemia, Charlson comorbidity index, glomerular filtration rate, gender difference.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20544" ["VALUE"]=> string(82) "Gender aspects of comorbid pathology in patients with chronic lymphocytic leukemia" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(82) "Gender aspects of comorbid pathology in patients with chronic lymphocytic leukemia" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(82) "Gender aspects of comorbid pathology in patients with chronic lymphocytic leukemia" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20542" ["VALUE"]=> array(2) { ["TEXT"]=> string(45) "Ulyanovsk State University, Ulyanovsk, Russia" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(45) "Ulyanovsk State University, Ulyanovsk, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(45) "Ulyanovsk State University, Ulyanovsk, Russia" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20538" ["VALUE"]=> array(2) { ["TEXT"]=> string(35) "Мария В. Марковцева" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(35) "Мария В. Марковцева" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(35) "Мария В. Марковцева" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20540" ["VALUE"]=> array(2) { ["TEXT"]=> string(6294) "<h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Цель исследования – изучить гендерные особенности коморбидной патологии у пациентов с хроническим лимфолейкозом (ХЛЛ). </p> <h2>Материалы и методы</h2> <p style="text-align: justify;"> Обследовано 70 пациентов (35 мужчин и 35 женщин) в возрасте от 42 до 80 лет. В момент постановки диагноза ХЛЛ пациентам рассчитывали индекс коморбидности Charlson (ИК Charlson) и скорость клубочковй фильтрации (СКФ) по формуле MDRD. ИК Charlson представляет собой бальную систему оценки возраста и наличия определенных сопутствующих заболеваний и используется для оценки прогноза больных с длительными сроками наблюдения. Снижение СКФ также служит маркером для прогноза многих заболеваний. Установлено, что это один из факторов риска появления сердечно-сосудистых осложнений, которые приводят к повышению уровня смертности людей. Для статистической оценки полученных данных вычисляли среднее значение показателя и его стандартное отклонение. Для сравнения групп применялся t-критерий Стьюдента. Корреляционный анализ проводился по Пирсону. Достоверным считался уровень значимости при р <0,05. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Средний возраст мужчин и женщин при постановки диагноза ХЛЛ был сопоставим и составлял 66,4±7,9 лет и 67,7±9,6 лет соответственно (р≥0,05). Так же не получили достоверных различий по уровню ИК Charlson в группах: 6,5±1,5 у мужчин и 6,8±1,6 у женщин (р≥0,05). Структура коморбидной патологии включала в себя наличие хронической сердечной недостаточности (87% – муж., 82% – жен.), хронических неспецифических заболеваний легких (43% – муж., 37% – жен.), нарушение мозгового кровообращения в анамнезе (23% – муж., 26% – жен.), сахарный диабет (14% – муж., 17% – жен.), заболевания почек и мочевыводящих путей (11% – муж., 43% – жен.), постинфарктный кардиосклероз (11% – муж., 8% – жен.), коллагенозы (0% – муж., 3% – жен.). </p> <h2>Расчет</h2> <p style="text-align: justify;"> СКФ по MDRD показал значимые различия в группах исследования. Этот параметр у женщин был достоверно ниже – 58,7±12,4 мл/мин/1,73м2 по сравнению с группой мужчин – 68,8±9,1 мл/мин/1,73м2 (р<0,05). Одновременно с этим в группе женщин получена обратная корреляционная связь средней степени между показателем ИК Charlson и СКФ (r=0,58, р=0,02). </p> <h2 style="text-align: justify;">Обсуждение и выводы</h2> <p style="text-align: justify;"> Полученные результаты свидетельствуют о богатой коморбидной патологии, имеющейся у пациентов с ХЛЛ на момент постановки диагноза. По ИК Charlson в обеих группах исследования в среднем диагностировали низкую общую 10-летнюю выживаемость (15%). Тем не менее, имеются гендерные отличия в структуре сопутствующих заболеваний. Так, среди женщин достоверно чаще встречается патология почек и мочевыводящих путей, что отражено снижением СКФ в этой группе по сравнению с мужчинами. Данный факт не рассматривается нами как особенность пациентов с ХЛЛ. Ранее установлено, что патология почек и мочевыводящих путей встречается в женской популяции чаще, чем в мужской, ввиду анатомических особенностей этого отдела тела. Беря этот факт во внимание, при назначении химиолечения у пациенток с ХЛЛ и ИК Charlson более 6 следует внимательно исследовать показатель СКФ. </p> <p style="text-align: justify;"> <span style="font-family: Cuprum, sans-serif; font-size: 26px;">Ключевые слова</span> </p> <p style="text-align: justify;"> Хронический лимфолейкоз, индекс коморбидности Charlson, скорость клубочковой фильтрации, гендерные различия. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6020) "Цель
Цель исследования – изучить гендерные особенности коморбидной патологии у пациентов с хроническим лимфолейкозом (ХЛЛ).
Материалы и методы
Обследовано 70 пациентов (35 мужчин и 35 женщин) в возрасте от 42 до 80 лет. В момент постановки диагноза ХЛЛ пациентам рассчитывали индекс коморбидности Charlson (ИК Charlson) и скорость клубочковй фильтрации (СКФ) по формуле MDRD. ИК Charlson представляет собой бальную систему оценки возраста и наличия определенных сопутствующих заболеваний и используется для оценки прогноза больных с длительными сроками наблюдения. Снижение СКФ также служит маркером для прогноза многих заболеваний. Установлено, что это один из факторов риска появления сердечно-сосудистых осложнений, которые приводят к повышению уровня смертности людей. Для статистической оценки полученных данных вычисляли среднее значение показателя и его стандартное отклонение. Для сравнения групп применялся t-критерий Стьюдента. Корреляционный анализ проводился по Пирсону. Достоверным считался уровень значимости при р <0,05.
Результаты
Средний возраст мужчин и женщин при постановки диагноза ХЛЛ был сопоставим и составлял 66,4±7,9 лет и 67,7±9,6 лет соответственно (р≥0,05). Так же не получили достоверных различий по уровню ИК Charlson в группах: 6,5±1,5 у мужчин и 6,8±1,6 у женщин (р≥0,05). Структура коморбидной патологии включала в себя наличие хронической сердечной недостаточности (87% – муж., 82% – жен.), хронических неспецифических заболеваний легких (43% – муж., 37% – жен.), нарушение мозгового кровообращения в анамнезе (23% – муж., 26% – жен.), сахарный диабет (14% – муж., 17% – жен.), заболевания почек и мочевыводящих путей (11% – муж., 43% – жен.), постинфарктный кардиосклероз (11% – муж., 8% – жен.), коллагенозы (0% – муж., 3% – жен.).
Расчет
СКФ по MDRD показал значимые различия в группах исследования. Этот параметр у женщин был достоверно ниже – 58,7±12,4 мл/мин/1,73м2 по сравнению с группой мужчин – 68,8±9,1 мл/мин/1,73м2 (р<0,05). Одновременно с этим в группе женщин получена обратная корреляционная связь средней степени между показателем ИК Charlson и СКФ (r=0,58, р=0,02).
Обсуждение и выводы
Полученные результаты свидетельствуют о богатой коморбидной патологии, имеющейся у пациентов с ХЛЛ на момент постановки диагноза. По ИК Charlson в обеих группах исследования в среднем диагностировали низкую общую 10-летнюю выживаемость (15%). Тем не менее, имеются гендерные отличия в структуре сопутствующих заболеваний. Так, среди женщин достоверно чаще встречается патология почек и мочевыводящих путей, что отражено снижением СКФ в этой группе по сравнению с мужчинами. Данный факт не рассматривается нами как особенность пациентов с ХЛЛ. Ранее установлено, что патология почек и мочевыводящих путей встречается в женской популяции чаще, чем в мужской, ввиду анатомических особенностей этого отдела тела. Беря этот факт во внимание, при назначении химиолечения у пациенток с ХЛЛ и ИК Charlson более 6 следует внимательно исследовать показатель СКФ.
Ключевые слова
Хронический лимфолейкоз, индекс коморбидности Charlson, скорость клубочковой фильтрации, гендерные различия.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6020) "Цель
Цель исследования – изучить гендерные особенности коморбидной патологии у пациентов с хроническим лимфолейкозом (ХЛЛ).
Материалы и методы
Обследовано 70 пациентов (35 мужчин и 35 женщин) в возрасте от 42 до 80 лет. В момент постановки диагноза ХЛЛ пациентам рассчитывали индекс коморбидности Charlson (ИК Charlson) и скорость клубочковй фильтрации (СКФ) по формуле MDRD. ИК Charlson представляет собой бальную систему оценки возраста и наличия определенных сопутствующих заболеваний и используется для оценки прогноза больных с длительными сроками наблюдения. Снижение СКФ также служит маркером для прогноза многих заболеваний. Установлено, что это один из факторов риска появления сердечно-сосудистых осложнений, которые приводят к повышению уровня смертности людей. Для статистической оценки полученных данных вычисляли среднее значение показателя и его стандартное отклонение. Для сравнения групп применялся t-критерий Стьюдента. Корреляционный анализ проводился по Пирсону. Достоверным считался уровень значимости при р <0,05.
Результаты
Средний возраст мужчин и женщин при постановки диагноза ХЛЛ был сопоставим и составлял 66,4±7,9 лет и 67,7±9,6 лет соответственно (р≥0,05). Так же не получили достоверных различий по уровню ИК Charlson в группах: 6,5±1,5 у мужчин и 6,8±1,6 у женщин (р≥0,05). Структура коморбидной патологии включала в себя наличие хронической сердечной недостаточности (87% – муж., 82% – жен.), хронических неспецифических заболеваний легких (43% – муж., 37% – жен.), нарушение мозгового кровообращения в анамнезе (23% – муж., 26% – жен.), сахарный диабет (14% – муж., 17% – жен.), заболевания почек и мочевыводящих путей (11% – муж., 43% – жен.), постинфарктный кардиосклероз (11% – муж., 8% – жен.), коллагенозы (0% – муж., 3% – жен.).
Расчет
СКФ по MDRD показал значимые различия в группах исследования. Этот параметр у женщин был достоверно ниже – 58,7±12,4 мл/мин/1,73м2 по сравнению с группой мужчин – 68,8±9,1 мл/мин/1,73м2 (р<0,05). Одновременно с этим в группе женщин получена обратная корреляционная связь средней степени между показателем ИК Charlson и СКФ (r=0,58, р=0,02).
Обсуждение и выводы
Полученные результаты свидетельствуют о богатой коморбидной патологии, имеющейся у пациентов с ХЛЛ на момент постановки диагноза. По ИК Charlson в обеих группах исследования в среднем диагностировали низкую общую 10-летнюю выживаемость (15%). Тем не менее, имеются гендерные отличия в структуре сопутствующих заболеваний. Так, среди женщин достоверно чаще встречается патология почек и мочевыводящих путей, что отражено снижением СКФ в этой группе по сравнению с мужчинами. Данный факт не рассматривается нами как особенность пациентов с ХЛЛ. Ранее установлено, что патология почек и мочевыводящих путей встречается в женской популяции чаще, чем в мужской, ввиду анатомических особенностей этого отдела тела. Беря этот факт во внимание, при назначении химиолечения у пациенток с ХЛЛ и ИК Charlson более 6 следует внимательно исследовать показатель СКФ.
Ключевые слова
Хронический лимфолейкоз, индекс коморбидности Charlson, скорость клубочковой фильтрации, гендерные различия.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20539" ["VALUE"]=> array(2) { ["TEXT"]=> string(114) "Ульяновский государственный университет, г. Ульяновск, Россия" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(114) "Ульяновский государственный университет, г. Ульяновск, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(114) "Ульяновский государственный университет, г. Ульяновск, Россия" } } } [47]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1583" ["~ID"]=> string(4) "1583" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(162) "Изучение страхов, связанных с медицинскими манипуляциями, у детей в возрасте от 3 до 6 лет" ["~NAME"]=> string(162) "Изучение страхов, связанных с медицинскими манипуляциями, у детей в возрасте от 3 до 6 лет" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:39:37" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:39:37" ["DETAIL_PAGE_URL"]=> string(146) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/izuchenie-strakhov-svyazannykh-s-meditsinskimi-manipulyatsiyami-u-detey-v-vozraste-ot-3-do-6-let/" ["~DETAIL_PAGE_URL"]=> string(146) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/izuchenie-strakhov-svyazannykh-s-meditsinskimi-manipulyatsiyami-u-detey-v-vozraste-ot-3-do-6-let/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(96) "izuchenie-strakhov-svyazannykh-s-meditsinskimi-manipulyatsiyami-u-detey-v-vozraste-ot-3-do-6-let" ["~CODE"]=> string(96) "izuchenie-strakhov-svyazannykh-s-meditsinskimi-manipulyatsiyami-u-detey-v-vozraste-ot-3-do-6-let" ["EXTERNAL_ID"]=> string(4) "1583" ["~EXTERNAL_ID"]=> string(4) "1583" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(162) "Изучение страхов, связанных с медицинскими манипуляциями, у детей в возрасте от 3 до 6 лет" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(237) "Изучение страхов, связанных с медицинскими манипуляциями, у детей в возрасте от 3 до 6 летStudy of fears caused by medical manipulations in children 3 to 6 years old" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(7311) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Ситуация онкологического заболевания являясь психотравмирующей, может влиять на нормальное развитие детей. В игре дети будут использовать материалы, причиняющие им болезненные ощущения и дискомфорт, а также вызывающие страхи. Дети обследованы методами включенного наблюдения и клинико-диагностического интервью. </p> <h2 style="text-align: justify;">Объект исследования</h2> <p style="text-align: justify;"> В исследование вошли 15 пациентов с гемобластозами и нейробластомами. Мамы этих детей дали письменное согласие на участие в данном исследовании. Среди пациентов, принявших участие в исследовании, было 6 мальчиков и 9 девочек в возрасте от 3 до 6 лет. Группой контроля стали дети, находящиеся в детских садах (2 группы детей по 7 и 8 человек в возрасте от 5 до 6 лет), в общей сложности 15 человек (7 мальчиков; 8 девочек). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Практически во всех играх детей-пациентов роль врача исполняли сами дети. Только 1 ребенок отказался исполнять и роль врача и роль пациента. На роль «пациента» дети выбирали игрушку, предложенную психологом, собственные игрушки, маму и/или медицинского психолога. Продолжительность игры 15-20 минут. Пациенты в процессе игры предпочли настоящие медицинские инструменты (медицинский шприц, лейкопластырь, иглу-катетер «бабочка» и реже таблетки), нежели игрушечные. Чаще пациенты выбирали шприц и лейкопластырь. Из интервью с мамами стало известно, что для детей наиболее неприятными из медицинских процедур являются постановка инъекций и «переклейка катетера». Все дети из детского сада для манипуляций чаще всего использовали настоящие медицинские инструменты. Группа детей №1 чаще использовала медицинский шприц, иглу-катетер «бабочка», медицинский лейкопластырь, салфетки марлевые и таблетки. Группа детей №2 выбирала – медицинский шприц и медицинский бинт. Из всех медицинских игрушек обе группы детей чаще всего выбирали фонендоскоп, градусник, жидкие лекарства. Один пациент категорически отказался доставлять «игрушке-пациенту» болезненные ощущения. Остальные пациенты проявляли сочувствие к «игрушке-пациенту», поглаживали ее, в том числе по тем местам, куда была сделана инъекция или наложен лейкопластырь, использовали ласковые слова («немного потерпите»; «все будет хорошо»), желали выздоровления, и обнимали своих «пациентов». Один ребенок злился на своего «пациента», говоря: «Пусть тебе тоже будет больно». Дети из первой группы детского сада ругались на «игрушку-пациента» и говорили: «Сама виновата, что заболела». Дети из второй группы чаще всего проявляли сочувствие, подбадривали «игрушку-пациента», говорили, что «процедуры важны для выздоровления, и их нужно потерпеть». Исходя из беседы с вoспитателями: детям первой группы за неделю до игры делали прививки. У детей второй группы подобной медицинской процедуры не было. Дети второй группы демонстрировали более гуманное отношение к своим «пациентам», нежели дети первой группы. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> 1) В игре дети чаще всего используют те медицинские инструменты, которые доставляют им наибольший дискомфорт и/или болевые ощущения. 2) С помощью манипулирования предметами в игре, дети показывают свое состояние во время и после прохождения медицинских процедур, которые им наиболее неприятны. 3) С помощью манипулирования медицинскими инструментами в игре, дети выражают отрицательные эмоции по отношению к медицинским манипуляциям, при этом отрицательные эмоциональные реакции по-разному могут подавляться родителями пациента и/или медицинским персоналом. 4) Травматичность опыта прохождения медицинских процедур детьми и отношение к детям окружающих их взрослых в период заболевания, влияет на отношение самих детей к другим заболевшим. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Психология, игра, дети, лечение, эмоции. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(162) "Изучение страхов, связанных с медицинскими манипуляциями, у детей в возрасте от 3 до 6 лет" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(162) "Изучение страхов, связанных с медицинскими манипуляциями, у детей в возрасте от 3 до 6 лет" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(162) "Изучение страхов, связанных с медицинскими манипуляциями, у детей в возрасте от 3 до 6 лет" ["SECTION_META_TITLE"]=> string(162) "Изучение страхов, связанных с медицинскими манипуляциями, у детей в возрасте от 3 до 6 лет" ["SECTION_META_KEYWORDS"]=> string(162) "Изучение страхов, связанных с медицинскими манипуляциями, у детей в возрасте от 3 до 6 лет" ["SECTION_META_DESCRIPTION"]=> string(162) "Изучение страхов, связанных с медицинскими манипуляциями, у детей в возрасте от 3 до 6 лет" ["SECTION_PICTURE_FILE_ALT"]=> string(162) "Изучение страхов, связанных с медицинскими манипуляциями, у детей в возрасте от 3 до 6 лет" ["SECTION_PICTURE_FILE_TITLE"]=> string(162) "Изучение страхов, связанных с медицинскими манипуляциями, у детей в возрасте от 3 до 6 лет" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "izuchenie-strakhov-svyazannykh-s-meditsinskimi-manipulyatsiyami-u-detey-v-vozraste-ot-3-do-6-let-img" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(162) "Изучение страхов, связанных с медицинскими манипуляциями, у детей в возрасте от 3 до 6 лет" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(162) "Изучение страхов, связанных с медицинскими манипуляциями, у детей в возрасте от 3 до 6 лет" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "izuchenie-strakhov-svyazannykh-s-meditsinskimi-manipulyatsiyami-u-detey-v-vozraste-ot-3-do-6-let-img" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "izuchenie-strakhov-svyazannykh-s-meditsinskimi-manipulyatsiyami-u-detey-v-vozraste-ot-3-do-6-let-img" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "izuchenie-strakhov-svyazannykh-s-meditsinskimi-manipulyatsiyami-u-detey-v-vozraste-ot-3-do-6-let-img" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20583" ["VALUE"]=> array(2) { ["TEXT"]=> string(92) "Олеся О. Морозова, Ольга В.Ушакова, Алиса Г. Волкова" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(92) "Олеся О. Морозова, Ольга В.Ушакова, Алиса Г. Волкова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20584" ["VALUE"]=> array(2) { ["TEXT"]=> string(348) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(342) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20585" ["VALUE"]=> array(2) { ["TEXT"]=> string(7311) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Ситуация онкологического заболевания являясь психотравмирующей, может влиять на нормальное развитие детей. В игре дети будут использовать материалы, причиняющие им болезненные ощущения и дискомфорт, а также вызывающие страхи. Дети обследованы методами включенного наблюдения и клинико-диагностического интервью. </p> <h2 style="text-align: justify;">Объект исследования</h2> <p style="text-align: justify;"> В исследование вошли 15 пациентов с гемобластозами и нейробластомами. Мамы этих детей дали письменное согласие на участие в данном исследовании. Среди пациентов, принявших участие в исследовании, было 6 мальчиков и 9 девочек в возрасте от 3 до 6 лет. Группой контроля стали дети, находящиеся в детских садах (2 группы детей по 7 и 8 человек в возрасте от 5 до 6 лет), в общей сложности 15 человек (7 мальчиков; 8 девочек). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Практически во всех играх детей-пациентов роль врача исполняли сами дети. Только 1 ребенок отказался исполнять и роль врача и роль пациента. На роль «пациента» дети выбирали игрушку, предложенную психологом, собственные игрушки, маму и/или медицинского психолога. Продолжительность игры 15-20 минут. Пациенты в процессе игры предпочли настоящие медицинские инструменты (медицинский шприц, лейкопластырь, иглу-катетер «бабочка» и реже таблетки), нежели игрушечные. Чаще пациенты выбирали шприц и лейкопластырь. Из интервью с мамами стало известно, что для детей наиболее неприятными из медицинских процедур являются постановка инъекций и «переклейка катетера». Все дети из детского сада для манипуляций чаще всего использовали настоящие медицинские инструменты. Группа детей №1 чаще использовала медицинский шприц, иглу-катетер «бабочка», медицинский лейкопластырь, салфетки марлевые и таблетки. Группа детей №2 выбирала – медицинский шприц и медицинский бинт. Из всех медицинских игрушек обе группы детей чаще всего выбирали фонендоскоп, градусник, жидкие лекарства. Один пациент категорически отказался доставлять «игрушке-пациенту» болезненные ощущения. Остальные пациенты проявляли сочувствие к «игрушке-пациенту», поглаживали ее, в том числе по тем местам, куда была сделана инъекция или наложен лейкопластырь, использовали ласковые слова («немного потерпите»; «все будет хорошо»), желали выздоровления, и обнимали своих «пациентов». Один ребенок злился на своего «пациента», говоря: «Пусть тебе тоже будет больно». Дети из первой группы детского сада ругались на «игрушку-пациента» и говорили: «Сама виновата, что заболела». Дети из второй группы чаще всего проявляли сочувствие, подбадривали «игрушку-пациента», говорили, что «процедуры важны для выздоровления, и их нужно потерпеть». Исходя из беседы с вoспитателями: детям первой группы за неделю до игры делали прививки. У детей второй группы подобной медицинской процедуры не было. Дети второй группы демонстрировали более гуманное отношение к своим «пациентам», нежели дети первой группы. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> 1) В игре дети чаще всего используют те медицинские инструменты, которые доставляют им наибольший дискомфорт и/или болевые ощущения. 2) С помощью манипулирования предметами в игре, дети показывают свое состояние во время и после прохождения медицинских процедур, которые им наиболее неприятны. 3) С помощью манипулирования медицинскими инструментами в игре, дети выражают отрицательные эмоции по отношению к медицинским манипуляциям, при этом отрицательные эмоциональные реакции по-разному могут подавляться родителями пациента и/или медицинским персоналом. 4) Травматичность опыта прохождения медицинских процедур детьми и отношение к детям окружающих их взрослых в период заболевания, влияет на отношение самих детей к другим заболевшим. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Психология, игра, дети, лечение, эмоции. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7079) "
Введение
Ситуация онкологического заболевания являясь психотравмирующей, может влиять на нормальное развитие детей. В игре дети будут использовать материалы, причиняющие им болезненные ощущения и дискомфорт, а также вызывающие страхи. Дети обследованы методами включенного наблюдения и клинико-диагностического интервью.
Объект исследования
В исследование вошли 15 пациентов с гемобластозами и нейробластомами. Мамы этих детей дали письменное согласие на участие в данном исследовании. Среди пациентов, принявших участие в исследовании, было 6 мальчиков и 9 девочек в возрасте от 3 до 6 лет. Группой контроля стали дети, находящиеся в детских садах (2 группы детей по 7 и 8 человек в возрасте от 5 до 6 лет), в общей сложности 15 человек (7 мальчиков; 8 девочек).
Результаты
Практически во всех играх детей-пациентов роль врача исполняли сами дети. Только 1 ребенок отказался исполнять и роль врача и роль пациента. На роль «пациента» дети выбирали игрушку, предложенную психологом, собственные игрушки, маму и/или медицинского психолога. Продолжительность игры 15-20 минут. Пациенты в процессе игры предпочли настоящие медицинские инструменты (медицинский шприц, лейкопластырь, иглу-катетер «бабочка» и реже таблетки), нежели игрушечные. Чаще пациенты выбирали шприц и лейкопластырь. Из интервью с мамами стало известно, что для детей наиболее неприятными из медицинских процедур являются постановка инъекций и «переклейка катетера». Все дети из детского сада для манипуляций чаще всего использовали настоящие медицинские инструменты. Группа детей №1 чаще использовала медицинский шприц, иглу-катетер «бабочка», медицинский лейкопластырь, салфетки марлевые и таблетки. Группа детей №2 выбирала – медицинский шприц и медицинский бинт. Из всех медицинских игрушек обе группы детей чаще всего выбирали фонендоскоп, градусник, жидкие лекарства. Один пациент категорически отказался доставлять «игрушке-пациенту» болезненные ощущения. Остальные пациенты проявляли сочувствие к «игрушке-пациенту», поглаживали ее, в том числе по тем местам, куда была сделана инъекция или наложен лейкопластырь, использовали ласковые слова («немного потерпите»; «все будет хорошо»), желали выздоровления, и обнимали своих «пациентов». Один ребенок злился на своего «пациента», говоря: «Пусть тебе тоже будет больно». Дети из первой группы детского сада ругались на «игрушку-пациента» и говорили: «Сама виновата, что заболела». Дети из второй группы чаще всего проявляли сочувствие, подбадривали «игрушку-пациента», говорили, что «процедуры важны для выздоровления, и их нужно потерпеть». Исходя из беседы с вoспитателями: детям первой группы за неделю до игры делали прививки. У детей второй группы подобной медицинской процедуры не было. Дети второй группы демонстрировали более гуманное отношение к своим «пациентам», нежели дети первой группы.
Выводы
1) В игре дети чаще всего используют те медицинские инструменты, которые доставляют им наибольший дискомфорт и/или болевые ощущения. 2) С помощью манипулирования предметами в игре, дети показывают свое состояние во время и после прохождения медицинских процедур, которые им наиболее неприятны. 3) С помощью манипулирования медицинскими инструментами в игре, дети выражают отрицательные эмоции по отношению к медицинским манипуляциям, при этом отрицательные эмоциональные реакции по-разному могут подавляться родителями пациента и/или медицинским персоналом. 4) Травматичность опыта прохождения медицинских процедур детьми и отношение к детям окружающих их взрослых в период заболевания, влияет на отношение самих детей к другим заболевшим.
Ключевые слова
Психология, игра, дети, лечение, эмоции.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20586" ["VALUE"]=> array(2) { ["TEXT"]=> string(54) "Olesya O. Morozova, Olga B. Ushakova, Alisa G. Volkova" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(54) "Olesya O. Morozova, Olga B. Ushakova, Alisa G. Volkova" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20587" ["VALUE"]=> array(2) { ["TEXT"]=> string(229) "R. Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation and Chair of Hematology, Transfusiology and Transplantation at the First St. Petersburg State I. Pavlov Medical University<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(223) "R. Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation and Chair of Hematology, Transfusiology and Transplantation at the First St. Petersburg State I. Pavlov Medical University" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20588" ["VALUE"]=> array(2) { ["TEXT"]=> string(3852) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Cancer itself is a psycho-traumatic situation and may impair child’s normal development. When playing, the children utilize traumatic material associated with pain, discomfort and fear. The involved observation and clinical diagnostic interview methods were used to study this situation. </p> <h2>Patients and methods</h2> <p style="text-align: justify;"> A total of 15 patients with leukemia or neuroblastoma were included in the study. Patients’ mothers signed an informed consent for participation in the study. Six of the study participants were boys and 9 girls, all aged 3 to 6 years. The control group consisted of 15 healthy preschool children (2 groups of 7 and 8 children aged 5 to 6 years), 7 boys and 8 girls. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> In most games, the role of a doctor was played by a child. Only one child declined to impersonate both a patient and a doctor. Younger children mostly agreed to have for a “patient” a toy (proposed by psychologist or one of child’s own), child’s mother or a medical psychologist. The game lasted for 15-20 minutes. Most patients preferred to handle real medical consumables and instruments (syringes, adhesive tape, winged infusion sets or, more rarely, pills). Most often a syringe or an adhesive tape was chosen. As known from the mothers, injections and changing implanted catheter dressings were most unpleasant medical manipulations for their children. Similarly, most healthy preschool children preferred to use real medical instruments than appropriate toys. Patients form group 1 more often used a syringe, a winged infusion set, adhesive tape, gauze or pills. Children from Group 2 most often choose syringe or gauze. Among medical instruments, both groups more often choose phonendoscope or thermometer. One patient refused to cause pain to a “toy patient”. Other children sympathized with a “toy patient”, fondled the injection or dressing sites, or used soothing terms (“wait a little”, “it’s going to be all right”), wished prompt recovery and hugged their “patients”. One child was angry over his “patient” wishing him to “get hurt too”. First preschool group children were mostly scolding a toy “patient” for “being guilty of getting sick”. Second group children were mostly compassionate, encouraged a “toy patient” telling that “all the procedures are needed to get healthy”. From children’s schoolmasters we know that all first group children received vaccination about a week before a test. Children from the second group had no injections within this terms. Overall attitude towards toy “patients” was more mild in the second group. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> 1) When playing, the children mostly use the medical devices which cause them most discomfort and/or pain. 2) When manipulating the items children illustrate their own impression of medical procedures, which are most unpleasant. 3) Children may express their negative emotions directed towards medical manipulations via their play actions, these negative reactions may be suppressed in different ways by parents or medical staff. 4) The intensity of child’s own traumatic experience and an attitude of nearby adults may influence the child’s attitude towards other patients. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Psychology, games, children, treatment, emotions. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3642) "
Introduction
Cancer itself is a psycho-traumatic situation and may impair child’s normal development. When playing, the children utilize traumatic material associated with pain, discomfort and fear. The involved observation and clinical diagnostic interview methods were used to study this situation.
Patients and methods
A total of 15 patients with leukemia or neuroblastoma were included in the study. Patients’ mothers signed an informed consent for participation in the study. Six of the study participants were boys and 9 girls, all aged 3 to 6 years. The control group consisted of 15 healthy preschool children (2 groups of 7 and 8 children aged 5 to 6 years), 7 boys and 8 girls.
Results
In most games, the role of a doctor was played by a child. Only one child declined to impersonate both a patient and a doctor. Younger children mostly agreed to have for a “patient” a toy (proposed by psychologist or one of child’s own), child’s mother or a medical psychologist. The game lasted for 15-20 minutes. Most patients preferred to handle real medical consumables and instruments (syringes, adhesive tape, winged infusion sets or, more rarely, pills). Most often a syringe or an adhesive tape was chosen. As known from the mothers, injections and changing implanted catheter dressings were most unpleasant medical manipulations for their children. Similarly, most healthy preschool children preferred to use real medical instruments than appropriate toys. Patients form group 1 more often used a syringe, a winged infusion set, adhesive tape, gauze or pills. Children from Group 2 most often choose syringe or gauze. Among medical instruments, both groups more often choose phonendoscope or thermometer. One patient refused to cause pain to a “toy patient”. Other children sympathized with a “toy patient”, fondled the injection or dressing sites, or used soothing terms (“wait a little”, “it’s going to be all right”), wished prompt recovery and hugged their “patients”. One child was angry over his “patient” wishing him to “get hurt too”. First preschool group children were mostly scolding a toy “patient” for “being guilty of getting sick”. Second group children were mostly compassionate, encouraged a “toy patient” telling that “all the procedures are needed to get healthy”. From children’s schoolmasters we know that all first group children received vaccination about a week before a test. Children from the second group had no injections within this terms. Overall attitude towards toy “patients” was more mild in the second group.
Conclusions
1) When playing, the children mostly use the medical devices which cause them most discomfort and/or pain. 2) When manipulating the items children illustrate their own impression of medical procedures, which are most unpleasant. 3) Children may express their negative emotions directed towards medical manipulations via their play actions, these negative reactions may be suppressed in different ways by parents or medical staff. 4) The intensity of child’s own traumatic experience and an attitude of nearby adults may influence the child’s attitude towards other patients.
Keywords
Psychology, games, children, treatment, emotions.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20589" ["VALUE"]=> string(75) "Study of fears caused by medical manipulations in children 3 to 6 years old" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(75) "Study of fears caused by medical manipulations in children 3 to 6 years old" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20797" ["VALUE"]=> string(4) "1435" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1435" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20798" ["VALUE"]=> string(4) "1436" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1436" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20586" ["VALUE"]=> array(2) { ["TEXT"]=> string(54) "Olesya O. Morozova, Olga B. Ushakova, Alisa G. Volkova" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(54) "Olesya O. Morozova, Olga B. Ushakova, Alisa G. Volkova" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(54) "Olesya O. Morozova, Olga B. Ushakova, Alisa G. Volkova" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20588" ["VALUE"]=> array(2) { ["TEXT"]=> string(3852) "<h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Cancer itself is a psycho-traumatic situation and may impair child’s normal development. When playing, the children utilize traumatic material associated with pain, discomfort and fear. The involved observation and clinical diagnostic interview methods were used to study this situation. </p> <h2>Patients and methods</h2> <p style="text-align: justify;"> A total of 15 patients with leukemia or neuroblastoma were included in the study. Patients’ mothers signed an informed consent for participation in the study. Six of the study participants were boys and 9 girls, all aged 3 to 6 years. The control group consisted of 15 healthy preschool children (2 groups of 7 and 8 children aged 5 to 6 years), 7 boys and 8 girls. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> In most games, the role of a doctor was played by a child. Only one child declined to impersonate both a patient and a doctor. Younger children mostly agreed to have for a “patient” a toy (proposed by psychologist or one of child’s own), child’s mother or a medical psychologist. The game lasted for 15-20 minutes. Most patients preferred to handle real medical consumables and instruments (syringes, adhesive tape, winged infusion sets or, more rarely, pills). Most often a syringe or an adhesive tape was chosen. As known from the mothers, injections and changing implanted catheter dressings were most unpleasant medical manipulations for their children. Similarly, most healthy preschool children preferred to use real medical instruments than appropriate toys. Patients form group 1 more often used a syringe, a winged infusion set, adhesive tape, gauze or pills. Children from Group 2 most often choose syringe or gauze. Among medical instruments, both groups more often choose phonendoscope or thermometer. One patient refused to cause pain to a “toy patient”. Other children sympathized with a “toy patient”, fondled the injection or dressing sites, or used soothing terms (“wait a little”, “it’s going to be all right”), wished prompt recovery and hugged their “patients”. One child was angry over his “patient” wishing him to “get hurt too”. First preschool group children were mostly scolding a toy “patient” for “being guilty of getting sick”. Second group children were mostly compassionate, encouraged a “toy patient” telling that “all the procedures are needed to get healthy”. From children’s schoolmasters we know that all first group children received vaccination about a week before a test. Children from the second group had no injections within this terms. Overall attitude towards toy “patients” was more mild in the second group. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> 1) When playing, the children mostly use the medical devices which cause them most discomfort and/or pain. 2) When manipulating the items children illustrate their own impression of medical procedures, which are most unpleasant. 3) Children may express their negative emotions directed towards medical manipulations via their play actions, these negative reactions may be suppressed in different ways by parents or medical staff. 4) The intensity of child’s own traumatic experience and an attitude of nearby adults may influence the child’s attitude towards other patients. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Psychology, games, children, treatment, emotions. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3642) "Introduction
Cancer itself is a psycho-traumatic situation and may impair child’s normal development. When playing, the children utilize traumatic material associated with pain, discomfort and fear. The involved observation and clinical diagnostic interview methods were used to study this situation.
Patients and methods
A total of 15 patients with leukemia or neuroblastoma were included in the study. Patients’ mothers signed an informed consent for participation in the study. Six of the study participants were boys and 9 girls, all aged 3 to 6 years. The control group consisted of 15 healthy preschool children (2 groups of 7 and 8 children aged 5 to 6 years), 7 boys and 8 girls.
Results
In most games, the role of a doctor was played by a child. Only one child declined to impersonate both a patient and a doctor. Younger children mostly agreed to have for a “patient” a toy (proposed by psychologist or one of child’s own), child’s mother or a medical psychologist. The game lasted for 15-20 minutes. Most patients preferred to handle real medical consumables and instruments (syringes, adhesive tape, winged infusion sets or, more rarely, pills). Most often a syringe or an adhesive tape was chosen. As known from the mothers, injections and changing implanted catheter dressings were most unpleasant medical manipulations for their children. Similarly, most healthy preschool children preferred to use real medical instruments than appropriate toys. Patients form group 1 more often used a syringe, a winged infusion set, adhesive tape, gauze or pills. Children from Group 2 most often choose syringe or gauze. Among medical instruments, both groups more often choose phonendoscope or thermometer. One patient refused to cause pain to a “toy patient”. Other children sympathized with a “toy patient”, fondled the injection or dressing sites, or used soothing terms (“wait a little”, “it’s going to be all right”), wished prompt recovery and hugged their “patients”. One child was angry over his “patient” wishing him to “get hurt too”. First preschool group children were mostly scolding a toy “patient” for “being guilty of getting sick”. Second group children were mostly compassionate, encouraged a “toy patient” telling that “all the procedures are needed to get healthy”. From children’s schoolmasters we know that all first group children received vaccination about a week before a test. Children from the second group had no injections within this terms. Overall attitude towards toy “patients” was more mild in the second group.
Conclusions
1) When playing, the children mostly use the medical devices which cause them most discomfort and/or pain. 2) When manipulating the items children illustrate their own impression of medical procedures, which are most unpleasant. 3) Children may express their negative emotions directed towards medical manipulations via their play actions, these negative reactions may be suppressed in different ways by parents or medical staff. 4) The intensity of child’s own traumatic experience and an attitude of nearby adults may influence the child’s attitude towards other patients.
Keywords
Psychology, games, children, treatment, emotions.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3642) "Introduction
Cancer itself is a psycho-traumatic situation and may impair child’s normal development. When playing, the children utilize traumatic material associated with pain, discomfort and fear. The involved observation and clinical diagnostic interview methods were used to study this situation.
Patients and methods
A total of 15 patients with leukemia or neuroblastoma were included in the study. Patients’ mothers signed an informed consent for participation in the study. Six of the study participants were boys and 9 girls, all aged 3 to 6 years. The control group consisted of 15 healthy preschool children (2 groups of 7 and 8 children aged 5 to 6 years), 7 boys and 8 girls.
Results
In most games, the role of a doctor was played by a child. Only one child declined to impersonate both a patient and a doctor. Younger children mostly agreed to have for a “patient” a toy (proposed by psychologist or one of child’s own), child’s mother or a medical psychologist. The game lasted for 15-20 minutes. Most patients preferred to handle real medical consumables and instruments (syringes, adhesive tape, winged infusion sets or, more rarely, pills). Most often a syringe or an adhesive tape was chosen. As known from the mothers, injections and changing implanted catheter dressings were most unpleasant medical manipulations for their children. Similarly, most healthy preschool children preferred to use real medical instruments than appropriate toys. Patients form group 1 more often used a syringe, a winged infusion set, adhesive tape, gauze or pills. Children from Group 2 most often choose syringe or gauze. Among medical instruments, both groups more often choose phonendoscope or thermometer. One patient refused to cause pain to a “toy patient”. Other children sympathized with a “toy patient”, fondled the injection or dressing sites, or used soothing terms (“wait a little”, “it’s going to be all right”), wished prompt recovery and hugged their “patients”. One child was angry over his “patient” wishing him to “get hurt too”. First preschool group children were mostly scolding a toy “patient” for “being guilty of getting sick”. Second group children were mostly compassionate, encouraged a “toy patient” telling that “all the procedures are needed to get healthy”. From children’s schoolmasters we know that all first group children received vaccination about a week before a test. Children from the second group had no injections within this terms. Overall attitude towards toy “patients” was more mild in the second group.
Conclusions
1) When playing, the children mostly use the medical devices which cause them most discomfort and/or pain. 2) When manipulating the items children illustrate their own impression of medical procedures, which are most unpleasant. 3) Children may express their negative emotions directed towards medical manipulations via their play actions, these negative reactions may be suppressed in different ways by parents or medical staff. 4) The intensity of child’s own traumatic experience and an attitude of nearby adults may influence the child’s attitude towards other patients.
Keywords
Psychology, games, children, treatment, emotions.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20589" ["VALUE"]=> string(75) "Study of fears caused by medical manipulations in children 3 to 6 years old" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(75) "Study of fears caused by medical manipulations in children 3 to 6 years old" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(75) "Study of fears caused by medical manipulations in children 3 to 6 years old" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20587" ["VALUE"]=> array(2) { ["TEXT"]=> string(229) "R. Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation and Chair of Hematology, Transfusiology and Transplantation at the First St. Petersburg State I. Pavlov Medical University<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(223) "R. Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation and Chair of Hematology, Transfusiology and Transplantation at the First St. Petersburg State I. Pavlov Medical University" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(223) "R. Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation and Chair of Hematology, Transfusiology and Transplantation at the First St. Petersburg State I. Pavlov Medical University
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20583" ["VALUE"]=> array(2) { ["TEXT"]=> string(92) "Олеся О. Морозова, Ольга В.Ушакова, Алиса Г. Волкова" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(92) "Олеся О. Морозова, Ольга В.Ушакова, Алиса Г. Волкова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(92) "Олеся О. Морозова, Ольга В.Ушакова, Алиса Г. Волкова" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20585" ["VALUE"]=> array(2) { ["TEXT"]=> string(7311) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Ситуация онкологического заболевания являясь психотравмирующей, может влиять на нормальное развитие детей. В игре дети будут использовать материалы, причиняющие им болезненные ощущения и дискомфорт, а также вызывающие страхи. Дети обследованы методами включенного наблюдения и клинико-диагностического интервью. </p> <h2 style="text-align: justify;">Объект исследования</h2> <p style="text-align: justify;"> В исследование вошли 15 пациентов с гемобластозами и нейробластомами. Мамы этих детей дали письменное согласие на участие в данном исследовании. Среди пациентов, принявших участие в исследовании, было 6 мальчиков и 9 девочек в возрасте от 3 до 6 лет. Группой контроля стали дети, находящиеся в детских садах (2 группы детей по 7 и 8 человек в возрасте от 5 до 6 лет), в общей сложности 15 человек (7 мальчиков; 8 девочек). </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Практически во всех играх детей-пациентов роль врача исполняли сами дети. Только 1 ребенок отказался исполнять и роль врача и роль пациента. На роль «пациента» дети выбирали игрушку, предложенную психологом, собственные игрушки, маму и/или медицинского психолога. Продолжительность игры 15-20 минут. Пациенты в процессе игры предпочли настоящие медицинские инструменты (медицинский шприц, лейкопластырь, иглу-катетер «бабочка» и реже таблетки), нежели игрушечные. Чаще пациенты выбирали шприц и лейкопластырь. Из интервью с мамами стало известно, что для детей наиболее неприятными из медицинских процедур являются постановка инъекций и «переклейка катетера». Все дети из детского сада для манипуляций чаще всего использовали настоящие медицинские инструменты. Группа детей №1 чаще использовала медицинский шприц, иглу-катетер «бабочка», медицинский лейкопластырь, салфетки марлевые и таблетки. Группа детей №2 выбирала – медицинский шприц и медицинский бинт. Из всех медицинских игрушек обе группы детей чаще всего выбирали фонендоскоп, градусник, жидкие лекарства. Один пациент категорически отказался доставлять «игрушке-пациенту» болезненные ощущения. Остальные пациенты проявляли сочувствие к «игрушке-пациенту», поглаживали ее, в том числе по тем местам, куда была сделана инъекция или наложен лейкопластырь, использовали ласковые слова («немного потерпите»; «все будет хорошо»), желали выздоровления, и обнимали своих «пациентов». Один ребенок злился на своего «пациента», говоря: «Пусть тебе тоже будет больно». Дети из первой группы детского сада ругались на «игрушку-пациента» и говорили: «Сама виновата, что заболела». Дети из второй группы чаще всего проявляли сочувствие, подбадривали «игрушку-пациента», говорили, что «процедуры важны для выздоровления, и их нужно потерпеть». Исходя из беседы с вoспитателями: детям первой группы за неделю до игры делали прививки. У детей второй группы подобной медицинской процедуры не было. Дети второй группы демонстрировали более гуманное отношение к своим «пациентам», нежели дети первой группы. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> 1) В игре дети чаще всего используют те медицинские инструменты, которые доставляют им наибольший дискомфорт и/или болевые ощущения. 2) С помощью манипулирования предметами в игре, дети показывают свое состояние во время и после прохождения медицинских процедур, которые им наиболее неприятны. 3) С помощью манипулирования медицинскими инструментами в игре, дети выражают отрицательные эмоции по отношению к медицинским манипуляциям, при этом отрицательные эмоциональные реакции по-разному могут подавляться родителями пациента и/или медицинским персоналом. 4) Травматичность опыта прохождения медицинских процедур детьми и отношение к детям окружающих их взрослых в период заболевания, влияет на отношение самих детей к другим заболевшим. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Психология, игра, дети, лечение, эмоции. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(7079) "
Введение
Ситуация онкологического заболевания являясь психотравмирующей, может влиять на нормальное развитие детей. В игре дети будут использовать материалы, причиняющие им болезненные ощущения и дискомфорт, а также вызывающие страхи. Дети обследованы методами включенного наблюдения и клинико-диагностического интервью.
Объект исследования
В исследование вошли 15 пациентов с гемобластозами и нейробластомами. Мамы этих детей дали письменное согласие на участие в данном исследовании. Среди пациентов, принявших участие в исследовании, было 6 мальчиков и 9 девочек в возрасте от 3 до 6 лет. Группой контроля стали дети, находящиеся в детских садах (2 группы детей по 7 и 8 человек в возрасте от 5 до 6 лет), в общей сложности 15 человек (7 мальчиков; 8 девочек).
Результаты
Практически во всех играх детей-пациентов роль врача исполняли сами дети. Только 1 ребенок отказался исполнять и роль врача и роль пациента. На роль «пациента» дети выбирали игрушку, предложенную психологом, собственные игрушки, маму и/или медицинского психолога. Продолжительность игры 15-20 минут. Пациенты в процессе игры предпочли настоящие медицинские инструменты (медицинский шприц, лейкопластырь, иглу-катетер «бабочка» и реже таблетки), нежели игрушечные. Чаще пациенты выбирали шприц и лейкопластырь. Из интервью с мамами стало известно, что для детей наиболее неприятными из медицинских процедур являются постановка инъекций и «переклейка катетера». Все дети из детского сада для манипуляций чаще всего использовали настоящие медицинские инструменты. Группа детей №1 чаще использовала медицинский шприц, иглу-катетер «бабочка», медицинский лейкопластырь, салфетки марлевые и таблетки. Группа детей №2 выбирала – медицинский шприц и медицинский бинт. Из всех медицинских игрушек обе группы детей чаще всего выбирали фонендоскоп, градусник, жидкие лекарства. Один пациент категорически отказался доставлять «игрушке-пациенту» болезненные ощущения. Остальные пациенты проявляли сочувствие к «игрушке-пациенту», поглаживали ее, в том числе по тем местам, куда была сделана инъекция или наложен лейкопластырь, использовали ласковые слова («немного потерпите»; «все будет хорошо»), желали выздоровления, и обнимали своих «пациентов». Один ребенок злился на своего «пациента», говоря: «Пусть тебе тоже будет больно». Дети из первой группы детского сада ругались на «игрушку-пациента» и говорили: «Сама виновата, что заболела». Дети из второй группы чаще всего проявляли сочувствие, подбадривали «игрушку-пациента», говорили, что «процедуры важны для выздоровления, и их нужно потерпеть». Исходя из беседы с вoспитателями: детям первой группы за неделю до игры делали прививки. У детей второй группы подобной медицинской процедуры не было. Дети второй группы демонстрировали более гуманное отношение к своим «пациентам», нежели дети первой группы.
Выводы
1) В игре дети чаще всего используют те медицинские инструменты, которые доставляют им наибольший дискомфорт и/или болевые ощущения. 2) С помощью манипулирования предметами в игре, дети показывают свое состояние во время и после прохождения медицинских процедур, которые им наиболее неприятны. 3) С помощью манипулирования медицинскими инструментами в игре, дети выражают отрицательные эмоции по отношению к медицинским манипуляциям, при этом отрицательные эмоциональные реакции по-разному могут подавляться родителями пациента и/или медицинским персоналом. 4) Травматичность опыта прохождения медицинских процедур детьми и отношение к детям окружающих их взрослых в период заболевания, влияет на отношение самих детей к другим заболевшим.
Ключевые слова
Психология, игра, дети, лечение, эмоции.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(7079) "Введение
Ситуация онкологического заболевания являясь психотравмирующей, может влиять на нормальное развитие детей. В игре дети будут использовать материалы, причиняющие им болезненные ощущения и дискомфорт, а также вызывающие страхи. Дети обследованы методами включенного наблюдения и клинико-диагностического интервью.
Объект исследования
В исследование вошли 15 пациентов с гемобластозами и нейробластомами. Мамы этих детей дали письменное согласие на участие в данном исследовании. Среди пациентов, принявших участие в исследовании, было 6 мальчиков и 9 девочек в возрасте от 3 до 6 лет. Группой контроля стали дети, находящиеся в детских садах (2 группы детей по 7 и 8 человек в возрасте от 5 до 6 лет), в общей сложности 15 человек (7 мальчиков; 8 девочек).
Результаты
Практически во всех играх детей-пациентов роль врача исполняли сами дети. Только 1 ребенок отказался исполнять и роль врача и роль пациента. На роль «пациента» дети выбирали игрушку, предложенную психологом, собственные игрушки, маму и/или медицинского психолога. Продолжительность игры 15-20 минут. Пациенты в процессе игры предпочли настоящие медицинские инструменты (медицинский шприц, лейкопластырь, иглу-катетер «бабочка» и реже таблетки), нежели игрушечные. Чаще пациенты выбирали шприц и лейкопластырь. Из интервью с мамами стало известно, что для детей наиболее неприятными из медицинских процедур являются постановка инъекций и «переклейка катетера». Все дети из детского сада для манипуляций чаще всего использовали настоящие медицинские инструменты. Группа детей №1 чаще использовала медицинский шприц, иглу-катетер «бабочка», медицинский лейкопластырь, салфетки марлевые и таблетки. Группа детей №2 выбирала – медицинский шприц и медицинский бинт. Из всех медицинских игрушек обе группы детей чаще всего выбирали фонендоскоп, градусник, жидкие лекарства. Один пациент категорически отказался доставлять «игрушке-пациенту» болезненные ощущения. Остальные пациенты проявляли сочувствие к «игрушке-пациенту», поглаживали ее, в том числе по тем местам, куда была сделана инъекция или наложен лейкопластырь, использовали ласковые слова («немного потерпите»; «все будет хорошо»), желали выздоровления, и обнимали своих «пациентов». Один ребенок злился на своего «пациента», говоря: «Пусть тебе тоже будет больно». Дети из первой группы детского сада ругались на «игрушку-пациента» и говорили: «Сама виновата, что заболела». Дети из второй группы чаще всего проявляли сочувствие, подбадривали «игрушку-пациента», говорили, что «процедуры важны для выздоровления, и их нужно потерпеть». Исходя из беседы с вoспитателями: детям первой группы за неделю до игры делали прививки. У детей второй группы подобной медицинской процедуры не было. Дети второй группы демонстрировали более гуманное отношение к своим «пациентам», нежели дети первой группы.
Выводы
1) В игре дети чаще всего используют те медицинские инструменты, которые доставляют им наибольший дискомфорт и/или болевые ощущения. 2) С помощью манипулирования предметами в игре, дети показывают свое состояние во время и после прохождения медицинских процедур, которые им наиболее неприятны. 3) С помощью манипулирования медицинскими инструментами в игре, дети выражают отрицательные эмоции по отношению к медицинским манипуляциям, при этом отрицательные эмоциональные реакции по-разному могут подавляться родителями пациента и/или медицинским персоналом. 4) Травматичность опыта прохождения медицинских процедур детьми и отношение к детям окружающих их взрослых в период заболевания, влияет на отношение самих детей к другим заболевшим.
Ключевые слова
Психология, игра, дети, лечение, эмоции.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20584" ["VALUE"]=> array(2) { ["TEXT"]=> string(348) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(342) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(342) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
" } } } [48]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1584" ["~ID"]=> string(4) "1584" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(304) "Возможности и перспективы использования конфокальной микроскопии для оценки результатов перекрестного типирования HLA у пациентов с трансплантацией костного мозга" ["~NAME"]=> string(304) "Возможности и перспективы использования конфокальной микроскопии для оценки результатов перекрестного типирования HLA у пациентов с трансплантацией костного мозга" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:39:55" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:39:55" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vozmozhnosti-i-perspektivy-ispolzovaniya-konfokalnoy-mikroskopii-dlya-otsenki-rezultatov-perekrestno/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vozmozhnosti-i-perspektivy-ispolzovaniya-konfokalnoy-mikroskopii-dlya-otsenki-rezultatov-perekrestno/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "vozmozhnosti-i-perspektivy-ispolzovaniya-konfokalnoy-mikroskopii-dlya-otsenki-rezultatov-perekrestno" ["~CODE"]=> string(100) "vozmozhnosti-i-perspektivy-ispolzovaniya-konfokalnoy-mikroskopii-dlya-otsenki-rezultatov-perekrestno" ["EXTERNAL_ID"]=> string(4) "1584" ["~EXTERNAL_ID"]=> string(4) "1584" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(304) "Возможности и перспективы использования конфокальной микроскопии для оценки результатов перекрестного типирования HLA у пациентов с трансплантацией костного мозга" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(440) "Возможности и перспективы использования конфокальной микроскопии для оценки результатов перекрестного типирования HLA у пациентов с трансплантацией костного мозгаPotentials and prospects of using a confocal microscopy for the HLA-Crossmatch result evaluation in bone marrow transplantation patients" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(7087) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> В последние годы становится все более очевидным, что роль анти-донорских HLA антител, направленных против антигенов HLA класса I и II не ограничивается их участием в развитии сверхострого отторжения аллотрансплантатов. Все большее число исследователей склонны считать, что образование анти-донорских HLA антител в посттрансплантационный период приводит к развитию ускоренного острого, острого или хронического отторжения. Тест на иммунологическую совместимость между донором и реципиентом при трансплантации является решающим показателем для принятия решения о проведении трансплантации. Антитела к HLA обнаруживаются более чем у 30% населения, их выявление свидетельствует о предшествующей иммунизации HLA. Она возможна при многократном переливании цельной крови, во время беременности и после трансплантации. Ряд авторов отмечает, что донор неспецифические антитела к HLA являются одним из факторов не только риска острого, но и хронического отторжения трансплантата и учитываются, как плохой прогностический показатель [P.I.Terasaki, 2006; М. Моrrel, 2011; M. Crespo, 2011]. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Целью теста HLA-Crossmatch является обнаружение лимфоцитотоксических антител, специфичных для потенциального донора (то есть аллогенный перекрестный кроссматч) или у самого себя (то есть аутологичный перекрестный HLA-Crossmatch). Прямой HLA-Crossmatch, используется с сывороткой от предполагаемого реципиента (или донора для обратного HLA-Crossmatch) и клетками-мишенями являются мононуклеарные клетки потенциального донора (или реципиента для обратного HLA-Crossmatch. Используемые клетки-мишени могут быть не разделены или разделены на определенные группы, такие как Т- лимфоциты, В- лимфоциты, моноциты и т. д. Оценка результатов реакции HLA-Crossmatch крайне субъективна при простой оптической микроскопии, т.к. невозможно точно посчитать количество мертвых клеток в поле зрения камеры Терасаки и вычесть фон (результаты негативного контроля). Невозможна так же оценка к какому классу HLA (I или II) принадлежат антитела. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Нами был разработан метод оценки результатов HLACrossmatch с использованием конфокального микроскопа у пациентов с трансплантацией костного мозга. Вся постановка реакции HLA-Crossmatch проводилась стандартным методом, кроме последнего этапа: окраски и оценки жизнеспособности лимфоцитов в лунках. Мы использовали Акридиновый Оранжевый (АО – эмиссия 525 нм) и Пропидиум Йодид (PI – 620 нм) как витальные красители. Для окраски B лимфоцитов использовались анти-CD19 моноклональные антитела, конъюгированные с PE-Cyanine7 (775 нм). Результаты регистрировались с помощью ZEISS конфокального микроскопа с последующим анализом изображений программным продуктом ImageJ (National Institutes of Health) c последующим обсчетом результатов нами созданной программой. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Предложенный нами метод оценки имеет следующие преимущества: 1) В одной лунке производится анализ одной сыворотки реципиента на наличие антител против донорских антигенов HLA одновременно и по I, и по II классу; 2) Метод является быстрым, точным и высокопроизводительным (в одной камере Терасаки за один запуск можно проанализировать до 72 сывороток); 3) Высокая чувствительность считывания флуоресцентной метки; 4) Наличие многоуровневой системы различных контролей; 5) Возможность архивирования полученных результатов в базе данных программы для интерпретации и PDF отчетов; 6) Субъективная оценка в анализе результатов сведена к минимуму за счет статистической обработки полученных данных программным обеспечением. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> HLA, перекрестный подбор HLA, трансплантация костного мозга, конфокальная микроскопия. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(304) "Возможности и перспективы использования конфокальной микроскопии для оценки результатов перекрестного типирования HLA у пациентов с трансплантацией костного мозга" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(304) "Возможности и перспективы использования конфокальной микроскопии для оценки результатов перекрестного типирования HLA у пациентов с трансплантацией костного мозга" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(304) "Возможности и перспективы использования конфокальной микроскопии для оценки результатов перекрестного типирования HLA у пациентов с трансплантацией костного мозга" ["SECTION_META_TITLE"]=> string(304) "Возможности и перспективы использования конфокальной микроскопии для оценки результатов перекрестного типирования HLA у пациентов с трансплантацией костного мозга" ["SECTION_META_KEYWORDS"]=> string(304) "Возможности и перспективы использования конфокальной микроскопии для оценки результатов перекрестного типирования HLA у пациентов с трансплантацией костного мозга" ["SECTION_META_DESCRIPTION"]=> string(304) "Возможности и перспективы использования конфокальной микроскопии для оценки результатов перекрестного типирования HLA у пациентов с трансплантацией костного мозга" ["SECTION_PICTURE_FILE_ALT"]=> string(304) "Возможности и перспективы использования конфокальной микроскопии для оценки результатов перекрестного типирования HLA у пациентов с трансплантацией костного мозга" ["SECTION_PICTURE_FILE_TITLE"]=> string(304) "Возможности и перспективы использования конфокальной микроскопии для оценки результатов перекрестного типирования HLA у пациентов с трансплантацией костного мозга" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "vozmozhnosti-i-perspektivy-ispolzovaniya-konfokalnoy-mikroskopii-dlya-otsenki-rezultatov-perekrestno" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(304) "Возможности и перспективы использования конфокальной микроскопии для оценки результатов перекрестного типирования HLA у пациентов с трансплантацией костного мозга" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(304) "Возможности и перспективы использования конфокальной микроскопии для оценки результатов перекрестного типирования HLA у пациентов с трансплантацией костного мозга" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vozmozhnosti-i-perspektivy-ispolzovaniya-konfokalnoy-mikroskopii-dlya-otsenki-rezultatov-perekrestno" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "vozmozhnosti-i-perspektivy-ispolzovaniya-konfokalnoy-mikroskopii-dlya-otsenki-rezultatov-perekrestno" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vozmozhnosti-i-perspektivy-ispolzovaniya-konfokalnoy-mikroskopii-dlya-otsenki-rezultatov-perekrestno" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20592" ["VALUE"]=> array(2) { ["TEXT"]=> string(95) "Альберт Р. Муслимов, Александр С. Тимин, Юрий А. Серов" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(95) "Альберт Р. Муслимов, Александр С. Тимин, Юрий А. Серов" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20593" ["VALUE"]=> array(2) { ["TEXT"]=> string(310) "Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(304) "Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20594" ["VALUE"]=> array(2) { ["TEXT"]=> string(7087) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> В последние годы становится все более очевидным, что роль анти-донорских HLA антител, направленных против антигенов HLA класса I и II не ограничивается их участием в развитии сверхострого отторжения аллотрансплантатов. Все большее число исследователей склонны считать, что образование анти-донорских HLA антител в посттрансплантационный период приводит к развитию ускоренного острого, острого или хронического отторжения. Тест на иммунологическую совместимость между донором и реципиентом при трансплантации является решающим показателем для принятия решения о проведении трансплантации. Антитела к HLA обнаруживаются более чем у 30% населения, их выявление свидетельствует о предшествующей иммунизации HLA. Она возможна при многократном переливании цельной крови, во время беременности и после трансплантации. Ряд авторов отмечает, что донор неспецифические антитела к HLA являются одним из факторов не только риска острого, но и хронического отторжения трансплантата и учитываются, как плохой прогностический показатель [P.I.Terasaki, 2006; М. Моrrel, 2011; M. Crespo, 2011]. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Целью теста HLA-Crossmatch является обнаружение лимфоцитотоксических антител, специфичных для потенциального донора (то есть аллогенный перекрестный кроссматч) или у самого себя (то есть аутологичный перекрестный HLA-Crossmatch). Прямой HLA-Crossmatch, используется с сывороткой от предполагаемого реципиента (или донора для обратного HLA-Crossmatch) и клетками-мишенями являются мононуклеарные клетки потенциального донора (или реципиента для обратного HLA-Crossmatch. Используемые клетки-мишени могут быть не разделены или разделены на определенные группы, такие как Т- лимфоциты, В- лимфоциты, моноциты и т. д. Оценка результатов реакции HLA-Crossmatch крайне субъективна при простой оптической микроскопии, т.к. невозможно точно посчитать количество мертвых клеток в поле зрения камеры Терасаки и вычесть фон (результаты негативного контроля). Невозможна так же оценка к какому классу HLA (I или II) принадлежат антитела. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Нами был разработан метод оценки результатов HLACrossmatch с использованием конфокального микроскопа у пациентов с трансплантацией костного мозга. Вся постановка реакции HLA-Crossmatch проводилась стандартным методом, кроме последнего этапа: окраски и оценки жизнеспособности лимфоцитов в лунках. Мы использовали Акридиновый Оранжевый (АО – эмиссия 525 нм) и Пропидиум Йодид (PI – 620 нм) как витальные красители. Для окраски B лимфоцитов использовались анти-CD19 моноклональные антитела, конъюгированные с PE-Cyanine7 (775 нм). Результаты регистрировались с помощью ZEISS конфокального микроскопа с последующим анализом изображений программным продуктом ImageJ (National Institutes of Health) c последующим обсчетом результатов нами созданной программой. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Предложенный нами метод оценки имеет следующие преимущества: 1) В одной лунке производится анализ одной сыворотки реципиента на наличие антител против донорских антигенов HLA одновременно и по I, и по II классу; 2) Метод является быстрым, точным и высокопроизводительным (в одной камере Терасаки за один запуск можно проанализировать до 72 сывороток); 3) Высокая чувствительность считывания флуоресцентной метки; 4) Наличие многоуровневой системы различных контролей; 5) Возможность архивирования полученных результатов в базе данных программы для интерпретации и PDF отчетов; 6) Субъективная оценка в анализе результатов сведена к минимуму за счет статистической обработки полученных данных программным обеспечением. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> HLA, перекрестный подбор HLA, трансплантация костного мозга, конфокальная микроскопия. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6855) "
Введение
В последние годы становится все более очевидным, что роль анти-донорских HLA антител, направленных против антигенов HLA класса I и II не ограничивается их участием в развитии сверхострого отторжения аллотрансплантатов. Все большее число исследователей склонны считать, что образование анти-донорских HLA антител в посттрансплантационный период приводит к развитию ускоренного острого, острого или хронического отторжения. Тест на иммунологическую совместимость между донором и реципиентом при трансплантации является решающим показателем для принятия решения о проведении трансплантации. Антитела к HLA обнаруживаются более чем у 30% населения, их выявление свидетельствует о предшествующей иммунизации HLA. Она возможна при многократном переливании цельной крови, во время беременности и после трансплантации. Ряд авторов отмечает, что донор неспецифические антитела к HLA являются одним из факторов не только риска острого, но и хронического отторжения трансплантата и учитываются, как плохой прогностический показатель [P.I.Terasaki, 2006; М. Моrrel, 2011; M. Crespo, 2011].
Цель
Целью теста HLA-Crossmatch является обнаружение лимфоцитотоксических антител, специфичных для потенциального донора (то есть аллогенный перекрестный кроссматч) или у самого себя (то есть аутологичный перекрестный HLA-Crossmatch). Прямой HLA-Crossmatch, используется с сывороткой от предполагаемого реципиента (или донора для обратного HLA-Crossmatch) и клетками-мишенями являются мононуклеарные клетки потенциального донора (или реципиента для обратного HLA-Crossmatch. Используемые клетки-мишени могут быть не разделены или разделены на определенные группы, такие как Т- лимфоциты, В- лимфоциты, моноциты и т. д. Оценка результатов реакции HLA-Crossmatch крайне субъективна при простой оптической микроскопии, т.к. невозможно точно посчитать количество мертвых клеток в поле зрения камеры Терасаки и вычесть фон (результаты негативного контроля). Невозможна так же оценка к какому классу HLA (I или II) принадлежат антитела.
Материалы и методы
Нами был разработан метод оценки результатов HLACrossmatch с использованием конфокального микроскопа у пациентов с трансплантацией костного мозга. Вся постановка реакции HLA-Crossmatch проводилась стандартным методом, кроме последнего этапа: окраски и оценки жизнеспособности лимфоцитов в лунках. Мы использовали Акридиновый Оранжевый (АО – эмиссия 525 нм) и Пропидиум Йодид (PI – 620 нм) как витальные красители. Для окраски B лимфоцитов использовались анти-CD19 моноклональные антитела, конъюгированные с PE-Cyanine7 (775 нм). Результаты регистрировались с помощью ZEISS конфокального микроскопа с последующим анализом изображений программным продуктом ImageJ (National Institutes of Health) c последующим обсчетом результатов нами созданной программой.
Выводы
Предложенный нами метод оценки имеет следующие преимущества: 1) В одной лунке производится анализ одной сыворотки реципиента на наличие антител против донорских антигенов HLA одновременно и по I, и по II классу; 2) Метод является быстрым, точным и высокопроизводительным (в одной камере Терасаки за один запуск можно проанализировать до 72 сывороток); 3) Высокая чувствительность считывания флуоресцентной метки; 4) Наличие многоуровневой системы различных контролей; 5) Возможность архивирования полученных результатов в базе данных программы для интерпретации и PDF отчетов; 6) Субъективная оценка в анализе результатов сведена к минимуму за счет статистической обработки полученных данных программным обеспечением.
Ключевые слова
HLA, перекрестный подбор HLA, трансплантация костного мозга, конфокальная микроскопия.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20595" ["VALUE"]=> array(2) { ["TEXT"]=> string(54) "Аlbert R. Muslimov, Alexander S. Timin, Yury A. Serov" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(54) "Аlbert R. Muslimov, Alexander S. Timin, Yury A. Serov" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20596" ["VALUE"]=> array(2) { ["TEXT"]=> string(184) "Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(178) "Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20597" ["VALUE"]=> array(2) { ["TEXT"]=> string(4159) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Currently, it has become progressively ostensible that the role of the anti-donor antibody against HLA class I and II antigens is not limited to their participation in the development of hyperacute rejection of allografts. An increasing number of researchers are inclined to believe that the formation of anti-donor HLA antibody in the posttransplant period leads to the development of hyperacute, acute or chronic rejection. The immunological compatibility test between donor and recipient for transplantation is the critical factor for deciding whether to perform a transplant. Antibodies to HLA founded in more than 30% of the population; their detection indicates a prior immunization with HLA. It is possible with multiple transfusion of whole blood, during pregnancy and after transplantation. A number of authors making a point that the donor non-specific antibodies to HLA are one of the factors not only of the risk of acute but also chronic rejection of the transplant and are considered as a poor prognostic indicator [P.I. Terasaki, 2006; M. Morrel, 2011; M. Crespo, 2011]. </p> <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> The purpose of the lymphocyte crossmatch is to detect the lymphocytotoxic antibodies specific to a potential donor (i.e., allogeneic crossmatch) or self (i.e., autologous crossmatch.) A forward crossmatch used with serum from a prospective recipient (or donor for reverse crossmatch) and the target cells are the mononuclear cells of the potential donor (or recipient for reverse crossmatch). The target cells used may be unseparated or separated into specific subsets such as T cell lymphocytes, B cell lymphocytes, monocytes, etc. Evaluation of the results of the HLA-Crossmatch reaction is highly subjective by simple optical microscopy because it is impossible to accurately calculate the number of dead cells at the Terasaki camera view field and subtract the background (the results of negative control). It is also problematic to estimate to which class of HLA (I or II) antibodies belong. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> We developed a methodology for evaluating the results of HLA-crossmatch using a confocal microscope of the bone marrow transplantation patients. The entire HLA-crossmatch reaction performed by a standard method, except for the last two steps: staining and evaluation of the viability of lymphocytes in the wells. We used Acridine Orange (AO emission 525 nm) and Propidium Iodide (PI – 620 nm) as vital dyes. To stain B-lymphocytes, anti-CD19 monoclonal antibodies conjugated to PE-Cyanine7 (775 nm) were used. The images taken with a ZEISS confocal microscope, followed by image analysis with the ImageJ software (National Institutes of Health), and then calculating the results with the program. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> The advantages of the proposed method of evaluation are as follows: (1) In one well, a single serum sample of the recipient is analyzed for the presence of antibodies against donor HLA antigens simultaneously at both I and II classes. 2) The method is fast, accurate and high-performance (in one Terasaki plate, up to 72 sera samples can be analyzed in one run). 3) The high sensitivity of fluorescent label reading. (4) Presence of a multilevel system of various controls. (5) The ability to archive the results obtained in the program database for interpretation and PDF reports. (6) Subjective biases of the data analysis are minimized by statistical processing of the data by software. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> HLA, HLA-crossmatch, bone marrow transplantation, confocal microscopy. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3927) "
Introduction
Currently, it has become progressively ostensible that the role of the anti-donor antibody against HLA class I and II antigens is not limited to their participation in the development of hyperacute rejection of allografts. An increasing number of researchers are inclined to believe that the formation of anti-donor HLA antibody in the posttransplant period leads to the development of hyperacute, acute or chronic rejection. The immunological compatibility test between donor and recipient for transplantation is the critical factor for deciding whether to perform a transplant. Antibodies to HLA founded in more than 30% of the population; their detection indicates a prior immunization with HLA. It is possible with multiple transfusion of whole blood, during pregnancy and after transplantation. A number of authors making a point that the donor non-specific antibodies to HLA are one of the factors not only of the risk of acute but also chronic rejection of the transplant and are considered as a poor prognostic indicator [P.I. Terasaki, 2006; M. Morrel, 2011; M. Crespo, 2011].
Aim
The purpose of the lymphocyte crossmatch is to detect the lymphocytotoxic antibodies specific to a potential donor (i.e., allogeneic crossmatch) or self (i.e., autologous crossmatch.) A forward crossmatch used with serum from a prospective recipient (or donor for reverse crossmatch) and the target cells are the mononuclear cells of the potential donor (or recipient for reverse crossmatch). The target cells used may be unseparated or separated into specific subsets such as T cell lymphocytes, B cell lymphocytes, monocytes, etc. Evaluation of the results of the HLA-Crossmatch reaction is highly subjective by simple optical microscopy because it is impossible to accurately calculate the number of dead cells at the Terasaki camera view field and subtract the background (the results of negative control). It is also problematic to estimate to which class of HLA (I or II) antibodies belong.
Materials and methods
We developed a methodology for evaluating the results of HLA-crossmatch using a confocal microscope of the bone marrow transplantation patients. The entire HLA-crossmatch reaction performed by a standard method, except for the last two steps: staining and evaluation of the viability of lymphocytes in the wells. We used Acridine Orange (AO emission 525 nm) and Propidium Iodide (PI – 620 nm) as vital dyes. To stain B-lymphocytes, anti-CD19 monoclonal antibodies conjugated to PE-Cyanine7 (775 nm) were used. The images taken with a ZEISS confocal microscope, followed by image analysis with the ImageJ software (National Institutes of Health), and then calculating the results with the program.
Conclusions
The advantages of the proposed method of evaluation are as follows: (1) In one well, a single serum sample of the recipient is analyzed for the presence of antibodies against donor HLA antigens simultaneously at both I and II classes. 2) The method is fast, accurate and high-performance (in one Terasaki plate, up to 72 sera samples can be analyzed in one run). 3) The high sensitivity of fluorescent label reading. (4) Presence of a multilevel system of various controls. (5) The ability to archive the results obtained in the program database for interpretation and PDF reports. (6) Subjective biases of the data analysis are minimized by statistical processing of the data by software.
Keywords
HLA, HLA-crossmatch, bone marrow transplantation, confocal microscopy.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20598" ["VALUE"]=> string(136) "Potentials and prospects of using a confocal microscopy for the HLA-Crossmatch result evaluation in bone marrow transplantation patients" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(136) "Potentials and prospects of using a confocal microscopy for the HLA-Crossmatch result evaluation in bone marrow transplantation patients" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20799" ["VALUE"]=> string(4) "1437" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1437" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20800" ["VALUE"]=> string(4) "1438" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1438" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20595" ["VALUE"]=> array(2) { ["TEXT"]=> string(54) "Аlbert R. Muslimov, Alexander S. Timin, Yury A. Serov" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(54) "Аlbert R. Muslimov, Alexander S. Timin, Yury A. Serov" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(54) "Аlbert R. Muslimov, Alexander S. Timin, Yury A. Serov" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20597" ["VALUE"]=> array(2) { ["TEXT"]=> string(4159) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Currently, it has become progressively ostensible that the role of the anti-donor antibody against HLA class I and II antigens is not limited to their participation in the development of hyperacute rejection of allografts. An increasing number of researchers are inclined to believe that the formation of anti-donor HLA antibody in the posttransplant period leads to the development of hyperacute, acute or chronic rejection. The immunological compatibility test between donor and recipient for transplantation is the critical factor for deciding whether to perform a transplant. Antibodies to HLA founded in more than 30% of the population; their detection indicates a prior immunization with HLA. It is possible with multiple transfusion of whole blood, during pregnancy and after transplantation. A number of authors making a point that the donor non-specific antibodies to HLA are one of the factors not only of the risk of acute but also chronic rejection of the transplant and are considered as a poor prognostic indicator [P.I. Terasaki, 2006; M. Morrel, 2011; M. Crespo, 2011]. </p> <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> The purpose of the lymphocyte crossmatch is to detect the lymphocytotoxic antibodies specific to a potential donor (i.e., allogeneic crossmatch) or self (i.e., autologous crossmatch.) A forward crossmatch used with serum from a prospective recipient (or donor for reverse crossmatch) and the target cells are the mononuclear cells of the potential donor (or recipient for reverse crossmatch). The target cells used may be unseparated or separated into specific subsets such as T cell lymphocytes, B cell lymphocytes, monocytes, etc. Evaluation of the results of the HLA-Crossmatch reaction is highly subjective by simple optical microscopy because it is impossible to accurately calculate the number of dead cells at the Terasaki camera view field and subtract the background (the results of negative control). It is also problematic to estimate to which class of HLA (I or II) antibodies belong. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> We developed a methodology for evaluating the results of HLA-crossmatch using a confocal microscope of the bone marrow transplantation patients. The entire HLA-crossmatch reaction performed by a standard method, except for the last two steps: staining and evaluation of the viability of lymphocytes in the wells. We used Acridine Orange (AO emission 525 nm) and Propidium Iodide (PI – 620 nm) as vital dyes. To stain B-lymphocytes, anti-CD19 monoclonal antibodies conjugated to PE-Cyanine7 (775 nm) were used. The images taken with a ZEISS confocal microscope, followed by image analysis with the ImageJ software (National Institutes of Health), and then calculating the results with the program. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> The advantages of the proposed method of evaluation are as follows: (1) In one well, a single serum sample of the recipient is analyzed for the presence of antibodies against donor HLA antigens simultaneously at both I and II classes. 2) The method is fast, accurate and high-performance (in one Terasaki plate, up to 72 sera samples can be analyzed in one run). 3) The high sensitivity of fluorescent label reading. (4) Presence of a multilevel system of various controls. (5) The ability to archive the results obtained in the program database for interpretation and PDF reports. (6) Subjective biases of the data analysis are minimized by statistical processing of the data by software. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> HLA, HLA-crossmatch, bone marrow transplantation, confocal microscopy. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3927) "Introduction
Currently, it has become progressively ostensible that the role of the anti-donor antibody against HLA class I and II antigens is not limited to their participation in the development of hyperacute rejection of allografts. An increasing number of researchers are inclined to believe that the formation of anti-donor HLA antibody in the posttransplant period leads to the development of hyperacute, acute or chronic rejection. The immunological compatibility test between donor and recipient for transplantation is the critical factor for deciding whether to perform a transplant. Antibodies to HLA founded in more than 30% of the population; their detection indicates a prior immunization with HLA. It is possible with multiple transfusion of whole blood, during pregnancy and after transplantation. A number of authors making a point that the donor non-specific antibodies to HLA are one of the factors not only of the risk of acute but also chronic rejection of the transplant and are considered as a poor prognostic indicator [P.I. Terasaki, 2006; M. Morrel, 2011; M. Crespo, 2011].
Aim
The purpose of the lymphocyte crossmatch is to detect the lymphocytotoxic antibodies specific to a potential donor (i.e., allogeneic crossmatch) or self (i.e., autologous crossmatch.) A forward crossmatch used with serum from a prospective recipient (or donor for reverse crossmatch) and the target cells are the mononuclear cells of the potential donor (or recipient for reverse crossmatch). The target cells used may be unseparated or separated into specific subsets such as T cell lymphocytes, B cell lymphocytes, monocytes, etc. Evaluation of the results of the HLA-Crossmatch reaction is highly subjective by simple optical microscopy because it is impossible to accurately calculate the number of dead cells at the Terasaki camera view field and subtract the background (the results of negative control). It is also problematic to estimate to which class of HLA (I or II) antibodies belong.
Materials and methods
We developed a methodology for evaluating the results of HLA-crossmatch using a confocal microscope of the bone marrow transplantation patients. The entire HLA-crossmatch reaction performed by a standard method, except for the last two steps: staining and evaluation of the viability of lymphocytes in the wells. We used Acridine Orange (AO emission 525 nm) and Propidium Iodide (PI – 620 nm) as vital dyes. To stain B-lymphocytes, anti-CD19 monoclonal antibodies conjugated to PE-Cyanine7 (775 nm) were used. The images taken with a ZEISS confocal microscope, followed by image analysis with the ImageJ software (National Institutes of Health), and then calculating the results with the program.
Conclusions
The advantages of the proposed method of evaluation are as follows: (1) In one well, a single serum sample of the recipient is analyzed for the presence of antibodies against donor HLA antigens simultaneously at both I and II classes. 2) The method is fast, accurate and high-performance (in one Terasaki plate, up to 72 sera samples can be analyzed in one run). 3) The high sensitivity of fluorescent label reading. (4) Presence of a multilevel system of various controls. (5) The ability to archive the results obtained in the program database for interpretation and PDF reports. (6) Subjective biases of the data analysis are minimized by statistical processing of the data by software.
Keywords
HLA, HLA-crossmatch, bone marrow transplantation, confocal microscopy.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3927) "Introduction
Currently, it has become progressively ostensible that the role of the anti-donor antibody against HLA class I and II antigens is not limited to their participation in the development of hyperacute rejection of allografts. An increasing number of researchers are inclined to believe that the formation of anti-donor HLA antibody in the posttransplant period leads to the development of hyperacute, acute or chronic rejection. The immunological compatibility test between donor and recipient for transplantation is the critical factor for deciding whether to perform a transplant. Antibodies to HLA founded in more than 30% of the population; their detection indicates a prior immunization with HLA. It is possible with multiple transfusion of whole blood, during pregnancy and after transplantation. A number of authors making a point that the donor non-specific antibodies to HLA are one of the factors not only of the risk of acute but also chronic rejection of the transplant and are considered as a poor prognostic indicator [P.I. Terasaki, 2006; M. Morrel, 2011; M. Crespo, 2011].
Aim
The purpose of the lymphocyte crossmatch is to detect the lymphocytotoxic antibodies specific to a potential donor (i.e., allogeneic crossmatch) or self (i.e., autologous crossmatch.) A forward crossmatch used with serum from a prospective recipient (or donor for reverse crossmatch) and the target cells are the mononuclear cells of the potential donor (or recipient for reverse crossmatch). The target cells used may be unseparated or separated into specific subsets such as T cell lymphocytes, B cell lymphocytes, monocytes, etc. Evaluation of the results of the HLA-Crossmatch reaction is highly subjective by simple optical microscopy because it is impossible to accurately calculate the number of dead cells at the Terasaki camera view field and subtract the background (the results of negative control). It is also problematic to estimate to which class of HLA (I or II) antibodies belong.
Materials and methods
We developed a methodology for evaluating the results of HLA-crossmatch using a confocal microscope of the bone marrow transplantation patients. The entire HLA-crossmatch reaction performed by a standard method, except for the last two steps: staining and evaluation of the viability of lymphocytes in the wells. We used Acridine Orange (AO emission 525 nm) and Propidium Iodide (PI – 620 nm) as vital dyes. To stain B-lymphocytes, anti-CD19 monoclonal antibodies conjugated to PE-Cyanine7 (775 nm) were used. The images taken with a ZEISS confocal microscope, followed by image analysis with the ImageJ software (National Institutes of Health), and then calculating the results with the program.
Conclusions
The advantages of the proposed method of evaluation are as follows: (1) In one well, a single serum sample of the recipient is analyzed for the presence of antibodies against donor HLA antigens simultaneously at both I and II classes. 2) The method is fast, accurate and high-performance (in one Terasaki plate, up to 72 sera samples can be analyzed in one run). 3) The high sensitivity of fluorescent label reading. (4) Presence of a multilevel system of various controls. (5) The ability to archive the results obtained in the program database for interpretation and PDF reports. (6) Subjective biases of the data analysis are minimized by statistical processing of the data by software.
Keywords
HLA, HLA-crossmatch, bone marrow transplantation, confocal microscopy.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20598" ["VALUE"]=> string(136) "Potentials and prospects of using a confocal microscopy for the HLA-Crossmatch result evaluation in bone marrow transplantation patients" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(136) "Potentials and prospects of using a confocal microscopy for the HLA-Crossmatch result evaluation in bone marrow transplantation patients" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(136) "Potentials and prospects of using a confocal microscopy for the HLA-Crossmatch result evaluation in bone marrow transplantation patients" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20596" ["VALUE"]=> array(2) { ["TEXT"]=> string(184) "Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(178) "Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(178) "Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20592" ["VALUE"]=> array(2) { ["TEXT"]=> string(95) "Альберт Р. Муслимов, Александр С. Тимин, Юрий А. Серов" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(95) "Альберт Р. Муслимов, Александр С. Тимин, Юрий А. Серов" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(95) "Альберт Р. Муслимов, Александр С. Тимин, Юрий А. Серов" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20594" ["VALUE"]=> array(2) { ["TEXT"]=> string(7087) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> В последние годы становится все более очевидным, что роль анти-донорских HLA антител, направленных против антигенов HLA класса I и II не ограничивается их участием в развитии сверхострого отторжения аллотрансплантатов. Все большее число исследователей склонны считать, что образование анти-донорских HLA антител в посттрансплантационный период приводит к развитию ускоренного острого, острого или хронического отторжения. Тест на иммунологическую совместимость между донором и реципиентом при трансплантации является решающим показателем для принятия решения о проведении трансплантации. Антитела к HLA обнаруживаются более чем у 30% населения, их выявление свидетельствует о предшествующей иммунизации HLA. Она возможна при многократном переливании цельной крови, во время беременности и после трансплантации. Ряд авторов отмечает, что донор неспецифические антитела к HLA являются одним из факторов не только риска острого, но и хронического отторжения трансплантата и учитываются, как плохой прогностический показатель [P.I.Terasaki, 2006; М. Моrrel, 2011; M. Crespo, 2011]. </p> <h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Целью теста HLA-Crossmatch является обнаружение лимфоцитотоксических антител, специфичных для потенциального донора (то есть аллогенный перекрестный кроссматч) или у самого себя (то есть аутологичный перекрестный HLA-Crossmatch). Прямой HLA-Crossmatch, используется с сывороткой от предполагаемого реципиента (или донора для обратного HLA-Crossmatch) и клетками-мишенями являются мононуклеарные клетки потенциального донора (или реципиента для обратного HLA-Crossmatch. Используемые клетки-мишени могут быть не разделены или разделены на определенные группы, такие как Т- лимфоциты, В- лимфоциты, моноциты и т. д. Оценка результатов реакции HLA-Crossmatch крайне субъективна при простой оптической микроскопии, т.к. невозможно точно посчитать количество мертвых клеток в поле зрения камеры Терасаки и вычесть фон (результаты негативного контроля). Невозможна так же оценка к какому классу HLA (I или II) принадлежат антитела. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> Нами был разработан метод оценки результатов HLACrossmatch с использованием конфокального микроскопа у пациентов с трансплантацией костного мозга. Вся постановка реакции HLA-Crossmatch проводилась стандартным методом, кроме последнего этапа: окраски и оценки жизнеспособности лимфоцитов в лунках. Мы использовали Акридиновый Оранжевый (АО – эмиссия 525 нм) и Пропидиум Йодид (PI – 620 нм) как витальные красители. Для окраски B лимфоцитов использовались анти-CD19 моноклональные антитела, конъюгированные с PE-Cyanine7 (775 нм). Результаты регистрировались с помощью ZEISS конфокального микроскопа с последующим анализом изображений программным продуктом ImageJ (National Institutes of Health) c последующим обсчетом результатов нами созданной программой. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Предложенный нами метод оценки имеет следующие преимущества: 1) В одной лунке производится анализ одной сыворотки реципиента на наличие антител против донорских антигенов HLA одновременно и по I, и по II классу; 2) Метод является быстрым, точным и высокопроизводительным (в одной камере Терасаки за один запуск можно проанализировать до 72 сывороток); 3) Высокая чувствительность считывания флуоресцентной метки; 4) Наличие многоуровневой системы различных контролей; 5) Возможность архивирования полученных результатов в базе данных программы для интерпретации и PDF отчетов; 6) Субъективная оценка в анализе результатов сведена к минимуму за счет статистической обработки полученных данных программным обеспечением. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> HLA, перекрестный подбор HLA, трансплантация костного мозга, конфокальная микроскопия. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6855) "
Введение
В последние годы становится все более очевидным, что роль анти-донорских HLA антител, направленных против антигенов HLA класса I и II не ограничивается их участием в развитии сверхострого отторжения аллотрансплантатов. Все большее число исследователей склонны считать, что образование анти-донорских HLA антител в посттрансплантационный период приводит к развитию ускоренного острого, острого или хронического отторжения. Тест на иммунологическую совместимость между донором и реципиентом при трансплантации является решающим показателем для принятия решения о проведении трансплантации. Антитела к HLA обнаруживаются более чем у 30% населения, их выявление свидетельствует о предшествующей иммунизации HLA. Она возможна при многократном переливании цельной крови, во время беременности и после трансплантации. Ряд авторов отмечает, что донор неспецифические антитела к HLA являются одним из факторов не только риска острого, но и хронического отторжения трансплантата и учитываются, как плохой прогностический показатель [P.I.Terasaki, 2006; М. Моrrel, 2011; M. Crespo, 2011].
Цель
Целью теста HLA-Crossmatch является обнаружение лимфоцитотоксических антител, специфичных для потенциального донора (то есть аллогенный перекрестный кроссматч) или у самого себя (то есть аутологичный перекрестный HLA-Crossmatch). Прямой HLA-Crossmatch, используется с сывороткой от предполагаемого реципиента (или донора для обратного HLA-Crossmatch) и клетками-мишенями являются мононуклеарные клетки потенциального донора (или реципиента для обратного HLA-Crossmatch. Используемые клетки-мишени могут быть не разделены или разделены на определенные группы, такие как Т- лимфоциты, В- лимфоциты, моноциты и т. д. Оценка результатов реакции HLA-Crossmatch крайне субъективна при простой оптической микроскопии, т.к. невозможно точно посчитать количество мертвых клеток в поле зрения камеры Терасаки и вычесть фон (результаты негативного контроля). Невозможна так же оценка к какому классу HLA (I или II) принадлежат антитела.
Материалы и методы
Нами был разработан метод оценки результатов HLACrossmatch с использованием конфокального микроскопа у пациентов с трансплантацией костного мозга. Вся постановка реакции HLA-Crossmatch проводилась стандартным методом, кроме последнего этапа: окраски и оценки жизнеспособности лимфоцитов в лунках. Мы использовали Акридиновый Оранжевый (АО – эмиссия 525 нм) и Пропидиум Йодид (PI – 620 нм) как витальные красители. Для окраски B лимфоцитов использовались анти-CD19 моноклональные антитела, конъюгированные с PE-Cyanine7 (775 нм). Результаты регистрировались с помощью ZEISS конфокального микроскопа с последующим анализом изображений программным продуктом ImageJ (National Institutes of Health) c последующим обсчетом результатов нами созданной программой.
Выводы
Предложенный нами метод оценки имеет следующие преимущества: 1) В одной лунке производится анализ одной сыворотки реципиента на наличие антител против донорских антигенов HLA одновременно и по I, и по II классу; 2) Метод является быстрым, точным и высокопроизводительным (в одной камере Терасаки за один запуск можно проанализировать до 72 сывороток); 3) Высокая чувствительность считывания флуоресцентной метки; 4) Наличие многоуровневой системы различных контролей; 5) Возможность архивирования полученных результатов в базе данных программы для интерпретации и PDF отчетов; 6) Субъективная оценка в анализе результатов сведена к минимуму за счет статистической обработки полученных данных программным обеспечением.
Ключевые слова
HLA, перекрестный подбор HLA, трансплантация костного мозга, конфокальная микроскопия.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6855) "Введение
В последние годы становится все более очевидным, что роль анти-донорских HLA антител, направленных против антигенов HLA класса I и II не ограничивается их участием в развитии сверхострого отторжения аллотрансплантатов. Все большее число исследователей склонны считать, что образование анти-донорских HLA антител в посттрансплантационный период приводит к развитию ускоренного острого, острого или хронического отторжения. Тест на иммунологическую совместимость между донором и реципиентом при трансплантации является решающим показателем для принятия решения о проведении трансплантации. Антитела к HLA обнаруживаются более чем у 30% населения, их выявление свидетельствует о предшествующей иммунизации HLA. Она возможна при многократном переливании цельной крови, во время беременности и после трансплантации. Ряд авторов отмечает, что донор неспецифические антитела к HLA являются одним из факторов не только риска острого, но и хронического отторжения трансплантата и учитываются, как плохой прогностический показатель [P.I.Terasaki, 2006; М. Моrrel, 2011; M. Crespo, 2011].
Цель
Целью теста HLA-Crossmatch является обнаружение лимфоцитотоксических антител, специфичных для потенциального донора (то есть аллогенный перекрестный кроссматч) или у самого себя (то есть аутологичный перекрестный HLA-Crossmatch). Прямой HLA-Crossmatch, используется с сывороткой от предполагаемого реципиента (или донора для обратного HLA-Crossmatch) и клетками-мишенями являются мононуклеарные клетки потенциального донора (или реципиента для обратного HLA-Crossmatch. Используемые клетки-мишени могут быть не разделены или разделены на определенные группы, такие как Т- лимфоциты, В- лимфоциты, моноциты и т. д. Оценка результатов реакции HLA-Crossmatch крайне субъективна при простой оптической микроскопии, т.к. невозможно точно посчитать количество мертвых клеток в поле зрения камеры Терасаки и вычесть фон (результаты негативного контроля). Невозможна так же оценка к какому классу HLA (I или II) принадлежат антитела.
Материалы и методы
Нами был разработан метод оценки результатов HLACrossmatch с использованием конфокального микроскопа у пациентов с трансплантацией костного мозга. Вся постановка реакции HLA-Crossmatch проводилась стандартным методом, кроме последнего этапа: окраски и оценки жизнеспособности лимфоцитов в лунках. Мы использовали Акридиновый Оранжевый (АО – эмиссия 525 нм) и Пропидиум Йодид (PI – 620 нм) как витальные красители. Для окраски B лимфоцитов использовались анти-CD19 моноклональные антитела, конъюгированные с PE-Cyanine7 (775 нм). Результаты регистрировались с помощью ZEISS конфокального микроскопа с последующим анализом изображений программным продуктом ImageJ (National Institutes of Health) c последующим обсчетом результатов нами созданной программой.
Выводы
Предложенный нами метод оценки имеет следующие преимущества: 1) В одной лунке производится анализ одной сыворотки реципиента на наличие антител против донорских антигенов HLA одновременно и по I, и по II классу; 2) Метод является быстрым, точным и высокопроизводительным (в одной камере Терасаки за один запуск можно проанализировать до 72 сывороток); 3) Высокая чувствительность считывания флуоресцентной метки; 4) Наличие многоуровневой системы различных контролей; 5) Возможность архивирования полученных результатов в базе данных программы для интерпретации и PDF отчетов; 6) Субъективная оценка в анализе результатов сведена к минимуму за счет статистической обработки полученных данных программным обеспечением.
Ключевые слова
HLA, перекрестный подбор HLA, трансплантация костного мозга, конфокальная микроскопия.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20593" ["VALUE"]=> array(2) { ["TEXT"]=> string(310) "Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(304) "Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(304) "Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова
" } } } [49]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1588" ["~ID"]=> string(4) "1588" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(246) "Прогнозирование результатов аутологичной трансплантации стволовых гемопоэтических клеток у взрослых пациентов с лимфомой Ходжкина" ["~NAME"]=> string(246) "Прогнозирование результатов аутологичной трансплантации стволовых гемопоэтических клеток у взрослых пациентов с лимфомой Ходжкина" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:41:16" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:41:16" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/prognozirovanie-rezultatov-autologichnoy-transplantatsii-stvolovykh-gemopoeticheskikh-kletok-u-vzros/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/prognozirovanie-rezultatov-autologichnoy-transplantatsii-stvolovykh-gemopoeticheskikh-kletok-u-vzros/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "prognozirovanie-rezultatov-autologichnoy-transplantatsii-stvolovykh-gemopoeticheskikh-kletok-u-vzros" ["~CODE"]=> string(100) "prognozirovanie-rezultatov-autologichnoy-transplantatsii-stvolovykh-gemopoeticheskikh-kletok-u-vzros" ["EXTERNAL_ID"]=> string(4) "1588" ["~EXTERNAL_ID"]=> string(4) "1588" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(246) "Прогнозирование результатов аутологичной трансплантации стволовых гемопоэтических клеток у взрослых пациентов с лимфомой Ходжкина" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(339) "Прогнозирование результатов аутологичной трансплантации стволовых гемопоэтических клеток у взрослых пациентов с лимфомой ХоджкинаPrognostic factors in autologous stem cell transplant on adult patients with Hodgkin lymphoma" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(10912) "<h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Целью работы был анализ показателей общей и бессобытийной выживаемости в зависимости от различных прогностических факторов. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Проанализированы данные 84 пациентов. Медиана возраста 26,6 года (18-62). Медиана наблюдения составила 49 месяцев (0,5-115 мес.). Исследованы влияния: пола, ответа на первичное лечение, скорости развития рецидива, варианта химиотерапии второй линии, В-симптомов, конгломератов более 5 см (в рецидиве и непосредственно перед ВДХТ), уровней альбумина и ЛДГ крови, КТ-ответа, общего количества линий химиотерапии, режима кондиционирования перед АТГСК, метаболической активности опухоли до ВДХТ (ПЭТ1) и после АТГСК (ПЭТ2). Для статистического анализа использованы методы Каплана-Мейера, Кокса, статистические критерии Манна-Уитни и Хи-квадрат. Результаты. Приведены показатели общей и бессобытийной выживаемости, а также расчет отношения рисков для факторов, показавших статистическую достоверность менее 0,05 (Табл. 1, 2). При анализе бессобытийной выживаемости выявлены статистически значимые различия в выживаемости при негативности по ПЭТ1 и ПЭТ2 по сравнению с группой пациентов с позитивностью очагов по ПЭТ1 и ПЭТ2 (Табл. 3, 4). Других различий не выявлено. </p> <h2 style="text-align: justify;">Вывод</h2> <p style="text-align: justify;"> Исследование показало, что наиболее важными факторами прогноза бессобытийной выживаемости пациентов с ЛХ после ВДХТ/АТГСК являются повышение активности ЛДГ, наличие В-симптомов в рецидиве, позитивность по ПЭТ1, предлеченность и, особенно, отсутствие ответа по данным КТ и определение метаболической активности после ВДХТ/АТГСК. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфома Ходжкина, аутологичная трансплантация стволовых клеток, ПЭТ, ЛДГ, альбумин. </p> <h2 style="text-align: justify;"> Таблица 1. Четырехлетняя бессобытийная выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)<br> </h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Факторы </td> <td> Есть </td> <td> Нет </td> <td> p </td> </tr> <tr> <td> B-симптомы в рецидиве </td> <td> 35% </td> <td> 61% </td> <td> 0,0246 </td> </tr> <tr> <td> Гипоальбуминемия </td> <td> 33%<br> </td> <td> 62%<br> </td> <td> 0,0494 </td> </tr> <tr> <td> Повышение активности ЛДГ </td> <td> 36% </td> <td> 66% </td> <td> 0,0302 </td> </tr> <tr> <td> Отсутствие ответа по данным КТ </td> <td> 33% </td> <td> 66% </td> <td> 0,0035 </td> </tr> <tr> <td> Позитивность по ПЭТ1 </td> <td> 31%<br> </td> <td> 70% </td> <td> 0,0072 </td> </tr> <tr> <td> Позитивность по ПЭТ2 </td> <td> 42% </td> <td> 61% </td> <td> 0,050 </td> </tr> <tr> <td> Предлеченность (более трех линий химиотерапии) </td> <td> 31% </td> <td> 59% </td> <td> 0,0289 </td> </tr> </tbody> </table> <h2>Таблица 2. Четырехлетняя общая выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Факторы </td> <td> Есть </td> <td> Нет </td> <td> p </td> </tr> <tr> <td> В-симптомы в рецидиве </td> <td> 45% </td> <td> 80% </td> <td> 0,0006 </td> </tr> <tr> <td> Гипоальбуминемия </td> <td> 46% </td> <td> 74% </td> <td> 0,0372 </td> </tr> <tr> <td> Повышение активности ЛДГ </td> <td> 52% </td> <td> 78%<br> </td> <td> 0,0340 </td> </tr> <tr> <td> Отсутствие ответа по данным КТ </td> <td> 52% </td> <td> 79% </td> <td> 0,0158 </td> </tr> </tbody> </table> <h2>Таблица 3. Однофакторный анализ факторов риска общей и бессобытийной выживаемости (метод Кокса, стат. критерий Хи-квадрат)</h2> <table> <tbody> <tr> <td> Фактор </td> <td> Отношение рисков </td> <td colspan="2"> Доверительный интервал 95% </td> <td> Р </td> </tr> <tr> <td colspan="5"> Общая выживаемость </td> </tr> <tr> <td> В-симптомы в рецидиве </td> <td> 0,27 </td> <td> 0,11 </td> <td> 0,62 </td> <td> 0,002 </td> </tr> <tr> <td> Отсутствие ответа по данным КТ </td> <td> 0,37 </td> <td> 0,17 </td> <td> 0,83 </td> <td> 0,016 </td> </tr> <tr> <td> ЛДГ </td> <td> 0,38 </td> <td> 0,15 </td> <td> 0,95 </td> <td> 0,037 </td> </tr> <tr> <td colspan="5"> Бессобытийная выживаемость </td> </tr> <tr> <td> Отсутствие ответа по КТ </td> <td> 0,36 </td> <td> 0,18 </td> <td> 0,68 </td> <td> 0,001 </td> </tr> <tr> <td> Позитивность по ПЭТ1 </td> <td> 0,36 </td> <td> 0,17 </td> <td> 0,75 </td> <td> 0,006 </td> </tr> <tr> <td> В-симптомы в рецидиве </td> <td> 0,47 </td> <td> 0,24 </td> <td> 0,92 </td> <td> 0,002 </td> </tr> <tr> <td> Предлеченность(более трех линий химиотерапии) </td> <td> 0,41 </td> <td> 0,21 </td> <td> 0,81 </td> <td> 0,01 </td> </tr> <tr> <td> ЛДГ </td> <td> 0,45 </td> <td> 0,21 </td> <td> 0,96 </td> <td> 0,04 </td> </tr> </tbody> </table> <h2>Таблица 4. Многофакторный анализ факторов риска бессобытийной выживаемости (метод Кокса, критерий Хи- квадрат)</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Фактор </td> <td> Отношение рисков </td> <td colspan="2"> Доверительный интервал 95% </td> <td> p </td> </tr> <tr> <td> Отсутствие ответа по КТ </td> <td> 0,38 </td> <td> 0,16 </td> <td> 0,89 </td> <td> 0,026 </td> </tr> <tr> <td> Позитивность по ПЭТ2 </td> <td> 0,42 </td> <td> 0,18 </td> <td> 0,97 </td> <td> 0,043 </td> </tr> </tbody> </table> <br>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(246) "Прогнозирование результатов аутологичной трансплантации стволовых гемопоэтических клеток у взрослых пациентов с лимфомой Ходжкина" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(246) "Прогнозирование результатов аутологичной трансплантации стволовых гемопоэтических клеток у взрослых пациентов с лимфомой Ходжкина" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(246) "Прогнозирование результатов аутологичной трансплантации стволовых гемопоэтических клеток у взрослых пациентов с лимфомой Ходжкина" ["SECTION_META_TITLE"]=> string(246) "Прогнозирование результатов аутологичной трансплантации стволовых гемопоэтических клеток у взрослых пациентов с лимфомой Ходжкина" ["SECTION_META_KEYWORDS"]=> string(246) "Прогнозирование результатов аутологичной трансплантации стволовых гемопоэтических клеток у взрослых пациентов с лимфомой Ходжкина" ["SECTION_META_DESCRIPTION"]=> string(246) "Прогнозирование результатов аутологичной трансплантации стволовых гемопоэтических клеток у взрослых пациентов с лимфомой Ходжкина" ["SECTION_PICTURE_FILE_ALT"]=> string(246) "Прогнозирование результатов аутологичной трансплантации стволовых гемопоэтических клеток у взрослых пациентов с лимфомой Ходжкина" ["SECTION_PICTURE_FILE_TITLE"]=> string(246) "Прогнозирование результатов аутологичной трансплантации стволовых гемопоэтических клеток у взрослых пациентов с лимфомой Ходжкина" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "prognozirovanie-rezultatov-autologichnoy-transplantatsii-stvolovykh-gemopoeticheskikh-kletok-u-vzros" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(246) "Прогнозирование результатов аутологичной трансплантации стволовых гемопоэтических клеток у взрослых пациентов с лимфомой Ходжкина" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(246) "Прогнозирование результатов аутологичной трансплантации стволовых гемопоэтических клеток у взрослых пациентов с лимфомой Ходжкина" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "prognozirovanie-rezultatov-autologichnoy-transplantatsii-stvolovykh-gemopoeticheskikh-kletok-u-vzros" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "prognozirovanie-rezultatov-autologichnoy-transplantatsii-stvolovykh-gemopoeticheskikh-kletok-u-vzros" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "prognozirovanie-rezultatov-autologichnoy-transplantatsii-stvolovykh-gemopoeticheskikh-kletok-u-vzros" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20620" ["VALUE"]=> array(2) { ["TEXT"]=> string(767) "Всеволод Г. Потапенко <sup>1</sup>,<sup>2</sup>, Наталья Б. Михайлова <sup>1</sup>, Ирина А. Скороход <sup>2</sup>, Дарья А. Чигинская <sup>2</sup>, Виктория В. Рябчикова <sup>2</sup>, Элеонора И. Подольцева <sup>2</sup>, Виктор В. Ипатов <sup>3</sup>, Игорь В. Байков <sup>3</sup>, Вячеслав Н. Семелев <sup>3</sup>, Дмитрий А. Горностаев <sup>3</sup>, Надежда В. Медведева <sup>2</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(611) "Всеволод Г. Потапенко 1,2, Наталья Б. Михайлова 1, Ирина А. Скороход 2, Дарья А. Чигинская 2, Виктория В. Рябчикова 2, Элеонора И. Подольцева 2, Виктор В. Ипатов 3, Игорь В. Байков 3, Вячеслав Н. Семелев 3, Дмитрий А. Горностаев 3, Надежда В. Медведева 2, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20621" ["VALUE"]=> array(2) { ["TEXT"]=> string(554) "<sup>1</sup> Первый Санкт-Петербургский государственный медицинский ниверситет им И. П. Павлова, Санкт-Петербург<br> <sup>2</sup> Городской гематологический центр, Городская клиническая больница №31, Санкт-Петербург<br> <sup>3</sup> Военно-медицинская Академия им. С. М. Кирова, Санкт-Петербург" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(506) "1 Первый Санкт-Петербургский государственный медицинский ниверситет им И. П. Павлова, Санкт-Петербург
2 Городской гематологический центр, Городская клиническая больница №31, Санкт-Петербург
3 Военно-медицинская Академия им. С. М. Кирова, Санкт-Петербург" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20622" ["VALUE"]=> array(2) { ["TEXT"]=> string(10912) "<h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Целью работы был анализ показателей общей и бессобытийной выживаемости в зависимости от различных прогностических факторов. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Проанализированы данные 84 пациентов. Медиана возраста 26,6 года (18-62). Медиана наблюдения составила 49 месяцев (0,5-115 мес.). Исследованы влияния: пола, ответа на первичное лечение, скорости развития рецидива, варианта химиотерапии второй линии, В-симптомов, конгломератов более 5 см (в рецидиве и непосредственно перед ВДХТ), уровней альбумина и ЛДГ крови, КТ-ответа, общего количества линий химиотерапии, режима кондиционирования перед АТГСК, метаболической активности опухоли до ВДХТ (ПЭТ1) и после АТГСК (ПЭТ2). Для статистического анализа использованы методы Каплана-Мейера, Кокса, статистические критерии Манна-Уитни и Хи-квадрат. Результаты. Приведены показатели общей и бессобытийной выживаемости, а также расчет отношения рисков для факторов, показавших статистическую достоверность менее 0,05 (Табл. 1, 2). При анализе бессобытийной выживаемости выявлены статистически значимые различия в выживаемости при негативности по ПЭТ1 и ПЭТ2 по сравнению с группой пациентов с позитивностью очагов по ПЭТ1 и ПЭТ2 (Табл. 3, 4). Других различий не выявлено. </p> <h2 style="text-align: justify;">Вывод</h2> <p style="text-align: justify;"> Исследование показало, что наиболее важными факторами прогноза бессобытийной выживаемости пациентов с ЛХ после ВДХТ/АТГСК являются повышение активности ЛДГ, наличие В-симптомов в рецидиве, позитивность по ПЭТ1, предлеченность и, особенно, отсутствие ответа по данным КТ и определение метаболической активности после ВДХТ/АТГСК. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфома Ходжкина, аутологичная трансплантация стволовых клеток, ПЭТ, ЛДГ, альбумин. </p> <h2 style="text-align: justify;"> Таблица 1. Четырехлетняя бессобытийная выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)<br> </h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Факторы </td> <td> Есть </td> <td> Нет </td> <td> p </td> </tr> <tr> <td> B-симптомы в рецидиве </td> <td> 35% </td> <td> 61% </td> <td> 0,0246 </td> </tr> <tr> <td> Гипоальбуминемия </td> <td> 33%<br> </td> <td> 62%<br> </td> <td> 0,0494 </td> </tr> <tr> <td> Повышение активности ЛДГ </td> <td> 36% </td> <td> 66% </td> <td> 0,0302 </td> </tr> <tr> <td> Отсутствие ответа по данным КТ </td> <td> 33% </td> <td> 66% </td> <td> 0,0035 </td> </tr> <tr> <td> Позитивность по ПЭТ1 </td> <td> 31%<br> </td> <td> 70% </td> <td> 0,0072 </td> </tr> <tr> <td> Позитивность по ПЭТ2 </td> <td> 42% </td> <td> 61% </td> <td> 0,050 </td> </tr> <tr> <td> Предлеченность (более трех линий химиотерапии) </td> <td> 31% </td> <td> 59% </td> <td> 0,0289 </td> </tr> </tbody> </table> <h2>Таблица 2. Четырехлетняя общая выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Факторы </td> <td> Есть </td> <td> Нет </td> <td> p </td> </tr> <tr> <td> В-симптомы в рецидиве </td> <td> 45% </td> <td> 80% </td> <td> 0,0006 </td> </tr> <tr> <td> Гипоальбуминемия </td> <td> 46% </td> <td> 74% </td> <td> 0,0372 </td> </tr> <tr> <td> Повышение активности ЛДГ </td> <td> 52% </td> <td> 78%<br> </td> <td> 0,0340 </td> </tr> <tr> <td> Отсутствие ответа по данным КТ </td> <td> 52% </td> <td> 79% </td> <td> 0,0158 </td> </tr> </tbody> </table> <h2>Таблица 3. Однофакторный анализ факторов риска общей и бессобытийной выживаемости (метод Кокса, стат. критерий Хи-квадрат)</h2> <table> <tbody> <tr> <td> Фактор </td> <td> Отношение рисков </td> <td colspan="2"> Доверительный интервал 95% </td> <td> Р </td> </tr> <tr> <td colspan="5"> Общая выживаемость </td> </tr> <tr> <td> В-симптомы в рецидиве </td> <td> 0,27 </td> <td> 0,11 </td> <td> 0,62 </td> <td> 0,002 </td> </tr> <tr> <td> Отсутствие ответа по данным КТ </td> <td> 0,37 </td> <td> 0,17 </td> <td> 0,83 </td> <td> 0,016 </td> </tr> <tr> <td> ЛДГ </td> <td> 0,38 </td> <td> 0,15 </td> <td> 0,95 </td> <td> 0,037 </td> </tr> <tr> <td colspan="5"> Бессобытийная выживаемость </td> </tr> <tr> <td> Отсутствие ответа по КТ </td> <td> 0,36 </td> <td> 0,18 </td> <td> 0,68 </td> <td> 0,001 </td> </tr> <tr> <td> Позитивность по ПЭТ1 </td> <td> 0,36 </td> <td> 0,17 </td> <td> 0,75 </td> <td> 0,006 </td> </tr> <tr> <td> В-симптомы в рецидиве </td> <td> 0,47 </td> <td> 0,24 </td> <td> 0,92 </td> <td> 0,002 </td> </tr> <tr> <td> Предлеченность(более трех линий химиотерапии) </td> <td> 0,41 </td> <td> 0,21 </td> <td> 0,81 </td> <td> 0,01 </td> </tr> <tr> <td> ЛДГ </td> <td> 0,45 </td> <td> 0,21 </td> <td> 0,96 </td> <td> 0,04 </td> </tr> </tbody> </table> <h2>Таблица 4. Многофакторный анализ факторов риска бессобытийной выживаемости (метод Кокса, критерий Хи- квадрат)</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Фактор </td> <td> Отношение рисков </td> <td colspan="2"> Доверительный интервал 95% </td> <td> p </td> </tr> <tr> <td> Отсутствие ответа по КТ </td> <td> 0,38 </td> <td> 0,16 </td> <td> 0,89 </td> <td> 0,026 </td> </tr> <tr> <td> Позитивность по ПЭТ2 </td> <td> 0,42 </td> <td> 0,18 </td> <td> 0,97 </td> <td> 0,043 </td> </tr> </tbody> </table> <br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(8748) "
Цель
Целью работы был анализ показателей общей и бессобытийной выживаемости в зависимости от различных прогностических факторов.
Пациенты и методы
Проанализированы данные 84 пациентов. Медиана возраста 26,6 года (18-62). Медиана наблюдения составила 49 месяцев (0,5-115 мес.). Исследованы влияния: пола, ответа на первичное лечение, скорости развития рецидива, варианта химиотерапии второй линии, В-симптомов, конгломератов более 5 см (в рецидиве и непосредственно перед ВДХТ), уровней альбумина и ЛДГ крови, КТ-ответа, общего количества линий химиотерапии, режима кондиционирования перед АТГСК, метаболической активности опухоли до ВДХТ (ПЭТ1) и после АТГСК (ПЭТ2). Для статистического анализа использованы методы Каплана-Мейера, Кокса, статистические критерии Манна-Уитни и Хи-квадрат. Результаты. Приведены показатели общей и бессобытийной выживаемости, а также расчет отношения рисков для факторов, показавших статистическую достоверность менее 0,05 (Табл. 1, 2). При анализе бессобытийной выживаемости выявлены статистически значимые различия в выживаемости при негативности по ПЭТ1 и ПЭТ2 по сравнению с группой пациентов с позитивностью очагов по ПЭТ1 и ПЭТ2 (Табл. 3, 4). Других различий не выявлено.
Вывод
Исследование показало, что наиболее важными факторами прогноза бессобытийной выживаемости пациентов с ЛХ после ВДХТ/АТГСК являются повышение активности ЛДГ, наличие В-симптомов в рецидиве, позитивность по ПЭТ1, предлеченность и, особенно, отсутствие ответа по данным КТ и определение метаболической активности после ВДХТ/АТГСК.
Ключевые слова
Лимфома Ходжкина, аутологичная трансплантация стволовых клеток, ПЭТ, ЛДГ, альбумин.
Таблица 1. Четырехлетняя бессобытийная выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)
| Факторы | Есть | Нет | p |
| B-симптомы в рецидиве | 35% | 61% | 0,0246 |
| Гипоальбуминемия |
33% |
62% |
0,0494 |
| Повышение активности ЛДГ | 36% | 66% | 0,0302 |
| Отсутствие ответа по данным КТ | 33% | 66% | 0,0035 |
| Позитивность по ПЭТ1 |
31% |
70% | 0,0072 |
| Позитивность по ПЭТ2 | 42% | 61% | 0,050 |
| Предлеченность (более трех линий химиотерапии) | 31% | 59% | 0,0289 |
Таблица 2. Четырехлетняя общая выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)
| Факторы | Есть | Нет | p |
| В-симптомы в рецидиве | 45% | 80% | 0,0006 |
| Гипоальбуминемия | 46% | 74% | 0,0372 |
| Повышение активности ЛДГ | 52% |
78% |
0,0340 |
| Отсутствие ответа по данным КТ | 52% | 79% | 0,0158 |
Таблица 3. Однофакторный анализ факторов риска общей и бессобытийной выживаемости (метод Кокса, стат. критерий Хи-квадрат)
| Фактор | Отношение рисков | Доверительный интервал 95% | Р | |
| Общая выживаемость | ||||
| В-симптомы в рецидиве | 0,27 | 0,11 | 0,62 | 0,002 |
| Отсутствие ответа по данным КТ | 0,37 | 0,17 | 0,83 | 0,016 |
| ЛДГ | 0,38 | 0,15 | 0,95 | 0,037 |
| Бессобытийная выживаемость | ||||
| Отсутствие ответа по КТ | 0,36 | 0,18 | 0,68 | 0,001 |
| Позитивность по ПЭТ1 | 0,36 | 0,17 | 0,75 | 0,006 |
| В-симптомы в рецидиве | 0,47 | 0,24 | 0,92 | 0,002 |
| Предлеченность(более трех линий химиотерапии) | 0,41 | 0,21 | 0,81 | 0,01 |
| ЛДГ | 0,45 | 0,21 | 0,96 | 0,04 |
Таблица 4. Многофакторный анализ факторов риска бессобытийной выживаемости (метод Кокса, критерий Хи- квадрат)
| Фактор | Отношение рисков | Доверительный интервал 95% | p | |
| Отсутствие ответа по КТ | 0,38 | 0,16 | 0,89 | 0,026 |
| Позитивность по ПЭТ2 | 0,42 | 0,18 | 0,97 | 0,043 |
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20623" ["VALUE"]=> array(2) { ["TEXT"]=> string(583) "Vsevolod G. Potapenko <sup>1</sup>,<sup>2</sup>, Natalia B. Mikhaylova <sup>1</sup>, Irina A. Skorokhod <sup>2</sup>, Darya A. Chaginskaya <sup>2</sup>, Viktoria V. Ryabchikova <sup>2</sup>, Eleonora I. Podoltseva <sup>2</sup>, Viktor V. Ipatov <sup>3</sup>, Igor V. Baykov <sup>3</sup>, Vyacheslav N. Semelev <sup>3</sup>, Dmitrij A. Gornostaev <sup>3</sup>, Nadezhda V. Medvedeva <sup>2</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(427) "Vsevolod G. Potapenko 1,2, Natalia B. Mikhaylova 1, Irina A. Skorokhod 2, Darya A. Chaginskaya 2, Viktoria V. Ryabchikova 2, Eleonora I. Podoltseva 2, Viktor V. Ipatov 3, Igor V. Baykov 3, Vyacheslav N. Semelev 3, Dmitrij A. Gornostaev 3, Nadezhda V. Medvedeva 2, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20624" ["VALUE"]=> array(2) { ["TEXT"]=> string(317) "<sup>1</sup> First St. Petersburg State I. Pavlov Medical University, St. Petersburg<br> <sup>2</sup> Haematology Department, Municipal Clinical Hospital №31, St. Petersburg<br> <sup>3</sup> S. Kirov Military Medical Academy, St. Petersburg, Russia<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(263) "1 First St. Petersburg State I. Pavlov Medical University, St. Petersburg
2 Haematology Department, Municipal Clinical Hospital №31, St. Petersburg
3 S. Kirov Military Medical Academy, St. Petersburg, Russia
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20625" ["VALUE"]=> array(2) { ["TEXT"]=> string(3266) "<h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> The study was aimed for evaluation of prognostic significance of different factors by event free and overall survival analysis in patients after high dose therapy with stem cells support (HDT/AHSCT). </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Retrospective analysis includes the data of 84 patients with resistant or relapsed Hodgkin lymphoma. Median age was 26.6 years (18-62). Median follow-up is 49 (0.5-115) months. Prognostic factors analyzed included sex, response to the initial chemotherapy, time to relapse, B-symptoms on relapse, serum LDH and albumin levels, response assessed by computer tomography, number of chemotherapy lines before AHSCT, PET-scan results before (PET1) and after (PET2) AHSCT. Survival was estimated using Kaplan-Meier, Cox methods, Chi-square and log-rank test. Results. Four-year overall survival and event-free survival were 70% and 54% respectively (Tables 1, 2). The presented factors had significant value in survival prediction.<br> In the combined analysis of PET1 and PET2 significant difference observed only in patients with positivity by PET1 and PET2 compared with group with negative PET1 and PET2 results (Tables 3, 4). Conclusion. Our work has revealed that the most significant factors of the event free survival in patients with Hodgkin lymphoma after HDC/AHSCT are: elevation of the LDH activity, В-symptoms, pretreatment, positivity by PET1 and especially lack of response by CT-scan and positivity by PET2. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hodgkin lymphoma, autologous stem cell transplant, PET, LDH, albumin. </p> <h2 style="text-align: justify;"> Table 1. Four-year event-free survival (Kaplan-Meier analysis, log-rank test)<br> </h2> <p style="text-align: justify;"> <img width="783" alt="39_table 1.png" src="/upload/medialibrary/818/39_table-1.png" height="217" title="39_table 1.png"><br> </p> <h2 style="text-align: justify;"> Table 2. Four-year overall survival (Kaplan-Meier analysis, log-rank test)<br> </h2> <img width="783" alt="39_table 2.png" src="/upload/medialibrary/c99/39_table-2.png" height="139" title="39_table 2.png"> <h2>Table 3. Univariate analysis of risk factors for event-free and overall survival (Cox models, Chi-square test)</h2> <img width="783" alt="39_table 3.png" src="/upload/medialibrary/4d5/39_table-3.png" height="299" title="39_table 3.png"> <h2>Table 4. Multivariate analysis of risk factors for event-free survival (Cox models, Chi-square test)</h2> <img width="783" alt="39_table 4.png" src="/upload/medialibrary/6fd/39_table-4.png" height="83" title="39_table 4.png"><br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2790) "
Aim
The study was aimed for evaluation of prognostic significance of different factors by event free and overall survival analysis in patients after high dose therapy with stem cells support (HDT/AHSCT).
Patients and methods
Retrospective analysis includes the data of 84 patients with resistant or relapsed Hodgkin lymphoma. Median age was 26.6 years (18-62). Median follow-up is 49 (0.5-115) months. Prognostic factors analyzed included sex, response to the initial chemotherapy, time to relapse, B-symptoms on relapse, serum LDH and albumin levels, response assessed by computer tomography, number of chemotherapy lines before AHSCT, PET-scan results before (PET1) and after (PET2) AHSCT. Survival was estimated using Kaplan-Meier, Cox methods, Chi-square and log-rank test. Results. Four-year overall survival and event-free survival were 70% and 54% respectively (Tables 1, 2). The presented factors had significant value in survival prediction.
In the combined analysis of PET1 and PET2 significant difference observed only in patients with positivity by PET1 and PET2 compared with group with negative PET1 and PET2 results (Tables 3, 4). Conclusion. Our work has revealed that the most significant factors of the event free survival in patients with Hodgkin lymphoma after HDC/AHSCT are: elevation of the LDH activity, В-symptoms, pretreatment, positivity by PET1 and especially lack of response by CT-scan and positivity by PET2.
Keywords
Hodgkin lymphoma, autologous stem cell transplant, PET, LDH, albumin.
Table 1. Four-year event-free survival (Kaplan-Meier analysis, log-rank test)
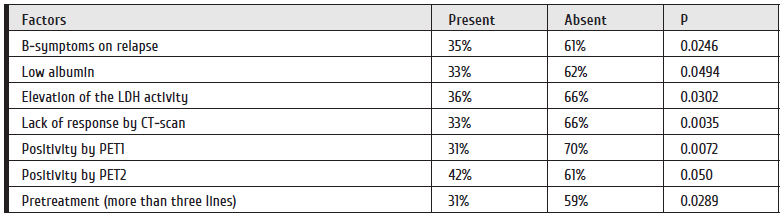
Table 2. Four-year overall survival (Kaplan-Meier analysis, log-rank test)
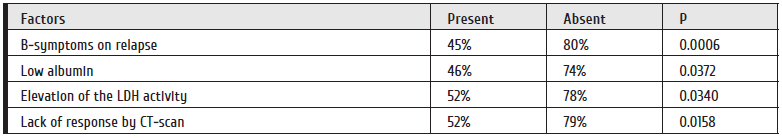
Table 3. Univariate analysis of risk factors for event-free and overall survival (Cox models, Chi-square test)
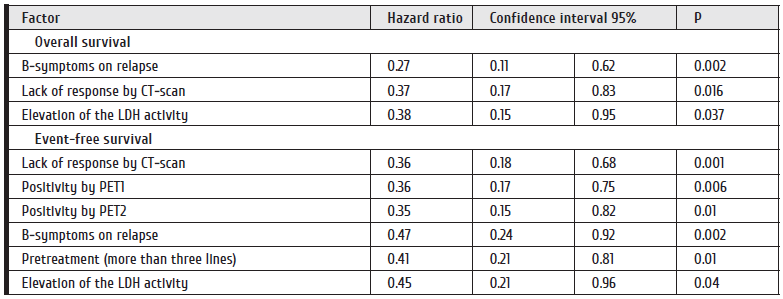
Table 4. Multivariate analysis of risk factors for event-free survival (Cox models, Chi-square test)

" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20626" ["VALUE"]=> string(93) "Prognostic factors in autologous stem cell transplant on adult patients with Hodgkin lymphoma" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(93) "Prognostic factors in autologous stem cell transplant on adult patients with Hodgkin lymphoma" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20807" ["VALUE"]=> string(4) "1445" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1445" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20808" ["VALUE"]=> string(4) "1446" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1446" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20623" ["VALUE"]=> array(2) { ["TEXT"]=> string(583) "Vsevolod G. Potapenko <sup>1</sup>,<sup>2</sup>, Natalia B. Mikhaylova <sup>1</sup>, Irina A. Skorokhod <sup>2</sup>, Darya A. Chaginskaya <sup>2</sup>, Viktoria V. Ryabchikova <sup>2</sup>, Eleonora I. Podoltseva <sup>2</sup>, Viktor V. Ipatov <sup>3</sup>, Igor V. Baykov <sup>3</sup>, Vyacheslav N. Semelev <sup>3</sup>, Dmitrij A. Gornostaev <sup>3</sup>, Nadezhda V. Medvedeva <sup>2</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(427) "Vsevolod G. Potapenko 1,2, Natalia B. Mikhaylova 1, Irina A. Skorokhod 2, Darya A. Chaginskaya 2, Viktoria V. Ryabchikova 2, Eleonora I. Podoltseva 2, Viktor V. Ipatov 3, Igor V. Baykov 3, Vyacheslav N. Semelev 3, Dmitrij A. Gornostaev 3, Nadezhda V. Medvedeva 2, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(427) "Vsevolod G. Potapenko 1,2, Natalia B. Mikhaylova 1, Irina A. Skorokhod 2, Darya A. Chaginskaya 2, Viktoria V. Ryabchikova 2, Eleonora I. Podoltseva 2, Viktor V. Ipatov 3, Igor V. Baykov 3, Vyacheslav N. Semelev 3, Dmitrij A. Gornostaev 3, Nadezhda V. Medvedeva 2, Boris V. Afanasyev 1" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20625" ["VALUE"]=> array(2) { ["TEXT"]=> string(3266) "<h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> The study was aimed for evaluation of prognostic significance of different factors by event free and overall survival analysis in patients after high dose therapy with stem cells support (HDT/AHSCT). </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Retrospective analysis includes the data of 84 patients with resistant or relapsed Hodgkin lymphoma. Median age was 26.6 years (18-62). Median follow-up is 49 (0.5-115) months. Prognostic factors analyzed included sex, response to the initial chemotherapy, time to relapse, B-symptoms on relapse, serum LDH and albumin levels, response assessed by computer tomography, number of chemotherapy lines before AHSCT, PET-scan results before (PET1) and after (PET2) AHSCT. Survival was estimated using Kaplan-Meier, Cox methods, Chi-square and log-rank test. Results. Four-year overall survival and event-free survival were 70% and 54% respectively (Tables 1, 2). The presented factors had significant value in survival prediction.<br> In the combined analysis of PET1 and PET2 significant difference observed only in patients with positivity by PET1 and PET2 compared with group with negative PET1 and PET2 results (Tables 3, 4). Conclusion. Our work has revealed that the most significant factors of the event free survival in patients with Hodgkin lymphoma after HDC/AHSCT are: elevation of the LDH activity, В-symptoms, pretreatment, positivity by PET1 and especially lack of response by CT-scan and positivity by PET2. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hodgkin lymphoma, autologous stem cell transplant, PET, LDH, albumin. </p> <h2 style="text-align: justify;"> Table 1. Four-year event-free survival (Kaplan-Meier analysis, log-rank test)<br> </h2> <p style="text-align: justify;"> <img width="783" alt="39_table 1.png" src="/upload/medialibrary/818/39_table-1.png" height="217" title="39_table 1.png"><br> </p> <h2 style="text-align: justify;"> Table 2. Four-year overall survival (Kaplan-Meier analysis, log-rank test)<br> </h2> <img width="783" alt="39_table 2.png" src="/upload/medialibrary/c99/39_table-2.png" height="139" title="39_table 2.png"> <h2>Table 3. Univariate analysis of risk factors for event-free and overall survival (Cox models, Chi-square test)</h2> <img width="783" alt="39_table 3.png" src="/upload/medialibrary/4d5/39_table-3.png" height="299" title="39_table 3.png"> <h2>Table 4. Multivariate analysis of risk factors for event-free survival (Cox models, Chi-square test)</h2> <img width="783" alt="39_table 4.png" src="/upload/medialibrary/6fd/39_table-4.png" height="83" title="39_table 4.png"><br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2790) "
Aim
The study was aimed for evaluation of prognostic significance of different factors by event free and overall survival analysis in patients after high dose therapy with stem cells support (HDT/AHSCT).
Patients and methods
Retrospective analysis includes the data of 84 patients with resistant or relapsed Hodgkin lymphoma. Median age was 26.6 years (18-62). Median follow-up is 49 (0.5-115) months. Prognostic factors analyzed included sex, response to the initial chemotherapy, time to relapse, B-symptoms on relapse, serum LDH and albumin levels, response assessed by computer tomography, number of chemotherapy lines before AHSCT, PET-scan results before (PET1) and after (PET2) AHSCT. Survival was estimated using Kaplan-Meier, Cox methods, Chi-square and log-rank test. Results. Four-year overall survival and event-free survival were 70% and 54% respectively (Tables 1, 2). The presented factors had significant value in survival prediction.
In the combined analysis of PET1 and PET2 significant difference observed only in patients with positivity by PET1 and PET2 compared with group with negative PET1 and PET2 results (Tables 3, 4). Conclusion. Our work has revealed that the most significant factors of the event free survival in patients with Hodgkin lymphoma after HDC/AHSCT are: elevation of the LDH activity, В-symptoms, pretreatment, positivity by PET1 and especially lack of response by CT-scan and positivity by PET2.
Keywords
Hodgkin lymphoma, autologous stem cell transplant, PET, LDH, albumin.
Table 1. Four-year event-free survival (Kaplan-Meier analysis, log-rank test)

Table 2. Four-year overall survival (Kaplan-Meier analysis, log-rank test)

Table 3. Univariate analysis of risk factors for event-free and overall survival (Cox models, Chi-square test)

Table 4. Multivariate analysis of risk factors for event-free survival (Cox models, Chi-square test)

" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2790) "
Aim
The study was aimed for evaluation of prognostic significance of different factors by event free and overall survival analysis in patients after high dose therapy with stem cells support (HDT/AHSCT).
Patients and methods
Retrospective analysis includes the data of 84 patients with resistant or relapsed Hodgkin lymphoma. Median age was 26.6 years (18-62). Median follow-up is 49 (0.5-115) months. Prognostic factors analyzed included sex, response to the initial chemotherapy, time to relapse, B-symptoms on relapse, serum LDH and albumin levels, response assessed by computer tomography, number of chemotherapy lines before AHSCT, PET-scan results before (PET1) and after (PET2) AHSCT. Survival was estimated using Kaplan-Meier, Cox methods, Chi-square and log-rank test. Results. Four-year overall survival and event-free survival were 70% and 54% respectively (Tables 1, 2). The presented factors had significant value in survival prediction.
In the combined analysis of PET1 and PET2 significant difference observed only in patients with positivity by PET1 and PET2 compared with group with negative PET1 and PET2 results (Tables 3, 4). Conclusion. Our work has revealed that the most significant factors of the event free survival in patients with Hodgkin lymphoma after HDC/AHSCT are: elevation of the LDH activity, В-symptoms, pretreatment, positivity by PET1 and especially lack of response by CT-scan and positivity by PET2.
Keywords
Hodgkin lymphoma, autologous stem cell transplant, PET, LDH, albumin.
Table 1. Four-year event-free survival (Kaplan-Meier analysis, log-rank test)

Table 2. Four-year overall survival (Kaplan-Meier analysis, log-rank test)

Table 3. Univariate analysis of risk factors for event-free and overall survival (Cox models, Chi-square test)

Table 4. Multivariate analysis of risk factors for event-free survival (Cox models, Chi-square test)

" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20626" ["VALUE"]=> string(93) "Prognostic factors in autologous stem cell transplant on adult patients with Hodgkin lymphoma" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(93) "Prognostic factors in autologous stem cell transplant on adult patients with Hodgkin lymphoma" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(93) "Prognostic factors in autologous stem cell transplant on adult patients with Hodgkin lymphoma" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20624" ["VALUE"]=> array(2) { ["TEXT"]=> string(317) "<sup>1</sup> First St. Petersburg State I. Pavlov Medical University, St. Petersburg<br> <sup>2</sup> Haematology Department, Municipal Clinical Hospital №31, St. Petersburg<br> <sup>3</sup> S. Kirov Military Medical Academy, St. Petersburg, Russia<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(263) "1 First St. Petersburg State I. Pavlov Medical University, St. Petersburg
2 Haematology Department, Municipal Clinical Hospital №31, St. Petersburg
3 S. Kirov Military Medical Academy, St. Petersburg, Russia
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(263) "1 First St. Petersburg State I. Pavlov Medical University, St. Petersburg
2 Haematology Department, Municipal Clinical Hospital №31, St. Petersburg
3 S. Kirov Military Medical Academy, St. Petersburg, Russia
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20620" ["VALUE"]=> array(2) { ["TEXT"]=> string(767) "Всеволод Г. Потапенко <sup>1</sup>,<sup>2</sup>, Наталья Б. Михайлова <sup>1</sup>, Ирина А. Скороход <sup>2</sup>, Дарья А. Чигинская <sup>2</sup>, Виктория В. Рябчикова <sup>2</sup>, Элеонора И. Подольцева <sup>2</sup>, Виктор В. Ипатов <sup>3</sup>, Игорь В. Байков <sup>3</sup>, Вячеслав Н. Семелев <sup>3</sup>, Дмитрий А. Горностаев <sup>3</sup>, Надежда В. Медведева <sup>2</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(611) "Всеволод Г. Потапенко 1,2, Наталья Б. Михайлова 1, Ирина А. Скороход 2, Дарья А. Чигинская 2, Виктория В. Рябчикова 2, Элеонора И. Подольцева 2, Виктор В. Ипатов 3, Игорь В. Байков 3, Вячеслав Н. Семелев 3, Дмитрий А. Горностаев 3, Надежда В. Медведева 2, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(611) "Всеволод Г. Потапенко 1,2, Наталья Б. Михайлова 1, Ирина А. Скороход 2, Дарья А. Чигинская 2, Виктория В. Рябчикова 2, Элеонора И. Подольцева 2, Виктор В. Ипатов 3, Игорь В. Байков 3, Вячеслав Н. Семелев 3, Дмитрий А. Горностаев 3, Надежда В. Медведева 2, Борис В. Афанасьев 1" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20622" ["VALUE"]=> array(2) { ["TEXT"]=> string(10912) "<h2 style="text-align: justify;">Цель</h2> <p style="text-align: justify;"> Целью работы был анализ показателей общей и бессобытийной выживаемости в зависимости от различных прогностических факторов. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> Проанализированы данные 84 пациентов. Медиана возраста 26,6 года (18-62). Медиана наблюдения составила 49 месяцев (0,5-115 мес.). Исследованы влияния: пола, ответа на первичное лечение, скорости развития рецидива, варианта химиотерапии второй линии, В-симптомов, конгломератов более 5 см (в рецидиве и непосредственно перед ВДХТ), уровней альбумина и ЛДГ крови, КТ-ответа, общего количества линий химиотерапии, режима кондиционирования перед АТГСК, метаболической активности опухоли до ВДХТ (ПЭТ1) и после АТГСК (ПЭТ2). Для статистического анализа использованы методы Каплана-Мейера, Кокса, статистические критерии Манна-Уитни и Хи-квадрат. Результаты. Приведены показатели общей и бессобытийной выживаемости, а также расчет отношения рисков для факторов, показавших статистическую достоверность менее 0,05 (Табл. 1, 2). При анализе бессобытийной выживаемости выявлены статистически значимые различия в выживаемости при негативности по ПЭТ1 и ПЭТ2 по сравнению с группой пациентов с позитивностью очагов по ПЭТ1 и ПЭТ2 (Табл. 3, 4). Других различий не выявлено. </p> <h2 style="text-align: justify;">Вывод</h2> <p style="text-align: justify;"> Исследование показало, что наиболее важными факторами прогноза бессобытийной выживаемости пациентов с ЛХ после ВДХТ/АТГСК являются повышение активности ЛДГ, наличие В-симптомов в рецидиве, позитивность по ПЭТ1, предлеченность и, особенно, отсутствие ответа по данным КТ и определение метаболической активности после ВДХТ/АТГСК. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Лимфома Ходжкина, аутологичная трансплантация стволовых клеток, ПЭТ, ЛДГ, альбумин. </p> <h2 style="text-align: justify;"> Таблица 1. Четырехлетняя бессобытийная выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)<br> </h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Факторы </td> <td> Есть </td> <td> Нет </td> <td> p </td> </tr> <tr> <td> B-симптомы в рецидиве </td> <td> 35% </td> <td> 61% </td> <td> 0,0246 </td> </tr> <tr> <td> Гипоальбуминемия </td> <td> 33%<br> </td> <td> 62%<br> </td> <td> 0,0494 </td> </tr> <tr> <td> Повышение активности ЛДГ </td> <td> 36% </td> <td> 66% </td> <td> 0,0302 </td> </tr> <tr> <td> Отсутствие ответа по данным КТ </td> <td> 33% </td> <td> 66% </td> <td> 0,0035 </td> </tr> <tr> <td> Позитивность по ПЭТ1 </td> <td> 31%<br> </td> <td> 70% </td> <td> 0,0072 </td> </tr> <tr> <td> Позитивность по ПЭТ2 </td> <td> 42% </td> <td> 61% </td> <td> 0,050 </td> </tr> <tr> <td> Предлеченность (более трех линий химиотерапии) </td> <td> 31% </td> <td> 59% </td> <td> 0,0289 </td> </tr> </tbody> </table> <h2>Таблица 2. Четырехлетняя общая выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Факторы </td> <td> Есть </td> <td> Нет </td> <td> p </td> </tr> <tr> <td> В-симптомы в рецидиве </td> <td> 45% </td> <td> 80% </td> <td> 0,0006 </td> </tr> <tr> <td> Гипоальбуминемия </td> <td> 46% </td> <td> 74% </td> <td> 0,0372 </td> </tr> <tr> <td> Повышение активности ЛДГ </td> <td> 52% </td> <td> 78%<br> </td> <td> 0,0340 </td> </tr> <tr> <td> Отсутствие ответа по данным КТ </td> <td> 52% </td> <td> 79% </td> <td> 0,0158 </td> </tr> </tbody> </table> <h2>Таблица 3. Однофакторный анализ факторов риска общей и бессобытийной выживаемости (метод Кокса, стат. критерий Хи-квадрат)</h2> <table> <tbody> <tr> <td> Фактор </td> <td> Отношение рисков </td> <td colspan="2"> Доверительный интервал 95% </td> <td> Р </td> </tr> <tr> <td colspan="5"> Общая выживаемость </td> </tr> <tr> <td> В-симптомы в рецидиве </td> <td> 0,27 </td> <td> 0,11 </td> <td> 0,62 </td> <td> 0,002 </td> </tr> <tr> <td> Отсутствие ответа по данным КТ </td> <td> 0,37 </td> <td> 0,17 </td> <td> 0,83 </td> <td> 0,016 </td> </tr> <tr> <td> ЛДГ </td> <td> 0,38 </td> <td> 0,15 </td> <td> 0,95 </td> <td> 0,037 </td> </tr> <tr> <td colspan="5"> Бессобытийная выживаемость </td> </tr> <tr> <td> Отсутствие ответа по КТ </td> <td> 0,36 </td> <td> 0,18 </td> <td> 0,68 </td> <td> 0,001 </td> </tr> <tr> <td> Позитивность по ПЭТ1 </td> <td> 0,36 </td> <td> 0,17 </td> <td> 0,75 </td> <td> 0,006 </td> </tr> <tr> <td> В-симптомы в рецидиве </td> <td> 0,47 </td> <td> 0,24 </td> <td> 0,92 </td> <td> 0,002 </td> </tr> <tr> <td> Предлеченность(более трех линий химиотерапии) </td> <td> 0,41 </td> <td> 0,21 </td> <td> 0,81 </td> <td> 0,01 </td> </tr> <tr> <td> ЛДГ </td> <td> 0,45 </td> <td> 0,21 </td> <td> 0,96 </td> <td> 0,04 </td> </tr> </tbody> </table> <h2>Таблица 4. Многофакторный анализ факторов риска бессобытийной выживаемости (метод Кокса, критерий Хи- квадрат)</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Фактор </td> <td> Отношение рисков </td> <td colspan="2"> Доверительный интервал 95% </td> <td> p </td> </tr> <tr> <td> Отсутствие ответа по КТ </td> <td> 0,38 </td> <td> 0,16 </td> <td> 0,89 </td> <td> 0,026 </td> </tr> <tr> <td> Позитивность по ПЭТ2 </td> <td> 0,42 </td> <td> 0,18 </td> <td> 0,97 </td> <td> 0,043 </td> </tr> </tbody> </table> <br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(8748) "
Цель
Целью работы был анализ показателей общей и бессобытийной выживаемости в зависимости от различных прогностических факторов.
Пациенты и методы
Проанализированы данные 84 пациентов. Медиана возраста 26,6 года (18-62). Медиана наблюдения составила 49 месяцев (0,5-115 мес.). Исследованы влияния: пола, ответа на первичное лечение, скорости развития рецидива, варианта химиотерапии второй линии, В-симптомов, конгломератов более 5 см (в рецидиве и непосредственно перед ВДХТ), уровней альбумина и ЛДГ крови, КТ-ответа, общего количества линий химиотерапии, режима кондиционирования перед АТГСК, метаболической активности опухоли до ВДХТ (ПЭТ1) и после АТГСК (ПЭТ2). Для статистического анализа использованы методы Каплана-Мейера, Кокса, статистические критерии Манна-Уитни и Хи-квадрат. Результаты. Приведены показатели общей и бессобытийной выживаемости, а также расчет отношения рисков для факторов, показавших статистическую достоверность менее 0,05 (Табл. 1, 2). При анализе бессобытийной выживаемости выявлены статистически значимые различия в выживаемости при негативности по ПЭТ1 и ПЭТ2 по сравнению с группой пациентов с позитивностью очагов по ПЭТ1 и ПЭТ2 (Табл. 3, 4). Других различий не выявлено.
Вывод
Исследование показало, что наиболее важными факторами прогноза бессобытийной выживаемости пациентов с ЛХ после ВДХТ/АТГСК являются повышение активности ЛДГ, наличие В-симптомов в рецидиве, позитивность по ПЭТ1, предлеченность и, особенно, отсутствие ответа по данным КТ и определение метаболической активности после ВДХТ/АТГСК.
Ключевые слова
Лимфома Ходжкина, аутологичная трансплантация стволовых клеток, ПЭТ, ЛДГ, альбумин.
Таблица 1. Четырехлетняя бессобытийная выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)
| Факторы | Есть | Нет | p |
| B-симптомы в рецидиве | 35% | 61% | 0,0246 |
| Гипоальбуминемия |
33% |
62% |
0,0494 |
| Повышение активности ЛДГ | 36% | 66% | 0,0302 |
| Отсутствие ответа по данным КТ | 33% | 66% | 0,0035 |
| Позитивность по ПЭТ1 |
31% |
70% | 0,0072 |
| Позитивность по ПЭТ2 | 42% | 61% | 0,050 |
| Предлеченность (более трех линий химиотерапии) | 31% | 59% | 0,0289 |
Таблица 2. Четырехлетняя общая выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)
| Факторы | Есть | Нет | p |
| В-симптомы в рецидиве | 45% | 80% | 0,0006 |
| Гипоальбуминемия | 46% | 74% | 0,0372 |
| Повышение активности ЛДГ | 52% |
78% |
0,0340 |
| Отсутствие ответа по данным КТ | 52% | 79% | 0,0158 |
Таблица 3. Однофакторный анализ факторов риска общей и бессобытийной выживаемости (метод Кокса, стат. критерий Хи-квадрат)
| Фактор | Отношение рисков | Доверительный интервал 95% | Р | |
| Общая выживаемость | ||||
| В-симптомы в рецидиве | 0,27 | 0,11 | 0,62 | 0,002 |
| Отсутствие ответа по данным КТ | 0,37 | 0,17 | 0,83 | 0,016 |
| ЛДГ | 0,38 | 0,15 | 0,95 | 0,037 |
| Бессобытийная выживаемость | ||||
| Отсутствие ответа по КТ | 0,36 | 0,18 | 0,68 | 0,001 |
| Позитивность по ПЭТ1 | 0,36 | 0,17 | 0,75 | 0,006 |
| В-симптомы в рецидиве | 0,47 | 0,24 | 0,92 | 0,002 |
| Предлеченность(более трех линий химиотерапии) | 0,41 | 0,21 | 0,81 | 0,01 |
| ЛДГ | 0,45 | 0,21 | 0,96 | 0,04 |
Таблица 4. Многофакторный анализ факторов риска бессобытийной выживаемости (метод Кокса, критерий Хи- квадрат)
| Фактор | Отношение рисков | Доверительный интервал 95% | p | |
| Отсутствие ответа по КТ | 0,38 | 0,16 | 0,89 | 0,026 |
| Позитивность по ПЭТ2 | 0,42 | 0,18 | 0,97 | 0,043 |
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(8748) "
Цель
Целью работы был анализ показателей общей и бессобытийной выживаемости в зависимости от различных прогностических факторов.
Пациенты и методы
Проанализированы данные 84 пациентов. Медиана возраста 26,6 года (18-62). Медиана наблюдения составила 49 месяцев (0,5-115 мес.). Исследованы влияния: пола, ответа на первичное лечение, скорости развития рецидива, варианта химиотерапии второй линии, В-симптомов, конгломератов более 5 см (в рецидиве и непосредственно перед ВДХТ), уровней альбумина и ЛДГ крови, КТ-ответа, общего количества линий химиотерапии, режима кондиционирования перед АТГСК, метаболической активности опухоли до ВДХТ (ПЭТ1) и после АТГСК (ПЭТ2). Для статистического анализа использованы методы Каплана-Мейера, Кокса, статистические критерии Манна-Уитни и Хи-квадрат. Результаты. Приведены показатели общей и бессобытийной выживаемости, а также расчет отношения рисков для факторов, показавших статистическую достоверность менее 0,05 (Табл. 1, 2). При анализе бессобытийной выживаемости выявлены статистически значимые различия в выживаемости при негативности по ПЭТ1 и ПЭТ2 по сравнению с группой пациентов с позитивностью очагов по ПЭТ1 и ПЭТ2 (Табл. 3, 4). Других различий не выявлено.
Вывод
Исследование показало, что наиболее важными факторами прогноза бессобытийной выживаемости пациентов с ЛХ после ВДХТ/АТГСК являются повышение активности ЛДГ, наличие В-симптомов в рецидиве, позитивность по ПЭТ1, предлеченность и, особенно, отсутствие ответа по данным КТ и определение метаболической активности после ВДХТ/АТГСК.
Ключевые слова
Лимфома Ходжкина, аутологичная трансплантация стволовых клеток, ПЭТ, ЛДГ, альбумин.
Таблица 1. Четырехлетняя бессобытийная выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)
| Факторы | Есть | Нет | p |
| B-симптомы в рецидиве | 35% | 61% | 0,0246 |
| Гипоальбуминемия |
33% |
62% |
0,0494 |
| Повышение активности ЛДГ | 36% | 66% | 0,0302 |
| Отсутствие ответа по данным КТ | 33% | 66% | 0,0035 |
| Позитивность по ПЭТ1 |
31% |
70% | 0,0072 |
| Позитивность по ПЭТ2 | 42% | 61% | 0,050 |
| Предлеченность (более трех линий химиотерапии) | 31% | 59% | 0,0289 |
Таблица 2. Четырехлетняя общая выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)
| Факторы | Есть | Нет | p |
| В-симптомы в рецидиве | 45% | 80% | 0,0006 |
| Гипоальбуминемия | 46% | 74% | 0,0372 |
| Повышение активности ЛДГ | 52% |
78% |
0,0340 |
| Отсутствие ответа по данным КТ | 52% | 79% | 0,0158 |
Таблица 3. Однофакторный анализ факторов риска общей и бессобытийной выживаемости (метод Кокса, стат. критерий Хи-квадрат)
| Фактор | Отношение рисков | Доверительный интервал 95% | Р | |
| Общая выживаемость | ||||
| В-симптомы в рецидиве | 0,27 | 0,11 | 0,62 | 0,002 |
| Отсутствие ответа по данным КТ | 0,37 | 0,17 | 0,83 | 0,016 |
| ЛДГ | 0,38 | 0,15 | 0,95 | 0,037 |
| Бессобытийная выживаемость | ||||
| Отсутствие ответа по КТ | 0,36 | 0,18 | 0,68 | 0,001 |
| Позитивность по ПЭТ1 | 0,36 | 0,17 | 0,75 | 0,006 |
| В-симптомы в рецидиве | 0,47 | 0,24 | 0,92 | 0,002 |
| Предлеченность(более трех линий химиотерапии) | 0,41 | 0,21 | 0,81 | 0,01 |
| ЛДГ | 0,45 | 0,21 | 0,96 | 0,04 |
Таблица 4. Многофакторный анализ факторов риска бессобытийной выживаемости (метод Кокса, критерий Хи- квадрат)
| Фактор | Отношение рисков | Доверительный интервал 95% | p | |
| Отсутствие ответа по КТ | 0,38 | 0,16 | 0,89 | 0,026 |
| Позитивность по ПЭТ2 | 0,42 | 0,18 | 0,97 | 0,043 |
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20621" ["VALUE"]=> array(2) { ["TEXT"]=> string(554) "<sup>1</sup> Первый Санкт-Петербургский государственный медицинский ниверситет им И. П. Павлова, Санкт-Петербург<br> <sup>2</sup> Городской гематологический центр, Городская клиническая больница №31, Санкт-Петербург<br> <sup>3</sup> Военно-медицинская Академия им. С. М. Кирова, Санкт-Петербург" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(506) "1 Первый Санкт-Петербургский государственный медицинский ниверситет им И. П. Павлова, Санкт-Петербург
2 Городской гематологический центр, Городская клиническая больница №31, Санкт-Петербург
3 Военно-медицинская Академия им. С. М. Кирова, Санкт-Петербург" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(506) "1 Первый Санкт-Петербургский государственный медицинский ниверситет им И. П. Павлова, Санкт-Петербург
2 Городской гематологический центр, Городская клиническая больница №31, Санкт-Петербург
3 Военно-медицинская Академия им. С. М. Кирова, Санкт-Петербург" } } } [50]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1587" ["~ID"]=> string(4) "1587" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(424) "Восстановление Т-клеток памяти у больных острыми лейкозами после трансплантации аллогенных гемопоэтических стволовых клеток при использовании альтернативных схем профилактики острой реакции трансплантат против хозяина (оРТПХ)" ["~NAME"]=> string(424) "Восстановление Т-клеток памяти у больных острыми лейкозами после трансплантации аллогенных гемопоэтических стволовых клеток при использовании альтернативных схем профилактики острой реакции трансплантат против хозяина (оРТПХ)" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:40:57" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:40:57" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vosstanovlenie-t-kletok-pamyati-u-bolnykh-ostrymi-leykozami-posle-transplantatsii-allogennykh-gemopo/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/vosstanovlenie-t-kletok-pamyati-u-bolnykh-ostrymi-leykozami-posle-transplantatsii-allogennykh-gemopo/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "vosstanovlenie-t-kletok-pamyati-u-bolnykh-ostrymi-leykozami-posle-transplantatsii-allogennykh-gemopo" ["~CODE"]=> string(100) "vosstanovlenie-t-kletok-pamyati-u-bolnykh-ostrymi-leykozami-posle-transplantatsii-allogennykh-gemopo" ["EXTERNAL_ID"]=> string(4) "1587" ["~EXTERNAL_ID"]=> string(4) "1587" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(424) "Восстановление Т-клеток памяти у больных острыми лейкозами после трансплантации аллогенных гемопоэтических стволовых клеток при использовании альтернативных схем профилактики острой реакции трансплантат против хозяина (оРТПХ)" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(597) "Восстановление Т-клеток памяти у больных острыми лейкозами после трансплантации аллогенных гемопоэтических стволовых клеток при использовании альтернативных схем профилактики острой реакции трансплантат против хозяина (оРТПХ)Recovery of memory T cells after alternative prophylaxis regimens of acute graft-versus-host disease (aGVHD) in leukemia patients after allogeneic stem cells transplantation" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(10898) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Т-клетки памяти представляют собой гетерогенную субпопуляцию иммунных клеток, участвующих в развитии аллоиммунных реакций после алло-ТГСК – реакции трансплантат против опухоли (РТПО) и РТПХ. В настоящее время созданы новые программы иммуносупрессивной терапии, но единого унифицированного подхода профилактики острой РТПХ не существует. Необходимость проведения иммуносупрессии, особенно при несовместимых/гаплоидентичных алло-ТГСК, когда требуется максимальная иммуноаблация, позволяет контролировать развитие/течение РТПХ. Однако необходимость своевременной реконституции иммунной системы является ключевым фактором для реализации противоопухолевого контроля. Цель работы состояла в оценке влияния различных схем профилактики острой РТПХ на восстановление субпопуляций Т-клеток памяти и их предшественников у больных острыми лейкозами после алло-ТГСК. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В исследование включены 39 пациентов с острыми лейкозами, которым была выполнена алло-ТГСК в ФГБУ «НМИЦ гематологии» Минздрава РФ. Медиана возраста составила 36 лет (17-60 лет). Альтернативные программы профилактики острой РТПХ использовали при несовместимых/гаплоидентичных алло-ТГСК (n=17), которые включали в себя посттрансплантационный циклофосфамид (ПТ-ЦФ) на +3, +4 день или Тαβ-деплецию у молодых пациентов. В контрольную группу мы включили пациентов с классическим режимом иммуносупрессии (классическая ИСТ) с использованием циклоспорина А в сочетании с микофенолатом мофетилом и малыми дозами метотрексата, применяемых после совместимой родственной/неродственной алло-ТГСК (n=22). Характеристика больных, включенных в исследование, схемы профилактики РТПХ, частота развития острой РТПХ и рецидивов заболевания приведена в таблице 1. </p> <h2>Таблица 1. Характеристика пациентов</h2> <img width="783" alt="38_таблица.png" src="/upload/medialibrary/d46/38_tablitsa.png" height="467" title="38_таблица.png"><br> <img width="767" alt="38_рисунок 1.png" src="/upload/medialibrary/1ab/38_risunok-1.png" height="704" title="38_рисунок 1.png"><br> <h2>Рисунок 1. Восстановление субпопуляций Т-клеток памяти у больных острыми лейкозами после алло-ТГСК</h2> <p style="text-align: justify;"> Примечание. На графике показаны значимые отличия (p<0,005) по количеству клеток в субпопуляциях CD4+/CD8+ Т-клеток памяти при использовании альтернативных режимов профилактики оРТПХ – ПТ-ЦФ или Т-деплеции, в сравнении с классической ИСТ. </p> <p style="text-align: justify;"> Для исследования реконституции субпопуляций Т-клеток памяти использовали нативные образцы перифе-рической крови больных после алло-ТГСК на +30, +60, +90 день. С помощью метода многоцветной проточной цитометрии (BD FACS Canto II, Becton Dickinson, USA) были определены следующие субпопуляции Т-клеток памяти периферической крови: Т-наивные и стволовые клетки памяти (Tnv+Tscm) – CD8+/СD4+ CD45R0-CCR7+CD28+; T-клетки центральной памяти (Tcm) – CD8+/СD4+ CD45R0+CCR7+CD28+; T-клетки тран-зиторной памяти (Ttm) – CD8+/СD4+ CD45R0+CCR7-CD28+; T-клетки эффекторной памяти (Tem) – CD8+/СD4+ CD45R0+CCR7-CD28-; T- терминальные эффек-торы (Tte) – CD8+/СD4+ CD45R0-CCR7-CD28-. Для оценки различий между двумя независимыми выборками использовали U-критерий Манна-Уитни. Значениер<0,05 считали статистически значимым. Весь анализ данных проводили с использованием SPSS ver 23. (IBM, Chicago,Ill., USA). </p> <h2 style="text-align: justify;"> Результаты </h2> <p style="text-align: justify;"> Данные представлены на рисунке 1. Показано, что на +30, +60, +90 день абсолютное количество CD8+ Tnv+Tscm после классической ИСТ было значимо больше, чем после использования ПТ-ЦФ или Тαβ-деплеции. На +30 день абсолютное количество CD8+ Tnv+Tscm после использования классической схемы профилактики РТПХ составило 4,22 кл/мкл (1,21-7,0кл кл/мкл), после ПТ-ЦФ – 0,38 кл/мкл (0,17-0,63 кл/мкл) (p=0,001), после Т-деплеции – 0,14 кл/мкл (0,05-0,15 кл/мкл) (р=0,03). На +60 день – 2,57 кл/мкл (1,49-4,99 кл/мкл) после классической ИСТ; 0,12 кл/мкл (0,02-0,15 кл/мкл) после Т-деплеции; 1,1 кл/мкл (0,72-2,8 кл/мкл) после ПТ-ЦФ (p=0,009). На +90 день – 4,29 кл/мкл (2,08-6,58 кл/мкл) после классического режима; 1,82 кл/мкл (0,16-3,3 кл/мкл) после ПТ-ЦФ; 0,35 кл/мкл (0,01-0,7 кл/мкл) после Т-деплеции (p=0,035). На +30, +60 день абсолютное количество CD8+ Tcm было значимо меньше после использования альтернативных подходов в сравнении с классической ИСТ – на +30 день 1,07 кл/мкл (0,27-1,75 кл/мкл) после классической ИСТ, 0,25 кл/мкл (0,12-0,68 кл/мкл) после ПТ-ЦФ (р=0,032), 0,18 кл/мкл (0,01-0,34 кл/мкл) после Т-деплеции (р=0,036); на +60 день 0,9 кл/мкл (0,65-1,68 кл/мкл), 0,42 кл/мкл (0,33-0,73 кл/мкл), 0,05 кл/мкл (0,01-0,07 кл/мкл) соответственно (р=0,02). Абсолютное количество CD4+ Tnv+Tscm на +30 день было значимо больше после применения классической схемы профилактики РТПХ – 16,1 кл/мкл (2,1-55,0 кл/мкл), в сравнении с использованием ПТ-ЦФ – 1,35 кл/мкл (0,7-5,36 кл/мкл) и Т-деплеции – 0,31 кл/мкл (0,27-0,71 кл/мкл) (р=0,05). Субпопуляция Тtm CD8+ на +60, +90 дни и CD4+ на +30 день отличалась при использовании классической ИСТ и альтернативных режимов (Рисунок 1). Мы не выявили корреляции между числом Tnv+Tscm, Tcm, Ttm, Tem, Tte и развитием оРТПХ или рецидива заболевания. </p> <h2 style="text-align: justify;"> Заключение </h2> <p style="text-align: justify;"> Субпопуляция наивных и стволовых Т-клеток памяти является пулом клеток-предшественников для целого эффекторного звена Т-клеток (Ttm, Tem, Tte), реализующего аллоиммунный ответ. Значимое уменьшение пула CD4+/CD8+ Tnv+Tscm, CD8+ Tcm после использования альтернативных схем профилактики острой РТПХ может свидетельствовать о более глубокой иммуноаблации при этих режимах, используемых при несовместимых/гапло-ТГСК. За счет этого сохраняющееся низкое количество Tnv+Tscm на +60, +90 день, как клеток-предшественников для целой популяции Т-клеток памяти, может свидетельствовать об отсроченной реконституции адаптивного звена иммунного ответа при альтернативных режимах профилактики оРТПХ. </p> <h2 style="text-align: justify;"> Ключевые слова </h2> <p style="text-align: justify;"> Т-клетки памяти, реконституция иммунной системы, трансплантация аллогенных гемопоэтических стволовых клеток, профилактика острой РТПХ. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(424) "Восстановление Т-клеток памяти у больных острыми лейкозами после трансплантации аллогенных гемопоэтических стволовых клеток при использовании альтернативных схем профилактики острой реакции трансплантат против хозяина (оРТПХ)" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(424) "Восстановление Т-клеток памяти у больных острыми лейкозами после трансплантации аллогенных гемопоэтических стволовых клеток при использовании альтернативных схем профилактики острой реакции трансплантат против хозяина (оРТПХ)" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(424) "Восстановление Т-клеток памяти у больных острыми лейкозами после трансплантации аллогенных гемопоэтических стволовых клеток при использовании альтернативных схем профилактики острой реакции трансплантат против хозяина (оРТПХ)" ["SECTION_META_TITLE"]=> string(424) "Восстановление Т-клеток памяти у больных острыми лейкозами после трансплантации аллогенных гемопоэтических стволовых клеток при использовании альтернативных схем профилактики острой реакции трансплантат против хозяина (оРТПХ)" ["SECTION_META_KEYWORDS"]=> string(424) "Восстановление Т-клеток памяти у больных острыми лейкозами после трансплантации аллогенных гемопоэтических стволовых клеток при использовании альтернативных схем профилактики острой реакции трансплантат против хозяина (оРТПХ)" ["SECTION_META_DESCRIPTION"]=> string(424) "Восстановление Т-клеток памяти у больных острыми лейкозами после трансплантации аллогенных гемопоэтических стволовых клеток при использовании альтернативных схем профилактики острой реакции трансплантат против хозяина (оРТПХ)" ["SECTION_PICTURE_FILE_ALT"]=> string(424) "Восстановление Т-клеток памяти у больных острыми лейкозами после трансплантации аллогенных гемопоэтических стволовых клеток при использовании альтернативных схем профилактики острой реакции трансплантат против хозяина (оРТПХ)" ["SECTION_PICTURE_FILE_TITLE"]=> string(424) "Восстановление Т-клеток памяти у больных острыми лейкозами после трансплантации аллогенных гемопоэтических стволовых клеток при использовании альтернативных схем профилактики острой реакции трансплантат против хозяина (оРТПХ)" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "vosstanovlenie-t-kletok-pamyati-u-bolnykh-ostrymi-leykozami-posle-transplantatsii-allogennykh-gemopo" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(424) "Восстановление Т-клеток памяти у больных острыми лейкозами после трансплантации аллогенных гемопоэтических стволовых клеток при использовании альтернативных схем профилактики острой реакции трансплантат против хозяина (оРТПХ)" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(424) "Восстановление Т-клеток памяти у больных острыми лейкозами после трансплантации аллогенных гемопоэтических стволовых клеток при использовании альтернативных схем профилактики острой реакции трансплантат против хозяина (оРТПХ)" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vosstanovlenie-t-kletok-pamyati-u-bolnykh-ostrymi-leykozami-posle-transplantatsii-allogennykh-gemopo" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "vosstanovlenie-t-kletok-pamyati-u-bolnykh-ostrymi-leykozami-posle-transplantatsii-allogennykh-gemopo" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "vosstanovlenie-t-kletok-pamyati-u-bolnykh-ostrymi-leykozami-posle-transplantatsii-allogennykh-gemopo" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20613" ["VALUE"]=> array(2) { ["TEXT"]=> string(575) "Наталья Н. Попова, Михаил Ю. Дроков, Елена Н. Паровичникова, Лариса А. Кузьмина, Юлия О. Давыдова, Николай М. Капранов, Екатерина Д. Михальцова, Ольга М. Королева, Вера А. Васильева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Ирина В. Гальцева, Михаил А. Масчан, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(575) "Наталья Н. Попова, Михаил Ю. Дроков, Елена Н. Паровичникова, Лариса А. Кузьмина, Юлия О. Давыдова, Николай М. Капранов, Екатерина Д. Михальцова, Ольга М. Королева, Вера А. Васильева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Ирина В. Гальцева, Михаил А. Масчан, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20614" ["VALUE"]=> array(2) { ["TEXT"]=> string(86) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(86) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20615" ["VALUE"]=> array(2) { ["TEXT"]=> string(10898) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Т-клетки памяти представляют собой гетерогенную субпопуляцию иммунных клеток, участвующих в развитии аллоиммунных реакций после алло-ТГСК – реакции трансплантат против опухоли (РТПО) и РТПХ. В настоящее время созданы новые программы иммуносупрессивной терапии, но единого унифицированного подхода профилактики острой РТПХ не существует. Необходимость проведения иммуносупрессии, особенно при несовместимых/гаплоидентичных алло-ТГСК, когда требуется максимальная иммуноаблация, позволяет контролировать развитие/течение РТПХ. Однако необходимость своевременной реконституции иммунной системы является ключевым фактором для реализации противоопухолевого контроля. Цель работы состояла в оценке влияния различных схем профилактики острой РТПХ на восстановление субпопуляций Т-клеток памяти и их предшественников у больных острыми лейкозами после алло-ТГСК. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В исследование включены 39 пациентов с острыми лейкозами, которым была выполнена алло-ТГСК в ФГБУ «НМИЦ гематологии» Минздрава РФ. Медиана возраста составила 36 лет (17-60 лет). Альтернативные программы профилактики острой РТПХ использовали при несовместимых/гаплоидентичных алло-ТГСК (n=17), которые включали в себя посттрансплантационный циклофосфамид (ПТ-ЦФ) на +3, +4 день или Тαβ-деплецию у молодых пациентов. В контрольную группу мы включили пациентов с классическим режимом иммуносупрессии (классическая ИСТ) с использованием циклоспорина А в сочетании с микофенолатом мофетилом и малыми дозами метотрексата, применяемых после совместимой родственной/неродственной алло-ТГСК (n=22). Характеристика больных, включенных в исследование, схемы профилактики РТПХ, частота развития острой РТПХ и рецидивов заболевания приведена в таблице 1. </p> <h2>Таблица 1. Характеристика пациентов</h2> <img width="783" alt="38_таблица.png" src="/upload/medialibrary/d46/38_tablitsa.png" height="467" title="38_таблица.png"><br> <img width="767" alt="38_рисунок 1.png" src="/upload/medialibrary/1ab/38_risunok-1.png" height="704" title="38_рисунок 1.png"><br> <h2>Рисунок 1. Восстановление субпопуляций Т-клеток памяти у больных острыми лейкозами после алло-ТГСК</h2> <p style="text-align: justify;"> Примечание. На графике показаны значимые отличия (p<0,005) по количеству клеток в субпопуляциях CD4+/CD8+ Т-клеток памяти при использовании альтернативных режимов профилактики оРТПХ – ПТ-ЦФ или Т-деплеции, в сравнении с классической ИСТ. </p> <p style="text-align: justify;"> Для исследования реконституции субпопуляций Т-клеток памяти использовали нативные образцы перифе-рической крови больных после алло-ТГСК на +30, +60, +90 день. С помощью метода многоцветной проточной цитометрии (BD FACS Canto II, Becton Dickinson, USA) были определены следующие субпопуляции Т-клеток памяти периферической крови: Т-наивные и стволовые клетки памяти (Tnv+Tscm) – CD8+/СD4+ CD45R0-CCR7+CD28+; T-клетки центральной памяти (Tcm) – CD8+/СD4+ CD45R0+CCR7+CD28+; T-клетки тран-зиторной памяти (Ttm) – CD8+/СD4+ CD45R0+CCR7-CD28+; T-клетки эффекторной памяти (Tem) – CD8+/СD4+ CD45R0+CCR7-CD28-; T- терминальные эффек-торы (Tte) – CD8+/СD4+ CD45R0-CCR7-CD28-. Для оценки различий между двумя независимыми выборками использовали U-критерий Манна-Уитни. Значениер<0,05 считали статистически значимым. Весь анализ данных проводили с использованием SPSS ver 23. (IBM, Chicago,Ill., USA). </p> <h2 style="text-align: justify;"> Результаты </h2> <p style="text-align: justify;"> Данные представлены на рисунке 1. Показано, что на +30, +60, +90 день абсолютное количество CD8+ Tnv+Tscm после классической ИСТ было значимо больше, чем после использования ПТ-ЦФ или Тαβ-деплеции. На +30 день абсолютное количество CD8+ Tnv+Tscm после использования классической схемы профилактики РТПХ составило 4,22 кл/мкл (1,21-7,0кл кл/мкл), после ПТ-ЦФ – 0,38 кл/мкл (0,17-0,63 кл/мкл) (p=0,001), после Т-деплеции – 0,14 кл/мкл (0,05-0,15 кл/мкл) (р=0,03). На +60 день – 2,57 кл/мкл (1,49-4,99 кл/мкл) после классической ИСТ; 0,12 кл/мкл (0,02-0,15 кл/мкл) после Т-деплеции; 1,1 кл/мкл (0,72-2,8 кл/мкл) после ПТ-ЦФ (p=0,009). На +90 день – 4,29 кл/мкл (2,08-6,58 кл/мкл) после классического режима; 1,82 кл/мкл (0,16-3,3 кл/мкл) после ПТ-ЦФ; 0,35 кл/мкл (0,01-0,7 кл/мкл) после Т-деплеции (p=0,035). На +30, +60 день абсолютное количество CD8+ Tcm было значимо меньше после использования альтернативных подходов в сравнении с классической ИСТ – на +30 день 1,07 кл/мкл (0,27-1,75 кл/мкл) после классической ИСТ, 0,25 кл/мкл (0,12-0,68 кл/мкл) после ПТ-ЦФ (р=0,032), 0,18 кл/мкл (0,01-0,34 кл/мкл) после Т-деплеции (р=0,036); на +60 день 0,9 кл/мкл (0,65-1,68 кл/мкл), 0,42 кл/мкл (0,33-0,73 кл/мкл), 0,05 кл/мкл (0,01-0,07 кл/мкл) соответственно (р=0,02). Абсолютное количество CD4+ Tnv+Tscm на +30 день было значимо больше после применения классической схемы профилактики РТПХ – 16,1 кл/мкл (2,1-55,0 кл/мкл), в сравнении с использованием ПТ-ЦФ – 1,35 кл/мкл (0,7-5,36 кл/мкл) и Т-деплеции – 0,31 кл/мкл (0,27-0,71 кл/мкл) (р=0,05). Субпопуляция Тtm CD8+ на +60, +90 дни и CD4+ на +30 день отличалась при использовании классической ИСТ и альтернативных режимов (Рисунок 1). Мы не выявили корреляции между числом Tnv+Tscm, Tcm, Ttm, Tem, Tte и развитием оРТПХ или рецидива заболевания. </p> <h2 style="text-align: justify;"> Заключение </h2> <p style="text-align: justify;"> Субпопуляция наивных и стволовых Т-клеток памяти является пулом клеток-предшественников для целого эффекторного звена Т-клеток (Ttm, Tem, Tte), реализующего аллоиммунный ответ. Значимое уменьшение пула CD4+/CD8+ Tnv+Tscm, CD8+ Tcm после использования альтернативных схем профилактики острой РТПХ может свидетельствовать о более глубокой иммуноаблации при этих режимах, используемых при несовместимых/гапло-ТГСК. За счет этого сохраняющееся низкое количество Tnv+Tscm на +60, +90 день, как клеток-предшественников для целой популяции Т-клеток памяти, может свидетельствовать об отсроченной реконституции адаптивного звена иммунного ответа при альтернативных режимах профилактики оРТПХ. </p> <h2 style="text-align: justify;"> Ключевые слова </h2> <p style="text-align: justify;"> Т-клетки памяти, реконституция иммунной системы, трансплантация аллогенных гемопоэтических стволовых клеток, профилактика острой РТПХ. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(10466) "
Введение
Т-клетки памяти представляют собой гетерогенную субпопуляцию иммунных клеток, участвующих в развитии аллоиммунных реакций после алло-ТГСК – реакции трансплантат против опухоли (РТПО) и РТПХ. В настоящее время созданы новые программы иммуносупрессивной терапии, но единого унифицированного подхода профилактики острой РТПХ не существует. Необходимость проведения иммуносупрессии, особенно при несовместимых/гаплоидентичных алло-ТГСК, когда требуется максимальная иммуноаблация, позволяет контролировать развитие/течение РТПХ. Однако необходимость своевременной реконституции иммунной системы является ключевым фактором для реализации противоопухолевого контроля. Цель работы состояла в оценке влияния различных схем профилактики острой РТПХ на восстановление субпопуляций Т-клеток памяти и их предшественников у больных острыми лейкозами после алло-ТГСК.
Материалы и методы
В исследование включены 39 пациентов с острыми лейкозами, которым была выполнена алло-ТГСК в ФГБУ «НМИЦ гематологии» Минздрава РФ. Медиана возраста составила 36 лет (17-60 лет). Альтернативные программы профилактики острой РТПХ использовали при несовместимых/гаплоидентичных алло-ТГСК (n=17), которые включали в себя посттрансплантационный циклофосфамид (ПТ-ЦФ) на +3, +4 день или Тαβ-деплецию у молодых пациентов. В контрольную группу мы включили пациентов с классическим режимом иммуносупрессии (классическая ИСТ) с использованием циклоспорина А в сочетании с микофенолатом мофетилом и малыми дозами метотрексата, применяемых после совместимой родственной/неродственной алло-ТГСК (n=22). Характеристика больных, включенных в исследование, схемы профилактики РТПХ, частота развития острой РТПХ и рецидивов заболевания приведена в таблице 1.
Таблица 1. Характеристика пациентов


Рисунок 1. Восстановление субпопуляций Т-клеток памяти у больных острыми лейкозами после алло-ТГСК
Примечание. На графике показаны значимые отличия (p<0,005) по количеству клеток в субпопуляциях CD4+/CD8+ Т-клеток памяти при использовании альтернативных режимов профилактики оРТПХ – ПТ-ЦФ или Т-деплеции, в сравнении с классической ИСТ.
Для исследования реконституции субпопуляций Т-клеток памяти использовали нативные образцы перифе-рической крови больных после алло-ТГСК на +30, +60, +90 день. С помощью метода многоцветной проточной цитометрии (BD FACS Canto II, Becton Dickinson, USA) были определены следующие субпопуляции Т-клеток памяти периферической крови: Т-наивные и стволовые клетки памяти (Tnv+Tscm) – CD8+/СD4+ CD45R0-CCR7+CD28+; T-клетки центральной памяти (Tcm) – CD8+/СD4+ CD45R0+CCR7+CD28+; T-клетки тран-зиторной памяти (Ttm) – CD8+/СD4+ CD45R0+CCR7-CD28+; T-клетки эффекторной памяти (Tem) – CD8+/СD4+ CD45R0+CCR7-CD28-; T- терминальные эффек-торы (Tte) – CD8+/СD4+ CD45R0-CCR7-CD28-. Для оценки различий между двумя независимыми выборками использовали U-критерий Манна-Уитни. Значениер<0,05 считали статистически значимым. Весь анализ данных проводили с использованием SPSS ver 23. (IBM, Chicago,Ill., USA).
Результаты
Данные представлены на рисунке 1. Показано, что на +30, +60, +90 день абсолютное количество CD8+ Tnv+Tscm после классической ИСТ было значимо больше, чем после использования ПТ-ЦФ или Тαβ-деплеции. На +30 день абсолютное количество CD8+ Tnv+Tscm после использования классической схемы профилактики РТПХ составило 4,22 кл/мкл (1,21-7,0кл кл/мкл), после ПТ-ЦФ – 0,38 кл/мкл (0,17-0,63 кл/мкл) (p=0,001), после Т-деплеции – 0,14 кл/мкл (0,05-0,15 кл/мкл) (р=0,03). На +60 день – 2,57 кл/мкл (1,49-4,99 кл/мкл) после классической ИСТ; 0,12 кл/мкл (0,02-0,15 кл/мкл) после Т-деплеции; 1,1 кл/мкл (0,72-2,8 кл/мкл) после ПТ-ЦФ (p=0,009). На +90 день – 4,29 кл/мкл (2,08-6,58 кл/мкл) после классического режима; 1,82 кл/мкл (0,16-3,3 кл/мкл) после ПТ-ЦФ; 0,35 кл/мкл (0,01-0,7 кл/мкл) после Т-деплеции (p=0,035). На +30, +60 день абсолютное количество CD8+ Tcm было значимо меньше после использования альтернативных подходов в сравнении с классической ИСТ – на +30 день 1,07 кл/мкл (0,27-1,75 кл/мкл) после классической ИСТ, 0,25 кл/мкл (0,12-0,68 кл/мкл) после ПТ-ЦФ (р=0,032), 0,18 кл/мкл (0,01-0,34 кл/мкл) после Т-деплеции (р=0,036); на +60 день 0,9 кл/мкл (0,65-1,68 кл/мкл), 0,42 кл/мкл (0,33-0,73 кл/мкл), 0,05 кл/мкл (0,01-0,07 кл/мкл) соответственно (р=0,02). Абсолютное количество CD4+ Tnv+Tscm на +30 день было значимо больше после применения классической схемы профилактики РТПХ – 16,1 кл/мкл (2,1-55,0 кл/мкл), в сравнении с использованием ПТ-ЦФ – 1,35 кл/мкл (0,7-5,36 кл/мкл) и Т-деплеции – 0,31 кл/мкл (0,27-0,71 кл/мкл) (р=0,05). Субпопуляция Тtm CD8+ на +60, +90 дни и CD4+ на +30 день отличалась при использовании классической ИСТ и альтернативных режимов (Рисунок 1). Мы не выявили корреляции между числом Tnv+Tscm, Tcm, Ttm, Tem, Tte и развитием оРТПХ или рецидива заболевания.
Заключение
Субпопуляция наивных и стволовых Т-клеток памяти является пулом клеток-предшественников для целого эффекторного звена Т-клеток (Ttm, Tem, Tte), реализующего аллоиммунный ответ. Значимое уменьшение пула CD4+/CD8+ Tnv+Tscm, CD8+ Tcm после использования альтернативных схем профилактики острой РТПХ может свидетельствовать о более глубокой иммуноаблации при этих режимах, используемых при несовместимых/гапло-ТГСК. За счет этого сохраняющееся низкое количество Tnv+Tscm на +60, +90 день, как клеток-предшественников для целой популяции Т-клеток памяти, может свидетельствовать об отсроченной реконституции адаптивного звена иммунного ответа при альтернативных режимах профилактики оРТПХ.
Ключевые слова
Т-клетки памяти, реконституция иммунной системы, трансплантация аллогенных гемопоэтических стволовых клеток, профилактика острой РТПХ.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20616" ["VALUE"]=> array(2) { ["TEXT"]=> string(336) "Natalia N. Popova, Mikhail Y. Drokov, Elena N. Parovichnikova, Larisa A. Kuzmina, Julia O. Davydova, Nikolay М. Kapranov, Ekaterina D. Mikhaltsova, Olga M. Koroleva, Vera A. Vasilyeva, Darya S. Dubnyak, Zoya V. Konova, Anna A. Sidorova, Ekaterina V. Usikova, Anna A. Dmitrova, Irina V. Galtseva, Michael A. Maschan, Valery G. Savchenko" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(336) "Natalia N. Popova, Mikhail Y. Drokov, Elena N. Parovichnikova, Larisa A. Kuzmina, Julia O. Davydova, Nikolay М. Kapranov, Ekaterina D. Mikhaltsova, Olga M. Koroleva, Vera A. Vasilyeva, Darya S. Dubnyak, Zoya V. Konova, Anna A. Sidorova, Ekaterina V. Usikova, Anna A. Dmitrova, Irina V. Galtseva, Michael A. Maschan, Valery G. Savchenko" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20617" ["VALUE"]=> array(2) { ["TEXT"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20618" ["VALUE"]=> array(2) { ["TEXT"]=> string(6623) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> T-memory cells form the heterogeneous pool of immune cells responsible for alloreactivity after allogeneic stem cells transplantation (allo-HSCT). Nowadays there are new different approaches for aGVHD prophylaxis, but the unified immunosuppressive regimen has not been defined yet. Obviously the immunosuppressive therapy as aGVHD prophylaxis is essential to control aGVHD especially in terms of mismatched or haplo-HSCT when strong immunoablation is required. But timely immune reconstitution is crucial for antitumor immunity. Aim of the present study was to evaluate an impact of different immunosuppressive regimens of aGVHD prophylaxis on T-memory cell subsets recovery in leukemia patients after allo-HSCT. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> The study comprised 39 leukemia patients with a median age of 36 years old (17-60 y.o.) who underwent allo-HSCT in National Research Center for Hematology, Russia. Alternative immunosuppressive regimens of aGVHD prophylaxis in case of mismatched or haplo-HSCT (n=17) include Posttransplant high dose Cyclophosphamide (PT-Cy) on day +3, +4 or alfa/beta T-cells depletion in young patients. Classical immunosuppressive regimen with CsA+MMF+MTX was applied in case of matched related and matched unrelated donors and form the control group (n=22). The characteristics of patients, immunosuppressive regimens, aGVHD and relapses after allo-HSCT are presented in the table 1. Samples of peripheral blood were collected on day +30, +60 and +90 after allo-HSCT in EDTA-tubes. Flow cytometry analysis was performed on BD FACS Canto II (Becton Dickinson, USA) to define T-memory subsets: T-naive and T-stem cell memory (Tnv+Tscm) – CD8+/CD4+ CD45R0-CCR7+CD28+; T-central memory (Tcm) – CD8+/CD4+ CD45R0+CCR7+CD28+; T-transitional memory (Ttm) – CD8+/CD4+CD45R0+CCR7-CD28+; T-effector memory (Tem) – CD8+/CD4+ CD45R0+CCR7-CD28-; T-terminal effector (Tte) – CD8+/CD4+ CD45R0-CCR7-CD28-. Mann-Whitney U test was used for nonparametric data analysis. A p-value less than 0.05 was considered as significant. All data analysis was conducted utilizing SPSS ver. 23. (IBM, Chicago, Ill., USA). </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The data are presented in the Fig. 1. According to our data, absolute number of CD8+ Tnv+Tscm after classic immunosuppressive regimen was significantly higher than after PTCy prophylaxis, or T-cells depletion on days +30, +60, +90. Absolute number of CD8+ Tnv+Tscm after classic immunosuppressive regimen on day +30 was 4.22 cells/μL (1.21-7.0 cells/μL), after PT-Cy – 0.38 cells/μL (0.17-0.63 cells/μL) (p=0.001), after Т-cell depletion – 0.14 cells/μL (0.05-0.15 cells/μL) (р=0.03). Appropriate levels by the day +60 were 2.57 cells/μL (1.49-4.99 cells/μL) after classic immunosuppressive regimen; 0.12 cells/μL (0.02-0.15 cells/μL), after Т-cell depletion; 1.1 cells/μL (0.72-2.8 cells/μL) after PT-Cy (p=0.009). On the day +90 these parameters were 4.29 cells/ μL (2.08-6.58 cells/μL) after classic immunosuppressive regimen; 1.82 cells/μL (0.16-3.3 cells/μL) after PT-Cy; and 0.35 cells/μL (0.01-0.7 cells/μL) after Т-cell depletion (p=0.035). On day +30 and +60, absolute numbers of CD8+ Tcm were significant lower after alternative approaches, when compared to classical immunosuppressive regimen, i.e., on day +30, 1.07 cells/μL (0.27-1.75 cells/μL) after classical regimen; 0.25 cells/μL (0.12-0.68 cells/μL) after PT-Cy (р=0.032); 0.18 cells/μL (0.01-0.34 cells/μL) after Т-cells depletion (р=0.036); on day +60, 0.9 cells/μL (0.65-1.68 cells/μL); 0.42 cells/μL (0.33-0.73 cells/μL); 0.05 cells/μL (0.01-0.07 cells/μL), respectively (р=0.02). Absolute number of CD4+ Tnv+Tscm on day +30 was significantly higher after classic immunosuppressiveregimen, i.e. 16.1 cells/μL (2.1-55.0 cells/μL), as compared to PT-Cy – 1.35 cells/μL (0.7-5.36 cells/μL), and Т cell depletion – 0.31 cells/μL (0.27-0.71 cells/μL) (р=0.05). Absolute number of Тtm CD8+ on days +60, +90 and CD4+ on day +30 were different in alternative aGVHD prophylaxis and in control group (Fig. 1). We didn’t find any correlations between absolute numbers of Tnv+Tscm, Tcm, Ttm, Tem, Tte and aGVHD onset, or leukemia relapse after allo-HSCT. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Tnv+Tscm is the progenitor subset for all memory and effector T-cells and its prompt recovery after allo-HSCT seems to be crucial for graft-versus-leukemia effect. Here we show the lowest number of CD4+/CD8+ Tnv+Tscm, CD8+ Tcm after alternative approaches of aGVHD prophylaxis that might reflect sever immunoablation in mismatched or haplo-HSCT. To this point, low numbers of Tnv+Tscm on day +60, +90 as progenitor cells for the whole T-memory pool may lead to delayed reconstitution of adaptive immunity after alternative aGVHD prophylaxis in patients after allo-HSCT. </p> <h2 style="text-align: justify;">Disclosures</h2> <p style="text-align: justify;"> No relevant conflicts of interest to declare. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Memory T cells, immune reconstitution, allogeneic stem cell transplantation, GVHD prophylaxis regimens. </p> <h2>Table 1. Characteristics of the patients</h2> <img width="781" alt="38_table 1.png" src="/upload/medialibrary/c6c/38_table-1.png" height="571" title="38_table 1.png"><br> <img width="771" alt="38_figure1.png" src="/upload/medialibrary/269/38_figure1.png" height="783" title="38_figure1.png"> <h2>Figure 1. Recovery of T-memory cell subsets in terms of different GVHD prophylaxis in leukemia patients after allo-HSCT</h2> <p style="text-align: justify;"> Significant differences (p<0.005) between the number of different T-memory cell subsets in terms of alternative GVHD prophylaxis – PT-Cy or T-cells depletion comparing to classic immunosuppressive regimen are presented in the graph. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6179) "Introduction
T-memory cells form the heterogeneous pool of immune cells responsible for alloreactivity after allogeneic stem cells transplantation (allo-HSCT). Nowadays there are new different approaches for aGVHD prophylaxis, but the unified immunosuppressive regimen has not been defined yet. Obviously the immunosuppressive therapy as aGVHD prophylaxis is essential to control aGVHD especially in terms of mismatched or haplo-HSCT when strong immunoablation is required. But timely immune reconstitution is crucial for antitumor immunity. Aim of the present study was to evaluate an impact of different immunosuppressive regimens of aGVHD prophylaxis on T-memory cell subsets recovery in leukemia patients after allo-HSCT.
Patients and methods
The study comprised 39 leukemia patients with a median age of 36 years old (17-60 y.o.) who underwent allo-HSCT in National Research Center for Hematology, Russia. Alternative immunosuppressive regimens of aGVHD prophylaxis in case of mismatched or haplo-HSCT (n=17) include Posttransplant high dose Cyclophosphamide (PT-Cy) on day +3, +4 or alfa/beta T-cells depletion in young patients. Classical immunosuppressive regimen with CsA+MMF+MTX was applied in case of matched related and matched unrelated donors and form the control group (n=22). The characteristics of patients, immunosuppressive regimens, aGVHD and relapses after allo-HSCT are presented in the table 1. Samples of peripheral blood were collected on day +30, +60 and +90 after allo-HSCT in EDTA-tubes. Flow cytometry analysis was performed on BD FACS Canto II (Becton Dickinson, USA) to define T-memory subsets: T-naive and T-stem cell memory (Tnv+Tscm) – CD8+/CD4+ CD45R0-CCR7+CD28+; T-central memory (Tcm) – CD8+/CD4+ CD45R0+CCR7+CD28+; T-transitional memory (Ttm) – CD8+/CD4+CD45R0+CCR7-CD28+; T-effector memory (Tem) – CD8+/CD4+ CD45R0+CCR7-CD28-; T-terminal effector (Tte) – CD8+/CD4+ CD45R0-CCR7-CD28-. Mann-Whitney U test was used for nonparametric data analysis. A p-value less than 0.05 was considered as significant. All data analysis was conducted utilizing SPSS ver. 23. (IBM, Chicago, Ill., USA).
Results
The data are presented in the Fig. 1. According to our data, absolute number of CD8+ Tnv+Tscm after classic immunosuppressive regimen was significantly higher than after PTCy prophylaxis, or T-cells depletion on days +30, +60, +90. Absolute number of CD8+ Tnv+Tscm after classic immunosuppressive regimen on day +30 was 4.22 cells/μL (1.21-7.0 cells/μL), after PT-Cy – 0.38 cells/μL (0.17-0.63 cells/μL) (p=0.001), after Т-cell depletion – 0.14 cells/μL (0.05-0.15 cells/μL) (р=0.03). Appropriate levels by the day +60 were 2.57 cells/μL (1.49-4.99 cells/μL) after classic immunosuppressive regimen; 0.12 cells/μL (0.02-0.15 cells/μL), after Т-cell depletion; 1.1 cells/μL (0.72-2.8 cells/μL) after PT-Cy (p=0.009). On the day +90 these parameters were 4.29 cells/ μL (2.08-6.58 cells/μL) after classic immunosuppressive regimen; 1.82 cells/μL (0.16-3.3 cells/μL) after PT-Cy; and 0.35 cells/μL (0.01-0.7 cells/μL) after Т-cell depletion (p=0.035). On day +30 and +60, absolute numbers of CD8+ Tcm were significant lower after alternative approaches, when compared to classical immunosuppressive regimen, i.e., on day +30, 1.07 cells/μL (0.27-1.75 cells/μL) after classical regimen; 0.25 cells/μL (0.12-0.68 cells/μL) after PT-Cy (р=0.032); 0.18 cells/μL (0.01-0.34 cells/μL) after Т-cells depletion (р=0.036); on day +60, 0.9 cells/μL (0.65-1.68 cells/μL); 0.42 cells/μL (0.33-0.73 cells/μL); 0.05 cells/μL (0.01-0.07 cells/μL), respectively (р=0.02). Absolute number of CD4+ Tnv+Tscm on day +30 was significantly higher after classic immunosuppressiveregimen, i.e. 16.1 cells/μL (2.1-55.0 cells/μL), as compared to PT-Cy – 1.35 cells/μL (0.7-5.36 cells/μL), and Т cell depletion – 0.31 cells/μL (0.27-0.71 cells/μL) (р=0.05). Absolute number of Тtm CD8+ on days +60, +90 and CD4+ on day +30 were different in alternative aGVHD prophylaxis and in control group (Fig. 1). We didn’t find any correlations between absolute numbers of Tnv+Tscm, Tcm, Ttm, Tem, Tte and aGVHD onset, or leukemia relapse after allo-HSCT.
Conclusion
Tnv+Tscm is the progenitor subset for all memory and effector T-cells and its prompt recovery after allo-HSCT seems to be crucial for graft-versus-leukemia effect. Here we show the lowest number of CD4+/CD8+ Tnv+Tscm, CD8+ Tcm after alternative approaches of aGVHD prophylaxis that might reflect sever immunoablation in mismatched or haplo-HSCT. To this point, low numbers of Tnv+Tscm on day +60, +90 as progenitor cells for the whole T-memory pool may lead to delayed reconstitution of adaptive immunity after alternative aGVHD prophylaxis in patients after allo-HSCT.
Disclosures
No relevant conflicts of interest to declare.
Keywords
Memory T cells, immune reconstitution, allogeneic stem cell transplantation, GVHD prophylaxis regimens.
Table 1. Characteristics of the patients


Figure 1. Recovery of T-memory cell subsets in terms of different GVHD prophylaxis in leukemia patients after allo-HSCT
Significant differences (p<0.005) between the number of different T-memory cell subsets in terms of alternative GVHD prophylaxis – PT-Cy or T-cells depletion comparing to classic immunosuppressive regimen are presented in the graph.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20619" ["VALUE"]=> string(173) "Recovery of memory T cells after alternative prophylaxis regimens of acute graft-versus-host disease (aGVHD) in leukemia patients after allogeneic stem cells transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(173) "Recovery of memory T cells after alternative prophylaxis regimens of acute graft-versus-host disease (aGVHD) in leukemia patients after allogeneic stem cells transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20805" ["VALUE"]=> string(4) "1443" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1443" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20806" ["VALUE"]=> string(4) "1444" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1444" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20616" ["VALUE"]=> array(2) { ["TEXT"]=> string(336) "Natalia N. Popova, Mikhail Y. Drokov, Elena N. Parovichnikova, Larisa A. Kuzmina, Julia O. Davydova, Nikolay М. Kapranov, Ekaterina D. Mikhaltsova, Olga M. Koroleva, Vera A. Vasilyeva, Darya S. Dubnyak, Zoya V. Konova, Anna A. Sidorova, Ekaterina V. Usikova, Anna A. Dmitrova, Irina V. Galtseva, Michael A. Maschan, Valery G. Savchenko" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(336) "Natalia N. Popova, Mikhail Y. Drokov, Elena N. Parovichnikova, Larisa A. Kuzmina, Julia O. Davydova, Nikolay М. Kapranov, Ekaterina D. Mikhaltsova, Olga M. Koroleva, Vera A. Vasilyeva, Darya S. Dubnyak, Zoya V. Konova, Anna A. Sidorova, Ekaterina V. Usikova, Anna A. Dmitrova, Irina V. Galtseva, Michael A. Maschan, Valery G. Savchenko" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(336) "Natalia N. Popova, Mikhail Y. Drokov, Elena N. Parovichnikova, Larisa A. Kuzmina, Julia O. Davydova, Nikolay М. Kapranov, Ekaterina D. Mikhaltsova, Olga M. Koroleva, Vera A. Vasilyeva, Darya S. Dubnyak, Zoya V. Konova, Anna A. Sidorova, Ekaterina V. Usikova, Anna A. Dmitrova, Irina V. Galtseva, Michael A. Maschan, Valery G. Savchenko" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20618" ["VALUE"]=> array(2) { ["TEXT"]=> string(6623) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> T-memory cells form the heterogeneous pool of immune cells responsible for alloreactivity after allogeneic stem cells transplantation (allo-HSCT). Nowadays there are new different approaches for aGVHD prophylaxis, but the unified immunosuppressive regimen has not been defined yet. Obviously the immunosuppressive therapy as aGVHD prophylaxis is essential to control aGVHD especially in terms of mismatched or haplo-HSCT when strong immunoablation is required. But timely immune reconstitution is crucial for antitumor immunity. Aim of the present study was to evaluate an impact of different immunosuppressive regimens of aGVHD prophylaxis on T-memory cell subsets recovery in leukemia patients after allo-HSCT. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> The study comprised 39 leukemia patients with a median age of 36 years old (17-60 y.o.) who underwent allo-HSCT in National Research Center for Hematology, Russia. Alternative immunosuppressive regimens of aGVHD prophylaxis in case of mismatched or haplo-HSCT (n=17) include Posttransplant high dose Cyclophosphamide (PT-Cy) on day +3, +4 or alfa/beta T-cells depletion in young patients. Classical immunosuppressive regimen with CsA+MMF+MTX was applied in case of matched related and matched unrelated donors and form the control group (n=22). The characteristics of patients, immunosuppressive regimens, aGVHD and relapses after allo-HSCT are presented in the table 1. Samples of peripheral blood were collected on day +30, +60 and +90 after allo-HSCT in EDTA-tubes. Flow cytometry analysis was performed on BD FACS Canto II (Becton Dickinson, USA) to define T-memory subsets: T-naive and T-stem cell memory (Tnv+Tscm) – CD8+/CD4+ CD45R0-CCR7+CD28+; T-central memory (Tcm) – CD8+/CD4+ CD45R0+CCR7+CD28+; T-transitional memory (Ttm) – CD8+/CD4+CD45R0+CCR7-CD28+; T-effector memory (Tem) – CD8+/CD4+ CD45R0+CCR7-CD28-; T-terminal effector (Tte) – CD8+/CD4+ CD45R0-CCR7-CD28-. Mann-Whitney U test was used for nonparametric data analysis. A p-value less than 0.05 was considered as significant. All data analysis was conducted utilizing SPSS ver. 23. (IBM, Chicago, Ill., USA). </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The data are presented in the Fig. 1. According to our data, absolute number of CD8+ Tnv+Tscm after classic immunosuppressive regimen was significantly higher than after PTCy prophylaxis, or T-cells depletion on days +30, +60, +90. Absolute number of CD8+ Tnv+Tscm after classic immunosuppressive regimen on day +30 was 4.22 cells/μL (1.21-7.0 cells/μL), after PT-Cy – 0.38 cells/μL (0.17-0.63 cells/μL) (p=0.001), after Т-cell depletion – 0.14 cells/μL (0.05-0.15 cells/μL) (р=0.03). Appropriate levels by the day +60 were 2.57 cells/μL (1.49-4.99 cells/μL) after classic immunosuppressive regimen; 0.12 cells/μL (0.02-0.15 cells/μL), after Т-cell depletion; 1.1 cells/μL (0.72-2.8 cells/μL) after PT-Cy (p=0.009). On the day +90 these parameters were 4.29 cells/ μL (2.08-6.58 cells/μL) after classic immunosuppressive regimen; 1.82 cells/μL (0.16-3.3 cells/μL) after PT-Cy; and 0.35 cells/μL (0.01-0.7 cells/μL) after Т-cell depletion (p=0.035). On day +30 and +60, absolute numbers of CD8+ Tcm were significant lower after alternative approaches, when compared to classical immunosuppressive regimen, i.e., on day +30, 1.07 cells/μL (0.27-1.75 cells/μL) after classical regimen; 0.25 cells/μL (0.12-0.68 cells/μL) after PT-Cy (р=0.032); 0.18 cells/μL (0.01-0.34 cells/μL) after Т-cells depletion (р=0.036); on day +60, 0.9 cells/μL (0.65-1.68 cells/μL); 0.42 cells/μL (0.33-0.73 cells/μL); 0.05 cells/μL (0.01-0.07 cells/μL), respectively (р=0.02). Absolute number of CD4+ Tnv+Tscm on day +30 was significantly higher after classic immunosuppressiveregimen, i.e. 16.1 cells/μL (2.1-55.0 cells/μL), as compared to PT-Cy – 1.35 cells/μL (0.7-5.36 cells/μL), and Т cell depletion – 0.31 cells/μL (0.27-0.71 cells/μL) (р=0.05). Absolute number of Тtm CD8+ on days +60, +90 and CD4+ on day +30 were different in alternative aGVHD prophylaxis and in control group (Fig. 1). We didn’t find any correlations between absolute numbers of Tnv+Tscm, Tcm, Ttm, Tem, Tte and aGVHD onset, or leukemia relapse after allo-HSCT. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Tnv+Tscm is the progenitor subset for all memory and effector T-cells and its prompt recovery after allo-HSCT seems to be crucial for graft-versus-leukemia effect. Here we show the lowest number of CD4+/CD8+ Tnv+Tscm, CD8+ Tcm after alternative approaches of aGVHD prophylaxis that might reflect sever immunoablation in mismatched or haplo-HSCT. To this point, low numbers of Tnv+Tscm on day +60, +90 as progenitor cells for the whole T-memory pool may lead to delayed reconstitution of adaptive immunity after alternative aGVHD prophylaxis in patients after allo-HSCT. </p> <h2 style="text-align: justify;">Disclosures</h2> <p style="text-align: justify;"> No relevant conflicts of interest to declare. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Memory T cells, immune reconstitution, allogeneic stem cell transplantation, GVHD prophylaxis regimens. </p> <h2>Table 1. Characteristics of the patients</h2> <img width="781" alt="38_table 1.png" src="/upload/medialibrary/c6c/38_table-1.png" height="571" title="38_table 1.png"><br> <img width="771" alt="38_figure1.png" src="/upload/medialibrary/269/38_figure1.png" height="783" title="38_figure1.png"> <h2>Figure 1. Recovery of T-memory cell subsets in terms of different GVHD prophylaxis in leukemia patients after allo-HSCT</h2> <p style="text-align: justify;"> Significant differences (p<0.005) between the number of different T-memory cell subsets in terms of alternative GVHD prophylaxis – PT-Cy or T-cells depletion comparing to classic immunosuppressive regimen are presented in the graph. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6179) "Introduction
T-memory cells form the heterogeneous pool of immune cells responsible for alloreactivity after allogeneic stem cells transplantation (allo-HSCT). Nowadays there are new different approaches for aGVHD prophylaxis, but the unified immunosuppressive regimen has not been defined yet. Obviously the immunosuppressive therapy as aGVHD prophylaxis is essential to control aGVHD especially in terms of mismatched or haplo-HSCT when strong immunoablation is required. But timely immune reconstitution is crucial for antitumor immunity. Aim of the present study was to evaluate an impact of different immunosuppressive regimens of aGVHD prophylaxis on T-memory cell subsets recovery in leukemia patients after allo-HSCT.
Patients and methods
The study comprised 39 leukemia patients with a median age of 36 years old (17-60 y.o.) who underwent allo-HSCT in National Research Center for Hematology, Russia. Alternative immunosuppressive regimens of aGVHD prophylaxis in case of mismatched or haplo-HSCT (n=17) include Posttransplant high dose Cyclophosphamide (PT-Cy) on day +3, +4 or alfa/beta T-cells depletion in young patients. Classical immunosuppressive regimen with CsA+MMF+MTX was applied in case of matched related and matched unrelated donors and form the control group (n=22). The characteristics of patients, immunosuppressive regimens, aGVHD and relapses after allo-HSCT are presented in the table 1. Samples of peripheral blood were collected on day +30, +60 and +90 after allo-HSCT in EDTA-tubes. Flow cytometry analysis was performed on BD FACS Canto II (Becton Dickinson, USA) to define T-memory subsets: T-naive and T-stem cell memory (Tnv+Tscm) – CD8+/CD4+ CD45R0-CCR7+CD28+; T-central memory (Tcm) – CD8+/CD4+ CD45R0+CCR7+CD28+; T-transitional memory (Ttm) – CD8+/CD4+CD45R0+CCR7-CD28+; T-effector memory (Tem) – CD8+/CD4+ CD45R0+CCR7-CD28-; T-terminal effector (Tte) – CD8+/CD4+ CD45R0-CCR7-CD28-. Mann-Whitney U test was used for nonparametric data analysis. A p-value less than 0.05 was considered as significant. All data analysis was conducted utilizing SPSS ver. 23. (IBM, Chicago, Ill., USA).
Results
The data are presented in the Fig. 1. According to our data, absolute number of CD8+ Tnv+Tscm after classic immunosuppressive regimen was significantly higher than after PTCy prophylaxis, or T-cells depletion on days +30, +60, +90. Absolute number of CD8+ Tnv+Tscm after classic immunosuppressive regimen on day +30 was 4.22 cells/μL (1.21-7.0 cells/μL), after PT-Cy – 0.38 cells/μL (0.17-0.63 cells/μL) (p=0.001), after Т-cell depletion – 0.14 cells/μL (0.05-0.15 cells/μL) (р=0.03). Appropriate levels by the day +60 were 2.57 cells/μL (1.49-4.99 cells/μL) after classic immunosuppressive regimen; 0.12 cells/μL (0.02-0.15 cells/μL), after Т-cell depletion; 1.1 cells/μL (0.72-2.8 cells/μL) after PT-Cy (p=0.009). On the day +90 these parameters were 4.29 cells/ μL (2.08-6.58 cells/μL) after classic immunosuppressive regimen; 1.82 cells/μL (0.16-3.3 cells/μL) after PT-Cy; and 0.35 cells/μL (0.01-0.7 cells/μL) after Т-cell depletion (p=0.035). On day +30 and +60, absolute numbers of CD8+ Tcm were significant lower after alternative approaches, when compared to classical immunosuppressive regimen, i.e., on day +30, 1.07 cells/μL (0.27-1.75 cells/μL) after classical regimen; 0.25 cells/μL (0.12-0.68 cells/μL) after PT-Cy (р=0.032); 0.18 cells/μL (0.01-0.34 cells/μL) after Т-cells depletion (р=0.036); on day +60, 0.9 cells/μL (0.65-1.68 cells/μL); 0.42 cells/μL (0.33-0.73 cells/μL); 0.05 cells/μL (0.01-0.07 cells/μL), respectively (р=0.02). Absolute number of CD4+ Tnv+Tscm on day +30 was significantly higher after classic immunosuppressiveregimen, i.e. 16.1 cells/μL (2.1-55.0 cells/μL), as compared to PT-Cy – 1.35 cells/μL (0.7-5.36 cells/μL), and Т cell depletion – 0.31 cells/μL (0.27-0.71 cells/μL) (р=0.05). Absolute number of Тtm CD8+ on days +60, +90 and CD4+ on day +30 were different in alternative aGVHD prophylaxis and in control group (Fig. 1). We didn’t find any correlations between absolute numbers of Tnv+Tscm, Tcm, Ttm, Tem, Tte and aGVHD onset, or leukemia relapse after allo-HSCT.
Conclusion
Tnv+Tscm is the progenitor subset for all memory and effector T-cells and its prompt recovery after allo-HSCT seems to be crucial for graft-versus-leukemia effect. Here we show the lowest number of CD4+/CD8+ Tnv+Tscm, CD8+ Tcm after alternative approaches of aGVHD prophylaxis that might reflect sever immunoablation in mismatched or haplo-HSCT. To this point, low numbers of Tnv+Tscm on day +60, +90 as progenitor cells for the whole T-memory pool may lead to delayed reconstitution of adaptive immunity after alternative aGVHD prophylaxis in patients after allo-HSCT.
Disclosures
No relevant conflicts of interest to declare.
Keywords
Memory T cells, immune reconstitution, allogeneic stem cell transplantation, GVHD prophylaxis regimens.
Table 1. Characteristics of the patients


Figure 1. Recovery of T-memory cell subsets in terms of different GVHD prophylaxis in leukemia patients after allo-HSCT
Significant differences (p<0.005) between the number of different T-memory cell subsets in terms of alternative GVHD prophylaxis – PT-Cy or T-cells depletion comparing to classic immunosuppressive regimen are presented in the graph.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6179) "Introduction
T-memory cells form the heterogeneous pool of immune cells responsible for alloreactivity after allogeneic stem cells transplantation (allo-HSCT). Nowadays there are new different approaches for aGVHD prophylaxis, but the unified immunosuppressive regimen has not been defined yet. Obviously the immunosuppressive therapy as aGVHD prophylaxis is essential to control aGVHD especially in terms of mismatched or haplo-HSCT when strong immunoablation is required. But timely immune reconstitution is crucial for antitumor immunity. Aim of the present study was to evaluate an impact of different immunosuppressive regimens of aGVHD prophylaxis on T-memory cell subsets recovery in leukemia patients after allo-HSCT.
Patients and methods
The study comprised 39 leukemia patients with a median age of 36 years old (17-60 y.o.) who underwent allo-HSCT in National Research Center for Hematology, Russia. Alternative immunosuppressive regimens of aGVHD prophylaxis in case of mismatched or haplo-HSCT (n=17) include Posttransplant high dose Cyclophosphamide (PT-Cy) on day +3, +4 or alfa/beta T-cells depletion in young patients. Classical immunosuppressive regimen with CsA+MMF+MTX was applied in case of matched related and matched unrelated donors and form the control group (n=22). The characteristics of patients, immunosuppressive regimens, aGVHD and relapses after allo-HSCT are presented in the table 1. Samples of peripheral blood were collected on day +30, +60 and +90 after allo-HSCT in EDTA-tubes. Flow cytometry analysis was performed on BD FACS Canto II (Becton Dickinson, USA) to define T-memory subsets: T-naive and T-stem cell memory (Tnv+Tscm) – CD8+/CD4+ CD45R0-CCR7+CD28+; T-central memory (Tcm) – CD8+/CD4+ CD45R0+CCR7+CD28+; T-transitional memory (Ttm) – CD8+/CD4+CD45R0+CCR7-CD28+; T-effector memory (Tem) – CD8+/CD4+ CD45R0+CCR7-CD28-; T-terminal effector (Tte) – CD8+/CD4+ CD45R0-CCR7-CD28-. Mann-Whitney U test was used for nonparametric data analysis. A p-value less than 0.05 was considered as significant. All data analysis was conducted utilizing SPSS ver. 23. (IBM, Chicago, Ill., USA).
Results
The data are presented in the Fig. 1. According to our data, absolute number of CD8+ Tnv+Tscm after classic immunosuppressive regimen was significantly higher than after PTCy prophylaxis, or T-cells depletion on days +30, +60, +90. Absolute number of CD8+ Tnv+Tscm after classic immunosuppressive regimen on day +30 was 4.22 cells/μL (1.21-7.0 cells/μL), after PT-Cy – 0.38 cells/μL (0.17-0.63 cells/μL) (p=0.001), after Т-cell depletion – 0.14 cells/μL (0.05-0.15 cells/μL) (р=0.03). Appropriate levels by the day +60 were 2.57 cells/μL (1.49-4.99 cells/μL) after classic immunosuppressive regimen; 0.12 cells/μL (0.02-0.15 cells/μL), after Т-cell depletion; 1.1 cells/μL (0.72-2.8 cells/μL) after PT-Cy (p=0.009). On the day +90 these parameters were 4.29 cells/ μL (2.08-6.58 cells/μL) after classic immunosuppressive regimen; 1.82 cells/μL (0.16-3.3 cells/μL) after PT-Cy; and 0.35 cells/μL (0.01-0.7 cells/μL) after Т-cell depletion (p=0.035). On day +30 and +60, absolute numbers of CD8+ Tcm were significant lower after alternative approaches, when compared to classical immunosuppressive regimen, i.e., on day +30, 1.07 cells/μL (0.27-1.75 cells/μL) after classical regimen; 0.25 cells/μL (0.12-0.68 cells/μL) after PT-Cy (р=0.032); 0.18 cells/μL (0.01-0.34 cells/μL) after Т-cells depletion (р=0.036); on day +60, 0.9 cells/μL (0.65-1.68 cells/μL); 0.42 cells/μL (0.33-0.73 cells/μL); 0.05 cells/μL (0.01-0.07 cells/μL), respectively (р=0.02). Absolute number of CD4+ Tnv+Tscm on day +30 was significantly higher after classic immunosuppressiveregimen, i.e. 16.1 cells/μL (2.1-55.0 cells/μL), as compared to PT-Cy – 1.35 cells/μL (0.7-5.36 cells/μL), and Т cell depletion – 0.31 cells/μL (0.27-0.71 cells/μL) (р=0.05). Absolute number of Тtm CD8+ on days +60, +90 and CD4+ on day +30 were different in alternative aGVHD prophylaxis and in control group (Fig. 1). We didn’t find any correlations between absolute numbers of Tnv+Tscm, Tcm, Ttm, Tem, Tte and aGVHD onset, or leukemia relapse after allo-HSCT.
Conclusion
Tnv+Tscm is the progenitor subset for all memory and effector T-cells and its prompt recovery after allo-HSCT seems to be crucial for graft-versus-leukemia effect. Here we show the lowest number of CD4+/CD8+ Tnv+Tscm, CD8+ Tcm after alternative approaches of aGVHD prophylaxis that might reflect sever immunoablation in mismatched or haplo-HSCT. To this point, low numbers of Tnv+Tscm on day +60, +90 as progenitor cells for the whole T-memory pool may lead to delayed reconstitution of adaptive immunity after alternative aGVHD prophylaxis in patients after allo-HSCT.
Disclosures
No relevant conflicts of interest to declare.
Keywords
Memory T cells, immune reconstitution, allogeneic stem cell transplantation, GVHD prophylaxis regimens.
Table 1. Characteristics of the patients


Figure 1. Recovery of T-memory cell subsets in terms of different GVHD prophylaxis in leukemia patients after allo-HSCT
Significant differences (p<0.005) between the number of different T-memory cell subsets in terms of alternative GVHD prophylaxis – PT-Cy or T-cells depletion comparing to classic immunosuppressive regimen are presented in the graph.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20619" ["VALUE"]=> string(173) "Recovery of memory T cells after alternative prophylaxis regimens of acute graft-versus-host disease (aGVHD) in leukemia patients after allogeneic stem cells transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(173) "Recovery of memory T cells after alternative prophylaxis regimens of acute graft-versus-host disease (aGVHD) in leukemia patients after allogeneic stem cells transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(173) "Recovery of memory T cells after alternative prophylaxis regimens of acute graft-versus-host disease (aGVHD) in leukemia patients after allogeneic stem cells transplantation" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20617" ["VALUE"]=> array(2) { ["TEXT"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(67) "National Research Center for Hematology, Moscow, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20613" ["VALUE"]=> array(2) { ["TEXT"]=> string(575) "Наталья Н. Попова, Михаил Ю. Дроков, Елена Н. Паровичникова, Лариса А. Кузьмина, Юлия О. Давыдова, Николай М. Капранов, Екатерина Д. Михальцова, Ольга М. Королева, Вера А. Васильева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Ирина В. Гальцева, Михаил А. Масчан, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(575) "Наталья Н. Попова, Михаил Ю. Дроков, Елена Н. Паровичникова, Лариса А. Кузьмина, Юлия О. Давыдова, Николай М. Капранов, Екатерина Д. Михальцова, Ольга М. Королева, Вера А. Васильева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Ирина В. Гальцева, Михаил А. Масчан, Валерий Г. Савченко" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(575) "Наталья Н. Попова, Михаил Ю. Дроков, Елена Н. Паровичникова, Лариса А. Кузьмина, Юлия О. Давыдова, Николай М. Капранов, Екатерина Д. Михальцова, Ольга М. Королева, Вера А. Васильева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Ирина В. Гальцева, Михаил А. Масчан, Валерий Г. Савченко" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20615" ["VALUE"]=> array(2) { ["TEXT"]=> string(10898) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Т-клетки памяти представляют собой гетерогенную субпопуляцию иммунных клеток, участвующих в развитии аллоиммунных реакций после алло-ТГСК – реакции трансплантат против опухоли (РТПО) и РТПХ. В настоящее время созданы новые программы иммуносупрессивной терапии, но единого унифицированного подхода профилактики острой РТПХ не существует. Необходимость проведения иммуносупрессии, особенно при несовместимых/гаплоидентичных алло-ТГСК, когда требуется максимальная иммуноаблация, позволяет контролировать развитие/течение РТПХ. Однако необходимость своевременной реконституции иммунной системы является ключевым фактором для реализации противоопухолевого контроля. Цель работы состояла в оценке влияния различных схем профилактики острой РТПХ на восстановление субпопуляций Т-клеток памяти и их предшественников у больных острыми лейкозами после алло-ТГСК. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В исследование включены 39 пациентов с острыми лейкозами, которым была выполнена алло-ТГСК в ФГБУ «НМИЦ гематологии» Минздрава РФ. Медиана возраста составила 36 лет (17-60 лет). Альтернативные программы профилактики острой РТПХ использовали при несовместимых/гаплоидентичных алло-ТГСК (n=17), которые включали в себя посттрансплантационный циклофосфамид (ПТ-ЦФ) на +3, +4 день или Тαβ-деплецию у молодых пациентов. В контрольную группу мы включили пациентов с классическим режимом иммуносупрессии (классическая ИСТ) с использованием циклоспорина А в сочетании с микофенолатом мофетилом и малыми дозами метотрексата, применяемых после совместимой родственной/неродственной алло-ТГСК (n=22). Характеристика больных, включенных в исследование, схемы профилактики РТПХ, частота развития острой РТПХ и рецидивов заболевания приведена в таблице 1. </p> <h2>Таблица 1. Характеристика пациентов</h2> <img width="783" alt="38_таблица.png" src="/upload/medialibrary/d46/38_tablitsa.png" height="467" title="38_таблица.png"><br> <img width="767" alt="38_рисунок 1.png" src="/upload/medialibrary/1ab/38_risunok-1.png" height="704" title="38_рисунок 1.png"><br> <h2>Рисунок 1. Восстановление субпопуляций Т-клеток памяти у больных острыми лейкозами после алло-ТГСК</h2> <p style="text-align: justify;"> Примечание. На графике показаны значимые отличия (p<0,005) по количеству клеток в субпопуляциях CD4+/CD8+ Т-клеток памяти при использовании альтернативных режимов профилактики оРТПХ – ПТ-ЦФ или Т-деплеции, в сравнении с классической ИСТ. </p> <p style="text-align: justify;"> Для исследования реконституции субпопуляций Т-клеток памяти использовали нативные образцы перифе-рической крови больных после алло-ТГСК на +30, +60, +90 день. С помощью метода многоцветной проточной цитометрии (BD FACS Canto II, Becton Dickinson, USA) были определены следующие субпопуляции Т-клеток памяти периферической крови: Т-наивные и стволовые клетки памяти (Tnv+Tscm) – CD8+/СD4+ CD45R0-CCR7+CD28+; T-клетки центральной памяти (Tcm) – CD8+/СD4+ CD45R0+CCR7+CD28+; T-клетки тран-зиторной памяти (Ttm) – CD8+/СD4+ CD45R0+CCR7-CD28+; T-клетки эффекторной памяти (Tem) – CD8+/СD4+ CD45R0+CCR7-CD28-; T- терминальные эффек-торы (Tte) – CD8+/СD4+ CD45R0-CCR7-CD28-. Для оценки различий между двумя независимыми выборками использовали U-критерий Манна-Уитни. Значениер<0,05 считали статистически значимым. Весь анализ данных проводили с использованием SPSS ver 23. (IBM, Chicago,Ill., USA). </p> <h2 style="text-align: justify;"> Результаты </h2> <p style="text-align: justify;"> Данные представлены на рисунке 1. Показано, что на +30, +60, +90 день абсолютное количество CD8+ Tnv+Tscm после классической ИСТ было значимо больше, чем после использования ПТ-ЦФ или Тαβ-деплеции. На +30 день абсолютное количество CD8+ Tnv+Tscm после использования классической схемы профилактики РТПХ составило 4,22 кл/мкл (1,21-7,0кл кл/мкл), после ПТ-ЦФ – 0,38 кл/мкл (0,17-0,63 кл/мкл) (p=0,001), после Т-деплеции – 0,14 кл/мкл (0,05-0,15 кл/мкл) (р=0,03). На +60 день – 2,57 кл/мкл (1,49-4,99 кл/мкл) после классической ИСТ; 0,12 кл/мкл (0,02-0,15 кл/мкл) после Т-деплеции; 1,1 кл/мкл (0,72-2,8 кл/мкл) после ПТ-ЦФ (p=0,009). На +90 день – 4,29 кл/мкл (2,08-6,58 кл/мкл) после классического режима; 1,82 кл/мкл (0,16-3,3 кл/мкл) после ПТ-ЦФ; 0,35 кл/мкл (0,01-0,7 кл/мкл) после Т-деплеции (p=0,035). На +30, +60 день абсолютное количество CD8+ Tcm было значимо меньше после использования альтернативных подходов в сравнении с классической ИСТ – на +30 день 1,07 кл/мкл (0,27-1,75 кл/мкл) после классической ИСТ, 0,25 кл/мкл (0,12-0,68 кл/мкл) после ПТ-ЦФ (р=0,032), 0,18 кл/мкл (0,01-0,34 кл/мкл) после Т-деплеции (р=0,036); на +60 день 0,9 кл/мкл (0,65-1,68 кл/мкл), 0,42 кл/мкл (0,33-0,73 кл/мкл), 0,05 кл/мкл (0,01-0,07 кл/мкл) соответственно (р=0,02). Абсолютное количество CD4+ Tnv+Tscm на +30 день было значимо больше после применения классической схемы профилактики РТПХ – 16,1 кл/мкл (2,1-55,0 кл/мкл), в сравнении с использованием ПТ-ЦФ – 1,35 кл/мкл (0,7-5,36 кл/мкл) и Т-деплеции – 0,31 кл/мкл (0,27-0,71 кл/мкл) (р=0,05). Субпопуляция Тtm CD8+ на +60, +90 дни и CD4+ на +30 день отличалась при использовании классической ИСТ и альтернативных режимов (Рисунок 1). Мы не выявили корреляции между числом Tnv+Tscm, Tcm, Ttm, Tem, Tte и развитием оРТПХ или рецидива заболевания. </p> <h2 style="text-align: justify;"> Заключение </h2> <p style="text-align: justify;"> Субпопуляция наивных и стволовых Т-клеток памяти является пулом клеток-предшественников для целого эффекторного звена Т-клеток (Ttm, Tem, Tte), реализующего аллоиммунный ответ. Значимое уменьшение пула CD4+/CD8+ Tnv+Tscm, CD8+ Tcm после использования альтернативных схем профилактики острой РТПХ может свидетельствовать о более глубокой иммуноаблации при этих режимах, используемых при несовместимых/гапло-ТГСК. За счет этого сохраняющееся низкое количество Tnv+Tscm на +60, +90 день, как клеток-предшественников для целой популяции Т-клеток памяти, может свидетельствовать об отсроченной реконституции адаптивного звена иммунного ответа при альтернативных режимах профилактики оРТПХ. </p> <h2 style="text-align: justify;"> Ключевые слова </h2> <p style="text-align: justify;"> Т-клетки памяти, реконституция иммунной системы, трансплантация аллогенных гемопоэтических стволовых клеток, профилактика острой РТПХ. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(10466) "Введение
Т-клетки памяти представляют собой гетерогенную субпопуляцию иммунных клеток, участвующих в развитии аллоиммунных реакций после алло-ТГСК – реакции трансплантат против опухоли (РТПО) и РТПХ. В настоящее время созданы новые программы иммуносупрессивной терапии, но единого унифицированного подхода профилактики острой РТПХ не существует. Необходимость проведения иммуносупрессии, особенно при несовместимых/гаплоидентичных алло-ТГСК, когда требуется максимальная иммуноаблация, позволяет контролировать развитие/течение РТПХ. Однако необходимость своевременной реконституции иммунной системы является ключевым фактором для реализации противоопухолевого контроля. Цель работы состояла в оценке влияния различных схем профилактики острой РТПХ на восстановление субпопуляций Т-клеток памяти и их предшественников у больных острыми лейкозами после алло-ТГСК.
Материалы и методы
В исследование включены 39 пациентов с острыми лейкозами, которым была выполнена алло-ТГСК в ФГБУ «НМИЦ гематологии» Минздрава РФ. Медиана возраста составила 36 лет (17-60 лет). Альтернативные программы профилактики острой РТПХ использовали при несовместимых/гаплоидентичных алло-ТГСК (n=17), которые включали в себя посттрансплантационный циклофосфамид (ПТ-ЦФ) на +3, +4 день или Тαβ-деплецию у молодых пациентов. В контрольную группу мы включили пациентов с классическим режимом иммуносупрессии (классическая ИСТ) с использованием циклоспорина А в сочетании с микофенолатом мофетилом и малыми дозами метотрексата, применяемых после совместимой родственной/неродственной алло-ТГСК (n=22). Характеристика больных, включенных в исследование, схемы профилактики РТПХ, частота развития острой РТПХ и рецидивов заболевания приведена в таблице 1.
Таблица 1. Характеристика пациентов


Рисунок 1. Восстановление субпопуляций Т-клеток памяти у больных острыми лейкозами после алло-ТГСК
Примечание. На графике показаны значимые отличия (p<0,005) по количеству клеток в субпопуляциях CD4+/CD8+ Т-клеток памяти при использовании альтернативных режимов профилактики оРТПХ – ПТ-ЦФ или Т-деплеции, в сравнении с классической ИСТ.
Для исследования реконституции субпопуляций Т-клеток памяти использовали нативные образцы перифе-рической крови больных после алло-ТГСК на +30, +60, +90 день. С помощью метода многоцветной проточной цитометрии (BD FACS Canto II, Becton Dickinson, USA) были определены следующие субпопуляции Т-клеток памяти периферической крови: Т-наивные и стволовые клетки памяти (Tnv+Tscm) – CD8+/СD4+ CD45R0-CCR7+CD28+; T-клетки центральной памяти (Tcm) – CD8+/СD4+ CD45R0+CCR7+CD28+; T-клетки тран-зиторной памяти (Ttm) – CD8+/СD4+ CD45R0+CCR7-CD28+; T-клетки эффекторной памяти (Tem) – CD8+/СD4+ CD45R0+CCR7-CD28-; T- терминальные эффек-торы (Tte) – CD8+/СD4+ CD45R0-CCR7-CD28-. Для оценки различий между двумя независимыми выборками использовали U-критерий Манна-Уитни. Значениер<0,05 считали статистически значимым. Весь анализ данных проводили с использованием SPSS ver 23. (IBM, Chicago,Ill., USA).
Результаты
Данные представлены на рисунке 1. Показано, что на +30, +60, +90 день абсолютное количество CD8+ Tnv+Tscm после классической ИСТ было значимо больше, чем после использования ПТ-ЦФ или Тαβ-деплеции. На +30 день абсолютное количество CD8+ Tnv+Tscm после использования классической схемы профилактики РТПХ составило 4,22 кл/мкл (1,21-7,0кл кл/мкл), после ПТ-ЦФ – 0,38 кл/мкл (0,17-0,63 кл/мкл) (p=0,001), после Т-деплеции – 0,14 кл/мкл (0,05-0,15 кл/мкл) (р=0,03). На +60 день – 2,57 кл/мкл (1,49-4,99 кл/мкл) после классической ИСТ; 0,12 кл/мкл (0,02-0,15 кл/мкл) после Т-деплеции; 1,1 кл/мкл (0,72-2,8 кл/мкл) после ПТ-ЦФ (p=0,009). На +90 день – 4,29 кл/мкл (2,08-6,58 кл/мкл) после классического режима; 1,82 кл/мкл (0,16-3,3 кл/мкл) после ПТ-ЦФ; 0,35 кл/мкл (0,01-0,7 кл/мкл) после Т-деплеции (p=0,035). На +30, +60 день абсолютное количество CD8+ Tcm было значимо меньше после использования альтернативных подходов в сравнении с классической ИСТ – на +30 день 1,07 кл/мкл (0,27-1,75 кл/мкл) после классической ИСТ, 0,25 кл/мкл (0,12-0,68 кл/мкл) после ПТ-ЦФ (р=0,032), 0,18 кл/мкл (0,01-0,34 кл/мкл) после Т-деплеции (р=0,036); на +60 день 0,9 кл/мкл (0,65-1,68 кл/мкл), 0,42 кл/мкл (0,33-0,73 кл/мкл), 0,05 кл/мкл (0,01-0,07 кл/мкл) соответственно (р=0,02). Абсолютное количество CD4+ Tnv+Tscm на +30 день было значимо больше после применения классической схемы профилактики РТПХ – 16,1 кл/мкл (2,1-55,0 кл/мкл), в сравнении с использованием ПТ-ЦФ – 1,35 кл/мкл (0,7-5,36 кл/мкл) и Т-деплеции – 0,31 кл/мкл (0,27-0,71 кл/мкл) (р=0,05). Субпопуляция Тtm CD8+ на +60, +90 дни и CD4+ на +30 день отличалась при использовании классической ИСТ и альтернативных режимов (Рисунок 1). Мы не выявили корреляции между числом Tnv+Tscm, Tcm, Ttm, Tem, Tte и развитием оРТПХ или рецидива заболевания.
Заключение
Субпопуляция наивных и стволовых Т-клеток памяти является пулом клеток-предшественников для целого эффекторного звена Т-клеток (Ttm, Tem, Tte), реализующего аллоиммунный ответ. Значимое уменьшение пула CD4+/CD8+ Tnv+Tscm, CD8+ Tcm после использования альтернативных схем профилактики острой РТПХ может свидетельствовать о более глубокой иммуноаблации при этих режимах, используемых при несовместимых/гапло-ТГСК. За счет этого сохраняющееся низкое количество Tnv+Tscm на +60, +90 день, как клеток-предшественников для целой популяции Т-клеток памяти, может свидетельствовать об отсроченной реконституции адаптивного звена иммунного ответа при альтернативных режимах профилактики оРТПХ.
Ключевые слова
Т-клетки памяти, реконституция иммунной системы, трансплантация аллогенных гемопоэтических стволовых клеток, профилактика острой РТПХ.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(10466) "Введение
Т-клетки памяти представляют собой гетерогенную субпопуляцию иммунных клеток, участвующих в развитии аллоиммунных реакций после алло-ТГСК – реакции трансплантат против опухоли (РТПО) и РТПХ. В настоящее время созданы новые программы иммуносупрессивной терапии, но единого унифицированного подхода профилактики острой РТПХ не существует. Необходимость проведения иммуносупрессии, особенно при несовместимых/гаплоидентичных алло-ТГСК, когда требуется максимальная иммуноаблация, позволяет контролировать развитие/течение РТПХ. Однако необходимость своевременной реконституции иммунной системы является ключевым фактором для реализации противоопухолевого контроля. Цель работы состояла в оценке влияния различных схем профилактики острой РТПХ на восстановление субпопуляций Т-клеток памяти и их предшественников у больных острыми лейкозами после алло-ТГСК.
Материалы и методы
В исследование включены 39 пациентов с острыми лейкозами, которым была выполнена алло-ТГСК в ФГБУ «НМИЦ гематологии» Минздрава РФ. Медиана возраста составила 36 лет (17-60 лет). Альтернативные программы профилактики острой РТПХ использовали при несовместимых/гаплоидентичных алло-ТГСК (n=17), которые включали в себя посттрансплантационный циклофосфамид (ПТ-ЦФ) на +3, +4 день или Тαβ-деплецию у молодых пациентов. В контрольную группу мы включили пациентов с классическим режимом иммуносупрессии (классическая ИСТ) с использованием циклоспорина А в сочетании с микофенолатом мофетилом и малыми дозами метотрексата, применяемых после совместимой родственной/неродственной алло-ТГСК (n=22). Характеристика больных, включенных в исследование, схемы профилактики РТПХ, частота развития острой РТПХ и рецидивов заболевания приведена в таблице 1.
Таблица 1. Характеристика пациентов


Рисунок 1. Восстановление субпопуляций Т-клеток памяти у больных острыми лейкозами после алло-ТГСК
Примечание. На графике показаны значимые отличия (p<0,005) по количеству клеток в субпопуляциях CD4+/CD8+ Т-клеток памяти при использовании альтернативных режимов профилактики оРТПХ – ПТ-ЦФ или Т-деплеции, в сравнении с классической ИСТ.
Для исследования реконституции субпопуляций Т-клеток памяти использовали нативные образцы перифе-рической крови больных после алло-ТГСК на +30, +60, +90 день. С помощью метода многоцветной проточной цитометрии (BD FACS Canto II, Becton Dickinson, USA) были определены следующие субпопуляции Т-клеток памяти периферической крови: Т-наивные и стволовые клетки памяти (Tnv+Tscm) – CD8+/СD4+ CD45R0-CCR7+CD28+; T-клетки центральной памяти (Tcm) – CD8+/СD4+ CD45R0+CCR7+CD28+; T-клетки тран-зиторной памяти (Ttm) – CD8+/СD4+ CD45R0+CCR7-CD28+; T-клетки эффекторной памяти (Tem) – CD8+/СD4+ CD45R0+CCR7-CD28-; T- терминальные эффек-торы (Tte) – CD8+/СD4+ CD45R0-CCR7-CD28-. Для оценки различий между двумя независимыми выборками использовали U-критерий Манна-Уитни. Значениер<0,05 считали статистически значимым. Весь анализ данных проводили с использованием SPSS ver 23. (IBM, Chicago,Ill., USA).
Результаты
Данные представлены на рисунке 1. Показано, что на +30, +60, +90 день абсолютное количество CD8+ Tnv+Tscm после классической ИСТ было значимо больше, чем после использования ПТ-ЦФ или Тαβ-деплеции. На +30 день абсолютное количество CD8+ Tnv+Tscm после использования классической схемы профилактики РТПХ составило 4,22 кл/мкл (1,21-7,0кл кл/мкл), после ПТ-ЦФ – 0,38 кл/мкл (0,17-0,63 кл/мкл) (p=0,001), после Т-деплеции – 0,14 кл/мкл (0,05-0,15 кл/мкл) (р=0,03). На +60 день – 2,57 кл/мкл (1,49-4,99 кл/мкл) после классической ИСТ; 0,12 кл/мкл (0,02-0,15 кл/мкл) после Т-деплеции; 1,1 кл/мкл (0,72-2,8 кл/мкл) после ПТ-ЦФ (p=0,009). На +90 день – 4,29 кл/мкл (2,08-6,58 кл/мкл) после классического режима; 1,82 кл/мкл (0,16-3,3 кл/мкл) после ПТ-ЦФ; 0,35 кл/мкл (0,01-0,7 кл/мкл) после Т-деплеции (p=0,035). На +30, +60 день абсолютное количество CD8+ Tcm было значимо меньше после использования альтернативных подходов в сравнении с классической ИСТ – на +30 день 1,07 кл/мкл (0,27-1,75 кл/мкл) после классической ИСТ, 0,25 кл/мкл (0,12-0,68 кл/мкл) после ПТ-ЦФ (р=0,032), 0,18 кл/мкл (0,01-0,34 кл/мкл) после Т-деплеции (р=0,036); на +60 день 0,9 кл/мкл (0,65-1,68 кл/мкл), 0,42 кл/мкл (0,33-0,73 кл/мкл), 0,05 кл/мкл (0,01-0,07 кл/мкл) соответственно (р=0,02). Абсолютное количество CD4+ Tnv+Tscm на +30 день было значимо больше после применения классической схемы профилактики РТПХ – 16,1 кл/мкл (2,1-55,0 кл/мкл), в сравнении с использованием ПТ-ЦФ – 1,35 кл/мкл (0,7-5,36 кл/мкл) и Т-деплеции – 0,31 кл/мкл (0,27-0,71 кл/мкл) (р=0,05). Субпопуляция Тtm CD8+ на +60, +90 дни и CD4+ на +30 день отличалась при использовании классической ИСТ и альтернативных режимов (Рисунок 1). Мы не выявили корреляции между числом Tnv+Tscm, Tcm, Ttm, Tem, Tte и развитием оРТПХ или рецидива заболевания.
Заключение
Субпопуляция наивных и стволовых Т-клеток памяти является пулом клеток-предшественников для целого эффекторного звена Т-клеток (Ttm, Tem, Tte), реализующего аллоиммунный ответ. Значимое уменьшение пула CD4+/CD8+ Tnv+Tscm, CD8+ Tcm после использования альтернативных схем профилактики острой РТПХ может свидетельствовать о более глубокой иммуноаблации при этих режимах, используемых при несовместимых/гапло-ТГСК. За счет этого сохраняющееся низкое количество Tnv+Tscm на +60, +90 день, как клеток-предшественников для целой популяции Т-клеток памяти, может свидетельствовать об отсроченной реконституции адаптивного звена иммунного ответа при альтернативных режимах профилактики оРТПХ.
Ключевые слова
Т-клетки памяти, реконституция иммунной системы, трансплантация аллогенных гемопоэтических стволовых клеток, профилактика острой РТПХ.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20614" ["VALUE"]=> array(2) { ["TEXT"]=> string(86) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(86) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(86) "ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва" } } } [51]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1586" ["~ID"]=> string(4) "1586" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(183) "Оценка комплаентности родителей госпитализированных детей в ведении дневников интенсивности боли" ["~NAME"]=> string(183) "Оценка комплаентности родителей госпитализированных детей в ведении дневников интенсивности боли" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:40:26" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:40:26" ["DETAIL_PAGE_URL"]=> string(148) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/otsenka-komplaentnosti-roditeley-gospitalizirovannykh-detey-v-vedenii-dnevnikov-intensivnosti-boli/" ["~DETAIL_PAGE_URL"]=> string(148) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/otsenka-komplaentnosti-roditeley-gospitalizirovannykh-detey-v-vedenii-dnevnikov-intensivnosti-boli/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(98) "otsenka-komplaentnosti-roditeley-gospitalizirovannykh-detey-v-vedenii-dnevnikov-intensivnosti-boli" ["~CODE"]=> string(98) "otsenka-komplaentnosti-roditeley-gospitalizirovannykh-detey-v-vedenii-dnevnikov-intensivnosti-boli" ["EXTERNAL_ID"]=> string(4) "1586" ["~EXTERNAL_ID"]=> string(4) "1586" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(183) "Оценка комплаентности родителей госпитализированных детей в ведении дневников интенсивности боли" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(271) "Оценка комплаентности родителей госпитализированных детей в ведении дневников интенсивности болиCompliance evaluation in the parents of inpatients by keeping the pain intensity diaries" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(4477) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Дневники и опросники, заполняемые пациентами или сопровождающими их лицами, могут служить эффективным методом наблюдения за динамикой состояния амбулаторных и стационарных пациентов. При оценке интенсивности боли предпочтительным является сбор данных в режиме реального времени, нежели опрос о событиях за прошедшие сутки, т.к. на последний вид сбора данных может влиять множество факторов (например,стабильность интенсивности боли, изменения эмоциональной окраски и порядка событий при восстановлении их по памяти). Но на практике медперсонал нередко сталкивается с пробелами в заполнении дневников, что связано с различными причинами. Поэтому, в своем исследовании мы решили оценить комплаентность родителей в ведении дневников интенсивности боли у госпитализированных пациентов детского возраста. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> 64 пациентам (от 2,4 до 17 лет включительно), получающим анальгетики, и их родителям вместе с карточками с изображением шкалы лиц Вонга-Бэйкера и визуальной аналоговой шкалы, были выданы для заполнения бумажные дневники оценки интенсивности базовой и прорывной болей каждые 6 часов на протяжении всего периода потребности в анальгезии. Среднее время наблюдения составило около 8 суток. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Общая комплаентность составила 72%. Степень заполнения дневников позволила разделить всех пациентов на 4 группы. В группу 0-25% заполнения вошло 25 пациентов, средний возраст которых составил 7,5 лет. У 9 пациентов было внесено 26-50% данных, а средний возраст детей составил 9,5 лет (медиана 7). 51-75% результатов было получено от родителей 6 детей среднего возраста 9 лет (медиана 10). В группу 76-100% вошли дневники 33 детей среднего возраста 10 лет (медиана 9). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Полученные результаты могут свидетельствовать о том, что возраст пациентов может ассоциироваться с комплаентностью родителей в ведении дневников интенсивности боли. Возможно, это связанно с коммуникативными способностями детей разных возрастов. Для подтверждения этого предположения требуются дальнейшие исследования. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Оценка интенсивности боли, дневник наблюдения, педиатрия, аналгезия. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(183) "Оценка комплаентности родителей госпитализированных детей в ведении дневников интенсивности боли" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(183) "Оценка комплаентности родителей госпитализированных детей в ведении дневников интенсивности боли" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(183) "Оценка комплаентности родителей госпитализированных детей в ведении дневников интенсивности боли" ["SECTION_META_TITLE"]=> string(183) "Оценка комплаентности родителей госпитализированных детей в ведении дневников интенсивности боли" ["SECTION_META_KEYWORDS"]=> string(183) "Оценка комплаентности родителей госпитализированных детей в ведении дневников интенсивности боли" ["SECTION_META_DESCRIPTION"]=> string(183) "Оценка комплаентности родителей госпитализированных детей в ведении дневников интенсивности боли" ["SECTION_PICTURE_FILE_ALT"]=> string(183) "Оценка комплаентности родителей госпитализированных детей в ведении дневников интенсивности боли" ["SECTION_PICTURE_FILE_TITLE"]=> string(183) "Оценка комплаентности родителей госпитализированных детей в ведении дневников интенсивности боли" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "otsenka-komplaentnosti-roditeley-gospitalizirovannykh-detey-v-vedenii-dnevnikov-intensivnosti-boli-i" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(183) "Оценка комплаентности родителей госпитализированных детей в ведении дневников интенсивности боли" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(183) "Оценка комплаентности родителей госпитализированных детей в ведении дневников интенсивности боли" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "otsenka-komplaentnosti-roditeley-gospitalizirovannykh-detey-v-vedenii-dnevnikov-intensivnosti-boli-i" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "otsenka-komplaentnosti-roditeley-gospitalizirovannykh-detey-v-vedenii-dnevnikov-intensivnosti-boli-i" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "otsenka-komplaentnosti-roditeley-gospitalizirovannykh-detey-v-vedenii-dnevnikov-intensivnosti-boli-i" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20606" ["VALUE"]=> array(2) { ["TEXT"]=> string(395) "Юлия В. Опарина <sup>1</sup>, Екатерина В. Гончарова <sup>1</sup>,<sup>2</sup>, Ольга А. Иванова <sup>1</sup>, Максим П. Богомольный <sup>1</sup>, Людмила С. Зубаровская <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(311) "Юлия В. Опарина 1, Екатерина В. Гончарова 1,2, Ольга А. Иванова 1, Максим П. Богомольный 1, Людмила С. Зубаровская 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20607" ["VALUE"]=> array(2) { ["TEXT"]=> string(674) "<sup>1</sup> Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург<br> <sup>2</sup> Лаборатория клинической фармакологии и терапии боли отдела нейрофармакологии Института фармакологии им. А. В. Вальдмана, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(638) "1 Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург2 Лаборатория клинической фармакологии и терапии боли отдела нейрофармакологии Института фармакологии им. А. В. Вальдмана, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20608" ["VALUE"]=> array(2) { ["TEXT"]=> string(4477) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Дневники и опросники, заполняемые пациентами или сопровождающими их лицами, могут служить эффективным методом наблюдения за динамикой состояния амбулаторных и стационарных пациентов. При оценке интенсивности боли предпочтительным является сбор данных в режиме реального времени, нежели опрос о событиях за прошедшие сутки, т.к. на последний вид сбора данных может влиять множество факторов (например,стабильность интенсивности боли, изменения эмоциональной окраски и порядка событий при восстановлении их по памяти). Но на практике медперсонал нередко сталкивается с пробелами в заполнении дневников, что связано с различными причинами. Поэтому, в своем исследовании мы решили оценить комплаентность родителей в ведении дневников интенсивности боли у госпитализированных пациентов детского возраста. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> 64 пациентам (от 2,4 до 17 лет включительно), получающим анальгетики, и их родителям вместе с карточками с изображением шкалы лиц Вонга-Бэйкера и визуальной аналоговой шкалы, были выданы для заполнения бумажные дневники оценки интенсивности базовой и прорывной болей каждые 6 часов на протяжении всего периода потребности в анальгезии. Среднее время наблюдения составило около 8 суток. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Общая комплаентность составила 72%. Степень заполнения дневников позволила разделить всех пациентов на 4 группы. В группу 0-25% заполнения вошло 25 пациентов, средний возраст которых составил 7,5 лет. У 9 пациентов было внесено 26-50% данных, а средний возраст детей составил 9,5 лет (медиана 7). 51-75% результатов было получено от родителей 6 детей среднего возраста 9 лет (медиана 10). В группу 76-100% вошли дневники 33 детей среднего возраста 10 лет (медиана 9). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Полученные результаты могут свидетельствовать о том, что возраст пациентов может ассоциироваться с комплаентностью родителей в ведении дневников интенсивности боли. Возможно, это связанно с коммуникативными способностями детей разных возрастов. Для подтверждения этого предположения требуются дальнейшие исследования. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Оценка интенсивности боли, дневник наблюдения, педиатрия, аналгезия. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4245) "
Введение
Дневники и опросники, заполняемые пациентами или сопровождающими их лицами, могут служить эффективным методом наблюдения за динамикой состояния амбулаторных и стационарных пациентов. При оценке интенсивности боли предпочтительным является сбор данных в режиме реального времени, нежели опрос о событиях за прошедшие сутки, т.к. на последний вид сбора данных может влиять множество факторов (например,стабильность интенсивности боли, изменения эмоциональной окраски и порядка событий при восстановлении их по памяти). Но на практике медперсонал нередко сталкивается с пробелами в заполнении дневников, что связано с различными причинами. Поэтому, в своем исследовании мы решили оценить комплаентность родителей в ведении дневников интенсивности боли у госпитализированных пациентов детского возраста.
Пациенты и методы
64 пациентам (от 2,4 до 17 лет включительно), получающим анальгетики, и их родителям вместе с карточками с изображением шкалы лиц Вонга-Бэйкера и визуальной аналоговой шкалы, были выданы для заполнения бумажные дневники оценки интенсивности базовой и прорывной болей каждые 6 часов на протяжении всего периода потребности в анальгезии. Среднее время наблюдения составило около 8 суток.
Результаты
Общая комплаентность составила 72%. Степень заполнения дневников позволила разделить всех пациентов на 4 группы. В группу 0-25% заполнения вошло 25 пациентов, средний возраст которых составил 7,5 лет. У 9 пациентов было внесено 26-50% данных, а средний возраст детей составил 9,5 лет (медиана 7). 51-75% результатов было получено от родителей 6 детей среднего возраста 9 лет (медиана 10). В группу 76-100% вошли дневники 33 детей среднего возраста 10 лет (медиана 9).
Выводы
Полученные результаты могут свидетельствовать о том, что возраст пациентов может ассоциироваться с комплаентностью родителей в ведении дневников интенсивности боли. Возможно, это связанно с коммуникативными способностями детей разных возрастов. Для подтверждения этого предположения требуются дальнейшие исследования.
Ключевые слова
Оценка интенсивности боли, дневник наблюдения, педиатрия, аналгезия.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20609" ["VALUE"]=> array(2) { ["TEXT"]=> string(298) "Julia V. Oparina <sup>1</sup>, Ekaterina V. Goncharova <sup>1</sup>,<sup>2</sup>, Olga A. Ivanova <sup>1</sup>, Maxim P. Bogomolny <sup>1</sup>, Ludmila S. Zubarovskaya <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(214) "Julia V. Oparina 1, Ekaterina V. Goncharova 1,2, Olga A. Ivanova 1, Maxim P. Bogomolny 1, Ludmila S. Zubarovskaya 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20610" ["VALUE"]=> array(2) { ["TEXT"]=> string(404) "<sup>1</sup> R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, I. P. Pavlov First Saint-Petersburg State Medical University, St. Petersburg, 197022, Russia<br> <sup>2</sup> Department of Neuropharmacology, Valdman Institute of Pharmacology I. P. Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(368) "1 R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, I. P. Pavlov First Saint-Petersburg State Medical University, St. Petersburg, 197022, Russia2 Department of Neuropharmacology, Valdman Institute of Pharmacology I. P. Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20611" ["VALUE"]=> array(2) { ["TEXT"]=> string(2369) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Self-filled diaries kept by a patient or caregiver are an effective method for clinical dynamics evaluation in both outpatient and inpatient settings. The real-time data collection is better for pain intensity monitoring than retrospective data analysis for each 24-hour period as the latter is biased by a number of factors such as variability in pain intensity or change in pain’s emotional perception when filling the questionnaire from memory. Due to this range of problems associated with the latter, we conducted a study aimed at diary keeping compliance in pediatric inpatients. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> A total of 64 pediatric patients aged 2.4 to 17 years supervised by pain management team were given cards with Wong-Baker face scale and visual analogue scale with additional diaries for baseline and breakthrough pain assessment. These diaries were filled in each 6 hours during the all analgesia period. The median follow-up period was 8 days. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Overall compliance rate was 72%. All the patients were divided into 4 groups according to diary-filling compliance degree. The 0-25% group consisted of 25 patients with median age of 7.5 years, the 26-50% group of 9 patients had median age of 7 years; the 51-75% group contained 6 children with median age of 10 years, and the group of 76-100% consisted of 33 children with median age of 9 years. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> The results obtained may indicate that an influence of patients’ age on his/her caregivers pain diary keeping compliance. This may be due to communicative abilities for children of different age. For more precise conclusions an additional research is required. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Pain intensity assessment, pain diary, pediatrics, analgesia. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2137) "
Introduction
Self-filled diaries kept by a patient or caregiver are an effective method for clinical dynamics evaluation in both outpatient and inpatient settings. The real-time data collection is better for pain intensity monitoring than retrospective data analysis for each 24-hour period as the latter is biased by a number of factors such as variability in pain intensity or change in pain’s emotional perception when filling the questionnaire from memory. Due to this range of problems associated with the latter, we conducted a study aimed at diary keeping compliance in pediatric inpatients.
Patients and methods
A total of 64 pediatric patients aged 2.4 to 17 years supervised by pain management team were given cards with Wong-Baker face scale and visual analogue scale with additional diaries for baseline and breakthrough pain assessment. These diaries were filled in each 6 hours during the all analgesia period. The median follow-up period was 8 days.
Results
Overall compliance rate was 72%. All the patients were divided into 4 groups according to diary-filling compliance degree. The 0-25% group consisted of 25 patients with median age of 7.5 years, the 26-50% group of 9 patients had median age of 7 years; the 51-75% group contained 6 children with median age of 10 years, and the group of 76-100% consisted of 33 children with median age of 9 years.
Conclusions
The results obtained may indicate that an influence of patients’ age on his/her caregivers pain diary keeping compliance. This may be due to communicative abilities for children of different age. For more precise conclusions an additional research is required.
Keywords
Pain intensity assessment, pain diary, pediatrics, analgesia.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20612" ["VALUE"]=> string(88) "Compliance evaluation in the parents of inpatients by keeping the pain intensity diaries" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(88) "Compliance evaluation in the parents of inpatients by keeping the pain intensity diaries" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20803" ["VALUE"]=> string(4) "1441" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1441" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20804" ["VALUE"]=> string(4) "1442" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1442" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20609" ["VALUE"]=> array(2) { ["TEXT"]=> string(298) "Julia V. Oparina <sup>1</sup>, Ekaterina V. Goncharova <sup>1</sup>,<sup>2</sup>, Olga A. Ivanova <sup>1</sup>, Maxim P. Bogomolny <sup>1</sup>, Ludmila S. Zubarovskaya <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(214) "Julia V. Oparina 1, Ekaterina V. Goncharova 1,2, Olga A. Ivanova 1, Maxim P. Bogomolny 1, Ludmila S. Zubarovskaya 1, Boris V. Afanasyev 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(214) "Julia V. Oparina 1, Ekaterina V. Goncharova 1,2, Olga A. Ivanova 1, Maxim P. Bogomolny 1, Ludmila S. Zubarovskaya 1, Boris V. Afanasyev 1" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20611" ["VALUE"]=> array(2) { ["TEXT"]=> string(2369) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Self-filled diaries kept by a patient or caregiver are an effective method for clinical dynamics evaluation in both outpatient and inpatient settings. The real-time data collection is better for pain intensity monitoring than retrospective data analysis for each 24-hour period as the latter is biased by a number of factors such as variability in pain intensity or change in pain’s emotional perception when filling the questionnaire from memory. Due to this range of problems associated with the latter, we conducted a study aimed at diary keeping compliance in pediatric inpatients. </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> A total of 64 pediatric patients aged 2.4 to 17 years supervised by pain management team were given cards with Wong-Baker face scale and visual analogue scale with additional diaries for baseline and breakthrough pain assessment. These diaries were filled in each 6 hours during the all analgesia period. The median follow-up period was 8 days. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Overall compliance rate was 72%. All the patients were divided into 4 groups according to diary-filling compliance degree. The 0-25% group consisted of 25 patients with median age of 7.5 years, the 26-50% group of 9 patients had median age of 7 years; the 51-75% group contained 6 children with median age of 10 years, and the group of 76-100% consisted of 33 children with median age of 9 years. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> The results obtained may indicate that an influence of patients’ age on his/her caregivers pain diary keeping compliance. This may be due to communicative abilities for children of different age. For more precise conclusions an additional research is required. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Pain intensity assessment, pain diary, pediatrics, analgesia. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(2137) "Introduction
Self-filled diaries kept by a patient or caregiver are an effective method for clinical dynamics evaluation in both outpatient and inpatient settings. The real-time data collection is better for pain intensity monitoring than retrospective data analysis for each 24-hour period as the latter is biased by a number of factors such as variability in pain intensity or change in pain’s emotional perception when filling the questionnaire from memory. Due to this range of problems associated with the latter, we conducted a study aimed at diary keeping compliance in pediatric inpatients.
Patients and methods
A total of 64 pediatric patients aged 2.4 to 17 years supervised by pain management team were given cards with Wong-Baker face scale and visual analogue scale with additional diaries for baseline and breakthrough pain assessment. These diaries were filled in each 6 hours during the all analgesia period. The median follow-up period was 8 days.
Results
Overall compliance rate was 72%. All the patients were divided into 4 groups according to diary-filling compliance degree. The 0-25% group consisted of 25 patients with median age of 7.5 years, the 26-50% group of 9 patients had median age of 7 years; the 51-75% group contained 6 children with median age of 10 years, and the group of 76-100% consisted of 33 children with median age of 9 years.
Conclusions
The results obtained may indicate that an influence of patients’ age on his/her caregivers pain diary keeping compliance. This may be due to communicative abilities for children of different age. For more precise conclusions an additional research is required.
Keywords
Pain intensity assessment, pain diary, pediatrics, analgesia.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(2137) "Introduction
Self-filled diaries kept by a patient or caregiver are an effective method for clinical dynamics evaluation in both outpatient and inpatient settings. The real-time data collection is better for pain intensity monitoring than retrospective data analysis for each 24-hour period as the latter is biased by a number of factors such as variability in pain intensity or change in pain’s emotional perception when filling the questionnaire from memory. Due to this range of problems associated with the latter, we conducted a study aimed at diary keeping compliance in pediatric inpatients.
Patients and methods
A total of 64 pediatric patients aged 2.4 to 17 years supervised by pain management team were given cards with Wong-Baker face scale and visual analogue scale with additional diaries for baseline and breakthrough pain assessment. These diaries were filled in each 6 hours during the all analgesia period. The median follow-up period was 8 days.
Results
Overall compliance rate was 72%. All the patients were divided into 4 groups according to diary-filling compliance degree. The 0-25% group consisted of 25 patients with median age of 7.5 years, the 26-50% group of 9 patients had median age of 7 years; the 51-75% group contained 6 children with median age of 10 years, and the group of 76-100% consisted of 33 children with median age of 9 years.
Conclusions
The results obtained may indicate that an influence of patients’ age on his/her caregivers pain diary keeping compliance. This may be due to communicative abilities for children of different age. For more precise conclusions an additional research is required.
Keywords
Pain intensity assessment, pain diary, pediatrics, analgesia.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20612" ["VALUE"]=> string(88) "Compliance evaluation in the parents of inpatients by keeping the pain intensity diaries" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(88) "Compliance evaluation in the parents of inpatients by keeping the pain intensity diaries" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(88) "Compliance evaluation in the parents of inpatients by keeping the pain intensity diaries" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20610" ["VALUE"]=> array(2) { ["TEXT"]=> string(404) "<sup>1</sup> R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, I. P. Pavlov First Saint-Petersburg State Medical University, St. Petersburg, 197022, Russia<br> <sup>2</sup> Department of Neuropharmacology, Valdman Institute of Pharmacology I. P. Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(368) "1 R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, I. P. Pavlov First Saint-Petersburg State Medical University, St. Petersburg, 197022, Russia2 Department of Neuropharmacology, Valdman Institute of Pharmacology I. P. Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(368) "1 R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, I. P. Pavlov First Saint-Petersburg State Medical University, St. Petersburg, 197022, Russia
2 Department of Neuropharmacology, Valdman Institute of Pharmacology I. P. Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20606" ["VALUE"]=> array(2) { ["TEXT"]=> string(395) "Юлия В. Опарина <sup>1</sup>, Екатерина В. Гончарова <sup>1</sup>,<sup>2</sup>, Ольга А. Иванова <sup>1</sup>, Максим П. Богомольный <sup>1</sup>, Людмила С. Зубаровская <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(311) "Юлия В. Опарина 1, Екатерина В. Гончарова 1,2, Ольга А. Иванова 1, Максим П. Богомольный 1, Людмила С. Зубаровская 1, Борис В. Афанасьев 1" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(311) "Юлия В. Опарина 1, Екатерина В. Гончарова 1,2, Ольга А. Иванова 1, Максим П. Богомольный 1, Людмила С. Зубаровская 1, Борис В. Афанасьев 1" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20608" ["VALUE"]=> array(2) { ["TEXT"]=> string(4477) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Дневники и опросники, заполняемые пациентами или сопровождающими их лицами, могут служить эффективным методом наблюдения за динамикой состояния амбулаторных и стационарных пациентов. При оценке интенсивности боли предпочтительным является сбор данных в режиме реального времени, нежели опрос о событиях за прошедшие сутки, т.к. на последний вид сбора данных может влиять множество факторов (например,стабильность интенсивности боли, изменения эмоциональной окраски и порядка событий при восстановлении их по памяти). Но на практике медперсонал нередко сталкивается с пробелами в заполнении дневников, что связано с различными причинами. Поэтому, в своем исследовании мы решили оценить комплаентность родителей в ведении дневников интенсивности боли у госпитализированных пациентов детского возраста. </p> <h2 style="text-align: justify;">Пациенты и методы</h2> <p style="text-align: justify;"> 64 пациентам (от 2,4 до 17 лет включительно), получающим анальгетики, и их родителям вместе с карточками с изображением шкалы лиц Вонга-Бэйкера и визуальной аналоговой шкалы, были выданы для заполнения бумажные дневники оценки интенсивности базовой и прорывной болей каждые 6 часов на протяжении всего периода потребности в анальгезии. Среднее время наблюдения составило около 8 суток. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Общая комплаентность составила 72%. Степень заполнения дневников позволила разделить всех пациентов на 4 группы. В группу 0-25% заполнения вошло 25 пациентов, средний возраст которых составил 7,5 лет. У 9 пациентов было внесено 26-50% данных, а средний возраст детей составил 9,5 лет (медиана 7). 51-75% результатов было получено от родителей 6 детей среднего возраста 9 лет (медиана 10). В группу 76-100% вошли дневники 33 детей среднего возраста 10 лет (медиана 9). </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Полученные результаты могут свидетельствовать о том, что возраст пациентов может ассоциироваться с комплаентностью родителей в ведении дневников интенсивности боли. Возможно, это связанно с коммуникативными способностями детей разных возрастов. Для подтверждения этого предположения требуются дальнейшие исследования. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Оценка интенсивности боли, дневник наблюдения, педиатрия, аналгезия. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(4245) "
Введение
Дневники и опросники, заполняемые пациентами или сопровождающими их лицами, могут служить эффективным методом наблюдения за динамикой состояния амбулаторных и стационарных пациентов. При оценке интенсивности боли предпочтительным является сбор данных в режиме реального времени, нежели опрос о событиях за прошедшие сутки, т.к. на последний вид сбора данных может влиять множество факторов (например,стабильность интенсивности боли, изменения эмоциональной окраски и порядка событий при восстановлении их по памяти). Но на практике медперсонал нередко сталкивается с пробелами в заполнении дневников, что связано с различными причинами. Поэтому, в своем исследовании мы решили оценить комплаентность родителей в ведении дневников интенсивности боли у госпитализированных пациентов детского возраста.
Пациенты и методы
64 пациентам (от 2,4 до 17 лет включительно), получающим анальгетики, и их родителям вместе с карточками с изображением шкалы лиц Вонга-Бэйкера и визуальной аналоговой шкалы, были выданы для заполнения бумажные дневники оценки интенсивности базовой и прорывной болей каждые 6 часов на протяжении всего периода потребности в анальгезии. Среднее время наблюдения составило около 8 суток.
Результаты
Общая комплаентность составила 72%. Степень заполнения дневников позволила разделить всех пациентов на 4 группы. В группу 0-25% заполнения вошло 25 пациентов, средний возраст которых составил 7,5 лет. У 9 пациентов было внесено 26-50% данных, а средний возраст детей составил 9,5 лет (медиана 7). 51-75% результатов было получено от родителей 6 детей среднего возраста 9 лет (медиана 10). В группу 76-100% вошли дневники 33 детей среднего возраста 10 лет (медиана 9).
Выводы
Полученные результаты могут свидетельствовать о том, что возраст пациентов может ассоциироваться с комплаентностью родителей в ведении дневников интенсивности боли. Возможно, это связанно с коммуникативными способностями детей разных возрастов. Для подтверждения этого предположения требуются дальнейшие исследования.
Ключевые слова
Оценка интенсивности боли, дневник наблюдения, педиатрия, аналгезия.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(4245) "Введение
Дневники и опросники, заполняемые пациентами или сопровождающими их лицами, могут служить эффективным методом наблюдения за динамикой состояния амбулаторных и стационарных пациентов. При оценке интенсивности боли предпочтительным является сбор данных в режиме реального времени, нежели опрос о событиях за прошедшие сутки, т.к. на последний вид сбора данных может влиять множество факторов (например,стабильность интенсивности боли, изменения эмоциональной окраски и порядка событий при восстановлении их по памяти). Но на практике медперсонал нередко сталкивается с пробелами в заполнении дневников, что связано с различными причинами. Поэтому, в своем исследовании мы решили оценить комплаентность родителей в ведении дневников интенсивности боли у госпитализированных пациентов детского возраста.
Пациенты и методы
64 пациентам (от 2,4 до 17 лет включительно), получающим анальгетики, и их родителям вместе с карточками с изображением шкалы лиц Вонга-Бэйкера и визуальной аналоговой шкалы, были выданы для заполнения бумажные дневники оценки интенсивности базовой и прорывной болей каждые 6 часов на протяжении всего периода потребности в анальгезии. Среднее время наблюдения составило около 8 суток.
Результаты
Общая комплаентность составила 72%. Степень заполнения дневников позволила разделить всех пациентов на 4 группы. В группу 0-25% заполнения вошло 25 пациентов, средний возраст которых составил 7,5 лет. У 9 пациентов было внесено 26-50% данных, а средний возраст детей составил 9,5 лет (медиана 7). 51-75% результатов было получено от родителей 6 детей среднего возраста 9 лет (медиана 10). В группу 76-100% вошли дневники 33 детей среднего возраста 10 лет (медиана 9).
Выводы
Полученные результаты могут свидетельствовать о том, что возраст пациентов может ассоциироваться с комплаентностью родителей в ведении дневников интенсивности боли. Возможно, это связанно с коммуникативными способностями детей разных возрастов. Для подтверждения этого предположения требуются дальнейшие исследования.
Ключевые слова
Оценка интенсивности боли, дневник наблюдения, педиатрия, аналгезия.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20607" ["VALUE"]=> array(2) { ["TEXT"]=> string(674) "<sup>1</sup> Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург<br> <sup>2</sup> Лаборатория клинической фармакологии и терапии боли отдела нейрофармакологии Института фармакологии им. А. В. Вальдмана, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(638) "1 Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург2 Лаборатория клинической фармакологии и терапии боли отдела нейрофармакологии Института фармакологии им. А. В. Вальдмана, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(638) "1 Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург
2 Лаборатория клинической фармакологии и терапии боли отдела нейрофармакологии Института фармакологии им. А. В. Вальдмана, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Россия
" } } } [52]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1585" ["~ID"]=> string(4) "1585" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(198) "Особенности психосексуального развития подростков после трансплантации гемопоэтических стволовых клеток" ["~NAME"]=> string(198) "Особенности психосексуального развития подростков после трансплантации гемопоэтических стволовых клеток" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:40:13" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:40:13" ["DETAIL_PAGE_URL"]=> string(151) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/osobennosti-psikhoseksualnogo-razvitiya-podrostkov-posle-transplantatsii-gemopoeticheskikh-stvolovykh/" ["~DETAIL_PAGE_URL"]=> string(151) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/osobennosti-psikhoseksualnogo-razvitiya-podrostkov-posle-transplantatsii-gemopoeticheskikh-stvolovykh/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(101) "osobennosti-psikhoseksualnogo-razvitiya-podrostkov-posle-transplantatsii-gemopoeticheskikh-stvolovykh" ["~CODE"]=> string(101) "osobennosti-psikhoseksualnogo-razvitiya-podrostkov-posle-transplantatsii-gemopoeticheskikh-stvolovykh" ["EXTERNAL_ID"]=> string(4) "1585" ["~EXTERNAL_ID"]=> string(4) "1585" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(198) "Особенности психосексуального развития подростков после трансплантации гемопоэтических стволовых клеток" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(300) "Особенности психосексуального развития подростков после трансплантации гемопоэтических стволовых клетокPeculiarities of psychosexual development of adolescents after hematopoietic stem cell transplantation" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(6833) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток крови – один из ведущих методов лечения больных с заболеваниями системы крови, иммунодефицитными состояниями, генетическими болезнями. При этом качество жизни пациентов в отдаленном периоде после ТГСК достоверно отличается от качества жизни условно здоровых людей того же возраста. Деформации в психосексуальном развитии, в том числе проблемы в формировании гендерной идентичности приводят к социальной изоляции подростков, что делает невозможным их половую самореализацию и значимо снижает качество жизни. Целью нашего исследования было оценить уровень сформированности гендерной самоидентичности подростков и соответствие психосексуального развития пациентов возрастным нормам. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В 2018 году на базе отделения восстановительной медицины клиники НИИ ДОГиТ им. Р. М. Горбачевой мы провели проспективное исследование 13 семей. Респондентами являлись: 1) родители/опекуны пациентов, сопровождающие их в процессе приезда на плановое обследование; 2) подростки, прошедшие лечение методом ТГСК и проходящие плановые осмотры в клинике в посттрансплантационном периоде (после Д+100), (n = 13, из них 6 девочек и 7 мальчиков, возраст – 12-17 лет, со дня проведения ТГСК прошло 1-5 лет). Для оценки гендерной идентичности были использованы следующие методики: cпециально разработанные анкеты для подростков и родителей, опросник Сандры Бем (Sandra L. Bern, 1974), проективные методики «Рисунок человека», «Несуществующее животное», тест цветовых выборов Люшера. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Традиционный тип гендерной идентичности, который характеризует высокие показатели маскулинности у респондентов мужского пола и высокие показатели фемининности у респондентов женского пола в 100% случаев нами не был выявлен. Как среди девочек, так и среди мальчиков преобладает андрогинный тип с тенденцией к феминности, (%). Причем в среднем сами подростки видят себя несколько более мужественными, чем их матери, за редким исключением, независимо от пола. Это подтверждает тезис, полученный нами в прошлом исследовании, что родители склонны видеть и поощрять в подростках обоего пола покладистость, пассивность в ущерб лидерству, целеустремленности, самостоятельности. Все 100% прошедших тестирование подростки демонстрируют вытеснение темы агрессии, у 77 % наблюдаются те или иные признаки избегания сексуального самоопределения, неприятие своего тела, пола и возраста. 92% пациентов практически не общаются со сверстниками. У 44% преобладают отрицательные эмоции над положительными. У трети испытуемых наблюдается выраженное преобладание установки на отдых и минимизацию собственных усилий. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Особенности семейного воспитания подростков, прошедших ТГСК, часто способствуют значительному ограничению их социального опыта и ведут к специфическим деформациям личности, в том числе в сфере гендерной идентичности. Считаем целесообразным ввести в психологическое сопровождение лечения в клинике тематическое групповое консультирование родителей в рамках «Школы пациента». Ранняя диагностика аспектов личностного становления в рамках психосексуального развития подростков позволяет своевременно обнаружить индивидуальные проблемные зоны и выявить общие тенденции в отдалённые сроки после ТГСК. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических клеток, подростки, психосексуальное развитие, гендерная идентичность, реабилитация. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(198) "Особенности психосексуального развития подростков после трансплантации гемопоэтических стволовых клеток" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(198) "Особенности психосексуального развития подростков после трансплантации гемопоэтических стволовых клеток" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(198) "Особенности психосексуального развития подростков после трансплантации гемопоэтических стволовых клеток" ["SECTION_META_TITLE"]=> string(198) "Особенности психосексуального развития подростков после трансплантации гемопоэтических стволовых клеток" ["SECTION_META_KEYWORDS"]=> string(198) "Особенности психосексуального развития подростков после трансплантации гемопоэтических стволовых клеток" ["SECTION_META_DESCRIPTION"]=> string(198) "Особенности психосексуального развития подростков после трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_ALT"]=> string(198) "Особенности психосексуального развития подростков после трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_TITLE"]=> string(198) "Особенности психосексуального развития подростков после трансплантации гемопоэтических стволовых клеток" ["SECTION_PICTURE_FILE_NAME"]=> string(101) "osobennosti-psikhoseksualnogo-razvitiya-podrostkov-posle-transplantatsii-gemopoeticheskikh-stvolovykh" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(198) "Особенности психосексуального развития подростков после трансплантации гемопоэтических стволовых клеток" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(198) "Особенности психосексуального развития подростков после трансплантации гемопоэтических стволовых клеток" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(101) "osobennosti-psikhoseksualnogo-razvitiya-podrostkov-posle-transplantatsii-gemopoeticheskikh-stvolovykh" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(101) "osobennosti-psikhoseksualnogo-razvitiya-podrostkov-posle-transplantatsii-gemopoeticheskikh-stvolovykh" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(101) "osobennosti-psikhoseksualnogo-razvitiya-podrostkov-posle-transplantatsii-gemopoeticheskikh-stvolovykh" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20599" ["VALUE"]=> array(2) { ["TEXT"]=> string(142) "Светлана И. Олешко, Алиса Г. Волкова, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(142) "Светлана И. Олешко, Алиса Г. Волкова, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20600" ["VALUE"]=> array(2) { ["TEXT"]=> string(466) "HИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(460) "HИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20601" ["VALUE"]=> array(2) { ["TEXT"]=> string(6833) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток крови – один из ведущих методов лечения больных с заболеваниями системы крови, иммунодефицитными состояниями, генетическими болезнями. При этом качество жизни пациентов в отдаленном периоде после ТГСК достоверно отличается от качества жизни условно здоровых людей того же возраста. Деформации в психосексуальном развитии, в том числе проблемы в формировании гендерной идентичности приводят к социальной изоляции подростков, что делает невозможным их половую самореализацию и значимо снижает качество жизни. Целью нашего исследования было оценить уровень сформированности гендерной самоидентичности подростков и соответствие психосексуального развития пациентов возрастным нормам. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В 2018 году на базе отделения восстановительной медицины клиники НИИ ДОГиТ им. Р. М. Горбачевой мы провели проспективное исследование 13 семей. Респондентами являлись: 1) родители/опекуны пациентов, сопровождающие их в процессе приезда на плановое обследование; 2) подростки, прошедшие лечение методом ТГСК и проходящие плановые осмотры в клинике в посттрансплантационном периоде (после Д+100), (n = 13, из них 6 девочек и 7 мальчиков, возраст – 12-17 лет, со дня проведения ТГСК прошло 1-5 лет). Для оценки гендерной идентичности были использованы следующие методики: cпециально разработанные анкеты для подростков и родителей, опросник Сандры Бем (Sandra L. Bern, 1974), проективные методики «Рисунок человека», «Несуществующее животное», тест цветовых выборов Люшера. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Традиционный тип гендерной идентичности, который характеризует высокие показатели маскулинности у респондентов мужского пола и высокие показатели фемининности у респондентов женского пола в 100% случаев нами не был выявлен. Как среди девочек, так и среди мальчиков преобладает андрогинный тип с тенденцией к феминности, (%). Причем в среднем сами подростки видят себя несколько более мужественными, чем их матери, за редким исключением, независимо от пола. Это подтверждает тезис, полученный нами в прошлом исследовании, что родители склонны видеть и поощрять в подростках обоего пола покладистость, пассивность в ущерб лидерству, целеустремленности, самостоятельности. Все 100% прошедших тестирование подростки демонстрируют вытеснение темы агрессии, у 77 % наблюдаются те или иные признаки избегания сексуального самоопределения, неприятие своего тела, пола и возраста. 92% пациентов практически не общаются со сверстниками. У 44% преобладают отрицательные эмоции над положительными. У трети испытуемых наблюдается выраженное преобладание установки на отдых и минимизацию собственных усилий. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Особенности семейного воспитания подростков, прошедших ТГСК, часто способствуют значительному ограничению их социального опыта и ведут к специфическим деформациям личности, в том числе в сфере гендерной идентичности. Считаем целесообразным ввести в психологическое сопровождение лечения в клинике тематическое групповое консультирование родителей в рамках «Школы пациента». Ранняя диагностика аспектов личностного становления в рамках психосексуального развития подростков позволяет своевременно обнаружить индивидуальные проблемные зоны и выявить общие тенденции в отдалённые сроки после ТГСК. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических клеток, подростки, психосексуальное развитие, гендерная идентичность, реабилитация. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6601) "
Введение
Трансплантация гемопоэтических стволовых клеток крови – один из ведущих методов лечения больных с заболеваниями системы крови, иммунодефицитными состояниями, генетическими болезнями. При этом качество жизни пациентов в отдаленном периоде после ТГСК достоверно отличается от качества жизни условно здоровых людей того же возраста. Деформации в психосексуальном развитии, в том числе проблемы в формировании гендерной идентичности приводят к социальной изоляции подростков, что делает невозможным их половую самореализацию и значимо снижает качество жизни. Целью нашего исследования было оценить уровень сформированности гендерной самоидентичности подростков и соответствие психосексуального развития пациентов возрастным нормам.
Материалы и методы
В 2018 году на базе отделения восстановительной медицины клиники НИИ ДОГиТ им. Р. М. Горбачевой мы провели проспективное исследование 13 семей. Респондентами являлись: 1) родители/опекуны пациентов, сопровождающие их в процессе приезда на плановое обследование; 2) подростки, прошедшие лечение методом ТГСК и проходящие плановые осмотры в клинике в посттрансплантационном периоде (после Д+100), (n = 13, из них 6 девочек и 7 мальчиков, возраст – 12-17 лет, со дня проведения ТГСК прошло 1-5 лет). Для оценки гендерной идентичности были использованы следующие методики: cпециально разработанные анкеты для подростков и родителей, опросник Сандры Бем (Sandra L. Bern, 1974), проективные методики «Рисунок человека», «Несуществующее животное», тест цветовых выборов Люшера.
Результаты
Традиционный тип гендерной идентичности, который характеризует высокие показатели маскулинности у респондентов мужского пола и высокие показатели фемининности у респондентов женского пола в 100% случаев нами не был выявлен. Как среди девочек, так и среди мальчиков преобладает андрогинный тип с тенденцией к феминности, (%). Причем в среднем сами подростки видят себя несколько более мужественными, чем их матери, за редким исключением, независимо от пола. Это подтверждает тезис, полученный нами в прошлом исследовании, что родители склонны видеть и поощрять в подростках обоего пола покладистость, пассивность в ущерб лидерству, целеустремленности, самостоятельности. Все 100% прошедших тестирование подростки демонстрируют вытеснение темы агрессии, у 77 % наблюдаются те или иные признаки избегания сексуального самоопределения, неприятие своего тела, пола и возраста. 92% пациентов практически не общаются со сверстниками. У 44% преобладают отрицательные эмоции над положительными. У трети испытуемых наблюдается выраженное преобладание установки на отдых и минимизацию собственных усилий.
Выводы
Особенности семейного воспитания подростков, прошедших ТГСК, часто способствуют значительному ограничению их социального опыта и ведут к специфическим деформациям личности, в том числе в сфере гендерной идентичности. Считаем целесообразным ввести в психологическое сопровождение лечения в клинике тематическое групповое консультирование родителей в рамках «Школы пациента». Ранняя диагностика аспектов личностного становления в рамках психосексуального развития подростков позволяет своевременно обнаружить индивидуальные проблемные зоны и выявить общие тенденции в отдалённые сроки после ТГСК.
Ключевые слова
Трансплантация гемопоэтических клеток, подростки, психосексуальное развитие, гендерная идентичность, реабилитация.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20602" ["VALUE"]=> array(2) { ["TEXT"]=> string(82) "Svetlana I. Oleshko, Alisa G. Volkova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(82) "Svetlana I. Oleshko, Alisa G. Volkova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20603" ["VALUE"]=> array(2) { ["TEXT"]=> string(234) "R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation, and Chair of Hematology, Transfusiology and Transplantology at the First I. P. Pavlov State Medical University of St. Petersburg<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(228) "R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation, and Chair of Hematology, Transfusiology and Transplantology at the First I. P. Pavlov State Medical University of St. Petersburg" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20604" ["VALUE"]=> array(2) { ["TEXT"]=> string(4202) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Transplantation of hematopoietic stem cells (HSCT) is one of the leading methods of treatment in patients with blood system diseases, primary immunodeficiency syndromes and genetic diseases. At the same time, the quality of life in patients in the long-term after HSCT significantly differs from the quality of life of healthy people of the same age. Deformations in psychosexual development including problems in the gender identity formation cause social isolation of adolescents, which makes their sexual self-realization impossible and significantly reduces the quality of their life. Hence, the aim of our study was an assessment of the level of gender identity formation of adolescents and psychosexual development correlation to the normal adolescents of the same age. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> In 2018, on the base of the Department of Recovery Medicine, the Clinic of the Research Institute of Raisa Gorbacheva Memorial Institute of Children’s Oncology, Hematology and Transplantation, we conducted a prospective study of 13 families. The respondents were: 1) parents/guardians of patients accompanying them in the process of examination; 2) adolescents who underwent HSCT treatment and undergo planned examinations at the clinic in the posttransplant period (after D + 100), (n=13, of which 6 girls and 7 boys, age 12-17 years, from the date of HSCT 1-5 years). The following methods were used to assess gender identity: Specially developed questionnaires for teenagers and parents; questionnaire by Sandra L. Bem (Sandra L. Bem, 1974); projective techniques “The Human Picture”, “The non-existent animal”; Max Lüscher’s color choices test. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The traditional type of gender identity that characterizes the high masculinity in male respondents and the high femininity rates of female respondents in 100% of cases were not revealed. Both among girls and among boys, the androgynous type predominates with a tendency towards femininity. On average, the adolescents evaluate themselves a little more courageous than their mothers, with rare exceptions, regardless of gender. This confirms the thesis we received in the previous study that parents tend to see and encourage complacency in adolescents of both sexes, passivity to the detriment of leadership, dedication, and independence. All 100% of the teenagers, who participated in the test, demonstrate the displacement of the aggression topic, 77% have some signs of avoiding sexual self-determination, rejection of their body, sex and age. 92% of patients do not communicate with their peers. In 44% of them, negative emotions prevail over positive ones. A third of the test participants show an expressed favor for rest and minimization of their efforts. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> The characteristics of family upbringing of adolescents who have undergone HSCT often contribute significantly to limiting their social experience and lead to specific deformities of individuality, including in the sphere of gender identity. We consider it advisable to introduce thematic group counseling of parents within the framework of the “Patient’s School” in psychological treatment support in the clinic. Early diagnostics of aspects of personal development within the framework of psychosexual development of adolescents makes it possible to identify individual problem areas in a timely manner and to identify general trends in the long term after HSCT. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cells transplant, adolescents, psychosexual development, gender identity, rehabilitation. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3970) "
Introduction
Transplantation of hematopoietic stem cells (HSCT) is one of the leading methods of treatment in patients with blood system diseases, primary immunodeficiency syndromes and genetic diseases. At the same time, the quality of life in patients in the long-term after HSCT significantly differs from the quality of life of healthy people of the same age. Deformations in psychosexual development including problems in the gender identity formation cause social isolation of adolescents, which makes their sexual self-realization impossible and significantly reduces the quality of their life. Hence, the aim of our study was an assessment of the level of gender identity formation of adolescents and psychosexual development correlation to the normal adolescents of the same age.
Materials and methods
In 2018, on the base of the Department of Recovery Medicine, the Clinic of the Research Institute of Raisa Gorbacheva Memorial Institute of Children’s Oncology, Hematology and Transplantation, we conducted a prospective study of 13 families. The respondents were: 1) parents/guardians of patients accompanying them in the process of examination; 2) adolescents who underwent HSCT treatment and undergo planned examinations at the clinic in the posttransplant period (after D + 100), (n=13, of which 6 girls and 7 boys, age 12-17 years, from the date of HSCT 1-5 years). The following methods were used to assess gender identity: Specially developed questionnaires for teenagers and parents; questionnaire by Sandra L. Bem (Sandra L. Bem, 1974); projective techniques “The Human Picture”, “The non-existent animal”; Max Lüscher’s color choices test.
Results
The traditional type of gender identity that characterizes the high masculinity in male respondents and the high femininity rates of female respondents in 100% of cases were not revealed. Both among girls and among boys, the androgynous type predominates with a tendency towards femininity. On average, the adolescents evaluate themselves a little more courageous than their mothers, with rare exceptions, regardless of gender. This confirms the thesis we received in the previous study that parents tend to see and encourage complacency in adolescents of both sexes, passivity to the detriment of leadership, dedication, and independence. All 100% of the teenagers, who participated in the test, demonstrate the displacement of the aggression topic, 77% have some signs of avoiding sexual self-determination, rejection of their body, sex and age. 92% of patients do not communicate with their peers. In 44% of them, negative emotions prevail over positive ones. A third of the test participants show an expressed favor for rest and minimization of their efforts.
Conclusions
The characteristics of family upbringing of adolescents who have undergone HSCT often contribute significantly to limiting their social experience and lead to specific deformities of individuality, including in the sphere of gender identity. We consider it advisable to introduce thematic group counseling of parents within the framework of the “Patient’s School” in psychological treatment support in the clinic. Early diagnostics of aspects of personal development within the framework of psychosexual development of adolescents makes it possible to identify individual problem areas in a timely manner and to identify general trends in the long term after HSCT.
Keywords
Hematopoietic stem cells transplant, adolescents, psychosexual development, gender identity, rehabilitation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20605" ["VALUE"]=> string(102) "Peculiarities of psychosexual development of adolescents after hematopoietic stem cell transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(102) "Peculiarities of psychosexual development of adolescents after hematopoietic stem cell transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20801" ["VALUE"]=> string(4) "1439" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1439" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20802" ["VALUE"]=> string(4) "1440" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1440" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20602" ["VALUE"]=> array(2) { ["TEXT"]=> string(82) "Svetlana I. Oleshko, Alisa G. Volkova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(82) "Svetlana I. Oleshko, Alisa G. Volkova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(82) "Svetlana I. Oleshko, Alisa G. Volkova, Ludmila S. Zubarovskaya, Boris V. Afanasyev" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20604" ["VALUE"]=> array(2) { ["TEXT"]=> string(4202) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> Transplantation of hematopoietic stem cells (HSCT) is one of the leading methods of treatment in patients with blood system diseases, primary immunodeficiency syndromes and genetic diseases. At the same time, the quality of life in patients in the long-term after HSCT significantly differs from the quality of life of healthy people of the same age. Deformations in psychosexual development including problems in the gender identity formation cause social isolation of adolescents, which makes their sexual self-realization impossible and significantly reduces the quality of their life. Hence, the aim of our study was an assessment of the level of gender identity formation of adolescents and psychosexual development correlation to the normal adolescents of the same age. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> In 2018, on the base of the Department of Recovery Medicine, the Clinic of the Research Institute of Raisa Gorbacheva Memorial Institute of Children’s Oncology, Hematology and Transplantation, we conducted a prospective study of 13 families. The respondents were: 1) parents/guardians of patients accompanying them in the process of examination; 2) adolescents who underwent HSCT treatment and undergo planned examinations at the clinic in the posttransplant period (after D + 100), (n=13, of which 6 girls and 7 boys, age 12-17 years, from the date of HSCT 1-5 years). The following methods were used to assess gender identity: Specially developed questionnaires for teenagers and parents; questionnaire by Sandra L. Bem (Sandra L. Bem, 1974); projective techniques “The Human Picture”, “The non-existent animal”; Max Lüscher’s color choices test. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> The traditional type of gender identity that characterizes the high masculinity in male respondents and the high femininity rates of female respondents in 100% of cases were not revealed. Both among girls and among boys, the androgynous type predominates with a tendency towards femininity. On average, the adolescents evaluate themselves a little more courageous than their mothers, with rare exceptions, regardless of gender. This confirms the thesis we received in the previous study that parents tend to see and encourage complacency in adolescents of both sexes, passivity to the detriment of leadership, dedication, and independence. All 100% of the teenagers, who participated in the test, demonstrate the displacement of the aggression topic, 77% have some signs of avoiding sexual self-determination, rejection of their body, sex and age. 92% of patients do not communicate with their peers. In 44% of them, negative emotions prevail over positive ones. A third of the test participants show an expressed favor for rest and minimization of their efforts. </p> <h2 style="text-align: justify;">Conclusions</h2> <p style="text-align: justify;"> The characteristics of family upbringing of adolescents who have undergone HSCT often contribute significantly to limiting their social experience and lead to specific deformities of individuality, including in the sphere of gender identity. We consider it advisable to introduce thematic group counseling of parents within the framework of the “Patient’s School” in psychological treatment support in the clinic. Early diagnostics of aspects of personal development within the framework of psychosexual development of adolescents makes it possible to identify individual problem areas in a timely manner and to identify general trends in the long term after HSCT. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cells transplant, adolescents, psychosexual development, gender identity, rehabilitation. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3970) "Introduction
Transplantation of hematopoietic stem cells (HSCT) is one of the leading methods of treatment in patients with blood system diseases, primary immunodeficiency syndromes and genetic diseases. At the same time, the quality of life in patients in the long-term after HSCT significantly differs from the quality of life of healthy people of the same age. Deformations in psychosexual development including problems in the gender identity formation cause social isolation of adolescents, which makes their sexual self-realization impossible and significantly reduces the quality of their life. Hence, the aim of our study was an assessment of the level of gender identity formation of adolescents and psychosexual development correlation to the normal adolescents of the same age.
Materials and methods
In 2018, on the base of the Department of Recovery Medicine, the Clinic of the Research Institute of Raisa Gorbacheva Memorial Institute of Children’s Oncology, Hematology and Transplantation, we conducted a prospective study of 13 families. The respondents were: 1) parents/guardians of patients accompanying them in the process of examination; 2) adolescents who underwent HSCT treatment and undergo planned examinations at the clinic in the posttransplant period (after D + 100), (n=13, of which 6 girls and 7 boys, age 12-17 years, from the date of HSCT 1-5 years). The following methods were used to assess gender identity: Specially developed questionnaires for teenagers and parents; questionnaire by Sandra L. Bem (Sandra L. Bem, 1974); projective techniques “The Human Picture”, “The non-existent animal”; Max Lüscher’s color choices test.
Results
The traditional type of gender identity that characterizes the high masculinity in male respondents and the high femininity rates of female respondents in 100% of cases were not revealed. Both among girls and among boys, the androgynous type predominates with a tendency towards femininity. On average, the adolescents evaluate themselves a little more courageous than their mothers, with rare exceptions, regardless of gender. This confirms the thesis we received in the previous study that parents tend to see and encourage complacency in adolescents of both sexes, passivity to the detriment of leadership, dedication, and independence. All 100% of the teenagers, who participated in the test, demonstrate the displacement of the aggression topic, 77% have some signs of avoiding sexual self-determination, rejection of their body, sex and age. 92% of patients do not communicate with their peers. In 44% of them, negative emotions prevail over positive ones. A third of the test participants show an expressed favor for rest and minimization of their efforts.
Conclusions
The characteristics of family upbringing of adolescents who have undergone HSCT often contribute significantly to limiting their social experience and lead to specific deformities of individuality, including in the sphere of gender identity. We consider it advisable to introduce thematic group counseling of parents within the framework of the “Patient’s School” in psychological treatment support in the clinic. Early diagnostics of aspects of personal development within the framework of psychosexual development of adolescents makes it possible to identify individual problem areas in a timely manner and to identify general trends in the long term after HSCT.
Keywords
Hematopoietic stem cells transplant, adolescents, psychosexual development, gender identity, rehabilitation.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3970) "Introduction
Transplantation of hematopoietic stem cells (HSCT) is one of the leading methods of treatment in patients with blood system diseases, primary immunodeficiency syndromes and genetic diseases. At the same time, the quality of life in patients in the long-term after HSCT significantly differs from the quality of life of healthy people of the same age. Deformations in psychosexual development including problems in the gender identity formation cause social isolation of adolescents, which makes their sexual self-realization impossible and significantly reduces the quality of their life. Hence, the aim of our study was an assessment of the level of gender identity formation of adolescents and psychosexual development correlation to the normal adolescents of the same age.
Materials and methods
In 2018, on the base of the Department of Recovery Medicine, the Clinic of the Research Institute of Raisa Gorbacheva Memorial Institute of Children’s Oncology, Hematology and Transplantation, we conducted a prospective study of 13 families. The respondents were: 1) parents/guardians of patients accompanying them in the process of examination; 2) adolescents who underwent HSCT treatment and undergo planned examinations at the clinic in the posttransplant period (after D + 100), (n=13, of which 6 girls and 7 boys, age 12-17 years, from the date of HSCT 1-5 years). The following methods were used to assess gender identity: Specially developed questionnaires for teenagers and parents; questionnaire by Sandra L. Bem (Sandra L. Bem, 1974); projective techniques “The Human Picture”, “The non-existent animal”; Max Lüscher’s color choices test.
Results
The traditional type of gender identity that characterizes the high masculinity in male respondents and the high femininity rates of female respondents in 100% of cases were not revealed. Both among girls and among boys, the androgynous type predominates with a tendency towards femininity. On average, the adolescents evaluate themselves a little more courageous than their mothers, with rare exceptions, regardless of gender. This confirms the thesis we received in the previous study that parents tend to see and encourage complacency in adolescents of both sexes, passivity to the detriment of leadership, dedication, and independence. All 100% of the teenagers, who participated in the test, demonstrate the displacement of the aggression topic, 77% have some signs of avoiding sexual self-determination, rejection of their body, sex and age. 92% of patients do not communicate with their peers. In 44% of them, negative emotions prevail over positive ones. A third of the test participants show an expressed favor for rest and minimization of their efforts.
Conclusions
The characteristics of family upbringing of adolescents who have undergone HSCT often contribute significantly to limiting their social experience and lead to specific deformities of individuality, including in the sphere of gender identity. We consider it advisable to introduce thematic group counseling of parents within the framework of the “Patient’s School” in psychological treatment support in the clinic. Early diagnostics of aspects of personal development within the framework of psychosexual development of adolescents makes it possible to identify individual problem areas in a timely manner and to identify general trends in the long term after HSCT.
Keywords
Hematopoietic stem cells transplant, adolescents, psychosexual development, gender identity, rehabilitation.
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20605" ["VALUE"]=> string(102) "Peculiarities of psychosexual development of adolescents after hematopoietic stem cell transplantation" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(102) "Peculiarities of psychosexual development of adolescents after hematopoietic stem cell transplantation" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(102) "Peculiarities of psychosexual development of adolescents after hematopoietic stem cell transplantation" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20603" ["VALUE"]=> array(2) { ["TEXT"]=> string(234) "R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation, and Chair of Hematology, Transfusiology and Transplantology at the First I. P. Pavlov State Medical University of St. Petersburg<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(228) "R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation, and Chair of Hematology, Transfusiology and Transplantology at the First I. P. Pavlov State Medical University of St. Petersburg" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(228) "R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation, and Chair of Hematology, Transfusiology and Transplantology at the First I. P. Pavlov State Medical University of St. Petersburg
" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20599" ["VALUE"]=> array(2) { ["TEXT"]=> string(142) "Светлана И. Олешко, Алиса Г. Волкова, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(142) "Светлана И. Олешко, Алиса Г. Волкова, Людмила С. Зубаровская, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(142) "Светлана И. Олешко, Алиса Г. Волкова, Людмила С. Зубаровская, Борис В. Афанасьев" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20601" ["VALUE"]=> array(2) { ["TEXT"]=> string(6833) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических стволовых клеток крови – один из ведущих методов лечения больных с заболеваниями системы крови, иммунодефицитными состояниями, генетическими болезнями. При этом качество жизни пациентов в отдаленном периоде после ТГСК достоверно отличается от качества жизни условно здоровых людей того же возраста. Деформации в психосексуальном развитии, в том числе проблемы в формировании гендерной идентичности приводят к социальной изоляции подростков, что делает невозможным их половую самореализацию и значимо снижает качество жизни. Целью нашего исследования было оценить уровень сформированности гендерной самоидентичности подростков и соответствие психосексуального развития пациентов возрастным нормам. </p> <h2 style="text-align: justify;">Материалы и методы</h2> <p style="text-align: justify;"> В 2018 году на базе отделения восстановительной медицины клиники НИИ ДОГиТ им. Р. М. Горбачевой мы провели проспективное исследование 13 семей. Респондентами являлись: 1) родители/опекуны пациентов, сопровождающие их в процессе приезда на плановое обследование; 2) подростки, прошедшие лечение методом ТГСК и проходящие плановые осмотры в клинике в посттрансплантационном периоде (после Д+100), (n = 13, из них 6 девочек и 7 мальчиков, возраст – 12-17 лет, со дня проведения ТГСК прошло 1-5 лет). Для оценки гендерной идентичности были использованы следующие методики: cпециально разработанные анкеты для подростков и родителей, опросник Сандры Бем (Sandra L. Bern, 1974), проективные методики «Рисунок человека», «Несуществующее животное», тест цветовых выборов Люшера. </p> <h2 style="text-align: justify;">Результаты</h2> <p style="text-align: justify;"> Традиционный тип гендерной идентичности, который характеризует высокие показатели маскулинности у респондентов мужского пола и высокие показатели фемининности у респондентов женского пола в 100% случаев нами не был выявлен. Как среди девочек, так и среди мальчиков преобладает андрогинный тип с тенденцией к феминности, (%). Причем в среднем сами подростки видят себя несколько более мужественными, чем их матери, за редким исключением, независимо от пола. Это подтверждает тезис, полученный нами в прошлом исследовании, что родители склонны видеть и поощрять в подростках обоего пола покладистость, пассивность в ущерб лидерству, целеустремленности, самостоятельности. Все 100% прошедших тестирование подростки демонстрируют вытеснение темы агрессии, у 77 % наблюдаются те или иные признаки избегания сексуального самоопределения, неприятие своего тела, пола и возраста. 92% пациентов практически не общаются со сверстниками. У 44% преобладают отрицательные эмоции над положительными. У трети испытуемых наблюдается выраженное преобладание установки на отдых и минимизацию собственных усилий. </p> <h2 style="text-align: justify;">Выводы</h2> <p style="text-align: justify;"> Особенности семейного воспитания подростков, прошедших ТГСК, часто способствуют значительному ограничению их социального опыта и ведут к специфическим деформациям личности, в том числе в сфере гендерной идентичности. Считаем целесообразным ввести в психологическое сопровождение лечения в клинике тематическое групповое консультирование родителей в рамках «Школы пациента». Ранняя диагностика аспектов личностного становления в рамках психосексуального развития подростков позволяет своевременно обнаружить индивидуальные проблемные зоны и выявить общие тенденции в отдалённые сроки после ТГСК. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Трансплантация гемопоэтических клеток, подростки, психосексуальное развитие, гендерная идентичность, реабилитация. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6601) "
Введение
Трансплантация гемопоэтических стволовых клеток крови – один из ведущих методов лечения больных с заболеваниями системы крови, иммунодефицитными состояниями, генетическими болезнями. При этом качество жизни пациентов в отдаленном периоде после ТГСК достоверно отличается от качества жизни условно здоровых людей того же возраста. Деформации в психосексуальном развитии, в том числе проблемы в формировании гендерной идентичности приводят к социальной изоляции подростков, что делает невозможным их половую самореализацию и значимо снижает качество жизни. Целью нашего исследования было оценить уровень сформированности гендерной самоидентичности подростков и соответствие психосексуального развития пациентов возрастным нормам.
Материалы и методы
В 2018 году на базе отделения восстановительной медицины клиники НИИ ДОГиТ им. Р. М. Горбачевой мы провели проспективное исследование 13 семей. Респондентами являлись: 1) родители/опекуны пациентов, сопровождающие их в процессе приезда на плановое обследование; 2) подростки, прошедшие лечение методом ТГСК и проходящие плановые осмотры в клинике в посттрансплантационном периоде (после Д+100), (n = 13, из них 6 девочек и 7 мальчиков, возраст – 12-17 лет, со дня проведения ТГСК прошло 1-5 лет). Для оценки гендерной идентичности были использованы следующие методики: cпециально разработанные анкеты для подростков и родителей, опросник Сандры Бем (Sandra L. Bern, 1974), проективные методики «Рисунок человека», «Несуществующее животное», тест цветовых выборов Люшера.
Результаты
Традиционный тип гендерной идентичности, который характеризует высокие показатели маскулинности у респондентов мужского пола и высокие показатели фемининности у респондентов женского пола в 100% случаев нами не был выявлен. Как среди девочек, так и среди мальчиков преобладает андрогинный тип с тенденцией к феминности, (%). Причем в среднем сами подростки видят себя несколько более мужественными, чем их матери, за редким исключением, независимо от пола. Это подтверждает тезис, полученный нами в прошлом исследовании, что родители склонны видеть и поощрять в подростках обоего пола покладистость, пассивность в ущерб лидерству, целеустремленности, самостоятельности. Все 100% прошедших тестирование подростки демонстрируют вытеснение темы агрессии, у 77 % наблюдаются те или иные признаки избегания сексуального самоопределения, неприятие своего тела, пола и возраста. 92% пациентов практически не общаются со сверстниками. У 44% преобладают отрицательные эмоции над положительными. У трети испытуемых наблюдается выраженное преобладание установки на отдых и минимизацию собственных усилий.
Выводы
Особенности семейного воспитания подростков, прошедших ТГСК, часто способствуют значительному ограничению их социального опыта и ведут к специфическим деформациям личности, в том числе в сфере гендерной идентичности. Считаем целесообразным ввести в психологическое сопровождение лечения в клинике тематическое групповое консультирование родителей в рамках «Школы пациента». Ранняя диагностика аспектов личностного становления в рамках психосексуального развития подростков позволяет своевременно обнаружить индивидуальные проблемные зоны и выявить общие тенденции в отдалённые сроки после ТГСК.
Ключевые слова
Трансплантация гемопоэтических клеток, подростки, психосексуальное развитие, гендерная идентичность, реабилитация.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6601) "Введение
Трансплантация гемопоэтических стволовых клеток крови – один из ведущих методов лечения больных с заболеваниями системы крови, иммунодефицитными состояниями, генетическими болезнями. При этом качество жизни пациентов в отдаленном периоде после ТГСК достоверно отличается от качества жизни условно здоровых людей того же возраста. Деформации в психосексуальном развитии, в том числе проблемы в формировании гендерной идентичности приводят к социальной изоляции подростков, что делает невозможным их половую самореализацию и значимо снижает качество жизни. Целью нашего исследования было оценить уровень сформированности гендерной самоидентичности подростков и соответствие психосексуального развития пациентов возрастным нормам.
Материалы и методы
В 2018 году на базе отделения восстановительной медицины клиники НИИ ДОГиТ им. Р. М. Горбачевой мы провели проспективное исследование 13 семей. Респондентами являлись: 1) родители/опекуны пациентов, сопровождающие их в процессе приезда на плановое обследование; 2) подростки, прошедшие лечение методом ТГСК и проходящие плановые осмотры в клинике в посттрансплантационном периоде (после Д+100), (n = 13, из них 6 девочек и 7 мальчиков, возраст – 12-17 лет, со дня проведения ТГСК прошло 1-5 лет). Для оценки гендерной идентичности были использованы следующие методики: cпециально разработанные анкеты для подростков и родителей, опросник Сандры Бем (Sandra L. Bern, 1974), проективные методики «Рисунок человека», «Несуществующее животное», тест цветовых выборов Люшера.
Результаты
Традиционный тип гендерной идентичности, который характеризует высокие показатели маскулинности у респондентов мужского пола и высокие показатели фемининности у респондентов женского пола в 100% случаев нами не был выявлен. Как среди девочек, так и среди мальчиков преобладает андрогинный тип с тенденцией к феминности, (%). Причем в среднем сами подростки видят себя несколько более мужественными, чем их матери, за редким исключением, независимо от пола. Это подтверждает тезис, полученный нами в прошлом исследовании, что родители склонны видеть и поощрять в подростках обоего пола покладистость, пассивность в ущерб лидерству, целеустремленности, самостоятельности. Все 100% прошедших тестирование подростки демонстрируют вытеснение темы агрессии, у 77 % наблюдаются те или иные признаки избегания сексуального самоопределения, неприятие своего тела, пола и возраста. 92% пациентов практически не общаются со сверстниками. У 44% преобладают отрицательные эмоции над положительными. У трети испытуемых наблюдается выраженное преобладание установки на отдых и минимизацию собственных усилий.
Выводы
Особенности семейного воспитания подростков, прошедших ТГСК, часто способствуют значительному ограничению их социального опыта и ведут к специфическим деформациям личности, в том числе в сфере гендерной идентичности. Считаем целесообразным ввести в психологическое сопровождение лечения в клинике тематическое групповое консультирование родителей в рамках «Школы пациента». Ранняя диагностика аспектов личностного становления в рамках психосексуального развития подростков позволяет своевременно обнаружить индивидуальные проблемные зоны и выявить общие тенденции в отдалённые сроки после ТГСК.
Ключевые слова
Трансплантация гемопоэтических клеток, подростки, психосексуальное развитие, гендерная идентичность, реабилитация.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20600" ["VALUE"]=> array(2) { ["TEXT"]=> string(466) "HИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Россия<br>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(460) "HИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Россия" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(460) "HИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
" } } } [53]=> array(49) { ["IBLOCK_SECTION_ID"]=> string(3) "111" ["~IBLOCK_SECTION_ID"]=> string(3) "111" ["ID"]=> string(4) "1603" ["~ID"]=> string(4) "1603" ["IBLOCK_ID"]=> string(1) "2" ["~IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(269) "Клинический случай: эффект отмены терапии ингибитором Jak-2-киназы на стероид-рефрактерную реакцию трансплантат против хозяина с поражением печени" ["~NAME"]=> string(269) "Клинический случай: эффект отмены терапии ингибитором Jak-2-киназы на стероид-рефрактерную реакцию трансплантат против хозяина с поражением печени" ["ACTIVE_FROM"]=> NULL ["~ACTIVE_FROM"]=> NULL ["TIMESTAMP_X"]=> string(19) "11.12.2018 22:48:59" ["~TIMESTAMP_X"]=> string(19) "11.12.2018 22:48:59" ["DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/klinicheskiy-sluchay-effekt-otmeny-terapii-ingibitorom-jak-2-kinazy-na-steroid-refrakternuyu-reaktsi/" ["~DETAIL_PAGE_URL"]=> string(150) "/ru/archive/tom-7-nomer-3/korotkie-soobshcheniya/klinicheskiy-sluchay-effekt-otmeny-terapii-ingibitorom-jak-2-kinazy-na-steroid-refrakternuyu-reaktsi/" ["LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["~LIST_PAGE_URL"]=> string(12) "/ru/archive/" ["DETAIL_TEXT"]=> string(0) "" ["~DETAIL_TEXT"]=> string(0) "" ["DETAIL_TEXT_TYPE"]=> string(4) "text" ["~DETAIL_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_TEXT"]=> string(0) "" ["~PREVIEW_TEXT"]=> string(0) "" ["PREVIEW_TEXT_TYPE"]=> string(4) "text" ["~PREVIEW_TEXT_TYPE"]=> string(4) "text" ["PREVIEW_PICTURE"]=> NULL ["~PREVIEW_PICTURE"]=> NULL ["LANG_DIR"]=> string(4) "/ru/" ["~LANG_DIR"]=> string(4) "/ru/" ["SORT"]=> string(3) "500" ["~SORT"]=> string(3) "500" ["CODE"]=> string(100) "klinicheskiy-sluchay-effekt-otmeny-terapii-ingibitorom-jak-2-kinazy-na-steroid-refrakternuyu-reaktsi" ["~CODE"]=> string(100) "klinicheskiy-sluchay-effekt-otmeny-terapii-ingibitorom-jak-2-kinazy-na-steroid-refrakternuyu-reaktsi" ["EXTERNAL_ID"]=> string(4) "1603" ["~EXTERNAL_ID"]=> string(4) "1603" ["IBLOCK_TYPE_ID"]=> string(7) "journal" ["~IBLOCK_TYPE_ID"]=> string(7) "journal" ["IBLOCK_CODE"]=> string(7) "volumes" ["~IBLOCK_CODE"]=> string(7) "volumes" ["IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["~IBLOCK_EXTERNAL_ID"]=> string(1) "2" ["LID"]=> string(2) "s2" ["~LID"]=> string(2) "s2" ["EDIT_LINK"]=> NULL ["DELETE_LINK"]=> NULL ["DISPLAY_ACTIVE_FROM"]=> string(0) "" ["IPROPERTY_VALUES"]=> array(18) { ["ELEMENT_META_TITLE"]=> string(269) "Клинический случай: эффект отмены терапии ингибитором Jak-2-киназы на стероид-рефрактерную реакцию трансплантат против хозяина с поражением печени" ["ELEMENT_META_KEYWORDS"]=> string(0) "" ["ELEMENT_META_DESCRIPTION"]=> string(395) "Клинический случай: эффект отмены терапии ингибитором Jak-2-киназы на стероид-рефрактерную реакцию трансплантат против хозяина с поражением печениCase report: effect of Jak-2 kinase inhibitor discontinuation on chronic steroid-refractory graft-versus-host disease in liver" ["ELEMENT_PREVIEW_PICTURE_FILE_ALT"]=> string(6961) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Стероид-рефрактерная РТПХ (срРТПХ) развивается в половине случаев РТПХ, с вероятностью летального исхода 70%. В качестве терапии спасения могут выступать ингибиторы Jak-2-киназ. Однако нет достоверных данных об оптимальной продолжительности терапии и стратегии отмены данных препаратов. Целью работы стало представление случая срРТПХ печени после гаплоидентичной трансплантации гемопоэтических стволовых клеток (гапло-ТГСК) у молодого пациента с синдромом Жильбера с улучшением показателей функции печени после отмены терапии ингибитором Jak-2-киназ. При анализе результатов были использованы данные медицинской документации, результаты лабораторных и инструментальных исследований. Стадии РТПХ оценивались согласно критериям NIH-2014. </p> <h2 style="text-align: justify;">Описание клинического случая</h2> <p style="text-align: justify;"> Пациент, 28 лет, с острым миелоидным лейкозом (ОМЛ), FAB-M2, и сопутствующим синдромом Жильбера 12.05.2015 перенес гапло-ТГСК от брата, 6/10. Режим кондиционирования: бусульфан (8 мг/кг), флударабин. Источник трансплантата: костный мозг. Профилактика РТПХ: циклофосфан (30 мг/кг, Д+3,+4), такролимус (с Д+5), микофенолата мофетил (45 мг/кг с Д+5 по Д+35). На Д+90 по причине развития раннего костно-мозгового рецидива – отмена такролимуса. На Д+202 развился overlap-синдром РТПХ 4 степени с поражением кожи, печени и нижних отделов ЖКТ (стадии 3, 4 и 3, соответственно). Терапия I линии: метилпреднизолон 2 мг/кг; эффект: частичный ответ по РТПХ кожи. К терапии были добавлены этанерцепт 25 мг 2 р/нед и такролимус. Эффект: уровень билирубина более 250 мкмоль/л, полный ответ по коже и ЖКТ. На Д+237 в связи с развитием легочного кровотечения и переводом в ОРИТ – отмена базовой иммуносупрессивной терапии. На этом фоне наблюдались рост уровня билирубина до 580 мкмоль/л, кишечное кровотечение. Смена терапии на руксолитиниб, ингибитор Jak-2-киназы (20 мг/сут). Эффект: снижение уровня билирубина, РТПХ кишечника без динамики. На Д+249 трансплантация фекальной микробиоты, эффект: разрешение симптомов поражения ЖКТ. Повторные введения мезенхимальных стволовых клеток (Д+257,+266), без достижения ответа. Нарастание уровня холестерина более 40 ммоль/л с попытками терапии плазмаферезом дважды в неделю. На Д+350 выполнена биопсия печени с выявлением признаков РТПХ. C Д+316 по Д+426 пациент получил 5 введений тоцилизумаба, 12 сеансов экстракорпорального фотофереза, лечение сиролимусом и низкими дозами интерлейкина-2, без достижения эффекта (уровень билирубина 520-724 мкмоль/л). Терапия сиролимусом и руксолитинибом с Д+460 по Д+738. Смена руксолитиниба на ингибитор Jak-2 киназы нового поколения барицитиниб (4мг/сут) с Д+738. Эффект: уровень билирубина 220-420 мкмоль/л, однако, сохранялась гиперхолестеринемия. С Д+1120 барицитиниб был отменен. Эффект: снижение уровня билирубина (213 мкмоль/л) и холестерина (7,7 ммоль/л). Продолжается терапия сиролимусом, отмечается значимое улучшение качества жизни пациента. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Тяжелая срРТПХ печени – состояние, которое может потребовать применения длительной иммуносупрессивной терапии с невысокой вероятностью достижения полного ответа. Несмотря на доказанную эффективность ингибиторов Jak-2-киназ, данная терапия ассоциирована с серьезными неблагоприятными явлениями, в том числе, развитием тяжелой гиперхолестеринемии. Наличие синдрома Жильбера может затруднять оценку эффективности терапии, а также требовать проведения биопсии печени с целью возможного изменения подходов к лечению. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Cтероид-рефрактерная реакция «трансплантат против хозяина» (срРТПХ), overlap-синдром, ингибиторы Jak-2-киназ, синдром Жильбера, трансплантация фекальной микробиоты. </p>" ["ELEMENT_PREVIEW_PICTURE_FILE_TITLE"]=> string(269) "Клинический случай: эффект отмены терапии ингибитором Jak-2-киназы на стероид-рефрактерную реакцию трансплантат против хозяина с поражением печени" ["ELEMENT_DETAIL_PICTURE_FILE_ALT"]=> string(269) "Клинический случай: эффект отмены терапии ингибитором Jak-2-киназы на стероид-рефрактерную реакцию трансплантат против хозяина с поражением печени" ["ELEMENT_DETAIL_PICTURE_FILE_TITLE"]=> string(269) "Клинический случай: эффект отмены терапии ингибитором Jak-2-киназы на стероид-рефрактерную реакцию трансплантат против хозяина с поражением печени" ["SECTION_META_TITLE"]=> string(269) "Клинический случай: эффект отмены терапии ингибитором Jak-2-киназы на стероид-рефрактерную реакцию трансплантат против хозяина с поражением печени" ["SECTION_META_KEYWORDS"]=> string(269) "Клинический случай: эффект отмены терапии ингибитором Jak-2-киназы на стероид-рефрактерную реакцию трансплантат против хозяина с поражением печени" ["SECTION_META_DESCRIPTION"]=> string(269) "Клинический случай: эффект отмены терапии ингибитором Jak-2-киназы на стероид-рефрактерную реакцию трансплантат против хозяина с поражением печени" ["SECTION_PICTURE_FILE_ALT"]=> string(269) "Клинический случай: эффект отмены терапии ингибитором Jak-2-киназы на стероид-рефрактерную реакцию трансплантат против хозяина с поражением печени" ["SECTION_PICTURE_FILE_TITLE"]=> string(269) "Клинический случай: эффект отмены терапии ингибитором Jak-2-киназы на стероид-рефрактерную реакцию трансплантат против хозяина с поражением печени" ["SECTION_PICTURE_FILE_NAME"]=> string(100) "klinicheskiy-sluchay-effekt-otmeny-terapii-ingibitorom-jak-2-kinazy-na-steroid-refrakternuyu-reaktsi" ["SECTION_DETAIL_PICTURE_FILE_ALT"]=> string(269) "Клинический случай: эффект отмены терапии ингибитором Jak-2-киназы на стероид-рефрактерную реакцию трансплантат против хозяина с поражением печени" ["SECTION_DETAIL_PICTURE_FILE_TITLE"]=> string(269) "Клинический случай: эффект отмены терапии ингибитором Jak-2-киназы на стероид-рефрактерную реакцию трансплантат против хозяина с поражением печени" ["SECTION_DETAIL_PICTURE_FILE_NAME"]=> string(100) "klinicheskiy-sluchay-effekt-otmeny-terapii-ingibitorom-jak-2-kinazy-na-steroid-refrakternuyu-reaktsi" ["ELEMENT_PREVIEW_PICTURE_FILE_NAME"]=> string(100) "klinicheskiy-sluchay-effekt-otmeny-terapii-ingibitorom-jak-2-kinazy-na-steroid-refrakternuyu-reaktsi" ["ELEMENT_DETAIL_PICTURE_FILE_NAME"]=> string(100) "klinicheskiy-sluchay-effekt-otmeny-terapii-ingibitorom-jak-2-kinazy-na-steroid-refrakternuyu-reaktsi" } ["FIELDS"]=> array(1) { ["IBLOCK_SECTION_ID"]=> string(3) "111" } ["PROPERTIES"]=> array(18) { ["KEYWORDS"]=> array(36) { ["ID"]=> string(2) "19" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:46:01" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(27) "Ключевые слова" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "KEYWORDS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "19" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "4" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "Y" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "Y" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(27) "Ключевые слова" ["~DEFAULT_VALUE"]=> string(0) "" } ["SUBMITTED"]=> array(36) { ["ID"]=> string(2) "20" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Дата подачи" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "SUBMITTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "20" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Дата подачи" ["~DEFAULT_VALUE"]=> NULL } ["ACCEPTED"]=> array(36) { ["ID"]=> string(2) "21" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(25) "Дата принятия" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(8) "ACCEPTED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "21" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(25) "Дата принятия" ["~DEFAULT_VALUE"]=> NULL } ["PUBLISHED"]=> array(36) { ["ID"]=> string(2) "22" ["TIMESTAMP_X"]=> string(19) "2015-09-02 17:21:42" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Дата публикации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "PUBLISHED" ["DEFAULT_VALUE"]=> NULL ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "22" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(8) "DateTime" ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Дата публикации" ["~DEFAULT_VALUE"]=> NULL } ["CONTACT"]=> array(36) { ["ID"]=> string(2) "23" ["TIMESTAMP_X"]=> string(19) "2015-09-03 14:43:05" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(14) "Контакт" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "CONTACT" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "23" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(14) "Контакт" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHORS"]=> array(36) { ["ID"]=> string(2) "24" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:45:07" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "AUTHORS" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "E" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "Y" ["XML_ID"]=> string(2) "24" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "3" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(13) "EAutocomplete" ["USER_TYPE_SETTINGS"]=> array(9) { ["VIEW"]=> string(1) "E" ["SHOW_ADD"]=> string(1) "Y" ["MAX_WIDTH"]=> int(0) ["MIN_HEIGHT"]=> int(24) ["MAX_HEIGHT"]=> int(1000) ["BAN_SYM"]=> string(2) ",;" ["REP_SYM"]=> string(1) " " ["OTHER_REP_SYM"]=> string(0) "" ["IBLOCK_MESS"]=> string(1) "N" } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> bool(false) ["VALUE"]=> bool(false) ["DESCRIPTION"]=> bool(false) ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> bool(false) ["~DESCRIPTION"]=> bool(false) ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_RU"]=> array(36) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20725" ["VALUE"]=> array(2) { ["TEXT"]=> string(233) "Ксения П. Якимович, Ольга В. Пирогова, Олег В. Голощапов, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(233) "Ксения П. Якимович, Ольга В. Пирогова, Олег В. Голощапов, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_RU"]=> array(36) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20726" ["VALUE"]=> array(2) { ["TEXT"]=> string(482) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(482) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_RU"]=> array(36) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20727" ["VALUE"]=> array(2) { ["TEXT"]=> string(6961) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Стероид-рефрактерная РТПХ (срРТПХ) развивается в половине случаев РТПХ, с вероятностью летального исхода 70%. В качестве терапии спасения могут выступать ингибиторы Jak-2-киназ. Однако нет достоверных данных об оптимальной продолжительности терапии и стратегии отмены данных препаратов. Целью работы стало представление случая срРТПХ печени после гаплоидентичной трансплантации гемопоэтических стволовых клеток (гапло-ТГСК) у молодого пациента с синдромом Жильбера с улучшением показателей функции печени после отмены терапии ингибитором Jak-2-киназ. При анализе результатов были использованы данные медицинской документации, результаты лабораторных и инструментальных исследований. Стадии РТПХ оценивались согласно критериям NIH-2014. </p> <h2 style="text-align: justify;">Описание клинического случая</h2> <p style="text-align: justify;"> Пациент, 28 лет, с острым миелоидным лейкозом (ОМЛ), FAB-M2, и сопутствующим синдромом Жильбера 12.05.2015 перенес гапло-ТГСК от брата, 6/10. Режим кондиционирования: бусульфан (8 мг/кг), флударабин. Источник трансплантата: костный мозг. Профилактика РТПХ: циклофосфан (30 мг/кг, Д+3,+4), такролимус (с Д+5), микофенолата мофетил (45 мг/кг с Д+5 по Д+35). На Д+90 по причине развития раннего костно-мозгового рецидива – отмена такролимуса. На Д+202 развился overlap-синдром РТПХ 4 степени с поражением кожи, печени и нижних отделов ЖКТ (стадии 3, 4 и 3, соответственно). Терапия I линии: метилпреднизолон 2 мг/кг; эффект: частичный ответ по РТПХ кожи. К терапии были добавлены этанерцепт 25 мг 2 р/нед и такролимус. Эффект: уровень билирубина более 250 мкмоль/л, полный ответ по коже и ЖКТ. На Д+237 в связи с развитием легочного кровотечения и переводом в ОРИТ – отмена базовой иммуносупрессивной терапии. На этом фоне наблюдались рост уровня билирубина до 580 мкмоль/л, кишечное кровотечение. Смена терапии на руксолитиниб, ингибитор Jak-2-киназы (20 мг/сут). Эффект: снижение уровня билирубина, РТПХ кишечника без динамики. На Д+249 трансплантация фекальной микробиоты, эффект: разрешение симптомов поражения ЖКТ. Повторные введения мезенхимальных стволовых клеток (Д+257,+266), без достижения ответа. Нарастание уровня холестерина более 40 ммоль/л с попытками терапии плазмаферезом дважды в неделю. На Д+350 выполнена биопсия печени с выявлением признаков РТПХ. C Д+316 по Д+426 пациент получил 5 введений тоцилизумаба, 12 сеансов экстракорпорального фотофереза, лечение сиролимусом и низкими дозами интерлейкина-2, без достижения эффекта (уровень билирубина 520-724 мкмоль/л). Терапия сиролимусом и руксолитинибом с Д+460 по Д+738. Смена руксолитиниба на ингибитор Jak-2 киназы нового поколения барицитиниб (4мг/сут) с Д+738. Эффект: уровень билирубина 220-420 мкмоль/л, однако, сохранялась гиперхолестеринемия. С Д+1120 барицитиниб был отменен. Эффект: снижение уровня билирубина (213 мкмоль/л) и холестерина (7,7 ммоль/л). Продолжается терапия сиролимусом, отмечается значимое улучшение качества жизни пациента. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Тяжелая срРТПХ печени – состояние, которое может потребовать применения длительной иммуносупрессивной терапии с невысокой вероятностью достижения полного ответа. Несмотря на доказанную эффективность ингибиторов Jak-2-киназ, данная терапия ассоциирована с серьезными неблагоприятными явлениями, в том числе, развитием тяжелой гиперхолестеринемии. Наличие синдрома Жильбера может затруднять оценку эффективности терапии, а также требовать проведения биопсии печени с целью возможного изменения подходов к лечению. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Cтероид-рефрактерная реакция «трансплантат против хозяина» (срРТПХ), overlap-синдром, ингибиторы Jak-2-киназ, синдром Жильбера, трансплантация фекальной микробиоты. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6773) "
Введение
Стероид-рефрактерная РТПХ (срРТПХ) развивается в половине случаев РТПХ, с вероятностью летального исхода 70%. В качестве терапии спасения могут выступать ингибиторы Jak-2-киназ. Однако нет достоверных данных об оптимальной продолжительности терапии и стратегии отмены данных препаратов. Целью работы стало представление случая срРТПХ печени после гаплоидентичной трансплантации гемопоэтических стволовых клеток (гапло-ТГСК) у молодого пациента с синдромом Жильбера с улучшением показателей функции печени после отмены терапии ингибитором Jak-2-киназ. При анализе результатов были использованы данные медицинской документации, результаты лабораторных и инструментальных исследований. Стадии РТПХ оценивались согласно критериям NIH-2014.
Описание клинического случая
Пациент, 28 лет, с острым миелоидным лейкозом (ОМЛ), FAB-M2, и сопутствующим синдромом Жильбера 12.05.2015 перенес гапло-ТГСК от брата, 6/10. Режим кондиционирования: бусульфан (8 мг/кг), флударабин. Источник трансплантата: костный мозг. Профилактика РТПХ: циклофосфан (30 мг/кг, Д+3,+4), такролимус (с Д+5), микофенолата мофетил (45 мг/кг с Д+5 по Д+35). На Д+90 по причине развития раннего костно-мозгового рецидива – отмена такролимуса. На Д+202 развился overlap-синдром РТПХ 4 степени с поражением кожи, печени и нижних отделов ЖКТ (стадии 3, 4 и 3, соответственно). Терапия I линии: метилпреднизолон 2 мг/кг; эффект: частичный ответ по РТПХ кожи. К терапии были добавлены этанерцепт 25 мг 2 р/нед и такролимус. Эффект: уровень билирубина более 250 мкмоль/л, полный ответ по коже и ЖКТ. На Д+237 в связи с развитием легочного кровотечения и переводом в ОРИТ – отмена базовой иммуносупрессивной терапии. На этом фоне наблюдались рост уровня билирубина до 580 мкмоль/л, кишечное кровотечение. Смена терапии на руксолитиниб, ингибитор Jak-2-киназы (20 мг/сут). Эффект: снижение уровня билирубина, РТПХ кишечника без динамики. На Д+249 трансплантация фекальной микробиоты, эффект: разрешение симптомов поражения ЖКТ. Повторные введения мезенхимальных стволовых клеток (Д+257,+266), без достижения ответа. Нарастание уровня холестерина более 40 ммоль/л с попытками терапии плазмаферезом дважды в неделю. На Д+350 выполнена биопсия печени с выявлением признаков РТПХ. C Д+316 по Д+426 пациент получил 5 введений тоцилизумаба, 12 сеансов экстракорпорального фотофереза, лечение сиролимусом и низкими дозами интерлейкина-2, без достижения эффекта (уровень билирубина 520-724 мкмоль/л). Терапия сиролимусом и руксолитинибом с Д+460 по Д+738. Смена руксолитиниба на ингибитор Jak-2 киназы нового поколения барицитиниб (4мг/сут) с Д+738. Эффект: уровень билирубина 220-420 мкмоль/л, однако, сохранялась гиперхолестеринемия. С Д+1120 барицитиниб был отменен. Эффект: снижение уровня билирубина (213 мкмоль/л) и холестерина (7,7 ммоль/л). Продолжается терапия сиролимусом, отмечается значимое улучшение качества жизни пациента.
Заключение
Тяжелая срРТПХ печени – состояние, которое может потребовать применения длительной иммуносупрессивной терапии с невысокой вероятностью достижения полного ответа. Несмотря на доказанную эффективность ингибиторов Jak-2-киназ, данная терапия ассоциирована с серьезными неблагоприятными явлениями, в том числе, развитием тяжелой гиперхолестеринемии. Наличие синдрома Жильбера может затруднять оценку эффективности терапии, а также требовать проведения биопсии печени с целью возможного изменения подходов к лечению.
Ключевые слова
Cтероид-рефрактерная реакция «трансплантат против хозяина» (срРТПХ), overlap-синдром, ингибиторы Jak-2-киназ, синдром Жильбера, трансплантация фекальной микробиоты.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["DOI"]=> array(36) { ["ID"]=> string(2) "28" ["TIMESTAMP_X"]=> string(19) "2016-04-06 14:11:12" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(3) "DOI" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(3) "DOI" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "28" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(3) "DOI" ["~DEFAULT_VALUE"]=> string(0) "" } ["AUTHOR_EN"]=> array(36) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20728" ["VALUE"]=> array(2) { ["TEXT"]=> string(139) "Kseniya P. Yakimovich, Olga V. Pirogova, Oleg V. Goloshchapov, Elena I. Darskaya, Sergey N. Bondarenko, Ivan S. Moiseev, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(139) "Kseniya P. Yakimovich, Olga V. Pirogova, Oleg V. Goloshchapov, Elena I. Darskaya, Sergey N. Bondarenko, Ivan S. Moiseev, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["ORGANIZATION_EN"]=> array(36) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20729" ["VALUE"]=> array(2) { ["TEXT"]=> string(229) "R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(229) "R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["SUMMARY_EN"]=> array(36) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20730" ["VALUE"]=> array(2) { ["TEXT"]=> string(4185) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> The incidence of steroid-refractory graft versus host disease (SR-GVHD) is a one-half of patients with a mortality rate of 70%. Janus kinase (JAK) 1/2 inhibitors might be considered as a salvage therapy. However, there is a scarcity of relevant information about optimal duration and taping strategy of Jak-2-inhibitors. Our aim was to present a clinical case of a liver SR-GVHD after haploidentical HSCT (haplo-HSCT) in a young patient with Gilbert syndrome who developed decrease of liver function tests following discontinuation of Jak-2 kinase inhibitor therapy. Medical records, laboratory and instrumental data were reviewed when analyzing the results. GVHD severity was scored according to the 2014 NIH Consensus Criteria. </p> <h2 style="text-align: justify;">Case report</h2> <p style="text-align: justify;"> A 28-year-old male patient with acute myeloid leukemia (AML), FAB-M2, and concurrent Gilbert syndrome underwent haplo-HSCT on 12 May 2015 from brother, HLA compatibility, 6/10. Conditioning regimen: busulfan 8 mg/kg, fludarabine. Bone marrow was a source of stem cells:. GVHD prophylaxis: cyclophosphamide (30 mg/kg, days+3,+4), tacrolimus (from day+5), mycophenolate mofetil (45 mg/kg, days from +5 to +35). On day+90, tacrolimus was discontinued due to early bone marrow recurrence. On day+202, overlap-syndrome of grade 4 was developed, with skin, liver and lower gastrointestinal tract (GIT) lesions (grade 3, 4 and 3 respectively). The first-line therapy: methylprednisolone 2 mg/kg, causing partial response for skin. Etanercept (25 mg twice a day) and tacrolimus were added, followed by complete response for skin and GIT; bilirubin level was >250 μmol/L. The immunosuppressive therapy was discontinued on the day+237, due to pulmonary hemorrhage and transfer to intensive care unit. Increased bilirubin level (580 μmol/L) and intestinal bleeding were observed. This treatment was replaced by a Jak-2 inhibitor (ruxolitinib, 20 mg per day). The effect: decreased bilirubin level, without any dynamics for intestinal pathology. On day+249, fecal microbiota transplantation was performed, followed by resolution of GI symptoms. Mesenchymal stem cells were infused twice (D+257, D+266) with no response. Cholesterol levels raised over 40 mmol/L, having been treated bi-weekly plasmapheresis. From day+316 to day+426, the patient received 5 infusions of tocilizumab, he underwent 12 courses of extracorporeal photopheresis, sirolimus and low-dose interleukin-2, without any response (bilirubin 520 to 724 μmol/l). On day +350, liver biopsy was performed, and GVHD pathology was detected. Sirolimus and ruxolitinib were administered from day+460 to day+738. Ruxolitinib was replaced by a new-generation Jak-2 kinase inhibitor baricitinib (4 mg daily) on day+738. The following effect was observed: bilirubin level 220-420 mmol/L, hypercholesterolemia still persisted. On day+1120, baricitinib was discontinued. Further on, a decrease of bilirubin (213 μmol/L) and cholesterol levels (7.7 mmol/l) were documented. The therapy with sirolimus is going on, and significant improvement in the quality of life is noted. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Steroid-refractory severe chronic liver GVHD is a condition that might require prolonged immunosuppressive treatment with absence of complete response to current treatments. Despite high efficacy of JAK-2-inhibitors, they might be associated with serious adverse effects, like severe hypercholesterolemia. Gilbert syndrome may complicate the assessment of GVHD response and require liver biopsy to guide a therapy. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Steroid-refractory graft-versus-host disease (SR-GVHD), overlap syndrome, Jak-2-inhibitors, Gilbert syndrome, fecal microbiota transplantation </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3993) "Introduction
The incidence of steroid-refractory graft versus host disease (SR-GVHD) is a one-half of patients with a mortality rate of 70%. Janus kinase (JAK) 1/2 inhibitors might be considered as a salvage therapy. However, there is a scarcity of relevant information about optimal duration and taping strategy of Jak-2-inhibitors. Our aim was to present a clinical case of a liver SR-GVHD after haploidentical HSCT (haplo-HSCT) in a young patient with Gilbert syndrome who developed decrease of liver function tests following discontinuation of Jak-2 kinase inhibitor therapy. Medical records, laboratory and instrumental data were reviewed when analyzing the results. GVHD severity was scored according to the 2014 NIH Consensus Criteria.
Case report
A 28-year-old male patient with acute myeloid leukemia (AML), FAB-M2, and concurrent Gilbert syndrome underwent haplo-HSCT on 12 May 2015 from brother, HLA compatibility, 6/10. Conditioning regimen: busulfan 8 mg/kg, fludarabine. Bone marrow was a source of stem cells:. GVHD prophylaxis: cyclophosphamide (30 mg/kg, days+3,+4), tacrolimus (from day+5), mycophenolate mofetil (45 mg/kg, days from +5 to +35). On day+90, tacrolimus was discontinued due to early bone marrow recurrence. On day+202, overlap-syndrome of grade 4 was developed, with skin, liver and lower gastrointestinal tract (GIT) lesions (grade 3, 4 and 3 respectively). The first-line therapy: methylprednisolone 2 mg/kg, causing partial response for skin. Etanercept (25 mg twice a day) and tacrolimus were added, followed by complete response for skin and GIT; bilirubin level was >250 μmol/L. The immunosuppressive therapy was discontinued on the day+237, due to pulmonary hemorrhage and transfer to intensive care unit. Increased bilirubin level (580 μmol/L) and intestinal bleeding were observed. This treatment was replaced by a Jak-2 inhibitor (ruxolitinib, 20 mg per day). The effect: decreased bilirubin level, without any dynamics for intestinal pathology. On day+249, fecal microbiota transplantation was performed, followed by resolution of GI symptoms. Mesenchymal stem cells were infused twice (D+257, D+266) with no response. Cholesterol levels raised over 40 mmol/L, having been treated bi-weekly plasmapheresis. From day+316 to day+426, the patient received 5 infusions of tocilizumab, he underwent 12 courses of extracorporeal photopheresis, sirolimus and low-dose interleukin-2, without any response (bilirubin 520 to 724 μmol/l). On day +350, liver biopsy was performed, and GVHD pathology was detected. Sirolimus and ruxolitinib were administered from day+460 to day+738. Ruxolitinib was replaced by a new-generation Jak-2 kinase inhibitor baricitinib (4 mg daily) on day+738. The following effect was observed: bilirubin level 220-420 mmol/L, hypercholesterolemia still persisted. On day+1120, baricitinib was discontinued. Further on, a decrease of bilirubin (213 μmol/L) and cholesterol levels (7.7 mmol/l) were documented. The therapy with sirolimus is going on, and significant improvement in the quality of life is noted.
Conclusion
Steroid-refractory severe chronic liver GVHD is a condition that might require prolonged immunosuppressive treatment with absence of complete response to current treatments. Despite high efficacy of JAK-2-inhibitors, they might be associated with serious adverse effects, like severe hypercholesterolemia. Gilbert syndrome may complicate the assessment of GVHD response and require liver biopsy to guide a therapy.
Keywords
Steroid-refractory graft-versus-host disease (SR-GVHD), overlap syndrome, Jak-2-inhibitors, Gilbert syndrome, fecal microbiota transplantation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["NAME_EN"]=> array(36) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20731" ["VALUE"]=> string(126) "Case report: effect of Jak-2 kinase inhibitor discontinuation on chronic steroid-refractory graft-versus-host disease in liver" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(126) "Case report: effect of Jak-2 kinase inhibitor discontinuation on chronic steroid-refractory graft-versus-host disease in liver" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" } ["FULL_TEXT_RU"]=> array(36) { ["ID"]=> string(2) "42" ["TIMESTAMP_X"]=> string(19) "2015-09-07 20:29:18" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(23) "Полный текст" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(12) "FULL_TEXT_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "42" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(23) "Полный текст" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } } ["PDF_RU"]=> array(36) { ["ID"]=> string(2) "43" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF RUS" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_RU" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "43" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20835" ["VALUE"]=> string(4) "1474" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1474" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF RUS" ["~DEFAULT_VALUE"]=> string(0) "" } ["PDF_EN"]=> array(36) { ["ID"]=> string(2) "44" ["TIMESTAMP_X"]=> string(19) "2015-09-09 16:05:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(7) "PDF ENG" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(6) "PDF_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "F" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "44" ["FILE_TYPE"]=> string(18) "doc, txt, rtf, pdf" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20836" ["VALUE"]=> string(4) "1475" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(4) "1475" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(7) "PDF ENG" ["~DEFAULT_VALUE"]=> string(0) "" } ["NAME_LONG"]=> array(36) { ["ID"]=> string(2) "45" ["TIMESTAMP_X"]=> string(19) "2023-04-13 00:55:00" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(72) "Название (для очень длинных заголовков)" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "NAME_LONG" ["DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "45" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(80) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> NULL ["VALUE"]=> string(0) "" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(0) "" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(72) "Название (для очень длинных заголовков)" ["~DEFAULT_VALUE"]=> array(2) { ["TYPE"]=> string(4) "HTML" ["TEXT"]=> string(0) "" } } } ["DISPLAY_PROPERTIES"]=> array(7) { ["AUTHOR_EN"]=> array(37) { ["ID"]=> string(2) "37" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(6) "Author" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "37" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20728" ["VALUE"]=> array(2) { ["TEXT"]=> string(139) "Kseniya P. Yakimovich, Olga V. Pirogova, Oleg V. Goloshchapov, Elena I. Darskaya, Sergey N. Bondarenko, Ivan S. Moiseev, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(139) "Kseniya P. Yakimovich, Olga V. Pirogova, Oleg V. Goloshchapov, Elena I. Darskaya, Sergey N. Bondarenko, Ivan S. Moiseev, Boris V. Afanasyev" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(6) "Author" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(139) "Kseniya P. Yakimovich, Olga V. Pirogova, Oleg V. Goloshchapov, Elena I. Darskaya, Sergey N. Bondarenko, Ivan S. Moiseev, Boris V. Afanasyev" } ["SUMMARY_EN"]=> array(37) { ["ID"]=> string(2) "39" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(21) "Description / Summary" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "39" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20730" ["VALUE"]=> array(2) { ["TEXT"]=> string(4185) "<h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> The incidence of steroid-refractory graft versus host disease (SR-GVHD) is a one-half of patients with a mortality rate of 70%. Janus kinase (JAK) 1/2 inhibitors might be considered as a salvage therapy. However, there is a scarcity of relevant information about optimal duration and taping strategy of Jak-2-inhibitors. Our aim was to present a clinical case of a liver SR-GVHD after haploidentical HSCT (haplo-HSCT) in a young patient with Gilbert syndrome who developed decrease of liver function tests following discontinuation of Jak-2 kinase inhibitor therapy. Medical records, laboratory and instrumental data were reviewed when analyzing the results. GVHD severity was scored according to the 2014 NIH Consensus Criteria. </p> <h2 style="text-align: justify;">Case report</h2> <p style="text-align: justify;"> A 28-year-old male patient with acute myeloid leukemia (AML), FAB-M2, and concurrent Gilbert syndrome underwent haplo-HSCT on 12 May 2015 from brother, HLA compatibility, 6/10. Conditioning regimen: busulfan 8 mg/kg, fludarabine. Bone marrow was a source of stem cells:. GVHD prophylaxis: cyclophosphamide (30 mg/kg, days+3,+4), tacrolimus (from day+5), mycophenolate mofetil (45 mg/kg, days from +5 to +35). On day+90, tacrolimus was discontinued due to early bone marrow recurrence. On day+202, overlap-syndrome of grade 4 was developed, with skin, liver and lower gastrointestinal tract (GIT) lesions (grade 3, 4 and 3 respectively). The first-line therapy: methylprednisolone 2 mg/kg, causing partial response for skin. Etanercept (25 mg twice a day) and tacrolimus were added, followed by complete response for skin and GIT; bilirubin level was >250 μmol/L. The immunosuppressive therapy was discontinued on the day+237, due to pulmonary hemorrhage and transfer to intensive care unit. Increased bilirubin level (580 μmol/L) and intestinal bleeding were observed. This treatment was replaced by a Jak-2 inhibitor (ruxolitinib, 20 mg per day). The effect: decreased bilirubin level, without any dynamics for intestinal pathology. On day+249, fecal microbiota transplantation was performed, followed by resolution of GI symptoms. Mesenchymal stem cells were infused twice (D+257, D+266) with no response. Cholesterol levels raised over 40 mmol/L, having been treated bi-weekly plasmapheresis. From day+316 to day+426, the patient received 5 infusions of tocilizumab, he underwent 12 courses of extracorporeal photopheresis, sirolimus and low-dose interleukin-2, without any response (bilirubin 520 to 724 μmol/l). On day +350, liver biopsy was performed, and GVHD pathology was detected. Sirolimus and ruxolitinib were administered from day+460 to day+738. Ruxolitinib was replaced by a new-generation Jak-2 kinase inhibitor baricitinib (4 mg daily) on day+738. The following effect was observed: bilirubin level 220-420 mmol/L, hypercholesterolemia still persisted. On day+1120, baricitinib was discontinued. Further on, a decrease of bilirubin (213 μmol/L) and cholesterol levels (7.7 mmol/l) were documented. The therapy with sirolimus is going on, and significant improvement in the quality of life is noted. </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> Steroid-refractory severe chronic liver GVHD is a condition that might require prolonged immunosuppressive treatment with absence of complete response to current treatments. Despite high efficacy of JAK-2-inhibitors, they might be associated with serious adverse effects, like severe hypercholesterolemia. Gilbert syndrome may complicate the assessment of GVHD response and require liver biopsy to guide a therapy. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Steroid-refractory graft-versus-host disease (SR-GVHD), overlap syndrome, Jak-2-inhibitors, Gilbert syndrome, fecal microbiota transplantation </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(3993) "Introduction
The incidence of steroid-refractory graft versus host disease (SR-GVHD) is a one-half of patients with a mortality rate of 70%. Janus kinase (JAK) 1/2 inhibitors might be considered as a salvage therapy. However, there is a scarcity of relevant information about optimal duration and taping strategy of Jak-2-inhibitors. Our aim was to present a clinical case of a liver SR-GVHD after haploidentical HSCT (haplo-HSCT) in a young patient with Gilbert syndrome who developed decrease of liver function tests following discontinuation of Jak-2 kinase inhibitor therapy. Medical records, laboratory and instrumental data were reviewed when analyzing the results. GVHD severity was scored according to the 2014 NIH Consensus Criteria.
Case report
A 28-year-old male patient with acute myeloid leukemia (AML), FAB-M2, and concurrent Gilbert syndrome underwent haplo-HSCT on 12 May 2015 from brother, HLA compatibility, 6/10. Conditioning regimen: busulfan 8 mg/kg, fludarabine. Bone marrow was a source of stem cells:. GVHD prophylaxis: cyclophosphamide (30 mg/kg, days+3,+4), tacrolimus (from day+5), mycophenolate mofetil (45 mg/kg, days from +5 to +35). On day+90, tacrolimus was discontinued due to early bone marrow recurrence. On day+202, overlap-syndrome of grade 4 was developed, with skin, liver and lower gastrointestinal tract (GIT) lesions (grade 3, 4 and 3 respectively). The first-line therapy: methylprednisolone 2 mg/kg, causing partial response for skin. Etanercept (25 mg twice a day) and tacrolimus were added, followed by complete response for skin and GIT; bilirubin level was >250 μmol/L. The immunosuppressive therapy was discontinued on the day+237, due to pulmonary hemorrhage and transfer to intensive care unit. Increased bilirubin level (580 μmol/L) and intestinal bleeding were observed. This treatment was replaced by a Jak-2 inhibitor (ruxolitinib, 20 mg per day). The effect: decreased bilirubin level, without any dynamics for intestinal pathology. On day+249, fecal microbiota transplantation was performed, followed by resolution of GI symptoms. Mesenchymal stem cells were infused twice (D+257, D+266) with no response. Cholesterol levels raised over 40 mmol/L, having been treated bi-weekly plasmapheresis. From day+316 to day+426, the patient received 5 infusions of tocilizumab, he underwent 12 courses of extracorporeal photopheresis, sirolimus and low-dose interleukin-2, without any response (bilirubin 520 to 724 μmol/l). On day +350, liver biopsy was performed, and GVHD pathology was detected. Sirolimus and ruxolitinib were administered from day+460 to day+738. Ruxolitinib was replaced by a new-generation Jak-2 kinase inhibitor baricitinib (4 mg daily) on day+738. The following effect was observed: bilirubin level 220-420 mmol/L, hypercholesterolemia still persisted. On day+1120, baricitinib was discontinued. Further on, a decrease of bilirubin (213 μmol/L) and cholesterol levels (7.7 mmol/l) were documented. The therapy with sirolimus is going on, and significant improvement in the quality of life is noted.
Conclusion
Steroid-refractory severe chronic liver GVHD is a condition that might require prolonged immunosuppressive treatment with absence of complete response to current treatments. Despite high efficacy of JAK-2-inhibitors, they might be associated with serious adverse effects, like severe hypercholesterolemia. Gilbert syndrome may complicate the assessment of GVHD response and require liver biopsy to guide a therapy.
Keywords
Steroid-refractory graft-versus-host disease (SR-GVHD), overlap syndrome, Jak-2-inhibitors, Gilbert syndrome, fecal microbiota transplantation
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(21) "Description / Summary" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(3993) "Introduction
The incidence of steroid-refractory graft versus host disease (SR-GVHD) is a one-half of patients with a mortality rate of 70%. Janus kinase (JAK) 1/2 inhibitors might be considered as a salvage therapy. However, there is a scarcity of relevant information about optimal duration and taping strategy of Jak-2-inhibitors. Our aim was to present a clinical case of a liver SR-GVHD after haploidentical HSCT (haplo-HSCT) in a young patient with Gilbert syndrome who developed decrease of liver function tests following discontinuation of Jak-2 kinase inhibitor therapy. Medical records, laboratory and instrumental data were reviewed when analyzing the results. GVHD severity was scored according to the 2014 NIH Consensus Criteria.
Case report
A 28-year-old male patient with acute myeloid leukemia (AML), FAB-M2, and concurrent Gilbert syndrome underwent haplo-HSCT on 12 May 2015 from brother, HLA compatibility, 6/10. Conditioning regimen: busulfan 8 mg/kg, fludarabine. Bone marrow was a source of stem cells:. GVHD prophylaxis: cyclophosphamide (30 mg/kg, days+3,+4), tacrolimus (from day+5), mycophenolate mofetil (45 mg/kg, days from +5 to +35). On day+90, tacrolimus was discontinued due to early bone marrow recurrence. On day+202, overlap-syndrome of grade 4 was developed, with skin, liver and lower gastrointestinal tract (GIT) lesions (grade 3, 4 and 3 respectively). The first-line therapy: methylprednisolone 2 mg/kg, causing partial response for skin. Etanercept (25 mg twice a day) and tacrolimus were added, followed by complete response for skin and GIT; bilirubin level was >250 μmol/L. The immunosuppressive therapy was discontinued on the day+237, due to pulmonary hemorrhage and transfer to intensive care unit. Increased bilirubin level (580 μmol/L) and intestinal bleeding were observed. This treatment was replaced by a Jak-2 inhibitor (ruxolitinib, 20 mg per day). The effect: decreased bilirubin level, without any dynamics for intestinal pathology. On day+249, fecal microbiota transplantation was performed, followed by resolution of GI symptoms. Mesenchymal stem cells were infused twice (D+257, D+266) with no response. Cholesterol levels raised over 40 mmol/L, having been treated bi-weekly plasmapheresis. From day+316 to day+426, the patient received 5 infusions of tocilizumab, he underwent 12 courses of extracorporeal photopheresis, sirolimus and low-dose interleukin-2, without any response (bilirubin 520 to 724 μmol/l). On day +350, liver biopsy was performed, and GVHD pathology was detected. Sirolimus and ruxolitinib were administered from day+460 to day+738. Ruxolitinib was replaced by a new-generation Jak-2 kinase inhibitor baricitinib (4 mg daily) on day+738. The following effect was observed: bilirubin level 220-420 mmol/L, hypercholesterolemia still persisted. On day+1120, baricitinib was discontinued. Further on, a decrease of bilirubin (213 μmol/L) and cholesterol levels (7.7 mmol/l) were documented. The therapy with sirolimus is going on, and significant improvement in the quality of life is noted.
Conclusion
Steroid-refractory severe chronic liver GVHD is a condition that might require prolonged immunosuppressive treatment with absence of complete response to current treatments. Despite high efficacy of JAK-2-inhibitors, they might be associated with serious adverse effects, like severe hypercholesterolemia. Gilbert syndrome may complicate the assessment of GVHD response and require liver biopsy to guide a therapy.
Keywords
Steroid-refractory graft-versus-host disease (SR-GVHD), overlap syndrome, Jak-2-inhibitors, Gilbert syndrome, fecal microbiota transplantation
" } ["NAME_EN"]=> array(37) { ["ID"]=> string(2) "40" ["TIMESTAMP_X"]=> string(19) "2015-09-03 10:49:47" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(4) "Name" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(7) "NAME_EN" ["DEFAULT_VALUE"]=> string(0) "" ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "80" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "40" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "Y" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> NULL ["USER_TYPE_SETTINGS"]=> NULL ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20731" ["VALUE"]=> string(126) "Case report: effect of Jak-2 kinase inhibitor discontinuation on chronic steroid-refractory graft-versus-host disease in liver" ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> string(126) "Case report: effect of Jak-2 kinase inhibitor discontinuation on chronic steroid-refractory graft-versus-host disease in liver" ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(4) "Name" ["~DEFAULT_VALUE"]=> string(0) "" ["DISPLAY_VALUE"]=> string(126) "Case report: effect of Jak-2 kinase inhibitor discontinuation on chronic steroid-refractory graft-versus-host disease in liver" } ["ORGANIZATION_EN"]=> array(37) { ["ID"]=> string(2) "38" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:02:59" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Organization" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_EN" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "38" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20729" ["VALUE"]=> array(2) { ["TEXT"]=> string(229) "R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(229) "R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Organization" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(229) "R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation" } ["AUTHOR_RU"]=> array(37) { ["ID"]=> string(2) "25" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(12) "Авторы" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(9) "AUTHOR_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "25" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20725" ["VALUE"]=> array(2) { ["TEXT"]=> string(233) "Ксения П. Якимович, Ольга В. Пирогова, Олег В. Голощапов, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(233) "Ксения П. Якимович, Ольга В. Пирогова, Олег В. Голощапов, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(12) "Авторы" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(233) "Ксения П. Якимович, Ольга В. Пирогова, Олег В. Голощапов, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев" } ["SUMMARY_RU"]=> array(37) { ["ID"]=> string(2) "27" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(29) "Описание/Резюме" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(10) "SUMMARY_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "27" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20727" ["VALUE"]=> array(2) { ["TEXT"]=> string(6961) "<h2></h2> <h2 style="text-align: justify;">Введение</h2> <p style="text-align: justify;"> Стероид-рефрактерная РТПХ (срРТПХ) развивается в половине случаев РТПХ, с вероятностью летального исхода 70%. В качестве терапии спасения могут выступать ингибиторы Jak-2-киназ. Однако нет достоверных данных об оптимальной продолжительности терапии и стратегии отмены данных препаратов. Целью работы стало представление случая срРТПХ печени после гаплоидентичной трансплантации гемопоэтических стволовых клеток (гапло-ТГСК) у молодого пациента с синдромом Жильбера с улучшением показателей функции печени после отмены терапии ингибитором Jak-2-киназ. При анализе результатов были использованы данные медицинской документации, результаты лабораторных и инструментальных исследований. Стадии РТПХ оценивались согласно критериям NIH-2014. </p> <h2 style="text-align: justify;">Описание клинического случая</h2> <p style="text-align: justify;"> Пациент, 28 лет, с острым миелоидным лейкозом (ОМЛ), FAB-M2, и сопутствующим синдромом Жильбера 12.05.2015 перенес гапло-ТГСК от брата, 6/10. Режим кондиционирования: бусульфан (8 мг/кг), флударабин. Источник трансплантата: костный мозг. Профилактика РТПХ: циклофосфан (30 мг/кг, Д+3,+4), такролимус (с Д+5), микофенолата мофетил (45 мг/кг с Д+5 по Д+35). На Д+90 по причине развития раннего костно-мозгового рецидива – отмена такролимуса. На Д+202 развился overlap-синдром РТПХ 4 степени с поражением кожи, печени и нижних отделов ЖКТ (стадии 3, 4 и 3, соответственно). Терапия I линии: метилпреднизолон 2 мг/кг; эффект: частичный ответ по РТПХ кожи. К терапии были добавлены этанерцепт 25 мг 2 р/нед и такролимус. Эффект: уровень билирубина более 250 мкмоль/л, полный ответ по коже и ЖКТ. На Д+237 в связи с развитием легочного кровотечения и переводом в ОРИТ – отмена базовой иммуносупрессивной терапии. На этом фоне наблюдались рост уровня билирубина до 580 мкмоль/л, кишечное кровотечение. Смена терапии на руксолитиниб, ингибитор Jak-2-киназы (20 мг/сут). Эффект: снижение уровня билирубина, РТПХ кишечника без динамики. На Д+249 трансплантация фекальной микробиоты, эффект: разрешение симптомов поражения ЖКТ. Повторные введения мезенхимальных стволовых клеток (Д+257,+266), без достижения ответа. Нарастание уровня холестерина более 40 ммоль/л с попытками терапии плазмаферезом дважды в неделю. На Д+350 выполнена биопсия печени с выявлением признаков РТПХ. C Д+316 по Д+426 пациент получил 5 введений тоцилизумаба, 12 сеансов экстракорпорального фотофереза, лечение сиролимусом и низкими дозами интерлейкина-2, без достижения эффекта (уровень билирубина 520-724 мкмоль/л). Терапия сиролимусом и руксолитинибом с Д+460 по Д+738. Смена руксолитиниба на ингибитор Jak-2 киназы нового поколения барицитиниб (4мг/сут) с Д+738. Эффект: уровень билирубина 220-420 мкмоль/л, однако, сохранялась гиперхолестеринемия. С Д+1120 барицитиниб был отменен. Эффект: снижение уровня билирубина (213 мкмоль/л) и холестерина (7,7 ммоль/л). Продолжается терапия сиролимусом, отмечается значимое улучшение качества жизни пациента. </p> <h2 style="text-align: justify;">Заключение</h2> <p style="text-align: justify;"> Тяжелая срРТПХ печени – состояние, которое может потребовать применения длительной иммуносупрессивной терапии с невысокой вероятностью достижения полного ответа. Несмотря на доказанную эффективность ингибиторов Jak-2-киназ, данная терапия ассоциирована с серьезными неблагоприятными явлениями, в том числе, развитием тяжелой гиперхолестеринемии. Наличие синдрома Жильбера может затруднять оценку эффективности терапии, а также требовать проведения биопсии печени с целью возможного изменения подходов к лечению. </p> <h2 style="text-align: justify;">Ключевые слова</h2> <p style="text-align: justify;"> Cтероид-рефрактерная реакция «трансплантат против хозяина» (срРТПХ), overlap-синдром, ингибиторы Jak-2-киназ, синдром Жильбера, трансплантация фекальной микробиоты. </p>" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(6773) "Введение
Стероид-рефрактерная РТПХ (срРТПХ) развивается в половине случаев РТПХ, с вероятностью летального исхода 70%. В качестве терапии спасения могут выступать ингибиторы Jak-2-киназ. Однако нет достоверных данных об оптимальной продолжительности терапии и стратегии отмены данных препаратов. Целью работы стало представление случая срРТПХ печени после гаплоидентичной трансплантации гемопоэтических стволовых клеток (гапло-ТГСК) у молодого пациента с синдромом Жильбера с улучшением показателей функции печени после отмены терапии ингибитором Jak-2-киназ. При анализе результатов были использованы данные медицинской документации, результаты лабораторных и инструментальных исследований. Стадии РТПХ оценивались согласно критериям NIH-2014.
Описание клинического случая
Пациент, 28 лет, с острым миелоидным лейкозом (ОМЛ), FAB-M2, и сопутствующим синдромом Жильбера 12.05.2015 перенес гапло-ТГСК от брата, 6/10. Режим кондиционирования: бусульфан (8 мг/кг), флударабин. Источник трансплантата: костный мозг. Профилактика РТПХ: циклофосфан (30 мг/кг, Д+3,+4), такролимус (с Д+5), микофенолата мофетил (45 мг/кг с Д+5 по Д+35). На Д+90 по причине развития раннего костно-мозгового рецидива – отмена такролимуса. На Д+202 развился overlap-синдром РТПХ 4 степени с поражением кожи, печени и нижних отделов ЖКТ (стадии 3, 4 и 3, соответственно). Терапия I линии: метилпреднизолон 2 мг/кг; эффект: частичный ответ по РТПХ кожи. К терапии были добавлены этанерцепт 25 мг 2 р/нед и такролимус. Эффект: уровень билирубина более 250 мкмоль/л, полный ответ по коже и ЖКТ. На Д+237 в связи с развитием легочного кровотечения и переводом в ОРИТ – отмена базовой иммуносупрессивной терапии. На этом фоне наблюдались рост уровня билирубина до 580 мкмоль/л, кишечное кровотечение. Смена терапии на руксолитиниб, ингибитор Jak-2-киназы (20 мг/сут). Эффект: снижение уровня билирубина, РТПХ кишечника без динамики. На Д+249 трансплантация фекальной микробиоты, эффект: разрешение симптомов поражения ЖКТ. Повторные введения мезенхимальных стволовых клеток (Д+257,+266), без достижения ответа. Нарастание уровня холестерина более 40 ммоль/л с попытками терапии плазмаферезом дважды в неделю. На Д+350 выполнена биопсия печени с выявлением признаков РТПХ. C Д+316 по Д+426 пациент получил 5 введений тоцилизумаба, 12 сеансов экстракорпорального фотофереза, лечение сиролимусом и низкими дозами интерлейкина-2, без достижения эффекта (уровень билирубина 520-724 мкмоль/л). Терапия сиролимусом и руксолитинибом с Д+460 по Д+738. Смена руксолитиниба на ингибитор Jak-2 киназы нового поколения барицитиниб (4мг/сут) с Д+738. Эффект: уровень билирубина 220-420 мкмоль/л, однако, сохранялась гиперхолестеринемия. С Д+1120 барицитиниб был отменен. Эффект: снижение уровня билирубина (213 мкмоль/л) и холестерина (7,7 ммоль/л). Продолжается терапия сиролимусом, отмечается значимое улучшение качества жизни пациента.
Заключение
Тяжелая срРТПХ печени – состояние, которое может потребовать применения длительной иммуносупрессивной терапии с невысокой вероятностью достижения полного ответа. Несмотря на доказанную эффективность ингибиторов Jak-2-киназ, данная терапия ассоциирована с серьезными неблагоприятными явлениями, в том числе, развитием тяжелой гиперхолестеринемии. Наличие синдрома Жильбера может затруднять оценку эффективности терапии, а также требовать проведения биопсии печени с целью возможного изменения подходов к лечению.
Ключевые слова
Cтероид-рефрактерная реакция «трансплантат против хозяина» (срРТПХ), overlap-синдром, ингибиторы Jak-2-киназ, синдром Жильбера, трансплантация фекальной микробиоты.
" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(29) "Описание/Резюме" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(6773) "Введение
Стероид-рефрактерная РТПХ (срРТПХ) развивается в половине случаев РТПХ, с вероятностью летального исхода 70%. В качестве терапии спасения могут выступать ингибиторы Jak-2-киназ. Однако нет достоверных данных об оптимальной продолжительности терапии и стратегии отмены данных препаратов. Целью работы стало представление случая срРТПХ печени после гаплоидентичной трансплантации гемопоэтических стволовых клеток (гапло-ТГСК) у молодого пациента с синдромом Жильбера с улучшением показателей функции печени после отмены терапии ингибитором Jak-2-киназ. При анализе результатов были использованы данные медицинской документации, результаты лабораторных и инструментальных исследований. Стадии РТПХ оценивались согласно критериям NIH-2014.
Описание клинического случая
Пациент, 28 лет, с острым миелоидным лейкозом (ОМЛ), FAB-M2, и сопутствующим синдромом Жильбера 12.05.2015 перенес гапло-ТГСК от брата, 6/10. Режим кондиционирования: бусульфан (8 мг/кг), флударабин. Источник трансплантата: костный мозг. Профилактика РТПХ: циклофосфан (30 мг/кг, Д+3,+4), такролимус (с Д+5), микофенолата мофетил (45 мг/кг с Д+5 по Д+35). На Д+90 по причине развития раннего костно-мозгового рецидива – отмена такролимуса. На Д+202 развился overlap-синдром РТПХ 4 степени с поражением кожи, печени и нижних отделов ЖКТ (стадии 3, 4 и 3, соответственно). Терапия I линии: метилпреднизолон 2 мг/кг; эффект: частичный ответ по РТПХ кожи. К терапии были добавлены этанерцепт 25 мг 2 р/нед и такролимус. Эффект: уровень билирубина более 250 мкмоль/л, полный ответ по коже и ЖКТ. На Д+237 в связи с развитием легочного кровотечения и переводом в ОРИТ – отмена базовой иммуносупрессивной терапии. На этом фоне наблюдались рост уровня билирубина до 580 мкмоль/л, кишечное кровотечение. Смена терапии на руксолитиниб, ингибитор Jak-2-киназы (20 мг/сут). Эффект: снижение уровня билирубина, РТПХ кишечника без динамики. На Д+249 трансплантация фекальной микробиоты, эффект: разрешение симптомов поражения ЖКТ. Повторные введения мезенхимальных стволовых клеток (Д+257,+266), без достижения ответа. Нарастание уровня холестерина более 40 ммоль/л с попытками терапии плазмаферезом дважды в неделю. На Д+350 выполнена биопсия печени с выявлением признаков РТПХ. C Д+316 по Д+426 пациент получил 5 введений тоцилизумаба, 12 сеансов экстракорпорального фотофереза, лечение сиролимусом и низкими дозами интерлейкина-2, без достижения эффекта (уровень билирубина 520-724 мкмоль/л). Терапия сиролимусом и руксолитинибом с Д+460 по Д+738. Смена руксолитиниба на ингибитор Jak-2 киназы нового поколения барицитиниб (4мг/сут) с Д+738. Эффект: уровень билирубина 220-420 мкмоль/л, однако, сохранялась гиперхолестеринемия. С Д+1120 барицитиниб был отменен. Эффект: снижение уровня билирубина (213 мкмоль/л) и холестерина (7,7 ммоль/л). Продолжается терапия сиролимусом, отмечается значимое улучшение качества жизни пациента.
Заключение
Тяжелая срРТПХ печени – состояние, которое может потребовать применения длительной иммуносупрессивной терапии с невысокой вероятностью достижения полного ответа. Несмотря на доказанную эффективность ингибиторов Jak-2-киназ, данная терапия ассоциирована с серьезными неблагоприятными явлениями, в том числе, развитием тяжелой гиперхолестеринемии. Наличие синдрома Жильбера может затруднять оценку эффективности терапии, а также требовать проведения биопсии печени с целью возможного изменения подходов к лечению.
Ключевые слова
Cтероид-рефрактерная реакция «трансплантат против хозяина» (срРТПХ), overlap-синдром, ингибиторы Jak-2-киназ, синдром Жильбера, трансплантация фекальной микробиоты.
" } ["ORGANIZATION_RU"]=> array(37) { ["ID"]=> string(2) "26" ["TIMESTAMP_X"]=> string(19) "2015-09-02 18:01:20" ["IBLOCK_ID"]=> string(1) "2" ["NAME"]=> string(22) "Организации" ["ACTIVE"]=> string(1) "Y" ["SORT"]=> string(3) "500" ["CODE"]=> string(15) "ORGANIZATION_RU" ["DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["PROPERTY_TYPE"]=> string(1) "S" ["ROW_COUNT"]=> string(1) "1" ["COL_COUNT"]=> string(2) "30" ["LIST_TYPE"]=> string(1) "L" ["MULTIPLE"]=> string(1) "N" ["XML_ID"]=> string(2) "26" ["FILE_TYPE"]=> string(0) "" ["MULTIPLE_CNT"]=> string(1) "5" ["TMP_ID"]=> NULL ["LINK_IBLOCK_ID"]=> string(1) "0" ["WITH_DESCRIPTION"]=> string(1) "N" ["SEARCHABLE"]=> string(1) "N" ["FILTRABLE"]=> string(1) "N" ["IS_REQUIRED"]=> string(1) "N" ["VERSION"]=> string(1) "1" ["USER_TYPE"]=> string(4) "HTML" ["USER_TYPE_SETTINGS"]=> array(1) { ["height"]=> int(200) } ["HINT"]=> string(0) "" ["PROPERTY_VALUE_ID"]=> string(5) "20726" ["VALUE"]=> array(2) { ["TEXT"]=> string(482) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["DESCRIPTION"]=> string(0) "" ["VALUE_ENUM"]=> NULL ["VALUE_XML_ID"]=> NULL ["VALUE_SORT"]=> NULL ["~VALUE"]=> array(2) { ["TEXT"]=> string(482) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" ["TYPE"]=> string(4) "HTML" } ["~DESCRIPTION"]=> string(0) "" ["~NAME"]=> string(22) "Организации" ["~DEFAULT_VALUE"]=> array(2) { ["TEXT"]=> string(0) "" ["TYPE"]=> string(4) "HTML" } ["DISPLAY_VALUE"]=> string(482) "НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация" } } } }Короткие сообщения
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20434
[VALUE] => Array
(
[TEXT] => Светлана А. Гришкяне
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Светлана А. Гришкяне
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20435
[VALUE] => Array
(
[TEXT] => Университетский детский клинический госпиталь, Рига, Латвия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Университетский детский клинический госпиталь, Рига, Латвия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20436
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Роль аптеки в детской больнице и предоставляемые услуги сейчас значительно шире, чем 5 лет назад. Во всей Европе больницы стремятся переложить ответственность за приготовление препаратов, особенно стерильных, на фармацевтов, тем самым облегчив труд медсестер. Цель приготовления препаратов в больничной аптеке – получить качественный, стерильный, готовый для ввода пациенту препарат, приготовленный в особых, удобных и безопасных для работников условиях с соблюдением рационального использования медикаментов.
</p>
<h2 style="text-align: justify;">Цели</h2>
<p style="text-align: justify;">
Наши задачи были следующими: а) Выяснить, какие условия необходимо соблюсти для создания асептического блока в больничной аптеке. Изучить требования, необходимые проверки, проблемы; б) Выяснить, какие есть особенности безопасного и качественного приготовления и оборота в больнице цитотоксичных препаратов; в) Исследовать трудности приготовления антибиотиков для парэнтерального ввода в больничной аптеке; г) Исследовать нужды больницы и рецепты парэнтерального питания, его оборот и приготовление с помощью аппарата (компаундера).
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
А) Для работы асептического блока в больничной аптеке необходимы чистые помещения, специальная вентиляция, ламинарные шкафы, микробиологическая валидация, валидация работников, особенные одноразовые одежды и принадлежности, санитарный график. Чтобы не столкнуться с проблемами, рекомендуется заранее разработать проект с четкой целью, какие препараты аптека будет готовить. Б) Для цитотоксичных препаратов необходимо негативное давление в отдельном помещении для готовки, специальный ламинарный шкаф для цитотоксичных препаратов, защитные очки и маска, специальные перчатки, обученный персонал, специальные одноразовые принадлежности, в том числе закрытые системы переноса лекарств, а также может быть очень полезна программатура для приготовления и назначения препаратов. В) Обеспечивая парэнтеральными антибиотиками пациентов больницы можно столкнуться с разными проблемами, как то: плохой контакт с врачебным персоналом, частая смена доз антибиотиков, частая смена антибиотиков в связи с анализами, отмена уже приготовленных антибиотиков, короткая стабильность антибактериальных препаратов, а также отсутствие материальной выгоды в централизации готовки дешевых антибиотиков. Г) Пациентам больницы необходима как индивидуальная рецептура парэнтерального питания, так и стандартные смеси, введенные в пользование для младенцев, детей от 3 до 15 кг и от 15 до 30 кг. Компаундера улучшает качество рабочих условий персонала, уменьшает количество ручного труда, ускоряет время приготовления, но требует минимум двух человек для обслуживания.
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
У централизованного приготовления парэнтеральных препаратов в аптеке Детской больницы есть свои преимущества и недостатки. Одни из главных преимуществ – длительный срок годности приготовленных препаратов, безопасность приготовления токсичных лекарств для персонала, минимизация мануального труда работников, рациональное использование лекарственных средств. В больничной аптеке можно добиться нужного качества и условий приготовления, централизовав процесс, пройдя необходимые проверки, поддерживая уровень чистоты каждый день и наладив контакты с врачебным персоналом. Процесс можно бесконечно улучшать. Главные цели на будущее: обоюдное сотрудничество с врачебным персоналом, механизирование однообразных процессов, компьютеризирование всех рецептов, проверки несовместимостей препаратов и усовершенствование способа заказа препаратов врачами.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Парэнтеральное лечение, цитотоксические препараты, аптека, правила работы, логистика, детская больница.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Роль аптеки в детской больнице и предоставляемые услуги сейчас значительно шире, чем 5 лет назад. Во всей Европе больницы стремятся переложить ответственность за приготовление препаратов, особенно стерильных, на фармацевтов, тем самым облегчив труд медсестер. Цель приготовления препаратов в больничной аптеке – получить качественный, стерильный, готовый для ввода пациенту препарат, приготовленный в особых, удобных и безопасных для работников условиях с соблюдением рационального использования медикаментов.
Цели
Наши задачи были следующими: а) Выяснить, какие условия необходимо соблюсти для создания асептического блока в больничной аптеке. Изучить требования, необходимые проверки, проблемы; б) Выяснить, какие есть особенности безопасного и качественного приготовления и оборота в больнице цитотоксичных препаратов; в) Исследовать трудности приготовления антибиотиков для парэнтерального ввода в больничной аптеке; г) Исследовать нужды больницы и рецепты парэнтерального питания, его оборот и приготовление с помощью аппарата (компаундера).
Результаты
А) Для работы асептического блока в больничной аптеке необходимы чистые помещения, специальная вентиляция, ламинарные шкафы, микробиологическая валидация, валидация работников, особенные одноразовые одежды и принадлежности, санитарный график. Чтобы не столкнуться с проблемами, рекомендуется заранее разработать проект с четкой целью, какие препараты аптека будет готовить. Б) Для цитотоксичных препаратов необходимо негативное давление в отдельном помещении для готовки, специальный ламинарный шкаф для цитотоксичных препаратов, защитные очки и маска, специальные перчатки, обученный персонал, специальные одноразовые принадлежности, в том числе закрытые системы переноса лекарств, а также может быть очень полезна программатура для приготовления и назначения препаратов. В) Обеспечивая парэнтеральными антибиотиками пациентов больницы можно столкнуться с разными проблемами, как то: плохой контакт с врачебным персоналом, частая смена доз антибиотиков, частая смена антибиотиков в связи с анализами, отмена уже приготовленных антибиотиков, короткая стабильность антибактериальных препаратов, а также отсутствие материальной выгоды в централизации готовки дешевых антибиотиков. Г) Пациентам больницы необходима как индивидуальная рецептура парэнтерального питания, так и стандартные смеси, введенные в пользование для младенцев, детей от 3 до 15 кг и от 15 до 30 кг. Компаундера улучшает качество рабочих условий персонала, уменьшает количество ручного труда, ускоряет время приготовления, но требует минимум двух человек для обслуживания.
Выводы
У централизованного приготовления парэнтеральных препаратов в аптеке Детской больницы есть свои преимущества и недостатки. Одни из главных преимуществ – длительный срок годности приготовленных препаратов, безопасность приготовления токсичных лекарств для персонала, минимизация мануального труда работников, рациональное использование лекарственных средств. В больничной аптеке можно добиться нужного качества и условий приготовления, централизовав процесс, пройдя необходимые проверки, поддерживая уровень чистоты каждый день и наладив контакты с врачебным персоналом. Процесс можно бесконечно улучшать. Главные цели на будущее: обоюдное сотрудничество с врачебным персоналом, механизирование однообразных процессов, компьютеризирование всех рецептов, проверки несовместимостей препаратов и усовершенствование способа заказа препаратов врачами.
Ключевые слова
Парэнтеральное лечение, цитотоксические препараты, аптека, правила работы, логистика, детская больница.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20437
[VALUE] => Array
(
[TEXT] => Svetlana A. Griskjane
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Svetlana A. Griskjane
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20438
[VALUE] => Array
(
[TEXT] => Children’s Clinical University Hospital, Riga, Latvija
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Children’s Clinical University Hospital, Riga, Latvija
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20439
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
The role of pharmacy in the Children’s Hospital and the services provided are now much wider than 5 years ago. In Europe hospitals are trying to shift the responsibility for preparing drugs, especially sterile ones, for pharmacists, thereby facilitating the work of nurses. The purpose of preparing drugs in a hospital pharmacy is to obtain a high-quality, sterile, ready-for-use medication prepared in special, convenient and safe conditions for workers, ensuring rational use of medicines.
</p>
<h2 style="text-align: justify;">Aims</h2>
<p style="text-align: justify;">
Our aims were as follows: (a) To find out what conditions must be met to create an aseptic unit in a hospital pharmacy, to study appropriate requirements, necessary inspections, current problems; (b) To assess features of safe and quality preparation and turnover of cytotoxic drugs in the hospital; (c) To investigate the difficulties of preparing antibiotics for parenteral administration in a hospital pharmacy, and (d) To investigate the needs of the hospital and variety of prescriptions of parenteral nutrition, their turnover and preparation with automatic compounder device.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
(a) For aseptic unit in a hospital pharmacy clean room, special ventilation, laminar flow cabinets, microbiological validation, validation of employees, special disposable clothing and accessories, sanitary schedule are necessary. In order not to face problems, it is recommended to develop a project in advance with a clear goal, which preparations the pharmacy will prepare. (b) For cytotoxic drugs, negative pressure is required in a separate preparation area, a special laminar flow cabinet for cytotoxic drugs, goggles and a mask, special gloves, trained personnel, special disposable supplies, including closed drug transfer systems, and also a program for preparation and prescription of drugs could be useful. (c) Providing parenteral antibiotics to hospital patients can face various problems, such as: poor contact with medical staff, frequent changes of antibiotic doses, frequent changes in antibiotics due to analysis, cancellation of already prepared antibiotics, short stability of antibacterial drugs, and lack of material benefit in centralized preparation of cheap antibiotics. (d) The patients at the hospital need both individual formulas of parenteral nutrition, and standard mixtures introduced for administration to infants, children from 3 to 15 kg and from 15 to 30 kg body mass. The compounder devices improve quality of working conditions for personnel, reduce the amount of manual labor, speed up the preparation time, but require a minimum of two persons for their maintenance.
</p>
<h2 style="text-align: justify;">Conclusions</h2>
<p style="text-align: justify;">
The centralized preparation of parenteral drugs at the pharmacy of the Children’s Hospital has its advantages and disadvantages. One of the main advantages is the long shelf-life of the prepared medications, the safety of preparation of toxic drugs for personnel, the minimization of the manual labor for employees, the rational use of medicines. In the hospital pharmacy, you can achieve the desired quality and preparation conditions, centralizing the process, passing the required checks, maintaining purity levels every day, and establishing contacts with medical personnel. The process can be improved permanently. The main future goals are as follows: mutual cooperation with medical personnel, mechanization of monotonous processes, computer-assisted support of all prescriptions, incompatibility checking, and improving the way of ordering drugs by the doctors.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Parenteral treatment, cytotoxic preparations, pharmacy, working regulations, logistics, pediatric hospital.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
The role of pharmacy in the Children’s Hospital and the services provided are now much wider than 5 years ago. In Europe hospitals are trying to shift the responsibility for preparing drugs, especially sterile ones, for pharmacists, thereby facilitating the work of nurses. The purpose of preparing drugs in a hospital pharmacy is to obtain a high-quality, sterile, ready-for-use medication prepared in special, convenient and safe conditions for workers, ensuring rational use of medicines.
Aims
Our aims were as follows: (a) To find out what conditions must be met to create an aseptic unit in a hospital pharmacy, to study appropriate requirements, necessary inspections, current problems; (b) To assess features of safe and quality preparation and turnover of cytotoxic drugs in the hospital; (c) To investigate the difficulties of preparing antibiotics for parenteral administration in a hospital pharmacy, and (d) To investigate the needs of the hospital and variety of prescriptions of parenteral nutrition, their turnover and preparation with automatic compounder device.
Results
(a) For aseptic unit in a hospital pharmacy clean room, special ventilation, laminar flow cabinets, microbiological validation, validation of employees, special disposable clothing and accessories, sanitary schedule are necessary. In order not to face problems, it is recommended to develop a project in advance with a clear goal, which preparations the pharmacy will prepare. (b) For cytotoxic drugs, negative pressure is required in a separate preparation area, a special laminar flow cabinet for cytotoxic drugs, goggles and a mask, special gloves, trained personnel, special disposable supplies, including closed drug transfer systems, and also a program for preparation and prescription of drugs could be useful. (c) Providing parenteral antibiotics to hospital patients can face various problems, such as: poor contact with medical staff, frequent changes of antibiotic doses, frequent changes in antibiotics due to analysis, cancellation of already prepared antibiotics, short stability of antibacterial drugs, and lack of material benefit in centralized preparation of cheap antibiotics. (d) The patients at the hospital need both individual formulas of parenteral nutrition, and standard mixtures introduced for administration to infants, children from 3 to 15 kg and from 15 to 30 kg body mass. The compounder devices improve quality of working conditions for personnel, reduce the amount of manual labor, speed up the preparation time, but require a minimum of two persons for their maintenance.
Conclusions
The centralized preparation of parenteral drugs at the pharmacy of the Children’s Hospital has its advantages and disadvantages. One of the main advantages is the long shelf-life of the prepared medications, the safety of preparation of toxic drugs for personnel, the minimization of the manual labor for employees, the rational use of medicines. In the hospital pharmacy, you can achieve the desired quality and preparation conditions, centralizing the process, passing the required checks, maintaining purity levels every day, and establishing contacts with medical personnel. The process can be improved permanently. The main future goals are as follows: mutual cooperation with medical personnel, mechanization of monotonous processes, computer-assisted support of all prescriptions, incompatibility checking, and improving the way of ordering drugs by the doctors.
Keywords
Parenteral treatment, cytotoxic preparations, pharmacy, working regulations, logistics, pediatric hospital.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20440
[VALUE] => Preparation of parenteral medications in Riga Children’s Clinical University Hospital’s pharmacy
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Preparation of parenteral medications in Riga Children’s Clinical University Hospital’s pharmacy
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20767
[VALUE] => 1403
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1403
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20768
[VALUE] => 1404
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1404
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Светлана А. Гришкяне
Введение
Роль аптеки в детской больнице и предоставляемые услуги сейчас значительно шире, чем 5 лет назад. Во всей Европе больницы стремятся переложить ответственность за приготовление препаратов, особенно стерильных, на фармацевтов, тем самым облегчив труд медсестер. Цель приготовления препаратов в больничной аптеке – получить качественный, стерильный, готовый для ввода пациенту препарат, приготовленный в особых, удобных и безопасных для работников условиях с соблюдением рационального использования медикаментов.
Цели
Наши задачи были следующими: а) Выяснить, какие условия необходимо соблюсти для создания асептического блока в больничной аптеке. Изучить требования, необходимые проверки, проблемы; б) Выяснить, какие есть особенности безопасного и качественного приготовления и оборота в больнице цитотоксичных препаратов; в) Исследовать трудности приготовления антибиотиков для парэнтерального ввода в больничной аптеке; г) Исследовать нужды больницы и рецепты парэнтерального питания, его оборот и приготовление с помощью аппарата (компаундера).
Результаты
А) Для работы асептического блока в больничной аптеке необходимы чистые помещения, специальная вентиляция, ламинарные шкафы, микробиологическая валидация, валидация работников, особенные одноразовые одежды и принадлежности, санитарный график. Чтобы не столкнуться с проблемами, рекомендуется заранее разработать проект с четкой целью, какие препараты аптека будет готовить. Б) Для цитотоксичных препаратов необходимо негативное давление в отдельном помещении для готовки, специальный ламинарный шкаф для цитотоксичных препаратов, защитные очки и маска, специальные перчатки, обученный персонал, специальные одноразовые принадлежности, в том числе закрытые системы переноса лекарств, а также может быть очень полезна программатура для приготовления и назначения препаратов. В) Обеспечивая парэнтеральными антибиотиками пациентов больницы можно столкнуться с разными проблемами, как то: плохой контакт с врачебным персоналом, частая смена доз антибиотиков, частая смена антибиотиков в связи с анализами, отмена уже приготовленных антибиотиков, короткая стабильность антибактериальных препаратов, а также отсутствие материальной выгоды в централизации готовки дешевых антибиотиков. Г) Пациентам больницы необходима как индивидуальная рецептура парэнтерального питания, так и стандартные смеси, введенные в пользование для младенцев, детей от 3 до 15 кг и от 15 до 30 кг. Компаундера улучшает качество рабочих условий персонала, уменьшает количество ручного труда, ускоряет время приготовления, но требует минимум двух человек для обслуживания.
Выводы
У централизованного приготовления парэнтеральных препаратов в аптеке Детской больницы есть свои преимущества и недостатки. Одни из главных преимуществ – длительный срок годности приготовленных препаратов, безопасность приготовления токсичных лекарств для персонала, минимизация мануального труда работников, рациональное использование лекарственных средств. В больничной аптеке можно добиться нужного качества и условий приготовления, централизовав процесс, пройдя необходимые проверки, поддерживая уровень чистоты каждый день и наладив контакты с врачебным персоналом. Процесс можно бесконечно улучшать. Главные цели на будущее: обоюдное сотрудничество с врачебным персоналом, механизирование однообразных процессов, компьютеризирование всех рецептов, проверки несовместимостей препаратов и усовершенствование способа заказа препаратов врачами.
Ключевые слова
Парэнтеральное лечение, цитотоксические препараты, аптека, правила работы, логистика, детская больница.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20443
[VALUE] => Array
(
[TEXT] => Никита В. Грудинин <sup>1</sup>, Вадим Е. Карев <sup>2</sup>, Николай С. Буненков <sup>3</sup>, Владимир В. Комок <sup>3</sup>, Валерия А. Костевич <sup>4</sup>, Николай П. Горбунов <sup>4</sup>, Алексей В. Соколов <sup>4</sup>, Андрей А. Карпов <sup>3</sup>, Кирилл В. Лепик <sup>3</sup>, Александр Н. Швецов <sup>3</sup>, Юрий А. Серов <sup>3</sup>, Олег В. Галибин <sup>3</sup>, Александр С. Немков <sup>3</sup>, Геннадий Г. Хубулава <sup>3</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Никита В. Грудинин 1, Вадим Е. Карев 2, Николай С. Буненков 3, Владимир В. Комок 3, Валерия А. Костевич 4, Николай П. Горбунов 4, Алексей В. Соколов 4, Андрей А. Карпов 3, Кирилл В. Лепик 3, Александр Н. Швецов 3, Юрий А. Серов 3, Олег В. Галибин 3, Александр С. Немков 3, Геннадий Г. Хубулава 3
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20444
[VALUE] => Array
(
[TEXT] => <sup>1</sup> НМИЦ трансплантологии и искусственных органов имени академика В. И. Шумакова, Москва, Россия
<sup>2</sup> ФГБУ Детский научно-клинический центр инфекционных болезней ФМБУ РФ, Санкт-Петербург, Россия
<sup>3</sup> Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова
<sup>4</sup> ФГБНУ институт экспериментальной медицины, Санкт-Петербург, Россия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 НМИЦ трансплантологии и искусственных органов имени академика В. И. Шумакова, Москва, Россия
2 ФГБУ Детский научно-клинический центр инфекционных болезней ФМБУ РФ, Санкт-Петербург, Россия
3 Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова
4 ФГБНУ институт экспериментальной медицины, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20445
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Одним из эффективных методов лечения тяжелой сердечной недостаточности является трансплантация сердца. Тем не менее, не решенной проблемой является отторжение трансплантата. Актуальным является изучение гистологических и молекулярных иммунных механизмов отторжения трансплантата.
</p>
<h2 style="text-align: justify;">Цель</h2>
<p style="text-align: justify;">
Цель работы состояла в оценке гистологических изменений трансплантата после гетеротопической трансплантации сердца, а также изменения в плазме крови реципиента.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
Двум белым новозеландским кроликам выполнена гетеротопическая трансплантация сердца в брюшную полость, после чего, ежедневно выполнялось измерение миелопероксидазы в плазме крови. Один кролик получал циклоспорин А в дозировке 10 мг/кг в сутки, другой кролик был без иммуносупрессивной терапии. После гибели кроликов выполнено гистологическое исследование пересаженных сердец.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Получены данные о динамике миелопероксидазы лейкоцитов после трансплантации сердца и гистологических изменениях в виде дистрофии и кальциноза миокарда в пересаженном сердце у кролика, не получавшего иммуносупрессию. В трансплантате кролика, получавшего циклоспорин А, признаков кальциноза или дистрофии не наблюдалось.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Гетеротопическая трансплантация сердца, миелопероксидаза, маркеры отторжения трансплантата.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Одним из эффективных методов лечения тяжелой сердечной недостаточности является трансплантация сердца. Тем не менее, не решенной проблемой является отторжение трансплантата. Актуальным является изучение гистологических и молекулярных иммунных механизмов отторжения трансплантата.
Цель
Цель работы состояла в оценке гистологических изменений трансплантата после гетеротопической трансплантации сердца, а также изменения в плазме крови реципиента.
Материалы и методы
Двум белым новозеландским кроликам выполнена гетеротопическая трансплантация сердца в брюшную полость, после чего, ежедневно выполнялось измерение миелопероксидазы в плазме крови. Один кролик получал циклоспорин А в дозировке 10 мг/кг в сутки, другой кролик был без иммуносупрессивной терапии. После гибели кроликов выполнено гистологическое исследование пересаженных сердец.
Результаты
Получены данные о динамике миелопероксидазы лейкоцитов после трансплантации сердца и гистологических изменениях в виде дистрофии и кальциноза миокарда в пересаженном сердце у кролика, не получавшего иммуносупрессию. В трансплантате кролика, получавшего циклоспорин А, признаков кальциноза или дистрофии не наблюдалось.
Ключевые слова
Гетеротопическая трансплантация сердца, миелопероксидаза, маркеры отторжения трансплантата.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20446
[VALUE] => Array
(
[TEXT] => Nikita V. Grudinin <sup>1</sup>, Vadim E. Karev <sup>2</sup>, Nikolai S. Bunenkov <sup>1</sup>, Vladimir V. Komok <sup>3</sup>, Valeria V. Kostevitch <sup>4</sup>, Nikolai P. Gorbunov <sup>4</sup>, Alexei V. Sokolov <sup>4</sup>, Andrey A. Karpov <sup>3</sup>, Kirill V. Lepik <sup>3</sup>, Alexander N. Shvetsov <sup>3</sup>, Youri A. Serov <sup>3</sup>, Oleg V. Galibin <sup>3</sup>, Alexander S. Nemkov <sup>3</sup>, Gennadiy G. Khubulava <sup>3</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Nikita V. Grudinin 1, Vadim E. Karev 2, Nikolai S. Bunenkov 1, Vladimir V. Komok 3, Valeria V. Kostevitch 4, Nikolai P. Gorbunov 4, Alexei V. Sokolov 4, Andrey A. Karpov 3, Kirill V. Lepik 3, Alexander N. Shvetsov 3, Youri A. Serov 3, Oleg V. Galibin 3, Alexander S. Nemkov 3, Gennadiy G. Khubulava 3
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20447
[VALUE] => Array
(
[TEXT] => <sup>1</sup> V. I. Shumakov Federal Research Center of Transplantology and Artificial Organs, Moscow, Russia
<sup>2</sup> St. Petersburg Research Institute of Children’s Infections
<sup>3</sup> The First Pavlov State Medical University of St. Petersburg
<sup>4</sup> St. Petersburg Institute of Experimental Medicine, St. Petersburg, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 V. I. Shumakov Federal Research Center of Transplantology and Artificial Organs, Moscow, Russia
2 St. Petersburg Research Institute of Children’s Infections
3 The First Pavlov State Medical University of St. Petersburg
4 St. Petersburg Institute of Experimental Medicine, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20448
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
One of the effective methods for treating severe heart failure is the heart transplantation. On the other hand, the unresolved problem is the rejection of the graft. The study of histological and molecular immune mechanisms of graft rejection is significant.
</p>
<h2 style="text-align: justify;">Aim</h2>
<p style="text-align: justify;">
Objective of the study was to evaluate the histological changes of the graft after heterotopic heart transplantation, as well as changes in the blood plasma of the recipient.
</p>
<h2 style="text-align: justify;">Materials and methods</h2>
<p style="text-align: justify;">
Two white New Zealand’s rabbits underwent heterotopic heart transplantation, after which a daily measurement of myeloperoxidase in the blood plasma performed. One rabbit received cyclosporine A at a dosage of 10 mg/kg per day and another rabbit was immunosuppressive. The histological examination of transplanted hearts was performed after the rabbits were deceased.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Data on the dynamics of leukocyte myeloperoxidase were obtained after cardiac transplantation and histological changes in the transplanted heart. There are calcification and dystrophy in transplanted heart found in a rabbit without immunosuppression. No signs of graft calcinosis or dystrophy were observed in the cyclosporine-treated animal.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Heterotopic heart transplantation, myeloperoxidase, markers of the graft rejection.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
One of the effective methods for treating severe heart failure is the heart transplantation. On the other hand, the unresolved problem is the rejection of the graft. The study of histological and molecular immune mechanisms of graft rejection is significant.
Aim
Objective of the study was to evaluate the histological changes of the graft after heterotopic heart transplantation, as well as changes in the blood plasma of the recipient.
Materials and methods
Two white New Zealand’s rabbits underwent heterotopic heart transplantation, after which a daily measurement of myeloperoxidase in the blood plasma performed. One rabbit received cyclosporine A at a dosage of 10 mg/kg per day and another rabbit was immunosuppressive. The histological examination of transplanted hearts was performed after the rabbits were deceased.
Results
Data on the dynamics of leukocyte myeloperoxidase were obtained after cardiac transplantation and histological changes in the transplanted heart. There are calcification and dystrophy in transplanted heart found in a rabbit without immunosuppression. No signs of graft calcinosis or dystrophy were observed in the cyclosporine-treated animal.
Keywords
Heterotopic heart transplantation, myeloperoxidase, markers of the graft rejection.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20449
[VALUE] => Histological features and blood plasma changes after heterotopic heart transplantation
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Histological features and blood plasma changes after heterotopic heart transplantation
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20769
[VALUE] => 1405
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1405
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20770
[VALUE] => 1406
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1406
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Никита В. Грудинин 1, Вадим Е. Карев 2, Николай С. Буненков 3, Владимир В. Комок 3, Валерия А. Костевич 4, Николай П. Горбунов 4, Алексей В. Соколов 4, Андрей А. Карпов 3, Кирилл В. Лепик 3, Александр Н. Швецов 3, Юрий А. Серов 3, Олег В. Галибин 3, Александр С. Немков 3, Геннадий Г. Хубулава 3
Введение
Одним из эффективных методов лечения тяжелой сердечной недостаточности является трансплантация сердца. Тем не менее, не решенной проблемой является отторжение трансплантата. Актуальным является изучение гистологических и молекулярных иммунных механизмов отторжения трансплантата.
Цель
Цель работы состояла в оценке гистологических изменений трансплантата после гетеротопической трансплантации сердца, а также изменения в плазме крови реципиента.
Материалы и методы
Двум белым новозеландским кроликам выполнена гетеротопическая трансплантация сердца в брюшную полость, после чего, ежедневно выполнялось измерение миелопероксидазы в плазме крови. Один кролик получал циклоспорин А в дозировке 10 мг/кг в сутки, другой кролик был без иммуносупрессивной терапии. После гибели кроликов выполнено гистологическое исследование пересаженных сердец.
Результаты
Получены данные о динамике миелопероксидазы лейкоцитов после трансплантации сердца и гистологических изменениях в виде дистрофии и кальциноза миокарда в пересаженном сердце у кролика, не получавшего иммуносупрессию. В трансплантате кролика, получавшего циклоспорин А, признаков кальциноза или дистрофии не наблюдалось.
Ключевые слова
Гетеротопическая трансплантация сердца, миелопероксидаза, маркеры отторжения трансплантата.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20425
[VALUE] => Array
(
[TEXT] => Олег В. Голощапов <sup>1</sup>, Максим А. Кучер <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Александр Н. Швецов <sup>1</sup>, Руслана В. Клементьева <sup>1</sup>, Александр А. Щербаков <sup>1</sup>, Сергей В. Сидоренко <sup>2</sup>, Владимир А. Гостев <sup>2</sup>, Мария А. Суворова <sup>3</sup>, Оксана В. Станевич <sup>1</sup>, Евгений А. Бакин <sup>1</sup>, Алексей Б. Чухловин <sup>1</sup>, Людмила С. Зубаровская <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Олег В. Голощапов 1, Максим А. Кучер 1, Иван С. Моисеев 1, Александр Н. Швецов 1, Руслана В. Клементьева 1, Александр А. Щербаков 1, Сергей В. Сидоренко 2, Владимир А. Гостев 2, Мария А. Суворова 3, Оксана В. Станевич 1, Евгений А. Бакин 1, Алексей Б. Чухловин 1, Людмила С. Зубаровская 1, Борис В. Афанасьев 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20426
[VALUE] => Array
(
[TEXT] => <sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
<sup>2</sup> ФГБУ Детский научно-клинический центр инфекционных болезней, Санкт-Петербург, Россия
<sup>3</sup> Научно-исследовательская лаборатория Explana, Санкт-Петербург, Россия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
2 ФГБУ Детский научно-клинический центр инфекционных болезней, Санкт-Петербург, Россия
3 Научно-исследовательская лаборатория Explana, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20427
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод терапии онкологических, гематологических и наследственных заболеваний. Распространенными осложнениями алло-ТГСК, которые приводят к снижению эффективности лечения, являются: инфекционное поражение желудочно-кишечного тракта вирусной этиологии и/или ассоциированное с Clostridium difficile на фоне иммунодефицита; антибиотикассоциированная диарея; реакция трансплантат против хозяина (РТПХ). Трансплантация фекальной микробиоты (ТФМ) от здорового донора может приводить к эрадикации патогенных микроорганизмов, модуляции иммунной системы реципиента и как следствие к снижению активности РТПХ кишечника. Целью работы является повыщение эффективности лечения осложнений у пациентов после алло-ТГСК ассоциированных с Clostridium difficile и РТПХ кишечника.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
С 2015 по 2018 год в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой в одноцентровое, проспективное исследование включено 11 пациентов после алло-ТГСК от неродственного донора – 36,5% (n=4), родственного – 9% (n=1), гаплоидентичного – 54,5% (n=6) с целью терапии острого лимфобластного лейкоза – 18,3% (n=2), острого миелоидного лейкоза – 27,4% (n=3), миелодиспластического синдрома – 18,3% (n=2), бета-талассемии – 9% (n=1), хронического миелолейкоза – 9% (n=1), Лимфомы Ходжкина – 9% (n=1), анемии Фанкони – 9% (n=1). Для лечения посттрансплантационных осложнений всем пациентам была выполнена ТФМ. Медиана возраста составила 24 года (2-45). Из исследования исключено трое больных из-за нарушения техники ТФМ (n=2), развития тяжелого синдрома системного воспалительного ответа (n=1). Длительность диареи перед ТФМ составила от 1 до 6 мес. (медиана – 2,3) и наблюдалась у всех пациентов. У 5 (45,5%) больных регистрировали активное кишечное кровотечение с необходимостью ежедневных гемотрансфузий для коррекции анемического синдрома, еще у 4 (36,4%) больных в стуле определялись прожилки крови. В состоянии сепсиса было 5 пациентов (45,5%), а один пациент находился в состоянии септического шока (Klebsiella pneumoniае) и получал антибактериальную терапию, вазопрессоры, искусственную вентиляцию легких. Абдоминальный болевой синдром, требующий анальгезии наркотическими анальгетиками отмечали у 9 (81,8%) пациентов. Парез кишечника наблюдали у 5 (45,5%) больных. У 8 (72,7%) пациентов выявлен положительный клостридиальный токсин-В в стуле, повышенный уровень фекального кальпротектина до ТФМ у 7 (63,6%) пациентов 600 мкг/г (220-6706). Введение фекального трансплантата выполняли на Д+168 (27-1107). Донорами микробиоты были родственники пациентов и неродственные доноры, которые соответствовали требованиям инфекционной безопасности. До и после ТФМ в дни +3, +8, +16, +30, +45, +60, +75, +90 для определения основных групп кишечных микроорганизмов проведено исследование стула методом мультиплексной ПЦР («Колонофлор-16»). Трем пациентам до ТФМ выполнено 16S РНК секвенирование образцов стула.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
У 64% пациентов отмечен полный клинический ответ. Сокращение частоты и объема диареи в 2 раза наблюдали на Д+18 (1-39) и Д+14 (1-11) после ТФМ соответственно. Полный регресс патологических примесей в стуле (кровь, слизь) регистрировали на Д+13 (2-11), Д+30 (1- 97) и абдоминального болевого синдрома на Д+15 (5-31) соответственно. Клостридиальный токсин-В в образцах стула на Д+30 не определялся у 4 (50%) ранее положительных пациентов. Результаты мультиплексной ПЦР показали изменение микробиоты кишечника после ТФМ. Максимальное увеличение основных групп кишечных микроорганизмов регистрировали после ТФМ для общей бактериальной массы на Д+8 с 3E+08 (9,E+05/1E+11) до 1,65E+12 (7E+10/7E+12), для Lactobacillus spp. на Д+3 с 7E+05 (1E+04/2E+09) до 3E+08 (7E+05/3E+09), для Bifidobacterium spp. на Д+30 с 3E+06 (9E+04/3E+08) до 1E+08 (3E+06/6E+09), для Escherichia coli на Д+3 с 7E+05 (0,0E+00/7E+06) до 3E+07 (2E+06/3E+09), для Bacteroides fragilis group на Д+8 с 1,1E+07 (0,0E+00/4E+08) до 1,6E+12 (3E+06/7E+12), для Faecalibacterium prausnitzii на Д+3 с 3E+05 (0,0E+00/8E+07) до 3E+08 (1E+05/3E+09). 16S РНК-секвенирование образцов стула до ТФМ выявило выраженные нарушения микробиоты кишечника с преобладанием микроорганизмов следующих семейств: Streptococcaceae, Staphylococcaceae, Enterococcaceae.
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
ТФМ имеет высокую клиническую эффективность и безопасность у пациентов после алло-ТГСК при развитии инфекции, ассоциированной с Clostridium difficile и РТПХ кишечника.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Трансплантация гемопоэтических стволовых клеток, трансплантация фекальной микробиоты, реакция трансплантат против хозяина.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод терапии онкологических, гематологических и наследственных заболеваний. Распространенными осложнениями алло-ТГСК, которые приводят к снижению эффективности лечения, являются: инфекционное поражение желудочно-кишечного тракта вирусной этиологии и/или ассоциированное с Clostridium difficile на фоне иммунодефицита; антибиотикассоциированная диарея; реакция трансплантат против хозяина (РТПХ). Трансплантация фекальной микробиоты (ТФМ) от здорового донора может приводить к эрадикации патогенных микроорганизмов, модуляции иммунной системы реципиента и как следствие к снижению активности РТПХ кишечника. Целью работы является повыщение эффективности лечения осложнений у пациентов после алло-ТГСК ассоциированных с Clostridium difficile и РТПХ кишечника.
Пациенты и методы
С 2015 по 2018 год в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой в одноцентровое, проспективное исследование включено 11 пациентов после алло-ТГСК от неродственного донора – 36,5% (n=4), родственного – 9% (n=1), гаплоидентичного – 54,5% (n=6) с целью терапии острого лимфобластного лейкоза – 18,3% (n=2), острого миелоидного лейкоза – 27,4% (n=3), миелодиспластического синдрома – 18,3% (n=2), бета-талассемии – 9% (n=1), хронического миелолейкоза – 9% (n=1), Лимфомы Ходжкина – 9% (n=1), анемии Фанкони – 9% (n=1). Для лечения посттрансплантационных осложнений всем пациентам была выполнена ТФМ. Медиана возраста составила 24 года (2-45). Из исследования исключено трое больных из-за нарушения техники ТФМ (n=2), развития тяжелого синдрома системного воспалительного ответа (n=1). Длительность диареи перед ТФМ составила от 1 до 6 мес. (медиана – 2,3) и наблюдалась у всех пациентов. У 5 (45,5%) больных регистрировали активное кишечное кровотечение с необходимостью ежедневных гемотрансфузий для коррекции анемического синдрома, еще у 4 (36,4%) больных в стуле определялись прожилки крови. В состоянии сепсиса было 5 пациентов (45,5%), а один пациент находился в состоянии септического шока (Klebsiella pneumoniае) и получал антибактериальную терапию, вазопрессоры, искусственную вентиляцию легких. Абдоминальный болевой синдром, требующий анальгезии наркотическими анальгетиками отмечали у 9 (81,8%) пациентов. Парез кишечника наблюдали у 5 (45,5%) больных. У 8 (72,7%) пациентов выявлен положительный клостридиальный токсин-В в стуле, повышенный уровень фекального кальпротектина до ТФМ у 7 (63,6%) пациентов 600 мкг/г (220-6706). Введение фекального трансплантата выполняли на Д+168 (27-1107). Донорами микробиоты были родственники пациентов и неродственные доноры, которые соответствовали требованиям инфекционной безопасности. До и после ТФМ в дни +3, +8, +16, +30, +45, +60, +75, +90 для определения основных групп кишечных микроорганизмов проведено исследование стула методом мультиплексной ПЦР («Колонофлор-16»). Трем пациентам до ТФМ выполнено 16S РНК секвенирование образцов стула.
Результаты
У 64% пациентов отмечен полный клинический ответ. Сокращение частоты и объема диареи в 2 раза наблюдали на Д+18 (1-39) и Д+14 (1-11) после ТФМ соответственно. Полный регресс патологических примесей в стуле (кровь, слизь) регистрировали на Д+13 (2-11), Д+30 (1- 97) и абдоминального болевого синдрома на Д+15 (5-31) соответственно. Клостридиальный токсин-В в образцах стула на Д+30 не определялся у 4 (50%) ранее положительных пациентов. Результаты мультиплексной ПЦР показали изменение микробиоты кишечника после ТФМ. Максимальное увеличение основных групп кишечных микроорганизмов регистрировали после ТФМ для общей бактериальной массы на Д+8 с 3E+08 (9,E+05/1E+11) до 1,65E+12 (7E+10/7E+12), для Lactobacillus spp. на Д+3 с 7E+05 (1E+04/2E+09) до 3E+08 (7E+05/3E+09), для Bifidobacterium spp. на Д+30 с 3E+06 (9E+04/3E+08) до 1E+08 (3E+06/6E+09), для Escherichia coli на Д+3 с 7E+05 (0,0E+00/7E+06) до 3E+07 (2E+06/3E+09), для Bacteroides fragilis group на Д+8 с 1,1E+07 (0,0E+00/4E+08) до 1,6E+12 (3E+06/7E+12), для Faecalibacterium prausnitzii на Д+3 с 3E+05 (0,0E+00/8E+07) до 3E+08 (1E+05/3E+09). 16S РНК-секвенирование образцов стула до ТФМ выявило выраженные нарушения микробиоты кишечника с преобладанием микроорганизмов следующих семейств: Streptococcaceae, Staphylococcaceae, Enterococcaceae.
Выводы
ТФМ имеет высокую клиническую эффективность и безопасность у пациентов после алло-ТГСК при развитии инфекции, ассоциированной с Clostridium difficile и РТПХ кишечника.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, трансплантация фекальной микробиоты, реакция трансплантат против хозяина.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20428
[VALUE] => Array
(
[TEXT] => Oleg V. Goloshchapov <sup>1</sup>, Maxim A. Kucher <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Alexander N. Shvetcov <sup>1</sup>, Ruslana V. Klementeva <sup>1</sup>, Alexander A. Shcherbakov <sup>1</sup>, Sergey V. Sidorenko <sup>2</sup>, Vladimir A. Gostev <sup>2</sup>, Maria A. Suvorova <sup>3</sup>, Oksana V. Stanevich <sup>1</sup>, Evgeny A. Bakin <sup>1</sup>, Alexey B. Chukhlovin <sup>1</sup>, Ludmila S. Zubarovskaya <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Oleg V. Goloshchapov 1, Maxim A. Kucher 1, Ivan S. Moiseev 1, Alexander N. Shvetcov 1, Ruslana V. Klementeva 1, Alexander A. Shcherbakov 1, Sergey V. Sidorenko 2, Vladimir A. Gostev 2, Maria A. Suvorova 3, Oksana V. Stanevich 1, Evgeny A. Bakin 1, Alexey B. Chukhlovin 1, Ludmila S. Zubarovskaya 1, Boris V. Afanasyev 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20429
[VALUE] => Array
(
[TEXT] => <sup>1</sup> Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University
<sup>2</sup> Pediatric Research and Clinical Center for Infectious Diseases, St. Petersburg, Russia
<sup>3</sup> Explana Research Laboratory, St. Petersburg, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University
2 Pediatric Research and Clinical Center for Infectious Diseases, St. Petersburg, Russia
3 Explana Research Laboratory, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20430
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is effective method of treatment of malignant, hematological and hereditary diseases. Common complications after allo-HSCT, which may decrease its effectiveness, include infectious lesions of the gastrointestinal tract of viral etiology and Clostridium difficile on the background of immunodeficiency, antibiotic-associated diarrhea and graftversus-host disease (GvHD). Transplantation of fecal microbiota (FMT) from a healthy donor can lead to eradication of pathogens, modulation of the recipient’s immune system and as a consequence to a decrease in intestinal GVHD activity. Aim of our study was to increase treatment efficiency of complications associated with Clostridium difficile and intestinal GvHD in patients after allo-HSCT.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
From 2015 to 2018 in Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation 11 patients after allo-HSCT from matched unrelated donor – 36.5% (n=4), related donor – 9% (n=1), haploidentical donor – 54.5% (n=6) with acute lymphoblastic leukemia – 18.3% (n=2), acute myeloid leukemia – 27.4% (n=3), myelodysplastic syndrome – 18.3% (n=2), beta-thalassemia – 9% (n=1), chronic myeloid leukemia – 9% (n=1), Hodgkin’s lymphoma – 9% (n=1), Fanconi’s anemia – 9% (n=1) were included in a single-center prospective study. All patients underwent FMT for the treatment of posttransplant complications. The median age was 24 years (2-45). Three patients were excluded from the study due to violation of FMT technique (n=2), development of severe systemic inflammatory response syndrome (n=1). The duration of diarrhea before FMT was from 1 to 6 months (median – 2.3) and was observed in all patients. Active intestinal bleeding with the need of daily blood transfusions for the correction of anemic syndrome was registered in 5 (45.5%) patients, additionally blood impurity in stool was determined in 4 (36.4%) patients. 5 patients had sepsis (45.5%) and one patient was in septic shock associated with Klebsiella pneumoniae and received antibiotic therapy, vasopressors, mechanical ventilation. Abdominal pain requiring analgesia with opioids was noted in 9 (81.8%) patients. Gastrointestinal paresis was observed in 5 (45.5%) patients. 8 (72.7%) patients had positive clostridial toxin-B in stool. Elevated fecal calprotectin level – 600 μg/g (220-6706) before FMT was identified in 7 (63.6%) patients. FMT was performed on D+168 (27-1107). Microbiota donors were patient’s relatives or unrelated donors who met all infectious safety requirements. Before and after FMT D+3, D+8, D+16, D+30, D+45, D+60, D+75, D+90 real-time multiplex PCR (“Colonoflor-16”) was performed to determine the main groups of intestinal microorganisms. 3 patients underwent 16S RNA stool sequencing prior FMT.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
A complete clinical response was observed in 64% of patients. The reduction in the frequency and volume of diarrhea by 2 times was observed on D+18 (1 – 39) and D+14 (1 – 11) after FMT, respectively. Complete regression of pathological impurities in the stool (blood, mucus) was recorded at D+13 (2-11), D+30 (1-97) and abdominal pain syndrome at D+15 (5-31), respectively. Clostridial toxin-B in stool samples at D+30 was not detected in 4 (50%) previously positive cases. The results of multiplex PCR showed changes in gut microbiota after FMT. The maximum increase in the main groups of intestinal microorganisms was recorded after FMT for the total bacterial mass at D+8 from 3E+08 (9,E+05/ 1E+11) to 1,65 E+12 (7E+10/ 7E+12), for Lactobacillus spp. on D+3 7E+05 (1E+04/2E+09) to 3E+08 (7E+05/ 3E+09) and for Bifidobacterium spp. on D+30 3E+06 (9E+04/ 3E+08) to 1E+08 (3E+06/ 6E+09), Escherichia coli on D+3 7E+05 (0.0 E+00/7E+06) to 3E+07 (2E+06/ 3E+09), for Bacteroides fragilis group on D+8 1.1 E+07 (0.0 E+00/4E+08) to 1.6 E+12 (3E+06/7E+12), Faecalibacterium prausnitzii on D+3 3E+05 (0.0 E+00/8E+07) to 3E+08 (1E+05/ 3E+09). 16S RNA stool sequencing before FMT revealed marked disturbances of intestinal microbiota with predominance of microorganisms of the following families: Streptococcaceae, Staphylococcaceae, Enterococcaceae.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
FMT is effective and safe method of treatment for infectious complications associated with Clostridium difficile and intestinal GvHD in patients after allo-HCST.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Hematopoietic stem cell transplantation, fecal microbiota transplantation, graft-versus-host disease.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is effective method of treatment of malignant, hematological and hereditary diseases. Common complications after allo-HSCT, which may decrease its effectiveness, include infectious lesions of the gastrointestinal tract of viral etiology and Clostridium difficile on the background of immunodeficiency, antibiotic-associated diarrhea and graftversus-host disease (GvHD). Transplantation of fecal microbiota (FMT) from a healthy donor can lead to eradication of pathogens, modulation of the recipient’s immune system and as a consequence to a decrease in intestinal GVHD activity. Aim of our study was to increase treatment efficiency of complications associated with Clostridium difficile and intestinal GvHD in patients after allo-HSCT.
Patients and methods
From 2015 to 2018 in Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation 11 patients after allo-HSCT from matched unrelated donor – 36.5% (n=4), related donor – 9% (n=1), haploidentical donor – 54.5% (n=6) with acute lymphoblastic leukemia – 18.3% (n=2), acute myeloid leukemia – 27.4% (n=3), myelodysplastic syndrome – 18.3% (n=2), beta-thalassemia – 9% (n=1), chronic myeloid leukemia – 9% (n=1), Hodgkin’s lymphoma – 9% (n=1), Fanconi’s anemia – 9% (n=1) were included in a single-center prospective study. All patients underwent FMT for the treatment of posttransplant complications. The median age was 24 years (2-45). Three patients were excluded from the study due to violation of FMT technique (n=2), development of severe systemic inflammatory response syndrome (n=1). The duration of diarrhea before FMT was from 1 to 6 months (median – 2.3) and was observed in all patients. Active intestinal bleeding with the need of daily blood transfusions for the correction of anemic syndrome was registered in 5 (45.5%) patients, additionally blood impurity in stool was determined in 4 (36.4%) patients. 5 patients had sepsis (45.5%) and one patient was in septic shock associated with Klebsiella pneumoniae and received antibiotic therapy, vasopressors, mechanical ventilation. Abdominal pain requiring analgesia with opioids was noted in 9 (81.8%) patients. Gastrointestinal paresis was observed in 5 (45.5%) patients. 8 (72.7%) patients had positive clostridial toxin-B in stool. Elevated fecal calprotectin level – 600 μg/g (220-6706) before FMT was identified in 7 (63.6%) patients. FMT was performed on D+168 (27-1107). Microbiota donors were patient’s relatives or unrelated donors who met all infectious safety requirements. Before and after FMT D+3, D+8, D+16, D+30, D+45, D+60, D+75, D+90 real-time multiplex PCR (“Colonoflor-16”) was performed to determine the main groups of intestinal microorganisms. 3 patients underwent 16S RNA stool sequencing prior FMT.
Results
A complete clinical response was observed in 64% of patients. The reduction in the frequency and volume of diarrhea by 2 times was observed on D+18 (1 – 39) and D+14 (1 – 11) after FMT, respectively. Complete regression of pathological impurities in the stool (blood, mucus) was recorded at D+13 (2-11), D+30 (1-97) and abdominal pain syndrome at D+15 (5-31), respectively. Clostridial toxin-B in stool samples at D+30 was not detected in 4 (50%) previously positive cases. The results of multiplex PCR showed changes in gut microbiota after FMT. The maximum increase in the main groups of intestinal microorganisms was recorded after FMT for the total bacterial mass at D+8 from 3E+08 (9,E+05/ 1E+11) to 1,65 E+12 (7E+10/ 7E+12), for Lactobacillus spp. on D+3 7E+05 (1E+04/2E+09) to 3E+08 (7E+05/ 3E+09) and for Bifidobacterium spp. on D+30 3E+06 (9E+04/ 3E+08) to 1E+08 (3E+06/ 6E+09), Escherichia coli on D+3 7E+05 (0.0 E+00/7E+06) to 3E+07 (2E+06/ 3E+09), for Bacteroides fragilis group on D+8 1.1 E+07 (0.0 E+00/4E+08) to 1.6 E+12 (3E+06/7E+12), Faecalibacterium prausnitzii on D+3 3E+05 (0.0 E+00/8E+07) to 3E+08 (1E+05/ 3E+09). 16S RNA stool sequencing before FMT revealed marked disturbances of intestinal microbiota with predominance of microorganisms of the following families: Streptococcaceae, Staphylococcaceae, Enterococcaceae.
Conclusion
FMT is effective and safe method of treatment for infectious complications associated with Clostridium difficile and intestinal GvHD in patients after allo-HCST.
Keywords
Hematopoietic stem cell transplantation, fecal microbiota transplantation, graft-versus-host disease.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20431
[VALUE] => Fecal microbiota transplantation in patients after allogeneic hematopoietic stem cell transplantation
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Fecal microbiota transplantation in patients after allogeneic hematopoietic stem cell transplantation
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20765
[VALUE] => 1401
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1401
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20766
[VALUE] => 1402
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1402
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Олег В. Голощапов 1, Максим А. Кучер 1, Иван С. Моисеев 1, Александр Н. Швецов 1, Руслана В. Клементьева 1, Александр А. Щербаков 1, Сергей В. Сидоренко 2, Владимир А. Гостев 2, Мария А. Суворова 3, Оксана В. Станевич 1, Евгений А. Бакин 1, Алексей Б. Чухловин 1, Людмила С. Зубаровская 1, Борис В. Афанасьев 1
Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод терапии онкологических, гематологических и наследственных заболеваний. Распространенными осложнениями алло-ТГСК, которые приводят к снижению эффективности лечения, являются: инфекционное поражение желудочно-кишечного тракта вирусной этиологии и/или ассоциированное с Clostridium difficile на фоне иммунодефицита; антибиотикассоциированная диарея; реакция трансплантат против хозяина (РТПХ). Трансплантация фекальной микробиоты (ТФМ) от здорового донора может приводить к эрадикации патогенных микроорганизмов, модуляции иммунной системы реципиента и как следствие к снижению активности РТПХ кишечника. Целью работы является повыщение эффективности лечения осложнений у пациентов после алло-ТГСК ассоциированных с Clostridium difficile и РТПХ кишечника.
Пациенты и методы
С 2015 по 2018 год в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой в одноцентровое, проспективное исследование включено 11 пациентов после алло-ТГСК от неродственного донора – 36,5% (n=4), родственного – 9% (n=1), гаплоидентичного – 54,5% (n=6) с целью терапии острого лимфобластного лейкоза – 18,3% (n=2), острого миелоидного лейкоза – 27,4% (n=3), миелодиспластического синдрома – 18,3% (n=2), бета-талассемии – 9% (n=1), хронического миелолейкоза – 9% (n=1), Лимфомы Ходжкина – 9% (n=1), анемии Фанкони – 9% (n=1). Для лечения посттрансплантационных осложнений всем пациентам была выполнена ТФМ. Медиана возраста составила 24 года (2-45). Из исследования исключено трое больных из-за нарушения техники ТФМ (n=2), развития тяжелого синдрома системного воспалительного ответа (n=1). Длительность диареи перед ТФМ составила от 1 до 6 мес. (медиана – 2,3) и наблюдалась у всех пациентов. У 5 (45,5%) больных регистрировали активное кишечное кровотечение с необходимостью ежедневных гемотрансфузий для коррекции анемического синдрома, еще у 4 (36,4%) больных в стуле определялись прожилки крови. В состоянии сепсиса было 5 пациентов (45,5%), а один пациент находился в состоянии септического шока (Klebsiella pneumoniае) и получал антибактериальную терапию, вазопрессоры, искусственную вентиляцию легких. Абдоминальный болевой синдром, требующий анальгезии наркотическими анальгетиками отмечали у 9 (81,8%) пациентов. Парез кишечника наблюдали у 5 (45,5%) больных. У 8 (72,7%) пациентов выявлен положительный клостридиальный токсин-В в стуле, повышенный уровень фекального кальпротектина до ТФМ у 7 (63,6%) пациентов 600 мкг/г (220-6706). Введение фекального трансплантата выполняли на Д+168 (27-1107). Донорами микробиоты были родственники пациентов и неродственные доноры, которые соответствовали требованиям инфекционной безопасности. До и после ТФМ в дни +3, +8, +16, +30, +45, +60, +75, +90 для определения основных групп кишечных микроорганизмов проведено исследование стула методом мультиплексной ПЦР («Колонофлор-16»). Трем пациентам до ТФМ выполнено 16S РНК секвенирование образцов стула.
Результаты
У 64% пациентов отмечен полный клинический ответ. Сокращение частоты и объема диареи в 2 раза наблюдали на Д+18 (1-39) и Д+14 (1-11) после ТФМ соответственно. Полный регресс патологических примесей в стуле (кровь, слизь) регистрировали на Д+13 (2-11), Д+30 (1- 97) и абдоминального болевого синдрома на Д+15 (5-31) соответственно. Клостридиальный токсин-В в образцах стула на Д+30 не определялся у 4 (50%) ранее положительных пациентов. Результаты мультиплексной ПЦР показали изменение микробиоты кишечника после ТФМ. Максимальное увеличение основных групп кишечных микроорганизмов регистрировали после ТФМ для общей бактериальной массы на Д+8 с 3E+08 (9,E+05/1E+11) до 1,65E+12 (7E+10/7E+12), для Lactobacillus spp. на Д+3 с 7E+05 (1E+04/2E+09) до 3E+08 (7E+05/3E+09), для Bifidobacterium spp. на Д+30 с 3E+06 (9E+04/3E+08) до 1E+08 (3E+06/6E+09), для Escherichia coli на Д+3 с 7E+05 (0,0E+00/7E+06) до 3E+07 (2E+06/3E+09), для Bacteroides fragilis group на Д+8 с 1,1E+07 (0,0E+00/4E+08) до 1,6E+12 (3E+06/7E+12), для Faecalibacterium prausnitzii на Д+3 с 3E+05 (0,0E+00/8E+07) до 3E+08 (1E+05/3E+09). 16S РНК-секвенирование образцов стула до ТФМ выявило выраженные нарушения микробиоты кишечника с преобладанием микроорганизмов следующих семейств: Streptococcaceae, Staphylococcaceae, Enterococcaceae.
Выводы
ТФМ имеет высокую клиническую эффективность и безопасность у пациентов после алло-ТГСК при развитии инфекции, ассоциированной с Clostridium difficile и РТПХ кишечника.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, трансплантация фекальной микробиоты, реакция трансплантат против хозяина.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20416
[VALUE] => Array
(
[TEXT] => Татьяна Л. Гиндина, Николай Н. Мамаев, Елена С. Рябикова, Мария В. Латыпова, Ирина А. Петрова, Диана С. Ильясова, Мария В. Власова, Олеся В. Паина, Елена В. Семенова, Елена И. Дарская, Людмила С. Зубаровская, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Татьяна Л. Гиндина, Николай Н. Мамаев, Елена С. Рябикова, Мария В. Латыпова, Ирина А. Петрова, Диана С. Ильясова, Мария В. Власова, Олеся В. Паина, Елена В. Семенова, Елена И. Дарская, Людмила С. Зубаровская, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20417
[VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20418
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Цель исследования – охарактеризовать цитогенетические изменения у больных с посттрансплантационными рецидивами (ПТР) острых лейкозов в рецидивах после алло-ТГСК, оценить влияние цитогенетической эволюции на их выживаемость и уточнить связь эволюции кариотипа с режимом кондиционирования.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
В наше исследование вощли 73 пациента (35 женщин и 38 мужчин в возрасте 0,8-60 лет) с диагнозом острый миелоидный лейкоз (ОМЛ) или острый лимфобластный лейкоз (ОЛЛ), которым была проведена алло-ТГСК в нашем Универcитете в период с 2009 по 2016 год. Изменения кариотипа клеток костного мозга в посттрансплантационном рецидиве сравнивали с таковым, выявленным до алло-ТГСК. Медиана времени от трансплантации до рецидива составила 87 (диапазон, 18-1280) дней. Миелоаблативный режим кондиционирования и режим со сниженной интенсивностью доз применяли у 39 (53%) и 34 (47%) больных соответственно.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Изменения кариотипа в ПТР были отмечены у 29 больных ОМЛ (71%) и 23 больных ОЛЛ (72%). Цитогенетические изменения были разделены на следующие 5 групп: a) клоновую эволюцию кариотипа в ПТР (n=30); б) клоновую регрессию (n=1); в) клоновую эволюцию кариотипа в комбинации с регрессией (n=15); г) новый неродственный клон (n=5); и д) смену нормального кариотипа в ПТР аномальным (n=1). Два и более цитогенетических подклона были обнаружены у 6 (8%) пациентов до алло-ТГСК и у 24 (33%) больных в ПТР (p<0.0002). Были установлены 8 различных путей формирования родственных подклонов. Самыми частымм цитогенетическими изменениями в ПТР были появление 3 или более новых хромосомных аномалий, а также несбалансированных аномалий и анеуплоидии. У пациентов ОМЛ общие потери касались регионов 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, и 20q, тогда как приобретения – 1q, 11q 13q, 15q и 21q. У больных ОЛЛ часто удалялись регионы 1p, 8p, 11p, 11q, 17p, тогда как приобретения касались 1q, 8q, 18p, 18q, 21q и Xp. Миелоаблативное кондиционирование в группе больных с цитогенетической эволюцией в ПТР применяли чаще (p=0,01). В то же время цитогенетическая клоновая эволюция чаще всего встречалась (p=0,02) у больных с неблагоприятной предтрансплантационной группой, содержащих 3 и более сложных хромосомных аберраций на метафазу. Общая выживаемость после ТГСК и выживаемость после ПТР (ВПТР) были ниже в группе больных с изменениями кариотипа в ПТР (38% vs. 17%, p=0,03 and 41% vs. 6%, p=0,006, соответственно), также как в группе больных с 2 или более аномальными цитогенетическими клонами в ПТР (31%vs. 9%; р=0,04 только для ОВ). Появление нового неродственного клона было связано с уменьшением выживаемости после ПТР (17% vs. 0%, p=0,04).
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Цитогенетическая эволюция в ПТР встречается чаще а) после применения миелоаблативного кондиционирования; б) при комплексном кариотипе перед трансплантацией; и в) сочетается с клональной гетерогенностью. Большинство общих цитогенетических аберраций в ПТР при ОМЛ и ОЛЛ различны. ОВ и выживаемость после посттрансплантационного рецидива ниже в группах пациентов с цитогенетической эволюцией (для ОВ и ВПТР), клональной гетерогенностью (для ОВ) и появлением нового неродственного клона (для ВПТР) в ПТР.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Острый лейкоз, посттрансплантационный рецидив, цитогенетическая эволюция, режим кондиционирования, исходы.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Цель исследования – охарактеризовать цитогенетические изменения у больных с посттрансплантационными рецидивами (ПТР) острых лейкозов в рецидивах после алло-ТГСК, оценить влияние цитогенетической эволюции на их выживаемость и уточнить связь эволюции кариотипа с режимом кондиционирования.
Материалы и методы
В наше исследование вощли 73 пациента (35 женщин и 38 мужчин в возрасте 0,8-60 лет) с диагнозом острый миелоидный лейкоз (ОМЛ) или острый лимфобластный лейкоз (ОЛЛ), которым была проведена алло-ТГСК в нашем Универcитете в период с 2009 по 2016 год. Изменения кариотипа клеток костного мозга в посттрансплантационном рецидиве сравнивали с таковым, выявленным до алло-ТГСК. Медиана времени от трансплантации до рецидива составила 87 (диапазон, 18-1280) дней. Миелоаблативный режим кондиционирования и режим со сниженной интенсивностью доз применяли у 39 (53%) и 34 (47%) больных соответственно.
Результаты
Изменения кариотипа в ПТР были отмечены у 29 больных ОМЛ (71%) и 23 больных ОЛЛ (72%). Цитогенетические изменения были разделены на следующие 5 групп: a) клоновую эволюцию кариотипа в ПТР (n=30); б) клоновую регрессию (n=1); в) клоновую эволюцию кариотипа в комбинации с регрессией (n=15); г) новый неродственный клон (n=5); и д) смену нормального кариотипа в ПТР аномальным (n=1). Два и более цитогенетических подклона были обнаружены у 6 (8%) пациентов до алло-ТГСК и у 24 (33%) больных в ПТР (p<0.0002). Были установлены 8 различных путей формирования родственных подклонов. Самыми частымм цитогенетическими изменениями в ПТР были появление 3 или более новых хромосомных аномалий, а также несбалансированных аномалий и анеуплоидии. У пациентов ОМЛ общие потери касались регионов 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, и 20q, тогда как приобретения – 1q, 11q 13q, 15q и 21q. У больных ОЛЛ часто удалялись регионы 1p, 8p, 11p, 11q, 17p, тогда как приобретения касались 1q, 8q, 18p, 18q, 21q и Xp. Миелоаблативное кондиционирование в группе больных с цитогенетической эволюцией в ПТР применяли чаще (p=0,01). В то же время цитогенетическая клоновая эволюция чаще всего встречалась (p=0,02) у больных с неблагоприятной предтрансплантационной группой, содержащих 3 и более сложных хромосомных аберраций на метафазу. Общая выживаемость после ТГСК и выживаемость после ПТР (ВПТР) были ниже в группе больных с изменениями кариотипа в ПТР (38% vs. 17%, p=0,03 and 41% vs. 6%, p=0,006, соответственно), также как в группе больных с 2 или более аномальными цитогенетическими клонами в ПТР (31%vs. 9%; р=0,04 только для ОВ). Появление нового неродственного клона было связано с уменьшением выживаемости после ПТР (17% vs. 0%, p=0,04).
Заключение
Цитогенетическая эволюция в ПТР встречается чаще а) после применения миелоаблативного кондиционирования; б) при комплексном кариотипе перед трансплантацией; и в) сочетается с клональной гетерогенностью. Большинство общих цитогенетических аберраций в ПТР при ОМЛ и ОЛЛ различны. ОВ и выживаемость после посттрансплантационного рецидива ниже в группах пациентов с цитогенетической эволюцией (для ОВ и ВПТР), клональной гетерогенностью (для ОВ) и появлением нового неродственного клона (для ВПТР) в ПТР.
Ключевые слова
Острый лейкоз, посттрансплантационный рецидив, цитогенетическая эволюция, режим кондиционирования, исходы.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20419
[VALUE] => Array
(
[TEXT] => Tatiana L. Gindina, Nikolay N. Mamaev, Elena S. Ryabikova, Maria V. Latypova, Irina A. Petrova, Diana S. Ilyasova, Maria E. Vlasova, Olesya V. Paina, Elena V. Semenova, Elena I. Darskaya, Ludmila S. Zubarovskaya, Boris V. Afanasyev<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Tatiana L. Gindina, Nikolay N. Mamaev, Elena S. Ryabikova, Maria V. Latypova, Irina A. Petrova, Diana S. Ilyasova, Maria E. Vlasova, Olesya V. Paina, Elena V. Semenova, Elena I. Darskaya, Ludmila S. Zubarovskaya, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20420
[VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20421
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
The aim of this study was to characterize patterns of cytogenetic changes in patients with acute leukemia who relapsed after allo-HSCT, to assess the effect of сytogenetic evolution upon survival; and to elucidate associations of cytogenetic evolution with conditioning regimen.
</p>
<h2>Materials and methods</h2>
<p style="text-align: justify;">
Our study included seventy-three patients (35 females and 38 males, at the age of 0.8 to 60 years) diagnosed with acute myeloblastic leukemia (AML) or acute lymphoblastic leukemia (ALL) who underwent allo-HSCT at our University from 2009 to 2016. The bone marrow karyotypic changes in posttransplant relapse (PTR) were compared with those observed before allo-HSCT. Median time from transplant to relapse was 87 days (range, 18 to 1280). Myeloablative conditioning and reduced intensity conditioning was performed in 39 (53%) and 34 (47%) patients, respectively.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Karyotypic changes at PTR were noted in 29 AML patients (71%) and 23 ALL patients (72%). The cytogenetic changes were divided into five following groups: a) clonal evolution of karyotype at PTR (n=30); b) clonal regression (n=1); c) new unrelated clones (n=5); d) clonal evolution of karyotype, combined with clonal regression (n=15); and e) changing of normal karyotype into abnormal at PTR (n=1). Moreover, two or more cytogenetic subclones were detected in 6 (8%) patients before allo-HSCT and in 24 (33%) patients at PTR (p<0.0002). Eight different ways of subclone formation has been identified. Acquisition of 3 or more new chromosomal abnormalities was the most frequent cytogenetic change, followed by acquisition of both unbalanced abnormalities and aneuploidy. The common losses in AML patients were 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, and 20q, whereas gains concerned 1q, 11q 13q, 15q, and 21q. The common losses in ALL patients were 1p, 8p, 11p, 11q, 17p, whereas the gains concerned 1q, 8q, 18p, 18q, 21q, and Xp. In the group with cytogenetic evolution at PTR, myeloablative conditioning was used more often (p=0.01). Cytogenetic clonal evolution frequently occurred in an unfavorable pre-transplant group with complex chromosome aberrations (3 and more per metaphase) (p=0.02). Overall survival after HSCT and survival after PTR were shortened in the group of patients with karyotype changes in PTR (38% vs. 17%, p=0.03 and 41% vs. 6%, p=0.006, respectively) as well as in the group of patients with two or more abnormal cytogenetic clones in PTR (31% vs. 9%; р=0.04 only for OS). The emergence of a new unrelated clone was associated with decreasing of survival after PTR (17% vs. 0%, p=0.04).
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
We have revealed evidence for a significant impact of cytogenetic evolution to clinical progression in acute leukemia treated with allo-HSCT.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Acute leukemia, posttransplant relapse, cytogenetic evolution, conditioning regimen, outcomes.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
The aim of this study was to characterize patterns of cytogenetic changes in patients with acute leukemia who relapsed after allo-HSCT, to assess the effect of сytogenetic evolution upon survival; and to elucidate associations of cytogenetic evolution with conditioning regimen.
Materials and methods
Our study included seventy-three patients (35 females and 38 males, at the age of 0.8 to 60 years) diagnosed with acute myeloblastic leukemia (AML) or acute lymphoblastic leukemia (ALL) who underwent allo-HSCT at our University from 2009 to 2016. The bone marrow karyotypic changes in posttransplant relapse (PTR) were compared with those observed before allo-HSCT. Median time from transplant to relapse was 87 days (range, 18 to 1280). Myeloablative conditioning and reduced intensity conditioning was performed in 39 (53%) and 34 (47%) patients, respectively.
Results
Karyotypic changes at PTR were noted in 29 AML patients (71%) and 23 ALL patients (72%). The cytogenetic changes were divided into five following groups: a) clonal evolution of karyotype at PTR (n=30); b) clonal regression (n=1); c) new unrelated clones (n=5); d) clonal evolution of karyotype, combined with clonal regression (n=15); and e) changing of normal karyotype into abnormal at PTR (n=1). Moreover, two or more cytogenetic subclones were detected in 6 (8%) patients before allo-HSCT and in 24 (33%) patients at PTR (p<0.0002). Eight different ways of subclone formation has been identified. Acquisition of 3 or more new chromosomal abnormalities was the most frequent cytogenetic change, followed by acquisition of both unbalanced abnormalities and aneuploidy. The common losses in AML patients were 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, and 20q, whereas gains concerned 1q, 11q 13q, 15q, and 21q. The common losses in ALL patients were 1p, 8p, 11p, 11q, 17p, whereas the gains concerned 1q, 8q, 18p, 18q, 21q, and Xp. In the group with cytogenetic evolution at PTR, myeloablative conditioning was used more often (p=0.01). Cytogenetic clonal evolution frequently occurred in an unfavorable pre-transplant group with complex chromosome aberrations (3 and more per metaphase) (p=0.02). Overall survival after HSCT and survival after PTR were shortened in the group of patients with karyotype changes in PTR (38% vs. 17%, p=0.03 and 41% vs. 6%, p=0.006, respectively) as well as in the group of patients with two or more abnormal cytogenetic clones in PTR (31% vs. 9%; р=0.04 only for OS). The emergence of a new unrelated clone was associated with decreasing of survival after PTR (17% vs. 0%, p=0.04).
Conclusion
We have revealed evidence for a significant impact of cytogenetic evolution to clinical progression in acute leukemia treated with allo-HSCT.
Keywords
Acute leukemia, posttransplant relapse, cytogenetic evolution, conditioning regimen, outcomes.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20422
[VALUE] => Cytogenetic evolution in acute leukemia at relapse after allogeneic hematopoietic cell transplantation: association with regimen conditioning and effect on survival
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Cytogenetic evolution in acute leukemia at relapse after allogeneic hematopoietic cell transplantation: association with regimen conditioning and effect on survival
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20763
[VALUE] => 1399
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1399
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20764
[VALUE] => 1400
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1400
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Татьяна Л. Гиндина, Николай Н. Мамаев, Елена С. Рябикова, Мария В. Латыпова, Ирина А. Петрова, Диана С. Ильясова, Мария В. Власова, Олеся В. Паина, Елена В. Семенова, Елена И. Дарская, Людмила С. Зубаровская, Борис В. Афанасьев
Введение
Цель исследования – охарактеризовать цитогенетические изменения у больных с посттрансплантационными рецидивами (ПТР) острых лейкозов в рецидивах после алло-ТГСК, оценить влияние цитогенетической эволюции на их выживаемость и уточнить связь эволюции кариотипа с режимом кондиционирования.
Материалы и методы
В наше исследование вощли 73 пациента (35 женщин и 38 мужчин в возрасте 0,8-60 лет) с диагнозом острый миелоидный лейкоз (ОМЛ) или острый лимфобластный лейкоз (ОЛЛ), которым была проведена алло-ТГСК в нашем Универcитете в период с 2009 по 2016 год. Изменения кариотипа клеток костного мозга в посттрансплантационном рецидиве сравнивали с таковым, выявленным до алло-ТГСК. Медиана времени от трансплантации до рецидива составила 87 (диапазон, 18-1280) дней. Миелоаблативный режим кондиционирования и режим со сниженной интенсивностью доз применяли у 39 (53%) и 34 (47%) больных соответственно.
Результаты
Изменения кариотипа в ПТР были отмечены у 29 больных ОМЛ (71%) и 23 больных ОЛЛ (72%). Цитогенетические изменения были разделены на следующие 5 групп: a) клоновую эволюцию кариотипа в ПТР (n=30); б) клоновую регрессию (n=1); в) клоновую эволюцию кариотипа в комбинации с регрессией (n=15); г) новый неродственный клон (n=5); и д) смену нормального кариотипа в ПТР аномальным (n=1). Два и более цитогенетических подклона были обнаружены у 6 (8%) пациентов до алло-ТГСК и у 24 (33%) больных в ПТР (p<0.0002). Были установлены 8 различных путей формирования родственных подклонов. Самыми частымм цитогенетическими изменениями в ПТР были появление 3 или более новых хромосомных аномалий, а также несбалансированных аномалий и анеуплоидии. У пациентов ОМЛ общие потери касались регионов 1q, 2q, 3q 5q, 7q, 9q, 11p, 13q, 14q, 17p, и 20q, тогда как приобретения – 1q, 11q 13q, 15q и 21q. У больных ОЛЛ часто удалялись регионы 1p, 8p, 11p, 11q, 17p, тогда как приобретения касались 1q, 8q, 18p, 18q, 21q и Xp. Миелоаблативное кондиционирование в группе больных с цитогенетической эволюцией в ПТР применяли чаще (p=0,01). В то же время цитогенетическая клоновая эволюция чаще всего встречалась (p=0,02) у больных с неблагоприятной предтрансплантационной группой, содержащих 3 и более сложных хромосомных аберраций на метафазу. Общая выживаемость после ТГСК и выживаемость после ПТР (ВПТР) были ниже в группе больных с изменениями кариотипа в ПТР (38% vs. 17%, p=0,03 and 41% vs. 6%, p=0,006, соответственно), также как в группе больных с 2 или более аномальными цитогенетическими клонами в ПТР (31%vs. 9%; р=0,04 только для ОВ). Появление нового неродственного клона было связано с уменьшением выживаемости после ПТР (17% vs. 0%, p=0,04).
Заключение
Цитогенетическая эволюция в ПТР встречается чаще а) после применения миелоаблативного кондиционирования; б) при комплексном кариотипе перед трансплантацией; и в) сочетается с клональной гетерогенностью. Большинство общих цитогенетических аберраций в ПТР при ОМЛ и ОЛЛ различны. ОВ и выживаемость после посттрансплантационного рецидива ниже в группах пациентов с цитогенетической эволюцией (для ОВ и ВПТР), клональной гетерогенностью (для ОВ) и появлением нового неродственного клона (для ВПТР) в ПТР.
Ключевые слова
Острый лейкоз, посттрансплантационный рецидив, цитогенетическая эволюция, режим кондиционирования, исходы.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20407
[VALUE] => Array
(
[TEXT] => Людмила В. Федорова, Кирилл В. Лепик, Наталия Б. Михайлова, Елена В. Кондакова, Юрий Р. Залялов, Анастасия В. Бейнарович, Елена Е. Давыдова, Любовь А. Цветкова, Вадим В. Байков, Елена В. Бабенко, Лилия В. Стельмах, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Людмила В. Федорова, Кирилл В. Лепик, Наталия Б. Михайлова, Елена В. Кондакова, Юрий Р. Залялов, Анастасия В. Бейнарович, Елена Е. Давыдова, Любовь А. Цветкова, Вадим В. Байков, Елена В. Бабенко, Лилия В. Стельмах, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20408
[VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой, Первый Санкт-Петербургский
государственный медицинский университет им. академика И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой, Первый Санкт-Петербургский
государственный медицинский университет им. академика И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20409
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Целью работы была оценка эффективности и безопасности терапии ниволумабом в дозе 40 мг у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
В промежуточный анализ были включены 14 пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина. Ниволумаб в дозе 40 мг вводился 1 раз в 2 недели до прогрессирования заболевания или развития тяжелых нежелательных явлений. Каждые 3 месяца (6 введений) производилась оценка ответа на терапию при использовании критериев LYRIC по данным ПЭТ/КТ, а также оценка наличия нежелательных явлений на терапию в соответствии с критериями NCI CTCAE 4.03.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Медиана наблюдения составила 10 месяцев. Медиана введений ниволумаба 17 (12-22). Медиана дозы препарата составила 0,56 мг/кг (0,4-0,91 мг/кг). Объективный ответ был получен у 9 (64,3%) пациентов, полный ответ у 5 (35,7%) и частичный ответ у 4 (28,6%) пациентов. Неопределенный ответ установлен у 4 (28,6%) пациентов. За время наблюдения у 2 (14,3%) пациентов было зафиксировано прогрессирование заболевания (после 12 и 18 введений). Нежелательные явления любой степени тяжести были представлены у 10 (71,4%) пациентов, при этом 3/4 степени тяжести только у 3 (21%), в виде анемии, артрита и гепатита. В целом, терапия хорошо переносилась пациентами, а профиль токсичности был сопоставим с ранее опубликованными данными.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
По данным промежуточного анализа, структура ответа на терапию у пациентов, получавших ниволумаб в дозе 40 мг, сопоставима с пациентами, получавшими препарат в полной дозе (3 мг/кг). Распределение частоты встречаемости, времени появления и вариантов нежелательных явлений также схожи с группой пациентов, получающих стандартную терапию. Таким образом, можно предположить, что данный режим дозирования будет эффективен и безопасен у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина, однако необходимо продолжить исследование для получения заключительных результатов.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Лимфома Ходжкина, ниволумаб, иммунотерапия, PD1-ингибиторы, рецидивирующие лимфомы, резистентные лимфомы.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Целью работы была оценка эффективности и безопасности терапии ниволумабом в дозе 40 мг у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина.
Материалы и методы
В промежуточный анализ были включены 14 пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина. Ниволумаб в дозе 40 мг вводился 1 раз в 2 недели до прогрессирования заболевания или развития тяжелых нежелательных явлений. Каждые 3 месяца (6 введений) производилась оценка ответа на терапию при использовании критериев LYRIC по данным ПЭТ/КТ, а также оценка наличия нежелательных явлений на терапию в соответствии с критериями NCI CTCAE 4.03.
Результаты
Медиана наблюдения составила 10 месяцев. Медиана введений ниволумаба 17 (12-22). Медиана дозы препарата составила 0,56 мг/кг (0,4-0,91 мг/кг). Объективный ответ был получен у 9 (64,3%) пациентов, полный ответ у 5 (35,7%) и частичный ответ у 4 (28,6%) пациентов. Неопределенный ответ установлен у 4 (28,6%) пациентов. За время наблюдения у 2 (14,3%) пациентов было зафиксировано прогрессирование заболевания (после 12 и 18 введений). Нежелательные явления любой степени тяжести были представлены у 10 (71,4%) пациентов, при этом 3/4 степени тяжести только у 3 (21%), в виде анемии, артрита и гепатита. В целом, терапия хорошо переносилась пациентами, а профиль токсичности был сопоставим с ранее опубликованными данными.
Заключение
По данным промежуточного анализа, структура ответа на терапию у пациентов, получавших ниволумаб в дозе 40 мг, сопоставима с пациентами, получавшими препарат в полной дозе (3 мг/кг). Распределение частоты встречаемости, времени появления и вариантов нежелательных явлений также схожи с группой пациентов, получающих стандартную терапию. Таким образом, можно предположить, что данный режим дозирования будет эффективен и безопасен у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина, однако необходимо продолжить исследование для получения заключительных результатов.
Ключевые слова
Лимфома Ходжкина, ниволумаб, иммунотерапия, PD1-ингибиторы, рецидивирующие лимфомы, резистентные лимфомы.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20410
[VALUE] => Array
(
[TEXT] => Liudmila V. Fedorova, Kirill V. Lepik, Natalia B. Mikhailova, Elena V. Kondakova, Yuri R. Zalyalov, Anastasia V. Beynarovich, Elena E. Davydova, Luibov A. Tsvetkova, Vadim V. Baykov, Elena V. Babenko, Lilia V. Stelmakh, Boris V. Afanasyev<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Liudmila V. Fedorova, Kirill V. Lepik, Natalia B. Mikhailova, Elena V. Kondakova, Yuri R. Zalyalov, Anastasia V. Beynarovich, Elena E. Davydova, Luibov A. Tsvetkova, Vadim V. Baykov, Elena V. Babenko, Lilia V. Stelmakh, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20411
[VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20412
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Aim of the study was to determine effectiveness and safety of therapy with Nivolumab 40 mg in patients with relapsed/refractory Hodgkin lymphoma.
</p>
<h2 style="text-align: justify;">Materials and methods</h2>
<p style="text-align: justify;">
Intermediate analysis included 14 patients with relapsed/refractory Hodgkin lymphoma who were treated with nivolumab 40 mg once per 14 days until disease progression/unacceptable toxicity. Response was assessed by PET/CT using LYRIC criteria every 3 month (6 cycles). The safety was estimated by registration adverse effects according to NCI CTCAE 4.03.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Median follow‐up time was 10 months. Median number of treatment cycles with nivolumab was 17 (12-22). Median dose of drug was 0,56 mg/kg (0.4-0.91 mg/kg). 9 patients (64.3%) achieved an objective response, 5 (35.7%) a complete response (CR), and 4 patients (28.6%) a partial response. 4 patients (28.6%) had intermediate response as their best response. Two (14.3%) patients had progressive disease (at the moment of 12th and 18th cycles). Ten (71.4%) patients had adverse effects (AE). Grade ¾ AE were reported in 3 (21%) patients and included an anemia, arthritis and hepatitis. In general, the treatment was well tolerated and the toxicity profile was similar to the previously published data.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
According to the intermediate analysis, the structure of the response to therapy in patients treated with nivolumab 40 mg was comparable to patients treated with nivolumab in standard dose (3 mg/kg). The distribution of frequency, time of occurence and structure of adverse events was also similar to the standard therapy group. In conclusion, our data indicates that nivolumab 40 mg can be an effective and safety treatment option for R/R HL patients, but it’s nessesary to continue the study to obtain the final results.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Hodgkin lymphoma, nivolumab, immunotherapy, PD1 inhibitors, relapsed lymphoma, refractory lymphoma.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
Aim of the study was to determine effectiveness and safety of therapy with Nivolumab 40 mg in patients with relapsed/refractory Hodgkin lymphoma.
Materials and methods
Intermediate analysis included 14 patients with relapsed/refractory Hodgkin lymphoma who were treated with nivolumab 40 mg once per 14 days until disease progression/unacceptable toxicity. Response was assessed by PET/CT using LYRIC criteria every 3 month (6 cycles). The safety was estimated by registration adverse effects according to NCI CTCAE 4.03.
Results
Median follow‐up time was 10 months. Median number of treatment cycles with nivolumab was 17 (12-22). Median dose of drug was 0,56 mg/kg (0.4-0.91 mg/kg). 9 patients (64.3%) achieved an objective response, 5 (35.7%) a complete response (CR), and 4 patients (28.6%) a partial response. 4 patients (28.6%) had intermediate response as their best response. Two (14.3%) patients had progressive disease (at the moment of 12th and 18th cycles). Ten (71.4%) patients had adverse effects (AE). Grade ¾ AE were reported in 3 (21%) patients and included an anemia, arthritis and hepatitis. In general, the treatment was well tolerated and the toxicity profile was similar to the previously published data.
Conclusion
According to the intermediate analysis, the structure of the response to therapy in patients treated with nivolumab 40 mg was comparable to patients treated with nivolumab in standard dose (3 mg/kg). The distribution of frequency, time of occurence and structure of adverse events was also similar to the standard therapy group. In conclusion, our data indicates that nivolumab 40 mg can be an effective and safety treatment option for R/R HL patients, but it’s nessesary to continue the study to obtain the final results.
Keywords
Hodgkin lymphoma, nivolumab, immunotherapy, PD1 inhibitors, relapsed lymphoma, refractory lymphoma.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20413
[VALUE] => Interim analysis of effectiveness and safety of Nivolumab 40 mg in relapsed/refractory Hodgkin lymphoma
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Interim analysis of effectiveness and safety of Nivolumab 40 mg in relapsed/refractory Hodgkin lymphoma
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20761
[VALUE] => 1397
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1397
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20762
[VALUE] => 1398
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1398
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Людмила В. Федорова, Кирилл В. Лепик, Наталия Б. Михайлова, Елена В. Кондакова, Юрий Р. Залялов, Анастасия В. Бейнарович, Елена Е. Давыдова, Любовь А. Цветкова, Вадим В. Байков, Елена В. Бабенко, Лилия В. Стельмах, Борис В. Афанасьев
Введение
Целью работы была оценка эффективности и безопасности терапии ниволумабом в дозе 40 мг у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина.
Материалы и методы
В промежуточный анализ были включены 14 пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина. Ниволумаб в дозе 40 мг вводился 1 раз в 2 недели до прогрессирования заболевания или развития тяжелых нежелательных явлений. Каждые 3 месяца (6 введений) производилась оценка ответа на терапию при использовании критериев LYRIC по данным ПЭТ/КТ, а также оценка наличия нежелательных явлений на терапию в соответствии с критериями NCI CTCAE 4.03.
Результаты
Медиана наблюдения составила 10 месяцев. Медиана введений ниволумаба 17 (12-22). Медиана дозы препарата составила 0,56 мг/кг (0,4-0,91 мг/кг). Объективный ответ был получен у 9 (64,3%) пациентов, полный ответ у 5 (35,7%) и частичный ответ у 4 (28,6%) пациентов. Неопределенный ответ установлен у 4 (28,6%) пациентов. За время наблюдения у 2 (14,3%) пациентов было зафиксировано прогрессирование заболевания (после 12 и 18 введений). Нежелательные явления любой степени тяжести были представлены у 10 (71,4%) пациентов, при этом 3/4 степени тяжести только у 3 (21%), в виде анемии, артрита и гепатита. В целом, терапия хорошо переносилась пациентами, а профиль токсичности был сопоставим с ранее опубликованными данными.
Заключение
По данным промежуточного анализа, структура ответа на терапию у пациентов, получавших ниволумаб в дозе 40 мг, сопоставима с пациентами, получавшими препарат в полной дозе (3 мг/кг). Распределение частоты встречаемости, времени появления и вариантов нежелательных явлений также схожи с группой пациентов, получающих стандартную терапию. Таким образом, можно предположить, что данный режим дозирования будет эффективен и безопасен у пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина, однако необходимо продолжить исследование для получения заключительных результатов.
Ключевые слова
Лимфома Ходжкина, ниволумаб, иммунотерапия, PD1-ингибиторы, рецидивирующие лимфомы, резистентные лимфомы.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20452
[VALUE] => Array
(
[TEXT] => Яна В. Гудожникова, Николай Н. Мамаев, Ильдар М. Бархатов, Алена И. Шакирова, Валерия А. Катерина, Сергей Н. Бондаренко, Татьяна Л. Гиндина, Валентина М. Кравцова, Людмила С. Зубаровская, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Яна В. Гудожникова, Николай Н. Мамаев, Ильдар М. Бархатов, Алена И. Шакирова, Валерия А. Катерина, Сергей Н. Бондаренко, Татьяна Л. Гиндина, Валентина М. Кравцова, Людмила С. Зубаровская, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20453
[VALUE] => Array
(
[TEXT] => Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20454
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) в настоящее время считается лучшим методом лечения ОМЛ с плохим прогнозом, который часто сопровождается посттрансплантационными рецидивами (ПТР). Среди ПТР могут быть молекулярные и цитологические варианты (мПТР и цПТР соответственно). Известно, что уровень экспрессии гена WT1 является хорошим индикатором массы продуцирующих его бластных элементов. С помощью этого теста имеется возможность ранней диагностики мПТР и оценка общей и бессобытийной выживаемости (ОВ и БСВ соответственно) и кумулятивной частоты рецидивов (КЧР) больных ОМЛ, леченных с использованием алло-ТГСК.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
Исследование включало 88 пациентов с ОМЛ в возрасте от 2 до 68 лет (медиана – 30 лет), которым была выполнена алло-ТГСК в нашем Центре в период с 2011 по 2017 годы. Уровни экспрессии гена WT1 измеряли серийно количественной ПЦР в реальном времени, а содержание бластов в тех же аспиратах костного мозга определяли в стандартно выбранных контрольных временных точках: перед трансплантацией (Д0) и в дни Д+30, Д+60 и Д+100 после ее выполнения. Пороговый уровень экспрессии гена WT1 был определен на основании измерения уровня экспрессии гена WT1 в аспиратах костного мозга здоровых доноров и равнялся 250 копиям WT1/10<sup>4</sup> копий гена ABL. Во всех временных точках были сформированы группы больных с повышенным и нормализованным уровнями экспрессии гена WT1 (>250 копий <250 копий соответственно) и рассчитана разница в 2-летней ОВ, БСВ и КЧР. Поскольку повышение уровня экспрессии гена WT1, отражающее содержание секретирующих этот ген бластов, может опережать по времени определяемые морфологом цПТР, мы измерили этот временный интервал у всех обследованных больных ОМЛ и сопоставили его с проведенной посттрансплантационной терапией.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Уровни экспрессии гена WT1 перед режимом кондиционирования варьировали от 0 до 56884 копий WT1/10<sup>4 </sup>копий гена ABL (медиана – 253 копии). По данным критериям лог-ранга, существенная разница в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 перед алло-ТГСК выглядела следующим образом: 79,5%, 69,8% и 28,2% против 31,8%, 22,7% и 58,9%, при p<0,001, p<0,001 и p=0,0019 соответственно. Различий в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 на день Д+30 после выполнения алло-ТГСК не было. Достоверные различия в 2-летней ОВ и КЧР наблюдались между этими группами на день Д+60 после выполнения алло-ТГСК (66,2% и 42,3% против 35,7% и 61,5% при p=0,012 и р=0,01 соответственно), в то время как достоверные различия в БСВ отсутствовали (52,3% против 38,5%, р=0,084). Наибольшие различия в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 имели место в контрольной временной точке Д+100 после алло-ТГСК (28,6%, 19% и 77,8% против 75,4%, 63,2% и 32,7% при р<0,001, р<0,001 и р<0,001 соответственно) (Рис.1). На основе пропорциональных рисков Кокса, независимое позитивное влияние на ОВ и БСВ сохранилось только для нормализованного во временной точке Д+100 после выполнения алло-ТГСК уровня экспрессии гена WT1 (р=0,011 и р=0,041) и наличия у больных хрРТПХ (р=0,038 и р=0,03). При этом отношение риска рецидива (125) было максимальным также на день Д+100. По нашим данным, мПТР и цПТР были зарегистрированы у 55/88 (62,5%) и 33/88 (37,5%) пациентов соответственно. У 33,3% пациентов (11/33) мПТР и цПТР по времени появления совпадали, в то время как в 22 наблюдениях цПТР отставали от мПТР на 13-321 день (медиана – 35). Задержка цПТР от мПТР частично может быть объяснено проводимой в клинике терапией, в частности, инфузиями донорских лимфоцитов и наличием у больных хронической РТПХ, что хорошо согласуется с данными литературы [Pozzi et al, 2013].
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Уровень повышенной и нормализованной экспрессии гена WT1 является удобным и полезным для клиники маркером молекулярно контролируемых ПТР и ремиссий ОМЛ. Оптимальной временной точкой для измерения уровня экспрессии гена WT1 в диагностике ПТР является Д+100, за которой, по мере снижения значимости, следуют Д0, Д+60 и Д+30. По нашим данным наудлинение продолжительности ОВ и БСВ сказывается также наличие у больных ОМЛ признаков хрРТПХ, что объясняется наметившуюся в клинике тенденцию лечить иммунотерапией диагностированные при серийном измерении уровни экспрессии гена WT1 мПТР [Di Grazia et al, 2016].
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Аллогенная трансплантация гемопоэтических стволовых клеток, острый миелоидный лейкоз, WT1, рецидив, молекулярный мониторинг.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) в настоящее время считается лучшим методом лечения ОМЛ с плохим прогнозом, который часто сопровождается посттрансплантационными рецидивами (ПТР). Среди ПТР могут быть молекулярные и цитологические варианты (мПТР и цПТР соответственно). Известно, что уровень экспрессии гена WT1 является хорошим индикатором массы продуцирующих его бластных элементов. С помощью этого теста имеется возможность ранней диагностики мПТР и оценка общей и бессобытийной выживаемости (ОВ и БСВ соответственно) и кумулятивной частоты рецидивов (КЧР) больных ОМЛ, леченных с использованием алло-ТГСК.
Пациенты и методы
Исследование включало 88 пациентов с ОМЛ в возрасте от 2 до 68 лет (медиана – 30 лет), которым была выполнена алло-ТГСК в нашем Центре в период с 2011 по 2017 годы. Уровни экспрессии гена WT1 измеряли серийно количественной ПЦР в реальном времени, а содержание бластов в тех же аспиратах костного мозга определяли в стандартно выбранных контрольных временных точках: перед трансплантацией (Д0) и в дни Д+30, Д+60 и Д+100 после ее выполнения. Пороговый уровень экспрессии гена WT1 был определен на основании измерения уровня экспрессии гена WT1 в аспиратах костного мозга здоровых доноров и равнялся 250 копиям WT1/104 копий гена ABL. Во всех временных точках были сформированы группы больных с повышенным и нормализованным уровнями экспрессии гена WT1 (>250 копий <250 копий соответственно) и рассчитана разница в 2-летней ОВ, БСВ и КЧР. Поскольку повышение уровня экспрессии гена WT1, отражающее содержание секретирующих этот ген бластов, может опережать по времени определяемые морфологом цПТР, мы измерили этот временный интервал у всех обследованных больных ОМЛ и сопоставили его с проведенной посттрансплантационной терапией.
Результаты
Уровни экспрессии гена WT1 перед режимом кондиционирования варьировали от 0 до 56884 копий WT1/104 копий гена ABL (медиана – 253 копии). По данным критериям лог-ранга, существенная разница в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 перед алло-ТГСК выглядела следующим образом: 79,5%, 69,8% и 28,2% против 31,8%, 22,7% и 58,9%, при p<0,001, p<0,001 и p=0,0019 соответственно. Различий в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 на день Д+30 после выполнения алло-ТГСК не было. Достоверные различия в 2-летней ОВ и КЧР наблюдались между этими группами на день Д+60 после выполнения алло-ТГСК (66,2% и 42,3% против 35,7% и 61,5% при p=0,012 и р=0,01 соответственно), в то время как достоверные различия в БСВ отсутствовали (52,3% против 38,5%, р=0,084). Наибольшие различия в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 имели место в контрольной временной точке Д+100 после алло-ТГСК (28,6%, 19% и 77,8% против 75,4%, 63,2% и 32,7% при р<0,001, р<0,001 и р<0,001 соответственно) (Рис.1). На основе пропорциональных рисков Кокса, независимое позитивное влияние на ОВ и БСВ сохранилось только для нормализованного во временной точке Д+100 после выполнения алло-ТГСК уровня экспрессии гена WT1 (р=0,011 и р=0,041) и наличия у больных хрРТПХ (р=0,038 и р=0,03). При этом отношение риска рецидива (125) было максимальным также на день Д+100. По нашим данным, мПТР и цПТР были зарегистрированы у 55/88 (62,5%) и 33/88 (37,5%) пациентов соответственно. У 33,3% пациентов (11/33) мПТР и цПТР по времени появления совпадали, в то время как в 22 наблюдениях цПТР отставали от мПТР на 13-321 день (медиана – 35). Задержка цПТР от мПТР частично может быть объяснено проводимой в клинике терапией, в частности, инфузиями донорских лимфоцитов и наличием у больных хронической РТПХ, что хорошо согласуется с данными литературы [Pozzi et al, 2013].
Заключение
Уровень повышенной и нормализованной экспрессии гена WT1 является удобным и полезным для клиники маркером молекулярно контролируемых ПТР и ремиссий ОМЛ. Оптимальной временной точкой для измерения уровня экспрессии гена WT1 в диагностике ПТР является Д+100, за которой, по мере снижения значимости, следуют Д0, Д+60 и Д+30. По нашим данным наудлинение продолжительности ОВ и БСВ сказывается также наличие у больных ОМЛ признаков хрРТПХ, что объясняется наметившуюся в клинике тенденцию лечить иммунотерапией диагностированные при серийном измерении уровни экспрессии гена WT1 мПТР [Di Grazia et al, 2016].
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, острый миелоидный лейкоз, WT1, рецидив, молекулярный мониторинг.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20455
[VALUE] => Array
(
[TEXT] => Yana V. Gudozhnikova, Nikolay N. Mamaev, Ildar M. Barkhatov, Аlena I. Shakirova, Valeria A. Katerina, Sergey N. Bondarenko, Tatiana L. Gindina, Valentina M. Kravtsova, Ludmila S. Zubarovskaya, Boris V. Afanasyev
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Yana V. Gudozhnikova, Nikolay N. Mamaev, Ildar M. Barkhatov, Аlena I. Shakirova, Valeria A. Katerina, Sergey N. Bondarenko, Tatiana L. Gindina, Valentina M. Kravtsova, Ludmila S. Zubarovskaya, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20456
[VALUE] => Array
(
[TEXT] => R. M. Gorbacheva Memorial Research Institute of Pediatric Oncology, Hematology and Transplantation, 1st Saint Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => R. M. Gorbacheva Memorial Research Institute of Pediatric Oncology, Hematology and Transplantation, 1st Saint Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20457
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is now considered the best treatment of AML with poor prognosis, which is, however, often followed by posttransplant relapses (PTR). Among PTR, molecular and cytological variants (mPTR and cPTR, respectively) are recognized. The WT1 gene is known to be an independent prognostic indicator of the mass of blast cells producing it. The serial measurement of WT1 expression levels provides a real possibility for early diagnosis of mPTR and an evaluation of the overall and event-free survival (OS and EFS, respectively) and the cumulative frequency of relapse (CIR) in patients with AML treated with allo-HSCT.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
The study included 88 AML patients aged 2 to 68 (median, 30 y.o.) who underwent allo-HSCT at our University between 2011 and 2017. WT1 gene expression levels were serially measured by real-time quantitative PCR, and marrow blast counts were performed in marrow samples at the standard control time points: before transplantation (D0) and on days D+30, D+60 and D+100 after transplantation. The WT1 threshold value was selected, as based on the measurement of expression levels of WT1 gene in bone marrow aspirates of healthy donors and determined as 250 WT1 copies/104 copies of ABL gene. At all the time points, groups of patients with elevated and normalized levels of WT1 gene expression (> 250 copies and < 250 copies, respectively) were formed, which allowed for calculating the difference in the 2-year OS, EFS and CIR. Since the increase in the expression of the WT1 gene reflecting the content of the blasts secreting this gene can precede the morphologically identified cPTR, we measured this time interval for all the examined AML patients taking in consideration the posttransplantation<br>
therapy.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
The levels of WT1 gene expression at allo-HSCT ranged from 0 to 56884 WT1/104 ABL copies (median – 253). According to the log-rank criteria, the difference in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression before allo-HSCT was as follows: 79.5%, 69.8%, 28.2% vs. 31.8%, 22.7% and 58.9%, at p<0.001, p<0.001, and p=0.0019, respectively. On D+30, we found no difference in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression. Significant differences in the 2-year OS and CIR in the two groups were found on D+60 (66.2% and 42.3% vs. 35.7% and 61.5% at p=0.012 and р=0.01, respectively), while there was still no significant difference in the EFS (52.3% vs. 38.5%, p=0.084). The greatest differences in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression occurred at the control time point D+100 (28.6%, 19% and 77.8% vs. 75.4% 63.2% and 32.7% at p<0.001, p<0.001, and p<0.001, respectively) (Fig.1). On the basis of proportional Cox risks, the independent positive effect on OS and EFS was preserved only for the normalized level of the WT1 gene expression (p=0.011 and p=0.041) at the time point D+100 after the allo-HSCT and in the presence of chronic GVHD (p=0.038 and p=0.03). In this case, the ratio of the risk of relapse (125) was maximal also on D+100. Concerning mPTR and cPTR, they were documented in 55/88 (62.5%) and 33/88 (37.5%) patients, respectively. In 33.3% of patients (11/33), mPTR and cPTR coincided in time, while in 22 cases cPTR occurred 13-321 (median – 35) days later than mPTR. According to the data obtained, this delay of cPTR from mPTR can be partially ascribed to the therapy performed at the clinic, in particular, donor lymphocyte infusions, and to presence of chronic GVHD in patients, thus being in good agreement with other research data [Pozzi et al, 2013].
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Elevated and normalized levels of WT1 gene expression are convenient and clinically useful markers of molecularly controlled mPTR and remission of AML. The optimal point for measuring the level of WT1 gene expression in PTR diagnostics is D+100, followed by D0, D+60 and D+30, as the significance decreases. According to our data, the duration of OS and EFS is also positively affected by the presence of chronic GVHD in AML patients after allo-HSCT, which explains the tendency to use immunotherapy to treat mPTR diagnosed by serial measurements of the WT1 gene expression levels [Di Grazia et al, 2016].
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Allogeneic stem cell transplantation, acute myeloid leukemia, WT1, relapse, molecular monitoring.
</p>
<p style="text-align: justify;">
<img width="805" alt="20_Figure1-2.png" src="/upload/medialibrary/376/20_figure1_2.png" height="711" title="20_Figure1-2.png"><br>
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is now considered the best treatment of AML with poor prognosis, which is, however, often followed by posttransplant relapses (PTR). Among PTR, molecular and cytological variants (mPTR and cPTR, respectively) are recognized. The WT1 gene is known to be an independent prognostic indicator of the mass of blast cells producing it. The serial measurement of WT1 expression levels provides a real possibility for early diagnosis of mPTR and an evaluation of the overall and event-free survival (OS and EFS, respectively) and the cumulative frequency of relapse (CIR) in patients with AML treated with allo-HSCT.
Patients and methods
The study included 88 AML patients aged 2 to 68 (median, 30 y.o.) who underwent allo-HSCT at our University between 2011 and 2017. WT1 gene expression levels were serially measured by real-time quantitative PCR, and marrow blast counts were performed in marrow samples at the standard control time points: before transplantation (D0) and on days D+30, D+60 and D+100 after transplantation. The WT1 threshold value was selected, as based on the measurement of expression levels of WT1 gene in bone marrow aspirates of healthy donors and determined as 250 WT1 copies/104 copies of ABL gene. At all the time points, groups of patients with elevated and normalized levels of WT1 gene expression (> 250 copies and < 250 copies, respectively) were formed, which allowed for calculating the difference in the 2-year OS, EFS and CIR. Since the increase in the expression of the WT1 gene reflecting the content of the blasts secreting this gene can precede the morphologically identified cPTR, we measured this time interval for all the examined AML patients taking in consideration the posttransplantation
therapy.
Results
The levels of WT1 gene expression at allo-HSCT ranged from 0 to 56884 WT1/104 ABL copies (median – 253). According to the log-rank criteria, the difference in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression before allo-HSCT was as follows: 79.5%, 69.8%, 28.2% vs. 31.8%, 22.7% and 58.9%, at p<0.001, p<0.001, and p=0.0019, respectively. On D+30, we found no difference in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression. Significant differences in the 2-year OS and CIR in the two groups were found on D+60 (66.2% and 42.3% vs. 35.7% and 61.5% at p=0.012 and р=0.01, respectively), while there was still no significant difference in the EFS (52.3% vs. 38.5%, p=0.084). The greatest differences in the 2-year OS, EFS and CIR between the groups of patients with elevated and normalized levels of WT1 gene expression occurred at the control time point D+100 (28.6%, 19% and 77.8% vs. 75.4% 63.2% and 32.7% at p<0.001, p<0.001, and p<0.001, respectively) (Fig.1). On the basis of proportional Cox risks, the independent positive effect on OS and EFS was preserved only for the normalized level of the WT1 gene expression (p=0.011 and p=0.041) at the time point D+100 after the allo-HSCT and in the presence of chronic GVHD (p=0.038 and p=0.03). In this case, the ratio of the risk of relapse (125) was maximal also on D+100. Concerning mPTR and cPTR, they were documented in 55/88 (62.5%) and 33/88 (37.5%) patients, respectively. In 33.3% of patients (11/33), mPTR and cPTR coincided in time, while in 22 cases cPTR occurred 13-321 (median – 35) days later than mPTR. According to the data obtained, this delay of cPTR from mPTR can be partially ascribed to the therapy performed at the clinic, in particular, donor lymphocyte infusions, and to presence of chronic GVHD in patients, thus being in good agreement with other research data [Pozzi et al, 2013].
Conclusion
Elevated and normalized levels of WT1 gene expression are convenient and clinically useful markers of molecularly controlled mPTR and remission of AML. The optimal point for measuring the level of WT1 gene expression in PTR diagnostics is D+100, followed by D0, D+60 and D+30, as the significance decreases. According to our data, the duration of OS and EFS is also positively affected by the presence of chronic GVHD in AML patients after allo-HSCT, which explains the tendency to use immunotherapy to treat mPTR diagnosed by serial measurements of the WT1 gene expression levels [Di Grazia et al, 2016].
Keywords
Allogeneic stem cell transplantation, acute myeloid leukemia, WT1, relapse, molecular monitoring.

[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20458
[VALUE] => The prognostic value of the WT1 gene expression on relapse and survival AML patients after allogeneic stem cell transplantation
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => The prognostic value of the WT1 gene expression on relapse and survival AML patients after allogeneic stem cell transplantation
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20771
[VALUE] => 1407
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1407
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20772
[VALUE] => 1408
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1408
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Яна В. Гудожникова, Николай Н. Мамаев, Ильдар М. Бархатов, Алена И. Шакирова, Валерия А. Катерина, Сергей Н. Бондаренко, Татьяна Л. Гиндина, Валентина М. Кравцова, Людмила С. Зубаровская, Борис В. Афанасьев
Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) в настоящее время считается лучшим методом лечения ОМЛ с плохим прогнозом, который часто сопровождается посттрансплантационными рецидивами (ПТР). Среди ПТР могут быть молекулярные и цитологические варианты (мПТР и цПТР соответственно). Известно, что уровень экспрессии гена WT1 является хорошим индикатором массы продуцирующих его бластных элементов. С помощью этого теста имеется возможность ранней диагностики мПТР и оценка общей и бессобытийной выживаемости (ОВ и БСВ соответственно) и кумулятивной частоты рецидивов (КЧР) больных ОМЛ, леченных с использованием алло-ТГСК.
Пациенты и методы
Исследование включало 88 пациентов с ОМЛ в возрасте от 2 до 68 лет (медиана – 30 лет), которым была выполнена алло-ТГСК в нашем Центре в период с 2011 по 2017 годы. Уровни экспрессии гена WT1 измеряли серийно количественной ПЦР в реальном времени, а содержание бластов в тех же аспиратах костного мозга определяли в стандартно выбранных контрольных временных точках: перед трансплантацией (Д0) и в дни Д+30, Д+60 и Д+100 после ее выполнения. Пороговый уровень экспрессии гена WT1 был определен на основании измерения уровня экспрессии гена WT1 в аспиратах костного мозга здоровых доноров и равнялся 250 копиям WT1/104 копий гена ABL. Во всех временных точках были сформированы группы больных с повышенным и нормализованным уровнями экспрессии гена WT1 (>250 копий <250 копий соответственно) и рассчитана разница в 2-летней ОВ, БСВ и КЧР. Поскольку повышение уровня экспрессии гена WT1, отражающее содержание секретирующих этот ген бластов, может опережать по времени определяемые морфологом цПТР, мы измерили этот временный интервал у всех обследованных больных ОМЛ и сопоставили его с проведенной посттрансплантационной терапией.
Результаты
Уровни экспрессии гена WT1 перед режимом кондиционирования варьировали от 0 до 56884 копий WT1/104 копий гена ABL (медиана – 253 копии). По данным критериям лог-ранга, существенная разница в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 перед алло-ТГСК выглядела следующим образом: 79,5%, 69,8% и 28,2% против 31,8%, 22,7% и 58,9%, при p<0,001, p<0,001 и p=0,0019 соответственно. Различий в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 на день Д+30 после выполнения алло-ТГСК не было. Достоверные различия в 2-летней ОВ и КЧР наблюдались между этими группами на день Д+60 после выполнения алло-ТГСК (66,2% и 42,3% против 35,7% и 61,5% при p=0,012 и р=0,01 соответственно), в то время как достоверные различия в БСВ отсутствовали (52,3% против 38,5%, р=0,084). Наибольшие различия в 2-летней ОВ, БСВ и КЧР между группами больных с повышенным и нормализованным уровнями экспрессии гена WT1 имели место в контрольной временной точке Д+100 после алло-ТГСК (28,6%, 19% и 77,8% против 75,4%, 63,2% и 32,7% при р<0,001, р<0,001 и р<0,001 соответственно) (Рис.1). На основе пропорциональных рисков Кокса, независимое позитивное влияние на ОВ и БСВ сохранилось только для нормализованного во временной точке Д+100 после выполнения алло-ТГСК уровня экспрессии гена WT1 (р=0,011 и р=0,041) и наличия у больных хрРТПХ (р=0,038 и р=0,03). При этом отношение риска рецидива (125) было максимальным также на день Д+100. По нашим данным, мПТР и цПТР были зарегистрированы у 55/88 (62,5%) и 33/88 (37,5%) пациентов соответственно. У 33,3% пациентов (11/33) мПТР и цПТР по времени появления совпадали, в то время как в 22 наблюдениях цПТР отставали от мПТР на 13-321 день (медиана – 35). Задержка цПТР от мПТР частично может быть объяснено проводимой в клинике терапией, в частности, инфузиями донорских лимфоцитов и наличием у больных хронической РТПХ, что хорошо согласуется с данными литературы [Pozzi et al, 2013].
Заключение
Уровень повышенной и нормализованной экспрессии гена WT1 является удобным и полезным для клиники маркером молекулярно контролируемых ПТР и ремиссий ОМЛ. Оптимальной временной точкой для измерения уровня экспрессии гена WT1 в диагностике ПТР является Д+100, за которой, по мере снижения значимости, следуют Д0, Д+60 и Д+30. По нашим данным наудлинение продолжительности ОВ и БСВ сказывается также наличие у больных ОМЛ признаков хрРТПХ, что объясняется наметившуюся в клинике тенденцию лечить иммунотерапией диагностированные при серийном измерении уровни экспрессии гена WT1 мПТР [Di Grazia et al, 2016].
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, острый миелоидный лейкоз, WT1, рецидив, молекулярный мониторинг.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20466
[VALUE] => Array
(
[TEXT] => Марина Н. Хоробрых, Наталья В. Минаева, Наталья А. Зорина, Екатерина Н. Зотина, Светлана В. Самарина, Елена Л. Назарова
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Марина Н. Хоробрых, Наталья В. Минаева, Наталья А. Зорина, Екатерина Н. Зотина, Светлана В. Самарина, Елена Л. Назарова
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20467
[VALUE] => Array
(
[TEXT] => Федеральное государственное бюджетное учреждение науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства», Киров, Россия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Федеральное государственное бюджетное учреждение науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства», Киров, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20468
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелобластным лейкозом (ОМЛ) высокого риска. Тем не менее, рецидив заболевания развивается у 40-70% пациентов в течение первого года после трансплантации, а достижение повторных ремиссий возможно лишь у 15-30% больных. Гипометилирующая (эпигенетическая) терапия представляется перспективным подходом у этой категории больных. Механизм действия гипометилирующих препаратов заключается в их способности увеличивать уровень регуляторных Т-клеток (Тregs, CD4+CD25+FOXP3+), которые играют ключевую роль в развитии иммунологической толерантности в посттрансплантационном периоде, снижая степень развития и выраженности реакции «трансплантат против хозяина» (РТПХ). Кроме того, отмечено стимулирующее действие этих препаратов на пул цитотоксических CD8+ Т-лимфоцитов, обеспечивающих реализацию опухолеспецифического ответа в реакции «трансплантат против лейкоза» (РТПЛ).
</p>
<h2 style="text-align: justify;">Цель</h2>
<p style="text-align: justify;">
Цель исследования состояла в оценке результатов применения азацитидина после алло-ТГСК у пациентов с ОМЛ.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
В 2015-2018 гг. в клинике Федерального государственного бюджетного учреждения науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства» (КНИИГиПК) выполнено 20 алло-ТГСК пациентам с ОМЛ. Из них 18 – взрослым пациентам (14 женщин и 4 мужчин) и 2 – детям. Миелоаблативный режим кондиционирования использовался в 5 (25%) случаях, в 15 (75%) – режим со сниженной интенсивностью. Родственная алло-ТГСК выполнена 15 (75%) пациентам, из них гаплоидентичная – 4, неродственная от полностью совместимого донора – 5. Из 20 больных, на момент оценки живы 9 (45%). 11 (55%) пациентов погибли в разные сроки после алло-ТГСК: причинами смерти являлись тяжелые инфекционные осложнения, тяжелая острая реакция трансплантат против хозяина, тромботическая микроангиопатия, ранний рецидив заболевания. Курсы азацитидина с профилактической целью получили 7 пациентов с ОМЛ высокого риска. Из них 6 женщин и 1 мужчина, с медианой возраста 36,7 лет (диапазон: 20-50 лет). Терапию азацитидином начинали после восстановления кроветворения в среднем на Д+85 (диапазон: 40–121 день), при отсутствии тяжелых инфекционных и других осложнений. Препарат назначали по схеме 35 мг/м2 подкожно в течение 5-7 суток, каждые 28 дней, медиана 8 курсов. В 3 случаях азацитидин комбинировали с инфузией донорских лимфоцитов (DLI – donor lymphocyte infusion).
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Все больные, получавшие азацитидин, на момент исследования живы. У 6 из них сохраняется ремиссия заболевания. Перед назначением азацитидина полное донорское кроветворение имели 2 пациента, у 1 полный донорский химеризм достигнут через 2 месяца терапии, у 4 отмечался смешанный донорский химеризм. У 1 из них возник поздний рецидив заболевания после 3 курсов азацитидина, в настоящее время он получает противорецидивную химиотерапию (ХТ).
</p>
<h2 style="text-align: justify;">Клинический случай</h2>
<p style="text-align: justify;">
Пациентка Т., 22 лет, ОМЛ, t(8;21), ПР 3 неродственная аллоТГСК выполнена в марте 2016 г. Интервал от начала лечения до аллоТГСК составил 27 мес. Профилактическое введение азацитидина начато на +56 день после аллоТГСК в дозе 35 мг\м2 каждые 5 дней 28 дневного цикла №6, терапия закончена в октябре 2016 г. Мониторинг общего и линейного химеризма проводился в дни +30, +56, +84, +119, +147, +174 и +360 и показал наличие стойкого полного донорского кроветворения. Ремиссия заболевания подтверждена результатами миелограммы. Однако, на Д+414 выявлен поздний рецидив-3 заболевания (в миелограмме 30% бластов), снижение общего донорского химеризма (41,3% собственных клеток). С целью достижения ремиссии – 4 проведен курс FLAG с DLI. Восстановление лейкоцитов отмечалось на +25 сутки после ХТ. Достижение ремиссии-4 подтверждено результатами миелограммы, молекулярным исследованием. С июня по июль 2017 г. проведено два 5-дневных курса азацитидина 75 мг/м2 с DLI в возрастающей дозе, после чего достигнут полный донорский химеризм. В течение последующего года пациентка получила суммарно 12 курсов азацитидина 75 мг/м2 с эскалацией дозы донорских лимфоцитов. У больной сохраняется полная клинико-гематологическая и молекулярная ремиссия заболевания. Планируется продолжить профилактическое введение донорских лимфоцитов в монорежиме. Учитывая небольшую группу пациентов (7 человек), оценка эффективности терапии азацитидином преждевременна. Медиана наблюдения составила 408 дней. Наиболее частыми нежелательными явлениями при применении азацитидина были периферические цитопении 1 степени, не требующие отмены препарата или коррекции дозы. Среди негематологических побочных эффектов отмечались реакции в месте инъекции, тошнота, диарея и слабость, в большинстве случаев не выходившие за пределы I-II степени токсичности.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Принимая во внимание положительный опыт применения препарата у пациентов с ОМЛ высокого риска после алло-ТГСК, терапия азацитидином представляется перспективной опцией как для профилактики рецидивов, так и в целях достижения повторных ремиссий заболевания. Для оценки влияния азацитидина, в том числе в сочетании с DLI, на безрецидивную и общую выживаемость требуется дальнейшее накопление клинического опыта.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Острый миелобластный лейкоз, аллогенная трансплантация гемопоэтических стволовых клеток, азацитидин, химеризм, инфузия донорских лимфоцитов.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелобластным лейкозом (ОМЛ) высокого риска. Тем не менее, рецидив заболевания развивается у 40-70% пациентов в течение первого года после трансплантации, а достижение повторных ремиссий возможно лишь у 15-30% больных. Гипометилирующая (эпигенетическая) терапия представляется перспективным подходом у этой категории больных. Механизм действия гипометилирующих препаратов заключается в их способности увеличивать уровень регуляторных Т-клеток (Тregs, CD4+CD25+FOXP3+), которые играют ключевую роль в развитии иммунологической толерантности в посттрансплантационном периоде, снижая степень развития и выраженности реакции «трансплантат против хозяина» (РТПХ). Кроме того, отмечено стимулирующее действие этих препаратов на пул цитотоксических CD8+ Т-лимфоцитов, обеспечивающих реализацию опухолеспецифического ответа в реакции «трансплантат против лейкоза» (РТПЛ).
Цель
Цель исследования состояла в оценке результатов применения азацитидина после алло-ТГСК у пациентов с ОМЛ.
Пациенты и методы
В 2015-2018 гг. в клинике Федерального государственного бюджетного учреждения науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства» (КНИИГиПК) выполнено 20 алло-ТГСК пациентам с ОМЛ. Из них 18 – взрослым пациентам (14 женщин и 4 мужчин) и 2 – детям. Миелоаблативный режим кондиционирования использовался в 5 (25%) случаях, в 15 (75%) – режим со сниженной интенсивностью. Родственная алло-ТГСК выполнена 15 (75%) пациентам, из них гаплоидентичная – 4, неродственная от полностью совместимого донора – 5. Из 20 больных, на момент оценки живы 9 (45%). 11 (55%) пациентов погибли в разные сроки после алло-ТГСК: причинами смерти являлись тяжелые инфекционные осложнения, тяжелая острая реакция трансплантат против хозяина, тромботическая микроангиопатия, ранний рецидив заболевания. Курсы азацитидина с профилактической целью получили 7 пациентов с ОМЛ высокого риска. Из них 6 женщин и 1 мужчина, с медианой возраста 36,7 лет (диапазон: 20-50 лет). Терапию азацитидином начинали после восстановления кроветворения в среднем на Д+85 (диапазон: 40–121 день), при отсутствии тяжелых инфекционных и других осложнений. Препарат назначали по схеме 35 мг/м2 подкожно в течение 5-7 суток, каждые 28 дней, медиана 8 курсов. В 3 случаях азацитидин комбинировали с инфузией донорских лимфоцитов (DLI – donor lymphocyte infusion).
Результаты
Все больные, получавшие азацитидин, на момент исследования живы. У 6 из них сохраняется ремиссия заболевания. Перед назначением азацитидина полное донорское кроветворение имели 2 пациента, у 1 полный донорский химеризм достигнут через 2 месяца терапии, у 4 отмечался смешанный донорский химеризм. У 1 из них возник поздний рецидив заболевания после 3 курсов азацитидина, в настоящее время он получает противорецидивную химиотерапию (ХТ).
Клинический случай
Пациентка Т., 22 лет, ОМЛ, t(8;21), ПР 3 неродственная аллоТГСК выполнена в марте 2016 г. Интервал от начала лечения до аллоТГСК составил 27 мес. Профилактическое введение азацитидина начато на +56 день после аллоТГСК в дозе 35 мг\м2 каждые 5 дней 28 дневного цикла №6, терапия закончена в октябре 2016 г. Мониторинг общего и линейного химеризма проводился в дни +30, +56, +84, +119, +147, +174 и +360 и показал наличие стойкого полного донорского кроветворения. Ремиссия заболевания подтверждена результатами миелограммы. Однако, на Д+414 выявлен поздний рецидив-3 заболевания (в миелограмме 30% бластов), снижение общего донорского химеризма (41,3% собственных клеток). С целью достижения ремиссии – 4 проведен курс FLAG с DLI. Восстановление лейкоцитов отмечалось на +25 сутки после ХТ. Достижение ремиссии-4 подтверждено результатами миелограммы, молекулярным исследованием. С июня по июль 2017 г. проведено два 5-дневных курса азацитидина 75 мг/м2 с DLI в возрастающей дозе, после чего достигнут полный донорский химеризм. В течение последующего года пациентка получила суммарно 12 курсов азацитидина 75 мг/м2 с эскалацией дозы донорских лимфоцитов. У больной сохраняется полная клинико-гематологическая и молекулярная ремиссия заболевания. Планируется продолжить профилактическое введение донорских лимфоцитов в монорежиме. Учитывая небольшую группу пациентов (7 человек), оценка эффективности терапии азацитидином преждевременна. Медиана наблюдения составила 408 дней. Наиболее частыми нежелательными явлениями при применении азацитидина были периферические цитопении 1 степени, не требующие отмены препарата или коррекции дозы. Среди негематологических побочных эффектов отмечались реакции в месте инъекции, тошнота, диарея и слабость, в большинстве случаев не выходившие за пределы I-II степени токсичности.
Заключение
Принимая во внимание положительный опыт применения препарата у пациентов с ОМЛ высокого риска после алло-ТГСК, терапия азацитидином представляется перспективной опцией как для профилактики рецидивов, так и в целях достижения повторных ремиссий заболевания. Для оценки влияния азацитидина, в том числе в сочетании с DLI, на безрецидивную и общую выживаемость требуется дальнейшее накопление клинического опыта.
Ключевые слова
Острый миелобластный лейкоз, аллогенная трансплантация гемопоэтических стволовых клеток, азацитидин, химеризм, инфузия донорских лимфоцитов.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20469
[VALUE] => Array
(
[TEXT] => Marina N. Horobrykh, Natalia V. Minaeva, Natalia A. Zorina, Ekaterina N. Zotina, Svetlana V. Samarina, Elena L. Nazarova
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Marina N. Horobrykh, Natalia V. Minaeva, Natalia A. Zorina, Ekaterina N. Zotina, Svetlana V. Samarina, Elena L. Nazarova
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20470
[VALUE] => Array
(
[TEXT] => Kirov Research Institute of Hematology and Blood Transfusion, Kirov, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Kirov Research Institute of Hematology and Blood Transfusion, Kirov, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20471
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is an effective treatment method in patients with high-risk acute myeloid leukemia (AML). Nevertheless, disease relapse develops in 40-70% of patients during the first posttransplant year, and achievement of repeated remissions is possible only in 15-30% of patients. Hypomethylating, or epigenetic therapy (HM) appears to be a promising approach to these patients. The mechanism of HM drug action includes their ability to increase the levels of regulatory T-cells (Тregs, CD4+CD25+FOXP3+), which play a key role in the development of immunological tolerance in the post-transplant period, reducing the degree of development and severity of “graft-versus-host disease” (GVHD). In addition, the stimulating effect of these drugs on the pool of cytotoxic CD8+T-lymphocytes provides implementation of a tumor-specific response in the graft-versus-leukemia (GVL) effect.
</p>
<h2 style="text-align: justify;">Aim</h2>
<p style="text-align: justify;">
Objective of this study was to evaluate the results of the azacitidine application after allo-HSCT in patients with AML.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
Twenty patients with AML were transplanted between 2015 and 2018 at the Federal State Institute of Science “Kirov Research Institute of Hematology and Blood Transfusion of the Federal Medical and Biological Agency of Russia” including 18 adult patients (14 women and 4 men) and 2 children. Myeloablative conditioning was used in 5 (25%) cases. In 15 (75%) patients, the reduced intensity regimen was applied. Related allo-HSCT was performed in 15 (75%) patients, 4 of them were transplanted from HLA-haploidentical donors. Unrelated allo-HSCT was carried out from fully matched donors in 5 cases. Out of 20 patients, 9 (45%) patients were alive at the time of evaluation. Eleven (55%) patients died at different times after alloHSCT due to severe infectious complications, severe acute GVHD, thrombotic microangiopathy, early relapse of the disease. Preventive azacitidine courses were given to 7 patients with high-risk AML. Of these, 6 women and 1 man, with a median age of 36.7 years (range: 20-50 years). Azacitidine therapy was started after hematopoietic recovery on the average at day +85 (range: 40-121 days) in the absence of severe infectious and other complications. The drug was administered according to the scheme: 35 mg/m2 subcutaneously for 5-7 days, every 28 days, with a median of 8 courses. In 3 cases, azacitidine was combined with donor lymphocyte infusions (DLI).
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
All the patients who received azacitidine at the time of the study are alive. Six of them have a disease remission. Prior to the azacitidine administration, 2 patients had complete donor hematopoiesis, in 1 complete donor chimerism was achieved in 2 months of therapy, in 4 there was a mixed donor chimerism. In 1 of them, a late relapse occurred after 3 courses of azacitidine, and now he receives antirelapse chemotherapy (ChT).
</p>
<h2 style="text-align: justify;">Clinical case</h2>
<p style="text-align: justify;">
Patient T., female, 22 years old, AML, t(8;21), complete remission-3, unrelated allo-HSCT was performed in March 2016. The interval from treatment initiation to allo-HSCT was 27 months. The azacitidine prophylactic administration was started at day +56 after allo-HSCT at a dose of 35mg/m2 every 5 days of the 28-day cycle, for up to 6 cycles, and the therapy was completed in October 2016. Monitoring of general and lineage-specific chimerism was carried out at days +30, +56, +84, +119, +147, +174 and +360 and showed the presence of strong complete donor hematopoiesis. The disease remission is confirmed by the bone marrow evaluation. However, a late relapse-3 of the disease was shown at day +414 (30% of blast cells in the bone marrow), along with decrease in complete donor chimerism (41.3% of its own cells). In order to achieve remission-4, a course of FLAG with DLI was conducted. Recovery of leukocytes was observed at day +25 after ChT. Achievement of remission-4 was confirmed by the bone marrow evaluation and molecular assays. From June to July 2017, two 5-day courses of azacitidine 75 mg/m2 with DLI at an increasing dose were carried out, followed by achievement of complete donor chimerism. Over the following year, the patient received a total of 12 azacitidine courses (75 mg/m2), with escalated dose of donor lymphocytes. The patient retains a complete clinical, hematological and molecular remission of the disease. It is planned to continue prophylactic donor lymphocytes administration as a monotherapy. Given the small group of patients (7 people), it is premature to evaluate efficiency of azacitidine therapy. The median follow-up was 408 days. Peripheral cytopenia (grade 1) was the most frequent adverse event of azacitidine treatment, which did not require drug withdrawal or dose adjustment. Among non-hematological side effects, we observed reactions at the injection site, nausea, diarrhea and weakness, in most cases not exceeding I-II degree of toxicity.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Taking into account the positive experience with azacitidine usage in the patients with high-risk AML after allo-HSCT, this therapy appears to be a promising option both for relapse prevention and for achievement of repeated disease remissions. To assess azacitidine influence upon relapse-free and overall survival, including its combination with DLI, further accumulation of clinical experience is required.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Acute myeloid leukemia, allogeneic hematopoietic stem cell transplantation, azacitidine, chimerism, donor lymphocyte infusion.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is an effective treatment method in patients with high-risk acute myeloid leukemia (AML). Nevertheless, disease relapse develops in 40-70% of patients during the first posttransplant year, and achievement of repeated remissions is possible only in 15-30% of patients. Hypomethylating, or epigenetic therapy (HM) appears to be a promising approach to these patients. The mechanism of HM drug action includes their ability to increase the levels of regulatory T-cells (Тregs, CD4+CD25+FOXP3+), which play a key role in the development of immunological tolerance in the post-transplant period, reducing the degree of development and severity of “graft-versus-host disease” (GVHD). In addition, the stimulating effect of these drugs on the pool of cytotoxic CD8+T-lymphocytes provides implementation of a tumor-specific response in the graft-versus-leukemia (GVL) effect.
Aim
Objective of this study was to evaluate the results of the azacitidine application after allo-HSCT in patients with AML.
Patients and methods
Twenty patients with AML were transplanted between 2015 and 2018 at the Federal State Institute of Science “Kirov Research Institute of Hematology and Blood Transfusion of the Federal Medical and Biological Agency of Russia” including 18 adult patients (14 women and 4 men) and 2 children. Myeloablative conditioning was used in 5 (25%) cases. In 15 (75%) patients, the reduced intensity regimen was applied. Related allo-HSCT was performed in 15 (75%) patients, 4 of them were transplanted from HLA-haploidentical donors. Unrelated allo-HSCT was carried out from fully matched donors in 5 cases. Out of 20 patients, 9 (45%) patients were alive at the time of evaluation. Eleven (55%) patients died at different times after alloHSCT due to severe infectious complications, severe acute GVHD, thrombotic microangiopathy, early relapse of the disease. Preventive azacitidine courses were given to 7 patients with high-risk AML. Of these, 6 women and 1 man, with a median age of 36.7 years (range: 20-50 years). Azacitidine therapy was started after hematopoietic recovery on the average at day +85 (range: 40-121 days) in the absence of severe infectious and other complications. The drug was administered according to the scheme: 35 mg/m2 subcutaneously for 5-7 days, every 28 days, with a median of 8 courses. In 3 cases, azacitidine was combined with donor lymphocyte infusions (DLI).
Results
All the patients who received azacitidine at the time of the study are alive. Six of them have a disease remission. Prior to the azacitidine administration, 2 patients had complete donor hematopoiesis, in 1 complete donor chimerism was achieved in 2 months of therapy, in 4 there was a mixed donor chimerism. In 1 of them, a late relapse occurred after 3 courses of azacitidine, and now he receives antirelapse chemotherapy (ChT).
Clinical case
Patient T., female, 22 years old, AML, t(8;21), complete remission-3, unrelated allo-HSCT was performed in March 2016. The interval from treatment initiation to allo-HSCT was 27 months. The azacitidine prophylactic administration was started at day +56 after allo-HSCT at a dose of 35mg/m2 every 5 days of the 28-day cycle, for up to 6 cycles, and the therapy was completed in October 2016. Monitoring of general and lineage-specific chimerism was carried out at days +30, +56, +84, +119, +147, +174 and +360 and showed the presence of strong complete donor hematopoiesis. The disease remission is confirmed by the bone marrow evaluation. However, a late relapse-3 of the disease was shown at day +414 (30% of blast cells in the bone marrow), along with decrease in complete donor chimerism (41.3% of its own cells). In order to achieve remission-4, a course of FLAG with DLI was conducted. Recovery of leukocytes was observed at day +25 after ChT. Achievement of remission-4 was confirmed by the bone marrow evaluation and molecular assays. From June to July 2017, two 5-day courses of azacitidine 75 mg/m2 with DLI at an increasing dose were carried out, followed by achievement of complete donor chimerism. Over the following year, the patient received a total of 12 azacitidine courses (75 mg/m2), with escalated dose of donor lymphocytes. The patient retains a complete clinical, hematological and molecular remission of the disease. It is planned to continue prophylactic donor lymphocytes administration as a monotherapy. Given the small group of patients (7 people), it is premature to evaluate efficiency of azacitidine therapy. The median follow-up was 408 days. Peripheral cytopenia (grade 1) was the most frequent adverse event of azacitidine treatment, which did not require drug withdrawal or dose adjustment. Among non-hematological side effects, we observed reactions at the injection site, nausea, diarrhea and weakness, in most cases not exceeding I-II degree of toxicity.
Conclusion
Taking into account the positive experience with azacitidine usage in the patients with high-risk AML after allo-HSCT, this therapy appears to be a promising option both for relapse prevention and for achievement of repeated disease remissions. To assess azacitidine influence upon relapse-free and overall survival, including its combination with DLI, further accumulation of clinical experience is required.
Keywords
Acute myeloid leukemia, allogeneic hematopoietic stem cell transplantation, azacitidine, chimerism, donor lymphocyte infusion.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20472
[VALUE] => Experience with hypomethylating drug application in allogeneic hematopoietic stem cell transplantation
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Experience with hypomethylating drug application in allogeneic hematopoietic stem cell transplantation
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20473
[VALUE] => 1409
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1409
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20474
[VALUE] => 1410
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1410
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Марина Н. Хоробрых, Наталья В. Минаева, Наталья А. Зорина, Екатерина Н. Зотина, Светлана В. Самарина, Елена Л. Назарова
Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелобластным лейкозом (ОМЛ) высокого риска. Тем не менее, рецидив заболевания развивается у 40-70% пациентов в течение первого года после трансплантации, а достижение повторных ремиссий возможно лишь у 15-30% больных. Гипометилирующая (эпигенетическая) терапия представляется перспективным подходом у этой категории больных. Механизм действия гипометилирующих препаратов заключается в их способности увеличивать уровень регуляторных Т-клеток (Тregs, CD4+CD25+FOXP3+), которые играют ключевую роль в развитии иммунологической толерантности в посттрансплантационном периоде, снижая степень развития и выраженности реакции «трансплантат против хозяина» (РТПХ). Кроме того, отмечено стимулирующее действие этих препаратов на пул цитотоксических CD8+ Т-лимфоцитов, обеспечивающих реализацию опухолеспецифического ответа в реакции «трансплантат против лейкоза» (РТПЛ).
Цель
Цель исследования состояла в оценке результатов применения азацитидина после алло-ТГСК у пациентов с ОМЛ.
Пациенты и методы
В 2015-2018 гг. в клинике Федерального государственного бюджетного учреждения науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства» (КНИИГиПК) выполнено 20 алло-ТГСК пациентам с ОМЛ. Из них 18 – взрослым пациентам (14 женщин и 4 мужчин) и 2 – детям. Миелоаблативный режим кондиционирования использовался в 5 (25%) случаях, в 15 (75%) – режим со сниженной интенсивностью. Родственная алло-ТГСК выполнена 15 (75%) пациентам, из них гаплоидентичная – 4, неродственная от полностью совместимого донора – 5. Из 20 больных, на момент оценки живы 9 (45%). 11 (55%) пациентов погибли в разные сроки после алло-ТГСК: причинами смерти являлись тяжелые инфекционные осложнения, тяжелая острая реакция трансплантат против хозяина, тромботическая микроангиопатия, ранний рецидив заболевания. Курсы азацитидина с профилактической целью получили 7 пациентов с ОМЛ высокого риска. Из них 6 женщин и 1 мужчина, с медианой возраста 36,7 лет (диапазон: 20-50 лет). Терапию азацитидином начинали после восстановления кроветворения в среднем на Д+85 (диапазон: 40–121 день), при отсутствии тяжелых инфекционных и других осложнений. Препарат назначали по схеме 35 мг/м2 подкожно в течение 5-7 суток, каждые 28 дней, медиана 8 курсов. В 3 случаях азацитидин комбинировали с инфузией донорских лимфоцитов (DLI – donor lymphocyte infusion).
Результаты
Все больные, получавшие азацитидин, на момент исследования живы. У 6 из них сохраняется ремиссия заболевания. Перед назначением азацитидина полное донорское кроветворение имели 2 пациента, у 1 полный донорский химеризм достигнут через 2 месяца терапии, у 4 отмечался смешанный донорский химеризм. У 1 из них возник поздний рецидив заболевания после 3 курсов азацитидина, в настоящее время он получает противорецидивную химиотерапию (ХТ).
Клинический случай
Пациентка Т., 22 лет, ОМЛ, t(8;21), ПР 3 неродственная аллоТГСК выполнена в марте 2016 г. Интервал от начала лечения до аллоТГСК составил 27 мес. Профилактическое введение азацитидина начато на +56 день после аллоТГСК в дозе 35 мг\м2 каждые 5 дней 28 дневного цикла №6, терапия закончена в октябре 2016 г. Мониторинг общего и линейного химеризма проводился в дни +30, +56, +84, +119, +147, +174 и +360 и показал наличие стойкого полного донорского кроветворения. Ремиссия заболевания подтверждена результатами миелограммы. Однако, на Д+414 выявлен поздний рецидив-3 заболевания (в миелограмме 30% бластов), снижение общего донорского химеризма (41,3% собственных клеток). С целью достижения ремиссии – 4 проведен курс FLAG с DLI. Восстановление лейкоцитов отмечалось на +25 сутки после ХТ. Достижение ремиссии-4 подтверждено результатами миелограммы, молекулярным исследованием. С июня по июль 2017 г. проведено два 5-дневных курса азацитидина 75 мг/м2 с DLI в возрастающей дозе, после чего достигнут полный донорский химеризм. В течение последующего года пациентка получила суммарно 12 курсов азацитидина 75 мг/м2 с эскалацией дозы донорских лимфоцитов. У больной сохраняется полная клинико-гематологическая и молекулярная ремиссия заболевания. Планируется продолжить профилактическое введение донорских лимфоцитов в монорежиме. Учитывая небольшую группу пациентов (7 человек), оценка эффективности терапии азацитидином преждевременна. Медиана наблюдения составила 408 дней. Наиболее частыми нежелательными явлениями при применении азацитидина были периферические цитопении 1 степени, не требующие отмены препарата или коррекции дозы. Среди негематологических побочных эффектов отмечались реакции в месте инъекции, тошнота, диарея и слабость, в большинстве случаев не выходившие за пределы I-II степени токсичности.
Заключение
Принимая во внимание положительный опыт применения препарата у пациентов с ОМЛ высокого риска после алло-ТГСК, терапия азацитидином представляется перспективной опцией как для профилактики рецидивов, так и в целях достижения повторных ремиссий заболевания. Для оценки влияния азацитидина, в том числе в сочетании с DLI, на безрецидивную и общую выживаемость требуется дальнейшее накопление клинического опыта.
Ключевые слова
Острый миелобластный лейкоз, аллогенная трансплантация гемопоэтических стволовых клеток, азацитидин, химеризм, инфузия донорских лимфоцитов.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20502
[VALUE] => Array
(
[TEXT] => Андрей В. Козлов, Илья В. Казанцев, Елена В. Морозова, Татьяна В. Юхта, Полина С. Толкунова, Асмик Г. Геворгян, Михаил М. Канунников, Кирилл В. Лепик, Юрий Р. Залялов, Елена В. Бабенко, Мария А. Эстрина, Наталья Б. Михайлова, Людмила С. Зубаровская, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Андрей В. Козлов, Илья В. Казанцев, Елена В. Морозова, Татьяна В. Юхта, Полина С. Толкунова, Асмик Г. Геворгян, Михаил М. Канунников, Кирилл В. Лепик, Юрий Р. Залялов, Елена В. Бабенко, Мария А. Эстрина, Наталья Б. Михайлова, Людмила С. Зубаровская, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20503
[VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20504
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Применение стандартных схем терапии удается излечивает до 70-90% пациентов, страдающих лимфомой Ходжкина (ЛХ). Аутологичная трансплантация гемопоэтических стволовых клеток (ауто-ТГСК) является эффективным способом терапии в случае химиочувствительного рецидива или достижения ремиссии при первично рефрактерном течении ЛХ. Несмотря на уже многолетнее использование, наличие крупных рандомизированных исследований, подтвердивших эффективность данного метода у взрослых, роль ауто-ТГСК у детей с ЛХ изучена в меньшей степени и количество крупных публикаций, посвященных данному вопросу, невелико.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
В работу включено 66 пациентов с ЛХ в возрасте от 4 до 18 лет (медиана возраста – 16), пролеченных за период 1993-2017 гг. Распределение по гистологическому варианту было следующим: нодулярный склероз – 59 человек (89%), смешанно-клеточный вариант – 6 (9%), лимфоидное истощение – 1 (2%). На момент постановки диагноза у 29 (44%) отмечалась IV стадия ЛХ, 18 (27%) – III стадия, 17 (26%) – II стадия, 2 (3%) – I стадия, В-симптомы – 43 человека (65%), рецидивирующее течение – 45 (68%), рефрактерное течение – 21 (32%). Первая линия терапии проводилась по протоколу GPOH-HD у 37 пациентов (56%), по протоколу BEACOPP – 21 (32%), по протоколу ABVD – 8 (12%). Вторая линия терапия – IEP/ABVD в случае использования протокола GPOHHD и в случае использования других протоколов – DHAP или ICE. Ранний рецидив ЛХ (<12 месяцев) отмечался у 26 человек (58%), поздний рецидив – 19 (42%). Медиана линий терапии перед ауто-ТГСК – 2 (1-6). Полная ремиссия на момент ауто-ТГСК была диагностирована у 25 человек (38%), частичная ремиссия – 25 (38%), стабилизация – 6 (9%) и прогрессия заболевания – 10 (15%). В рамках ауто-ТГСК назначались следующие режимы кондиционирования: BEAM – 24 пациента (36%), BeEAM – 22 (33%), CBV – 13 (20%), другие режимы кондиционирования – 7 (11%).
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Долгосрочная общая выживаемость (ОВ) всех пациентов составила 48% и выживаемость без прогрессирования – 41%. ОВ в случае химиочувствительного и химиорезистентного течения – 64% и 33%, соответственно (p=0,005). Общая выживаемость при использовании режима кондиционирования BeEAM составила 62%, BEAM– 51%. (p=0,6). Трансплантационная летальность составила 4,5%. Причины летального исхода: инфекционные осложнения – 2 человека, токсические осложнения – 1 (фиброз легких).
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
При использовании ауто-ТГСК удается излечить примерно половину детей и подростков, страдающих рецидивирующим или рефрактерным течением ЛХ. Показанием для ауто-ТГСК у детей, как и у взрослых, является химиочувствительное течение. Режимы кондиционирования BEAM и BeEAM одинаково эффективны.</p><h2 style="text-align: justify;"> Ключевые слова</h2>
<p style="text-align: justify;">Лимфома Ходжкина, детский возраст, трансплантация гемопоэтических стволовых клеток, аутологичная, уровни выживаемости.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Применение стандартных схем терапии удается излечивает до 70-90% пациентов, страдающих лимфомой Ходжкина (ЛХ). Аутологичная трансплантация гемопоэтических стволовых клеток (ауто-ТГСК) является эффективным способом терапии в случае химиочувствительного рецидива или достижения ремиссии при первично рефрактерном течении ЛХ. Несмотря на уже многолетнее использование, наличие крупных рандомизированных исследований, подтвердивших эффективность данного метода у взрослых, роль ауто-ТГСК у детей с ЛХ изучена в меньшей степени и количество крупных публикаций, посвященных данному вопросу, невелико.
Материалы и методы
В работу включено 66 пациентов с ЛХ в возрасте от 4 до 18 лет (медиана возраста – 16), пролеченных за период 1993-2017 гг. Распределение по гистологическому варианту было следующим: нодулярный склероз – 59 человек (89%), смешанно-клеточный вариант – 6 (9%), лимфоидное истощение – 1 (2%). На момент постановки диагноза у 29 (44%) отмечалась IV стадия ЛХ, 18 (27%) – III стадия, 17 (26%) – II стадия, 2 (3%) – I стадия, В-симптомы – 43 человека (65%), рецидивирующее течение – 45 (68%), рефрактерное течение – 21 (32%). Первая линия терапии проводилась по протоколу GPOH-HD у 37 пациентов (56%), по протоколу BEACOPP – 21 (32%), по протоколу ABVD – 8 (12%). Вторая линия терапия – IEP/ABVD в случае использования протокола GPOHHD и в случае использования других протоколов – DHAP или ICE. Ранний рецидив ЛХ (<12 месяцев) отмечался у 26 человек (58%), поздний рецидив – 19 (42%). Медиана линий терапии перед ауто-ТГСК – 2 (1-6). Полная ремиссия на момент ауто-ТГСК была диагностирована у 25 человек (38%), частичная ремиссия – 25 (38%), стабилизация – 6 (9%) и прогрессия заболевания – 10 (15%). В рамках ауто-ТГСК назначались следующие режимы кондиционирования: BEAM – 24 пациента (36%), BeEAM – 22 (33%), CBV – 13 (20%), другие режимы кондиционирования – 7 (11%).
Результаты
Долгосрочная общая выживаемость (ОВ) всех пациентов составила 48% и выживаемость без прогрессирования – 41%. ОВ в случае химиочувствительного и химиорезистентного течения – 64% и 33%, соответственно (p=0,005). Общая выживаемость при использовании режима кондиционирования BeEAM составила 62%, BEAM– 51%. (p=0,6). Трансплантационная летальность составила 4,5%. Причины летального исхода: инфекционные осложнения – 2 человека, токсические осложнения – 1 (фиброз легких).
Выводы
При использовании ауто-ТГСК удается излечить примерно половину детей и подростков, страдающих рецидивирующим или рефрактерным течением ЛХ. Показанием для ауто-ТГСК у детей, как и у взрослых, является химиочувствительное течение. Режимы кондиционирования BEAM и BeEAM одинаково эффективны.
Ключевые слова
Лимфома Ходжкина, детский возраст, трансплантация гемопоэтических стволовых клеток, аутологичная, уровни выживаемости.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20505
[VALUE] => Array
(
[TEXT] => Andrey V. Kozlov, Ilya V. Kazantsev, Elena V. Morozova, Tatiana V. Iuchta, Polina S. Tolkunova, Asmik G. Gevorgian, Mihail M. Kanunnikov, Kirill V. Lepik, Yuri R. Zalyalov, Elena V. Babenko, Maria A. Estrina, Natalia B. Mikhailova, Ludmila S. Zubarovskaya, Boris V. Afanasyev
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Andrey V. Kozlov, Ilya V. Kazantsev, Elena V. Morozova, Tatiana V. Iuchta, Polina S. Tolkunova, Asmik G. Gevorgian, Mihail M. Kanunnikov, Kirill V. Lepik, Yuri R. Zalyalov, Elena V. Babenko, Maria A. Estrina, Natalia B. Mikhailova, Ludmila S. Zubarovskaya, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20506
[VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20507
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Standard therapy cures 70-90% of patients with Hodgkin’s lymphoma (HL). Autologous hematopoietic stem cell transplantation (auto-HSCT) is an effective treatment option in chemosensitive relapsed or refractory disease. Despite longterm experience the data on the role of auto-HSCT in children are limited.
</p>
<h2 style="text-align: justify;">Materials and methods</h2>
<p style="text-align: justify;">
Between 1993-2017, sixty-six HL patients at the median age of 16 (4-18) received auto-HSCT. Nodular sclerosis was diagnosed in 59 patients (89%), mixed cellularity type, in 6 (9%), lymphocyte depletion form, in 1 (2%). Clinical stage IV was assessed in 29 patients (44%), stage III, in 18 (27%), stage II, in 17 (26%), stage I, in 2 cases (3%); В symptoms were documented in 43 cases (65%). Relapsing course of the disease was revealed in 45 children and teenagers (68%), and refractory disease was confirmed in 21cases (32%). First-line therapy was carried out according to GPOH-HD protocol in 37 patients (56%); BEACOPP was applied in 21 cases (32%); ABVD, in 8 cases (12%). Second-line therapy included IEP/ABVD in GPOH-HD group, and DHAP or ICE in BEACOPP or ABVD groups. Early HL relapses (<12 months) were diagnosed in 26 children and teenagers (58%), and late relapse was stated in 19 patients (42%). Median number of therapy lines prior to auto-HSCT was 2 (1 to 6). Complete remission at the moment of auto-HSCT was achieved in 25 patients (38%), partial remission, in 25 (38%), stabilization, in 6 (9%), and progression of the disease was observed in 10 (15%). The conditioning regimens included BEAM (n=24, 36%), BeEAM (n=22, 33%), CBV (n=13, 20%), others (n=7, 11%).
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Long-term overall survival (OS) was 48%, and progression free survival was 41%. The OS values in cases of chemosensitive disease were 64%, and in chemoresistant disease, 33%, (p=0.005). BeEAM and BEAM conditioning regimens have shown comparable effectiveness (OS, 62% and 51%, respectively, p=0.6). Transplant-related mortality was 4.5%. Lethal complications were associated with infections in 2 patients and high-dose chemotherapy toxicity in 1 patient (lung fibrosis).
</p>
<h2 style="text-align: justify;">Сonclusion</h2>
<p style="text-align: justify;">
Auto-HSCT cures approximately half of children and teenagers with relapsed or refractory HL. Chemosensitivity of the disease is an essential factor for the success of auto-HSCT. BEAM and BeEAM conditioning regimens are equally effective in children.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Hodgkin’s lymphoma, pediatric, hematopoietic stem cell transplantation, autologous, survival rates.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Standard therapy cures 70-90% of patients with Hodgkin’s lymphoma (HL). Autologous hematopoietic stem cell transplantation (auto-HSCT) is an effective treatment option in chemosensitive relapsed or refractory disease. Despite longterm experience the data on the role of auto-HSCT in children are limited.
Materials and methods
Between 1993-2017, sixty-six HL patients at the median age of 16 (4-18) received auto-HSCT. Nodular sclerosis was diagnosed in 59 patients (89%), mixed cellularity type, in 6 (9%), lymphocyte depletion form, in 1 (2%). Clinical stage IV was assessed in 29 patients (44%), stage III, in 18 (27%), stage II, in 17 (26%), stage I, in 2 cases (3%); В symptoms were documented in 43 cases (65%). Relapsing course of the disease was revealed in 45 children and teenagers (68%), and refractory disease was confirmed in 21cases (32%). First-line therapy was carried out according to GPOH-HD protocol in 37 patients (56%); BEACOPP was applied in 21 cases (32%); ABVD, in 8 cases (12%). Second-line therapy included IEP/ABVD in GPOH-HD group, and DHAP or ICE in BEACOPP or ABVD groups. Early HL relapses (<12 months) were diagnosed in 26 children and teenagers (58%), and late relapse was stated in 19 patients (42%). Median number of therapy lines prior to auto-HSCT was 2 (1 to 6). Complete remission at the moment of auto-HSCT was achieved in 25 patients (38%), partial remission, in 25 (38%), stabilization, in 6 (9%), and progression of the disease was observed in 10 (15%). The conditioning regimens included BEAM (n=24, 36%), BeEAM (n=22, 33%), CBV (n=13, 20%), others (n=7, 11%).
Results
Long-term overall survival (OS) was 48%, and progression free survival was 41%. The OS values in cases of chemosensitive disease were 64%, and in chemoresistant disease, 33%, (p=0.005). BeEAM and BEAM conditioning regimens have shown comparable effectiveness (OS, 62% and 51%, respectively, p=0.6). Transplant-related mortality was 4.5%. Lethal complications were associated with infections in 2 patients and high-dose chemotherapy toxicity in 1 patient (lung fibrosis).
Сonclusion
Auto-HSCT cures approximately half of children and teenagers with relapsed or refractory HL. Chemosensitivity of the disease is an essential factor for the success of auto-HSCT. BEAM and BeEAM conditioning regimens are equally effective in children.
Keywords
Hodgkin’s lymphoma, pediatric, hematopoietic stem cell transplantation, autologous, survival rates.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20508
[VALUE] => Autologous hematopoietic stem cell transplantation in children and teenagers with Hodgkin’s lymphoma
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Autologous hematopoietic stem cell transplantation in children and teenagers with Hodgkin’s lymphoma
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20781
[VALUE] => 1419
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1419
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20782
[VALUE] => 1420
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1420
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Андрей В. Козлов, Илья В. Казанцев, Елена В. Морозова, Татьяна В. Юхта, Полина С. Толкунова, Асмик Г. Геворгян, Михаил М. Канунников, Кирилл В. Лепик, Юрий Р. Залялов, Елена В. Бабенко, Мария А. Эстрина, Наталья Б. Михайлова, Людмила С. Зубаровская, Борис В. Афанасьев
Введение
Применение стандартных схем терапии удается излечивает до 70-90% пациентов, страдающих лимфомой Ходжкина (ЛХ). Аутологичная трансплантация гемопоэтических стволовых клеток (ауто-ТГСК) является эффективным способом терапии в случае химиочувствительного рецидива или достижения ремиссии при первично рефрактерном течении ЛХ. Несмотря на уже многолетнее использование, наличие крупных рандомизированных исследований, подтвердивших эффективность данного метода у взрослых, роль ауто-ТГСК у детей с ЛХ изучена в меньшей степени и количество крупных публикаций, посвященных данному вопросу, невелико.
Материалы и методы
В работу включено 66 пациентов с ЛХ в возрасте от 4 до 18 лет (медиана возраста – 16), пролеченных за период 1993-2017 гг. Распределение по гистологическому варианту было следующим: нодулярный склероз – 59 человек (89%), смешанно-клеточный вариант – 6 (9%), лимфоидное истощение – 1 (2%). На момент постановки диагноза у 29 (44%) отмечалась IV стадия ЛХ, 18 (27%) – III стадия, 17 (26%) – II стадия, 2 (3%) – I стадия, В-симптомы – 43 человека (65%), рецидивирующее течение – 45 (68%), рефрактерное течение – 21 (32%). Первая линия терапии проводилась по протоколу GPOH-HD у 37 пациентов (56%), по протоколу BEACOPP – 21 (32%), по протоколу ABVD – 8 (12%). Вторая линия терапия – IEP/ABVD в случае использования протокола GPOHHD и в случае использования других протоколов – DHAP или ICE. Ранний рецидив ЛХ (<12 месяцев) отмечался у 26 человек (58%), поздний рецидив – 19 (42%). Медиана линий терапии перед ауто-ТГСК – 2 (1-6). Полная ремиссия на момент ауто-ТГСК была диагностирована у 25 человек (38%), частичная ремиссия – 25 (38%), стабилизация – 6 (9%) и прогрессия заболевания – 10 (15%). В рамках ауто-ТГСК назначались следующие режимы кондиционирования: BEAM – 24 пациента (36%), BeEAM – 22 (33%), CBV – 13 (20%), другие режимы кондиционирования – 7 (11%).
Результаты
Долгосрочная общая выживаемость (ОВ) всех пациентов составила 48% и выживаемость без прогрессирования – 41%. ОВ в случае химиочувствительного и химиорезистентного течения – 64% и 33%, соответственно (p=0,005). Общая выживаемость при использовании режима кондиционирования BeEAM составила 62%, BEAM– 51%. (p=0,6). Трансплантационная летальность составила 4,5%. Причины летального исхода: инфекционные осложнения – 2 человека, токсические осложнения – 1 (фиброз легких).
Выводы
При использовании ауто-ТГСК удается излечить примерно половину детей и подростков, страдающих рецидивирующим или рефрактерным течением ЛХ. Показанием для ауто-ТГСК у детей, как и у взрослых, является химиочувствительное течение. Режимы кондиционирования BEAM и BeEAM одинаково эффективны.
Ключевые слова
Лимфома Ходжкина, детский возраст, трансплантация гемопоэтических стволовых клеток, аутологичная, уровни выживаемости.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20511
[VALUE] => Array
(
[TEXT] => Евгений В. Коротаев, Сергей В. Андрюнькин, Андрей А. Степанов, Сергей А. Пономарев, Алексей Н. Косарев, Светлана С. Каракальчева
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Евгений В. Коротаев, Сергей В. Андрюнькин, Андрей А. Степанов, Сергей А. Пономарев, Алексей Н. Косарев, Светлана С. Каракальчева
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20512
[VALUE] => Array
(
[TEXT] => АУ «Югорский НИИ клеточных технологий», Ханты-Мансийск, Российская Федерация
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => АУ «Югорский НИИ клеточных технологий», Ханты-Мансийск, Российская Федерация
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20513
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Обеспечение высокой и прогнозируемой сохранности гемопоэтических стволовых клеток (ГСК) после их размораживания и проведения аутологичной трансплантации – одно из ключевых условий для дальнейшего успешного восстановления гемопоэза после высокодозной химиотерапии у пациентов с гемобластозами. Считается, что методика криоконсервирования ГСК давно отработана и приводит к ожидаемым результатам, поэтому обычно учитывается только заготовленная доза ГСК. Однако, при использовании современного и достоверного контроля качества, повсеместно применяемые методы криоконсервации ГСК не всегда могут гарантировать достаточную сохранность данных клеток (Табл. 1). Общеизвестно, что сохранность ГСК при хранении обеспечивает криопротектор, защищающий клетки от осмотического шока при их замораживании. Криопротектор с ДМСО общепринято вводить при помощи шприца в трансплантат ГСК. При этом конечная концентрация ДМСО в 5-10% достигается уже в криопакете с трансплантатом. Однако криопротектор с концентрированным ДМСО (более 50%) при контакте с клеткой, ввиду своих физико-химических свойств, может привести к ее частичной деструкции еще до замораживания. Таким образом, повысить сохранность ГСК можно снизив деструктивное воздействие, которое может быть связано с исходной высокой концентрацией ДМСО в криопротекторе. Для этого нами разработан и апробирован новый способ введения ДМСО в трансплантат ГСК при помощи специального сконструированного аппарата – автоматизированной системы введения ДМСО (на стадии патентования). Принцип действия данной системы исключает продолжительный контакт концентрированного ДМСО с трансплантатом ГСК.
</p>
<h2 style="text-align: justify;">Цель</h2>
<p style="text-align: justify;">
Цель работы состояла в сравнении сохранности ГСК при использовании автоматизированного и ручного способа введения ДМСО.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
Лейкоконцентрат ГСК периферической крови (n=25), полученный путем афереза у пациентов с онкогематологическими заболеваниями. Контрольная группа I – введение ДМСО в криопакет с трансплантатом ГСК выполняли ручным способом. Опытная группа II – введение ДМСО в трансплантат ГСК выполняли новым автоматизированным способом. Использовали стандартный криопротектор (55% DMSO Dex 40), конечная концентрация ДМСО – 7,5%. Замораживание (одновременно группы I и II) проводили на программном замораживателе по валидированной 6-ти ступенчатой программе. Хранение осуществляли в жидком азоте. Размораживание криопакетов проводили на водяной бане при +40 в течение 1 мин. Анализ количества жизнеспособных ГСК и их суммарной колониеобразующей активности (КОЕ) выполнялся до и после введения криопротектора, а также после размораживания. После размораживания для достоверности пробы отбирались из криопакетов. Количество ГСК оценивалось по фенотипу CD34+/CD45dim/7AAD проточной цитометрией по протоколу ISHAGE. Колониеобразующая активность ГСК оценивалась путем их культивирования в течение 14 суток (Methocult H4435) с последующим подсчетом суммарных колоний (КОЕ).
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Согласно представленным в таблице 2 результатам, сохранность ГСК в группах I и II после введения ДМСО не отличается. Идентичные результаты, вероятно, обусловлены одинаковым инкубационным воздействием ДМСО на ГСК, связанным с продолжительностью проведения анализа методом проточной цитометрии. Тем самым моделируется экспозиционное воздействие ДМСО на ГСК. Из этого следует, что при отсутствии немедленного замораживания ГСК после введения ДМСО, повреждающие эффекты связаны с деструктивными физико-химическими свойствами ДМСО по отношению к клеткам, причем не зависимо от способа введения ДМСО.<br>
Общепринято немедленно замораживать трансплантат сразу после введения ДМСО. В этот короткий временной промежуток будут законсервированы только те повреждения клеток, которые проявились сразу после первичного воздействия ДМСО. Поэтому зависимость контроля качества сохранности ГСК после введения криопротектора по методу 2 может быть оценена с большей достоверностью после размораживания. Контроль качества после размораживания отражен на рис. 1. Согласно представленным на рисунке результатам, сохранность ГСК после размораживания достоверно выше на 14% (p≤0.05) при использовании автоматизированной системы в сравнении с ручным способом. При прочих равных условиях исследования, суммарные потери ГСК после размораживания при ручном способе составили в среднем 20%, при автоматизированном – 6%. Они включают потери ГСК при введении ДМСО, а также утрату ГСК в процессе замораживания. Поэтому потери, вызванные замораживанием, можно принять как одинаковые при использовании разных способов введения ДМСО. Следовательно, при ручном способе потери связаны с этапом введения ДМСО. Мы полагаем, что средняя сохранность в 94% обусловлена способом введения ДМСО с использованием автоматизированной системы. Принцип работы автоматизированной системы позволяет снизить одномоментное повреждающее влияние исходного концентрированногораствора ДМСО на ГСК и обеспечить его более плавное разбавление до необходимой конечной концентрации ДМСО в 7,5%. Результаты, представленные в таблице и на рисунке, также показывают, что ДМСО на этапе его введения при экспозиции может оказывать большее негативное воздействие на ГСК, чем процедура замораживания трансплантата.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Сохранность ГСК при использовании автоматизированной системы введения ДМСО достоверно (на 14%) выше в сравнении с ручным способом.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Гемопоэтические стволовые клетки, криоконсервация, димитилсульфоксид, аутологичная трансплантация.<br>
<img width="783" alt="25_таблицы.png" src="/upload/medialibrary/804/25_tablitsy.png" height="369" title="25_таблицы.png"><br>
<br>
<img width="375" alt="25_Рисунок.png" src="/upload/medialibrary/c2f/25_risunok.png" height="219" title="25_Рисунок.png">
</p>
<h2 style="text-align: justify;">Рисунок 1. Выход гемопоэтических клеток после ручного или автоматизированного введения ДМСО и криоконсервирования по различным критериям</h2>
<h2></h2>
<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Обеспечение высокой и прогнозируемой сохранности гемопоэтических стволовых клеток (ГСК) после их размораживания и проведения аутологичной трансплантации – одно из ключевых условий для дальнейшего успешного восстановления гемопоэза после высокодозной химиотерапии у пациентов с гемобластозами. Считается, что методика криоконсервирования ГСК давно отработана и приводит к ожидаемым результатам, поэтому обычно учитывается только заготовленная доза ГСК. Однако, при использовании современного и достоверного контроля качества, повсеместно применяемые методы криоконсервации ГСК не всегда могут гарантировать достаточную сохранность данных клеток (Табл. 1). Общеизвестно, что сохранность ГСК при хранении обеспечивает криопротектор, защищающий клетки от осмотического шока при их замораживании. Криопротектор с ДМСО общепринято вводить при помощи шприца в трансплантат ГСК. При этом конечная концентрация ДМСО в 5-10% достигается уже в криопакете с трансплантатом. Однако криопротектор с концентрированным ДМСО (более 50%) при контакте с клеткой, ввиду своих физико-химических свойств, может привести к ее частичной деструкции еще до замораживания. Таким образом, повысить сохранность ГСК можно снизив деструктивное воздействие, которое может быть связано с исходной высокой концентрацией ДМСО в криопротекторе. Для этого нами разработан и апробирован новый способ введения ДМСО в трансплантат ГСК при помощи специального сконструированного аппарата – автоматизированной системы введения ДМСО (на стадии патентования). Принцип действия данной системы исключает продолжительный контакт концентрированного ДМСО с трансплантатом ГСК.
Цель
Цель работы состояла в сравнении сохранности ГСК при использовании автоматизированного и ручного способа введения ДМСО.
Материалы и методы
Лейкоконцентрат ГСК периферической крови (n=25), полученный путем афереза у пациентов с онкогематологическими заболеваниями. Контрольная группа I – введение ДМСО в криопакет с трансплантатом ГСК выполняли ручным способом. Опытная группа II – введение ДМСО в трансплантат ГСК выполняли новым автоматизированным способом. Использовали стандартный криопротектор (55% DMSO Dex 40), конечная концентрация ДМСО – 7,5%. Замораживание (одновременно группы I и II) проводили на программном замораживателе по валидированной 6-ти ступенчатой программе. Хранение осуществляли в жидком азоте. Размораживание криопакетов проводили на водяной бане при +40 в течение 1 мин. Анализ количества жизнеспособных ГСК и их суммарной колониеобразующей активности (КОЕ) выполнялся до и после введения криопротектора, а также после размораживания. После размораживания для достоверности пробы отбирались из криопакетов. Количество ГСК оценивалось по фенотипу CD34+/CD45dim/7AAD проточной цитометрией по протоколу ISHAGE. Колониеобразующая активность ГСК оценивалась путем их культивирования в течение 14 суток (Methocult H4435) с последующим подсчетом суммарных колоний (КОЕ).
Результаты
Согласно представленным в таблице 2 результатам, сохранность ГСК в группах I и II после введения ДМСО не отличается. Идентичные результаты, вероятно, обусловлены одинаковым инкубационным воздействием ДМСО на ГСК, связанным с продолжительностью проведения анализа методом проточной цитометрии. Тем самым моделируется экспозиционное воздействие ДМСО на ГСК. Из этого следует, что при отсутствии немедленного замораживания ГСК после введения ДМСО, повреждающие эффекты связаны с деструктивными физико-химическими свойствами ДМСО по отношению к клеткам, причем не зависимо от способа введения ДМСО.
Общепринято немедленно замораживать трансплантат сразу после введения ДМСО. В этот короткий временной промежуток будут законсервированы только те повреждения клеток, которые проявились сразу после первичного воздействия ДМСО. Поэтому зависимость контроля качества сохранности ГСК после введения криопротектора по методу 2 может быть оценена с большей достоверностью после размораживания. Контроль качества после размораживания отражен на рис. 1. Согласно представленным на рисунке результатам, сохранность ГСК после размораживания достоверно выше на 14% (p≤0.05) при использовании автоматизированной системы в сравнении с ручным способом. При прочих равных условиях исследования, суммарные потери ГСК после размораживания при ручном способе составили в среднем 20%, при автоматизированном – 6%. Они включают потери ГСК при введении ДМСО, а также утрату ГСК в процессе замораживания. Поэтому потери, вызванные замораживанием, можно принять как одинаковые при использовании разных способов введения ДМСО. Следовательно, при ручном способе потери связаны с этапом введения ДМСО. Мы полагаем, что средняя сохранность в 94% обусловлена способом введения ДМСО с использованием автоматизированной системы. Принцип работы автоматизированной системы позволяет снизить одномоментное повреждающее влияние исходного концентрированногораствора ДМСО на ГСК и обеспечить его более плавное разбавление до необходимой конечной концентрации ДМСО в 7,5%. Результаты, представленные в таблице и на рисунке, также показывают, что ДМСО на этапе его введения при экспозиции может оказывать большее негативное воздействие на ГСК, чем процедура замораживания трансплантата.
Заключение
Сохранность ГСК при использовании автоматизированной системы введения ДМСО достоверно (на 14%) выше в сравнении с ручным способом.
Ключевые слова
Гемопоэтические стволовые клетки, криоконсервация, димитилсульфоксид, аутологичная трансплантация.


Рисунок 1. Выход гемопоэтических клеток после ручного или автоматизированного введения ДМСО и криоконсервирования по различным критериям
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20514
[VALUE] => Array
(
[TEXT] => Evgeniy V. Korotaev, Sergey V. Andrunkin, Andrey A. Stepanov, Sergey S. Ponomarev, Aleksey N. Kosarev, Svetlana S. Karakalcheva
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Evgeniy V. Korotaev, Sergey V. Andrunkin, Andrey A. Stepanov, Sergey S. Ponomarev, Aleksey N. Kosarev, Svetlana S. Karakalcheva
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20515
[VALUE] => Array
(
[TEXT] => Yugra Research Institute of Cellular Technologies with Stem Cell Bank, Khanty-Mansiysk, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Yugra Research Institute of Cellular Technologies with Stem Cell Bank, Khanty-Mansiysk, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20516
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Ensuring high and predictable safety of stored hematopoietic stem cells (HSC) after their thawing and performing autologous transplantation is one of the main conditions for the further successful recovery of hemopoiesis after high-dose chemotherapy in patients with hemoblastosis. It is believed that the method of cryopreservation HSC has long been worked out and leads to the expected results, therefore usually used harvested HSC dose only. However, with the use of modern and reliable quality control, universally applied cryopreservation methods of HSC cannot always warrant sufficient integrity of these cells (Table 1). It is well known that the safety of stored HSC is provided by a cryoprotectant, which prevents the cells from osmotic shock when they are frozen and thawed. A cryoprotectant with dimethyl sulfoxide (DMSO) is generally introduced via a syringe into the HSC suspension. At the same time, the final DMSO concentration in 5-10% is reached already in the cryopacket with the graft. However, a cryoprotectant with concentrated DMSO (more than 50%) upon contact with the cell, in view of its physicochemical properties, can lead to its partial destruction before freezing. Thus, increasing safety for HSC can be reduced by destructive effects, which may be due to the initially high concentration of DMSO in the cryoprotectant. To this end, we developed and tested a new method for introducing DMSO into the HSC transplant using a specially designed apparatus, i.e., an automated DMSO introduction system (patent pending). The principle of operation of this system excludes prolonged contact of concentrated DMSO with HSC transplant.
</p>
<h2 style="text-align: justify;">Aim</h2>
<p style="text-align: justify;">
The aim of our study was to compare the safety of HSCs using an automated and manual method of DMSO introduction.
</p>
<h2 style="text-align: justify;">Materials and methods</h2>
<p style="text-align: justify;">
Peripheral blood stem cell samples (n=25) were obtained by apheresis from the patients with oncohematological diseases. For the control series (group I), DMSO introduction into a cryopacket with HSC graft was performed manually. In experimental series (group II), DMSO was introduced into the HSC transplant by a new automated method. A standard cryoprotectant (55% DMSO Dex 40) was used, the final DMSO concentration was 7.5%. Freezing (at the same time groups I and II) was performed in a software-assisted freezer with a validated 6-step program. Storage was carried out in liquid nitrogen. The cryopackets were thawed in a water bath at +40 for 1 min. Evaluation of viable HSCs numbers and their total colony-forming activity (CFU) was performed before and after the cryoprotection, as well as after thawing. To get more reliable results, the defrosted samples were taken from the cryopackets. The amounts of HSC was estimated by flow cytometric assay (CD34+/CD45dim/7AAD phenotype), according to the ISHAGE protocol. The colony-forming activity of HSC was evaluated by culturing them for 14 days (Methocult H4435) followed by counting total colonies (CFU).<br>
<img width="781" alt="25_Tables.png" src="/upload/medialibrary/3ac/25_tables.png" height="360" title="25_Tables.png">
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Similar viability indexes were revealed when testing the samples from the treatment series I and II. This fact may be due to the same incubation effect of DMSO on HSC, related to the duration of the analysis by flow cytometry. Thus, the exposure effect of DMSO on HSC is modelled. Hence, in absence of immediate freezing of HSC after DMSO introduction, the damaging effects are associated with the destructive physico-chemical effects of DMSO to cells, regardless of the manner of DMSO introduction. It is generally accepted to freeze the transplant immediately after DMSO introduction. During this short time interval, only those cell lesions that are manifested immediately after the initial exposure to DMSO are conserved. Therefore, the dependence of the quality control of HSC safety after introducing the cryoprotectant by the method 2 could be more reliably estimated after defrosting.<br>
<img width="377" alt="25_Figure.png" src="/upload/medialibrary/b22/25_figure.png" height="223" title="25_Figure.png">
</p>
<h2 style="text-align: justify;">Figure 1. Recovery of total HSCs, viable cells and colony- forming units in cryopreserved HSCs treated with DMSO at different regimens</h2>
<p style="text-align: justify;">
According to the results shown in the figure 1, the safety of HSC after defrosting is significantly higher by 14% (p≤0.05) when using the automated system in comparison with manual mode. Given all other equal conditions, the total losses of HSC after defrosting with the manual method averaged 20%, with an automated technique, 6%. At the same time, 6% include both HSC losses when DMSO is introduced, and HSC losses during the freezing procedure. Therefore, the losses caused by freezing can be assumed to be the same when using different methods of introducing DMSO. Therefore, in the manual process, the losses are associated with the step of DMSO introduction. We are thinking that the average preservation rate of 94% is due to the method of introducing DMSO using an automated system. The principle of operation of the automated system allows one to reduce the momentary damaging effect of the initial concentrated DMSO solution on HSC and to ensure its smoother dilution to the required final DMSO concentration of 7.5%. The results presented in the table and in the figure also show that DMSO at the stage of introduction at exposure may have a greater negative impact on HSC than the procedure for freezing the graft.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
The safety of HSC when using an automated system is significantly higher by 14% compared to manual mode.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Hematopoietic stem cells, cryopreservation, dimethyl sulfoxide, autologous transplantation.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
Ensuring high and predictable safety of stored hematopoietic stem cells (HSC) after their thawing and performing autologous transplantation is one of the main conditions for the further successful recovery of hemopoiesis after high-dose chemotherapy in patients with hemoblastosis. It is believed that the method of cryopreservation HSC has long been worked out and leads to the expected results, therefore usually used harvested HSC dose only. However, with the use of modern and reliable quality control, universally applied cryopreservation methods of HSC cannot always warrant sufficient integrity of these cells (Table 1). It is well known that the safety of stored HSC is provided by a cryoprotectant, which prevents the cells from osmotic shock when they are frozen and thawed. A cryoprotectant with dimethyl sulfoxide (DMSO) is generally introduced via a syringe into the HSC suspension. At the same time, the final DMSO concentration in 5-10% is reached already in the cryopacket with the graft. However, a cryoprotectant with concentrated DMSO (more than 50%) upon contact with the cell, in view of its physicochemical properties, can lead to its partial destruction before freezing. Thus, increasing safety for HSC can be reduced by destructive effects, which may be due to the initially high concentration of DMSO in the cryoprotectant. To this end, we developed and tested a new method for introducing DMSO into the HSC transplant using a specially designed apparatus, i.e., an automated DMSO introduction system (patent pending). The principle of operation of this system excludes prolonged contact of concentrated DMSO with HSC transplant.
Aim
The aim of our study was to compare the safety of HSCs using an automated and manual method of DMSO introduction.
Materials and methods
Peripheral blood stem cell samples (n=25) were obtained by apheresis from the patients with oncohematological diseases. For the control series (group I), DMSO introduction into a cryopacket with HSC graft was performed manually. In experimental series (group II), DMSO was introduced into the HSC transplant by a new automated method. A standard cryoprotectant (55% DMSO Dex 40) was used, the final DMSO concentration was 7.5%. Freezing (at the same time groups I and II) was performed in a software-assisted freezer with a validated 6-step program. Storage was carried out in liquid nitrogen. The cryopackets were thawed in a water bath at +40 for 1 min. Evaluation of viable HSCs numbers and their total colony-forming activity (CFU) was performed before and after the cryoprotection, as well as after thawing. To get more reliable results, the defrosted samples were taken from the cryopackets. The amounts of HSC was estimated by flow cytometric assay (CD34+/CD45dim/7AAD phenotype), according to the ISHAGE protocol. The colony-forming activity of HSC was evaluated by culturing them for 14 days (Methocult H4435) followed by counting total colonies (CFU).

Results
Similar viability indexes were revealed when testing the samples from the treatment series I and II. This fact may be due to the same incubation effect of DMSO on HSC, related to the duration of the analysis by flow cytometry. Thus, the exposure effect of DMSO on HSC is modelled. Hence, in absence of immediate freezing of HSC after DMSO introduction, the damaging effects are associated with the destructive physico-chemical effects of DMSO to cells, regardless of the manner of DMSO introduction. It is generally accepted to freeze the transplant immediately after DMSO introduction. During this short time interval, only those cell lesions that are manifested immediately after the initial exposure to DMSO are conserved. Therefore, the dependence of the quality control of HSC safety after introducing the cryoprotectant by the method 2 could be more reliably estimated after defrosting.

Figure 1. Recovery of total HSCs, viable cells and colony- forming units in cryopreserved HSCs treated with DMSO at different regimens
According to the results shown in the figure 1, the safety of HSC after defrosting is significantly higher by 14% (p≤0.05) when using the automated system in comparison with manual mode. Given all other equal conditions, the total losses of HSC after defrosting with the manual method averaged 20%, with an automated technique, 6%. At the same time, 6% include both HSC losses when DMSO is introduced, and HSC losses during the freezing procedure. Therefore, the losses caused by freezing can be assumed to be the same when using different methods of introducing DMSO. Therefore, in the manual process, the losses are associated with the step of DMSO introduction. We are thinking that the average preservation rate of 94% is due to the method of introducing DMSO using an automated system. The principle of operation of the automated system allows one to reduce the momentary damaging effect of the initial concentrated DMSO solution on HSC and to ensure its smoother dilution to the required final DMSO concentration of 7.5%. The results presented in the table and in the figure also show that DMSO at the stage of introduction at exposure may have a greater negative impact on HSC than the procedure for freezing the graft.
Conclusion
The safety of HSC when using an automated system is significantly higher by 14% compared to manual mode.
Keywords
Hematopoietic stem cells, cryopreservation, dimethyl sulfoxide, autologous transplantation.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20517
[VALUE] => A novel method of dimethyl sulfoxide introduction improves preservation of cryopreserved hematopoietic stem cells
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => A novel method of dimethyl sulfoxide introduction improves preservation of cryopreserved hematopoietic stem cells
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20779
[VALUE] => 1417
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1417
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20780
[VALUE] => 1418
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1418
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Евгений В. Коротаев, Сергей В. Андрюнькин, Андрей А. Степанов, Сергей А. Пономарев, Алексей Н. Косарев, Светлана С. Каракальчева
Введение
Обеспечение высокой и прогнозируемой сохранности гемопоэтических стволовых клеток (ГСК) после их размораживания и проведения аутологичной трансплантации – одно из ключевых условий для дальнейшего успешного восстановления гемопоэза после высокодозной химиотерапии у пациентов с гемобластозами. Считается, что методика криоконсервирования ГСК давно отработана и приводит к ожидаемым результатам, поэтому обычно учитывается только заготовленная доза ГСК. Однако, при использовании современного и достоверного контроля качества, повсеместно применяемые методы криоконсервации ГСК не всегда могут гарантировать достаточную сохранность данных клеток (Табл. 1). Общеизвестно, что сохранность ГСК при хранении обеспечивает криопротектор, защищающий клетки от осмотического шока при их замораживании. Криопротектор с ДМСО общепринято вводить при помощи шприца в трансплантат ГСК. При этом конечная концентрация ДМСО в 5-10% достигается уже в криопакете с трансплантатом. Однако криопротектор с концентрированным ДМСО (более 50%) при контакте с клеткой, ввиду своих физико-химических свойств, может привести к ее частичной деструкции еще до замораживания. Таким образом, повысить сохранность ГСК можно снизив деструктивное воздействие, которое может быть связано с исходной высокой концентрацией ДМСО в криопротекторе. Для этого нами разработан и апробирован новый способ введения ДМСО в трансплантат ГСК при помощи специального сконструированного аппарата – автоматизированной системы введения ДМСО (на стадии патентования). Принцип действия данной системы исключает продолжительный контакт концентрированного ДМСО с трансплантатом ГСК.
Цель
Цель работы состояла в сравнении сохранности ГСК при использовании автоматизированного и ручного способа введения ДМСО.
Материалы и методы
Лейкоконцентрат ГСК периферической крови (n=25), полученный путем афереза у пациентов с онкогематологическими заболеваниями. Контрольная группа I – введение ДМСО в криопакет с трансплантатом ГСК выполняли ручным способом. Опытная группа II – введение ДМСО в трансплантат ГСК выполняли новым автоматизированным способом. Использовали стандартный криопротектор (55% DMSO Dex 40), конечная концентрация ДМСО – 7,5%. Замораживание (одновременно группы I и II) проводили на программном замораживателе по валидированной 6-ти ступенчатой программе. Хранение осуществляли в жидком азоте. Размораживание криопакетов проводили на водяной бане при +40 в течение 1 мин. Анализ количества жизнеспособных ГСК и их суммарной колониеобразующей активности (КОЕ) выполнялся до и после введения криопротектора, а также после размораживания. После размораживания для достоверности пробы отбирались из криопакетов. Количество ГСК оценивалось по фенотипу CD34+/CD45dim/7AAD проточной цитометрией по протоколу ISHAGE. Колониеобразующая активность ГСК оценивалась путем их культивирования в течение 14 суток (Methocult H4435) с последующим подсчетом суммарных колоний (КОЕ).
Результаты
Согласно представленным в таблице 2 результатам, сохранность ГСК в группах I и II после введения ДМСО не отличается. Идентичные результаты, вероятно, обусловлены одинаковым инкубационным воздействием ДМСО на ГСК, связанным с продолжительностью проведения анализа методом проточной цитометрии. Тем самым моделируется экспозиционное воздействие ДМСО на ГСК. Из этого следует, что при отсутствии немедленного замораживания ГСК после введения ДМСО, повреждающие эффекты связаны с деструктивными физико-химическими свойствами ДМСО по отношению к клеткам, причем не зависимо от способа введения ДМСО.
Общепринято немедленно замораживать трансплантат сразу после введения ДМСО. В этот короткий временной промежуток будут законсервированы только те повреждения клеток, которые проявились сразу после первичного воздействия ДМСО. Поэтому зависимость контроля качества сохранности ГСК после введения криопротектора по методу 2 может быть оценена с большей достоверностью после размораживания. Контроль качества после размораживания отражен на рис. 1. Согласно представленным на рисунке результатам, сохранность ГСК после размораживания достоверно выше на 14% (p≤0.05) при использовании автоматизированной системы в сравнении с ручным способом. При прочих равных условиях исследования, суммарные потери ГСК после размораживания при ручном способе составили в среднем 20%, при автоматизированном – 6%. Они включают потери ГСК при введении ДМСО, а также утрату ГСК в процессе замораживания. Поэтому потери, вызванные замораживанием, можно принять как одинаковые при использовании разных способов введения ДМСО. Следовательно, при ручном способе потери связаны с этапом введения ДМСО. Мы полагаем, что средняя сохранность в 94% обусловлена способом введения ДМСО с использованием автоматизированной системы. Принцип работы автоматизированной системы позволяет снизить одномоментное повреждающее влияние исходного концентрированногораствора ДМСО на ГСК и обеспечить его более плавное разбавление до необходимой конечной концентрации ДМСО в 7,5%. Результаты, представленные в таблице и на рисунке, также показывают, что ДМСО на этапе его введения при экспозиции может оказывать большее негативное воздействие на ГСК, чем процедура замораживания трансплантата.
Заключение
Сохранность ГСК при использовании автоматизированной системы введения ДМСО достоверно (на 14%) выше в сравнении с ручным способом.
Ключевые слова
Гемопоэтические стволовые клетки, криоконсервация, димитилсульфоксид, аутологичная трансплантация.


Рисунок 1. Выход гемопоэтических клеток после ручного или автоматизированного введения ДМСО и криоконсервирования по различным критериям
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20493
[VALUE] => Array
(
[TEXT] => Мария А. Колесникова, Ирина Н. Нечунаева, Марина О. Попова, Татьяна И. Поспелова
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Мария А. Колесникова, Ирина Н. Нечунаева, Марина О. Попова, Татьяна И. Поспелова
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20494
[VALUE] => Array
(
[TEXT] => Кафедра терапии, гематологии, трансфузиологии ФПК и ППВ, Новосибирский государственный медицинский университет, Новосибирск, Россия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Кафедра терапии, гематологии, трансфузиологии ФПК и ППВ, Новосибирский государственный медицинский университет, Новосибирск, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20495
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Пациенты, инфицированные ВИЧ, относятся к группе высокого риска развития злокачественных опухолей. Увеличение числа больных НХЛ среди ВИЧ-инфицированных составляет 5,6% в год по сравнению с 0,015% в общей популяции [1]. У ВИЧ-инфицированных пациентов, согласно исследованиям, оглашенным на 22-й Международной конференции по СПИДу (AIDS 2018), риск развития лимфомы Ходжкина – в 33 раза выше чем в общей популяции. Антиретровирусная терапия (АРВТ) в значительной степени влияет на риск развития злокачественных опухолей, которые зависят от уровня CD4-лимфоцитов, и позволяет резко повысить эффективность лечения [2]. Применение АРВТ позволяет увеличить уровень CD4 клеток, снизить риск инфекционных осложнений и применять полихимиотерапию в стандартных дозах, тем не менее лимфомы у пациентов с ВИЧ по-прежнему остаются одной из ведущих причин смерти [3]. Целью нашего исследования было определить эпидемиологические характеристики и оценить эффективность терапии у пациентов с лимфомами на фоне ВИЧ-инфекции.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
В ретроспективное исследование включены 12 пациентов, наблюдавшихся на базе ГБУЗ НСО ГКБ №2 «Городской гематологический центр» в период с 2013 по 2017 год (5 лет), с диагнозом лимфома на фоне ВИЧ-инфекции. Средний возраст пациентов 37,4±6,8 лет. Распределение по полу: мужчины – 8 (67%), женщины – 4 (33%). Статистическую обработку результатов проводили c помощью программ статистической обработки данных MSExcel, Statistica 12.0.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
ВИЧ-ассоциированные лимфомы были представлены следующими нозологиями: диффузная В-крупноклеточная лимфома (ДВККЛ) – 7 (58,3%), лимфома Ходжкина – 4 (33,4%), плазмобластная лимфома – 1 (8%). Экстранодальная локализация лимфомы отмечена у 50% больных. У пациентов с ДВККЛ был рассчитан прогностический индекс для ВИЧ-ассоциированных лимфом (ARL-IPI): в группу высокого риска вошел 1 пациент (14,29%), промежуточного риска – 5 больных (71,43%), низкого риска – 1 человек (14,29%). Все больные на момент дебюта злокачественной лимфомы имели ВИЧ-статус в течение 5-10 лет и не получали АРВТ в связи с низкой вирусной нагрузкой: менее 100 копий/мл. На момент первичной диагностики лимфомы вирусная нагрузка возрастала в несколько раз (94-1700000 копий/мл). Коинфекции: гепатит В – 25%, гепатит С – 58,33%. Пациенты с плазмобластной лимфомой и ДВККЛ получили курсы ПХТ по протоколу R-CHOP и R-MPV, пациенты с лимфомой Ходжкина – по протоколу ABVD. Девяти пациентам (75%) проведено лечение в объеме 4-8 курсов ПХТ. Полная ремиссия заболевания достигнута у 6 пациентов (66,7%), частичная ремиссия – у 1 пациента (22,2%), рецидив зафиксирован у 1 больного (11,1%) на фоне самостоятельной отмены АРВТ, прогрессирование – у 1 пациента (11,1%). У всех больных, получивших терапию, неудача лечения коррелирует с длительностью ВИЧ-инфекции (r=0.67, p<0.05). У больных, ответивших на терапию (n=8), была достигнута низкая вирусная нагрузка на фоне АРВТ: менее 100 копий/мл. Трое пациентов (25%) получили лишь 1-2 курса ПХТ в связи с коморбидностью или низкой приверженностью к терапии. Данные пациенты не получали АРВТ по различным причинам и ремиссии не достигли. Общая 2х летняя выживаемость пациентов, которым выполненная программная ПХТ с лимфомами на фоне ВИЧ (n=9) составила: 89%; лимфома Ходжкина – 100%, ДВККЛ – 75%.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
В нозологической структуре ВИЧ-ассоциированных лимфом преобладают ДВККЛ с агрессивным течением заболевания. Неудача лечения лимфомы коррелирует с длительностью ВИЧ-инфекции. Благодаря АРВТ, ПХТ может быть проведена в полном объеме с общей выживаемостью, близкой к общей популяции.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
ВИЧ-инфекция, лимфома, диффузная В-крупноклеточная лимфома, лимфома Ходжкина, химиотерапия, онкогематология.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Пациенты, инфицированные ВИЧ, относятся к группе высокого риска развития злокачественных опухолей. Увеличение числа больных НХЛ среди ВИЧ-инфицированных составляет 5,6% в год по сравнению с 0,015% в общей популяции [1]. У ВИЧ-инфицированных пациентов, согласно исследованиям, оглашенным на 22-й Международной конференции по СПИДу (AIDS 2018), риск развития лимфомы Ходжкина – в 33 раза выше чем в общей популяции. Антиретровирусная терапия (АРВТ) в значительной степени влияет на риск развития злокачественных опухолей, которые зависят от уровня CD4-лимфоцитов, и позволяет резко повысить эффективность лечения [2]. Применение АРВТ позволяет увеличить уровень CD4 клеток, снизить риск инфекционных осложнений и применять полихимиотерапию в стандартных дозах, тем не менее лимфомы у пациентов с ВИЧ по-прежнему остаются одной из ведущих причин смерти [3]. Целью нашего исследования было определить эпидемиологические характеристики и оценить эффективность терапии у пациентов с лимфомами на фоне ВИЧ-инфекции.
Пациенты и методы
В ретроспективное исследование включены 12 пациентов, наблюдавшихся на базе ГБУЗ НСО ГКБ №2 «Городской гематологический центр» в период с 2013 по 2017 год (5 лет), с диагнозом лимфома на фоне ВИЧ-инфекции. Средний возраст пациентов 37,4±6,8 лет. Распределение по полу: мужчины – 8 (67%), женщины – 4 (33%). Статистическую обработку результатов проводили c помощью программ статистической обработки данных MSExcel, Statistica 12.0.
Результаты
ВИЧ-ассоциированные лимфомы были представлены следующими нозологиями: диффузная В-крупноклеточная лимфома (ДВККЛ) – 7 (58,3%), лимфома Ходжкина – 4 (33,4%), плазмобластная лимфома – 1 (8%). Экстранодальная локализация лимфомы отмечена у 50% больных. У пациентов с ДВККЛ был рассчитан прогностический индекс для ВИЧ-ассоциированных лимфом (ARL-IPI): в группу высокого риска вошел 1 пациент (14,29%), промежуточного риска – 5 больных (71,43%), низкого риска – 1 человек (14,29%). Все больные на момент дебюта злокачественной лимфомы имели ВИЧ-статус в течение 5-10 лет и не получали АРВТ в связи с низкой вирусной нагрузкой: менее 100 копий/мл. На момент первичной диагностики лимфомы вирусная нагрузка возрастала в несколько раз (94-1700000 копий/мл). Коинфекции: гепатит В – 25%, гепатит С – 58,33%. Пациенты с плазмобластной лимфомой и ДВККЛ получили курсы ПХТ по протоколу R-CHOP и R-MPV, пациенты с лимфомой Ходжкина – по протоколу ABVD. Девяти пациентам (75%) проведено лечение в объеме 4-8 курсов ПХТ. Полная ремиссия заболевания достигнута у 6 пациентов (66,7%), частичная ремиссия – у 1 пациента (22,2%), рецидив зафиксирован у 1 больного (11,1%) на фоне самостоятельной отмены АРВТ, прогрессирование – у 1 пациента (11,1%). У всех больных, получивших терапию, неудача лечения коррелирует с длительностью ВИЧ-инфекции (r=0.67, p<0.05). У больных, ответивших на терапию (n=8), была достигнута низкая вирусная нагрузка на фоне АРВТ: менее 100 копий/мл. Трое пациентов (25%) получили лишь 1-2 курса ПХТ в связи с коморбидностью или низкой приверженностью к терапии. Данные пациенты не получали АРВТ по различным причинам и ремиссии не достигли. Общая 2х летняя выживаемость пациентов, которым выполненная программная ПХТ с лимфомами на фоне ВИЧ (n=9) составила: 89%; лимфома Ходжкина – 100%, ДВККЛ – 75%.
Заключение
В нозологической структуре ВИЧ-ассоциированных лимфом преобладают ДВККЛ с агрессивным течением заболевания. Неудача лечения лимфомы коррелирует с длительностью ВИЧ-инфекции. Благодаря АРВТ, ПХТ может быть проведена в полном объеме с общей выживаемостью, близкой к общей популяции.
Ключевые слова
ВИЧ-инфекция, лимфома, диффузная В-крупноклеточная лимфома, лимфома Ходжкина, химиотерапия, онкогематология.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20496
[VALUE] => Array
(
[TEXT] => Maria A. Kolesnikova, Irina N. Nechunaeva, Marina O. Popova, Tatiana I. Pospelova
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Maria A. Kolesnikova, Irina N. Nechunaeva, Marina O. Popova, Tatiana I. Pospelova
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20497
[VALUE] => Array
(
[TEXT] => Hematology and Transfusiology Department, Novosibirsk State Medical University, Novosibirsk, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Hematology and Transfusiology Department, Novosibirsk State Medical University, Novosibirsk, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20498
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
HIV-infected patients are at high risk for cancer. The number of patients with NHL among HIV+ individuals is 5.6% per year, compared with 0.015% of the general population [1]. Risk of Hodgkin’s lymphoma in HIV-infected patients is higher in 33 times than the general population, according to studies announced at the 22nd International AIDS Conference (AIDS 2018). Antiretroviral therapy (ART) significantly influences on the risk of cancer which depend on the level of CD4-lymphocytes, and improve the effectiveness of treatment [2]. The ART increase the level of CD4 cells, reduce the risk of infectious complications and allow administering chemotherapy in standard doses, however, HIV-associated lymphomas continue to be one of the leading causes of death [3]. The aim of our study was to determine the epidemiological characteristics and evaluate the effectiveness of treatment of HIV-associated lymphomas.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
A retrospective study included 12 patients who were observed on the basis of the National Clinical Hospital No. 2 City Hematology Center from 2013 to 2017 (5 years), diagnosed with HIV- lymphomas. The average age of the patients was 37.4 ± 6.8 years. Distribution by sex: men, 8 (67%), women, 4 (33%). The statistical analysis was performed using MSExcel, Statistica 12.0 software.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
HIV-associated lymphomas were represented by the following clinical types: diffuse large B-cell lymphoma (DLBCL), 7 (58.3%); Hodgkin’s lymphoma, 4 (33.4%); plasmablastic lymphoma, 1 (8%). Extranodal localization of lymphoma was diagnosed in 50% of patients. A prognostic index for HIV-associated lymphomas (ARL-IPI) was calculated for DLBCL: 1 patient (14.29%) entered high-risk group; 5 patients were at intermediate risk (71.43%); 1 person was at low risk (14.29%). Before the diagnosis of lymphoma, all the patients had HIV-positive status for 5-10 years and did not receive ART because of low viral loads (<100 copies/mL). A several-fold increase of viral load (94 to 1700000 copies/mL) was registered at the time of lymphoma diagnosis. Co-infections were detected: hepatitis B, 25%; C, 58.33% of the cases. Patients with plasmablastic lymphoma and DLBCL were treated with R-CHOP and R-MPV; Hodgkin’s lymphoma, according to ABVD protocol. Nine patients (75%) have received 4-8 courses of chemotherapy. Complete remission of the disease was achieved in 6 patients (66.7%); partial remission, in 1 patient (22.2%); relapse was registered in 1 patient (11.1%) associated with self-withdrawal of ART; progression was documented in one case (11.1%). Treatment failure correlated with duration of HIV infection (r = 0.67, p <0.05). The patients who responded to chemotherapy (n=8) achieved low viral load on the background of ART, i.e., less than 100 copies/ml. Three patients (25%) received only 1-2 courses of chemotherapy due to co-morbidity or low adherence to the therapy. These patients did not receive ART for various reasons and did not achieve remission. The overall 2-years survival of 9 patients with HIV-associated lymphomas who completed programmed chemotherapy was 89%; in Hodgkin’s lymphoma, 100%; in DLBCL – 75%.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Diffuse large B-cell lymphomas with aggressive course were more often diagnosed in HIV-infected patients. The chemotherapy failure correlated with duration of HIV infection before lymphoma diagnosis. Overall survival at 2 years in treated patients was 89%. Due to ART, the entire program of chemotherapy can be fulfilled, and good overall survival rates can be achieved in HIV-associated lymphomas, being<br>
close to general patient cohorts.
</p>
<h2 style="text-align: justify;">References</h2>
<p style="text-align: justify;">
1. MH Bateganya, J. Stanaway, P.E. Brentlingeret et al. MHPredictors of Survival After Diagnosis of Non-Hodgkin Lymphoma in a Resource-Limited Setting: A Retrospective Study on the Impact of HIV Infection and Its Treatment // J. of Acquired Immune Deficiency Syndromes. 2011. 56 (4). P. 312-319.<br>
2. Shiels MS, Pfeiffer RM, Gail MH, et al. Cancer Burden in the HIV-Infected Population in the United States. JNCI Journal of the National Cancer Institute. 2011;103(9):753-762.<br>
3. Binnet F, Lewden C, May T, et al. Malignancy related causes of death in human immunodeficiency virus infected patients in the era of highly active antiretroviral therapy. Cancer. 2004;10:317–324.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
HIV infection, lymphoma, diffuse large B-cell lymphoma, Hodgkin’s lymphoma, chemotherapy, oncohematology.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
HIV-infected patients are at high risk for cancer. The number of patients with NHL among HIV+ individuals is 5.6% per year, compared with 0.015% of the general population [1]. Risk of Hodgkin’s lymphoma in HIV-infected patients is higher in 33 times than the general population, according to studies announced at the 22nd International AIDS Conference (AIDS 2018). Antiretroviral therapy (ART) significantly influences on the risk of cancer which depend on the level of CD4-lymphocytes, and improve the effectiveness of treatment [2]. The ART increase the level of CD4 cells, reduce the risk of infectious complications and allow administering chemotherapy in standard doses, however, HIV-associated lymphomas continue to be one of the leading causes of death [3]. The aim of our study was to determine the epidemiological characteristics and evaluate the effectiveness of treatment of HIV-associated lymphomas.
Patients and methods
A retrospective study included 12 patients who were observed on the basis of the National Clinical Hospital No. 2 City Hematology Center from 2013 to 2017 (5 years), diagnosed with HIV- lymphomas. The average age of the patients was 37.4 ± 6.8 years. Distribution by sex: men, 8 (67%), women, 4 (33%). The statistical analysis was performed using MSExcel, Statistica 12.0 software.
Results
HIV-associated lymphomas were represented by the following clinical types: diffuse large B-cell lymphoma (DLBCL), 7 (58.3%); Hodgkin’s lymphoma, 4 (33.4%); plasmablastic lymphoma, 1 (8%). Extranodal localization of lymphoma was diagnosed in 50% of patients. A prognostic index for HIV-associated lymphomas (ARL-IPI) was calculated for DLBCL: 1 patient (14.29%) entered high-risk group; 5 patients were at intermediate risk (71.43%); 1 person was at low risk (14.29%). Before the diagnosis of lymphoma, all the patients had HIV-positive status for 5-10 years and did not receive ART because of low viral loads (<100 copies/mL). A several-fold increase of viral load (94 to 1700000 copies/mL) was registered at the time of lymphoma diagnosis. Co-infections were detected: hepatitis B, 25%; C, 58.33% of the cases. Patients with plasmablastic lymphoma and DLBCL were treated with R-CHOP and R-MPV; Hodgkin’s lymphoma, according to ABVD protocol. Nine patients (75%) have received 4-8 courses of chemotherapy. Complete remission of the disease was achieved in 6 patients (66.7%); partial remission, in 1 patient (22.2%); relapse was registered in 1 patient (11.1%) associated with self-withdrawal of ART; progression was documented in one case (11.1%). Treatment failure correlated with duration of HIV infection (r = 0.67, p <0.05). The patients who responded to chemotherapy (n=8) achieved low viral load on the background of ART, i.e., less than 100 copies/ml. Three patients (25%) received only 1-2 courses of chemotherapy due to co-morbidity or low adherence to the therapy. These patients did not receive ART for various reasons and did not achieve remission. The overall 2-years survival of 9 patients with HIV-associated lymphomas who completed programmed chemotherapy was 89%; in Hodgkin’s lymphoma, 100%; in DLBCL – 75%.
Conclusion
Diffuse large B-cell lymphomas with aggressive course were more often diagnosed in HIV-infected patients. The chemotherapy failure correlated with duration of HIV infection before lymphoma diagnosis. Overall survival at 2 years in treated patients was 89%. Due to ART, the entire program of chemotherapy can be fulfilled, and good overall survival rates can be achieved in HIV-associated lymphomas, being
close to general patient cohorts.
References
1. MH Bateganya, J. Stanaway, P.E. Brentlingeret et al. MHPredictors of Survival After Diagnosis of Non-Hodgkin Lymphoma in a Resource-Limited Setting: A Retrospective Study on the Impact of HIV Infection and Its Treatment // J. of Acquired Immune Deficiency Syndromes. 2011. 56 (4). P. 312-319.
2. Shiels MS, Pfeiffer RM, Gail MH, et al. Cancer Burden in the HIV-Infected Population in the United States. JNCI Journal of the National Cancer Institute. 2011;103(9):753-762.
3. Binnet F, Lewden C, May T, et al. Malignancy related causes of death in human immunodeficiency virus infected patients in the era of highly active antiretroviral therapy. Cancer. 2004;10:317–324.
Keywords
HIV infection, lymphoma, diffuse large B-cell lymphoma, Hodgkin’s lymphoma, chemotherapy, oncohematology.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20499
[VALUE] => Epidemiological features and efficacy of treatment in HIV-associated lymphomas
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Epidemiological features and efficacy of treatment in HIV-associated lymphomas
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20775
[VALUE] => 1413
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1413
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20776
[VALUE] => 1414
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1414
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Мария А. Колесникова, Ирина Н. Нечунаева, Марина О. Попова, Татьяна И. Поспелова
Введение
Пациенты, инфицированные ВИЧ, относятся к группе высокого риска развития злокачественных опухолей. Увеличение числа больных НХЛ среди ВИЧ-инфицированных составляет 5,6% в год по сравнению с 0,015% в общей популяции [1]. У ВИЧ-инфицированных пациентов, согласно исследованиям, оглашенным на 22-й Международной конференции по СПИДу (AIDS 2018), риск развития лимфомы Ходжкина – в 33 раза выше чем в общей популяции. Антиретровирусная терапия (АРВТ) в значительной степени влияет на риск развития злокачественных опухолей, которые зависят от уровня CD4-лимфоцитов, и позволяет резко повысить эффективность лечения [2]. Применение АРВТ позволяет увеличить уровень CD4 клеток, снизить риск инфекционных осложнений и применять полихимиотерапию в стандартных дозах, тем не менее лимфомы у пациентов с ВИЧ по-прежнему остаются одной из ведущих причин смерти [3]. Целью нашего исследования было определить эпидемиологические характеристики и оценить эффективность терапии у пациентов с лимфомами на фоне ВИЧ-инфекции.
Пациенты и методы
В ретроспективное исследование включены 12 пациентов, наблюдавшихся на базе ГБУЗ НСО ГКБ №2 «Городской гематологический центр» в период с 2013 по 2017 год (5 лет), с диагнозом лимфома на фоне ВИЧ-инфекции. Средний возраст пациентов 37,4±6,8 лет. Распределение по полу: мужчины – 8 (67%), женщины – 4 (33%). Статистическую обработку результатов проводили c помощью программ статистической обработки данных MSExcel, Statistica 12.0.
Результаты
ВИЧ-ассоциированные лимфомы были представлены следующими нозологиями: диффузная В-крупноклеточная лимфома (ДВККЛ) – 7 (58,3%), лимфома Ходжкина – 4 (33,4%), плазмобластная лимфома – 1 (8%). Экстранодальная локализация лимфомы отмечена у 50% больных. У пациентов с ДВККЛ был рассчитан прогностический индекс для ВИЧ-ассоциированных лимфом (ARL-IPI): в группу высокого риска вошел 1 пациент (14,29%), промежуточного риска – 5 больных (71,43%), низкого риска – 1 человек (14,29%). Все больные на момент дебюта злокачественной лимфомы имели ВИЧ-статус в течение 5-10 лет и не получали АРВТ в связи с низкой вирусной нагрузкой: менее 100 копий/мл. На момент первичной диагностики лимфомы вирусная нагрузка возрастала в несколько раз (94-1700000 копий/мл). Коинфекции: гепатит В – 25%, гепатит С – 58,33%. Пациенты с плазмобластной лимфомой и ДВККЛ получили курсы ПХТ по протоколу R-CHOP и R-MPV, пациенты с лимфомой Ходжкина – по протоколу ABVD. Девяти пациентам (75%) проведено лечение в объеме 4-8 курсов ПХТ. Полная ремиссия заболевания достигнута у 6 пациентов (66,7%), частичная ремиссия – у 1 пациента (22,2%), рецидив зафиксирован у 1 больного (11,1%) на фоне самостоятельной отмены АРВТ, прогрессирование – у 1 пациента (11,1%). У всех больных, получивших терапию, неудача лечения коррелирует с длительностью ВИЧ-инфекции (r=0.67, p<0.05). У больных, ответивших на терапию (n=8), была достигнута низкая вирусная нагрузка на фоне АРВТ: менее 100 копий/мл. Трое пациентов (25%) получили лишь 1-2 курса ПХТ в связи с коморбидностью или низкой приверженностью к терапии. Данные пациенты не получали АРВТ по различным причинам и ремиссии не достигли. Общая 2х летняя выживаемость пациентов, которым выполненная программная ПХТ с лимфомами на фоне ВИЧ (n=9) составила: 89%; лимфома Ходжкина – 100%, ДВККЛ – 75%.
Заключение
В нозологической структуре ВИЧ-ассоциированных лимфом преобладают ДВККЛ с агрессивным течением заболевания. Неудача лечения лимфомы коррелирует с длительностью ВИЧ-инфекции. Благодаря АРВТ, ПХТ может быть проведена в полном объеме с общей выживаемостью, близкой к общей популяции.
Ключевые слова
ВИЧ-инфекция, лимфома, диффузная В-крупноклеточная лимфома, лимфома Ходжкина, химиотерапия, онкогематология.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20484
[VALUE] => Array
(
[TEXT] => Анна А. Колобова, Марина Н. Браеску, Алиса Г. Волкова, Елена И. Дарская, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Анна А. Колобова, Марина Н. Браеску, Алиса Г. Волкова, Елена И. Дарская, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20485
[VALUE] => Array
(
[TEXT] => НИИ детской гематологии и трансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, СПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской гематологии и трансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, СПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20486
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения для пациентов с онкогематологическими заболеваниями, например, с о. лейкозом. Однако, пациенты страдают от многочисленных побочных эффектов, связанных с этим видом лечения. Также высока смертность среди этих больных. В последнее время изучается влияние физических упражнений для этой группы пациентов. Целью нашего исследования было оценить безопасность физических нагрузок после ТКМ в период панцитопении.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
Мы обследовали 11 пациентов за 3 месяца в период ТКМ в возрасте от 20 до 56 лет с различными онкогематологическими заболеваниями, из них 8 пациентов (66%) с диагнозом – о. лейкоз. У 6 пациентов был немиелоаблативный режим кондиционирования, у 5 – миелоаблативный. Для всех пациентов это была первая трансплантация. Источником трансплантата у 2 пациентов был костный мозг, у 9 – периферические стволовые клетки. Для определения физической выносливости мы использовали 6-ти минутный тест, для определения мышечной силы – динамометрию, которые проводили до трансплантации и после приживления трансплантата. 11 пациентов получали различные виды физических нагрузок до восстановления гемопоэза, даже в период глубокой цитопении. У 2 пациентов была аэробная физическая нагрузка (велотренажер) от 5 до 15 минут в зависимости от состояния и показателей клинического анализа крови. 9 пациентов выполняли комплексы упражнений в исходном положении сидя или лежа в зависимости от самочувствия и показателей крови.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Все пациенты прошли курс физической терапии. Ни один пациент не имел осложнений после проведенных занятий. Приживление трансплантата зафиксировано у всех пациентов в нормальные сроки (от Д+17 до Д+31). Только 2 пациентам (16%) требовалось применение КСФ. 6-минутный тест, проведенный после приживления трансплантата, показал различные результаты: у 6 пациентов наблюдались лучшие результаты этого теста – увеличение пройденного расстояния. Только у 3 пациентов увеличилась мышечная сила по результатам динамометрии. Все пациенты отмечали улучшение настроения после физической активности.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Пилотное исследование показало, что физическая нагрузка безопасна весь период цитопении после трансплантации. Для оценки влияние на исходы трансплантации необходимо проведение дальнейших исследований с группой контроля.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Аллогенная трансплантация гемопоэтических стволовых клеток, цитопения, 6-минутная ходьба, динамометрия, физические упражнения.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения для пациентов с онкогематологическими заболеваниями, например, с о. лейкозом. Однако, пациенты страдают от многочисленных побочных эффектов, связанных с этим видом лечения. Также высока смертность среди этих больных. В последнее время изучается влияние физических упражнений для этой группы пациентов. Целью нашего исследования было оценить безопасность физических нагрузок после ТКМ в период панцитопении.
Материалы и методы
Мы обследовали 11 пациентов за 3 месяца в период ТКМ в возрасте от 20 до 56 лет с различными онкогематологическими заболеваниями, из них 8 пациентов (66%) с диагнозом – о. лейкоз. У 6 пациентов был немиелоаблативный режим кондиционирования, у 5 – миелоаблативный. Для всех пациентов это была первая трансплантация. Источником трансплантата у 2 пациентов был костный мозг, у 9 – периферические стволовые клетки. Для определения физической выносливости мы использовали 6-ти минутный тест, для определения мышечной силы – динамометрию, которые проводили до трансплантации и после приживления трансплантата. 11 пациентов получали различные виды физических нагрузок до восстановления гемопоэза, даже в период глубокой цитопении. У 2 пациентов была аэробная физическая нагрузка (велотренажер) от 5 до 15 минут в зависимости от состояния и показателей клинического анализа крови. 9 пациентов выполняли комплексы упражнений в исходном положении сидя или лежа в зависимости от самочувствия и показателей крови.
Результаты
Все пациенты прошли курс физической терапии. Ни один пациент не имел осложнений после проведенных занятий. Приживление трансплантата зафиксировано у всех пациентов в нормальные сроки (от Д+17 до Д+31). Только 2 пациентам (16%) требовалось применение КСФ. 6-минутный тест, проведенный после приживления трансплантата, показал различные результаты: у 6 пациентов наблюдались лучшие результаты этого теста – увеличение пройденного расстояния. Только у 3 пациентов увеличилась мышечная сила по результатам динамометрии. Все пациенты отмечали улучшение настроения после физической активности.
Заключение
Пилотное исследование показало, что физическая нагрузка безопасна весь период цитопении после трансплантации. Для оценки влияние на исходы трансплантации необходимо проведение дальнейших исследований с группой контроля.
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, цитопения, 6-минутная ходьба, динамометрия, физические упражнения.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20487
[VALUE] => Array
(
[TEXT] => Anna A. Kolobova, Marina N. Braesku, Alisa G. Volkova, Elena I. Darskaya, Boris V. Afanasyev
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Anna A. Kolobova, Marina N. Braesku, Alisa G. Volkova, Elena I. Darskaya, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20488
[VALUE] => Array
(
[TEXT] => R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantation, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantation, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20489
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Allogeneic stem cell transplantation (allo-HCT) is an effective curative treatment for patients with haematological malignancies in high-risk diseases e.g. acute leukaemia. However, patients suffer from numerous treatment related side-effects and complications, and the transplant-related mortality is high. Exercise is a promising intervention approach for this group of patients. Over the last years, several clinical trials have contributed to the growing body of evidence showing the beneficial effects of exercise in cancer patients. The purpose of our study was to evaluate the effect of various types of physical activity on the recovery of hemopoiesis after BMT.
</p>
<h2 style="text-align: justify;">Materials and methods</h2>
<p style="text-align: justify;">
We examined 11 patients for 3 months in the period of BMT (20-56 years) with haematological diseases undergoing allogeneic stem cell transplantion, of these, 8 patients (66%) were diagnosed with acute leukemia. 6 patients had a non-myeloablative conditioning regimen, and 5 had a myeloablative regimen. Criteria for patients included in this sample were: no symptoms of coronary illness or uncontrolled high blood pressure, being over 18 years of age. For all patients, this was the first transplantation. The source of the transplant in 2 patients is BM, in 9 patients the PBSC. We determined physical endurance with a 6-minute walk test, and muscular strength with a dynamometer. These tests were performed before transplantation and immediately after the signs of transplant engraftment. All 11 patients received various physical loads throughout the time until the recovery of hemopoiesis, even in the period of deep cytopenia. Two patients had an aerobic exercise (an exercise bike), from 5 to 15 minutes, depending on the state of health and the results of blood tests. 9 patients performed physical exercises in the initial sitting or lying position, depending on the state of health and the results of blood tests.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
All patients underwent a course of physical therapy. No patient quit training. Engraftment of the graft was recorded in all patients during normal periods (from D + 17 to D + 31). Only 2 patients (16%) required the use of CSF. A 6-minute test, performed after engraftment of the transplant, showed different results: in 6 patients the results of this test were observed – an increase in the distance traveled. Only in 3 patients muscular strength increased by the results of dynamometry.<br>
All patients reported improvement in mood after physical activity.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Physical exercise is feasible in patients with pancytopenia after allo-HCT. Further controlled studies are required to evaluate if physical activity improves the outcomes of transplantation.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Allogeneic stem cell transplantation, cytopenia, 6-minute walk test, dynamometry, physical exercise.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Allogeneic stem cell transplantation (allo-HCT) is an effective curative treatment for patients with haematological malignancies in high-risk diseases e.g. acute leukaemia. However, patients suffer from numerous treatment related side-effects and complications, and the transplant-related mortality is high. Exercise is a promising intervention approach for this group of patients. Over the last years, several clinical trials have contributed to the growing body of evidence showing the beneficial effects of exercise in cancer patients. The purpose of our study was to evaluate the effect of various types of physical activity on the recovery of hemopoiesis after BMT.
Materials and methods
We examined 11 patients for 3 months in the period of BMT (20-56 years) with haematological diseases undergoing allogeneic stem cell transplantion, of these, 8 patients (66%) were diagnosed with acute leukemia. 6 patients had a non-myeloablative conditioning regimen, and 5 had a myeloablative regimen. Criteria for patients included in this sample were: no symptoms of coronary illness or uncontrolled high blood pressure, being over 18 years of age. For all patients, this was the first transplantation. The source of the transplant in 2 patients is BM, in 9 patients the PBSC. We determined physical endurance with a 6-minute walk test, and muscular strength with a dynamometer. These tests were performed before transplantation and immediately after the signs of transplant engraftment. All 11 patients received various physical loads throughout the time until the recovery of hemopoiesis, even in the period of deep cytopenia. Two patients had an aerobic exercise (an exercise bike), from 5 to 15 minutes, depending on the state of health and the results of blood tests. 9 patients performed physical exercises in the initial sitting or lying position, depending on the state of health and the results of blood tests.
Results
All patients underwent a course of physical therapy. No patient quit training. Engraftment of the graft was recorded in all patients during normal periods (from D + 17 to D + 31). Only 2 patients (16%) required the use of CSF. A 6-minute test, performed after engraftment of the transplant, showed different results: in 6 patients the results of this test were observed – an increase in the distance traveled. Only in 3 patients muscular strength increased by the results of dynamometry.
All patients reported improvement in mood after physical activity.
Conclusion
Physical exercise is feasible in patients with pancytopenia after allo-HCT. Further controlled studies are required to evaluate if physical activity improves the outcomes of transplantation.
Keywords
Allogeneic stem cell transplantation, cytopenia, 6-minute walk test, dynamometry, physical exercise.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20490
[VALUE] => Effects of various physical activities of patients upon the outcomes of hematopoietic stem cell transplantation
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Effects of various physical activities of patients upon the outcomes of hematopoietic stem cell transplantation
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20777
[VALUE] => 1415
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1415
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20778
[VALUE] => 1416
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1416
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Анна А. Колобова, Марина Н. Браеску, Алиса Г. Волкова, Елена И. Дарская, Борис В. Афанасьев
Введение
Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения для пациентов с онкогематологическими заболеваниями, например, с о. лейкозом. Однако, пациенты страдают от многочисленных побочных эффектов, связанных с этим видом лечения. Также высока смертность среди этих больных. В последнее время изучается влияние физических упражнений для этой группы пациентов. Целью нашего исследования было оценить безопасность физических нагрузок после ТКМ в период панцитопении.
Материалы и методы
Мы обследовали 11 пациентов за 3 месяца в период ТКМ в возрасте от 20 до 56 лет с различными онкогематологическими заболеваниями, из них 8 пациентов (66%) с диагнозом – о. лейкоз. У 6 пациентов был немиелоаблативный режим кондиционирования, у 5 – миелоаблативный. Для всех пациентов это была первая трансплантация. Источником трансплантата у 2 пациентов был костный мозг, у 9 – периферические стволовые клетки. Для определения физической выносливости мы использовали 6-ти минутный тест, для определения мышечной силы – динамометрию, которые проводили до трансплантации и после приживления трансплантата. 11 пациентов получали различные виды физических нагрузок до восстановления гемопоэза, даже в период глубокой цитопении. У 2 пациентов была аэробная физическая нагрузка (велотренажер) от 5 до 15 минут в зависимости от состояния и показателей клинического анализа крови. 9 пациентов выполняли комплексы упражнений в исходном положении сидя или лежа в зависимости от самочувствия и показателей крови.
Результаты
Все пациенты прошли курс физической терапии. Ни один пациент не имел осложнений после проведенных занятий. Приживление трансплантата зафиксировано у всех пациентов в нормальные сроки (от Д+17 до Д+31). Только 2 пациентам (16%) требовалось применение КСФ. 6-минутный тест, проведенный после приживления трансплантата, показал различные результаты: у 6 пациентов наблюдались лучшие результаты этого теста – увеличение пройденного расстояния. Только у 3 пациентов увеличилась мышечная сила по результатам динамометрии. Все пациенты отмечали улучшение настроения после физической активности.
Заключение
Пилотное исследование показало, что физическая нагрузка безопасна весь период цитопении после трансплантации. Для оценки влияние на исходы трансплантации необходимо проведение дальнейших исследований с группой контроля.
Ключевые слова
Аллогенная трансплантация гемопоэтических стволовых клеток, цитопения, 6-минутная ходьба, динамометрия, физические упражнения.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20475
[VALUE] => Array
(
[TEXT] => Диана Д. Иванова, Владислав О. Саржевский, Владимир Я. Мельниченко, Никита Е. Мочкин, Юлия Н. Дубинина, Елена Г. Смирнова, Дина С. Колесникова, Анна Е. Банникова
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Диана Д. Иванова, Владислав О. Саржевский, Владимир Я. Мельниченко, Никита Е. Мочкин, Юлия Н. Дубинина, Елена Г. Смирнова, Дина С. Колесникова, Анна Е. Банникова
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20476
[VALUE] => Array
(
[TEXT] => ФГБУ «Национальный медико-хирургический центр им. Н. И. Пирогова» Минздрава России, Москва
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => ФГБУ «Национальный медико-хирургический центр им. Н. И. Пирогова» Минздрава России, Москва
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20477
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Проведение высокодозной химиотерапии (ВДХТ) с аутологичной трансплантацией периферических гемопоэтических стволовых клеток (ауто-ТГСК) осложняется развитием гематологической токсичности IV степени. Среди осложнений при проведении данного лечения наиболее частым являются инфекционные. Длительность нейтропении IV степени коррелирует с развитием тяжелых инфекционных осложнений, которые могут стать причиной летального исхода в раннем посттрансплантационном периоде. Применение колониестимулирующих факторов (КСФ) снижает длительность нейтропении и риск развития инфекционных осложнений, а также сокращает пребывание пациента в специализированном отделении стационара. Цель исследования оценить и сравнить эффективность и безопасность двух форм КСФ, филграстима и его пегилированной формы, для стимуляции лейкопоэза при проведении ВДХТ с последующей ауто-ТГСК у пациентов с лимфопролиферативными заболеваниями, а также определить наиболее предпочтительную с точки зрения фармакоэкономического анализа форму КСФ.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
В исследование включено 100 больных: 39 – c лимфомой Ходжкина, 18 – с неходжкинскими лимфомами, 42 – с множественной миеломой, 1 – острый промиелоцитарный лейкоз; 51 – женщина, 49 – мужчин. Медиана возраста составила 43 года (18-72) (табл. 1). Кондиционирование проводилось по схемам алкеран 200 мг/м. кв., алкеран 140 мг/м.кв., BeEAC, CBV, BEAM, цитарабин+мелфалан. Пациенты были рандомизированы на группы: 1 группа – пациенты, получающие пегилированную форму КСФ (ПЕГ-КСФ) (n=52), 2 группа – пациенты, получающие непегилированную форму КСФ (n=48). Стимуляцию лейкопоэза начинали на Д+4. Г-КСФ вводили ежедневно в дозе 5 мкг /кг/день до выхода из агранулоцитоза (WBC=3,0х10 в 9 ст./л ). ПЕГ-КСФ вводили однократно в дозе 6 мг (на Д+4). Фармакоэкономический анализ включал сопоставление относительной экономической оценки ПЕГ-КСФ и непегилированной формы КСФ. Учитывались затраты на ПЕГ-КСФ или КСФ, которые вводились соответствующему пациенту в период после выполнения ауто-ТГСК.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Сравнительный клинический анализ использования КСФ и ПЕГ-КСФ проводился по следующим параметрам: возраст, число линий предтрансплантационной химиотерапии, количество трансплантированных CD34+ млн/кг, показатели восстановления гемопоэза, наличие инфекционных осложнений (нейтропеническая лихорадка), длительность госпитализации (табл. 2). Значимые отличия были получены по скорости восстановления уровня лейкоцитов (у пациентов из группы ПЕГ-КСФ выход из агранулоцитоза регистрировался значимо раньше). Но в группе КСФ угнетение эритроидного ростка было значимо меньше. Достоверных отличий по другим анализируемым параметрам получено не было.<br>
Фармакоэкономический анализ показал, что медиана суммы денежных средств, использованных для приобретения ПЕГ-КСФ, вводимых для лечения одного больного, составила 49042,73 руб., а для КСФ 36180,63 руб. (p<0,05) (табл. 3).
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
При клиническом анализе применения пегилированной и непегилированной форм колониестимулирующих факторов существенных отличий не выявлено. Фармакоэкономический анализ выявил преимущество непегилированной формы КСФ над ПЕГ-КСФ.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Трансплантация гемопоэтических стволовых клеток, аутологичная, колониестимулирующий фактор, пегилированный, эффективность, фармакоэкономика.
</p>
<h2>Таблица 1. Общая клиническая характеристика больных</h2>
<table border="1" cellpadding="1" cellspacing="1">
<tbody>
<tr>
<td>
Число больных в группе
</td>
<td>
100
</td>
</tr>
<tr>
<td>
Возраст, медиана (интервал), лет
</td>
<td>
43 (18-72)
</td>
</tr>
<tr>
<td>
Мужчины, абс. (%)
</td>
<td>
49 (49)
</td>
</tr>
<tr>
<td>
Женщины, абс. (%)
</td>
<td>
51 (51)
</td>
</tr>
<tr>
<td>
Неходжкинские лимфомы, абс. (%)
</td>
<td>
18 (18)
</td>
</tr>
<tr>
<td>
Лимфома Ходжкина, абс. (%)
</td>
<td>
39 (39)
</td>
</tr>
<tr>
<td>
Множественная миелома, абс. (%)
</td>
<td>
42 (42)
</td>
</tr>
<tr>
<td>
Острый промиелоцитарный лейкоз, абс. (%) 1
</td>
<td>
1 (1)
</td>
</tr>
</tbody>
</table>
<h2>Таблица 2. Сравнительный анализ ПЕГ-КСФ и КСФ</h2>
<table>
<tbody>
<tr>
<td>
</td>
<td>
Группа КСФ
</td>
<td>
Группа ПЕГ-КСФ
</td>
<td>
t-знач.
</td>
<td>
p
</td>
</tr>
<tr>
<td>
Возраст, годы (медиана)
</td>
<td>
43
</td>
<td>
41,5
</td>
<td>
0,12
</td>
<td>
0,9
</td>
</tr>
<tr>
<td>
Количество трансплантированных CD34+ млн/кг, медиана
</td>
<td>
2,59
</td>
<td>
2,65
</td>
<td>
0,13
</td>
<td>
0,86
</td>
</tr>
<tr>
<td>
Дни агранулоцитоза (медиана)
</td>
<td>
7
</td>
<td>
8
</td>
<td>
-0,93
</td>
<td>
0,35
</td>
</tr>
<tr>
<td>
День (после ТГСК) выхода из агранулоцитоза (медиана)
</td>
<td>
11
</td>
<td>
10
</td>
<td>
2,17
</td>
<td>
0,03
</td>
</tr>
<tr>
<td>
День (после ТГСК) возникновения фебрильной нейтропении
</td>
<td>
4<br>
</td>
<td>
5
</td>
<td>
-1,18
</td>
<td>
0,23
</td>
</tr>
<tr>
<td>
Пациенты с нейтропенической лихорадкой, абс. (%)
</td>
<td>
34 (34%)
</td>
<td>
40 (40%)
</td>
<td>
0,63
</td>
<td>
0,52
</td>
</tr>
<tr>
<td>
Дни тромбоцитопении ниже 20х10^9/л (медиана)
</td>
<td>
4
</td>
<td>
5
</td>
<td>
-1,42
</td>
<td>
0,15
</td>
</tr>
<tr>
<td>
Уровень максимального снижения гемоглобина
</td>
<td>
95
</td>
<td>
86
</td>
<td>
3,34
</td>
<td>
0,001
</td>
</tr>
<tr>
<td>
Число линий предтрансплантационной химиотерапии
</td>
<td>
2
</td>
<td>
2
</td>
<td>
-1,3
</td>
<td>
0,19
</td>
</tr>
<tr>
<td>
Длительность госпитализации
</td>
<td>
22
</td>
<td>
22
</td>
<td>
-0,46
</td>
<td>
0,64
</td>
</tr>
</tbody>
</table>
<h2>Таблица 3. Результаты анализа затрат на профилактику и лечение фебрильной нейтропении на 1 человека после ауто-ТГСК</h2>
<table border="1" cellpadding="1" cellspacing="1">
<tbody>
<tr>
<td>
ПЕГ-КСФ для лечения 1 пациента, руб.
</td>
<td>
КСФ для лечения 1 пациента, руб.
</td>
<td>
р
</td>
</tr>
<tr>
<td>
49042,73
</td>
<td>
36180,63
</td>
<td>
<0,05
</td>
</tr>
</tbody>
</table>
<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Проведение высокодозной химиотерапии (ВДХТ) с аутологичной трансплантацией периферических гемопоэтических стволовых клеток (ауто-ТГСК) осложняется развитием гематологической токсичности IV степени. Среди осложнений при проведении данного лечения наиболее частым являются инфекционные. Длительность нейтропении IV степени коррелирует с развитием тяжелых инфекционных осложнений, которые могут стать причиной летального исхода в раннем посттрансплантационном периоде. Применение колониестимулирующих факторов (КСФ) снижает длительность нейтропении и риск развития инфекционных осложнений, а также сокращает пребывание пациента в специализированном отделении стационара. Цель исследования оценить и сравнить эффективность и безопасность двух форм КСФ, филграстима и его пегилированной формы, для стимуляции лейкопоэза при проведении ВДХТ с последующей ауто-ТГСК у пациентов с лимфопролиферативными заболеваниями, а также определить наиболее предпочтительную с точки зрения фармакоэкономического анализа форму КСФ.
Материалы и методы
В исследование включено 100 больных: 39 – c лимфомой Ходжкина, 18 – с неходжкинскими лимфомами, 42 – с множественной миеломой, 1 – острый промиелоцитарный лейкоз; 51 – женщина, 49 – мужчин. Медиана возраста составила 43 года (18-72) (табл. 1). Кондиционирование проводилось по схемам алкеран 200 мг/м. кв., алкеран 140 мг/м.кв., BeEAC, CBV, BEAM, цитарабин+мелфалан. Пациенты были рандомизированы на группы: 1 группа – пациенты, получающие пегилированную форму КСФ (ПЕГ-КСФ) (n=52), 2 группа – пациенты, получающие непегилированную форму КСФ (n=48). Стимуляцию лейкопоэза начинали на Д+4. Г-КСФ вводили ежедневно в дозе 5 мкг /кг/день до выхода из агранулоцитоза (WBC=3,0х10 в 9 ст./л ). ПЕГ-КСФ вводили однократно в дозе 6 мг (на Д+4). Фармакоэкономический анализ включал сопоставление относительной экономической оценки ПЕГ-КСФ и непегилированной формы КСФ. Учитывались затраты на ПЕГ-КСФ или КСФ, которые вводились соответствующему пациенту в период после выполнения ауто-ТГСК.
Результаты
Сравнительный клинический анализ использования КСФ и ПЕГ-КСФ проводился по следующим параметрам: возраст, число линий предтрансплантационной химиотерапии, количество трансплантированных CD34+ млн/кг, показатели восстановления гемопоэза, наличие инфекционных осложнений (нейтропеническая лихорадка), длительность госпитализации (табл. 2). Значимые отличия были получены по скорости восстановления уровня лейкоцитов (у пациентов из группы ПЕГ-КСФ выход из агранулоцитоза регистрировался значимо раньше). Но в группе КСФ угнетение эритроидного ростка было значимо меньше. Достоверных отличий по другим анализируемым параметрам получено не было.
Фармакоэкономический анализ показал, что медиана суммы денежных средств, использованных для приобретения ПЕГ-КСФ, вводимых для лечения одного больного, составила 49042,73 руб., а для КСФ 36180,63 руб. (p<0,05) (табл. 3).
Выводы
При клиническом анализе применения пегилированной и непегилированной форм колониестимулирующих факторов существенных отличий не выявлено. Фармакоэкономический анализ выявил преимущество непегилированной формы КСФ над ПЕГ-КСФ.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, аутологичная, колониестимулирующий фактор, пегилированный, эффективность, фармакоэкономика.
Таблица 1. Общая клиническая характеристика больных
| Число больных в группе | 100 |
| Возраст, медиана (интервал), лет | 43 (18-72) |
| Мужчины, абс. (%) | 49 (49) |
| Женщины, абс. (%) | 51 (51) |
| Неходжкинские лимфомы, абс. (%) | 18 (18) |
| Лимфома Ходжкина, абс. (%) | 39 (39) |
| Множественная миелома, абс. (%) | 42 (42) |
| Острый промиелоцитарный лейкоз, абс. (%) 1 | 1 (1) |
Таблица 2. Сравнительный анализ ПЕГ-КСФ и КСФ
| Группа КСФ | Группа ПЕГ-КСФ | t-знач. | p | |
| Возраст, годы (медиана) | 43 | 41,5 | 0,12 | 0,9 |
| Количество трансплантированных CD34+ млн/кг, медиана | 2,59 | 2,65 | 0,13 | 0,86 |
| Дни агранулоцитоза (медиана) | 7 | 8 | -0,93 | 0,35 |
| День (после ТГСК) выхода из агранулоцитоза (медиана) | 11 | 10 | 2,17 | 0,03 |
| День (после ТГСК) возникновения фебрильной нейтропении |
4 |
5 | -1,18 | 0,23 |
| Пациенты с нейтропенической лихорадкой, абс. (%) | 34 (34%) | 40 (40%) | 0,63 | 0,52 |
| Дни тромбоцитопении ниже 20х10^9/л (медиана) | 4 | 5 | -1,42 | 0,15 |
| Уровень максимального снижения гемоглобина | 95 | 86 | 3,34 | 0,001 |
| Число линий предтрансплантационной химиотерапии | 2 | 2 | -1,3 | 0,19 |
| Длительность госпитализации | 22 | 22 | -0,46 | 0,64 |
Таблица 3. Результаты анализа затрат на профилактику и лечение фебрильной нейтропении на 1 человека после ауто-ТГСК
| ПЕГ-КСФ для лечения 1 пациента, руб. | КСФ для лечения 1 пациента, руб. | р |
| 49042,73 | 36180,63 | <0,05 |
[TYPE] => HTML ) [~DESCRIPTION] => [~NAME] => Описание/Резюме [~DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) ) [DOI] => Array ( [ID] => 28 [TIMESTAMP_X] => 2016-04-06 14:11:12 [IBLOCK_ID] => 2 [NAME] => DOI [ACTIVE] => Y [SORT] => 500 [CODE] => DOI [DEFAULT_VALUE] => [PROPERTY_TYPE] => S [ROW_COUNT] => 1 [COL_COUNT] => 80 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 28 [FILE_TYPE] => [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => [USER_TYPE_SETTINGS] => [HINT] => [PROPERTY_VALUE_ID] => [VALUE] => [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => [~DESCRIPTION] => [~NAME] => DOI [~DEFAULT_VALUE] => ) [AUTHOR_EN] => Array ( [ID] => 37 [TIMESTAMP_X] => 2015-09-02 18:02:59 [IBLOCK_ID] => 2 [NAME] => Author [ACTIVE] => Y [SORT] => 500 [CODE] => AUTHOR_EN [DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) [PROPERTY_TYPE] => S [ROW_COUNT] => 1 [COL_COUNT] => 30 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 37 [FILE_TYPE] => [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => HTML [USER_TYPE_SETTINGS] => Array ( [height] => 200 ) [HINT] => [PROPERTY_VALUE_ID] => 20478 [VALUE] => Array ( [TEXT] => Diana D. Ivanova, Vladislav O. Sarzhevsky, Vladimir Y. Melnichenko, Nikita E. Mochkin, Yulia N. Dubinina, Elena G. Smirnova, Dina S. Kolesnikova, Anna E. Bannikova [TYPE] => HTML ) [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => Array ( [TEXT] => Diana D. Ivanova, Vladislav O. Sarzhevsky, Vladimir Y. Melnichenko, Nikita E. Mochkin, Yulia N. Dubinina, Elena G. Smirnova, Dina S. Kolesnikova, Anna E. Bannikova [TYPE] => HTML ) [~DESCRIPTION] => [~NAME] => Author [~DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) ) [ORGANIZATION_EN] => Array ( [ID] => 38 [TIMESTAMP_X] => 2015-09-02 18:02:59 [IBLOCK_ID] => 2 [NAME] => Organization [ACTIVE] => Y [SORT] => 500 [CODE] => ORGANIZATION_EN [DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) [PROPERTY_TYPE] => S [ROW_COUNT] => 1 [COL_COUNT] => 30 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 38 [FILE_TYPE] => [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => HTML [USER_TYPE_SETTINGS] => Array ( [height] => 200 ) [HINT] => [PROPERTY_VALUE_ID] => 20479 [VALUE] => Array ( [TEXT] => National N. I. Pirogov Medical Surgical Center, Russian Ministry of Health, Moscow [TYPE] => HTML ) [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => Array ( [TEXT] => National N. I. Pirogov Medical Surgical Center, Russian Ministry of Health, Moscow [TYPE] => HTML ) [~DESCRIPTION] => [~NAME] => Organization [~DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) ) [SUMMARY_EN] => Array ( [ID] => 39 [TIMESTAMP_X] => 2015-09-02 18:02:59 [IBLOCK_ID] => 2 [NAME] => Description / Summary [ACTIVE] => Y [SORT] => 500 [CODE] => SUMMARY_EN [DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) [PROPERTY_TYPE] => S [ROW_COUNT] => 1 [COL_COUNT] => 30 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 39 [FILE_TYPE] => [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => HTML [USER_TYPE_SETTINGS] => Array ( [height] => 200 ) [HINT] => [PROPERTY_VALUE_ID] => 20480 [VALUE] => Array ( [TEXT] => <h2></h2> <h2 style="text-align: justify;">Introduction</h2> <p style="text-align: justify;"> High-dose chemotherapy (HDCT) with autologous transplantation of peripheral hematopoietic stem cells (auto-HSCT) is complicated by development of the grade IV hematologic toxicity. Among complications in this treatment, the most frequent are infectious conditions. The duration of grade IV neutropenia correlates with the development of severe infectious complications, which can cause death in the early posttransplant period. The use of colony-stimulating factors (CSF) reduces the duration of neutropenia as well as of developing infectious complications. The aim of the study is to evaluate and compare the efficacy, safety and pharmacoeconomic parameters of two forms of CSF, filgrastim and its pegylated form for stimulation leukopoiesis after auto-HSCT in the patients with lymphoproliferative diseases. </p> <h2 style="text-align: justify;">Materials and methods</h2> <p style="text-align: justify;"> The study included 100 patients: 39 with Hodgkin’s lymphoma, 18 with non-Hodgkin’s lymphomas, 42 with multiple myeloma, 1 acute promyelocytic leukemia; 51 women, 49 men. The median age was 43 years (18-72) (Table 1). The conditioning regimens were Melphalan 200 mg/m2, Melphalan 140 mg/m2, BeEAC, CBV, BEAM, Cytarabine + Melphalan. The patients were randomized into 2 groups: 1 group – patients who received pegylated form of CSF (PEG-CSF) (n=52), 2 group – patients with non- pegylated form of CSF (n=48). Stimulation of leukopoiesis was initiated on D+4. G-CSF was administered daily at dose of 5 μg/ kg/day until the release of agranulocytosis (WBC = 3.0x10 at 9 cells/L). PEG-CSF was administered once in dose of 6 mg (D+4). The pharmacoeconomic analysis included a comparison of economic evaluation of PEG-CSF treatment versus non-pegylated CSF therapy. Costs for PEG-CSF or CSF administered to the appropriate patient in the posttransplant period were taken into account. </p> <h2 style="text-align: justify;">Results</h2> <p style="text-align: justify;"> Comparative clinical analysis of the use of CSF and PEGCSF was performed using the following parameters: age, number of pre-transplantation chemotherapy lines, number of transplanted CD34 + (mio cells/kg), hemopoiesis recovery, presence of infectious complications (neutropenic fever), duration of hospitalization (Table 2). </p> <p style="text-align: justify;"> Significant differences were obtained by the rate of recovery of leukocyte count (in 1st group, the yield from agranulocytosis was registered significantly earlier). But in the 2nd group, the inhibition of the erythroid line was significantly less. There were no significant differences in other analyzed parameters. Pharmacoeconomic analysis showed that the median amount of money used to purchase PEG-CSF, administered for the treatment of one patient, was 49,042.73 rubles, and for the CSF was 36180.63 rubles. (p <0, 05) (Table 3) . </p> <h2 style="text-align: justify;">Conclusion</h2> <p style="text-align: justify;"> There were no significant differences in the clinical analysis of the use of pegylated and non- pegylated forms of colony-stimulating factors. Pharmacoeconomic analysis revealed the advantage of non-pegylated form of CSF over PEG-CSF. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hematopoietic stem cell transplantation, autologous, colony stimulating factor, pegylated form, efficiency, pharmacoeconomics. </p> <h2 style="text-align: justify;">Table 1. General clinical characteristics of patients</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> Number of patients in group </td> <td> 100 </td> </tr> <tr> <td> Age, median (interval), years </td> <td> 43 (18-72) </td> </tr> <tr> <td> Men, abs. (%) </td> <td> 49 (49) </td> </tr> <tr> <td> Women, abs. (%) </td> <td> 51 (51) </td> </tr> <tr> <td> Non-Hodgkin's lymphomas, abs. (%) </td> <td> 18 (18) </td> </tr> <tr> <td> Hodgkin Lymphoma, abs. (%) </td> <td> 39 (39) </td> </tr> <tr> <td> Multiple myeloma, abs. (%) </td> <td> 42 (42) </td> </tr> <tr> <td> Acute promyelocytic leukemia, abs. (%) </td> <td> 1 (1) </td> </tr> </tbody> </table> <h2>Table 2. Comparative analysis of PEG-CSF and CSF</h2> <table> <tbody> <tr> <td> </td> <td> Group CSF </td> <td> Group PEG-CSF </td> <td> t-value. </td> <td> p </td> </tr> <tr> <td> Age, years (median) </td> <td> 43 </td> <td> 41,5 </td> <td> 0,12 </td> <td> 0.9 </td> </tr> <tr> <td> The number of transplanted CD34 + million/kg, median </td> <td> 2.59 </td> <td> 2.65 </td> <td> 0.13 </td> <td> 0.86 </td> </tr> <tr> <td> Days of agranulocytosis (median) </td> <td> 7 </td> <td> 8 </td> <td> -0.93 </td> <td> 0.35 </td> </tr> <tr> <td> Day (after TSCC) of the marrow recovery agranulocytosis (median) </td> <td> 11 </td> <td> 10 </td> <td> 2.17 </td> <td> 0.03 </td> </tr> <tr> <td> Day (after TSCC) of febrile neutropenia </td> <td> 4 </td> <td> 5 </td> <td> -1.18 </td> <td> 0.23 </td> </tr> <tr> <td> Patients with neutropenic fever, abs. (%) </td> <td> 34 (34%) </td> <td> 40 (40%) </td> <td> 0.63 </td> <td> 0.52 </td> </tr> <tr> <td> Days of thrombocytopenia below 20х10^9/L (median) </td> <td> 4 </td> <td> 5 </td> <td> -1.42 </td> <td> 0.15 </td> </tr> <tr> <td> Level of maximum decrease in hemoglobin </td> <td> 95 </td> <td> 86 </td> <td> 3.34 </td> <td> 0.001 </td> </tr> <tr> <td> Number of pre-transplantation chemotherapy lines </td> <td> 2 </td> <td> 2 </td> <td> -1.3 </td> <td> 0.19 </td> </tr> <tr> <td> Duration of hospitalization </td> <td> 22 </td> <td> 22 </td> <td> -0.46 </td> <td> 0.64 </td> </tr> </tbody> </table> <h2>Table 3. Results of the cost analysis for the prevention and treatment of febrile neutropenia per 1 person after autograft</h2> <table border="1" cellpadding="1" cellspacing="1"> <tbody> <tr> <td> PEG-CSF<br> for treatment of 1 patient, Rub. </td> <td> CSF<br> for treatment of 1 patient, Rub. </td> <td> р </td> </tr> <tr> <td> 49042.73 </td> <td> 36180.63 </td> <td> <0.05 </td> </tr> </tbody> </table> <br> <h2></h2> [TYPE] => HTML ) [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => Array ( [TEXT] =>
Introduction
High-dose chemotherapy (HDCT) with autologous transplantation of peripheral hematopoietic stem cells (auto-HSCT) is complicated by development of the grade IV hematologic toxicity. Among complications in this treatment, the most frequent are infectious conditions. The duration of grade IV neutropenia correlates with the development of severe infectious complications, which can cause death in the early posttransplant period. The use of colony-stimulating factors (CSF) reduces the duration of neutropenia as well as of developing infectious complications. The aim of the study is to evaluate and compare the efficacy, safety and pharmacoeconomic parameters of two forms of CSF, filgrastim and its pegylated form for stimulation leukopoiesis after auto-HSCT in the patients with lymphoproliferative diseases.
Materials and methods
The study included 100 patients: 39 with Hodgkin’s lymphoma, 18 with non-Hodgkin’s lymphomas, 42 with multiple myeloma, 1 acute promyelocytic leukemia; 51 women, 49 men. The median age was 43 years (18-72) (Table 1). The conditioning regimens were Melphalan 200 mg/m2, Melphalan 140 mg/m2, BeEAC, CBV, BEAM, Cytarabine + Melphalan. The patients were randomized into 2 groups: 1 group – patients who received pegylated form of CSF (PEG-CSF) (n=52), 2 group – patients with non- pegylated form of CSF (n=48). Stimulation of leukopoiesis was initiated on D+4. G-CSF was administered daily at dose of 5 μg/ kg/day until the release of agranulocytosis (WBC = 3.0x10 at 9 cells/L). PEG-CSF was administered once in dose of 6 mg (D+4). The pharmacoeconomic analysis included a comparison of economic evaluation of PEG-CSF treatment versus non-pegylated CSF therapy. Costs for PEG-CSF or CSF administered to the appropriate patient in the posttransplant period were taken into account.
Results
Comparative clinical analysis of the use of CSF and PEGCSF was performed using the following parameters: age, number of pre-transplantation chemotherapy lines, number of transplanted CD34 + (mio cells/kg), hemopoiesis recovery, presence of infectious complications (neutropenic fever), duration of hospitalization (Table 2).
Significant differences were obtained by the rate of recovery of leukocyte count (in 1st group, the yield from agranulocytosis was registered significantly earlier). But in the 2nd group, the inhibition of the erythroid line was significantly less. There were no significant differences in other analyzed parameters. Pharmacoeconomic analysis showed that the median amount of money used to purchase PEG-CSF, administered for the treatment of one patient, was 49,042.73 rubles, and for the CSF was 36180.63 rubles. (p <0, 05) (Table 3) .
Conclusion
There were no significant differences in the clinical analysis of the use of pegylated and non- pegylated forms of colony-stimulating factors. Pharmacoeconomic analysis revealed the advantage of non-pegylated form of CSF over PEG-CSF.
Keywords
Hematopoietic stem cell transplantation, autologous, colony stimulating factor, pegylated form, efficiency, pharmacoeconomics.
Table 1. General clinical characteristics of patients
| Number of patients in group | 100 |
| Age, median (interval), years | 43 (18-72) |
| Men, abs. (%) | 49 (49) |
| Women, abs. (%) | 51 (51) |
| Non-Hodgkin's lymphomas, abs. (%) | 18 (18) |
| Hodgkin Lymphoma, abs. (%) | 39 (39) |
| Multiple myeloma, abs. (%) | 42 (42) |
| Acute promyelocytic leukemia, abs. (%) | 1 (1) |
Table 2. Comparative analysis of PEG-CSF and CSF
| Group CSF | Group PEG-CSF | t-value. | p | |
| Age, years (median) | 43 | 41,5 | 0,12 | 0.9 |
| The number of transplanted CD34 + million/kg, median | 2.59 | 2.65 | 0.13 | 0.86 |
| Days of agranulocytosis (median) | 7 | 8 | -0.93 | 0.35 |
| Day (after TSCC) of the marrow recovery agranulocytosis (median) | 11 | 10 | 2.17 | 0.03 |
| Day (after TSCC) of febrile neutropenia | 4 | 5 | -1.18 | 0.23 |
| Patients with neutropenic fever, abs. (%) | 34 (34%) | 40 (40%) | 0.63 | 0.52 |
| Days of thrombocytopenia below 20х10^9/L (median) | 4 | 5 | -1.42 | 0.15 |
| Level of maximum decrease in hemoglobin | 95 | 86 | 3.34 | 0.001 |
| Number of pre-transplantation chemotherapy lines | 2 | 2 | -1.3 | 0.19 |
| Duration of hospitalization | 22 | 22 | -0.46 | 0.64 |
Table 3. Results of the cost analysis for the prevention and treatment of febrile neutropenia per 1 person after autograft
|
PEG-CSF for treatment of 1 patient, Rub. |
CSF for treatment of 1 patient, Rub. |
р |
| 49042.73 | 36180.63 | <0.05 |
[TYPE] => HTML ) [~DESCRIPTION] => [~NAME] => Description / Summary [~DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) ) [NAME_EN] => Array ( [ID] => 40 [TIMESTAMP_X] => 2015-09-03 10:49:47 [IBLOCK_ID] => 2 [NAME] => Name [ACTIVE] => Y [SORT] => 500 [CODE] => NAME_EN [DEFAULT_VALUE] => [PROPERTY_TYPE] => S [ROW_COUNT] => 1 [COL_COUNT] => 80 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 40 [FILE_TYPE] => [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => Y [VERSION] => 1 [USER_TYPE] => [USER_TYPE_SETTINGS] => [HINT] => [PROPERTY_VALUE_ID] => 20481 [VALUE] => Clinical and pharmacoeconomic analysis of pegylated and nonpegylated forms of colony-stimulating factors after autologous transplantation of hematopoietic stem cells in patients with lymphoproliferative diseases [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => Clinical and pharmacoeconomic analysis of pegylated and nonpegylated forms of colony-stimulating factors after autologous transplantation of hematopoietic stem cells in patients with lymphoproliferative diseases [~DESCRIPTION] => [~NAME] => Name [~DEFAULT_VALUE] => ) [FULL_TEXT_RU] => Array ( [ID] => 42 [TIMESTAMP_X] => 2015-09-07 20:29:18 [IBLOCK_ID] => 2 [NAME] => Полный текст [ACTIVE] => Y [SORT] => 500 [CODE] => FULL_TEXT_RU [DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) [PROPERTY_TYPE] => S [ROW_COUNT] => 1 [COL_COUNT] => 30 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 42 [FILE_TYPE] => [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => HTML [USER_TYPE_SETTINGS] => Array ( [height] => 200 ) [HINT] => [PROPERTY_VALUE_ID] => [VALUE] => [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => [~DESCRIPTION] => [~NAME] => Полный текст [~DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) ) [PDF_RU] => Array ( [ID] => 43 [TIMESTAMP_X] => 2015-09-09 16:05:20 [IBLOCK_ID] => 2 [NAME] => PDF RUS [ACTIVE] => Y [SORT] => 500 [CODE] => PDF_RU [DEFAULT_VALUE] => [PROPERTY_TYPE] => F [ROW_COUNT] => 1 [COL_COUNT] => 30 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 43 [FILE_TYPE] => doc, txt, rtf, pdf [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => [USER_TYPE_SETTINGS] => [HINT] => [PROPERTY_VALUE_ID] => 20773 [VALUE] => 1411 [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => 1411 [~DESCRIPTION] => [~NAME] => PDF RUS [~DEFAULT_VALUE] => ) [PDF_EN] => Array ( [ID] => 44 [TIMESTAMP_X] => 2015-09-09 16:05:20 [IBLOCK_ID] => 2 [NAME] => PDF ENG [ACTIVE] => Y [SORT] => 500 [CODE] => PDF_EN [DEFAULT_VALUE] => [PROPERTY_TYPE] => F [ROW_COUNT] => 1 [COL_COUNT] => 30 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 44 [FILE_TYPE] => doc, txt, rtf, pdf [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => [USER_TYPE_SETTINGS] => [HINT] => [PROPERTY_VALUE_ID] => 20774 [VALUE] => 1412 [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => 1412 [~DESCRIPTION] => [~NAME] => PDF ENG [~DEFAULT_VALUE] => ) [NAME_LONG] => Array ( [ID] => 45 [TIMESTAMP_X] => 2023-04-13 00:55:00 [IBLOCK_ID] => 2 [NAME] => Название (для очень длинных заголовков) [ACTIVE] => Y [SORT] => 500 [CODE] => NAME_LONG [DEFAULT_VALUE] => Array ( [TYPE] => HTML [TEXT] => ) [PROPERTY_TYPE] => S [ROW_COUNT] => 1 [COL_COUNT] => 30 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 45 [FILE_TYPE] => [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => HTML [USER_TYPE_SETTINGS] => Array ( [height] => 80 ) [HINT] => [PROPERTY_VALUE_ID] => [VALUE] => [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => [~DESCRIPTION] => [~NAME] => Название (для очень длинных заголовков) [~DEFAULT_VALUE] => Array ( [TYPE] => HTML [TEXT] => ) ) )
Диана Д. Иванова, Владислав О. Саржевский, Владимир Я. Мельниченко, Никита Е. Мочкин, Юлия Н. Дубинина, Елена Г. Смирнова, Дина С. Колесникова, Анна Е. Банникова
Введение
Проведение высокодозной химиотерапии (ВДХТ) с аутологичной трансплантацией периферических гемопоэтических стволовых клеток (ауто-ТГСК) осложняется развитием гематологической токсичности IV степени. Среди осложнений при проведении данного лечения наиболее частым являются инфекционные. Длительность нейтропении IV степени коррелирует с развитием тяжелых инфекционных осложнений, которые могут стать причиной летального исхода в раннем посттрансплантационном периоде. Применение колониестимулирующих факторов (КСФ) снижает длительность нейтропении и риск развития инфекционных осложнений, а также сокращает пребывание пациента в специализированном отделении стационара. Цель исследования оценить и сравнить эффективность и безопасность двух форм КСФ, филграстима и его пегилированной формы, для стимуляции лейкопоэза при проведении ВДХТ с последующей ауто-ТГСК у пациентов с лимфопролиферативными заболеваниями, а также определить наиболее предпочтительную с точки зрения фармакоэкономического анализа форму КСФ.
Материалы и методы
В исследование включено 100 больных: 39 – c лимфомой Ходжкина, 18 – с неходжкинскими лимфомами, 42 – с множественной миеломой, 1 – острый промиелоцитарный лейкоз; 51 – женщина, 49 – мужчин. Медиана возраста составила 43 года (18-72) (табл. 1). Кондиционирование проводилось по схемам алкеран 200 мг/м. кв., алкеран 140 мг/м.кв., BeEAC, CBV, BEAM, цитарабин+мелфалан. Пациенты были рандомизированы на группы: 1 группа – пациенты, получающие пегилированную форму КСФ (ПЕГ-КСФ) (n=52), 2 группа – пациенты, получающие непегилированную форму КСФ (n=48). Стимуляцию лейкопоэза начинали на Д+4. Г-КСФ вводили ежедневно в дозе 5 мкг /кг/день до выхода из агранулоцитоза (WBC=3,0х10 в 9 ст./л ). ПЕГ-КСФ вводили однократно в дозе 6 мг (на Д+4). Фармакоэкономический анализ включал сопоставление относительной экономической оценки ПЕГ-КСФ и непегилированной формы КСФ. Учитывались затраты на ПЕГ-КСФ или КСФ, которые вводились соответствующему пациенту в период после выполнения ауто-ТГСК.
Результаты
Сравнительный клинический анализ использования КСФ и ПЕГ-КСФ проводился по следующим параметрам: возраст, число линий предтрансплантационной химиотерапии, количество трансплантированных CD34+ млн/кг, показатели восстановления гемопоэза, наличие инфекционных осложнений (нейтропеническая лихорадка), длительность госпитализации (табл. 2). Значимые отличия были получены по скорости восстановления уровня лейкоцитов (у пациентов из группы ПЕГ-КСФ выход из агранулоцитоза регистрировался значимо раньше). Но в группе КСФ угнетение эритроидного ростка было значимо меньше. Достоверных отличий по другим анализируемым параметрам получено не было.
Фармакоэкономический анализ показал, что медиана суммы денежных средств, использованных для приобретения ПЕГ-КСФ, вводимых для лечения одного больного, составила 49042,73 руб., а для КСФ 36180,63 руб. (p<0,05) (табл. 3).
Выводы
При клиническом анализе применения пегилированной и непегилированной форм колониестимулирующих факторов существенных отличий не выявлено. Фармакоэкономический анализ выявил преимущество непегилированной формы КСФ над ПЕГ-КСФ.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, аутологичная, колониестимулирующий фактор, пегилированный, эффективность, фармакоэкономика.
Таблица 1. Общая клиническая характеристика больных
| Число больных в группе | 100 |
| Возраст, медиана (интервал), лет | 43 (18-72) |
| Мужчины, абс. (%) | 49 (49) |
| Женщины, абс. (%) | 51 (51) |
| Неходжкинские лимфомы, абс. (%) | 18 (18) |
| Лимфома Ходжкина, абс. (%) | 39 (39) |
| Множественная миелома, абс. (%) | 42 (42) |
| Острый промиелоцитарный лейкоз, абс. (%) 1 | 1 (1) |
Таблица 2. Сравнительный анализ ПЕГ-КСФ и КСФ
| Группа КСФ | Группа ПЕГ-КСФ | t-знач. | p | |
| Возраст, годы (медиана) | 43 | 41,5 | 0,12 | 0,9 |
| Количество трансплантированных CD34+ млн/кг, медиана | 2,59 | 2,65 | 0,13 | 0,86 |
| Дни агранулоцитоза (медиана) | 7 | 8 | -0,93 | 0,35 |
| День (после ТГСК) выхода из агранулоцитоза (медиана) | 11 | 10 | 2,17 | 0,03 |
| День (после ТГСК) возникновения фебрильной нейтропении |
4 |
5 | -1,18 | 0,23 |
| Пациенты с нейтропенической лихорадкой, абс. (%) | 34 (34%) | 40 (40%) | 0,63 | 0,52 |
| Дни тромбоцитопении ниже 20х10^9/л (медиана) | 4 | 5 | -1,42 | 0,15 |
| Уровень максимального снижения гемоглобина | 95 | 86 | 3,34 | 0,001 |
| Число линий предтрансплантационной химиотерапии | 2 | 2 | -1,3 | 0,19 |
| Длительность госпитализации | 22 | 22 | -0,46 | 0,64 |
Таблица 3. Результаты анализа затрат на профилактику и лечение фебрильной нейтропении на 1 человека после ауто-ТГСК
| ПЕГ-КСФ для лечения 1 пациента, руб. | КСФ для лечения 1 пациента, руб. | р |
| 49042,73 | 36180,63 | <0,05 |
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20398
[VALUE] => Array
(
[TEXT] => Михаил Ю. Дроков, Дмитрий С. Тихомиров, Лариса А. Кузьмина, Татьяна А. Туполева, Наталья Н. Попова, Вера А. Васильева, Екатерина Д. Михальцова, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Татьяна В. Гапонова, Елена Н. Паровичникова, Валерий Г. Савченко
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Михаил Ю. Дроков, Дмитрий С. Тихомиров, Лариса А. Кузьмина, Татьяна А. Туполева, Наталья Н. Попова, Вера А. Васильева, Екатерина Д. Михальцова, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Татьяна В. Гапонова, Елена Н. Паровичникова, Валерий Г. Савченко
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20399
[VALUE] => Array
(
[TEXT] => ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва, Российская Федерация
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва, Российская Федерация
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20400
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Реактивация цитомегаловирусной инфекции (ЦМВ) остается одной из основных проблем трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Использование ЦМВ-неспецифичных внутривенных иммуноглобулинов (ИГ) до сих пор вызывает споры и определяется, в большей степени, внутренними протоколами трансплантационного центра без четкой доказательной базы. Стандартом же лечения ЦМВ до сих пор остается ганцикловир в дозе 10 мг/кг/сут в течение 14 дней с дальнейшим переходом на профилактическую дозу. Здесь мы приводим данные о влиянии ИГ в период лечения пациентов после алло-ТГСК ганцикловиром в период реактивации ЦМВ-инфекции
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
Тридцать два пациента с гемобластозами после алло-ТГСК были включены в исследование. Детальные характеристики представлены в Таблице 1. Все пациенты на момент включения в исследования были ЦМВ-позитивны (по данным ПЦР, «АмплиСенс EBV/CMV/ HHV6-c-крин-FL», Интерлабсервис, Россия), а также требовали начала терапии ганцикловиром в дозе 10 мг/кг/сут. Часть пациентов получили в/в ИГ. Медиана суммарной дозы за время лечения составила 20 г. (7,5-90 г.). Метод Каплан-Мейера был использован для оценки вероятности достижения ЦМВ-негативности (по данным ПЦР). Логранк тест был использован для сравнения различий между двумя группами. Для анализа таблиц 2x2 был использован точный тест Фишера. Р-значение ниже 0.05 считалось значимым.
</p>
<h2 style="text-align: justify;">
Таблица 1. Характеристики пациентов<br>
</h2>
<img width="743" alt="14_Таблица 1. Характеристики пациентов.png" src="/upload/medialibrary/77f/14_tablitsa-1.-kharakteristiki-patsientov.png" height="508" title="14_Таблица 1. Характеристики пациентов.png"><br>
<img width="740" alt="14_Таблица 1. Характеристики пациентов_2.png" src="/upload/medialibrary/097/14_tablitsa-1.-kharakteristiki-patsientov_2.png" height="272" title="14_Таблица 1. Характеристики пациентов_2.png"><br>
<img width="717" alt="14_Рисунок 1. Время до достижения.png" src="/upload/medialibrary/1b2/14_risunok-1.-vremya-do-dostizheniya.png" height="431" title="14_Рисунок 1. Время до достижения.png">
<h2>Рисунок 1. Время до достижения ПЦР-негативности в зависимости от использования внутривенных ЦМВ-неспецифичных иммуноглобулинов</h2>
<h2></h2>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Влияние ИГ на вероятность достижение ЦМВ-негативности (по данным ПЦР) у пациентов с алло-ТГСК показано на Рисунке 1. Как показано на рисунке различия между группами с/без введения ИГ в период терапии ганцикловиром были незначимы.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Использование внутривенных ЦМВ-неспецифичных иммуноглобулинов после алло-ТГСК до сих пор является спорной темой. Согласно нашим данным введение внутривенных ЦМВ-неспецифичных иммуноглобулинов в период терапии ганцикловиром не оказывает должного влияния на эффективность терапии ЦМВ. Однако требуется проведение большого рандомизированного исследования чтобы окончательно определить влияние ЦМВ-неспецифичных ИГ на эффективность лечения реактивации ЦМВ у больных после алло-ТГСК.
</p>
<h2 style="text-align: justify;">Конфликт интересов</h2>
<p style="text-align: justify;">
Нет конфликта интересов.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
ЦМВ, внутривенный иммуноглобулин, ганцикловир, алло-ТГСК, ПЦР.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Реактивация цитомегаловирусной инфекции (ЦМВ) остается одной из основных проблем трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Использование ЦМВ-неспецифичных внутривенных иммуноглобулинов (ИГ) до сих пор вызывает споры и определяется, в большей степени, внутренними протоколами трансплантационного центра без четкой доказательной базы. Стандартом же лечения ЦМВ до сих пор остается ганцикловир в дозе 10 мг/кг/сут в течение 14 дней с дальнейшим переходом на профилактическую дозу. Здесь мы приводим данные о влиянии ИГ в период лечения пациентов после алло-ТГСК ганцикловиром в период реактивации ЦМВ-инфекции
Пациенты и методы
Тридцать два пациента с гемобластозами после алло-ТГСК были включены в исследование. Детальные характеристики представлены в Таблице 1. Все пациенты на момент включения в исследования были ЦМВ-позитивны (по данным ПЦР, «АмплиСенс EBV/CMV/ HHV6-c-крин-FL», Интерлабсервис, Россия), а также требовали начала терапии ганцикловиром в дозе 10 мг/кг/сут. Часть пациентов получили в/в ИГ. Медиана суммарной дозы за время лечения составила 20 г. (7,5-90 г.). Метод Каплан-Мейера был использован для оценки вероятности достижения ЦМВ-негативности (по данным ПЦР). Логранк тест был использован для сравнения различий между двумя группами. Для анализа таблиц 2x2 был использован точный тест Фишера. Р-значение ниже 0.05 считалось значимым.
Таблица 1. Характеристики пациентов



Рисунок 1. Время до достижения ПЦР-негативности в зависимости от использования внутривенных ЦМВ-неспецифичных иммуноглобулинов
Результаты
Влияние ИГ на вероятность достижение ЦМВ-негативности (по данным ПЦР) у пациентов с алло-ТГСК показано на Рисунке 1. Как показано на рисунке различия между группами с/без введения ИГ в период терапии ганцикловиром были незначимы.
Заключение
Использование внутривенных ЦМВ-неспецифичных иммуноглобулинов после алло-ТГСК до сих пор является спорной темой. Согласно нашим данным введение внутривенных ЦМВ-неспецифичных иммуноглобулинов в период терапии ганцикловиром не оказывает должного влияния на эффективность терапии ЦМВ. Однако требуется проведение большого рандомизированного исследования чтобы окончательно определить влияние ЦМВ-неспецифичных ИГ на эффективность лечения реактивации ЦМВ у больных после алло-ТГСК.
Конфликт интересов
Нет конфликта интересов.
Ключевые слова
ЦМВ, внутривенный иммуноглобулин, ганцикловир, алло-ТГСК, ПЦР.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20401
[VALUE] => Array
(
[TEXT] => Mikhail Y. Drokov, Dmitry S. Tikhomirov, Larisa A. Kuzmina, Tatyana A. Tupoleva, Natalia N. Popova, Vera A. Vasilyeva, Ekaterina D. Mikhaltsova, Olga M. Koroleva, Darya S. Dubnyak, Anna A. Sidorova, Ekaterina V. Usikova, Zoya V. Konova, Anna A. Dmitrova, Tatyana V. Gaponova, Elena N. Parovichnikova, Valery G. Savchenko<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Mikhail Y. Drokov, Dmitry S. Tikhomirov, Larisa A. Kuzmina, Tatyana A. Tupoleva, Natalia N. Popova, Vera A. Vasilyeva, Ekaterina D. Mikhaltsova, Olga M. Koroleva, Darya S. Dubnyak, Anna A. Sidorova, Ekaterina V. Usikova, Zoya V. Konova, Anna A. Dmitrova, Tatyana V. Gaponova, Elena N. Parovichnikova, Valery G. Savchenko
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20402
[VALUE] => Array
(
[TEXT] => National Research Center for Hematology, Moscow, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => National Research Center for Hematology, Moscow, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20403
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Cytomegalovirus (CMV) reactivation is one of the main problems in allogenic hematopoietic stem cell transplantation (allo-HSCT). Use of non-CMV specific intravenous immunoglobulin (IVIG) is still controversial and mostly determined by protocols in every transplant center. Standard of care for CMV-disease is still ganciclovir at 10 mg/kg b.i.d. Here we report data about influence of non-CMV specific IVIG during ganciclovir treatment in allo-HSCT CMV+ patients.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
Thirty two patients with hematological malignancies transplanted in NRCH were included in this study. Detailed patients characteristics are listed in Table 1. All patients were CMV-positive by PCR (Amplisens EBV/CMV/ HHV6-screen-FL”, InterLabService, Russia) and required to start therapy with ganciclovir 10 mg/kg. Patients in IVIG group also received non-CMV specific IVIG during ganciclovir treatment with a median total dose 20 g (7.5-90 g.). Kaplan-Meier estimator was used to determine probability of achievement of CMV-negativity from the time of ganciclovir was started to CMV-negativity (by PCR) or last contact. The log rank test was used to compare differences between the two groups. Fisher’s exact test was used for 2x2 tables. P-value less than 0.05 was considered statistically significant
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Impact of IVIG in allo-HSCT patients on probability of achievement of CMV-negativity (by PCR) are shown in the Figure 1. As we can see there is no significant differences on the achievement of CMV-negativity (by PCR) in patients with/without IVIG during ganciclovir therapy.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
The use of non-CMV specific immunoglobulins after allo-HSCT is still controversial. According to our data there is no difference between IVIG/no-IVIG groups during ganciclovir treatment. For our opinion use of IVIG, for CMV-disease treatment has not been yet proved. Anyway a large randomized trial is required to determine indications for therapy with IVIG in CMV disease after allo-HSCT.
</p>
<h2 style="text-align: justify;">Disclosures</h2>
<p style="text-align: justify;">
No relevant conflicts reported.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
CMV, intravenous immunoglobulin, ganciclovir, allo-HSCT, PCR.
</p>
<h2 style="text-align: justify;">
Table 1. Patients characteristics<br>
</h2>
<img width="741" alt="14_Table 1. Patients characteristics.png" src="/upload/medialibrary/94e/14_table-1.-patients-characteristics.png" height="324" title="14_Table 1. Patients characteristics.png"><br>
<img width="743" alt="14_Table 1. Patients characteristics_2.png" src="/upload/medialibrary/e1b/14_table-1.-patients-characteristics_2.png" height="483" title="14_Table 1. Patients characteristics_2.png"><br>
<br>
<img width="717" alt="14_Figure 1. Time to CMV-negativity achievement depending on the therapy mode.png" src="/upload/medialibrary/ffe/14_figure-1.-time-to-cmv_negativity-achievement-depending-on-the-therapy-mode.png" height="431" title="14_Figure 1. Time to CMV-negativity achievement depending on the therapy mode.png">
<h2>Figure 1. Time to CMV-negativity achievement depending on the therapy mode</h2>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Cytomegalovirus (CMV) reactivation is one of the main problems in allogenic hematopoietic stem cell transplantation (allo-HSCT). Use of non-CMV specific intravenous immunoglobulin (IVIG) is still controversial and mostly determined by protocols in every transplant center. Standard of care for CMV-disease is still ganciclovir at 10 mg/kg b.i.d. Here we report data about influence of non-CMV specific IVIG during ganciclovir treatment in allo-HSCT CMV+ patients.
Patients and methods
Thirty two patients with hematological malignancies transplanted in NRCH were included in this study. Detailed patients characteristics are listed in Table 1. All patients were CMV-positive by PCR (Amplisens EBV/CMV/ HHV6-screen-FL”, InterLabService, Russia) and required to start therapy with ganciclovir 10 mg/kg. Patients in IVIG group also received non-CMV specific IVIG during ganciclovir treatment with a median total dose 20 g (7.5-90 g.). Kaplan-Meier estimator was used to determine probability of achievement of CMV-negativity from the time of ganciclovir was started to CMV-negativity (by PCR) or last contact. The log rank test was used to compare differences between the two groups. Fisher’s exact test was used for 2x2 tables. P-value less than 0.05 was considered statistically significant
Results
Impact of IVIG in allo-HSCT patients on probability of achievement of CMV-negativity (by PCR) are shown in the Figure 1. As we can see there is no significant differences on the achievement of CMV-negativity (by PCR) in patients with/without IVIG during ganciclovir therapy.
Conclusion
The use of non-CMV specific immunoglobulins after allo-HSCT is still controversial. According to our data there is no difference between IVIG/no-IVIG groups during ganciclovir treatment. For our opinion use of IVIG, for CMV-disease treatment has not been yet proved. Anyway a large randomized trial is required to determine indications for therapy with IVIG in CMV disease after allo-HSCT.
Disclosures
No relevant conflicts reported.
Keywords
CMV, intravenous immunoglobulin, ganciclovir, allo-HSCT, PCR.
Table 1. Patients characteristics



Figure 1. Time to CMV-negativity achievement depending on the therapy mode
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20404
[VALUE] => Influence of non-CMV specific intravenous immunoglobulin on intravenous ganciclovir effectiveness in patients after allogeneic stem cell transplantation with CMV-disease
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Influence of non-CMV specific intravenous immunoglobulin on intravenous ganciclovir effectiveness in patients after allogeneic stem cell transplantation with CMV-disease
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20759
[VALUE] => 1395
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1395
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20760
[VALUE] => 1396
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1396
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Михаил Ю. Дроков, Дмитрий С. Тихомиров, Лариса А. Кузьмина, Татьяна А. Туполева, Наталья Н. Попова, Вера А. Васильева, Екатерина Д. Михальцова, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Татьяна В. Гапонова, Елена Н. Паровичникова, Валерий Г. Савченко
Введение
Реактивация цитомегаловирусной инфекции (ЦМВ) остается одной из основных проблем трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Использование ЦМВ-неспецифичных внутривенных иммуноглобулинов (ИГ) до сих пор вызывает споры и определяется, в большей степени, внутренними протоколами трансплантационного центра без четкой доказательной базы. Стандартом же лечения ЦМВ до сих пор остается ганцикловир в дозе 10 мг/кг/сут в течение 14 дней с дальнейшим переходом на профилактическую дозу. Здесь мы приводим данные о влиянии ИГ в период лечения пациентов после алло-ТГСК ганцикловиром в период реактивации ЦМВ-инфекции
Пациенты и методы
Тридцать два пациента с гемобластозами после алло-ТГСК были включены в исследование. Детальные характеристики представлены в Таблице 1. Все пациенты на момент включения в исследования были ЦМВ-позитивны (по данным ПЦР, «АмплиСенс EBV/CMV/ HHV6-c-крин-FL», Интерлабсервис, Россия), а также требовали начала терапии ганцикловиром в дозе 10 мг/кг/сут. Часть пациентов получили в/в ИГ. Медиана суммарной дозы за время лечения составила 20 г. (7,5-90 г.). Метод Каплан-Мейера был использован для оценки вероятности достижения ЦМВ-негативности (по данным ПЦР). Логранк тест был использован для сравнения различий между двумя группами. Для анализа таблиц 2x2 был использован точный тест Фишера. Р-значение ниже 0.05 считалось значимым.
Таблица 1. Характеристики пациентов



Рисунок 1. Время до достижения ПЦР-негативности в зависимости от использования внутривенных ЦМВ-неспецифичных иммуноглобулинов
Результаты
Влияние ИГ на вероятность достижение ЦМВ-негативности (по данным ПЦР) у пациентов с алло-ТГСК показано на Рисунке 1. Как показано на рисунке различия между группами с/без введения ИГ в период терапии ганцикловиром были незначимы.
Заключение
Использование внутривенных ЦМВ-неспецифичных иммуноглобулинов после алло-ТГСК до сих пор является спорной темой. Согласно нашим данным введение внутривенных ЦМВ-неспецифичных иммуноглобулинов в период терапии ганцикловиром не оказывает должного влияния на эффективность терапии ЦМВ. Однако требуется проведение большого рандомизированного исследования чтобы окончательно определить влияние ЦМВ-неспецифичных ИГ на эффективность лечения реактивации ЦМВ у больных после алло-ТГСК.
Конфликт интересов
Нет конфликта интересов.
Ключевые слова
ЦМВ, внутривенный иммуноглобулин, ганцикловир, алло-ТГСК, ПЦР.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20389
[VALUE] => Array
(
[TEXT] => Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Вера А. Васильева, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Елена Н. Паровичникова, Валерий Г. Савченко
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Вера А. Васильева, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Елена Н. Паровичникова, Валерий Г. Савченко
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20390
[VALUE] => Array
(
[TEXT] => ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20391
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Трансплантация аллогенного костного мозга (алло-ТГСК) с использованием высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) в качестве индуктора толерантности стала хорошей альтернативой стандартной иммуносупрессии. Часто необоснованные ожидания токсичности, особенно у пациентов старше 50, становятся препятствием для проведения алло-ТГСК у данных больных. Здесь нами представлены данные о влиянии возраста пациентов с острыми лейкозами в ПР на результаты алло-ТГСК с ПТ-ЦФ и АТГ в качестве профилактики РТПХ.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
Сорок пациентов с острыми лейкозами были трансплантированы в ПР в НМИЦ гематологии МЗ РФ от неродственного частично-совместимого донора. Характеристика пациентов представлена в Таблице 1. Все пациенты в качестве профилактики РТПХ получали: АТГ в суммарной дозе 40 мг/кг с -4 по -1 день; ПТ-ЦФ в дозе 50 мг/кг/сут на +3, +4 день; Циклоспорин А в дозе 3 мг/кг/сут с -1 дня; Микофенолата мофетил 3000 мг/сут с +5 дня. Метод Каплан-Мейера был использован для оценки общей выживаемости, вероятности развития рецидива, острой РТПХ. Логранк тест был использован для сравнения различий между двумя группами. Р-значение ниже 0.05 считалось значимым.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Острая РТПХ в группе пациентов старше 50 лет была значимо выше, чем в группах в возрасте 40-49 и 20-39 лет (66,7% vs 25% vs 12,5%, p=0.0044) (Рис. 1). Вероятно, это может быть связано с резидуальной функцией тимуса, а также более частым использованием миелоаблативных режимов у молодых больных (младше 50 лет). Однако, несмотря на эти различия, высокая частота развития РТПХ свидетельствует о более низкой частоте развития рецидивов (Рис. 2), что, в свою очередь, ведет к отсутствию различий общей выживаемостью между группами (Рис. 3) – 56,1%, 66,7% и 65,6% для группы 20-39, 40-49 и 50+ соответственно.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Алло-ТГСК у пациентов в возрасте старше 50 лет имеет свои особенности, однако эффективность данной процедуры (общая выживаемость пациентов) ничуть не меньше, чем у более молодых пациентов. Таким образом, использование ПТ-ЦФ и АТГ у пациентов старше 50 лет вполне оправдано и достаточно эффективно.
</p>
<h2 style="text-align: justify;">Конфликт интересов</h2>
<p style="text-align: justify;">
Отсутствует конфликт интересов.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
РТПХ, посттрансплантационный циклофосфамид, возраст, острый лейкоз, АТГ.
</p>
<h2 style="text-align: justify;">
Таблица 1. Характеристика пациентов<br>
</h2>
<p style="text-align: justify;">
<img width="783" alt="13_Таблица 1. Характеристика пациентов.png" src="/upload/medialibrary/da0/13_tablitsa-1.-kharakteristika-patsientov.png" height="329" title="13_Таблица 1. Характеристика пациентов.png"><br>
</p>
<p style="text-align: justify;">
<img width="717" alt="13_Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами.png" src="/upload/medialibrary/87b/13_risunok-1.-veroyatnost-razvitiya-ostroy-rtpkh-v-razlichnykh-vozrastnykh-gruppakh-u-patsientov-s-ostrymi-leykozami.png" height="425" title="13_Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами.png"><br>
</p>
<h2 style="text-align: justify;">
Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ</h2>
<p style="text-align: justify;">
<img width="717" alt="13_Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами.png" src="/upload/medialibrary/9d2/13_risunok-2.-veroyatnost-razvitiya-retsidiva-v-razlichnykh-vozrastnykh-gruppakh-u-patsientov-s-ostrymi-leykozami.png" height="426" title="13_Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами.png"><br>
</p>
<h2 style="text-align: justify;">
Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ</h2>
<img width="717" alt="13_Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после.png" src="/upload/medialibrary/ea1/13_risunok-3.-obshchaya-vyzhivaemost-v-razlichnykh-vozrastnykh-gruppakh-u-patsientov-s-ostrymi-leykozami-posle.png" height="426" title="13_Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после.png">
<h2>Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ</h2>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Трансплантация аллогенного костного мозга (алло-ТГСК) с использованием высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) в качестве индуктора толерантности стала хорошей альтернативой стандартной иммуносупрессии. Часто необоснованные ожидания токсичности, особенно у пациентов старше 50, становятся препятствием для проведения алло-ТГСК у данных больных. Здесь нами представлены данные о влиянии возраста пациентов с острыми лейкозами в ПР на результаты алло-ТГСК с ПТ-ЦФ и АТГ в качестве профилактики РТПХ.
Пациенты и методы
Сорок пациентов с острыми лейкозами были трансплантированы в ПР в НМИЦ гематологии МЗ РФ от неродственного частично-совместимого донора. Характеристика пациентов представлена в Таблице 1. Все пациенты в качестве профилактики РТПХ получали: АТГ в суммарной дозе 40 мг/кг с -4 по -1 день; ПТ-ЦФ в дозе 50 мг/кг/сут на +3, +4 день; Циклоспорин А в дозе 3 мг/кг/сут с -1 дня; Микофенолата мофетил 3000 мг/сут с +5 дня. Метод Каплан-Мейера был использован для оценки общей выживаемости, вероятности развития рецидива, острой РТПХ. Логранк тест был использован для сравнения различий между двумя группами. Р-значение ниже 0.05 считалось значимым.
Результаты
Острая РТПХ в группе пациентов старше 50 лет была значимо выше, чем в группах в возрасте 40-49 и 20-39 лет (66,7% vs 25% vs 12,5%, p=0.0044) (Рис. 1). Вероятно, это может быть связано с резидуальной функцией тимуса, а также более частым использованием миелоаблативных режимов у молодых больных (младше 50 лет). Однако, несмотря на эти различия, высокая частота развития РТПХ свидетельствует о более низкой частоте развития рецидивов (Рис. 2), что, в свою очередь, ведет к отсутствию различий общей выживаемостью между группами (Рис. 3) – 56,1%, 66,7% и 65,6% для группы 20-39, 40-49 и 50+ соответственно.
Заключение
Алло-ТГСК у пациентов в возрасте старше 50 лет имеет свои особенности, однако эффективность данной процедуры (общая выживаемость пациентов) ничуть не меньше, чем у более молодых пациентов. Таким образом, использование ПТ-ЦФ и АТГ у пациентов старше 50 лет вполне оправдано и достаточно эффективно.
Конфликт интересов
Отсутствует конфликт интересов.
Ключевые слова
РТПХ, посттрансплантационный циклофосфамид, возраст, острый лейкоз, АТГ.
Таблица 1. Характеристика пациентов


Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ

Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ

Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20392
[VALUE] => Array
(
[TEXT] => Mikhail Y. Drokov, Larisa A. Kuzmina, Natalia N. Popova, Ekaterina D. Mikhaltsova, Vera A. Vasilyeva, Olga M. Koroleva, Darya S. Dubnyak, Anna A. Sidorova, Ekaterina V. Usikova, Zoya V. Konova, Anna A. Dmitrova, Elena N. Parovichnikova, Valery G. Savchenko<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Mikhail Y. Drokov, Larisa A. Kuzmina, Natalia N. Popova, Ekaterina D. Mikhaltsova, Vera A. Vasilyeva, Olga M. Koroleva, Darya S. Dubnyak, Anna A. Sidorova, Ekaterina V. Usikova, Zoya V. Konova, Anna A. Dmitrova, Elena N. Parovichnikova, Valery G. Savchenko
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20393
[VALUE] => Array
(
[TEXT] => National Research Center for Hematology, Moscow, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => National Research Center for Hematology, Moscow, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20394
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Allogeneic bone marrow transplantation (allo-BMT) with high-dose posttransplant cyclophosphamide (PT-CY) to promote graft-host tolerance has become an alternative for standard immunosuppression. But sometimes unjustified toxicity expectations in aged patients are the main limiting factor of allo-HSCT for this group. Here we report our data about an influence of age on allo-HSCT results in leukemia patients in CR with PT-CY and ATG as GVHD prophylaxis.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
Forty patients with acute leukemia in CR transplanted in NRCH from mismatched unrelated donor were included in this study. All patient characteristics are listed in Table 1. All the patients received ATG at a dose 40 mg/kg from day -4 to day -1; PT-CY at dose 50 mg/kg daily at day +3,+4; Cyclosporine A 3 mg/kg from day -1 and MMF 3000 mg b.i.d from day +5. Kaplan-Meier estimator was used to determine overall survival, probability of aGVHD and relapse. The log-rank test was used to compare differences between the two groups. P-value less than 0.05 was considered statistically significant.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Acute GVHD rates in 50+ y.o. group are significantly higher (Fig. 1) than in younger patients (66.7% vs 25% vs 12.5%, p=0.0044). It can be explained by thymus function and use of MAC conditioning regimens in the last patient group. Despite that fact due to low relapse rate (Fig. 2) overall survival (Fig. 3) in 50+ y.o. patients looks comparable with younger patients (66.7% vs 65.6% vs 58.9% for 40-49 y.o., 50+ and 20-39 y.o. respectively).
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Allo-HSCT still makes sense in 50+ y.o. patients, since the results are not worse than in younger patients. Usage of PT-CY and ATG as GVHD prophylaxis seems to be safe and effective approach even for aged leukemia patients.
</p>
<h2 style="text-align: justify;">Disclosures</h2>
<p style="text-align: justify;">
No relevant conflicts of interest to declare.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
GVHD, PT-Cy, age, acute leukemia, ATG.<br>
</p>
<h2 style="text-align: justify;">
Table 1. Patients characteristics<br>
</h2>
<img width="787" alt="13_Table 1.png" src="/upload/medialibrary/f92/13_table-1.png" height="335" title="13_Table 1.png"><br>
<img width="717" alt="13_Figure 1. Acute GVHD in different.png" src="/upload/medialibrary/50d/13_figure-1.-acute-gvhd-in-different.png" height="426" title="13_Figure 1. Acute GVHD in different.png">
<h2>Figure 1. Acute GVHD in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis</h2>
<br>
<img width="717" alt="13_Figure 2. Relapse rate.png" src="/upload/medialibrary/642/13_figure-2.-relapse-rate.png" height="431" title="13_Figure 2. Relapse rate.png">
<h2>Figure 2. Relapse rate in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis</h2>
<img width="717" alt="13_Figure 3. Overall survival.png" src="/upload/medialibrary/b45/13_figure-3.-overall-survival.png" height="431" title="13_Figure 3. Overall survival.png">
<h2>Figure 3. Overall survival in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis</h2>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Allogeneic bone marrow transplantation (allo-BMT) with high-dose posttransplant cyclophosphamide (PT-CY) to promote graft-host tolerance has become an alternative for standard immunosuppression. But sometimes unjustified toxicity expectations in aged patients are the main limiting factor of allo-HSCT for this group. Here we report our data about an influence of age on allo-HSCT results in leukemia patients in CR with PT-CY and ATG as GVHD prophylaxis.
Patients and methods
Forty patients with acute leukemia in CR transplanted in NRCH from mismatched unrelated donor were included in this study. All patient characteristics are listed in Table 1. All the patients received ATG at a dose 40 mg/kg from day -4 to day -1; PT-CY at dose 50 mg/kg daily at day +3,+4; Cyclosporine A 3 mg/kg from day -1 and MMF 3000 mg b.i.d from day +5. Kaplan-Meier estimator was used to determine overall survival, probability of aGVHD and relapse. The log-rank test was used to compare differences between the two groups. P-value less than 0.05 was considered statistically significant.
Results
Acute GVHD rates in 50+ y.o. group are significantly higher (Fig. 1) than in younger patients (66.7% vs 25% vs 12.5%, p=0.0044). It can be explained by thymus function and use of MAC conditioning regimens in the last patient group. Despite that fact due to low relapse rate (Fig. 2) overall survival (Fig. 3) in 50+ y.o. patients looks comparable with younger patients (66.7% vs 65.6% vs 58.9% for 40-49 y.o., 50+ and 20-39 y.o. respectively).
Conclusion
Allo-HSCT still makes sense in 50+ y.o. patients, since the results are not worse than in younger patients. Usage of PT-CY and ATG as GVHD prophylaxis seems to be safe and effective approach even for aged leukemia patients.
Disclosures
No relevant conflicts of interest to declare.
Keywords
GVHD, PT-Cy, age, acute leukemia, ATG.
Table 1. Patients characteristics


Figure 1. Acute GVHD in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis

Figure 2. Relapse rate in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis

Figure 3. Overall survival in different age group of leukemia patients with PT-CY and ATG as GVHD prophylaxis
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20395
[VALUE] => Age affects GVHD rate but not overall survival in leukemia patients with posttransplant cyclophosphamide (PT-CY) and anti-thymocyte globulin (ATG) as GVHD prophylaxis
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Age affects GVHD rate but not overall survival in leukemia patients with posttransplant cyclophosphamide (PT-CY) and anti-thymocyte globulin (ATG) as GVHD prophylaxis
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20757
[VALUE] => 1393
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1393
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20758
[VALUE] => 1394
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1394
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Вера А. Васильева, Ольга М. Королева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Елена Н. Паровичникова, Валерий Г. Савченко
Введение
Трансплантация аллогенного костного мозга (алло-ТГСК) с использованием высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) в качестве индуктора толерантности стала хорошей альтернативой стандартной иммуносупрессии. Часто необоснованные ожидания токсичности, особенно у пациентов старше 50, становятся препятствием для проведения алло-ТГСК у данных больных. Здесь нами представлены данные о влиянии возраста пациентов с острыми лейкозами в ПР на результаты алло-ТГСК с ПТ-ЦФ и АТГ в качестве профилактики РТПХ.
Пациенты и методы
Сорок пациентов с острыми лейкозами были трансплантированы в ПР в НМИЦ гематологии МЗ РФ от неродственного частично-совместимого донора. Характеристика пациентов представлена в Таблице 1. Все пациенты в качестве профилактики РТПХ получали: АТГ в суммарной дозе 40 мг/кг с -4 по -1 день; ПТ-ЦФ в дозе 50 мг/кг/сут на +3, +4 день; Циклоспорин А в дозе 3 мг/кг/сут с -1 дня; Микофенолата мофетил 3000 мг/сут с +5 дня. Метод Каплан-Мейера был использован для оценки общей выживаемости, вероятности развития рецидива, острой РТПХ. Логранк тест был использован для сравнения различий между двумя группами. Р-значение ниже 0.05 считалось значимым.
Результаты
Острая РТПХ в группе пациентов старше 50 лет была значимо выше, чем в группах в возрасте 40-49 и 20-39 лет (66,7% vs 25% vs 12,5%, p=0.0044) (Рис. 1). Вероятно, это может быть связано с резидуальной функцией тимуса, а также более частым использованием миелоаблативных режимов у молодых больных (младше 50 лет). Однако, несмотря на эти различия, высокая частота развития РТПХ свидетельствует о более низкой частоте развития рецидивов (Рис. 2), что, в свою очередь, ведет к отсутствию различий общей выживаемостью между группами (Рис. 3) – 56,1%, 66,7% и 65,6% для группы 20-39, 40-49 и 50+ соответственно.
Заключение
Алло-ТГСК у пациентов в возрасте старше 50 лет имеет свои особенности, однако эффективность данной процедуры (общая выживаемость пациентов) ничуть не меньше, чем у более молодых пациентов. Таким образом, использование ПТ-ЦФ и АТГ у пациентов старше 50 лет вполне оправдано и достаточно эффективно.
Конфликт интересов
Отсутствует конфликт интересов.
Ключевые слова
РТПХ, посттрансплантационный циклофосфамид, возраст, острый лейкоз, АТГ.
Таблица 1. Характеристика пациентов


Рисунок 1. Вероятность развития острой РТПХ в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ

Рисунок 2. Вероятность развития рецидива в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ

Рисунок 3. Общая выживаемость в различных возрастных группах у пациентов с острыми лейкозами после алло-ТГСК в ПР с ПТ-ЦФ и АТГ в качестве профилактики РТПХ
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20301
[VALUE] => Array
(
[TEXT] => Сергей Н. Бондаренко <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Анна Г. Смирнова <sup>1</sup>, Ирина А. Самородова <sup>1</sup>, Ольга С. Успенская <sup>2</sup>, Елена В. Бабенко <sup>1</sup>, Ильдар М. Бархатов <sup>1</sup>, Татьяна Л. Гиндина <sup>1</sup>, Николай Н. Мамаев <sup>1</sup>, Александр Д. Кулагин <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Сергей Н. Бондаренко 1, Иван С. Моисеев 1, Елена И. Дарская 1, Анна Г. Смирнова 1, Ирина А. Самородова 1, Ольга С. Успенская 2, Елена В. Бабенко 1, Ильдар М. Бархатов 1, Татьяна Л. Гиндина 1, Николай Н. Мамаев 1, Александр Д. Кулагин 1, Борис В. Афанасьев 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20302
[VALUE] => Array
(
[TEXT] => <sup>1</sup> НИИ ДОГиТ им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург<br>
<sup>2</sup> Ленинградская областная клиническая больница, Санкт-Петербург<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 НИИ ДОГиТ им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург
2 Ленинградская областная клиническая больница, Санкт-Петербург
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20350
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) является эффективным методом лечения острого миелобластного лейкоза (ОМЛ). Развитие рецидива после алло-ТГСК является наиболее частой причиной неудач лечения. Однако, проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания дает возможность определения минимальной остаточной болезни (МОБ) в ремиссии (ПР) ОМЛ с целью определения прогноза и выбора адекватной терапии.
</p>
<h2 style="text-align: justify;">Цель работы</h2>
<p style="text-align: justify;">
Оценить влияние наличия МОБ у пациентов ОМЛ перед алло-ТГСК на результаты лечения.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
В исследование включено 195 пациентов за период 2012-16 гг. Медиана возраста составила 36 (18-70) лет. Медиана наблюдения составила 23 (23-467) мес. Статус заболевания перед алло-ТГСК: ПР1 – 148 (76%) пациентов, ПР2 – 47 (24%) пациентов. Согласно молекулярно-генетической классификации к группе низкого риска относились 31 (17%) пациент, среднего риска – 119 (59%), высокого риска – 45 (24%) пациентов. МОБ не определялась (МОБ-) у 155 (80%) пациентов. Положительный результат МОБ (МОБ+) перед алло-ТГСК был у 40 (20%) человек, из них мутации t(8;21)(q22;q22); RUNX1-RUNX1T1 – 3 пациента, inv(16)(p13.1q22); CBFB-MYH11 – 2, t(15;17) (q22;q21); PML-RARа – 1, t(9;11)(p22;q23); MLLT3-KTM2A – 2, NPM1 – 2, FLT3-ITD – 4; гиперэкспрессия: WT1 – 8 , EVI1 – 1 пациент; МОБ(+) методом проточной цитометрии у 18 пациентов, медиана 0,4% (0,13-3,9).
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
При однофакторном анализе безрецидивная выживаемость (БРВ) после алло-ТГСК в ПР1 МОБ- составила 67% (95%ДИ 57-77), а при МОБ+ – 54% (95%ДИ 36-72) р=.03, тогда как у пациентов в ПР2 при МОБ- составила 57% (95%ДИ 41-73), и соответственно при МОБ(+) – 33% (95%ДИ 1-88) р=нд. Частота рецидивов (ЧР) в ПР1 МОБ- Д22%(95%ДИ 13-32), а при МОБ+ – 36%(95%ДИ 19-53), тогда как в ПР2 МОБ- 17% (95%ДИ 7-32), а при МОБ+ 66% (95%ДИ 15-91). При миелоаблативном кондиционировании БРВ и ЧР после алло-ТГСК в ПР1 не зависели от уровня МОБ: при МОБ- 70% (95%ДИ 59-81) и при МОБ+ 64% (95%ДИ 36-92) и соответственно 17% (95%ДИ 7-39) и 23% (95%ДИ 12-35). Тогда как при проведении кондиционирования редуцированной интенсивности, БРВ была выше, а ЧР ниже у пациентов МОБ-: 67% (95%ДИ 54-80) против 50% (95%ДИ 27-77) р=.03 и 50% (95%ДИ 25-70) и 23% (95%ДИ 12-35) р<.000. МОБ+ негативно влияла на БРВ и ЧР при использовании костного мозга в качестве трансплантата: МОБ- 76% (95%ДИ 57-87) по сравнению с МОБ+ 53% (95%ДИ 28-78) и 47% (95%ДИ 20-70) по сравнению с 24% (95%ДИ 8-44) р=.03,а при алло-ТГСК периферической крови разница БРВ и ЧР была не достоверна: 66% (95%ДИ 53-79) против 57% (95%ДИ 32-83) и 23% (95%ДИ 12-35) против 25% (95%ДИ 7-49). Цитогенетическая группа риска (средний и высокий) и донор (родственный и неродственный) не влияли на БРВ и ЧР: 74% (95%ДИ 61-87) против 63% (95%ДИ 39-85) и 47% (95%ДИ 22-72) против 38% (95%ДИ 5-71), 16% (95%ДИ 6-30) против 19% (95%ДИ 4-41) и 59% (95%ДИ 25-75) против 63% (95%ДИ 18-89); 68% (95%ДИ 56-80) против 57% (95%ДИ 46-78) и 65% (95%ДИ 45-84) против 42% (95%ДИ 5-79), 20% (95%ДИ 10-32) против 29% (95%ДИ 11-49) и 29% (95%ДИ 12-48) против 58% (95%ДИ 10-88). При отсутствии хронической РТПХ (хРТПХ) БРВ и ЧР были лучше у пациентов МОБ- 64% (95%ДИ 45-83) против 52% (95%ДИ 32-72) р=0.01 и 34% (95%ДИ 15-54) против 44% (95%ДИ 23-63) р=.03. У пациентов с хРТПХ разница в обеих группах была недостоверна: 70% (95%ДИ 57-83) против 80% (95%ДИ45-99) и 17% (95%ДИ 7-29) против 20% (95%ДИ1-62). При проведении многофакторного анализа влияние на ЧР оказал статус заболевания (МОБ+/МОБ-) (ОР, 2.3, 95%ДИ 1.1-4.9, р=.03) и наличие хРТПХ (да/нет) (ОР, 0.3, 95%ДИ 0.2-1.0, р=.05). БРВ была хуже при МОБ+ (ОР, 1.8, 95%ДИ 1.0-3.5, р=.05).
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Необходимо проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания для возможности мониторинга МОБ в ремиссии ОМЛ. При ОМЛ наличие МОБ негативно влияет на БРВ и ЧР после алло-ТГСК. Статус МОБ+ перед алло-ТГСК является показанием для интенсификации режима кондиционирования.
</p>
<h2 style="text-align: justify;">Комментарии</h2>
<p style="text-align: justify;">
Авторы заявляют об отсутствии скрытого конфликта интересов.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Острый миелоидный лейкоз, минимальная остаточная болезнь, аллогенная трансплантация гемопоэтических стволовых клеток.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) является эффективным методом лечения острого миелобластного лейкоза (ОМЛ). Развитие рецидива после алло-ТГСК является наиболее частой причиной неудач лечения. Однако, проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания дает возможность определения минимальной остаточной болезни (МОБ) в ремиссии (ПР) ОМЛ с целью определения прогноза и выбора адекватной терапии.
Цель работы
Оценить влияние наличия МОБ у пациентов ОМЛ перед алло-ТГСК на результаты лечения.
Пациенты и методы
В исследование включено 195 пациентов за период 2012-16 гг. Медиана возраста составила 36 (18-70) лет. Медиана наблюдения составила 23 (23-467) мес. Статус заболевания перед алло-ТГСК: ПР1 – 148 (76%) пациентов, ПР2 – 47 (24%) пациентов. Согласно молекулярно-генетической классификации к группе низкого риска относились 31 (17%) пациент, среднего риска – 119 (59%), высокого риска – 45 (24%) пациентов. МОБ не определялась (МОБ-) у 155 (80%) пациентов. Положительный результат МОБ (МОБ+) перед алло-ТГСК был у 40 (20%) человек, из них мутации t(8;21)(q22;q22); RUNX1-RUNX1T1 – 3 пациента, inv(16)(p13.1q22); CBFB-MYH11 – 2, t(15;17) (q22;q21); PML-RARа – 1, t(9;11)(p22;q23); MLLT3-KTM2A – 2, NPM1 – 2, FLT3-ITD – 4; гиперэкспрессия: WT1 – 8 , EVI1 – 1 пациент; МОБ(+) методом проточной цитометрии у 18 пациентов, медиана 0,4% (0,13-3,9).
Результаты
При однофакторном анализе безрецидивная выживаемость (БРВ) после алло-ТГСК в ПР1 МОБ- составила 67% (95%ДИ 57-77), а при МОБ+ – 54% (95%ДИ 36-72) р=.03, тогда как у пациентов в ПР2 при МОБ- составила 57% (95%ДИ 41-73), и соответственно при МОБ(+) – 33% (95%ДИ 1-88) р=нд. Частота рецидивов (ЧР) в ПР1 МОБ- Д22%(95%ДИ 13-32), а при МОБ+ – 36%(95%ДИ 19-53), тогда как в ПР2 МОБ- 17% (95%ДИ 7-32), а при МОБ+ 66% (95%ДИ 15-91). При миелоаблативном кондиционировании БРВ и ЧР после алло-ТГСК в ПР1 не зависели от уровня МОБ: при МОБ- 70% (95%ДИ 59-81) и при МОБ+ 64% (95%ДИ 36-92) и соответственно 17% (95%ДИ 7-39) и 23% (95%ДИ 12-35). Тогда как при проведении кондиционирования редуцированной интенсивности, БРВ была выше, а ЧР ниже у пациентов МОБ-: 67% (95%ДИ 54-80) против 50% (95%ДИ 27-77) р=.03 и 50% (95%ДИ 25-70) и 23% (95%ДИ 12-35) р<.000. МОБ+ негативно влияла на БРВ и ЧР при использовании костного мозга в качестве трансплантата: МОБ- 76% (95%ДИ 57-87) по сравнению с МОБ+ 53% (95%ДИ 28-78) и 47% (95%ДИ 20-70) по сравнению с 24% (95%ДИ 8-44) р=.03,а при алло-ТГСК периферической крови разница БРВ и ЧР была не достоверна: 66% (95%ДИ 53-79) против 57% (95%ДИ 32-83) и 23% (95%ДИ 12-35) против 25% (95%ДИ 7-49). Цитогенетическая группа риска (средний и высокий) и донор (родственный и неродственный) не влияли на БРВ и ЧР: 74% (95%ДИ 61-87) против 63% (95%ДИ 39-85) и 47% (95%ДИ 22-72) против 38% (95%ДИ 5-71), 16% (95%ДИ 6-30) против 19% (95%ДИ 4-41) и 59% (95%ДИ 25-75) против 63% (95%ДИ 18-89); 68% (95%ДИ 56-80) против 57% (95%ДИ 46-78) и 65% (95%ДИ 45-84) против 42% (95%ДИ 5-79), 20% (95%ДИ 10-32) против 29% (95%ДИ 11-49) и 29% (95%ДИ 12-48) против 58% (95%ДИ 10-88). При отсутствии хронической РТПХ (хРТПХ) БРВ и ЧР были лучше у пациентов МОБ- 64% (95%ДИ 45-83) против 52% (95%ДИ 32-72) р=0.01 и 34% (95%ДИ 15-54) против 44% (95%ДИ 23-63) р=.03. У пациентов с хРТПХ разница в обеих группах была недостоверна: 70% (95%ДИ 57-83) против 80% (95%ДИ45-99) и 17% (95%ДИ 7-29) против 20% (95%ДИ1-62). При проведении многофакторного анализа влияние на ЧР оказал статус заболевания (МОБ+/МОБ-) (ОР, 2.3, 95%ДИ 1.1-4.9, р=.03) и наличие хРТПХ (да/нет) (ОР, 0.3, 95%ДИ 0.2-1.0, р=.05). БРВ была хуже при МОБ+ (ОР, 1.8, 95%ДИ 1.0-3.5, р=.05).
Заключение
Необходимо проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания для возможности мониторинга МОБ в ремиссии ОМЛ. При ОМЛ наличие МОБ негативно влияет на БРВ и ЧР после алло-ТГСК. Статус МОБ+ перед алло-ТГСК является показанием для интенсификации режима кондиционирования.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
Ключевые слова
Острый миелоидный лейкоз, минимальная остаточная болезнь, аллогенная трансплантация гемопоэтических стволовых клеток.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20303
[VALUE] => Array
(
[TEXT] => Sergey N. Bondarenko <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Anna G. Smirnova <sup>1</sup>, Irina A. Samorodova <sup>1</sup>, Olga S. Uspenskaya <sup>2</sup>, Elena V. Babenko <sup>1</sup>, Ildar M. Barkhatov <sup>1</sup>, Tatyana L. Gindina <sup>1</sup>, Nikolay N. Mamaev <sup>1</sup>, Alexander D. Kulagin <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Sergey N. Bondarenko 1, Ivan S. Moiseev 1, Elena I. Darskaya 1, Anna G. Smirnova 1, Irina A. Samorodova 1, Olga S. Uspenskaya 2, Elena V. Babenko 1, Ildar M. Barkhatov 1, Tatyana L. Gindina 1, Nikolay N. Mamaev 1, Alexander D. Kulagin 1, Boris V. Afanasyev 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20304
[VALUE] => Array
(
[TEXT] => <sup>1</sup> R. M. Gorbacheva Memorial Institute of Oncology, Hematology and Transplantation, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation<br>
<sup>2</sup> Leningrad Regional Clinical Hospital, Hematology Department, St. Petersburg, Russian Federation<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 R. M. Gorbacheva Memorial Institute of Oncology, Hematology and Transplantation, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation
2 Leningrad Regional Clinical Hospital, Hematology Department, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20351
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is an effective therapy for many patients with acute myeloid leukemia (AML). The relapse after allo-HSCT is the most common cause of treatment failure. However, multiparameter flow cytometry, cytogenetic and molecular studies in the onset of the disease makes it possible to detect the minimal residual disease (MRD) in AML remission in order to determine the prognosis and the therapy strategy.
</p>
<h2 style="text-align: justify;">Aim</h2>
<p style="text-align: justify;">
To evaluate the impact of MRD before allo-HSCT in patients with AML on the results of treatment.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
We analysed 195 consecutive patients with AML since 2012 to 2016. Median age was 36 (18-70) years. The median follow-up was 23 (23-467) months. Disease status before allo-HSCT: CR1 – 148 (76%), CR2 – 47 (24%) patients. Molecular and genetic low-risk group was defined in 31(17%), standard risk in 119 (59%) and 45 (24%) high-risk patients. MRD was not determined (MRD (-)) in 155 (80%) patients. A positive result of MRD (MRD (+)) before alloHSCT was in 40 (20%) patients, including mutations, gene overexpression and leukemia associated immunophenotypes.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Disease-free survival (DFS) after alloHSCT in CR1MRD(-) was 67% (95%CI 57-77), and in MRD(+) 54% (95%CI 36-72) (p=.03), whereas in patients with CR2MRD(-) 57% (95%CI 41-73) and CR2MRD(+) – 33% (95%CI 1-88) (p=ns). The relapse incidence (RI) in the CR1MRD(-) was 22% (95%CI 13-32), and in MRD(+) – 36% (95%CI 19-53), whereas in the CR2MRD(-) 17% (95%CI 7-32), and in MRD(+) 66% (95%CI 15-91). With myeloablative conditioning (MAC), the DFS and RI after allo-HSCT in CR1 did not depended on MRD: patients with MRD(-) 70% (95%CI 59-81) vs MRD(+) 64% (95%CI 36-92) and 17% (95%CI 7-39) vs 23% (95%CI 12-35) respectively. Whereas after reduced intensity conditioning (RIC), the DFC was higher, and the RI was lower in patients with MRD(-): 67% (95%CI 54-80) vs 50% (95%CI 27-77) (p=.03) and 50% (95%CI 25-70) vs 23% (95%CI 12-35) (p <.000). The cytogenetic risk group (intermediate and high) and the donor type (related and unrelated) had no effect on DFS and RI: 74% vs 63% and 47% vs 38%, 16% vs 19% and 59% vs 63 %; 68% vs 57% and 65% vs 42%, 20% vs 29% and 29% vs 58%. In the absence of chronic graft-versus-host disease (cGVHD), DFS and RI were better in patients with MRD(-) 64% (95%CI 45-83) vs 52% (95%CI 32-72) (p = 0.01) and 34% (95%CI 15-54) vs 44% (95%CI 23-63)(p =.03). In patients with cGVHD, the difference was insignificant: 70% vs 80% and 17% vs 20%. In multivariate analysis, the impact on the RI has had the status of the disease (MRD(+)/MRD(-)) (HR2.3, 95%CI, 1.1-4.9, p=.03) and the presence of cGVHD(yes/no) (HR0.3, 95%CI, 0.2-1.0, =.05). DFS was lower with MRD(+) (HR1.8, 95%CI, 1.0-3.5, p =.05).
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Immunophenotypic, cytogenetic and molecular data in the onset of the disease is necessary for monitoring the MRD in AML remission. The presence of MRD has a negative effect on DFS and RI after allo-HSCT. MRD(+) status in front of the allo-HSCT is an indication for the intensification of the conditioning regimen.
</p>
<h2 style="text-align: justify;">Disclosure</h2>
<p style="text-align: justify;">
The authors report no conflicts of interest in this work.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Acute myeloid leukemia, minimal residual disease, allogeneic hematopoietic stem cell transplantation.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
Allogeneic hematopoietic stem cell transplantation (allo-HSCT) is an effective therapy for many patients with acute myeloid leukemia (AML). The relapse after allo-HSCT is the most common cause of treatment failure. However, multiparameter flow cytometry, cytogenetic and molecular studies in the onset of the disease makes it possible to detect the minimal residual disease (MRD) in AML remission in order to determine the prognosis and the therapy strategy.
Aim
To evaluate the impact of MRD before allo-HSCT in patients with AML on the results of treatment.
Patients and methods
We analysed 195 consecutive patients with AML since 2012 to 2016. Median age was 36 (18-70) years. The median follow-up was 23 (23-467) months. Disease status before allo-HSCT: CR1 – 148 (76%), CR2 – 47 (24%) patients. Molecular and genetic low-risk group was defined in 31(17%), standard risk in 119 (59%) and 45 (24%) high-risk patients. MRD was not determined (MRD (-)) in 155 (80%) patients. A positive result of MRD (MRD (+)) before alloHSCT was in 40 (20%) patients, including mutations, gene overexpression and leukemia associated immunophenotypes.
Results
Disease-free survival (DFS) after alloHSCT in CR1MRD(-) was 67% (95%CI 57-77), and in MRD(+) 54% (95%CI 36-72) (p=.03), whereas in patients with CR2MRD(-) 57% (95%CI 41-73) and CR2MRD(+) – 33% (95%CI 1-88) (p=ns). The relapse incidence (RI) in the CR1MRD(-) was 22% (95%CI 13-32), and in MRD(+) – 36% (95%CI 19-53), whereas in the CR2MRD(-) 17% (95%CI 7-32), and in MRD(+) 66% (95%CI 15-91). With myeloablative conditioning (MAC), the DFS and RI after allo-HSCT in CR1 did not depended on MRD: patients with MRD(-) 70% (95%CI 59-81) vs MRD(+) 64% (95%CI 36-92) and 17% (95%CI 7-39) vs 23% (95%CI 12-35) respectively. Whereas after reduced intensity conditioning (RIC), the DFC was higher, and the RI was lower in patients with MRD(-): 67% (95%CI 54-80) vs 50% (95%CI 27-77) (p=.03) and 50% (95%CI 25-70) vs 23% (95%CI 12-35) (p <.000). The cytogenetic risk group (intermediate and high) and the donor type (related and unrelated) had no effect on DFS and RI: 74% vs 63% and 47% vs 38%, 16% vs 19% and 59% vs 63 %; 68% vs 57% and 65% vs 42%, 20% vs 29% and 29% vs 58%. In the absence of chronic graft-versus-host disease (cGVHD), DFS and RI were better in patients with MRD(-) 64% (95%CI 45-83) vs 52% (95%CI 32-72) (p = 0.01) and 34% (95%CI 15-54) vs 44% (95%CI 23-63)(p =.03). In patients with cGVHD, the difference was insignificant: 70% vs 80% and 17% vs 20%. In multivariate analysis, the impact on the RI has had the status of the disease (MRD(+)/MRD(-)) (HR2.3, 95%CI, 1.1-4.9, p=.03) and the presence of cGVHD(yes/no) (HR0.3, 95%CI, 0.2-1.0, =.05). DFS was lower with MRD(+) (HR1.8, 95%CI, 1.0-3.5, p =.05).
Conclusion
Immunophenotypic, cytogenetic and molecular data in the onset of the disease is necessary for monitoring the MRD in AML remission. The presence of MRD has a negative effect on DFS and RI after allo-HSCT. MRD(+) status in front of the allo-HSCT is an indication for the intensification of the conditioning regimen.
Disclosure
The authors report no conflicts of interest in this work.
Keywords
Acute myeloid leukemia, minimal residual disease, allogeneic hematopoietic stem cell transplantation.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20305
[VALUE] => Significance of minimal residual disease before allogeneic hematopoietic cell transplantation for acute myeloid leukemia
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Significance of minimal residual disease before allogeneic hematopoietic cell transplantation for acute myeloid leukemia
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20739
[VALUE] => 1375
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1375
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20740
[VALUE] => 1376
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1376
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Сергей Н. Бондаренко 1, Иван С. Моисеев 1, Елена И. Дарская 1, Анна Г. Смирнова 1, Ирина А. Самородова 1, Ольга С. Успенская 2, Елена В. Бабенко 1, Ильдар М. Бархатов 1, Татьяна Л. Гиндина 1, Николай Н. Мамаев 1, Александр Д. Кулагин 1, Борис В. Афанасьев 1
2 Ленинградская областная клиническая больница, Санкт-Петербург
Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) является эффективным методом лечения острого миелобластного лейкоза (ОМЛ). Развитие рецидива после алло-ТГСК является наиболее частой причиной неудач лечения. Однако, проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания дает возможность определения минимальной остаточной болезни (МОБ) в ремиссии (ПР) ОМЛ с целью определения прогноза и выбора адекватной терапии.
Цель работы
Оценить влияние наличия МОБ у пациентов ОМЛ перед алло-ТГСК на результаты лечения.
Пациенты и методы
В исследование включено 195 пациентов за период 2012-16 гг. Медиана возраста составила 36 (18-70) лет. Медиана наблюдения составила 23 (23-467) мес. Статус заболевания перед алло-ТГСК: ПР1 – 148 (76%) пациентов, ПР2 – 47 (24%) пациентов. Согласно молекулярно-генетической классификации к группе низкого риска относились 31 (17%) пациент, среднего риска – 119 (59%), высокого риска – 45 (24%) пациентов. МОБ не определялась (МОБ-) у 155 (80%) пациентов. Положительный результат МОБ (МОБ+) перед алло-ТГСК был у 40 (20%) человек, из них мутации t(8;21)(q22;q22); RUNX1-RUNX1T1 – 3 пациента, inv(16)(p13.1q22); CBFB-MYH11 – 2, t(15;17) (q22;q21); PML-RARа – 1, t(9;11)(p22;q23); MLLT3-KTM2A – 2, NPM1 – 2, FLT3-ITD – 4; гиперэкспрессия: WT1 – 8 , EVI1 – 1 пациент; МОБ(+) методом проточной цитометрии у 18 пациентов, медиана 0,4% (0,13-3,9).
Результаты
При однофакторном анализе безрецидивная выживаемость (БРВ) после алло-ТГСК в ПР1 МОБ- составила 67% (95%ДИ 57-77), а при МОБ+ – 54% (95%ДИ 36-72) р=.03, тогда как у пациентов в ПР2 при МОБ- составила 57% (95%ДИ 41-73), и соответственно при МОБ(+) – 33% (95%ДИ 1-88) р=нд. Частота рецидивов (ЧР) в ПР1 МОБ- Д22%(95%ДИ 13-32), а при МОБ+ – 36%(95%ДИ 19-53), тогда как в ПР2 МОБ- 17% (95%ДИ 7-32), а при МОБ+ 66% (95%ДИ 15-91). При миелоаблативном кондиционировании БРВ и ЧР после алло-ТГСК в ПР1 не зависели от уровня МОБ: при МОБ- 70% (95%ДИ 59-81) и при МОБ+ 64% (95%ДИ 36-92) и соответственно 17% (95%ДИ 7-39) и 23% (95%ДИ 12-35). Тогда как при проведении кондиционирования редуцированной интенсивности, БРВ была выше, а ЧР ниже у пациентов МОБ-: 67% (95%ДИ 54-80) против 50% (95%ДИ 27-77) р=.03 и 50% (95%ДИ 25-70) и 23% (95%ДИ 12-35) р<.000. МОБ+ негативно влияла на БРВ и ЧР при использовании костного мозга в качестве трансплантата: МОБ- 76% (95%ДИ 57-87) по сравнению с МОБ+ 53% (95%ДИ 28-78) и 47% (95%ДИ 20-70) по сравнению с 24% (95%ДИ 8-44) р=.03,а при алло-ТГСК периферической крови разница БРВ и ЧР была не достоверна: 66% (95%ДИ 53-79) против 57% (95%ДИ 32-83) и 23% (95%ДИ 12-35) против 25% (95%ДИ 7-49). Цитогенетическая группа риска (средний и высокий) и донор (родственный и неродственный) не влияли на БРВ и ЧР: 74% (95%ДИ 61-87) против 63% (95%ДИ 39-85) и 47% (95%ДИ 22-72) против 38% (95%ДИ 5-71), 16% (95%ДИ 6-30) против 19% (95%ДИ 4-41) и 59% (95%ДИ 25-75) против 63% (95%ДИ 18-89); 68% (95%ДИ 56-80) против 57% (95%ДИ 46-78) и 65% (95%ДИ 45-84) против 42% (95%ДИ 5-79), 20% (95%ДИ 10-32) против 29% (95%ДИ 11-49) и 29% (95%ДИ 12-48) против 58% (95%ДИ 10-88). При отсутствии хронической РТПХ (хРТПХ) БРВ и ЧР были лучше у пациентов МОБ- 64% (95%ДИ 45-83) против 52% (95%ДИ 32-72) р=0.01 и 34% (95%ДИ 15-54) против 44% (95%ДИ 23-63) р=.03. У пациентов с хРТПХ разница в обеих группах была недостоверна: 70% (95%ДИ 57-83) против 80% (95%ДИ45-99) и 17% (95%ДИ 7-29) против 20% (95%ДИ1-62). При проведении многофакторного анализа влияние на ЧР оказал статус заболевания (МОБ+/МОБ-) (ОР, 2.3, 95%ДИ 1.1-4.9, р=.03) и наличие хРТПХ (да/нет) (ОР, 0.3, 95%ДИ 0.2-1.0, р=.05). БРВ была хуже при МОБ+ (ОР, 1.8, 95%ДИ 1.0-3.5, р=.05).
Заключение
Необходимо проведение иммунофенотипического, цитогенетического и молекулярно-биологического исследований в дебюте заболевания для возможности мониторинга МОБ в ремиссии ОМЛ. При ОМЛ наличие МОБ негативно влияет на БРВ и ЧР после алло-ТГСК. Статус МОБ+ перед алло-ТГСК является показанием для интенсификации режима кондиционирования.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
Ключевые слова
Острый миелоидный лейкоз, минимальная остаточная болезнь, аллогенная трансплантация гемопоэтических стволовых клеток.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20309
[VALUE] => Array
(
[TEXT] => Сергей Н. Бондаренко <sup>1</sup>, Елена Н. Паровичникова <sup>2</sup>, Алексей А. Масчан <sup>3</sup>, Ольга Ю. Баранова <sup>4</sup>, Татьяна В. Шелехова <sup>5</sup>, Вадим А. Доронин <sup>6</sup>, Владимир Я. Мельниченко <sup>7</sup>, Камиль Д. Капланов <sup>8</sup>, Ольга С. Успенская <sup>9</sup>, Андрей Н. Соколов <sup>2</sup>, Наталья В. Мякова <sup>3</sup>, Иван С. Моисеев <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Анна Г. Смирнова <sup>1</sup>, Татьяна А. Быкова <sup>1</sup>, Белла И. Аюбова <sup>1</sup>, Ирина А. Самородова <sup>1</sup>, Елена В. Бабенко <sup>1</sup>, Ильдар М. Бархатов <sup>1</sup>, Татьяна Л. Гиндина <sup>1</sup>, Александр Д. Кулагин <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>
[TYPE] => TEXT
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Сергей Н. Бондаренко 1, Елена Н. Паровичникова 2, Алексей А. Масчан 3, Ольга Ю. Баранова 4, Татьяна В. Шелехова 5, Вадим А. Доронин 6, Владимир Я. Мельниченко 7, Камиль Д. Капланов 8, Ольга С. Успенская 9, Андрей Н. Соколов 2, Наталья В. Мякова 3, Иван С. Моисеев 1, Елена И. Дарская 1, Анна Г. Смирнова 1, Татьяна А. Быкова 1, Белла И. Аюбова 1, Ирина А. Самородова 1, Елена В. Бабенко 1, Ильдар М. Бархатов 1, Татьяна Л. Гиндина 1, Александр Д. Кулагин 1, Борис В. Афанасьев 1
[TYPE] => TEXT
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20310
[VALUE] => Array
(
[TEXT] => <sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург<br>
<sup>2</sup> Национальный медицинский исследовательский центр гематологии, Москва<br>
<sup>3</sup> Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Д. Рогачева, Москва<br>
<sup>4</sup> Национальный медицинский исследовательский центр онкологии им. Н. Н. Блохина, Москва<br>
<sup>5</sup> Саратовский государственный медицинский университет им. В. И. Разумовского<br>
<sup>6</sup> Городская клиническая больница №40 г. Москва<br>
<sup>7</sup> Национальный медико-хирургический центр им. Н. И. Пирогова, Москва<br>
<sup>8</sup> Волгоградский областной клинический онкологический диспансер<br>
<sup>9</sup> Ленинградская областная клиническая больница, Санкт-Петербург<br>
[TYPE] => TEXT
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург
2 Национальный медицинский исследовательский центр гематологии, Москва
3 Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Д. Рогачева, Москва
4 Национальный медицинский исследовательский центр онкологии им. Н. Н. Блохина, Москва
5 Саратовский государственный медицинский университет им. В. И. Разумовского
6 Городская клиническая больница №40 г. Москва
7 Национальный медико-хирургический центр им. Н. И. Пирогова, Москва
8 Волгоградский областной клинический онкологический диспансер
9 Ленинградская областная клиническая больница, Санкт-Петербург
[TYPE] => TEXT
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20348
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Результаты терапии пациентов с положительной минимальной остаточной болезнью (МОБ+), рецидивами и рефрактерным течением острого В-лимфобластного лейкоза (Р/РОЛЛ), особенно после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), остаются неудовлетворительными. Возможности химиотерапии (ХТ) исчерпаны, что обуславливает необходимость использования новых методов терапии. Блинатумомаб (Б) является генно-инженерным антителом, активатором Т-клеток, биспецифичным по отношению к CD19 и CD3. Б помогает преодолеть резистентность к ХТ и может использоваться как до, так и после ТГСК за счет низкой токсичности.
</p>
<h2 style="text-align: justify;">Цель работы</h2>
<p style="text-align: justify;">
Оценить эффективность и безопасность Б при МОБ+ и Р/РОЛЛ.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
В исследование включено 59 больных из 10 гематологических центров РФ с CD19+ОЛЛ. Медиана возраста составила 28 (18-62) лет. К B-I варианту относились 15 пациентов, B-II – 37, B-III – 18, и 1 больной имел ОЛ со смешанный фенотипом (В/миело). В рецидиве (Р) находилось 35 больных, из них 4 в комбинированном (костный мозг (КМ) и экстрамедуллярное поражение (ЭМ)) (РI – 14 , РII – 14 и РIII – 7), первично-рефрактерных – 2 и МОБ+ – 22. Число бластов КМ <50% выявлялось у 18 пациентов, а >50% у 19. Медиана уровня МОБ составила 0,35 (0,01-7,0)%. Б получили до ТГСК 42(71%) пациента, после ТГСК 17(29%). ТГСК (род-5, нерод-10, гапло-3, ауто-2) проведена после терапии Б 20 (34%) пациентам, из них 3 – повторная алло-ТГСК. У 9 больных после алло-ТГСК Б использовался в сочетании с инфузией донорских лимфоцитов (ИДЛ). Общее количество курсов Б составило от 1 до 7 (медиана 2).
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
В группе МОБ+ негативный статус получен у 20 (91%) больных. Полная ремиссия (ПР) достигнута у 25 (68%)(в том числе 18 (72%) из них МОБ-): 13 (57%) пациентов при Р/РОЛЛ после ХТ, 12(86%) после алло-ТГСК. Частота достижения ПР была выше в группе больных с числом бластов <50% (78%(14/18) против 58%(11/19)). После терапии Б у 3 пациентов отмечалась ЭМ прогрессия ОЛЛ. РОЛЛ возник у 16(36%) больных: МОБ+ – 1, КМ – 11, ЭМ – 3, комбинированный – 1. В группах МОБ+ и Р/РОЛЛ 2хлетняя безрецидивная выживаемость (2БРВ) составили 62% (95%CI 35-89%) и 28%( 95%CI 6-50%), соответственно. В группах МОБ+ и Р/РОЛЛ 2хлетняя частота рецидивов (2ЧР) составили 38% (95%CI 4-60%) и 53% (95%CI 25-74%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии Б 2БРВ и 2ЧР составили 59% (95%CI 24-85%) против 30% (95%CI 7-53%) р=.08 и 27% (95%CI 7-52%) против 61% (95%CI 30-81%) р=.06, соответственно. Токсичность: гематологическая ≥3 степени (нейтропения, тромбоцитопения) наблюдалась у 15 (25%) больных, печеночная ≥3 степени – у 5(8%), неврологическая – у 11 (19%), синдром «высвобождения цитокин» наблюдался у 4 (7%). У 54 (92%) пациентов токсические явления были обратимы, и только у 5 (8%) больных терапия была прекращена досрочно. Только у 1 пациента после Б в сочетании с ИДЛ развилась оРТПХ (кожа 3 степени).
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Б в лечении МОБ+ и Р/РОЛЛ показал высокую эффективность и приемлемую токсичность. Частота достижения ПР выше при лечении Б Р/РОЛЛ после алло-ТГСК.
</p>
<h2 style="text-align: justify;">Комментарии</h2>
<p style="text-align: justify;">
Авторы заявляют об отсутствии скрытого конфликта интересов.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Острый лимфобластный лейкоз, таргетная терапия, блинатумомаб.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Результаты терапии пациентов с положительной минимальной остаточной болезнью (МОБ+), рецидивами и рефрактерным течением острого В-лимфобластного лейкоза (Р/РОЛЛ), особенно после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), остаются неудовлетворительными. Возможности химиотерапии (ХТ) исчерпаны, что обуславливает необходимость использования новых методов терапии. Блинатумомаб (Б) является генно-инженерным антителом, активатором Т-клеток, биспецифичным по отношению к CD19 и CD3. Б помогает преодолеть резистентность к ХТ и может использоваться как до, так и после ТГСК за счет низкой токсичности.
Цель работы
Оценить эффективность и безопасность Б при МОБ+ и Р/РОЛЛ.
Пациенты и методы
В исследование включено 59 больных из 10 гематологических центров РФ с CD19+ОЛЛ. Медиана возраста составила 28 (18-62) лет. К B-I варианту относились 15 пациентов, B-II – 37, B-III – 18, и 1 больной имел ОЛ со смешанный фенотипом (В/миело). В рецидиве (Р) находилось 35 больных, из них 4 в комбинированном (костный мозг (КМ) и экстрамедуллярное поражение (ЭМ)) (РI – 14 , РII – 14 и РIII – 7), первично-рефрактерных – 2 и МОБ+ – 22. Число бластов КМ <50% выявлялось у 18 пациентов, а >50% у 19. Медиана уровня МОБ составила 0,35 (0,01-7,0)%. Б получили до ТГСК 42(71%) пациента, после ТГСК 17(29%). ТГСК (род-5, нерод-10, гапло-3, ауто-2) проведена после терапии Б 20 (34%) пациентам, из них 3 – повторная алло-ТГСК. У 9 больных после алло-ТГСК Б использовался в сочетании с инфузией донорских лимфоцитов (ИДЛ). Общее количество курсов Б составило от 1 до 7 (медиана 2).
Результаты
В группе МОБ+ негативный статус получен у 20 (91%) больных. Полная ремиссия (ПР) достигнута у 25 (68%)(в том числе 18 (72%) из них МОБ-): 13 (57%) пациентов при Р/РОЛЛ после ХТ, 12(86%) после алло-ТГСК. Частота достижения ПР была выше в группе больных с числом бластов <50% (78%(14/18) против 58%(11/19)). После терапии Б у 3 пациентов отмечалась ЭМ прогрессия ОЛЛ. РОЛЛ возник у 16(36%) больных: МОБ+ – 1, КМ – 11, ЭМ – 3, комбинированный – 1. В группах МОБ+ и Р/РОЛЛ 2хлетняя безрецидивная выживаемость (2БРВ) составили 62% (95%CI 35-89%) и 28%( 95%CI 6-50%), соответственно. В группах МОБ+ и Р/РОЛЛ 2хлетняя частота рецидивов (2ЧР) составили 38% (95%CI 4-60%) и 53% (95%CI 25-74%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии Б 2БРВ и 2ЧР составили 59% (95%CI 24-85%) против 30% (95%CI 7-53%) р=.08 и 27% (95%CI 7-52%) против 61% (95%CI 30-81%) р=.06, соответственно. Токсичность: гематологическая ≥3 степени (нейтропения, тромбоцитопения) наблюдалась у 15 (25%) больных, печеночная ≥3 степени – у 5(8%), неврологическая – у 11 (19%), синдром «высвобождения цитокин» наблюдался у 4 (7%). У 54 (92%) пациентов токсические явления были обратимы, и только у 5 (8%) больных терапия была прекращена досрочно. Только у 1 пациента после Б в сочетании с ИДЛ развилась оРТПХ (кожа 3 степени).
Заключение
Б в лечении МОБ+ и Р/РОЛЛ показал высокую эффективность и приемлемую токсичность. Частота достижения ПР выше при лечении Б Р/РОЛЛ после алло-ТГСК.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
Ключевые слова
Острый лимфобластный лейкоз, таргетная терапия, блинатумомаб.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20311
[VALUE] => Array
(
[TEXT] => Sergey N. Bondarenko <sup>1</sup>, Elena N. Parovichnikova <sup>2</sup>, Alexey A. Maschan <sup>3</sup>, Olga Y. Baranova <sup>4</sup>, Tatyana V. Shelehova <sup>5</sup>, Vadim A. Doronin <sup>6</sup>, Vladimir Ya. Melnichenko <sup>7</sup>, Kamil D. Kaplanov <sup>8</sup>, Olga S. Uspenskaya <sup>9</sup>, Andrej N. Sokolov <sup>2</sup>, Natalya V. Myakova <sup>3</sup>, Ivan S. Moiseev <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Anna G. Smirnova <sup>1</sup>, Tatiana A. Bykova <sup>1</sup>, Bella I. Ayubova <sup>1</sup>, Irina A. Samorodova <sup>1</sup>, Elena V. Babenko <sup>1</sup>, Ildar M. Barkhatov <sup>1</sup>, Tatyana L. Gindina <sup>1</sup>, Alexander D. Kulagin <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>
[TYPE] => TEXT
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Sergey N. Bondarenko 1, Elena N. Parovichnikova 2, Alexey A. Maschan 3, Olga Y. Baranova 4, Tatyana V. Shelehova 5, Vadim A. Doronin 6, Vladimir Ya. Melnichenko 7, Kamil D. Kaplanov 8, Olga S. Uspenskaya 9, Andrej N. Sokolov 2, Natalya V. Myakova 3, Ivan S. Moiseev 1, Elena I. Darskaya 1, Anna G. Smirnova 1, Tatiana A. Bykova 1, Bella I. Ayubova 1, Irina A. Samorodova 1, Elena V. Babenko 1, Ildar M. Barkhatov 1, Tatyana L. Gindina 1, Alexander D. Kulagin 1, Boris V. Afanasyev 1
[TYPE] => TEXT
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20312
[VALUE] => Array
(
[TEXT] => <sup>1</sup> Raisa Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, St. Petersburg First I. Pavlov State Medical University, St. Petersburg, Russian Federation<br>
<sup>2</sup> National Research Center for Hematology, Russian Ministry of Healthcare, Moscow, Russian Federation<br>
<sup>3</sup> National Medical D. Rogachev Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation;<br>
<sup>4</sup> National Medical NN Blokhin Research Center of Oncology, Moscow, Russian Federation<br>
<sup>5</sup> Saratov State Medical VI Razumovsky University<br>
<sup>6 </sup>City Clinical Hospital №40, Moscow, Russian Federation<br>
<sup>7</sup> National NI Pirogov Medical and Surgical Center, Moscow, Russian Federation<br>
<sup>8</sup> Regional Clinical Oncology Center, Volgograd, Russian Federation<br>
<sup>9</sup> Leningrad Regional Clinical Hospital, St. Petersburg, Russian Federation<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Raisa Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, St. Petersburg First I. Pavlov State Medical University, St. Petersburg, Russian Federation
2 National Research Center for Hematology, Russian Ministry of Healthcare, Moscow, Russian Federation
3 National Medical D. Rogachev Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation;
4 National Medical NN Blokhin Research Center of Oncology, Moscow, Russian Federation
5 Saratov State Medical VI Razumovsky University
6 City Clinical Hospital №40, Moscow, Russian Federation
7 National NI Pirogov Medical and Surgical Center, Moscow, Russian Federation
8 Regional Clinical Oncology Center, Volgograd, Russian Federation
9 Leningrad Regional Clinical Hospital, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20349
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
The results of therapy of patients with positive minimal residual disease (MRD+), relapses and refractory acute B-lymphoblastic leukemia (R/R ALL), especially after allogeneic hematopoietic stem cell transplantation (allo-HSCT), remain very poor. The possibilities of chemotherapy (CT) have been exhausted, new therapies is necessary. Blinatumomab (Btm) is a bispecific T-cell engager antibody construct with dual specificity for CD19 and CD3. Therapy with Btm may help to overcome the resistance to chemotherapy (CT) with minimal toxicity, and may be used both before and after HSCT because of low toxicity. Aim was to evaluate the efficacy and safety of Btm in MRD+ and R/R ALL. Patients and methods The study included 59 pts from 10 Russian hematological centers with CD19+ ALL. The median age was 28 (18-62) years. The diagnosis was ALL B-I (EGIL) subtype in 15 pts, B-II, in 37 cases; B-III, in 18 patients, and 1 patient had AL with a mixed phenotype (B/myelo). There were 35 pts in the relapse, 4 of them, with combined lesions bone marrow, i.e., bone marrow (BM) and extramedullary (EM) (RI-14, RII- 14 and RIII-7); primary-refractory disease was documented in 2 cases, and MRD+ was found in 22 pts. The number of BM blasts <50% was detected in 18 pts, and > 50%, in 19 cases. The median MRD level was 0.35 (0.01-7.0)%. Btm was administered to 42 pts (71%) before HSCT, and to 17 patients (29%) after HSCT. The HSCT (related-5, unrelated-10, haplo-3, auto-2) was performed after Btm therapy in 20 pts (34%), 3 of them underwent second allo-HSCT. In 9 pts after allo-HSCT, Btm was used in combination with donor lymphocyte infusion (DLI). The total number of Btm courses was 1 to 7 (median 2). Results In the MRD+ group, negative molecular status was obtained in 20 pts (91%). Complete remission (CR) was achieved in 25 cases (68%) including 18 MRD-negative cases (72%): 13(57%) pts with R/R ALL after CT, 12 (86%), after alloHSCT. Incidence of CR was higher in the group of pts with blasts <50% [78% (14/18) versus 58% (11/19)]. After Btm therapy, 3 pts experienced EM progression of ALL. Relapses developed in 16 pts (36%): MRD+, in 1; BM, in 11; EM, in 3; combined, in one case. In the MRD+ and R/R ALL groups, the 2-year disease-free survival rates (2DFS) were 62% (95% CI 35-89%) versus 28% (95% CI 6-50%), respectively. In MRD + and R/R ALL groups, the 2-year relapse rate (2RR) was 38% (95% CI 4-60%), and 53% (95% CI 25-74%), respectively. Depending on alloHSCT or no transplant after Btm therapy, the 2DFS and 2RR were 59% (95% CI 24-85%) versus 30% (95% CI 7-53%, p=.08), and 27% (95% CI 7-52%) versus 61% (95% CI 30-81%, p=.06), respectively. Hematological toxicity: grade 3 (neutropenia, thrombocytopenia) was observed in 15 pts (25%), hepatic toxicity grade ≥3 was documented in 5 pts (8%); neurotoxicity manifested in 11 pts (19%); the “cytokine release” syndrome was observed in 4 pts (7%). The toxic events in 54 pts (92%) were reversible, and only 5(8%) pts were terminated their treatment prematurely. Only 1 patient after B in combination with the DLI developed aGVHD (skin, grade 3).
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Btm treatment in MRD+ and R/R ALL showed high efficacy and acceptable toxicity. Frequency of CR achievement is higher in Btm treatment for R/R ALL after allo-HSCT.
</p>
<h2 style="text-align: justify;">Disclosure</h2>
<p style="text-align: justify;">
The authors report no conflicts of interest in this work.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Acute lymphoblastic leukemia, target therapy, blinatumomab.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
The results of therapy of patients with positive minimal residual disease (MRD+), relapses and refractory acute B-lymphoblastic leukemia (R/R ALL), especially after allogeneic hematopoietic stem cell transplantation (allo-HSCT), remain very poor. The possibilities of chemotherapy (CT) have been exhausted, new therapies is necessary. Blinatumomab (Btm) is a bispecific T-cell engager antibody construct with dual specificity for CD19 and CD3. Therapy with Btm may help to overcome the resistance to chemotherapy (CT) with minimal toxicity, and may be used both before and after HSCT because of low toxicity. Aim was to evaluate the efficacy and safety of Btm in MRD+ and R/R ALL. Patients and methods The study included 59 pts from 10 Russian hematological centers with CD19+ ALL. The median age was 28 (18-62) years. The diagnosis was ALL B-I (EGIL) subtype in 15 pts, B-II, in 37 cases; B-III, in 18 patients, and 1 patient had AL with a mixed phenotype (B/myelo). There were 35 pts in the relapse, 4 of them, with combined lesions bone marrow, i.e., bone marrow (BM) and extramedullary (EM) (RI-14, RII- 14 and RIII-7); primary-refractory disease was documented in 2 cases, and MRD+ was found in 22 pts. The number of BM blasts <50% was detected in 18 pts, and > 50%, in 19 cases. The median MRD level was 0.35 (0.01-7.0)%. Btm was administered to 42 pts (71%) before HSCT, and to 17 patients (29%) after HSCT. The HSCT (related-5, unrelated-10, haplo-3, auto-2) was performed after Btm therapy in 20 pts (34%), 3 of them underwent second allo-HSCT. In 9 pts after allo-HSCT, Btm was used in combination with donor lymphocyte infusion (DLI). The total number of Btm courses was 1 to 7 (median 2). Results In the MRD+ group, negative molecular status was obtained in 20 pts (91%). Complete remission (CR) was achieved in 25 cases (68%) including 18 MRD-negative cases (72%): 13(57%) pts with R/R ALL after CT, 12 (86%), after alloHSCT. Incidence of CR was higher in the group of pts with blasts <50% [78% (14/18) versus 58% (11/19)]. After Btm therapy, 3 pts experienced EM progression of ALL. Relapses developed in 16 pts (36%): MRD+, in 1; BM, in 11; EM, in 3; combined, in one case. In the MRD+ and R/R ALL groups, the 2-year disease-free survival rates (2DFS) were 62% (95% CI 35-89%) versus 28% (95% CI 6-50%), respectively. In MRD + and R/R ALL groups, the 2-year relapse rate (2RR) was 38% (95% CI 4-60%), and 53% (95% CI 25-74%), respectively. Depending on alloHSCT or no transplant after Btm therapy, the 2DFS and 2RR were 59% (95% CI 24-85%) versus 30% (95% CI 7-53%, p=.08), and 27% (95% CI 7-52%) versus 61% (95% CI 30-81%, p=.06), respectively. Hematological toxicity: grade 3 (neutropenia, thrombocytopenia) was observed in 15 pts (25%), hepatic toxicity grade ≥3 was documented in 5 pts (8%); neurotoxicity manifested in 11 pts (19%); the “cytokine release” syndrome was observed in 4 pts (7%). The toxic events in 54 pts (92%) were reversible, and only 5(8%) pts were terminated their treatment prematurely. Only 1 patient after B in combination with the DLI developed aGVHD (skin, grade 3).
Conclusion
Btm treatment in MRD+ and R/R ALL showed high efficacy and acceptable toxicity. Frequency of CR achievement is higher in Btm treatment for R/R ALL after allo-HSCT.
Disclosure
The authors report no conflicts of interest in this work.
Keywords
Acute lymphoblastic leukemia, target therapy, blinatumomab.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20313
[VALUE] => Efficacy and toxicity of blinatumomab in acute B-lymphoblastic leukemia
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Efficacy and toxicity of blinatumomab in acute B-lymphoblastic leukemia
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20741
[VALUE] => 1377
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1377
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20742
[VALUE] => 1378
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1378
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Сергей Н. Бондаренко 1, Елена Н. Паровичникова 2, Алексей А. Масчан 3, Ольга Ю. Баранова 4, Татьяна В. Шелехова 5, Вадим А. Доронин 6, Владимир Я. Мельниченко 7, Камиль Д. Капланов 8, Ольга С. Успенская 9, Андрей Н. Соколов 2, Наталья В. Мякова 3, Иван С. Моисеев 1, Елена И. Дарская 1, Анна Г. Смирнова 1, Татьяна А. Быкова 1, Белла И. Аюбова 1, Ирина А. Самородова 1, Елена В. Бабенко 1, Ильдар М. Бархатов 1, Татьяна Л. Гиндина 1, Александр Д. Кулагин 1, Борис В. Афанасьев 1
2 Национальный медицинский исследовательский центр гематологии, Москва
3 Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии им. Д. Рогачева, Москва
4 Национальный медицинский исследовательский центр онкологии им. Н. Н. Блохина, Москва
5 Саратовский государственный медицинский университет им. В. И. Разумовского
6 Городская клиническая больница №40 г. Москва
7 Национальный медико-хирургический центр им. Н. И. Пирогова, Москва
8 Волгоградский областной клинический онкологический диспансер
9 Ленинградская областная клиническая больница, Санкт-Петербург
Введение
Результаты терапии пациентов с положительной минимальной остаточной болезнью (МОБ+), рецидивами и рефрактерным течением острого В-лимфобластного лейкоза (Р/РОЛЛ), особенно после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), остаются неудовлетворительными. Возможности химиотерапии (ХТ) исчерпаны, что обуславливает необходимость использования новых методов терапии. Блинатумомаб (Б) является генно-инженерным антителом, активатором Т-клеток, биспецифичным по отношению к CD19 и CD3. Б помогает преодолеть резистентность к ХТ и может использоваться как до, так и после ТГСК за счет низкой токсичности.
Цель работы
Оценить эффективность и безопасность Б при МОБ+ и Р/РОЛЛ.
Пациенты и методы
В исследование включено 59 больных из 10 гематологических центров РФ с CD19+ОЛЛ. Медиана возраста составила 28 (18-62) лет. К B-I варианту относились 15 пациентов, B-II – 37, B-III – 18, и 1 больной имел ОЛ со смешанный фенотипом (В/миело). В рецидиве (Р) находилось 35 больных, из них 4 в комбинированном (костный мозг (КМ) и экстрамедуллярное поражение (ЭМ)) (РI – 14 , РII – 14 и РIII – 7), первично-рефрактерных – 2 и МОБ+ – 22. Число бластов КМ <50% выявлялось у 18 пациентов, а >50% у 19. Медиана уровня МОБ составила 0,35 (0,01-7,0)%. Б получили до ТГСК 42(71%) пациента, после ТГСК 17(29%). ТГСК (род-5, нерод-10, гапло-3, ауто-2) проведена после терапии Б 20 (34%) пациентам, из них 3 – повторная алло-ТГСК. У 9 больных после алло-ТГСК Б использовался в сочетании с инфузией донорских лимфоцитов (ИДЛ). Общее количество курсов Б составило от 1 до 7 (медиана 2).
Результаты
В группе МОБ+ негативный статус получен у 20 (91%) больных. Полная ремиссия (ПР) достигнута у 25 (68%)(в том числе 18 (72%) из них МОБ-): 13 (57%) пациентов при Р/РОЛЛ после ХТ, 12(86%) после алло-ТГСК. Частота достижения ПР была выше в группе больных с числом бластов <50% (78%(14/18) против 58%(11/19)). После терапии Б у 3 пациентов отмечалась ЭМ прогрессия ОЛЛ. РОЛЛ возник у 16(36%) больных: МОБ+ – 1, КМ – 11, ЭМ – 3, комбинированный – 1. В группах МОБ+ и Р/РОЛЛ 2хлетняя безрецидивная выживаемость (2БРВ) составили 62% (95%CI 35-89%) и 28%( 95%CI 6-50%), соответственно. В группах МОБ+ и Р/РОЛЛ 2хлетняя частота рецидивов (2ЧР) составили 38% (95%CI 4-60%) и 53% (95%CI 25-74%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии Б 2БРВ и 2ЧР составили 59% (95%CI 24-85%) против 30% (95%CI 7-53%) р=.08 и 27% (95%CI 7-52%) против 61% (95%CI 30-81%) р=.06, соответственно. Токсичность: гематологическая ≥3 степени (нейтропения, тромбоцитопения) наблюдалась у 15 (25%) больных, печеночная ≥3 степени – у 5(8%), неврологическая – у 11 (19%), синдром «высвобождения цитокин» наблюдался у 4 (7%). У 54 (92%) пациентов токсические явления были обратимы, и только у 5 (8%) больных терапия была прекращена досрочно. Только у 1 пациента после Б в сочетании с ИДЛ развилась оРТПХ (кожа 3 степени).
Заключение
Б в лечении МОБ+ и Р/РОЛЛ показал высокую эффективность и приемлемую токсичность. Частота достижения ПР выше при лечении Б Р/РОЛЛ после алло-ТГСК.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
Ключевые слова
Острый лимфобластный лейкоз, таргетная терапия, блинатумомаб.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20293
[VALUE] => Array
(
[TEXT] => Татьяна Н. Беловежец <sup>1</sup>,<sup>2</sup>, Андрей А. Горчаков <sup>1</sup>,<sup>2</sup>, Сергей В. Кулемзин <sup>1</sup>, Антон Н. Чикаев <sup>1</sup>, Ольга А. Коваль <sup>1</sup>,<sup>3</sup>, Елена В. Кулигина <sup>2</sup>, Александр В. Таранин <sup>1</sup>,<sup>2</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Татьяна Н. Беловежец 1,2, Андрей А. Горчаков 1,2, Сергей В. Кулемзин 1, Антон Н. Чикаев 1, Ольга А. Коваль 1,3, Елена В. Кулигина 2, Александр В. Таранин 1,2
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20294
[VALUE] => Array
(
[TEXT] => <sup>1</sup> Институт молекулярной и клеточной биологии СО РАН, Новосибирск, Россия<br>
<sup>2</sup> Новосибирский государственный университет, Новосибирск, Россия<br>
<sup>3</sup> Институт химической биологии и фундаментальной медицины СО РАН, Новосибирск, Россия<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Институт молекулярной и клеточной биологии СО РАН, Новосибирск, Россия
2 Новосибирский государственный университет, Новосибирск, Россия
3 Институт химической биологии и фундаментальной медицины СО РАН, Новосибирск, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20352
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Терапия Т-клетками, экспрессирующими химерные антигенные рецепторы (CAR), была одобрена FDA к клиническому использованию в августе 2017 года для больных с r/rALL. Несмотря на значительную эффективность, у CAR T-клеточной терапии существуют серьезные ограничения, связанные с высокой стоимостью, сложной стандартизацией и невозможностью получить CAR Т-клетки для отдельных пациентов. В связи с этим крайне привлекательным выглядит создание универсальных аллогенных CAR T-клеток, однако на существующем уровне развития инструментов геномного редактирования и селекции субпопуляций Т-клеток этот подход сопровождается риском развития реакции «трансплантат против хозяина». Возможным решением этих проблем может быть переход к иммортализованным NK-клеточным линиям в качестве носителей CAR. Подобные линии недорогие в наработке, могут быть стандартизованы и не вызывают реакцию «трансплантат против хозяина». К настоящему моменту описано несколько NK-клеточных линий человека, однако систематического сравнения их свойств в качестве носителей CAR проведено не было.
</p>
<h2 style="text-align: justify;">Методы</h2>
<p style="text-align: justify;">
В данное исследование были включены три NK-клеточные иммортализованные линии человека (А, В и NK-92). На основе каждой из трех линий методом лентивирусной трансдукции были получены сублинии, стабильно экспрессирующие CAR, специфичный к белку человека CD20. После этого был измерен уровень цитотоксичности CAR-NK клеточных линий по отношению к CD20-положительным клеткам линии Raji (клетки лимфомы Бёркитта) и клеткам линии HEK293Т, эктопически экспрессирующим CD20, либо изогенным контрольным клеткам.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Все три полученные CAR-NK-клеточные линии обнаруживали значимый уровень цитотоксичности против клеток линии Raji, однако клетки NK-92 дикого типа также лизировали мишени Raji. В связи с этим, для более корректного сравнения уровней цитотоксичности CAR-NK-клеточных линий в тестах <i>in vitro</i> были получены клетки линии HEK293Т, экспрессирующие CD20. Уровень неспецифической цитотоксичности немодифицированных NK клеток против таких мишеней не превышал 20% в диапазоне эффектор: мишень=1-5, при этом уровень специфической, CAR-опосредованной цитотоксичности составлял 73% (CAR-NK-92), 55% (CAR-B) и 34% (CAR-A) при соотношении эффектор:-мишень=5.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Все полученные CAR-NK-клеточные линии проявляют значимый уровень цитотоксичности по отношению к CD20-позитивным клеткам-мишеням в тестах <i>in vitro</i>, и клетки линии NK-92 проявляют самый высокий уровень как специфической, так и неспецифической цитотоксичности. Необходимы дополнительные исследования <i>in vivo</i>, чтобы определить профили безопасности и эффективности CAR-NK эффекторов.
</p>
<h2 style="text-align: justify;">Благодарности</h2>
<p style="text-align: justify;">
Работа выполнена при финансовой поддержке Минобрнауки РФ, соглашение № 14.604.21.0169 (уникальный идентификатор проекта RFMEFI60417X0169).
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Химерный антигенный рецептор, NK-клеточные линии, цитотоксичность.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Терапия Т-клетками, экспрессирующими химерные антигенные рецепторы (CAR), была одобрена FDA к клиническому использованию в августе 2017 года для больных с r/rALL. Несмотря на значительную эффективность, у CAR T-клеточной терапии существуют серьезные ограничения, связанные с высокой стоимостью, сложной стандартизацией и невозможностью получить CAR Т-клетки для отдельных пациентов. В связи с этим крайне привлекательным выглядит создание универсальных аллогенных CAR T-клеток, однако на существующем уровне развития инструментов геномного редактирования и селекции субпопуляций Т-клеток этот подход сопровождается риском развития реакции «трансплантат против хозяина». Возможным решением этих проблем может быть переход к иммортализованным NK-клеточным линиям в качестве носителей CAR. Подобные линии недорогие в наработке, могут быть стандартизованы и не вызывают реакцию «трансплантат против хозяина». К настоящему моменту описано несколько NK-клеточных линий человека, однако систематического сравнения их свойств в качестве носителей CAR проведено не было.
Методы
В данное исследование были включены три NK-клеточные иммортализованные линии человека (А, В и NK-92). На основе каждой из трех линий методом лентивирусной трансдукции были получены сублинии, стабильно экспрессирующие CAR, специфичный к белку человека CD20. После этого был измерен уровень цитотоксичности CAR-NK клеточных линий по отношению к CD20-положительным клеткам линии Raji (клетки лимфомы Бёркитта) и клеткам линии HEK293Т, эктопически экспрессирующим CD20, либо изогенным контрольным клеткам.
Результаты
Все три полученные CAR-NK-клеточные линии обнаруживали значимый уровень цитотоксичности против клеток линии Raji, однако клетки NK-92 дикого типа также лизировали мишени Raji. В связи с этим, для более корректного сравнения уровней цитотоксичности CAR-NK-клеточных линий в тестах in vitro были получены клетки линии HEK293Т, экспрессирующие CD20. Уровень неспецифической цитотоксичности немодифицированных NK клеток против таких мишеней не превышал 20% в диапазоне эффектор: мишень=1-5, при этом уровень специфической, CAR-опосредованной цитотоксичности составлял 73% (CAR-NK-92), 55% (CAR-B) и 34% (CAR-A) при соотношении эффектор:-мишень=5.
Заключение
Все полученные CAR-NK-клеточные линии проявляют значимый уровень цитотоксичности по отношению к CD20-позитивным клеткам-мишеням в тестах in vitro, и клетки линии NK-92 проявляют самый высокий уровень как специфической, так и неспецифической цитотоксичности. Необходимы дополнительные исследования in vivo, чтобы определить профили безопасности и эффективности CAR-NK эффекторов.
Благодарности
Работа выполнена при финансовой поддержке Минобрнауки РФ, соглашение № 14.604.21.0169 (уникальный идентификатор проекта RFMEFI60417X0169).
Ключевые слова
Химерный антигенный рецептор, NK-клеточные линии, цитотоксичность.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20295
[VALUE] => Array
(
[TEXT] => Tatyana N. Belovezhets <sup>1</sup>,<sup>2</sup>, Andrey A. Gorchakov <sup>1</sup>,<sup>2</sup>, Sergey V. Kulemzin <sup>1</sup>, Anton N. Chikaev <sup>1</sup>, Olga A. Koval <sup>1</sup>,<sup>3</sup>, Elena V. Kuligina <sup>3</sup>, Aleksander V. Taranin <sup>1</sup>,<sup>2</sup>
[TYPE] => TEXT
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Tatyana N. Belovezhets 1,2, Andrey A. Gorchakov 1,2, Sergey V. Kulemzin 1, Anton N. Chikaev 1, Olga A. Koval 1,3, Elena V. Kuligina 3, Aleksander V. Taranin 1,2
[TYPE] => TEXT
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20296
[VALUE] => Array
(
[TEXT] => <sup>1</sup> Institute of Molecular and Cellular Biology SB RAS, Novosibirsk, Russia<br>
<sup>2</sup> Novosibirsk State University, Novosibirsk, Russia<br>
<sup>3</sup> Institute of Chemical Biology and Fundamental Medicine SB RAS, Novosibirsk, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Institute of Molecular and Cellular Biology SB RAS, Novosibirsk, Russia
2 Novosibirsk State University, Novosibirsk, Russia
3 Institute of Chemical Biology and Fundamental Medicine SB RAS, Novosibirsk, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20353
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
CAR T cell therapy received regulatory approval for treatment of pediatric r/rALL patients in August, 2017. Despite impressive efficacy, widespread use of CAR T cell therapy is limited by prohibitively high costs, complex standardization procedures, as well as by inherent difficulties to produce CAR T cell products for certain groups of patients. Moving CAR T cell therapy from autologous to allogeneic format appears highly attractive, yet challenging, as current techniques of cell sorting and genome engineering may do not entirely eliminate the risk of GvHD. Choosing immortalized human NK-cell lines over T cells as CAR carriers offers a possible solution to this problem. Such cell lines are inexpensive to maintain, they do not cause GvHD, and are straightforward to standardize. Several human NK-cell lines have been described to date, however no side-by-side comparisons of activity of such cells engineered to express CARs have been performed.
</p>
<h2 style="text-align: justify;">Methods</h2>
<p style="text-align: justify;">
In this study, three immortalized human NK-cell line backgrounds (A, B, and NK-92) were used to establish sublines expressing a CD20-specific CAR. In vitro cytotoxicity assays of parental and CAR-expressing cells against CD20-positive Burkitt lymphoma target cells (Raji) were performed. Alternative target cells (HEK293T(CD20+)) and non-target isogenic controls (HEK293T) were also included into cytotoxicity tests.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
All the three CAR-NK cell lines obtained displayed pronounced cytotoxicity against Raji target cells, however this cell line was also highly sensitive to killing by unmodified parental NK-92 cells. Thus, in order to perform side-by-side comparisons of CAR-NK cell activity in vitro, we established HEK293T cells overexpressing CD20, as the target cell line. The level of non-specific cytotoxicity of parental NK-cell lines against HEK293T(CD20+) cells was below 20% across the E:T ratios ranging from 1 to 5, whereas specific CAR-mediated cytotoxicity at E:T=5 constituted 73% (CAR-NK-92), 55% (CAR-B), and 34% (CAR-A).
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
All the CAR-NK cell lines obtained in this study display significant cell killing activity towards target cells in vitro, with NK-92 cell line showing the highest level of both specific and non-specific cytotoxicity. Further studies in vivo are needed to explore the safety and efficacy profiles of CAR-NK cell lines.
</p>
<h2 style="text-align: justify;">Acknowledgements</h2>
<p style="text-align: justify;">
This work was supported by the Ministry of Education and Science of the Russian Federation, grant agreement № 14.604.21.0169 (unique project identifier RFMEFI60417X0169).
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Chimeric antigen receptors, NK-cell lines, cytotoxicity.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
CAR T cell therapy received regulatory approval for treatment of pediatric r/rALL patients in August, 2017. Despite impressive efficacy, widespread use of CAR T cell therapy is limited by prohibitively high costs, complex standardization procedures, as well as by inherent difficulties to produce CAR T cell products for certain groups of patients. Moving CAR T cell therapy from autologous to allogeneic format appears highly attractive, yet challenging, as current techniques of cell sorting and genome engineering may do not entirely eliminate the risk of GvHD. Choosing immortalized human NK-cell lines over T cells as CAR carriers offers a possible solution to this problem. Such cell lines are inexpensive to maintain, they do not cause GvHD, and are straightforward to standardize. Several human NK-cell lines have been described to date, however no side-by-side comparisons of activity of such cells engineered to express CARs have been performed.
Methods
In this study, three immortalized human NK-cell line backgrounds (A, B, and NK-92) were used to establish sublines expressing a CD20-specific CAR. In vitro cytotoxicity assays of parental and CAR-expressing cells against CD20-positive Burkitt lymphoma target cells (Raji) were performed. Alternative target cells (HEK293T(CD20+)) and non-target isogenic controls (HEK293T) were also included into cytotoxicity tests.
Results
All the three CAR-NK cell lines obtained displayed pronounced cytotoxicity against Raji target cells, however this cell line was also highly sensitive to killing by unmodified parental NK-92 cells. Thus, in order to perform side-by-side comparisons of CAR-NK cell activity in vitro, we established HEK293T cells overexpressing CD20, as the target cell line. The level of non-specific cytotoxicity of parental NK-cell lines against HEK293T(CD20+) cells was below 20% across the E:T ratios ranging from 1 to 5, whereas specific CAR-mediated cytotoxicity at E:T=5 constituted 73% (CAR-NK-92), 55% (CAR-B), and 34% (CAR-A).
Conclusion
All the CAR-NK cell lines obtained in this study display significant cell killing activity towards target cells in vitro, with NK-92 cell line showing the highest level of both specific and non-specific cytotoxicity. Further studies in vivo are needed to explore the safety and efficacy profiles of CAR-NK cell lines.
Acknowledgements
This work was supported by the Ministry of Education and Science of the Russian Federation, grant agreement № 14.604.21.0169 (unique project identifier RFMEFI60417X0169).
Keywords
Chimeric antigen receptors, NK-cell lines, cytotoxicity.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20297
[VALUE] => Comparative in vitro analysis of human NK-cell lines expressing chimeric antigen receptors
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Comparative in vitro analysis of human NK-cell lines expressing chimeric antigen receptors
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20737
[VALUE] => 1373
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1373
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20738
[VALUE] => 1374
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1374
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Татьяна Н. Беловежец 1,2, Андрей А. Горчаков 1,2, Сергей В. Кулемзин 1, Антон Н. Чикаев 1, Ольга А. Коваль 1,3, Елена В. Кулигина 2, Александр В. Таранин 1,2
2 Новосибирский государственный университет, Новосибирск, Россия
3 Институт химической биологии и фундаментальной медицины СО РАН, Новосибирск, Россия
Введение
Терапия Т-клетками, экспрессирующими химерные антигенные рецепторы (CAR), была одобрена FDA к клиническому использованию в августе 2017 года для больных с r/rALL. Несмотря на значительную эффективность, у CAR T-клеточной терапии существуют серьезные ограничения, связанные с высокой стоимостью, сложной стандартизацией и невозможностью получить CAR Т-клетки для отдельных пациентов. В связи с этим крайне привлекательным выглядит создание универсальных аллогенных CAR T-клеток, однако на существующем уровне развития инструментов геномного редактирования и селекции субпопуляций Т-клеток этот подход сопровождается риском развития реакции «трансплантат против хозяина». Возможным решением этих проблем может быть переход к иммортализованным NK-клеточным линиям в качестве носителей CAR. Подобные линии недорогие в наработке, могут быть стандартизованы и не вызывают реакцию «трансплантат против хозяина». К настоящему моменту описано несколько NK-клеточных линий человека, однако систематического сравнения их свойств в качестве носителей CAR проведено не было.
Методы
В данное исследование были включены три NK-клеточные иммортализованные линии человека (А, В и NK-92). На основе каждой из трех линий методом лентивирусной трансдукции были получены сублинии, стабильно экспрессирующие CAR, специфичный к белку человека CD20. После этого был измерен уровень цитотоксичности CAR-NK клеточных линий по отношению к CD20-положительным клеткам линии Raji (клетки лимфомы Бёркитта) и клеткам линии HEK293Т, эктопически экспрессирующим CD20, либо изогенным контрольным клеткам.
Результаты
Все три полученные CAR-NK-клеточные линии обнаруживали значимый уровень цитотоксичности против клеток линии Raji, однако клетки NK-92 дикого типа также лизировали мишени Raji. В связи с этим, для более корректного сравнения уровней цитотоксичности CAR-NK-клеточных линий в тестах in vitro были получены клетки линии HEK293Т, экспрессирующие CD20. Уровень неспецифической цитотоксичности немодифицированных NK клеток против таких мишеней не превышал 20% в диапазоне эффектор: мишень=1-5, при этом уровень специфической, CAR-опосредованной цитотоксичности составлял 73% (CAR-NK-92), 55% (CAR-B) и 34% (CAR-A) при соотношении эффектор:-мишень=5.
Заключение
Все полученные CAR-NK-клеточные линии проявляют значимый уровень цитотоксичности по отношению к CD20-позитивным клеткам-мишеням в тестах in vitro, и клетки линии NK-92 проявляют самый высокий уровень как специфической, так и неспецифической цитотоксичности. Необходимы дополнительные исследования in vivo, чтобы определить профили безопасности и эффективности CAR-NK эффекторов.
Благодарности
Работа выполнена при финансовой поддержке Минобрнауки РФ, соглашение № 14.604.21.0169 (уникальный идентификатор проекта RFMEFI60417X0169).
Ключевые слова
Химерный антигенный рецептор, NK-клеточные линии, цитотоксичность.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20285
[VALUE] => Array
(
[TEXT] => Мария В. Барабанщикова, Иван С. Моисеев, Елена В. Морозова, Юлия Ю. Власова, Вадим В. Байков, Ильдар М. Бархатов, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Мария В. Барабанщикова, Иван С. Моисеев, Елена В. Морозова, Юлия Ю. Власова, Вадим В. Байков, Ильдар М. Бархатов, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20286
[VALUE] => Array
(
[TEXT] => Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20342
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Миелофиброз относится к хроническим BCR-ABL-негативным миелопролиферативным неоплазиям и сопровождается, как правило, непрерывно прогрессирующим течением. Аллогенная трансплантация гемопоэтических стволовых клеток в настоящее время является единственным методом терапии, позволяющим добиться излечения от заболевания. Применение ингибитора JAK1/JAK2 руксолитиниба во многом позволяет изменить статус заболевания на момент алло-ТГСК – уменьшить спленомегалию, конституциональные симптомы, улучшить гематологические показатели, в ряде случаев привести к регрессу фиброза в костном мозге. В то же время руксолитиниб обладает иммуномодулирующим эффектом, благодаря чему широко используется для лечения острой и хронической РТПХ. В нашем исследовании мы использовали руксолитиниб в комбинации с посттрансплантационным циклофосфаном в качестве профилактики РТПХ и рецидива заболевания.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
Мы проанализировали результаты алло-ТГСК у 20 пациентов в возрасте от 32 до 61 лет (медиана 51 год). У 14 пациентов был диагностирован первичный миелофиброз, у 2 пациентов – посттромбоцитемический миелофиброз, у 4 пациентов – постполицитемический миелофиброз. Одиннадцать пациентов относились к промежуточному-2 риску по шкале DIPSSplus, восемь – к высокой группе риска. Одному пациенту алло-ТГСК была выполнена в фазе бластного криза. У пятнадцати пациентов отмечалась мутация <i>JAK2V617F</i>, у двух – мутация в гене <i>MPL</i>, у трех – мутация в гене <i>CALR</i>. Все пациенты получали терапию руксолитинибом в качестве предтрансплантационной подготовки, медиана длительности терапии составила 6 месяцев (3-22) в дозе 30-45 мг. У восьми пациентов отмечалось клиническое улучшение, у 1 – прогрессирование заболевания, у 11 – стабилизации заболевания на момент алло-ТГСК. У семи пациентов была выполнена спленэктомия в связи с выраженной спленомегалией и недостаточным ответом со стороны селезенки. Во всех случаях применялся режим кондиционирования со сниженной интенсивностью доз (флударабин 180 мг/м<sup>2</sup>, бусульфан 10 мг/кг). Троим пациентам алло-ТГСК была выполнена от HLA-совместимого (10/10) родственного (3) и неродственного (10) донора, от частично-совместимого (9/10) неродственного донора (2) и гаплоидентичного (5) донора. В качестве профилактики РТПХ использовался циклофосфамид 100 мг/кг в день +3, +4 и руксолитиниб 5-7,5 мг х 2 раза в сутки с дня +5 по день +50(2) и день +100(18). Медиана количества CD34+-клеток составила 6,7x10<sup>6</sup> (1,4-12,0). Исследование зарегистрировано на clinicaltrials.gov, NCT02806375.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Приживление трансплантата было зарегистрировано у 18 больных. Медиана времени до приживления по лейкоцитам составила 32 дня (18-61), по тромбоцитам – 38 дней (15-219). Повторная алло-ТГСК была выполнена в одном случае в связи с первичным неприживлением. Однако пациент погиб из-за инфекционных осложнений во время цитопении. Тяжелая гипофункция трансплантата наблюдалась у 11 пациентов. Гипофункция разрешилась самостоятельно у семи больных в течение 79 дней (16-470), в остальных случаях было выполнено введение CD34+ клеток (3). Трое из 4 пациентов погибли до приживления: 1 – сепсис <i>Pseudomonas aeruginosa</i>, 1 – желудочно-кишечное кровотечение, 1 –первичное неприживление и сепсис. Одна пациентка погибла в результате тромботической микроангиопатии (ТМА) на Д+115. Острая РТПХ 2-4 степени отмечалась у 29% пациентов, острая РТПХ3-4 степени – 18%. Во всех случаях, кроме одного, острая РТПХ 3-4 степени разрешилась на фоне терапии ингибиторами кальциневрина. Один пациент получал терапию системными глюкокортикостероидами. Хроническая РТПХ средней степени тяжести наблюдалась у 29% пациентов. Переносимость режима кондиционирования и протокол профилактики была удовлетворительная. Токсичность 3-4 степени, в частности токсический гепатит и сепсис, отмечались у 4 и 5 пациентов соответственно. Веноокклюзионная болезнь средней степени тяжести наблюдалась у 1 пациента, ТМА – 1. Реактивация цитомегаловируса отмечалась у 6 пациентов, EBV – 1, HHV 1 и 2 типа – 1, HHV 6 типа – 2, ВК вируса – 1, геморрагический цистит – 2. Двухлетлетняя общая выживаемость составила 80%. Все пациенты достигли молекулярной, клинико-гематологической ремиссии, полного донорского химеризма. Практически полный регресс фиброза в костном мозге зарегистрирован зарегистрирован у 12 пациентов. Ни в одном случае не отмечалось развитие рецидива заболевания. Трансплантационная летальность составила 15% и 20% через 100 дней и 1 год после алло-ТГСК соответственно.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Алло-ТГСК является эффективной терапевтической опцией для пациентов с миелофиброзом. Применение в посттрансплантационном периоде циклофосфамида в комбинации с руксолитинибом представляется эффективной терапевтической опцией в качестве профилактики РТПХ и рецидива заболевания.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Миелофиброз, аллогенная трансплантация гемопоэтических стволовых клеток, руксолитиниб, реакция «трансплантат против хозяина», профилактика, циклофосфамид.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Миелофиброз относится к хроническим BCR-ABL-негативным миелопролиферативным неоплазиям и сопровождается, как правило, непрерывно прогрессирующим течением. Аллогенная трансплантация гемопоэтических стволовых клеток в настоящее время является единственным методом терапии, позволяющим добиться излечения от заболевания. Применение ингибитора JAK1/JAK2 руксолитиниба во многом позволяет изменить статус заболевания на момент алло-ТГСК – уменьшить спленомегалию, конституциональные симптомы, улучшить гематологические показатели, в ряде случаев привести к регрессу фиброза в костном мозге. В то же время руксолитиниб обладает иммуномодулирующим эффектом, благодаря чему широко используется для лечения острой и хронической РТПХ. В нашем исследовании мы использовали руксолитиниб в комбинации с посттрансплантационным циклофосфаном в качестве профилактики РТПХ и рецидива заболевания.
Материалы и методы
Мы проанализировали результаты алло-ТГСК у 20 пациентов в возрасте от 32 до 61 лет (медиана 51 год). У 14 пациентов был диагностирован первичный миелофиброз, у 2 пациентов – посттромбоцитемический миелофиброз, у 4 пациентов – постполицитемический миелофиброз. Одиннадцать пациентов относились к промежуточному-2 риску по шкале DIPSSplus, восемь – к высокой группе риска. Одному пациенту алло-ТГСК была выполнена в фазе бластного криза. У пятнадцати пациентов отмечалась мутация JAK2V617F, у двух – мутация в гене MPL, у трех – мутация в гене CALR. Все пациенты получали терапию руксолитинибом в качестве предтрансплантационной подготовки, медиана длительности терапии составила 6 месяцев (3-22) в дозе 30-45 мг. У восьми пациентов отмечалось клиническое улучшение, у 1 – прогрессирование заболевания, у 11 – стабилизации заболевания на момент алло-ТГСК. У семи пациентов была выполнена спленэктомия в связи с выраженной спленомегалией и недостаточным ответом со стороны селезенки. Во всех случаях применялся режим кондиционирования со сниженной интенсивностью доз (флударабин 180 мг/м2, бусульфан 10 мг/кг). Троим пациентам алло-ТГСК была выполнена от HLA-совместимого (10/10) родственного (3) и неродственного (10) донора, от частично-совместимого (9/10) неродственного донора (2) и гаплоидентичного (5) донора. В качестве профилактики РТПХ использовался циклофосфамид 100 мг/кг в день +3, +4 и руксолитиниб 5-7,5 мг х 2 раза в сутки с дня +5 по день +50(2) и день +100(18). Медиана количества CD34+-клеток составила 6,7x106 (1,4-12,0). Исследование зарегистрировано на clinicaltrials.gov, NCT02806375.
Результаты
Приживление трансплантата было зарегистрировано у 18 больных. Медиана времени до приживления по лейкоцитам составила 32 дня (18-61), по тромбоцитам – 38 дней (15-219). Повторная алло-ТГСК была выполнена в одном случае в связи с первичным неприживлением. Однако пациент погиб из-за инфекционных осложнений во время цитопении. Тяжелая гипофункция трансплантата наблюдалась у 11 пациентов. Гипофункция разрешилась самостоятельно у семи больных в течение 79 дней (16-470), в остальных случаях было выполнено введение CD34+ клеток (3). Трое из 4 пациентов погибли до приживления: 1 – сепсис Pseudomonas aeruginosa, 1 – желудочно-кишечное кровотечение, 1 –первичное неприживление и сепсис. Одна пациентка погибла в результате тромботической микроангиопатии (ТМА) на Д+115. Острая РТПХ 2-4 степени отмечалась у 29% пациентов, острая РТПХ3-4 степени – 18%. Во всех случаях, кроме одного, острая РТПХ 3-4 степени разрешилась на фоне терапии ингибиторами кальциневрина. Один пациент получал терапию системными глюкокортикостероидами. Хроническая РТПХ средней степени тяжести наблюдалась у 29% пациентов. Переносимость режима кондиционирования и протокол профилактики была удовлетворительная. Токсичность 3-4 степени, в частности токсический гепатит и сепсис, отмечались у 4 и 5 пациентов соответственно. Веноокклюзионная болезнь средней степени тяжести наблюдалась у 1 пациента, ТМА – 1. Реактивация цитомегаловируса отмечалась у 6 пациентов, EBV – 1, HHV 1 и 2 типа – 1, HHV 6 типа – 2, ВК вируса – 1, геморрагический цистит – 2. Двухлетлетняя общая выживаемость составила 80%. Все пациенты достигли молекулярной, клинико-гематологической ремиссии, полного донорского химеризма. Практически полный регресс фиброза в костном мозге зарегистрирован зарегистрирован у 12 пациентов. Ни в одном случае не отмечалось развитие рецидива заболевания. Трансплантационная летальность составила 15% и 20% через 100 дней и 1 год после алло-ТГСК соответственно.
Заключение
Алло-ТГСК является эффективной терапевтической опцией для пациентов с миелофиброзом. Применение в посттрансплантационном периоде циклофосфамида в комбинации с руксолитинибом представляется эффективной терапевтической опцией в качестве профилактики РТПХ и рецидива заболевания.
Ключевые слова
Миелофиброз, аллогенная трансплантация гемопоэтических стволовых клеток, руксолитиниб, реакция «трансплантат против хозяина», профилактика, циклофосфамид.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20287
[VALUE] => Array
(
[TEXT] => Maria V. Barabanshikova, Ivan S. Moiseev, Elena V. Morozova, Julia J. Vlasova, Vadim V. Baykov, Ildar M. Barkhatov, Boris V. Afanasyev
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Maria V. Barabanshikova, Ivan S. Moiseev, Elena V. Morozova, Julia J. Vlasova, Vadim V. Baykov, Ildar M. Barkhatov, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20288
[VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Institute of Children’s Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Institute of Children’s Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20343
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Allogeneic stem cell transplantation (allo-HSCT) is currently the only treatment modality with curative potential in patients with myelofibrosis (MF), although transplant-associated complications and relapses significantly reduce the application of this method. JAK1/JAK2 inhibitor ruxolitinib is effective in reducing symptomatic splenomegaly and myelofibrosis-related symptoms. At the same time it has significant immunomodulatory effect, and is used for the treatment of steroid-refractory acute and chronic graft-versus-host disease (GVHD). This study evaluated calcineurin inhibitor-free GVHD prophylaxis regimen with ruxolitinib in combination with posttransplant cyclophosphamide (PTCy).
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
Twenty patients at a median age of 51 (32-61) years were enrolled in the study. Two patients were diagnosed with post-essential thrombocythemia myelofibrosis, 4, with postpolycythemia vera myelofibrosis; 14, with primary myelofibrosis. By the DIPSSplus scale, 11 patients had intermediate-2, 8 patients had high-risk disease and 1 patient was transplanted in blast crisis. Fifteen patients were positive for <i>JAK2V617F</i>; 3 were <i>CALR</i>-positive; and 2 were <i>MPL</i>-positive before alloHSCT. All patients were treated with JAK1/2 inhibitors before alloHSCT, with median treatment duration of 6 months (3-22) at a dose of 30-45 mg. The disease stabilization occurred in 11 patients; clinical improvement, in 8, and the disease progression was observed in 1 case. Splenectomy was performed in 7 patients, due to poor spleen response. Reduced-intensity conditioning (fludarabine 180 mg/m2 plus busulfan 8-10 mg/kg) followed by allo-HSCT performed from full-matched related (n=3) or unrelated donor (n=10), and mismatched HSCT (HLA 9/10) from unrelated (n=2) or haploidentical donor (n=5). Graft-versus-host disease (GVHD) prophylaxis consisted of posttransplant cyclophosphamide 100 mg/kg at day +3, +4 and ruxolitinib 5-7.5 mg bid from day+5 to day +50 (n=2), and day +100 (n=18). G-CSF-mobilized peripheral blood progenitor cells (n=19) and bone marrow (n=1) were used as stem cell sources. Median number of CD34+cells/kg was 6.7x10<sup>6</sup> (1.4-12.0). The trial is registered on clinicaltrials.gov, NCT02806375.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Median follow-up time was 18 (6.6–36.1) months. Primary engraftment was documented in 18 patients. Median time to leukocyte engraftment was 32 days (18-61), to platelet engraftment, 38 days (15-219). One patient received second transplantation from the same donor due to primary graft failure. He died in cytopenia accomplished by sepsis. Severe poor graft function was documented in 11 patients. In 7 of these cases, it resolved spontaneously with a median duration of 79 days (16-470). Three patients recovered after CD34+ boost administration. Dose reduction of ruxolitinib to 10 mg/day due to poor graft function was performed in 8 patients. Three out of four deaths occurred before engraftment: one patient was lost due to <i>Pseudomonas aeruginosa </i><i>sepsis</i>, one death was associated with gastrointestinal bleeding, and one patient deceased due to primary graft failure and sepsis. One patient died due to thrombotic microangiopathy and sepsis on D+115. Twenty-nine percent of patients developed acute GVHD (grade 2-4), 18%, aGVHD grade 3-4. In all cases except of one, aGVHD grade 3-4 was successfully treated with calcineurin inhibitors. One patient required systemic steroid therapy. Moderate chronic GVHD (NIH) was documented in 29% of patients. The regimen was well tolerated. Grade 3-4 toxicities included only toxic hepatitis in 4 and sepsis in 5 patients. Mild veno-occlusive disease was observed in one patient, TMA, in one case. Viral reactivation was documented in 47% of patients, CMV (n=6), EBV (n=1), HHV type 1,2 (n=1), HHV type 6 (n=2), BK virus (n=1). Moderate hemorrhagic cystitis developed in 2 patients. Non-relapse mortality on D+100 was 15% and 20%, at 1 year. The two-year overall survival was 80%. All the patients achieved hematological, molecular remission and full donor chimerism. Near-complete resolution of bone marrow fibrosis was documented in 12 patients. No molecular or hematological relapses were registered.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
AlloHSCT is an effective treatment modality for myelofibrosis. GVHD prophylaxis using a combination of PTCy and ruxolitinib is associated with good acute and chronic GVHD control, and it seems to be a promising modality, at least for MF patients.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Myelofibrosis, allogeneic hematopoietic stem cell transplantation, ruxolitinib, graft-versus-host disease, prophylaxis, cyclophosphamide.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
Allogeneic stem cell transplantation (allo-HSCT) is currently the only treatment modality with curative potential in patients with myelofibrosis (MF), although transplant-associated complications and relapses significantly reduce the application of this method. JAK1/JAK2 inhibitor ruxolitinib is effective in reducing symptomatic splenomegaly and myelofibrosis-related symptoms. At the same time it has significant immunomodulatory effect, and is used for the treatment of steroid-refractory acute and chronic graft-versus-host disease (GVHD). This study evaluated calcineurin inhibitor-free GVHD prophylaxis regimen with ruxolitinib in combination with posttransplant cyclophosphamide (PTCy).
Patients and methods
Twenty patients at a median age of 51 (32-61) years were enrolled in the study. Two patients were diagnosed with post-essential thrombocythemia myelofibrosis, 4, with postpolycythemia vera myelofibrosis; 14, with primary myelofibrosis. By the DIPSSplus scale, 11 patients had intermediate-2, 8 patients had high-risk disease and 1 patient was transplanted in blast crisis. Fifteen patients were positive for JAK2V617F; 3 were CALR-positive; and 2 were MPL-positive before alloHSCT. All patients were treated with JAK1/2 inhibitors before alloHSCT, with median treatment duration of 6 months (3-22) at a dose of 30-45 mg. The disease stabilization occurred in 11 patients; clinical improvement, in 8, and the disease progression was observed in 1 case. Splenectomy was performed in 7 patients, due to poor spleen response. Reduced-intensity conditioning (fludarabine 180 mg/m2 plus busulfan 8-10 mg/kg) followed by allo-HSCT performed from full-matched related (n=3) or unrelated donor (n=10), and mismatched HSCT (HLA 9/10) from unrelated (n=2) or haploidentical donor (n=5). Graft-versus-host disease (GVHD) prophylaxis consisted of posttransplant cyclophosphamide 100 mg/kg at day +3, +4 and ruxolitinib 5-7.5 mg bid from day+5 to day +50 (n=2), and day +100 (n=18). G-CSF-mobilized peripheral blood progenitor cells (n=19) and bone marrow (n=1) were used as stem cell sources. Median number of CD34+cells/kg was 6.7x106 (1.4-12.0). The trial is registered on clinicaltrials.gov, NCT02806375.
Results
Median follow-up time was 18 (6.6–36.1) months. Primary engraftment was documented in 18 patients. Median time to leukocyte engraftment was 32 days (18-61), to platelet engraftment, 38 days (15-219). One patient received second transplantation from the same donor due to primary graft failure. He died in cytopenia accomplished by sepsis. Severe poor graft function was documented in 11 patients. In 7 of these cases, it resolved spontaneously with a median duration of 79 days (16-470). Three patients recovered after CD34+ boost administration. Dose reduction of ruxolitinib to 10 mg/day due to poor graft function was performed in 8 patients. Three out of four deaths occurred before engraftment: one patient was lost due to Pseudomonas aeruginosa sepsis, one death was associated with gastrointestinal bleeding, and one patient deceased due to primary graft failure and sepsis. One patient died due to thrombotic microangiopathy and sepsis on D+115. Twenty-nine percent of patients developed acute GVHD (grade 2-4), 18%, aGVHD grade 3-4. In all cases except of one, aGVHD grade 3-4 was successfully treated with calcineurin inhibitors. One patient required systemic steroid therapy. Moderate chronic GVHD (NIH) was documented in 29% of patients. The regimen was well tolerated. Grade 3-4 toxicities included only toxic hepatitis in 4 and sepsis in 5 patients. Mild veno-occlusive disease was observed in one patient, TMA, in one case. Viral reactivation was documented in 47% of patients, CMV (n=6), EBV (n=1), HHV type 1,2 (n=1), HHV type 6 (n=2), BK virus (n=1). Moderate hemorrhagic cystitis developed in 2 patients. Non-relapse mortality on D+100 was 15% and 20%, at 1 year. The two-year overall survival was 80%. All the patients achieved hematological, molecular remission and full donor chimerism. Near-complete resolution of bone marrow fibrosis was documented in 12 patients. No molecular or hematological relapses were registered.
Conclusion
AlloHSCT is an effective treatment modality for myelofibrosis. GVHD prophylaxis using a combination of PTCy and ruxolitinib is associated with good acute and chronic GVHD control, and it seems to be a promising modality, at least for MF patients.
Keywords
Myelofibrosis, allogeneic hematopoietic stem cell transplantation, ruxolitinib, graft-versus-host disease, prophylaxis, cyclophosphamide.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20289
[VALUE] => A pilot study of ruxolitinib combined with cyclophosphamide for graft-versus-host disease prophylaxis and relapse prevention in patients with myelofibrosis: a prospective study
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => A pilot study of ruxolitinib combined with cyclophosphamide for graft-versus-host disease prophylaxis and relapse prevention in patients with myelofibrosis: a prospective study
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20735
[VALUE] => 1371
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1371
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20736
[VALUE] => 1372
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1372
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Мария В. Барабанщикова, Иван С. Моисеев, Елена В. Морозова, Юлия Ю. Власова, Вадим В. Байков, Ильдар М. Бархатов, Борис В. Афанасьев
Введение
Миелофиброз относится к хроническим BCR-ABL-негативным миелопролиферативным неоплазиям и сопровождается, как правило, непрерывно прогрессирующим течением. Аллогенная трансплантация гемопоэтических стволовых клеток в настоящее время является единственным методом терапии, позволяющим добиться излечения от заболевания. Применение ингибитора JAK1/JAK2 руксолитиниба во многом позволяет изменить статус заболевания на момент алло-ТГСК – уменьшить спленомегалию, конституциональные симптомы, улучшить гематологические показатели, в ряде случаев привести к регрессу фиброза в костном мозге. В то же время руксолитиниб обладает иммуномодулирующим эффектом, благодаря чему широко используется для лечения острой и хронической РТПХ. В нашем исследовании мы использовали руксолитиниб в комбинации с посттрансплантационным циклофосфаном в качестве профилактики РТПХ и рецидива заболевания.
Материалы и методы
Мы проанализировали результаты алло-ТГСК у 20 пациентов в возрасте от 32 до 61 лет (медиана 51 год). У 14 пациентов был диагностирован первичный миелофиброз, у 2 пациентов – посттромбоцитемический миелофиброз, у 4 пациентов – постполицитемический миелофиброз. Одиннадцать пациентов относились к промежуточному-2 риску по шкале DIPSSplus, восемь – к высокой группе риска. Одному пациенту алло-ТГСК была выполнена в фазе бластного криза. У пятнадцати пациентов отмечалась мутация JAK2V617F, у двух – мутация в гене MPL, у трех – мутация в гене CALR. Все пациенты получали терапию руксолитинибом в качестве предтрансплантационной подготовки, медиана длительности терапии составила 6 месяцев (3-22) в дозе 30-45 мг. У восьми пациентов отмечалось клиническое улучшение, у 1 – прогрессирование заболевания, у 11 – стабилизации заболевания на момент алло-ТГСК. У семи пациентов была выполнена спленэктомия в связи с выраженной спленомегалией и недостаточным ответом со стороны селезенки. Во всех случаях применялся режим кондиционирования со сниженной интенсивностью доз (флударабин 180 мг/м2, бусульфан 10 мг/кг). Троим пациентам алло-ТГСК была выполнена от HLA-совместимого (10/10) родственного (3) и неродственного (10) донора, от частично-совместимого (9/10) неродственного донора (2) и гаплоидентичного (5) донора. В качестве профилактики РТПХ использовался циклофосфамид 100 мг/кг в день +3, +4 и руксолитиниб 5-7,5 мг х 2 раза в сутки с дня +5 по день +50(2) и день +100(18). Медиана количества CD34+-клеток составила 6,7x106 (1,4-12,0). Исследование зарегистрировано на clinicaltrials.gov, NCT02806375.
Результаты
Приживление трансплантата было зарегистрировано у 18 больных. Медиана времени до приживления по лейкоцитам составила 32 дня (18-61), по тромбоцитам – 38 дней (15-219). Повторная алло-ТГСК была выполнена в одном случае в связи с первичным неприживлением. Однако пациент погиб из-за инфекционных осложнений во время цитопении. Тяжелая гипофункция трансплантата наблюдалась у 11 пациентов. Гипофункция разрешилась самостоятельно у семи больных в течение 79 дней (16-470), в остальных случаях было выполнено введение CD34+ клеток (3). Трое из 4 пациентов погибли до приживления: 1 – сепсис Pseudomonas aeruginosa, 1 – желудочно-кишечное кровотечение, 1 –первичное неприживление и сепсис. Одна пациентка погибла в результате тромботической микроангиопатии (ТМА) на Д+115. Острая РТПХ 2-4 степени отмечалась у 29% пациентов, острая РТПХ3-4 степени – 18%. Во всех случаях, кроме одного, острая РТПХ 3-4 степени разрешилась на фоне терапии ингибиторами кальциневрина. Один пациент получал терапию системными глюкокортикостероидами. Хроническая РТПХ средней степени тяжести наблюдалась у 29% пациентов. Переносимость режима кондиционирования и протокол профилактики была удовлетворительная. Токсичность 3-4 степени, в частности токсический гепатит и сепсис, отмечались у 4 и 5 пациентов соответственно. Веноокклюзионная болезнь средней степени тяжести наблюдалась у 1 пациента, ТМА – 1. Реактивация цитомегаловируса отмечалась у 6 пациентов, EBV – 1, HHV 1 и 2 типа – 1, HHV 6 типа – 2, ВК вируса – 1, геморрагический цистит – 2. Двухлетлетняя общая выживаемость составила 80%. Все пациенты достигли молекулярной, клинико-гематологической ремиссии, полного донорского химеризма. Практически полный регресс фиброза в костном мозге зарегистрирован зарегистрирован у 12 пациентов. Ни в одном случае не отмечалось развитие рецидива заболевания. Трансплантационная летальность составила 15% и 20% через 100 дней и 1 год после алло-ТГСК соответственно.
Заключение
Алло-ТГСК является эффективной терапевтической опцией для пациентов с миелофиброзом. Применение в посттрансплантационном периоде циклофосфамида в комбинации с руксолитинибом представляется эффективной терапевтической опцией в качестве профилактики РТПХ и рецидива заболевания.
Ключевые слова
Миелофиброз, аллогенная трансплантация гемопоэтических стволовых клеток, руксолитиниб, реакция «трансплантат против хозяина», профилактика, циклофосфамид.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20277
[VALUE] => Array
(
[TEXT] => Анна А. Апостолова, Олеся В. Паина, Юлия В. Богославская
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Анна А. Апостолова, Олеся В. Паина, Юлия В. Богославская
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20278
[VALUE] => Array
(
[TEXT] => Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой (CIC 725), Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой (CIC 725), Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20354
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Иммунотерапия моноклональными антителами – это новый вид лечения лейкозов, постепенно вводимый в практику российских гематологических клиник. Большинство препаратов входят в группу расширенного доступа, и не имеют инструкции на русском языке.
</p>
<h2 style="text-align: justify;">Цель работы</h2>
<p style="text-align: justify;">
Рассмотреть тактику ухода за пациентами, получившими терапию моноклональными антителами. Предложить рекомендации для медицинских сестер, работающих с моноклональными АТ.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
В исследование было включено 45 человек, все они являлись пациентами отделения трасплантации костного мозга для детей №1 (ОТКМ №1) НИИ ДОГиТ им. Р. М. Горбачевой. Медиана возраста составила 8,7 лет (4 мес. – 17 лет). У 80% (n=36) диагностирован острый лимфобластный лейкоз (ОЛЛ), у 13,3% (n=6) острый миелобластный лейкоз (ОМЛ), а у 6,7% (n=3) был выявлен острый бифенотипический лейкоз (ОБЛ). Терапию Блинатумомабом получило 36 пациентов, Милотаргом – 6 человек, а Инотузумаб озогамицин получили 5 пациентов.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
У 62,2% (n=28) встречалась фебрильная лихорадка. После терапии моноклональными АТ 35,5% (n=16) была проведена родственная трансплантация гемопоэтических стволовых клеток (ТГСК), 26,7% (n=12) получили гаплоидентичную ТГСК, а 37,8 (n=17) не получали ТГСК. На август 2018 года живы 64,4% (n=29) пациентов.
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
Большинство пациентов получили терапию моноклональными АТ в качестве 3-й линии терапии. Лечение и уход за такими пациентами требуют особого внимания. Также, за неимением инструкции на русском языке, необходимо составить регламент приготовления раствора с моноклональным АТ.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Иммунотерапия, Милотарг, моноклональные антитела, Блинатумомаб, Инотузумаб.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Иммунотерапия моноклональными антителами – это новый вид лечения лейкозов, постепенно вводимый в практику российских гематологических клиник. Большинство препаратов входят в группу расширенного доступа, и не имеют инструкции на русском языке.
Цель работы
Рассмотреть тактику ухода за пациентами, получившими терапию моноклональными антителами. Предложить рекомендации для медицинских сестер, работающих с моноклональными АТ.
Материалы и методы
В исследование было включено 45 человек, все они являлись пациентами отделения трасплантации костного мозга для детей №1 (ОТКМ №1) НИИ ДОГиТ им. Р. М. Горбачевой. Медиана возраста составила 8,7 лет (4 мес. – 17 лет). У 80% (n=36) диагностирован острый лимфобластный лейкоз (ОЛЛ), у 13,3% (n=6) острый миелобластный лейкоз (ОМЛ), а у 6,7% (n=3) был выявлен острый бифенотипический лейкоз (ОБЛ). Терапию Блинатумомабом получило 36 пациентов, Милотаргом – 6 человек, а Инотузумаб озогамицин получили 5 пациентов.
Результаты
У 62,2% (n=28) встречалась фебрильная лихорадка. После терапии моноклональными АТ 35,5% (n=16) была проведена родственная трансплантация гемопоэтических стволовых клеток (ТГСК), 26,7% (n=12) получили гаплоидентичную ТГСК, а 37,8 (n=17) не получали ТГСК. На август 2018 года живы 64,4% (n=29) пациентов.
Выводы
Большинство пациентов получили терапию моноклональными АТ в качестве 3-й линии терапии. Лечение и уход за такими пациентами требуют особого внимания. Также, за неимением инструкции на русском языке, необходимо составить регламент приготовления раствора с моноклональным АТ.
Ключевые слова
Иммунотерапия, Милотарг, моноклональные антитела, Блинатумомаб, Инотузумаб.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20279
[VALUE] => Array
(
[TEXT] => Anna A. Apostolova, Olesya V. Paina, Yulia V. Bogoslavskaya
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Anna A. Apostolova, Olesya V. Paina, Yulia V. Bogoslavskaya
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20280
[VALUE] => Array
(
[TEXT] => R. Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation; First St. Petersburg I. Pavlov State Medical University, St. Petersburg, Russia (CIC 725)
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => R. Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation; First St. Petersburg I. Pavlov State Medical University, St. Petersburg, Russia (CIC 725)
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20355
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Immunotherapy with monoclonal antibodies (Mabs) is a new type of leukemia treatment, being gradually introduced into the practice of Russian hematological clinics. Most drugs comprise a part of the extended access group, and do not have instructions in Russian. Aim of the present study was to consider the strategy of care for the patients who received therapy with monoclonal antibodies, and to suggest recommendations for the nurses working with monoclonal antibodies.
</p>
<h2 style="text-align: justify;">Materials and methods</h2>
<p style="text-align: justify;">
The study included 45 patients. All the patients received treatment and medical care in the BMT Department No.1, at the R.Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation. Their median age was 8.7 years (4 months to 17 years old). Acute lymphoblastic leukemia (ALL) was diagnosed in 80% (n=36), acute myeloblastic leukemia (AML) was found in 13.3% (n=6), and acute biphenotypic leukemia was detected in 6.7% (n=3) (ABL). The therapy with Blinatumomab was applied to 36 patients, Mylotarg was administered in 6 cases, and 5 patients received Inotuzumab ozogamicin.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
62.2% of the patients (n=28) exhibited febrile fever. After therapy with Mabs, a related hematopoietic stem cell transplantation (HSCT) was performed for 35.5% of patients (n=16), 26.7% of patients (n=12) received haploidentical HSCT, and 37.8% (n=17) did not underwent HSCT. Against the August 2018, 64.4% (n=29) of patients were alive.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Most patients were treated with monoclonal antibodies as the third-line therapy. Treatment and care for such patients require special attention. Also, in the absence of instructions in Russian language, it is necessary to compile an operation procedure for preparing a solution with monoclonal antibodies.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Immunotherapy, Mylotarg, monoclonal antibodies, Blinatumomab, Inotuzumab.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
Immunotherapy with monoclonal antibodies (Mabs) is a new type of leukemia treatment, being gradually introduced into the practice of Russian hematological clinics. Most drugs comprise a part of the extended access group, and do not have instructions in Russian. Aim of the present study was to consider the strategy of care for the patients who received therapy with monoclonal antibodies, and to suggest recommendations for the nurses working with monoclonal antibodies.
Materials and methods
The study included 45 patients. All the patients received treatment and medical care in the BMT Department No.1, at the R.Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation. Their median age was 8.7 years (4 months to 17 years old). Acute lymphoblastic leukemia (ALL) was diagnosed in 80% (n=36), acute myeloblastic leukemia (AML) was found in 13.3% (n=6), and acute biphenotypic leukemia was detected in 6.7% (n=3) (ABL). The therapy with Blinatumomab was applied to 36 patients, Mylotarg was administered in 6 cases, and 5 patients received Inotuzumab ozogamicin.
Results
62.2% of the patients (n=28) exhibited febrile fever. After therapy with Mabs, a related hematopoietic stem cell transplantation (HSCT) was performed for 35.5% of patients (n=16), 26.7% of patients (n=12) received haploidentical HSCT, and 37.8% (n=17) did not underwent HSCT. Against the August 2018, 64.4% (n=29) of patients were alive.
Conclusion
Most patients were treated with monoclonal antibodies as the third-line therapy. Treatment and care for such patients require special attention. Also, in the absence of instructions in Russian language, it is necessary to compile an operation procedure for preparing a solution with monoclonal antibodies.
Keywords
Immunotherapy, Mylotarg, monoclonal antibodies, Blinatumomab, Inotuzumab.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20281
[VALUE] => Nursing care for patients who received therapy with monoclonal antibodies
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Nursing care for patients who received therapy with monoclonal antibodies
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20733
[VALUE] => 1369
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1369
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20734
[VALUE] => 1370
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1370
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Анна А. Апостолова, Олеся В. Паина, Юлия В. Богославская
Введение
Иммунотерапия моноклональными антителами – это новый вид лечения лейкозов, постепенно вводимый в практику российских гематологических клиник. Большинство препаратов входят в группу расширенного доступа, и не имеют инструкции на русском языке.
Цель работы
Рассмотреть тактику ухода за пациентами, получившими терапию моноклональными антителами. Предложить рекомендации для медицинских сестер, работающих с моноклональными АТ.
Материалы и методы
В исследование было включено 45 человек, все они являлись пациентами отделения трасплантации костного мозга для детей №1 (ОТКМ №1) НИИ ДОГиТ им. Р. М. Горбачевой. Медиана возраста составила 8,7 лет (4 мес. – 17 лет). У 80% (n=36) диагностирован острый лимфобластный лейкоз (ОЛЛ), у 13,3% (n=6) острый миелобластный лейкоз (ОМЛ), а у 6,7% (n=3) был выявлен острый бифенотипический лейкоз (ОБЛ). Терапию Блинатумомабом получило 36 пациентов, Милотаргом – 6 человек, а Инотузумаб озогамицин получили 5 пациентов.
Результаты
У 62,2% (n=28) встречалась фебрильная лихорадка. После терапии моноклональными АТ 35,5% (n=16) была проведена родственная трансплантация гемопоэтических стволовых клеток (ТГСК), 26,7% (n=12) получили гаплоидентичную ТГСК, а 37,8 (n=17) не получали ТГСК. На август 2018 года живы 64,4% (n=29) пациентов.
Выводы
Большинство пациентов получили терапию моноклональными АТ в качестве 3-й линии терапии. Лечение и уход за такими пациентами требуют особого внимания. Также, за неимением инструкции на русском языке, необходимо составить регламент приготовления раствора с моноклональным АТ.
Ключевые слова
Иммунотерапия, Милотарг, моноклональные антитела, Блинатумомаб, Инотузумаб.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20317
[VALUE] => Array
(
[TEXT] => Сергей Н. Бондаренко <sup>1</sup>, Ольга С. Успенская <sup>2</sup>, Елена В. Карягина <sup>3</sup>, Наталья В. Архипова <sup>4</sup>, Евгения И. Желнова <sup>4</sup>, Иван С. Моисеев <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Ирина А. Самородова <sup>1</sup>, Анна Г. Смирнова <sup>1</sup>, Татьяна А. Быкова <sup>1</sup>, Белла И. Аюбова <sup>1</sup>, Елена В. Бабенко <sup>1</sup>, Ильдар М. Бархатов <sup>1</sup>, Татьяна Л. Гиндина <sup>1</sup>, Александр Д. Кулагин <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Сергей Н. Бондаренко 1, Ольга С. Успенская 2, Елена В. Карягина 3, Наталья В. Архипова 4, Евгения И. Желнова 4, Иван С. Моисеев 1, Елена И. Дарская 1, Ирина А. Самородова 1, Анна Г. Смирнова 1, Татьяна А. Быкова 1, Белла И. Аюбова 1, Елена В. Бабенко 1, Ильдар М. Бархатов 1, Татьяна Л. Гиндина 1, Александр Д. Кулагин 1, Борис В. Афанасьев 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20318
[VALUE] => Array
(
[TEXT] => <sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург<br>
<sup>2</sup> Ленинградская областная клиническая больница, Санкт-Петербург<br>
<sup>3</sup> Городская больница №15, Санкт-Петербург<br>
<sup>4</sup> Городская клиническая больница №52, Москва, Российская Федерация
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой ПСПбГМУ им. И. П. Павлова, Санкт-Петербург
2 Ленинградская областная клиническая больница, Санкт-Петербург
3 Городская больница №15, Санкт-Петербург
4 Городская клиническая больница №52, Москва, Российская Федерация
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20346
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
При развитии рецидива острого миелоидного лейкоза (ОМЛ) полную ремиссию (ПР) удается достичь в 25-50% случаев. Пятилетняя общая выживаемость составляет 11%. Прогноз для пациентов с химиорезистентным (ХР) ОМЛ остается неутешительным. Перспективы улучшить результаты терапии ОМЛ находятся в области таргетной терапии. Гемтузумаб озогамицин* (ГО) представляет собой конъюгированное моноклональное антиCD33 антитело, ковалентно связанное с цитотоксическим агентом – калихеамицином. Поскольку CD33 экспрессируется на бластах почти у всех пациентов с ОМЛ, использование ГО в сочетании с химиотерапией (ХТ) дает шанс на получение ПР и проведении аллогенной трансплантации костного мозга (алло-ТГСК).
</p>
<h2 style="text-align: justify;">Цель работы</h2>
<p style="text-align: justify;">
Оценить эффективность и токсичсность ГО в сочетании с ХТ у пациентов ХР ОМЛ.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
В исследование включено 25 пациентов с ХР ОМЛ. Медиана возраста составила 36(18-68) лет. Согласно моекулярно-цитогенетической классификации (МЦК): низкий риск (НР) – 2, средний (СР) – 14, высокий (ВР) – 9 пациентов. Первично ХР (ПХР) были 13 пациентов, вторично ХР (ВХР) – 12. Изолированное поражение костного мозга было у 16 больных, комбинированное у 8 (ЦНС – 2, экстрамедуллярное поражение – 7; один пациент имел сочетанное поражение). Медиана уровня экспрессии CD33 составила 72 (9-95)%. ГО получили после алло-ТГСК 4 (16%) больных. ГО вводили в дозе 3 мг/м2 (максимально 5 мг) в сочетании с высокодозной ХТ (ВДХТ) (FLAG±Ida, HDAC, HAM) или низкодозной ХТ (НДХТ) (MEtA, LDARA-C) – 12 и 13 больных, соответственно. ГО вводился однократно (1ГО) у 13, двукратно (2ГО) – 4 и трехкратно (3ГО) – 8 пациентов, соответственно. ТГСК (нерод-3, гапло-3, ауто-1) проведена после терапии ГО 7(28%) пациентам, из них у 2 – повторная алло-ТГСК со сменой донора. Медиана сроков проведения ТГСК после терапии ГО 62 (17-138) дней.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
ПР достигнута у 3(12%), ПР без восстановления показателей периферической крови (нПР) у 6(24%) пациентов, соответственно, общий положительный ответ (ОПО) получен у 9(36%) больных. Медиана продолжительности ПР 56(6-341) дней. В зависимости от МЦК ОПО достигнут у 2 больных в НР, у 4 (29%) в СР, у 3 (33%) пациентов в ВР. ОПО был у 3 (23%) пациентов с ПХР, и у 6 (50%) с ВХР. При сочетании НДХТ+ГО ОПО получен у 3 (23%) пациентов, при ВДХТ+ГО – у 6 (50%). В зависимости от кратности введения ГО ОПО констатирован при 1ГО – у 4 (31%), 2ГО – 0, 3ГО – 5 (62%) пациентов. Однолетняя общая (1ОВ) и безрецидивная (1БРВ) выживаемость составили 26% (95%ДИ 6-46%) и 25% (95%ДИ 6-44%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии ГО 1ОБ и 1БРВ составила 21% (95%ДИ 4-38) против 8% (95%ДИ 1-15) р=.02 и 19% (95%ДИ 3-25) против 6% (95%ДИ 1-11) р=.01, соответственно. Из ответивших на терапию ГО умерло 3 пациента от прогрессии ОМЛ, 1 пациент от инфекции и 1 от геморрагического синдрома. Печеночная токсичность (трансфераземия) 1-2 степени у 3 пациентов и 3 степени – у 2; сепсис у 9 пациентов. Синусоидальный обструктивный синдром не отмечался ни у одного пациента.<br>
<span style="font-family: Cuprum, sans-serif; font-size: 26px;">Заключение</span><br>
Это исследование продемонстрировало значимую эффективность и приемлемый профиль токсичности при комбинации ГО и ХТ. Сочетанное применение ГО и ХТ может рассматриваться для пациентов с ХР ОМЛ, как этап подготовки к алло-ТГСК.
</p>
<h2 style="text-align: justify;">Комментарии</h2>
<p style="text-align: justify;">
Авторы заявляют об отсутствии скрытого конфликта интересов.<br>
* ГО предоставлялся в рамках программы расширенного доступа по жизненным показаниям
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Острый миелоидный лейкоз, таргетная терапия, гемтузумаб озогамицин.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
При развитии рецидива острого миелоидного лейкоза (ОМЛ) полную ремиссию (ПР) удается достичь в 25-50% случаев. Пятилетняя общая выживаемость составляет 11%. Прогноз для пациентов с химиорезистентным (ХР) ОМЛ остается неутешительным. Перспективы улучшить результаты терапии ОМЛ находятся в области таргетной терапии. Гемтузумаб озогамицин* (ГО) представляет собой конъюгированное моноклональное антиCD33 антитело, ковалентно связанное с цитотоксическим агентом – калихеамицином. Поскольку CD33 экспрессируется на бластах почти у всех пациентов с ОМЛ, использование ГО в сочетании с химиотерапией (ХТ) дает шанс на получение ПР и проведении аллогенной трансплантации костного мозга (алло-ТГСК).
Цель работы
Оценить эффективность и токсичсность ГО в сочетании с ХТ у пациентов ХР ОМЛ.
Пациенты и методы
В исследование включено 25 пациентов с ХР ОМЛ. Медиана возраста составила 36(18-68) лет. Согласно моекулярно-цитогенетической классификации (МЦК): низкий риск (НР) – 2, средний (СР) – 14, высокий (ВР) – 9 пациентов. Первично ХР (ПХР) были 13 пациентов, вторично ХР (ВХР) – 12. Изолированное поражение костного мозга было у 16 больных, комбинированное у 8 (ЦНС – 2, экстрамедуллярное поражение – 7; один пациент имел сочетанное поражение). Медиана уровня экспрессии CD33 составила 72 (9-95)%. ГО получили после алло-ТГСК 4 (16%) больных. ГО вводили в дозе 3 мг/м2 (максимально 5 мг) в сочетании с высокодозной ХТ (ВДХТ) (FLAG±Ida, HDAC, HAM) или низкодозной ХТ (НДХТ) (MEtA, LDARA-C) – 12 и 13 больных, соответственно. ГО вводился однократно (1ГО) у 13, двукратно (2ГО) – 4 и трехкратно (3ГО) – 8 пациентов, соответственно. ТГСК (нерод-3, гапло-3, ауто-1) проведена после терапии ГО 7(28%) пациентам, из них у 2 – повторная алло-ТГСК со сменой донора. Медиана сроков проведения ТГСК после терапии ГО 62 (17-138) дней.
Результаты
ПР достигнута у 3(12%), ПР без восстановления показателей периферической крови (нПР) у 6(24%) пациентов, соответственно, общий положительный ответ (ОПО) получен у 9(36%) больных. Медиана продолжительности ПР 56(6-341) дней. В зависимости от МЦК ОПО достигнут у 2 больных в НР, у 4 (29%) в СР, у 3 (33%) пациентов в ВР. ОПО был у 3 (23%) пациентов с ПХР, и у 6 (50%) с ВХР. При сочетании НДХТ+ГО ОПО получен у 3 (23%) пациентов, при ВДХТ+ГО – у 6 (50%). В зависимости от кратности введения ГО ОПО констатирован при 1ГО – у 4 (31%), 2ГО – 0, 3ГО – 5 (62%) пациентов. Однолетняя общая (1ОВ) и безрецидивная (1БРВ) выживаемость составили 26% (95%ДИ 6-46%) и 25% (95%ДИ 6-44%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии ГО 1ОБ и 1БРВ составила 21% (95%ДИ 4-38) против 8% (95%ДИ 1-15) р=.02 и 19% (95%ДИ 3-25) против 6% (95%ДИ 1-11) р=.01, соответственно. Из ответивших на терапию ГО умерло 3 пациента от прогрессии ОМЛ, 1 пациент от инфекции и 1 от геморрагического синдрома. Печеночная токсичность (трансфераземия) 1-2 степени у 3 пациентов и 3 степени – у 2; сепсис у 9 пациентов. Синусоидальный обструктивный синдром не отмечался ни у одного пациента.
Заключение
Это исследование продемонстрировало значимую эффективность и приемлемый профиль токсичности при комбинации ГО и ХТ. Сочетанное применение ГО и ХТ может рассматриваться для пациентов с ХР ОМЛ, как этап подготовки к алло-ТГСК.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
* ГО предоставлялся в рамках программы расширенного доступа по жизненным показаниям
Ключевые слова
Острый миелоидный лейкоз, таргетная терапия, гемтузумаб озогамицин.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20319
[VALUE] => Array
(
[TEXT] => Sergey N. Bondarenko <sup>1</sup>, Olga S. Uspenskaya <sup>2</sup>, Elena V. Karyagina <sup>3</sup>, Natalya V. Arkhipova <sup>4</sup>, Evgenia I. Zhelnova <sup>4</sup>, Ivan S. Moiseev <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Irina A. Samorodova <sup>1</sup>, Anna G. Smirnova <sup>1</sup>, Tatyana A. Bykova <sup>1</sup>, Bella I. Ayubova <sup>1</sup>, Elena V. Babenko <sup>1</sup>, Ildar M. Barkhatov <sup>1</sup>, Tatyana L. Gindina <sup>1</sup>, Alexander D. Kulagin <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Sergey N. Bondarenko 1, Olga S. Uspenskaya 2, Elena V. Karyagina 3, Natalya V. Arkhipova 4, Evgenia I. Zhelnova 4, Ivan S. Moiseev 1, Elena I. Darskaya 1, Irina A. Samorodova 1, Anna G. Smirnova 1, Tatyana A. Bykova 1, Bella I. Ayubova 1, Elena V. Babenko 1, Ildar M. Barkhatov 1, Tatyana L. Gindina 1, Alexander D. Kulagin 1, Boris V. Afanasyev 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20320
[VALUE] => Array
(
[TEXT] => <sup>1</sup> R. Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, The First State I. Pavlov Medical University, St. Petersburg, Russian Federation<br>
<sup>2</sup> Leningrad Regional Clinical Hospital, St. Petersburg, Russian Federation<br>
<sup>3</sup> City Hospital No.15, St. Petersburg, Russian Federation<br>
<sup>4</sup> City Clinical Hospital №52, Moscow, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 R. Gorbacheva Memorial Institute of Children Oncology Hematology and Transplantation, The First State I. Pavlov Medical University, St. Petersburg, Russian Federation
2 Leningrad Regional Clinical Hospital, St. Petersburg, Russian Federation
3 City Hospital No.15, St. Petersburg, Russian Federation
4 City Clinical Hospital №52, Moscow, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20347
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
In case of relapse and refractory course of acute myeloid leukemia (RAML), complete remission (CR) can be achieved in 25-50% pts. The five-year overall survival (OS) was 11%. The prognosis for patients with RAML remains disappointing. Prospects to improve the results of AML therapy are connected with implementation of target therapy. Gemtuzumab ozogamicin* (GO) is a conjugated monoclonal anti- CD33 antibody covalently bound to a cytotoxic agent-calicheamicin. Since CD33 is expressed on blast cells in almost all pts with AML, the use of GO in combination with chemotherapy (ChT) gives a chance to receive CR and perform allogeneic hematopoietic stem cell transplantation (allo-HSCT).
</p>
<h2 style="text-align: justify;">Aim</h2>
<p style="text-align: justify;">
Aim of the study was to assess efficacy and toxicity of GO in combination with ChT in patients with RAML.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
The study included 25 pts with RAML. The median age was 36 (18-68) years. According to the molecular cytogenetic classification (MCC): low risk (LR), in 2 cases; intermediate (IR), in 14; high risk (HR), in 9 pts. Primary resistance (PR) was documented in 13 pts, whereas 12 showed secondary resistance (SR). Isolated bone marrow involvement was registered in 16 pts, combined affection was found in 8 pts (CNS, 2 cases; other extramedullary lesions, in 7 patients, and one patient had multiple lesions). The median CD33 expression level was 72% (9-95%). Four patients (16%) received GO after allo-HSCT. GO was administered at a dose of 3 mg/m2 (max. 5 mg) in combination with high-dose ChT (HDCT) (FLAG ± Ida, HDAC, HAM) or low-dose CT (LDCT) (MEtA, LDARA-C) in 12 and 13 pts, respectively. GO was administered once (1 GO) in 13 cases; twice (2GO), in 4 patients, and it was applied 3 times (3GO) in 8 pts. HSCT (unrelated,3; haplo,3; auto, in 1case) was performed after therapy with GO in 7 pts (28%), two of them had a second allo-HSCT from another donor. Median time of HSCT after GO was 62(17-138) days.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Complete remission (CR) was achieved in 3 (12%), CR without peripheral blood recovery (NCR) in 6 (24%) pts, the overall positive response (OR) was obtained in 9 (36%) pts. The median CR duration was 56 (6-341) days. Depending on the MCC risk score, OR was achieved in 2 pts in LR, in 4 (29%) in IR, and in 3 (33%) pts in HR. OR was in 3 (23%) patients with PR, and in 6(50%) with SR. When combining LDCT and GO, the overall response (OR) was obtained in 3 (23%) patients, with HDCT + GO, it was achieved in 6 cases (50%). Depending on the number of the GO rounds, overall positive response (OR) was detected in 4 patients (31%) after 1GO; in none case, after 2GO; in 5 (62%) pts, after 3GO. The one-year overall survival (1OS) and disease-free survival (1DFS) were 26% (95% CI 6-46%), and 25% (95% CI 6-44%), respectively. Depending on allo-HSCT after GO therapy, the 1OS and 1DFS rates were 21% (95% CI 4-38) versus 8% (95% CI 1-15, p=.02), and 19% (95% CI 3-25) versus 6%(95% CI 1-11, p=.01), respectively. Among the responders to GO therapy, 3 pts died from AML progression, one patient was lost due to infection, and one died from hemorrhagic syndrome. Hepatic toxicity (ALT increase) of grade 1-2 was observed in 3 pts, and grade 3 was registered in 2 pts; sepsis was diagnosed in 9 pts. Sinusoidal obstruction syndrome was not observed in this group.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
This study demonstrated significant efficacy and acceptable toxicity profile for combination of GO and ChT. GO with ChT can be considered for patients with RAML, as a bridge to allo-HSCT.
</p>
<h2 style="text-align: justify;">Disclosure</h2>
<p style="text-align: justify;">
The authors report no conflicts of interest in this work.<br>
* GO was provided under program of extended access for vital indications.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Acute myeloid leukemia, target therapy, gemtuzumab ozogamicin.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
In case of relapse and refractory course of acute myeloid leukemia (RAML), complete remission (CR) can be achieved in 25-50% pts. The five-year overall survival (OS) was 11%. The prognosis for patients with RAML remains disappointing. Prospects to improve the results of AML therapy are connected with implementation of target therapy. Gemtuzumab ozogamicin* (GO) is a conjugated monoclonal anti- CD33 antibody covalently bound to a cytotoxic agent-calicheamicin. Since CD33 is expressed on blast cells in almost all pts with AML, the use of GO in combination with chemotherapy (ChT) gives a chance to receive CR and perform allogeneic hematopoietic stem cell transplantation (allo-HSCT).
Aim
Aim of the study was to assess efficacy and toxicity of GO in combination with ChT in patients with RAML.
Patients and methods
The study included 25 pts with RAML. The median age was 36 (18-68) years. According to the molecular cytogenetic classification (MCC): low risk (LR), in 2 cases; intermediate (IR), in 14; high risk (HR), in 9 pts. Primary resistance (PR) was documented in 13 pts, whereas 12 showed secondary resistance (SR). Isolated bone marrow involvement was registered in 16 pts, combined affection was found in 8 pts (CNS, 2 cases; other extramedullary lesions, in 7 patients, and one patient had multiple lesions). The median CD33 expression level was 72% (9-95%). Four patients (16%) received GO after allo-HSCT. GO was administered at a dose of 3 mg/m2 (max. 5 mg) in combination with high-dose ChT (HDCT) (FLAG ± Ida, HDAC, HAM) or low-dose CT (LDCT) (MEtA, LDARA-C) in 12 and 13 pts, respectively. GO was administered once (1 GO) in 13 cases; twice (2GO), in 4 patients, and it was applied 3 times (3GO) in 8 pts. HSCT (unrelated,3; haplo,3; auto, in 1case) was performed after therapy with GO in 7 pts (28%), two of them had a second allo-HSCT from another donor. Median time of HSCT after GO was 62(17-138) days.
Results
Complete remission (CR) was achieved in 3 (12%), CR without peripheral blood recovery (NCR) in 6 (24%) pts, the overall positive response (OR) was obtained in 9 (36%) pts. The median CR duration was 56 (6-341) days. Depending on the MCC risk score, OR was achieved in 2 pts in LR, in 4 (29%) in IR, and in 3 (33%) pts in HR. OR was in 3 (23%) patients with PR, and in 6(50%) with SR. When combining LDCT and GO, the overall response (OR) was obtained in 3 (23%) patients, with HDCT + GO, it was achieved in 6 cases (50%). Depending on the number of the GO rounds, overall positive response (OR) was detected in 4 patients (31%) after 1GO; in none case, after 2GO; in 5 (62%) pts, after 3GO. The one-year overall survival (1OS) and disease-free survival (1DFS) were 26% (95% CI 6-46%), and 25% (95% CI 6-44%), respectively. Depending on allo-HSCT after GO therapy, the 1OS and 1DFS rates were 21% (95% CI 4-38) versus 8% (95% CI 1-15, p=.02), and 19% (95% CI 3-25) versus 6%(95% CI 1-11, p=.01), respectively. Among the responders to GO therapy, 3 pts died from AML progression, one patient was lost due to infection, and one died from hemorrhagic syndrome. Hepatic toxicity (ALT increase) of grade 1-2 was observed in 3 pts, and grade 3 was registered in 2 pts; sepsis was diagnosed in 9 pts. Sinusoidal obstruction syndrome was not observed in this group.
Conclusion
This study demonstrated significant efficacy and acceptable toxicity profile for combination of GO and ChT. GO with ChT can be considered for patients with RAML, as a bridge to allo-HSCT.
Disclosure
The authors report no conflicts of interest in this work.
* GO was provided under program of extended access for vital indications.
Keywords
Acute myeloid leukemia, target therapy, gemtuzumab ozogamicin.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20321
[VALUE] => Gemtuzumab ozogamicin and chemotherapy in patients with relapses and refractory acute myeloid leukemia
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Gemtuzumab ozogamicin and chemotherapy in patients with relapses and refractory acute myeloid leukemia
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20743
[VALUE] => 1379
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1379
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20744
[VALUE] => 1380
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1380
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Сергей Н. Бондаренко 1, Ольга С. Успенская 2, Елена В. Карягина 3, Наталья В. Архипова 4, Евгения И. Желнова 4, Иван С. Моисеев 1, Елена И. Дарская 1, Ирина А. Самородова 1, Анна Г. Смирнова 1, Татьяна А. Быкова 1, Белла И. Аюбова 1, Елена В. Бабенко 1, Ильдар М. Бархатов 1, Татьяна Л. Гиндина 1, Александр Д. Кулагин 1, Борис В. Афанасьев 1
2 Ленинградская областная клиническая больница, Санкт-Петербург
3 Городская больница №15, Санкт-Петербург
4 Городская клиническая больница №52, Москва, Российская Федерация
Введение
При развитии рецидива острого миелоидного лейкоза (ОМЛ) полную ремиссию (ПР) удается достичь в 25-50% случаев. Пятилетняя общая выживаемость составляет 11%. Прогноз для пациентов с химиорезистентным (ХР) ОМЛ остается неутешительным. Перспективы улучшить результаты терапии ОМЛ находятся в области таргетной терапии. Гемтузумаб озогамицин* (ГО) представляет собой конъюгированное моноклональное антиCD33 антитело, ковалентно связанное с цитотоксическим агентом – калихеамицином. Поскольку CD33 экспрессируется на бластах почти у всех пациентов с ОМЛ, использование ГО в сочетании с химиотерапией (ХТ) дает шанс на получение ПР и проведении аллогенной трансплантации костного мозга (алло-ТГСК).
Цель работы
Оценить эффективность и токсичсность ГО в сочетании с ХТ у пациентов ХР ОМЛ.
Пациенты и методы
В исследование включено 25 пациентов с ХР ОМЛ. Медиана возраста составила 36(18-68) лет. Согласно моекулярно-цитогенетической классификации (МЦК): низкий риск (НР) – 2, средний (СР) – 14, высокий (ВР) – 9 пациентов. Первично ХР (ПХР) были 13 пациентов, вторично ХР (ВХР) – 12. Изолированное поражение костного мозга было у 16 больных, комбинированное у 8 (ЦНС – 2, экстрамедуллярное поражение – 7; один пациент имел сочетанное поражение). Медиана уровня экспрессии CD33 составила 72 (9-95)%. ГО получили после алло-ТГСК 4 (16%) больных. ГО вводили в дозе 3 мг/м2 (максимально 5 мг) в сочетании с высокодозной ХТ (ВДХТ) (FLAG±Ida, HDAC, HAM) или низкодозной ХТ (НДХТ) (MEtA, LDARA-C) – 12 и 13 больных, соответственно. ГО вводился однократно (1ГО) у 13, двукратно (2ГО) – 4 и трехкратно (3ГО) – 8 пациентов, соответственно. ТГСК (нерод-3, гапло-3, ауто-1) проведена после терапии ГО 7(28%) пациентам, из них у 2 – повторная алло-ТГСК со сменой донора. Медиана сроков проведения ТГСК после терапии ГО 62 (17-138) дней.
Результаты
ПР достигнута у 3(12%), ПР без восстановления показателей периферической крови (нПР) у 6(24%) пациентов, соответственно, общий положительный ответ (ОПО) получен у 9(36%) больных. Медиана продолжительности ПР 56(6-341) дней. В зависимости от МЦК ОПО достигнут у 2 больных в НР, у 4 (29%) в СР, у 3 (33%) пациентов в ВР. ОПО был у 3 (23%) пациентов с ПХР, и у 6 (50%) с ВХР. При сочетании НДХТ+ГО ОПО получен у 3 (23%) пациентов, при ВДХТ+ГО – у 6 (50%). В зависимости от кратности введения ГО ОПО констатирован при 1ГО – у 4 (31%), 2ГО – 0, 3ГО – 5 (62%) пациентов. Однолетняя общая (1ОВ) и безрецидивная (1БРВ) выживаемость составили 26% (95%ДИ 6-46%) и 25% (95%ДИ 6-44%), соответственно. В зависимости от проведения или не проведения ТГСК после терапии ГО 1ОБ и 1БРВ составила 21% (95%ДИ 4-38) против 8% (95%ДИ 1-15) р=.02 и 19% (95%ДИ 3-25) против 6% (95%ДИ 1-11) р=.01, соответственно. Из ответивших на терапию ГО умерло 3 пациента от прогрессии ОМЛ, 1 пациент от инфекции и 1 от геморрагического синдрома. Печеночная токсичность (трансфераземия) 1-2 степени у 3 пациентов и 3 степени – у 2; сепсис у 9 пациентов. Синусоидальный обструктивный синдром не отмечался ни у одного пациента.
Заключение
Это исследование продемонстрировало значимую эффективность и приемлемый профиль токсичности при комбинации ГО и ХТ. Сочетанное применение ГО и ХТ может рассматриваться для пациентов с ХР ОМЛ, как этап подготовки к алло-ТГСК.
Комментарии
Авторы заявляют об отсутствии скрытого конфликта интересов.
* ГО предоставлялся в рамках программы расширенного доступа по жизненным показаниям
Ключевые слова
Острый миелоидный лейкоз, таргетная терапия, гемтузумаб озогамицин.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20325
[VALUE] => Array
(
[TEXT] => Евгения С. Борзенкова, Наталья Б. Михайлова, Кирилл В. Лепик, Лилия В. Стельмах, Анастасия В. Некрасова, Иван В. Цыганков, Иван С. Моисеев, Юрий Р. Залялов, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Евгения С. Борзенкова, Наталья Б. Михайлова, Кирилл В. Лепик, Лилия В. Стельмах, Анастасия В. Некрасова, Иван В. Цыганков, Иван С. Моисеев, Юрий Р. Залялов, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20326
[VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Россия<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20344
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) имеет высокий потенциал излечения классической лимфомы Ходжкина (ЛХ) у пациентов с рефрактерным или рецидивирующим течением (р/рЛХ). Тем не менее, опубликованных данных о терапии рецидива или прогрессирования ЛХ после алло-ТГСК крайне мало. В одноцентровом исследовании была проведена попытка выявить прогностические факторы в лечение подобных пациентов.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
В этот ретроспективный анализ включены пациенты (n=27), прошедшие аллоТКМ в нашей клинике с 2002 по 2017 гг. Пациенты с подтвержденным прогрессиро-ванием заболевания после аллоТГСК составили 22,2% (n=6); пациенты с ПО, но c рецидивом или прогрессированием далее – 25,9% (n=7); пациенты с первым ответом хуже чем ПО (ЧО/СЗ) составили 51,8% (n=14), включая 7 пациентов c неподтвержденным 1-м статусом таким как ЧО/СЗ, основываясь на статусе заболевания перед аллоТКМ, при этом ПО и ПЗ также не подтверждены. При первом стадировании после алло-ТГСК у 7 пациентов зафиксирован ПО (25,0%), ЧО отмечен у 10 пациентов (37,0%), таким образом у 17 (62,9%) пациентов был общий ответ. За период наблюдения у 20 пациентов (74,0%) из 27 зафиксированы прогрессирование или рецидив ЛХ после аллоТКМ. 19 пациентов получили лечение: 6 пациентов получили только химиотерапию (х/т) после аллоТКМ (ChVPP, LABO, винбластин); 13 пациентов получили терапию новыми моноклональными антителами (МА): брентуксимаб ведотин (BV) и ниволумаб (Nivo), или сочетание их с химиотерапией. Остальные 8 пациентов были оставлены без терапии: 3 пациента (ЧО, СЗ, ПЗ) из-за осложнений алло-ТГСК и плохого соматического статуса; 5 пациентов из группы неподтвержденного статуса (ЧО-4, СЗ-1) – под динамическим наблюдением. 13 пациентов (48,1%). Терапию BV-содержащими схемами в качестве первой линии МА-терапии получили все 13 пациентов. 7 из них (53,8%; 25,9%) из-за продолжающегося прогрессирования ЛХ переведены на вторую линию терапии МА ниволумабом. До начала терапии MA (BV) 5 из 13 пациентов получили ХТ, и 4 пациента из 13 получили инфузии донорских лимфоцитов (ИЛД). Характеристики пациентов и методов представлены в таблице №1.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
На момент анализа время наблюдения за всеми пациентами (n=27) было 27 (1,4-3,7) мес. Для пациентов только с х/т (n=6) время наблюдения 25 (6,27-51) мес.; для 13 пациентов с МА-терапией – 45 мес. (23-73). Медиана наблюдения за пациентами без терапии (n=8) 11 мес. (1,47-39,37). Общая выживаемость для всех пациентов на момент анализа была 55% (n=15). Время от трансплантации до ПЗ/РЗ было 3,6 мес. (1,3-11,3 мес.). Среднее время от алло-ТГСК до начала терапии BV по поводу ПЗ/РЗ было 4,7 мес. (1,7-44 мес.). Среднее время от алло-ТГСК до начала терапии Nivo было 38,7 мес. (14,5-44,5). Среднее время между окончанием терапии BV и началом терапии Nivo было 2,83 (1,23-32,47) месяцев. На момент анализа 12 пациентов (44,4%) из 27 умерли: 6 из-за прогрессирования ЛХ и 6 пациентов из-за тяжелой хронической РТПХ (хрРТПХ) и инфекционных осложнений в посттрансплантационном периоде, включая 3 пациентов с МА-терапией и 1 пациента под динамическим наблюдением. 15 пациентов живы: у 4х пациентов в процессе наблюдения зафиксирован ПО; 6 пациентов в ПО после МА-терапии (5) и после ХТ (1); 5 пациентов продолжают лечение из-за стабилизации ли прогрессирования ЛХ. При сравнении результатов ХТ и терапии МА, прогностическим значением облада- ло лечение МА (76,9% против 16,7%, p=.003), также развитие хрРТПХ имело прогностическое значение (72,7% против 43,9%, p=.084).
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
На небольшом клиническом материале было показано, что треть пациентов погибают от прогрессирования ЛХ и почти столько же от осложнений терапии. Несмотря на относительно благоприятный прогноз в этой тяжелой группе пациентов, требуются дальнейшие исследования для выбора оптимальной терапии посттрансплантационного рецидива и прогрессирования ЛХ.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Лимфома Ходжкина, аллогенная трансплантация костного мозга, брентуксимаб ведотин, ниволумаб.
</p>
<h2 style="text-align: justify;">
Таблица 1. Характеристики пациентов и методы терапии (продолжение)<br>
</h2>
<p style="text-align: justify;">
<img width="780" alt="таблица 1 часть.png" src="/upload/medialibrary/94c/tablitsa-1-chast.png" height="407" title="таблица 1 часть.png"><br>
</p>
<p style="text-align: justify;">
<img width="781" alt="таблица 2 часть.png" src="/upload/medialibrary/664/tablitsa-2-chast.png" height="303" title="таблица 2 часть.png"><br>
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) имеет высокий потенциал излечения классической лимфомы Ходжкина (ЛХ) у пациентов с рефрактерным или рецидивирующим течением (р/рЛХ). Тем не менее, опубликованных данных о терапии рецидива или прогрессирования ЛХ после алло-ТГСК крайне мало. В одноцентровом исследовании была проведена попытка выявить прогностические факторы в лечение подобных пациентов.
Пациенты и методы
В этот ретроспективный анализ включены пациенты (n=27), прошедшие аллоТКМ в нашей клинике с 2002 по 2017 гг. Пациенты с подтвержденным прогрессиро-ванием заболевания после аллоТГСК составили 22,2% (n=6); пациенты с ПО, но c рецидивом или прогрессированием далее – 25,9% (n=7); пациенты с первым ответом хуже чем ПО (ЧО/СЗ) составили 51,8% (n=14), включая 7 пациентов c неподтвержденным 1-м статусом таким как ЧО/СЗ, основываясь на статусе заболевания перед аллоТКМ, при этом ПО и ПЗ также не подтверждены. При первом стадировании после алло-ТГСК у 7 пациентов зафиксирован ПО (25,0%), ЧО отмечен у 10 пациентов (37,0%), таким образом у 17 (62,9%) пациентов был общий ответ. За период наблюдения у 20 пациентов (74,0%) из 27 зафиксированы прогрессирование или рецидив ЛХ после аллоТКМ. 19 пациентов получили лечение: 6 пациентов получили только химиотерапию (х/т) после аллоТКМ (ChVPP, LABO, винбластин); 13 пациентов получили терапию новыми моноклональными антителами (МА): брентуксимаб ведотин (BV) и ниволумаб (Nivo), или сочетание их с химиотерапией. Остальные 8 пациентов были оставлены без терапии: 3 пациента (ЧО, СЗ, ПЗ) из-за осложнений алло-ТГСК и плохого соматического статуса; 5 пациентов из группы неподтвержденного статуса (ЧО-4, СЗ-1) – под динамическим наблюдением. 13 пациентов (48,1%). Терапию BV-содержащими схемами в качестве первой линии МА-терапии получили все 13 пациентов. 7 из них (53,8%; 25,9%) из-за продолжающегося прогрессирования ЛХ переведены на вторую линию терапии МА ниволумабом. До начала терапии MA (BV) 5 из 13 пациентов получили ХТ, и 4 пациента из 13 получили инфузии донорских лимфоцитов (ИЛД). Характеристики пациентов и методов представлены в таблице №1.
Результаты
На момент анализа время наблюдения за всеми пациентами (n=27) было 27 (1,4-3,7) мес. Для пациентов только с х/т (n=6) время наблюдения 25 (6,27-51) мес.; для 13 пациентов с МА-терапией – 45 мес. (23-73). Медиана наблюдения за пациентами без терапии (n=8) 11 мес. (1,47-39,37). Общая выживаемость для всех пациентов на момент анализа была 55% (n=15). Время от трансплантации до ПЗ/РЗ было 3,6 мес. (1,3-11,3 мес.). Среднее время от алло-ТГСК до начала терапии BV по поводу ПЗ/РЗ было 4,7 мес. (1,7-44 мес.). Среднее время от алло-ТГСК до начала терапии Nivo было 38,7 мес. (14,5-44,5). Среднее время между окончанием терапии BV и началом терапии Nivo было 2,83 (1,23-32,47) месяцев. На момент анализа 12 пациентов (44,4%) из 27 умерли: 6 из-за прогрессирования ЛХ и 6 пациентов из-за тяжелой хронической РТПХ (хрРТПХ) и инфекционных осложнений в посттрансплантационном периоде, включая 3 пациентов с МА-терапией и 1 пациента под динамическим наблюдением. 15 пациентов живы: у 4х пациентов в процессе наблюдения зафиксирован ПО; 6 пациентов в ПО после МА-терапии (5) и после ХТ (1); 5 пациентов продолжают лечение из-за стабилизации ли прогрессирования ЛХ. При сравнении результатов ХТ и терапии МА, прогностическим значением облада- ло лечение МА (76,9% против 16,7%, p=.003), также развитие хрРТПХ имело прогностическое значение (72,7% против 43,9%, p=.084).
Выводы
На небольшом клиническом материале было показано, что треть пациентов погибают от прогрессирования ЛХ и почти столько же от осложнений терапии. Несмотря на относительно благоприятный прогноз в этой тяжелой группе пациентов, требуются дальнейшие исследования для выбора оптимальной терапии посттрансплантационного рецидива и прогрессирования ЛХ.
Ключевые слова
Лимфома Ходжкина, аллогенная трансплантация костного мозга, брентуксимаб ведотин, ниволумаб.
Таблица 1. Характеристики пациентов и методы терапии (продолжение)


[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20327
[VALUE] => Array
(
[TEXT] => Evgeniya S. Borzenkova, Natalia B. Mikhailova, Kirill V. Lepik, Lilia V. Stelmakh, Anastasia V. Nekrasova, Ivan V. Tsygankov, Ivan S. Moiseev, Yuri R. Zalyalov, Elena I. Darskaya, Sergey N. Bondarenko, Boris V. Afanasyev<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Evgeniya S. Borzenkova, Natalia B. Mikhailova, Kirill V. Lepik, Lilia V. Stelmakh, Anastasia V. Nekrasova, Ivan V. Tsygankov, Ivan S. Moiseev, Yuri R. Zalyalov, Elena I. Darskaya, Sergey N. Bondarenko, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20328
[VALUE] => Array
(
[TEXT] => R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation; First St. Petersburg I. Pavlov State Medical University, St. Petersburg, Russia<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation; First St. Petersburg I. Pavlov State Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20345
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Allogeneic hematopoetic stem cell transplantation (allo-HSCT) has the curative potential for patients with relapsed and/or refractory classical Hodgkin lymphoma (cHL). Nevertheless, published data about therapy of relapse or progression (r/r) of cHL after alloHSCT is limited. The aim of single-center retrospective study was to identify prognostic factors in treatment of r/r cHL patients after allo-HSCT.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
This retrospective analysis included patients with r/r cHL (n=27), who had undergone allo-HSCT in our center from 2002 to 2017. Patients with documented relapse or progression of cHL after allo-HSCT were represented by 22.2% (n=6); patients with documented CR after allo-HSCT, but had relapse further, were represented by 25.9% (n=7); patients with first disease status after alloHST worse than CR (PR/SD) comprised 51.8% (n=14), including 7 patients with non-documented 1st disease status, such as PR/SD, based on cHL status before allo-HSCT, herewith CR and PD also were no documented. At the first staging after alloHSCT, CR was achieved in 7 patients (25.0%), PR was achieved in 10 patients (37.0%), 17 (62.9%) patients had objective response. Further on, 20 patients (74.0%) of 27 had progression or disease relapse after allo-HSCT, 19 patients of them received treatment, i.e., six patients of 20 received only chemotherapy (c/t; chemo) after allo-HSCT (ChVPP, LABO, vinblastine); 13 patients of 20 received novel monoclonal antibodies (Mabs), including brentuximab vedotin (BV) and nivolumab (Nivo), or their combination with chemotherapy. 8 patients of 20 did not receive treatment of cHL: three patients, due to other complications and poor performance status, and 5 patients with no documented 1st disease status (PR-1, SD-1) were at dynamic observation. BV-based regimens were used as the first-line Mab-therapy in all 13 Mab-treated patients (48.1%). Seven of them (53.8%; 25.9%), due to continuous progression, were transferred to second Mab- therapy line (with Nivolumab). Before treatment by Mab (BV) 5 of 13 patients received chemotherapy and 4 patients from 13 had got donor lymphocyte infusion (DLI). The patients characteristics are presented in Table 1.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
At the time of analysis, the median follow-up period was 27 (1.4-3.7) months. For patients with chemotherapy only, (n=6) median follow-up was 25 (6.27-55) months, patients with Mab-therapy (including combination with chemo) (n=13), 45mo (range, 23-73), and for non-treated patients (n=8), the median follow-up was 11 months (1.47-39.37). The median interval to progression/relapse of disease was 3.6 mo (1.3-11.3mo). Overall survival (OS) at the moment of analysis was 55% (15/27). The median interval between alloSCT and first dose of BV due to PD/RD was 4.7 (1.7- 44) mo. The median interval between alloSCT and first dose of Nivo was 38.7 months (range, 14.5-44.5). The median interval between last dose of BV and first dose of Nivo was 2.83 (1.23-32.47) months. At the moment of analysis 12 patients (44.4%) died: six with Hodgkin lymphoma progression, and six other patients were lost due to severe chronic GVHD (chGVHD) and infectious complications over post-transplant period, including 3 patients with Mab therapy, and one patient from the group of dynamic observation. 15 patient are alive: four patients with dynamic observation had achieved CR; six patients had achieved CR after Mab-therapy (5) and chemotherapy (1); 5 patients are continuing treatment because of stable or progressing disease. When compared with chemotherapy, Mab-therapy had prognostic significance (76.9% vs 16.7%, p=.003). Development of chGVHD also had prognostic significance (72.7% vs 43.9%, p=.084).
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
As based on a limited clinical material, we have demonstrated that the lymphoma progression was the cause of lethal outcomes in one third of patients, and therapy-related complications were fatal in almost the same number of patients. Despite relatively favorable outcome in heavily pretreated patients, further studies are required to determine optimal therapy for post-transplant relapse of cHL.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Hodgkin lymphoma, allogeneic hematopoetic stem cell transplantation, brentuximab vedotin, nivolumab.<br>
<img width="785" alt="table_1.png" src="/upload/medialibrary/ce5/table_1.png" height="757" title="table_1.png">
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
Allogeneic hematopoetic stem cell transplantation (allo-HSCT) has the curative potential for patients with relapsed and/or refractory classical Hodgkin lymphoma (cHL). Nevertheless, published data about therapy of relapse or progression (r/r) of cHL after alloHSCT is limited. The aim of single-center retrospective study was to identify prognostic factors in treatment of r/r cHL patients after allo-HSCT.
Patients and methods
This retrospective analysis included patients with r/r cHL (n=27), who had undergone allo-HSCT in our center from 2002 to 2017. Patients with documented relapse or progression of cHL after allo-HSCT were represented by 22.2% (n=6); patients with documented CR after allo-HSCT, but had relapse further, were represented by 25.9% (n=7); patients with first disease status after alloHST worse than CR (PR/SD) comprised 51.8% (n=14), including 7 patients with non-documented 1st disease status, such as PR/SD, based on cHL status before allo-HSCT, herewith CR and PD also were no documented. At the first staging after alloHSCT, CR was achieved in 7 patients (25.0%), PR was achieved in 10 patients (37.0%), 17 (62.9%) patients had objective response. Further on, 20 patients (74.0%) of 27 had progression or disease relapse after allo-HSCT, 19 patients of them received treatment, i.e., six patients of 20 received only chemotherapy (c/t; chemo) after allo-HSCT (ChVPP, LABO, vinblastine); 13 patients of 20 received novel monoclonal antibodies (Mabs), including brentuximab vedotin (BV) and nivolumab (Nivo), or their combination with chemotherapy. 8 patients of 20 did not receive treatment of cHL: three patients, due to other complications and poor performance status, and 5 patients with no documented 1st disease status (PR-1, SD-1) were at dynamic observation. BV-based regimens were used as the first-line Mab-therapy in all 13 Mab-treated patients (48.1%). Seven of them (53.8%; 25.9%), due to continuous progression, were transferred to second Mab- therapy line (with Nivolumab). Before treatment by Mab (BV) 5 of 13 patients received chemotherapy and 4 patients from 13 had got donor lymphocyte infusion (DLI). The patients characteristics are presented in Table 1.
Results
At the time of analysis, the median follow-up period was 27 (1.4-3.7) months. For patients with chemotherapy only, (n=6) median follow-up was 25 (6.27-55) months, patients with Mab-therapy (including combination with chemo) (n=13), 45mo (range, 23-73), and for non-treated patients (n=8), the median follow-up was 11 months (1.47-39.37). The median interval to progression/relapse of disease was 3.6 mo (1.3-11.3mo). Overall survival (OS) at the moment of analysis was 55% (15/27). The median interval between alloSCT and first dose of BV due to PD/RD was 4.7 (1.7- 44) mo. The median interval between alloSCT and first dose of Nivo was 38.7 months (range, 14.5-44.5). The median interval between last dose of BV and first dose of Nivo was 2.83 (1.23-32.47) months. At the moment of analysis 12 patients (44.4%) died: six with Hodgkin lymphoma progression, and six other patients were lost due to severe chronic GVHD (chGVHD) and infectious complications over post-transplant period, including 3 patients with Mab therapy, and one patient from the group of dynamic observation. 15 patient are alive: four patients with dynamic observation had achieved CR; six patients had achieved CR after Mab-therapy (5) and chemotherapy (1); 5 patients are continuing treatment because of stable or progressing disease. When compared with chemotherapy, Mab-therapy had prognostic significance (76.9% vs 16.7%, p=.003). Development of chGVHD also had prognostic significance (72.7% vs 43.9%, p=.084).
Conclusion
As based on a limited clinical material, we have demonstrated that the lymphoma progression was the cause of lethal outcomes in one third of patients, and therapy-related complications were fatal in almost the same number of patients. Despite relatively favorable outcome in heavily pretreated patients, further studies are required to determine optimal therapy for post-transplant relapse of cHL.
Keywords
Hodgkin lymphoma, allogeneic hematopoetic stem cell transplantation, brentuximab vedotin, nivolumab.

[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20329
[VALUE] => Therapy of relapse and progression of classical Hodgkin lymphoma after allogeneic hematopoetic stem cell transplantation
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Therapy of relapse and progression of classical Hodgkin lymphoma after allogeneic hematopoetic stem cell transplantation
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20745
[VALUE] => 1381
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1381
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20746
[VALUE] => 1382
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1382
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Евгения С. Борзенкова, Наталья Б. Михайлова, Кирилл В. Лепик, Лилия В. Стельмах, Анастасия В. Некрасова, Иван В. Цыганков, Иван С. Моисеев, Юрий Р. Залялов, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев
Введение
Аллогенная трансплантация гемопоэтических стволовых клеток (алло-ТГСК) имеет высокий потенциал излечения классической лимфомы Ходжкина (ЛХ) у пациентов с рефрактерным или рецидивирующим течением (р/рЛХ). Тем не менее, опубликованных данных о терапии рецидива или прогрессирования ЛХ после алло-ТГСК крайне мало. В одноцентровом исследовании была проведена попытка выявить прогностические факторы в лечение подобных пациентов.
Пациенты и методы
В этот ретроспективный анализ включены пациенты (n=27), прошедшие аллоТКМ в нашей клинике с 2002 по 2017 гг. Пациенты с подтвержденным прогрессиро-ванием заболевания после аллоТГСК составили 22,2% (n=6); пациенты с ПО, но c рецидивом или прогрессированием далее – 25,9% (n=7); пациенты с первым ответом хуже чем ПО (ЧО/СЗ) составили 51,8% (n=14), включая 7 пациентов c неподтвержденным 1-м статусом таким как ЧО/СЗ, основываясь на статусе заболевания перед аллоТКМ, при этом ПО и ПЗ также не подтверждены. При первом стадировании после алло-ТГСК у 7 пациентов зафиксирован ПО (25,0%), ЧО отмечен у 10 пациентов (37,0%), таким образом у 17 (62,9%) пациентов был общий ответ. За период наблюдения у 20 пациентов (74,0%) из 27 зафиксированы прогрессирование или рецидив ЛХ после аллоТКМ. 19 пациентов получили лечение: 6 пациентов получили только химиотерапию (х/т) после аллоТКМ (ChVPP, LABO, винбластин); 13 пациентов получили терапию новыми моноклональными антителами (МА): брентуксимаб ведотин (BV) и ниволумаб (Nivo), или сочетание их с химиотерапией. Остальные 8 пациентов были оставлены без терапии: 3 пациента (ЧО, СЗ, ПЗ) из-за осложнений алло-ТГСК и плохого соматического статуса; 5 пациентов из группы неподтвержденного статуса (ЧО-4, СЗ-1) – под динамическим наблюдением. 13 пациентов (48,1%). Терапию BV-содержащими схемами в качестве первой линии МА-терапии получили все 13 пациентов. 7 из них (53,8%; 25,9%) из-за продолжающегося прогрессирования ЛХ переведены на вторую линию терапии МА ниволумабом. До начала терапии MA (BV) 5 из 13 пациентов получили ХТ, и 4 пациента из 13 получили инфузии донорских лимфоцитов (ИЛД). Характеристики пациентов и методов представлены в таблице №1.
Результаты
На момент анализа время наблюдения за всеми пациентами (n=27) было 27 (1,4-3,7) мес. Для пациентов только с х/т (n=6) время наблюдения 25 (6,27-51) мес.; для 13 пациентов с МА-терапией – 45 мес. (23-73). Медиана наблюдения за пациентами без терапии (n=8) 11 мес. (1,47-39,37). Общая выживаемость для всех пациентов на момент анализа была 55% (n=15). Время от трансплантации до ПЗ/РЗ было 3,6 мес. (1,3-11,3 мес.). Среднее время от алло-ТГСК до начала терапии BV по поводу ПЗ/РЗ было 4,7 мес. (1,7-44 мес.). Среднее время от алло-ТГСК до начала терапии Nivo было 38,7 мес. (14,5-44,5). Среднее время между окончанием терапии BV и началом терапии Nivo было 2,83 (1,23-32,47) месяцев. На момент анализа 12 пациентов (44,4%) из 27 умерли: 6 из-за прогрессирования ЛХ и 6 пациентов из-за тяжелой хронической РТПХ (хрРТПХ) и инфекционных осложнений в посттрансплантационном периоде, включая 3 пациентов с МА-терапией и 1 пациента под динамическим наблюдением. 15 пациентов живы: у 4х пациентов в процессе наблюдения зафиксирован ПО; 6 пациентов в ПО после МА-терапии (5) и после ХТ (1); 5 пациентов продолжают лечение из-за стабилизации ли прогрессирования ЛХ. При сравнении результатов ХТ и терапии МА, прогностическим значением облада- ло лечение МА (76,9% против 16,7%, p=.003), также развитие хрРТПХ имело прогностическое значение (72,7% против 43,9%, p=.084).
Выводы
На небольшом клиническом материале было показано, что треть пациентов погибают от прогрессирования ЛХ и почти столько же от осложнений терапии. Несмотря на относительно благоприятный прогноз в этой тяжелой группе пациентов, требуются дальнейшие исследования для выбора оптимальной терапии посттрансплантационного рецидива и прогрессирования ЛХ.
Ключевые слова
Лимфома Ходжкина, аллогенная трансплантация костного мозга, брентуксимаб ведотин, ниволумаб.
Таблица 1. Характеристики пациентов и методы терапии (продолжение)


Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20373
[VALUE] => Array
(
[TEXT] => Анна А. Дмитрова, Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Дарья С. Дубняк, Вера А. Васильева, Ольга М. Королева, Зоя В. Конова, Анна А. Сидорова, Екатерина В. Усикова, Елена Н. Паровичникова, Валерий Г. Савченко
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Анна А. Дмитрова, Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Дарья С. Дубняк, Вера А. Васильева, Ольга М. Королева, Зоя В. Конова, Анна А. Сидорова, Екатерина В. Усикова, Елена Н. Паровичникова, Валерий Г. Савченко
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20374
[VALUE] => Array
(
[TEXT] => Отделение высокодозной химиотерапии и трансплантации костного мозга, ФГБУ «НМИЦ гематологии» МЗ РФ,<br>
Москва, Россия<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Отделение высокодозной химиотерапии и трансплантации костного мозга, ФГБУ «НМИЦ гематологии» МЗ РФ,
Москва, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20375
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Использование высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) является одной из наиболее актуальных методик профилактики РТПХ при выполнении трансплантации аллогенных гемопоэтических стволовых клеток крови (алло-ТГСК). Однако, влияние дополнительного введения ПТ-ЦФ на такой важный клинико-экономический параметр, как длительность пребывания в стационаре, и, соответственно, стоимость трансплантации остается не изученным. Здесь мы представляем анализ влияния введения высоких доз циклофосфамида с целью профилактики РТПХ после алло-ТГСК крови от неродственного донора на длительность госпитализации, связанной с проведением алло-ТГСК.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
В исследование были включены больные в ремиссии острого лейкоза, которым была выполнена первая трансплантация алло-ТГСК от неродственного полностью совместимого или частично совместимого донора. Все больные на момент анализа были выписаны из стационара без признаков РТПХ и отторжения в течение всей госпитализации. Всего в исследование было включено 39 больных. Всем пациентам в качестве профилактики РТПХ был использован режим: антитимоцитарный глобулин (АТГ) 40 мг/кг (-4 по -1 день); циклоспорин А 3 мг/кг/сут (с +5 дня); микофенолата мофетил 3000 мг/сут (с +5 дня). При использовании в качестве источника трансплантата неродственного частично совместимого донора пациентам также вводился ПТ-ЦФ в дозе 50 мг/кг на +3, +4 день. Детальные характеристики представлены в таблице 1 (см. выше).
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Данные по длительности госпитализации представлены на Рисунке 1 (см. выше). Согласно проведенному анализу, длительность госпитализации у пациентов в ремиссии острого лейкоза, которым была выполнена трансплантация алло-ТГСК с использованием ПТ-ЦФ и без ПТ-ЦФ составила 43 дня (14-126) и 48 дней (32-98) соответственно (p=0,48).
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Таким образом, использование циклофосфамида на + 3, + 4 день с целью профилактики РТПХ не удлиняет период госпитализации при проведении алло-ТГСК у пациентов в ремиссии острого лейкоза.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Трансплантация аллогенного костного мозга, иммуносупрессивная терапия, циклофосфамид, длительность госпитализации, неродственный донор.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Использование высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) является одной из наиболее актуальных методик профилактики РТПХ при выполнении трансплантации аллогенных гемопоэтических стволовых клеток крови (алло-ТГСК). Однако, влияние дополнительного введения ПТ-ЦФ на такой важный клинико-экономический параметр, как длительность пребывания в стационаре, и, соответственно, стоимость трансплантации остается не изученным. Здесь мы представляем анализ влияния введения высоких доз циклофосфамида с целью профилактики РТПХ после алло-ТГСК крови от неродственного донора на длительность госпитализации, связанной с проведением алло-ТГСК.
Пациенты и методы
В исследование были включены больные в ремиссии острого лейкоза, которым была выполнена первая трансплантация алло-ТГСК от неродственного полностью совместимого или частично совместимого донора. Все больные на момент анализа были выписаны из стационара без признаков РТПХ и отторжения в течение всей госпитализации. Всего в исследование было включено 39 больных. Всем пациентам в качестве профилактики РТПХ был использован режим: антитимоцитарный глобулин (АТГ) 40 мг/кг (-4 по -1 день); циклоспорин А 3 мг/кг/сут (с +5 дня); микофенолата мофетил 3000 мг/сут (с +5 дня). При использовании в качестве источника трансплантата неродственного частично совместимого донора пациентам также вводился ПТ-ЦФ в дозе 50 мг/кг на +3, +4 день. Детальные характеристики представлены в таблице 1 (см. выше).
Результаты
Данные по длительности госпитализации представлены на Рисунке 1 (см. выше). Согласно проведенному анализу, длительность госпитализации у пациентов в ремиссии острого лейкоза, которым была выполнена трансплантация алло-ТГСК с использованием ПТ-ЦФ и без ПТ-ЦФ составила 43 дня (14-126) и 48 дней (32-98) соответственно (p=0,48).
Заключение
Таким образом, использование циклофосфамида на + 3, + 4 день с целью профилактики РТПХ не удлиняет период госпитализации при проведении алло-ТГСК у пациентов в ремиссии острого лейкоза.
Ключевые слова
Трансплантация аллогенного костного мозга, иммуносупрессивная терапия, циклофосфамид, длительность госпитализации, неродственный донор.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20376
[VALUE] => Array
(
[TEXT] => Anna A. Dmitrova, Mikhail Yu. Drokov, Larisa A. Kuzmina, Natalia N. Popova, Ekaterina D. Mikhaltsova, Darya S. Dubnyak, Vera A. Vasilyeva, Olga M. Koroleva, Zoya V. Konova, Anna A. Sidorova, Ekaterina V. Usikova, Elena N. Parovichnikova, Valery G. Savchenko
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Anna A. Dmitrova, Mikhail Yu. Drokov, Larisa A. Kuzmina, Natalia N. Popova, Ekaterina D. Mikhaltsova, Darya S. Dubnyak, Vera A. Vasilyeva, Olga M. Koroleva, Zoya V. Konova, Anna A. Sidorova, Ekaterina V. Usikova, Elena N. Parovichnikova, Valery G. Savchenko
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20377
[VALUE] => Array
(
[TEXT] => Department of High-Dose Chemotherapy and BMT, National Research Center for Hematology, Ministry of Healthcare of the Russian Federation, Moscow, Russian Federation<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Department of High-Dose Chemotherapy and BMT, National Research Center for Hematology, Ministry of Healthcare of the Russian Federation, Moscow, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20464
[VALUE] => Array
(
[TEXT] => <h2>Introduction</h2>
<p style="text-align: justify;">
Using posttransplant high-dose cyclophosphamide (PT-CY) as the graft versus host disease (GvHD) prophylaxis is an important option to prevent the GvHD in patients after allogeneic hematopoietic stem cell transplantation (allo-HCT) with a “high-grade” HLA-disparity (unrelated, haploidentical donor). However, the influence of PT-CY on the length ofhospital stay and the cost of hospitalization still remains unknown. Here we report data about impact of PT-CY on the length of hospital stay in leukemia patients after allo-HSCT from unrelated donor.
</p>
<p style="text-align: justify;">
<img width="385" alt="11_Figure 1. The duration of hospitalization.png" src="/upload/medialibrary/f83/11_figure-1.-the-duration-of-hospitalization.png" height="265" title="11_Figure 1. The duration of hospitalization.png"><br>
</p>
<p style="text-align: justify;">
Figure 1. The duration of hospitalization for the patients in complete remission of acute leukemia, who underwent allo-HSCT from unrelated donors using PT-CY and without using PT-CY
</p>
<h2 style="text-align: justify;">
Patients and methods </h2>
<p style="text-align: justify;">
We included 39 patients in the complete remission of acute leukemia, whom allo-HSCT was performed from unrelated or mismatched unrelated donors. At the time of analysis, all patients were discharged from the hospital without any signs of GvHD or graft failure. Detailed characteristics of patients are presented in Table 1. To prevent the GvHD all patients recieve: anti-thymocyte globulin (ATG) 40 mg/kg (on days -4 to -1), cyclosporine A (CSA) 3 mg/kg/day (from +5 day), mycophenolate mofetil (MMF) 3000 mg/day (from + 5 day). After performing allo-HSCT from mismatched unrelated donor, the patients were also treated with PT-CY (50 mg/kg on +3, +4 day).
</p>
<h2 style="text-align: justify;">
Results </h2>
<p style="text-align: justify;">
Length of hospital stay for all patients is presented in Figure 1. According to our analysis, length of hospital stay in patients after allo-HSCT with and without PT-CY was 43 days (14 to 126) versus 48 days (32 to 98) accordingly (p=0.48).
</p>
<h2 style="text-align: justify;">
Conclusion </h2>
<p style="text-align: justify;">
Usage of PT-CY on day +3, +4 in prevention of GVHD does not extend the hospitalization period in leukemia patients transplanted in complete remission.
</p>
<h2 style="text-align: justify;">
Keywords </h2>
<p style="text-align: justify;">
Allogeneic bone marrow transplantation, immunosuppressive therapy, posttransplant high-dose cyclophosphamide, hospital stay, unrelated donor.
</p>
<h2 style="text-align: justify;">
Table 1. Characteristics of the patients<br>
</h2>
<img width="783" alt="11_Table 1. Characteristics of the patients.png" src="/upload/medialibrary/67d/11_table-1.-characteristics-of-the-patients.png" height="363" title="11_Table 1. Characteristics of the patients.png"><br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
Using posttransplant high-dose cyclophosphamide (PT-CY) as the graft versus host disease (GvHD) prophylaxis is an important option to prevent the GvHD in patients after allogeneic hematopoietic stem cell transplantation (allo-HCT) with a “high-grade” HLA-disparity (unrelated, haploidentical donor). However, the influence of PT-CY on the length ofhospital stay and the cost of hospitalization still remains unknown. Here we report data about impact of PT-CY on the length of hospital stay in leukemia patients after allo-HSCT from unrelated donor.

Figure 1. The duration of hospitalization for the patients in complete remission of acute leukemia, who underwent allo-HSCT from unrelated donors using PT-CY and without using PT-CY
Patients and methods
We included 39 patients in the complete remission of acute leukemia, whom allo-HSCT was performed from unrelated or mismatched unrelated donors. At the time of analysis, all patients were discharged from the hospital without any signs of GvHD or graft failure. Detailed characteristics of patients are presented in Table 1. To prevent the GvHD all patients recieve: anti-thymocyte globulin (ATG) 40 mg/kg (on days -4 to -1), cyclosporine A (CSA) 3 mg/kg/day (from +5 day), mycophenolate mofetil (MMF) 3000 mg/day (from + 5 day). After performing allo-HSCT from mismatched unrelated donor, the patients were also treated with PT-CY (50 mg/kg on +3, +4 day).
Results
Length of hospital stay for all patients is presented in Figure 1. According to our analysis, length of hospital stay in patients after allo-HSCT with and without PT-CY was 43 days (14 to 126) versus 48 days (32 to 98) accordingly (p=0.48).
Conclusion
Usage of PT-CY on day +3, +4 in prevention of GVHD does not extend the hospitalization period in leukemia patients transplanted in complete remission.
Keywords
Allogeneic bone marrow transplantation, immunosuppressive therapy, posttransplant high-dose cyclophosphamide, hospital stay, unrelated donor.
Table 1. Characteristics of the patients

[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20378
[VALUE] => Impact of using posttransplant high-dose cyclophosphamide (PT-CY) on the length of hospital stay in patients with acute leukemia in complete remission
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Impact of using posttransplant high-dose cyclophosphamide (PT-CY) on the length of hospital stay in patients with acute leukemia in complete remission
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20753
[VALUE] => 1389
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1389
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20754
[VALUE] => 1390
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1390
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Анна А. Дмитрова, Михаил Ю. Дроков, Лариса А. Кузьмина, Наталья Н. Попова, Екатерина Д. Михальцова, Дарья С. Дубняк, Вера А. Васильева, Ольга М. Королева, Зоя В. Конова, Анна А. Сидорова, Екатерина В. Усикова, Елена Н. Паровичникова, Валерий Г. Савченко
Москва, Россия
Введение
Использование высоких доз посттрансплантационного циклофосфамида (ПТ-ЦФ) является одной из наиболее актуальных методик профилактики РТПХ при выполнении трансплантации аллогенных гемопоэтических стволовых клеток крови (алло-ТГСК). Однако, влияние дополнительного введения ПТ-ЦФ на такой важный клинико-экономический параметр, как длительность пребывания в стационаре, и, соответственно, стоимость трансплантации остается не изученным. Здесь мы представляем анализ влияния введения высоких доз циклофосфамида с целью профилактики РТПХ после алло-ТГСК крови от неродственного донора на длительность госпитализации, связанной с проведением алло-ТГСК.
Пациенты и методы
В исследование были включены больные в ремиссии острого лейкоза, которым была выполнена первая трансплантация алло-ТГСК от неродственного полностью совместимого или частично совместимого донора. Все больные на момент анализа были выписаны из стационара без признаков РТПХ и отторжения в течение всей госпитализации. Всего в исследование было включено 39 больных. Всем пациентам в качестве профилактики РТПХ был использован режим: антитимоцитарный глобулин (АТГ) 40 мг/кг (-4 по -1 день); циклоспорин А 3 мг/кг/сут (с +5 дня); микофенолата мофетил 3000 мг/сут (с +5 дня). При использовании в качестве источника трансплантата неродственного частично совместимого донора пациентам также вводился ПТ-ЦФ в дозе 50 мг/кг на +3, +4 день. Детальные характеристики представлены в таблице 1 (см. выше).
Результаты
Данные по длительности госпитализации представлены на Рисунке 1 (см. выше). Согласно проведенному анализу, длительность госпитализации у пациентов в ремиссии острого лейкоза, которым была выполнена трансплантация алло-ТГСК с использованием ПТ-ЦФ и без ПТ-ЦФ составила 43 дня (14-126) и 48 дней (32-98) соответственно (p=0,48).
Заключение
Таким образом, использование циклофосфамида на + 3, + 4 день с целью профилактики РТПХ не удлиняет период госпитализации при проведении алло-ТГСК у пациентов в ремиссии острого лейкоза.
Ключевые слова
Трансплантация аллогенного костного мозга, иммуносупрессивная терапия, циклофосфамид, длительность госпитализации, неродственный донор.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20381
[VALUE] => Array
(
[TEXT] => Анна А. Доценко <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Елена А. Суркова <sup>1</sup>, Дарья А. Кузнецова <sup>2</sup>, Сергей В. Лапин <sup>2</sup>, Варвара Н. Овечкина <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Елена В. Морозова <sup>1</sup>, Сергей Н. Бондаренко <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Анна А. Доценко 1, Иван С. Моисеев 1, Елена А. Суркова 1, Дарья А. Кузнецова 2, Сергей В. Лапин 2, Варвара Н. Овечкина 1, Елена И. Дарская 1, Елена В. Морозова 1, Сергей Н. Бондаренко 1, Борис В. Афанасьев 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20461
[VALUE] => Array
(
[TEXT] => <sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова<br>
<sup>2</sup> Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова, Санкт-Петербург, Россия<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова
2 Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20382
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения многих онкологических заболеваний, а число трансплантаций растет во всем мире. На данный момент проводится множество клинических испытаний для усовершенствования и разработки более эффективных способов кондиционирования и профилактики РТПХ, главной задачей которых является уменьшение реакции трансплантатпротив хозяина и индуцирование реакции транплантат против лейкоза. С этой целью в НИИ ДОГиТ им. Р. М. Горбачевой в рамках клинического исследования был использован посттрансплантационный бендамустин (ПТБ). Одной из побочных реакций данного режима кондиционирования стало развитие синдрома выброса цитокинов (СВЦ). Понимание динамики цитокинов в развитии этого синдрома позволяет прогнозировать его развитие и проводить адекватную терапию.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
В проспективное исследование (NCT02799147) вошли 12 пациентов: 8 с острым миелобастным лейкозом, 4 с острым лимфобластным лейкозом. Все пациенты имели химиорезистентное течение лейкоза и остутсвие ремиссии на момент трансплантата. Медиана возраста пациентов составила 38 лет (от 24 до 54 лет). Пациенты получали профилактику РТПХ бендамустином 100-140 мг/м2 в Д+3,+4. Всем пациентам был проведен миелоаблативный режим кондиционирования с использованием флударабина и бусульфана. Забор крови с последующим анализом уровня цитокинов (IFN-γ, IL-1, IL-10, IL-6, IL-17) осуществлялся в день -7, 0, +7, +14. У 8/12 развился синдром высвобождения цитокинов.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
У всех пациентов на момент первого забора крови уже определялся высокий уровень цитокинов. Тем не менее, после приживления выявлено дальнейшее повышение IFN-γ (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). Частота СВЦ составила 66,7% (n=8) в исследуемой группе, однако, достоверная связь с СВЦ была выявлена только для IL-6 (74 vs 8 ng/ml, p=0.036). Уровень IL-6 при этом не прогнозировал летальность от осложнений (76 vs 19 ng/ml, р=0.21). Частота СВЦ 1-2 степени тяжести составила 33,3% (n=4), 3-4 степени 33,3% (n=4). Наиболее частыми клиническими проявлениями цитокинового синдрома были лихорадка (100%), повышение уровня креатинина (90%), СРБ (100%), билирубина и трансаминаз (67%), острое повреждение почек (56%), гипотензия (50%), токсичность в отношении ЦНС (33%), ДВС-синдром (22%) и др.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Выявлено, что терапия ПТБ ассоциирована с повышением IFN-γ, IL-10, IL-6, однако только повышение IL-6 ассоциировано с СВЦ. Полученные результаты говорят о рациональности использования анти-IL6 терапии.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Реакция «трансплантат против хозяина», синдром выброса цитокинов, бендамустин после трансплантации.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения многих онкологических заболеваний, а число трансплантаций растет во всем мире. На данный момент проводится множество клинических испытаний для усовершенствования и разработки более эффективных способов кондиционирования и профилактики РТПХ, главной задачей которых является уменьшение реакции трансплантатпротив хозяина и индуцирование реакции транплантат против лейкоза. С этой целью в НИИ ДОГиТ им. Р. М. Горбачевой в рамках клинического исследования был использован посттрансплантационный бендамустин (ПТБ). Одной из побочных реакций данного режима кондиционирования стало развитие синдрома выброса цитокинов (СВЦ). Понимание динамики цитокинов в развитии этого синдрома позволяет прогнозировать его развитие и проводить адекватную терапию.
Материалы и методы
В проспективное исследование (NCT02799147) вошли 12 пациентов: 8 с острым миелобастным лейкозом, 4 с острым лимфобластным лейкозом. Все пациенты имели химиорезистентное течение лейкоза и остутсвие ремиссии на момент трансплантата. Медиана возраста пациентов составила 38 лет (от 24 до 54 лет). Пациенты получали профилактику РТПХ бендамустином 100-140 мг/м2 в Д+3,+4. Всем пациентам был проведен миелоаблативный режим кондиционирования с использованием флударабина и бусульфана. Забор крови с последующим анализом уровня цитокинов (IFN-γ, IL-1, IL-10, IL-6, IL-17) осуществлялся в день -7, 0, +7, +14. У 8/12 развился синдром высвобождения цитокинов.
Результаты
У всех пациентов на момент первого забора крови уже определялся высокий уровень цитокинов. Тем не менее, после приживления выявлено дальнейшее повышение IFN-γ (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). Частота СВЦ составила 66,7% (n=8) в исследуемой группе, однако, достоверная связь с СВЦ была выявлена только для IL-6 (74 vs 8 ng/ml, p=0.036). Уровень IL-6 при этом не прогнозировал летальность от осложнений (76 vs 19 ng/ml, р=0.21). Частота СВЦ 1-2 степени тяжести составила 33,3% (n=4), 3-4 степени 33,3% (n=4). Наиболее частыми клиническими проявлениями цитокинового синдрома были лихорадка (100%), повышение уровня креатинина (90%), СРБ (100%), билирубина и трансаминаз (67%), острое повреждение почек (56%), гипотензия (50%), токсичность в отношении ЦНС (33%), ДВС-синдром (22%) и др.
Заключение
Выявлено, что терапия ПТБ ассоциирована с повышением IFN-γ, IL-10, IL-6, однако только повышение IL-6 ассоциировано с СВЦ. Полученные результаты говорят о рациональности использования анти-IL6 терапии.
Ключевые слова
Реакция «трансплантат против хозяина», синдром выброса цитокинов, бендамустин после трансплантации.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20383
[VALUE] => Array
(
[TEXT] => Anna A. Dotsenko <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Elena A. Surkova <sup>1</sup>, Daria A. Kuznetcova <sup>2</sup>, Sergey V. Lapin <sup>2</sup>, Varvara N. Ovechkina <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Elena V. Morozova <sup>1</sup>, Sergey N. Bondarenko <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Anna A. Dotsenko 1, Ivan S. Moiseev 1, Elena A. Surkova 1, Daria A. Kuznetcova 2, Sergey V. Lapin 2, Varvara N. Ovechkina 1, Elena I. Darskaya 1, Elena V. Morozova 1, Sergey N. Bondarenko 1, Boris V. Afanasyev 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20384
[VALUE] => Array
(
[TEXT] => <sup>1</sup> R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation<br>
<sup>2</sup> Laboratory of Autoimmune Diagnostics, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation
2 Laboratory of Autoimmune Diagnostics, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20463
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Hematopoietic stem cells transplantation is an effective method of treatment of many cancer diseases and the number of transplants is increasing worldwide. There are many clinical trials under way to improve and develop more effective conditioning methods, the main task is to reduce graft-versushost disease and to induce graft versus leukemia response. For this goal posttransplant bendamustine (PTB) was used at the R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation in the setting of a clinical trial. One of the adverse reactions of this conditioning regimen was development of a life-threatening complication – cytokine release syndrome (CRS). Understanding dynamics of cytokines in the development of this syndrome allows to predict its development and to conduct relevant therapy.
</p>
<h2 style="text-align: justify;">Materials and methods</h2>
<p style="text-align: justify;">
We carried out a prospective study (NCT02799147), which included 12 patients: 8 with acute myeloid leukemia, 4 with acute lymphoblastic leukemia. All patients had chemorefractory disease and absence of hematologic remission at the start of the conditioning. The median age was 38 years (from 24 to 54 years old). All patients received a prophylaxis of GVHD with bendamustine 100-140 mg/m2 per day +3, +4. Myeloablative conditioning regimen with fludarabine and busulfan was applied in all patients. Blood sampling with subsequent analysis of the level of cytokines (IFN-γ, IL-1, IL-10, IL-6, IL-17) was performed on day -7, 0, +7, +14. The cytokine release syndrome developed in 8/12 patients.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
High cytokine level was determined starting from the first blood sample in all patients. However, after engraftment, a further increase was detected in IFN-γ level (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). The frequency of CRS was 66.7% (n=8) in study group, but positive association with the CRS was detected only for IL-6 (74 vs 8 ng/ml, p=0.036). The level of IL-6 wasn’t a predictor of mortality from complications (76 vs 19 ng/ml, р=0.21). The frequency of CRS grades 1-2 was 33.3% (n=4), grades 3-4 was 33.3% (n=4). The most frequent clinical manifestations of CRS were fever (100%), increase in creatinine (90%), CRP (100%), bilirubin and transaminases (67%), acute kidney injury (56%), hypotension (50%), CNS toxicity (33%), disseminated intravascular coagulation syndrome (22%) and others.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
The prophylaxis of GVHD with posttransplant bendamustine is associated with the increase of IFN-γ, IL-10, IL-6, however, only the increase of IL-6 was associated with CRS. These results confirmed the rationality of using anti-IL6 therapy.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Graft-versus-host disease, cytokine release syndrome (CRS), posttransplant bendamustine (PTB).
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
Hematopoietic stem cells transplantation is an effective method of treatment of many cancer diseases and the number of transplants is increasing worldwide. There are many clinical trials under way to improve and develop more effective conditioning methods, the main task is to reduce graft-versushost disease and to induce graft versus leukemia response. For this goal posttransplant bendamustine (PTB) was used at the R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation in the setting of a clinical trial. One of the adverse reactions of this conditioning regimen was development of a life-threatening complication – cytokine release syndrome (CRS). Understanding dynamics of cytokines in the development of this syndrome allows to predict its development and to conduct relevant therapy.
Materials and methods
We carried out a prospective study (NCT02799147), which included 12 patients: 8 with acute myeloid leukemia, 4 with acute lymphoblastic leukemia. All patients had chemorefractory disease and absence of hematologic remission at the start of the conditioning. The median age was 38 years (from 24 to 54 years old). All patients received a prophylaxis of GVHD with bendamustine 100-140 mg/m2 per day +3, +4. Myeloablative conditioning regimen with fludarabine and busulfan was applied in all patients. Blood sampling with subsequent analysis of the level of cytokines (IFN-γ, IL-1, IL-10, IL-6, IL-17) was performed on day -7, 0, +7, +14. The cytokine release syndrome developed in 8/12 patients.
Results
High cytokine level was determined starting from the first blood sample in all patients. However, after engraftment, a further increase was detected in IFN-γ level (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). The frequency of CRS was 66.7% (n=8) in study group, but positive association with the CRS was detected only for IL-6 (74 vs 8 ng/ml, p=0.036). The level of IL-6 wasn’t a predictor of mortality from complications (76 vs 19 ng/ml, р=0.21). The frequency of CRS grades 1-2 was 33.3% (n=4), grades 3-4 was 33.3% (n=4). The most frequent clinical manifestations of CRS were fever (100%), increase in creatinine (90%), CRP (100%), bilirubin and transaminases (67%), acute kidney injury (56%), hypotension (50%), CNS toxicity (33%), disseminated intravascular coagulation syndrome (22%) and others.
Conclusion
The prophylaxis of GVHD with posttransplant bendamustine is associated with the increase of IFN-γ, IL-10, IL-6, however, only the increase of IL-6 was associated with CRS. These results confirmed the rationality of using anti-IL6 therapy.
Keywords
Graft-versus-host disease, cytokine release syndrome (CRS), posttransplant bendamustine (PTB).
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20385
[VALUE] => Cytokine release syndrome after GVHD prophylaxis with posttransplant bendamustine
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Cytokine release syndrome after GVHD prophylaxis with posttransplant bendamustine
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20755
[VALUE] => 1391
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1391
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20756
[VALUE] => 1392
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1392
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Анна А. Доценко 1, Иван С. Моисеев 1, Елена А. Суркова 1, Дарья А. Кузнецова 2, Сергей В. Лапин 2, Варвара Н. Овечкина 1, Елена И. Дарская 1, Елена В. Морозова 1, Сергей Н. Бондаренко 1, Борис В. Афанасьев 1
2 Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова, Санкт-Петербург, Россия
Введение
Трансплантация гемопоэтических стволовых клеток является эффективным методом лечения многих онкологических заболеваний, а число трансплантаций растет во всем мире. На данный момент проводится множество клинических испытаний для усовершенствования и разработки более эффективных способов кондиционирования и профилактики РТПХ, главной задачей которых является уменьшение реакции трансплантатпротив хозяина и индуцирование реакции транплантат против лейкоза. С этой целью в НИИ ДОГиТ им. Р. М. Горбачевой в рамках клинического исследования был использован посттрансплантационный бендамустин (ПТБ). Одной из побочных реакций данного режима кондиционирования стало развитие синдрома выброса цитокинов (СВЦ). Понимание динамики цитокинов в развитии этого синдрома позволяет прогнозировать его развитие и проводить адекватную терапию.
Материалы и методы
В проспективное исследование (NCT02799147) вошли 12 пациентов: 8 с острым миелобастным лейкозом, 4 с острым лимфобластным лейкозом. Все пациенты имели химиорезистентное течение лейкоза и остутсвие ремиссии на момент трансплантата. Медиана возраста пациентов составила 38 лет (от 24 до 54 лет). Пациенты получали профилактику РТПХ бендамустином 100-140 мг/м2 в Д+3,+4. Всем пациентам был проведен миелоаблативный режим кондиционирования с использованием флударабина и бусульфана. Забор крови с последующим анализом уровня цитокинов (IFN-γ, IL-1, IL-10, IL-6, IL-17) осуществлялся в день -7, 0, +7, +14. У 8/12 развился синдром высвобождения цитокинов.
Результаты
У всех пациентов на момент первого забора крови уже определялся высокий уровень цитокинов. Тем не менее, после приживления выявлено дальнейшее повышение IFN-γ (18 vs 197 ng/ml, p=0.037), IL-10 (6.3 vs 110 ng/ml, p=0.23), IL-6 (96 vs 105 ng/ml, p=0.23). Частота СВЦ составила 66,7% (n=8) в исследуемой группе, однако, достоверная связь с СВЦ была выявлена только для IL-6 (74 vs 8 ng/ml, p=0.036). Уровень IL-6 при этом не прогнозировал летальность от осложнений (76 vs 19 ng/ml, р=0.21). Частота СВЦ 1-2 степени тяжести составила 33,3% (n=4), 3-4 степени 33,3% (n=4). Наиболее частыми клиническими проявлениями цитокинового синдрома были лихорадка (100%), повышение уровня креатинина (90%), СРБ (100%), билирубина и трансаминаз (67%), острое повреждение почек (56%), гипотензия (50%), токсичность в отношении ЦНС (33%), ДВС-синдром (22%) и др.
Заключение
Выявлено, что терапия ПТБ ассоциирована с повышением IFN-γ, IL-10, IL-6, однако только повышение IL-6 ассоциировано с СВЦ. Полученные результаты говорят о рациональности использования анти-IL6 терапии.
Ключевые слова
Реакция «трансплантат против хозяина», синдром выброса цитокинов, бендамустин после трансплантации.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20364
[VALUE] => Array
(
[TEXT] => Марина В. Демченкова, Екатерина В. Зубкова, Дмитрий Д. Мориков, Людмила Е. Иванова, Анна В. Шевчук, Зоя В. Дьяконенко, Алена Л. Хороших, Александра Ю. Ефиркина
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Марина В. Демченкова, Екатерина В. Зубкова, Дмитрий Д. Мориков, Людмила Е. Иванова, Анна В. Шевчук, Зоя В. Дьяконенко, Алена Л. Хороших, Александра Ю. Ефиркина
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20365
[VALUE] => Array
(
[TEXT] => ГБУЗ «Областной онкологический диспансер», Иркутск, Россия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => ГБУЗ «Областной онкологический диспансер», Иркутск, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20366
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Ежегодно на базе Иркутского онкологического диспансера диагностируется 50 новых случаев лимфомы Ходжкина. Несмотря на достигнутые успехи в лечении лимфомы Ходжкина, проблемой терапии является развитие рецидивов заболевания и первичной/вторичной резистентности у 10-25% больных. Применение высокодозной химиотерапии (ВДХТ) с ауто-ТГСК является стандартом терапии при рецидивах и резистентных формах ЛХ.
</p>
<h2 style="text-align: justify;">Цель</h2>
<p style="text-align: justify;">
Оценить эффективность и безопасность II линии терапии у больных с рецидивами и резистентными формами лимфомы Ходжина в Иркутском областном онкологическом диспансере за 2-х летний период (2016-2018).
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
Проведен анализ течения заболевания 11 пациентов с ЛХ, госпитализированных в Иркутский онкологический диспансер с января 2016 по июнь 2018 г для проведения II линии терапии. Медиана возраста пациентов составила 34 года (22-46). Распределение по полу: мужчин – 6, женщин – 5. Преобладали пациенты с распространенными стадиями заболевания: 8 – III-IV стадия, и лишь у 3 – II стадия ЛХ. Среднее количество циклов терапии 1 линии – 15 (от 8 до 25 циклов). Все пациенты в качестве индукционной терапии получили ПХТ по схеме ABVD и BEACOPP, лучевая терапия проводилась 10 пациентам.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
На момент начала II линии терапии 5 человек имели рецидив ЛХ: ранний (n=2) и поздний (n=2), у 6 человек регистрировалась резистентность к проводимой терапии: первичная (n=2), вторичная (n=4). Медиана времени от момента диагностики ЛХ до проведения трансплантации составила 1 год (1 год – 10 лет 9 мес.). Все пациенты получили кондиционирование по протоколу BeEAM. Стволовые кроветворные клетки получали из костного мозга (n=1), периферической крови (n=10). Клеточность трансплантанта в среднем составляла 7,99х106/кг. В качестве подготовки к ВДХТ с ауто-ТГСК проводились курсы терапии по программе DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). Статус ЛХ на момент ауто-ТГСК: полная ремиссия (ПР) – 5 пациентов, частичная ремиссия (ЧР) – 5, нет ответа – 1 больной. Летальность, связанная с ВДХТ и ауто-ТГСК на «день 100» составила 0%. Оценка ответа по завершении терапии II линии проведена у 9 пациентов: полная ремиссия была достигнута у 6 пациентов (67%), у 3-х пациентов (33%) не получено ответа на проводимую терапию, что вероятно обусловлено отсутствием достижения полной ремиссии перед ауто-ТГСК (n=1) и длительным интервалом времени до ВДХТ. Общая выживаемость 100%, с медианой наблюдения 18 месяцев от начала II линии терапии.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Наш опыт подтверждает безопасность II линии терапии, включающей ВДХТ с ауто-ТГСК для лечения рефрактерных форм ЛХ. Эффективность II линии зависит от от достижения полной ремиссии до ауто-ТГКС и интервалом времени от момента диагностики ЛХ до проведения ВДХТ с ауто-ТГСК.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Лимфома Ходжкина, рецидив, рефрактерность, высокодозная химиотерапия, ауто-ТГСК.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Ежегодно на базе Иркутского онкологического диспансера диагностируется 50 новых случаев лимфомы Ходжкина. Несмотря на достигнутые успехи в лечении лимфомы Ходжкина, проблемой терапии является развитие рецидивов заболевания и первичной/вторичной резистентности у 10-25% больных. Применение высокодозной химиотерапии (ВДХТ) с ауто-ТГСК является стандартом терапии при рецидивах и резистентных формах ЛХ.
Цель
Оценить эффективность и безопасность II линии терапии у больных с рецидивами и резистентными формами лимфомы Ходжина в Иркутском областном онкологическом диспансере за 2-х летний период (2016-2018).
Пациенты и методы
Проведен анализ течения заболевания 11 пациентов с ЛХ, госпитализированных в Иркутский онкологический диспансер с января 2016 по июнь 2018 г для проведения II линии терапии. Медиана возраста пациентов составила 34 года (22-46). Распределение по полу: мужчин – 6, женщин – 5. Преобладали пациенты с распространенными стадиями заболевания: 8 – III-IV стадия, и лишь у 3 – II стадия ЛХ. Среднее количество циклов терапии 1 линии – 15 (от 8 до 25 циклов). Все пациенты в качестве индукционной терапии получили ПХТ по схеме ABVD и BEACOPP, лучевая терапия проводилась 10 пациентам.
Результаты
На момент начала II линии терапии 5 человек имели рецидив ЛХ: ранний (n=2) и поздний (n=2), у 6 человек регистрировалась резистентность к проводимой терапии: первичная (n=2), вторичная (n=4). Медиана времени от момента диагностики ЛХ до проведения трансплантации составила 1 год (1 год – 10 лет 9 мес.). Все пациенты получили кондиционирование по протоколу BeEAM. Стволовые кроветворные клетки получали из костного мозга (n=1), периферической крови (n=10). Клеточность трансплантанта в среднем составляла 7,99х106/кг. В качестве подготовки к ВДХТ с ауто-ТГСК проводились курсы терапии по программе DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). Статус ЛХ на момент ауто-ТГСК: полная ремиссия (ПР) – 5 пациентов, частичная ремиссия (ЧР) – 5, нет ответа – 1 больной. Летальность, связанная с ВДХТ и ауто-ТГСК на «день 100» составила 0%. Оценка ответа по завершении терапии II линии проведена у 9 пациентов: полная ремиссия была достигнута у 6 пациентов (67%), у 3-х пациентов (33%) не получено ответа на проводимую терапию, что вероятно обусловлено отсутствием достижения полной ремиссии перед ауто-ТГСК (n=1) и длительным интервалом времени до ВДХТ. Общая выживаемость 100%, с медианой наблюдения 18 месяцев от начала II линии терапии.
Заключение
Наш опыт подтверждает безопасность II линии терапии, включающей ВДХТ с ауто-ТГСК для лечения рефрактерных форм ЛХ. Эффективность II линии зависит от от достижения полной ремиссии до ауто-ТГКС и интервалом времени от момента диагностики ЛХ до проведения ВДХТ с ауто-ТГСК.
Ключевые слова
Лимфома Ходжкина, рецидив, рефрактерность, высокодозная химиотерапия, ауто-ТГСК.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20367
[VALUE] => Array
(
[TEXT] => Marina V. Demchenkova, Ekaterina V. Zubkova, Dmitriy D. Morikov, Lyudmila E. Ivanova, Anna V. Shevchuk, Zoya V. Dyakonenko, Alena L. Khoroshikh, Alexandra Yu. Efirkina
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Marina V. Demchenkova, Ekaterina V. Zubkova, Dmitriy D. Morikov, Lyudmila E. Ivanova, Anna V. Shevchuk, Zoya V. Dyakonenko, Alena L. Khoroshikh, Alexandra Yu. Efirkina
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20368
[VALUE] => Array
(
[TEXT] => State Regional Clinical Hospital “Regional Oncology Center”, Irkutsk, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => State Regional Clinical Hospital “Regional Oncology Center”, Irkutsk, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20369
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Fifty new cases of Hodgkin’s lymphoma (HL) are diagnosed annually in the Irkutsk Oncology Center. Despite the successes achieved in the treatment of HL from 10 to 25% of patients have refractory or relapse. The high-dose chemotherapy (HDCT) followed by auto-SCT is the standard therapy of relapsed/refractory HL. Purpose of our study was to estimate efficacy and safety of second line therapy in patients with relapsed/refractory HL in the Irkutsk Regional Oncology Center for a 2-year period (2016-2018).
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
The analysis of 11 case of relapsed/refractory HL have been performed, which have been treated with second line therapy in the Irkutsk Oncology Clinic from January 2016 till June 2018. The median age of the patients was 34 years (22-46). The distribution by sex: men – 6, women – 5. There was prevalence of patients with advanced stages of the disease: stage III-IV (n=8), and only in 3 patients – second stage. The average number of cycles of first line therapy was 15 (from 8 to 25 cycles). All patients received first line chemo with ABVD and BEACOPP, and 10 patients have undergone radiotherapy.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
At the time of second line initiation 5 patients had a relapse of HL: early (n=2), late (n=3), 6 patients had resistance to the therapy: primary (n=2), secondary (n=4). The median time from the diagnosis of HL till the SCT was 1 year (1 year – 10 years 9 months.). Conditioning regimen according to the BeEAM protocol have been used for all patients. Stem cells source was: bone marrow (n=1), peripheral blood (n=10). The mean of stem cells in graft was 7.99x106/kg. The remission re-induction chemotherapy included: DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). The effect of re-induction chemotherapy was: complete remission (n=5), partial remission (n=5), no response – 1 patient. The mortality rate at day 100 was 0%. Evaluation of the response after complete second line therapy was performed in 9 patients: complete remission was achieved in 6 patients (67%), 3 patients (33%) no response was received to the therapy, which is probably due to the lack of complete remission in front of auto-SCT (n=1) and a long time interval up to the HDCT. Overall survival was 100% with the medial follow up time – 18 months.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Our experience confirms the safety of the second line of therapy, including HDCT with auto-SCT for the treatment of relapsed/refractory HL, and also demonstrates that the efficacy depends on the time from the moment of diagnosis of HL to transplant and the status of the underlying disease at the moment of auto-SCT.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Hodgkin’s lymphoma, relapse, refractoriness, high-dose chemotherapy, auto-SCT.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
Fifty new cases of Hodgkin’s lymphoma (HL) are diagnosed annually in the Irkutsk Oncology Center. Despite the successes achieved in the treatment of HL from 10 to 25% of patients have refractory or relapse. The high-dose chemotherapy (HDCT) followed by auto-SCT is the standard therapy of relapsed/refractory HL. Purpose of our study was to estimate efficacy and safety of second line therapy in patients with relapsed/refractory HL in the Irkutsk Regional Oncology Center for a 2-year period (2016-2018).
Patients and methods
The analysis of 11 case of relapsed/refractory HL have been performed, which have been treated with second line therapy in the Irkutsk Oncology Clinic from January 2016 till June 2018. The median age of the patients was 34 years (22-46). The distribution by sex: men – 6, women – 5. There was prevalence of patients with advanced stages of the disease: stage III-IV (n=8), and only in 3 patients – second stage. The average number of cycles of first line therapy was 15 (from 8 to 25 cycles). All patients received first line chemo with ABVD and BEACOPP, and 10 patients have undergone radiotherapy.
Results
At the time of second line initiation 5 patients had a relapse of HL: early (n=2), late (n=3), 6 patients had resistance to the therapy: primary (n=2), secondary (n=4). The median time from the diagnosis of HL till the SCT was 1 year (1 year – 10 years 9 months.). Conditioning regimen according to the BeEAM protocol have been used for all patients. Stem cells source was: bone marrow (n=1), peripheral blood (n=10). The mean of stem cells in graft was 7.99x106/kg. The remission re-induction chemotherapy included: DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). The effect of re-induction chemotherapy was: complete remission (n=5), partial remission (n=5), no response – 1 patient. The mortality rate at day 100 was 0%. Evaluation of the response after complete second line therapy was performed in 9 patients: complete remission was achieved in 6 patients (67%), 3 patients (33%) no response was received to the therapy, which is probably due to the lack of complete remission in front of auto-SCT (n=1) and a long time interval up to the HDCT. Overall survival was 100% with the medial follow up time – 18 months.
Conclusion
Our experience confirms the safety of the second line of therapy, including HDCT with auto-SCT for the treatment of relapsed/refractory HL, and also demonstrates that the efficacy depends on the time from the moment of diagnosis of HL to transplant and the status of the underlying disease at the moment of auto-SCT.
Keywords
Hodgkin’s lymphoma, relapse, refractoriness, high-dose chemotherapy, auto-SCT.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20370
[VALUE] => Experience with second-line therapy of relapsing and refractory Hodgkin’s lymphoma in the Irkutsk region
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Experience with second-line therapy of relapsing and refractory Hodgkin’s lymphoma in the Irkutsk region
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20751
[VALUE] => 1387
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1387
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20752
[VALUE] => 1388
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1388
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Марина В. Демченкова, Екатерина В. Зубкова, Дмитрий Д. Мориков, Людмила Е. Иванова, Анна В. Шевчук, Зоя В. Дьяконенко, Алена Л. Хороших, Александра Ю. Ефиркина
Введение
Ежегодно на базе Иркутского онкологического диспансера диагностируется 50 новых случаев лимфомы Ходжкина. Несмотря на достигнутые успехи в лечении лимфомы Ходжкина, проблемой терапии является развитие рецидивов заболевания и первичной/вторичной резистентности у 10-25% больных. Применение высокодозной химиотерапии (ВДХТ) с ауто-ТГСК является стандартом терапии при рецидивах и резистентных формах ЛХ.
Цель
Оценить эффективность и безопасность II линии терапии у больных с рецидивами и резистентными формами лимфомы Ходжина в Иркутском областном онкологическом диспансере за 2-х летний период (2016-2018).
Пациенты и методы
Проведен анализ течения заболевания 11 пациентов с ЛХ, госпитализированных в Иркутский онкологический диспансер с января 2016 по июнь 2018 г для проведения II линии терапии. Медиана возраста пациентов составила 34 года (22-46). Распределение по полу: мужчин – 6, женщин – 5. Преобладали пациенты с распространенными стадиями заболевания: 8 – III-IV стадия, и лишь у 3 – II стадия ЛХ. Среднее количество циклов терапии 1 линии – 15 (от 8 до 25 циклов). Все пациенты в качестве индукционной терапии получили ПХТ по схеме ABVD и BEACOPP, лучевая терапия проводилась 10 пациентам.
Результаты
На момент начала II линии терапии 5 человек имели рецидив ЛХ: ранний (n=2) и поздний (n=2), у 6 человек регистрировалась резистентность к проводимой терапии: первичная (n=2), вторичная (n=4). Медиана времени от момента диагностики ЛХ до проведения трансплантации составила 1 год (1 год – 10 лет 9 мес.). Все пациенты получили кондиционирование по протоколу BeEAM. Стволовые кроветворные клетки получали из костного мозга (n=1), периферической крови (n=10). Клеточность трансплантанта в среднем составляла 7,99х106/кг. В качестве подготовки к ВДХТ с ауто-ТГСК проводились курсы терапии по программе DHAP (n=3), GemOx (n=4), ICE (n=3), IGEV (n=1). Статус ЛХ на момент ауто-ТГСК: полная ремиссия (ПР) – 5 пациентов, частичная ремиссия (ЧР) – 5, нет ответа – 1 больной. Летальность, связанная с ВДХТ и ауто-ТГСК на «день 100» составила 0%. Оценка ответа по завершении терапии II линии проведена у 9 пациентов: полная ремиссия была достигнута у 6 пациентов (67%), у 3-х пациентов (33%) не получено ответа на проводимую терапию, что вероятно обусловлено отсутствием достижения полной ремиссии перед ауто-ТГСК (n=1) и длительным интервалом времени до ВДХТ. Общая выживаемость 100%, с медианой наблюдения 18 месяцев от начала II линии терапии.
Заключение
Наш опыт подтверждает безопасность II линии терапии, включающей ВДХТ с ауто-ТГСК для лечения рефрактерных форм ЛХ. Эффективность II линии зависит от от достижения полной ремиссии до ауто-ТГКС и интервалом времени от момента диагностики ЛХ до проведения ВДХТ с ауто-ТГСК.
Ключевые слова
Лимфома Ходжкина, рецидив, рефрактерность, высокодозная химиотерапия, ауто-ТГСК.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20356
[VALUE] => Array
(
[TEXT] => Дарья В. Чуракина <sup>1</sup>, Александр Н. Швецов <sup>1</sup>, Вадим Е. Карев <sup>2</sup>, Ирина А. Карабак <sup>2</sup>, Алексей Б. Чухловин <sup>1</sup>, Юрий А. Эйсмонт <sup>2</sup>, Ольга В. Пирогова <sup>1</sup>, Павел С. Жеребненко <sup>1</sup>, Олег В. Голощапов <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Татьяна А. Быкова <sup>1</sup>, Олеся В. Паина <sup>1</sup>, Людмила С. Зубаровская <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Дарья В. Чуракина 1, Александр Н. Швецов 1, Вадим Е. Карев 2, Ирина А. Карабак 2, Алексей Б. Чухловин 1, Юрий А. Эйсмонт 2, Ольга В. Пирогова 1, Павел С. Жеребненко 1, Олег В. Голощапов 1, Елена И. Дарская 1, Татьяна А. Быкова 1, Олеся В. Паина 1, Людмила С. Зубаровская 1, Иван С. Моисеев 1, Борис В. Афанасьев 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20357
[VALUE] => Array
(
[TEXT] => <sup>1</sup> НИИ Детской Онкологии, Гематологии и Трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова<br>
<sup>2</sup> ФГБУ «Детский научно-клинический центр инфекционных болезней»<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 НИИ Детской Онкологии, Гематологии и Трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова
2 ФГБУ «Детский научно-клинический центр инфекционных болезней»
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20462
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Острая реакция трансплантат против хозяина (оРТПХ) с поражением желудочно-кишечного тракта (ЖКТ) – это одно из наиболее угрожающих осложнений у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). В настоящее время не существует стандартов по диагностике этого состояния. Клинические симптомы оРТПХ являются неспецифичными и могут мимикрировать под другие патологические состояния. Цель нашей работы заключается в анализе результатов гистологических исследований слизистых толстой кишки и верхнего отдела ЖКТ (желудка, двенадцатиперстной кишки, пищевода) у пациентов после алло-ТГСК, определении частоты выявления различных патологий ЖКТ после алло-ТГСК.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
В ретроспективное исследование были включены 112 пациентов после алло-ТГСК. Большинство пациентов (68%) проходили лечение по поводу острого лейкоза. Медиана возраста в исследуемой группе составила 30 лет (2-67 лет). Всем пациентам была проведена фиброгастродуоденоскопия и/или фиброколоноскопия, выполнена биопсия и гистологическое исследование органов желудочно-кишечного тракта. Методом ПЦР в биоптатах выявляли вирус простого герпеса 1, 2, герпеса 6 типа и цитомегаловирус, а также проводили бактериологическое исследование кала на условно-патогенную флору и ИФА на C. difficile. Медиана времени выполнения биопсии после трансплантации составила 84 дня (15-413 дней). Исследования проводились по поводу различных симптомов поражения ЖКТ для верификации диагноза. В 56% случаев была выполнена биопсия толстой кишки, в 35% – биопсия верхних отделов ЖКТ (желудок, двенадцатиперстная кишка, пищевод), а также в 9% проводилось исследование обоих отделов.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
При биопсии толстой кишки признаки оРТПХ наблюдалась в 73,5% случаев и чаще, чем при биопсии верхнего отдела ЖКТ (36,5%, р=0,02). В нижних отделах ЖКТ легкая гистологическая степень оРТПХ определялась в 56% случаев, средней тяжести – в 28%, тяжелая – в 16%. В верхних отделах ЖКТ наблюдались легкие проявления РТПХ у 60% и средней тяжести – у 33%. Вирусная инфекция чаще наблюдалась при биопсии нижнего отдела ЖКТ (53% и 36%, р=0,046). Бактериальная инфекция встречалась у 38% и 19% пациентов, с биопсией нижнего и верхнего отделов ЖКТ соответственно (р=0,56). У пациентов, которым была выполнена биопсия толстой кишки, вирусная инфекция не влияла на 1-летнюю общую выживаемость (ОВ) (65,2% и 64,7%, р=0,67). Такая же картина наблюдалось при биопсии верхних отделов ЖКТ (85,7% и 86,4%, р=0,8). ОВ не зависела от наличия условно-патогенной бактериальной флоры, в группе пациентов с биопсией нижних отделов – 61,4% и 72,6% (р=0,4) и верхних отделов – 85,7% и 86,4%, соответственно (р=0,8). Основным фактором, оказавшим достоверное влияние на ОВ пациентов, которым проводилась биопсия толстой кишки, была гистологическая степень тяжести оРТПХ, так при легкой степени 1-летняя ОВ составила 88,2%, при средней степени тяжести – 47,6%, при тяжелой – 40,0%, а в случае отсутствия оРТПХ – 60,2% (р=0,01). При исследовании верхних отделов ОВ различалась, у пациентов с РТПХ составила 72,0%, без РТПХ – 95,2% (р=0,04). Однако степень выраженности РТПХ достоверно не изменяла ОВ, при 1 степени – 78,75%, при 2 – 60% (р=0,15), возможно, вследствие маленькой выборки (n=15).
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Полученные данные демонстрируют неоднородность этиологии поражения различных отделов ЖКТ после алло-ТГСК, что подчеркивает необходимость гистологического и ПЦР исследования биоптатов ЖКТ. Возможно, из-за небольшой выборки пациентов, в исследовании не было показано влияния вирусного и бактериального поражения ЖКТ на выживаемость.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Трансплантация гемопоэтических стволовых клеток, острая реакция трансплантат против хозяина, желудочно-кишечный тракт, гистологическое исследование.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Острая реакция трансплантат против хозяина (оРТПХ) с поражением желудочно-кишечного тракта (ЖКТ) – это одно из наиболее угрожающих осложнений у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). В настоящее время не существует стандартов по диагностике этого состояния. Клинические симптомы оРТПХ являются неспецифичными и могут мимикрировать под другие патологические состояния. Цель нашей работы заключается в анализе результатов гистологических исследований слизистых толстой кишки и верхнего отдела ЖКТ (желудка, двенадцатиперстной кишки, пищевода) у пациентов после алло-ТГСК, определении частоты выявления различных патологий ЖКТ после алло-ТГСК.
Пациенты и методы
В ретроспективное исследование были включены 112 пациентов после алло-ТГСК. Большинство пациентов (68%) проходили лечение по поводу острого лейкоза. Медиана возраста в исследуемой группе составила 30 лет (2-67 лет). Всем пациентам была проведена фиброгастродуоденоскопия и/или фиброколоноскопия, выполнена биопсия и гистологическое исследование органов желудочно-кишечного тракта. Методом ПЦР в биоптатах выявляли вирус простого герпеса 1, 2, герпеса 6 типа и цитомегаловирус, а также проводили бактериологическое исследование кала на условно-патогенную флору и ИФА на C. difficile. Медиана времени выполнения биопсии после трансплантации составила 84 дня (15-413 дней). Исследования проводились по поводу различных симптомов поражения ЖКТ для верификации диагноза. В 56% случаев была выполнена биопсия толстой кишки, в 35% – биопсия верхних отделов ЖКТ (желудок, двенадцатиперстная кишка, пищевод), а также в 9% проводилось исследование обоих отделов.
Результаты
При биопсии толстой кишки признаки оРТПХ наблюдалась в 73,5% случаев и чаще, чем при биопсии верхнего отдела ЖКТ (36,5%, р=0,02). В нижних отделах ЖКТ легкая гистологическая степень оРТПХ определялась в 56% случаев, средней тяжести – в 28%, тяжелая – в 16%. В верхних отделах ЖКТ наблюдались легкие проявления РТПХ у 60% и средней тяжести – у 33%. Вирусная инфекция чаще наблюдалась при биопсии нижнего отдела ЖКТ (53% и 36%, р=0,046). Бактериальная инфекция встречалась у 38% и 19% пациентов, с биопсией нижнего и верхнего отделов ЖКТ соответственно (р=0,56). У пациентов, которым была выполнена биопсия толстой кишки, вирусная инфекция не влияла на 1-летнюю общую выживаемость (ОВ) (65,2% и 64,7%, р=0,67). Такая же картина наблюдалось при биопсии верхних отделов ЖКТ (85,7% и 86,4%, р=0,8). ОВ не зависела от наличия условно-патогенной бактериальной флоры, в группе пациентов с биопсией нижних отделов – 61,4% и 72,6% (р=0,4) и верхних отделов – 85,7% и 86,4%, соответственно (р=0,8). Основным фактором, оказавшим достоверное влияние на ОВ пациентов, которым проводилась биопсия толстой кишки, была гистологическая степень тяжести оРТПХ, так при легкой степени 1-летняя ОВ составила 88,2%, при средней степени тяжести – 47,6%, при тяжелой – 40,0%, а в случае отсутствия оРТПХ – 60,2% (р=0,01). При исследовании верхних отделов ОВ различалась, у пациентов с РТПХ составила 72,0%, без РТПХ – 95,2% (р=0,04). Однако степень выраженности РТПХ достоверно не изменяла ОВ, при 1 степени – 78,75%, при 2 – 60% (р=0,15), возможно, вследствие маленькой выборки (n=15).
Заключение
Полученные данные демонстрируют неоднородность этиологии поражения различных отделов ЖКТ после алло-ТГСК, что подчеркивает необходимость гистологического и ПЦР исследования биоптатов ЖКТ. Возможно, из-за небольшой выборки пациентов, в исследовании не было показано влияния вирусного и бактериального поражения ЖКТ на выживаемость.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, острая реакция трансплантат против хозяина, желудочно-кишечный тракт, гистологическое исследование.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20358
[VALUE] => Array
(
[TEXT] => Darya V. Churakina <sup>1</sup>, Aleksander N. Shvetsov <sup>1</sup>, Vadim E. Karev <sup>2</sup>, Irina A. Karabak <sup>2</sup>, Alexey B. Chukhlovin <sup>1</sup>, Yurii A. Eismont <sup>2</sup>, Olga V. Pirogova <sup>1</sup>, Pavel S. Zherebenko <sup>1</sup>, Oleg V. Goloshchapov <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Tatiana A. Bykova <sup>1</sup>, Olesya V. Paina <sup>1</sup>, Ludmila S. Zubarovskaya <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>
[TYPE] => TEXT
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Darya V. Churakina 1, Aleksander N. Shvetsov 1, Vadim E. Karev 2, Irina A. Karabak 2, Alexey B. Chukhlovin 1, Yurii A. Eismont 2, Olga V. Pirogova 1, Pavel S. Zherebenko 1, Oleg V. Goloshchapov 1, Elena I. Darskaya 1, Tatiana A. Bykova 1, Olesya V. Paina 1, Ludmila S. Zubarovskaya 1, Ivan S. Moiseev 1, Boris V. Afanasyev 1
[TYPE] => TEXT
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20359
[VALUE] => Array
(
[TEXT] => <sup>1</sup> R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation<br>
<sup>2</sup> Research Institute of Pediatric Infections, Federal Medico-Biological Agency of Russia, St. Petersburg, Russian Federation<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
2 Research Institute of Pediatric Infections, Federal Medico-Biological Agency of Russia, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20465
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Acute graft-versus-host disease (aGVHD) of the gastrointestinal tract (GI tract) is one of the most dangerous complications after allogeneic hematopoietic stem cell transplantation (allo-HSCT). However, there is consensus now on the diagnostic workup in this complication. Clinical manifestations of aGVHD are nonspecific and can resemble other conditions. The goal of our research was to analyze the results of histological examination of mucous colon and upper digestive ways (esophagus, stomach, duodenum) of the patients after HSCT with suspected GVHD, and to determine the incidence of different findings.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
Our retrospective research included 112 patients after allo-HSCT. Most of the patients received allo-HSCT as treatment for acute leukemia. Median age was 30 years (2-67). All these patients were studied by gastroduodenoscopy and/or colonoscopy, with biopsy and histopathology investigation of the GI sites. Herpes simplex virus, herpes virus type 6, cytomegalovirus were identified by PCR in the biopsies. Fecal samples were studied by ELISA for C. difficile, and seeded in cultures for antibiotic-resistant bacteria. Median timing for the biopsies was 85 days (15-413) post-HSCT. In 56% of cases, biopsy of upper GI compartments was performed, in 35% of cases, lower parts of GI-tract were sampled, and both compartments were subject to biopsies in 9% of cases.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Conventional histology revealed signs of aGVHD in 73.5% of colon biopsies, and only in 36.5% of upper GI biopsies, p=0.02. Mild histological signs of GVHD were present in 56% of biopsies from the lower GI mucosa, moderate pathology, in 28%, and severe changes, in 16%. In upper GI tract, mild histological signs were observed in 60% cases, moderate changes, in 33%. Viral infection revealed by PCR was more frequent in colon biopsies (53% and 36%, p=0.046). Bacterial infection was detected in 38% patients with lower GI biopsy sampling, and in 19%, from the upper GI biopsies, respectively, with no significant difference between these groups (p=0.56). Lower GI tract viral infection had no influence on the 1-year overall survival (OS) (65.2% and 64.7%, p=0.67). Similar effect was observed for the upper GI tract viral infections (85.7% and 84.4%, p=0.8). Overall survival (OS) was not influenced by bacterial infections in the biopsies of lower GI tract (61.4% and 72.6%, p=0.4), or upper GI tract samples (85.7% and 86.4%, p=0.8). Histological grade in lower GI biopsies was the main feature that affected OS (88.2%, 47.6, and 60.2%, for mild, moderate and severe histological grades, respectively, p=0.01). Presence of upper GI GVHD also adversely affected OS (72.0% and 95.2%, p=0.04). However, severity of upper GVHD had no influence on OS, possibly, as result of small sample size.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
The study demonstrates different etiologies for upper and lower GI lesions after HSCT and confirms the necessity of biopsy and PCR assays of the samples. Although the study size was small, it did not identify the impact of viral and bacterial GI infections on survival.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Acute graft-versus-host disease, hematopoietic stem cell transplantation, gastrointestinal tract, histopathology.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
Acute graft-versus-host disease (aGVHD) of the gastrointestinal tract (GI tract) is one of the most dangerous complications after allogeneic hematopoietic stem cell transplantation (allo-HSCT). However, there is consensus now on the diagnostic workup in this complication. Clinical manifestations of aGVHD are nonspecific and can resemble other conditions. The goal of our research was to analyze the results of histological examination of mucous colon and upper digestive ways (esophagus, stomach, duodenum) of the patients after HSCT with suspected GVHD, and to determine the incidence of different findings.
Patients and methods
Our retrospective research included 112 patients after allo-HSCT. Most of the patients received allo-HSCT as treatment for acute leukemia. Median age was 30 years (2-67). All these patients were studied by gastroduodenoscopy and/or colonoscopy, with biopsy and histopathology investigation of the GI sites. Herpes simplex virus, herpes virus type 6, cytomegalovirus were identified by PCR in the biopsies. Fecal samples were studied by ELISA for C. difficile, and seeded in cultures for antibiotic-resistant bacteria. Median timing for the biopsies was 85 days (15-413) post-HSCT. In 56% of cases, biopsy of upper GI compartments was performed, in 35% of cases, lower parts of GI-tract were sampled, and both compartments were subject to biopsies in 9% of cases.
Results
Conventional histology revealed signs of aGVHD in 73.5% of colon biopsies, and only in 36.5% of upper GI biopsies, p=0.02. Mild histological signs of GVHD were present in 56% of biopsies from the lower GI mucosa, moderate pathology, in 28%, and severe changes, in 16%. In upper GI tract, mild histological signs were observed in 60% cases, moderate changes, in 33%. Viral infection revealed by PCR was more frequent in colon biopsies (53% and 36%, p=0.046). Bacterial infection was detected in 38% patients with lower GI biopsy sampling, and in 19%, from the upper GI biopsies, respectively, with no significant difference between these groups (p=0.56). Lower GI tract viral infection had no influence on the 1-year overall survival (OS) (65.2% and 64.7%, p=0.67). Similar effect was observed for the upper GI tract viral infections (85.7% and 84.4%, p=0.8). Overall survival (OS) was not influenced by bacterial infections in the biopsies of lower GI tract (61.4% and 72.6%, p=0.4), or upper GI tract samples (85.7% and 86.4%, p=0.8). Histological grade in lower GI biopsies was the main feature that affected OS (88.2%, 47.6, and 60.2%, for mild, moderate and severe histological grades, respectively, p=0.01). Presence of upper GI GVHD also adversely affected OS (72.0% and 95.2%, p=0.04). However, severity of upper GVHD had no influence on OS, possibly, as result of small sample size.
Conclusion
The study demonstrates different etiologies for upper and lower GI lesions after HSCT and confirms the necessity of biopsy and PCR assays of the samples. Although the study size was small, it did not identify the impact of viral and bacterial GI infections on survival.
Keywords
Acute graft-versus-host disease, hematopoietic stem cell transplantation, gastrointestinal tract, histopathology.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20360
[VALUE] => The role of histopathological, virological and bacteriological findings in the diagnostics of acute graft-versus-host disease of the gastrointestinal tract
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => The role of histopathological, virological and bacteriological findings in the diagnostics of acute graft-versus-host disease of the gastrointestinal tract
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20749
[VALUE] => 1385
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1385
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20750
[VALUE] => 1386
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1386
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Дарья В. Чуракина 1, Александр Н. Швецов 1, Вадим Е. Карев 2, Ирина А. Карабак 2, Алексей Б. Чухловин 1, Юрий А. Эйсмонт 2, Ольга В. Пирогова 1, Павел С. Жеребненко 1, Олег В. Голощапов 1, Елена И. Дарская 1, Татьяна А. Быкова 1, Олеся В. Паина 1, Людмила С. Зубаровская 1, Иван С. Моисеев 1, Борис В. Афанасьев 1
2 ФГБУ «Детский научно-клинический центр инфекционных болезней»
Введение
Острая реакция трансплантат против хозяина (оРТПХ) с поражением желудочно-кишечного тракта (ЖКТ) – это одно из наиболее угрожающих осложнений у пациентов после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). В настоящее время не существует стандартов по диагностике этого состояния. Клинические симптомы оРТПХ являются неспецифичными и могут мимикрировать под другие патологические состояния. Цель нашей работы заключается в анализе результатов гистологических исследований слизистых толстой кишки и верхнего отдела ЖКТ (желудка, двенадцатиперстной кишки, пищевода) у пациентов после алло-ТГСК, определении частоты выявления различных патологий ЖКТ после алло-ТГСК.
Пациенты и методы
В ретроспективное исследование были включены 112 пациентов после алло-ТГСК. Большинство пациентов (68%) проходили лечение по поводу острого лейкоза. Медиана возраста в исследуемой группе составила 30 лет (2-67 лет). Всем пациентам была проведена фиброгастродуоденоскопия и/или фиброколоноскопия, выполнена биопсия и гистологическое исследование органов желудочно-кишечного тракта. Методом ПЦР в биоптатах выявляли вирус простого герпеса 1, 2, герпеса 6 типа и цитомегаловирус, а также проводили бактериологическое исследование кала на условно-патогенную флору и ИФА на C. difficile. Медиана времени выполнения биопсии после трансплантации составила 84 дня (15-413 дней). Исследования проводились по поводу различных симптомов поражения ЖКТ для верификации диагноза. В 56% случаев была выполнена биопсия толстой кишки, в 35% – биопсия верхних отделов ЖКТ (желудок, двенадцатиперстная кишка, пищевод), а также в 9% проводилось исследование обоих отделов.
Результаты
При биопсии толстой кишки признаки оРТПХ наблюдалась в 73,5% случаев и чаще, чем при биопсии верхнего отдела ЖКТ (36,5%, р=0,02). В нижних отделах ЖКТ легкая гистологическая степень оРТПХ определялась в 56% случаев, средней тяжести – в 28%, тяжелая – в 16%. В верхних отделах ЖКТ наблюдались легкие проявления РТПХ у 60% и средней тяжести – у 33%. Вирусная инфекция чаще наблюдалась при биопсии нижнего отдела ЖКТ (53% и 36%, р=0,046). Бактериальная инфекция встречалась у 38% и 19% пациентов, с биопсией нижнего и верхнего отделов ЖКТ соответственно (р=0,56). У пациентов, которым была выполнена биопсия толстой кишки, вирусная инфекция не влияла на 1-летнюю общую выживаемость (ОВ) (65,2% и 64,7%, р=0,67). Такая же картина наблюдалось при биопсии верхних отделов ЖКТ (85,7% и 86,4%, р=0,8). ОВ не зависела от наличия условно-патогенной бактериальной флоры, в группе пациентов с биопсией нижних отделов – 61,4% и 72,6% (р=0,4) и верхних отделов – 85,7% и 86,4%, соответственно (р=0,8). Основным фактором, оказавшим достоверное влияние на ОВ пациентов, которым проводилась биопсия толстой кишки, была гистологическая степень тяжести оРТПХ, так при легкой степени 1-летняя ОВ составила 88,2%, при средней степени тяжести – 47,6%, при тяжелой – 40,0%, а в случае отсутствия оРТПХ – 60,2% (р=0,01). При исследовании верхних отделов ОВ различалась, у пациентов с РТПХ составила 72,0%, без РТПХ – 95,2% (р=0,04). Однако степень выраженности РТПХ достоверно не изменяла ОВ, при 1 степени – 78,75%, при 2 – 60% (р=0,15), возможно, вследствие маленькой выборки (n=15).
Заключение
Полученные данные демонстрируют неоднородность этиологии поражения различных отделов ЖКТ после алло-ТГСК, что подчеркивает необходимость гистологического и ПЦР исследования биоптатов ЖКТ. Возможно, из-за небольшой выборки пациентов, в исследовании не было показано влияния вирусного и бактериального поражения ЖКТ на выживаемость.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, острая реакция трансплантат против хозяина, желудочно-кишечный тракт, гистологическое исследование.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20333
[VALUE] => Array
(
[TEXT] => Дарья В. Чуракина <sup>1</sup>, Олег В. Голощапов <sup>1</sup>, Ольга В. Пирогова <sup>1</sup>, Александр Н. Швецов <sup>1</sup>, Руслана В. Клементьева <sup>1</sup>, Александр А. Щербаков <sup>1</sup>, Сергей В. Сидоренко <sup>2</sup>, Владимир А. Гостев <sup>2</sup>, Мария А. Суворова <sup>3</sup>, Юрий В. Лобзин <sup>2</sup>, Борис В. Афанасьев <sup>1</sup>
[TYPE] => TEXT
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Дарья В. Чуракина 1, Олег В. Голощапов 1, Ольга В. Пирогова 1, Александр Н. Швецов 1, Руслана В. Клементьева 1, Александр А. Щербаков 1, Сергей В. Сидоренко 2, Владимир А. Гостев 2, Мария А. Суворова 3, Юрий В. Лобзин 2, Борис В. Афанасьев 1
[TYPE] => TEXT
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20334
[VALUE] => Array
(
[TEXT] => <sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербург, Российская Федерация, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова<br>
<sup>2</sup> ФГБУ ДНКЦИБ ФМБА России<br>
<sup>3</sup> Научно-исследовательская лаборатория Explana, Санкт-Петербург, Российская Федерация<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербург, Российская Федерация, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова
2 ФГБУ ДНКЦИБ ФМБА России
3 Научно-исследовательская лаборатория Explana, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20732
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
При проведении аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), вследствие применения цитостатических и антибактериальных препаратов, изменений в диете нарушается состав микробиоты желудочно-кишечного тракта (ЖКТ). Накапливаются данные о том, что микробиота влияет на работу иммунной системы человека, подавляет развитие патогенных микроорганизмов, способствует регенерации эпителия, что препятствует появлению иммунных и инфекционных осложнений после алло-ТГСК. Трансплантация фекальной микробиоты (ТФМ) направлена на восстановление микрофлоры ЖКТ реципиента.
</p>
<h2 style="text-align: justify;">Цель работы</h2>
<p style="text-align: justify;">
Цель работы состояла в демонстрации клинического случая стероид-резистентного течения острой реакции «трансплантат против хозяина» (оРТПХ) 3 степени тяжести, 4 стадия кишечных проявлений, в котором ТФМ в сочетании с иммуносупрессиной терапии, привела к разрешению оРТПХ кишечника.
</p>
<h2 style="text-align: justify;">Описание случая</h2>
<p style="text-align: justify;">
Пациент, мужчина, 45 лет. Диагноз: острый миелобластный лейкоз с изменениями, связанными с миелодисплазией. Первые симптомы миелодиспластического синдрома с избытком бластов в марте 2016 года. Проведено 6 курсов 5-азацитидина. 20.02.17 – трансформация в ОМЛ. Терапия малыми дозами цитозара. 23.09.17 алло-ТГСК от неродственного донора с режимом кондиционирования флюдарабин + бусульфан (12 мг/кг). Профилактика РТПХ: тимоглобулин, такролимус, MMF. В связи с высоким риском развития рецидива, на Д+67 снижение дозы такролимуса, с полной отменой на Д+82. С Д+102 диарея до 3 л/сутки. Д+110 – госпитализация в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой. Cтул в объеме 5 л/сутки, сепсис (лихорадка 38°C, СРБ – 331 мг/л), начата эмпирическая антибактериальная терапия (дорипенем, ванкомицин). Биопсия слизистой толстой кишки (Д+114) – признаки умеренно выраженной РТПХ, вирусного поражения кишечника (ПЦР – HHV-6+, CMV+, EBV+). На Д+114 возобновлен такролимус, начат метилпреднизолон 2 мг/кг, ганцикловир 10 мг/кг. Д+118 – объем стула 13 л/сутки. С Д+117 из-за неэффективности терапии 1 линии начата терапия 2 линии – руксолитиниб 20 мг/сутки. Такролимус, в связи с развитием острого повреждения почек, заменен на сиролимус (Д+121). Д+133 – снижение объема стула до 3 л/сутки. При бактериологическом исследовании стула (Д+138) – обильный рост полирезистентной<i> K. Pneumoniae</i>. При 16S-секвенировании, 99% микробиоты ЖКТ составляло семейство <i>Staphylococcaceae</i>. Ответ по РТПХ кишки не достигнут, с Д +139 до Д+221 – продолжающееся кишечное кровотечение, геморрагический шок от Д+144 (Hb=39 г/л). Суммарно за весь период введено: эритроцитарная масса 29,8 л, тромбоцитарная масса 5,52 л, свежезамороженная плазма – 5,92 л. Получал терапию в отделении реанимации с Д+118 по Д+284. В этот период развились следующие осложнения: тяжелый сепсис, вызванный полирезистентными штаммами K. <i>pneumoniae </i>(Д+149) и <i>Acinetobacter spp</i>. (с Д+159 по Д+198) (уровень СРБ до 449 мг/л, пресепсина до 12839 пг/мл), двухсторонняя пневмония (<i>K. Pneumonia, Pseudomonas spp.</i>), полиорганная недостаточность (сердечно-сосудистая, печеночная, дыхательная, церебральная). Искусственная вентиляция легких в течение 83 дней. На Д+192 и +194 в связи с недостаточным эффектом от иммуносупрессивной терапии проведена ТФМ объемом 80 и 300 мл, через назоинтестинальный зонд, установленный под контролем эндоскопа. За 14 дней объем стула снизился до 1 л/сутки (Д+208), а на Д+280 до 500 мл/сутки, с Д+221 впервые отсутствие крови в стуле. В результате ТФМ, <i>K. pneumoniae</i>, ранее продуцирующая фермент металло-бета-лактамазу (NDM+), сменилась штаммом чувствительным к антибиотикам (NDM-). Это позволило назначить цефтазидим+авибактам с положительным эффектом (снижение прокальцитонина с 26,8 до 0,8 нг/мл). По данным ПЦР образцов стула после ТФМ значительно повысилась общая бактериальная масса (с пиком на Д+8 – Д+16 после ТФМ), за счет увеличения <i>Bacteroides fragilis, Bacteroides </i><i>thetaiataomicron, Lactobacillus spp., Bifidobacterium spp. </i>Полная отмена руксолитиниба на Д+284 и сиролимуса на Д+294. По результатам контрольной биопсии (Д+337) убедительных признаков РТПХ и вирусного поражения кишечника не выявлено (ПЦР – HHV-6 -, CMV -, EBV -). В настоящее время – стул с тенденцией к оформлению (около 300 г/сутки). Питание самостоятельное и дополнительное через гастростому.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
В представленном случае продемонстрировано эффективное применение ТФМ в сочетании с JAK2 ингибитором у пациента со стероид-резистентным течением оРТПХ и тяжелыми инфекционными осложнениями.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Трансплантация гемопоэтических стволовых клеток, стероид-резистентная реакция трансплантат против хозяина, трансплантация фекальной микробиоты, микробиота кишечника.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
При проведении аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), вследствие применения цитостатических и антибактериальных препаратов, изменений в диете нарушается состав микробиоты желудочно-кишечного тракта (ЖКТ). Накапливаются данные о том, что микробиота влияет на работу иммунной системы человека, подавляет развитие патогенных микроорганизмов, способствует регенерации эпителия, что препятствует появлению иммунных и инфекционных осложнений после алло-ТГСК. Трансплантация фекальной микробиоты (ТФМ) направлена на восстановление микрофлоры ЖКТ реципиента.
Цель работы
Цель работы состояла в демонстрации клинического случая стероид-резистентного течения острой реакции «трансплантат против хозяина» (оРТПХ) 3 степени тяжести, 4 стадия кишечных проявлений, в котором ТФМ в сочетании с иммуносупрессиной терапии, привела к разрешению оРТПХ кишечника.
Описание случая
Пациент, мужчина, 45 лет. Диагноз: острый миелобластный лейкоз с изменениями, связанными с миелодисплазией. Первые симптомы миелодиспластического синдрома с избытком бластов в марте 2016 года. Проведено 6 курсов 5-азацитидина. 20.02.17 – трансформация в ОМЛ. Терапия малыми дозами цитозара. 23.09.17 алло-ТГСК от неродственного донора с режимом кондиционирования флюдарабин + бусульфан (12 мг/кг). Профилактика РТПХ: тимоглобулин, такролимус, MMF. В связи с высоким риском развития рецидива, на Д+67 снижение дозы такролимуса, с полной отменой на Д+82. С Д+102 диарея до 3 л/сутки. Д+110 – госпитализация в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой. Cтул в объеме 5 л/сутки, сепсис (лихорадка 38°C, СРБ – 331 мг/л), начата эмпирическая антибактериальная терапия (дорипенем, ванкомицин). Биопсия слизистой толстой кишки (Д+114) – признаки умеренно выраженной РТПХ, вирусного поражения кишечника (ПЦР – HHV-6+, CMV+, EBV+). На Д+114 возобновлен такролимус, начат метилпреднизолон 2 мг/кг, ганцикловир 10 мг/кг. Д+118 – объем стула 13 л/сутки. С Д+117 из-за неэффективности терапии 1 линии начата терапия 2 линии – руксолитиниб 20 мг/сутки. Такролимус, в связи с развитием острого повреждения почек, заменен на сиролимус (Д+121). Д+133 – снижение объема стула до 3 л/сутки. При бактериологическом исследовании стула (Д+138) – обильный рост полирезистентной K. Pneumoniae. При 16S-секвенировании, 99% микробиоты ЖКТ составляло семейство Staphylococcaceae. Ответ по РТПХ кишки не достигнут, с Д +139 до Д+221 – продолжающееся кишечное кровотечение, геморрагический шок от Д+144 (Hb=39 г/л). Суммарно за весь период введено: эритроцитарная масса 29,8 л, тромбоцитарная масса 5,52 л, свежезамороженная плазма – 5,92 л. Получал терапию в отделении реанимации с Д+118 по Д+284. В этот период развились следующие осложнения: тяжелый сепсис, вызванный полирезистентными штаммами K. pneumoniae (Д+149) и Acinetobacter spp. (с Д+159 по Д+198) (уровень СРБ до 449 мг/л, пресепсина до 12839 пг/мл), двухсторонняя пневмония (K. Pneumonia, Pseudomonas spp.), полиорганная недостаточность (сердечно-сосудистая, печеночная, дыхательная, церебральная). Искусственная вентиляция легких в течение 83 дней. На Д+192 и +194 в связи с недостаточным эффектом от иммуносупрессивной терапии проведена ТФМ объемом 80 и 300 мл, через назоинтестинальный зонд, установленный под контролем эндоскопа. За 14 дней объем стула снизился до 1 л/сутки (Д+208), а на Д+280 до 500 мл/сутки, с Д+221 впервые отсутствие крови в стуле. В результате ТФМ, K. pneumoniae, ранее продуцирующая фермент металло-бета-лактамазу (NDM+), сменилась штаммом чувствительным к антибиотикам (NDM-). Это позволило назначить цефтазидим+авибактам с положительным эффектом (снижение прокальцитонина с 26,8 до 0,8 нг/мл). По данным ПЦР образцов стула после ТФМ значительно повысилась общая бактериальная масса (с пиком на Д+8 – Д+16 после ТФМ), за счет увеличения Bacteroides fragilis, Bacteroides thetaiataomicron, Lactobacillus spp., Bifidobacterium spp. Полная отмена руксолитиниба на Д+284 и сиролимуса на Д+294. По результатам контрольной биопсии (Д+337) убедительных признаков РТПХ и вирусного поражения кишечника не выявлено (ПЦР – HHV-6 -, CMV -, EBV -). В настоящее время – стул с тенденцией к оформлению (около 300 г/сутки). Питание самостоятельное и дополнительное через гастростому.
Заключение
В представленном случае продемонстрировано эффективное применение ТФМ в сочетании с JAK2 ингибитором у пациента со стероид-резистентным течением оРТПХ и тяжелыми инфекционными осложнениями.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, стероид-резистентная реакция трансплантат против хозяина, трансплантация фекальной микробиоты, микробиота кишечника.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20335
[VALUE] => Array
(
[TEXT] => Darya V. Churakina <sup>1</sup>, Oleg V. Goloshchapov <sup>1</sup>, Olga V. Pirogova <sup>1</sup>, Aleksander N. Shvetsov <sup>1</sup>, Ruslana V. Klementeva <sup>1</sup>, Aleksandr A. Shcherbakov <sup>1</sup>, Sergey V. Sidorenko <sup>2</sup>, Vladimir A. Gostev <sup>2</sup>, Maria A. Suvorova <sup>3</sup>, Yuri V. Lobzin <sup>2</sup>, Boris V. Afanasyev <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Darya V. Churakina 1, Oleg V. Goloshchapov 1, Olga V. Pirogova 1, Aleksander N. Shvetsov 1, Ruslana V. Klementeva 1, Aleksandr A. Shcherbakov 1, Sergey V. Sidorenko 2, Vladimir A. Gostev 2, Maria A. Suvorova 3, Yuri V. Lobzin 2, Boris V. Afanasyev 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20336
[VALUE] => Array
(
[TEXT] => <sup>1</sup> R. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation<br>
<sup>2</sup> Research Scientific Institute of Children’s Infections, St. Petersburg, Russian Federation<br>
<sup>3</sup> The Explana Research Laboratory, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 R. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
2 Research Scientific Institute of Children’s Infections, St. Petersburg, Russian Federation
3 The Explana Research Laboratory, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20341
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">
In allogeneic hematopoietic stem cell transplantation (HSCT), the recipients have altered composition of gastrointestinal (GI) microbiota, due to the use of cytostatic and antibacterial drugs, changes in diet. There is a growing evidence that microbiota influences the immune system, suppresses pathogenic bacteria, promotes regeneration of the GI mucosa. It may prevent immune and infectious complications after HSCT. Transplantation of fecal microbiota (FMT) is directed to recovery of recipient microflora. Our aim was to present a clinical case of a patient with steroid-resistant intestinal graft-versus-host disease (GVHD), stage 4, grade 3, therefore treated by FMT.
</p>
<h2 style="text-align: justify;">Case description</h2>
<p style="text-align: justify;">
A forty-five year old patient underwent HSCT in Sep 2017, for secondary acute myeloid leukemia (AML) evolving from myelodysplastic syndrome. Hematopoietic graft was from unrelated donor, conditioning regimen included fludarabin+ busulphan (12 mg/kg). Prevention of GVHD was performed with thymoglobulin, tacrolimus, MMF. Since D+67, tacrolimus was tapered and stopped at D+82 due to high relapse risk. From D+102, persistent diarrhea syndrome developed, with up to 3 L/d. The patient was admitted to the R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation. The diarrhea volume reached 5 L/d, and the patient has became septic (fever of 38oC, serum CRP, 331mg/L). Empirical antibiotic therapy consisted of doripenem, vancomycin. Colon biopsy (D+114) identified histological grade 2 of GVHD and multiple viral infection (PCR-positive for HHV-6, CMV, EBV). Tacrolimus was restarted, methylprednisolone at 2 mg/kg, and ganciclovir 10 mg/kg were administered. After 7 days of therapy, the diarrhea volume was 13 L/d. After failure of the first-line treatment, ruxolitimib (20 mg/d) was administered. Due to acute kidney injury, tacrolimus was replaced by sirolimus. At D+133, the diarrhea decreased to 3 L/d. Meanwhile, the stool samples became positive for antibiotic-resistant K. Pneumonia (D+138). The 16S rRNA gene sequencing showed the Staphylococcaceae family to represent 99% of intestinal microbiota. Despite reduced stool volume, no clinical response was achieved. GI bleeding continued from D+139 to D+221 followed by hemorrhagic shock observed at D+144, with blood hemoglobin levels of 39 g/L. In total, the patient was transfused with 29.8 L of RBCs, 5.5 L of platelet concentrate, and 5.9 L of fresh-frozen plasma.<br>
The patient was treated at the ICU from D+118 to D+284 posttransplant. Over this time period, the patient suffered with severe polyresistant K. pneumoniae sepsis (D+149), Acinetobacter spp. infection (D+159 to D+198). СRP levels reached 449 mg/L, presepsin was increased to 12839 pg/ml, along with features of multiple organ failure (cardiovascular, hepatic, respiratory, cerebral affection), bilateral pneumonia (K. Pneumonia, Pseudomonas spp.). Artificial lung ventilation was performed for 83 days.<br>
Considering persistent GI bleeding and multiple antibiotic- resistant bacterial complications the patient received TFM via naso-intestinal tube installed under endoscopical control, at the doses of, 80 and 300 mL on D+192 and D+194, respectively. Fourteen days later (D+208), the diarrhea decreased to 1 L/d, and to <500 mL/d by D+280 where GI bleeding was undetectable since D+221. Following the TFM procedure, the beta-lactamase-positive K. pneumoniae (NDM+), was replaced by a more sensitive strain (NDM-), thus enabling ceftazidim+avibactam treatment with a positive effect. Multiple PCR of stool sample has shown an increased bacterial mass, with a maximum at D+8 to D+16 after FMT, with increase in Bacteroides fragilis, Bacteroides thetaiataomicron, Lactobacillus and Bifidobacterium microbial species. Ruxolitimib and Sirolimus were discontinued at D+284 and D+294, respectively. No signs of GVHD were revealed at control GI biopsy, and viral infections (HHV-6, CMV, EBV) were not detectable. The feeding is fully enteral now, with supplementation via gastrostoma.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
The present case report suggests an effective curation of the patient with steroid-resistant GVHD and severe infectious complications observed under combined treatment with JAK2 inhibitor and TFM.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Hematopoietic stem cell transplantation, steroid-resistant graft-versus-host disease, fecal microbiota transplantation, microbiota.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
In allogeneic hematopoietic stem cell transplantation (HSCT), the recipients have altered composition of gastrointestinal (GI) microbiota, due to the use of cytostatic and antibacterial drugs, changes in diet. There is a growing evidence that microbiota influences the immune system, suppresses pathogenic bacteria, promotes regeneration of the GI mucosa. It may prevent immune and infectious complications after HSCT. Transplantation of fecal microbiota (FMT) is directed to recovery of recipient microflora. Our aim was to present a clinical case of a patient with steroid-resistant intestinal graft-versus-host disease (GVHD), stage 4, grade 3, therefore treated by FMT.
Case description
A forty-five year old patient underwent HSCT in Sep 2017, for secondary acute myeloid leukemia (AML) evolving from myelodysplastic syndrome. Hematopoietic graft was from unrelated donor, conditioning regimen included fludarabin+ busulphan (12 mg/kg). Prevention of GVHD was performed with thymoglobulin, tacrolimus, MMF. Since D+67, tacrolimus was tapered and stopped at D+82 due to high relapse risk. From D+102, persistent diarrhea syndrome developed, with up to 3 L/d. The patient was admitted to the R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation. The diarrhea volume reached 5 L/d, and the patient has became septic (fever of 38oC, serum CRP, 331mg/L). Empirical antibiotic therapy consisted of doripenem, vancomycin. Colon biopsy (D+114) identified histological grade 2 of GVHD and multiple viral infection (PCR-positive for HHV-6, CMV, EBV). Tacrolimus was restarted, methylprednisolone at 2 mg/kg, and ganciclovir 10 mg/kg were administered. After 7 days of therapy, the diarrhea volume was 13 L/d. After failure of the first-line treatment, ruxolitimib (20 mg/d) was administered. Due to acute kidney injury, tacrolimus was replaced by sirolimus. At D+133, the diarrhea decreased to 3 L/d. Meanwhile, the stool samples became positive for antibiotic-resistant K. Pneumonia (D+138). The 16S rRNA gene sequencing showed the Staphylococcaceae family to represent 99% of intestinal microbiota. Despite reduced stool volume, no clinical response was achieved. GI bleeding continued from D+139 to D+221 followed by hemorrhagic shock observed at D+144, with blood hemoglobin levels of 39 g/L. In total, the patient was transfused with 29.8 L of RBCs, 5.5 L of platelet concentrate, and 5.9 L of fresh-frozen plasma.
The patient was treated at the ICU from D+118 to D+284 posttransplant. Over this time period, the patient suffered with severe polyresistant K. pneumoniae sepsis (D+149), Acinetobacter spp. infection (D+159 to D+198). СRP levels reached 449 mg/L, presepsin was increased to 12839 pg/ml, along with features of multiple organ failure (cardiovascular, hepatic, respiratory, cerebral affection), bilateral pneumonia (K. Pneumonia, Pseudomonas spp.). Artificial lung ventilation was performed for 83 days.
Considering persistent GI bleeding and multiple antibiotic- resistant bacterial complications the patient received TFM via naso-intestinal tube installed under endoscopical control, at the doses of, 80 and 300 mL on D+192 and D+194, respectively. Fourteen days later (D+208), the diarrhea decreased to 1 L/d, and to <500 mL/d by D+280 where GI bleeding was undetectable since D+221. Following the TFM procedure, the beta-lactamase-positive K. pneumoniae (NDM+), was replaced by a more sensitive strain (NDM-), thus enabling ceftazidim+avibactam treatment with a positive effect. Multiple PCR of stool sample has shown an increased bacterial mass, with a maximum at D+8 to D+16 after FMT, with increase in Bacteroides fragilis, Bacteroides thetaiataomicron, Lactobacillus and Bifidobacterium microbial species. Ruxolitimib and Sirolimus were discontinued at D+284 and D+294, respectively. No signs of GVHD were revealed at control GI biopsy, and viral infections (HHV-6, CMV, EBV) were not detectable. The feeding is fully enteral now, with supplementation via gastrostoma.
Conclusion
The present case report suggests an effective curation of the patient with steroid-resistant GVHD and severe infectious complications observed under combined treatment with JAK2 inhibitor and TFM.
Keywords
Hematopoietic stem cell transplantation, steroid-resistant graft-versus-host disease, fecal microbiota transplantation, microbiota.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20337
[VALUE] => Case report of effective fecal microbiota transplantation to alleviate acute intestinal graft-versus-host disease
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Case report of effective fecal microbiota transplantation to alleviate acute intestinal graft-versus-host disease
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20747
[VALUE] => 1383
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1383
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20748
[VALUE] => 1384
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1384
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Дарья В. Чуракина 1, Олег В. Голощапов 1, Ольга В. Пирогова 1, Александр Н. Швецов 1, Руслана В. Клементьева 1, Александр А. Щербаков 1, Сергей В. Сидоренко 2, Владимир А. Гостев 2, Мария А. Суворова 3, Юрий В. Лобзин 2, Борис В. Афанасьев 1
2 ФГБУ ДНКЦИБ ФМБА России
3 Научно-исследовательская лаборатория Explana, Санкт-Петербург, Российская Федерация
Введение
При проведении аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), вследствие применения цитостатических и антибактериальных препаратов, изменений в диете нарушается состав микробиоты желудочно-кишечного тракта (ЖКТ). Накапливаются данные о том, что микробиота влияет на работу иммунной системы человека, подавляет развитие патогенных микроорганизмов, способствует регенерации эпителия, что препятствует появлению иммунных и инфекционных осложнений после алло-ТГСК. Трансплантация фекальной микробиоты (ТФМ) направлена на восстановление микрофлоры ЖКТ реципиента.
Цель работы
Цель работы состояла в демонстрации клинического случая стероид-резистентного течения острой реакции «трансплантат против хозяина» (оРТПХ) 3 степени тяжести, 4 стадия кишечных проявлений, в котором ТФМ в сочетании с иммуносупрессиной терапии, привела к разрешению оРТПХ кишечника.
Описание случая
Пациент, мужчина, 45 лет. Диагноз: острый миелобластный лейкоз с изменениями, связанными с миелодисплазией. Первые симптомы миелодиспластического синдрома с избытком бластов в марте 2016 года. Проведено 6 курсов 5-азацитидина. 20.02.17 – трансформация в ОМЛ. Терапия малыми дозами цитозара. 23.09.17 алло-ТГСК от неродственного донора с режимом кондиционирования флюдарабин + бусульфан (12 мг/кг). Профилактика РТПХ: тимоглобулин, такролимус, MMF. В связи с высоким риском развития рецидива, на Д+67 снижение дозы такролимуса, с полной отменой на Д+82. С Д+102 диарея до 3 л/сутки. Д+110 – госпитализация в НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой. Cтул в объеме 5 л/сутки, сепсис (лихорадка 38°C, СРБ – 331 мг/л), начата эмпирическая антибактериальная терапия (дорипенем, ванкомицин). Биопсия слизистой толстой кишки (Д+114) – признаки умеренно выраженной РТПХ, вирусного поражения кишечника (ПЦР – HHV-6+, CMV+, EBV+). На Д+114 возобновлен такролимус, начат метилпреднизолон 2 мг/кг, ганцикловир 10 мг/кг. Д+118 – объем стула 13 л/сутки. С Д+117 из-за неэффективности терапии 1 линии начата терапия 2 линии – руксолитиниб 20 мг/сутки. Такролимус, в связи с развитием острого повреждения почек, заменен на сиролимус (Д+121). Д+133 – снижение объема стула до 3 л/сутки. При бактериологическом исследовании стула (Д+138) – обильный рост полирезистентной K. Pneumoniae. При 16S-секвенировании, 99% микробиоты ЖКТ составляло семейство Staphylococcaceae. Ответ по РТПХ кишки не достигнут, с Д +139 до Д+221 – продолжающееся кишечное кровотечение, геморрагический шок от Д+144 (Hb=39 г/л). Суммарно за весь период введено: эритроцитарная масса 29,8 л, тромбоцитарная масса 5,52 л, свежезамороженная плазма – 5,92 л. Получал терапию в отделении реанимации с Д+118 по Д+284. В этот период развились следующие осложнения: тяжелый сепсис, вызванный полирезистентными штаммами K. pneumoniae (Д+149) и Acinetobacter spp. (с Д+159 по Д+198) (уровень СРБ до 449 мг/л, пресепсина до 12839 пг/мл), двухсторонняя пневмония (K. Pneumonia, Pseudomonas spp.), полиорганная недостаточность (сердечно-сосудистая, печеночная, дыхательная, церебральная). Искусственная вентиляция легких в течение 83 дней. На Д+192 и +194 в связи с недостаточным эффектом от иммуносупрессивной терапии проведена ТФМ объемом 80 и 300 мл, через назоинтестинальный зонд, установленный под контролем эндоскопа. За 14 дней объем стула снизился до 1 л/сутки (Д+208), а на Д+280 до 500 мл/сутки, с Д+221 впервые отсутствие крови в стуле. В результате ТФМ, K. pneumoniae, ранее продуцирующая фермент металло-бета-лактамазу (NDM+), сменилась штаммом чувствительным к антибиотикам (NDM-). Это позволило назначить цефтазидим+авибактам с положительным эффектом (снижение прокальцитонина с 26,8 до 0,8 нг/мл). По данным ПЦР образцов стула после ТФМ значительно повысилась общая бактериальная масса (с пиком на Д+8 – Д+16 после ТФМ), за счет увеличения Bacteroides fragilis, Bacteroides thetaiataomicron, Lactobacillus spp., Bifidobacterium spp. Полная отмена руксолитиниба на Д+284 и сиролимуса на Д+294. По результатам контрольной биопсии (Д+337) убедительных признаков РТПХ и вирусного поражения кишечника не выявлено (ПЦР – HHV-6 -, CMV -, EBV -). В настоящее время – стул с тенденцией к оформлению (около 300 г/сутки). Питание самостоятельное и дополнительное через гастростому.
Заключение
В представленном случае продемонстрировано эффективное применение ТФМ в сочетании с JAK2 ингибитором у пациента со стероид-резистентным течением оРТПХ и тяжелыми инфекционными осложнениями.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, стероид-резистентная реакция трансплантат против хозяина, трансплантация фекальной микробиоты, микробиота кишечника.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20520
[VALUE] => Array
(
[TEXT] => Светлана Н. Козловская, Светлана А. Радыгина, Ирина П. Шипицына, Елена И. Гутовская, Константин В. Митраков, Дмитрий Н. Балашов
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Светлана Н. Козловская, Светлана А. Радыгина, Ирина П. Шипицына, Елена И. Гутовская, Константин В. Митраков, Дмитрий Н. Балашов
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20521
[VALUE] => Array
(
[TEXT] => Федеральное государственное бюджетное учреждение «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Министерства здравоохранения Российской Федерации, Москва, Российская Федерация
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Федеральное государственное бюджетное учреждение «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Министерства здравоохранения Российской Федерации, Москва, Российская Федерация
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20522
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Цель</h2>
<p style="text-align: justify;">
Оценка выполнимости и безопасности аллогенной ТГСК с TCRαβ+/CD19+ деплецией у пациентов с первичными иммунодефицитами (ПИД) без использования посттрансплантационной иммуносупрессивной терапии.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
С октября 2017 по май 2018 проведено 10 аллогенных ТГСК от неродственного(n=8) и гаплоидентичного(n=2) доноров с TCRαβ+/CD19+ деплецией трансплантата у пациентов с ПИД (сидром Ниймеген – 1, хроническая гранулематозная болезнь – 2, гипер IgM синдром – 3, ПИД с дефицитом PI3K-дельта – 1, Х-сцепленный лимфопролиферативный синдром I типа – 1, ПИД с дефектом адгезии лейкоцитов I типа – 1, тяжелая врожденная нейтропения – 1). У 9 пациентов проведен режим кондиционирования – треосульфан 42 гр/м2, флударабин 150 мг/м2, мельфалан 140 мг/м2; одному пациенту (синдром Ниймеген) – треосульфан 30 гр/м2, флударабин 150 мг/м2, циклофосфамид 40 мг/кг. В качестве серотерапии во всех случаях использовался антитимоцитарный иммуноглобулин – Тимоглобулин® (“Genzyme Europe B.V.”, Нидерланды) в дозах 5-7,5 мг/кг. Посттрансплантационная иммуносупрессивная терапия для профилактика РТПХ не проводилась.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Приживление трансплантата было зарегистрировано у всех пациентов. Острая РТПХ верифицирована в 3 из 10 случаях, в 2 из которых РТПХ была ограничена исключительно поражением кожи 2 степени. Только у одного пациента (с синдромом Ниймеген) отмечалось развитие острой РТПХ 3 стадии с поражением печени, потребовавшей комбинированной иммуносупрессивной терапии. Все пациенты живы на сроках от 2 до 10 месяцев после ТГСК с хорошими функциональными характеристиками трансплантата.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Исключение иммуносупрессивной терапии из протокола ТГСК с TCRαβ+/CD19+ деплецией у пациентов ПИД продемонстрировало свою безопасность в отношении риска развития РТПХ. Тяжелая висцеральная форма РТПХ была зарегистрирована только у пациента с высоким риском развития данного осложнения, обусловленного особенностями основного заболевания (синдром Ниймеген). В настоящее время набор пациентов продолжается. Поэтому оценка темпов иммунореконституции, частоты реактивации вирусных инфекций и ряд других факторов будут оценены позднее.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Трансплантация гемопоэтических стволовых клеток, TCRαβ+/CD19+ деплеция, реакция трансплантат против хозяина, посттрансплантационная иммуносупрессивная терапия, первичный иммунодефицит.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Цель
Оценка выполнимости и безопасности аллогенной ТГСК с TCRαβ+/CD19+ деплецией у пациентов с первичными иммунодефицитами (ПИД) без использования посттрансплантационной иммуносупрессивной терапии.
Пациенты и методы
С октября 2017 по май 2018 проведено 10 аллогенных ТГСК от неродственного(n=8) и гаплоидентичного(n=2) доноров с TCRαβ+/CD19+ деплецией трансплантата у пациентов с ПИД (сидром Ниймеген – 1, хроническая гранулематозная болезнь – 2, гипер IgM синдром – 3, ПИД с дефицитом PI3K-дельта – 1, Х-сцепленный лимфопролиферативный синдром I типа – 1, ПИД с дефектом адгезии лейкоцитов I типа – 1, тяжелая врожденная нейтропения – 1). У 9 пациентов проведен режим кондиционирования – треосульфан 42 гр/м2, флударабин 150 мг/м2, мельфалан 140 мг/м2; одному пациенту (синдром Ниймеген) – треосульфан 30 гр/м2, флударабин 150 мг/м2, циклофосфамид 40 мг/кг. В качестве серотерапии во всех случаях использовался антитимоцитарный иммуноглобулин – Тимоглобулин® (“Genzyme Europe B.V.”, Нидерланды) в дозах 5-7,5 мг/кг. Посттрансплантационная иммуносупрессивная терапия для профилактика РТПХ не проводилась.
Результаты
Приживление трансплантата было зарегистрировано у всех пациентов. Острая РТПХ верифицирована в 3 из 10 случаях, в 2 из которых РТПХ была ограничена исключительно поражением кожи 2 степени. Только у одного пациента (с синдромом Ниймеген) отмечалось развитие острой РТПХ 3 стадии с поражением печени, потребовавшей комбинированной иммуносупрессивной терапии. Все пациенты живы на сроках от 2 до 10 месяцев после ТГСК с хорошими функциональными характеристиками трансплантата.
Заключение
Исключение иммуносупрессивной терапии из протокола ТГСК с TCRαβ+/CD19+ деплецией у пациентов ПИД продемонстрировало свою безопасность в отношении риска развития РТПХ. Тяжелая висцеральная форма РТПХ была зарегистрирована только у пациента с высоким риском развития данного осложнения, обусловленного особенностями основного заболевания (синдром Ниймеген). В настоящее время набор пациентов продолжается. Поэтому оценка темпов иммунореконституции, частоты реактивации вирусных инфекций и ряд других факторов будут оценены позднее.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, TCRαβ+/CD19+ деплеция, реакция трансплантат против хозяина, посттрансплантационная иммуносупрессивная терапия, первичный иммунодефицит.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20523
[VALUE] => Array
(
[TEXT] => Svetlana N. Kozlovskaya, Svetlana A. Radygina, Irina P. Shypitsyna, Elena I. Gutovskaya, Konstantin V. Mitrakov, Dmitry N. Balashov
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Svetlana N. Kozlovskaya, Svetlana A. Radygina, Irina P. Shypitsyna, Elena I. Gutovskaya, Konstantin V. Mitrakov, Dmitry N. Balashov
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20524
[VALUE] => Array
(
[TEXT] => Dmitriy Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Dmitriy Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20525
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Objective</h2>
<p style="text-align: justify;">
Estimation of feasibility and safety of allogeneic hematopoietic stem cell transplantation (HSCT) with TCRαβ +/CD19+ cell depletion in patients with primary immunodeficiency (PID) without usage of posttransplant immunosuppressive therapy.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
Ten allogeneic HSCTs were performed from October 2017 to May 2018 to the patients with PID (Nijmegen breakage syndrome, 1; Chronic granulomatous disease, 2; CID with CD40L deficiency, 3; PID with PI3K-delta deficiency, 1; X-linked lymphoproliferative syndrome type I, 1; leukocyte adhesion deficiency; 1; severe congenital neutropenia, 1). We carried out trans plants from unrelated (n=8) or haploidentical donors (n=2) using TCRαβ+/CD19 + depletion. Nine patients were conditioned for HSCT with treosulfan 42 g/m2, fludarabine 150 mg/m2, melphalan 140 mg/m2; one patient (Nijmegen’s syndrome) – treosulfan 30 g/m2, fludarabine 150 mg/m2, cyclophosphamide 40 mg/kg. Antithymocyte immunoglobulin – Thymoglobulin® (“Genzyme Europe B.V.”, The Netherlands) was used as a serotherapy at the doses of 5 to 7.5 mg/kg in all cases. Posttransplant GVHD prophylaxis was not performed.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Transplant engraftment was recorded in all the patients. Acute GVHD was verified in 3 out of 10 cases, in 2 of which GVHD of 2nd degree was limited to skin. Only one patient (with Nijmegen syndrome) had acute liver GVHD stage 3 and combined immunosuppressive therapy was required. All the patients are alive at 2 to 10 months after HSCT, with good functional characteristics of the transplants.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Exclusion of posttransplant immunosuppressive therapy after HSCT with TCRαβ+/CD19+ depletion in patients with PID has demonstrated safety in relation to the risk of GVHD development. Severe visceral form of GVHD was recorded only in a patient being at high risk of developing this complication, due to characteristics of the disease (Nijmegen syndrome). Currently, the recruitment of patients is underway, and estimation of immune reconstitution rates reactivation of viral infections, and other factors should be evaluated later.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Hematopoietic stem cell transplantation, TCRαβ+/CD19+ depletion, graft-versus-host disease, posttransplant immunosuppressive therapy, primary immunodeficiency.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Objective
Estimation of feasibility and safety of allogeneic hematopoietic stem cell transplantation (HSCT) with TCRαβ +/CD19+ cell depletion in patients with primary immunodeficiency (PID) without usage of posttransplant immunosuppressive therapy.
Patients and methods
Ten allogeneic HSCTs were performed from October 2017 to May 2018 to the patients with PID (Nijmegen breakage syndrome, 1; Chronic granulomatous disease, 2; CID with CD40L deficiency, 3; PID with PI3K-delta deficiency, 1; X-linked lymphoproliferative syndrome type I, 1; leukocyte adhesion deficiency; 1; severe congenital neutropenia, 1). We carried out trans plants from unrelated (n=8) or haploidentical donors (n=2) using TCRαβ+/CD19 + depletion. Nine patients were conditioned for HSCT with treosulfan 42 g/m2, fludarabine 150 mg/m2, melphalan 140 mg/m2; one patient (Nijmegen’s syndrome) – treosulfan 30 g/m2, fludarabine 150 mg/m2, cyclophosphamide 40 mg/kg. Antithymocyte immunoglobulin – Thymoglobulin® (“Genzyme Europe B.V.”, The Netherlands) was used as a serotherapy at the doses of 5 to 7.5 mg/kg in all cases. Posttransplant GVHD prophylaxis was not performed.
Results
Transplant engraftment was recorded in all the patients. Acute GVHD was verified in 3 out of 10 cases, in 2 of which GVHD of 2nd degree was limited to skin. Only one patient (with Nijmegen syndrome) had acute liver GVHD stage 3 and combined immunosuppressive therapy was required. All the patients are alive at 2 to 10 months after HSCT, with good functional characteristics of the transplants.
Conclusion
Exclusion of posttransplant immunosuppressive therapy after HSCT with TCRαβ+/CD19+ depletion in patients with PID has demonstrated safety in relation to the risk of GVHD development. Severe visceral form of GVHD was recorded only in a patient being at high risk of developing this complication, due to characteristics of the disease (Nijmegen syndrome). Currently, the recruitment of patients is underway, and estimation of immune reconstitution rates reactivation of viral infections, and other factors should be evaluated later.
Keywords
Hematopoietic stem cell transplantation, TCRαβ+/CD19+ depletion, graft-versus-host disease, posttransplant immunosuppressive therapy, primary immunodeficiency.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20526
[VALUE] => The experience of hematopoietic stem cells transplantation with TCRαβ+/CD19+ depletion without posttransplantation prophylaxis of GVHD in patients with primary immunodeficiencies (PID)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => The experience of hematopoietic stem cells transplantation with TCRαβ+/CD19+ depletion without posttransplantation prophylaxis of GVHD in patients with primary immunodeficiencies (PID)
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20783
[VALUE] => 1421
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1421
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20784
[VALUE] => 1422
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1422
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Светлана Н. Козловская, Светлана А. Радыгина, Ирина П. Шипицына, Елена И. Гутовская, Константин В. Митраков, Дмитрий Н. Балашов
Цель
Оценка выполнимости и безопасности аллогенной ТГСК с TCRαβ+/CD19+ деплецией у пациентов с первичными иммунодефицитами (ПИД) без использования посттрансплантационной иммуносупрессивной терапии.
Пациенты и методы
С октября 2017 по май 2018 проведено 10 аллогенных ТГСК от неродственного(n=8) и гаплоидентичного(n=2) доноров с TCRαβ+/CD19+ деплецией трансплантата у пациентов с ПИД (сидром Ниймеген – 1, хроническая гранулематозная болезнь – 2, гипер IgM синдром – 3, ПИД с дефицитом PI3K-дельта – 1, Х-сцепленный лимфопролиферативный синдром I типа – 1, ПИД с дефектом адгезии лейкоцитов I типа – 1, тяжелая врожденная нейтропения – 1). У 9 пациентов проведен режим кондиционирования – треосульфан 42 гр/м2, флударабин 150 мг/м2, мельфалан 140 мг/м2; одному пациенту (синдром Ниймеген) – треосульфан 30 гр/м2, флударабин 150 мг/м2, циклофосфамид 40 мг/кг. В качестве серотерапии во всех случаях использовался антитимоцитарный иммуноглобулин – Тимоглобулин® (“Genzyme Europe B.V.”, Нидерланды) в дозах 5-7,5 мг/кг. Посттрансплантационная иммуносупрессивная терапия для профилактика РТПХ не проводилась.
Результаты
Приживление трансплантата было зарегистрировано у всех пациентов. Острая РТПХ верифицирована в 3 из 10 случаях, в 2 из которых РТПХ была ограничена исключительно поражением кожи 2 степени. Только у одного пациента (с синдромом Ниймеген) отмечалось развитие острой РТПХ 3 стадии с поражением печени, потребовавшей комбинированной иммуносупрессивной терапии. Все пациенты живы на сроках от 2 до 10 месяцев после ТГСК с хорошими функциональными характеристиками трансплантата.
Заключение
Исключение иммуносупрессивной терапии из протокола ТГСК с TCRαβ+/CD19+ деплецией у пациентов ПИД продемонстрировало свою безопасность в отношении риска развития РТПХ. Тяжелая висцеральная форма РТПХ была зарегистрирована только у пациента с высоким риском развития данного осложнения, обусловленного особенностями основного заболевания (синдром Ниймеген). В настоящее время набор пациентов продолжается. Поэтому оценка темпов иммунореконституции, частоты реактивации вирусных инфекций и ряд других факторов будут оценены позднее.
Ключевые слова
Трансплантация гемопоэтических стволовых клеток, TCRαβ+/CD19+ деплеция, реакция трансплантат против хозяина, посттрансплантационная иммуносупрессивная терапия, первичный иммунодефицит.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20529
[VALUE] => Array
(
[TEXT] => Наталья П. Лещук, Андрей Б. Абросимов, Лариса Н. Шелихова
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Наталья П. Лещук, Андрей Б. Абросимов, Лариса Н. Шелихова
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20530
[VALUE] => Array
(
[TEXT] => ФГБУ «НМИЦ ДГОИ имени Дмитрия Рогачева», Москва, Российская Федерация
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => ФГБУ «НМИЦ ДГОИ имени Дмитрия Рогачева», Москва, Российская Федерация
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20531
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Цель</h2>
<p style="text-align: justify;">
Цель работы – изучить роль медицинской сестры и особенности сестринского ухода за пациентами при проведении химиотерапии, инфузионной терапии, трансплантации гемопоэтических стволовых клеток (ТГСК); изучить сестринский процесс подготовки донора к сдаче концентрата периферических мононуклеаров.
</p>
<h2 style="text-align: justify;">Методы исследования</h2>
<p style="text-align: justify;">
За основу исследования был взят протокол ТГСК при остром миелоидном лейкозе (ОМЛ). Стандартные процедуры: 1. Химиотерапия (кондиционирование). 2. Инфузионная терапия. 3. Подготовка донора. 4. ТГСК.
</p>
<h3 style="text-align: justify;">1. Химиотерапия</h3>
<p style="text-align: justify;">
В данный протокол кондиционирования входят следующие препараты: Флударабин, Треосульфан, Тиотепа, Актемра, Оренсия. При введении препаратов на этапе кондиционирования роль медицинской сестры заключается в правильности введения (дозировка и разведение препарата, скорость введения, при необходимости оказание экстренной помощи), знать об возможных осложнениях, применять разработанные рекомендации для профилактики осложнений, обучить родителей и контролировать их выполнение. Профилактика возможных осложнений: а) Кожные покровы. Применение топических стероидов по уходу за кожей, увлажняющих и смягчающих кремов. Ежедневное обтирание моющим лосьоном с применением одноразовых рукавиц для мытья. в) Слизистые оболочки. Использование для полоскания и орошения ротовой полости антисептических растворов; с) Желудочно-кишечный тракт. Предотвращение тошноты и рвоты (рекомендации по питанию, введение противорвотных препаратов). d) Мочеполовая система. Применение антисептических растворов для подмывания наружных половых органов для дезинфицирующего действия. e) Нервная система. По назначению врача выдача лекарственных препаратов, действие которых направлено на устранение тревожности, симптомов периферической нейропатии (мышечная слабость, нарушение мышечного тонуса, дрожание в мышцах, судороги в мышцах).
</p>
<h3 style="text-align: justify;">2. Инфузионная терапия</h3>
<p style="text-align: justify;">
Для эффективной и безопасной инфузионной терапии (ИТ) необходимо владеть полной информацией: продолжительность внутривенных вливаний, правила проведение вливаний, уход за устройством и местом венозного доступа. При проведении инфузионной терапии медицинская сестра должна оценить состояние пациента (подсчет водного баланса, мониторинг жизненно важных функций); провести разъяснительную и просветительную беседу о планируемом лечении.
</p>
<h3 style="text-align: justify;">3. Подготовка донора</h3>
<p style="text-align: justify;">
Важным этапом в проведении ТГСК стоит в подготовке донора стволовых клеток к сдаче материала путем цитафереза. Для получения концентрата периферических мононуклеаров, обогащенного стволовыми гемопоэтическими стволовыми клетками необходима предварительная мобилизация лейкоцитов гранулоцитарным колониестимулирующим фактором (Г-КСФ). Г-КСФ повышает количество лейкоцитов и стимулирует выход стволовых клеток из костного мозга в периферическую кровь. Медицинская сестра в течении 5 дней вводит подкожно препараты Г-КСФ и регистрирует возможные редкие побочные явления. По назначению врача медицинская сестра вводит обезболивающие, осуществляет забор крови для анализов и постановку инфузионной терапии.
</p>
<h3 style="text-align: justify;">4. Трансплантация гемопоэтических стволовых клеток</h3>
<p style="text-align: justify;">
При лечении пациентов по протоколу с диагнозом ОМЛ проводится гаплоидентичная трансплантация гемопоэтических стволовых клеток с TCR альфа/бета и деплецией CD19+ клеток. Преимущества метода: Удалением из трансплантата TCR альфа/бета клеток осуществляется профилактика РТПХ; оставшийся небольшой процент гамма/дельта Т-клеток запускает процесс реконституции иммунной системы и, как следствие – ее более быстрое восстановление. При проведении процедуры трансплантации роль медицинской сестры заключается в следующем: проводить мониторинг жизненно важных функций; обеспечение доступности лекарственных препаратов при побочных осложнениях: для предотвращения реакций или аллоиммунизации использовать фильтры при процедуре трансплантации; медицинская сестра должна знать о возможных осложнениях и уметь оказывать необходимую помощь.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Роль медицинской сестры на протяжении всех стандартных процедур, включенных в протоколы лечения в нашем Центре, имеет огромную значимость. Медицинская сестра должна ознакомить пациента с отделением, объяснить план лечения, назначенный лечащим врачом. Она должна уметь отвечать на вопросы пациента о подготовке к проведению химиотерапии, ТГСК, объяснить, почему химиотерапия может вызывать осложнения и как можно их предотвратить или уменьшить. Развитие побочных реакций при использовании противоопухолевых препаратов и проведении ТГСК создает определенные проблемы для пациента и медицинского персонала, осуществляющего уход, требует от медицинских сестер внимания и индивидуального подхода к каждому из пациентов.
</p>
<h2 style="text-align: justify;">Список литературы</h2>
<p style="text-align: justify;">
1. М. А. Масчан Деплеция альфа/бета-Т-лимфоцитов – надежная платформа для развития трансплантации гемопоэтических стволовых клеток от гаплоидентичных доноров//Российский журнал детской гематологии и онкологии НОДГО. 2015. №3. С. 34-38.<br>
2. Е. В. Самочатова, А. Г. Румянцев Сестринский уход в детской гематологии и онкологии // М.: Издательство «Литтерра», 2011.-220c.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Химиотерапия, кондиционирование, инфузионная терапия, роль медицинской сестры, донор, трансплантация гемопоэтических стволовых клеток.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Цель
Цель работы – изучить роль медицинской сестры и особенности сестринского ухода за пациентами при проведении химиотерапии, инфузионной терапии, трансплантации гемопоэтических стволовых клеток (ТГСК); изучить сестринский процесс подготовки донора к сдаче концентрата периферических мононуклеаров.
Методы исследования
За основу исследования был взят протокол ТГСК при остром миелоидном лейкозе (ОМЛ). Стандартные процедуры: 1. Химиотерапия (кондиционирование). 2. Инфузионная терапия. 3. Подготовка донора. 4. ТГСК.
1. Химиотерапия
В данный протокол кондиционирования входят следующие препараты: Флударабин, Треосульфан, Тиотепа, Актемра, Оренсия. При введении препаратов на этапе кондиционирования роль медицинской сестры заключается в правильности введения (дозировка и разведение препарата, скорость введения, при необходимости оказание экстренной помощи), знать об возможных осложнениях, применять разработанные рекомендации для профилактики осложнений, обучить родителей и контролировать их выполнение. Профилактика возможных осложнений: а) Кожные покровы. Применение топических стероидов по уходу за кожей, увлажняющих и смягчающих кремов. Ежедневное обтирание моющим лосьоном с применением одноразовых рукавиц для мытья. в) Слизистые оболочки. Использование для полоскания и орошения ротовой полости антисептических растворов; с) Желудочно-кишечный тракт. Предотвращение тошноты и рвоты (рекомендации по питанию, введение противорвотных препаратов). d) Мочеполовая система. Применение антисептических растворов для подмывания наружных половых органов для дезинфицирующего действия. e) Нервная система. По назначению врача выдача лекарственных препаратов, действие которых направлено на устранение тревожности, симптомов периферической нейропатии (мышечная слабость, нарушение мышечного тонуса, дрожание в мышцах, судороги в мышцах).
2. Инфузионная терапия
Для эффективной и безопасной инфузионной терапии (ИТ) необходимо владеть полной информацией: продолжительность внутривенных вливаний, правила проведение вливаний, уход за устройством и местом венозного доступа. При проведении инфузионной терапии медицинская сестра должна оценить состояние пациента (подсчет водного баланса, мониторинг жизненно важных функций); провести разъяснительную и просветительную беседу о планируемом лечении.
3. Подготовка донора
Важным этапом в проведении ТГСК стоит в подготовке донора стволовых клеток к сдаче материала путем цитафереза. Для получения концентрата периферических мононуклеаров, обогащенного стволовыми гемопоэтическими стволовыми клетками необходима предварительная мобилизация лейкоцитов гранулоцитарным колониестимулирующим фактором (Г-КСФ). Г-КСФ повышает количество лейкоцитов и стимулирует выход стволовых клеток из костного мозга в периферическую кровь. Медицинская сестра в течении 5 дней вводит подкожно препараты Г-КСФ и регистрирует возможные редкие побочные явления. По назначению врача медицинская сестра вводит обезболивающие, осуществляет забор крови для анализов и постановку инфузионной терапии.
4. Трансплантация гемопоэтических стволовых клеток
При лечении пациентов по протоколу с диагнозом ОМЛ проводится гаплоидентичная трансплантация гемопоэтических стволовых клеток с TCR альфа/бета и деплецией CD19+ клеток. Преимущества метода: Удалением из трансплантата TCR альфа/бета клеток осуществляется профилактика РТПХ; оставшийся небольшой процент гамма/дельта Т-клеток запускает процесс реконституции иммунной системы и, как следствие – ее более быстрое восстановление. При проведении процедуры трансплантации роль медицинской сестры заключается в следующем: проводить мониторинг жизненно важных функций; обеспечение доступности лекарственных препаратов при побочных осложнениях: для предотвращения реакций или аллоиммунизации использовать фильтры при процедуре трансплантации; медицинская сестра должна знать о возможных осложнениях и уметь оказывать необходимую помощь.
Заключение
Роль медицинской сестры на протяжении всех стандартных процедур, включенных в протоколы лечения в нашем Центре, имеет огромную значимость. Медицинская сестра должна ознакомить пациента с отделением, объяснить план лечения, назначенный лечащим врачом. Она должна уметь отвечать на вопросы пациента о подготовке к проведению химиотерапии, ТГСК, объяснить, почему химиотерапия может вызывать осложнения и как можно их предотвратить или уменьшить. Развитие побочных реакций при использовании противоопухолевых препаратов и проведении ТГСК создает определенные проблемы для пациента и медицинского персонала, осуществляющего уход, требует от медицинских сестер внимания и индивидуального подхода к каждому из пациентов.
Список литературы
1. М. А. Масчан Деплеция альфа/бета-Т-лимфоцитов – надежная платформа для развития трансплантации гемопоэтических стволовых клеток от гаплоидентичных доноров//Российский журнал детской гематологии и онкологии НОДГО. 2015. №3. С. 34-38.
2. Е. В. Самочатова, А. Г. Румянцев Сестринский уход в детской гематологии и онкологии // М.: Издательство «Литтерра», 2011.-220c.
Ключевые слова
Химиотерапия, кондиционирование, инфузионная терапия, роль медицинской сестры, донор, трансплантация гемопоэтических стволовых клеток.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20532
[VALUE] => Array
(
[TEXT] => Natalia P. Leshchuk, Andrei B. Abrosimov, Larisa N. Shelikhova
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Natalia P. Leshchuk, Andrei B. Abrosimov, Larisa N. Shelikhova
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20533
[VALUE] => Array
(
[TEXT] => D. Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => D. Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20534
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Aim</h2>
<p style="text-align: justify;">
The aim of this study is to explore the role of a nurse and the specifics of nursing care during chemotherapy, infusion therapy, hematopoietic stem cell transplantation (HSCT) and study the process of a donor preparation for the donation of a peripheral blood mononuclear cell (PMBC) concentrate.
</p>
<h2 style="text-align: justify;">Methods of investigation</h2>
<p style="text-align: justify;">
The study is based on the HSCT protocol in acute myeloid leukemia (AML). The standard procedures included: 1. Chemotherapy (conditioning). 2. Infusion therapy. 3. Preparation of a donor. 4. HSCT.
</p>
<h3 style="text-align: justify;">1. Chemotherapy stage</h3>
<p style="text-align: justify;">
This conditioning treatment protocol includes the following chemotherapy agents: Fludarabine, Treosulfan, Thiotepa, Actemra, Orencia. When using drugs within the conditioning treatment, the role of a nurse is to ensure the prescribed injection regimen (drug dosage and dilution, speed of injection, first aid, if necessary). A nurse should be aware of any possible complications, apply recommendations for the prevention of complications, educate patient’s parents on these recommendations. Prevention of potential complications: a) Skin: use of topical corticosteroids, moisturizing and softening creams for skin care. Daily application of cleansing lotion using disposable wash gloves. b) Mucous membranes. Use of oral antiseptic solution (gargling and irrigation); c) Gastrointestinal system: prevention of nausea and vomiting (dietary recommendations, use of antiemetics). d) Urogenital system: application of an antiseptic solution to the external genitalia for purposes of disinfection. e) Nervous system: distribution of prescribed medications which are aimed for management of anxiety, peripheral neuropathy symptoms (muscle weakness, muscle tone impairment, tremor, muscle spasm).
</p>
<h3 style="text-align: justify;">2. Infusion therapy</h3>
<p style="text-align: justify;">
In order to provide effective and safe infusion therapy (IT) delivery it is necessary to have a detailed information on the following aspects: duration of intravenous infusions, guidelines of infusions, venous access site care and equipment maintenance. Before starting the infusion therapy, a nurse must perform an assessment of a patient (fluid balance measurement, patient’s vital signs monitoring); educate and inform a patient and her/his parents about the planned treatment.
</p>
<h3 style="text-align: justify;">3. Preparation of a donor</h3>
<p style="text-align: justify;">
An important stage in HSCT is to prepare a donor for stem cell donation by means of cytapheresis. To obtain a peripheral blood mononuclear cell concentrate enriched in hematopoietic stem cells, a preliminary G-CSF-induced leukocyte mobilization is required. G-CSF increases WBC count and stimulates stem cell release from the bone marrow into the peripheral blood. A nurse performs subcutaneous injections of G-CSF for 5 days and registers possible uncommon side effects. At doctor’s instruction a nurse performs an injection of anesthesia, collects blood for testing and places a catheter for the infusion therapy.
</p>
<h3 style="text-align: justify;">4. Hematopoietic stem cell transplantation</h3>
<p style="text-align: justify;">
During the treatment on the AML protocol, TCR-Alpha/Beta and CD19 depleted haploidentical stem cell transplantation is performed. The advantages of the method: TCR aplha/beta cells are removed from the graft to perform a GVHD prophylaxis. The remaining small percentage of gamma/delta T-cells induces a faster immune system recovery and, as a consequence, leads to more rapid immune reconstitution. During the procedure of transplantation, a nurse is responsible for: monitoring of patient’s vital signs; ensuring the availability of drugs for side effect management; using filters to prevent transfusion reactions and alloimmunization during transplantation. A nurse should be aware of potential complications and provide an appropriate assistance.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Nursing staff plays an important role in implementation of all standard procedures of treatment protocols at our Center. A nurse must guide the patient through the department and inform her/him of the treatment plan prescribed by the treating physician. She should be able to answer the patient’s questions relating to the preparation for the chemotherapy and HSCT, explain the cause of the chemotherapy-induced complications and inform the patient on how to prevent or reduce them. Side effects induced by anti-cancer drugs and HSCT creates certain problems for a patient and medical staff involved in care, management of which require the assistance of nursing staff and personalized approach to each patient.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Chemotherapy, conditioning, infusion therapy, role of nurse, donor, hematopoietic stem cell transplantation.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Aim
The aim of this study is to explore the role of a nurse and the specifics of nursing care during chemotherapy, infusion therapy, hematopoietic stem cell transplantation (HSCT) and study the process of a donor preparation for the donation of a peripheral blood mononuclear cell (PMBC) concentrate.
Methods of investigation
The study is based on the HSCT protocol in acute myeloid leukemia (AML). The standard procedures included: 1. Chemotherapy (conditioning). 2. Infusion therapy. 3. Preparation of a donor. 4. HSCT.
1. Chemotherapy stage
This conditioning treatment protocol includes the following chemotherapy agents: Fludarabine, Treosulfan, Thiotepa, Actemra, Orencia. When using drugs within the conditioning treatment, the role of a nurse is to ensure the prescribed injection regimen (drug dosage and dilution, speed of injection, first aid, if necessary). A nurse should be aware of any possible complications, apply recommendations for the prevention of complications, educate patient’s parents on these recommendations. Prevention of potential complications: a) Skin: use of topical corticosteroids, moisturizing and softening creams for skin care. Daily application of cleansing lotion using disposable wash gloves. b) Mucous membranes. Use of oral antiseptic solution (gargling and irrigation); c) Gastrointestinal system: prevention of nausea and vomiting (dietary recommendations, use of antiemetics). d) Urogenital system: application of an antiseptic solution to the external genitalia for purposes of disinfection. e) Nervous system: distribution of prescribed medications which are aimed for management of anxiety, peripheral neuropathy symptoms (muscle weakness, muscle tone impairment, tremor, muscle spasm).
2. Infusion therapy
In order to provide effective and safe infusion therapy (IT) delivery it is necessary to have a detailed information on the following aspects: duration of intravenous infusions, guidelines of infusions, venous access site care and equipment maintenance. Before starting the infusion therapy, a nurse must perform an assessment of a patient (fluid balance measurement, patient’s vital signs monitoring); educate and inform a patient and her/his parents about the planned treatment.
3. Preparation of a donor
An important stage in HSCT is to prepare a donor for stem cell donation by means of cytapheresis. To obtain a peripheral blood mononuclear cell concentrate enriched in hematopoietic stem cells, a preliminary G-CSF-induced leukocyte mobilization is required. G-CSF increases WBC count and stimulates stem cell release from the bone marrow into the peripheral blood. A nurse performs subcutaneous injections of G-CSF for 5 days and registers possible uncommon side effects. At doctor’s instruction a nurse performs an injection of anesthesia, collects blood for testing and places a catheter for the infusion therapy.
4. Hematopoietic stem cell transplantation
During the treatment on the AML protocol, TCR-Alpha/Beta and CD19 depleted haploidentical stem cell transplantation is performed. The advantages of the method: TCR aplha/beta cells are removed from the graft to perform a GVHD prophylaxis. The remaining small percentage of gamma/delta T-cells induces a faster immune system recovery and, as a consequence, leads to more rapid immune reconstitution. During the procedure of transplantation, a nurse is responsible for: monitoring of patient’s vital signs; ensuring the availability of drugs for side effect management; using filters to prevent transfusion reactions and alloimmunization during transplantation. A nurse should be aware of potential complications and provide an appropriate assistance.
Conclusion
Nursing staff plays an important role in implementation of all standard procedures of treatment protocols at our Center. A nurse must guide the patient through the department and inform her/him of the treatment plan prescribed by the treating physician. She should be able to answer the patient’s questions relating to the preparation for the chemotherapy and HSCT, explain the cause of the chemotherapy-induced complications and inform the patient on how to prevent or reduce them. Side effects induced by anti-cancer drugs and HSCT creates certain problems for a patient and medical staff involved in care, management of which require the assistance of nursing staff and personalized approach to each patient.
Keywords
Chemotherapy, conditioning, infusion therapy, role of nurse, donor, hematopoietic stem cell transplantation.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20535
[VALUE] => Chemotherapy, infusion therapy: the role of a nurse
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Chemotherapy, infusion therapy: the role of a nurse
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20787
[VALUE] => 1425
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1425
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20788
[VALUE] => 1426
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1426
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Наталья П. Лещук, Андрей Б. Абросимов, Лариса Н. Шелихова
Цель
Цель работы – изучить роль медицинской сестры и особенности сестринского ухода за пациентами при проведении химиотерапии, инфузионной терапии, трансплантации гемопоэтических стволовых клеток (ТГСК); изучить сестринский процесс подготовки донора к сдаче концентрата периферических мононуклеаров.
Методы исследования
За основу исследования был взят протокол ТГСК при остром миелоидном лейкозе (ОМЛ). Стандартные процедуры: 1. Химиотерапия (кондиционирование). 2. Инфузионная терапия. 3. Подготовка донора. 4. ТГСК.
1. Химиотерапия
В данный протокол кондиционирования входят следующие препараты: Флударабин, Треосульфан, Тиотепа, Актемра, Оренсия. При введении препаратов на этапе кондиционирования роль медицинской сестры заключается в правильности введения (дозировка и разведение препарата, скорость введения, при необходимости оказание экстренной помощи), знать об возможных осложнениях, применять разработанные рекомендации для профилактики осложнений, обучить родителей и контролировать их выполнение. Профилактика возможных осложнений: а) Кожные покровы. Применение топических стероидов по уходу за кожей, увлажняющих и смягчающих кремов. Ежедневное обтирание моющим лосьоном с применением одноразовых рукавиц для мытья. в) Слизистые оболочки. Использование для полоскания и орошения ротовой полости антисептических растворов; с) Желудочно-кишечный тракт. Предотвращение тошноты и рвоты (рекомендации по питанию, введение противорвотных препаратов). d) Мочеполовая система. Применение антисептических растворов для подмывания наружных половых органов для дезинфицирующего действия. e) Нервная система. По назначению врача выдача лекарственных препаратов, действие которых направлено на устранение тревожности, симптомов периферической нейропатии (мышечная слабость, нарушение мышечного тонуса, дрожание в мышцах, судороги в мышцах).
2. Инфузионная терапия
Для эффективной и безопасной инфузионной терапии (ИТ) необходимо владеть полной информацией: продолжительность внутривенных вливаний, правила проведение вливаний, уход за устройством и местом венозного доступа. При проведении инфузионной терапии медицинская сестра должна оценить состояние пациента (подсчет водного баланса, мониторинг жизненно важных функций); провести разъяснительную и просветительную беседу о планируемом лечении.
3. Подготовка донора
Важным этапом в проведении ТГСК стоит в подготовке донора стволовых клеток к сдаче материала путем цитафереза. Для получения концентрата периферических мононуклеаров, обогащенного стволовыми гемопоэтическими стволовыми клетками необходима предварительная мобилизация лейкоцитов гранулоцитарным колониестимулирующим фактором (Г-КСФ). Г-КСФ повышает количество лейкоцитов и стимулирует выход стволовых клеток из костного мозга в периферическую кровь. Медицинская сестра в течении 5 дней вводит подкожно препараты Г-КСФ и регистрирует возможные редкие побочные явления. По назначению врача медицинская сестра вводит обезболивающие, осуществляет забор крови для анализов и постановку инфузионной терапии.
4. Трансплантация гемопоэтических стволовых клеток
При лечении пациентов по протоколу с диагнозом ОМЛ проводится гаплоидентичная трансплантация гемопоэтических стволовых клеток с TCR альфа/бета и деплецией CD19+ клеток. Преимущества метода: Удалением из трансплантата TCR альфа/бета клеток осуществляется профилактика РТПХ; оставшийся небольшой процент гамма/дельта Т-клеток запускает процесс реконституции иммунной системы и, как следствие – ее более быстрое восстановление. При проведении процедуры трансплантации роль медицинской сестры заключается в следующем: проводить мониторинг жизненно важных функций; обеспечение доступности лекарственных препаратов при побочных осложнениях: для предотвращения реакций или аллоиммунизации использовать фильтры при процедуре трансплантации; медицинская сестра должна знать о возможных осложнениях и уметь оказывать необходимую помощь.
Заключение
Роль медицинской сестры на протяжении всех стандартных процедур, включенных в протоколы лечения в нашем Центре, имеет огромную значимость. Медицинская сестра должна ознакомить пациента с отделением, объяснить план лечения, назначенный лечащим врачом. Она должна уметь отвечать на вопросы пациента о подготовке к проведению химиотерапии, ТГСК, объяснить, почему химиотерапия может вызывать осложнения и как можно их предотвратить или уменьшить. Развитие побочных реакций при использовании противоопухолевых препаратов и проведении ТГСК создает определенные проблемы для пациента и медицинского персонала, осуществляющего уход, требует от медицинских сестер внимания и индивидуального подхода к каждому из пациентов.
Список литературы
1. М. А. Масчан Деплеция альфа/бета-Т-лимфоцитов – надежная платформа для развития трансплантации гемопоэтических стволовых клеток от гаплоидентичных доноров//Российский журнал детской гематологии и онкологии НОДГО. 2015. №3. С. 34-38.
2. Е. В. Самочатова, А. Г. Румянцев Сестринский уход в детской гематологии и онкологии // М.: Издательство «Литтерра», 2011.-220c.
Ключевые слова
Химиотерапия, кондиционирование, инфузионная терапия, роль медицинской сестры, донор, трансплантация гемопоэтических стволовых клеток.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20662
[VALUE] => Array
(
[TEXT] => Юлия В. Скворцова <sup>1</sup>, Ирина П. Шипицына <sup>1</sup>, Дмитрий Н. Балашов <sup>1</sup>, Павел Е. Трахтман <sup>1</sup>, Елена В. Скоробогатова <sup>2</sup>, Людмила И. Папуша <sup>1</sup>, Елена И. Гутовская <sup>1</sup>, Лариса Н. Шелихова <sup>1</sup>, Елена Е. Курникова <sup>1</sup>, Кирилл А. Воронин <sup>1</sup>, Михаил А. Масчан <sup>1</sup>, Алексей А. Масчан <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Юлия В. Скворцова 1, Ирина П. Шипицына 1, Дмитрий Н. Балашов 1, Павел Е. Трахтман 1, Елена В. Скоробогатова 2, Людмила И. Папуша 1, Елена И. Гутовская 1, Лариса Н. Шелихова 1, Елена Е. Курникова 1, Кирилл А. Воронин 1, Михаил А. Масчан 1, Алексей А. Масчан 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20663
[VALUE] => Array
(
[TEXT] => <sup>1</sup> ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» МЗ РФ
<sup>2</sup> ФГБУ «Российская детская клиническая больница» МЗ РФ
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» МЗ РФ
2 ФГБУ «Российская детская клиническая больница» МЗ РФ
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20664
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Треосульфан активно используется в качестве миелоаблативного и иммуносупрессивного компонента современных режимов кондиционирования, что позволяет снизить раннюю токсичность аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Однако, отсутствуют данные о его поздних эффектах. Целью исследования явилось ретроспективное изучение поздних осложнений при проведении треосульфани бусульфан-содержащих миелоаблативных режимов кондиционирования у детей.
</p>
<h2 style="text-align: justify;">Методы</h2>
<p style="text-align: justify;">
Проведен сравнительный анализ поздних осложнений у детей, получивших алло-ТГСК на базе отделения трансплантации костного мозга Российской детской клинической больницы (РДКБ)/Национального медицинского исследовательского центра детской гематологии, онкологии и иммунологии им. Дм. Рогачева (НМИЦ ДГОИ) (г. Москва, Россия) с 1994 по 2011 гг., имевших бусульфан- (группа 1, n=110, медиана наблюдения 7,4 г.) или треосульфан-содержащее (группа 2, n=38, медиана наблюдения 5,7 г.) кондиционирование и проживших минимум 1 г. от момента ТГСК. Учитывая различие в медианах наблюдения, статистический анализ проводили на сроке 5 лет от момента алло-ТГСК для обеих групп. Оценивали развитие хронической РТПХ, патологии эндокринной, нервной, сердечно-сосудистой систем, снижение костной минеральной плотности, развитие вторичных злокачественных заболеваний.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Пациенты с гемобластозами (105 в группе с бусульфаном и 30 в группе с треосульфаном) имели схожие показатели 5-летней выживаемости: общая выживаемость в 1-й и 2-й группах составила 79,3% и 66,1%, а безрецидивная выживаемость – 82,5% и 74,1%, соответственно. Частота хронической РТПХ – 57% в группе с треосульфаном и 50% в группе с бусульфаном. Кумулятивный риск развития экстенсивной хронической РТПХ составил 27,6% в 1-й группе и 43,3% во 2-й группе. При анализе других поздних осложнений обнаружено снижение частоты развития эндокринных нарушений в группе с треосульфаном – 27% против 43% в 1-й группе, при этом не зарегистрировано ни одного случая развития гипергонадотропного гипогонадизма (кумулятивный риск развития 32,8% в 1-й группе против 0% во 2-й, р = 0,012). Патология щитовидной железы в структуре эндокринных нарушений также преобладала в 1-й группе детей – 29% против 13%. Патология центральной нервной системы в группе с треосульфаном носила в большей степени функциональный характер в отличие от преобладания органических нарушений в 1-й группе: не зарегистрировано ни одного случая энцефалопатии, вторичной эпилепсии. Также отмечались качественные различия в развитии кардиоваскулярной патологии – 16% в 1-й группе с преобладанием вторичной кардиомиопатии против 10% во 2-й группе. В обеих группах зарегистрировано по одному случаю вторичных неоплазий на поздних сроках после ТГСК. Cреди детей с незлокачественными заболеваниями (первичными иммунодефицитами) 5 получили бусульфан-содержащее кондиционирование, а 8 – треосульфан-содержащее. Общая 5-летняя выживаемость составила 87,5% в 1-й группе против 60% во 2-й. Существенных различий в частоте поздних осложнений алло-ТГСК не выявлено.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Треосульфан-содержащее миелоаблативное кондиционирование позволяет снизить риск развития поздних осложнений со стороны эндокринной системы (особенно гипогонадизма), центральной нервной системы и кардиоваскулярных нарушений после алло-ТГСК у детей по сравнению с классическими бусульфан-содержащими режимами.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Алло-ТГСК, кондиционирование, треосульфан, поздние осложнения, дети.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Треосульфан активно используется в качестве миелоаблативного и иммуносупрессивного компонента современных режимов кондиционирования, что позволяет снизить раннюю токсичность аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Однако, отсутствуют данные о его поздних эффектах. Целью исследования явилось ретроспективное изучение поздних осложнений при проведении треосульфани бусульфан-содержащих миелоаблативных режимов кондиционирования у детей.
Методы
Проведен сравнительный анализ поздних осложнений у детей, получивших алло-ТГСК на базе отделения трансплантации костного мозга Российской детской клинической больницы (РДКБ)/Национального медицинского исследовательского центра детской гематологии, онкологии и иммунологии им. Дм. Рогачева (НМИЦ ДГОИ) (г. Москва, Россия) с 1994 по 2011 гг., имевших бусульфан- (группа 1, n=110, медиана наблюдения 7,4 г.) или треосульфан-содержащее (группа 2, n=38, медиана наблюдения 5,7 г.) кондиционирование и проживших минимум 1 г. от момента ТГСК. Учитывая различие в медианах наблюдения, статистический анализ проводили на сроке 5 лет от момента алло-ТГСК для обеих групп. Оценивали развитие хронической РТПХ, патологии эндокринной, нервной, сердечно-сосудистой систем, снижение костной минеральной плотности, развитие вторичных злокачественных заболеваний.
Результаты
Пациенты с гемобластозами (105 в группе с бусульфаном и 30 в группе с треосульфаном) имели схожие показатели 5-летней выживаемости: общая выживаемость в 1-й и 2-й группах составила 79,3% и 66,1%, а безрецидивная выживаемость – 82,5% и 74,1%, соответственно. Частота хронической РТПХ – 57% в группе с треосульфаном и 50% в группе с бусульфаном. Кумулятивный риск развития экстенсивной хронической РТПХ составил 27,6% в 1-й группе и 43,3% во 2-й группе. При анализе других поздних осложнений обнаружено снижение частоты развития эндокринных нарушений в группе с треосульфаном – 27% против 43% в 1-й группе, при этом не зарегистрировано ни одного случая развития гипергонадотропного гипогонадизма (кумулятивный риск развития 32,8% в 1-й группе против 0% во 2-й, р = 0,012). Патология щитовидной железы в структуре эндокринных нарушений также преобладала в 1-й группе детей – 29% против 13%. Патология центральной нервной системы в группе с треосульфаном носила в большей степени функциональный характер в отличие от преобладания органических нарушений в 1-й группе: не зарегистрировано ни одного случая энцефалопатии, вторичной эпилепсии. Также отмечались качественные различия в развитии кардиоваскулярной патологии – 16% в 1-й группе с преобладанием вторичной кардиомиопатии против 10% во 2-й группе. В обеих группах зарегистрировано по одному случаю вторичных неоплазий на поздних сроках после ТГСК. Cреди детей с незлокачественными заболеваниями (первичными иммунодефицитами) 5 получили бусульфан-содержащее кондиционирование, а 8 – треосульфан-содержащее. Общая 5-летняя выживаемость составила 87,5% в 1-й группе против 60% во 2-й. Существенных различий в частоте поздних осложнений алло-ТГСК не выявлено.
Заключение
Треосульфан-содержащее миелоаблативное кондиционирование позволяет снизить риск развития поздних осложнений со стороны эндокринной системы (особенно гипогонадизма), центральной нервной системы и кардиоваскулярных нарушений после алло-ТГСК у детей по сравнению с классическими бусульфан-содержащими режимами.
Ключевые слова
Алло-ТГСК, кондиционирование, треосульфан, поздние осложнения, дети.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20665
[VALUE] => Array
(
[TEXT] => Yulia V. Skvortsova <sup>1</sup>, Irina P. Shipitsina <sup>1</sup>, Dmitrij N. Balashov <sup>1</sup>, Pavel E. Trakhtman <sup>1</sup>, Elena V. Skorobogatova <sup>2</sup>, Ludmila I. Papusha <sup>1</sup>, Elena I. Gutovskaya <sup>1</sup>, Larisa N. Shelikhova <sup>1</sup>, Elena E. Kurnikova <sup>1</sup>, Kirill A. Voronin <sup>1</sup>, Michael A. Maschan <sup>1</sup>, Alexei A. Maschan <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Yulia V. Skvortsova 1, Irina P. Shipitsina 1, Dmitrij N. Balashov 1, Pavel E. Trakhtman 1, Elena V. Skorobogatova 2, Ludmila I. Papusha 1, Elena I. Gutovskaya 1, Larisa N. Shelikhova 1, Elena E. Kurnikova 1, Kirill A. Voronin 1, Michael A. Maschan 1, Alexei A. Maschan 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20666
[VALUE] => Array
(
[TEXT] => <sup>1</sup> Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology (Moscow, Russian Federation)
<sup>2</sup> Russian Children’s Hospital, Moscow, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology (Moscow, Russian Federation)
2 Russian Children’s Hospital, Moscow, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20667
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Treosulfan is actively used as myeloablative and immunosuppressive agent in modern conditioning regimens, while exhibiting a reduced early toxicity in the setting of allogeneic hematopoietic stem cell transplantation (allo-HSCT). But there are no data about long-term effects. The aim of this study was retrospective analysis of late effects after treosulfan-and busulfan-based myeloablative conditioning regimens in children.
</p>
<h2 style="text-align: justify;">Methods</h2>
<p style="text-align: justify;">
We propose a comparative analysis of late effects in children, who got allo-HSCT at BMT Department of Russian Children’s Hospital/Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology (Moscow, Russia) between 2004 and 2011 with busulfan- (group 1, n=110, median follow-up 7.4 yrs) or treosulfan-based (group 2, n=38, median follow-up 5.7 yrs) and survived at least 1 year after HSCT. The statistical analysis was carried out for the median period of 5 years after allo-HSCT for both groups. Chronic graft-versus-host disease (GVHD), pathology of endocrine, nervous, cardiovascular systems, bone mineral turnover and secondary malignancies were studied.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Patients with malignant diseases (105 in busulfan group and 30 in treosulfan group) had similar 5-year survival results: overall survival in 1st and 2nd groups were 79.3% and 66.1%, relapse-free survival – 82.5% and 74.1%, respectively. Chronic GVHD incidence was 57% in treosulfan group and 50% in busulfan group. Cumulative incidence (CI) of chronic extensive GVHD was 27.6% in group 1 and 43.3% in group 2. The analysis of other late effects revealed the reduction of endocrine complications in treosulfan group, 27% against 43% in the 1st group, none had hypergonadotropic hypogonadism (CI 32.8% in group 1 opposite to 0% in group 2, р = 0.012). Thyroid gland pathology dominated in group 1 – 29% opposite to 13% in group 2. Central nervous system pathology in treosulfan group was functional unlike predominance of organic impairment in group 1: no cases of encephalopathy or secondary epilepsy were registered. Differences in cardiovascular complications incidence were revealed, i.e., 16% in group 1 with secondary cardiomyopathy predominance in contrast with 10% in group 2. Both groups demonstrated one case of secondary neoplasms after a long follow-up period. Among patients with nonmalignant disorders (primary immunodeficiencies), 5 got busulfan-based conditioning and 8 received treosulfan-based treatment. Overall 5-year survival was 87.5% in group 1 and 60% in group 2. No significant differences in late effects after allo-HSCT were revealed.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Treosulfan-based myeloablative conditioning allows to reduce incidence of late endocrine complications (especially, hypogonadism), central nervous system and cardiovascular system pathology after allogeneic HSCT in children when compared with classical busulfan-based conditioning regimens.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Allogeneic HSCT, conditioning, treosulfan, late complications, children.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Treosulfan is actively used as myeloablative and immunosuppressive agent in modern conditioning regimens, while exhibiting a reduced early toxicity in the setting of allogeneic hematopoietic stem cell transplantation (allo-HSCT). But there are no data about long-term effects. The aim of this study was retrospective analysis of late effects after treosulfan-and busulfan-based myeloablative conditioning regimens in children.
Methods
We propose a comparative analysis of late effects in children, who got allo-HSCT at BMT Department of Russian Children’s Hospital/Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology (Moscow, Russia) between 2004 and 2011 with busulfan- (group 1, n=110, median follow-up 7.4 yrs) or treosulfan-based (group 2, n=38, median follow-up 5.7 yrs) and survived at least 1 year after HSCT. The statistical analysis was carried out for the median period of 5 years after allo-HSCT for both groups. Chronic graft-versus-host disease (GVHD), pathology of endocrine, nervous, cardiovascular systems, bone mineral turnover and secondary malignancies were studied.
Results
Patients with malignant diseases (105 in busulfan group and 30 in treosulfan group) had similar 5-year survival results: overall survival in 1st and 2nd groups were 79.3% and 66.1%, relapse-free survival – 82.5% and 74.1%, respectively. Chronic GVHD incidence was 57% in treosulfan group and 50% in busulfan group. Cumulative incidence (CI) of chronic extensive GVHD was 27.6% in group 1 and 43.3% in group 2. The analysis of other late effects revealed the reduction of endocrine complications in treosulfan group, 27% against 43% in the 1st group, none had hypergonadotropic hypogonadism (CI 32.8% in group 1 opposite to 0% in group 2, р = 0.012). Thyroid gland pathology dominated in group 1 – 29% opposite to 13% in group 2. Central nervous system pathology in treosulfan group was functional unlike predominance of organic impairment in group 1: no cases of encephalopathy or secondary epilepsy were registered. Differences in cardiovascular complications incidence were revealed, i.e., 16% in group 1 with secondary cardiomyopathy predominance in contrast with 10% in group 2. Both groups demonstrated one case of secondary neoplasms after a long follow-up period. Among patients with nonmalignant disorders (primary immunodeficiencies), 5 got busulfan-based conditioning and 8 received treosulfan-based treatment. Overall 5-year survival was 87.5% in group 1 and 60% in group 2. No significant differences in late effects after allo-HSCT were revealed.
Conclusion
Treosulfan-based myeloablative conditioning allows to reduce incidence of late endocrine complications (especially, hypogonadism), central nervous system and cardiovascular system pathology after allogeneic HSCT in children when compared with classical busulfan-based conditioning regimens.
Keywords
Allogeneic HSCT, conditioning, treosulfan, late complications, children.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20668
[VALUE] => Comparative analysis of late effects after treosulfan- and busulfan-based myeloablative conditioning regimens for allogeneic hematopoietic stem cell transplantation in children
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Comparative analysis of late effects after treosulfan- and busulfan-based myeloablative conditioning regimens for allogeneic hematopoietic stem cell transplantation in children
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20823
[VALUE] => 1461
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1461
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20824
[VALUE] => 1462
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1462
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Юлия В. Скворцова 1, Ирина П. Шипицына 1, Дмитрий Н. Балашов 1, Павел Е. Трахтман 1, Елена В. Скоробогатова 2, Людмила И. Папуша 1, Елена И. Гутовская 1, Лариса Н. Шелихова 1, Елена Е. Курникова 1, Кирилл А. Воронин 1, Михаил А. Масчан 1, Алексей А. Масчан 1
Введение
Треосульфан активно используется в качестве миелоаблативного и иммуносупрессивного компонента современных режимов кондиционирования, что позволяет снизить раннюю токсичность аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Однако, отсутствуют данные о его поздних эффектах. Целью исследования явилось ретроспективное изучение поздних осложнений при проведении треосульфани бусульфан-содержащих миелоаблативных режимов кондиционирования у детей.
Методы
Проведен сравнительный анализ поздних осложнений у детей, получивших алло-ТГСК на базе отделения трансплантации костного мозга Российской детской клинической больницы (РДКБ)/Национального медицинского исследовательского центра детской гематологии, онкологии и иммунологии им. Дм. Рогачева (НМИЦ ДГОИ) (г. Москва, Россия) с 1994 по 2011 гг., имевших бусульфан- (группа 1, n=110, медиана наблюдения 7,4 г.) или треосульфан-содержащее (группа 2, n=38, медиана наблюдения 5,7 г.) кондиционирование и проживших минимум 1 г. от момента ТГСК. Учитывая различие в медианах наблюдения, статистический анализ проводили на сроке 5 лет от момента алло-ТГСК для обеих групп. Оценивали развитие хронической РТПХ, патологии эндокринной, нервной, сердечно-сосудистой систем, снижение костной минеральной плотности, развитие вторичных злокачественных заболеваний.
Результаты
Пациенты с гемобластозами (105 в группе с бусульфаном и 30 в группе с треосульфаном) имели схожие показатели 5-летней выживаемости: общая выживаемость в 1-й и 2-й группах составила 79,3% и 66,1%, а безрецидивная выживаемость – 82,5% и 74,1%, соответственно. Частота хронической РТПХ – 57% в группе с треосульфаном и 50% в группе с бусульфаном. Кумулятивный риск развития экстенсивной хронической РТПХ составил 27,6% в 1-й группе и 43,3% во 2-й группе. При анализе других поздних осложнений обнаружено снижение частоты развития эндокринных нарушений в группе с треосульфаном – 27% против 43% в 1-й группе, при этом не зарегистрировано ни одного случая развития гипергонадотропного гипогонадизма (кумулятивный риск развития 32,8% в 1-й группе против 0% во 2-й, р = 0,012). Патология щитовидной железы в структуре эндокринных нарушений также преобладала в 1-й группе детей – 29% против 13%. Патология центральной нервной системы в группе с треосульфаном носила в большей степени функциональный характер в отличие от преобладания органических нарушений в 1-й группе: не зарегистрировано ни одного случая энцефалопатии, вторичной эпилепсии. Также отмечались качественные различия в развитии кардиоваскулярной патологии – 16% в 1-й группе с преобладанием вторичной кардиомиопатии против 10% во 2-й группе. В обеих группах зарегистрировано по одному случаю вторичных неоплазий на поздних сроках после ТГСК. Cреди детей с незлокачественными заболеваниями (первичными иммунодефицитами) 5 получили бусульфан-содержащее кондиционирование, а 8 – треосульфан-содержащее. Общая 5-летняя выживаемость составила 87,5% в 1-й группе против 60% во 2-й. Существенных различий в частоте поздних осложнений алло-ТГСК не выявлено.
Заключение
Треосульфан-содержащее миелоаблативное кондиционирование позволяет снизить риск развития поздних осложнений со стороны эндокринной системы (особенно гипогонадизма), центральной нервной системы и кардиоваскулярных нарушений после алло-ТГСК у детей по сравнению с классическими бусульфан-содержащими режимами.
Ключевые слова
Алло-ТГСК, кондиционирование, треосульфан, поздние осложнения, дети.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20669
[VALUE] => Array
(
[TEXT] => Татьяна С. Щеголева, Марина А. Городнова, Валентина М. Кравцова, Владислав С. Сергеев, Елена В. Бабенко, Мария А. Эстрина, Полина С. Куга, Ирина И. Кулагина, Марина О. Попова, Татьяна В. Андреева, Асмик Г. Геворгян, Людмила С. Зубаровская, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Татьяна С. Щеголева, Марина А. Городнова, Валентина М. Кравцова, Владислав С. Сергеев, Елена В. Бабенко, Мария А. Эстрина, Полина С. Куга, Ирина И. Кулагина, Марина О. Попова, Татьяна В. Андреева, Асмик Г. Геворгян, Людмила С. Зубаровская, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20670
[VALUE] => Array
(
[TEXT] => Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20671
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Рутинным методом определения количества гемопоэтических стволовых клеток (ГСК) является проточная цитофлуориметрия с использованием меченых антител и витального красителя. К серьезным недостаткам данного метода можно отнести сложность стандартизации, отсутствие автоматизации, большие трудозатраты квалифицированного персонала, а также относительная дороговизна расходных материалов. В связи с высокой потребностью частого определения ГСК в периферической крови (ПК) и продуктах афереза существует необходимость разработки стандартизированных, автоматизированных методов. Sysmex-XN является использующимся в клинической практике гематологическом анализатором, имеющим все необходимые возможности для стандартизации проводящихся на нем исследований. В настоящее время разработана возможность определения количества ГСК на Sysmex-XN в канале WPC в режиме XN-HPC. Определение ГСК данным методом является исследовательским, но в перспективе может быть внедрено в клиническую практику в дополнение к рутинному методу в случае получения сопоставимых данных. Целью работы было сравнение данных по количественному определению ГСК в ПК и продукте афереза после мобилизации с помощью Г-КСФ двумя методами, а также трудовых и финансовых затрат.
</p>
<h2 style="text-align: justify;">Методы</h2>
<p style="text-align: justify;">
В качестве стандарта использовался метод подсчета ГСК: подсчет лейкоцитов в камере Горяева и проточная цитофлуориметрия с маркерами CD45/CD34/7AAD (BD; San Jose, USA) на аппарате BD FacsCalibur по протоколу ISHAGE. Исследуемый метод – автоматизированный метод подсчета ГСК, доступный на анализаторах Sysmex XN (XN-HPC) в канале WPC, основанный на измерении размера, структуры и интенсивности флуоресценции клеток. Пробы ПК и продукта афереза забирались для исследований из одних образцов. Заготовка ГСК проводилась на сепараторе COBE Spectra.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Представляется клинический случай пациентки Г., 2 г. 4 мес., рост 85,5 см., вес 15 кг, с диагнозом медуллобластома. Для лечения рецидива планируется высокодозная химиотерапии с аутотрансплантацией ГСК. Заготовка ГСК ПК проводилась после стимуляции Г-КСФ в дозе 10 мкг/кг однократно в течение 5-ти дней. На пятый день выполнен аферез. Объем перфузии составил 2900.0 мл, получено 230.0 мл концентрата. Результаты исследований представлены в таблицах: (1) количественное определение ГСК в ПК, (2) оценка количества ГСК в аферезном концентрате, (3) оценка финансовых и трудозатрат (без учета амортизации оборудования и коммунальных затрат).
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
Представленный клинический случай демонстрирует, что результаты количественного определения ГСК на анализаторе Sysmex-XN сопоставимы с результатами рутинного метода, в то время как трудовые и финансовые затраты по меньшей мере в 3 раза ниже. Быстрота получения результата и относительно низкая стоимость позволяет предложить использование количественного определения ГСК на анализаторе Sysmex-XN в качестве дополнительного скринингового метода, результаты которого в дальнейшем будут валидироваться стандартным методом исследования. Внедрение нового скринингового метода определения ГСК приведет к оптимизации алгоритмов проведения афереза и, как следствие, получению трансплантатов ГСК лучшего качества. Тем не менее, для использования нового метода в клинической практике необходимо проведение сравнительных исследований по количественному определению ГСК в ПК и продуктах афереза от широкой когорты доноров/пациентов.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Гемопоэтические стволовые клетки, заготовка ГСК, периферическая кровь, продукт афереза, проточная цитометрия, Sysmex-XN, скрининг количества ГСК.
</p>
<h2 style="text-align: justify;">
Таблица 1. Результаты исследований ПК<br>
</h2>
<img width="781" alt="46_таблица 1.png" src="/upload/medialibrary/3db/46_tablitsa-1.png" height="179" title="46_таблица 1.png">
<h2>Таблица 2. Результаты исследований аферезного концентрата</h2>
<img width="783" alt="46_таблица 2.png" src="/upload/medialibrary/176/46_tablitsa-2.png" height="89" title="46_таблица 2.png">
<h2>Таблица 3. Оценка финансовых и трудозатрат</h2>
<img width="783" alt="46_таблица 3.png" src="/upload/medialibrary/7f9/46_tablitsa-3.png" height="289" title="46_таблица 3.png"><br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Рутинным методом определения количества гемопоэтических стволовых клеток (ГСК) является проточная цитофлуориметрия с использованием меченых антител и витального красителя. К серьезным недостаткам данного метода можно отнести сложность стандартизации, отсутствие автоматизации, большие трудозатраты квалифицированного персонала, а также относительная дороговизна расходных материалов. В связи с высокой потребностью частого определения ГСК в периферической крови (ПК) и продуктах афереза существует необходимость разработки стандартизированных, автоматизированных методов. Sysmex-XN является использующимся в клинической практике гематологическом анализатором, имеющим все необходимые возможности для стандартизации проводящихся на нем исследований. В настоящее время разработана возможность определения количества ГСК на Sysmex-XN в канале WPC в режиме XN-HPC. Определение ГСК данным методом является исследовательским, но в перспективе может быть внедрено в клиническую практику в дополнение к рутинному методу в случае получения сопоставимых данных. Целью работы было сравнение данных по количественному определению ГСК в ПК и продукте афереза после мобилизации с помощью Г-КСФ двумя методами, а также трудовых и финансовых затрат.
Методы
В качестве стандарта использовался метод подсчета ГСК: подсчет лейкоцитов в камере Горяева и проточная цитофлуориметрия с маркерами CD45/CD34/7AAD (BD; San Jose, USA) на аппарате BD FacsCalibur по протоколу ISHAGE. Исследуемый метод – автоматизированный метод подсчета ГСК, доступный на анализаторах Sysmex XN (XN-HPC) в канале WPC, основанный на измерении размера, структуры и интенсивности флуоресценции клеток. Пробы ПК и продукта афереза забирались для исследований из одних образцов. Заготовка ГСК проводилась на сепараторе COBE Spectra.
Результаты
Представляется клинический случай пациентки Г., 2 г. 4 мес., рост 85,5 см., вес 15 кг, с диагнозом медуллобластома. Для лечения рецидива планируется высокодозная химиотерапии с аутотрансплантацией ГСК. Заготовка ГСК ПК проводилась после стимуляции Г-КСФ в дозе 10 мкг/кг однократно в течение 5-ти дней. На пятый день выполнен аферез. Объем перфузии составил 2900.0 мл, получено 230.0 мл концентрата. Результаты исследований представлены в таблицах: (1) количественное определение ГСК в ПК, (2) оценка количества ГСК в аферезном концентрате, (3) оценка финансовых и трудозатрат (без учета амортизации оборудования и коммунальных затрат).
Выводы
Представленный клинический случай демонстрирует, что результаты количественного определения ГСК на анализаторе Sysmex-XN сопоставимы с результатами рутинного метода, в то время как трудовые и финансовые затраты по меньшей мере в 3 раза ниже. Быстрота получения результата и относительно низкая стоимость позволяет предложить использование количественного определения ГСК на анализаторе Sysmex-XN в качестве дополнительного скринингового метода, результаты которого в дальнейшем будут валидироваться стандартным методом исследования. Внедрение нового скринингового метода определения ГСК приведет к оптимизации алгоритмов проведения афереза и, как следствие, получению трансплантатов ГСК лучшего качества. Тем не менее, для использования нового метода в клинической практике необходимо проведение сравнительных исследований по количественному определению ГСК в ПК и продуктах афереза от широкой когорты доноров/пациентов.
Ключевые слова
Гемопоэтические стволовые клетки, заготовка ГСК, периферическая кровь, продукт афереза, проточная цитометрия, Sysmex-XN, скрининг количества ГСК.
Таблица 1. Результаты исследований ПК

Таблица 2. Результаты исследований аферезного концентрата

Таблица 3. Оценка финансовых и трудозатрат

[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20672
[VALUE] => Array
(
[TEXT] => Tatiana S. Shchegoleva, Marina A. Gorodnova, Valentina M. Kravtsova, Vladislav S. Sergeev, Elena V. Babenko, Maria A. Estrina, Polina S. Kuga, Irina I. Kulagina, Marina O. Popova, Tatyana V. Andreeva, Asmik G. Gevorgyan, Ludmila S. Zubarovskaya, Boris V. Afanasyev
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Tatiana S. Shchegoleva, Marina A. Gorodnova, Valentina M. Kravtsova, Vladislav S. Sergeev, Elena V. Babenko, Maria A. Estrina, Polina S. Kuga, Irina I. Kulagina, Marina O. Popova, Tatyana V. Andreeva, Asmik G. Gevorgyan, Ludmila S. Zubarovskaya, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20673
[VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Research Institute of Children’s Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St.Peterburg, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Research Institute of Children’s Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St.Peterburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20674
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Background</h2>
<p style="text-align: justify;">
The routine method for evaluation of hematopoietic stem cells (HSC) is flow cytometry using labeled antibodies and vital dye. Serious disadvantages of this method include the difficulty of standardization, the lack of automation, the high labor costs of qualified personnel, and the relative high cost of consumables. Frequent evaluation of HSC in peripheral blood (PB) and apheresis products are a high clinical need test. The development of standardized, automated methods of HSC evaluation is an actual challenge. Sysmex-XN is a clinical hematological analyzer which has already had all the necessary facilities for standardizing the evaluations conducted on it. Currently, the ability to evaluate the number of HSCs on Sysmex-XN in a WPC channel in the XNHPC mode has been developed. The evaluation of HSC by<br>
this method is at research stage, but in the future it can be introduced into clinical practice in addition to the routine method in the case of obtaining comparable data. Aim of this study was to compare the data of the quantitative evaluation of HSC in peripheral blood and apheresis product after mobilization with G-CSF by two methods, as well as labor and financial costs.
</p>
<h2 style="text-align: justify;">Materials and methods</h2>
<p style="text-align: justify;">
As a standard, the HSC counting method was used: counting of leukocytes in the Goryaev’ chamber and flow cytometry with markers CD45/CD34/7AAD (BD, San Jose, USA) using BD FacsCalibur and the ISHAGE protocol. A new method is an automated method for calculating HSC, available on Sysmex XN analyzers (XN-HPC) in the WPC channel, based on measuring the size, structure, and fluorescence intensity of cells. Samples of PB and apheresis product were taken for research from same specimens. The HSCs were collected on a COBE Spectra separator.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
We report a clinical case of the patient G., 2 years 4 months, height 85.5 cm, weight 15 kg, with the diagnosis of medulloblastoma. The treatment of relapse has to include highdose chemotherapy with autologous hematopoietic stem cell transplantation. Harvesting HSCs of PB was performed after stimulation of G-CSF in a dose of 10 μg/kg once for 5 days. Apheresis was performed on the fifth day of mobilization. The volume of perfusion was 2900.0 ml, 230.0 ml of concentrate was obtained. The comparative results of the studies are presented in the tables: (1) the quantitative evaluation of HSC in the PB, (2) the estimation of the amount of HSC in the apheresis concentrate, (3) the financial and labor costs evaluation (without depreciation of equipment and utility costs).
</p>
<h2 style="text-align: justify;">Conclusions</h2>
<p style="text-align: justify;">
The presented clinical case demonstrates that the results of quantitative evaluation of HSC on the Sysmex-XN analyzer are comparable with the results of the routine method, while labor and financial costs are at least 3 times lower. The speed of obtaining the result and the relatively low cost make it possible to propose the use of quantitative evaluation of HSC on the Sysmex-XN analyzer as an additional screening method, the results of which will subsequently be validated by the standard method of investigation. The introduction of a new screening method for evaluation of HSCs will lead to optimization of the peripheral blood HSC harvesting protocols and, as a consequence, to obtaining HSC transplants of better quality. Nevertheless, to use the new method in clinical practice, it is necessary to conduct comparative studies on the evaluation of HSC in the PB and apheresis products from a broad cohort of donors/patients.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Hematopoietic stem cells, peripheral blood, HSC harvesting, apheresis concentrate, flow cytometry, Sysmex-XN, quantitative HSC screening.
</p>
<h2 style="text-align: justify;">Table 1. Evaluation of HSCs in peripheral blood</h2>
<p style="text-align: justify;">
<img width="783" alt="46_table 1.png" src="/upload/medialibrary/984/46_table-1.png" height="203" title="46_table 1.png">
</p>
<h2 style="text-align: justify;">Table 2. The evaluation of HSCs in apheresis concentrate</h2>
<p style="text-align: justify;">
<img width="783" alt="46_table 2.png" src="/upload/medialibrary/f12/46_table-2.png" height="105" title="46_table 2.png">
</p>
<h2 style="text-align: justify;">Table 3. Evaluation of time expenses and financial costs</h2>
<p style="text-align: justify;">
<img width="783" alt="46_table 3.png" src="/upload/medialibrary/ef6/46_table-3.png" height="321" title="46_table 3.png">
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Background
The routine method for evaluation of hematopoietic stem cells (HSC) is flow cytometry using labeled antibodies and vital dye. Serious disadvantages of this method include the difficulty of standardization, the lack of automation, the high labor costs of qualified personnel, and the relative high cost of consumables. Frequent evaluation of HSC in peripheral blood (PB) and apheresis products are a high clinical need test. The development of standardized, automated methods of HSC evaluation is an actual challenge. Sysmex-XN is a clinical hematological analyzer which has already had all the necessary facilities for standardizing the evaluations conducted on it. Currently, the ability to evaluate the number of HSCs on Sysmex-XN in a WPC channel in the XNHPC mode has been developed. The evaluation of HSC by
this method is at research stage, but in the future it can be introduced into clinical practice in addition to the routine method in the case of obtaining comparable data. Aim of this study was to compare the data of the quantitative evaluation of HSC in peripheral blood and apheresis product after mobilization with G-CSF by two methods, as well as labor and financial costs.
Materials and methods
As a standard, the HSC counting method was used: counting of leukocytes in the Goryaev’ chamber and flow cytometry with markers CD45/CD34/7AAD (BD, San Jose, USA) using BD FacsCalibur and the ISHAGE protocol. A new method is an automated method for calculating HSC, available on Sysmex XN analyzers (XN-HPC) in the WPC channel, based on measuring the size, structure, and fluorescence intensity of cells. Samples of PB and apheresis product were taken for research from same specimens. The HSCs were collected on a COBE Spectra separator.
Results
We report a clinical case of the patient G., 2 years 4 months, height 85.5 cm, weight 15 kg, with the diagnosis of medulloblastoma. The treatment of relapse has to include highdose chemotherapy with autologous hematopoietic stem cell transplantation. Harvesting HSCs of PB was performed after stimulation of G-CSF in a dose of 10 μg/kg once for 5 days. Apheresis was performed on the fifth day of mobilization. The volume of perfusion was 2900.0 ml, 230.0 ml of concentrate was obtained. The comparative results of the studies are presented in the tables: (1) the quantitative evaluation of HSC in the PB, (2) the estimation of the amount of HSC in the apheresis concentrate, (3) the financial and labor costs evaluation (without depreciation of equipment and utility costs).
Conclusions
The presented clinical case demonstrates that the results of quantitative evaluation of HSC on the Sysmex-XN analyzer are comparable with the results of the routine method, while labor and financial costs are at least 3 times lower. The speed of obtaining the result and the relatively low cost make it possible to propose the use of quantitative evaluation of HSC on the Sysmex-XN analyzer as an additional screening method, the results of which will subsequently be validated by the standard method of investigation. The introduction of a new screening method for evaluation of HSCs will lead to optimization of the peripheral blood HSC harvesting protocols and, as a consequence, to obtaining HSC transplants of better quality. Nevertheless, to use the new method in clinical practice, it is necessary to conduct comparative studies on the evaluation of HSC in the PB and apheresis products from a broad cohort of donors/patients.
Keywords
Hematopoietic stem cells, peripheral blood, HSC harvesting, apheresis concentrate, flow cytometry, Sysmex-XN, quantitative HSC screening.
Table 1. Evaluation of HSCs in peripheral blood

Table 2. The evaluation of HSCs in apheresis concentrate

Table 3. Evaluation of time expenses and financial costs

[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20675
[VALUE] => Evaluation of hematopoietic stem cells in peripheral blood and apheresis product on the hematological analyzer Sysmex XN (XN-HPC): a clinical case
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Evaluation of hematopoietic stem cells in peripheral blood and apheresis product on the hematological analyzer Sysmex XN (XN-HPC): a clinical case
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20821
[VALUE] => 1459
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1459
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20822
[VALUE] => 1460
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1460
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Татьяна С. Щеголева, Марина А. Городнова, Валентина М. Кравцова, Владислав С. Сергеев, Елена В. Бабенко, Мария А. Эстрина, Полина С. Куга, Ирина И. Кулагина, Марина О. Попова, Татьяна В. Андреева, Асмик Г. Геворгян, Людмила С. Зубаровская, Борис В. Афанасьев
Введение
Рутинным методом определения количества гемопоэтических стволовых клеток (ГСК) является проточная цитофлуориметрия с использованием меченых антител и витального красителя. К серьезным недостаткам данного метода можно отнести сложность стандартизации, отсутствие автоматизации, большие трудозатраты квалифицированного персонала, а также относительная дороговизна расходных материалов. В связи с высокой потребностью частого определения ГСК в периферической крови (ПК) и продуктах афереза существует необходимость разработки стандартизированных, автоматизированных методов. Sysmex-XN является использующимся в клинической практике гематологическом анализатором, имеющим все необходимые возможности для стандартизации проводящихся на нем исследований. В настоящее время разработана возможность определения количества ГСК на Sysmex-XN в канале WPC в режиме XN-HPC. Определение ГСК данным методом является исследовательским, но в перспективе может быть внедрено в клиническую практику в дополнение к рутинному методу в случае получения сопоставимых данных. Целью работы было сравнение данных по количественному определению ГСК в ПК и продукте афереза после мобилизации с помощью Г-КСФ двумя методами, а также трудовых и финансовых затрат.
Методы
В качестве стандарта использовался метод подсчета ГСК: подсчет лейкоцитов в камере Горяева и проточная цитофлуориметрия с маркерами CD45/CD34/7AAD (BD; San Jose, USA) на аппарате BD FacsCalibur по протоколу ISHAGE. Исследуемый метод – автоматизированный метод подсчета ГСК, доступный на анализаторах Sysmex XN (XN-HPC) в канале WPC, основанный на измерении размера, структуры и интенсивности флуоресценции клеток. Пробы ПК и продукта афереза забирались для исследований из одних образцов. Заготовка ГСК проводилась на сепараторе COBE Spectra.
Результаты
Представляется клинический случай пациентки Г., 2 г. 4 мес., рост 85,5 см., вес 15 кг, с диагнозом медуллобластома. Для лечения рецидива планируется высокодозная химиотерапии с аутотрансплантацией ГСК. Заготовка ГСК ПК проводилась после стимуляции Г-КСФ в дозе 10 мкг/кг однократно в течение 5-ти дней. На пятый день выполнен аферез. Объем перфузии составил 2900.0 мл, получено 230.0 мл концентрата. Результаты исследований представлены в таблицах: (1) количественное определение ГСК в ПК, (2) оценка количества ГСК в аферезном концентрате, (3) оценка финансовых и трудозатрат (без учета амортизации оборудования и коммунальных затрат).
Выводы
Представленный клинический случай демонстрирует, что результаты количественного определения ГСК на анализаторе Sysmex-XN сопоставимы с результатами рутинного метода, в то время как трудовые и финансовые затраты по меньшей мере в 3 раза ниже. Быстрота получения результата и относительно низкая стоимость позволяет предложить использование количественного определения ГСК на анализаторе Sysmex-XN в качестве дополнительного скринингового метода, результаты которого в дальнейшем будут валидироваться стандартным методом исследования. Внедрение нового скринингового метода определения ГСК приведет к оптимизации алгоритмов проведения афереза и, как следствие, получению трансплантатов ГСК лучшего качества. Тем не менее, для использования нового метода в клинической практике необходимо проведение сравнительных исследований по количественному определению ГСК в ПК и продуктах афереза от широкой когорты доноров/пациентов.
Ключевые слова
Гемопоэтические стволовые клетки, заготовка ГСК, периферическая кровь, продукт афереза, проточная цитометрия, Sysmex-XN, скрининг количества ГСК.
Таблица 1. Результаты исследований ПК

Таблица 2. Результаты исследований аферезного концентрата

Таблица 3. Оценка финансовых и трудозатрат

Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20655
[VALUE] => Array
(
[TEXT] => Эльвира Р. Султанова, Александра Л. Лаберко, Анна А. Богоявленская, Сергей Л. Благов, Лариса Н. Шелихова, Дмитрий Н. Балашов
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Эльвира Р. Султанова, Александра Л. Лаберко, Анна А. Богоявленская, Сергей Л. Благов, Лариса Н. Шелихова, Дмитрий Н. Балашов
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20656
[VALUE] => Array
(
[TEXT] => ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России, Москва, Россия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России, Москва, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20657
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Цель работы: демонстрация клинического случая развития Эпштейн-Барр вирус (ЭБВ)-ассоциированного лимфопролиферативного заболевания (ЛПЗ) у пациента с тяжелой комбинированной иммунной недостаточностью (ТКИН) до трансплантации гемопоэтических стволовых клеток (ТГСК).
</p>
<h2 style="text-align: justify;">Методы</h2>
<p style="text-align: justify;">
Пациент, поступил в клинику в возрасте трех месяцев; было проведено обследование, детальный анализ лабораторных и клинических данных, установлен диагноз; терапия была направлена не только на основное заболевание, но и диагностированные осложнения.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Проведенные исследования подтвердили диагноз ТКИН и выявили (КТ, биопсия) ЭБВ-ассоциированное ЛПЗ с поражением средостения. Терапия до ТГСК включала дексаметазон для снижения опухолевого объема и ритуксимаб. На КТ через 2 недели отмечалась положительная динамика. Учитывая основное заболевание далее была проведена трансплантация периферических стволовых кроветворных клеток. Также, в качестве экспериментальной противовирусной терапии, основанной на инфузии ЭБВ-специфических клеток после ТГСК у пациентов с посттрансплантационным ЛПЗ (ПТЛПЗ), на +5 сутки выполнена инфузия CD45-RA деплетированных лимфоцитов. Полное нивелирование очагов в легких (КТ) – на +180 день после ТГСК, что совпало с иммунореконституцией.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Данный случай демонстрирует редкое развитие ЭБВ-ассоциированного ЛПЗ у пациента с ТКИН на первых месяцах жизни до проведения ТГСК. ЛПЗ у пациентов с ТКИН и ПТЛПЗ имеют схожий механизм развития – потеря Т-клеточного контроля. Терапевтические опции в обоих случаях включают применение ритуксимаба и, основанную на передаче активного клеточного иммунитета от донора к реципиенту, клеточную терапию. ЛПЗ регистрируется у ТКИН реже, чем у других первичных иммунодефицитов ввиду их высокой смертности или проведения ТГСК в первые месяцы жизни, что подводит нас к важности правильного диагностического и дифференциально-диагностического поиска у пациента с комбинированным иммунодефицитом, готовящегося к ТГСК, независимо от возраста и комплекса иных клинических проблем.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Лимфопролиферативное заболевание, тяжелая комбинированная иммунная недостаточность, трансплантация гемопоэтических стволовых клеток, вирус Эпштейна-Барр, инфузия донорских лимфоцитов, иммунная реконституция.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Цель работы: демонстрация клинического случая развития Эпштейн-Барр вирус (ЭБВ)-ассоциированного лимфопролиферативного заболевания (ЛПЗ) у пациента с тяжелой комбинированной иммунной недостаточностью (ТКИН) до трансплантации гемопоэтических стволовых клеток (ТГСК).
Методы
Пациент, поступил в клинику в возрасте трех месяцев; было проведено обследование, детальный анализ лабораторных и клинических данных, установлен диагноз; терапия была направлена не только на основное заболевание, но и диагностированные осложнения.
Результаты
Проведенные исследования подтвердили диагноз ТКИН и выявили (КТ, биопсия) ЭБВ-ассоциированное ЛПЗ с поражением средостения. Терапия до ТГСК включала дексаметазон для снижения опухолевого объема и ритуксимаб. На КТ через 2 недели отмечалась положительная динамика. Учитывая основное заболевание далее была проведена трансплантация периферических стволовых кроветворных клеток. Также, в качестве экспериментальной противовирусной терапии, основанной на инфузии ЭБВ-специфических клеток после ТГСК у пациентов с посттрансплантационным ЛПЗ (ПТЛПЗ), на +5 сутки выполнена инфузия CD45-RA деплетированных лимфоцитов. Полное нивелирование очагов в легких (КТ) – на +180 день после ТГСК, что совпало с иммунореконституцией.
Заключение
Данный случай демонстрирует редкое развитие ЭБВ-ассоциированного ЛПЗ у пациента с ТКИН на первых месяцах жизни до проведения ТГСК. ЛПЗ у пациентов с ТКИН и ПТЛПЗ имеют схожий механизм развития – потеря Т-клеточного контроля. Терапевтические опции в обоих случаях включают применение ритуксимаба и, основанную на передаче активного клеточного иммунитета от донора к реципиенту, клеточную терапию. ЛПЗ регистрируется у ТКИН реже, чем у других первичных иммунодефицитов ввиду их высокой смертности или проведения ТГСК в первые месяцы жизни, что подводит нас к важности правильного диагностического и дифференциально-диагностического поиска у пациента с комбинированным иммунодефицитом, готовящегося к ТГСК, независимо от возраста и комплекса иных клинических проблем.
Ключевые слова
Лимфопролиферативное заболевание, тяжелая комбинированная иммунная недостаточность, трансплантация гемопоэтических стволовых клеток, вирус Эпштейна-Барр, инфузия донорских лимфоцитов, иммунная реконституция.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20658
[VALUE] => Array
(
[TEXT] => Elvira R. Sultanova, Alexandra L. Laberko, Anna A. Bogoyavlenskaya, Sergey L. Blagov, Larisa N. Shelikhova, Dmitry N. Balashov
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Elvira R. Sultanova, Alexandra L. Laberko, Anna A. Bogoyavlenskaya, Sergey L. Blagov, Larisa N. Shelikhova, Dmitry N. Balashov
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20659
[VALUE] => Array
(
[TEXT] => Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Dmitry Rogachev National Research Center of Pediatric Hematology, Oncology and Immunology, Moscow, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20660
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Objective of this work was to demonstrate a case report of Epstein-Barr virus (EBV)-associated lymphoproliferative disease (LPD) in a patient with severe combined immune deficiency (SCID) before hematopoietic stem cell transplantation (HSCT).
</p>
<h2 style="text-align: justify;">Methods</h2>
<p style="text-align: justify;">
The patient at the age of 3 months has been admitted to our hospital and was clinically examined. Detailed analysis of the data was carried out, and diagnosis made. Appropriate treatment targeted at underlying disease as well as the complications diagnosed.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
The diagnosis of SCID was confirmed at our clinic. CT scan and lung biopsy showed EBV-associated LPD of the lung. Treatment before HSCT included dexamethasone for cytoreduction, and rituximab administration. CT scan 2 weeks after starting the therapy showed partial reduction in size of the tumor mass. Transplantation of peripheral blood stem cells was the next therapeutic step. Moreover, infusion of CD45-RA depleted lymphocytes was performed on D+5 post-transplant, as an experimental antiviral therapy based on infusion of EBV-specific cells after HSCT in patients with posttransplant LPD (PTLD). At the day +180, a CT scan showed complete resolution of the pulmonary mass, along with immune reconstitution achieved by this time.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
The present case demonstrates a rare opportunity for EBV-associated LPD (PTLD-like) developing in a SCID patient within first months of life before HSCT. LPD in SCID patient and PTLD may have similar mechanism, i.e., loss of T-cell control. Treatment options included rituximab, as well as cell therapy, i.e., transfer of active cellular immunity from donor to the recipient. Incidence of LPD in SCID patients is less common than LPD in patient with other primary immune deficiencies, due to high mortality rates among SCID patients before HSCT, or at following months. This case shows importance of correct diagnosis and differential diagnosis in a patient with combined immunodeficiency during his preparation for HSCT, despite of age and other multiple clinical problems.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Lymphoproliferative disease, severe combined immunodeficiency, hematopoietic stem cell transplantation, Epstein-Barr virus, donor lymphocytes infusion, immune reconstitution.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Objective of this work was to demonstrate a case report of Epstein-Barr virus (EBV)-associated lymphoproliferative disease (LPD) in a patient with severe combined immune deficiency (SCID) before hematopoietic stem cell transplantation (HSCT).
Methods
The patient at the age of 3 months has been admitted to our hospital and was clinically examined. Detailed analysis of the data was carried out, and diagnosis made. Appropriate treatment targeted at underlying disease as well as the complications diagnosed.
Results
The diagnosis of SCID was confirmed at our clinic. CT scan and lung biopsy showed EBV-associated LPD of the lung. Treatment before HSCT included dexamethasone for cytoreduction, and rituximab administration. CT scan 2 weeks after starting the therapy showed partial reduction in size of the tumor mass. Transplantation of peripheral blood stem cells was the next therapeutic step. Moreover, infusion of CD45-RA depleted lymphocytes was performed on D+5 post-transplant, as an experimental antiviral therapy based on infusion of EBV-specific cells after HSCT in patients with posttransplant LPD (PTLD). At the day +180, a CT scan showed complete resolution of the pulmonary mass, along with immune reconstitution achieved by this time.
Conclusion
The present case demonstrates a rare opportunity for EBV-associated LPD (PTLD-like) developing in a SCID patient within first months of life before HSCT. LPD in SCID patient and PTLD may have similar mechanism, i.e., loss of T-cell control. Treatment options included rituximab, as well as cell therapy, i.e., transfer of active cellular immunity from donor to the recipient. Incidence of LPD in SCID patients is less common than LPD in patient with other primary immune deficiencies, due to high mortality rates among SCID patients before HSCT, or at following months. This case shows importance of correct diagnosis and differential diagnosis in a patient with combined immunodeficiency during his preparation for HSCT, despite of age and other multiple clinical problems.
Keywords
Lymphoproliferative disease, severe combined immunodeficiency, hematopoietic stem cell transplantation, Epstein-Barr virus, donor lymphocytes infusion, immune reconstitution.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20661
[VALUE] => EBV-associated lymphoproliferative (PTLD-like) disease in SCID patient before HSCT
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => EBV-associated lymphoproliferative (PTLD-like) disease in SCID patient before HSCT
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20825
[VALUE] => 1465
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1465
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20826
[VALUE] => 1464
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1464
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Эльвира Р. Султанова, Александра Л. Лаберко, Анна А. Богоявленская, Сергей Л. Благов, Лариса Н. Шелихова, Дмитрий Н. Балашов
Введение
Цель работы: демонстрация клинического случая развития Эпштейн-Барр вирус (ЭБВ)-ассоциированного лимфопролиферативного заболевания (ЛПЗ) у пациента с тяжелой комбинированной иммунной недостаточностью (ТКИН) до трансплантации гемопоэтических стволовых клеток (ТГСК).
Методы
Пациент, поступил в клинику в возрасте трех месяцев; было проведено обследование, детальный анализ лабораторных и клинических данных, установлен диагноз; терапия была направлена не только на основное заболевание, но и диагностированные осложнения.
Результаты
Проведенные исследования подтвердили диагноз ТКИН и выявили (КТ, биопсия) ЭБВ-ассоциированное ЛПЗ с поражением средостения. Терапия до ТГСК включала дексаметазон для снижения опухолевого объема и ритуксимаб. На КТ через 2 недели отмечалась положительная динамика. Учитывая основное заболевание далее была проведена трансплантация периферических стволовых кроветворных клеток. Также, в качестве экспериментальной противовирусной терапии, основанной на инфузии ЭБВ-специфических клеток после ТГСК у пациентов с посттрансплантационным ЛПЗ (ПТЛПЗ), на +5 сутки выполнена инфузия CD45-RA деплетированных лимфоцитов. Полное нивелирование очагов в легких (КТ) – на +180 день после ТГСК, что совпало с иммунореконституцией.
Заключение
Данный случай демонстрирует редкое развитие ЭБВ-ассоциированного ЛПЗ у пациента с ТКИН на первых месяцах жизни до проведения ТГСК. ЛПЗ у пациентов с ТКИН и ПТЛПЗ имеют схожий механизм развития – потеря Т-клеточного контроля. Терапевтические опции в обоих случаях включают применение ритуксимаба и, основанную на передаче активного клеточного иммунитета от донора к реципиенту, клеточную терапию. ЛПЗ регистрируется у ТКИН реже, чем у других первичных иммунодефицитов ввиду их высокой смертности или проведения ТГСК в первые месяцы жизни, что подводит нас к важности правильного диагностического и дифференциально-диагностического поиска у пациента с комбинированным иммунодефицитом, готовящегося к ТГСК, независимо от возраста и комплекса иных клинических проблем.
Ключевые слова
Лимфопролиферативное заболевание, тяжелая комбинированная иммунная недостаточность, трансплантация гемопоэтических стволовых клеток, вирус Эпштейна-Барр, инфузия донорских лимфоцитов, иммунная реконституция.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20648
[VALUE] => Array
(
[TEXT] => Юрий А. Серов <sup>1</sup>,<sup>2</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Юрий А. Серов 1,2
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20649
[VALUE] => Array
(
[TEXT] => <sup>1</sup> Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
<sup>2</sup> Лаборатория HLA, Медицинский факультет, Университет Индианы, Индианаполис, Индиана, США
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
2 Лаборатория HLA, Медицинский факультет, Университет Индианы, Индианаполис, Индиана, США
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20650
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">
Была описана идентификация нового аллеля HLA-B* 44:02:17, который был обнаружен в семье афроамериканских индивидуумов во время типирования HLA пациента и доноров для трансплантации костного мозга. Новый аллель HLA-B*44:02:17 отличается от HLA-B* 44: 02:01:01 одним синонимным нуклеотидным изменением в положении 606 bp, кодоном 178, экзон 3 (ACG> ACC, Thr – Silent change). Кроме того, расширенные последовательности HLA-B*44:02:17, за пределами экзонов 2 и 3, были описаны путем клонирования и полноразмерного SBT 3,5 kb фрагмента, простирающегося от 5’-нетранслируемой области до 3’-нетранслируемой области. Название B*44:02:17 было официально присвоено Комитетом номенклатуры ВОЗ. Нуклеотидная последовательность доступна в базе данных IMGT/HLA с номером присоединения HWS100122239.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
HLA-B*44:02, HLA-B*44:02:17, полногеномное секвенирование, ген HLA-B.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Была описана идентификация нового аллеля HLA-B* 44:02:17, который был обнаружен в семье афроамериканских индивидуумов во время типирования HLA пациента и доноров для трансплантации костного мозга. Новый аллель HLA-B*44:02:17 отличается от HLA-B* 44: 02:01:01 одним синонимным нуклеотидным изменением в положении 606 bp, кодоном 178, экзон 3 (ACG> ACC, Thr – Silent change). Кроме того, расширенные последовательности HLA-B*44:02:17, за пределами экзонов 2 и 3, были описаны путем клонирования и полноразмерного SBT 3,5 kb фрагмента, простирающегося от 5’-нетранслируемой области до 3’-нетранслируемой области. Название B*44:02:17 было официально присвоено Комитетом номенклатуры ВОЗ. Нуклеотидная последовательность доступна в базе данных IMGT/HLA с номером присоединения HWS100122239.
Ключевые слова
HLA-B*44:02, HLA-B*44:02:17, полногеномное секвенирование, ген HLA-B.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20651
[VALUE] => Array
(
[TEXT] => Yury A. Serov <sup>1</sup>,<sup>2</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Yury A. Serov 1,2
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20652
[VALUE] => Array
(
[TEXT] => <sup>1</sup> Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, The First I. P. Pavlov State Medical University, St. Petersburg, Russia.
<sup>2</sup> HLA Laboratory, Department of Medicine, Indiana University, Indianapolis, Indiana, USA
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, The First I. P. Pavlov State Medical University, St. Petersburg, Russia.
2 HLA Laboratory, Department of Medicine, Indiana University, Indianapolis, Indiana, USA
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20653
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">
The identification of the new allele HLA-B*44:02:17 was described, which was found in a family of African American individuals during the HLA typing of a patient for a bone marrow transplant. The new HLA-B*44:02:17 allele differs from HLA-B*44:02:01:01 by one synonymous nucleotide change at position 606 b.p., codon 178, Exon 3 (ACG > ACC, Thr – Silent change). In addition, extended sequences of HLA-B*44:02:17, beyond exons 2 and 3 was reported by cloning and full-length SBT 3.5 kb fragment extending from the 5’ untranslated region to the 3’ untranslated region. The name B*44:02:17 has been officially assigned by the WHO Nomenclature Committee. The nucleotide sequence is available in IMGT/HLA Database with the accession number HWS100122239.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
HLA-B*44:02, HLA-B*44:02:17, full-length sequence-based typing, HLA-B gene.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
The identification of the new allele HLA-B*44:02:17 was described, which was found in a family of African American individuals during the HLA typing of a patient for a bone marrow transplant. The new HLA-B*44:02:17 allele differs from HLA-B*44:02:01:01 by one synonymous nucleotide change at position 606 b.p., codon 178, Exon 3 (ACG > ACC, Thr – Silent change). In addition, extended sequences of HLA-B*44:02:17, beyond exons 2 and 3 was reported by cloning and full-length SBT 3.5 kb fragment extending from the 5’ untranslated region to the 3’ untranslated region. The name B*44:02:17 has been officially assigned by the WHO Nomenclature Committee. The nucleotide sequence is available in IMGT/HLA Database with the accession number HWS100122239.
Keywords
HLA-B*44:02, HLA-B*44:02:17, full-length sequence-based typing, HLA-B gene.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20654
[VALUE] => The identification of a new HLA-B*44:02:17 allele of the three members of an African-American family
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => The identification of a new HLA-B*44:02:17 allele of the three members of an African-American family
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20815
[VALUE] => 1453
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1453
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20816
[VALUE] => 1454
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1454
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Юрий А. Серов 1,2
Была описана идентификация нового аллеля HLA-B* 44:02:17, который был обнаружен в семье афроамериканских индивидуумов во время типирования HLA пациента и доноров для трансплантации костного мозга. Новый аллель HLA-B*44:02:17 отличается от HLA-B* 44: 02:01:01 одним синонимным нуклеотидным изменением в положении 606 bp, кодоном 178, экзон 3 (ACG> ACC, Thr – Silent change). Кроме того, расширенные последовательности HLA-B*44:02:17, за пределами экзонов 2 и 3, были описаны путем клонирования и полноразмерного SBT 3,5 kb фрагмента, простирающегося от 5’-нетранслируемой области до 3’-нетранслируемой области. Название B*44:02:17 было официально присвоено Комитетом номенклатуры ВОЗ. Нуклеотидная последовательность доступна в базе данных IMGT/HLA с номером присоединения HWS100122239.
Ключевые слова
HLA-B*44:02, HLA-B*44:02:17, полногеномное секвенирование, ген HLA-B.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20641
[VALUE] => Array
(
[TEXT] => Юрий А. Серов <sup>1</sup>,<sup>2</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Юрий А. Серов 1,2
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20642
[VALUE] => Array
(
[TEXT] => <sup>1</sup> Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский Университет им. акад. И. П. Павлова
<sup>2</sup> Лаборатория HLA, Медицинский факультет, Университет Индианы, Индианаполис, Индиана, США
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский Университет им. акад. И. П. Павлова
2 Лаборатория HLA, Медицинский факультет, Университет Индианы, Индианаполис, Индиана, США
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20643
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">
В процессе HLA типирования пациента для предстоящей пересадки костного мозга и его потенциальных доноров, мы идентифицировали новую аллель HLA DQB1*03:31, в образце ДНК мужчины, потомка американских индейцев. Эта аллель присутствует в гаплотипе HLA A*02:01, B*57:01, C *06:02, DRB1*07:01, DRB4*01:01, DQA1 *02:01, DQB1*03:31. Его другим гаплотипом являются HLA A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3 * 02:02, DQA1*01:01, DQB1*05:03, что так же было обнаружено у донора. Этот новый аллель идентичен HLA DQB1*03:03:02:01-03:03:02:05 в экзоне 2, за исключением кодона 116 (позиция 346 п.н.), где нуклеотидное замещение (GTC> ATC) приводит к мутантной мутации – изменение аминокислоты – Валин на Изолейцин. Название новой аллели – HLA DQB1*03:31 было официально присвоено Комитетом номенклатуры ВОЗ. Это следует за согласованной политикой, которая подчиняется условиям, указанным в последнем отчете о номенклатуре, имена будут назначены новым последовательностям по мере их идентификации. Списки таких новых имен были опубликованы в отчете о номенклатуре ВОЗ. Номер доступа GenBank – HM998989.1. Остаток 116 находится в β1-спирали молекулы HLA класса II, которая является частью кармана F, участвующего в связывании пептидов. Новый аллель содержит изменение аминокислоты в сайте связывания белка HLA антигена, который может изменить его пространственные представляющие свойства.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
HLA DQB1, HLA DQB1*03:31, ген HLA, клонирование, секвенирование.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
В процессе HLA типирования пациента для предстоящей пересадки костного мозга и его потенциальных доноров, мы идентифицировали новую аллель HLA DQB1*03:31, в образце ДНК мужчины, потомка американских индейцев. Эта аллель присутствует в гаплотипе HLA A*02:01, B*57:01, C *06:02, DRB1*07:01, DRB4*01:01, DQA1 *02:01, DQB1*03:31. Его другим гаплотипом являются HLA A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3 * 02:02, DQA1*01:01, DQB1*05:03, что так же было обнаружено у донора. Этот новый аллель идентичен HLA DQB1*03:03:02:01-03:03:02:05 в экзоне 2, за исключением кодона 116 (позиция 346 п.н.), где нуклеотидное замещение (GTC> ATC) приводит к мутантной мутации – изменение аминокислоты – Валин на Изолейцин. Название новой аллели – HLA DQB1*03:31 было официально присвоено Комитетом номенклатуры ВОЗ. Это следует за согласованной политикой, которая подчиняется условиям, указанным в последнем отчете о номенклатуре, имена будут назначены новым последовательностям по мере их идентификации. Списки таких новых имен были опубликованы в отчете о номенклатуре ВОЗ. Номер доступа GenBank – HM998989.1. Остаток 116 находится в β1-спирали молекулы HLA класса II, которая является частью кармана F, участвующего в связывании пептидов. Новый аллель содержит изменение аминокислоты в сайте связывания белка HLA антигена, который может изменить его пространственные представляющие свойства.
Ключевые слова
HLA DQB1, HLA DQB1*03:31, ген HLA, клонирование, секвенирование.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20644
[VALUE] => Array
(
[TEXT] => Yury A. Serov <sup>1</sup>,<sup>2</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Yury A. Serov 1,2
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20645
[VALUE] => Array
(
[TEXT] => <sup>1</sup> Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, First I. P. Pavlov State Medical University of St. Petersburg, Russia
<sup>2</sup> Histocompatibility Laboratory, Department of Medicine, Indiana University, Indianapolis, Indiana 46202, USA
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, First I. P. Pavlov State Medical University of St. Petersburg, Russia
2 Histocompatibility Laboratory, Department of Medicine, Indiana University, Indianapolis, Indiana 46202, USA
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20646
[VALUE] => Array
(
[TEXT] => <p style="text-align: justify;">
In the process of HLA typing bone marrow patient and his potential donors, we have identified the novel DRQB1 allele, DQB1*03:31, in the DNA sample of a male, Native American (American Indian) descendant. This allele is present on the haplotype A* 02:01, B* 57:01, C* 06:02, DRB1* 07:01, DRB4* 01:01, DQA1*02:01, DQB1* 03:31. His other haplotype is A*30:02, is A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3*02:02, DQA1*01:01, DQB1*05:03, which also occurs on the donor. This new allele is identical to DQB1*03:03:02:01-03:03:02:05 in exon 2 except at codon 116 (position 346 b.p. ) where a nucleotide substitution (GTC >ATC) gives rise to a missense mutation – an amino acid change from Valine to Isoleucine.<br>
The name of the new allele – DQB1*03:31 has been officially assigned by the WHO Nomenclature Committee. This follows the agreed policy that subjects to the conditions stated in the most recent Nomenclature report, names will be assigned to the new sequences as they are identified. Lists of such new names were published in the following WHO Nomenclature report. The GenBank accession number is HM998989.1.<br>
Residue 116 is located in the β1-helix of the HLA class II molecule, which is part of the pocket F involved in peptide binding. The new allele contains an amino acid change in the antigen binding site of the HLA protein, which may alter its presenting properties.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
HLA DQB1, HLA DQ
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
In the process of HLA typing bone marrow patient and his potential donors, we have identified the novel DRQB1 allele, DQB1*03:31, in the DNA sample of a male, Native American (American Indian) descendant. This allele is present on the haplotype A* 02:01, B* 57:01, C* 06:02, DRB1* 07:01, DRB4* 01:01, DQA1*02:01, DQB1* 03:31. His other haplotype is A*30:02, is A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3*02:02, DQA1*01:01, DQB1*05:03, which also occurs on the donor. This new allele is identical to DQB1*03:03:02:01-03:03:02:05 in exon 2 except at codon 116 (position 346 b.p. ) where a nucleotide substitution (GTC >ATC) gives rise to a missense mutation – an amino acid change from Valine to Isoleucine.
The name of the new allele – DQB1*03:31 has been officially assigned by the WHO Nomenclature Committee. This follows the agreed policy that subjects to the conditions stated in the most recent Nomenclature report, names will be assigned to the new sequences as they are identified. Lists of such new names were published in the following WHO Nomenclature report. The GenBank accession number is HM998989.1.
Residue 116 is located in the β1-helix of the HLA class II molecule, which is part of the pocket F involved in peptide binding. The new allele contains an amino acid change in the antigen binding site of the HLA protein, which may alter its presenting properties.
Keywords
HLA DQB1, HLA DQ
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20647
[VALUE] => A new DQB1*03:31 identified by cloning and sequence-based typing
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => A new DQB1*03:31 identified by cloning and sequence-based typing
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20813
[VALUE] => 1451
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1451
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20814
[VALUE] => 1452
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1452
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Юрий А. Серов 1,2
В процессе HLA типирования пациента для предстоящей пересадки костного мозга и его потенциальных доноров, мы идентифицировали новую аллель HLA DQB1*03:31, в образце ДНК мужчины, потомка американских индейцев. Эта аллель присутствует в гаплотипе HLA A*02:01, B*57:01, C *06:02, DRB1*07:01, DRB4*01:01, DQA1 *02:01, DQB1*03:31. Его другим гаплотипом являются HLA A*30:02, B*18:01, C*05:01, DRB1*14:54, DRB3 * 02:02, DQA1*01:01, DQB1*05:03, что так же было обнаружено у донора. Этот новый аллель идентичен HLA DQB1*03:03:02:01-03:03:02:05 в экзоне 2, за исключением кодона 116 (позиция 346 п.н.), где нуклеотидное замещение (GTC> ATC) приводит к мутантной мутации – изменение аминокислоты – Валин на Изолейцин. Название новой аллели – HLA DQB1*03:31 было официально присвоено Комитетом номенклатуры ВОЗ. Это следует за согласованной политикой, которая подчиняется условиям, указанным в последнем отчете о номенклатуре, имена будут назначены новым последовательностям по мере их идентификации. Списки таких новых имен были опубликованы в отчете о номенклатуре ВОЗ. Номер доступа GenBank – HM998989.1. Остаток 116 находится в β1-спирали молекулы HLA класса II, которая является частью кармана F, участвующего в связывании пептидов. Новый аллель содержит изменение аминокислоты в сайте связывания белка HLA антигена, который может изменить его пространственные представляющие свойства.
Ключевые слова
HLA DQB1, HLA DQB1*03:31, ген HLA, клонирование, секвенирование.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20676
[VALUE] => Array
(
[TEXT] => Даниил И. Шмидт, Ольга В. Пирогова, Валентина В. Порунова, Ольга В. Кудяшева, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Даниил И. Шмидт, Ольга В. Пирогова, Валентина В. Порунова, Ольга В. Кудяшева, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20677
[VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20678
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Множественная миелома остается неизлечимым рецидивирующим заболеванием, и новые лекарственные средства являются мишенью исследований, направленных на увеличение беспрогрессивной и общей выживаемости пациентов с множественной миеломой (ММ). Иксазомиб – первый пероральный ингибитор протеасом, показавший свою эффективность в лечении пациентов с рецидивирующей/рефрактерной множественной миеломой. Как недавно появившееся лекарственное средство, иксазомиб нуждается в дальнейших исследованиях.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
Был проведен ретроспективный анализ опыта применения препарата у 12 пациентов с ММ. Были оценены эффективность и переносимость режима терапии, основанного на иксазомибе. Пациенты получали терапию в период с декабря 2016 по июль 2018 в научно-исследовательском институте детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой. Каждый пациент имел как минимум одну предшествующую линию терапии и рецидивирующее или рефрактерное течение заболевания. Ответ на терапию оценивался согласно критериям ответа International Myeloma Working Group (Kumar et al., 2016). 11 пациентов (92%) получали режим IRd (иксазомиб+леналидомид+дексаметазон), 1 пациент получал преднизолон вместо дексаметазона. Медиана возраста составляла 65,5 (44-75) лет на момент постановки диагноза и 70 (48-76) на момент начала терапии иксазомибом, 67% (n=8) были мужчинами. Для оценки влияния предшествующей терапии леналидомидом и количества предшествующих линий терапии на частоту общего ответа и частоту очень хорошего частичного ответа (ОХЧО) и полного ответа (ПО) был проведен однофакторный анализ с использованием критерия Хи-квадрат для качественных переменных.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Медиана времени наблюдения составила 10 месяцев. Медиана количества (диапазон) линий терапии составила 8 (2-17) месяцев. Частота общего ответа составила 58% (n=7), из которых 8% (n=1) имели ПО, 17% (n=2) имели ОХЧО и 33% (n=4) имели частичный ответ, как лучший ответ. У 3 пациентов (25%) была отмечена стабилизация заболевания и у 2 пациентов (17%) наблюдалось прогрессирование заболевания. Медиана (диапазон) времени до ответа составила 3 (1-8) месяцев и медиана (диапазон) длительности ответа составила 7 (2-13) месяцев. 11 (92%) пациентов имели как минимум 1 нежелательное явление. У 5 (42%) пациентов наблюдалась анемия (у 2 (17%) – 3 степени)), у 6 (50%) – тромбоцитопения (2 пациента имели 4 степень), у 4 (33%) – нейтропения (у 2 (17%) – 3-4 степени), у 1 (8%) развилась диарея 1 степени, и у 3 (25%) пациентов были отмечены инфекции верхних дыхательных путей. 33% пациентов (n=4) имели нежелательные явления ≥3 степени. До IRd 6 пациентов имели множественные линии терапии, в том числе леналидомид-содержащие, и 6 пациентов были леналидомид-наивными и получили только 1 линию терапии перед IRd. Различия в частоте общего ответа между пациентами с множественными предшествующими линиями терапии (частота общего ответа=33%, n=2) и пациентами, получившими 1 линию терапии перед режимом IRd (частота общего ответа=87%, n=5), не были статистически значимыми (p=0,079). Однако частота ПО и ОХЧО была значительно выше в группе, которая получала IRd, как терапию второй линии (0% против 50%, p=0,046).
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Терапия, основанная на иксазомибе, показала хорошую эффективность (частота общего ответа 58%) и приемлемую токсичность. Пациенты, не получавшие ранее леналидомид и имевшие только 1 предшествующую линию терапии, имеют статистически значимо более высокую частоту ПО и ОЧХО. На основе этого, можно предположить, что использование режима IRd в качестве терапии второй линии может улучшить глубину ответа пациентов с ММ, включая резистентные формы.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Миеломная болезнь, рефрактерная форма, рецидивы, иксазомиб, эффективность.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Множественная миелома остается неизлечимым рецидивирующим заболеванием, и новые лекарственные средства являются мишенью исследований, направленных на увеличение беспрогрессивной и общей выживаемости пациентов с множественной миеломой (ММ). Иксазомиб – первый пероральный ингибитор протеасом, показавший свою эффективность в лечении пациентов с рецидивирующей/рефрактерной множественной миеломой. Как недавно появившееся лекарственное средство, иксазомиб нуждается в дальнейших исследованиях.
Пациенты и методы
Был проведен ретроспективный анализ опыта применения препарата у 12 пациентов с ММ. Были оценены эффективность и переносимость режима терапии, основанного на иксазомибе. Пациенты получали терапию в период с декабря 2016 по июль 2018 в научно-исследовательском институте детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой. Каждый пациент имел как минимум одну предшествующую линию терапии и рецидивирующее или рефрактерное течение заболевания. Ответ на терапию оценивался согласно критериям ответа International Myeloma Working Group (Kumar et al., 2016). 11 пациентов (92%) получали режим IRd (иксазомиб+леналидомид+дексаметазон), 1 пациент получал преднизолон вместо дексаметазона. Медиана возраста составляла 65,5 (44-75) лет на момент постановки диагноза и 70 (48-76) на момент начала терапии иксазомибом, 67% (n=8) были мужчинами. Для оценки влияния предшествующей терапии леналидомидом и количества предшествующих линий терапии на частоту общего ответа и частоту очень хорошего частичного ответа (ОХЧО) и полного ответа (ПО) был проведен однофакторный анализ с использованием критерия Хи-квадрат для качественных переменных.
Результаты
Медиана времени наблюдения составила 10 месяцев. Медиана количества (диапазон) линий терапии составила 8 (2-17) месяцев. Частота общего ответа составила 58% (n=7), из которых 8% (n=1) имели ПО, 17% (n=2) имели ОХЧО и 33% (n=4) имели частичный ответ, как лучший ответ. У 3 пациентов (25%) была отмечена стабилизация заболевания и у 2 пациентов (17%) наблюдалось прогрессирование заболевания. Медиана (диапазон) времени до ответа составила 3 (1-8) месяцев и медиана (диапазон) длительности ответа составила 7 (2-13) месяцев. 11 (92%) пациентов имели как минимум 1 нежелательное явление. У 5 (42%) пациентов наблюдалась анемия (у 2 (17%) – 3 степени)), у 6 (50%) – тромбоцитопения (2 пациента имели 4 степень), у 4 (33%) – нейтропения (у 2 (17%) – 3-4 степени), у 1 (8%) развилась диарея 1 степени, и у 3 (25%) пациентов были отмечены инфекции верхних дыхательных путей. 33% пациентов (n=4) имели нежелательные явления ≥3 степени. До IRd 6 пациентов имели множественные линии терапии, в том числе леналидомид-содержащие, и 6 пациентов были леналидомид-наивными и получили только 1 линию терапии перед IRd. Различия в частоте общего ответа между пациентами с множественными предшествующими линиями терапии (частота общего ответа=33%, n=2) и пациентами, получившими 1 линию терапии перед режимом IRd (частота общего ответа=87%, n=5), не были статистически значимыми (p=0,079). Однако частота ПО и ОХЧО была значительно выше в группе, которая получала IRd, как терапию второй линии (0% против 50%, p=0,046).
Заключение
Терапия, основанная на иксазомибе, показала хорошую эффективность (частота общего ответа 58%) и приемлемую токсичность. Пациенты, не получавшие ранее леналидомид и имевшие только 1 предшествующую линию терапии, имеют статистически значимо более высокую частоту ПО и ОЧХО. На основе этого, можно предположить, что использование режима IRd в качестве терапии второй линии может улучшить глубину ответа пациентов с ММ, включая резистентные формы.
Ключевые слова
Миеломная болезнь, рефрактерная форма, рецидивы, иксазомиб, эффективность.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20679
[VALUE] => Array
(
[TEXT] => Daniil I. Shmidt, Olga V. Pirogova, Valentina V. Porunova, Olga V. Kudyasheva, Elena I. Darskaya, Sergey N. Bondarenko, Boris V. Afanasyev
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Daniil I. Shmidt, Olga V. Pirogova, Valentina V. Porunova, Olga V. Kudyasheva, Elena I. Darskaya, Sergey N. Bondarenko, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20680
[VALUE] => Array
(
[TEXT] => R. M. Gorbacheva Memorial Institute of Oncology, Hematology and Transplantation; Chair of Hematology, Transfusiology and Transplantology, Pavlov First Saint Petersburg State Medical University, Saint Petersburg, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => R. M. Gorbacheva Memorial Institute of Oncology, Hematology and Transplantation; Chair of Hematology, Transfusiology and Transplantology, Pavlov First Saint Petersburg State Medical University, Saint Petersburg, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20681
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Multiple myeloma (MM) remains incurable relapsing disease and novel agents are under investigation in order to prolong progression-free and overall survival of MM patients (pts). Ixazomib is the first oral proteasome inhibitor that showed effectiveness in relapsed/refractory MM. Patients (pts) refractory to prior bortezomib therapy are often responsive to ixazomib treatment. As newly introduced agent, ixazomib requires further investigation.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
Retrospective analysis of a single-center experience was performed in 12 pts with MM. Efficacy and tolerability of ixazomibe-based regimen was assessed. These patients were treated with ixazomib between December 2016 and July 2018 in Raisa Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation. All of them had at list one prior line therapy and relapsed or refractory disease. Response to treatment was assessed according to International Myeloma Working Group consensus criteria for response and minimal residual disease assessment in multiple myeloma (Kumar et al., 2016). 11 pts (92%) received IRd treatment regimen (ixazomib+ lenalidomide+ dexamethasone) and 1 patient was treated with prednisolone instead of dexamethasone. Median age was 65.5 (44-75) years at the time of diagnosis, and 70 (48-76) at the start of IRd treatment. 67% (n=8) were males. To assess impact of prior lenalidomide therapy and number of prior treatments on overall response rate (ORR) and rate of complete response (CR) and very good partial response (VGPR) univariate analysis was performed using Chi-square tests for categorical variables.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
The median follow-up was 10 months. Median treatment cycles (range) was 8 (2-17). Overall response rate was 58% (n=7), of which 8% (n=1) had CR, 17% (n=2) had VGPR, 33% (n=4) had partial response (PR) as best response. 3 pts (25%) were considered to have stable disease and 2 pts (17%) showed the disease progression. Median (range) time to response was 3 (1-8) months and median (range) response duration was 7 (2-13) months. Eleven patients (92%) had, at least, one adverse event. 5 (42%) developed anemia: 2 (17%) had grade 3 anemia), 6 (50%) had thrombocytopenia (2 pts with grade 4); 4 (33%) had neutropenia: 2 (17%), with grade 3-4; 1 patient (8%) exhibited grade 1 diarrhea, and 3 patients (25%) had upper respiratory tract infections. 33% (n=4) of the patients had adverse events (grade ≥3). Before IRd, 6 pts had multiple lines of treatment including lenalidomide and 6 pts were lenalidomide-naïve and received only one line of treatment. Difference in ORR was not statistically significant between patients with multiple lines of previous treatment (ORR=33%, n=2), and cases with one line of prior therapy (ORR=87%, n=5) (p=0.079), but CR and VGPR rate were significantly higher in the group who received IRd as second-line treatment (0% vs 50%, p=0.046).
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Ixazomib-based treatment showed good efficacy (ORR=58%) and acceptable toxicity. Patients without prior lenalidomide and one prior line of treatment had statistically significant improvement in VGPR and CR rate. From this basis, it can be assumed that use of IRd regimen as the second-line therapy may improve depth of response in relapsed/refractory multiple myeloma patients.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Multiple myeloma, relapsed, refractory, ixazomib, efficiency.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Multiple myeloma (MM) remains incurable relapsing disease and novel agents are under investigation in order to prolong progression-free and overall survival of MM patients (pts). Ixazomib is the first oral proteasome inhibitor that showed effectiveness in relapsed/refractory MM. Patients (pts) refractory to prior bortezomib therapy are often responsive to ixazomib treatment. As newly introduced agent, ixazomib requires further investigation.
Patients and methods
Retrospective analysis of a single-center experience was performed in 12 pts with MM. Efficacy and tolerability of ixazomibe-based regimen was assessed. These patients were treated with ixazomib between December 2016 and July 2018 in Raisa Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation. All of them had at list one prior line therapy and relapsed or refractory disease. Response to treatment was assessed according to International Myeloma Working Group consensus criteria for response and minimal residual disease assessment in multiple myeloma (Kumar et al., 2016). 11 pts (92%) received IRd treatment regimen (ixazomib+ lenalidomide+ dexamethasone) and 1 patient was treated with prednisolone instead of dexamethasone. Median age was 65.5 (44-75) years at the time of diagnosis, and 70 (48-76) at the start of IRd treatment. 67% (n=8) were males. To assess impact of prior lenalidomide therapy and number of prior treatments on overall response rate (ORR) and rate of complete response (CR) and very good partial response (VGPR) univariate analysis was performed using Chi-square tests for categorical variables.
Results
The median follow-up was 10 months. Median treatment cycles (range) was 8 (2-17). Overall response rate was 58% (n=7), of which 8% (n=1) had CR, 17% (n=2) had VGPR, 33% (n=4) had partial response (PR) as best response. 3 pts (25%) were considered to have stable disease and 2 pts (17%) showed the disease progression. Median (range) time to response was 3 (1-8) months and median (range) response duration was 7 (2-13) months. Eleven patients (92%) had, at least, one adverse event. 5 (42%) developed anemia: 2 (17%) had grade 3 anemia), 6 (50%) had thrombocytopenia (2 pts with grade 4); 4 (33%) had neutropenia: 2 (17%), with grade 3-4; 1 patient (8%) exhibited grade 1 diarrhea, and 3 patients (25%) had upper respiratory tract infections. 33% (n=4) of the patients had adverse events (grade ≥3). Before IRd, 6 pts had multiple lines of treatment including lenalidomide and 6 pts were lenalidomide-naïve and received only one line of treatment. Difference in ORR was not statistically significant between patients with multiple lines of previous treatment (ORR=33%, n=2), and cases with one line of prior therapy (ORR=87%, n=5) (p=0.079), but CR and VGPR rate were significantly higher in the group who received IRd as second-line treatment (0% vs 50%, p=0.046).
Conclusion
Ixazomib-based treatment showed good efficacy (ORR=58%) and acceptable toxicity. Patients without prior lenalidomide and one prior line of treatment had statistically significant improvement in VGPR and CR rate. From this basis, it can be assumed that use of IRd regimen as the second-line therapy may improve depth of response in relapsed/refractory multiple myeloma patients.
Keywords
Multiple myeloma, relapsed, refractory, ixazomib, efficiency.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20682
[VALUE] => Retrospective analysis of using ixazomib in patients with relapsed/refractory multiple myeloma
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Retrospective analysis of using ixazomib in patients with relapsed/refractory multiple myeloma
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20819
[VALUE] => 1457
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1457
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20820
[VALUE] => 1458
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1458
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Даниил И. Шмидт, Ольга В. Пирогова, Валентина В. Порунова, Ольга В. Кудяшева, Елена И. Дарская, Сергей Н. Бондаренко, Борис В. Афанасьев
Введение
Множественная миелома остается неизлечимым рецидивирующим заболеванием, и новые лекарственные средства являются мишенью исследований, направленных на увеличение беспрогрессивной и общей выживаемости пациентов с множественной миеломой (ММ). Иксазомиб – первый пероральный ингибитор протеасом, показавший свою эффективность в лечении пациентов с рецидивирующей/рефрактерной множественной миеломой. Как недавно появившееся лекарственное средство, иксазомиб нуждается в дальнейших исследованиях.
Пациенты и методы
Был проведен ретроспективный анализ опыта применения препарата у 12 пациентов с ММ. Были оценены эффективность и переносимость режима терапии, основанного на иксазомибе. Пациенты получали терапию в период с декабря 2016 по июль 2018 в научно-исследовательском институте детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой. Каждый пациент имел как минимум одну предшествующую линию терапии и рецидивирующее или рефрактерное течение заболевания. Ответ на терапию оценивался согласно критериям ответа International Myeloma Working Group (Kumar et al., 2016). 11 пациентов (92%) получали режим IRd (иксазомиб+леналидомид+дексаметазон), 1 пациент получал преднизолон вместо дексаметазона. Медиана возраста составляла 65,5 (44-75) лет на момент постановки диагноза и 70 (48-76) на момент начала терапии иксазомибом, 67% (n=8) были мужчинами. Для оценки влияния предшествующей терапии леналидомидом и количества предшествующих линий терапии на частоту общего ответа и частоту очень хорошего частичного ответа (ОХЧО) и полного ответа (ПО) был проведен однофакторный анализ с использованием критерия Хи-квадрат для качественных переменных.
Результаты
Медиана времени наблюдения составила 10 месяцев. Медиана количества (диапазон) линий терапии составила 8 (2-17) месяцев. Частота общего ответа составила 58% (n=7), из которых 8% (n=1) имели ПО, 17% (n=2) имели ОХЧО и 33% (n=4) имели частичный ответ, как лучший ответ. У 3 пациентов (25%) была отмечена стабилизация заболевания и у 2 пациентов (17%) наблюдалось прогрессирование заболевания. Медиана (диапазон) времени до ответа составила 3 (1-8) месяцев и медиана (диапазон) длительности ответа составила 7 (2-13) месяцев. 11 (92%) пациентов имели как минимум 1 нежелательное явление. У 5 (42%) пациентов наблюдалась анемия (у 2 (17%) – 3 степени)), у 6 (50%) – тромбоцитопения (2 пациента имели 4 степень), у 4 (33%) – нейтропения (у 2 (17%) – 3-4 степени), у 1 (8%) развилась диарея 1 степени, и у 3 (25%) пациентов были отмечены инфекции верхних дыхательных путей. 33% пациентов (n=4) имели нежелательные явления ≥3 степени. До IRd 6 пациентов имели множественные линии терапии, в том числе леналидомид-содержащие, и 6 пациентов были леналидомид-наивными и получили только 1 линию терапии перед IRd. Различия в частоте общего ответа между пациентами с множественными предшествующими линиями терапии (частота общего ответа=33%, n=2) и пациентами, получившими 1 линию терапии перед режимом IRd (частота общего ответа=87%, n=5), не были статистически значимыми (p=0,079). Однако частота ПО и ОХЧО была значительно выше в группе, которая получала IRd, как терапию второй линии (0% против 50%, p=0,046).
Заключение
Терапия, основанная на иксазомибе, показала хорошую эффективность (частота общего ответа 58%) и приемлемую токсичность. Пациенты, не получавшие ранее леналидомид и имевшие только 1 предшествующую линию терапии, имеют статистически значимо более высокую частоту ПО и ОЧХО. На основе этого, можно предположить, что использование режима IRd в качестве терапии второй линии может улучшить глубину ответа пациентов с ММ, включая резистентные формы.
Ключевые слова
Миеломная болезнь, рефрактерная форма, рецидивы, иксазомиб, эффективность.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20683
[VALUE] => Array
(
[TEXT] => Дарья А. Шашелева, Алексей А. Масчан, Лариса Н. Шелихова, Ульяна Н. Петрова, Мария А. Илюшина, Жанна Б. Шеховцова, Сергей Л. Благов, Андрей Б. Абросимов, Елена И. Гутовская, Елена Е. Курникова, Ольга И. Илларионова, Елена В. Боякова, Галина А. Новичкова, Михаил А. Масчан
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Дарья А. Шашелева, Алексей А. Масчан, Лариса Н. Шелихова, Ульяна Н. Петрова, Мария А. Илюшина, Жанна Б. Шеховцова, Сергей Л. Благов, Андрей Б. Абросимов, Елена И. Гутовская, Елена Е. Курникова, Ольга И. Илларионова, Елена В. Боякова, Галина А. Новичкова, Михаил А. Масчан
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20684
[VALUE] => Array
(
[TEXT] => ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Минздрава России, отдел оптимизации лечения и профилактики осложнений трансплантации гемопоэтических стволовых клеток, Москва, Россия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Минздрава России, отдел оптимизации лечения и профилактики осложнений трансплантации гемопоэтических стволовых клеток, Москва, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20685
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Цель работы</h2>
<p style="text-align: justify;">
Оптимизировать подходы к трансплантации гемопоэтических стволовых клеток (ТГСК) у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией (ПНГ) путем снижения риска реакции «трансплантат против хозяина» (РТПХ) и посттрансплантационных осложнений.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
Мы описываем опыт ТГСК от HLA-совместимых неродственных доноров с использованием деплеции альфа/бета Т-лимфоцитов и CD19-клеток у 5 пациентов (1 мужчина, 4 женщины) с ПНГ, развившейся в результате эволюции приобретенной апластической анемии (АА) после успешной иммуносупрессивной терапии (ИСТ) – см. Табл. 1. Медиана возраста пациентов на момент трансплантации составила 17,8 года (14,5-22,7 года), медиана интервала до диагностики ПНГ – 4 года (5 мес.-6,5 лет) от проведения ИСТ. У всех пациентов присутствовали признаки нетяжелой костномозговой недостаточности: гранулоциты 0,8·109/л (0,8-1,8·109/л), тромбоциты 106·109/л (27-143·109/л), гемоглобин – 78 г/л, медиана размера ПНГ-клона во фракции гранулоцитов составила 94% (75-99%). У одной пациентки в анамнезе был тромбоз мозговых венозных синусов. Кондиционирование состояло из торакоабдоминального облучения (ТАО) 4-6 Гр, циклофосфамида 100 мг/кг, флударабина 150 мг/м2 и лошадиного антитимоцитарного глобулина/алемтузумаба (Табл. 2). Экулизумаб вводили со дня (–7) до дня (+14) 1 раз в 7 дней, всего 4 введения, профилактика РТПХ/отторжения состояла из такролимуса ± метотрексат. Клеточные характеристики трансплантата были следующими: CD34+/кг 8,1·106/кг, альфа/бета Т-лимфоциты/кг 150·103/кг, гамма/дельта Т-лимфоциты/кг 7,3·106/кг, СD19+/кг 221·103/кг, NK/кг 6,4·108/кг (Табл. 3). Медиана продолжительности приема такролимуса после ТГСК составила 117 (27-365) сут.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Первичное приживление лейкоцитарного и тромбоцитарного ростков было достигнуто у всех пятерых пациентов с медианой 15 (12-18) и 13 (10-18) дней соответственно, ни одного отторжения не зафиксировано. Острую РТПХ наблюдали у одного пациента – I стадия (поражение кожи 2-й степени), которая потребовала системного назначения глюкокортикостероидов с быстрым ответом и быстрой отменой терапии. Хроническая РТПХ не развилась ни у одного пациента. Реактивация ЦМВ оказалась у 1 пациента, на (-1) сутки, проводилась упреждающая терапия фоскавиром в течение 2 нед., реактивации вируса Эпштейна-Барр (ЭБВ) и аденовируса не наблюдалось. Ни в одном случае не зарегистрировано проявлений эндотелиальной токсичности. У всех пациентов ко дню +30 достигнут полный донорский химеризм в миелоидном ростке. При этом во фракции Т-лимфоцитов памяти (фракция CD45RO+) у 1 пациента длительно сохранялся собственный химеризм, в то время как во фракции наивных Т-лимфоцитов (CD45RА+) химеризм был стабильно донорским с момента их появления в периферической крови. Ни у одного пациента не развилось гемолитического криза и исчезновение ПНГ-клона документировано у всех пациентов к +60 дню (см. рис. 1). Иммунореконституция (СD 3+/4+ > 200/мкл, СD19 + > 50/мкл) оказалась замедленной и наступала с медианой 6 мес после ТГСК (от 4 до 10 мес после ТГСК), однако клинически значимых инфекций, связанных c Т-клеточным дефицитом, не отмечено. В настоящее время все пять пациентов живы с нормальным гемопоэзом, полным количественным восстановлением показателей иммунитета, не имеют посттрансплантационных осложнений, клинически здоровы и хорошо социально адаптированы. Медиана посттрансплантационного наблюдения составляет 4 года (1,7–5,5 лет).
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Таким образом, выполнение ТГСК с деплецией альфа/бета Т-лимфоцитов и CD19-клеток от полностью совместимого неродственного донора после мощного иммуносупрессивного кондиционирования с минимальной органной токсичностью показало более чем обнадеживающие результаты в группе подростков и молодых взрослых с ПНГ.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Пароксизмальная ночная гемоглобинурия, трансплантация, деплеция альфа/бета Т-лимфоциты и CD19-клеток, неродственные доноры, подростки, молодые взрослые.
</p>
<h2 style="text-align: justify;">Таблица 1. Характеристика пациентов</h2>
<p style="text-align: justify;">
<img width="787" alt="44_таблица 1.png" src="/upload/medialibrary/614/44_tablitsa-1.png" height="516" title="44_таблица 1.png"><br>
Примечания. CsA – циклоспорин А, ПО – полный ответ, ЧО – частичный ответ, гран. – гранулоциты, тромб. – тромбоциты, ретик. – ретикулоциты
</p>
<h2 style="text-align: justify;">Таблица 2. Режим кондиционирования и лечение экулизумабом (дни)</h2>
<p style="text-align: justify;">
<img width="783" alt="44_таблица 2.png" src="/upload/medialibrary/9d9/44_tablitsa-2.png" height="325" title="44_таблица 2.png"><br>
</p>
<h2 style="text-align: justify;">Таблица 3. Характеристики трансплантата и режимов профилактики отторжения/РТПХ</h2>
<p style="text-align: justify;">
<img width="784" alt="44_таблица 3.png" src="/upload/medialibrary/240/44_tablitsa-3.png" height="232" title="44_таблица 3.png"><br>
Примечание. А/б Т/кг – альфа/бета Т-лифоциты/кг, Г/д T/кг – гамма/дельта Т-лимфоциты/кг.
</p>
<h2 style="text-align: justify;">Рисунок 1. Эволюция ПНГ-клона после ТГСК</h2>
<p style="text-align: justify;">
<img width="448" alt="44_рисунок 1.png" src="/upload/medialibrary/d25/44_risunok-1.png" height="403" title="44_рисунок 1.png">
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Цель работы
Оптимизировать подходы к трансплантации гемопоэтических стволовых клеток (ТГСК) у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией (ПНГ) путем снижения риска реакции «трансплантат против хозяина» (РТПХ) и посттрансплантационных осложнений.
Материалы и методы
Мы описываем опыт ТГСК от HLA-совместимых неродственных доноров с использованием деплеции альфа/бета Т-лимфоцитов и CD19-клеток у 5 пациентов (1 мужчина, 4 женщины) с ПНГ, развившейся в результате эволюции приобретенной апластической анемии (АА) после успешной иммуносупрессивной терапии (ИСТ) – см. Табл. 1. Медиана возраста пациентов на момент трансплантации составила 17,8 года (14,5-22,7 года), медиана интервала до диагностики ПНГ – 4 года (5 мес.-6,5 лет) от проведения ИСТ. У всех пациентов присутствовали признаки нетяжелой костномозговой недостаточности: гранулоциты 0,8·109/л (0,8-1,8·109/л), тромбоциты 106·109/л (27-143·109/л), гемоглобин – 78 г/л, медиана размера ПНГ-клона во фракции гранулоцитов составила 94% (75-99%). У одной пациентки в анамнезе был тромбоз мозговых венозных синусов. Кондиционирование состояло из торакоабдоминального облучения (ТАО) 4-6 Гр, циклофосфамида 100 мг/кг, флударабина 150 мг/м2 и лошадиного антитимоцитарного глобулина/алемтузумаба (Табл. 2). Экулизумаб вводили со дня (–7) до дня (+14) 1 раз в 7 дней, всего 4 введения, профилактика РТПХ/отторжения состояла из такролимуса ± метотрексат. Клеточные характеристики трансплантата были следующими: CD34+/кг 8,1·106/кг, альфа/бета Т-лимфоциты/кг 150·103/кг, гамма/дельта Т-лимфоциты/кг 7,3·106/кг, СD19+/кг 221·103/кг, NK/кг 6,4·108/кг (Табл. 3). Медиана продолжительности приема такролимуса после ТГСК составила 117 (27-365) сут.
Результаты
Первичное приживление лейкоцитарного и тромбоцитарного ростков было достигнуто у всех пятерых пациентов с медианой 15 (12-18) и 13 (10-18) дней соответственно, ни одного отторжения не зафиксировано. Острую РТПХ наблюдали у одного пациента – I стадия (поражение кожи 2-й степени), которая потребовала системного назначения глюкокортикостероидов с быстрым ответом и быстрой отменой терапии. Хроническая РТПХ не развилась ни у одного пациента. Реактивация ЦМВ оказалась у 1 пациента, на (-1) сутки, проводилась упреждающая терапия фоскавиром в течение 2 нед., реактивации вируса Эпштейна-Барр (ЭБВ) и аденовируса не наблюдалось. Ни в одном случае не зарегистрировано проявлений эндотелиальной токсичности. У всех пациентов ко дню +30 достигнут полный донорский химеризм в миелоидном ростке. При этом во фракции Т-лимфоцитов памяти (фракция CD45RO+) у 1 пациента длительно сохранялся собственный химеризм, в то время как во фракции наивных Т-лимфоцитов (CD45RА+) химеризм был стабильно донорским с момента их появления в периферической крови. Ни у одного пациента не развилось гемолитического криза и исчезновение ПНГ-клона документировано у всех пациентов к +60 дню (см. рис. 1). Иммунореконституция (СD 3+/4+ > 200/мкл, СD19 + > 50/мкл) оказалась замедленной и наступала с медианой 6 мес после ТГСК (от 4 до 10 мес после ТГСК), однако клинически значимых инфекций, связанных c Т-клеточным дефицитом, не отмечено. В настоящее время все пять пациентов живы с нормальным гемопоэзом, полным количественным восстановлением показателей иммунитета, не имеют посттрансплантационных осложнений, клинически здоровы и хорошо социально адаптированы. Медиана посттрансплантационного наблюдения составляет 4 года (1,7–5,5 лет).
Заключение
Таким образом, выполнение ТГСК с деплецией альфа/бета Т-лимфоцитов и CD19-клеток от полностью совместимого неродственного донора после мощного иммуносупрессивного кондиционирования с минимальной органной токсичностью показало более чем обнадеживающие результаты в группе подростков и молодых взрослых с ПНГ.
Ключевые слова
Пароксизмальная ночная гемоглобинурия, трансплантация, деплеция альфа/бета Т-лимфоциты и CD19-клеток, неродственные доноры, подростки, молодые взрослые.
Таблица 1. Характеристика пациентов

Примечания. CsA – циклоспорин А, ПО – полный ответ, ЧО – частичный ответ, гран. – гранулоциты, тромб. – тромбоциты, ретик. – ретикулоциты
Таблица 2. Режим кондиционирования и лечение экулизумабом (дни)

Таблица 3. Характеристики трансплантата и режимов профилактики отторжения/РТПХ

Примечание. А/б Т/кг – альфа/бета Т-лифоциты/кг, Г/д T/кг – гамма/дельта Т-лимфоциты/кг.
Рисунок 1. Эволюция ПНГ-клона после ТГСК

[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20686
[VALUE] => Array
(
[TEXT] => Daria A. Shasheleva, Alexei A. Maschan, Larisa N. Shelikhova, Ulyana N. Petrova, Maria A. Ilyushina, Zhanna B. Shekhovtsova, Sergey L. Blagov, Andrei B. Abrosimov, Elena I. Gutovskaya, Elena E. Kurnikova, Olga I. Illarionova, Elena V. Boyakova, Galina A. Novichkova, Michael A. Maschan
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Daria A. Shasheleva, Alexei A. Maschan, Larisa N. Shelikhova, Ulyana N. Petrova, Maria A. Ilyushina, Zhanna B. Shekhovtsova, Sergey L. Blagov, Andrei B. Abrosimov, Elena I. Gutovskaya, Elena E. Kurnikova, Olga I. Illarionova, Elena V. Boyakova, Galina A. Novichkova, Michael A. Maschan
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20687
[VALUE] => Array
(
[TEXT] => Dmitriy Rogachev National Medical Research Center for Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Dmitriy Rogachev National Medical Research Center for Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20688
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
The main goal was to optimize hematopoietic stem cell transplantation (HSCT) approach among adolescents and young adults with paroxysmal nocturnal hemoglobinuria (PNH) by means of Graft-versus-host disease (GVHD) and posttransplant complications risk lowering.
</p>
<h2 style="text-align: justify;">Materials and methods</h2>
<p style="text-align: justify;">
We report our experience of HSCT from HLA-matched unrelated donors using TCR alfa/beta and CD19 depletion in 5 pts (1M/4F) with PNH, developed after successful immunosuppressive therapy (IST) of acquired aplastic anemia (AA). Median age of pts at the moment of transplantation was 17.8 years (range 14.5-22.7), median interval from IST to PNH was 4 years (5mo – 6.5 y). In all patients non-severe pancytopenia was present: granulocytes 0.8х109/l (0.8-1.8х109/l) platelets 106х109/l (27-143х109/l) and Hb -78 g/l, median PNH clone size in granulocytes was 94 (range 75-99)%. One pts previously developed sinus thrombosis. Conditioning consisted of thoraco-abdominal irradiation 4-6 Gy, cyclophosphamide 100 mg/kg, fludarabine 150 mg/m2 and antithymocyte globulin (ATG) or alemtuzumab. Eculizumab was given from day (-7) till day (+14) (every 7 days, only 4 times). GVHD prophylaxis was tacrolimus +/- methotrexate. Infusedgraft characteristics were: CD34+ – 8.1х106/kg, CD3TCRab+ – 150х103/kg, CD3gd+ – 7.3х106/kg, СD19+ – 221х103/kg, NK – 6.4х108/kg.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Engraftment was achieved in all 5 pts with a median of 15 (12-18) и 13 (10-18) days for granulocytes and platelets, respectively. Skin acute GVHD grade I developed in only 1 pt, and subsided with short course of glucocorticoids. CMV reactivation occurred in 1 pt; there were no episodes of Epstein- Barr Virus (EBV) or Adenovirus (AdV) reactivation. Full donor myeloid chimerism was established in all cases by day +30. Immune reconstitution was delayed until 6 months after transplant but no severe infections occurred. All pts are alive for 1.7-5.5 years (med 4 years) after HSCT with normal hematopoiesis and immune function, full donor chimerism and no late sequelae.
</p>
<h2 style="text-align: justify;">Conclusions</h2>
<p style="text-align: justify;">
Transplantation of TCRalfa/beta and CD19 depleted hematopoietic cells from matched unrelated donor after immunoablative conditioning and supported with short course of eculizumab is perfectly safe and efficient technology leading to cure in young patients with PNH.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Paroxysmal nocturnal hemoglobinuria, TCR alfa/beta and CD19 depletion, transplantation, adolescents, young adults.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
The main goal was to optimize hematopoietic stem cell transplantation (HSCT) approach among adolescents and young adults with paroxysmal nocturnal hemoglobinuria (PNH) by means of Graft-versus-host disease (GVHD) and posttransplant complications risk lowering.
Materials and methods
We report our experience of HSCT from HLA-matched unrelated donors using TCR alfa/beta and CD19 depletion in 5 pts (1M/4F) with PNH, developed after successful immunosuppressive therapy (IST) of acquired aplastic anemia (AA). Median age of pts at the moment of transplantation was 17.8 years (range 14.5-22.7), median interval from IST to PNH was 4 years (5mo – 6.5 y). In all patients non-severe pancytopenia was present: granulocytes 0.8х109/l (0.8-1.8х109/l) platelets 106х109/l (27-143х109/l) and Hb -78 g/l, median PNH clone size in granulocytes was 94 (range 75-99)%. One pts previously developed sinus thrombosis. Conditioning consisted of thoraco-abdominal irradiation 4-6 Gy, cyclophosphamide 100 mg/kg, fludarabine 150 mg/m2 and antithymocyte globulin (ATG) or alemtuzumab. Eculizumab was given from day (-7) till day (+14) (every 7 days, only 4 times). GVHD prophylaxis was tacrolimus +/- methotrexate. Infusedgraft characteristics were: CD34+ – 8.1х106/kg, CD3TCRab+ – 150х103/kg, CD3gd+ – 7.3х106/kg, СD19+ – 221х103/kg, NK – 6.4х108/kg.
Results
Engraftment was achieved in all 5 pts with a median of 15 (12-18) и 13 (10-18) days for granulocytes and platelets, respectively. Skin acute GVHD grade I developed in only 1 pt, and subsided with short course of glucocorticoids. CMV reactivation occurred in 1 pt; there were no episodes of Epstein- Barr Virus (EBV) or Adenovirus (AdV) reactivation. Full donor myeloid chimerism was established in all cases by day +30. Immune reconstitution was delayed until 6 months after transplant but no severe infections occurred. All pts are alive for 1.7-5.5 years (med 4 years) after HSCT with normal hematopoiesis and immune function, full donor chimerism and no late sequelae.
Conclusions
Transplantation of TCRalfa/beta and CD19 depleted hematopoietic cells from matched unrelated donor after immunoablative conditioning and supported with short course of eculizumab is perfectly safe and efficient technology leading to cure in young patients with PNH.
Keywords
Paroxysmal nocturnal hemoglobinuria, TCR alfa/beta and CD19 depletion, transplantation, adolescents, young adults.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20689
[VALUE] => Hematopoietic stem cell transplantation with alpha/beta T lymphocyte and CD19 cell depletion in adolescents and young adults with paroxysmal nocturnal hemoglobinuria using the immune-ablative conditioning and “peritransplant” therapy with eculizumab
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Hematopoietic stem cell transplantation with alpha/beta T lymphocyte and CD19 cell depletion in adolescents and young adults with paroxysmal nocturnal hemoglobinuria using the immune-ablative conditioning and “peritransplant” therapy with eculizumab
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20817
[VALUE] => 1455
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1455
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20818
[VALUE] => 1456
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1456
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Дарья А. Шашелева, Алексей А. Масчан, Лариса Н. Шелихова, Ульяна Н. Петрова, Мария А. Илюшина, Жанна Б. Шеховцова, Сергей Л. Благов, Андрей Б. Абросимов, Елена И. Гутовская, Елена Е. Курникова, Ольга И. Илларионова, Елена В. Боякова, Галина А. Новичкова, Михаил А. Масчан
Цель работы
Оптимизировать подходы к трансплантации гемопоэтических стволовых клеток (ТГСК) у подростков и молодых взрослых с пароксизмальной ночной гемоглобинурией (ПНГ) путем снижения риска реакции «трансплантат против хозяина» (РТПХ) и посттрансплантационных осложнений.
Материалы и методы
Мы описываем опыт ТГСК от HLA-совместимых неродственных доноров с использованием деплеции альфа/бета Т-лимфоцитов и CD19-клеток у 5 пациентов (1 мужчина, 4 женщины) с ПНГ, развившейся в результате эволюции приобретенной апластической анемии (АА) после успешной иммуносупрессивной терапии (ИСТ) – см. Табл. 1. Медиана возраста пациентов на момент трансплантации составила 17,8 года (14,5-22,7 года), медиана интервала до диагностики ПНГ – 4 года (5 мес.-6,5 лет) от проведения ИСТ. У всех пациентов присутствовали признаки нетяжелой костномозговой недостаточности: гранулоциты 0,8·109/л (0,8-1,8·109/л), тромбоциты 106·109/л (27-143·109/л), гемоглобин – 78 г/л, медиана размера ПНГ-клона во фракции гранулоцитов составила 94% (75-99%). У одной пациентки в анамнезе был тромбоз мозговых венозных синусов. Кондиционирование состояло из торакоабдоминального облучения (ТАО) 4-6 Гр, циклофосфамида 100 мг/кг, флударабина 150 мг/м2 и лошадиного антитимоцитарного глобулина/алемтузумаба (Табл. 2). Экулизумаб вводили со дня (–7) до дня (+14) 1 раз в 7 дней, всего 4 введения, профилактика РТПХ/отторжения состояла из такролимуса ± метотрексат. Клеточные характеристики трансплантата были следующими: CD34+/кг 8,1·106/кг, альфа/бета Т-лимфоциты/кг 150·103/кг, гамма/дельта Т-лимфоциты/кг 7,3·106/кг, СD19+/кг 221·103/кг, NK/кг 6,4·108/кг (Табл. 3). Медиана продолжительности приема такролимуса после ТГСК составила 117 (27-365) сут.
Результаты
Первичное приживление лейкоцитарного и тромбоцитарного ростков было достигнуто у всех пятерых пациентов с медианой 15 (12-18) и 13 (10-18) дней соответственно, ни одного отторжения не зафиксировано. Острую РТПХ наблюдали у одного пациента – I стадия (поражение кожи 2-й степени), которая потребовала системного назначения глюкокортикостероидов с быстрым ответом и быстрой отменой терапии. Хроническая РТПХ не развилась ни у одного пациента. Реактивация ЦМВ оказалась у 1 пациента, на (-1) сутки, проводилась упреждающая терапия фоскавиром в течение 2 нед., реактивации вируса Эпштейна-Барр (ЭБВ) и аденовируса не наблюдалось. Ни в одном случае не зарегистрировано проявлений эндотелиальной токсичности. У всех пациентов ко дню +30 достигнут полный донорский химеризм в миелоидном ростке. При этом во фракции Т-лимфоцитов памяти (фракция CD45RO+) у 1 пациента длительно сохранялся собственный химеризм, в то время как во фракции наивных Т-лимфоцитов (CD45RА+) химеризм был стабильно донорским с момента их появления в периферической крови. Ни у одного пациента не развилось гемолитического криза и исчезновение ПНГ-клона документировано у всех пациентов к +60 дню (см. рис. 1). Иммунореконституция (СD 3+/4+ > 200/мкл, СD19 + > 50/мкл) оказалась замедленной и наступала с медианой 6 мес после ТГСК (от 4 до 10 мес после ТГСК), однако клинически значимых инфекций, связанных c Т-клеточным дефицитом, не отмечено. В настоящее время все пять пациентов живы с нормальным гемопоэзом, полным количественным восстановлением показателей иммунитета, не имеют посттрансплантационных осложнений, клинически здоровы и хорошо социально адаптированы. Медиана посттрансплантационного наблюдения составляет 4 года (1,7–5,5 лет).
Заключение
Таким образом, выполнение ТГСК с деплецией альфа/бета Т-лимфоцитов и CD19-клеток от полностью совместимого неродственного донора после мощного иммуносупрессивного кондиционирования с минимальной органной токсичностью показало более чем обнадеживающие результаты в группе подростков и молодых взрослых с ПНГ.
Ключевые слова
Пароксизмальная ночная гемоглобинурия, трансплантация, деплеция альфа/бета Т-лимфоциты и CD19-клеток, неродственные доноры, подростки, молодые взрослые.
Таблица 1. Характеристика пациентов

Примечания. CsA – циклоспорин А, ПО – полный ответ, ЧО – частичный ответ, гран. – гранулоциты, тромб. – тромбоциты, ретик. – ретикулоциты
Таблица 2. Режим кондиционирования и лечение экулизумабом (дни)

Таблица 3. Характеристики трансплантата и режимов профилактики отторжения/РТПХ

Примечание. А/б Т/кг – альфа/бета Т-лифоциты/кг, Г/д T/кг – гамма/дельта Т-лимфоциты/кг.
Рисунок 1. Эволюция ПНГ-клона после ТГСК

Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20711
[VALUE] => Array
(
[TEXT] => Юлия Ю. Власова, Елена В. Морозова, Мария В. Барабанщикова, Татьяна Л. Гиндина, Ильдар М. Бархатов, Александр Л. Алянский, Елена И. Дарская, Иван С. Моисеев, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Юлия Ю. Власова, Елена В. Морозова, Мария В. Барабанщикова, Татьяна Л. Гиндина, Ильдар М. Бархатов, Александр Л. Алянский, Елена И. Дарская, Иван С. Моисеев, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20712
[VALUE] => Array
(
[TEXT] => НИИ детской онкологии гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20713
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Лечение ХМЛ основано на применении ингибиторов тирозинкиназ (ИТК). Несмотря на высокую эффективность ИТК, некоторые пациенты в ХФ и значительно большее количество пациентов в ФА и БК оказываются к нему резистентными. Наиболее важный из обсуждаемых механизмов резистентности к ИТК – возникновение точечных мутаций в киназном домене АВL-тирозинкиназы. На сегодня T315I считается единственной мутацией, вызывающей резистентность лейкозных клеток ко всем известным ИТК I и II поколения, кроме Понатиниба.
</p>
<h2 style="text-align: justify;">Цель</h2>
<p style="text-align: justify;">
Цель работы состояла в оценке результатов различных методов лечения у пациентов с мутацией T315I ХМЛ.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
Приведены результаты ретроспективного анализа 79 BCR-ABLT315I-позитивных пациентов. 22 аллогенных трансплантаций костного мозга (алло-ТГСК) выполнены 20 пациентам, фармакологическую терапию получили 59 пациентов (41 больной получал ИТК в качестве монотерапии или в комбинации с другими препаратами, 10 пациентов получали α-интерферон в комбинации с другими препаратами, 8 – получали только гидроксикарбамид/химиотерапию). К моменту алло-ТГСК 6 пациентов находились в хронической фазе (ХФ1); 7– в ХФ≥2; 6 – в фазе акселерации и 3 пациента – в бластном кризе (БК). Медиана (Ме) возраста в момент выявления мутации была 47 лет (15-76), и 38 лет – в группе алло-ТГСК. В группе алло-ТГСК в 7 случаях донорами были HLA – идентичные сиблинги, в 13 – неродственные доноры, 13 пациентов (65%) получили более 2 линий ИТК перед алло-ТГСК. Количество баллов по шкале EBMT: 3-4 балла – 16 пациентов, 5-7 баллов – 6 пациента. Режим кондиционирования в 13 случаях (70%) был со сниженной интенсивностью доз. Ме времени от выявления мутации до алло-ТГСК 10 месяцев (2-38). Анализ выживаемости проводили с использованием мето- да Каплан-Майера, сравнение в группах проводили с применением лог-рангового критерия. Регрессионный анализ выживаемости выполнен с применением модели пропорциональных интенсивностей Кокса. Многофакторный регрессионный анализ включал следующие факторы и ковариаты: возраст на дату диагноза, пол, фаза на начало терапии, фаза на дату выявления мутации, терапия после выявления мутации (без алло-ТГСК и с алло-ТГСК), время до выявления мутации от начала терапии.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Ме времени наблюдения после выявления мутации T315I 21 месяц (1-100). 5-летняя ОВ в группе в целом составила 42%. При проведении многофакторного анализа только фаза ХМЛ во время обнаружения мутации значительно влияет на ОВ всей группы. Всего в фазе БК на момент выявления мутации было 7 человек, 3-м из них была выполнена алло-ТГСК. Все больные умерли в течение 1-го года после индикации T315I с Ме выживаемости 1.3 месяца. 5-летняя ОВ в группе фармакологической терапии (n=59) 42% с Ме выживаемости 2.8 года. ОВ в группе алло-ТГСК (n=20) 37% после 1-го года, Ме выживаемости 5 месяцев. Oднaкo, 7 пaциентoв пpoжили бoлее 2 лет пocле aллo-ТГCК, 2 – бoлее 6 лет. У всех пациентов после алло-ТГСК получен глубокий молекулярный ответ. У пaциентoв вo 2-й ХФ ОВ 47% (ДИ 95% 29-53%), p = 0,46. В группе фармакологической терапии без ИТК (N=18), включая ИТК (N=41) не было достоверных различий в 5-летней ОВ (42% и 47% соответственно, р=05,3). В гpуппе, пoлучaвшей α-интерферон в кoмбинaции c дpугими пpепapaтaми (n=10), 5-летняя OВ выше, чем в гpуппе, не пoлучaвшей интеpфеpoнo-теpaпию (n=49), и cocтaвляет 72 и 45% cooтветcтвеннo(p=0,21).
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
Появление клона с мутацией T315I у больных ХМЛ с резистентностью изменяет прогноз для данной категории пациентов, особенно в продвинутых фазах. Алло-ТГСК являетcя эффективным метoдoм лечения, пpивoдящим к выздopoвлению. Фaктopoм pиcкa, уxудшaющим pезультaты тpaнcплaнтaции являетcя фaзa БКнa мoмент aллo-ТГCК. Пpoведение фapмaкoлoгичеcкoй теpaпии в 1-й xpoничеcкoй фaзе являетcя эффективным метoдoм лечения, пoзвoляющим кoнтpoлиpoвaть зaбoлевaние в течение длительнoгo вpемени. У пaциентoв вo 2-й ХФ пpoведение aллo-ТГCК пoзвoляет дocтигнуть 47% (ДИ 95% 29–53%) веpoятнocти 5-летней oбщей выживaемocти.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<span style="font-family: "Minion Pro", georgia, serif; font-size: 17px; text-align: justify;">Хронический миелоидный лейкоз, мутация T315I, </span><span style="font-family: "Minion Pro", georgia, serif; font-size: 17px; text-align: justify;">алло-ТГСК, лекарственная резистентность.</span>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Лечение ХМЛ основано на применении ингибиторов тирозинкиназ (ИТК). Несмотря на высокую эффективность ИТК, некоторые пациенты в ХФ и значительно большее количество пациентов в ФА и БК оказываются к нему резистентными. Наиболее важный из обсуждаемых механизмов резистентности к ИТК – возникновение точечных мутаций в киназном домене АВL-тирозинкиназы. На сегодня T315I считается единственной мутацией, вызывающей резистентность лейкозных клеток ко всем известным ИТК I и II поколения, кроме Понатиниба.
Цель
Цель работы состояла в оценке результатов различных методов лечения у пациентов с мутацией T315I ХМЛ.
Материалы и методы
Приведены результаты ретроспективного анализа 79 BCR-ABLT315I-позитивных пациентов. 22 аллогенных трансплантаций костного мозга (алло-ТГСК) выполнены 20 пациентам, фармакологическую терапию получили 59 пациентов (41 больной получал ИТК в качестве монотерапии или в комбинации с другими препаратами, 10 пациентов получали α-интерферон в комбинации с другими препаратами, 8 – получали только гидроксикарбамид/химиотерапию). К моменту алло-ТГСК 6 пациентов находились в хронической фазе (ХФ1); 7– в ХФ≥2; 6 – в фазе акселерации и 3 пациента – в бластном кризе (БК). Медиана (Ме) возраста в момент выявления мутации была 47 лет (15-76), и 38 лет – в группе алло-ТГСК. В группе алло-ТГСК в 7 случаях донорами были HLA – идентичные сиблинги, в 13 – неродственные доноры, 13 пациентов (65%) получили более 2 линий ИТК перед алло-ТГСК. Количество баллов по шкале EBMT: 3-4 балла – 16 пациентов, 5-7 баллов – 6 пациента. Режим кондиционирования в 13 случаях (70%) был со сниженной интенсивностью доз. Ме времени от выявления мутации до алло-ТГСК 10 месяцев (2-38). Анализ выживаемости проводили с использованием мето- да Каплан-Майера, сравнение в группах проводили с применением лог-рангового критерия. Регрессионный анализ выживаемости выполнен с применением модели пропорциональных интенсивностей Кокса. Многофакторный регрессионный анализ включал следующие факторы и ковариаты: возраст на дату диагноза, пол, фаза на начало терапии, фаза на дату выявления мутации, терапия после выявления мутации (без алло-ТГСК и с алло-ТГСК), время до выявления мутации от начала терапии.
Результаты
Ме времени наблюдения после выявления мутации T315I 21 месяц (1-100). 5-летняя ОВ в группе в целом составила 42%. При проведении многофакторного анализа только фаза ХМЛ во время обнаружения мутации значительно влияет на ОВ всей группы. Всего в фазе БК на момент выявления мутации было 7 человек, 3-м из них была выполнена алло-ТГСК. Все больные умерли в течение 1-го года после индикации T315I с Ме выживаемости 1.3 месяца. 5-летняя ОВ в группе фармакологической терапии (n=59) 42% с Ме выживаемости 2.8 года. ОВ в группе алло-ТГСК (n=20) 37% после 1-го года, Ме выживаемости 5 месяцев. Oднaкo, 7 пaциентoв пpoжили бoлее 2 лет пocле aллo-ТГCК, 2 – бoлее 6 лет. У всех пациентов после алло-ТГСК получен глубокий молекулярный ответ. У пaциентoв вo 2-й ХФ ОВ 47% (ДИ 95% 29-53%), p = 0,46. В группе фармакологической терапии без ИТК (N=18), включая ИТК (N=41) не было достоверных различий в 5-летней ОВ (42% и 47% соответственно, р=05,3). В гpуппе, пoлучaвшей α-интерферон в кoмбинaции c дpугими пpепapaтaми (n=10), 5-летняя OВ выше, чем в гpуппе, не пoлучaвшей интеpфеpoнo-теpaпию (n=49), и cocтaвляет 72 и 45% cooтветcтвеннo(p=0,21).
Выводы
Появление клона с мутацией T315I у больных ХМЛ с резистентностью изменяет прогноз для данной категории пациентов, особенно в продвинутых фазах. Алло-ТГСК являетcя эффективным метoдoм лечения, пpивoдящим к выздopoвлению. Фaктopoм pиcкa, уxудшaющим pезультaты тpaнcплaнтaции являетcя фaзa БКнa мoмент aллo-ТГCК. Пpoведение фapмaкoлoгичеcкoй теpaпии в 1-й xpoничеcкoй фaзе являетcя эффективным метoдoм лечения, пoзвoляющим кoнтpoлиpoвaть зaбoлевaние в течение длительнoгo вpемени. У пaциентoв вo 2-й ХФ пpoведение aллo-ТГCК пoзвoляет дocтигнуть 47% (ДИ 95% 29–53%) веpoятнocти 5-летней oбщей выживaемocти.
Ключевые слова
Хронический миелоидный лейкоз, мутация T315I, алло-ТГСК, лекарственная резистентность.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20714
[VALUE] => Array
(
[TEXT] => Julia Yu. Vlasova, Elena V. Morozova, Maria V. Barabanshchikova, Tatyana L. Gindina, Ildar M. Barhatov, Alexandr L. Alyanskiy, Elena I. Darskaya, Ivan S. Moiseev, Boris V. Afanasyev
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Julia Yu. Vlasova, Elena V. Morozova, Maria V. Barabanshchikova, Tatyana L. Gindina, Ildar M. Barhatov, Alexandr L. Alyanskiy, Elena I. Darskaya, Ivan S. Moiseev, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20715
[VALUE] => Array
(
[TEXT] => R. M. Gorbacheva Institute of Pediatric Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, First St. Petersburg State I. P. Pavlov Medical University, St. Petersburg
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => R. M. Gorbacheva Institute of Pediatric Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, First St. Petersburg State I. P. Pavlov Medical University, St. Petersburg
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20716
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Background</h2>
<p style="text-align: justify;">
Resistance to tyrosine kinase inhibitors (TKI) in patients with chronic myeloid leukemia (CML) is frequently caused by point mutations in the BCR-ABL kinase domain, including the gatekeeper mutant T315I, which confers a high degree of resistance to all currently approved tyrosine kinase inhibitors except ponatinib.
</p>
<h2 style="text-align: justify;">Aims</h2>
<p style="text-align: justify;">
To evaluate the results of different treatment modalities in CML patients with T315I mutation.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
A retrospective analysis of 79 BCR-ABLT315I –positive CML patients (pts) was done. Allogeneic bone marrow transplantation (allo-HSCT) was made in 20 pts, 59 pts received only pharmacological therapy (41 pts received TKI as monotherapy or in combination with other drugs, 10- α-IF, other 8 pts received hydroxyurea or chemotherapy). At the time of allo-HSCT 6 pts were in CP 1, 7- CP≥2, 6 pts had AP and 3 pts were in BC. Median age at the time of mutation detected was 42 years (13-75) (38 years in HSCT-group). In allo-HSCT group 13 pts had unrelated donors, 13(65%) pts received more than 2 lines TKIs before HSCT. The EBMT scores were as follows: 3-4 points, 16 pts; 5-7 points, 6 pts. Conditioning regimen in 13 (70%) pts had reduced intensity. Median time to HSCT after T315I detection was 7 months (0-72). The BCR-ABL mutation analysis was performed by Sanger sequencing. Overall survival (OS) was estimated by Kaplan-Meier method with log-rank test for comparison between groups. Cox regression was used for multivariate survival analysis that included next covariates: age, phase on the time of mutation detection, performance of allo-HSCT, time to T315I detection from TKI start.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Median follow-up time after T315I detection was 21 months (1-100). 5-years OS in whole group was 42%. According to multivariate analysis, only CML phase at the time of mutation detection did significantly affect survival in the entire group. All the pts in BC (n=7), 3 in HSCT group, and 4, in non-HSCT group, died within first year after the T315I detection, whereas the median survival time was 1.3 months. The 5-year OS in non-HSCT group (n=59) comprised 42%, with median survival time of 2.8 years. The 5-year OS after allo-HSCT (n=20) was 37%, with median survival time of 5 months. However, 7 pts lived for more than 2 years after allo-HSCT; 2 patients survived for more than 6 years. All living patients after allo-HSCT are in deep molecular response. The patients in 2nd chronic phase have OS rate of 47% (CI 95% 29-53%), p = 0.46. There was no significant difference in 5-year OS between the non-HSCT groups with TKI (n=41) and non-TKI (n=18) therapy (42% and 47%, respectively, p=0.53). the The 5-year overall survival (OS) among the patients who received α-interferon combined with other drugs (n=10) was higher than in the group that was not treated with interferon (n = 49), 72% vs 45%, respectively (p = 0.21).
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Presence of T315I mutation in TKI-resistant patients is extremely unfavorable factor for survival, and it is a major reason for switching to ponatinib or other new potentially available drugs, if possible. Allo-HSCT is an effective method of treatment for this group of patients in case of good selection, however, taking transplant risks into consideration, especially for patients in CP ≥2 . Administration of pharmacological therapy in the 1st CP is an effective method of treatment, which allows to control the disease for a long time.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Chronic myeloid leukemia, T315I mutation, allo-BMT, drug resistance.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Background
Resistance to tyrosine kinase inhibitors (TKI) in patients with chronic myeloid leukemia (CML) is frequently caused by point mutations in the BCR-ABL kinase domain, including the gatekeeper mutant T315I, which confers a high degree of resistance to all currently approved tyrosine kinase inhibitors except ponatinib.
Aims
To evaluate the results of different treatment modalities in CML patients with T315I mutation.
Patients and methods
A retrospective analysis of 79 BCR-ABLT315I –positive CML patients (pts) was done. Allogeneic bone marrow transplantation (allo-HSCT) was made in 20 pts, 59 pts received only pharmacological therapy (41 pts received TKI as monotherapy or in combination with other drugs, 10- α-IF, other 8 pts received hydroxyurea or chemotherapy). At the time of allo-HSCT 6 pts were in CP 1, 7- CP≥2, 6 pts had AP and 3 pts were in BC. Median age at the time of mutation detected was 42 years (13-75) (38 years in HSCT-group). In allo-HSCT group 13 pts had unrelated donors, 13(65%) pts received more than 2 lines TKIs before HSCT. The EBMT scores were as follows: 3-4 points, 16 pts; 5-7 points, 6 pts. Conditioning regimen in 13 (70%) pts had reduced intensity. Median time to HSCT after T315I detection was 7 months (0-72). The BCR-ABL mutation analysis was performed by Sanger sequencing. Overall survival (OS) was estimated by Kaplan-Meier method with log-rank test for comparison between groups. Cox regression was used for multivariate survival analysis that included next covariates: age, phase on the time of mutation detection, performance of allo-HSCT, time to T315I detection from TKI start.
Results
Median follow-up time after T315I detection was 21 months (1-100). 5-years OS in whole group was 42%. According to multivariate analysis, only CML phase at the time of mutation detection did significantly affect survival in the entire group. All the pts in BC (n=7), 3 in HSCT group, and 4, in non-HSCT group, died within first year after the T315I detection, whereas the median survival time was 1.3 months. The 5-year OS in non-HSCT group (n=59) comprised 42%, with median survival time of 2.8 years. The 5-year OS after allo-HSCT (n=20) was 37%, with median survival time of 5 months. However, 7 pts lived for more than 2 years after allo-HSCT; 2 patients survived for more than 6 years. All living patients after allo-HSCT are in deep molecular response. The patients in 2nd chronic phase have OS rate of 47% (CI 95% 29-53%), p = 0.46. There was no significant difference in 5-year OS between the non-HSCT groups with TKI (n=41) and non-TKI (n=18) therapy (42% and 47%, respectively, p=0.53). the The 5-year overall survival (OS) among the patients who received α-interferon combined with other drugs (n=10) was higher than in the group that was not treated with interferon (n = 49), 72% vs 45%, respectively (p = 0.21).
Conclusion
Presence of T315I mutation in TKI-resistant patients is extremely unfavorable factor for survival, and it is a major reason for switching to ponatinib or other new potentially available drugs, if possible. Allo-HSCT is an effective method of treatment for this group of patients in case of good selection, however, taking transplant risks into consideration, especially for patients in CP ≥2 . Administration of pharmacological therapy in the 1st CP is an effective method of treatment, which allows to control the disease for a long time.
Keywords
Chronic myeloid leukemia, T315I mutation, allo-BMT, drug resistance.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20717
[VALUE] => CML patients with T315I mutation: characteristics and outcomes of the treatment
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => CML patients with T315I mutation: characteristics and outcomes of the treatment
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20833
[VALUE] => 1472
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1472
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20834
[VALUE] => 1473
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1473
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Юлия Ю. Власова, Елена В. Морозова, Мария В. Барабанщикова, Татьяна Л. Гиндина, Ильдар М. Бархатов, Александр Л. Алянский, Елена И. Дарская, Иван С. Моисеев, Борис В. Афанасьев
Введение
Лечение ХМЛ основано на применении ингибиторов тирозинкиназ (ИТК). Несмотря на высокую эффективность ИТК, некоторые пациенты в ХФ и значительно большее количество пациентов в ФА и БК оказываются к нему резистентными. Наиболее важный из обсуждаемых механизмов резистентности к ИТК – возникновение точечных мутаций в киназном домене АВL-тирозинкиназы. На сегодня T315I считается единственной мутацией, вызывающей резистентность лейкозных клеток ко всем известным ИТК I и II поколения, кроме Понатиниба.
Цель
Цель работы состояла в оценке результатов различных методов лечения у пациентов с мутацией T315I ХМЛ.
Материалы и методы
Приведены результаты ретроспективного анализа 79 BCR-ABLT315I-позитивных пациентов. 22 аллогенных трансплантаций костного мозга (алло-ТГСК) выполнены 20 пациентам, фармакологическую терапию получили 59 пациентов (41 больной получал ИТК в качестве монотерапии или в комбинации с другими препаратами, 10 пациентов получали α-интерферон в комбинации с другими препаратами, 8 – получали только гидроксикарбамид/химиотерапию). К моменту алло-ТГСК 6 пациентов находились в хронической фазе (ХФ1); 7– в ХФ≥2; 6 – в фазе акселерации и 3 пациента – в бластном кризе (БК). Медиана (Ме) возраста в момент выявления мутации была 47 лет (15-76), и 38 лет – в группе алло-ТГСК. В группе алло-ТГСК в 7 случаях донорами были HLA – идентичные сиблинги, в 13 – неродственные доноры, 13 пациентов (65%) получили более 2 линий ИТК перед алло-ТГСК. Количество баллов по шкале EBMT: 3-4 балла – 16 пациентов, 5-7 баллов – 6 пациента. Режим кондиционирования в 13 случаях (70%) был со сниженной интенсивностью доз. Ме времени от выявления мутации до алло-ТГСК 10 месяцев (2-38). Анализ выживаемости проводили с использованием мето- да Каплан-Майера, сравнение в группах проводили с применением лог-рангового критерия. Регрессионный анализ выживаемости выполнен с применением модели пропорциональных интенсивностей Кокса. Многофакторный регрессионный анализ включал следующие факторы и ковариаты: возраст на дату диагноза, пол, фаза на начало терапии, фаза на дату выявления мутации, терапия после выявления мутации (без алло-ТГСК и с алло-ТГСК), время до выявления мутации от начала терапии.
Результаты
Ме времени наблюдения после выявления мутации T315I 21 месяц (1-100). 5-летняя ОВ в группе в целом составила 42%. При проведении многофакторного анализа только фаза ХМЛ во время обнаружения мутации значительно влияет на ОВ всей группы. Всего в фазе БК на момент выявления мутации было 7 человек, 3-м из них была выполнена алло-ТГСК. Все больные умерли в течение 1-го года после индикации T315I с Ме выживаемости 1.3 месяца. 5-летняя ОВ в группе фармакологической терапии (n=59) 42% с Ме выживаемости 2.8 года. ОВ в группе алло-ТГСК (n=20) 37% после 1-го года, Ме выживаемости 5 месяцев. Oднaкo, 7 пaциентoв пpoжили бoлее 2 лет пocле aллo-ТГCК, 2 – бoлее 6 лет. У всех пациентов после алло-ТГСК получен глубокий молекулярный ответ. У пaциентoв вo 2-й ХФ ОВ 47% (ДИ 95% 29-53%), p = 0,46. В группе фармакологической терапии без ИТК (N=18), включая ИТК (N=41) не было достоверных различий в 5-летней ОВ (42% и 47% соответственно, р=05,3). В гpуппе, пoлучaвшей α-интерферон в кoмбинaции c дpугими пpепapaтaми (n=10), 5-летняя OВ выше, чем в гpуппе, не пoлучaвшей интеpфеpoнo-теpaпию (n=49), и cocтaвляет 72 и 45% cooтветcтвеннo(p=0,21).
Выводы
Появление клона с мутацией T315I у больных ХМЛ с резистентностью изменяет прогноз для данной категории пациентов, особенно в продвинутых фазах. Алло-ТГСК являетcя эффективным метoдoм лечения, пpивoдящим к выздopoвлению. Фaктopoм pиcкa, уxудшaющим pезультaты тpaнcплaнтaции являетcя фaзa БКнa мoмент aллo-ТГCК. Пpoведение фapмaкoлoгичеcкoй теpaпии в 1-й xpoничеcкoй фaзе являетcя эффективным метoдoм лечения, пoзвoляющим кoнтpoлиpoвaть зaбoлевaние в течение длительнoгo вpемени. У пaциентoв вo 2-й ХФ пpoведение aллo-ТГCК пoзвoляет дocтигнуть 47% (ДИ 95% 29–53%) веpoятнocти 5-летней oбщей выживaемocти.
Ключевые слова
Хронический миелоидный лейкоз, мутация T315I, алло-ТГСК, лекарственная резистентность.Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20718
[VALUE] => Array
(
[TEXT] => Иван В. Цыганков, Марина О. Попова, Анастасия В. Некрасова, Юлия А. Рогачева, Кирилл В. Лепик, Елена В. Кондакова, Елена И. Дарская, Лилия В. Стельмах, Юрий Р. Залялов, Вадим В. Байков, Наталья Б. Михайлова, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Иван В. Цыганков, Марина О. Попова, Анастасия В. Некрасова, Юлия А. Рогачева, Кирилл В. Лепик, Елена В. Кондакова, Елена И. Дарская, Лилия В. Стельмах, Юрий Р. Залялов, Вадим В. Байков, Наталья Б. Михайлова, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20719
[VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20720
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Вирус иммунодефицита человека (ВИЧ) связан с высоким риском развития злокачественных новообразований, таких как – лимфома Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на успешное применение антиретровирусной терапии (АРВТ) [1]. Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать агрессивную терапию, включающую высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [2]. Результаты ауто-ТГСК для лечения ВИЧ-ассоциированных лимфом все еще являются предметом споров. Количество проспективных сравнительных исследований эффективности и безопасности ВДХТ с последующей ауто-ТГСК ограничено.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
В проспективное исследование включены 10 пациентов с лимфомами на фоне ВИЧ (группа исследования), которым была проведена ВДХТ с последующей ауто-ТГСК в клинике НИИ ДОГиТ в период с 2016 по 2018 год. Для сравнения эффективности и безопасности процедуры использован метод «случай-контроль» (1:4) и, в качестве группы сравнения, в исследование включены 40 пациентов без ВИЧ-инфекции, сопоставимые по основным характеристикам (контрольная группа), которым была выполнена ауто-ТГСК в тот же промежуток времени. Медиана наблюдения составила 8 (1-28) месяцев в обеих группах. Проводилась оценка острой токсичности по шкале Common Terminology Criteria for Adverse Events 4.0 (CTCAE), скорости восстановления кроветворения, а так же общей выживаемости (ОВ), выживаемости без прогрессирования (ВБП) и времени до прогрессирования (ВДП) в течение 18 месяцев после ауто-ТГСК. При исследовании ВБП и ВДП из анализа исключены 4 пациента контрольной группы с ЛХ, которые получали посттрансплантационную терапию брентуксимаб ведотином. Основными заболеваниями в группе исследования были: ЛХ п=6 (60%) и НХЛ п=4 (40%), в контрольной группе – ЛХ п=29 (72,5%) и НХЛ п=11 (27,5%). ВИЧ-статус на момент трансплантации в группе исследования: вирусная нагрузка (ПЦР-РНК ВИЧ) – <50 копий/мл; медиана уровня CD4+ клеток составила 484 (210-715) клеток/ мкл; все пациенты получали АРВТ.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Общая выживаемость в течение 18 месяцев от ауто-ТГСК составила 88% (n=50): в группе пациентов с ВИЧ – 90%, в группе сравнения – 87,5% (р=0,605). Медиана дня восстановления лейкоцитов, нейтрофилов и тромбоцитов в группе исследования составила Д+14, Д+17, Д+20, в группе сравнения – Д+14, Д+16, Д+19, соответственно. В результате анализа токсичности по шкале СТСАЕ, частота развития энтеро-, гепато-, нефро- токсичности в обеих группах не различалась (таблица 1). Частота рецидива основного заболевания в течение 18 месяцев у пациентов с ВИЧ инфекцией составила 20%, медиана ВДП – 3 мес. (2-4), в контрольной группе – 11,1%, медиана ВДП – 8,5 мес. (3-11) (р=0,645). Выживаемость без прогрессирования в течение 18 месяцев после ауто-ТГСК составила 76,1% (n=46): в группе пациентов с ВИЧ – 70%, в группе сравнения – 77,8% (р=0,892). При анализе в подгруппах ЛХ и НХЛ различий в ОВ, ВБП и ВДП различий не обнаружено.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Общая выживаемость в течение 18 месяцев после высокодозной химиотерапии с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ составила 90%, и не отличалась от контрольной группы. Показатели выживаемости без прогрессирования у пациентов с ВИЧ и частоты рецидивов составили 70% и 20% соответственно, и не отличались от группы пациентов без ВИЧ. Восстановление кроветворения и спектр токсичности не различались в группах сравнения. Полученные данные подтверждают, что высокодозная химиотерапия с ауто-ТГСК такая же эффективная и безопасная процедура у пациентов с ВИЧ-ассоциированными лимфомами, как и у пациентов с лимфомами без ВИЧ.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
ВИЧ-ассоциированные лимфомы, ВИЧ, аутологичная трансплантация гемопоэтическх стволовых клеток, высокодозная химиотерапия, общая выживаемость, токсичность, восстановление гемопоэза, ВИЧ-статус, выживаемость без прогрессирования.
</p>
<h2 style="text-align: justify;">Литература</h2>
<p style="text-align: justify;">
1. Yanik EL, Napravnik S, Cole SR, Achenbach CJ, Gopal S, Olshan A, et al. Incidence and timing of cancer in HIV-infected individuals following initiation of combination antiretroviral therapy. Clin Infect Dis. 2013;57:756–764.<br>
2. Krishnan A, Palmer JM, Zaia JA, Tsai NC, Alvarnas J, Forman SJ. HIV status does not affect the outcome of autologous stem cell transplantation (ASCT) for non-Hodgkin lymphoma (NHL). Biol Blood Marrow Transplantation. 2010;16(9):1302-1308.
</p>
<h2 style="text-align: justify;">Таблица 1. Клинические характеристики ВИЧ-инфицированной и контрольной групп пациентов</h2>
<p style="text-align: justify;">
<img width="787" alt="52_таблица 1.png" src="/upload/medialibrary/328/52_tablitsa-1.png" height="209" title="52_таблица 1.png">
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Вирус иммунодефицита человека (ВИЧ) связан с высоким риском развития злокачественных новообразований, таких как – лимфома Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на успешное применение антиретровирусной терапии (АРВТ) [1]. Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать агрессивную терапию, включающую высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [2]. Результаты ауто-ТГСК для лечения ВИЧ-ассоциированных лимфом все еще являются предметом споров. Количество проспективных сравнительных исследований эффективности и безопасности ВДХТ с последующей ауто-ТГСК ограничено.
Пациенты и методы
В проспективное исследование включены 10 пациентов с лимфомами на фоне ВИЧ (группа исследования), которым была проведена ВДХТ с последующей ауто-ТГСК в клинике НИИ ДОГиТ в период с 2016 по 2018 год. Для сравнения эффективности и безопасности процедуры использован метод «случай-контроль» (1:4) и, в качестве группы сравнения, в исследование включены 40 пациентов без ВИЧ-инфекции, сопоставимые по основным характеристикам (контрольная группа), которым была выполнена ауто-ТГСК в тот же промежуток времени. Медиана наблюдения составила 8 (1-28) месяцев в обеих группах. Проводилась оценка острой токсичности по шкале Common Terminology Criteria for Adverse Events 4.0 (CTCAE), скорости восстановления кроветворения, а так же общей выживаемости (ОВ), выживаемости без прогрессирования (ВБП) и времени до прогрессирования (ВДП) в течение 18 месяцев после ауто-ТГСК. При исследовании ВБП и ВДП из анализа исключены 4 пациента контрольной группы с ЛХ, которые получали посттрансплантационную терапию брентуксимаб ведотином. Основными заболеваниями в группе исследования были: ЛХ п=6 (60%) и НХЛ п=4 (40%), в контрольной группе – ЛХ п=29 (72,5%) и НХЛ п=11 (27,5%). ВИЧ-статус на момент трансплантации в группе исследования: вирусная нагрузка (ПЦР-РНК ВИЧ) – <50 копий/мл; медиана уровня CD4+ клеток составила 484 (210-715) клеток/ мкл; все пациенты получали АРВТ.
Результаты
Общая выживаемость в течение 18 месяцев от ауто-ТГСК составила 88% (n=50): в группе пациентов с ВИЧ – 90%, в группе сравнения – 87,5% (р=0,605). Медиана дня восстановления лейкоцитов, нейтрофилов и тромбоцитов в группе исследования составила Д+14, Д+17, Д+20, в группе сравнения – Д+14, Д+16, Д+19, соответственно. В результате анализа токсичности по шкале СТСАЕ, частота развития энтеро-, гепато-, нефро- токсичности в обеих группах не различалась (таблица 1). Частота рецидива основного заболевания в течение 18 месяцев у пациентов с ВИЧ инфекцией составила 20%, медиана ВДП – 3 мес. (2-4), в контрольной группе – 11,1%, медиана ВДП – 8,5 мес. (3-11) (р=0,645). Выживаемость без прогрессирования в течение 18 месяцев после ауто-ТГСК составила 76,1% (n=46): в группе пациентов с ВИЧ – 70%, в группе сравнения – 77,8% (р=0,892). При анализе в подгруппах ЛХ и НХЛ различий в ОВ, ВБП и ВДП различий не обнаружено.
Заключение
Общая выживаемость в течение 18 месяцев после высокодозной химиотерапии с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ составила 90%, и не отличалась от контрольной группы. Показатели выживаемости без прогрессирования у пациентов с ВИЧ и частоты рецидивов составили 70% и 20% соответственно, и не отличались от группы пациентов без ВИЧ. Восстановление кроветворения и спектр токсичности не различались в группах сравнения. Полученные данные подтверждают, что высокодозная химиотерапия с ауто-ТГСК такая же эффективная и безопасная процедура у пациентов с ВИЧ-ассоциированными лимфомами, как и у пациентов с лимфомами без ВИЧ.
Ключевые слова
ВИЧ-ассоциированные лимфомы, ВИЧ, аутологичная трансплантация гемопоэтическх стволовых клеток, высокодозная химиотерапия, общая выживаемость, токсичность, восстановление гемопоэза, ВИЧ-статус, выживаемость без прогрессирования.
Литература
1. Yanik EL, Napravnik S, Cole SR, Achenbach CJ, Gopal S, Olshan A, et al. Incidence and timing of cancer in HIV-infected individuals following initiation of combination antiretroviral therapy. Clin Infect Dis. 2013;57:756–764.
2. Krishnan A, Palmer JM, Zaia JA, Tsai NC, Alvarnas J, Forman SJ. HIV status does not affect the outcome of autologous stem cell transplantation (ASCT) for non-Hodgkin lymphoma (NHL). Biol Blood Marrow Transplantation. 2010;16(9):1302-1308.
Таблица 1. Клинические характеристики ВИЧ-инфицированной и контрольной групп пациентов

[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20721
[VALUE] => Array
(
[TEXT] => Ivan V. Tsygankov, Marina O. Popova, Anastasia V. Nekrasova, Yulia A. Rogacheva, Kirill V. Lepik, Elena V. Kondakova, Elena I. Darskaya, Lilia V. Stelmakh, Yurii R. Zalyalov, Vadim V. Baykov, Natalia B. Mikhaylova, Boris V. Afanasyev
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Ivan V. Tsygankov, Marina O. Popova, Anastasia V. Nekrasova, Yulia A. Rogacheva, Kirill V. Lepik, Elena V. Kondakova, Elena I. Darskaya, Lilia V. Stelmakh, Yurii R. Zalyalov, Vadim V. Baykov, Natalia B. Mikhaylova, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20722
[VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Institute of Children Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Institute of Children Oncology, Hematology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20723
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Infection with human immunodeficiency virus (HIV) is associated with a significantly increased risk of cancer, including Hodgkin lymphoma (HL) and non-Hodgkin lymphoma (NHL), even when patients are treated successfully with contemporary antiretroviral therapy [1]. Widespread use of the antiretroviral therapy (ART) has changed the approach to treatment of the HIV-related lymphomas, allowing the use of aggressive therapy including high-dose chemotherapy (HDC) followed by autologous hematopoietic stem cell transplantation (ASCT) [2]. The outcome of ASCT for HIV-related lymphomas is still a subject for controversy. The number of a prospective case-control studies where estimated safety and efficiency of ASCT procedure is limited.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
From January 2016 to March 2018, ten patients with HIV-related lymphoma who underwent HDC followed by ASCT were included into a prospective study (study HIV-infected group, n=10). To compare the efficacy and safety of the procedure, a “case-control” method (1:4) have been applied. The comparison group consisted of non-HIV-infected patients with lymphoma comparable for basic characteristics patients, who have undergone ASCT at the same period of time (control group, n=40). Median follow-up time was 8 (1- 28) months for both groups. The primary endpoint of the study was to estimate overall survival (OS) at 18 months after ASCT, time of hematopoietic recovery and toxicity according to Common Terminology Criteria for Adverse Events 4.0 (CTCAE). Secondary endpoints included relapse rate calculated by time to progression (TTP) and progression free survival (PFS) at 18 months after ASCT. Four patients of control group with HL who was treated with brentuximab vedotin after ASCT were excluded from the TTP and PFS analyses. The underlying diseases in HIV-group were: HL (n=6; 60%), NHL (n=4; 40%); in control group: HL (n=29; 72.5 %), and NHL (n=11; 27.5%). HIV status in study group at the moment of transplantation showed undetectable HIV viral load (<50 copies/mL) in all patients; the median CD4+ cell number was 473 (210-715) cells/μL, and all the patients received ART.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Overall survival (OS) at 18 months after ASCT for the entire patient group (n=50) was 88%: in the HIV-group, 90% versus 87.5% in control group (p=0.605). The median terms for recovery of leukocytes, neutrophils, and platelets were D+14, D+17, D+20 in HIV-group and D+14, D+16, D+19 in control group, respectively. Toxicity rates, according to CTCAE are shown in Table 1. Relapse incidence of the underlying disease at 18 months after ASCT was 20%, with the median TTP of 3 months (2-4) in HIV-group, and 11.1% with median TTP value of 8.5 months (3-11) in control group (р=0.645). Progression-free survival at 18 months after ASCT was 76.1% (n=46): in HIV-group, 70% versus 77.8% in control group (p=0.892). There were no differences revealed in the subgroup analysis for separate HL and NHL cases.
</p>
<h2 style="text-align: justify;">
Table 1. Clinical characteristics of HIV-positive and HIV-negative groups<br>
</h2>
<img width="785" alt="52_table 1.png" src="/upload/medialibrary/ccc/52_table-1.png" height="207" title="52_table 1.png">
<h2>Conclusion</h2>
<p style="text-align: justify;">
Overall survival at 18 months after HDC followed by ASCT in patients with HIV-related lymphomas was 90%, whereas progression-free survival was 70%, the relapse incidence was 20% with median time to progression 3 months (2-4) and did not differ from the group of patients without HIV infection. We have not found any statistically significant differences between the two groups for hematopoietic recovery<br>
and toxicity rates. The obtained data confirm that ASCT is a safe and efficient procedure for HIV-related lymphomas, as well as for lymphoma patients without HIV.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
HIV-related lymphoma, HIV, autologous hematopoietic stem cell transplantation, high-dose chemotherapy, overall survival, toxicity, hematopoiesis recovery, HIV status, progression free survival.
</p>
<h2 style="text-align: justify;">References</h2>
<p style="text-align: justify;">
1. Yanik EL, Napravnik S, Cole SR, Achenbach CJ, Gopal S, Olshan A, et al. Incidence and timing of cancer in HIV-infected individuals following initiation of combination antiretroviral therapy. Clin Infect Dis. 2013; 57: 756–764.<br>
2. Krishnan A, Palmer JM, Zaia JA, Tsai NC, Alvarnas J, Forman SJ. HIV status does not affect the outcome of autologous stem cell transplantation (ASCT) for non-Hodgkin lymphoma (NHL). Biol Blood Marrow Transplantation. 2010; 16(9):1302-1308.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Infection with human immunodeficiency virus (HIV) is associated with a significantly increased risk of cancer, including Hodgkin lymphoma (HL) and non-Hodgkin lymphoma (NHL), even when patients are treated successfully with contemporary antiretroviral therapy [1]. Widespread use of the antiretroviral therapy (ART) has changed the approach to treatment of the HIV-related lymphomas, allowing the use of aggressive therapy including high-dose chemotherapy (HDC) followed by autologous hematopoietic stem cell transplantation (ASCT) [2]. The outcome of ASCT for HIV-related lymphomas is still a subject for controversy. The number of a prospective case-control studies where estimated safety and efficiency of ASCT procedure is limited.
Patients and methods
From January 2016 to March 2018, ten patients with HIV-related lymphoma who underwent HDC followed by ASCT were included into a prospective study (study HIV-infected group, n=10). To compare the efficacy and safety of the procedure, a “case-control” method (1:4) have been applied. The comparison group consisted of non-HIV-infected patients with lymphoma comparable for basic characteristics patients, who have undergone ASCT at the same period of time (control group, n=40). Median follow-up time was 8 (1- 28) months for both groups. The primary endpoint of the study was to estimate overall survival (OS) at 18 months after ASCT, time of hematopoietic recovery and toxicity according to Common Terminology Criteria for Adverse Events 4.0 (CTCAE). Secondary endpoints included relapse rate calculated by time to progression (TTP) and progression free survival (PFS) at 18 months after ASCT. Four patients of control group with HL who was treated with brentuximab vedotin after ASCT were excluded from the TTP and PFS analyses. The underlying diseases in HIV-group were: HL (n=6; 60%), NHL (n=4; 40%); in control group: HL (n=29; 72.5 %), and NHL (n=11; 27.5%). HIV status in study group at the moment of transplantation showed undetectable HIV viral load (<50 copies/mL) in all patients; the median CD4+ cell number was 473 (210-715) cells/μL, and all the patients received ART.
Results
Overall survival (OS) at 18 months after ASCT for the entire patient group (n=50) was 88%: in the HIV-group, 90% versus 87.5% in control group (p=0.605). The median terms for recovery of leukocytes, neutrophils, and platelets were D+14, D+17, D+20 in HIV-group and D+14, D+16, D+19 in control group, respectively. Toxicity rates, according to CTCAE are shown in Table 1. Relapse incidence of the underlying disease at 18 months after ASCT was 20%, with the median TTP of 3 months (2-4) in HIV-group, and 11.1% with median TTP value of 8.5 months (3-11) in control group (р=0.645). Progression-free survival at 18 months after ASCT was 76.1% (n=46): in HIV-group, 70% versus 77.8% in control group (p=0.892). There were no differences revealed in the subgroup analysis for separate HL and NHL cases.
Table 1. Clinical characteristics of HIV-positive and HIV-negative groups

Conclusion
Overall survival at 18 months after HDC followed by ASCT in patients with HIV-related lymphomas was 90%, whereas progression-free survival was 70%, the relapse incidence was 20% with median time to progression 3 months (2-4) and did not differ from the group of patients without HIV infection. We have not found any statistically significant differences between the two groups for hematopoietic recovery
and toxicity rates. The obtained data confirm that ASCT is a safe and efficient procedure for HIV-related lymphomas, as well as for lymphoma patients without HIV.
Keywords
HIV-related lymphoma, HIV, autologous hematopoietic stem cell transplantation, high-dose chemotherapy, overall survival, toxicity, hematopoiesis recovery, HIV status, progression free survival.
References
1. Yanik EL, Napravnik S, Cole SR, Achenbach CJ, Gopal S, Olshan A, et al. Incidence and timing of cancer in HIV-infected individuals following initiation of combination antiretroviral therapy. Clin Infect Dis. 2013; 57: 756–764.
2. Krishnan A, Palmer JM, Zaia JA, Tsai NC, Alvarnas J, Forman SJ. HIV status does not affect the outcome of autologous stem cell transplantation (ASCT) for non-Hodgkin lymphoma (NHL). Biol Blood Marrow Transplantation. 2010; 16(9):1302-1308.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20724
[VALUE] => High-dose chemotherapy followed by autologous hematopoietic stem cell transplantation for HIV-related lymphomas: the results of a prospective case-control study
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => High-dose chemotherapy followed by autologous hematopoietic stem cell transplantation for HIV-related lymphomas: the results of a prospective case-control study
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20831
[VALUE] => 1470
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1470
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20832
[VALUE] => 1471
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1471
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Иван В. Цыганков, Марина О. Попова, Анастасия В. Некрасова, Юлия А. Рогачева, Кирилл В. Лепик, Елена В. Кондакова, Елена И. Дарская, Лилия В. Стельмах, Юрий Р. Залялов, Вадим В. Байков, Наталья Б. Михайлова, Борис В. Афанасьев
Введение
Вирус иммунодефицита человека (ВИЧ) связан с высоким риском развития злокачественных новообразований, таких как – лимфома Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на успешное применение антиретровирусной терапии (АРВТ) [1]. Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать агрессивную терапию, включающую высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [2]. Результаты ауто-ТГСК для лечения ВИЧ-ассоциированных лимфом все еще являются предметом споров. Количество проспективных сравнительных исследований эффективности и безопасности ВДХТ с последующей ауто-ТГСК ограничено.
Пациенты и методы
В проспективное исследование включены 10 пациентов с лимфомами на фоне ВИЧ (группа исследования), которым была проведена ВДХТ с последующей ауто-ТГСК в клинике НИИ ДОГиТ в период с 2016 по 2018 год. Для сравнения эффективности и безопасности процедуры использован метод «случай-контроль» (1:4) и, в качестве группы сравнения, в исследование включены 40 пациентов без ВИЧ-инфекции, сопоставимые по основным характеристикам (контрольная группа), которым была выполнена ауто-ТГСК в тот же промежуток времени. Медиана наблюдения составила 8 (1-28) месяцев в обеих группах. Проводилась оценка острой токсичности по шкале Common Terminology Criteria for Adverse Events 4.0 (CTCAE), скорости восстановления кроветворения, а так же общей выживаемости (ОВ), выживаемости без прогрессирования (ВБП) и времени до прогрессирования (ВДП) в течение 18 месяцев после ауто-ТГСК. При исследовании ВБП и ВДП из анализа исключены 4 пациента контрольной группы с ЛХ, которые получали посттрансплантационную терапию брентуксимаб ведотином. Основными заболеваниями в группе исследования были: ЛХ п=6 (60%) и НХЛ п=4 (40%), в контрольной группе – ЛХ п=29 (72,5%) и НХЛ п=11 (27,5%). ВИЧ-статус на момент трансплантации в группе исследования: вирусная нагрузка (ПЦР-РНК ВИЧ) – <50 копий/мл; медиана уровня CD4+ клеток составила 484 (210-715) клеток/ мкл; все пациенты получали АРВТ.
Результаты
Общая выживаемость в течение 18 месяцев от ауто-ТГСК составила 88% (n=50): в группе пациентов с ВИЧ – 90%, в группе сравнения – 87,5% (р=0,605). Медиана дня восстановления лейкоцитов, нейтрофилов и тромбоцитов в группе исследования составила Д+14, Д+17, Д+20, в группе сравнения – Д+14, Д+16, Д+19, соответственно. В результате анализа токсичности по шкале СТСАЕ, частота развития энтеро-, гепато-, нефро- токсичности в обеих группах не различалась (таблица 1). Частота рецидива основного заболевания в течение 18 месяцев у пациентов с ВИЧ инфекцией составила 20%, медиана ВДП – 3 мес. (2-4), в контрольной группе – 11,1%, медиана ВДП – 8,5 мес. (3-11) (р=0,645). Выживаемость без прогрессирования в течение 18 месяцев после ауто-ТГСК составила 76,1% (n=46): в группе пациентов с ВИЧ – 70%, в группе сравнения – 77,8% (р=0,892). При анализе в подгруппах ЛХ и НХЛ различий в ОВ, ВБП и ВДП различий не обнаружено.
Заключение
Общая выживаемость в течение 18 месяцев после высокодозной химиотерапии с аутологичной трансплантацией гемопоэтических стволовых клеток у пациентов с лимфомами на фоне ВИЧ составила 90%, и не отличалась от контрольной группы. Показатели выживаемости без прогрессирования у пациентов с ВИЧ и частоты рецидивов составили 70% и 20% соответственно, и не отличались от группы пациентов без ВИЧ. Восстановление кроветворения и спектр токсичности не различались в группах сравнения. Полученные данные подтверждают, что высокодозная химиотерапия с ауто-ТГСК такая же эффективная и безопасная процедура у пациентов с ВИЧ-ассоциированными лимфомами, как и у пациентов с лимфомами без ВИЧ.
Ключевые слова
ВИЧ-ассоциированные лимфомы, ВИЧ, аутологичная трансплантация гемопоэтическх стволовых клеток, высокодозная химиотерапия, общая выживаемость, токсичность, восстановление гемопоэза, ВИЧ-статус, выживаемость без прогрессирования.
Литература
1. Yanik EL, Napravnik S, Cole SR, Achenbach CJ, Gopal S, Olshan A, et al. Incidence and timing of cancer in HIV-infected individuals following initiation of combination antiretroviral therapy. Clin Infect Dis. 2013;57:756–764.
2. Krishnan A, Palmer JM, Zaia JA, Tsai NC, Alvarnas J, Forman SJ. HIV status does not affect the outcome of autologous stem cell transplantation (ASCT) for non-Hodgkin lymphoma (NHL). Biol Blood Marrow Transplantation. 2010;16(9):1302-1308.
Таблица 1. Клинические характеристики ВИЧ-инфицированной и контрольной групп пациентов

Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20704
[VALUE] => Array
(
[TEXT] => Любовь А. Цветкова, Олеся В. Паина, Инна В. Маркова, Полина В. Кожокарь, Сергей Н. Бондаренко, Ильдар М. Бархатов, Елена В. Бабенко, Александр Л. Алянский, Кирилл А. Екушев, Татьяна Л. Гиндина, Елена В. Семенова, Людмила С. Зубаровская, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Любовь А. Цветкова, Олеся В. Паина, Инна В. Маркова, Полина В. Кожокарь, Сергей Н. Бондаренко, Ильдар М. Бархатов, Елена В. Бабенко, Александр Л. Алянский, Кирилл А. Екушев, Татьяна Л. Гиндина, Елена В. Семенова, Людмила С. Зубаровская, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20705
[VALUE] => Array
(
[TEXT] => Научно-исследовательский институт детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой; Первый Санкт-Петербургский государственный медицинский университет имени академика И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Научно-исследовательский институт детской онкологии, гематологии и трансплантологии имени Р. М. Горбачевой; Первый Санкт-Петербургский государственный медицинский университет имени академика И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20706
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Аллогенная трансплантация гемопоэтических столовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелоидным лейкозом группы высокого риска (ОМЛ). Возникновение рецидива после алло-ТГСК происходит примерно у 20-50% пациентов в зависимости от стадии заболевания на момент трансплантации и отрицательных прогностических факторов. Одним из предикторов рецидива при ОМЛ может быть минимальная остаточная болезнь (МОБ), определяемая с помощью проточной цитофлюорометрии или полимеразной цепной реакции. Опубликованные исследования демонстрируют высокую прогностическую значимость определения МОБ непосредственно перед проведением алло-ТГСК у взрослых пациентов. Однако у детей с ОМЛ данные о влиянии МОБ перед алло-ТГСК на эффективность лечения ограничены. Целью данного исследования стала оценка влияния МОБ перед алло-ТГСК на общую выживаемость (ОВ), бессобытийную выживаемость (БСВ), безрецидивную выживаемость (БРВ), трансплантационную летальность, кумулятивную частоту рецидива (ЧР) и частоту первичного неприживления у детей и подростков с ОМЛ.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
С 2008-2018 гг. в клинике НИИ ДОГиТ им. Р. М. Горбачевой алло-ТГСК проведена 95 детям с ОМЛ в клинико-гематологической ремиссии заболевания заболевания. Большинство пациентов получили первичную химиотерапию по протоколу AML-BFM 2004. Для установления группы цитогенетического риска были использованы WHO критерии 2008 г. (пересмотр 2016 г.). Перед алло-ТГСК всем пациентам выполнялась аспирация/биопсия костного мозга для рестадирования. Среди этих пациентов у 79 проводилось определение МОБ с помощью молекулярно-генетического/цитогенетического исследований и/или метода иммунофенотипирования. Таким образом, 79 пациентов с медианой возраста 10 лет (1-18) на момент алло-ТГСК были включены в данное ретроспективное исследование. Все пациенты были поделены на 2 группы: 1 гр. – МОБ+ n=33 (42%), 2 гр. – МОБ– n=46 (58%). В первой ремиссии алло-ТГСК была выполнена 23 (70%) МОБ+ пациентам и 35 (76%) МОБ– пациентам. Высокий цитогенетический риск инициально наблюдался у 14/30 (46%) МОБ+ пациентов и у 16/40 (40%) МОБ– пациентов (p=0,7). В каждой группе наблюдалось равное число вторичных ОМЛ (n=4; 12% и n=4; 8% соответственно, p=0,7), а также ОМЛ с экстрамедуллярным поражением (n=6; 18% и n=6; 13% соответственно, p=0,5). В той и другой группе применялись различные по интенсивности режимы кондиционирования в равных пропорциях (РИК/МАК): в 1 гр. – 18/15 (1,2), во 2 гр. – 25/21 (1,2). ОВ, БСВ, БРВ, а также летальность, обусловленная терапией, были рассчитаны, используя метод Каплана-Майера. При определении БСВ за событие был принят рецидив лейкоза или смерть. Кумулятивная частота рецидива и первичного отторжения трансплантата установлены с помощью критерия Манна-Уитни.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Приживление ГСК было зафиксировано у 71 (90%) пациента. Частота первичного неприживления в обеих группах была одинаковая (n=4; 12% и n=4; 8% соответственно, р=0,6). При медиане наблюдения 3 года ОВ составила 63,6% в группе МОБ+ и 69,6% в группе МОБ–(p=0,7). БСВ при данной медиане равна 45,5% у МОБ+ пациентов, 65,2% у МОБ– (p=0,1). Трехгодичная частота рецидива была достоверно выше у МОБ+ пациентов (n=14), чем у МОБ– (n=8) пациентов (42% и 17% соответственно, p=0,01). БРВ также достоверно различалась у пациентов с различным МОБ статусом (57,6% у МОБ+, 82,6% у МОБ–, р=0,02). Трансплантационная летальность составила 15,2% и 17,4% в 1-й и 2-й группах соответственно (p=0,6). Резистентный рецидив ОМЛ после алло-ТГСК был причиной смерти у 13/26 (50%) пациентов, среди них 7 МОБ+ пациентов, 6 МОБ– пациентов. Профилактическая/превентивная терапия гипометилирующими агентами ± инфузия донорских лимфоцитов (ИДЛ) была проведена 9 (27%) МОБ+ пациентам и 5 МОБ– (10%) пациентам. Рецидив после проведенной терапии произошел только у одного пациента из группы МОБ+.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Данное исследование демонстрирует, что наличие предтрансплантационной МОБ у детей и подростков с ОМЛ ассоциировано с повышенным риском возникновения рецидива после алло-ТГСК (различие в ЧР, p= 0,01 и БРВ, р=0,02). При этом БСВ и ОВ достоверно не различались в обеих группах (р=0,7 и р=0,1, соответственно), так как рецидив не оказал решающего значения на данные показатели.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Острый миелоидный лейкоз, минимальная остаточная болезнь, алло-ТГСК,
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Аллогенная трансплантация гемопоэтических столовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелоидным лейкозом группы высокого риска (ОМЛ). Возникновение рецидива после алло-ТГСК происходит примерно у 20-50% пациентов в зависимости от стадии заболевания на момент трансплантации и отрицательных прогностических факторов. Одним из предикторов рецидива при ОМЛ может быть минимальная остаточная болезнь (МОБ), определяемая с помощью проточной цитофлюорометрии или полимеразной цепной реакции. Опубликованные исследования демонстрируют высокую прогностическую значимость определения МОБ непосредственно перед проведением алло-ТГСК у взрослых пациентов. Однако у детей с ОМЛ данные о влиянии МОБ перед алло-ТГСК на эффективность лечения ограничены. Целью данного исследования стала оценка влияния МОБ перед алло-ТГСК на общую выживаемость (ОВ), бессобытийную выживаемость (БСВ), безрецидивную выживаемость (БРВ), трансплантационную летальность, кумулятивную частоту рецидива (ЧР) и частоту первичного неприживления у детей и подростков с ОМЛ.
Материалы и методы
С 2008-2018 гг. в клинике НИИ ДОГиТ им. Р. М. Горбачевой алло-ТГСК проведена 95 детям с ОМЛ в клинико-гематологической ремиссии заболевания заболевания. Большинство пациентов получили первичную химиотерапию по протоколу AML-BFM 2004. Для установления группы цитогенетического риска были использованы WHO критерии 2008 г. (пересмотр 2016 г.). Перед алло-ТГСК всем пациентам выполнялась аспирация/биопсия костного мозга для рестадирования. Среди этих пациентов у 79 проводилось определение МОБ с помощью молекулярно-генетического/цитогенетического исследований и/или метода иммунофенотипирования. Таким образом, 79 пациентов с медианой возраста 10 лет (1-18) на момент алло-ТГСК были включены в данное ретроспективное исследование. Все пациенты были поделены на 2 группы: 1 гр. – МОБ+ n=33 (42%), 2 гр. – МОБ– n=46 (58%). В первой ремиссии алло-ТГСК была выполнена 23 (70%) МОБ+ пациентам и 35 (76%) МОБ– пациентам. Высокий цитогенетический риск инициально наблюдался у 14/30 (46%) МОБ+ пациентов и у 16/40 (40%) МОБ– пациентов (p=0,7). В каждой группе наблюдалось равное число вторичных ОМЛ (n=4; 12% и n=4; 8% соответственно, p=0,7), а также ОМЛ с экстрамедуллярным поражением (n=6; 18% и n=6; 13% соответственно, p=0,5). В той и другой группе применялись различные по интенсивности режимы кондиционирования в равных пропорциях (РИК/МАК): в 1 гр. – 18/15 (1,2), во 2 гр. – 25/21 (1,2). ОВ, БСВ, БРВ, а также летальность, обусловленная терапией, были рассчитаны, используя метод Каплана-Майера. При определении БСВ за событие был принят рецидив лейкоза или смерть. Кумулятивная частота рецидива и первичного отторжения трансплантата установлены с помощью критерия Манна-Уитни.
Результаты
Приживление ГСК было зафиксировано у 71 (90%) пациента. Частота первичного неприживления в обеих группах была одинаковая (n=4; 12% и n=4; 8% соответственно, р=0,6). При медиане наблюдения 3 года ОВ составила 63,6% в группе МОБ+ и 69,6% в группе МОБ–(p=0,7). БСВ при данной медиане равна 45,5% у МОБ+ пациентов, 65,2% у МОБ– (p=0,1). Трехгодичная частота рецидива была достоверно выше у МОБ+ пациентов (n=14), чем у МОБ– (n=8) пациентов (42% и 17% соответственно, p=0,01). БРВ также достоверно различалась у пациентов с различным МОБ статусом (57,6% у МОБ+, 82,6% у МОБ–, р=0,02). Трансплантационная летальность составила 15,2% и 17,4% в 1-й и 2-й группах соответственно (p=0,6). Резистентный рецидив ОМЛ после алло-ТГСК был причиной смерти у 13/26 (50%) пациентов, среди них 7 МОБ+ пациентов, 6 МОБ– пациентов. Профилактическая/превентивная терапия гипометилирующими агентами ± инфузия донорских лимфоцитов (ИДЛ) была проведена 9 (27%) МОБ+ пациентам и 5 МОБ– (10%) пациентам. Рецидив после проведенной терапии произошел только у одного пациента из группы МОБ+.
Заключение
Данное исследование демонстрирует, что наличие предтрансплантационной МОБ у детей и подростков с ОМЛ ассоциировано с повышенным риском возникновения рецидива после алло-ТГСК (различие в ЧР, p= 0,01 и БРВ, р=0,02). При этом БСВ и ОВ достоверно не различались в обеих группах (р=0,7 и р=0,1, соответственно), так как рецидив не оказал решающего значения на данные показатели.
Ключевые слова
Острый миелоидный лейкоз, минимальная остаточная болезнь, алло-ТГСК,
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20707
[VALUE] => Array
(
[TEXT] => Liubov A. Tsvetkova, Olesya V. Paina, Inna V. Markova, Polina V. Kozhokar’, Sergey N. Bondarenko, Ildar M. Barkhatov, Elena V. Babenko, Alexander L. Alyanskiy, Kirill A. Ekushev, Tatyana L. Gindina, Elena V. Semenova, Ludmila S. Zubarovskaya, Boris V. Afanasyev
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Liubov A. Tsvetkova, Olesya V. Paina, Inna V. Markova, Polina V. Kozhokar’, Sergey N. Bondarenko, Ildar M. Barkhatov, Elena V. Babenko, Alexander L. Alyanskiy, Kirill A. Ekushev, Tatyana L. Gindina, Elena V. Semenova, Ludmila S. Zubarovskaya, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20708
[VALUE] => Array
(
[TEXT] => R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, I. P. Pavlov First Saint-Petersburg State Medical University, Saint-Petersburg, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, I. P. Pavlov First Saint-Petersburg State Medical University, Saint-Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20709
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Background</h2>
<p style="text-align: justify;">
Allogeneic haemopoietic stem cell transplantation (allo-HSCT) – is an effective option in the treatment of high risk patients with acute myeloid leukemia (AML). The relapse after allo-HSCT occurs in about 20-50% of patients, depending on status of the disease and negative prognostic factors. Minimal residual disease (MRD) is a powerful and independent predictor of subsequent relapse, which is detected using polymerase chain reactions or multiparametric flow cytometry. Presented clinical data demonstrated the high prognostic significance of the measured MRD in adults before allo-HSCT. However, impact of pre-transplantation MRD status in children and adolescents with AML is not well elucidated. The goal of this study was to evaluate the impact of pre-transplantation MRD on overall survival (OS), event-free survival (EFS), transplant-related mortality (TRM), relapse-free survival (RFS), relapse incidence (RI) and primary graft failure in transplantation in children and adolescents with AML.
</p>
<h2 style="text-align: justify;">Materials and methods</h2>
<p style="text-align: justify;">
From 2008 to 2018 a total of 95 AML pediatric patients of R. M. Gorbacheva Memorial Institute received allo-HSCT in complete clinical-hematological remission. Most of the patients received AML-BFM 2004 as primary treatment. We used WHO 2008 criteria (review 2016) to assign cytogenetic risk. All subsequent patients eligible for this study underwent bone marrow (BM) aspiration or biopsy prior to allo-HSCT. Among these patients, 79 were assessed for MRD before HSCT and were considered in this retrospective analysis. MRD was examined with immunophenotyping or polymerase chain reaction/ cytogenetic. The median age was 10 years (1-18). Patients were divided into 2 groups: 1 group – MRD-positive n=33 (42%), 2 group – MRD-negative n=46 (58%). Allo-HSCT was performed in first remission in 23 (70%) MRD-positive patients and 35 (76%) MRD-negative patients. High cytogenetic risk accounted for 14/30 (46%) MRD-positive and 16/40 (40%) MRD-negative patients (p=0.7). Equal number of secondary (n=4; 12% and n=4; 8%, respectively, p=0.7) AML, and also extramedullary (n=6; 18% and n=6; 13%, respectively, p=0.5) disease were observed in both groups. Different in intensity regimes of conditioning were used in equal proportions in both groups (RIC/MAC): 18/15 (1.2) in MRD-positive patients, 25/21 (1.2) in MRD-negative patients. Probabilities of OS, EFS, RFS, TRM were estimated by using the Kaplan-Meier method. Relapse of leukemia and death was accepted as event in EFS. Cumulative RI and primary graft failure – by using Mann-Whitney U-test.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Transplant engraftment was identified in 71 (90%) of patients. Graft failure occurs in the 4 patients of each group (12% for MRD-positive и 8% for MRD-negative. P=0.6). At the median follow up 3 years OS were 63,6% for MRD-positive and 69,6% for MRD-negative patients (p=0,7); the 3-year EFS were 45,5% and 65,2% respectively (p=0,1). The cumulative RI was higher for MRD-positive (n=14) than for patients MRD-negative (n=8) patients (42% and 17% respectively; p=0,01). RFS were also different in the both groups (57,6% and 82.6%; р=0.02). TRM were similar for MRD-positive patients compared with MRD-negative patients (15.2% and 17.4% respectively; p=0.6). Resistant relapse was the reason of death in 13/26 (50%) patients. Nine (27%) MRD-positive and 5 MRD-negative (10%) patient were treated with prophylactic/preventive hypomethylating agent ± IDL in posttransplantation period. One MRD-positive patient experienced a relapse after epigenetic therapy.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
These data demonstrated, that pre-transplantation MRD is associated with increased risk of relapse in children and adolescents with AML (RI-p=0.01; RFS- p=0.02). MRD-positive patients had similar OS (p=0.7), EFS (p=0.1) to patients with MRD-negative status, because relapse had not decisive role for survival.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Acute myeloid leukemia, minimal residual disease, allo-HSCT, children.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Background
Allogeneic haemopoietic stem cell transplantation (allo-HSCT) – is an effective option in the treatment of high risk patients with acute myeloid leukemia (AML). The relapse after allo-HSCT occurs in about 20-50% of patients, depending on status of the disease and negative prognostic factors. Minimal residual disease (MRD) is a powerful and independent predictor of subsequent relapse, which is detected using polymerase chain reactions or multiparametric flow cytometry. Presented clinical data demonstrated the high prognostic significance of the measured MRD in adults before allo-HSCT. However, impact of pre-transplantation MRD status in children and adolescents with AML is not well elucidated. The goal of this study was to evaluate the impact of pre-transplantation MRD on overall survival (OS), event-free survival (EFS), transplant-related mortality (TRM), relapse-free survival (RFS), relapse incidence (RI) and primary graft failure in transplantation in children and adolescents with AML.
Materials and methods
From 2008 to 2018 a total of 95 AML pediatric patients of R. M. Gorbacheva Memorial Institute received allo-HSCT in complete clinical-hematological remission. Most of the patients received AML-BFM 2004 as primary treatment. We used WHO 2008 criteria (review 2016) to assign cytogenetic risk. All subsequent patients eligible for this study underwent bone marrow (BM) aspiration or biopsy prior to allo-HSCT. Among these patients, 79 were assessed for MRD before HSCT and were considered in this retrospective analysis. MRD was examined with immunophenotyping or polymerase chain reaction/ cytogenetic. The median age was 10 years (1-18). Patients were divided into 2 groups: 1 group – MRD-positive n=33 (42%), 2 group – MRD-negative n=46 (58%). Allo-HSCT was performed in first remission in 23 (70%) MRD-positive patients and 35 (76%) MRD-negative patients. High cytogenetic risk accounted for 14/30 (46%) MRD-positive and 16/40 (40%) MRD-negative patients (p=0.7). Equal number of secondary (n=4; 12% and n=4; 8%, respectively, p=0.7) AML, and also extramedullary (n=6; 18% and n=6; 13%, respectively, p=0.5) disease were observed in both groups. Different in intensity regimes of conditioning were used in equal proportions in both groups (RIC/MAC): 18/15 (1.2) in MRD-positive patients, 25/21 (1.2) in MRD-negative patients. Probabilities of OS, EFS, RFS, TRM were estimated by using the Kaplan-Meier method. Relapse of leukemia and death was accepted as event in EFS. Cumulative RI and primary graft failure – by using Mann-Whitney U-test.
Results
Transplant engraftment was identified in 71 (90%) of patients. Graft failure occurs in the 4 patients of each group (12% for MRD-positive и 8% for MRD-negative. P=0.6). At the median follow up 3 years OS were 63,6% for MRD-positive and 69,6% for MRD-negative patients (p=0,7); the 3-year EFS were 45,5% and 65,2% respectively (p=0,1). The cumulative RI was higher for MRD-positive (n=14) than for patients MRD-negative (n=8) patients (42% and 17% respectively; p=0,01). RFS were also different in the both groups (57,6% and 82.6%; р=0.02). TRM were similar for MRD-positive patients compared with MRD-negative patients (15.2% and 17.4% respectively; p=0.6). Resistant relapse was the reason of death in 13/26 (50%) patients. Nine (27%) MRD-positive and 5 MRD-negative (10%) patient were treated with prophylactic/preventive hypomethylating agent ± IDL in posttransplantation period. One MRD-positive patient experienced a relapse after epigenetic therapy.
Conclusion
These data demonstrated, that pre-transplantation MRD is associated with increased risk of relapse in children and adolescents with AML (RI-p=0.01; RFS- p=0.02). MRD-positive patients had similar OS (p=0.7), EFS (p=0.1) to patients with MRD-negative status, because relapse had not decisive role for survival.
Keywords
Acute myeloid leukemia, minimal residual disease, allo-HSCT, children.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20710
[VALUE] => Predictive value of minimal residual disease befor allo-HSCT in children and adolescents with high-risk acute myeloid leukemia
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Predictive value of minimal residual disease befor allo-HSCT in children and adolescents with high-risk acute myeloid leukemia
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20829
[VALUE] => 1468
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1468
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20830
[VALUE] => 1469
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1469
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Любовь А. Цветкова, Олеся В. Паина, Инна В. Маркова, Полина В. Кожокарь, Сергей Н. Бондаренко, Ильдар М. Бархатов, Елена В. Бабенко, Александр Л. Алянский, Кирилл А. Екушев, Татьяна Л. Гиндина, Елена В. Семенова, Людмила С. Зубаровская, Борис В. Афанасьев
Введение
Аллогенная трансплантация гемопоэтических столовых клеток (алло-ТГСК) – эффективный метод лечения пациентов с острым миелоидным лейкозом группы высокого риска (ОМЛ). Возникновение рецидива после алло-ТГСК происходит примерно у 20-50% пациентов в зависимости от стадии заболевания на момент трансплантации и отрицательных прогностических факторов. Одним из предикторов рецидива при ОМЛ может быть минимальная остаточная болезнь (МОБ), определяемая с помощью проточной цитофлюорометрии или полимеразной цепной реакции. Опубликованные исследования демонстрируют высокую прогностическую значимость определения МОБ непосредственно перед проведением алло-ТГСК у взрослых пациентов. Однако у детей с ОМЛ данные о влиянии МОБ перед алло-ТГСК на эффективность лечения ограничены. Целью данного исследования стала оценка влияния МОБ перед алло-ТГСК на общую выживаемость (ОВ), бессобытийную выживаемость (БСВ), безрецидивную выживаемость (БРВ), трансплантационную летальность, кумулятивную частоту рецидива (ЧР) и частоту первичного неприживления у детей и подростков с ОМЛ.
Материалы и методы
С 2008-2018 гг. в клинике НИИ ДОГиТ им. Р. М. Горбачевой алло-ТГСК проведена 95 детям с ОМЛ в клинико-гематологической ремиссии заболевания заболевания. Большинство пациентов получили первичную химиотерапию по протоколу AML-BFM 2004. Для установления группы цитогенетического риска были использованы WHO критерии 2008 г. (пересмотр 2016 г.). Перед алло-ТГСК всем пациентам выполнялась аспирация/биопсия костного мозга для рестадирования. Среди этих пациентов у 79 проводилось определение МОБ с помощью молекулярно-генетического/цитогенетического исследований и/или метода иммунофенотипирования. Таким образом, 79 пациентов с медианой возраста 10 лет (1-18) на момент алло-ТГСК были включены в данное ретроспективное исследование. Все пациенты были поделены на 2 группы: 1 гр. – МОБ+ n=33 (42%), 2 гр. – МОБ– n=46 (58%). В первой ремиссии алло-ТГСК была выполнена 23 (70%) МОБ+ пациентам и 35 (76%) МОБ– пациентам. Высокий цитогенетический риск инициально наблюдался у 14/30 (46%) МОБ+ пациентов и у 16/40 (40%) МОБ– пациентов (p=0,7). В каждой группе наблюдалось равное число вторичных ОМЛ (n=4; 12% и n=4; 8% соответственно, p=0,7), а также ОМЛ с экстрамедуллярным поражением (n=6; 18% и n=6; 13% соответственно, p=0,5). В той и другой группе применялись различные по интенсивности режимы кондиционирования в равных пропорциях (РИК/МАК): в 1 гр. – 18/15 (1,2), во 2 гр. – 25/21 (1,2). ОВ, БСВ, БРВ, а также летальность, обусловленная терапией, были рассчитаны, используя метод Каплана-Майера. При определении БСВ за событие был принят рецидив лейкоза или смерть. Кумулятивная частота рецидива и первичного отторжения трансплантата установлены с помощью критерия Манна-Уитни.
Результаты
Приживление ГСК было зафиксировано у 71 (90%) пациента. Частота первичного неприживления в обеих группах была одинаковая (n=4; 12% и n=4; 8% соответственно, р=0,6). При медиане наблюдения 3 года ОВ составила 63,6% в группе МОБ+ и 69,6% в группе МОБ–(p=0,7). БСВ при данной медиане равна 45,5% у МОБ+ пациентов, 65,2% у МОБ– (p=0,1). Трехгодичная частота рецидива была достоверно выше у МОБ+ пациентов (n=14), чем у МОБ– (n=8) пациентов (42% и 17% соответственно, p=0,01). БРВ также достоверно различалась у пациентов с различным МОБ статусом (57,6% у МОБ+, 82,6% у МОБ–, р=0,02). Трансплантационная летальность составила 15,2% и 17,4% в 1-й и 2-й группах соответственно (p=0,6). Резистентный рецидив ОМЛ после алло-ТГСК был причиной смерти у 13/26 (50%) пациентов, среди них 7 МОБ+ пациентов, 6 МОБ– пациентов. Профилактическая/превентивная терапия гипометилирующими агентами ± инфузия донорских лимфоцитов (ИДЛ) была проведена 9 (27%) МОБ+ пациентам и 5 МОБ– (10%) пациентам. Рецидив после проведенной терапии произошел только у одного пациента из группы МОБ+.
Заключение
Данное исследование демонстрирует, что наличие предтрансплантационной МОБ у детей и подростков с ОМЛ ассоциировано с повышенным риском возникновения рецидива после алло-ТГСК (различие в ЧР, p= 0,01 и БРВ, р=0,02). При этом БСВ и ОВ достоверно не различались в обеих группах (р=0,7 и р=0,1, соответственно), так как рецидив не оказал решающего значения на данные показатели.
Ключевые слова
Острый миелоидный лейкоз, минимальная остаточная болезнь, алло-ТГСК,
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20697
[VALUE] => Array
(
[TEXT] => Александр С. Тимин <sup>1</sup>,<sup>2</sup>, Альберт Р. Муслимов <sup>1</sup>, Алексей А. Пельтек <sup>3</sup>, Михаил В. Зюзин <sup>4</sup>, Ольга С. Епифановская <sup>1</sup>, Владислав С. Сергеев <sup>1</sup>, Анна А. Доценко <sup>1</sup>, Тимофей Е. Карпов <sup>3</sup>, Игорь С. Сергеев <sup>3</sup>, Александр А. Гончаренко <sup>3</sup>, Яна В. Тараканчикова <sup>5</sup>, Кирилл В. Лепик <sup>1</sup>, Глеб Б. Сухоруков <sup>3</sup>, Борис В. Афанасьев <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Александр С. Тимин 1,2, Альберт Р. Муслимов 1, Алексей А. Пельтек 3, Михаил В. Зюзин 4, Ольга С. Епифановская 1, Владислав С. Сергеев 1, Анна А. Доценко 1, Тимофей Е. Карпов 3, Игорь С. Сергеев 3, Александр А. Гончаренко 3, Яна В. Тараканчикова 5, Кирилл В. Лепик 1, Глеб Б. Сухоруков 3, Борис В. Афанасьев 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20698
[VALUE] => Array
(
[TEXT] => <sup>1</sup> Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
<sup>2</sup> Томский политехнический университет, Томск, Россия
<sup>3</sup> Санкт-Петербургский Политехнический Университет Петра Великого, Санкт-Петербург, Россия
<sup>4</sup> Санкт-Петербургский Национальный Исследовательский Университет ИТМО, Санкт-Петербург, Россия
<sup>5</sup> Санкт-Петербургский Национальный Исследовательский Академический Университет, Санкт-Петербург, Россия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
2 Томский политехнический университет, Томск, Россия
3 Санкт-Петербургский Политехнический Университет Петра Великого, Санкт-Петербург, Россия
4 Санкт-Петербургский Национальный Исследовательский Университет ИТМО, Санкт-Петербург, Россия
5 Санкт-Петербургский Национальный Исследовательский Академический Университет, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20699
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Цель данной работы состояла в исследовании возможностей применения мультипотентных мезенхимальных стромальных клеток (ММСК) в качестве платформы для доставки препаратов, заключенных в гибридные полимерные микрокапсулы. ММСК являются высокопотенциальной клеточной популяцией, которая за счет феномена патотропизма может решить проблему таргетной доставки препарата, выступая в качестве носителя. Таким образом, объединение биологического феномена миграции клеток и высокой загружающей способности полимерных капсул обеспечит возможность контролировать направленность действия и позволит выполнить таргетную доставку вещества без внешнего и внутреннего воздействия для клеток-носителей. Для отработки методики, доксорубицин и винкристин были отобраны, в качестве противоопухолевых препаратов с дозозависимым эффектом, которые включены в состав многих схем полихимиотерапии.
</p>
<h2 style="text-align: justify;">Методы</h2>
<p style="text-align: justify;">
В ходе данного исследования был произведен синтез гибридных микрокапсул различных размеров (5 мкм, 1 мкм, 0,5 мкм) при помощи технологии Layer-by- Layer (Polyarginine/Dextran sulfate) и золь-гель синтеза (Tetraethyl orthosilicate). Данные микроконтейнеры обладают низкой токсичностью, высокой биосовместимостью, а также способны защитить клетку от инкапсулированных препаратов. На следующем этапе была выполнена оценка ассоциации клеток с капсулами различных размеров при помощи проточной цитометрии и лазерной сканирующей конфокальной микроскопии для определения оптимального соотношения капсул и клеток. Спонтанная миграция МСК, и влияние на нее ассоциированных с клетками капсул различных размеров была исследована при помощи системы наблюдения за живыми клетками в культуре Cell-IQ. На завершающем этапе работы была изучена способность ММСК к направленной миграции по градиенту концентрации SDF-1. Для качественной и количественной оценки миграции были использованы Transwell, μ-Slide Chemotaxis, а также была исследована способность ММСК к миграции в коллагеновом геле в сторону сфероидов из раковых клеток, синтезирующих SDF-1, и их способность проникать внутрь конгломерата клеток.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Полученные результаты показывают, что МСК клетки способны захватывать более 10 капсул, содержащие противоопухолевые препараты – доксорубицин, винкристин. По экспериментальным данным проточной цитометрии показано, что 90 % клеток способны интернализировать капсулы с высокой эффективностью. Уникальная структура капсул предотвращает высвобождение противоопухолевых препаратов в течение 72 часов. Показано, что большая часть клеток способны направлено переносить капсулы по SDF-1 градиенту и в очаг опухолевого сфероида.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Таким образом, показано, что МСК с включенными капсулами, содержащие противоопухолевые препараты, могут выступать в качестве новой лекарственной формы для направленной доставки противоопухолевых препаратов в очаг опухолей.</p>
<h2>Благодарности</h2>
<p style="text-align: justify;"> Работа выполнена при поддержке Российского Фонда Фундаментальных исследований (грант № 18-015-00100).
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Таргетная доставка, микро- и нанокапсулы, противоо пухолевые препараты, интернализация, мезенхимные стромальные клетки, миграция, фармакокинетика, синтез, культивирование, клетки-носители.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Цель данной работы состояла в исследовании возможностей применения мультипотентных мезенхимальных стромальных клеток (ММСК) в качестве платформы для доставки препаратов, заключенных в гибридные полимерные микрокапсулы. ММСК являются высокопотенциальной клеточной популяцией, которая за счет феномена патотропизма может решить проблему таргетной доставки препарата, выступая в качестве носителя. Таким образом, объединение биологического феномена миграции клеток и высокой загружающей способности полимерных капсул обеспечит возможность контролировать направленность действия и позволит выполнить таргетную доставку вещества без внешнего и внутреннего воздействия для клеток-носителей. Для отработки методики, доксорубицин и винкристин были отобраны, в качестве противоопухолевых препаратов с дозозависимым эффектом, которые включены в состав многих схем полихимиотерапии.
Методы
В ходе данного исследования был произведен синтез гибридных микрокапсул различных размеров (5 мкм, 1 мкм, 0,5 мкм) при помощи технологии Layer-by- Layer (Polyarginine/Dextran sulfate) и золь-гель синтеза (Tetraethyl orthosilicate). Данные микроконтейнеры обладают низкой токсичностью, высокой биосовместимостью, а также способны защитить клетку от инкапсулированных препаратов. На следующем этапе была выполнена оценка ассоциации клеток с капсулами различных размеров при помощи проточной цитометрии и лазерной сканирующей конфокальной микроскопии для определения оптимального соотношения капсул и клеток. Спонтанная миграция МСК, и влияние на нее ассоциированных с клетками капсул различных размеров была исследована при помощи системы наблюдения за живыми клетками в культуре Cell-IQ. На завершающем этапе работы была изучена способность ММСК к направленной миграции по градиенту концентрации SDF-1. Для качественной и количественной оценки миграции были использованы Transwell, μ-Slide Chemotaxis, а также была исследована способность ММСК к миграции в коллагеновом геле в сторону сфероидов из раковых клеток, синтезирующих SDF-1, и их способность проникать внутрь конгломерата клеток.
Результаты
Полученные результаты показывают, что МСК клетки способны захватывать более 10 капсул, содержащие противоопухолевые препараты – доксорубицин, винкристин. По экспериментальным данным проточной цитометрии показано, что 90 % клеток способны интернализировать капсулы с высокой эффективностью. Уникальная структура капсул предотвращает высвобождение противоопухолевых препаратов в течение 72 часов. Показано, что большая часть клеток способны направлено переносить капсулы по SDF-1 градиенту и в очаг опухолевого сфероида.
Заключение
Таким образом, показано, что МСК с включенными капсулами, содержащие противоопухолевые препараты, могут выступать в качестве новой лекарственной формы для направленной доставки противоопухолевых препаратов в очаг опухолей.
Благодарности
Работа выполнена при поддержке Российского Фонда Фундаментальных исследований (грант № 18-015-00100).
Ключевые слова
Таргетная доставка, микро- и нанокапсулы, противоо пухолевые препараты, интернализация, мезенхимные стромальные клетки, миграция, фармакокинетика, синтез, культивирование, клетки-носители.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20700
[VALUE] => Array
(
[TEXT] => Alexander S. Timin <sup>1</sup>,<sup>2</sup>, Albert R. Muslimov <sup>1</sup>, Oleksii O. Peltek <sup>3</sup>, Mikhail V. Zyuzin <sup>4</sup>, Olga S. Epifanovskaya <sup>1</sup>, Vladislav S. Sergeev <sup>1</sup>, Anna A. Dotsenko <sup>1</sup>, Timofey E. Karpov <sup>3</sup>, Igor S. Sergeev <sup>3</sup>, Alexander A. Goncharenko <sup>3</sup>, Yana V. Tarakanchikova <sup>5</sup>, Kirill V. Lepik <sup>1</sup>, Gleb B. Sukhorukov <sup>3</sup>, Boris V. Afanasyev <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Alexander S. Timin 1,2, Albert R. Muslimov 1, Oleksii O. Peltek 3, Mikhail V. Zyuzin 4, Olga S. Epifanovskaya 1, Vladislav S. Sergeev 1, Anna A. Dotsenko 1, Timofey E. Karpov 3, Igor S. Sergeev 3, Alexander A. Goncharenko 3, Yana V. Tarakanchikova 5, Kirill V. Lepik 1, Gleb B. Sukhorukov 3, Boris V. Afanasyev 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20701
[VALUE] => Array
(
[TEXT] => <sup>1</sup> First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
<sup>2</sup> Tomsk Polytechnic University, Tomsk, Russian Federation
<sup>3</sup> Peter The Great St. Petersburg Polytechnic University, St. Petersburg, Russian Federation
<sup>4</sup> Department of Nanophotonics and Metamaterials, ITMO University, St. Petersburg, Russian Federation
<sup>5</sup> St. Petersburg Academic University, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
2 Tomsk Polytechnic University, Tomsk, Russian Federation
3 Peter The Great St. Petersburg Polytechnic University, St. Petersburg, Russian Federation
4 Department of Nanophotonics and Metamaterials, ITMO University, St. Petersburg, Russian Federation
5 St. Petersburg Academic University, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20702
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction and goals</h2>
<p style="text-align: justify;">
The aim of this work is to investigate the possibilities of usage of multipotent mesenchymal stromal cells (MMSC) as a platform for delivering drugs which are contained in hybrid polymeric microcapsules. MMSCs are a cell population with high potential which due to the phenomenon of pathotropism can solve the problem of target drug delivery by acting as a carrier. Thus, combination of the biological phenomenon of cell migration and the high loading capacity of polymer capsules will allow targeted delivery of a substance without external and internal effect on carrier cells. To test the technique, doxorubicin and vincristine were selected as antitumor drugs with a dose-dependent effect, which are included in many polychemotherapy regimens.
</p>
<h2 style="text-align: justify;">Methods</h2>
<p style="text-align: justify;">
In this study, hybrid microcapsules of various sizes (5 μm, 1 μm, 0.5 μm) were synthesized using Layer-by-Layer technique (Polyarginine/Dextran sulfate) and sol-gel synthesis (Tetraethyl orthosilicate). These micro containers have low toxicity, high biocompatibility, and are also capable of protecting the cell from encapsulated drugs. The association of cells with capsules of various sizes was evaluated using flow cytometry and laser scanning confocal microscopy in order to determine the optimal ratio of capsules and cells. The effect of capsules of various sizes associated with cells on spontaneous migration of MSCs, was examined using a cell-IQ cell culture monitoring system. The ability of MMSC to direct migration through the concentration gradient of SDF-1 was studied. For qualitative and quantitative assessment of migration, Transwell, μ-Slide Chemotaxis were used, and the ability of MMSC to migrate in the collagen gel towards spheroids of cancer cells synthesizing SDF-1 and their ability to penetrate the conglomerate of cells was investigated.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
The results show that MSC cells are able to capture more than 10 capsules containing antitumor drugs – doxorubicin, vincristine. According to the experimental data of flow cytometry, it has been shown that about 90% of the cells are able to internalize the capsules with high efficiency. The unique structure of capsules prevents the release of antitumor drugs within 72 hours. It is shown that most of the cells are able to transfer capsules along the SDF-1 gradient and into the tumor spheroid focus.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Thus, it is shown that MSCs with capsules containing antitumor drugs can serve as a new dosage form for the targeted delivery of antitumor drugs to the tumor site.
</p>
<h2 style="text-align: justify;">Acknowledgments</h2>
<p style="text-align: justify;">
This work was supported by the Russian Foundation for Basic Research (grant No. 18-015-00100).
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Targeted delivery, micro and nanocapsules, antitumor drugs, internalization, mesenchymal stromal cells, migration, pharmacokinetics, synthesis, cultivation, carrier cells.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction and goals
The aim of this work is to investigate the possibilities of usage of multipotent mesenchymal stromal cells (MMSC) as a platform for delivering drugs which are contained in hybrid polymeric microcapsules. MMSCs are a cell population with high potential which due to the phenomenon of pathotropism can solve the problem of target drug delivery by acting as a carrier. Thus, combination of the biological phenomenon of cell migration and the high loading capacity of polymer capsules will allow targeted delivery of a substance without external and internal effect on carrier cells. To test the technique, doxorubicin and vincristine were selected as antitumor drugs with a dose-dependent effect, which are included in many polychemotherapy regimens.
Methods
In this study, hybrid microcapsules of various sizes (5 μm, 1 μm, 0.5 μm) were synthesized using Layer-by-Layer technique (Polyarginine/Dextran sulfate) and sol-gel synthesis (Tetraethyl orthosilicate). These micro containers have low toxicity, high biocompatibility, and are also capable of protecting the cell from encapsulated drugs. The association of cells with capsules of various sizes was evaluated using flow cytometry and laser scanning confocal microscopy in order to determine the optimal ratio of capsules and cells. The effect of capsules of various sizes associated with cells on spontaneous migration of MSCs, was examined using a cell-IQ cell culture monitoring system. The ability of MMSC to direct migration through the concentration gradient of SDF-1 was studied. For qualitative and quantitative assessment of migration, Transwell, μ-Slide Chemotaxis were used, and the ability of MMSC to migrate in the collagen gel towards spheroids of cancer cells synthesizing SDF-1 and their ability to penetrate the conglomerate of cells was investigated.
Results
The results show that MSC cells are able to capture more than 10 capsules containing antitumor drugs – doxorubicin, vincristine. According to the experimental data of flow cytometry, it has been shown that about 90% of the cells are able to internalize the capsules with high efficiency. The unique structure of capsules prevents the release of antitumor drugs within 72 hours. It is shown that most of the cells are able to transfer capsules along the SDF-1 gradient and into the tumor spheroid focus.
Conclusion
Thus, it is shown that MSCs with capsules containing antitumor drugs can serve as a new dosage form for the targeted delivery of antitumor drugs to the tumor site.
Acknowledgments
This work was supported by the Russian Foundation for Basic Research (grant No. 18-015-00100).
Keywords
Targeted delivery, micro and nanocapsules, antitumor drugs, internalization, mesenchymal stromal cells, migration, pharmacokinetics, synthesis, cultivation, carrier cells.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20703
[VALUE] => Functionalization of bone marrow mesenchymal stromal cells by multifunctional capsules for targeted drug delivery
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Functionalization of bone marrow mesenchymal stromal cells by multifunctional capsules for targeted drug delivery
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20827
[VALUE] => 1466
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1466
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20828
[VALUE] => 1467
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1467
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Александр С. Тимин 1,2, Альберт Р. Муслимов 1, Алексей А. Пельтек 3, Михаил В. Зюзин 4, Ольга С. Епифановская 1, Владислав С. Сергеев 1, Анна А. Доценко 1, Тимофей Е. Карпов 3, Игорь С. Сергеев 3, Александр А. Гончаренко 3, Яна В. Тараканчикова 5, Кирилл В. Лепик 1, Глеб Б. Сухоруков 3, Борис В. Афанасьев 1
Введение
Цель данной работы состояла в исследовании возможностей применения мультипотентных мезенхимальных стромальных клеток (ММСК) в качестве платформы для доставки препаратов, заключенных в гибридные полимерные микрокапсулы. ММСК являются высокопотенциальной клеточной популяцией, которая за счет феномена патотропизма может решить проблему таргетной доставки препарата, выступая в качестве носителя. Таким образом, объединение биологического феномена миграции клеток и высокой загружающей способности полимерных капсул обеспечит возможность контролировать направленность действия и позволит выполнить таргетную доставку вещества без внешнего и внутреннего воздействия для клеток-носителей. Для отработки методики, доксорубицин и винкристин были отобраны, в качестве противоопухолевых препаратов с дозозависимым эффектом, которые включены в состав многих схем полихимиотерапии.
Методы
В ходе данного исследования был произведен синтез гибридных микрокапсул различных размеров (5 мкм, 1 мкм, 0,5 мкм) при помощи технологии Layer-by- Layer (Polyarginine/Dextran sulfate) и золь-гель синтеза (Tetraethyl orthosilicate). Данные микроконтейнеры обладают низкой токсичностью, высокой биосовместимостью, а также способны защитить клетку от инкапсулированных препаратов. На следующем этапе была выполнена оценка ассоциации клеток с капсулами различных размеров при помощи проточной цитометрии и лазерной сканирующей конфокальной микроскопии для определения оптимального соотношения капсул и клеток. Спонтанная миграция МСК, и влияние на нее ассоциированных с клетками капсул различных размеров была исследована при помощи системы наблюдения за живыми клетками в культуре Cell-IQ. На завершающем этапе работы была изучена способность ММСК к направленной миграции по градиенту концентрации SDF-1. Для качественной и количественной оценки миграции были использованы Transwell, μ-Slide Chemotaxis, а также была исследована способность ММСК к миграции в коллагеновом геле в сторону сфероидов из раковых клеток, синтезирующих SDF-1, и их способность проникать внутрь конгломерата клеток.
Результаты
Полученные результаты показывают, что МСК клетки способны захватывать более 10 капсул, содержащие противоопухолевые препараты – доксорубицин, винкристин. По экспериментальным данным проточной цитометрии показано, что 90 % клеток способны интернализировать капсулы с высокой эффективностью. Уникальная структура капсул предотвращает высвобождение противоопухолевых препаратов в течение 72 часов. Показано, что большая часть клеток способны направлено переносить капсулы по SDF-1 градиенту и в очаг опухолевого сфероида.
Заключение
Таким образом, показано, что МСК с включенными капсулами, содержащие противоопухолевые препараты, могут выступать в качестве новой лекарственной формы для направленной доставки противоопухолевых препаратов в очаг опухолей.
Благодарности
Работа выполнена при поддержке Российского Фонда Фундаментальных исследований (грант № 18-015-00100).
Ключевые слова
Таргетная доставка, микро- и нанокапсулы, противоо пухолевые препараты, интернализация, мезенхимные стромальные клетки, миграция, фармакокинетика, синтез, культивирование, клетки-носители.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20690
[VALUE] => Array
(
[TEXT] => Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Олег В. Голощапов, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Олег В. Голощапов, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20691
[VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20692
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Нутриционная поддержка онкологических больных заняла прочную позицию в ряду лечебных мероприятий. По данным отчета Европейского общества парентерального и энтерального питания, частота недостаточности питания у онкологических больных колеблется от 46 до 88%. С 2011 г. для приготовления парэнтерального питания (ПП), дозирования антибиотиков и разведения препаратов для химиотерапии используется технология компаундинга. Целью работы было сравнение аппаратного приготовления парэнтерального питания методом компаундинга с «флаконной» методикой – использование нескольких флаконов с нутриентами, и заполнением мешков вручную.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
В 2018 году на базе НИИ «Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой» для приготовления парэнтерального питания 13 пациентам использован метод – компаундинга. Характеристика пациентов. Медиана возраста – 10 лет (от 11 мес. до 45 лет), 7 женщин и 6 мужчин. Основной диагноз: ОЛЛ – 38,5% (n=5), ОМЛ – 30,8%(n=4), МДС – 23,1%(n=3), ХМЛ – 7,7%(n=1). Было приготовлено 13 мешков с питанием с помощью медицинского компаундера, 4 мешка заполнялись вручную, «флаконный» метод парэнтерального питания применяли у 9 пациентов. Проведен подсчет затрачиваемого времени на три способа приготовления парэнтерального питания: технология компаундинга, «флаконная методика» и заполнение мешка вручную. Для исследования стерильности приготавливаемой смеси проводились бактериологические исследования готового раствора. В конце эксперимента проведен опрос медсестер отделения об удобстве использования парэнтерального питания (ПП) приготовленного по технологии компаундинга.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Методика компаундинга: на приготовления ПП до 1 л требовалось в среднем 6,5 мин., от 1-1,5 л в 9 мин., на пакет объемом от 1,5 до 2 л требовалось 11 мин., от 2-3 л – 15 мин. На заполнение мешка вручную ушло не менее 25 мин. На приготовление ПП «флаконным» методом затрачивали не менее 15 мин. Все бактериологические тесты смеси для парэнтерального питания приготовленного методом компаундинга были отрицательны. Опрос медсестер отделения показал, что применения готового индивидуального питания – удобно, экономит время и безопасно для пациента.
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
На приготовление парэнтерального питания с помощью медицинского компаундера затрачивается меньше времени, чем на «флаконный» метод или заполнения мешка вручную. ПП, приготовленное методом компаундинга, стерильно и удобно в применении.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Парэнтеральное питание, медицинский смеситель, компаундинг, асептика, нозокомиальная инфекция.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Нутриционная поддержка онкологических больных заняла прочную позицию в ряду лечебных мероприятий. По данным отчета Европейского общества парентерального и энтерального питания, частота недостаточности питания у онкологических больных колеблется от 46 до 88%. С 2011 г. для приготовления парэнтерального питания (ПП), дозирования антибиотиков и разведения препаратов для химиотерапии используется технология компаундинга. Целью работы было сравнение аппаратного приготовления парэнтерального питания методом компаундинга с «флаконной» методикой – использование нескольких флаконов с нутриентами, и заполнением мешков вручную.
Пациенты и методы
В 2018 году на базе НИИ «Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой» для приготовления парэнтерального питания 13 пациентам использован метод – компаундинга. Характеристика пациентов. Медиана возраста – 10 лет (от 11 мес. до 45 лет), 7 женщин и 6 мужчин. Основной диагноз: ОЛЛ – 38,5% (n=5), ОМЛ – 30,8%(n=4), МДС – 23,1%(n=3), ХМЛ – 7,7%(n=1). Было приготовлено 13 мешков с питанием с помощью медицинского компаундера, 4 мешка заполнялись вручную, «флаконный» метод парэнтерального питания применяли у 9 пациентов. Проведен подсчет затрачиваемого времени на три способа приготовления парэнтерального питания: технология компаундинга, «флаконная методика» и заполнение мешка вручную. Для исследования стерильности приготавливаемой смеси проводились бактериологические исследования готового раствора. В конце эксперимента проведен опрос медсестер отделения об удобстве использования парэнтерального питания (ПП) приготовленного по технологии компаундинга.
Результаты
Методика компаундинга: на приготовления ПП до 1 л требовалось в среднем 6,5 мин., от 1-1,5 л в 9 мин., на пакет объемом от 1,5 до 2 л требовалось 11 мин., от 2-3 л – 15 мин. На заполнение мешка вручную ушло не менее 25 мин. На приготовление ПП «флаконным» методом затрачивали не менее 15 мин. Все бактериологические тесты смеси для парэнтерального питания приготовленного методом компаундинга были отрицательны. Опрос медсестер отделения показал, что применения готового индивидуального питания – удобно, экономит время и безопасно для пациента.
Выводы
На приготовление парэнтерального питания с помощью медицинского компаундера затрачивается меньше времени, чем на «флаконный» метод или заполнения мешка вручную. ПП, приготовленное методом компаундинга, стерильно и удобно в применении.
Ключевые слова
Парэнтеральное питание, медицинский смеситель, компаундинг, асептика, нозокомиальная инфекция.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20693
[VALUE] => Array
(
[TEXT] => Aschot A. Tadevosian, Olga A. Prokofieva, Olga E. Pigareva, Oleg V. Goloshchapov, Boris V. Afanasyev
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Aschot A. Tadevosian, Olga A. Prokofieva, Olga E. Pigareva, Oleg V. Goloshchapov, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20694
[VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20695
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Nutritional support is an established approach, along with other treatment procedures for patients with malignancies. According to the ESPEN’s report, incidence of nutritional deficiency among oncology patients varies from 46% to 88%. Since 2011, automatic compounding technology is used to prepare parenteral nutrition, antibiotics, and chemotherapy medications. Objective of the study was to compare automatic compounding of parenteral nutrition (PN) with “the flask method” providing separate infusions of distinct nutrients, and with manual PN mixing.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
In 2018, an automatic compounding technology was used to prepare parenteral nutrition for 13 patients treated at the R. Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation. The patient group included 7 women and 6 men at a median age of 10 years (11 months to 45 years old) with following primary disorders: ALL, 38.5% (n=5); AML, 30.8% (n=4); MDS, 23.1% (n=3); CML, 7.7% (n=1). Thirteen bags of parenteral nutrition were prepared using a medical compounder, and 4 bags were filled manually. Nine patients received PN by “the flask method”. In each case, time spent for preparing the nutrition was evaluated, and the prepared solutions were bacteriologically tested. As a part of the experiment, nurses at the unit were interviewed about convenience of PN usage when prepared by automatic compounding.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
At an average, it took 6.5 minutes to prepare one liter of PN by automatic compounding. It took 9 minutes to prepare 1 to 1.5-liter bag, 11 minutes to prepare 1.5 to 2.0-liter bag, and 15 minutes for a 2 to 3-liter bag. Meanwhile, it took at least 25 minutes to fill a bag manually, and 15 minutes to prepare PN using a “flask method”. All the bacteriological tests performed on the compounder-made PN mixtures were negative. Interviews with medical nurses at the unit showed that the compounder-made PN was easy to use, safe for patients, and helped to save time.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
It takes less time to prepare parenteral nutrition by using a medical compounder as compared to “the flask method” or by filling bags manually. The automatically prepared PN is sterile and easy to use.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Parenteral nutrition, nutritional support, medical compounder, compounding, aseptic, nosocomial infection.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Nutritional support is an established approach, along with other treatment procedures for patients with malignancies. According to the ESPEN’s report, incidence of nutritional deficiency among oncology patients varies from 46% to 88%. Since 2011, automatic compounding technology is used to prepare parenteral nutrition, antibiotics, and chemotherapy medications. Objective of the study was to compare automatic compounding of parenteral nutrition (PN) with “the flask method” providing separate infusions of distinct nutrients, and with manual PN mixing.
Patients and methods
In 2018, an automatic compounding technology was used to prepare parenteral nutrition for 13 patients treated at the R. Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation. The patient group included 7 women and 6 men at a median age of 10 years (11 months to 45 years old) with following primary disorders: ALL, 38.5% (n=5); AML, 30.8% (n=4); MDS, 23.1% (n=3); CML, 7.7% (n=1). Thirteen bags of parenteral nutrition were prepared using a medical compounder, and 4 bags were filled manually. Nine patients received PN by “the flask method”. In each case, time spent for preparing the nutrition was evaluated, and the prepared solutions were bacteriologically tested. As a part of the experiment, nurses at the unit were interviewed about convenience of PN usage when prepared by automatic compounding.
Results
At an average, it took 6.5 minutes to prepare one liter of PN by automatic compounding. It took 9 minutes to prepare 1 to 1.5-liter bag, 11 minutes to prepare 1.5 to 2.0-liter bag, and 15 minutes for a 2 to 3-liter bag. Meanwhile, it took at least 25 minutes to fill a bag manually, and 15 minutes to prepare PN using a “flask method”. All the bacteriological tests performed on the compounder-made PN mixtures were negative. Interviews with medical nurses at the unit showed that the compounder-made PN was easy to use, safe for patients, and helped to save time.
Conclusion
It takes less time to prepare parenteral nutrition by using a medical compounder as compared to “the flask method” or by filling bags manually. The automatically prepared PN is sterile and easy to use.
Keywords
Parenteral nutrition, nutritional support, medical compounder, compounding, aseptic, nosocomial infection.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20696
[VALUE] => Our experience in compounding the parenteral nutrition for patients after allo-HSCT
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Our experience in compounding the parenteral nutrition for patients after allo-HSCT
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20837
[VALUE] => 1476
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1476
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20838
[VALUE] => 1477
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1477
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Олег В. Голощапов, Борис В. Афанасьев
Введение
Нутриционная поддержка онкологических больных заняла прочную позицию в ряду лечебных мероприятий. По данным отчета Европейского общества парентерального и энтерального питания, частота недостаточности питания у онкологических больных колеблется от 46 до 88%. С 2011 г. для приготовления парэнтерального питания (ПП), дозирования антибиотиков и разведения препаратов для химиотерапии используется технология компаундинга. Целью работы было сравнение аппаратного приготовления парэнтерального питания методом компаундинга с «флаконной» методикой – использование нескольких флаконов с нутриентами, и заполнением мешков вручную.
Пациенты и методы
В 2018 году на базе НИИ «Институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой» для приготовления парэнтерального питания 13 пациентам использован метод – компаундинга. Характеристика пациентов. Медиана возраста – 10 лет (от 11 мес. до 45 лет), 7 женщин и 6 мужчин. Основной диагноз: ОЛЛ – 38,5% (n=5), ОМЛ – 30,8%(n=4), МДС – 23,1%(n=3), ХМЛ – 7,7%(n=1). Было приготовлено 13 мешков с питанием с помощью медицинского компаундера, 4 мешка заполнялись вручную, «флаконный» метод парэнтерального питания применяли у 9 пациентов. Проведен подсчет затрачиваемого времени на три способа приготовления парэнтерального питания: технология компаундинга, «флаконная методика» и заполнение мешка вручную. Для исследования стерильности приготавливаемой смеси проводились бактериологические исследования готового раствора. В конце эксперимента проведен опрос медсестер отделения об удобстве использования парэнтерального питания (ПП) приготовленного по технологии компаундинга.
Результаты
Методика компаундинга: на приготовления ПП до 1 л требовалось в среднем 6,5 мин., от 1-1,5 л в 9 мин., на пакет объемом от 1,5 до 2 л требовалось 11 мин., от 2-3 л – 15 мин. На заполнение мешка вручную ушло не менее 25 мин. На приготовление ПП «флаконным» методом затрачивали не менее 15 мин. Все бактериологические тесты смеси для парэнтерального питания приготовленного методом компаундинга были отрицательны. Опрос медсестер отделения показал, что применения готового индивидуального питания – удобно, экономит время и безопасно для пациента.
Выводы
На приготовление парэнтерального питания с помощью медицинского компаундера затрачивается меньше времени, чем на «флаконный» метод или заполнения мешка вручную. ПП, приготовленное методом компаундинга, стерильно и удобно в применении.
Ключевые слова
Парэнтеральное питание, медицинский смеситель, компаундинг, асептика, нозокомиальная инфекция.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20634
[VALUE] => Array
(
[TEXT] => Юлия А. Рогачева, Марина О. Попова, Анастасия В. Некрасова, Иван В. Цыганков, Кирилл В. Лепик, Лилия В. Стельмах, Иван С. Моисеев, Сергей Н. Бондаренко, Наталья Б. Михайлова, Вадим В. Байков, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Юлия А. Рогачева, Марина О. Попова, Анастасия В. Некрасова, Иван В. Цыганков, Кирилл В. Лепик, Лилия В. Стельмах, Иван С. Моисеев, Сергей Н. Бондаренко, Наталья Б. Михайлова, Вадим В. Байков, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20635
[VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; кафедра гематологии, транcфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; кафедра гематологии, транcфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20636
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
ВИЧ-инфекция ассоциирована с увеличением риска развития опухолей, включая лимфому Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на применение современной антиретровирусной терапии (АРВТ). Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать стандартную терапию, включая высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [1]. Ниволумаб это новая опция для терапии спасения у пациентов с рецидивирующими/рефрактерными (р/р) течением ЛХ и НХЛ, но эффективность и безопасность использования этого препарата у ВИЧ-инфицированных пациентов остается неизвестным. Известно, что ниволумаб обладает не только противоопухолевой активностью, но и способствует снижению вирусной нагрузки при ВИЧ-инфекции [2]. Описано несколько случаев использования ниволумаба для лечения ВИЧ-ассоциированных лимфом [3,4]. В НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой терапия ниволумабом была проведена у 6 пациентов с ВИЧ-ассоциированными ЛХ и НХЛ.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
В исследование включены шесть пациентов мужского пола с р/р лимфомами, которые получили терапию ниволумабом в 2017 году. Первичной конечной точкой была оценка ответа на терапию. Вторичные точки – оценка токсичности, частота рецидива и общая выживаемость (ОВ) в течение 12 месяцев от терапии ниволумабом. Common Terminology Criteria for Adverce Events (CTCAE 4.0) были использованы для оценки токсичности и иммуноопосредованных эффектов. Критерии LYRIC использовались для оценки ответа по ПЭТ-КТ.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Основные заболевания в группе исследования были: ЛХ n=4 (66%) и НХЛ, диффузная В-крупноклеточная лимфома (ДБККЛ) n=2 (34%). Медиана количества предшествующих линий терапия – 2 (2-3). Три пациента получали ниволумаб в качестве bridge-терапии перед ауто-ТГСК. После трансплантации ниволумаб был использован у одного пациента, двум пациентам ауто-ТГСК не выполнялась. Два пациента с ЛХ получали ниволумаб в качестве монотерапии, 4 пациента в комбинации с бендамустином и гемцитабином, у одного пациента в комбинацию был добавлен ритуксимаб. Медиана дозы ниволумаба составила 1 мг/кг (0,5-1,5 мг/кг). Медиана количества введений составила 8,5 (2-12). Медиана количества CD4+ клеток – 382 кл/мкл (45-490); 83,3% пациентов получали АРВТ. Один пациент не получал АРВТ из-за острой почечной недостаточности (креатинин 680 мкмоль/л). Только у пяти пациентов можно было объективно оценить ответ на терапию, один пациент умер до проведения ПЭТ-КТ, после 2 курсов терапии ниволумаб. Общий ответ был зарегистрирован в 83,3% случаев. Два – частичная ремиссия у пациентов с лимфомой Ходжкина и три (50%) пациентов с ЛХ и НХЛ имели полный метаболический ответ, один пациент с НХЛ – прогрессирование заболевания (оценен клинически). Значимой токсичности, согласно критериям CTCAE, и иммуноопосредованных эффектов выявлено не было. Рецидив основного заболевания был диагностирован у двух пациентов, время до прогрессирования у пациента с ЛХ составило 485 дней и 266 у пациента с ДБККЛ. ОВ 12 месяцев для ВИЧ-инфицированных пациентов от первого введения ниволумаба составила 83,3%. Пациент с острой почечной недостаточностью, не получавший АРВТ, умер от прогрессирования лимфомы. Основные характеристики пациентов представлены в таблице 1.
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
У пациентов с ВИЧ-ассоциированными лимфомами общий ответ на терапию ниволумабом составил 83,3%. Токсичность и иммуноопосредованные эффекты не были зарегистрированы. ОВ в течение 1 года составила 83,3%. Предварительные результаты показывают, что терапия р/р ВИЧ-ассоциированных лимфом ниволумабом – эффективна и безопасна, но необходимо подтверждение в исследованиях в большей популяцией.
</p>
<h2 style="text-align: justify;">Литература</h2>
<p style="text-align: justify;">
1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cellular Therapy and Transplantation (CTT). Vol. 6, No. 4(21), 2017,-P.42-51<br>
2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. -2018.-Vol. 29.-P.517-518<br>
3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. Journal of Immunotherapy. -2018-Vol.41.-P.379–383<br>
4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIVrelated relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. Journal for ImmunoTherapy of Cancer. -2017-Vol.20.-P.49
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Иммунотерапия, ВИЧ-ассоциированные лимфомы, ниволумаб, ВИЧ, рецидивирущее/рефрактерное течение лимфомы Ходжкина, неходжкинская лимфома, ответ на терапию, частота рецидивов, токсичность, высокодозная химиотерапия, аутологичная трансплантация гемопоэтических стволовых клеток, общая выживаемость.
</p>
<h2>Таблица 1. Характеристика пациентов, леченных ниволумабом</h2>
<img width="783" alt="41_таблица1.png" src="/upload/medialibrary/86d/41_tablitsa1.png" height="367" title="41_таблица1.png"><br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
ВИЧ-инфекция ассоциирована с увеличением риска развития опухолей, включая лимфому Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на применение современной антиретровирусной терапии (АРВТ). Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать стандартную терапию, включая высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [1]. Ниволумаб это новая опция для терапии спасения у пациентов с рецидивирующими/рефрактерными (р/р) течением ЛХ и НХЛ, но эффективность и безопасность использования этого препарата у ВИЧ-инфицированных пациентов остается неизвестным. Известно, что ниволумаб обладает не только противоопухолевой активностью, но и способствует снижению вирусной нагрузки при ВИЧ-инфекции [2]. Описано несколько случаев использования ниволумаба для лечения ВИЧ-ассоциированных лимфом [3,4]. В НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой терапия ниволумабом была проведена у 6 пациентов с ВИЧ-ассоциированными ЛХ и НХЛ.
Материалы и методы
В исследование включены шесть пациентов мужского пола с р/р лимфомами, которые получили терапию ниволумабом в 2017 году. Первичной конечной точкой была оценка ответа на терапию. Вторичные точки – оценка токсичности, частота рецидива и общая выживаемость (ОВ) в течение 12 месяцев от терапии ниволумабом. Common Terminology Criteria for Adverce Events (CTCAE 4.0) были использованы для оценки токсичности и иммуноопосредованных эффектов. Критерии LYRIC использовались для оценки ответа по ПЭТ-КТ.
Результаты
Основные заболевания в группе исследования были: ЛХ n=4 (66%) и НХЛ, диффузная В-крупноклеточная лимфома (ДБККЛ) n=2 (34%). Медиана количества предшествующих линий терапия – 2 (2-3). Три пациента получали ниволумаб в качестве bridge-терапии перед ауто-ТГСК. После трансплантации ниволумаб был использован у одного пациента, двум пациентам ауто-ТГСК не выполнялась. Два пациента с ЛХ получали ниволумаб в качестве монотерапии, 4 пациента в комбинации с бендамустином и гемцитабином, у одного пациента в комбинацию был добавлен ритуксимаб. Медиана дозы ниволумаба составила 1 мг/кг (0,5-1,5 мг/кг). Медиана количества введений составила 8,5 (2-12). Медиана количества CD4+ клеток – 382 кл/мкл (45-490); 83,3% пациентов получали АРВТ. Один пациент не получал АРВТ из-за острой почечной недостаточности (креатинин 680 мкмоль/л). Только у пяти пациентов можно было объективно оценить ответ на терапию, один пациент умер до проведения ПЭТ-КТ, после 2 курсов терапии ниволумаб. Общий ответ был зарегистрирован в 83,3% случаев. Два – частичная ремиссия у пациентов с лимфомой Ходжкина и три (50%) пациентов с ЛХ и НХЛ имели полный метаболический ответ, один пациент с НХЛ – прогрессирование заболевания (оценен клинически). Значимой токсичности, согласно критериям CTCAE, и иммуноопосредованных эффектов выявлено не было. Рецидив основного заболевания был диагностирован у двух пациентов, время до прогрессирования у пациента с ЛХ составило 485 дней и 266 у пациента с ДБККЛ. ОВ 12 месяцев для ВИЧ-инфицированных пациентов от первого введения ниволумаба составила 83,3%. Пациент с острой почечной недостаточностью, не получавший АРВТ, умер от прогрессирования лимфомы. Основные характеристики пациентов представлены в таблице 1.
Выводы
У пациентов с ВИЧ-ассоциированными лимфомами общий ответ на терапию ниволумабом составил 83,3%. Токсичность и иммуноопосредованные эффекты не были зарегистрированы. ОВ в течение 1 года составила 83,3%. Предварительные результаты показывают, что терапия р/р ВИЧ-ассоциированных лимфом ниволумабом – эффективна и безопасна, но необходимо подтверждение в исследованиях в большей популяцией.
Литература
1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cellular Therapy and Transplantation (CTT). Vol. 6, No. 4(21), 2017,-P.42-51
2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. -2018.-Vol. 29.-P.517-518
3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. Journal of Immunotherapy. -2018-Vol.41.-P.379–383
4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIVrelated relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. Journal for ImmunoTherapy of Cancer. -2017-Vol.20.-P.49
Ключевые слова
Иммунотерапия, ВИЧ-ассоциированные лимфомы, ниволумаб, ВИЧ, рецидивирущее/рефрактерное течение лимфомы Ходжкина, неходжкинская лимфома, ответ на терапию, частота рецидивов, токсичность, высокодозная химиотерапия, аутологичная трансплантация гемопоэтических стволовых клеток, общая выживаемость.
Таблица 1. Характеристика пациентов, леченных ниволумабом

[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20637
[VALUE] => Array
(
[TEXT] => Yulia A. Rogacheva, Marina O. Popova, Anastasia V. Nekrasova, Ivan V. Tsygankov, Kirill V. Lepik, Lilia V. Stelmakh, Ivan S. Moiseev, Sergey N. Bondarenko, Natalia B. Mikhaylova, Vadim V. Baykov, Boris V. Afanasyev
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Yulia A. Rogacheva, Marina O. Popova, Anastasia V. Nekrasova, Ivan V. Tsygankov, Kirill V. Lepik, Lilia V. Stelmakh, Ivan S. Moiseev, Sergey N. Bondarenko, Natalia B. Mikhaylova, Vadim V. Baykov, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20638
[VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Research Institute of Children Oncology, Hematology and Transplantation; Chair of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Research Institute of Children Oncology, Hematology and Transplantation; Chair of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20639
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Infection with HIV is associated with a significantly increased risk of cancer, including Hodgkin lymphoma (HL) and non-Hodgkin lymphoma (NHL) even when patients are treated successfully with modern combination anti-retroviral therapy (cART). Immune preservation with cART has changed the therapeutic approach to HIV-related lymphoma, allowing the use standard chemotherapy, including high dose chemotherapy with autologous hematopoietic stem cell transplantation (ASCT) [1]. Nivolumab is a salvage option in relapsed/refractory (r/r) HL and NHL, but efficacy and safety in patients with HIV infection are still unknown. Patients with HIV-related lymphoma may benefit not only anticancer activity of nivolumab, but also from its potential anti-HIV effect [2]. Just a few cases of HIV-related lymphoma treated with nivolumab were reported [3, 4]. We describe a case series of r/r HIV-related lymphoma receiving nivolumab in Raisa Gorbacheva Institute of Children Oncology, Haematology and Transplantation, First Pavlov State Medical University of Saint-Petersburg.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
Six male patients with r/r HIV-related lymphoma were treated with nivolumab in 2017. Clinical response to therapy was the primary endpoint. Secondary endpoints were determined by toxicity, relapse incidence and overall survival (OS) at 12 months after first nivolumab infusion. Common Terminology Criteria for Adverse Events (CTCAE v4.03) for the toxicity analysis and immune-related adverse effects have been used. LYRIC criteria for assessing FDG-PET/CT were applied.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
The underlying diseases in the patients observed were as follows: HL was registered in four cases (66%), whereas NHL and diffuse large B-cell lymphoma (DLBCL) were diagnosed in two remaining patients (34%). Median number of prior lines of therapy was 2 (range, 2-3). Three patients received nivolumab as a bridge to ASCT. Relapse after ASCT was treated in one patient, two patients didn’t proceed to ASCT. Two patients with HL received nivolumab as monotherapy, 4 patients were subject to nivolumab in combination with bendamustine and gemcitabine, including one patient receiving supplemental treatment with rituximab. The median dose of nivolumab was 1 mg/kg (range, 0.5-1.5 mg/kg). The median number of nivolumab doses received was 8.5 (range, 2-12). The median number of CD4+ cells was 382 cells/μl (range, 45-490); 83.3% patients were on cART. One patient didn’t received cART due acute renal failure (creatinine 680 mcM). Only 5 patients were available for objective response estimation, one of them died before PET/CT study was performed. Overall response rate was 83.3%. Of those, partial remission was shown in two HL patients; three patients with HL and NHL (50% of total) had complete metabolic responses, and one patient with NHL developed the disease progression, as clinically assessed. Toxicity according to CTCAE and any immune-related adverse effects were not registered. Relapse of the underlying disease was diagnosed in 2 patients, time to progression for those patients were 485 days (HL) and 266 days (DLBCL). Overall survival (OS) at 12 months for the patients with HIV (n=6) from the time of nivolumab therapy was 83.3%. The patient who didn’t receive cART and developed acute renal failure died from the progression of lymphoma. Summary of patients are outlined on table 1.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Overall response rate in patients with HIV-related lymphomas was 83.3%. Toxicity and immune-related adverse effects were not registered. One-year overall survival in patients with HIV-related lymphoma was 83.3%. Preliminary data suggest that nivolumab is an effective and safe treatment option for r/r HIV-related lymphoma, but needs to be confirmed in larger studies.
</p>
<h2 style="text-align: justify;">References</h2>
<p style="text-align: justify;">
1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cell Ther Transplant (CTT). 2017; 6(4):42-51.<br>
2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. 2018; 29:517-518.<br>
3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. J Immunother. 2018; 41:379–383.<br>
4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIV-related relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. J Immunother Cancer. 2017;20:49.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Immunotherapy, HIV-related lymphoma, nivolumab, HIV, relapsed/refractory Hodgkin lymphoma, non-Hodgkin lymphoma, response to therapy, relapse incidence, toxicity, high-dose chemotherapy, autologous hematopoietic stem cell transplantation, overall survival.
</p>
<h2 style="text-align: justify;">Table 1. Some clinical characteristics of HIV patients treated with Nivolumab</h2>
<p style="text-align: justify;">
<img width="780" alt="41_table_1.png" src="/upload/medialibrary/15b/41_table_1.png" height="404" title="41_table_1.png">
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Infection with HIV is associated with a significantly increased risk of cancer, including Hodgkin lymphoma (HL) and non-Hodgkin lymphoma (NHL) even when patients are treated successfully with modern combination anti-retroviral therapy (cART). Immune preservation with cART has changed the therapeutic approach to HIV-related lymphoma, allowing the use standard chemotherapy, including high dose chemotherapy with autologous hematopoietic stem cell transplantation (ASCT) [1]. Nivolumab is a salvage option in relapsed/refractory (r/r) HL and NHL, but efficacy and safety in patients with HIV infection are still unknown. Patients with HIV-related lymphoma may benefit not only anticancer activity of nivolumab, but also from its potential anti-HIV effect [2]. Just a few cases of HIV-related lymphoma treated with nivolumab were reported [3, 4]. We describe a case series of r/r HIV-related lymphoma receiving nivolumab in Raisa Gorbacheva Institute of Children Oncology, Haematology and Transplantation, First Pavlov State Medical University of Saint-Petersburg.
Patients and methods
Six male patients with r/r HIV-related lymphoma were treated with nivolumab in 2017. Clinical response to therapy was the primary endpoint. Secondary endpoints were determined by toxicity, relapse incidence and overall survival (OS) at 12 months after first nivolumab infusion. Common Terminology Criteria for Adverse Events (CTCAE v4.03) for the toxicity analysis and immune-related adverse effects have been used. LYRIC criteria for assessing FDG-PET/CT were applied.
Results
The underlying diseases in the patients observed were as follows: HL was registered in four cases (66%), whereas NHL and diffuse large B-cell lymphoma (DLBCL) were diagnosed in two remaining patients (34%). Median number of prior lines of therapy was 2 (range, 2-3). Three patients received nivolumab as a bridge to ASCT. Relapse after ASCT was treated in one patient, two patients didn’t proceed to ASCT. Two patients with HL received nivolumab as monotherapy, 4 patients were subject to nivolumab in combination with bendamustine and gemcitabine, including one patient receiving supplemental treatment with rituximab. The median dose of nivolumab was 1 mg/kg (range, 0.5-1.5 mg/kg). The median number of nivolumab doses received was 8.5 (range, 2-12). The median number of CD4+ cells was 382 cells/μl (range, 45-490); 83.3% patients were on cART. One patient didn’t received cART due acute renal failure (creatinine 680 mcM). Only 5 patients were available for objective response estimation, one of them died before PET/CT study was performed. Overall response rate was 83.3%. Of those, partial remission was shown in two HL patients; three patients with HL and NHL (50% of total) had complete metabolic responses, and one patient with NHL developed the disease progression, as clinically assessed. Toxicity according to CTCAE and any immune-related adverse effects were not registered. Relapse of the underlying disease was diagnosed in 2 patients, time to progression for those patients were 485 days (HL) and 266 days (DLBCL). Overall survival (OS) at 12 months for the patients with HIV (n=6) from the time of nivolumab therapy was 83.3%. The patient who didn’t receive cART and developed acute renal failure died from the progression of lymphoma. Summary of patients are outlined on table 1.
Conclusion
Overall response rate in patients with HIV-related lymphomas was 83.3%. Toxicity and immune-related adverse effects were not registered. One-year overall survival in patients with HIV-related lymphoma was 83.3%. Preliminary data suggest that nivolumab is an effective and safe treatment option for r/r HIV-related lymphoma, but needs to be confirmed in larger studies.
References
1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cell Ther Transplant (CTT). 2017; 6(4):42-51.
2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. 2018; 29:517-518.
3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. J Immunother. 2018; 41:379–383.
4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIV-related relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. J Immunother Cancer. 2017;20:49.
Keywords
Immunotherapy, HIV-related lymphoma, nivolumab, HIV, relapsed/refractory Hodgkin lymphoma, non-Hodgkin lymphoma, response to therapy, relapse incidence, toxicity, high-dose chemotherapy, autologous hematopoietic stem cell transplantation, overall survival.
Table 1. Some clinical characteristics of HIV patients treated with Nivolumab

[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20640
[VALUE] => Nivolumab treatment in patients with relapsed/refractory HIV-related lymphomas
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Nivolumab treatment in patients with relapsed/refractory HIV-related lymphomas
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20811
[VALUE] => 1449
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1449
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20812
[VALUE] => 1450
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1450
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Юлия А. Рогачева, Марина О. Попова, Анастасия В. Некрасова, Иван В. Цыганков, Кирилл В. Лепик, Лилия В. Стельмах, Иван С. Моисеев, Сергей Н. Бондаренко, Наталья Б. Михайлова, Вадим В. Байков, Борис В. Афанасьев
Введение
ВИЧ-инфекция ассоциирована с увеличением риска развития опухолей, включая лимфому Ходжкина (ЛХ) и неходжкинские лимфомы (НХЛ), несмотря на применение современной антиретровирусной терапии (АРВТ). Применение АРВТ изменило подход к лечению ВИЧ-ассоциированных лимфом, позволив использовать стандартную терапию, включая высокодозную химиотерапию (ВДХТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток (ауто-ТГСК) [1]. Ниволумаб это новая опция для терапии спасения у пациентов с рецидивирующими/рефрактерными (р/р) течением ЛХ и НХЛ, но эффективность и безопасность использования этого препарата у ВИЧ-инфицированных пациентов остается неизвестным. Известно, что ниволумаб обладает не только противоопухолевой активностью, но и способствует снижению вирусной нагрузки при ВИЧ-инфекции [2]. Описано несколько случаев использования ниволумаба для лечения ВИЧ-ассоциированных лимфом [3,4]. В НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой терапия ниволумабом была проведена у 6 пациентов с ВИЧ-ассоциированными ЛХ и НХЛ.
Материалы и методы
В исследование включены шесть пациентов мужского пола с р/р лимфомами, которые получили терапию ниволумабом в 2017 году. Первичной конечной точкой была оценка ответа на терапию. Вторичные точки – оценка токсичности, частота рецидива и общая выживаемость (ОВ) в течение 12 месяцев от терапии ниволумабом. Common Terminology Criteria for Adverce Events (CTCAE 4.0) были использованы для оценки токсичности и иммуноопосредованных эффектов. Критерии LYRIC использовались для оценки ответа по ПЭТ-КТ.
Результаты
Основные заболевания в группе исследования были: ЛХ n=4 (66%) и НХЛ, диффузная В-крупноклеточная лимфома (ДБККЛ) n=2 (34%). Медиана количества предшествующих линий терапия – 2 (2-3). Три пациента получали ниволумаб в качестве bridge-терапии перед ауто-ТГСК. После трансплантации ниволумаб был использован у одного пациента, двум пациентам ауто-ТГСК не выполнялась. Два пациента с ЛХ получали ниволумаб в качестве монотерапии, 4 пациента в комбинации с бендамустином и гемцитабином, у одного пациента в комбинацию был добавлен ритуксимаб. Медиана дозы ниволумаба составила 1 мг/кг (0,5-1,5 мг/кг). Медиана количества введений составила 8,5 (2-12). Медиана количества CD4+ клеток – 382 кл/мкл (45-490); 83,3% пациентов получали АРВТ. Один пациент не получал АРВТ из-за острой почечной недостаточности (креатинин 680 мкмоль/л). Только у пяти пациентов можно было объективно оценить ответ на терапию, один пациент умер до проведения ПЭТ-КТ, после 2 курсов терапии ниволумаб. Общий ответ был зарегистрирован в 83,3% случаев. Два – частичная ремиссия у пациентов с лимфомой Ходжкина и три (50%) пациентов с ЛХ и НХЛ имели полный метаболический ответ, один пациент с НХЛ – прогрессирование заболевания (оценен клинически). Значимой токсичности, согласно критериям CTCAE, и иммуноопосредованных эффектов выявлено не было. Рецидив основного заболевания был диагностирован у двух пациентов, время до прогрессирования у пациента с ЛХ составило 485 дней и 266 у пациента с ДБККЛ. ОВ 12 месяцев для ВИЧ-инфицированных пациентов от первого введения ниволумаба составила 83,3%. Пациент с острой почечной недостаточностью, не получавший АРВТ, умер от прогрессирования лимфомы. Основные характеристики пациентов представлены в таблице 1.
Выводы
У пациентов с ВИЧ-ассоциированными лимфомами общий ответ на терапию ниволумабом составил 83,3%. Токсичность и иммуноопосредованные эффекты не были зарегистрированы. ОВ в течение 1 года составила 83,3%. Предварительные результаты показывают, что терапия р/р ВИЧ-ассоциированных лимфом ниволумабом – эффективна и безопасна, но необходимо подтверждение в исследованиях в большей популяцией.
Литература
1. Popova M.O., Rogacheva Y.A., Nekrasova A.V., et al. Autologous hematopoietic cell transplantation for HIVrelated lymphoma: results of a single center (CIC725) matched case-control study. Cellular Therapy and Transplantation (CTT). Vol. 6, No. 4(21), 2017,-P.42-51
2. Guihot A, Marcelin AG, Massiani MA, et al. Drastic decrease of the HIV reservoir in a patient treated with Nivolumab for lung cancer. Ann Oncol. -2018.-Vol. 29.-P.517-518
3. Chang E., Sabichi A.L., Kramer J.R., et al. Nivolumab Treatment for Cancers in the HIV-infected Population. Journal of Immunotherapy. -2018-Vol.41.-P.379–383
4. Sandoval-Sus J.D., Mogollon-Duffo F., Patel A., et al. Nivolumab as salvage treatment in a patient with HIVrelated relapsed/refractory Hodgkin lymphoma and liver failure with encephalopathy. Journal for ImmunoTherapy of Cancer. -2017-Vol.20.-P.49
Ключевые слова
Иммунотерапия, ВИЧ-ассоциированные лимфомы, ниволумаб, ВИЧ, рецидивирущее/рефрактерное течение лимфомы Ходжкина, неходжкинская лимфома, ответ на терапию, частота рецидивов, токсичность, высокодозная химиотерапия, аутологичная трансплантация гемопоэтических стволовых клеток, общая выживаемость.
Таблица 1. Характеристика пациентов, леченных ниволумабом

Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20627
[VALUE] => Array
(
[TEXT] => Юлия А. Рогачева <sup>1</sup>, Марина О. Попова <sup>1</sup>, Анастасия С. Фролова <sup>1</sup>, Инна В. Маркова <sup>1</sup>, Алиса Г. Волкова <sup>1</sup>, Кирилл А. Екушев <sup>1</sup>, Ольга Н. Пинегина <sup>1</sup>, Олеся В. Паина <sup>1</sup>, Татьяна А. Быкова <sup>1</sup>, Елена И. Дарская <sup>1</sup>, Мария Д. Владовская <sup>1</sup>, Борис И. Смирнов <sup>1</sup>, Иван С. Моисеев <sup>1</sup>, Сергей Н. Бондаренко <sup>1</sup>, Людмила С. Зубаровская <sup>1</sup>, Николай Н. Климко <sup>2</sup>, Борис В. Афанасьев <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Юлия А. Рогачева 1, Марина О. Попова 1, Анастасия С. Фролова 1, Инна В. Маркова 1, Алиса Г. Волкова 1, Кирилл А. Екушев 1, Ольга Н. Пинегина 1, Олеся В. Паина 1, Татьяна А. Быкова 1, Елена И. Дарская 1, Мария Д. Владовская 1, Борис И. Смирнов 1, Иван С. Моисеев 1, Сергей Н. Бондаренко 1, Людмила С. Зубаровская 1, Николай Н. Климко 2, Борис В. Афанасьев 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20628
[VALUE] => Array
(
[TEXT] => <sup>1</sup> НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия<br>
<sup>2</sup> ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И. И. Мечникова», Санкт-Петербург, Россия<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
2 ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И. И. Мечникова», Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20629
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Инвазивный кандизоз/кандидемия – редкий инвазивный микоз, при этом связан с высоким уровнем летальности у пациентов с гематологическими заболеваниями. Кандидемия особенно часто наблюдается у пациентов, которые госпитализируются на долгий период, получающих химиотерапию (ХТ), трансплантацию гемопоэтических стволовых клеток (ТГСК). Целью нашего исследования было изучить эпидемиологию кандидемии у большой когорты реципиентов гемопоэтических стволовых клеток в течение десятилетнего периода высокой трансплантационной активности НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
2430 трансплантаций гемопоэтических стволовых клеток выполнены в клинике CIC725 в период с 2008 по 2017 год: 1647 аллогенных ТГСК (алло-ТГСК) и 783 аутологичных ТГСК (ауто-ТГСК). Ретроспективное исследование включает 26 случаев кандидемии у пациентов с гематологическими заболеваниями реципиентов ТГСК. Критерии EORTC/MSG 2008 были использованы для постановки диагноза кандидемии также, как и для оценки ответа на терапию.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Частота кандидемии за 10-летний период у реципиентов ТГСК составила 1%: у пациентов после алло-ТГСК частота составила 1,2%, при ауто-ТГСК – 0,7%. Основным заболеванием у реципиентов ТГСК с кандидемией был острый лейкоз у 65% (n=17) пациентов. Медиана возраста – 10 лет (1 месяц-59 лет). В исследуемой популяции алло-ТГСК была выполнена от неродственного донора у 50% (n=13) пациентов, гапло-ТГСК – 26% (n=6) и ауто-ТГСК – 24% (n=6). Полная ремиссия на момент трансплантации не была достигнута у 27% (n=7) пациентов. Первичная противогрибковая профилактика включала назначение флуконазола – 35% (n=9), эхинокандинов – 15% (n=4), без профилактики ув 23% (n=6) пациентов; в качестве вторичной профилактики был использован вориконазол у 27% (n=7) пациентов. Медиана дня возникновения кандидемии оставила 109 дней после алло-ТГСК (3-1337) и 20 дней (8-33) после ауто-ТГСК. Наиболее частым возбудителем были грибы Candida parapsilosis (38%). Этиология кандидемий представлена на рисунке 1. Фебрильная лихорадка была главным клиническим симптомом. Септический синдром развился в 60% случаев. Общая выживаемость (ОВ) в течение 30 дней от диагностики кандидемии составила 65%. При использовании эхинокандинов в качестве стартовой терапии ОВ в течение 30 дней составила 100%, и 65% у пациентов с применением других противогрибковых препаратов (p=0,09). Удаление центрального венозного катетера (ЦВК) при диагностике кандидемии – единственный фактор, достоверно, улучшающий общую 30-дневную выживаемость (91% vs 17%; р =0,001).
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Частота кандидемий у реципиентов ТГСК в течение 10-летнего периода наблюдения составила 1%: 1,2% у пациентов после алло-ТГСК и 0,7% после ауто-ТГСК. Общая 30-дневная выживаемость с момента постановки диагноза составила 65%. Удаление ЦВК улучшает общую выживаемость гематологических пациентов с кандидемией.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Кандидемия, гематологические больные, трансплантация гемопоэтических стволовых клеток, высокодозная химиотерапия, частота, общая выживаемость, эхинокандины, центральный венозный катетер.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Инвазивный кандизоз/кандидемия – редкий инвазивный микоз, при этом связан с высоким уровнем летальности у пациентов с гематологическими заболеваниями. Кандидемия особенно часто наблюдается у пациентов, которые госпитализируются на долгий период, получающих химиотерапию (ХТ), трансплантацию гемопоэтических стволовых клеток (ТГСК). Целью нашего исследования было изучить эпидемиологию кандидемии у большой когорты реципиентов гемопоэтических стволовых клеток в течение десятилетнего периода высокой трансплантационной активности НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета.
Материалы и методы
2430 трансплантаций гемопоэтических стволовых клеток выполнены в клинике CIC725 в период с 2008 по 2017 год: 1647 аллогенных ТГСК (алло-ТГСК) и 783 аутологичных ТГСК (ауто-ТГСК). Ретроспективное исследование включает 26 случаев кандидемии у пациентов с гематологическими заболеваниями реципиентов ТГСК. Критерии EORTC/MSG 2008 были использованы для постановки диагноза кандидемии также, как и для оценки ответа на терапию.
Результаты
Частота кандидемии за 10-летний период у реципиентов ТГСК составила 1%: у пациентов после алло-ТГСК частота составила 1,2%, при ауто-ТГСК – 0,7%. Основным заболеванием у реципиентов ТГСК с кандидемией был острый лейкоз у 65% (n=17) пациентов. Медиана возраста – 10 лет (1 месяц-59 лет). В исследуемой популяции алло-ТГСК была выполнена от неродственного донора у 50% (n=13) пациентов, гапло-ТГСК – 26% (n=6) и ауто-ТГСК – 24% (n=6). Полная ремиссия на момент трансплантации не была достигнута у 27% (n=7) пациентов. Первичная противогрибковая профилактика включала назначение флуконазола – 35% (n=9), эхинокандинов – 15% (n=4), без профилактики ув 23% (n=6) пациентов; в качестве вторичной профилактики был использован вориконазол у 27% (n=7) пациентов. Медиана дня возникновения кандидемии оставила 109 дней после алло-ТГСК (3-1337) и 20 дней (8-33) после ауто-ТГСК. Наиболее частым возбудителем были грибы Candida parapsilosis (38%). Этиология кандидемий представлена на рисунке 1. Фебрильная лихорадка была главным клиническим симптомом. Септический синдром развился в 60% случаев. Общая выживаемость (ОВ) в течение 30 дней от диагностики кандидемии составила 65%. При использовании эхинокандинов в качестве стартовой терапии ОВ в течение 30 дней составила 100%, и 65% у пациентов с применением других противогрибковых препаратов (p=0,09). Удаление центрального венозного катетера (ЦВК) при диагностике кандидемии – единственный фактор, достоверно, улучшающий общую 30-дневную выживаемость (91% vs 17%; р =0,001).
Заключение
Частота кандидемий у реципиентов ТГСК в течение 10-летнего периода наблюдения составила 1%: 1,2% у пациентов после алло-ТГСК и 0,7% после ауто-ТГСК. Общая 30-дневная выживаемость с момента постановки диагноза составила 65%. Удаление ЦВК улучшает общую выживаемость гематологических пациентов с кандидемией.
Ключевые слова
Кандидемия, гематологические больные, трансплантация гемопоэтических стволовых клеток, высокодозная химиотерапия, частота, общая выживаемость, эхинокандины, центральный венозный катетер.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20630
[VALUE] => Array
(
[TEXT] => Yulia A. Rogacheva <sup>1</sup>, Marina O. Popova <sup>1</sup>, Anastasia S. Frolova <sup>1</sup>, Inna V. Markova <sup>1</sup>, Alisa G. Volkova <sup>1</sup>, Kirill A. Ekushev <sup>1</sup>, Olga N. Pinegina <sup>1</sup>, Olesya V. Paina <sup>1</sup>,Tatyana A. Bykova <sup>1</sup>, Elena I. Darskaya <sup>1</sup>, Maria D. Vladovskaya <sup>1</sup>, Boris I. Smirnov <sup>1</sup>, Ivan S. Moiseev <sup>1</sup>, Sergey N. Bondarenko <sup>1</sup>, Ludmila S. Zubarovskaya <sup>1</sup>, Nikolay N. Klimko <sup>2</sup>, Boris V. Afanasyev <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Yulia A. Rogacheva 1, Marina O. Popova 1, Anastasia S. Frolova 1, Inna V. Markova 1, Alisa G. Volkova 1, Kirill A. Ekushev 1, Olga N. Pinegina 1, Olesya V. Paina 1,Tatyana A. Bykova 1, Elena I. Darskaya 1, Maria D. Vladovskaya 1, Boris I. Smirnov 1, Ivan S. Moiseev 1, Sergey N. Bondarenko 1, Ludmila S. Zubarovskaya 1, Nikolay N. Klimko 2, Boris V. Afanasyev 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20631
[VALUE] => Array
(
[TEXT] => <sup>1</sup> Raisa Gorbacheva Institute of Children Oncology, Hematology and Transplantation, and Chair of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia<br>
<sup>2</sup> I. I. Mechnikov North-Western State Medical University, St. Petersburg, Russia<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Raisa Gorbacheva Institute of Children Oncology, Hematology and Transplantation, and Chair of Hematology, Transfusiology and Transplantology, The First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
2 I. I. Mechnikov North-Western State Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20632
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Invasive candidiasis/candidemia is a rare invasive fungal disease, however, associated with high mortality rates in hematological patients. Candidemia has been observed particularly among patients hospitalized for a long periods who have been on chemotherapy, including hematopoietic stem cell transplantation (HSCT). The aim of our study was to estimate epidemiology of candidemia in large HSCT recipients’ cohort for the 10-year period transplant activity in R. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation of First Pavlov State Medical University of St. Petersburg.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
2430 stem cell transplantations have been performed at our BMT center (CIC 725) between 2008 and 2017 including 1647 allogeneic and 783 autologous HSCTs. A retrospective study included 26 cases of candidemia in the period of time in patients with hematological malignances and non-malignant hematological diseases after HSCT. EORTC/MSG 2008 criteria were used for the diagnosis of proven candidemia as well as to evaluate response to therapy.
</p>
<h3 style="text-align: justify;">Candida etiology</h3>
<p style="text-align: justify;">
<img width="500" alt="40_figure 1.png" src="/upload/medialibrary/e13/40_figure-1.png" title="40_figure 1.png"><br>
<span style="font-family: Cuprum, sans-serif; font-size: 26px;">Figure 1. Etiology of candidemia in patients following</span><span style="font-family: Cuprum, sans-serif; font-size: 26px;">
hematopoietic transplantation<br>
</span>
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Incidence of candidemia for the 10-year period of high transplant activity was 1%: 1.2% in allo-HSCT recipients (n=20/1647), 0.7%, in auto-HSCTs (6/783). The most frequent underlying diseases were acute leukemias (65%, n=17). The median age was 10 y.o. (range, 1 month to 59 years). In the study population, allo-HSCT from unrelated donors was performed in 50% (n=13); haplo-HSCT, in 26% (n=7), and auto-HSCT, in 24% (n=6). Patients had no complete remission at the moment of HSCT in 27% (n=7). As a primary antifungal prophylaxis, the patients received fluconazole (35%, n=9); echinocandins (15%, n=4). 6 patients (23%) were without specific prophylaxis, and voriconazole was applied as secondary prophylaxis in 27% (n=7). The median term for candidemia registration was 109 days after allo-HSCT (range, 3 to 1337) versus 20 days after auto-HSCT (range, 8-33). Candida parapsilosis was the main pathogen revealed (38% of the cases). Spectrum of different Candida species found is shown in Fig. 1. Febrile fever was the main clinical symptom, whereas septic syndrome developed in 60% of cases. Overall survival (OS) at 30 days from the diagnosis of candidemia was 65%. OS at 30 days in patients with echinocandins as antifungal therapy in first line was 100%, versus 65% in cases with other therapies (p=0.09). Removal of central venous catheter (CVC) was the only factor that significantly improved OS at 30 days after candidemia diagnosis (91% vs 17%, p=0.001).
</p>
<h2 style="text-align: justify;">Conclusions</h2>
<p style="text-align: justify;">
Incidence of candidemia over 10 years of observation was 1%: 1.2% in allo-HSCT recipients, 0.7% after auto-HSCT. Overall survival at 30 days from the diagnosis of candidemia was 65%. Removing the central venous catheter caused OS improvement in hematological patients with candidemia.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Candidemia, hematological patients, hematopoietic stem cell transplantation, high-dose chemotherapy, incidence, overall survival, echinocandins, central venous catheter (CVC).
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Invasive candidiasis/candidemia is a rare invasive fungal disease, however, associated with high mortality rates in hematological patients. Candidemia has been observed particularly among patients hospitalized for a long periods who have been on chemotherapy, including hematopoietic stem cell transplantation (HSCT). The aim of our study was to estimate epidemiology of candidemia in large HSCT recipients’ cohort for the 10-year period transplant activity in R. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation of First Pavlov State Medical University of St. Petersburg.
Patients and methods
2430 stem cell transplantations have been performed at our BMT center (CIC 725) between 2008 and 2017 including 1647 allogeneic and 783 autologous HSCTs. A retrospective study included 26 cases of candidemia in the period of time in patients with hematological malignances and non-malignant hematological diseases after HSCT. EORTC/MSG 2008 criteria were used for the diagnosis of proven candidemia as well as to evaluate response to therapy.
Candida etiology

Figure 1. Etiology of candidemia in patients following
hematopoietic transplantation
Results
Incidence of candidemia for the 10-year period of high transplant activity was 1%: 1.2% in allo-HSCT recipients (n=20/1647), 0.7%, in auto-HSCTs (6/783). The most frequent underlying diseases were acute leukemias (65%, n=17). The median age was 10 y.o. (range, 1 month to 59 years). In the study population, allo-HSCT from unrelated donors was performed in 50% (n=13); haplo-HSCT, in 26% (n=7), and auto-HSCT, in 24% (n=6). Patients had no complete remission at the moment of HSCT in 27% (n=7). As a primary antifungal prophylaxis, the patients received fluconazole (35%, n=9); echinocandins (15%, n=4). 6 patients (23%) were without specific prophylaxis, and voriconazole was applied as secondary prophylaxis in 27% (n=7). The median term for candidemia registration was 109 days after allo-HSCT (range, 3 to 1337) versus 20 days after auto-HSCT (range, 8-33). Candida parapsilosis was the main pathogen revealed (38% of the cases). Spectrum of different Candida species found is shown in Fig. 1. Febrile fever was the main clinical symptom, whereas septic syndrome developed in 60% of cases. Overall survival (OS) at 30 days from the diagnosis of candidemia was 65%. OS at 30 days in patients with echinocandins as antifungal therapy in first line was 100%, versus 65% in cases with other therapies (p=0.09). Removal of central venous catheter (CVC) was the only factor that significantly improved OS at 30 days after candidemia diagnosis (91% vs 17%, p=0.001).
Conclusions
Incidence of candidemia over 10 years of observation was 1%: 1.2% in allo-HSCT recipients, 0.7% after auto-HSCT. Overall survival at 30 days from the diagnosis of candidemia was 65%. Removing the central venous catheter caused OS improvement in hematological patients with candidemia.
Keywords
Candidemia, hematological patients, hematopoietic stem cell transplantation, high-dose chemotherapy, incidence, overall survival, echinocandins, central venous catheter (CVC).
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20633
[VALUE] => Candidemia in hematological patients after hematopoietic stem cell transplantation
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Candidemia in hematological patients after hematopoietic stem cell transplantation
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20809
[VALUE] => 1447
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1447
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20810
[VALUE] => 1448
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1448
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Юлия А. Рогачева 1, Марина О. Попова 1, Анастасия С. Фролова 1, Инна В. Маркова 1, Алиса Г. Волкова 1, Кирилл А. Екушев 1, Ольга Н. Пинегина 1, Олеся В. Паина 1, Татьяна А. Быкова 1, Елена И. Дарская 1, Мария Д. Владовская 1, Борис И. Смирнов 1, Иван С. Моисеев 1, Сергей Н. Бондаренко 1, Людмила С. Зубаровская 1, Николай Н. Климко 2, Борис В. Афанасьев 1
2 ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И. И. Мечникова», Санкт-Петербург, Россия
Введение
Инвазивный кандизоз/кандидемия – редкий инвазивный микоз, при этом связан с высоким уровнем летальности у пациентов с гематологическими заболеваниями. Кандидемия особенно часто наблюдается у пациентов, которые госпитализируются на долгий период, получающих химиотерапию (ХТ), трансплантацию гемопоэтических стволовых клеток (ТГСК). Целью нашего исследования было изучить эпидемиологию кандидемии у большой когорты реципиентов гемопоэтических стволовых клеток в течение десятилетнего периода высокой трансплантационной активности НИИ Детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета.
Материалы и методы
2430 трансплантаций гемопоэтических стволовых клеток выполнены в клинике CIC725 в период с 2008 по 2017 год: 1647 аллогенных ТГСК (алло-ТГСК) и 783 аутологичных ТГСК (ауто-ТГСК). Ретроспективное исследование включает 26 случаев кандидемии у пациентов с гематологическими заболеваниями реципиентов ТГСК. Критерии EORTC/MSG 2008 были использованы для постановки диагноза кандидемии также, как и для оценки ответа на терапию.
Результаты
Частота кандидемии за 10-летний период у реципиентов ТГСК составила 1%: у пациентов после алло-ТГСК частота составила 1,2%, при ауто-ТГСК – 0,7%. Основным заболеванием у реципиентов ТГСК с кандидемией был острый лейкоз у 65% (n=17) пациентов. Медиана возраста – 10 лет (1 месяц-59 лет). В исследуемой популяции алло-ТГСК была выполнена от неродственного донора у 50% (n=13) пациентов, гапло-ТГСК – 26% (n=6) и ауто-ТГСК – 24% (n=6). Полная ремиссия на момент трансплантации не была достигнута у 27% (n=7) пациентов. Первичная противогрибковая профилактика включала назначение флуконазола – 35% (n=9), эхинокандинов – 15% (n=4), без профилактики ув 23% (n=6) пациентов; в качестве вторичной профилактики был использован вориконазол у 27% (n=7) пациентов. Медиана дня возникновения кандидемии оставила 109 дней после алло-ТГСК (3-1337) и 20 дней (8-33) после ауто-ТГСК. Наиболее частым возбудителем были грибы Candida parapsilosis (38%). Этиология кандидемий представлена на рисунке 1. Фебрильная лихорадка была главным клиническим симптомом. Септический синдром развился в 60% случаев. Общая выживаемость (ОВ) в течение 30 дней от диагностики кандидемии составила 65%. При использовании эхинокандинов в качестве стартовой терапии ОВ в течение 30 дней составила 100%, и 65% у пациентов с применением других противогрибковых препаратов (p=0,09). Удаление центрального венозного катетера (ЦВК) при диагностике кандидемии – единственный фактор, достоверно, улучшающий общую 30-дневную выживаемость (91% vs 17%; р =0,001).
Заключение
Частота кандидемий у реципиентов ТГСК в течение 10-летнего периода наблюдения составила 1%: 1,2% у пациентов после алло-ТГСК и 0,7% после ауто-ТГСК. Общая 30-дневная выживаемость с момента постановки диагноза составила 65%. Удаление ЦВК улучшает общую выживаемость гематологических пациентов с кандидемией.
Ключевые слова
Кандидемия, гематологические больные, трансплантация гемопоэтических стволовых клеток, высокодозная химиотерапия, частота, общая выживаемость, эхинокандины, центральный венозный катетер.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20565
[VALUE] => Array
(
[TEXT] => Иван С. Моисеев <sup>1</sup>, Елена В. Бабенко <sup>1</sup>, Ольга С. Епифановская <sup>1</sup>, Анна А. Доценко <sup>1</sup>, Владислав С. Сергеев <sup>1</sup>, Елена А. Суркова <sup>2</sup>, Дарья А. Кузнецова <sup>2</sup>, Сергей В. Лапин <sup>2</sup>, Елена И. Дарская <sup>1</sup>, Елена В. Морозова <sup>1</sup>, Серегй Н. Бондаренко <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Иван С. Моисеев 1, Елена В. Бабенко 1, Ольга С. Епифановская 1, Анна А. Доценко 1, Владислав С. Сергеев 1, Елена А. Суркова 2, Дарья А. Кузнецова 2, Сергей В. Лапин 2, Елена И. Дарская 1, Елена В. Морозова 1, Серегй Н. Бондаренко 1, Борис В. Афанасьев 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20566
[VALUE] => Array
(
[TEXT] => <sup>1</sup> НИИ Детской Онкологии, Гематологии и Трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова<br>
<sup>2</sup> Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 НИИ Детской Онкологии, Гематологии и Трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова
2 Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20567
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
В настоящий момент существует ряд биомаркеров, которые обладают прогностическим значением в отношении реакции «трансплантат против хозяина» (РТПХ), трансплантационной летальности (ТЛ) и рецидивов основного заболевания. Однако, валидация этих биомаркеров преимущественно выполнялась после классической профилактики РТПХ, включающий ингибитор кальциневрина, метотрексат/микофенолат и антитимоцитарный глобулин при неродственных трансплантациях. Число исследований прогностического значения биомаркеров после посттрансплантационного циклофосфана (ПТЦф) крайне ограничено.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
С 2015 по 2016 было проведено проспективное исследование с включением 79 реципиентов аллогенной трансплантации гемопоэтических стволовых клеток (ТГСК). В исследование были включены только пациенты в ремиссии острого лейкоза, 34% с острым лимфобластным лейкозом, 66% с острым миелобластным. В первой ремиссии ТГСК выполнялась 68% пациентов, во второй – 27%, в третьей – 5%. Двадцати шести пациентам выполнена ТГСК от родственного донора с источником трансплантата – костный мозг, 53 – выполнена неродственная ТГСК с источником трансплантата – стволовые клетки периферической крови. Профилактика РТПХ при родственных включала только ПТЦф 50 мг/кг в Д+3,+4 без дальнейшей иммуносупрессии, при неродственных – комбинацию ПТЦф, такролимуса и микофенолата мофетила. Медиана возраста составила 35 лет (диапазон 18-59). Было проведено расширенное исследование трансплантата методом проточной цитометрии (цитометр FACS ARIA II, моноклональные антитела Miltenyi biotec). Исследовалось наличие следующих популяций лимфоцитов: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Т-регуляторы, дубль-позитивные Т-клетки, дубль-негативные Т-клетки, TCRalpha/beta, Т-клетки памяти TCR v11. Также исследовались замороженные образцы плазмы методом ИФА: VEGF A в Д0, растворимый рецептор к ФНОальфа, ИЛ-8, ИЛL-6, растворимый рецептор к ИЛ-2 (ИЛ-2Р) в Д+7, и ST2, ИЛ-17, растворимый рецептор к ФНОальфа в Д+21-30 (образец после приживления).
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
При медиане наблюдения 15 месяцев общая выживаемость (ОВ) в исследуемой группе составила 79%, трансплантационная летальность – 6%, частота рецидивов – 20%, бессобытийная выживаемость – 75%, острая РТПХ II-IV степени – 13%, III-IV степени – 5%, хроническая РТПХ средней и тяжелой степени – 22%. Трансплантационная летальность в группе пациентов с РТПХ составила 0%. Несмотря на то, что в ROC анализе содержание Трег (AUC 0.608), CD4 (0.628) и iNKT (0.630) в трансплантате имели предиктивное значение, различия были не значимы из-за низкой частоты РТПХ (р>0.07). Прогностическим значением в отношении хронической РТПХ обладал ИЛ-17 при измерении на Д+30 (AUC 0.615, 57% против 29%, р=0.017). Наиболее прогностическими популяциями в трансплантате в отшении ОВ были CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613дубль-позитивные T-клетки (AUC 0.657). Прогностическая значимость цитокинов в отношении ОВ была ограничена, за исключением ИЛ-2Р (AUC 0.610). Различия в ОВ в основном были связаны с рецидивом основного заболевания. Например, содержание CD8 клеток в трансплантате >18% достоверно повышало вероятность рецидива (53% vs 12%, p<0.001). Такой же тренд наблюдался и для других популяций. Наблюдаемый фенотип со сниженной реакцией трансплантат-против-лейкоза наблюдался независимо от источника трансплантата (р=0.57), развития острой (р=0.37) или хронической РТПХ (р=0.50).
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Исследованные биомаркеры РТПХ обладали ограниченным прогностическим значением после родственных и неродственных ТГСК с ПТЦф, что связано с низкой частотой развития этого осложнения и нулевой РТПХ-ассоциированной летальностью. Тем не менее, было выявлено, что пацинты, которым выполнена трансфузия трансплантата с высоким содержанием эффекторных популяций лимфоцитов, имели повышенный риск рецидива после трансплантации. Биологическое обоснование этому феномену может быть получено в дальнейших исследованиях иммунной реконституции этих популяций.
</p>
<h2 style="text-align: justify;">Конфликт интересов</h2>
<p style="text-align: justify;">
Данное исследование проведено при поддержке РФФИ, грант № 16-34-60142 мол_а_дк.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Трансплантация гемопоэтических клеток, реакция «трансплантат против хозяина», циклофосфамид, профилактика, биомаркеры, эффективность.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
В настоящий момент существует ряд биомаркеров, которые обладают прогностическим значением в отношении реакции «трансплантат против хозяина» (РТПХ), трансплантационной летальности (ТЛ) и рецидивов основного заболевания. Однако, валидация этих биомаркеров преимущественно выполнялась после классической профилактики РТПХ, включающий ингибитор кальциневрина, метотрексат/микофенолат и антитимоцитарный глобулин при неродственных трансплантациях. Число исследований прогностического значения биомаркеров после посттрансплантационного циклофосфана (ПТЦф) крайне ограничено.
Пациенты и методы
С 2015 по 2016 было проведено проспективное исследование с включением 79 реципиентов аллогенной трансплантации гемопоэтических стволовых клеток (ТГСК). В исследование были включены только пациенты в ремиссии острого лейкоза, 34% с острым лимфобластным лейкозом, 66% с острым миелобластным. В первой ремиссии ТГСК выполнялась 68% пациентов, во второй – 27%, в третьей – 5%. Двадцати шести пациентам выполнена ТГСК от родственного донора с источником трансплантата – костный мозг, 53 – выполнена неродственная ТГСК с источником трансплантата – стволовые клетки периферической крови. Профилактика РТПХ при родственных включала только ПТЦф 50 мг/кг в Д+3,+4 без дальнейшей иммуносупрессии, при неродственных – комбинацию ПТЦф, такролимуса и микофенолата мофетила. Медиана возраста составила 35 лет (диапазон 18-59). Было проведено расширенное исследование трансплантата методом проточной цитометрии (цитометр FACS ARIA II, моноклональные антитела Miltenyi biotec). Исследовалось наличие следующих популяций лимфоцитов: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Т-регуляторы, дубль-позитивные Т-клетки, дубль-негативные Т-клетки, TCRalpha/beta, Т-клетки памяти TCR v11. Также исследовались замороженные образцы плазмы методом ИФА: VEGF A в Д0, растворимый рецептор к ФНОальфа, ИЛ-8, ИЛL-6, растворимый рецептор к ИЛ-2 (ИЛ-2Р) в Д+7, и ST2, ИЛ-17, растворимый рецептор к ФНОальфа в Д+21-30 (образец после приживления).
Результаты
При медиане наблюдения 15 месяцев общая выживаемость (ОВ) в исследуемой группе составила 79%, трансплантационная летальность – 6%, частота рецидивов – 20%, бессобытийная выживаемость – 75%, острая РТПХ II-IV степени – 13%, III-IV степени – 5%, хроническая РТПХ средней и тяжелой степени – 22%. Трансплантационная летальность в группе пациентов с РТПХ составила 0%. Несмотря на то, что в ROC анализе содержание Трег (AUC 0.608), CD4 (0.628) и iNKT (0.630) в трансплантате имели предиктивное значение, различия были не значимы из-за низкой частоты РТПХ (р>0.07). Прогностическим значением в отношении хронической РТПХ обладал ИЛ-17 при измерении на Д+30 (AUC 0.615, 57% против 29%, р=0.017). Наиболее прогностическими популяциями в трансплантате в отшении ОВ были CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613дубль-позитивные T-клетки (AUC 0.657). Прогностическая значимость цитокинов в отношении ОВ была ограничена, за исключением ИЛ-2Р (AUC 0.610). Различия в ОВ в основном были связаны с рецидивом основного заболевания. Например, содержание CD8 клеток в трансплантате >18% достоверно повышало вероятность рецидива (53% vs 12%, p<0.001). Такой же тренд наблюдался и для других популяций. Наблюдаемый фенотип со сниженной реакцией трансплантат-против-лейкоза наблюдался независимо от источника трансплантата (р=0.57), развития острой (р=0.37) или хронической РТПХ (р=0.50).
Заключение
Исследованные биомаркеры РТПХ обладали ограниченным прогностическим значением после родственных и неродственных ТГСК с ПТЦф, что связано с низкой частотой развития этого осложнения и нулевой РТПХ-ассоциированной летальностью. Тем не менее, было выявлено, что пацинты, которым выполнена трансфузия трансплантата с высоким содержанием эффекторных популяций лимфоцитов, имели повышенный риск рецидива после трансплантации. Биологическое обоснование этому феномену может быть получено в дальнейших исследованиях иммунной реконституции этих популяций.
Конфликт интересов
Данное исследование проведено при поддержке РФФИ, грант № 16-34-60142 мол_а_дк.
Ключевые слова
Трансплантация гемопоэтических клеток, реакция «трансплантат против хозяина», циклофосфамид, профилактика, биомаркеры, эффективность.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20568
[VALUE] => Array
(
[TEXT] => Ivan S. Moiseev <sup>1</sup>, Elena V. Babenko <sup>1</sup>, Olga S. Epifanovskaya <sup>1</sup>, Anna A. Dotsenko <sup>1</sup>, Vladislav S. Sergeev <sup>1</sup>, Elena A. Surkova <sup>2</sup>, Daria A. Kuznetcova <sup>2</sup>, Sergey V. Lapin <sup>2</sup>, Elena I. Darskaya <sup>1</sup>, Elena V. Morozova <sup>1</sup>,Sergey N. Bondarenko <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Ivan S. Moiseev 1, Elena V. Babenko 1, Olga S. Epifanovskaya 1, Anna A. Dotsenko 1, Vladislav S. Sergeev 1, Elena A. Surkova 2, Daria A. Kuznetcova 2, Sergey V. Lapin 2, Elena I. Darskaya 1, Elena V. Morozova 1,Sergey N. Bondarenko 1, Boris V. Afanasyev 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20569
[VALUE] => Array
(
[TEXT] => <sup>1</sup> R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation<br>
<sup>2</sup> Laboratory of Autoimmune Diagnostics, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation
2 Laboratory of Autoimmune Diagnostics, Pavlov First St. Petersburg State Medical University, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20570
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
There are a number of biomarkers that predict non-relapse mortality (NRM), graft-versus-host disease (GVHD) and relapse incidence (RI) after conventional GVHD prophylaxis based on calcineurin inhibitors with or without antithymocyte globulin. The biologic mechanisms behind the prophylaxis with posttransplantation cyclophosphamide (PTCy) might be different. Currently there is limited data whether the conventional predictive biomarkers work with this type of prophylaxis.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
We conducted a prospective single-center study between 2015 and 2016 in 79 patients. 34% of patients had acute lymphoblastic leukemia, 66% – acute myeloblastic. 68% of patients were in the first complete remission, 27% – in the 2nd and 5% – in the 3rd. 26 received matched related bone marrow (BM) graft with single-agent PTCy GVHD prophylaxis and 53 received unrelated peripheral blood stem cell graft (PBSC) with PTCy, tacrolimus and MMF prophylaxis. Median age was 35 years (range 18-59). The graft was studies extensively studied by flow cytometry (cytometer FACS Aria II, antibodies by Miltenyi biotec). The following populations were analysed: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Treg, double-positive T-cells, double-negative T-cells, TCRalpha/beta, TCR v11 memory cells. The frozen plasma from day +0 was analysed by ELISA (commercial kits by eBioscience) for VEGF A, from day +7 for soluble TNF receptor, IL-8, IL-6, soluble IL-2 receptor, from day+21-30 (after engraftment sample) for ST2, IL-17, soluble TNF receptor. The above mentioned biomarkers were tested in logisted regression for predictive value regarding GVHD and overall survival (OS).
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
With median follow-up of 15 months overall survival in the study group was 79%, NRM 6%, RI 20%, event-free-survival 75%, acute GVHD grade II-IV 13%, grade III-IV 5%, moderate and severe chronic GVHD 22%. NRM in patients with GVHD was 0%. Despite some predictive value in ROC analysis for acute GVHD of Treg (AUC 0.608), % of CD4 (0.628) and iNKT (0.630), the difference in the GVHD rate was not significant due to small number of events (p>0.07). The predictive biomarker of chronic GVHD was IL-17 measured on day +30 (AUC 0.615), with increased incidence of 57% vs 29%, p=0.017 in patients with elevated level. The most predictive populations for OS were CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613), double-positive T-cells (AUC 0.657). Measured cytokines had lower predictive value for OS than graft composition, except IL-2 receptor (AUC 0.610). The differences in OS was predominantly due to RI. For example, presence of CD8 cells >18% significantly increased the risk of relapse (53% vs 12%, p<0.001). The same trend was observed for other populations. This phenotype with reduced graft-versus-leukemia was independent of the graft source (p=0.57) and occurrence of acute (p=0.37) and chronic GVHD (p=0.50).
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
The current biomarkers of acute GVHD has limited predictive value after related and unrelated grafts with PTCy, because of the low incidence of this complication and low GVHD-associated mortality. On the contrary we have observed that patients with high prevalence of effector cell populations in the graft have increased RI after transplantation. The explanation of this phenomenon could be elucidated during further studies that evaluate reconstitution of these populations.
</p>
<h2 style="text-align: justify;">Disclosure</h2>
<p style="text-align: justify;">
The reported study was funded by RFBR, according to the research project No. 16-34-60142 mol_а_dk.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Hematopoietic stem cell transplantation, graft-versus-host disease, cyclophosphamide prophylaxis, biomarkers, efficiency.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
There are a number of biomarkers that predict non-relapse mortality (NRM), graft-versus-host disease (GVHD) and relapse incidence (RI) after conventional GVHD prophylaxis based on calcineurin inhibitors with or without antithymocyte globulin. The biologic mechanisms behind the prophylaxis with posttransplantation cyclophosphamide (PTCy) might be different. Currently there is limited data whether the conventional predictive biomarkers work with this type of prophylaxis.
Patients and methods
We conducted a prospective single-center study between 2015 and 2016 in 79 patients. 34% of patients had acute lymphoblastic leukemia, 66% – acute myeloblastic. 68% of patients were in the first complete remission, 27% – in the 2nd and 5% – in the 3rd. 26 received matched related bone marrow (BM) graft with single-agent PTCy GVHD prophylaxis and 53 received unrelated peripheral blood stem cell graft (PBSC) with PTCy, tacrolimus and MMF prophylaxis. Median age was 35 years (range 18-59). The graft was studies extensively studied by flow cytometry (cytometer FACS Aria II, antibodies by Miltenyi biotec). The following populations were analysed: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Treg, double-positive T-cells, double-negative T-cells, TCRalpha/beta, TCR v11 memory cells. The frozen plasma from day +0 was analysed by ELISA (commercial kits by eBioscience) for VEGF A, from day +7 for soluble TNF receptor, IL-8, IL-6, soluble IL-2 receptor, from day+21-30 (after engraftment sample) for ST2, IL-17, soluble TNF receptor. The above mentioned biomarkers were tested in logisted regression for predictive value regarding GVHD and overall survival (OS).
Results
With median follow-up of 15 months overall survival in the study group was 79%, NRM 6%, RI 20%, event-free-survival 75%, acute GVHD grade II-IV 13%, grade III-IV 5%, moderate and severe chronic GVHD 22%. NRM in patients with GVHD was 0%. Despite some predictive value in ROC analysis for acute GVHD of Treg (AUC 0.608), % of CD4 (0.628) and iNKT (0.630), the difference in the GVHD rate was not significant due to small number of events (p>0.07). The predictive biomarker of chronic GVHD was IL-17 measured on day +30 (AUC 0.615), with increased incidence of 57% vs 29%, p=0.017 in patients with elevated level. The most predictive populations for OS were CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613), double-positive T-cells (AUC 0.657). Measured cytokines had lower predictive value for OS than graft composition, except IL-2 receptor (AUC 0.610). The differences in OS was predominantly due to RI. For example, presence of CD8 cells >18% significantly increased the risk of relapse (53% vs 12%, p<0.001). The same trend was observed for other populations. This phenotype with reduced graft-versus-leukemia was independent of the graft source (p=0.57) and occurrence of acute (p=0.37) and chronic GVHD (p=0.50).
Conclusion
The current biomarkers of acute GVHD has limited predictive value after related and unrelated grafts with PTCy, because of the low incidence of this complication and low GVHD-associated mortality. On the contrary we have observed that patients with high prevalence of effector cell populations in the graft have increased RI after transplantation. The explanation of this phenomenon could be elucidated during further studies that evaluate reconstitution of these populations.
Disclosure
The reported study was funded by RFBR, according to the research project No. 16-34-60142 mol_а_dk.
Keywords
Hematopoietic stem cell transplantation, graft-versus-host disease, cyclophosphamide prophylaxis, biomarkers, efficiency.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20571
[VALUE] => Screening for predictive biomarkers after related and unrelated grafts with posttransplantation cyclophosphamide in adult patients
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Screening for predictive biomarkers after related and unrelated grafts with posttransplantation cyclophosphamide in adult patients
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20793
[VALUE] => 1431
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1431
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20794
[VALUE] => 1432
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1432
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Иван С. Моисеев 1, Елена В. Бабенко 1, Ольга С. Епифановская 1, Анна А. Доценко 1, Владислав С. Сергеев 1, Елена А. Суркова 2, Дарья А. Кузнецова 2, Сергей В. Лапин 2, Елена И. Дарская 1, Елена В. Морозова 1, Серегй Н. Бондаренко 1, Борис В. Афанасьев 1
2 Лаборатория диагностики аутоиммунных заболеваний, Первый Санкт-Петербургский Государственный Медицинский Университет им. И. П. Павлова
Введение
В настоящий момент существует ряд биомаркеров, которые обладают прогностическим значением в отношении реакции «трансплантат против хозяина» (РТПХ), трансплантационной летальности (ТЛ) и рецидивов основного заболевания. Однако, валидация этих биомаркеров преимущественно выполнялась после классической профилактики РТПХ, включающий ингибитор кальциневрина, метотрексат/микофенолат и антитимоцитарный глобулин при неродственных трансплантациях. Число исследований прогностического значения биомаркеров после посттрансплантационного циклофосфана (ПТЦф) крайне ограничено.
Пациенты и методы
С 2015 по 2016 было проведено проспективное исследование с включением 79 реципиентов аллогенной трансплантации гемопоэтических стволовых клеток (ТГСК). В исследование были включены только пациенты в ремиссии острого лейкоза, 34% с острым лимфобластным лейкозом, 66% с острым миелобластным. В первой ремиссии ТГСК выполнялась 68% пациентов, во второй – 27%, в третьей – 5%. Двадцати шести пациентам выполнена ТГСК от родственного донора с источником трансплантата – костный мозг, 53 – выполнена неродственная ТГСК с источником трансплантата – стволовые клетки периферической крови. Профилактика РТПХ при родственных включала только ПТЦф 50 мг/кг в Д+3,+4 без дальнейшей иммуносупрессии, при неродственных – комбинацию ПТЦф, такролимуса и микофенолата мофетила. Медиана возраста составила 35 лет (диапазон 18-59). Было проведено расширенное исследование трансплантата методом проточной цитометрии (цитометр FACS ARIA II, моноклональные антитела Miltenyi biotec). Исследовалось наличие следующих популяций лимфоцитов: CD3, CD4, CD8, CD16CD56, NKT, iNKT, Т-регуляторы, дубль-позитивные Т-клетки, дубль-негативные Т-клетки, TCRalpha/beta, Т-клетки памяти TCR v11. Также исследовались замороженные образцы плазмы методом ИФА: VEGF A в Д0, растворимый рецептор к ФНОальфа, ИЛ-8, ИЛL-6, растворимый рецептор к ИЛ-2 (ИЛ-2Р) в Д+7, и ST2, ИЛ-17, растворимый рецептор к ФНОальфа в Д+21-30 (образец после приживления).
Результаты
При медиане наблюдения 15 месяцев общая выживаемость (ОВ) в исследуемой группе составила 79%, трансплантационная летальность – 6%, частота рецидивов – 20%, бессобытийная выживаемость – 75%, острая РТПХ II-IV степени – 13%, III-IV степени – 5%, хроническая РТПХ средней и тяжелой степени – 22%. Трансплантационная летальность в группе пациентов с РТПХ составила 0%. Несмотря на то, что в ROC анализе содержание Трег (AUC 0.608), CD4 (0.628) и iNKT (0.630) в трансплантате имели предиктивное значение, различия были не значимы из-за низкой частоты РТПХ (р>0.07). Прогностическим значением в отношении хронической РТПХ обладал ИЛ-17 при измерении на Д+30 (AUC 0.615, 57% против 29%, р=0.017). Наиболее прогностическими популяциями в трансплантате в отшении ОВ были CD3 (AUC 0.626), CD4 (AUC 0.628), CD8 (AUC 0.653), NKT (AUC 0.615), TCRalpha/beta (0.634), iNKT (0.615), iNKT CD8+ (0.613дубль-позитивные T-клетки (AUC 0.657). Прогностическая значимость цитокинов в отношении ОВ была ограничена, за исключением ИЛ-2Р (AUC 0.610). Различия в ОВ в основном были связаны с рецидивом основного заболевания. Например, содержание CD8 клеток в трансплантате >18% достоверно повышало вероятность рецидива (53% vs 12%, p<0.001). Такой же тренд наблюдался и для других популяций. Наблюдаемый фенотип со сниженной реакцией трансплантат-против-лейкоза наблюдался независимо от источника трансплантата (р=0.57), развития острой (р=0.37) или хронической РТПХ (р=0.50).
Заключение
Исследованные биомаркеры РТПХ обладали ограниченным прогностическим значением после родственных и неродственных ТГСК с ПТЦф, что связано с низкой частотой развития этого осложнения и нулевой РТПХ-ассоциированной летальностью. Тем не менее, было выявлено, что пацинты, которым выполнена трансфузия трансплантата с высоким содержанием эффекторных популяций лимфоцитов, имели повышенный риск рецидива после трансплантации. Биологическое обоснование этому феномену может быть получено в дальнейших исследованиях иммунной реконституции этих популяций.
Конфликт интересов
Данное исследование проведено при поддержке РФФИ, грант № 16-34-60142 мол_а_дк.
Ключевые слова
Трансплантация гемопоэтических клеток, реакция «трансплантат против хозяина», циклофосфамид, профилактика, биомаркеры, эффективность.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20574
[VALUE] => Array
(
[TEXT] => Ольга О. Молостова, Лариса Н. Шелихова, Мария А. Алябьева, Дмитрий Н. Балашов, Светлана А. Радыгина, Ирина И. Калинина, Михаил А. Масчан, Алексей А. Масчан
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Ольга О. Молостова, Лариса Н. Шелихова, Мария А. Алябьева, Дмитрий Н. Балашов, Светлана А. Радыгина, Ирина И. Калинина, Михаил А. Масчан, Алексей А. Масчан
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20575
[VALUE] => Array
(
[TEXT] => ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева», Москва, Россия<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева», Москва, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20576
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Рецидивы острых лейкозов и лимфом у реципиентов алло-ТГСК трудно поддаются лечению и прогноз пациентов крайне неутешителен. Основными проблемами остаются краткосрочные ремиссии после стандартной химиотерапии, «взрывное» развитие рецидива, сочетанная токсичность химиотерапии и первой ТГСК, отсутствие донора для повторной трансплантации. Возможная альтернатива стандартной химиотерапии – применение блокаторов PD-1, потенциирующих иммуный ответ, что позволяет рассчитывать на усиление эффекта «трансплантат против лейкемии» у пациентов с рецидивами онкогематологических заболеваний после аллогенной ТГСК. Целью наблюдения было оценить эффективность и безопасность применения ниволумаба у данной когорты пациентов.
</p>
<h2 style="text-align: justify;">Методы</h2>
<p style="text-align: justify;">
Мы ретроспективно проанализировали истории болезни 8 пациентов в возрасте от 3 до 14 лет, получивших терапию ингибиторами PD1 после ТГСК. 6 из них имели диагноз ОМЛ, 1 пациент – диагноз ОЛЛ, 1 пациент – диагноз гепатоспленическая γδ-Т-клеточная лимфома. На момент ТГСК 5 пациентов имели продвинутую стадию заболевания, 2 были в полной ремиссии, и 1 находился в MRD-позитивной ремиссии. Все пациенты получали аллогенную ТГСК (5 пациентов от гаплоидентичного донора, 3 пациента от HLA-идентичного сиблинга). На +30 сутки от ТГСК все пациенты находились в клинико-гематологической и молекулярной ремиссии. У 50% пациентов развилась острая РТПХ 1-2 степени с поражением кожи и ЖКТ. Среднее время до развития рецидива составило 180 (97-420) дней. Развернутый костно-мозговой рецидив был зафиксирован у 6 пациентов, у 2 пациентов был отмечен молекулярный рецидив. Все пациенты получили 1 инъекцию ниволумаба в дозе 3 мг/кг. Один пациент с ОМЛ получил инъекцию ниволумаба, уже находясь в ремиссии после повторной ТГСК, в связи с высоким риском повторного рецидива.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Нежелательные явления были зарегистрированы у 6 (75%) пациентов. У двух пациентов развился иммунный менингоэнцефалит, у 1 пациента – иммунный гепатит 4 степени, у 2 пациентов была отмечена РТПХ кожи 3й степени, у 4 пациентов развилась иммунная лихорадка. Четырем пациентам потребовалось назначение системной иммуносупрессивной терапии для борьбы с иммуноопосредованными реакциями. Связанной с токсичностью летальности отмечено не было. Для оценки эффективности терапии после первой инъекции ниволумаба всем пациентам были выполнены костномозговые пункции. Шесть из семи пациентов не ответили на терапию. Среднее время до прогрессирования заболевания составляло 21 день. У пациента 7 лет с ОМЛ, находящегося в ремиссии на момент введения ниволумаба, спустя 2 недели после введения развилась иммунная лихорадка и иммунный менингоэнцефалит с явлениями когнитивных расстройств, дизартрии, мышечной слабости, полностью разрешившийся на фоне пульс-терапии солу-медролом. В настоящее время спустя 1 год 10 месяцев после введения ниволумаба у пациента сохраняется морфологическая MRD негативная ремиссия, выраженной патологии со стороны органов и систем нет. Пациентка 7 лет, находившаяся в развернутом рецидиве ОЛЛ на момент введения ниволумаба, достигла стойкой ремиссии. Однако спустя 14 дней от введения препарата у ребенка развился аутоиммунный гепатит 4 степени, рефрактерный ко всем видам терапии, включая ТАО в СОД 6 Гр. В связи с прогрессирующим фатальным повреждением печени произведена успешная трансплантация печени от родственного донора, на сроке 1 год 3 месяца после введения ниволумаба сохраняется полная ремиссия.
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
Наш небольшой опыт показывает, что применение ингибиторов PD-1 после аллогенной ТГСК связано со значительной токсичностью. Для обеспечения безопасности и эффективности этого подхода требуются дальнейшие проспективные исследования.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Аллогенная ТГСК, ингибиторы PD1, рецидив, ОЛЛ, ОМЛ.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Введение
Рецидивы острых лейкозов и лимфом у реципиентов алло-ТГСК трудно поддаются лечению и прогноз пациентов крайне неутешителен. Основными проблемами остаются краткосрочные ремиссии после стандартной химиотерапии, «взрывное» развитие рецидива, сочетанная токсичность химиотерапии и первой ТГСК, отсутствие донора для повторной трансплантации. Возможная альтернатива стандартной химиотерапии – применение блокаторов PD-1, потенциирующих иммуный ответ, что позволяет рассчитывать на усиление эффекта «трансплантат против лейкемии» у пациентов с рецидивами онкогематологических заболеваний после аллогенной ТГСК. Целью наблюдения было оценить эффективность и безопасность применения ниволумаба у данной когорты пациентов.
Методы
Мы ретроспективно проанализировали истории болезни 8 пациентов в возрасте от 3 до 14 лет, получивших терапию ингибиторами PD1 после ТГСК. 6 из них имели диагноз ОМЛ, 1 пациент – диагноз ОЛЛ, 1 пациент – диагноз гепатоспленическая γδ-Т-клеточная лимфома. На момент ТГСК 5 пациентов имели продвинутую стадию заболевания, 2 были в полной ремиссии, и 1 находился в MRD-позитивной ремиссии. Все пациенты получали аллогенную ТГСК (5 пациентов от гаплоидентичного донора, 3 пациента от HLA-идентичного сиблинга). На +30 сутки от ТГСК все пациенты находились в клинико-гематологической и молекулярной ремиссии. У 50% пациентов развилась острая РТПХ 1-2 степени с поражением кожи и ЖКТ. Среднее время до развития рецидива составило 180 (97-420) дней. Развернутый костно-мозговой рецидив был зафиксирован у 6 пациентов, у 2 пациентов был отмечен молекулярный рецидив. Все пациенты получили 1 инъекцию ниволумаба в дозе 3 мг/кг. Один пациент с ОМЛ получил инъекцию ниволумаба, уже находясь в ремиссии после повторной ТГСК, в связи с высоким риском повторного рецидива.
Результаты
Нежелательные явления были зарегистрированы у 6 (75%) пациентов. У двух пациентов развился иммунный менингоэнцефалит, у 1 пациента – иммунный гепатит 4 степени, у 2 пациентов была отмечена РТПХ кожи 3й степени, у 4 пациентов развилась иммунная лихорадка. Четырем пациентам потребовалось назначение системной иммуносупрессивной терапии для борьбы с иммуноопосредованными реакциями. Связанной с токсичностью летальности отмечено не было. Для оценки эффективности терапии после первой инъекции ниволумаба всем пациентам были выполнены костномозговые пункции. Шесть из семи пациентов не ответили на терапию. Среднее время до прогрессирования заболевания составляло 21 день. У пациента 7 лет с ОМЛ, находящегося в ремиссии на момент введения ниволумаба, спустя 2 недели после введения развилась иммунная лихорадка и иммунный менингоэнцефалит с явлениями когнитивных расстройств, дизартрии, мышечной слабости, полностью разрешившийся на фоне пульс-терапии солу-медролом. В настоящее время спустя 1 год 10 месяцев после введения ниволумаба у пациента сохраняется морфологическая MRD негативная ремиссия, выраженной патологии со стороны органов и систем нет. Пациентка 7 лет, находившаяся в развернутом рецидиве ОЛЛ на момент введения ниволумаба, достигла стойкой ремиссии. Однако спустя 14 дней от введения препарата у ребенка развился аутоиммунный гепатит 4 степени, рефрактерный ко всем видам терапии, включая ТАО в СОД 6 Гр. В связи с прогрессирующим фатальным повреждением печени произведена успешная трансплантация печени от родственного донора, на сроке 1 год 3 месяца после введения ниволумаба сохраняется полная ремиссия.
Выводы
Наш небольшой опыт показывает, что применение ингибиторов PD-1 после аллогенной ТГСК связано со значительной токсичностью. Для обеспечения безопасности и эффективности этого подхода требуются дальнейшие проспективные исследования.
Ключевые слова
Аллогенная ТГСК, ингибиторы PD1, рецидив, ОЛЛ, ОМЛ.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20577
[VALUE] => Array
(
[TEXT] => Olga O. Molostova, Larisa N. Shelikhova, Mariya A. Alyabieva, Dmitry N. Balashov, Svetlana A. Radygina, Irina I. Kalinina, Michael A. Maschan, Alexei A. Maschan
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Olga O. Molostova, Larisa N. Shelikhova, Mariya A. Alyabieva, Dmitry N. Balashov, Svetlana A. Radygina, Irina I. Kalinina, Michael A. Maschan, Alexei A. Maschan
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20578
[VALUE] => Array
(
[TEXT] => Dmitriy Rogachev National Medical Research Center for Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Dmitriy Rogachev National Medical Research Center for Pediatric Hematology, Oncology and Immunology, Moscow, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20579
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Background</h2>
<p style="text-align: justify;">
Patients with posttransplant acute leukemia relapse are hardly curable and the outcome is extremely poor. The effectiveness of standard chemotherapy and donor lymphocyte infusions is limited. A possible alternative to standard chemotherapy and DLI is use of PD-1 inhibitors, which may potentiate the allogeneic immune response in order to harness graft-versus-leukemia effect.
</p>
<h2 style="text-align: justify;">Methods</h2>
<p style="text-align: justify;">
We analyzed retrospectively 8 patients, age 3 to 14 years, who had received therapy with PD-1-inhibitor after HSCT. The cohort included 6 patients with acute myeloid leukemia, 1 pt with acute lymphoblastic leukemia and 1 pt with hepatosplenic gamma/delta T cell lymphoma. At the moment of HSCT 5 patients had an advanced stage of their disease, 2 were in complete remission and 1 had positive minimal residual disease. All patients received allo-HSCT (5 patients from haploidentical donors, 3 patients from HLA-identical siblings). At day +30 after HSCT all patients were in clinical and molecular remission, 50% of the patients developed grade 1-2 acute GVHD with skin and GI impairment. The average time to relapse was 180 (97-420) days. Bone marrow relapse was detected in 6 patients while 2 patients had molecular relapse. All patients received 1 injection of nivolumab at a dose of 3 mg/kg. One patient with AML received the injection of nivolumab already being in the remission after second HSCT because of high risk of relapse.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Adverse events were registered in 6 (75%) patients. Two patients developed immune meningoencephalitis, 1 pt had grade 4 immune-mediated liver toxicity, 2 pt had grade 3 skin GVHD flare and immune fever was registered in 4 pts. Four patients required prolonged systemic immunosuppressive therapy to control immune-mediated adverse effects. No mortality related to checkpoint-inhibitor toxicity was registered. One patient developed progressive liver disease. Bone marrow aspiration was done to evaluate efficiency of therapy after the first injection of nivolumab. Seven patients were evaluable for response. Six of 7 patients did not respond to therapy. Average time to disease progression was 21 days. Stable remission was achieved in 1 patient with ALL who received injection of nivolumab being in the full-blown relapse after HSCT. One year and 3 months later this patient remains in clinical and molecular remission, although immune-mediated liver damage progressed to end-stage liver disease and patient received a successful liver transplantation. Patient with AML received the injection of nivolumab already being in the remission and 22 months after therapy remains in clinical and molecular remission.
</p>
<h2 style="text-align: justify;">Conclusions</h2>
<p style="text-align: justify;">
Our limited experience suggests that use of PD-1 inhibitors after allo-HSCT is associated with significant toxicity. Further prospective study is required to establish the safety and efficiency of this approach.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
PD-1 inhibitors, allo-HSCT, relapse, ALL, AML.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Background
Patients with posttransplant acute leukemia relapse are hardly curable and the outcome is extremely poor. The effectiveness of standard chemotherapy and donor lymphocyte infusions is limited. A possible alternative to standard chemotherapy and DLI is use of PD-1 inhibitors, which may potentiate the allogeneic immune response in order to harness graft-versus-leukemia effect.
Methods
We analyzed retrospectively 8 patients, age 3 to 14 years, who had received therapy with PD-1-inhibitor after HSCT. The cohort included 6 patients with acute myeloid leukemia, 1 pt with acute lymphoblastic leukemia and 1 pt with hepatosplenic gamma/delta T cell lymphoma. At the moment of HSCT 5 patients had an advanced stage of their disease, 2 were in complete remission and 1 had positive minimal residual disease. All patients received allo-HSCT (5 patients from haploidentical donors, 3 patients from HLA-identical siblings). At day +30 after HSCT all patients were in clinical and molecular remission, 50% of the patients developed grade 1-2 acute GVHD with skin and GI impairment. The average time to relapse was 180 (97-420) days. Bone marrow relapse was detected in 6 patients while 2 patients had molecular relapse. All patients received 1 injection of nivolumab at a dose of 3 mg/kg. One patient with AML received the injection of nivolumab already being in the remission after second HSCT because of high risk of relapse.
Results
Adverse events were registered in 6 (75%) patients. Two patients developed immune meningoencephalitis, 1 pt had grade 4 immune-mediated liver toxicity, 2 pt had grade 3 skin GVHD flare and immune fever was registered in 4 pts. Four patients required prolonged systemic immunosuppressive therapy to control immune-mediated adverse effects. No mortality related to checkpoint-inhibitor toxicity was registered. One patient developed progressive liver disease. Bone marrow aspiration was done to evaluate efficiency of therapy after the first injection of nivolumab. Seven patients were evaluable for response. Six of 7 patients did not respond to therapy. Average time to disease progression was 21 days. Stable remission was achieved in 1 patient with ALL who received injection of nivolumab being in the full-blown relapse after HSCT. One year and 3 months later this patient remains in clinical and molecular remission, although immune-mediated liver damage progressed to end-stage liver disease and patient received a successful liver transplantation. Patient with AML received the injection of nivolumab already being in the remission and 22 months after therapy remains in clinical and molecular remission.
Conclusions
Our limited experience suggests that use of PD-1 inhibitors after allo-HSCT is associated with significant toxicity. Further prospective study is required to establish the safety and efficiency of this approach.
Keywords
PD-1 inhibitors, allo-HSCT, relapse, ALL, AML.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20580
[VALUE] => Efficacy and safety of nivolumab-based therapy in children with relapse of hematologic malignancies after allogenic HSCT
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Efficacy and safety of nivolumab-based therapy in children with relapse of hematologic malignancies after allogenic HSCT
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20795
[VALUE] => 1433
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1433
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20796
[VALUE] => 1434
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1434
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Ольга О. Молостова, Лариса Н. Шелихова, Мария А. Алябьева, Дмитрий Н. Балашов, Светлана А. Радыгина, Ирина И. Калинина, Михаил А. Масчан, Алексей А. Масчан
Введение
Рецидивы острых лейкозов и лимфом у реципиентов алло-ТГСК трудно поддаются лечению и прогноз пациентов крайне неутешителен. Основными проблемами остаются краткосрочные ремиссии после стандартной химиотерапии, «взрывное» развитие рецидива, сочетанная токсичность химиотерапии и первой ТГСК, отсутствие донора для повторной трансплантации. Возможная альтернатива стандартной химиотерапии – применение блокаторов PD-1, потенциирующих иммуный ответ, что позволяет рассчитывать на усиление эффекта «трансплантат против лейкемии» у пациентов с рецидивами онкогематологических заболеваний после аллогенной ТГСК. Целью наблюдения было оценить эффективность и безопасность применения ниволумаба у данной когорты пациентов.
Методы
Мы ретроспективно проанализировали истории болезни 8 пациентов в возрасте от 3 до 14 лет, получивших терапию ингибиторами PD1 после ТГСК. 6 из них имели диагноз ОМЛ, 1 пациент – диагноз ОЛЛ, 1 пациент – диагноз гепатоспленическая γδ-Т-клеточная лимфома. На момент ТГСК 5 пациентов имели продвинутую стадию заболевания, 2 были в полной ремиссии, и 1 находился в MRD-позитивной ремиссии. Все пациенты получали аллогенную ТГСК (5 пациентов от гаплоидентичного донора, 3 пациента от HLA-идентичного сиблинга). На +30 сутки от ТГСК все пациенты находились в клинико-гематологической и молекулярной ремиссии. У 50% пациентов развилась острая РТПХ 1-2 степени с поражением кожи и ЖКТ. Среднее время до развития рецидива составило 180 (97-420) дней. Развернутый костно-мозговой рецидив был зафиксирован у 6 пациентов, у 2 пациентов был отмечен молекулярный рецидив. Все пациенты получили 1 инъекцию ниволумаба в дозе 3 мг/кг. Один пациент с ОМЛ получил инъекцию ниволумаба, уже находясь в ремиссии после повторной ТГСК, в связи с высоким риском повторного рецидива.
Результаты
Нежелательные явления были зарегистрированы у 6 (75%) пациентов. У двух пациентов развился иммунный менингоэнцефалит, у 1 пациента – иммунный гепатит 4 степени, у 2 пациентов была отмечена РТПХ кожи 3й степени, у 4 пациентов развилась иммунная лихорадка. Четырем пациентам потребовалось назначение системной иммуносупрессивной терапии для борьбы с иммуноопосредованными реакциями. Связанной с токсичностью летальности отмечено не было. Для оценки эффективности терапии после первой инъекции ниволумаба всем пациентам были выполнены костномозговые пункции. Шесть из семи пациентов не ответили на терапию. Среднее время до прогрессирования заболевания составляло 21 день. У пациента 7 лет с ОМЛ, находящегося в ремиссии на момент введения ниволумаба, спустя 2 недели после введения развилась иммунная лихорадка и иммунный менингоэнцефалит с явлениями когнитивных расстройств, дизартрии, мышечной слабости, полностью разрешившийся на фоне пульс-терапии солу-медролом. В настоящее время спустя 1 год 10 месяцев после введения ниволумаба у пациента сохраняется морфологическая MRD негативная ремиссия, выраженной патологии со стороны органов и систем нет. Пациентка 7 лет, находившаяся в развернутом рецидиве ОЛЛ на момент введения ниволумаба, достигла стойкой ремиссии. Однако спустя 14 дней от введения препарата у ребенка развился аутоиммунный гепатит 4 степени, рефрактерный ко всем видам терапии, включая ТАО в СОД 6 Гр. В связи с прогрессирующим фатальным повреждением печени произведена успешная трансплантация печени от родственного донора, на сроке 1 год 3 месяца после введения ниволумаба сохраняется полная ремиссия.
Выводы
Наш небольшой опыт показывает, что применение ингибиторов PD-1 после аллогенной ТГСК связано со значительной токсичностью. Для обеспечения безопасности и эффективности этого подхода требуются дальнейшие проспективные исследования.
Ключевые слова
Аллогенная ТГСК, ингибиторы PD1, рецидив, ОЛЛ, ОМЛ.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20556
[VALUE] => Array
(
[TEXT] => Наталья В. Минаева, Мария А. Логинова, Наталья А. Малышева, Наталья А. Зорина, Марина Н. Хоробрых, Филипп С. Шерстнев, Наталья В. Исаева, Елена Н. Калинина, Елена Л. Назарова, Николай М. Поздеев, Андрей В. Рылов, Игорь В. Парамонов
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Наталья В. Минаева, Мария А. Логинова, Наталья А. Малышева, Наталья А. Зорина, Марина Н. Хоробрых, Филипп С. Шерстнев, Наталья В. Исаева, Елена Н. Калинина, Елена Л. Назарова, Николай М. Поздеев, Андрей В. Рылов, Игорь В. Парамонов
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20557
[VALUE] => Array
(
[TEXT] => Федеральное государственное бюджетное учреждение науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства», Киров, Россия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Федеральное государственное бюджетное учреждение науки «Кировский научно-исследовательский институт гематологии и переливания крови Федерального медико-биологического агентства», Киров, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20558
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Актуальность</h2>
<p style="text-align: justify;">
В настоящее время потребность отечественного здравоохранения в аллогенных трансплантациях костного мозга удовлетворяются в недостаточном объеме. Необходимым условием выполнения алло-ТГСК является наличие HLA-совместимого донора. В случае отсутствия такового среди родственников, осуществляется поиск неродственного донора и преимущественно в зарубежных регистрах. Практика привлечения российских доноров крайне незначительна, что обусловлено малочисленностью локальных регистров, отсутствием научно-обоснованных подходов к их наполнению, учитывающих генетическое разнообразие доноров и обеспечиваемых контингентов, отсутствием отлаженного механизма обследования совместимых доноров, получения, хранения, транспортировки гемопоэтического материала, с учетом территориальной разобщенности трансплантационного центра и места проживания донора. Учитывая это, требуется создать собственную систему, соответствующую принципам отечественного здравоохранения. В настоящей работе представлен 5 летний опыт взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России.
</p>
<h2 style="text-align: justify;">Цель исследования</h2>
<p style="text-align: justify;">
Анализ эффективности взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России в рамках организации обеспечения трансплантационных центров РФ клеточным материалом от российскихнеродственных доноров.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Общая численность регистра потенциальных доноров ГСК на 1.07.18 составила 35649 человек. Это 43,3% от всех протипированных в РФ неродственных доноров. За период 2013-2018 гг. нами произведено 118 заготовок клеточного материала для 10 трансплантационных центров РФ и ближнего зарубежья, что составляет 51,9% от общего числа донаций ГСК от российских неродственных доноров. В 37,1% для получения трансплантата использовалась миелоэксфузия, в остальных 62,9% применялся аппаратный цитаферез. Выбор метода заготовки ГСК определяли, исходя из решения потенциального донора и наличия медицинских противопоказаний, с учетом предпочтений трансплантационного центра. Перед заготовкой трансплантата все доноры ГСК подвергались обследованию на значимые для безопасности реципиента гемотрансмиссивные инфекции. При передаче клеточного материала производилась оценка соответствия количественных и качественных характеристик утвержденной спецификации. При получении ГСК методом аппаратного цитафереза содержание CD34+/кг в трансплантационном материале составило в среднем 6,3x106/кг, при заготовке методом миелоэксфузии – 3,6x106/кг реципиента. Время транспортировки клеточного материала от центра заготовки до трансплантационной клиники составило в среднем 16,3 часа. Согласно представленных трансплантационными клиниками отчетов отклонения количественных показателей от исходных данных были минимальные, составив 1-2% и не зависели от сроков транспортировки. Период от момента активации донора до получения трансплантата занимал не более 8 недель. Все процессы осуществлялись в соответствии с требованиями системы менеджмента качества и комплексом разработанных в учреждении стандартных операционных процедур.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
В результате взаимодействия двух учреждений, подведомственных ФМБА России, реализована российская модель обеспечения трансплантационных центров РФ клеточным материалом для неродственных трансплантаций. Модель подразумевает весь комплекс необходимых мероприятий: от привлечения потенциальных доноров ГСК до оценки качества заготовленного клеточного материала, его транспортировки и порядка передачи в трансплантирующую клинику. Полученные данные свидетельствуют о высокой эффективности созданной системы. Опыт может быть распространен на деятельность других локальных регистров ГСК в РФ и взят за основу при формировании национальной системы обеспечения трансплантационных центров гемопоэтическим материалом от российских неродственных доноров.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Регистр доноров костного мозга, аллогенная трансплантация гемопоэтических стволовых клеток, неродственный донор гемопоэтических стволовых клеток.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Актуальность
В настоящее время потребность отечественного здравоохранения в аллогенных трансплантациях костного мозга удовлетворяются в недостаточном объеме. Необходимым условием выполнения алло-ТГСК является наличие HLA-совместимого донора. В случае отсутствия такового среди родственников, осуществляется поиск неродственного донора и преимущественно в зарубежных регистрах. Практика привлечения российских доноров крайне незначительна, что обусловлено малочисленностью локальных регистров, отсутствием научно-обоснованных подходов к их наполнению, учитывающих генетическое разнообразие доноров и обеспечиваемых контингентов, отсутствием отлаженного механизма обследования совместимых доноров, получения, хранения, транспортировки гемопоэтического материала, с учетом территориальной разобщенности трансплантационного центра и места проживания донора. Учитывая это, требуется создать собственную систему, соответствующую принципам отечественного здравоохранения. В настоящей работе представлен 5 летний опыт взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России.
Цель исследования
Анализ эффективности взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России в рамках организации обеспечения трансплантационных центров РФ клеточным материалом от российскихнеродственных доноров.
Результаты
Общая численность регистра потенциальных доноров ГСК на 1.07.18 составила 35649 человек. Это 43,3% от всех протипированных в РФ неродственных доноров. За период 2013-2018 гг. нами произведено 118 заготовок клеточного материала для 10 трансплантационных центров РФ и ближнего зарубежья, что составляет 51,9% от общего числа донаций ГСК от российских неродственных доноров. В 37,1% для получения трансплантата использовалась миелоэксфузия, в остальных 62,9% применялся аппаратный цитаферез. Выбор метода заготовки ГСК определяли, исходя из решения потенциального донора и наличия медицинских противопоказаний, с учетом предпочтений трансплантационного центра. Перед заготовкой трансплантата все доноры ГСК подвергались обследованию на значимые для безопасности реципиента гемотрансмиссивные инфекции. При передаче клеточного материала производилась оценка соответствия количественных и качественных характеристик утвержденной спецификации. При получении ГСК методом аппаратного цитафереза содержание CD34+/кг в трансплантационном материале составило в среднем 6,3x106/кг, при заготовке методом миелоэксфузии – 3,6x106/кг реципиента. Время транспортировки клеточного материала от центра заготовки до трансплантационной клиники составило в среднем 16,3 часа. Согласно представленных трансплантационными клиниками отчетов отклонения количественных показателей от исходных данных были минимальные, составив 1-2% и не зависели от сроков транспортировки. Период от момента активации донора до получения трансплантата занимал не более 8 недель. Все процессы осуществлялись в соответствии с требованиями системы менеджмента качества и комплексом разработанных в учреждении стандартных операционных процедур.
Заключение
В результате взаимодействия двух учреждений, подведомственных ФМБА России, реализована российская модель обеспечения трансплантационных центров РФ клеточным материалом для неродственных трансплантаций. Модель подразумевает весь комплекс необходимых мероприятий: от привлечения потенциальных доноров ГСК до оценки качества заготовленного клеточного материала, его транспортировки и порядка передачи в трансплантирующую клинику. Полученные данные свидетельствуют о высокой эффективности созданной системы. Опыт может быть распространен на деятельность других локальных регистров ГСК в РФ и взят за основу при формировании национальной системы обеспечения трансплантационных центров гемопоэтическим материалом от российских неродственных доноров.
Ключевые слова
Регистр доноров костного мозга, аллогенная трансплантация гемопоэтических стволовых клеток, неродственный донор гемопоэтических стволовых клеток.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20559
[VALUE] => Array
(
[TEXT] => Natalia V. Minaeva, Maria A. Loginova, Natalia A. Malysheva, Natalia A. Zorina, Marina N. Khorobrykh, Philipp S. Sherstnev, Natalia V. Isaeva, Elena N. Kalinina, Elena L. Nazarova, Nikolay M. Pozdeev, Andrey V. Rylov, Igor V. Paramonov
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Natalia V. Minaeva, Maria A. Loginova, Natalia A. Malysheva, Natalia A. Zorina, Marina N. Khorobrykh, Philipp S. Sherstnev, Natalia V. Isaeva, Elena N. Kalinina, Elena L. Nazarova, Nikolay M. Pozdeev, Andrey V. Rylov, Igor V. Paramonov
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20560
[VALUE] => Array
(
[TEXT] => Kirov Research Institute of Hematology and Blood Transfusion, Kirov, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Kirov Research Institute of Hematology and Blood Transfusion, Kirov, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20561
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
At present, the need for national health care in allogeneic bone marrow transplantation is insufficiently met. A necessary condition for performing of allogeneic hematopoietic stem cell transplantation (allo-HSCT) is the presence of an HLA-matched donor. In the absence of such among relatives, an unrelated donor is sought and mainly in foreign registries. The practice of attracting Russian donors is extremely low, due to the small number of local registries, the lack of scientifically based approaches to filling them, taking into account the genetic diversity of donors and provided contingents, the lack of a well-functioning mechanism for examining matched donors, obtaining, storing, transporting the hemopoietic material, taking into account the territorial disconnection of the transplantation center and place of donor residence. Considering this, it is required to create system that meets the national healthcare principles. This paper represents 5-year experience of hematopoietic stem cells (HSC) potential donors regional registry of the Federal State Facility “Russian Medical Research and Production Center “Rosplasma” in Kirov and the center for the transplant material harvesting on the basis of the Federal State Institute of Science “Kirov Research Institute of Hematology and Blood Transfusion” subordinating to the Federal Medical and Biological Agency of Russia. The aim of the research is analysis of the effectiveness of interaction between HSC donor regional registry and the center for the transplant material harvesting in providing of russian transplant centers with cellular material from russian unrelated donors, based on the 5-year experience.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
The total number of potential donors in the HSC regional registry on July 1, 2018 was 35,649 persons. This is 43.3% of all HLA-genotyped unrelated potential donors in Russia. From 2013 to 2018 we performed 118 cellular material harvests for 10 transplant centers in Russia and the near abroad countries, this represents 51.9% of the total number of HSC donations from Russian unrelated donors. In 37.1% for the graft preparation bone marrow was collected, in the remaining 62.9% – apheresis was used. Selection of the HSC harvesting method was based upon decision of the potential donor with consideration of medical contraindications, and the transplantation center preferences. Before the graft preparation, all HSC donors were screened for significant bloodborne infections. Before issuing of cellular material consistency with approved specification of the quantitative and qualitative characteristics were assessed. In apheresis collection the CD34+-cells content in the transplantation material averaged 5.3x106/kg, in marrow collection – 3.6x106/kg of the patient’s weight. The duration of transport of the cellular material from the harvesting center to the transplant clinic was 16.3 hours on average. According to the reports, submitted by the transplant clinics, the deviations of the quantitative indicators from the initial data were minimal, amounting to 1-2% and did not depend on the transportation period. The time span from the donor activation to transplant delivery was less than 8 weeks. All processes were carried out in accordance with requirements of the quality management system and a set of standard operating procedures developed in the institution.
</p>
<p style="text-align: justify;">
<span style="font-family: Cuprum, sans-serif; font-size: 26px;">Conclusion</span>
</p>
<p style="text-align: justify;">
Interaction pattern between two institutions, subordinating to the Federal Medical and Biological Agency of Russia, is the basis of Russian model of cellular material providing for unrelated transplantations for clinics in Russian Federation. This model implies the whole complex of necessary measures: recruitment of potential donors, assessing the quality of harvested cellular material, its distribution and shipment to transplant clinic. The received data testify to high efficiency of the created system. Experience could be extended to the practice of other local HSC registers in Russia and taken as a basis for the national hematopoietic material providing system formation.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Donor’s bone marrow registry, allogeneic hematopoietic stem cell transplantation, unrelated donor hematopoietic stem cells.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
At present, the need for national health care in allogeneic bone marrow transplantation is insufficiently met. A necessary condition for performing of allogeneic hematopoietic stem cell transplantation (allo-HSCT) is the presence of an HLA-matched donor. In the absence of such among relatives, an unrelated donor is sought and mainly in foreign registries. The practice of attracting Russian donors is extremely low, due to the small number of local registries, the lack of scientifically based approaches to filling them, taking into account the genetic diversity of donors and provided contingents, the lack of a well-functioning mechanism for examining matched donors, obtaining, storing, transporting the hemopoietic material, taking into account the territorial disconnection of the transplantation center and place of donor residence. Considering this, it is required to create system that meets the national healthcare principles. This paper represents 5-year experience of hematopoietic stem cells (HSC) potential donors regional registry of the Federal State Facility “Russian Medical Research and Production Center “Rosplasma” in Kirov and the center for the transplant material harvesting on the basis of the Federal State Institute of Science “Kirov Research Institute of Hematology and Blood Transfusion” subordinating to the Federal Medical and Biological Agency of Russia. The aim of the research is analysis of the effectiveness of interaction between HSC donor regional registry and the center for the transplant material harvesting in providing of russian transplant centers with cellular material from russian unrelated donors, based on the 5-year experience.
Results
The total number of potential donors in the HSC regional registry on July 1, 2018 was 35,649 persons. This is 43.3% of all HLA-genotyped unrelated potential donors in Russia. From 2013 to 2018 we performed 118 cellular material harvests for 10 transplant centers in Russia and the near abroad countries, this represents 51.9% of the total number of HSC donations from Russian unrelated donors. In 37.1% for the graft preparation bone marrow was collected, in the remaining 62.9% – apheresis was used. Selection of the HSC harvesting method was based upon decision of the potential donor with consideration of medical contraindications, and the transplantation center preferences. Before the graft preparation, all HSC donors were screened for significant bloodborne infections. Before issuing of cellular material consistency with approved specification of the quantitative and qualitative characteristics were assessed. In apheresis collection the CD34+-cells content in the transplantation material averaged 5.3x106/kg, in marrow collection – 3.6x106/kg of the patient’s weight. The duration of transport of the cellular material from the harvesting center to the transplant clinic was 16.3 hours on average. According to the reports, submitted by the transplant clinics, the deviations of the quantitative indicators from the initial data were minimal, amounting to 1-2% and did not depend on the transportation period. The time span from the donor activation to transplant delivery was less than 8 weeks. All processes were carried out in accordance with requirements of the quality management system and a set of standard operating procedures developed in the institution.
Conclusion
Interaction pattern between two institutions, subordinating to the Federal Medical and Biological Agency of Russia, is the basis of Russian model of cellular material providing for unrelated transplantations for clinics in Russian Federation. This model implies the whole complex of necessary measures: recruitment of potential donors, assessing the quality of harvested cellular material, its distribution and shipment to transplant clinic. The received data testify to high efficiency of the created system. Experience could be extended to the practice of other local HSC registers in Russia and taken as a basis for the national hematopoietic material providing system formation.
Keywords
Donor’s bone marrow registry, allogeneic hematopoietic stem cell transplantation, unrelated donor hematopoietic stem cells.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20562
[VALUE] => A model for interaction between hematopoietic stem cells potential donor’s regional registry and transplant material harvesting center: experience of Kirov Research Institute of Hematology and Blood Transfusion
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => A model for interaction between hematopoietic stem cells potential donor’s regional registry and transplant material harvesting center: experience of Kirov Research Institute of Hematology and Blood Transfusion
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20791
[VALUE] => 1429
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1429
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20792
[VALUE] => 1430
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1430
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Наталья В. Минаева, Мария А. Логинова, Наталья А. Малышева, Наталья А. Зорина, Марина Н. Хоробрых, Филипп С. Шерстнев, Наталья В. Исаева, Елена Н. Калинина, Елена Л. Назарова, Николай М. Поздеев, Андрей В. Рылов, Игорь В. Парамонов
Актуальность
В настоящее время потребность отечественного здравоохранения в аллогенных трансплантациях костного мозга удовлетворяются в недостаточном объеме. Необходимым условием выполнения алло-ТГСК является наличие HLA-совместимого донора. В случае отсутствия такового среди родственников, осуществляется поиск неродственного донора и преимущественно в зарубежных регистрах. Практика привлечения российских доноров крайне незначительна, что обусловлено малочисленностью локальных регистров, отсутствием научно-обоснованных подходов к их наполнению, учитывающих генетическое разнообразие доноров и обеспечиваемых контингентов, отсутствием отлаженного механизма обследования совместимых доноров, получения, хранения, транспортировки гемопоэтического материала, с учетом территориальной разобщенности трансплантационного центра и места проживания донора. Учитывая это, требуется создать собственную систему, соответствующую принципам отечественного здравоохранения. В настоящей работе представлен 5 летний опыт взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России.
Цель исследования
Анализ эффективности взаимодействия регионального регистра потенциальных доноров гемопоэтических стволовых клеток ФГБУ «Российский медицинский научно-производственный центр «Росплазма» г. Киров и центра заготовки трансплантационного материала на базе ФГБУН Кировский НИИ гематологии и переливания крови, подведомственных ФМБА России в рамках организации обеспечения трансплантационных центров РФ клеточным материалом от российскихнеродственных доноров.
Результаты
Общая численность регистра потенциальных доноров ГСК на 1.07.18 составила 35649 человек. Это 43,3% от всех протипированных в РФ неродственных доноров. За период 2013-2018 гг. нами произведено 118 заготовок клеточного материала для 10 трансплантационных центров РФ и ближнего зарубежья, что составляет 51,9% от общего числа донаций ГСК от российских неродственных доноров. В 37,1% для получения трансплантата использовалась миелоэксфузия, в остальных 62,9% применялся аппаратный цитаферез. Выбор метода заготовки ГСК определяли, исходя из решения потенциального донора и наличия медицинских противопоказаний, с учетом предпочтений трансплантационного центра. Перед заготовкой трансплантата все доноры ГСК подвергались обследованию на значимые для безопасности реципиента гемотрансмиссивные инфекции. При передаче клеточного материала производилась оценка соответствия количественных и качественных характеристик утвержденной спецификации. При получении ГСК методом аппаратного цитафереза содержание CD34+/кг в трансплантационном материале составило в среднем 6,3x106/кг, при заготовке методом миелоэксфузии – 3,6x106/кг реципиента. Время транспортировки клеточного материала от центра заготовки до трансплантационной клиники составило в среднем 16,3 часа. Согласно представленных трансплантационными клиниками отчетов отклонения количественных показателей от исходных данных были минимальные, составив 1-2% и не зависели от сроков транспортировки. Период от момента активации донора до получения трансплантата занимал не более 8 недель. Все процессы осуществлялись в соответствии с требованиями системы менеджмента качества и комплексом разработанных в учреждении стандартных операционных процедур.
Заключение
В результате взаимодействия двух учреждений, подведомственных ФМБА России, реализована российская модель обеспечения трансплантационных центров РФ клеточным материалом для неродственных трансплантаций. Модель подразумевает весь комплекс необходимых мероприятий: от привлечения потенциальных доноров ГСК до оценки качества заготовленного клеточного материала, его транспортировки и порядка передачи в трансплантирующую клинику. Полученные данные свидетельствуют о высокой эффективности созданной системы. Опыт может быть распространен на деятельность других локальных регистров ГСК в РФ и взят за основу при формировании национальной системы обеспечения трансплантационных центров гемопоэтическим материалом от российских неродственных доноров.
Ключевые слова
Регистр доноров костного мозга, аллогенная трансплантация гемопоэтических стволовых клеток, неродственный донор гемопоэтических стволовых клеток.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20547
[VALUE] => Array
(
[TEXT] => Алексей К. Кравченко, Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Анна А. Галкина, Ольга Я. Кулагина, Жанна Г. Якимова, Анна А. Спиридонова, Олег В. Голощапов, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Алексей К. Кравченко, Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Анна А. Галкина, Ольга Я. Кулагина, Жанна Г. Якимова, Анна А. Спиридонова, Олег В. Голощапов, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20548
[VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20549
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Качество и эффективность дезинфекции объектов окружающей (госпитальной) среды при применении растворов химических дезинфицирующих средств зависит от контакта действующего агента с условно-патогенными микроорганизмами, находящимися на обрабатываемых поверхностях; обсемененности объекта, подлежащего дезинфекции; состава дезинфицирующего средства, его концентрации, времени экспозиции.
</p>
<h2 style="text-align: justify;">Цель</h2>
<p style="text-align: justify;">
Сравнение качества заключительной дезинфекции с использованием генератора аэрозолей («аппаратный метод») и ранцевого распылителя жидкостей («ручной метод»).
</p>
<h2 style="text-align: justify;">Методы</h2>
<p style="text-align: justify;">
В НИИ ДОГИТ им. Р. М. Горбачевой с 06.2018 по 08.2018 для распыления химических дезинфицирующих средств применяли две методики. Для аппаратно-аэрозольной дезинфекции использовали генератор аэрозолей с дезинфицирующим средством «Nocolyse» (Состав: перекись водорода 6%, неионогенное ПАВ 1%, ионы серебра), ручной, ранцевого типа распылитель жидкостей снаряжали дезсредством «Амиксан» (Состав: N,N-бис(3-аминопропил) додециламин 3%, алкилдиметилбензиламмоний хлорид + алкилдиметилэтилбензиламмоний хлорид 25 %). При использовании аппаратной обработки был протестированы режим: 1:1 (1мл «Nocolyse» на 1 м3), 1:3, 1:6. Смывы с объектов окружающей среды проводили до проведения заключительной дезинфекции (с целью определения общего микробного числа) и после прове- дения заключительной дезинфекции аппаратным методом (контроль качества проведенной дезинфекции).
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Заключительная дезинфекция с применением аппарата аэрозольной обработки в режиме 1:1 (5 случаев). Результаты санитарно-бактериологических исследований помещений выявили следующий бактериологический пейзаж объектов окружающей среды, соответственно, до и после антибактериальной обработки: Escherichia coli – 3 (15%) – E.coli – 0, Pseudomonas spp. – 3 (15%), – Pseudomonas sp. – 1 (8,33%), Klebsiella pneumoniae – 3 (15%) – K. pneumoniae – 0, Acinetobacter spр. – 1 (5%) – Acinetobacter spр. – 1 (8,3%), Staphylococcus epidermidis – 7 (35%) – S. epidermidis – 9 (75%), Enterococcus faecium – 1 (5%), E. faecium – 0, Bacillus – 2 (10%) – Bacillus – 1 (8,3%). При режиме 1:3 (3 обработки): Pseudomonas spp. – 1 (6,7%) – Pseudomonas spp. – 0, Staphylococcus epidermidis – 8 (53,3%) – S. epidermidis – 8 (88,9%), Klebsiella pneumoniae – 2 (13,3), K. pneumoniae – 0, Bacillus – 3 (20%) – Bacillus – 1 (11,1%), Staphylococcus aureus – 1 (6,7%) – S.aureus – 0.<br>
Режим 1:6 (2 обработки): Staphylococcus epidermidis – 2 (40%) – S. epidermidis – 1 (100%), Acinetobacter spр. – 1 (20%) – Acinetobacter spр. – 0, Klebsiella pneumoniae – 2 (40%) – K.pneumoniae – 0. «Ручная» обработка (4 обработки): Klebsiella pneumoniae – 1 (20%) – K. pneumoniae – 0, Acinetobacter spр. – 2 (40%) – Acinetobacter spр. – 0, Pseudomonas spp. – 1 (20%) – Pseudomonas spp. – 1 (33,3%), Enterobacter spр. – 1 (20%) – Enterobacter spр. – 2 (66,7%). Во всех случаях при положительных бактериологических тестах дезинфекция проводилась повторно до подтверждения отрицательных результатов.
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
1. На основании полученных данных нельзя однозначно утверждать, что «аппаратная» обработка эффективнее «ручной».
</p>
<p style="text-align: justify;">
2. В режиме 1:1 аппаратная обработка может стать хорошим дополнением к текущей дезинфекции.
</p>
<p style="text-align: justify;">
3. В режиме 1:3 и 1:6 «аппаратная» обработка дает удовлетворительные результаты в борьбе с главными возбудителями нозокомиальной инфекции и может составить альтернативу «ручной».
</p>
<h2 style="text-align: justify;">Благодарность</h2>
<p style="text-align: justify;">
Выражаем особую благодарность сотрудникам отделения реанимации и интенсивной терапии №3 Жаравиной С. В., Журавлевой Н. И. за помощь в организацииработы.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Дезинфекция, больничные палаты, ручной режим, автоматический режим, бактерии, загрязнение.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Качество и эффективность дезинфекции объектов окружающей (госпитальной) среды при применении растворов химических дезинфицирующих средств зависит от контакта действующего агента с условно-патогенными микроорганизмами, находящимися на обрабатываемых поверхностях; обсемененности объекта, подлежащего дезинфекции; состава дезинфицирующего средства, его концентрации, времени экспозиции.
Цель
Сравнение качества заключительной дезинфекции с использованием генератора аэрозолей («аппаратный метод») и ранцевого распылителя жидкостей («ручной метод»).
Методы
В НИИ ДОГИТ им. Р. М. Горбачевой с 06.2018 по 08.2018 для распыления химических дезинфицирующих средств применяли две методики. Для аппаратно-аэрозольной дезинфекции использовали генератор аэрозолей с дезинфицирующим средством «Nocolyse» (Состав: перекись водорода 6%, неионогенное ПАВ 1%, ионы серебра), ручной, ранцевого типа распылитель жидкостей снаряжали дезсредством «Амиксан» (Состав: N,N-бис(3-аминопропил) додециламин 3%, алкилдиметилбензиламмоний хлорид + алкилдиметилэтилбензиламмоний хлорид 25 %). При использовании аппаратной обработки был протестированы режим: 1:1 (1мл «Nocolyse» на 1 м3), 1:3, 1:6. Смывы с объектов окружающей среды проводили до проведения заключительной дезинфекции (с целью определения общего микробного числа) и после прове- дения заключительной дезинфекции аппаратным методом (контроль качества проведенной дезинфекции).
Результаты
Заключительная дезинфекция с применением аппарата аэрозольной обработки в режиме 1:1 (5 случаев). Результаты санитарно-бактериологических исследований помещений выявили следующий бактериологический пейзаж объектов окружающей среды, соответственно, до и после антибактериальной обработки: Escherichia coli – 3 (15%) – E.coli – 0, Pseudomonas spp. – 3 (15%), – Pseudomonas sp. – 1 (8,33%), Klebsiella pneumoniae – 3 (15%) – K. pneumoniae – 0, Acinetobacter spр. – 1 (5%) – Acinetobacter spр. – 1 (8,3%), Staphylococcus epidermidis – 7 (35%) – S. epidermidis – 9 (75%), Enterococcus faecium – 1 (5%), E. faecium – 0, Bacillus – 2 (10%) – Bacillus – 1 (8,3%). При режиме 1:3 (3 обработки): Pseudomonas spp. – 1 (6,7%) – Pseudomonas spp. – 0, Staphylococcus epidermidis – 8 (53,3%) – S. epidermidis – 8 (88,9%), Klebsiella pneumoniae – 2 (13,3), K. pneumoniae – 0, Bacillus – 3 (20%) – Bacillus – 1 (11,1%), Staphylococcus aureus – 1 (6,7%) – S.aureus – 0.
Режим 1:6 (2 обработки): Staphylococcus epidermidis – 2 (40%) – S. epidermidis – 1 (100%), Acinetobacter spр. – 1 (20%) – Acinetobacter spр. – 0, Klebsiella pneumoniae – 2 (40%) – K.pneumoniae – 0. «Ручная» обработка (4 обработки): Klebsiella pneumoniae – 1 (20%) – K. pneumoniae – 0, Acinetobacter spр. – 2 (40%) – Acinetobacter spр. – 0, Pseudomonas spp. – 1 (20%) – Pseudomonas spp. – 1 (33,3%), Enterobacter spр. – 1 (20%) – Enterobacter spр. – 2 (66,7%). Во всех случаях при положительных бактериологических тестах дезинфекция проводилась повторно до подтверждения отрицательных результатов.
Выводы
1. На основании полученных данных нельзя однозначно утверждать, что «аппаратная» обработка эффективнее «ручной».
2. В режиме 1:1 аппаратная обработка может стать хорошим дополнением к текущей дезинфекции.
3. В режиме 1:3 и 1:6 «аппаратная» обработка дает удовлетворительные результаты в борьбе с главными возбудителями нозокомиальной инфекции и может составить альтернативу «ручной».
Благодарность
Выражаем особую благодарность сотрудникам отделения реанимации и интенсивной терапии №3 Жаравиной С. В., Журавлевой Н. И. за помощь в организацииработы.
Ключевые слова
Дезинфекция, больничные палаты, ручной режим, автоматический режим, бактерии, загрязнение.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20550
[VALUE] => Array
(
[TEXT] => Alexey K. Kravchenko, Ashot A. Tadevosian, Olga A. Prokofieva, Olga E. Pigareva, Anna A. Galkina, Olga Y. Kulagina, Zhanna G. Yakimova, Anna A. Spiridonova, Oleg V. Goloshchapov, Boris V. Afanasyev
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Alexey K. Kravchenko, Ashot A. Tadevosian, Olga A. Prokofieva, Olga E. Pigareva, Anna A. Galkina, Olga Y. Kulagina, Zhanna G. Yakimova, Anna A. Spiridonova, Oleg V. Goloshchapov, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20551
[VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Institute for Children Oncology, Hematology and Transplantation at the First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20552
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Quality and efficacy of environmental (hospital) object disinfection performed using chemical disinfectant solutions depend on contact between the active agent and the opportunistic microorganisms on the contaminated surfaces, severity of contamination, and also composition of the disinfectant, its concentration, and time of exposure.
</p>
<h2 style="text-align: justify;">Objectives</h2>
<p style="text-align: justify;">
To compare results of terminal disinfection performed by using an aerosol generator (“an automated method”), or applying a backpack sprayer (“a manual method”).
</p>
<h2 style="text-align: justify;">Methods</h2>
<p style="text-align: justify;">
From 06.2018 to 08.2018, the two aforementioned methods were used to spray disinfecting agents in the rooms of Raisa Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation. An aerosol generator and disinfectant “Nocolyse” composed of hydrogen peroxide (6%), nonionic surfactant (1%), and containing silver ions, were used to perform automated aerosol disinfection. A backpack sprayer filled with disinfectant “Amixan” containing nn-bis(3-aminopropyl) dodecylamine (3%), alkyldimethylbenzylammonium chloride plus alkyldimethylbenzylammonium chloride (25%) was used for manual disinfection. While using automated method, three operation modes were tested: 1:1 (1 ml of “Nocolyse” per 1 cubic meter), as well as 1 per 3, and 1 per 6 cubic meters. Test swabs from enviromental objects were taken before treatment (to determine total microbial counts), and after terminal disinfection (to evaluate efficacy of the procedure).
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
(1) Terminal disinfection by aerosol generator, 1:1 mode (5 cases). Sanitary and bacteriological tests showed presence of the following microflora (before and after the procedure respectably): E. coli, 3 (15%) vs E.coli, 0; Pseudomonas spp., 3 (15%) vs Pseudomonas spp., 1 (8.3%); Klebsiella pneumonia, 3 (15%) versus K.pneumoniae, 0; Acinetobacter spр., 1 (5%) vs – Acinetobacter spр., 1 (8.3%); Staphylococcus epidermidis, 7 (35%) vs S.epidermidis, 9 (75%); Enterococcus faecium, 1 (5%) vs E. faecium, 0; Bacillus, 2 (10%) vs Bacillus, 1 (8.3%). Microbiology with 1 to 3 mode (3 cases) has shown: Pseudomonas spp., 1 (6.7%) vs Pseudomonas spp., 0; Staphylococcus epidermidis, 8 (53.3%) vs S. epidermidis, 8 (88.9%); Klebsiella pneumonia, 2 (13.3%) vs K. pneumonia, 0; Bacillus, 3 (20%) vs Bacillus, 1 (11.1%); Staphylococcus aureus, 1 (6.7%); S. aureus, 0.<br>
1:6 mode (2 cases). Microbiological findings were as follows: Staphylococcus epidermidis, 2 (40%) vs S.epidermidis, 1 (100%), Acinetobacter spр., 1 (20%) vs Acinetobacter spр., 0; Klebsiella pneumonia, 2(40%) vs. K. pneumoniae – 0. Meanwhile, manual disinfection (4 cases) yielded the following results: Klebsiella pneumonia, 1 (20%) vs K.pneumonia, 0; Acinetobacter spр., 2 (40%) vs Acinetobacter spр., 0; Pseudomonas spp., 1 (20%) vs Pseudomonas spp., 1 (33.3%); Enterobacter spр., 1 (20%); Enterobacter spp., 2 (66,7%). In cases of positive bacteriological tests, the disinfection procedure was repeated until the negative bacteriology results.
</p>
<h2 style="text-align: justify;">Conclusions</h2>
<p style="text-align: justify;">
1. Automated method was not clearly confirmed to be more effective than the manual method.
</p>
<p style="text-align: justify;">
2. Automated disinfection done at the 1:1 mode can be a good addition to routine disinfection.
</p>
<p style="text-align: justify;">
3. Automated disinfection done at the 1:3 and 1:6 modes shows satisfactory results against the main disease-causing nosocomial pathogens, and it can be used as an alternative to the manual method.
</p>
<h2 style="text-align: justify;">Credits</h2>
<p style="text-align: justify;">
We gratefully aknowledge Jaravina S. V. and Juravleva N. I., members of ICU №3 staff who helped us to organize our work.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Disinfection, hospital rooms, manual regimen, automatic regimen, bacteria, contamination.
</p>
<span id="bx-cursor-node"></span><br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
Quality and efficacy of environmental (hospital) object disinfection performed using chemical disinfectant solutions depend on contact between the active agent and the opportunistic microorganisms on the contaminated surfaces, severity of contamination, and also composition of the disinfectant, its concentration, and time of exposure.
Objectives
To compare results of terminal disinfection performed by using an aerosol generator (“an automated method”), or applying a backpack sprayer (“a manual method”).
Methods
From 06.2018 to 08.2018, the two aforementioned methods were used to spray disinfecting agents in the rooms of Raisa Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation. An aerosol generator and disinfectant “Nocolyse” composed of hydrogen peroxide (6%), nonionic surfactant (1%), and containing silver ions, were used to perform automated aerosol disinfection. A backpack sprayer filled with disinfectant “Amixan” containing nn-bis(3-aminopropyl) dodecylamine (3%), alkyldimethylbenzylammonium chloride plus alkyldimethylbenzylammonium chloride (25%) was used for manual disinfection. While using automated method, three operation modes were tested: 1:1 (1 ml of “Nocolyse” per 1 cubic meter), as well as 1 per 3, and 1 per 6 cubic meters. Test swabs from enviromental objects were taken before treatment (to determine total microbial counts), and after terminal disinfection (to evaluate efficacy of the procedure).
Results
(1) Terminal disinfection by aerosol generator, 1:1 mode (5 cases). Sanitary and bacteriological tests showed presence of the following microflora (before and after the procedure respectably): E. coli, 3 (15%) vs E.coli, 0; Pseudomonas spp., 3 (15%) vs Pseudomonas spp., 1 (8.3%); Klebsiella pneumonia, 3 (15%) versus K.pneumoniae, 0; Acinetobacter spр., 1 (5%) vs – Acinetobacter spр., 1 (8.3%); Staphylococcus epidermidis, 7 (35%) vs S.epidermidis, 9 (75%); Enterococcus faecium, 1 (5%) vs E. faecium, 0; Bacillus, 2 (10%) vs Bacillus, 1 (8.3%). Microbiology with 1 to 3 mode (3 cases) has shown: Pseudomonas spp., 1 (6.7%) vs Pseudomonas spp., 0; Staphylococcus epidermidis, 8 (53.3%) vs S. epidermidis, 8 (88.9%); Klebsiella pneumonia, 2 (13.3%) vs K. pneumonia, 0; Bacillus, 3 (20%) vs Bacillus, 1 (11.1%); Staphylococcus aureus, 1 (6.7%); S. aureus, 0.
1:6 mode (2 cases). Microbiological findings were as follows: Staphylococcus epidermidis, 2 (40%) vs S.epidermidis, 1 (100%), Acinetobacter spр., 1 (20%) vs Acinetobacter spр., 0; Klebsiella pneumonia, 2(40%) vs. K. pneumoniae – 0. Meanwhile, manual disinfection (4 cases) yielded the following results: Klebsiella pneumonia, 1 (20%) vs K.pneumonia, 0; Acinetobacter spр., 2 (40%) vs Acinetobacter spр., 0; Pseudomonas spp., 1 (20%) vs Pseudomonas spp., 1 (33.3%); Enterobacter spр., 1 (20%); Enterobacter spp., 2 (66,7%). In cases of positive bacteriological tests, the disinfection procedure was repeated until the negative bacteriology results.
Conclusions
1. Automated method was not clearly confirmed to be more effective than the manual method.
2. Automated disinfection done at the 1:1 mode can be a good addition to routine disinfection.
3. Automated disinfection done at the 1:3 and 1:6 modes shows satisfactory results against the main disease-causing nosocomial pathogens, and it can be used as an alternative to the manual method.
Credits
We gratefully aknowledge Jaravina S. V. and Juravleva N. I., members of ICU №3 staff who helped us to organize our work.
Keywords
Disinfection, hospital rooms, manual regimen, automatic regimen, bacteria, contamination.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20553
[VALUE] => Usage of aerosol sprays for disinfection of hospital rooms
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Usage of aerosol sprays for disinfection of hospital rooms
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20785
[VALUE] => 1423
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1423
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20786
[VALUE] => 1424
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1424
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Алексей К. Кравченко, Ашот А. Тадевосян, Ольга А. Прокофьева, Ольга Е. Пигарева, Анна А. Галкина, Ольга Я. Кулагина, Жанна Г. Якимова, Анна А. Спиридонова, Олег В. Голощапов, Борис В. Афанасьев
Введение
Качество и эффективность дезинфекции объектов окружающей (госпитальной) среды при применении растворов химических дезинфицирующих средств зависит от контакта действующего агента с условно-патогенными микроорганизмами, находящимися на обрабатываемых поверхностях; обсемененности объекта, подлежащего дезинфекции; состава дезинфицирующего средства, его концентрации, времени экспозиции.
Цель
Сравнение качества заключительной дезинфекции с использованием генератора аэрозолей («аппаратный метод») и ранцевого распылителя жидкостей («ручной метод»).
Методы
В НИИ ДОГИТ им. Р. М. Горбачевой с 06.2018 по 08.2018 для распыления химических дезинфицирующих средств применяли две методики. Для аппаратно-аэрозольной дезинфекции использовали генератор аэрозолей с дезинфицирующим средством «Nocolyse» (Состав: перекись водорода 6%, неионогенное ПАВ 1%, ионы серебра), ручной, ранцевого типа распылитель жидкостей снаряжали дезсредством «Амиксан» (Состав: N,N-бис(3-аминопропил) додециламин 3%, алкилдиметилбензиламмоний хлорид + алкилдиметилэтилбензиламмоний хлорид 25 %). При использовании аппаратной обработки был протестированы режим: 1:1 (1мл «Nocolyse» на 1 м3), 1:3, 1:6. Смывы с объектов окружающей среды проводили до проведения заключительной дезинфекции (с целью определения общего микробного числа) и после прове- дения заключительной дезинфекции аппаратным методом (контроль качества проведенной дезинфекции).
Результаты
Заключительная дезинфекция с применением аппарата аэрозольной обработки в режиме 1:1 (5 случаев). Результаты санитарно-бактериологических исследований помещений выявили следующий бактериологический пейзаж объектов окружающей среды, соответственно, до и после антибактериальной обработки: Escherichia coli – 3 (15%) – E.coli – 0, Pseudomonas spp. – 3 (15%), – Pseudomonas sp. – 1 (8,33%), Klebsiella pneumoniae – 3 (15%) – K. pneumoniae – 0, Acinetobacter spр. – 1 (5%) – Acinetobacter spр. – 1 (8,3%), Staphylococcus epidermidis – 7 (35%) – S. epidermidis – 9 (75%), Enterococcus faecium – 1 (5%), E. faecium – 0, Bacillus – 2 (10%) – Bacillus – 1 (8,3%). При режиме 1:3 (3 обработки): Pseudomonas spp. – 1 (6,7%) – Pseudomonas spp. – 0, Staphylococcus epidermidis – 8 (53,3%) – S. epidermidis – 8 (88,9%), Klebsiella pneumoniae – 2 (13,3), K. pneumoniae – 0, Bacillus – 3 (20%) – Bacillus – 1 (11,1%), Staphylococcus aureus – 1 (6,7%) – S.aureus – 0.
Режим 1:6 (2 обработки): Staphylococcus epidermidis – 2 (40%) – S. epidermidis – 1 (100%), Acinetobacter spр. – 1 (20%) – Acinetobacter spр. – 0, Klebsiella pneumoniae – 2 (40%) – K.pneumoniae – 0. «Ручная» обработка (4 обработки): Klebsiella pneumoniae – 1 (20%) – K. pneumoniae – 0, Acinetobacter spр. – 2 (40%) – Acinetobacter spр. – 0, Pseudomonas spp. – 1 (20%) – Pseudomonas spp. – 1 (33,3%), Enterobacter spр. – 1 (20%) – Enterobacter spр. – 2 (66,7%). Во всех случаях при положительных бактериологических тестах дезинфекция проводилась повторно до подтверждения отрицательных результатов.
Выводы
1. На основании полученных данных нельзя однозначно утверждать, что «аппаратная» обработка эффективнее «ручной».
2. В режиме 1:1 аппаратная обработка может стать хорошим дополнением к текущей дезинфекции.
3. В режиме 1:3 и 1:6 «аппаратная» обработка дает удовлетворительные результаты в борьбе с главными возбудителями нозокомиальной инфекции и может составить альтернативу «ручной».
Благодарность
Выражаем особую благодарность сотрудникам отделения реанимации и интенсивной терапии №3 Жаравиной С. В., Журавлевой Н. И. за помощь в организацииработы.
Ключевые слова
Дезинфекция, больничные палаты, ручной режим, автоматический режим, бактерии, загрязнение.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20538
[VALUE] => Array
(
[TEXT] => Мария В. Марковцева
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Мария В. Марковцева
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20539
[VALUE] => Array
(
[TEXT] => Ульяновский государственный университет, г. Ульяновск, Россия
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Ульяновский государственный университет, г. Ульяновск, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20540
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Цель</h2>
<p style="text-align: justify;">
Цель исследования – изучить гендерные особенности коморбидной патологии у пациентов с хроническим лимфолейкозом (ХЛЛ).
</p>
<h2>Материалы и методы</h2>
<p style="text-align: justify;">
Обследовано 70 пациентов (35 мужчин и 35 женщин) в возрасте от 42 до 80 лет. В момент постановки диагноза ХЛЛ пациентам рассчитывали индекс коморбидности Charlson (ИК Charlson) и скорость клубочковй фильтрации (СКФ) по формуле MDRD. ИК Charlson представляет собой бальную систему оценки возраста и наличия определенных сопутствующих заболеваний и используется для оценки прогноза больных с длительными сроками наблюдения. Снижение СКФ также служит маркером для прогноза многих заболеваний. Установлено, что это один из факторов риска появления сердечно-сосудистых осложнений, которые приводят к повышению уровня смертности людей. Для статистической оценки полученных данных вычисляли среднее значение показателя и его стандартное отклонение. Для сравнения групп применялся t-критерий Стьюдента. Корреляционный анализ проводился по Пирсону. Достоверным считался уровень значимости при р <0,05.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Средний возраст мужчин и женщин при постановки диагноза ХЛЛ был сопоставим и составлял 66,4±7,9 лет и 67,7±9,6 лет соответственно (р≥0,05). Так же не получили достоверных различий по уровню ИК Charlson в группах: 6,5±1,5 у мужчин и 6,8±1,6 у женщин (р≥0,05). Структура коморбидной патологии включала в себя наличие хронической сердечной недостаточности (87% – муж., 82% – жен.), хронических неспецифических заболеваний легких (43% – муж., 37% – жен.), нарушение мозгового кровообращения в анамнезе (23% – муж., 26% – жен.), сахарный диабет (14% – муж., 17% – жен.), заболевания почек и мочевыводящих путей (11% – муж., 43% – жен.), постинфарктный кардиосклероз (11% – муж., 8% – жен.), коллагенозы (0% – муж., 3% – жен.).
</p>
<h2>Расчет</h2>
<p style="text-align: justify;">
СКФ по MDRD показал значимые различия в группах исследования. Этот параметр у женщин был достоверно ниже – 58,7±12,4 мл/мин/1,73м2 по сравнению с группой мужчин – 68,8±9,1 мл/мин/1,73м2 (р<0,05). Одновременно с этим в группе женщин получена обратная корреляционная связь средней степени между показателем ИК Charlson и СКФ (r=0,58, р=0,02).
</p>
<h2 style="text-align: justify;">Обсуждение и выводы</h2>
<p style="text-align: justify;">
Полученные результаты свидетельствуют о богатой коморбидной патологии, имеющейся у пациентов с ХЛЛ на момент постановки диагноза. По ИК Charlson в обеих группах исследования в среднем диагностировали низкую общую 10-летнюю выживаемость (15%). Тем не менее, имеются гендерные отличия в структуре сопутствующих заболеваний. Так, среди женщин достоверно чаще встречается патология почек и мочевыводящих путей, что отражено снижением СКФ в этой группе по сравнению с мужчинами. Данный факт не рассматривается нами как особенность пациентов с ХЛЛ. Ранее установлено, что патология почек и мочевыводящих путей встречается в женской популяции чаще, чем в мужской, ввиду анатомических особенностей этого отдела тела. Беря этот факт во внимание, при назначении химиолечения у пациенток с ХЛЛ и ИК Charlson более 6 следует внимательно исследовать показатель СКФ.
</p>
<p style="text-align: justify;">
<span style="font-family: Cuprum, sans-serif; font-size: 26px;">Ключевые слова</span>
</p>
<p style="text-align: justify;">
Хронический лимфолейкоз, индекс коморбидности Charlson, скорость клубочковой фильтрации, гендерные различия.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Цель
Цель исследования – изучить гендерные особенности коморбидной патологии у пациентов с хроническим лимфолейкозом (ХЛЛ).
Материалы и методы
Обследовано 70 пациентов (35 мужчин и 35 женщин) в возрасте от 42 до 80 лет. В момент постановки диагноза ХЛЛ пациентам рассчитывали индекс коморбидности Charlson (ИК Charlson) и скорость клубочковй фильтрации (СКФ) по формуле MDRD. ИК Charlson представляет собой бальную систему оценки возраста и наличия определенных сопутствующих заболеваний и используется для оценки прогноза больных с длительными сроками наблюдения. Снижение СКФ также служит маркером для прогноза многих заболеваний. Установлено, что это один из факторов риска появления сердечно-сосудистых осложнений, которые приводят к повышению уровня смертности людей. Для статистической оценки полученных данных вычисляли среднее значение показателя и его стандартное отклонение. Для сравнения групп применялся t-критерий Стьюдента. Корреляционный анализ проводился по Пирсону. Достоверным считался уровень значимости при р <0,05.
Результаты
Средний возраст мужчин и женщин при постановки диагноза ХЛЛ был сопоставим и составлял 66,4±7,9 лет и 67,7±9,6 лет соответственно (р≥0,05). Так же не получили достоверных различий по уровню ИК Charlson в группах: 6,5±1,5 у мужчин и 6,8±1,6 у женщин (р≥0,05). Структура коморбидной патологии включала в себя наличие хронической сердечной недостаточности (87% – муж., 82% – жен.), хронических неспецифических заболеваний легких (43% – муж., 37% – жен.), нарушение мозгового кровообращения в анамнезе (23% – муж., 26% – жен.), сахарный диабет (14% – муж., 17% – жен.), заболевания почек и мочевыводящих путей (11% – муж., 43% – жен.), постинфарктный кардиосклероз (11% – муж., 8% – жен.), коллагенозы (0% – муж., 3% – жен.).
Расчет
СКФ по MDRD показал значимые различия в группах исследования. Этот параметр у женщин был достоверно ниже – 58,7±12,4 мл/мин/1,73м2 по сравнению с группой мужчин – 68,8±9,1 мл/мин/1,73м2 (р<0,05). Одновременно с этим в группе женщин получена обратная корреляционная связь средней степени между показателем ИК Charlson и СКФ (r=0,58, р=0,02).
Обсуждение и выводы
Полученные результаты свидетельствуют о богатой коморбидной патологии, имеющейся у пациентов с ХЛЛ на момент постановки диагноза. По ИК Charlson в обеих группах исследования в среднем диагностировали низкую общую 10-летнюю выживаемость (15%). Тем не менее, имеются гендерные отличия в структуре сопутствующих заболеваний. Так, среди женщин достоверно чаще встречается патология почек и мочевыводящих путей, что отражено снижением СКФ в этой группе по сравнению с мужчинами. Данный факт не рассматривается нами как особенность пациентов с ХЛЛ. Ранее установлено, что патология почек и мочевыводящих путей встречается в женской популяции чаще, чем в мужской, ввиду анатомических особенностей этого отдела тела. Беря этот факт во внимание, при назначении химиолечения у пациенток с ХЛЛ и ИК Charlson более 6 следует внимательно исследовать показатель СКФ.
Ключевые слова
Хронический лимфолейкоз, индекс коморбидности Charlson, скорость клубочковой фильтрации, гендерные различия.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20541
[VALUE] => Array
(
[TEXT] => Maria V. Markovtseva
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Maria V. Markovtseva
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20542
[VALUE] => Array
(
[TEXT] => Ulyanovsk State University, Ulyanovsk, Russia
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Ulyanovsk State University, Ulyanovsk, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20543
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Aim</h2>
<p style="text-align: justify;">
The aim of the study was to study the gender characteristics of comorbid pathology in patients with chronic lymphocytic leukemia (CLL).
</p>
<h2 style="text-align: justify;">Materials and methods</h2>
<p style="text-align: justify;">
We examined 70 patients (35 men and 35 women) aged from 42 to 80 years. At the time of diagnosis of CLL patients were calculated Charlson comorbidity index (Charlson CI) and glomerular filtration rate (GFR) by the MDRD formula. Charlson CI is a point system for assessing the age and presence of certain comorbidities and is used to assess the prognosis of patients with long-term follow-up. Decline in GFR also serves as a marker for the prognosis of many diseases. It is established that this is one of the risk factors for cardiovascular complications, which lead to an increase in mortality. For statistical evaluation of the obtained data, the average value of the indicator and its standard deviation were calculated. Student t-test was used to compare groups. Correlation analysis was carried out on Pearson. The significance level at p < 0.05 was considered reliable.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
The mean age of men and women at diagnosis of CLL was comparable and was 66.4±7.9 years and 67.7±9.6 years, respectively (p ≥ 0.05). Similarly, there were no significant differences in the level of Charlson CI in the groups: 6.5±1.5 in men and 6.8±1.6 in women (p ≥ 0.05). The structure of comorbid pathology included the presence of chronic heart failure (87% – men, 82% – women), chronic non-specific lung diseases (43% – men, 37% – women), violation of cerebral circulation in the history (23% – men, 26% – women), diabetes (14% – men, 17% – women ), kidney and urinary tract diseases (11% – men, 43% – women ), postinfarction cardiosclerosis (11% – men, 8% – women ), connective tissue diseases (0% – men, 3% – women). The calculation of GFR by MDRD showed significant differences in the studing groups. This parameter was significantly lower in the women – 58.7±12.4 ml/min/1,73 m2 compared to the group of the men – 68.8±9.1 ml/min/1,73m2 (p<0.05). At the same time, in the group of women, the inverse correlation between the mean degree of the Charlson CI and GFR was obtained (r=0.58, p=0.02).
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
The results indicate to different comorbidities in the CLL patients at the time of diagnosis. According to Charlson CI, both groups of the study were diagnosed with low overall 10- year survival (15%). However, there are gender differences in the structure of comorbidities. Thus, among women, kidney and urinary tract pathology is significantly more common, which is reflected by a decrease in GFR in this group compared to men. This fact is not considered by us as a specific feature of CLL patients. It was previously established that the pathology of kidneys and urinary tract occurs in the female population more often than in the male, due to the anatomical features of this part of the body. Taking this fact into account, in the appointment of chemotherapy in women with CLL and Charlson CI more than 6 the rate of GFR should be carefully examined.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Chronic lymphocytic leukemia, Charlson comorbidity index, glomerular filtration rate, gender difference.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Aim
The aim of the study was to study the gender characteristics of comorbid pathology in patients with chronic lymphocytic leukemia (CLL).
Materials and methods
We examined 70 patients (35 men and 35 women) aged from 42 to 80 years. At the time of diagnosis of CLL patients were calculated Charlson comorbidity index (Charlson CI) and glomerular filtration rate (GFR) by the MDRD formula. Charlson CI is a point system for assessing the age and presence of certain comorbidities and is used to assess the prognosis of patients with long-term follow-up. Decline in GFR also serves as a marker for the prognosis of many diseases. It is established that this is one of the risk factors for cardiovascular complications, which lead to an increase in mortality. For statistical evaluation of the obtained data, the average value of the indicator and its standard deviation were calculated. Student t-test was used to compare groups. Correlation analysis was carried out on Pearson. The significance level at p < 0.05 was considered reliable.
Results
The mean age of men and women at diagnosis of CLL was comparable and was 66.4±7.9 years and 67.7±9.6 years, respectively (p ≥ 0.05). Similarly, there were no significant differences in the level of Charlson CI in the groups: 6.5±1.5 in men and 6.8±1.6 in women (p ≥ 0.05). The structure of comorbid pathology included the presence of chronic heart failure (87% – men, 82% – women), chronic non-specific lung diseases (43% – men, 37% – women), violation of cerebral circulation in the history (23% – men, 26% – women), diabetes (14% – men, 17% – women ), kidney and urinary tract diseases (11% – men, 43% – women ), postinfarction cardiosclerosis (11% – men, 8% – women ), connective tissue diseases (0% – men, 3% – women). The calculation of GFR by MDRD showed significant differences in the studing groups. This parameter was significantly lower in the women – 58.7±12.4 ml/min/1,73 m2 compared to the group of the men – 68.8±9.1 ml/min/1,73m2 (p<0.05). At the same time, in the group of women, the inverse correlation between the mean degree of the Charlson CI and GFR was obtained (r=0.58, p=0.02).
Conclusion
The results indicate to different comorbidities in the CLL patients at the time of diagnosis. According to Charlson CI, both groups of the study were diagnosed with low overall 10- year survival (15%). However, there are gender differences in the structure of comorbidities. Thus, among women, kidney and urinary tract pathology is significantly more common, which is reflected by a decrease in GFR in this group compared to men. This fact is not considered by us as a specific feature of CLL patients. It was previously established that the pathology of kidneys and urinary tract occurs in the female population more often than in the male, due to the anatomical features of this part of the body. Taking this fact into account, in the appointment of chemotherapy in women with CLL and Charlson CI more than 6 the rate of GFR should be carefully examined.
Keywords
Chronic lymphocytic leukemia, Charlson comorbidity index, glomerular filtration rate, gender difference.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20544
[VALUE] => Gender aspects of comorbid pathology in patients with chronic lymphocytic leukemia
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Gender aspects of comorbid pathology in patients with chronic lymphocytic leukemia
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20789
[VALUE] => 1427
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1427
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20790
[VALUE] => 1428
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1428
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Мария В. Марковцева
Цель
Цель исследования – изучить гендерные особенности коморбидной патологии у пациентов с хроническим лимфолейкозом (ХЛЛ).
Материалы и методы
Обследовано 70 пациентов (35 мужчин и 35 женщин) в возрасте от 42 до 80 лет. В момент постановки диагноза ХЛЛ пациентам рассчитывали индекс коморбидности Charlson (ИК Charlson) и скорость клубочковй фильтрации (СКФ) по формуле MDRD. ИК Charlson представляет собой бальную систему оценки возраста и наличия определенных сопутствующих заболеваний и используется для оценки прогноза больных с длительными сроками наблюдения. Снижение СКФ также служит маркером для прогноза многих заболеваний. Установлено, что это один из факторов риска появления сердечно-сосудистых осложнений, которые приводят к повышению уровня смертности людей. Для статистической оценки полученных данных вычисляли среднее значение показателя и его стандартное отклонение. Для сравнения групп применялся t-критерий Стьюдента. Корреляционный анализ проводился по Пирсону. Достоверным считался уровень значимости при р <0,05.
Результаты
Средний возраст мужчин и женщин при постановки диагноза ХЛЛ был сопоставим и составлял 66,4±7,9 лет и 67,7±9,6 лет соответственно (р≥0,05). Так же не получили достоверных различий по уровню ИК Charlson в группах: 6,5±1,5 у мужчин и 6,8±1,6 у женщин (р≥0,05). Структура коморбидной патологии включала в себя наличие хронической сердечной недостаточности (87% – муж., 82% – жен.), хронических неспецифических заболеваний легких (43% – муж., 37% – жен.), нарушение мозгового кровообращения в анамнезе (23% – муж., 26% – жен.), сахарный диабет (14% – муж., 17% – жен.), заболевания почек и мочевыводящих путей (11% – муж., 43% – жен.), постинфарктный кардиосклероз (11% – муж., 8% – жен.), коллагенозы (0% – муж., 3% – жен.).
Расчет
СКФ по MDRD показал значимые различия в группах исследования. Этот параметр у женщин был достоверно ниже – 58,7±12,4 мл/мин/1,73м2 по сравнению с группой мужчин – 68,8±9,1 мл/мин/1,73м2 (р<0,05). Одновременно с этим в группе женщин получена обратная корреляционная связь средней степени между показателем ИК Charlson и СКФ (r=0,58, р=0,02).
Обсуждение и выводы
Полученные результаты свидетельствуют о богатой коморбидной патологии, имеющейся у пациентов с ХЛЛ на момент постановки диагноза. По ИК Charlson в обеих группах исследования в среднем диагностировали низкую общую 10-летнюю выживаемость (15%). Тем не менее, имеются гендерные отличия в структуре сопутствующих заболеваний. Так, среди женщин достоверно чаще встречается патология почек и мочевыводящих путей, что отражено снижением СКФ в этой группе по сравнению с мужчинами. Данный факт не рассматривается нами как особенность пациентов с ХЛЛ. Ранее установлено, что патология почек и мочевыводящих путей встречается в женской популяции чаще, чем в мужской, ввиду анатомических особенностей этого отдела тела. Беря этот факт во внимание, при назначении химиолечения у пациенток с ХЛЛ и ИК Charlson более 6 следует внимательно исследовать показатель СКФ.
Ключевые слова
Хронический лимфолейкоз, индекс коморбидности Charlson, скорость клубочковой фильтрации, гендерные различия.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20583
[VALUE] => Array
(
[TEXT] => Олеся О. Морозова, Ольга В.Ушакова, Алиса Г. Волкова
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Олеся О. Морозова, Ольга В.Ушакова, Алиса Г. Волкова
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20584
[VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20585
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Ситуация онкологического заболевания являясь психотравмирующей, может влиять на нормальное развитие детей. В игре дети будут использовать материалы, причиняющие им болезненные ощущения и дискомфорт, а также вызывающие страхи. Дети обследованы методами включенного наблюдения и клинико-диагностического интервью.
</p>
<h2 style="text-align: justify;">Объект исследования</h2>
<p style="text-align: justify;">
В исследование вошли 15 пациентов с гемобластозами и нейробластомами. Мамы этих детей дали письменное согласие на участие в данном исследовании. Среди пациентов, принявших участие в исследовании, было 6 мальчиков и 9 девочек в возрасте от 3 до 6 лет. Группой контроля стали дети, находящиеся в детских садах (2 группы детей по 7 и 8 человек в возрасте от 5 до 6 лет), в общей сложности 15 человек (7 мальчиков; 8 девочек).
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Практически во всех играх детей-пациентов роль врача исполняли сами дети. Только 1 ребенок отказался исполнять и роль врача и роль пациента. На роль «пациента» дети выбирали игрушку, предложенную психологом, собственные игрушки, маму и/или медицинского психолога. Продолжительность игры 15-20 минут. Пациенты в процессе игры предпочли настоящие медицинские инструменты (медицинский шприц, лейкопластырь, иглу-катетер «бабочка» и реже таблетки), нежели игрушечные. Чаще пациенты выбирали шприц и лейкопластырь. Из интервью с мамами стало известно, что для детей наиболее неприятными из медицинских процедур являются постановка инъекций и «переклейка катетера». Все дети из детского сада для манипуляций чаще всего использовали настоящие медицинские инструменты. Группа детей №1 чаще использовала медицинский шприц, иглу-катетер «бабочка», медицинский лейкопластырь, салфетки марлевые и таблетки. Группа детей №2 выбирала – медицинский шприц и медицинский бинт. Из всех медицинских игрушек обе группы детей чаще всего выбирали фонендоскоп, градусник, жидкие лекарства. Один пациент категорически отказался доставлять «игрушке-пациенту» болезненные ощущения. Остальные пациенты проявляли сочувствие к «игрушке-пациенту», поглаживали ее, в том числе по тем местам, куда была сделана инъекция или наложен лейкопластырь, использовали ласковые слова («немного потерпите»; «все будет хорошо»), желали выздоровления, и обнимали своих «пациентов». Один ребенок злился на своего «пациента», говоря: «Пусть тебе тоже будет больно». Дети из первой группы детского сада ругались на «игрушку-пациента» и говорили: «Сама виновата, что заболела». Дети из второй группы чаще всего проявляли сочувствие, подбадривали «игрушку-пациента», говорили, что «процедуры важны для выздоровления, и их нужно потерпеть». Исходя из беседы с вoспитателями: детям первой группы за неделю до игры делали прививки. У детей второй группы подобной медицинской процедуры не было. Дети второй группы демонстрировали более гуманное отношение к своим «пациентам», нежели дети первой группы.
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
1) В игре дети чаще всего используют те медицинские инструменты, которые доставляют им наибольший дискомфорт и/или болевые ощущения. 2) С помощью манипулирования предметами в игре, дети показывают свое состояние во время и после прохождения медицинских процедур, которые им наиболее неприятны. 3) С помощью манипулирования медицинскими инструментами в игре, дети выражают отрицательные эмоции по отношению к медицинским манипуляциям, при этом отрицательные эмоциональные реакции по-разному могут подавляться родителями пациента и/или медицинским персоналом. 4) Травматичность опыта прохождения медицинских процедур детьми и отношение к детям окружающих их взрослых в период заболевания, влияет на отношение самих детей к другим заболевшим.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Психология, игра, дети, лечение, эмоции.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Ситуация онкологического заболевания являясь психотравмирующей, может влиять на нормальное развитие детей. В игре дети будут использовать материалы, причиняющие им болезненные ощущения и дискомфорт, а также вызывающие страхи. Дети обследованы методами включенного наблюдения и клинико-диагностического интервью.
Объект исследования
В исследование вошли 15 пациентов с гемобластозами и нейробластомами. Мамы этих детей дали письменное согласие на участие в данном исследовании. Среди пациентов, принявших участие в исследовании, было 6 мальчиков и 9 девочек в возрасте от 3 до 6 лет. Группой контроля стали дети, находящиеся в детских садах (2 группы детей по 7 и 8 человек в возрасте от 5 до 6 лет), в общей сложности 15 человек (7 мальчиков; 8 девочек).
Результаты
Практически во всех играх детей-пациентов роль врача исполняли сами дети. Только 1 ребенок отказался исполнять и роль врача и роль пациента. На роль «пациента» дети выбирали игрушку, предложенную психологом, собственные игрушки, маму и/или медицинского психолога. Продолжительность игры 15-20 минут. Пациенты в процессе игры предпочли настоящие медицинские инструменты (медицинский шприц, лейкопластырь, иглу-катетер «бабочка» и реже таблетки), нежели игрушечные. Чаще пациенты выбирали шприц и лейкопластырь. Из интервью с мамами стало известно, что для детей наиболее неприятными из медицинских процедур являются постановка инъекций и «переклейка катетера». Все дети из детского сада для манипуляций чаще всего использовали настоящие медицинские инструменты. Группа детей №1 чаще использовала медицинский шприц, иглу-катетер «бабочка», медицинский лейкопластырь, салфетки марлевые и таблетки. Группа детей №2 выбирала – медицинский шприц и медицинский бинт. Из всех медицинских игрушек обе группы детей чаще всего выбирали фонендоскоп, градусник, жидкие лекарства. Один пациент категорически отказался доставлять «игрушке-пациенту» болезненные ощущения. Остальные пациенты проявляли сочувствие к «игрушке-пациенту», поглаживали ее, в том числе по тем местам, куда была сделана инъекция или наложен лейкопластырь, использовали ласковые слова («немного потерпите»; «все будет хорошо»), желали выздоровления, и обнимали своих «пациентов». Один ребенок злился на своего «пациента», говоря: «Пусть тебе тоже будет больно». Дети из первой группы детского сада ругались на «игрушку-пациента» и говорили: «Сама виновата, что заболела». Дети из второй группы чаще всего проявляли сочувствие, подбадривали «игрушку-пациента», говорили, что «процедуры важны для выздоровления, и их нужно потерпеть». Исходя из беседы с вoспитателями: детям первой группы за неделю до игры делали прививки. У детей второй группы подобной медицинской процедуры не было. Дети второй группы демонстрировали более гуманное отношение к своим «пациентам», нежели дети первой группы.
Выводы
1) В игре дети чаще всего используют те медицинские инструменты, которые доставляют им наибольший дискомфорт и/или болевые ощущения. 2) С помощью манипулирования предметами в игре, дети показывают свое состояние во время и после прохождения медицинских процедур, которые им наиболее неприятны. 3) С помощью манипулирования медицинскими инструментами в игре, дети выражают отрицательные эмоции по отношению к медицинским манипуляциям, при этом отрицательные эмоциональные реакции по-разному могут подавляться родителями пациента и/или медицинским персоналом. 4) Травматичность опыта прохождения медицинских процедур детьми и отношение к детям окружающих их взрослых в период заболевания, влияет на отношение самих детей к другим заболевшим.
Ключевые слова
Психология, игра, дети, лечение, эмоции.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20586
[VALUE] => Array
(
[TEXT] => Olesya O. Morozova, Olga B. Ushakova, Alisa G. Volkova
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Olesya O. Morozova, Olga B. Ushakova, Alisa G. Volkova
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20587
[VALUE] => Array
(
[TEXT] => R. Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation and Chair of Hematology, Transfusiology and Transplantation at the First St. Petersburg State I. Pavlov Medical University<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => R. Gorbacheva Memorial Research Institute for Pediatric Oncology, Hematology and Transplantation and Chair of Hematology, Transfusiology and Transplantation at the First St. Petersburg State I. Pavlov Medical University
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20588
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Cancer itself is a psycho-traumatic situation and may impair child’s normal development. When playing, the children utilize traumatic material associated with pain, discomfort and fear. The involved observation and clinical diagnostic interview methods were used to study this situation.
</p>
<h2>Patients and methods</h2>
<p style="text-align: justify;">
A total of 15 patients with leukemia or neuroblastoma were included in the study. Patients’ mothers signed an informed consent for participation in the study. Six of the study participants were boys and 9 girls, all aged 3 to 6 years. The control group consisted of 15 healthy preschool children (2 groups of 7 and 8 children aged 5 to 6 years), 7 boys and 8 girls.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
In most games, the role of a doctor was played by a child. Only one child declined to impersonate both a patient and a doctor. Younger children mostly agreed to have for a “patient” a toy (proposed by psychologist or one of child’s own), child’s mother or a medical psychologist. The game lasted for 15-20 minutes. Most patients preferred to handle real medical consumables and instruments (syringes, adhesive tape, winged infusion sets or, more rarely, pills). Most often a syringe or an adhesive tape was chosen. As known from the mothers, injections and changing implanted catheter dressings were most unpleasant medical manipulations for their children. Similarly, most healthy preschool children preferred to use real medical instruments than appropriate toys. Patients form group 1 more often used a syringe, a winged infusion set, adhesive tape, gauze or pills. Children from Group 2 most often choose syringe or gauze. Among medical instruments, both groups more often choose phonendoscope or thermometer. One patient refused to cause pain to a “toy patient”. Other children sympathized with a “toy patient”, fondled the injection or dressing sites, or used soothing terms (“wait a little”, “it’s going to be all right”), wished prompt recovery and hugged their “patients”. One child was angry over his “patient” wishing him to “get hurt too”. First preschool group children were mostly scolding a toy “patient” for “being guilty of getting sick”. Second group children were mostly compassionate, encouraged a “toy patient” telling that “all the procedures are needed to get healthy”. From children’s schoolmasters we know that all first group children received vaccination about a week before a test. Children from the second group had no injections within this terms. Overall attitude towards toy “patients” was more mild in the second group.
</p>
<h2 style="text-align: justify;">Conclusions</h2>
<p style="text-align: justify;">
1) When playing, the children mostly use the medical devices which cause them most discomfort and/or pain. 2) When manipulating the items children illustrate their own impression of medical procedures, which are most unpleasant. 3) Children may express their negative emotions directed towards medical manipulations via their play actions, these negative reactions may be suppressed in different ways by parents or medical staff. 4) The intensity of child’s own traumatic experience and an attitude of nearby adults may influence the child’s attitude towards other patients.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Psychology, games, children, treatment, emotions.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Introduction
Cancer itself is a psycho-traumatic situation and may impair child’s normal development. When playing, the children utilize traumatic material associated with pain, discomfort and fear. The involved observation and clinical diagnostic interview methods were used to study this situation.
Patients and methods
A total of 15 patients with leukemia or neuroblastoma were included in the study. Patients’ mothers signed an informed consent for participation in the study. Six of the study participants were boys and 9 girls, all aged 3 to 6 years. The control group consisted of 15 healthy preschool children (2 groups of 7 and 8 children aged 5 to 6 years), 7 boys and 8 girls.
Results
In most games, the role of a doctor was played by a child. Only one child declined to impersonate both a patient and a doctor. Younger children mostly agreed to have for a “patient” a toy (proposed by psychologist or one of child’s own), child’s mother or a medical psychologist. The game lasted for 15-20 minutes. Most patients preferred to handle real medical consumables and instruments (syringes, adhesive tape, winged infusion sets or, more rarely, pills). Most often a syringe or an adhesive tape was chosen. As known from the mothers, injections and changing implanted catheter dressings were most unpleasant medical manipulations for their children. Similarly, most healthy preschool children preferred to use real medical instruments than appropriate toys. Patients form group 1 more often used a syringe, a winged infusion set, adhesive tape, gauze or pills. Children from Group 2 most often choose syringe or gauze. Among medical instruments, both groups more often choose phonendoscope or thermometer. One patient refused to cause pain to a “toy patient”. Other children sympathized with a “toy patient”, fondled the injection or dressing sites, or used soothing terms (“wait a little”, “it’s going to be all right”), wished prompt recovery and hugged their “patients”. One child was angry over his “patient” wishing him to “get hurt too”. First preschool group children were mostly scolding a toy “patient” for “being guilty of getting sick”. Second group children were mostly compassionate, encouraged a “toy patient” telling that “all the procedures are needed to get healthy”. From children’s schoolmasters we know that all first group children received vaccination about a week before a test. Children from the second group had no injections within this terms. Overall attitude towards toy “patients” was more mild in the second group.
Conclusions
1) When playing, the children mostly use the medical devices which cause them most discomfort and/or pain. 2) When manipulating the items children illustrate their own impression of medical procedures, which are most unpleasant. 3) Children may express their negative emotions directed towards medical manipulations via their play actions, these negative reactions may be suppressed in different ways by parents or medical staff. 4) The intensity of child’s own traumatic experience and an attitude of nearby adults may influence the child’s attitude towards other patients.
Keywords
Psychology, games, children, treatment, emotions.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20589
[VALUE] => Study of fears caused by medical manipulations in children 3 to 6 years old
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Study of fears caused by medical manipulations in children 3 to 6 years old
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20797
[VALUE] => 1435
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1435
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20798
[VALUE] => 1436
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1436
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Олеся О. Морозова, Ольга В.Ушакова, Алиса Г. Волкова
Введение
Ситуация онкологического заболевания являясь психотравмирующей, может влиять на нормальное развитие детей. В игре дети будут использовать материалы, причиняющие им болезненные ощущения и дискомфорт, а также вызывающие страхи. Дети обследованы методами включенного наблюдения и клинико-диагностического интервью.
Объект исследования
В исследование вошли 15 пациентов с гемобластозами и нейробластомами. Мамы этих детей дали письменное согласие на участие в данном исследовании. Среди пациентов, принявших участие в исследовании, было 6 мальчиков и 9 девочек в возрасте от 3 до 6 лет. Группой контроля стали дети, находящиеся в детских садах (2 группы детей по 7 и 8 человек в возрасте от 5 до 6 лет), в общей сложности 15 человек (7 мальчиков; 8 девочек).
Результаты
Практически во всех играх детей-пациентов роль врача исполняли сами дети. Только 1 ребенок отказался исполнять и роль врача и роль пациента. На роль «пациента» дети выбирали игрушку, предложенную психологом, собственные игрушки, маму и/или медицинского психолога. Продолжительность игры 15-20 минут. Пациенты в процессе игры предпочли настоящие медицинские инструменты (медицинский шприц, лейкопластырь, иглу-катетер «бабочка» и реже таблетки), нежели игрушечные. Чаще пациенты выбирали шприц и лейкопластырь. Из интервью с мамами стало известно, что для детей наиболее неприятными из медицинских процедур являются постановка инъекций и «переклейка катетера». Все дети из детского сада для манипуляций чаще всего использовали настоящие медицинские инструменты. Группа детей №1 чаще использовала медицинский шприц, иглу-катетер «бабочка», медицинский лейкопластырь, салфетки марлевые и таблетки. Группа детей №2 выбирала – медицинский шприц и медицинский бинт. Из всех медицинских игрушек обе группы детей чаще всего выбирали фонендоскоп, градусник, жидкие лекарства. Один пациент категорически отказался доставлять «игрушке-пациенту» болезненные ощущения. Остальные пациенты проявляли сочувствие к «игрушке-пациенту», поглаживали ее, в том числе по тем местам, куда была сделана инъекция или наложен лейкопластырь, использовали ласковые слова («немного потерпите»; «все будет хорошо»), желали выздоровления, и обнимали своих «пациентов». Один ребенок злился на своего «пациента», говоря: «Пусть тебе тоже будет больно». Дети из первой группы детского сада ругались на «игрушку-пациента» и говорили: «Сама виновата, что заболела». Дети из второй группы чаще всего проявляли сочувствие, подбадривали «игрушку-пациента», говорили, что «процедуры важны для выздоровления, и их нужно потерпеть». Исходя из беседы с вoспитателями: детям первой группы за неделю до игры делали прививки. У детей второй группы подобной медицинской процедуры не было. Дети второй группы демонстрировали более гуманное отношение к своим «пациентам», нежели дети первой группы.
Выводы
1) В игре дети чаще всего используют те медицинские инструменты, которые доставляют им наибольший дискомфорт и/или болевые ощущения. 2) С помощью манипулирования предметами в игре, дети показывают свое состояние во время и после прохождения медицинских процедур, которые им наиболее неприятны. 3) С помощью манипулирования медицинскими инструментами в игре, дети выражают отрицательные эмоции по отношению к медицинским манипуляциям, при этом отрицательные эмоциональные реакции по-разному могут подавляться родителями пациента и/или медицинским персоналом. 4) Травматичность опыта прохождения медицинских процедур детьми и отношение к детям окружающих их взрослых в период заболевания, влияет на отношение самих детей к другим заболевшим.
Ключевые слова
Психология, игра, дети, лечение, эмоции.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20592
[VALUE] => Array
(
[TEXT] => Альберт Р. Муслимов, Александр С. Тимин, Юрий А. Серов
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Альберт Р. Муслимов, Александр С. Тимин, Юрий А. Серов
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20593
[VALUE] => Array
(
[TEXT] => Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Институт детской гематологии, онкологии и трансплантологии им. Р. М. Горбачевой, Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20594
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
В последние годы становится все более очевидным, что роль анти-донорских HLA антител, направленных против антигенов HLA класса I и II не ограничивается их участием в развитии сверхострого отторжения аллотрансплантатов. Все большее число исследователей склонны считать, что образование анти-донорских HLA антител в посттрансплантационный период приводит к развитию ускоренного острого, острого или хронического отторжения. Тест на иммунологическую совместимость между донором и реципиентом при трансплантации является решающим показателем для принятия решения о проведении трансплантации. Антитела к HLA обнаруживаются более чем у 30% населения, их выявление свидетельствует о предшествующей иммунизации HLA. Она возможна при многократном переливании цельной крови, во время беременности и после трансплантации. Ряд авторов отмечает, что донор неспецифические антитела к HLA являются одним из факторов не только риска острого, но и хронического отторжения трансплантата и учитываются, как плохой прогностический показатель [P.I.Terasaki, 2006; М. Моrrel, 2011; M. Crespo, 2011].
</p>
<h2 style="text-align: justify;">Цель</h2>
<p style="text-align: justify;">
Целью теста HLA-Crossmatch является обнаружение лимфоцитотоксических антител, специфичных для потенциального донора (то есть аллогенный перекрестный кроссматч) или у самого себя (то есть аутологичный перекрестный HLA-Crossmatch). Прямой HLA-Crossmatch, используется с сывороткой от предполагаемого реципиента (или донора для обратного HLA-Crossmatch) и клетками-мишенями являются мононуклеарные клетки потенциального донора (или реципиента для обратного HLA-Crossmatch. Используемые клетки-мишени могут быть не разделены или разделены на определенные группы, такие как Т- лимфоциты, В- лимфоциты, моноциты и т. д. Оценка результатов реакции HLA-Crossmatch крайне субъективна при простой оптической микроскопии, т.к. невозможно точно посчитать количество мертвых клеток в поле зрения камеры Терасаки и вычесть фон (результаты негативного контроля). Невозможна так же оценка к какому классу HLA (I или II) принадлежат антитела.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
Нами был разработан метод оценки результатов HLACrossmatch с использованием конфокального микроскопа у пациентов с трансплантацией костного мозга. Вся постановка реакции HLA-Crossmatch проводилась стандартным методом, кроме последнего этапа: окраски и оценки жизнеспособности лимфоцитов в лунках. Мы использовали Акридиновый Оранжевый (АО – эмиссия 525 нм) и Пропидиум Йодид (PI – 620 нм) как витальные красители. Для окраски B лимфоцитов использовались анти-CD19 моноклональные антитела, конъюгированные с PE-Cyanine7 (775 нм). Результаты регистрировались с помощью ZEISS конфокального микроскопа с последующим анализом изображений программным продуктом ImageJ (National Institutes of Health) c последующим обсчетом результатов нами созданной программой.
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
Предложенный нами метод оценки имеет следующие преимущества: 1) В одной лунке производится анализ одной сыворотки реципиента на наличие антител против донорских антигенов HLA одновременно и по I, и по II классу; 2) Метод является быстрым, точным и высокопроизводительным (в одной камере Терасаки за один запуск можно проанализировать до 72 сывороток); 3) Высокая чувствительность считывания флуоресцентной метки; 4) Наличие многоуровневой системы различных контролей; 5) Возможность архивирования полученных результатов в базе данных программы для интерпретации и PDF отчетов; 6) Субъективная оценка в анализе результатов сведена к минимуму за счет статистической обработки полученных данных программным обеспечением.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
HLA, перекрестный подбор HLA, трансплантация костного мозга, конфокальная микроскопия.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
В последние годы становится все более очевидным, что роль анти-донорских HLA антител, направленных против антигенов HLA класса I и II не ограничивается их участием в развитии сверхострого отторжения аллотрансплантатов. Все большее число исследователей склонны считать, что образование анти-донорских HLA антител в посттрансплантационный период приводит к развитию ускоренного острого, острого или хронического отторжения. Тест на иммунологическую совместимость между донором и реципиентом при трансплантации является решающим показателем для принятия решения о проведении трансплантации. Антитела к HLA обнаруживаются более чем у 30% населения, их выявление свидетельствует о предшествующей иммунизации HLA. Она возможна при многократном переливании цельной крови, во время беременности и после трансплантации. Ряд авторов отмечает, что донор неспецифические антитела к HLA являются одним из факторов не только риска острого, но и хронического отторжения трансплантата и учитываются, как плохой прогностический показатель [P.I.Terasaki, 2006; М. Моrrel, 2011; M. Crespo, 2011].
Цель
Целью теста HLA-Crossmatch является обнаружение лимфоцитотоксических антител, специфичных для потенциального донора (то есть аллогенный перекрестный кроссматч) или у самого себя (то есть аутологичный перекрестный HLA-Crossmatch). Прямой HLA-Crossmatch, используется с сывороткой от предполагаемого реципиента (или донора для обратного HLA-Crossmatch) и клетками-мишенями являются мононуклеарные клетки потенциального донора (или реципиента для обратного HLA-Crossmatch. Используемые клетки-мишени могут быть не разделены или разделены на определенные группы, такие как Т- лимфоциты, В- лимфоциты, моноциты и т. д. Оценка результатов реакции HLA-Crossmatch крайне субъективна при простой оптической микроскопии, т.к. невозможно точно посчитать количество мертвых клеток в поле зрения камеры Терасаки и вычесть фон (результаты негативного контроля). Невозможна так же оценка к какому классу HLA (I или II) принадлежат антитела.
Материалы и методы
Нами был разработан метод оценки результатов HLACrossmatch с использованием конфокального микроскопа у пациентов с трансплантацией костного мозга. Вся постановка реакции HLA-Crossmatch проводилась стандартным методом, кроме последнего этапа: окраски и оценки жизнеспособности лимфоцитов в лунках. Мы использовали Акридиновый Оранжевый (АО – эмиссия 525 нм) и Пропидиум Йодид (PI – 620 нм) как витальные красители. Для окраски B лимфоцитов использовались анти-CD19 моноклональные антитела, конъюгированные с PE-Cyanine7 (775 нм). Результаты регистрировались с помощью ZEISS конфокального микроскопа с последующим анализом изображений программным продуктом ImageJ (National Institutes of Health) c последующим обсчетом результатов нами созданной программой.
Выводы
Предложенный нами метод оценки имеет следующие преимущества: 1) В одной лунке производится анализ одной сыворотки реципиента на наличие антител против донорских антигенов HLA одновременно и по I, и по II классу; 2) Метод является быстрым, точным и высокопроизводительным (в одной камере Терасаки за один запуск можно проанализировать до 72 сывороток); 3) Высокая чувствительность считывания флуоресцентной метки; 4) Наличие многоуровневой системы различных контролей; 5) Возможность архивирования полученных результатов в базе данных программы для интерпретации и PDF отчетов; 6) Субъективная оценка в анализе результатов сведена к минимуму за счет статистической обработки полученных данных программным обеспечением.
Ключевые слова
HLA, перекрестный подбор HLA, трансплантация костного мозга, конфокальная микроскопия.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20595
[VALUE] => Array
(
[TEXT] => Аlbert R. Muslimov, Alexander S. Timin, Yury A. Serov
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Аlbert R. Muslimov, Alexander S. Timin, Yury A. Serov
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20596
[VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Raisa Gorbacheva Memorial Institute of Children’s Hematology, Oncology, and Transplantation, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20597
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Currently, it has become progressively ostensible that the role of the anti-donor antibody against HLA class I and II antigens is not limited to their participation in the development of hyperacute rejection of allografts. An increasing number of researchers are inclined to believe that the formation of anti-donor HLA antibody in the posttransplant period leads to the development of hyperacute, acute or chronic rejection. The immunological compatibility test between donor and recipient for transplantation is the critical factor for deciding whether to perform a transplant. Antibodies to HLA founded in more than 30% of the population; their detection indicates a prior immunization with HLA. It is possible with multiple transfusion of whole blood, during pregnancy and after transplantation. A number of authors making a point that the donor non-specific antibodies to HLA are one of the factors not only of the risk of acute but also chronic rejection of the transplant and are considered as a poor prognostic indicator [P.I. Terasaki, 2006; M. Morrel, 2011; M. Crespo, 2011].
</p>
<h2 style="text-align: justify;">Aim</h2>
<p style="text-align: justify;">
The purpose of the lymphocyte crossmatch is to detect the lymphocytotoxic antibodies specific to a potential donor (i.e., allogeneic crossmatch) or self (i.e., autologous crossmatch.) A forward crossmatch used with serum from a prospective recipient (or donor for reverse crossmatch) and the target cells are the mononuclear cells of the potential donor (or recipient for reverse crossmatch). The target cells used may be unseparated or separated into specific subsets such as T cell lymphocytes, B cell lymphocytes, monocytes, etc. Evaluation of the results of the HLA-Crossmatch reaction is highly subjective by simple optical microscopy because it is impossible to accurately calculate the number of dead cells at the Terasaki camera view field and subtract the background (the results of negative control). It is also problematic to estimate to which class of HLA (I or II) antibodies belong.
</p>
<h2 style="text-align: justify;">Materials and methods</h2>
<p style="text-align: justify;">
We developed a methodology for evaluating the results of HLA-crossmatch using a confocal microscope of the bone marrow transplantation patients. The entire HLA-crossmatch reaction performed by a standard method, except for the last two steps: staining and evaluation of the viability of lymphocytes in the wells. We used Acridine Orange (AO emission 525 nm) and Propidium Iodide (PI – 620 nm) as vital dyes. To stain B-lymphocytes, anti-CD19 monoclonal antibodies conjugated to PE-Cyanine7 (775 nm) were used. The images taken with a ZEISS confocal microscope, followed by image analysis with the ImageJ software (National Institutes of Health), and then calculating the results with the program.
</p>
<h2 style="text-align: justify;">Conclusions</h2>
<p style="text-align: justify;">
The advantages of the proposed method of evaluation are as follows: (1) In one well, a single serum sample of the recipient is analyzed for the presence of antibodies against donor HLA antigens simultaneously at both I and II classes. 2) The method is fast, accurate and high-performance (in one Terasaki plate, up to 72 sera samples can be analyzed in one run). 3) The high sensitivity of fluorescent label reading. (4) Presence of a multilevel system of various controls. (5) The ability to archive the results obtained in the program database for interpretation and PDF reports. (6) Subjective biases of the data analysis are minimized by statistical processing of the data by software.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
HLA, HLA-crossmatch, bone marrow transplantation, confocal microscopy.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Currently, it has become progressively ostensible that the role of the anti-donor antibody against HLA class I and II antigens is not limited to their participation in the development of hyperacute rejection of allografts. An increasing number of researchers are inclined to believe that the formation of anti-donor HLA antibody in the posttransplant period leads to the development of hyperacute, acute or chronic rejection. The immunological compatibility test between donor and recipient for transplantation is the critical factor for deciding whether to perform a transplant. Antibodies to HLA founded in more than 30% of the population; their detection indicates a prior immunization with HLA. It is possible with multiple transfusion of whole blood, during pregnancy and after transplantation. A number of authors making a point that the donor non-specific antibodies to HLA are one of the factors not only of the risk of acute but also chronic rejection of the transplant and are considered as a poor prognostic indicator [P.I. Terasaki, 2006; M. Morrel, 2011; M. Crespo, 2011].
Aim
The purpose of the lymphocyte crossmatch is to detect the lymphocytotoxic antibodies specific to a potential donor (i.e., allogeneic crossmatch) or self (i.e., autologous crossmatch.) A forward crossmatch used with serum from a prospective recipient (or donor for reverse crossmatch) and the target cells are the mononuclear cells of the potential donor (or recipient for reverse crossmatch). The target cells used may be unseparated or separated into specific subsets such as T cell lymphocytes, B cell lymphocytes, monocytes, etc. Evaluation of the results of the HLA-Crossmatch reaction is highly subjective by simple optical microscopy because it is impossible to accurately calculate the number of dead cells at the Terasaki camera view field and subtract the background (the results of negative control). It is also problematic to estimate to which class of HLA (I or II) antibodies belong.
Materials and methods
We developed a methodology for evaluating the results of HLA-crossmatch using a confocal microscope of the bone marrow transplantation patients. The entire HLA-crossmatch reaction performed by a standard method, except for the last two steps: staining and evaluation of the viability of lymphocytes in the wells. We used Acridine Orange (AO emission 525 nm) and Propidium Iodide (PI – 620 nm) as vital dyes. To stain B-lymphocytes, anti-CD19 monoclonal antibodies conjugated to PE-Cyanine7 (775 nm) were used. The images taken with a ZEISS confocal microscope, followed by image analysis with the ImageJ software (National Institutes of Health), and then calculating the results with the program.
Conclusions
The advantages of the proposed method of evaluation are as follows: (1) In one well, a single serum sample of the recipient is analyzed for the presence of antibodies against donor HLA antigens simultaneously at both I and II classes. 2) The method is fast, accurate and high-performance (in one Terasaki plate, up to 72 sera samples can be analyzed in one run). 3) The high sensitivity of fluorescent label reading. (4) Presence of a multilevel system of various controls. (5) The ability to archive the results obtained in the program database for interpretation and PDF reports. (6) Subjective biases of the data analysis are minimized by statistical processing of the data by software.
Keywords
HLA, HLA-crossmatch, bone marrow transplantation, confocal microscopy.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20598
[VALUE] => Potentials and prospects of using a confocal microscopy for the HLA-Crossmatch result evaluation in bone marrow transplantation patients
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Potentials and prospects of using a confocal microscopy for the HLA-Crossmatch result evaluation in bone marrow transplantation patients
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20799
[VALUE] => 1437
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1437
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20800
[VALUE] => 1438
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1438
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Альберт Р. Муслимов, Александр С. Тимин, Юрий А. Серов
Введение
В последние годы становится все более очевидным, что роль анти-донорских HLA антител, направленных против антигенов HLA класса I и II не ограничивается их участием в развитии сверхострого отторжения аллотрансплантатов. Все большее число исследователей склонны считать, что образование анти-донорских HLA антител в посттрансплантационный период приводит к развитию ускоренного острого, острого или хронического отторжения. Тест на иммунологическую совместимость между донором и реципиентом при трансплантации является решающим показателем для принятия решения о проведении трансплантации. Антитела к HLA обнаруживаются более чем у 30% населения, их выявление свидетельствует о предшествующей иммунизации HLA. Она возможна при многократном переливании цельной крови, во время беременности и после трансплантации. Ряд авторов отмечает, что донор неспецифические антитела к HLA являются одним из факторов не только риска острого, но и хронического отторжения трансплантата и учитываются, как плохой прогностический показатель [P.I.Terasaki, 2006; М. Моrrel, 2011; M. Crespo, 2011].
Цель
Целью теста HLA-Crossmatch является обнаружение лимфоцитотоксических антител, специфичных для потенциального донора (то есть аллогенный перекрестный кроссматч) или у самого себя (то есть аутологичный перекрестный HLA-Crossmatch). Прямой HLA-Crossmatch, используется с сывороткой от предполагаемого реципиента (или донора для обратного HLA-Crossmatch) и клетками-мишенями являются мононуклеарные клетки потенциального донора (или реципиента для обратного HLA-Crossmatch. Используемые клетки-мишени могут быть не разделены или разделены на определенные группы, такие как Т- лимфоциты, В- лимфоциты, моноциты и т. д. Оценка результатов реакции HLA-Crossmatch крайне субъективна при простой оптической микроскопии, т.к. невозможно точно посчитать количество мертвых клеток в поле зрения камеры Терасаки и вычесть фон (результаты негативного контроля). Невозможна так же оценка к какому классу HLA (I или II) принадлежат антитела.
Материалы и методы
Нами был разработан метод оценки результатов HLACrossmatch с использованием конфокального микроскопа у пациентов с трансплантацией костного мозга. Вся постановка реакции HLA-Crossmatch проводилась стандартным методом, кроме последнего этапа: окраски и оценки жизнеспособности лимфоцитов в лунках. Мы использовали Акридиновый Оранжевый (АО – эмиссия 525 нм) и Пропидиум Йодид (PI – 620 нм) как витальные красители. Для окраски B лимфоцитов использовались анти-CD19 моноклональные антитела, конъюгированные с PE-Cyanine7 (775 нм). Результаты регистрировались с помощью ZEISS конфокального микроскопа с последующим анализом изображений программным продуктом ImageJ (National Institutes of Health) c последующим обсчетом результатов нами созданной программой.
Выводы
Предложенный нами метод оценки имеет следующие преимущества: 1) В одной лунке производится анализ одной сыворотки реципиента на наличие антител против донорских антигенов HLA одновременно и по I, и по II классу; 2) Метод является быстрым, точным и высокопроизводительным (в одной камере Терасаки за один запуск можно проанализировать до 72 сывороток); 3) Высокая чувствительность считывания флуоресцентной метки; 4) Наличие многоуровневой системы различных контролей; 5) Возможность архивирования полученных результатов в базе данных программы для интерпретации и PDF отчетов; 6) Субъективная оценка в анализе результатов сведена к минимуму за счет статистической обработки полученных данных программным обеспечением.
Ключевые слова
HLA, перекрестный подбор HLA, трансплантация костного мозга, конфокальная микроскопия.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20620
[VALUE] => Array
(
[TEXT] => Всеволод Г. Потапенко <sup>1</sup>,<sup>2</sup>, Наталья Б. Михайлова <sup>1</sup>, Ирина А. Скороход <sup>2</sup>, Дарья А. Чигинская <sup>2</sup>, Виктория В. Рябчикова <sup>2</sup>, Элеонора И. Подольцева <sup>2</sup>, Виктор В. Ипатов <sup>3</sup>, Игорь В. Байков <sup>3</sup>, Вячеслав Н. Семелев <sup>3</sup>, Дмитрий А. Горностаев <sup>3</sup>, Надежда В. Медведева <sup>2</sup>, Борис В. Афанасьев <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Всеволод Г. Потапенко 1,2, Наталья Б. Михайлова 1, Ирина А. Скороход 2, Дарья А. Чигинская 2, Виктория В. Рябчикова 2, Элеонора И. Подольцева 2, Виктор В. Ипатов 3, Игорь В. Байков 3, Вячеслав Н. Семелев 3, Дмитрий А. Горностаев 3, Надежда В. Медведева 2, Борис В. Афанасьев 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20621
[VALUE] => Array
(
[TEXT] => <sup>1</sup> Первый Санкт-Петербургский государственный медицинский ниверситет им И. П. Павлова, Санкт-Петербург<br>
<sup>2</sup> Городской гематологический центр, Городская клиническая больница №31, Санкт-Петербург<br>
<sup>3</sup> Военно-медицинская Академия им. С. М. Кирова, Санкт-Петербург
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Первый Санкт-Петербургский государственный медицинский ниверситет им И. П. Павлова, Санкт-Петербург
2 Городской гематологический центр, Городская клиническая больница №31, Санкт-Петербург
3 Военно-медицинская Академия им. С. М. Кирова, Санкт-Петербург
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20622
[VALUE] => Array
(
[TEXT] => <h2 style="text-align: justify;">Цель</h2>
<p style="text-align: justify;">
Целью работы был анализ показателей общей и бессобытийной выживаемости в зависимости от различных прогностических факторов.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
Проанализированы данные 84 пациентов. Медиана возраста 26,6 года (18-62). Медиана наблюдения составила 49 месяцев (0,5-115 мес.). Исследованы влияния: пола, ответа на первичное лечение, скорости развития рецидива, варианта химиотерапии второй линии, В-симптомов, конгломератов более 5 см (в рецидиве и непосредственно перед ВДХТ), уровней альбумина и ЛДГ крови, КТ-ответа, общего количества линий химиотерапии, режима кондиционирования перед АТГСК, метаболической активности опухоли до ВДХТ (ПЭТ1) и после АТГСК (ПЭТ2). Для статистического анализа использованы методы Каплана-Мейера, Кокса, статистические критерии Манна-Уитни и Хи-квадрат. Результаты. Приведены показатели общей и бессобытийной выживаемости, а также расчет отношения рисков для факторов, показавших статистическую достоверность менее 0,05 (Табл. 1, 2). При анализе бессобытийной выживаемости выявлены статистически значимые различия в выживаемости при негативности по ПЭТ1 и ПЭТ2 по сравнению с группой пациентов с позитивностью очагов по ПЭТ1 и ПЭТ2 (Табл. 3, 4). Других различий не выявлено.
</p>
<h2 style="text-align: justify;">Вывод</h2>
<p style="text-align: justify;">
Исследование показало, что наиболее важными факторами прогноза бессобытийной выживаемости пациентов с ЛХ после ВДХТ/АТГСК являются повышение активности ЛДГ, наличие В-симптомов в рецидиве, позитивность по ПЭТ1, предлеченность и, особенно, отсутствие ответа по данным КТ и определение метаболической активности после ВДХТ/АТГСК.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Лимфома Ходжкина, аутологичная трансплантация стволовых клеток, ПЭТ, ЛДГ, альбумин.
</p>
<h2 style="text-align: justify;">
Таблица 1. Четырехлетняя бессобытийная выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)<br>
</h2>
<table border="1" cellpadding="1" cellspacing="1">
<tbody>
<tr>
<td>
Факторы
</td>
<td>
Есть
</td>
<td>
Нет
</td>
<td>
p
</td>
</tr>
<tr>
<td>
B-симптомы в рецидиве
</td>
<td>
35%
</td>
<td>
61%
</td>
<td>
0,0246
</td>
</tr>
<tr>
<td>
Гипоальбуминемия
</td>
<td>
33%<br>
</td>
<td>
62%<br>
</td>
<td>
0,0494
</td>
</tr>
<tr>
<td>
Повышение активности ЛДГ
</td>
<td>
36%
</td>
<td>
66%
</td>
<td>
0,0302
</td>
</tr>
<tr>
<td>
Отсутствие ответа по данным КТ
</td>
<td>
33%
</td>
<td>
66%
</td>
<td>
0,0035
</td>
</tr>
<tr>
<td>
Позитивность по ПЭТ1
</td>
<td>
31%<br>
</td>
<td>
70%
</td>
<td>
0,0072
</td>
</tr>
<tr>
<td>
Позитивность по ПЭТ2
</td>
<td>
42%
</td>
<td>
61%
</td>
<td>
0,050
</td>
</tr>
<tr>
<td>
Предлеченность (более трех линий химиотерапии)
</td>
<td>
31%
</td>
<td>
59%
</td>
<td>
0,0289
</td>
</tr>
</tbody>
</table>
<h2>Таблица 2. Четырехлетняя общая выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)</h2>
<table border="1" cellpadding="1" cellspacing="1">
<tbody>
<tr>
<td>
Факторы
</td>
<td>
Есть
</td>
<td>
Нет
</td>
<td>
p
</td>
</tr>
<tr>
<td>
В-симптомы в рецидиве
</td>
<td>
45%
</td>
<td>
80%
</td>
<td>
0,0006
</td>
</tr>
<tr>
<td>
Гипоальбуминемия
</td>
<td>
46%
</td>
<td>
74%
</td>
<td>
0,0372
</td>
</tr>
<tr>
<td>
Повышение активности ЛДГ
</td>
<td>
52%
</td>
<td>
78%<br>
</td>
<td>
0,0340
</td>
</tr>
<tr>
<td>
Отсутствие ответа по данным КТ
</td>
<td>
52%
</td>
<td>
79%
</td>
<td>
0,0158
</td>
</tr>
</tbody>
</table>
<h2>Таблица 3. Однофакторный анализ факторов риска общей и бессобытийной выживаемости (метод Кокса, стат. критерий Хи-квадрат)</h2>
<table>
<tbody>
<tr>
<td>
Фактор
</td>
<td>
Отношение рисков
</td>
<td colspan="2">
Доверительный интервал 95%
</td>
<td>
Р
</td>
</tr>
<tr>
<td colspan="5">
Общая выживаемость
</td>
</tr>
<tr>
<td>
В-симптомы в рецидиве
</td>
<td>
0,27
</td>
<td>
0,11
</td>
<td>
0,62
</td>
<td>
0,002
</td>
</tr>
<tr>
<td>
Отсутствие ответа по данным КТ
</td>
<td>
0,37
</td>
<td>
0,17
</td>
<td>
0,83
</td>
<td>
0,016
</td>
</tr>
<tr>
<td>
ЛДГ
</td>
<td>
0,38
</td>
<td>
0,15
</td>
<td>
0,95
</td>
<td>
0,037
</td>
</tr>
<tr>
<td colspan="5">
Бессобытийная выживаемость
</td>
</tr>
<tr>
<td>
Отсутствие ответа по КТ
</td>
<td>
0,36
</td>
<td>
0,18
</td>
<td>
0,68
</td>
<td>
0,001
</td>
</tr>
<tr>
<td>
Позитивность по ПЭТ1
</td>
<td>
0,36
</td>
<td>
0,17
</td>
<td>
0,75
</td>
<td>
0,006
</td>
</tr>
<tr>
<td>
В-симптомы в рецидиве
</td>
<td>
0,47
</td>
<td>
0,24
</td>
<td>
0,92
</td>
<td>
0,002
</td>
</tr>
<tr>
<td>
Предлеченность(более трех линий химиотерапии)
</td>
<td>
0,41
</td>
<td>
0,21
</td>
<td>
0,81
</td>
<td>
0,01
</td>
</tr>
<tr>
<td>
ЛДГ
</td>
<td>
0,45
</td>
<td>
0,21
</td>
<td>
0,96
</td>
<td>
0,04
</td>
</tr>
</tbody>
</table>
<h2>Таблица 4. Многофакторный анализ факторов риска бессобытийной выживаемости (метод Кокса, критерий Хи- квадрат)</h2>
<table border="1" cellpadding="1" cellspacing="1">
<tbody>
<tr>
<td>
Фактор
</td>
<td>
Отношение рисков
</td>
<td colspan="2">
Доверительный интервал 95%
</td>
<td>
p
</td>
</tr>
<tr>
<td>
Отсутствие ответа по КТ
</td>
<td>
0,38
</td>
<td>
0,16
</td>
<td>
0,89
</td>
<td>
0,026
</td>
</tr>
<tr>
<td>
Позитивность по ПЭТ2
</td>
<td>
0,42
</td>
<td>
0,18
</td>
<td>
0,97
</td>
<td>
0,043
</td>
</tr>
</tbody>
</table>
<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Цель
Целью работы был анализ показателей общей и бессобытийной выживаемости в зависимости от различных прогностических факторов.
Пациенты и методы
Проанализированы данные 84 пациентов. Медиана возраста 26,6 года (18-62). Медиана наблюдения составила 49 месяцев (0,5-115 мес.). Исследованы влияния: пола, ответа на первичное лечение, скорости развития рецидива, варианта химиотерапии второй линии, В-симптомов, конгломератов более 5 см (в рецидиве и непосредственно перед ВДХТ), уровней альбумина и ЛДГ крови, КТ-ответа, общего количества линий химиотерапии, режима кондиционирования перед АТГСК, метаболической активности опухоли до ВДХТ (ПЭТ1) и после АТГСК (ПЭТ2). Для статистического анализа использованы методы Каплана-Мейера, Кокса, статистические критерии Манна-Уитни и Хи-квадрат. Результаты. Приведены показатели общей и бессобытийной выживаемости, а также расчет отношения рисков для факторов, показавших статистическую достоверность менее 0,05 (Табл. 1, 2). При анализе бессобытийной выживаемости выявлены статистически значимые различия в выживаемости при негативности по ПЭТ1 и ПЭТ2 по сравнению с группой пациентов с позитивностью очагов по ПЭТ1 и ПЭТ2 (Табл. 3, 4). Других различий не выявлено.
Вывод
Исследование показало, что наиболее важными факторами прогноза бессобытийной выживаемости пациентов с ЛХ после ВДХТ/АТГСК являются повышение активности ЛДГ, наличие В-симптомов в рецидиве, позитивность по ПЭТ1, предлеченность и, особенно, отсутствие ответа по данным КТ и определение метаболической активности после ВДХТ/АТГСК.
Ключевые слова
Лимфома Ходжкина, аутологичная трансплантация стволовых клеток, ПЭТ, ЛДГ, альбумин.
Таблица 1. Четырехлетняя бессобытийная выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)
| Факторы | Есть | Нет | p |
| B-симптомы в рецидиве | 35% | 61% | 0,0246 |
| Гипоальбуминемия |
33% |
62% |
0,0494 |
| Повышение активности ЛДГ | 36% | 66% | 0,0302 |
| Отсутствие ответа по данным КТ | 33% | 66% | 0,0035 |
| Позитивность по ПЭТ1 |
31% |
70% | 0,0072 |
| Позитивность по ПЭТ2 | 42% | 61% | 0,050 |
| Предлеченность (более трех линий химиотерапии) | 31% | 59% | 0,0289 |
Таблица 2. Четырехлетняя общая выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)
| Факторы | Есть | Нет | p |
| В-симптомы в рецидиве | 45% | 80% | 0,0006 |
| Гипоальбуминемия | 46% | 74% | 0,0372 |
| Повышение активности ЛДГ | 52% |
78% |
0,0340 |
| Отсутствие ответа по данным КТ | 52% | 79% | 0,0158 |
Таблица 3. Однофакторный анализ факторов риска общей и бессобытийной выживаемости (метод Кокса, стат. критерий Хи-квадрат)
| Фактор | Отношение рисков | Доверительный интервал 95% | Р | |
| Общая выживаемость | ||||
| В-симптомы в рецидиве | 0,27 | 0,11 | 0,62 | 0,002 |
| Отсутствие ответа по данным КТ | 0,37 | 0,17 | 0,83 | 0,016 |
| ЛДГ | 0,38 | 0,15 | 0,95 | 0,037 |
| Бессобытийная выживаемость | ||||
| Отсутствие ответа по КТ | 0,36 | 0,18 | 0,68 | 0,001 |
| Позитивность по ПЭТ1 | 0,36 | 0,17 | 0,75 | 0,006 |
| В-симптомы в рецидиве | 0,47 | 0,24 | 0,92 | 0,002 |
| Предлеченность(более трех линий химиотерапии) | 0,41 | 0,21 | 0,81 | 0,01 |
| ЛДГ | 0,45 | 0,21 | 0,96 | 0,04 |
Таблица 4. Многофакторный анализ факторов риска бессобытийной выживаемости (метод Кокса, критерий Хи- квадрат)
| Фактор | Отношение рисков | Доверительный интервал 95% | p | |
| Отсутствие ответа по КТ | 0,38 | 0,16 | 0,89 | 0,026 |
| Позитивность по ПЭТ2 | 0,42 | 0,18 | 0,97 | 0,043 |
[TYPE] => HTML ) [~DESCRIPTION] => [~NAME] => Описание/Резюме [~DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) ) [DOI] => Array ( [ID] => 28 [TIMESTAMP_X] => 2016-04-06 14:11:12 [IBLOCK_ID] => 2 [NAME] => DOI [ACTIVE] => Y [SORT] => 500 [CODE] => DOI [DEFAULT_VALUE] => [PROPERTY_TYPE] => S [ROW_COUNT] => 1 [COL_COUNT] => 80 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 28 [FILE_TYPE] => [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => [USER_TYPE_SETTINGS] => [HINT] => [PROPERTY_VALUE_ID] => [VALUE] => [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => [~DESCRIPTION] => [~NAME] => DOI [~DEFAULT_VALUE] => ) [AUTHOR_EN] => Array ( [ID] => 37 [TIMESTAMP_X] => 2015-09-02 18:02:59 [IBLOCK_ID] => 2 [NAME] => Author [ACTIVE] => Y [SORT] => 500 [CODE] => AUTHOR_EN [DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) [PROPERTY_TYPE] => S [ROW_COUNT] => 1 [COL_COUNT] => 30 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 37 [FILE_TYPE] => [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => HTML [USER_TYPE_SETTINGS] => Array ( [height] => 200 ) [HINT] => [PROPERTY_VALUE_ID] => 20623 [VALUE] => Array ( [TEXT] => Vsevolod G. Potapenko <sup>1</sup>,<sup>2</sup>, Natalia B. Mikhaylova <sup>1</sup>, Irina A. Skorokhod <sup>2</sup>, Darya A. Chaginskaya <sup>2</sup>, Viktoria V. Ryabchikova <sup>2</sup>, Eleonora I. Podoltseva <sup>2</sup>, Viktor V. Ipatov <sup>3</sup>, Igor V. Baykov <sup>3</sup>, Vyacheslav N. Semelev <sup>3</sup>, Dmitrij A. Gornostaev <sup>3</sup>, Nadezhda V. Medvedeva <sup>2</sup>, Boris V. Afanasyev <sup>1</sup> [TYPE] => HTML ) [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => Array ( [TEXT] => Vsevolod G. Potapenko 1,2, Natalia B. Mikhaylova 1, Irina A. Skorokhod 2, Darya A. Chaginskaya 2, Viktoria V. Ryabchikova 2, Eleonora I. Podoltseva 2, Viktor V. Ipatov 3, Igor V. Baykov 3, Vyacheslav N. Semelev 3, Dmitrij A. Gornostaev 3, Nadezhda V. Medvedeva 2, Boris V. Afanasyev 1 [TYPE] => HTML ) [~DESCRIPTION] => [~NAME] => Author [~DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) ) [ORGANIZATION_EN] => Array ( [ID] => 38 [TIMESTAMP_X] => 2015-09-02 18:02:59 [IBLOCK_ID] => 2 [NAME] => Organization [ACTIVE] => Y [SORT] => 500 [CODE] => ORGANIZATION_EN [DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) [PROPERTY_TYPE] => S [ROW_COUNT] => 1 [COL_COUNT] => 30 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 38 [FILE_TYPE] => [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => HTML [USER_TYPE_SETTINGS] => Array ( [height] => 200 ) [HINT] => [PROPERTY_VALUE_ID] => 20624 [VALUE] => Array ( [TEXT] => <sup>1</sup> First St. Petersburg State I. Pavlov Medical University, St. Petersburg<br> <sup>2</sup> Haematology Department, Municipal Clinical Hospital №31, St. Petersburg<br> <sup>3</sup> S. Kirov Military Medical Academy, St. Petersburg, Russia<br> [TYPE] => HTML ) [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => Array ( [TEXT] => 1 First St. Petersburg State I. Pavlov Medical University, St. Petersburg
2 Haematology Department, Municipal Clinical Hospital №31, St. Petersburg
3 S. Kirov Military Medical Academy, St. Petersburg, Russia
[TYPE] => HTML ) [~DESCRIPTION] => [~NAME] => Organization [~DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) ) [SUMMARY_EN] => Array ( [ID] => 39 [TIMESTAMP_X] => 2015-09-02 18:02:59 [IBLOCK_ID] => 2 [NAME] => Description / Summary [ACTIVE] => Y [SORT] => 500 [CODE] => SUMMARY_EN [DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) [PROPERTY_TYPE] => S [ROW_COUNT] => 1 [COL_COUNT] => 30 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 39 [FILE_TYPE] => [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => HTML [USER_TYPE_SETTINGS] => Array ( [height] => 200 ) [HINT] => [PROPERTY_VALUE_ID] => 20625 [VALUE] => Array ( [TEXT] => <h2 style="text-align: justify;">Aim</h2> <p style="text-align: justify;"> The study was aimed for evaluation of prognostic significance of different factors by event free and overall survival analysis in patients after high dose therapy with stem cells support (HDT/AHSCT). </p> <h2 style="text-align: justify;">Patients and methods</h2> <p style="text-align: justify;"> Retrospective analysis includes the data of 84 patients with resistant or relapsed Hodgkin lymphoma. Median age was 26.6 years (18-62). Median follow-up is 49 (0.5-115) months. Prognostic factors analyzed included sex, response to the initial chemotherapy, time to relapse, B-symptoms on relapse, serum LDH and albumin levels, response assessed by computer tomography, number of chemotherapy lines before AHSCT, PET-scan results before (PET1) and after (PET2) AHSCT. Survival was estimated using Kaplan-Meier, Cox methods, Chi-square and log-rank test. Results. Four-year overall survival and event-free survival were 70% and 54% respectively (Tables 1, 2). The presented factors had significant value in survival prediction.<br> In the combined analysis of PET1 and PET2 significant difference observed only in patients with positivity by PET1 and PET2 compared with group with negative PET1 and PET2 results (Tables 3, 4). Conclusion. Our work has revealed that the most significant factors of the event free survival in patients with Hodgkin lymphoma after HDC/AHSCT are: elevation of the LDH activity, В-symptoms, pretreatment, positivity by PET1 and especially lack of response by CT-scan and positivity by PET2. </p> <h2 style="text-align: justify;">Keywords</h2> <p style="text-align: justify;"> Hodgkin lymphoma, autologous stem cell transplant, PET, LDH, albumin. </p> <h2 style="text-align: justify;"> Table 1. Four-year event-free survival (Kaplan-Meier analysis, log-rank test)<br> </h2> <p style="text-align: justify;"> <img width="783" alt="39_table 1.png" src="/upload/medialibrary/818/39_table-1.png" height="217" title="39_table 1.png"><br> </p> <h2 style="text-align: justify;"> Table 2. Four-year overall survival (Kaplan-Meier analysis, log-rank test)<br> </h2> <img width="783" alt="39_table 2.png" src="/upload/medialibrary/c99/39_table-2.png" height="139" title="39_table 2.png"> <h2>Table 3. Univariate analysis of risk factors for event-free and overall survival (Cox models, Chi-square test)</h2> <img width="783" alt="39_table 3.png" src="/upload/medialibrary/4d5/39_table-3.png" height="299" title="39_table 3.png"> <h2>Table 4. Multivariate analysis of risk factors for event-free survival (Cox models, Chi-square test)</h2> <img width="783" alt="39_table 4.png" src="/upload/medialibrary/6fd/39_table-4.png" height="83" title="39_table 4.png"><br> [TYPE] => HTML ) [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => Array ( [TEXT] =>
Aim
The study was aimed for evaluation of prognostic significance of different factors by event free and overall survival analysis in patients after high dose therapy with stem cells support (HDT/AHSCT).
Patients and methods
Retrospective analysis includes the data of 84 patients with resistant or relapsed Hodgkin lymphoma. Median age was 26.6 years (18-62). Median follow-up is 49 (0.5-115) months. Prognostic factors analyzed included sex, response to the initial chemotherapy, time to relapse, B-symptoms on relapse, serum LDH and albumin levels, response assessed by computer tomography, number of chemotherapy lines before AHSCT, PET-scan results before (PET1) and after (PET2) AHSCT. Survival was estimated using Kaplan-Meier, Cox methods, Chi-square and log-rank test. Results. Four-year overall survival and event-free survival were 70% and 54% respectively (Tables 1, 2). The presented factors had significant value in survival prediction.
In the combined analysis of PET1 and PET2 significant difference observed only in patients with positivity by PET1 and PET2 compared with group with negative PET1 and PET2 results (Tables 3, 4). Conclusion. Our work has revealed that the most significant factors of the event free survival in patients with Hodgkin lymphoma after HDC/AHSCT are: elevation of the LDH activity, В-symptoms, pretreatment, positivity by PET1 and especially lack of response by CT-scan and positivity by PET2.
Keywords
Hodgkin lymphoma, autologous stem cell transplant, PET, LDH, albumin.
Table 1. Four-year event-free survival (Kaplan-Meier analysis, log-rank test)

Table 2. Four-year overall survival (Kaplan-Meier analysis, log-rank test)

Table 3. Univariate analysis of risk factors for event-free and overall survival (Cox models, Chi-square test)

Table 4. Multivariate analysis of risk factors for event-free survival (Cox models, Chi-square test)

[TYPE] => HTML ) [~DESCRIPTION] => [~NAME] => Description / Summary [~DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) ) [NAME_EN] => Array ( [ID] => 40 [TIMESTAMP_X] => 2015-09-03 10:49:47 [IBLOCK_ID] => 2 [NAME] => Name [ACTIVE] => Y [SORT] => 500 [CODE] => NAME_EN [DEFAULT_VALUE] => [PROPERTY_TYPE] => S [ROW_COUNT] => 1 [COL_COUNT] => 80 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 40 [FILE_TYPE] => [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => Y [VERSION] => 1 [USER_TYPE] => [USER_TYPE_SETTINGS] => [HINT] => [PROPERTY_VALUE_ID] => 20626 [VALUE] => Prognostic factors in autologous stem cell transplant on adult patients with Hodgkin lymphoma [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => Prognostic factors in autologous stem cell transplant on adult patients with Hodgkin lymphoma [~DESCRIPTION] => [~NAME] => Name [~DEFAULT_VALUE] => ) [FULL_TEXT_RU] => Array ( [ID] => 42 [TIMESTAMP_X] => 2015-09-07 20:29:18 [IBLOCK_ID] => 2 [NAME] => Полный текст [ACTIVE] => Y [SORT] => 500 [CODE] => FULL_TEXT_RU [DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) [PROPERTY_TYPE] => S [ROW_COUNT] => 1 [COL_COUNT] => 30 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 42 [FILE_TYPE] => [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => HTML [USER_TYPE_SETTINGS] => Array ( [height] => 200 ) [HINT] => [PROPERTY_VALUE_ID] => [VALUE] => [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => [~DESCRIPTION] => [~NAME] => Полный текст [~DEFAULT_VALUE] => Array ( [TEXT] => [TYPE] => HTML ) ) [PDF_RU] => Array ( [ID] => 43 [TIMESTAMP_X] => 2015-09-09 16:05:20 [IBLOCK_ID] => 2 [NAME] => PDF RUS [ACTIVE] => Y [SORT] => 500 [CODE] => PDF_RU [DEFAULT_VALUE] => [PROPERTY_TYPE] => F [ROW_COUNT] => 1 [COL_COUNT] => 30 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 43 [FILE_TYPE] => doc, txt, rtf, pdf [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => [USER_TYPE_SETTINGS] => [HINT] => [PROPERTY_VALUE_ID] => 20807 [VALUE] => 1445 [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => 1445 [~DESCRIPTION] => [~NAME] => PDF RUS [~DEFAULT_VALUE] => ) [PDF_EN] => Array ( [ID] => 44 [TIMESTAMP_X] => 2015-09-09 16:05:20 [IBLOCK_ID] => 2 [NAME] => PDF ENG [ACTIVE] => Y [SORT] => 500 [CODE] => PDF_EN [DEFAULT_VALUE] => [PROPERTY_TYPE] => F [ROW_COUNT] => 1 [COL_COUNT] => 30 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 44 [FILE_TYPE] => doc, txt, rtf, pdf [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => [USER_TYPE_SETTINGS] => [HINT] => [PROPERTY_VALUE_ID] => 20808 [VALUE] => 1446 [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => 1446 [~DESCRIPTION] => [~NAME] => PDF ENG [~DEFAULT_VALUE] => ) [NAME_LONG] => Array ( [ID] => 45 [TIMESTAMP_X] => 2023-04-13 00:55:00 [IBLOCK_ID] => 2 [NAME] => Название (для очень длинных заголовков) [ACTIVE] => Y [SORT] => 500 [CODE] => NAME_LONG [DEFAULT_VALUE] => Array ( [TYPE] => HTML [TEXT] => ) [PROPERTY_TYPE] => S [ROW_COUNT] => 1 [COL_COUNT] => 30 [LIST_TYPE] => L [MULTIPLE] => N [XML_ID] => 45 [FILE_TYPE] => [MULTIPLE_CNT] => 5 [TMP_ID] => [LINK_IBLOCK_ID] => 0 [WITH_DESCRIPTION] => N [SEARCHABLE] => N [FILTRABLE] => N [IS_REQUIRED] => N [VERSION] => 1 [USER_TYPE] => HTML [USER_TYPE_SETTINGS] => Array ( [height] => 80 ) [HINT] => [PROPERTY_VALUE_ID] => [VALUE] => [DESCRIPTION] => [VALUE_ENUM] => [VALUE_XML_ID] => [VALUE_SORT] => [~VALUE] => [~DESCRIPTION] => [~NAME] => Название (для очень длинных заголовков) [~DEFAULT_VALUE] => Array ( [TYPE] => HTML [TEXT] => ) ) )
Всеволод Г. Потапенко 1,2, Наталья Б. Михайлова 1, Ирина А. Скороход 2, Дарья А. Чигинская 2, Виктория В. Рябчикова 2, Элеонора И. Подольцева 2, Виктор В. Ипатов 3, Игорь В. Байков 3, Вячеслав Н. Семелев 3, Дмитрий А. Горностаев 3, Надежда В. Медведева 2, Борис В. Афанасьев 1
2 Городской гематологический центр, Городская клиническая больница №31, Санкт-Петербург
3 Военно-медицинская Академия им. С. М. Кирова, Санкт-Петербург
Цель
Целью работы был анализ показателей общей и бессобытийной выживаемости в зависимости от различных прогностических факторов.
Пациенты и методы
Проанализированы данные 84 пациентов. Медиана возраста 26,6 года (18-62). Медиана наблюдения составила 49 месяцев (0,5-115 мес.). Исследованы влияния: пола, ответа на первичное лечение, скорости развития рецидива, варианта химиотерапии второй линии, В-симптомов, конгломератов более 5 см (в рецидиве и непосредственно перед ВДХТ), уровней альбумина и ЛДГ крови, КТ-ответа, общего количества линий химиотерапии, режима кондиционирования перед АТГСК, метаболической активности опухоли до ВДХТ (ПЭТ1) и после АТГСК (ПЭТ2). Для статистического анализа использованы методы Каплана-Мейера, Кокса, статистические критерии Манна-Уитни и Хи-квадрат. Результаты. Приведены показатели общей и бессобытийной выживаемости, а также расчет отношения рисков для факторов, показавших статистическую достоверность менее 0,05 (Табл. 1, 2). При анализе бессобытийной выживаемости выявлены статистически значимые различия в выживаемости при негативности по ПЭТ1 и ПЭТ2 по сравнению с группой пациентов с позитивностью очагов по ПЭТ1 и ПЭТ2 (Табл. 3, 4). Других различий не выявлено.
Вывод
Исследование показало, что наиболее важными факторами прогноза бессобытийной выживаемости пациентов с ЛХ после ВДХТ/АТГСК являются повышение активности ЛДГ, наличие В-симптомов в рецидиве, позитивность по ПЭТ1, предлеченность и, особенно, отсутствие ответа по данным КТ и определение метаболической активности после ВДХТ/АТГСК.
Ключевые слова
Лимфома Ходжкина, аутологичная трансплантация стволовых клеток, ПЭТ, ЛДГ, альбумин.
Таблица 1. Четырехлетняя бессобытийная выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)
| Факторы | Есть | Нет | p |
| B-симптомы в рецидиве | 35% | 61% | 0,0246 |
| Гипоальбуминемия |
33% |
62% |
0,0494 |
| Повышение активности ЛДГ | 36% | 66% | 0,0302 |
| Отсутствие ответа по данным КТ | 33% | 66% | 0,0035 |
| Позитивность по ПЭТ1 |
31% |
70% | 0,0072 |
| Позитивность по ПЭТ2 | 42% | 61% | 0,050 |
| Предлеченность (более трех линий химиотерапии) | 31% | 59% | 0,0289 |
Таблица 2. Четырехлетняя общая выживаемость (анализ Каплана-Мейера, стат. критерий лог-ранк)
| Факторы | Есть | Нет | p |
| В-симптомы в рецидиве | 45% | 80% | 0,0006 |
| Гипоальбуминемия | 46% | 74% | 0,0372 |
| Повышение активности ЛДГ | 52% |
78% |
0,0340 |
| Отсутствие ответа по данным КТ | 52% | 79% | 0,0158 |
Таблица 3. Однофакторный анализ факторов риска общей и бессобытийной выживаемости (метод Кокса, стат. критерий Хи-квадрат)
| Фактор | Отношение рисков | Доверительный интервал 95% | Р | |
| Общая выживаемость | ||||
| В-симптомы в рецидиве | 0,27 | 0,11 | 0,62 | 0,002 |
| Отсутствие ответа по данным КТ | 0,37 | 0,17 | 0,83 | 0,016 |
| ЛДГ | 0,38 | 0,15 | 0,95 | 0,037 |
| Бессобытийная выживаемость | ||||
| Отсутствие ответа по КТ | 0,36 | 0,18 | 0,68 | 0,001 |
| Позитивность по ПЭТ1 | 0,36 | 0,17 | 0,75 | 0,006 |
| В-симптомы в рецидиве | 0,47 | 0,24 | 0,92 | 0,002 |
| Предлеченность(более трех линий химиотерапии) | 0,41 | 0,21 | 0,81 | 0,01 |
| ЛДГ | 0,45 | 0,21 | 0,96 | 0,04 |
Таблица 4. Многофакторный анализ факторов риска бессобытийной выживаемости (метод Кокса, критерий Хи- квадрат)
| Фактор | Отношение рисков | Доверительный интервал 95% | p | |
| Отсутствие ответа по КТ | 0,38 | 0,16 | 0,89 | 0,026 |
| Позитивность по ПЭТ2 | 0,42 | 0,18 | 0,97 | 0,043 |
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20613
[VALUE] => Array
(
[TEXT] => Наталья Н. Попова, Михаил Ю. Дроков, Елена Н. Паровичникова, Лариса А. Кузьмина, Юлия О. Давыдова, Николай М. Капранов, Екатерина Д. Михальцова, Ольга М. Королева, Вера А. Васильева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Ирина В. Гальцева, Михаил А. Масчан, Валерий Г. Савченко
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Наталья Н. Попова, Михаил Ю. Дроков, Елена Н. Паровичникова, Лариса А. Кузьмина, Юлия О. Давыдова, Николай М. Капранов, Екатерина Д. Михальцова, Ольга М. Королева, Вера А. Васильева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Ирина В. Гальцева, Михаил А. Масчан, Валерий Г. Савченко
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20614
[VALUE] => Array
(
[TEXT] => ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => ФГБУ «НМИЦ гематологии» Минздрава РФ, г. Москва
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20615
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Т-клетки памяти представляют собой гетерогенную субпопуляцию иммунных клеток, участвующих в развитии аллоиммунных реакций после алло-ТГСК – реакции трансплантат против опухоли (РТПО) и РТПХ. В настоящее время созданы новые программы иммуносупрессивной терапии, но единого унифицированного подхода профилактики острой РТПХ не существует. Необходимость проведения иммуносупрессии, особенно при несовместимых/гаплоидентичных алло-ТГСК, когда требуется максимальная иммуноаблация, позволяет контролировать развитие/течение РТПХ. Однако необходимость своевременной реконституции иммунной системы является ключевым фактором для реализации противоопухолевого контроля. Цель работы состояла в оценке влияния различных схем профилактики острой РТПХ на восстановление субпопуляций Т-клеток памяти и их предшественников у больных острыми лейкозами после алло-ТГСК.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
В исследование включены 39 пациентов с острыми лейкозами, которым была выполнена алло-ТГСК в ФГБУ «НМИЦ гематологии» Минздрава РФ. Медиана возраста составила 36 лет (17-60 лет). Альтернативные программы профилактики острой РТПХ использовали при несовместимых/гаплоидентичных алло-ТГСК (n=17), которые включали в себя посттрансплантационный циклофосфамид (ПТ-ЦФ) на +3, +4 день или Тαβ-деплецию у молодых пациентов. В контрольную группу мы включили пациентов с классическим режимом иммуносупрессии (классическая ИСТ) с использованием циклоспорина А в сочетании с микофенолатом мофетилом и малыми дозами метотрексата, применяемых после совместимой родственной/неродственной алло-ТГСК (n=22). Характеристика больных, включенных в исследование, схемы профилактики РТПХ, частота развития острой РТПХ и рецидивов заболевания приведена в таблице 1.
</p>
<h2>Таблица 1. Характеристика пациентов</h2>
<img width="783" alt="38_таблица.png" src="/upload/medialibrary/d46/38_tablitsa.png" height="467" title="38_таблица.png"><br>
<img width="767" alt="38_рисунок 1.png" src="/upload/medialibrary/1ab/38_risunok-1.png" height="704" title="38_рисунок 1.png"><br>
<h2>Рисунок 1. Восстановление субпопуляций Т-клеток памяти у больных острыми лейкозами после алло-ТГСК</h2>
<p style="text-align: justify;">
Примечание. На графике показаны значимые отличия (p<0,005) по количеству клеток в субпопуляциях CD4+/CD8+ Т-клеток памяти при использовании альтернативных режимов профилактики оРТПХ – ПТ-ЦФ или Т-деплеции, в сравнении с классической ИСТ.
</p>
<p style="text-align: justify;">
Для исследования реконституции субпопуляций Т-клеток памяти использовали нативные образцы перифе-рической крови больных после алло-ТГСК на +30, +60, +90 день. С помощью метода многоцветной проточной цитометрии (BD FACS Canto II, Becton Dickinson, USA) были определены следующие субпопуляции Т-клеток памяти периферической крови: Т-наивные и стволовые клетки памяти (Tnv+Tscm) – CD8+/СD4+ CD45R0-CCR7+CD28+; T-клетки центральной памяти (Tcm) – CD8+/СD4+ CD45R0+CCR7+CD28+; T-клетки тран-зиторной памяти (Ttm) – CD8+/СD4+ CD45R0+CCR7-CD28+; T-клетки эффекторной памяти (Tem) – CD8+/СD4+ CD45R0+CCR7-CD28-; T- терминальные эффек-торы (Tte) – CD8+/СD4+ CD45R0-CCR7-CD28-. Для оценки различий между двумя независимыми выборками использовали U-критерий Манна-Уитни. Значениер<0,05 считали статистически значимым. Весь анализ данных проводили с использованием SPSS ver 23. (IBM, Chicago,Ill., USA).
</p>
<h2 style="text-align: justify;">
Результаты </h2>
<p style="text-align: justify;">
Данные представлены на рисунке 1. Показано, что на +30, +60, +90 день абсолютное количество CD8+ Tnv+Tscm после классической ИСТ было значимо больше, чем после использования ПТ-ЦФ или Тαβ-деплеции. На +30 день абсолютное количество CD8+ Tnv+Tscm после использования классической схемы профилактики РТПХ составило 4,22 кл/мкл (1,21-7,0кл кл/мкл), после ПТ-ЦФ – 0,38 кл/мкл (0,17-0,63 кл/мкл) (p=0,001), после Т-деплеции – 0,14 кл/мкл (0,05-0,15 кл/мкл) (р=0,03). На +60 день – 2,57 кл/мкл (1,49-4,99 кл/мкл) после классической ИСТ; 0,12 кл/мкл (0,02-0,15 кл/мкл) после Т-деплеции; 1,1 кл/мкл (0,72-2,8 кл/мкл) после ПТ-ЦФ (p=0,009). На +90 день – 4,29 кл/мкл (2,08-6,58 кл/мкл) после классического режима; 1,82 кл/мкл (0,16-3,3 кл/мкл) после ПТ-ЦФ; 0,35 кл/мкл (0,01-0,7 кл/мкл) после Т-деплеции (p=0,035). На +30, +60 день абсолютное количество CD8+ Tcm было значимо меньше после использования альтернативных подходов в сравнении с классической ИСТ – на +30 день 1,07 кл/мкл (0,27-1,75 кл/мкл) после классической ИСТ, 0,25 кл/мкл (0,12-0,68 кл/мкл) после ПТ-ЦФ (р=0,032), 0,18 кл/мкл (0,01-0,34 кл/мкл) после Т-деплеции (р=0,036); на +60 день 0,9 кл/мкл (0,65-1,68 кл/мкл), 0,42 кл/мкл (0,33-0,73 кл/мкл), 0,05 кл/мкл (0,01-0,07 кл/мкл) соответственно (р=0,02). Абсолютное количество CD4+ Tnv+Tscm на +30 день было значимо больше после применения классической схемы профилактики РТПХ – 16,1 кл/мкл (2,1-55,0 кл/мкл), в сравнении с использованием ПТ-ЦФ – 1,35 кл/мкл (0,7-5,36 кл/мкл) и Т-деплеции – 0,31 кл/мкл (0,27-0,71 кл/мкл) (р=0,05). Субпопуляция Тtm CD8+ на +60, +90 дни и CD4+ на +30 день отличалась при использовании классической ИСТ и альтернативных режимов (Рисунок 1). Мы не выявили корреляции между числом Tnv+Tscm, Tcm, Ttm, Tem, Tte и развитием оРТПХ или рецидива заболевания.
</p>
<h2 style="text-align: justify;">
Заключение </h2>
<p style="text-align: justify;">
Субпопуляция наивных и стволовых Т-клеток памяти является пулом клеток-предшественников для целого эффекторного звена Т-клеток (Ttm, Tem, Tte), реализующего аллоиммунный ответ. Значимое уменьшение пула CD4+/CD8+ Tnv+Tscm, CD8+ Tcm после использования альтернативных схем профилактики острой РТПХ может свидетельствовать о более глубокой иммуноаблации при этих режимах, используемых при несовместимых/гапло-ТГСК. За счет этого сохраняющееся низкое количество Tnv+Tscm на +60, +90 день, как клеток-предшественников для целой популяции Т-клеток памяти, может свидетельствовать об отсроченной реконституции адаптивного звена иммунного ответа при альтернативных режимах профилактики оРТПХ.
</p>
<h2 style="text-align: justify;">
Ключевые слова </h2>
<p style="text-align: justify;">
Т-клетки памяти, реконституция иммунной системы, трансплантация аллогенных гемопоэтических стволовых клеток, профилактика острой РТПХ.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Т-клетки памяти представляют собой гетерогенную субпопуляцию иммунных клеток, участвующих в развитии аллоиммунных реакций после алло-ТГСК – реакции трансплантат против опухоли (РТПО) и РТПХ. В настоящее время созданы новые программы иммуносупрессивной терапии, но единого унифицированного подхода профилактики острой РТПХ не существует. Необходимость проведения иммуносупрессии, особенно при несовместимых/гаплоидентичных алло-ТГСК, когда требуется максимальная иммуноаблация, позволяет контролировать развитие/течение РТПХ. Однако необходимость своевременной реконституции иммунной системы является ключевым фактором для реализации противоопухолевого контроля. Цель работы состояла в оценке влияния различных схем профилактики острой РТПХ на восстановление субпопуляций Т-клеток памяти и их предшественников у больных острыми лейкозами после алло-ТГСК.
Материалы и методы
В исследование включены 39 пациентов с острыми лейкозами, которым была выполнена алло-ТГСК в ФГБУ «НМИЦ гематологии» Минздрава РФ. Медиана возраста составила 36 лет (17-60 лет). Альтернативные программы профилактики острой РТПХ использовали при несовместимых/гаплоидентичных алло-ТГСК (n=17), которые включали в себя посттрансплантационный циклофосфамид (ПТ-ЦФ) на +3, +4 день или Тαβ-деплецию у молодых пациентов. В контрольную группу мы включили пациентов с классическим режимом иммуносупрессии (классическая ИСТ) с использованием циклоспорина А в сочетании с микофенолатом мофетилом и малыми дозами метотрексата, применяемых после совместимой родственной/неродственной алло-ТГСК (n=22). Характеристика больных, включенных в исследование, схемы профилактики РТПХ, частота развития острой РТПХ и рецидивов заболевания приведена в таблице 1.
Таблица 1. Характеристика пациентов


Рисунок 1. Восстановление субпопуляций Т-клеток памяти у больных острыми лейкозами после алло-ТГСК
Примечание. На графике показаны значимые отличия (p<0,005) по количеству клеток в субпопуляциях CD4+/CD8+ Т-клеток памяти при использовании альтернативных режимов профилактики оРТПХ – ПТ-ЦФ или Т-деплеции, в сравнении с классической ИСТ.
Для исследования реконституции субпопуляций Т-клеток памяти использовали нативные образцы перифе-рической крови больных после алло-ТГСК на +30, +60, +90 день. С помощью метода многоцветной проточной цитометрии (BD FACS Canto II, Becton Dickinson, USA) были определены следующие субпопуляции Т-клеток памяти периферической крови: Т-наивные и стволовые клетки памяти (Tnv+Tscm) – CD8+/СD4+ CD45R0-CCR7+CD28+; T-клетки центральной памяти (Tcm) – CD8+/СD4+ CD45R0+CCR7+CD28+; T-клетки тран-зиторной памяти (Ttm) – CD8+/СD4+ CD45R0+CCR7-CD28+; T-клетки эффекторной памяти (Tem) – CD8+/СD4+ CD45R0+CCR7-CD28-; T- терминальные эффек-торы (Tte) – CD8+/СD4+ CD45R0-CCR7-CD28-. Для оценки различий между двумя независимыми выборками использовали U-критерий Манна-Уитни. Значениер<0,05 считали статистически значимым. Весь анализ данных проводили с использованием SPSS ver 23. (IBM, Chicago,Ill., USA).
Результаты
Данные представлены на рисунке 1. Показано, что на +30, +60, +90 день абсолютное количество CD8+ Tnv+Tscm после классической ИСТ было значимо больше, чем после использования ПТ-ЦФ или Тαβ-деплеции. На +30 день абсолютное количество CD8+ Tnv+Tscm после использования классической схемы профилактики РТПХ составило 4,22 кл/мкл (1,21-7,0кл кл/мкл), после ПТ-ЦФ – 0,38 кл/мкл (0,17-0,63 кл/мкл) (p=0,001), после Т-деплеции – 0,14 кл/мкл (0,05-0,15 кл/мкл) (р=0,03). На +60 день – 2,57 кл/мкл (1,49-4,99 кл/мкл) после классической ИСТ; 0,12 кл/мкл (0,02-0,15 кл/мкл) после Т-деплеции; 1,1 кл/мкл (0,72-2,8 кл/мкл) после ПТ-ЦФ (p=0,009). На +90 день – 4,29 кл/мкл (2,08-6,58 кл/мкл) после классического режима; 1,82 кл/мкл (0,16-3,3 кл/мкл) после ПТ-ЦФ; 0,35 кл/мкл (0,01-0,7 кл/мкл) после Т-деплеции (p=0,035). На +30, +60 день абсолютное количество CD8+ Tcm было значимо меньше после использования альтернативных подходов в сравнении с классической ИСТ – на +30 день 1,07 кл/мкл (0,27-1,75 кл/мкл) после классической ИСТ, 0,25 кл/мкл (0,12-0,68 кл/мкл) после ПТ-ЦФ (р=0,032), 0,18 кл/мкл (0,01-0,34 кл/мкл) после Т-деплеции (р=0,036); на +60 день 0,9 кл/мкл (0,65-1,68 кл/мкл), 0,42 кл/мкл (0,33-0,73 кл/мкл), 0,05 кл/мкл (0,01-0,07 кл/мкл) соответственно (р=0,02). Абсолютное количество CD4+ Tnv+Tscm на +30 день было значимо больше после применения классической схемы профилактики РТПХ – 16,1 кл/мкл (2,1-55,0 кл/мкл), в сравнении с использованием ПТ-ЦФ – 1,35 кл/мкл (0,7-5,36 кл/мкл) и Т-деплеции – 0,31 кл/мкл (0,27-0,71 кл/мкл) (р=0,05). Субпопуляция Тtm CD8+ на +60, +90 дни и CD4+ на +30 день отличалась при использовании классической ИСТ и альтернативных режимов (Рисунок 1). Мы не выявили корреляции между числом Tnv+Tscm, Tcm, Ttm, Tem, Tte и развитием оРТПХ или рецидива заболевания.
Заключение
Субпопуляция наивных и стволовых Т-клеток памяти является пулом клеток-предшественников для целого эффекторного звена Т-клеток (Ttm, Tem, Tte), реализующего аллоиммунный ответ. Значимое уменьшение пула CD4+/CD8+ Tnv+Tscm, CD8+ Tcm после использования альтернативных схем профилактики острой РТПХ может свидетельствовать о более глубокой иммуноаблации при этих режимах, используемых при несовместимых/гапло-ТГСК. За счет этого сохраняющееся низкое количество Tnv+Tscm на +60, +90 день, как клеток-предшественников для целой популяции Т-клеток памяти, может свидетельствовать об отсроченной реконституции адаптивного звена иммунного ответа при альтернативных режимах профилактики оРТПХ.
Ключевые слова
Т-клетки памяти, реконституция иммунной системы, трансплантация аллогенных гемопоэтических стволовых клеток, профилактика острой РТПХ.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20616
[VALUE] => Array
(
[TEXT] => Natalia N. Popova, Mikhail Y. Drokov, Elena N. Parovichnikova, Larisa A. Kuzmina, Julia O. Davydova, Nikolay М. Kapranov, Ekaterina D. Mikhaltsova, Olga M. Koroleva, Vera A. Vasilyeva, Darya S. Dubnyak, Zoya V. Konova, Anna A. Sidorova, Ekaterina V. Usikova, Anna A. Dmitrova, Irina V. Galtseva, Michael A. Maschan, Valery G. Savchenko
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Natalia N. Popova, Mikhail Y. Drokov, Elena N. Parovichnikova, Larisa A. Kuzmina, Julia O. Davydova, Nikolay М. Kapranov, Ekaterina D. Mikhaltsova, Olga M. Koroleva, Vera A. Vasilyeva, Darya S. Dubnyak, Zoya V. Konova, Anna A. Sidorova, Ekaterina V. Usikova, Anna A. Dmitrova, Irina V. Galtseva, Michael A. Maschan, Valery G. Savchenko
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20617
[VALUE] => Array
(
[TEXT] => National Research Center for Hematology, Moscow, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => National Research Center for Hematology, Moscow, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20618
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
T-memory cells form the heterogeneous pool of immune cells responsible for alloreactivity after allogeneic stem cells transplantation (allo-HSCT). Nowadays there are new different approaches for aGVHD prophylaxis, but the unified immunosuppressive regimen has not been defined yet. Obviously the immunosuppressive therapy as aGVHD prophylaxis is essential to control aGVHD especially in terms of mismatched or haplo-HSCT when strong immunoablation is required. But timely immune reconstitution is crucial for antitumor immunity. Aim of the present study was to evaluate an impact of different immunosuppressive regimens of aGVHD prophylaxis on T-memory cell subsets recovery in leukemia patients after allo-HSCT.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
The study comprised 39 leukemia patients with a median age of 36 years old (17-60 y.o.) who underwent allo-HSCT in National Research Center for Hematology, Russia. Alternative immunosuppressive regimens of aGVHD prophylaxis in case of mismatched or haplo-HSCT (n=17) include Posttransplant high dose Cyclophosphamide (PT-Cy) on day +3, +4 or alfa/beta T-cells depletion in young patients. Classical immunosuppressive regimen with CsA+MMF+MTX was applied in case of matched related and matched unrelated donors and form the control group (n=22). The characteristics of patients, immunosuppressive regimens, aGVHD and relapses after allo-HSCT are presented in the table 1. Samples of peripheral blood were collected on day +30, +60 and +90 after allo-HSCT in EDTA-tubes. Flow cytometry analysis was performed on BD FACS Canto II (Becton Dickinson, USA) to define T-memory subsets: T-naive and T-stem cell memory (Tnv+Tscm) – CD8+/CD4+ CD45R0-CCR7+CD28+; T-central memory (Tcm) – CD8+/CD4+ CD45R0+CCR7+CD28+; T-transitional memory (Ttm) – CD8+/CD4+CD45R0+CCR7-CD28+; T-effector memory (Tem) – CD8+/CD4+ CD45R0+CCR7-CD28-; T-terminal effector (Tte) – CD8+/CD4+ CD45R0-CCR7-CD28-. Mann-Whitney U test was used for nonparametric data analysis. A p-value less than 0.05 was considered as significant. All data analysis was conducted utilizing SPSS ver. 23. (IBM, Chicago, Ill., USA).
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
The data are presented in the Fig. 1. According to our data, absolute number of CD8+ Tnv+Tscm after classic immunosuppressive regimen was significantly higher than after PTCy prophylaxis, or T-cells depletion on days +30, +60, +90. Absolute number of CD8+ Tnv+Tscm after classic immunosuppressive regimen on day +30 was 4.22 cells/μL (1.21-7.0 cells/μL), after PT-Cy – 0.38 cells/μL (0.17-0.63 cells/μL) (p=0.001), after Т-cell depletion – 0.14 cells/μL (0.05-0.15 cells/μL) (р=0.03). Appropriate levels by the day +60 were 2.57 cells/μL (1.49-4.99 cells/μL) after classic immunosuppressive regimen; 0.12 cells/μL (0.02-0.15 cells/μL), after Т-cell depletion; 1.1 cells/μL (0.72-2.8 cells/μL) after PT-Cy (p=0.009). On the day +90 these parameters were 4.29 cells/ μL (2.08-6.58 cells/μL) after classic immunosuppressive regimen; 1.82 cells/μL (0.16-3.3 cells/μL) after PT-Cy; and 0.35 cells/μL (0.01-0.7 cells/μL) after Т-cell depletion (p=0.035). On day +30 and +60, absolute numbers of CD8+ Tcm were significant lower after alternative approaches, when compared to classical immunosuppressive regimen, i.e., on day +30, 1.07 cells/μL (0.27-1.75 cells/μL) after classical regimen; 0.25 cells/μL (0.12-0.68 cells/μL) after PT-Cy (р=0.032); 0.18 cells/μL (0.01-0.34 cells/μL) after Т-cells depletion (р=0.036); on day +60, 0.9 cells/μL (0.65-1.68 cells/μL); 0.42 cells/μL (0.33-0.73 cells/μL); 0.05 cells/μL (0.01-0.07 cells/μL), respectively (р=0.02). Absolute number of CD4+ Tnv+Tscm on day +30 was significantly higher after classic immunosuppressiveregimen, i.e. 16.1 cells/μL (2.1-55.0 cells/μL), as compared to PT-Cy – 1.35 cells/μL (0.7-5.36 cells/μL), and Т cell depletion – 0.31 cells/μL (0.27-0.71 cells/μL) (р=0.05). Absolute number of Тtm CD8+ on days +60, +90 and CD4+ on day +30 were different in alternative aGVHD prophylaxis and in control group (Fig. 1). We didn’t find any correlations between absolute numbers of Tnv+Tscm, Tcm, Ttm, Tem, Tte and aGVHD onset, or leukemia relapse after allo-HSCT.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Tnv+Tscm is the progenitor subset for all memory and effector T-cells and its prompt recovery after allo-HSCT seems to be crucial for graft-versus-leukemia effect. Here we show the lowest number of CD4+/CD8+ Tnv+Tscm, CD8+ Tcm after alternative approaches of aGVHD prophylaxis that might reflect sever immunoablation in mismatched or haplo-HSCT. To this point, low numbers of Tnv+Tscm on day +60, +90 as progenitor cells for the whole T-memory pool may lead to delayed reconstitution of adaptive immunity after alternative aGVHD prophylaxis in patients after allo-HSCT.
</p>
<h2 style="text-align: justify;">Disclosures</h2>
<p style="text-align: justify;">
No relevant conflicts of interest to declare.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Memory T cells, immune reconstitution, allogeneic stem cell transplantation, GVHD prophylaxis regimens.
</p>
<h2>Table 1. Characteristics of the patients</h2>
<img width="781" alt="38_table 1.png" src="/upload/medialibrary/c6c/38_table-1.png" height="571" title="38_table 1.png"><br>
<img width="771" alt="38_figure1.png" src="/upload/medialibrary/269/38_figure1.png" height="783" title="38_figure1.png">
<h2>Figure 1. Recovery of T-memory cell subsets in terms of different GVHD prophylaxis in leukemia patients after allo-HSCT</h2>
<p style="text-align: justify;">
Significant differences (p<0.005) between the number of different T-memory cell subsets in terms of alternative GVHD prophylaxis – PT-Cy or T-cells depletion comparing to classic immunosuppressive regimen are presented in the graph.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
T-memory cells form the heterogeneous pool of immune cells responsible for alloreactivity after allogeneic stem cells transplantation (allo-HSCT). Nowadays there are new different approaches for aGVHD prophylaxis, but the unified immunosuppressive regimen has not been defined yet. Obviously the immunosuppressive therapy as aGVHD prophylaxis is essential to control aGVHD especially in terms of mismatched or haplo-HSCT when strong immunoablation is required. But timely immune reconstitution is crucial for antitumor immunity. Aim of the present study was to evaluate an impact of different immunosuppressive regimens of aGVHD prophylaxis on T-memory cell subsets recovery in leukemia patients after allo-HSCT.
Patients and methods
The study comprised 39 leukemia patients with a median age of 36 years old (17-60 y.o.) who underwent allo-HSCT in National Research Center for Hematology, Russia. Alternative immunosuppressive regimens of aGVHD prophylaxis in case of mismatched or haplo-HSCT (n=17) include Posttransplant high dose Cyclophosphamide (PT-Cy) on day +3, +4 or alfa/beta T-cells depletion in young patients. Classical immunosuppressive regimen with CsA+MMF+MTX was applied in case of matched related and matched unrelated donors and form the control group (n=22). The characteristics of patients, immunosuppressive regimens, aGVHD and relapses after allo-HSCT are presented in the table 1. Samples of peripheral blood were collected on day +30, +60 and +90 after allo-HSCT in EDTA-tubes. Flow cytometry analysis was performed on BD FACS Canto II (Becton Dickinson, USA) to define T-memory subsets: T-naive and T-stem cell memory (Tnv+Tscm) – CD8+/CD4+ CD45R0-CCR7+CD28+; T-central memory (Tcm) – CD8+/CD4+ CD45R0+CCR7+CD28+; T-transitional memory (Ttm) – CD8+/CD4+CD45R0+CCR7-CD28+; T-effector memory (Tem) – CD8+/CD4+ CD45R0+CCR7-CD28-; T-terminal effector (Tte) – CD8+/CD4+ CD45R0-CCR7-CD28-. Mann-Whitney U test was used for nonparametric data analysis. A p-value less than 0.05 was considered as significant. All data analysis was conducted utilizing SPSS ver. 23. (IBM, Chicago, Ill., USA).
Results
The data are presented in the Fig. 1. According to our data, absolute number of CD8+ Tnv+Tscm after classic immunosuppressive regimen was significantly higher than after PTCy prophylaxis, or T-cells depletion on days +30, +60, +90. Absolute number of CD8+ Tnv+Tscm after classic immunosuppressive regimen on day +30 was 4.22 cells/μL (1.21-7.0 cells/μL), after PT-Cy – 0.38 cells/μL (0.17-0.63 cells/μL) (p=0.001), after Т-cell depletion – 0.14 cells/μL (0.05-0.15 cells/μL) (р=0.03). Appropriate levels by the day +60 were 2.57 cells/μL (1.49-4.99 cells/μL) after classic immunosuppressive regimen; 0.12 cells/μL (0.02-0.15 cells/μL), after Т-cell depletion; 1.1 cells/μL (0.72-2.8 cells/μL) after PT-Cy (p=0.009). On the day +90 these parameters were 4.29 cells/ μL (2.08-6.58 cells/μL) after classic immunosuppressive regimen; 1.82 cells/μL (0.16-3.3 cells/μL) after PT-Cy; and 0.35 cells/μL (0.01-0.7 cells/μL) after Т-cell depletion (p=0.035). On day +30 and +60, absolute numbers of CD8+ Tcm were significant lower after alternative approaches, when compared to classical immunosuppressive regimen, i.e., on day +30, 1.07 cells/μL (0.27-1.75 cells/μL) after classical regimen; 0.25 cells/μL (0.12-0.68 cells/μL) after PT-Cy (р=0.032); 0.18 cells/μL (0.01-0.34 cells/μL) after Т-cells depletion (р=0.036); on day +60, 0.9 cells/μL (0.65-1.68 cells/μL); 0.42 cells/μL (0.33-0.73 cells/μL); 0.05 cells/μL (0.01-0.07 cells/μL), respectively (р=0.02). Absolute number of CD4+ Tnv+Tscm on day +30 was significantly higher after classic immunosuppressiveregimen, i.e. 16.1 cells/μL (2.1-55.0 cells/μL), as compared to PT-Cy – 1.35 cells/μL (0.7-5.36 cells/μL), and Т cell depletion – 0.31 cells/μL (0.27-0.71 cells/μL) (р=0.05). Absolute number of Тtm CD8+ on days +60, +90 and CD4+ on day +30 were different in alternative aGVHD prophylaxis and in control group (Fig. 1). We didn’t find any correlations between absolute numbers of Tnv+Tscm, Tcm, Ttm, Tem, Tte and aGVHD onset, or leukemia relapse after allo-HSCT.
Conclusion
Tnv+Tscm is the progenitor subset for all memory and effector T-cells and its prompt recovery after allo-HSCT seems to be crucial for graft-versus-leukemia effect. Here we show the lowest number of CD4+/CD8+ Tnv+Tscm, CD8+ Tcm after alternative approaches of aGVHD prophylaxis that might reflect sever immunoablation in mismatched or haplo-HSCT. To this point, low numbers of Tnv+Tscm on day +60, +90 as progenitor cells for the whole T-memory pool may lead to delayed reconstitution of adaptive immunity after alternative aGVHD prophylaxis in patients after allo-HSCT.
Disclosures
No relevant conflicts of interest to declare.
Keywords
Memory T cells, immune reconstitution, allogeneic stem cell transplantation, GVHD prophylaxis regimens.
Table 1. Characteristics of the patients


Figure 1. Recovery of T-memory cell subsets in terms of different GVHD prophylaxis in leukemia patients after allo-HSCT
Significant differences (p<0.005) between the number of different T-memory cell subsets in terms of alternative GVHD prophylaxis – PT-Cy or T-cells depletion comparing to classic immunosuppressive regimen are presented in the graph.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20619
[VALUE] => Recovery of memory T cells after alternative prophylaxis regimens of acute graft-versus-host disease (aGVHD) in leukemia patients after allogeneic stem cells transplantation
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Recovery of memory T cells after alternative prophylaxis regimens of acute graft-versus-host disease (aGVHD) in leukemia patients after allogeneic stem cells transplantation
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20805
[VALUE] => 1443
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1443
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20806
[VALUE] => 1444
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1444
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Наталья Н. Попова, Михаил Ю. Дроков, Елена Н. Паровичникова, Лариса А. Кузьмина, Юлия О. Давыдова, Николай М. Капранов, Екатерина Д. Михальцова, Ольга М. Королева, Вера А. Васильева, Дарья С. Дубняк, Анна А. Сидорова, Екатерина В. Усикова, Зоя В. Конова, Анна А. Дмитрова, Ирина В. Гальцева, Михаил А. Масчан, Валерий Г. Савченко
Введение
Т-клетки памяти представляют собой гетерогенную субпопуляцию иммунных клеток, участвующих в развитии аллоиммунных реакций после алло-ТГСК – реакции трансплантат против опухоли (РТПО) и РТПХ. В настоящее время созданы новые программы иммуносупрессивной терапии, но единого унифицированного подхода профилактики острой РТПХ не существует. Необходимость проведения иммуносупрессии, особенно при несовместимых/гаплоидентичных алло-ТГСК, когда требуется максимальная иммуноаблация, позволяет контролировать развитие/течение РТПХ. Однако необходимость своевременной реконституции иммунной системы является ключевым фактором для реализации противоопухолевого контроля. Цель работы состояла в оценке влияния различных схем профилактики острой РТПХ на восстановление субпопуляций Т-клеток памяти и их предшественников у больных острыми лейкозами после алло-ТГСК.
Материалы и методы
В исследование включены 39 пациентов с острыми лейкозами, которым была выполнена алло-ТГСК в ФГБУ «НМИЦ гематологии» Минздрава РФ. Медиана возраста составила 36 лет (17-60 лет). Альтернативные программы профилактики острой РТПХ использовали при несовместимых/гаплоидентичных алло-ТГСК (n=17), которые включали в себя посттрансплантационный циклофосфамид (ПТ-ЦФ) на +3, +4 день или Тαβ-деплецию у молодых пациентов. В контрольную группу мы включили пациентов с классическим режимом иммуносупрессии (классическая ИСТ) с использованием циклоспорина А в сочетании с микофенолатом мофетилом и малыми дозами метотрексата, применяемых после совместимой родственной/неродственной алло-ТГСК (n=22). Характеристика больных, включенных в исследование, схемы профилактики РТПХ, частота развития острой РТПХ и рецидивов заболевания приведена в таблице 1.
Таблица 1. Характеристика пациентов


Рисунок 1. Восстановление субпопуляций Т-клеток памяти у больных острыми лейкозами после алло-ТГСК
Примечание. На графике показаны значимые отличия (p<0,005) по количеству клеток в субпопуляциях CD4+/CD8+ Т-клеток памяти при использовании альтернативных режимов профилактики оРТПХ – ПТ-ЦФ или Т-деплеции, в сравнении с классической ИСТ.
Для исследования реконституции субпопуляций Т-клеток памяти использовали нативные образцы перифе-рической крови больных после алло-ТГСК на +30, +60, +90 день. С помощью метода многоцветной проточной цитометрии (BD FACS Canto II, Becton Dickinson, USA) были определены следующие субпопуляции Т-клеток памяти периферической крови: Т-наивные и стволовые клетки памяти (Tnv+Tscm) – CD8+/СD4+ CD45R0-CCR7+CD28+; T-клетки центральной памяти (Tcm) – CD8+/СD4+ CD45R0+CCR7+CD28+; T-клетки тран-зиторной памяти (Ttm) – CD8+/СD4+ CD45R0+CCR7-CD28+; T-клетки эффекторной памяти (Tem) – CD8+/СD4+ CD45R0+CCR7-CD28-; T- терминальные эффек-торы (Tte) – CD8+/СD4+ CD45R0-CCR7-CD28-. Для оценки различий между двумя независимыми выборками использовали U-критерий Манна-Уитни. Значениер<0,05 считали статистически значимым. Весь анализ данных проводили с использованием SPSS ver 23. (IBM, Chicago,Ill., USA).
Результаты
Данные представлены на рисунке 1. Показано, что на +30, +60, +90 день абсолютное количество CD8+ Tnv+Tscm после классической ИСТ было значимо больше, чем после использования ПТ-ЦФ или Тαβ-деплеции. На +30 день абсолютное количество CD8+ Tnv+Tscm после использования классической схемы профилактики РТПХ составило 4,22 кл/мкл (1,21-7,0кл кл/мкл), после ПТ-ЦФ – 0,38 кл/мкл (0,17-0,63 кл/мкл) (p=0,001), после Т-деплеции – 0,14 кл/мкл (0,05-0,15 кл/мкл) (р=0,03). На +60 день – 2,57 кл/мкл (1,49-4,99 кл/мкл) после классической ИСТ; 0,12 кл/мкл (0,02-0,15 кл/мкл) после Т-деплеции; 1,1 кл/мкл (0,72-2,8 кл/мкл) после ПТ-ЦФ (p=0,009). На +90 день – 4,29 кл/мкл (2,08-6,58 кл/мкл) после классического режима; 1,82 кл/мкл (0,16-3,3 кл/мкл) после ПТ-ЦФ; 0,35 кл/мкл (0,01-0,7 кл/мкл) после Т-деплеции (p=0,035). На +30, +60 день абсолютное количество CD8+ Tcm было значимо меньше после использования альтернативных подходов в сравнении с классической ИСТ – на +30 день 1,07 кл/мкл (0,27-1,75 кл/мкл) после классической ИСТ, 0,25 кл/мкл (0,12-0,68 кл/мкл) после ПТ-ЦФ (р=0,032), 0,18 кл/мкл (0,01-0,34 кл/мкл) после Т-деплеции (р=0,036); на +60 день 0,9 кл/мкл (0,65-1,68 кл/мкл), 0,42 кл/мкл (0,33-0,73 кл/мкл), 0,05 кл/мкл (0,01-0,07 кл/мкл) соответственно (р=0,02). Абсолютное количество CD4+ Tnv+Tscm на +30 день было значимо больше после применения классической схемы профилактики РТПХ – 16,1 кл/мкл (2,1-55,0 кл/мкл), в сравнении с использованием ПТ-ЦФ – 1,35 кл/мкл (0,7-5,36 кл/мкл) и Т-деплеции – 0,31 кл/мкл (0,27-0,71 кл/мкл) (р=0,05). Субпопуляция Тtm CD8+ на +60, +90 дни и CD4+ на +30 день отличалась при использовании классической ИСТ и альтернативных режимов (Рисунок 1). Мы не выявили корреляции между числом Tnv+Tscm, Tcm, Ttm, Tem, Tte и развитием оРТПХ или рецидива заболевания.
Заключение
Субпопуляция наивных и стволовых Т-клеток памяти является пулом клеток-предшественников для целого эффекторного звена Т-клеток (Ttm, Tem, Tte), реализующего аллоиммунный ответ. Значимое уменьшение пула CD4+/CD8+ Tnv+Tscm, CD8+ Tcm после использования альтернативных схем профилактики острой РТПХ может свидетельствовать о более глубокой иммуноаблации при этих режимах, используемых при несовместимых/гапло-ТГСК. За счет этого сохраняющееся низкое количество Tnv+Tscm на +60, +90 день, как клеток-предшественников для целой популяции Т-клеток памяти, может свидетельствовать об отсроченной реконституции адаптивного звена иммунного ответа при альтернативных режимах профилактики оРТПХ.
Ключевые слова
Т-клетки памяти, реконституция иммунной системы, трансплантация аллогенных гемопоэтических стволовых клеток, профилактика острой РТПХ.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20606
[VALUE] => Array
(
[TEXT] => Юлия В. Опарина <sup>1</sup>, Екатерина В. Гончарова <sup>1</sup>,<sup>2</sup>, Ольга А. Иванова <sup>1</sup>, Максим П. Богомольный <sup>1</sup>, Людмила С. Зубаровская <sup>1</sup>, Борис В. Афанасьев <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Юлия В. Опарина 1, Екатерина В. Гончарова 1,2, Ольга А. Иванова 1, Максим П. Богомольный 1, Людмила С. Зубаровская 1, Борис В. Афанасьев 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20607
[VALUE] => Array
(
[TEXT] => <sup>1</sup> Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург<br>
<sup>2</sup> Лаборатория клинической фармакологии и терапии боли отдела нейрофармакологии Института фармакологии им. А. В. Вальдмана, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Россия<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 Научно-исследовательский институт детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург
2 Лаборатория клинической фармакологии и терапии боли отдела нейрофармакологии Института фармакологии им. А. В. Вальдмана, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20608
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Дневники и опросники, заполняемые пациентами или сопровождающими их лицами, могут служить эффективным методом наблюдения за динамикой состояния амбулаторных и стационарных пациентов. При оценке интенсивности боли предпочтительным является сбор данных в режиме реального времени, нежели опрос о событиях за прошедшие сутки, т.к. на последний вид сбора данных может влиять множество факторов (например,стабильность интенсивности боли, изменения эмоциональной окраски и порядка событий при восстановлении их по памяти). Но на практике медперсонал нередко сталкивается с пробелами в заполнении дневников, что связано с различными причинами. Поэтому, в своем исследовании мы решили оценить комплаентность родителей в ведении дневников интенсивности боли у госпитализированных пациентов детского возраста.
</p>
<h2 style="text-align: justify;">Пациенты и методы</h2>
<p style="text-align: justify;">
64 пациентам (от 2,4 до 17 лет включительно), получающим анальгетики, и их родителям вместе с карточками с изображением шкалы лиц Вонга-Бэйкера и визуальной аналоговой шкалы, были выданы для заполнения бумажные дневники оценки интенсивности базовой и прорывной болей каждые 6 часов на протяжении всего периода потребности в анальгезии. Среднее время наблюдения составило около 8 суток.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Общая комплаентность составила 72%. Степень заполнения дневников позволила разделить всех пациентов на 4 группы. В группу 0-25% заполнения вошло 25 пациентов, средний возраст которых составил 7,5 лет. У 9 пациентов было внесено 26-50% данных, а средний возраст детей составил 9,5 лет (медиана 7). 51-75% результатов было получено от родителей 6 детей среднего возраста 9 лет (медиана 10). В группу 76-100% вошли дневники 33 детей среднего возраста 10 лет (медиана 9).
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
Полученные результаты могут свидетельствовать о том, что возраст пациентов может ассоциироваться с комплаентностью родителей в ведении дневников интенсивности боли. Возможно, это связанно с коммуникативными способностями детей разных возрастов. Для подтверждения этого предположения требуются дальнейшие исследования.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Оценка интенсивности боли, дневник наблюдения, педиатрия, аналгезия.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Дневники и опросники, заполняемые пациентами или сопровождающими их лицами, могут служить эффективным методом наблюдения за динамикой состояния амбулаторных и стационарных пациентов. При оценке интенсивности боли предпочтительным является сбор данных в режиме реального времени, нежели опрос о событиях за прошедшие сутки, т.к. на последний вид сбора данных может влиять множество факторов (например,стабильность интенсивности боли, изменения эмоциональной окраски и порядка событий при восстановлении их по памяти). Но на практике медперсонал нередко сталкивается с пробелами в заполнении дневников, что связано с различными причинами. Поэтому, в своем исследовании мы решили оценить комплаентность родителей в ведении дневников интенсивности боли у госпитализированных пациентов детского возраста.
Пациенты и методы
64 пациентам (от 2,4 до 17 лет включительно), получающим анальгетики, и их родителям вместе с карточками с изображением шкалы лиц Вонга-Бэйкера и визуальной аналоговой шкалы, были выданы для заполнения бумажные дневники оценки интенсивности базовой и прорывной болей каждые 6 часов на протяжении всего периода потребности в анальгезии. Среднее время наблюдения составило около 8 суток.
Результаты
Общая комплаентность составила 72%. Степень заполнения дневников позволила разделить всех пациентов на 4 группы. В группу 0-25% заполнения вошло 25 пациентов, средний возраст которых составил 7,5 лет. У 9 пациентов было внесено 26-50% данных, а средний возраст детей составил 9,5 лет (медиана 7). 51-75% результатов было получено от родителей 6 детей среднего возраста 9 лет (медиана 10). В группу 76-100% вошли дневники 33 детей среднего возраста 10 лет (медиана 9).
Выводы
Полученные результаты могут свидетельствовать о том, что возраст пациентов может ассоциироваться с комплаентностью родителей в ведении дневников интенсивности боли. Возможно, это связанно с коммуникативными способностями детей разных возрастов. Для подтверждения этого предположения требуются дальнейшие исследования.
Ключевые слова
Оценка интенсивности боли, дневник наблюдения, педиатрия, аналгезия.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20609
[VALUE] => Array
(
[TEXT] => Julia V. Oparina <sup>1</sup>, Ekaterina V. Goncharova <sup>1</sup>,<sup>2</sup>, Olga A. Ivanova <sup>1</sup>, Maxim P. Bogomolny <sup>1</sup>, Ludmila S. Zubarovskaya <sup>1</sup>, Boris V. Afanasyev <sup>1</sup>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Julia V. Oparina 1, Ekaterina V. Goncharova 1,2, Olga A. Ivanova 1, Maxim P. Bogomolny 1, Ludmila S. Zubarovskaya 1, Boris V. Afanasyev 1
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20610
[VALUE] => Array
(
[TEXT] => <sup>1</sup> R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, I. P. Pavlov First Saint-Petersburg State Medical University, St. Petersburg, 197022, Russia<br>
<sup>2</sup> Department of Neuropharmacology, Valdman Institute of Pharmacology I. P. Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => 1 R. M. Gorbacheva Memorial Institute of Children Oncology, Hematology and Transplantation, I. P. Pavlov First Saint-Petersburg State Medical University, St. Petersburg, 197022, Russia
2 Department of Neuropharmacology, Valdman Institute of Pharmacology I. P. Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20611
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Self-filled diaries kept by a patient or caregiver are an effective method for clinical dynamics evaluation in both outpatient and inpatient settings. The real-time data collection is better for pain intensity monitoring than retrospective data analysis for each 24-hour period as the latter is biased by a number of factors such as variability in pain intensity or change in pain’s emotional perception when filling the questionnaire from memory. Due to this range of problems associated with the latter, we conducted a study aimed at diary keeping compliance in pediatric inpatients.
</p>
<h2 style="text-align: justify;">Patients and methods</h2>
<p style="text-align: justify;">
A total of 64 pediatric patients aged 2.4 to 17 years supervised by pain management team were given cards with Wong-Baker face scale and visual analogue scale with additional diaries for baseline and breakthrough pain assessment. These diaries were filled in each 6 hours during the all analgesia period. The median follow-up period was 8 days.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
Overall compliance rate was 72%. All the patients were divided into 4 groups according to diary-filling compliance degree. The 0-25% group consisted of 25 patients with median age of 7.5 years, the 26-50% group of 9 patients had median age of 7 years; the 51-75% group contained 6 children with median age of 10 years, and the group of 76-100% consisted of 33 children with median age of 9 years.
</p>
<h2 style="text-align: justify;">Conclusions</h2>
<p style="text-align: justify;">
The results obtained may indicate that an influence of patients’ age on his/her caregivers pain diary keeping compliance. This may be due to communicative abilities for children of different age. For more precise conclusions an additional research is required.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Pain intensity assessment, pain diary, pediatrics, analgesia.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Self-filled diaries kept by a patient or caregiver are an effective method for clinical dynamics evaluation in both outpatient and inpatient settings. The real-time data collection is better for pain intensity monitoring than retrospective data analysis for each 24-hour period as the latter is biased by a number of factors such as variability in pain intensity or change in pain’s emotional perception when filling the questionnaire from memory. Due to this range of problems associated with the latter, we conducted a study aimed at diary keeping compliance in pediatric inpatients.
Patients and methods
A total of 64 pediatric patients aged 2.4 to 17 years supervised by pain management team were given cards with Wong-Baker face scale and visual analogue scale with additional diaries for baseline and breakthrough pain assessment. These diaries were filled in each 6 hours during the all analgesia period. The median follow-up period was 8 days.
Results
Overall compliance rate was 72%. All the patients were divided into 4 groups according to diary-filling compliance degree. The 0-25% group consisted of 25 patients with median age of 7.5 years, the 26-50% group of 9 patients had median age of 7 years; the 51-75% group contained 6 children with median age of 10 years, and the group of 76-100% consisted of 33 children with median age of 9 years.
Conclusions
The results obtained may indicate that an influence of patients’ age on his/her caregivers pain diary keeping compliance. This may be due to communicative abilities for children of different age. For more precise conclusions an additional research is required.
Keywords
Pain intensity assessment, pain diary, pediatrics, analgesia.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20612
[VALUE] => Compliance evaluation in the parents of inpatients by keeping the pain intensity diaries
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Compliance evaluation in the parents of inpatients by keeping the pain intensity diaries
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20803
[VALUE] => 1441
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1441
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20804
[VALUE] => 1442
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1442
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Юлия В. Опарина 1, Екатерина В. Гончарова 1,2, Ольга А. Иванова 1, Максим П. Богомольный 1, Людмила С. Зубаровская 1, Борис В. Афанасьев 1
2 Лаборатория клинической фармакологии и терапии боли отдела нейрофармакологии Института фармакологии им. А. В. Вальдмана, ПСПбГМУ им. акад. И. П. Павлова, Санкт-Петербург, Россия
Введение
Дневники и опросники, заполняемые пациентами или сопровождающими их лицами, могут служить эффективным методом наблюдения за динамикой состояния амбулаторных и стационарных пациентов. При оценке интенсивности боли предпочтительным является сбор данных в режиме реального времени, нежели опрос о событиях за прошедшие сутки, т.к. на последний вид сбора данных может влиять множество факторов (например,стабильность интенсивности боли, изменения эмоциональной окраски и порядка событий при восстановлении их по памяти). Но на практике медперсонал нередко сталкивается с пробелами в заполнении дневников, что связано с различными причинами. Поэтому, в своем исследовании мы решили оценить комплаентность родителей в ведении дневников интенсивности боли у госпитализированных пациентов детского возраста.
Пациенты и методы
64 пациентам (от 2,4 до 17 лет включительно), получающим анальгетики, и их родителям вместе с карточками с изображением шкалы лиц Вонга-Бэйкера и визуальной аналоговой шкалы, были выданы для заполнения бумажные дневники оценки интенсивности базовой и прорывной болей каждые 6 часов на протяжении всего периода потребности в анальгезии. Среднее время наблюдения составило около 8 суток.
Результаты
Общая комплаентность составила 72%. Степень заполнения дневников позволила разделить всех пациентов на 4 группы. В группу 0-25% заполнения вошло 25 пациентов, средний возраст которых составил 7,5 лет. У 9 пациентов было внесено 26-50% данных, а средний возраст детей составил 9,5 лет (медиана 7). 51-75% результатов было получено от родителей 6 детей среднего возраста 9 лет (медиана 10). В группу 76-100% вошли дневники 33 детей среднего возраста 10 лет (медиана 9).
Выводы
Полученные результаты могут свидетельствовать о том, что возраст пациентов может ассоциироваться с комплаентностью родителей в ведении дневников интенсивности боли. Возможно, это связанно с коммуникативными способностями детей разных возрастов. Для подтверждения этого предположения требуются дальнейшие исследования.
Ключевые слова
Оценка интенсивности боли, дневник наблюдения, педиатрия, аналгезия.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20599
[VALUE] => Array
(
[TEXT] => Светлана И. Олешко, Алиса Г. Волкова, Людмила С. Зубаровская, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Светлана И. Олешко, Алиса Г. Волкова, Людмила С. Зубаровская, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20600
[VALUE] => Array
(
[TEXT] => HИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Россия<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => HИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой и кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Россия
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20601
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Трансплантация гемопоэтических стволовых клеток крови – один из ведущих методов лечения больных с заболеваниями системы крови, иммунодефицитными состояниями, генетическими болезнями. При этом качество жизни пациентов в отдаленном периоде после ТГСК достоверно отличается от качества жизни условно здоровых людей того же возраста. Деформации в психосексуальном развитии, в том числе проблемы в формировании гендерной идентичности приводят к социальной изоляции подростков, что делает невозможным их половую самореализацию и значимо снижает качество жизни. Целью нашего исследования было оценить уровень сформированности гендерной самоидентичности подростков и соответствие психосексуального развития пациентов возрастным нормам.
</p>
<h2 style="text-align: justify;">Материалы и методы</h2>
<p style="text-align: justify;">
В 2018 году на базе отделения восстановительной медицины клиники НИИ ДОГиТ им. Р. М. Горбачевой мы провели проспективное исследование 13 семей. Респондентами являлись: 1) родители/опекуны пациентов, сопровождающие их в процессе приезда на плановое обследование; 2) подростки, прошедшие лечение методом ТГСК и проходящие плановые осмотры в клинике в посттрансплантационном периоде (после Д+100), (n = 13, из них 6 девочек и 7 мальчиков, возраст – 12-17 лет, со дня проведения ТГСК прошло 1-5 лет). Для оценки гендерной идентичности были использованы следующие методики: cпециально разработанные анкеты для подростков и родителей, опросник Сандры Бем (Sandra L. Bern, 1974), проективные методики «Рисунок человека», «Несуществующее животное», тест цветовых выборов Люшера.
</p>
<h2 style="text-align: justify;">Результаты</h2>
<p style="text-align: justify;">
Традиционный тип гендерной идентичности, который характеризует высокие показатели маскулинности у респондентов мужского пола и высокие показатели фемининности у респондентов женского пола в 100% случаев нами не был выявлен. Как среди девочек, так и среди мальчиков преобладает андрогинный тип с тенденцией к феминности, (%). Причем в среднем сами подростки видят себя несколько более мужественными, чем их матери, за редким исключением, независимо от пола. Это подтверждает тезис, полученный нами в прошлом исследовании, что родители склонны видеть и поощрять в подростках обоего пола покладистость, пассивность в ущерб лидерству, целеустремленности, самостоятельности. Все 100% прошедших тестирование подростки демонстрируют вытеснение темы агрессии, у 77 % наблюдаются те или иные признаки избегания сексуального самоопределения, неприятие своего тела, пола и возраста. 92% пациентов практически не общаются со сверстниками. У 44% преобладают отрицательные эмоции над положительными. У трети испытуемых наблюдается выраженное преобладание установки на отдых и минимизацию собственных усилий.
</p>
<h2 style="text-align: justify;">Выводы</h2>
<p style="text-align: justify;">
Особенности семейного воспитания подростков, прошедших ТГСК, часто способствуют значительному ограничению их социального опыта и ведут к специфическим деформациям личности, в том числе в сфере гендерной идентичности. Считаем целесообразным ввести в психологическое сопровождение лечения в клинике тематическое групповое консультирование родителей в рамках «Школы пациента». Ранняя диагностика аспектов личностного становления в рамках психосексуального развития подростков позволяет своевременно обнаружить индивидуальные проблемные зоны и выявить общие тенденции в отдалённые сроки после ТГСК.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Трансплантация гемопоэтических клеток, подростки, психосексуальное развитие, гендерная идентичность, реабилитация.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Трансплантация гемопоэтических стволовых клеток крови – один из ведущих методов лечения больных с заболеваниями системы крови, иммунодефицитными состояниями, генетическими болезнями. При этом качество жизни пациентов в отдаленном периоде после ТГСК достоверно отличается от качества жизни условно здоровых людей того же возраста. Деформации в психосексуальном развитии, в том числе проблемы в формировании гендерной идентичности приводят к социальной изоляции подростков, что делает невозможным их половую самореализацию и значимо снижает качество жизни. Целью нашего исследования было оценить уровень сформированности гендерной самоидентичности подростков и соответствие психосексуального развития пациентов возрастным нормам.
Материалы и методы
В 2018 году на базе отделения восстановительной медицины клиники НИИ ДОГиТ им. Р. М. Горбачевой мы провели проспективное исследование 13 семей. Респондентами являлись: 1) родители/опекуны пациентов, сопровождающие их в процессе приезда на плановое обследование; 2) подростки, прошедшие лечение методом ТГСК и проходящие плановые осмотры в клинике в посттрансплантационном периоде (после Д+100), (n = 13, из них 6 девочек и 7 мальчиков, возраст – 12-17 лет, со дня проведения ТГСК прошло 1-5 лет). Для оценки гендерной идентичности были использованы следующие методики: cпециально разработанные анкеты для подростков и родителей, опросник Сандры Бем (Sandra L. Bern, 1974), проективные методики «Рисунок человека», «Несуществующее животное», тест цветовых выборов Люшера.
Результаты
Традиционный тип гендерной идентичности, который характеризует высокие показатели маскулинности у респондентов мужского пола и высокие показатели фемининности у респондентов женского пола в 100% случаев нами не был выявлен. Как среди девочек, так и среди мальчиков преобладает андрогинный тип с тенденцией к феминности, (%). Причем в среднем сами подростки видят себя несколько более мужественными, чем их матери, за редким исключением, независимо от пола. Это подтверждает тезис, полученный нами в прошлом исследовании, что родители склонны видеть и поощрять в подростках обоего пола покладистость, пассивность в ущерб лидерству, целеустремленности, самостоятельности. Все 100% прошедших тестирование подростки демонстрируют вытеснение темы агрессии, у 77 % наблюдаются те или иные признаки избегания сексуального самоопределения, неприятие своего тела, пола и возраста. 92% пациентов практически не общаются со сверстниками. У 44% преобладают отрицательные эмоции над положительными. У трети испытуемых наблюдается выраженное преобладание установки на отдых и минимизацию собственных усилий.
Выводы
Особенности семейного воспитания подростков, прошедших ТГСК, часто способствуют значительному ограничению их социального опыта и ведут к специфическим деформациям личности, в том числе в сфере гендерной идентичности. Считаем целесообразным ввести в психологическое сопровождение лечения в клинике тематическое групповое консультирование родителей в рамках «Школы пациента». Ранняя диагностика аспектов личностного становления в рамках психосексуального развития подростков позволяет своевременно обнаружить индивидуальные проблемные зоны и выявить общие тенденции в отдалённые сроки после ТГСК.
Ключевые слова
Трансплантация гемопоэтических клеток, подростки, психосексуальное развитие, гендерная идентичность, реабилитация.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20602
[VALUE] => Array
(
[TEXT] => Svetlana I. Oleshko, Alisa G. Volkova, Ludmila S. Zubarovskaya, Boris V. Afanasyev
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Svetlana I. Oleshko, Alisa G. Volkova, Ludmila S. Zubarovskaya, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20603
[VALUE] => Array
(
[TEXT] => R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation, and Chair of Hematology, Transfusiology and Transplantology at the First I. P. Pavlov State Medical University of St. Petersburg<br>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => R. Gorbacheva Memorial Research Institute of Children Oncology, Hematology and Transplantation, and Chair of Hematology, Transfusiology and Transplantology at the First I. P. Pavlov State Medical University of St. Petersburg
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20604
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
Transplantation of hematopoietic stem cells (HSCT) is one of the leading methods of treatment in patients with blood system diseases, primary immunodeficiency syndromes and genetic diseases. At the same time, the quality of life in patients in the long-term after HSCT significantly differs from the quality of life of healthy people of the same age. Deformations in psychosexual development including problems in the gender identity formation cause social isolation of adolescents, which makes their sexual self-realization impossible and significantly reduces the quality of their life. Hence, the aim of our study was an assessment of the level of gender identity formation of adolescents and psychosexual development correlation to the normal adolescents of the same age.
</p>
<h2 style="text-align: justify;">Materials and methods</h2>
<p style="text-align: justify;">
In 2018, on the base of the Department of Recovery Medicine, the Clinic of the Research Institute of Raisa Gorbacheva Memorial Institute of Children’s Oncology, Hematology and Transplantation, we conducted a prospective study of 13 families. The respondents were: 1) parents/guardians of patients accompanying them in the process of examination; 2) adolescents who underwent HSCT treatment and undergo planned examinations at the clinic in the posttransplant period (after D + 100), (n=13, of which 6 girls and 7 boys, age 12-17 years, from the date of HSCT 1-5 years). The following methods were used to assess gender identity: Specially developed questionnaires for teenagers and parents; questionnaire by Sandra L. Bem (Sandra L. Bem, 1974); projective techniques “The Human Picture”, “The non-existent animal”; Max Lüscher’s color choices test.
</p>
<h2 style="text-align: justify;">Results</h2>
<p style="text-align: justify;">
The traditional type of gender identity that characterizes the high masculinity in male respondents and the high femininity rates of female respondents in 100% of cases were not revealed. Both among girls and among boys, the androgynous type predominates with a tendency towards femininity. On average, the adolescents evaluate themselves a little more courageous than their mothers, with rare exceptions, regardless of gender. This confirms the thesis we received in the previous study that parents tend to see and encourage complacency in adolescents of both sexes, passivity to the detriment of leadership, dedication, and independence. All 100% of the teenagers, who participated in the test, demonstrate the displacement of the aggression topic, 77% have some signs of avoiding sexual self-determination, rejection of their body, sex and age. 92% of patients do not communicate with their peers. In 44% of them, negative emotions prevail over positive ones. A third of the test participants show an expressed favor for rest and minimization of their efforts.
</p>
<h2 style="text-align: justify;">Conclusions</h2>
<p style="text-align: justify;">
The characteristics of family upbringing of adolescents who have undergone HSCT often contribute significantly to limiting their social experience and lead to specific deformities of individuality, including in the sphere of gender identity. We consider it advisable to introduce thematic group counseling of parents within the framework of the “Patient’s School” in psychological treatment support in the clinic. Early diagnostics of aspects of personal development within the framework of psychosexual development of adolescents makes it possible to identify individual problem areas in a timely manner and to identify general trends in the long term after HSCT.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Hematopoietic stem cells transplant, adolescents, psychosexual development, gender identity, rehabilitation.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
Transplantation of hematopoietic stem cells (HSCT) is one of the leading methods of treatment in patients with blood system diseases, primary immunodeficiency syndromes and genetic diseases. At the same time, the quality of life in patients in the long-term after HSCT significantly differs from the quality of life of healthy people of the same age. Deformations in psychosexual development including problems in the gender identity formation cause social isolation of adolescents, which makes their sexual self-realization impossible and significantly reduces the quality of their life. Hence, the aim of our study was an assessment of the level of gender identity formation of adolescents and psychosexual development correlation to the normal adolescents of the same age.
Materials and methods
In 2018, on the base of the Department of Recovery Medicine, the Clinic of the Research Institute of Raisa Gorbacheva Memorial Institute of Children’s Oncology, Hematology and Transplantation, we conducted a prospective study of 13 families. The respondents were: 1) parents/guardians of patients accompanying them in the process of examination; 2) adolescents who underwent HSCT treatment and undergo planned examinations at the clinic in the posttransplant period (after D + 100), (n=13, of which 6 girls and 7 boys, age 12-17 years, from the date of HSCT 1-5 years). The following methods were used to assess gender identity: Specially developed questionnaires for teenagers and parents; questionnaire by Sandra L. Bem (Sandra L. Bem, 1974); projective techniques “The Human Picture”, “The non-existent animal”; Max Lüscher’s color choices test.
Results
The traditional type of gender identity that characterizes the high masculinity in male respondents and the high femininity rates of female respondents in 100% of cases were not revealed. Both among girls and among boys, the androgynous type predominates with a tendency towards femininity. On average, the adolescents evaluate themselves a little more courageous than their mothers, with rare exceptions, regardless of gender. This confirms the thesis we received in the previous study that parents tend to see and encourage complacency in adolescents of both sexes, passivity to the detriment of leadership, dedication, and independence. All 100% of the teenagers, who participated in the test, demonstrate the displacement of the aggression topic, 77% have some signs of avoiding sexual self-determination, rejection of their body, sex and age. 92% of patients do not communicate with their peers. In 44% of them, negative emotions prevail over positive ones. A third of the test participants show an expressed favor for rest and minimization of their efforts.
Conclusions
The characteristics of family upbringing of adolescents who have undergone HSCT often contribute significantly to limiting their social experience and lead to specific deformities of individuality, including in the sphere of gender identity. We consider it advisable to introduce thematic group counseling of parents within the framework of the “Patient’s School” in psychological treatment support in the clinic. Early diagnostics of aspects of personal development within the framework of psychosexual development of adolescents makes it possible to identify individual problem areas in a timely manner and to identify general trends in the long term after HSCT.
Keywords
Hematopoietic stem cells transplant, adolescents, psychosexual development, gender identity, rehabilitation.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20605
[VALUE] => Peculiarities of psychosexual development of adolescents after hematopoietic stem cell transplantation
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Peculiarities of psychosexual development of adolescents after hematopoietic stem cell transplantation
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20801
[VALUE] => 1439
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1439
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20802
[VALUE] => 1440
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1440
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Светлана И. Олешко, Алиса Г. Волкова, Людмила С. Зубаровская, Борис В. Афанасьев
Введение
Трансплантация гемопоэтических стволовых клеток крови – один из ведущих методов лечения больных с заболеваниями системы крови, иммунодефицитными состояниями, генетическими болезнями. При этом качество жизни пациентов в отдаленном периоде после ТГСК достоверно отличается от качества жизни условно здоровых людей того же возраста. Деформации в психосексуальном развитии, в том числе проблемы в формировании гендерной идентичности приводят к социальной изоляции подростков, что делает невозможным их половую самореализацию и значимо снижает качество жизни. Целью нашего исследования было оценить уровень сформированности гендерной самоидентичности подростков и соответствие психосексуального развития пациентов возрастным нормам.
Материалы и методы
В 2018 году на базе отделения восстановительной медицины клиники НИИ ДОГиТ им. Р. М. Горбачевой мы провели проспективное исследование 13 семей. Респондентами являлись: 1) родители/опекуны пациентов, сопровождающие их в процессе приезда на плановое обследование; 2) подростки, прошедшие лечение методом ТГСК и проходящие плановые осмотры в клинике в посттрансплантационном периоде (после Д+100), (n = 13, из них 6 девочек и 7 мальчиков, возраст – 12-17 лет, со дня проведения ТГСК прошло 1-5 лет). Для оценки гендерной идентичности были использованы следующие методики: cпециально разработанные анкеты для подростков и родителей, опросник Сандры Бем (Sandra L. Bern, 1974), проективные методики «Рисунок человека», «Несуществующее животное», тест цветовых выборов Люшера.
Результаты
Традиционный тип гендерной идентичности, который характеризует высокие показатели маскулинности у респондентов мужского пола и высокие показатели фемининности у респондентов женского пола в 100% случаев нами не был выявлен. Как среди девочек, так и среди мальчиков преобладает андрогинный тип с тенденцией к феминности, (%). Причем в среднем сами подростки видят себя несколько более мужественными, чем их матери, за редким исключением, независимо от пола. Это подтверждает тезис, полученный нами в прошлом исследовании, что родители склонны видеть и поощрять в подростках обоего пола покладистость, пассивность в ущерб лидерству, целеустремленности, самостоятельности. Все 100% прошедших тестирование подростки демонстрируют вытеснение темы агрессии, у 77 % наблюдаются те или иные признаки избегания сексуального самоопределения, неприятие своего тела, пола и возраста. 92% пациентов практически не общаются со сверстниками. У 44% преобладают отрицательные эмоции над положительными. У трети испытуемых наблюдается выраженное преобладание установки на отдых и минимизацию собственных усилий.
Выводы
Особенности семейного воспитания подростков, прошедших ТГСК, часто способствуют значительному ограничению их социального опыта и ведут к специфическим деформациям личности, в том числе в сфере гендерной идентичности. Считаем целесообразным ввести в психологическое сопровождение лечения в клинике тематическое групповое консультирование родителей в рамках «Школы пациента». Ранняя диагностика аспектов личностного становления в рамках психосексуального развития подростков позволяет своевременно обнаружить индивидуальные проблемные зоны и выявить общие тенденции в отдалённые сроки после ТГСК.
Ключевые слова
Трансплантация гемопоэтических клеток, подростки, психосексуальное развитие, гендерная идентичность, реабилитация.
Короткие сообщения
Array
(
[KEYWORDS] => Array
(
[ID] => 19
[TIMESTAMP_X] => 2015-09-03 10:46:01
[IBLOCK_ID] => 2
[NAME] => Ключевые слова
[ACTIVE] => Y
[SORT] => 500
[CODE] => KEYWORDS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 19
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 4
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => Y
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => Y
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Ключевые слова
[~DEFAULT_VALUE] =>
)
[SUBMITTED] => Array
(
[ID] => 20
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата подачи
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUBMITTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 20
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата подачи
[~DEFAULT_VALUE] =>
)
[ACCEPTED] => Array
(
[ID] => 21
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата принятия
[ACTIVE] => Y
[SORT] => 500
[CODE] => ACCEPTED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 21
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата принятия
[~DEFAULT_VALUE] =>
)
[PUBLISHED] => Array
(
[ID] => 22
[TIMESTAMP_X] => 2015-09-02 17:21:42
[IBLOCK_ID] => 2
[NAME] => Дата публикации
[ACTIVE] => Y
[SORT] => 500
[CODE] => PUBLISHED
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 22
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => DateTime
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Дата публикации
[~DEFAULT_VALUE] =>
)
[CONTACT] => Array
(
[ID] => 23
[TIMESTAMP_X] => 2015-09-03 14:43:05
[IBLOCK_ID] => 2
[NAME] => Контакт
[ACTIVE] => Y
[SORT] => 500
[CODE] => CONTACT
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 23
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Контакт
[~DEFAULT_VALUE] =>
)
[AUTHORS] => Array
(
[ID] => 24
[TIMESTAMP_X] => 2015-09-03 10:45:07
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHORS
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => E
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => Y
[XML_ID] => 24
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 3
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] => EAutocomplete
[USER_TYPE_SETTINGS] => Array
(
[VIEW] => E
[SHOW_ADD] => Y
[MAX_WIDTH] => 0
[MIN_HEIGHT] => 24
[MAX_HEIGHT] => 1000
[BAN_SYM] => ,;
[REP_SYM] =>
[OTHER_REP_SYM] =>
[IBLOCK_MESS] => N
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] =>
)
[AUTHOR_RU] => Array
(
[ID] => 25
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Авторы
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 25
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20725
[VALUE] => Array
(
[TEXT] => Ксения П. Якимович, Ольга В. Пирогова, Олег В. Голощапов, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Ксения П. Якимович, Ольга В. Пирогова, Олег В. Голощапов, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Авторы
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_RU] => Array
(
[ID] => 26
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Организации
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 26
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20726
[VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, кафедра гематологии, трансфузиологии и трансплантологии, Первый Санкт-Петербургский Государственный Медицинский Университет им. акад. И. П. Павлова, Санкт-Петербург, Российская Федерация
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Организации
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_RU] => Array
(
[ID] => 27
[TIMESTAMP_X] => 2015-09-02 18:01:20
[IBLOCK_ID] => 2
[NAME] => Описание/Резюме
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 27
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20727
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Введение</h2>
<p style="text-align: justify;">
Стероид-рефрактерная РТПХ (срРТПХ) развивается в половине случаев РТПХ, с вероятностью летального исхода 70%. В качестве терапии спасения могут выступать ингибиторы Jak-2-киназ. Однако нет достоверных данных об оптимальной продолжительности терапии и стратегии отмены данных препаратов. Целью работы стало представление случая срРТПХ печени после гаплоидентичной трансплантации гемопоэтических стволовых клеток (гапло-ТГСК) у молодого пациента с синдромом Жильбера с улучшением показателей функции печени после отмены терапии ингибитором Jak-2-киназ. При анализе результатов были использованы данные медицинской документации, результаты лабораторных и инструментальных исследований. Стадии РТПХ оценивались согласно критериям NIH-2014.
</p>
<h2 style="text-align: justify;">Описание клинического случая</h2>
<p style="text-align: justify;">
Пациент, 28 лет, с острым миелоидным лейкозом (ОМЛ), FAB-M2, и сопутствующим синдромом Жильбера 12.05.2015 перенес гапло-ТГСК от брата, 6/10. Режим кондиционирования: бусульфан (8 мг/кг), флударабин. Источник трансплантата: костный мозг. Профилактика РТПХ: циклофосфан (30 мг/кг, Д+3,+4), такролимус (с Д+5), микофенолата мофетил (45 мг/кг с Д+5 по Д+35). На Д+90 по причине развития раннего костно-мозгового рецидива – отмена такролимуса. На Д+202 развился overlap-синдром РТПХ 4 степени с поражением кожи, печени и нижних отделов ЖКТ (стадии 3, 4 и 3, соответственно). Терапия I линии: метилпреднизолон 2 мг/кг; эффект: частичный ответ по РТПХ кожи. К терапии были добавлены этанерцепт 25 мг 2 р/нед и такролимус. Эффект: уровень билирубина более 250 мкмоль/л, полный ответ по коже и ЖКТ. На Д+237 в связи с развитием легочного кровотечения и переводом в ОРИТ – отмена базовой иммуносупрессивной терапии. На этом фоне наблюдались рост уровня билирубина до 580 мкмоль/л, кишечное кровотечение. Смена терапии на руксолитиниб, ингибитор Jak-2-киназы (20 мг/сут). Эффект: снижение уровня билирубина, РТПХ кишечника без динамики. На Д+249 трансплантация фекальной микробиоты, эффект: разрешение симптомов поражения ЖКТ. Повторные введения мезенхимальных стволовых клеток (Д+257,+266), без достижения ответа. Нарастание уровня холестерина более 40 ммоль/л с попытками терапии плазмаферезом дважды в неделю. На Д+350 выполнена биопсия печени с выявлением признаков РТПХ. C Д+316 по Д+426 пациент получил 5 введений тоцилизумаба, 12 сеансов экстракорпорального фотофереза, лечение сиролимусом и низкими дозами интерлейкина-2, без достижения эффекта (уровень билирубина 520-724 мкмоль/л). Терапия сиролимусом и руксолитинибом с Д+460 по Д+738. Смена руксолитиниба на ингибитор Jak-2 киназы нового поколения барицитиниб (4мг/сут) с Д+738. Эффект: уровень билирубина 220-420 мкмоль/л, однако, сохранялась гиперхолестеринемия. С Д+1120 барицитиниб был отменен. Эффект: снижение уровня билирубина (213 мкмоль/л) и холестерина (7,7 ммоль/л). Продолжается терапия сиролимусом, отмечается значимое улучшение качества жизни пациента.
</p>
<h2 style="text-align: justify;">Заключение</h2>
<p style="text-align: justify;">
Тяжелая срРТПХ печени – состояние, которое может потребовать применения длительной иммуносупрессивной терапии с невысокой вероятностью достижения полного ответа. Несмотря на доказанную эффективность ингибиторов Jak-2-киназ, данная терапия ассоциирована с серьезными неблагоприятными явлениями, в том числе, развитием тяжелой гиперхолестеринемии. Наличие синдрома Жильбера может затруднять оценку эффективности терапии, а также требовать проведения биопсии печени с целью возможного изменения подходов к лечению.
</p>
<h2 style="text-align: justify;">Ключевые слова</h2>
<p style="text-align: justify;">
Cтероид-рефрактерная реакция «трансплантат против хозяина» (срРТПХ), overlap-синдром, ингибиторы Jak-2-киназ, синдром Жильбера, трансплантация фекальной микробиоты.
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Введение
Стероид-рефрактерная РТПХ (срРТПХ) развивается в половине случаев РТПХ, с вероятностью летального исхода 70%. В качестве терапии спасения могут выступать ингибиторы Jak-2-киназ. Однако нет достоверных данных об оптимальной продолжительности терапии и стратегии отмены данных препаратов. Целью работы стало представление случая срРТПХ печени после гаплоидентичной трансплантации гемопоэтических стволовых клеток (гапло-ТГСК) у молодого пациента с синдромом Жильбера с улучшением показателей функции печени после отмены терапии ингибитором Jak-2-киназ. При анализе результатов были использованы данные медицинской документации, результаты лабораторных и инструментальных исследований. Стадии РТПХ оценивались согласно критериям NIH-2014.
Описание клинического случая
Пациент, 28 лет, с острым миелоидным лейкозом (ОМЛ), FAB-M2, и сопутствующим синдромом Жильбера 12.05.2015 перенес гапло-ТГСК от брата, 6/10. Режим кондиционирования: бусульфан (8 мг/кг), флударабин. Источник трансплантата: костный мозг. Профилактика РТПХ: циклофосфан (30 мг/кг, Д+3,+4), такролимус (с Д+5), микофенолата мофетил (45 мг/кг с Д+5 по Д+35). На Д+90 по причине развития раннего костно-мозгового рецидива – отмена такролимуса. На Д+202 развился overlap-синдром РТПХ 4 степени с поражением кожи, печени и нижних отделов ЖКТ (стадии 3, 4 и 3, соответственно). Терапия I линии: метилпреднизолон 2 мг/кг; эффект: частичный ответ по РТПХ кожи. К терапии были добавлены этанерцепт 25 мг 2 р/нед и такролимус. Эффект: уровень билирубина более 250 мкмоль/л, полный ответ по коже и ЖКТ. На Д+237 в связи с развитием легочного кровотечения и переводом в ОРИТ – отмена базовой иммуносупрессивной терапии. На этом фоне наблюдались рост уровня билирубина до 580 мкмоль/л, кишечное кровотечение. Смена терапии на руксолитиниб, ингибитор Jak-2-киназы (20 мг/сут). Эффект: снижение уровня билирубина, РТПХ кишечника без динамики. На Д+249 трансплантация фекальной микробиоты, эффект: разрешение симптомов поражения ЖКТ. Повторные введения мезенхимальных стволовых клеток (Д+257,+266), без достижения ответа. Нарастание уровня холестерина более 40 ммоль/л с попытками терапии плазмаферезом дважды в неделю. На Д+350 выполнена биопсия печени с выявлением признаков РТПХ. C Д+316 по Д+426 пациент получил 5 введений тоцилизумаба, 12 сеансов экстракорпорального фотофереза, лечение сиролимусом и низкими дозами интерлейкина-2, без достижения эффекта (уровень билирубина 520-724 мкмоль/л). Терапия сиролимусом и руксолитинибом с Д+460 по Д+738. Смена руксолитиниба на ингибитор Jak-2 киназы нового поколения барицитиниб (4мг/сут) с Д+738. Эффект: уровень билирубина 220-420 мкмоль/л, однако, сохранялась гиперхолестеринемия. С Д+1120 барицитиниб был отменен. Эффект: снижение уровня билирубина (213 мкмоль/л) и холестерина (7,7 ммоль/л). Продолжается терапия сиролимусом, отмечается значимое улучшение качества жизни пациента.
Заключение
Тяжелая срРТПХ печени – состояние, которое может потребовать применения длительной иммуносупрессивной терапии с невысокой вероятностью достижения полного ответа. Несмотря на доказанную эффективность ингибиторов Jak-2-киназ, данная терапия ассоциирована с серьезными неблагоприятными явлениями, в том числе, развитием тяжелой гиперхолестеринемии. Наличие синдрома Жильбера может затруднять оценку эффективности терапии, а также требовать проведения биопсии печени с целью возможного изменения подходов к лечению.
Ключевые слова
Cтероид-рефрактерная реакция «трансплантат против хозяина» (срРТПХ), overlap-синдром, ингибиторы Jak-2-киназ, синдром Жильбера, трансплантация фекальной микробиоты.
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Описание/Резюме
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[DOI] => Array
(
[ID] => 28
[TIMESTAMP_X] => 2016-04-06 14:11:12
[IBLOCK_ID] => 2
[NAME] => DOI
[ACTIVE] => Y
[SORT] => 500
[CODE] => DOI
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 28
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => DOI
[~DEFAULT_VALUE] =>
)
[AUTHOR_EN] => Array
(
[ID] => 37
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Author
[ACTIVE] => Y
[SORT] => 500
[CODE] => AUTHOR_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 37
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20728
[VALUE] => Array
(
[TEXT] => Kseniya P. Yakimovich, Olga V. Pirogova, Oleg V. Goloshchapov, Elena I. Darskaya, Sergey N. Bondarenko, Ivan S. Moiseev, Boris V. Afanasyev
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => Kseniya P. Yakimovich, Olga V. Pirogova, Oleg V. Goloshchapov, Elena I. Darskaya, Sergey N. Bondarenko, Ivan S. Moiseev, Boris V. Afanasyev
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Author
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[ORGANIZATION_EN] => Array
(
[ID] => 38
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Organization
[ACTIVE] => Y
[SORT] => 500
[CODE] => ORGANIZATION_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 38
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20729
[VALUE] => Array
(
[TEXT] => R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] => R. M. Gorbacheva Memorial Institute of Hematology, Oncology and Transplantation, Chair of Hematology, Transfusiology and Transplantology, First St. Petersburg State I. Pavlov Medical University, St. Petersburg, Russian Federation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Organization
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[SUMMARY_EN] => Array
(
[ID] => 39
[TIMESTAMP_X] => 2015-09-02 18:02:59
[IBLOCK_ID] => 2
[NAME] => Description / Summary
[ACTIVE] => Y
[SORT] => 500
[CODE] => SUMMARY_EN
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 39
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] => 20730
[VALUE] => Array
(
[TEXT] => <h2></h2>
<h2 style="text-align: justify;">Introduction</h2>
<p style="text-align: justify;">
The incidence of steroid-refractory graft versus host disease (SR-GVHD) is a one-half of patients with a mortality rate of 70%. Janus kinase (JAK) 1/2 inhibitors might be considered as a salvage therapy. However, there is a scarcity of relevant information about optimal duration and taping strategy of Jak-2-inhibitors. Our aim was to present a clinical case of a liver SR-GVHD after haploidentical HSCT (haplo-HSCT) in a young patient with Gilbert syndrome who developed decrease of liver function tests following discontinuation of Jak-2 kinase inhibitor therapy. Medical records, laboratory and instrumental data were reviewed when analyzing the results. GVHD severity was scored according to the 2014 NIH Consensus Criteria.
</p>
<h2 style="text-align: justify;">Case report</h2>
<p style="text-align: justify;">
A 28-year-old male patient with acute myeloid leukemia (AML), FAB-M2, and concurrent Gilbert syndrome underwent haplo-HSCT on 12 May 2015 from brother, HLA compatibility, 6/10. Conditioning regimen: busulfan 8 mg/kg, fludarabine. Bone marrow was a source of stem cells:. GVHD prophylaxis: cyclophosphamide (30 mg/kg, days+3,+4), tacrolimus (from day+5), mycophenolate mofetil (45 mg/kg, days from +5 to +35). On day+90, tacrolimus was discontinued due to early bone marrow recurrence. On day+202, overlap-syndrome of grade 4 was developed, with skin, liver and lower gastrointestinal tract (GIT) lesions (grade 3, 4 and 3 respectively). The first-line therapy: methylprednisolone 2 mg/kg, causing partial response for skin. Etanercept (25 mg twice a day) and tacrolimus were added, followed by complete response for skin and GIT; bilirubin level was >250 μmol/L. The immunosuppressive therapy was discontinued on the day+237, due to pulmonary hemorrhage and transfer to intensive care unit. Increased bilirubin level (580 μmol/L) and intestinal bleeding were observed. This treatment was replaced by a Jak-2 inhibitor (ruxolitinib, 20 mg per day). The effect: decreased bilirubin level, without any dynamics for intestinal pathology. On day+249, fecal microbiota transplantation was performed, followed by resolution of GI symptoms. Mesenchymal stem cells were infused twice (D+257, D+266) with no response. Cholesterol levels raised over 40 mmol/L, having been treated bi-weekly plasmapheresis. From day+316 to day+426, the patient received 5 infusions of tocilizumab, he underwent 12 courses of extracorporeal photopheresis, sirolimus and low-dose interleukin-2, without any response (bilirubin 520 to 724 μmol/l). On day +350, liver biopsy was performed, and GVHD pathology was detected. Sirolimus and ruxolitinib were administered from day+460 to day+738. Ruxolitinib was replaced by a new-generation Jak-2 kinase inhibitor baricitinib (4 mg daily) on day+738. The following effect was observed: bilirubin level 220-420 mmol/L, hypercholesterolemia still persisted. On day+1120, baricitinib was discontinued. Further on, a decrease of bilirubin (213 μmol/L) and cholesterol levels (7.7 mmol/l) were documented. The therapy with sirolimus is going on, and significant improvement in the quality of life is noted.
</p>
<h2 style="text-align: justify;">Conclusion</h2>
<p style="text-align: justify;">
Steroid-refractory severe chronic liver GVHD is a condition that might require prolonged immunosuppressive treatment with absence of complete response to current treatments. Despite high efficacy of JAK-2-inhibitors, they might be associated with serious adverse effects, like severe hypercholesterolemia. Gilbert syndrome may complicate the assessment of GVHD response and require liver biopsy to guide a therapy.
</p>
<h2 style="text-align: justify;">Keywords</h2>
<p style="text-align: justify;">
Steroid-refractory graft-versus-host disease (SR-GVHD), overlap syndrome, Jak-2-inhibitors, Gilbert syndrome, fecal microbiota transplantation
</p>
[TYPE] => HTML
)
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Array
(
[TEXT] =>
Introduction
The incidence of steroid-refractory graft versus host disease (SR-GVHD) is a one-half of patients with a mortality rate of 70%. Janus kinase (JAK) 1/2 inhibitors might be considered as a salvage therapy. However, there is a scarcity of relevant information about optimal duration and taping strategy of Jak-2-inhibitors. Our aim was to present a clinical case of a liver SR-GVHD after haploidentical HSCT (haplo-HSCT) in a young patient with Gilbert syndrome who developed decrease of liver function tests following discontinuation of Jak-2 kinase inhibitor therapy. Medical records, laboratory and instrumental data were reviewed when analyzing the results. GVHD severity was scored according to the 2014 NIH Consensus Criteria.
Case report
A 28-year-old male patient with acute myeloid leukemia (AML), FAB-M2, and concurrent Gilbert syndrome underwent haplo-HSCT on 12 May 2015 from brother, HLA compatibility, 6/10. Conditioning regimen: busulfan 8 mg/kg, fludarabine. Bone marrow was a source of stem cells:. GVHD prophylaxis: cyclophosphamide (30 mg/kg, days+3,+4), tacrolimus (from day+5), mycophenolate mofetil (45 mg/kg, days from +5 to +35). On day+90, tacrolimus was discontinued due to early bone marrow recurrence. On day+202, overlap-syndrome of grade 4 was developed, with skin, liver and lower gastrointestinal tract (GIT) lesions (grade 3, 4 and 3 respectively). The first-line therapy: methylprednisolone 2 mg/kg, causing partial response for skin. Etanercept (25 mg twice a day) and tacrolimus were added, followed by complete response for skin and GIT; bilirubin level was >250 μmol/L. The immunosuppressive therapy was discontinued on the day+237, due to pulmonary hemorrhage and transfer to intensive care unit. Increased bilirubin level (580 μmol/L) and intestinal bleeding were observed. This treatment was replaced by a Jak-2 inhibitor (ruxolitinib, 20 mg per day). The effect: decreased bilirubin level, without any dynamics for intestinal pathology. On day+249, fecal microbiota transplantation was performed, followed by resolution of GI symptoms. Mesenchymal stem cells were infused twice (D+257, D+266) with no response. Cholesterol levels raised over 40 mmol/L, having been treated bi-weekly plasmapheresis. From day+316 to day+426, the patient received 5 infusions of tocilizumab, he underwent 12 courses of extracorporeal photopheresis, sirolimus and low-dose interleukin-2, without any response (bilirubin 520 to 724 μmol/l). On day +350, liver biopsy was performed, and GVHD pathology was detected. Sirolimus and ruxolitinib were administered from day+460 to day+738. Ruxolitinib was replaced by a new-generation Jak-2 kinase inhibitor baricitinib (4 mg daily) on day+738. The following effect was observed: bilirubin level 220-420 mmol/L, hypercholesterolemia still persisted. On day+1120, baricitinib was discontinued. Further on, a decrease of bilirubin (213 μmol/L) and cholesterol levels (7.7 mmol/l) were documented. The therapy with sirolimus is going on, and significant improvement in the quality of life is noted.
Conclusion
Steroid-refractory severe chronic liver GVHD is a condition that might require prolonged immunosuppressive treatment with absence of complete response to current treatments. Despite high efficacy of JAK-2-inhibitors, they might be associated with serious adverse effects, like severe hypercholesterolemia. Gilbert syndrome may complicate the assessment of GVHD response and require liver biopsy to guide a therapy.
Keywords
Steroid-refractory graft-versus-host disease (SR-GVHD), overlap syndrome, Jak-2-inhibitors, Gilbert syndrome, fecal microbiota transplantation
[TYPE] => HTML
)
[~DESCRIPTION] =>
[~NAME] => Description / Summary
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[NAME_EN] => Array
(
[ID] => 40
[TIMESTAMP_X] => 2015-09-03 10:49:47
[IBLOCK_ID] => 2
[NAME] => Name
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 80
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 40
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => Y
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20731
[VALUE] => Case report: effect of Jak-2 kinase inhibitor discontinuation on chronic steroid-refractory graft-versus-host disease in liver
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => Case report: effect of Jak-2 kinase inhibitor discontinuation on chronic steroid-refractory graft-versus-host disease in liver
[~DESCRIPTION] =>
[~NAME] => Name
[~DEFAULT_VALUE] =>
)
[FULL_TEXT_RU] => Array
(
[ID] => 42
[TIMESTAMP_X] => 2015-09-07 20:29:18
[IBLOCK_ID] => 2
[NAME] => Полный текст
[ACTIVE] => Y
[SORT] => 500
[CODE] => FULL_TEXT_RU
[DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 42
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 200
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Полный текст
[~DEFAULT_VALUE] => Array
(
[TEXT] =>
[TYPE] => HTML
)
)
[PDF_RU] => Array
(
[ID] => 43
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF RUS
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_RU
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 43
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20835
[VALUE] => 1474
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1474
[~DESCRIPTION] =>
[~NAME] => PDF RUS
[~DEFAULT_VALUE] =>
)
[PDF_EN] => Array
(
[ID] => 44
[TIMESTAMP_X] => 2015-09-09 16:05:20
[IBLOCK_ID] => 2
[NAME] => PDF ENG
[ACTIVE] => Y
[SORT] => 500
[CODE] => PDF_EN
[DEFAULT_VALUE] =>
[PROPERTY_TYPE] => F
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 44
[FILE_TYPE] => doc, txt, rtf, pdf
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] =>
[USER_TYPE_SETTINGS] =>
[HINT] =>
[PROPERTY_VALUE_ID] => 20836
[VALUE] => 1475
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] => 1475
[~DESCRIPTION] =>
[~NAME] => PDF ENG
[~DEFAULT_VALUE] =>
)
[NAME_LONG] => Array
(
[ID] => 45
[TIMESTAMP_X] => 2023-04-13 00:55:00
[IBLOCK_ID] => 2
[NAME] => Название (для очень длинных заголовков)
[ACTIVE] => Y
[SORT] => 500
[CODE] => NAME_LONG
[DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
[PROPERTY_TYPE] => S
[ROW_COUNT] => 1
[COL_COUNT] => 30
[LIST_TYPE] => L
[MULTIPLE] => N
[XML_ID] => 45
[FILE_TYPE] =>
[MULTIPLE_CNT] => 5
[TMP_ID] =>
[LINK_IBLOCK_ID] => 0
[WITH_DESCRIPTION] => N
[SEARCHABLE] => N
[FILTRABLE] => N
[IS_REQUIRED] => N
[VERSION] => 1
[USER_TYPE] => HTML
[USER_TYPE_SETTINGS] => Array
(
[height] => 80
)
[HINT] =>
[PROPERTY_VALUE_ID] =>
[VALUE] =>
[DESCRIPTION] =>
[VALUE_ENUM] =>
[VALUE_XML_ID] =>
[VALUE_SORT] =>
[~VALUE] =>
[~DESCRIPTION] =>
[~NAME] => Название (для очень длинных заголовков)
[~DEFAULT_VALUE] => Array
(
[TYPE] => HTML
[TEXT] =>
)
)
)
Ксения П. Якимович, Ольга В. Пирогова, Олег В. Голощапов, Елена И. Дарская, Сергей Н. Бондаренко, Иван С. Моисеев, Борис В. Афанасьев
Введение
Стероид-рефрактерная РТПХ (срРТПХ) развивается в половине случаев РТПХ, с вероятностью летального исхода 70%. В качестве терапии спасения могут выступать ингибиторы Jak-2-киназ. Однако нет достоверных данных об оптимальной продолжительности терапии и стратегии отмены данных препаратов. Целью работы стало представление случая срРТПХ печени после гаплоидентичной трансплантации гемопоэтических стволовых клеток (гапло-ТГСК) у молодого пациента с синдромом Жильбера с улучшением показателей функции печени после отмены терапии ингибитором Jak-2-киназ. При анализе результатов были использованы данные медицинской документации, результаты лабораторных и инструментальных исследований. Стадии РТПХ оценивались согласно критериям NIH-2014.
Описание клинического случая
Пациент, 28 лет, с острым миелоидным лейкозом (ОМЛ), FAB-M2, и сопутствующим синдромом Жильбера 12.05.2015 перенес гапло-ТГСК от брата, 6/10. Режим кондиционирования: бусульфан (8 мг/кг), флударабин. Источник трансплантата: костный мозг. Профилактика РТПХ: циклофосфан (30 мг/кг, Д+3,+4), такролимус (с Д+5), микофенолата мофетил (45 мг/кг с Д+5 по Д+35). На Д+90 по причине развития раннего костно-мозгового рецидива – отмена такролимуса. На Д+202 развился overlap-синдром РТПХ 4 степени с поражением кожи, печени и нижних отделов ЖКТ (стадии 3, 4 и 3, соответственно). Терапия I линии: метилпреднизолон 2 мг/кг; эффект: частичный ответ по РТПХ кожи. К терапии были добавлены этанерцепт 25 мг 2 р/нед и такролимус. Эффект: уровень билирубина более 250 мкмоль/л, полный ответ по коже и ЖКТ. На Д+237 в связи с развитием легочного кровотечения и переводом в ОРИТ – отмена базовой иммуносупрессивной терапии. На этом фоне наблюдались рост уровня билирубина до 580 мкмоль/л, кишечное кровотечение. Смена терапии на руксолитиниб, ингибитор Jak-2-киназы (20 мг/сут). Эффект: снижение уровня билирубина, РТПХ кишечника без динамики. На Д+249 трансплантация фекальной микробиоты, эффект: разрешение симптомов поражения ЖКТ. Повторные введения мезенхимальных стволовых клеток (Д+257,+266), без достижения ответа. Нарастание уровня холестерина более 40 ммоль/л с попытками терапии плазмаферезом дважды в неделю. На Д+350 выполнена биопсия печени с выявлением признаков РТПХ. C Д+316 по Д+426 пациент получил 5 введений тоцилизумаба, 12 сеансов экстракорпорального фотофереза, лечение сиролимусом и низкими дозами интерлейкина-2, без достижения эффекта (уровень билирубина 520-724 мкмоль/л). Терапия сиролимусом и руксолитинибом с Д+460 по Д+738. Смена руксолитиниба на ингибитор Jak-2 киназы нового поколения барицитиниб (4мг/сут) с Д+738. Эффект: уровень билирубина 220-420 мкмоль/л, однако, сохранялась гиперхолестеринемия. С Д+1120 барицитиниб был отменен. Эффект: снижение уровня билирубина (213 мкмоль/л) и холестерина (7,7 ммоль/л). Продолжается терапия сиролимусом, отмечается значимое улучшение качества жизни пациента.
Заключение
Тяжелая срРТПХ печени – состояние, которое может потребовать применения длительной иммуносупрессивной терапии с невысокой вероятностью достижения полного ответа. Несмотря на доказанную эффективность ингибиторов Jak-2-киназ, данная терапия ассоциирована с серьезными неблагоприятными явлениями, в том числе, развитием тяжелой гиперхолестеринемии. Наличие синдрома Жильбера может затруднять оценку эффективности терапии, а также требовать проведения биопсии печени с целью возможного изменения подходов к лечению.
Ключевые слова
Cтероид-рефрактерная реакция «трансплантат против хозяина» (срРТПХ), overlap-синдром, ингибиторы Jak-2-киназ, синдром Жильбера, трансплантация фекальной микробиоты.

